SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh : Evina NIM : 078114073
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh : Evina NIM : 078114073
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
Kegigihan adalah semangat pantang menyerah
Yang harus kita miliki.
Dengan bekal kegigihan dan usaha yang konsisten,
Kesuksesan yang kita peroleh pasti berkualitas
dan membanggakan.
-andre wongso-
In this life we cannot always do great things.
But we can do small things with great love
~Mother Teresa
Karyaku ini kupersembahkan untuk:
Papa, Mama tercinta.
Akian, Sannie, dan Irine tersayang
v
Nama : Evina
Nomor Mahasiswa : 078114073
Demi perkembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
PENGARUH PROPORSI DRUG LOAD TERHADAP DISOLUSI DISPERSI PADAT SPRAY DRIED ISOLAT EKSTRAK RIMPANG KUNYIT (Curcuma
domestica C-95)-PVP K-25
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada
Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya ataupun memberi royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenamya.
Dibuat di Yogyakarta
Pada tanggal: 16 Februari 2011
Yang menyatakan
vi
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 16 Februari 2011 Penulis
vii
skripsi yang berjudul “Pengaruh Proporsi DrugLoad Terhadap Disolusi Dispersi Padat Spray Dried Isolat Ekstrak Rimpang Kunyit (Curcuma domestica C-95 )-PVP K-25” sebagai salah satu syarat untuk mencapai gelar Sarjana Farmasi (S. Farm.) di Universitas Sanata Dharma Yogyakarta.
Dalam penulisan skripsi ini, penulis banyak mendapatkan bantuan dari berbagai pihak, baik bimbingan, dorongan, maupun saran. Pada kesempatan ini, penulis ingin menyampaikan penghargaan dan ucapan terima kasih kepada:
1. Ipang Djunarko, M.Si., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Dewi Setyaningsih, M.Sc, Apt. selaku Dosen Pembimbing Utama atas bimbingan, dukungan, pengarahannya dari awal penelitian hingga penyusunan skripsi ini, dan telah menanggung semua biaya selama penelitian.
3. Lucia Wiwid Wijayanti, M.Si. selaku Dosen Pembimbing Pendamping atas bimbingan, dukungan, serta pengarahannya dari awal penelitian hingga penyusunan skripsi ini.
4. Rini Dwiastuti, M.Sc., Apt. selaku Dosen Penguji atas segala masukan dan bimbingan.
viii
8. Segenap dosen yang telah memberikan pengetahuan dan mendukung penulis dalam penyusunan skripsi ini.
9. Mas Bimo, Pak Musrifin, Mas Wagiran, Mas Iswandi, Mas Sigit, Mas Kunto, Mas Ottok, Pak Timbul, Mas Yono, Pak Parjiman, Mas Heru dan segenap Satpam terima kasih atas bantuan dan kerja samanya selama penelitian di laboratorium.
10.Pak Bambang, Mas Sigit, Mas Fariz, Mas Jink selaku Laboran Laboratorium Teknologi Farmasi Universitas Gadjah Mada atas bantuan dan kerja sama selama praktikum di laboratorium Universitas Gadjah Mada.
11.Eka Permatasari, Oki Christina dan Reka Sudi, tim seperjuangan atas bantuan dan kerja samanya. Yemima, Septi, Fanny, dan Daniel selaku teman satu bimbingan. Lia Natalia Setiomulyo, I Gusti Ngurah Agung Windra Wartana Putra, Sihendra atas semangat dan bantuan selama penyusunan skripsi.
12.Teman-teman farmasi 2007, baik minat FST 2007, kelas B 2007 yang tidak dapat disebut satu per satu. Serta teman praktikum kelompok B1 Terima kasih atas kebersamaannya selama di farmasi. Sukses selalu bagi kita semua. 13.Teman-teman Kamadhis Satya Dharma, Vidyasena Vihara Vidyaloka dan
ix
x
HALAMAN PERSETUJUAN PEMBIMBING ………. ii
HALAMAN PENGESAHAN ………... iii
HALAMAN PERSEMBAHAN ………. iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS……… PERNYATAAN KEASLIAN KARYA……….... v vi PRAKATA………. ………... vii
DAFTAR ISI ………... x
DAFTAR TABEL ………... xiii
DAFTAR GAMBAR ……….. xiv
DAFTAR LAMPIRAN ………... xv
INTISARI ……… xvi
ABSTRACT ……….. xvii
BAB I. PENGANTAR ……….... 1
A.Latar Belakang ………... 1
1. Perumusan masalah ………... 4
2. Keaslian penelitian ………... 4
3. Manfaat penelitian ………... 4
B.Tujuan Penelitian ………... 5
xi
1. Pengertian dispersi padat……….………….… 2. Mekanisme peningkatan disolusi………..
9
BAB III. METODE PENELITIAN ……… 19
A.Jenis dan Rancangan Penelitian ………... 19
B.Variabel Penelitian ………... 19
C.Definisi Operasional ………... 19
D.Bahan Penelitian ………... 20
E.Alat Penelitian ………... 21
F. Tata Cara Penelitian ………... 21
xii
G.Analisis Hasil ………... 25
BAB IV. PEMBAHASAN ……….. 27
A.Pembuatan Dispersi Padat Ekstrak Rimpang Kunyit- PVP K-25….... 27 B.Pembuatan Campuran Fisik………... 29 C.Penetapan Panjang Gelombang Maksimum Kurkumin………. 29 D.Pembuatan Kurva Baku Kurkumin……….……
E.Validasi Metode ……….…..
F. Uji Disolusi………...………..
G.Pengukuran Kadar Kurkumin……….
31 32 36 37 BAB V. KESIMPULAN DAN SARAN ……….
A. Kesimpulan……….
B. Saran………..
xiii
Tabel II. Parameter analitik………... 15
Tabel III. Nilai recovery ………... 16
Tabel IV. Kriteria presisi………... 16
Tabel V. Level dan kisaran untuk linearitas... 17
Tabel VI. Tabel VII. Tabel VIII. Proporsi drug load ……... Formula pembuatan dispersi padat………... Penentuan panjang gelombang maksimum... 22 28 31 Tabel IX. Konsentrasi kurva baku VS absorbansi ………... 32
Tabel X.
Hasil Korelasi spearman ………...
xiv
Gambar 2. Kurkumin ………..……... 7
Gambar 3. Hasil degradasi kurkumin dalam larutan...……..………. 7
Gambar 4. Struktur PVP ………...………... 8
Gambar 5. Spray dryer ………... 11
Gambar 6. Skema kerja Spektrofometer vis……… 13
Gambar 7. Grafik kurva baku ... 33
Gambar 8.
Gamabar 9.
Grafik drug load 0,6%...
Grafik drug load 1%... 39
40
Gambar 10.
Gambar 11.
Gambar 12.
Grafik drug load 2%...
Grafik drug load 0,6, 1, dan 2%...
Grafik Regresi Linier………. 41
42
xv
Lampiran 2. Pernyataan Jaminan Keaslian Bahan Kurkumin Standar Hasil
Sintesis………... 51
Lampiran 3. Pembuatan kurva baku kurkumin ... 52
Lampiran 4. Data orientasi PVP K-25……... 54
Lampiran 5. Perhitungan penimbangan dispersi padat dan campuran fisik………... 56
Lampiran 6. Data persen kurkumin terdisolusi dispersi padat dan campuran fisik……… 63
Lampiran 7. Grafik proporsi drug load 0,66, 1, 2%... 69
Lampiran 8. Data Normalitas, SPSS, Spearman……… 71
Lampiran 9. Scan panjang gelombang makmums... 81
xvi
kelarutaannya kurkumin memiliki kelarutan yang rendah pada air karena nilai log P yang kecil yaitu 2,56, hal ini menyebabkan bioavaibilitas kurkumin menjadi rendah.
Penelitian ini bertujuan untuk melihat pengaruh proporsi drug load terhadap disolusi kurkumin. Salah satu cara yang dipilih untuk meningkatkan disolusi kurkumin adalah dengan dispersi padat amorphous. Pembuatan dispersi padat isolat ekstrak rimpang kunyit (Curcume domestica C-95)-PVP K-25 dilakukan menggunakan metode spray drying. Penambahan pembawa, yaitu PVP K-25 dengan isolat ekstrak rimpang kunyit (Curcume domestica C-95) dibuat dengan proporsi drug load 0,6, 1, 2%. Hasil dispersi padat kemudian diuji disolusi kemudian ditetapkan kadar kurkuminnya menggunakan Spektrofotometer Vis.
Dari hasil diperoleh bahwa dispersi padat lebih dapat meningkatkan disolusi kurkumin secara signifikan dibandingkan dengan campuran fisik. Secara statistik dinyatakan bahwa tidak ada korelasi yang bermakna antara proporsi drug
load dengan disolusi kurkumin dari nilai p, yaitu 0,258.
Kata Kunci : isolat ekstrak rimpang kunyit, PVP K-25, dispersi padat, spray
xvii
solubility in water due to the small value of log P is 2.56, this causes bioavaibility curcumin is low.
This study aims to look at the effect of the proportion of drug load on the dissolution of curcumin. One way is chosen to increase the dissolution of curcumin is the solid amorphous dispersion. Preparation of solid dispersion isolates of turmeric extract (Curcuma domestica C-95)-PVP K-25 carried out using spray drying method. The addition of carrier, PVP K-25 with isolates of turmeric extract (Curcume domestica C-95) made with the proportion of drug load 0.6, 1, 2%. The results are then tested dissolution of solid dispersion and then set levels curcumin using Vis spectrophotometer.
From the results obtained that the more solid dispersion can increase the dissolution of curcumin significantly compared with physical mixtures. The statistics revealed that there was no significant correlation between the proportion of drug-loaded with curcumin dissolution of p values, namely 0.258.
1
BAB I
PENDAHULUAN
A. Latar Belakang
Kunyit merupakan rimpang berbentuk bulat panjang dan
bercabang-cabang. Kunyit tumbuh dengan baik di tanah yang tata pengairannya baik, curah
hujan 2.000 mm sampai 4.000 mm tiap tahun dan di tempat yang sedikit
terlindung. Tapi untuk menghasilkan rimpang yang lebih besar diperlukan tempat
yang lebih terbuka (Riwan, 2008).
Kunyit merupakan jenis temu-temuan yang mengandung senyawa kimia
yaitu minyak atsiri (mengandung senyawa-senyawa kimia seskuiterpen alkohol,
turmeron dan zingiberen) dan kurkuminoid (mengandung senyawa kurkumin dan
turunannya berwarna kuning yang meliputi desmetoksikurkumin dan
bisdesmetoksikurkumin) (Riwan,2008).
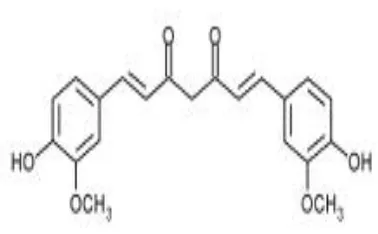
Kurkumin (1,7-bis-(4-hydroxy-3-methoxyphenyl)-1,6-heptadiene
-3,5-dione)adalah senyawa turunan fenolik dari hasil isolasi rimpang tanaman kunyit
(Curcuma longa) (Prasetyo, 2010) dan banyak digunakan sebagai fitokontituen
pada industri makanan (Paradkar, Ambike, Jadhav, dan Mahadik, 2003).
Kurkumin juga memiliki efek farmakologi sebagai anti inflamasi, anti mikrobial,
dan antikanker (Kaewnopparat, Kaewnopparat, Jangwang, Maneenaun,
Gambar 1. Struktur Kurkumin (Anonim, 2010)
Kurkumin merupakan zat warna kuning utama yang terdapat dalam
rhizoma Curcumae longa L. atau Curcuma domestica Val., yang lebih dikenal
dengan nama kunyit. Kurkumin beserta turunannya demetoksinya yaitu demetoksi
kurkumin dan bis-demetoksi kurkumin dikenal dengan nama kurkuminoid
(Martono , 1996).
Dalam hal kelarutaannya kurkumin memiliki kelarutan yang rendah pada
air karena nilai log P yang kecil, yaitu 2,56, hal ini menyebabkan bioavaibilitas
kurkumin menjadi rendah. Permasalahan bioavaibilitas yang timbul sering
dikaitkan dengan disolusi kurkumin yang rendah, dan kurkumin praktis tidak larut
dalam air.
Cara-cara yang digunakan untuk meningkatkan kelarutan kurkumin
adalah dengan membuatnya menjadi nanopartikel, pembentukan garam,
kompeksisasi dengan polimer, dan dengan membuat dispersi padat. Peningkatan
laju disolusi merupakan salah satu upaya yang dapat dilakukan untuk
memperbaiki permasalahan bioavaibilitas.
Salah satu cara yang dipilih untuk meningkatkan disolusi adalah dengan
dispersi padat amorphous. Dispersi padat amorphous dapat meningkatkan laju
padat terdiri dari pembawa hidrofilik dimana obat terdispersi secara molekular
atau dalam ukuran partikel yang kecil (Srinarong, Kouwen, Visser, Hinrichs, dan
Frijlink, 2009). Selain itu, ketika pembawa terdispersi secara molekular, bentuk
kristal dalam larutan menjadi bentuk amorphous sehingga air (H2
Polimer hidrofilik juga sering digunakan sebagai pembawa dalam
dispersi padat. Salah satu polimer yang paling sering digunakan adalah PVP
karena PVP dapat meningkatkan kelarutan dan disolusi dari obat yang
kelarutannya rendah (Kaewnopparat, dkk, 2009). Selain itu, PVP dapat
berinteraksi dengan banyak senyawa lipofilik, khususnya dalam dispersi padat.
Oleh karena itu, dispersi padat menunjukan interaksi seperti ikatan hidrogen
molekular antara kurkumin dengan PVP. Interaksi ini menyebabkan perubahan
struktur kristal kurkumin menjadi bentuk amorphous (Kaewnopparat, dkk, 2009). O) dapat
terjebak pada bentuk amorphous sehingga dapat meningkatkan kelarutannya
dalam air.
Polyvinylpirrolidone mempunyai nama lain, yaitu povidone. PVP yang
digunakan dalam penelitian terdapat banyak grade, yaitu PVP K-12, PVP K-17,
PVP K-25, PVP K-30, PVP K-90. Nilai K pada PVP menunjukkan nilai
karakterisasi dari berat molekulnya. Dalam penelitian ini yang digunakan adalah
PVP K-25 dengan berat molekul, yaitu 28000-34000 (Folttmann dan Quadir,
2008).
Dalam pembuatan dispersi padat, polimer hidrofilik yaitu PVP K-25 dan
serbuk kunyit didispersikan berdasarkan proporsi drug load. Peningkatan proporsi
laju disolusi. Hal ini menandakan kristalisasi obat yang disebabkan karena
terjadinya supersaturasi (Srinarong, dkk, 2009).
1. Perumusan masalah
Berdasarkan latar belakang diatas, masalah yang muncul adalah sebagai
berikut : Bagaimana pengaruh proporsi drug load terhadap disolusi dispersi padat
spray dried isolat ekstrak rimpang kunyit (Curcumae domecticae C-95)-PVP
K-25?
2. Keaslian penelitian
Sejauh yang penulis tahu sudah ada penelitian mengenai disolusi dispersi
padat kurkumin-PVP K-30 dengan judul Increase Solubility, Dissolution and
Physicochemical Studies of Curcumin-PVP K-30 Solid Disperse, Characterization
of Curcumin-PVP Solid Dispersion Obtained by Spray Drying,dll namun sejauh
penulis tahu belum ada penelitian mengenai pengaruh proporsi drug load terhadap
laju disolusi dispersi padat spray dried ekstrak rimpang kunyit (Curcumae
domecticae Rhizome)-PVP K-25.
3. Manfaat Penelitian
a. Manfaat teoritis
b.
. Penelitian diharapkan dapat menambah pengetahuan
yang baru mengenai kurkumin dan metode dispersi padat.
Manfaat praktis.
c.
Penelitian ini diharapkan dapat memberikan
pengetahuan mengenai pembuatan dispersi padat kurkumin dengan
menggunakan metode spray drying.
Manfaat metodologis. Penelitian ini diharapkan dapat menambah
sehingga dapat diaplikasikan dalam pengobatan menggunakan bahan
alam lipofilik.
B. Tujuan Penelitian
Penelitian ini dilakukan untuk mengetahui pengaruh proporsi drug load
terhadap laju disolusi dispersi padat spray dried isolate ekstrak rimpang kunyit
6
A. Ekstrak Rimpang Kunyit (Curcuma domestica Rhizome )
Kunyit merupakan rimpang berbentuk bulat panjang dan bercabang-cabang.
Kunyit tumbuh dengan baik di tanah yang tata pengairannya baik, curah hujan 2.000
mm sampai 4.000 mm tiap tahun dan di tempat yang sedikit terlindung. Tapi untuk
menghasilkan rimpang yang lebih besar diperlukan tempat yang lebih terbuka
(Riwan, 2008).
Kunyit merupakan jenis temu-temuan yang mengandung senyawa kimia
yaitu minyak atsiri (mengandung senyawa-senyawa kimia seskuiterpen alkohol,
turmeron dan zingiberen) dan kurkuminoid (mengandung senyawa kurkumin dan
turunannya berwarna kuning yang meliputi desmetoksikurkumin dan
bisdesmetoksikurkumin) (Riwan,2008).
Kurkumin adalah senyawa yang banyak digunakan sebagai fitokonstituen
pada industri makanan dan diperoleh dari ekstrak rimpang kunyit (Curcuma longa)
(Paradkar dkk., 2003). Selain itu, kurkumin memiliki efek farmakologi sebagai, anti
inflamasi, anti mikrobial, dan antikanker (Kaewnopparat, dkk., 2009).
Kurkumin (1,7-bis-(4-hydroxy-3-methoxyphenyl)-1,6-heptadiene-3,5-dione)
longa
Gambar 2. Kurkumin (Anonim, 2010)
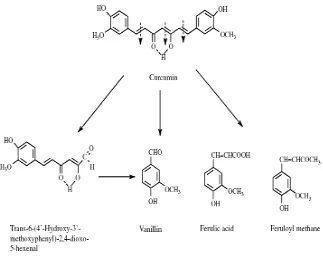
Kurkumin memiliki stabilitas yang baik pada pH asam, sedangkan pada pH
basa, kurkumin mudah mengalami dekomposisi atau degradasi (Tonnesen dan
Karlsen , 1985, Wang dkk., 1997).
). Senyawa tersebut memiliki dua gugus vinilguaiacol (karbonil tak jenuh) yang
saling dihubungkan dengan rantai alfa beta diketon (Prasetyo, 2010).
B. Polyvinylpyrrolidone K-25
Polyninylpyrrolidone (PVP) K-25 merupakan salah satu polimer yang
digunakan dalam pembuatan dispersi padat (Sutriyo, dkk, 2005). PVP dalam bentuk
polimer mempunyai rumus molekul ( C6H9
Gambar 4. Struktur PVP (Folttmann dan Quadir, 2008).
Polyvinylpirrolidone berupa serbuk putih atau putih kekuningan, berbau
lemah atau tidak berbau, higroskopik, mudah larut dalam air, etanol 95% P, dan
kloroform P, tidak larut dalam eter P. Bobot molekul PVP antara 10.000 hingga
700.000 (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1979).
PVP mempunyai nama lain, yaitu povidone. PVP yang digunakan dalam
penelitian terdapat banyak grade, yaitu PVP 12, PVP 17, PVP 25, PVP
K-30, PVP K-90. Nilai K pada PVP menunjukkan nilai karakterisasi dari berat
molekulnya.
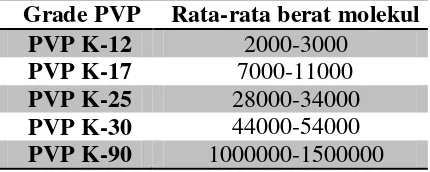
Tabel I. Grade PVP dan Berat molekul PVP (Foltmann dan Quadir, 2008) NO).
Grade PVP Rata-rata berat molekul
PVP K-12 2000-3000
PVP K-17 7000-11000
PVP K-25 28000-34000
PVP K-30 44000-54000
C. Dispersi Padat
1. Pengertian dispersi padat
Dispersi padat merupakan salah satu metode untuk meningkatkan kelarutan
dan bioavaibilitas dari obat yang memiliki kelarutan yang rendah dalam air (Li, dkk.,
2009). Dispersi padat merupakan dispersi dari satu atau lebih bahan aktif dalam
pembawa inert atau matriks pada keadaan padat ( Sutriyo, dkk., 2005). Pembuatan
dispersi padat dapat dilakukan dengan beberapa metode, antara lain: metode
peleburan (melting method), metode pelarutan (solvent method), dan metode
campuran (melting-solventmethod) (Chiou, dkk., 1971).
2. Mekanisme peningkatan disolusi
Dispersi padat amorphous dapat meningkatkan laju disolusi dari obat yang
memiliki kelarutan yang rendah. Secara umum dispersi padat terdiri dari pembawa
hidrofilik dimana obat terdispersi secara molekular atau dalam ukuran partikel yang
kecil (Srinarong, dkk., 2009).
Bila dispersi padat kontak dengan air, pembawa akan terlarut, dan obat
dilepaskan dengan ukuran partikel yang kecil (partikel koloidal). Oleh karena terjadi
peningkatan luas permukaan partikel obat, laju disolusi dan bioavailabilitasnya juga
mengalami peningkatan (Chaudhari, 2006).
Peningkatan laju disolusi dari dispersi padat menggunakan empat macam
a) Meningkatkan kemampuan pembasahan dari obat dengan kontak
langsung antara obat dengan matriks hidrofilik,
b) konsentrasi saturasi pada partikel kecil lebih besar dibandingkan pada
partikel besar,
c) meningkatkan luas permukaan, dan
d) energi yang dimiliki oleh obat dalam bentuk amorphous lebih tinggi
dibanding dengan bentuk kristalin (Waard, Hinrichs, Visser, Bologna,
dan Frijlink, 2007).
D. Spray Drying
1. Definisi
Spray drying adalah salah satu bentuk pengeringan yang tersedia untuk
mengubah cairan, bubur atau pasta viskositas rendah ke (bubuk bebas mengalir)
padat kering dalam satu operasi unit (Traub, 2008).
Metode pengeringan spray drying merupakan metode pengeringan yang
paling banyak digunakan dalam industri terutama industri makanan. Metode ini
mampu menghasilkan produk dalam bentuk bubuk atau serbuk (Rohman, 2008).
2. spray dryer
Cara kerja spray dryer adalah sebagai berikut yaitu pertama-tama seluruh
dengan cara diuapkan menggunakan atomizer. Air dari bahan yang telah berbentuk
tetesan-tetesan tersebut kemudian di kontakan dengan udara panas. Peristiwa
pengontakkan ini menyebabkan air dalam bentuk tetesan-tetesan tersebut mengering
dan berubah menjadi serbuk. Selanjutnya proses pemisahan antara uap panas dengan
serbuk dilakukan dengan cyclone atau penyaring. Setelah di pisahkan, serbuk
kemudian kembali diturunkan suhunya sesuai dengan kebutuhan produksi (Rohman,
2008).
Gambar 5. Spray dryer (Anonim, 2010)
E. Uji Disolusi
1. Definisi
Disolusi didefinisikan sebagai proses dimana suatu zat padat masuk ke
dalam pelarut menghasilkan suatu larutan. Secara sederhana, disolusi adalah proses
dimana zat padat melarut. Secara prinsip disolusi dikendalikan oleh afinitas antara zat
2. Metode uji disolusi
Beberapa metode pengujian disolusi yaitu rotating basket method, rotating
paddle method, reciprocating cylinder,flow-throught cell, paddle over disk (Troy,
2005). Selain itu cara melakukan uji disolusi dapat dilakukan dengan banyak metode
antara lain sebagai berikut.
a. Metode Wagner
Metode ini dapat menghitung tetapan kecepatan pelarutan (k) dengan
berdasarkan pada asumsi bahwa kondisi percobaan dalam keadaan sink, proses
pelarutan mengikuti orde satu, luas permukaan spesifik turun secara eksponensial
terhadap waktu.
b. Metode klasik
Metode ini menunjukkan jumlah zat aktif yang terlarut pada waktu t, yang
kemudian dikenal dengan T20, T50, T90 dan sebagainya. Metode ini hanya
menyebutkan satu titik saja, sehingga proses yang terjadi di luar (sebelum dan
sesudah) titik tersebut tidak diketahui. Titik tersebut menyatakan jumlah zat aktif
yang terlarut pada waktu tertentu (Hadi, 2007). Misalnya bisa dilihat nilai T80,
dimana itu menunjukkan waktu yang diperlukan untuk melarutkan 80% zat aktif
(Waard, dkk., 2007).
c. Jumlah zat aktif yang melarut pada waktu tertentu, misalnya C30 adalah dalam
waktu 30 menit zat aktif yang melarut sebanyak x mg atau x mg/ml (Shargel dan
F. Spektrofotometri UV-Vis
Spektrofotometer UV-Vis adalah instrumentasi analisis yang bermanfaat
untuk penentuan konsentrasi senyawa- senyawa yang dapat menyerap radiasi pada
daerah ultraviolet (200–400 nm) atau pada daerah sinar tampak (400-800 nm). Prinsip
penentuan Spektrofotometer UV-Vis adalah aplikasi dari hukum Lambert-Beer,
yaitu:
A= - log T = -log It / Io = ε . b. C
Dimana : A = Absorbansi dari sample yang diukur
T = Transmintasi
It= Intensitas sinar yang masuk
Io= Intensitas sinar yang diteruskan
ε = Koefisien ekstingsi
b= Tebal kuvet yang digunakan
C =Konsentrasi dari sampel (Sastrohamidjojo, 1991).
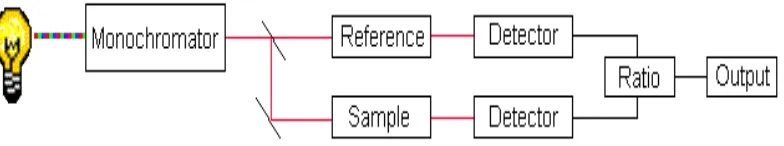
Skema kerja spektrofotometer UV-Vis, yaitu:
Gambar 6. Skema Kerja Spektrofotometer UV- Vis (Anonim, 2010).
Komponen- komponen yang digunakan dalam mengukur absorpsi radiasi uv atau vis
a) Sumber cahaya (UV and visible),
b) selektor panjang gelombang (monochromator),
c) wadah sample,
d) detektor, dan
e) signal processor and readout (Anonim, 2010).
G. Validasi Metode Analisis
Validasi metode analisis merupakan serangkaian prosedur yang digunakan
untuk membuktikan apakah suatu metode analisis yang kita gunakan tersebut taat
secara asas dan memberikan hasil yang sesuai dengan yang diharapkan dengan
akurasi dan presisi yang memadai (Mulja dan Suharman, 1995).
Menurut The United States Pharmacopeia 28, suatu metode atau prosedur
analisis dibagi menjadi empat kategori, yaitu :
1. Kategori I
2.
. Mencakup prosedur analisis kuantitatif, untuk menetapkan kadar
komponen utama bahan obat atau zat aktif dalam sediaan farmasi.
Kategori II
3.
. Mencakup prosedur analisis kualitatif dan kuantitatif yang digunakan
untuk menganalisis impurities ataupun degradation compounds dalam sediaan
farmasi.
Kategori III. Mencakup prosedur analisis yang digunakan untuk menentukan
karakteristik penampilan suatu sediaan farmasi, misalnya disolusi atau pelepasan
4. Kategori IV.
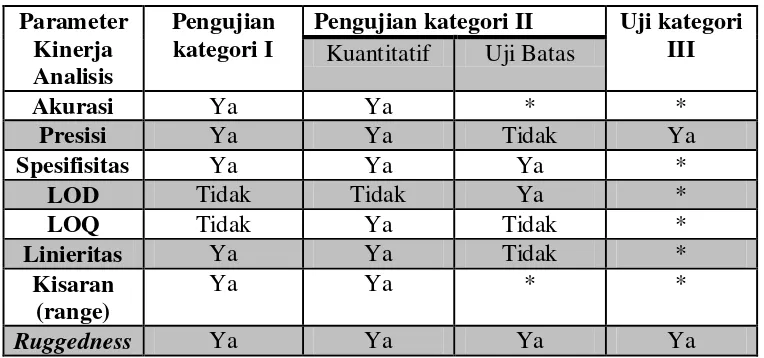
Tabel II. Parameter Analitik (Rohman, 2009)
Metode analitik yang digunakan untuk mengidentifikasi sediaan
farmasi.
Pengujian kategori II Uji kategori III
Kuantitatif Uji Batas
Akurasi Ya Ya * *
*mungkin dibutuhkan, tergantung pada uji spesifiknya
Parameter-parameter yang digunakan dalam validitas metode analisis
meliputi:
1. Akurasi
Akurasi atau kecermatan adalah ukuran yang menunjukkan derajat
kedekatan hasil analis dengan kadar analit yang sebenarnya. Akurasi dinyatakan
sebagai persen peroleh kembali (recovery) analit yang ditambahkan (Harmita, 2004).
Menurut Anonim (2004) rentang kesalahan yang diijinkan pada setiap
Tabel III. Nilai recovery (Guideline, 2004)
Presisi atau keseksamaan adalah ukuran yang menunjukkan derajat
kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari
rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil
dari campuran yang homogen (Harmita, 2004). Presisi biasanya dinyatakan dalam
koefisien variasi (CV). Suatu metode dinyatakan memiliki presisi yang baik apabila
memiliki CV < 2% tetapi kriteria ini fleksibel tergantung dari kondisi analit yang
diperiksa, jumlah sampel dan kondisi laboratorium. Berikut ketentuan nilai CV yang
dapat diterima (Harmita, 2004).
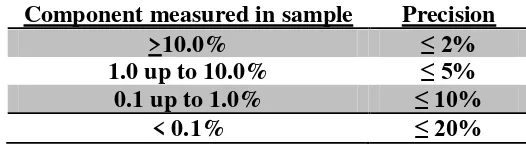
Tabel IV. Kriteria nilai presisi yang diijinkan (Guideline, 2004)
Component measured in sample Precision
>10.0% ≤ 2%
1.0 up to 10.0% ≤ 5%
0.1 up to 1.0% ≤ 10%
< 0.1% ≤ 20%
3. Linieritas
Linieritas merupakan kemampuan suatu metode memperoleh hasil- hasil uji
diberikan. Linieritas suatu metode merupakan ukuran seberapa baik kurva kalibrasi
yang menghubungkan antara respon ( y) dengan konsentrasi (x).
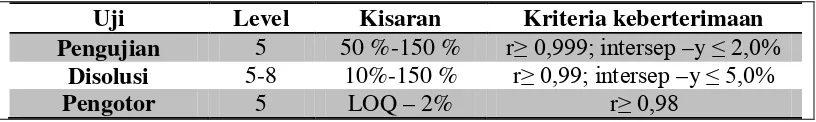
Tabel V. Level dan kisaran untuk menentukan linieritas (Rohman, 2009)
Uji Level Kisaran Kriteria keberterimaan
Pengujian 5 50 %-150 % r≥ 0,999; intersep –y ≤ 2,0%
Disolusi 5-8 10%-150 % r≥ 0,99; intersep –y ≤ 5,0%
Pengotor 5 LOQ – 2% r≥ 0,98
4. Spesifisitas
Spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat
tertentu saja secara cermat dan seksama dengan adanya komponen lain yang mungkin
ada dalam matriks sampel. Selektivitas metode ditentukan dengan membandingkan
hasil analisis sampel yang mengandung cemaran, hasil urai, senyawa sejenis,
senyawa asing lainnya atau pembawa plasebo dengan hasil analisis sampel tanpa
penambahan bahan-bahan tadi. Penyimpangan hasil merupakan selisih dari hasil uji
keduanya (Harmita, 2004).
H. Landasan Teori
Kunyit merupakan jenis temu-temuan yang mengandung senyawa kimia,
yaitu minyak atsiri (mengandung senyawa-senyawa kimia seskuiterpen alkohol,
turmeron dan zingiberen) dan kurkuminoid (mengandung senyawa kurkumin dan
turunannya berwarna kuning yang meliputi desmetoksikurkumin dan
Kurkumin merupakan senyawa polifenol berwarna kuning yang diperoleh
dari ekstrak rimpang kunyit (Curcuma longa), memiliki efek farmakologi sebagai
antioksidan, anti inflamasi, anti mikrobial, anti HIV, dan antikanker. Selain itu,
kurkumin juga banyak digunakan untuk penemuan obat baru.
Namun permasalahannya adalah kurkumin memiliki kelarutan yang rendah
pada air karena nilai log P yang kecil, yaitu 2,56. Oleh karena itu, menyebabkan nilai
bioavaibilitas kurkumin menjadi rendah. Salah satu cara untuk meningkatkan
kelarutan kurkumin adalah dengan mengubahnya menjadi dispersi padat.
Dispersi padat amorphous dapat meningkatkan laju disolusi dari obat yang
memiliki kelarutan yang rendah. Secara umum dispersi padat terdiri dari pembawa
hidrofilik dimana obat terdispersi secara molekular atau dalam ukuran partikel yang
kecil. Selain itu ketika pembawa terdispersi secara molekular, bentuk kristal dalam
larutan menjadi bentuk amorphous sehingga dapat meningkatkan kelarutannya
Dispersi padat dari kurkumin dibuat dengan metode Spray drying, yang dimana
menggunakan zat pembawa yaitu, PVP K-25 untuk meningkatkan laju disolusi dari
kurkumin.
I. Hipotesis
Proporsi drug load dispersi padat spray dried isolat ekstrak rimpang kunyit
19
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk dalam penelitian eksperimental dengan melakukan
percobaan dan tidak adanya manipulasi data yang diperoleh. Peneliti menambahkan
zat pembawa saat pembuatan dispersi padat untuk meningkatkan kecepatan disolusi
dari kurkumin.
B. Variabel Penelitian
1. Variabel bebas pada penelitian ini adalah proporsi drug load
2. Variabel tergantung pada penelitian ini adalah persen kurkumin terdisolusi.
3. Variabel pengacau
a. Variabel pengacau terkendali pada penelitian ini adalah cara penyimpanan
kurkumin (intensitas cahaya, dan suhu).
b. Variabel pengacau tak terkendali pada penelitian ini adalah suhu ruangan.
C. Definisi Operasional
1. Kurkumin (1,7-bis-(4-hydroxy-3-methoxyphenyl)-1,6-heptadiene-3,5-dione)
adalah senyawa turunan fenolik dari hasil isolasi rimpang tanaman kunyit
2. Polyninylpyrrolidone (PVP) merupakan serbuk berwarna putih kekuningan yang
bersifat higroskopis, memiliki bau khas samar, larut dalam air dan pelarut organik
lainnya, bebas larut dalam etanol dan dalam metanol, sedikit larut dalam aseton
3. Dispersi padat merupakan salah satu metode untuk meningkatkan kelarutan dan
bioavaibilitas dari obat yang memiliki kelarutan yang rendah dalam air. Dispersi
padat bisa dibuat dengan banyak cara salah satunya spray drying, yaitu salah satu
bentuk pengeringan yang tersedia untuk mengubah cairan, bubur atau pasta
viskositas rendah ke (bubuk bebas mengalir) padat kering.
.
4. Disolusi didefinisikan sebagai proses dimana suatu zat padat masuk ke dalam
pelarut menghasilkan suatu larutan, bila dispersi padat kontak dengan air maka
pembawa akan terlarut, dan obat dilepaskan dengan ukuran yang lebih kecil
(partikel koloidal), sehingga laju disolusi dan bioavailabilitasnya juga mengalami
peningkatan.
5. Spektrofotometer visibel merupakan instrument yang digunakan untuk mengukur
disolusi kurkumin.
D. Bahan – bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah kurkumin standar
(pemberian eksklusif dari prof. Dr. Sudibyo Martono, M.S.,Apt.) , serbuk ekstrak
rimpang kunyit (dari PT Phytochemindo Reksa) , PVP K-25 (PT Brataco), etanol
methanol p.a (E. Merck), cangkang kapsul keras ukuran 00 (PT Brataco), Natrium
klorida P, asam klorida (HCl) pekat.
E. Alat – alat Penelitian
Alat yang digunakan dalam penelitian ini adalah : Alat- alat gelas
(Pyrex-Germany), timbangan analitik (OHAUS Carat Series), spray dryer
(LabPlant-London), spektrofotometer UV-Vis (Perkin Elmer), alat uji disolusi (Sotax), stirer
magnetic (Labinco BV-Netherlands), ph indikator universal (Merck), dan desikator
F. Tata Cara Penelitian
1. Pembuatan dispersi padat
Untuk dispersi padat, kurkumin dilarutkan dengan etanol. PVP dilarutkan dengan
aquades. Larutan kurkumin dicampur dengan larutan PVP K-25 dengan proporsi
drug load yaitu 2 %, 1 %, dan 0,6 % . Pelarut dihilangkan dengan teknik I
dengan operating parameter sebagai berikut: suhu inlet, 110o C; suhu outlet ±70 o
Tabel VI. Proporsi drug load
C; feed rate 4 ml/ min.
PVP K-25 (mg)
Kurkumin ( mg) Drug load
2000 mg 40 mg 1,96 % ≈ 2%
4000 mg 40 mg 0,99 % ≈ 1%
2. Pembuatan serbuk campuran fisik
Campuran fisik disiapkan dengan mencampur secara manual x mg kurkumin dan
PVP K-25 dengan proporsi drug load 2 %, 1%, dan 0,6 % . Homogenkan
dengan mengaduk di atas mortar kemudiaan diayak.
3. Uji disolusi
Uji disolusi dilakukan terhadap dispersi padat, dan campuran fisik dengan
menggunakan alat uji disolusi. Medium disolusi terdiri dari 900 ml cairan
lambung buatan tanpa pepsin. Pembuatan medium disolusi mengacu pada
Farmakope IV. Kecepatan paddle diatur 50±0,1 rpm dan temperatur pengujian
37 ±0,5°C. Jumlah tiap sampel setara dengan 40 mg kurkumin. Setiap 5, 10, 15,
20, 30, 45 dan 60 menit, cuplikan sebanyak 5 ml diambil dan disaring, medium
disolusi diganti dengan 5 ml medium disolusi yang baru setelah pengambilan
cuplikan. Cuplikan diukur kadar kurkuminnya dengan Spektrofotometer visible pada λ 421,6 nm untuk cairan lambung buatan tanpa pepsin. Konsentrasi
kurkumin dihitung dan dinyatakan sebagai persentase kurkumin terlarut dari
jumlah rata-rata tiga kali replikasi pengukuran.
4. Validasi metode
a. Pembuatan larutan stok kurkumin
Sebanyak 10,0 mg serbuk kurkumin ditimbang seksama, masukkan ke dalam
b. Pembuatan larutan intermediet
Larutan stok kurkumin dipipet sebanyak 1,0 ml, masukkan ke dalam labu
ukur 10,0 ml. Encerkan dengan metanol p.a hingga tanda. Larutan
intermediet dibuat sebanyak 3 kali.
c. Penentuan panjang gelombang maksimum
Mengambil 0,4; 0,8; dan 1,2 ml dari larutan intermediet ke dalam labu 10
ml. Encerkan dengan methanol hingga tanda. Pengukuran λ maks dilakukan pada λ 300 – 600 nm sebanyak tiga kali. Melakukan hal yang sama pada
intermediate II dan intermediet III.panjang gelombang maksimum dilihat dari
profil kurvanya dan dilihat yang memberikan serapan maksimum.
d. Pembuatan kurva baku
Larutan intermediet diambil sebanyak 0,4 ml; 0,6 ml; 0,8 ml; 1,0 ml dan 1,2
ml, masukkan ke dalam labu ukur 10,0 ml. Encerkan dengan metanol p.a
hingga tanda. Larutan tersebut diukur serapannya pada panjang gelombang
maksimum. Replikasi sebanyak tiga kali. Data yang diperoleh dihitung
meggunakan regresi linier sehingga didapat persamaan kurva baku kurkumin.
e. Penetapan parameter akurasi (recovery)
Larutan intermediet diambil sebanyak 0,4 ml; 0,6 ml; 0,8 ml; 1,0 ml dan 1,2
ml, dimasukkan ke dalam labu ukur 10,0 ml. Diencerkan dengan metanol p.a
hingga tanda. Larutan intermediet diukur serapannya pada panjang
gelombang maksimum. Replikasi dilakukan sebanyak tiga kali. Menghitung
% recovery = kadar terukur
kadar terhitung x 100% f. Penetapan parameter presisi (koefisien variasi)
Larutan intermediet diambil sebanyak 0,4 ml dan 1,2 ml, masukkan ke dalam
labu ukur 10,0 ml. Encerkan dengan metanol p.a hingga tanda. Larutan
intermediet diukur serapannya pada panjang gelombang maksimum. Replikasi
dilakukan sebanyak 3 kali. Serapan yang diperoleh dimasukkan ke dalam
persamaan kurva baku untuk mengetahui kadar terukur, kemudian hitung
standar deviasi, dengan rumus:
CV = SD x
� x 100%
Keterangan :
SD = standar deviasi
x� = kadar rata-rata
CV = koefisien variasi
g. Penetapan parameter linieritas
Larutan intermediet diambil sebanyak 0,4 ml; 0,6 ml; 0,8 ml; 1,0 ml dan 1,2
ml, masukkan ke dalam labu ukur 10,0 ml. Encerkan dengan metanol p.a
hingga tanda. Larutan intermediet diukur serapannya pada panjang gelombang
maksimum. Replikasi dilakukan sebanyak tiga kali. Hitung nilai linieritas
G. Analisis Hasil
1. Analisis validasi metode
Validasi metode yang digunakan berdasarkan parameter berikut:
a. Akurasi
Akurasi metode analisis biasa disebut juga sebagai recovery dan dihitung
dengan rumus :
% recovery = kadar terukur
kadar terhitung x 100%
Metode digunakan untuk menganalisis bahan obat dengan kadar kurang dari
0,1%, maka rentang recovery yang digunakan yaitu 80-120%.
b. Presisi
Presisi dinyatakan dengan koefisien variasi, dengan rumus:
CV = 𝑆𝑆𝑆𝑆
𝑥𝑥̅ x 100%
Metode ini dikatakan baik bila nilai CV yang diperoleh < 2% makin kecil
nilai CV, presisi metode yang digunakan makin baik.
c. Linieritas
Parameter linieritas dilihat dari nilai koefisien korelasi (r) hasil pengukuran
larutan seri baku kurkumin. Metode dikatakan memiliki linieritas yang baik
2. Analisis statistik penetapan kadar kurkumin terlarut
Data uji disolusi kurkumin dibuat dalam bentuk kurva hubungan antara
jumlah persentase kurkumin terdisolusi terhadap waktu. Kemudian dilakukan
perhitungan statistik korelasi proporsi drug load terhadap waktu 60 menit
27
A. Pembuatan Dispersi Padat Kurkumin
Pembuatan dispersi padat bertujuan untuk meningkatkan disolusi obat yang
mempunyai kelarutan rendah. Dispersi padat kurkumin dibuat untuk meningkatkan
kelarutan kurkumin karena kurkumin memiliki kelarutan yang rendah. Dispersi
dibuat dengan mencampur 350,8772 mg isolat ekstrak rimpang kunyit (Curcuma
domestica C-95) yang dilarutkan dalam 125 ml etanol 70% dengan pembawa, yaitu
PVP K-25 sebanyak 2000, 4000, 6000 mg yang dilarutkan dalam 100 ml aquadest
dengan proporsi drug load seperti pada tabel VII. Campuran keduanya
dihomogenkan menggunakan magnetic stirrer.
Tabel VII. Formula pembuatan dispersi padat
PVP K-25 (mg)
Kurkumin ( mg) Drugload (%)
2000 40 1,96 ≈ 2
4000 40 0,99 ≈ 1
6000 40 0,66
Isolat ekstrak rimpang kunyit (Curcuma domestica C-95) yang digunakan
dalam penelitian didapat dari PT. Phytochemindo Reksa dengan komponen 97,20%
merupakan kurkuminoid yang tertera pada Certificate of Analysis dan dalam
Pembawa yang digunakan dalam pembuatan dispersi padat ini menggunakan PVP
K-25 dengan karakteristik, yaitu serbuk putih kekuningan dan bersifat higroskopik. PVP
K-25 merupakan polimer hidrofilik yang sering digunakan sebagai pembawa dalam
dispersi padat karena PVP K-25 dapat meningkatkan kelarutan dan disolusi dari obat
yang kelarutannya rendah dalam air. Selain itu, PVP K-25 dapat berinteraksi dengan
banyak senyawa lipofilik. Dalam dispersi padat, PVP K-25 menunjukkan interaksi
seperti ikatan hidrogen molekular antara kurkumin dengan PVP K-25. Interaksi ini
menyebabkan perubahan struktur kristal kurkumin menjadi bentuk amorphous
(Kaewnopparat, dkk, 2009).
Formula dibuat dengan tiga proporsi drug load, yakni 2, 1, dan 0,66%.
Menurut Srinarong (2009) dengan menurunnya proporsi drug load maka akan terjadi
peningkatan disolusi.
Dispersi padat isolat ekstrak rimpang kunyit (Curcuma domestica C-95)
-PVP K25 dibuat dengan alat spray dryer LabPlantdengan parameter, yaitu suhu inlet
110 o C, suhu exhaust 60oC - 70oC, pump speed 4 ml/menit, nozzle 1 mm. Cara kerja
dari alat Spray Dryer adalah dengan adanya uap panas akan mengubah cairan
campuran antara isolat ekstrak rimpang kunyit (Curcuma domestica C-95) dengan
PVP K-25 menjadi serbuk kering. Serbuk dispersi padat yang diperoleh berupa
serbuk dengan ukuran kecil, berwarna kekuningan, dan higroskopis. Serbuk
kemudian dibungkus dengan aluminium foil dan disimpan selama 24 jam dalam
jam dalam desikator sebelum diuji disolusi. Serbuk dispersi padat yang dihasilkan
kemudian dimasukkan ke dalam kapsul no 00 sesuai dengan perhitungan.
B. Pembuatan Campuran Fisik
Campuran fisik dibuat dengan mencampur homogen secara manual dalam
mortir antara isolat ekstrak rimpang kunyit (Curcuma domestica C-95) dengan PVP
K-25 dari hasil perhitungan hasil dispersi padat yang dimasukkan ke dalam kapsul
dibandingkan dengan jumlah dispersi padat yang dihasilkan, sehingga diperoleh
jumlah pembawa dan serbuk kunyit untuk campuran fisik. Campuran fisik diberi
perlakuan yang sama seperti dispersi padat yaitu dibungkus dibungkus dengan
aluminium foil dan disimpan selama 24 jam dalam desikator, kemudian dimasukkan
ke dalam kapsul No.00 dan disimpan lagi selama 24 jam dalam desikator sebelum
diuji disolusi. Hasil disolusi dari campuran fisik akan dibandingkan dengan dispersi
padat.
C. Penetapan Panjang Gelombang Maksimum Kurkumin
Penetapan panjang gelombang maksimum bertujuan untuk mendapatkan
panjang gelombang serapan maksimum dari kurkumin, sehingga dapat menunjukkan
sensitifitas yang baik serta untuk mendapatkan hasil pengukuran yang baik saat
dilakukan pengukuran ulang menggunakan panjang gelombang maksimum tersebut.
Penetapan panjang gelombang maksimum dilakukan dengan membuat
Tabel VIII. Penentuan panjang gelombang maksimum
mg/ml sebanyak tiga kali. Tiap larutan intermediet diukur menggunakan
spektrofotometer Vis dan dilihat pada panjang gelombang berapa absorbansi
maksimum paling banyak diberikan, yang dijadikan sebagai panjang gelombang
maksimum dari kurkumin dan digunakan untuk pengukuran berikutnya.
Pengukuran Konsentrasi Panjang gelombang
( nm)
Penentuan panjang gelombang maksimum dipilih dari nilai yang paling
sering muncul dari hasil pengukuran. Dari tabel diatas hasil pengukuran didapat
panjang gelombang maksimum kurkumin, yaitu 421,6 nm karena dari hasil
pengukuran panjang gelombang yang paling sering muncul adalah 421,6 nm.
Menurut Kaewnopparat (2009) teori panjang gelombang kurkumin adalah
421,0, nm yang diukur menggunakan spektrofotometer. Dari hasil pengukuran terjadi
pergeseran panjang gelombang untuk kurkumin sebesar 0,6 nm, hasil ini dikatakan
memenuhi syarat karena pergeseran panjang gelombang yang diijinkan adalah
D. Pembuatan Kurva Baku Kurkumin
Pembuatan kurva baku bertujuan untuk memperoleh persamaan regresi linier
yang akan digunakan untuk menghitung kadar kurkumin dalam serbuk dispersi padat.
Pembuatan kurva baku dibuat dari lima konsentrasi, yaitu 1,584.10-3 mg/ml, 2,376.10-3
mg/ml, 3,168.10-3 mg/ml, 3,960.10-3 mg/ml, dan 4,752.10-3
Menurut Rohman (2009) linieritas suatu metode merupakan ukuran
seberapa baik kurva kalibrasi yang menghubungkan antara respon (y) dengan
konsentrasi (x). Linieritas suatu kurva baku menunjukan bahwa kenaikan respon
sebanding dengan kenaikan konsentrasi baku yang digunakan.
mg/ml yang kemudian
diukur dengan spektrofotometer VIS pada λ 421,6 nm. Dilakukan tiga kali replikasi
dari seri kurva baku untuk mendapatkan nilai (r) yang baik yaitu lebih besar dari 0,99.
Tabel IX. Konsentrasi Kurva Baku vs Absorbansi
Dari persamaan kurva baku di atas hanya persamaan I dan III yang
memenuhi kriteria linieritas yang baik. Dari kedua persamaan kurva baku yang
diperoleh dipilih persamaan kurva baku yang paling linier. Menurut Rohman (2009)
untuk uji disolusi kriteria linieritas dengan harga r ≥ 0,99. Persamaan kurva baku
yang dipilih adalah persamaan kurva baku replikasi I, yaitu y = 152,3990 x – 0,017
karena mempunyai nilai r yang paling baik yaitu dengan nilai r = 0,9981. Pemilihan
ini karena nilai r dari replikasi I lebih baik diantara yang lain.
Gambar 7. Grafik kurva baku
E. Validasi metode
Validasi metode merupakan ukuran kesasihan suatu metode yang
digunakan. Validasi yang diuji meliputi linearitas, akurasi dan presisi. Akurasi
menggambarkan apakah suatu metode mengahasilkan nilai pengukuran yang sama
atau mendekati nilai sebenarnya, sedangkan presisi menunjukkan apakah metode
yang digunakan memiliki ketelitian sehingga pada pengulangan pengukuran akan
memghasilkan nilai yang sama. Recovery merupakan parameter untuk akurasi suatu
metode analisis. Berdasarkan perhitungan recovery diperoleh nilai recovery pada
level rendah, tengah maaupun tinggi.
1. Akurasi
Akurasi dibuat dengan mengukur larutan seri baku 1,584.10-3, 3,168.10-3, dan
4,752.10-3
% recovery = kadar terukur
kadar terhitung x 100%
mg/ml sebanyak 3 kali. Kemudian kadarnya dihitung dengan
memasukkan nilai absorbansi ke dalam persamaan kurva baku. Dan
masing-masing seri kurva baku dihitung recovery-nya dengan rumus :
Tabel X. Data perhitungan recovery
Level
Hasil dari perhitungan recovery untuk larutan seri baku 1,584. 10-3 mg/ml,
mg/ml,
Tabel XI. Nilai recovery (Anonim, 2004)
yaitu 98,41%. Menurut Guideline (2004) persamaan recovery suatu metode
analisis adalah 80 – 120% untuk kadar analit 0,1-1%.
% Active/ impurity
Karena sampel yang digunakan adalah sampel dengan kadar kecil yaitu
0,1-1% sehingga batas recovery yang diberikan juga lebih lebar yaitu 80-120%.
Recovery dari ketiga seri baku baik karena masuk dalam rentang recovery yang
diberikan, sehingga bisa dikatakan untuk metode ini memenuhi kriteria validasi
metode bagian akurasi.
2. Presisi
Presisi dihitung dari recovery, presisi yang baik bila nilai CV < 2%.
Menurut Guideline (2004) CV juga bergantung dari kadar analit sampelnya. Pada
pengukuran ini, kadar analit sampel, yaitu >0,1% atau dalam rentang 0,1-1,0%,
maka untuk nilai CV yang diacu adalah <10%.
Tabel XII. Nilai presisi (Anonim, 2004)
Dari ketiga baku nilai CV yang diperoleh larutan seri baku 1,584. 10-3
mg/ml yaitu 7,44%; untuk seri 3,168. 10-3 mg/ml yaitu 5,19% ; dan untuk seri
4,752. 10-3 mg/ml
3. Linearitas
yaitu 1,42%. Ketiga baku masih memenuhi kriteria presisi,
yaitu ≤ 10%, sehingga dapat dikatakan memenuhi validasi bagian presisi.
Linearitas dilakukan dengan mengukur lima larutan seri baku kurkumin
konsentrasi yaitu 1,584. 10-3, 2,376. 10-3 , 3,168. 10-3 , 3,960. 10-3 , dan 4,752. 10-3
Dari kurva baku diperoleh persamaan kurva baku y= 152,3990 x – 0,017,
dengan nilai A = -0,017 ; B = 152,39 dan r = 0,9981. Menurut Rohman (2009)
untuk uji disolusi r > 0,99. Sehingga linearitas dari metode ini dikatakan baik. mg/ml sebanyak 3 kali. Kemudian dibuat persamaaan kurva baku dengan
memasukkan nilai absorbansi vs kadar seri baku, di hitung nilai r. Lalu dipilih
nilai r yang paling baik yang digunakan untuk kurva baku.
4. LOD
LOD merupakan Limit of Detection, dimana ini merupakan kadar terkecil
yang dapat diukur dalam pengukuran kadar. Bila kadar yang akan di ukur berada
di bawah LOD, kadar tersebut tidak dapat terdeteksi. LOD diukur menggunakan
rumus 3 𝑥𝑥𝑆𝑆𝑆𝑆
Tabel XIII. Kurva baku
Dari perhitungan LOD di atas, diketahui bahwa LOD sebesar 2,4649. 10-5 mg/ml.
Jadi, untuk pembuatan dispersi padat dan campuran fisik yang dilakukan, jumlah
kurkumin yang terkandung di dalamnya sudah berada di atas LOD.
F. Uji Disolusi
Uji disolusi dilakukan untuk mengetahui profil disolusi kurkumin antara
dispersi padat dengan campuran fisik. Uji disolusi dilakukan menurut metode
rotating paddle method. Uji disolusi bertujuan untuk melihat pelepasan obat dalam
Konsentrasi ( mg/ml) Absorbansi
1,584. 10-3 mg/ml 0,236 A
2,376. 10-3 mg/ml 0,329 A
3,168. 10-3 mg/ml 0,461 A
3,960. 10-3 mg/ml 0,598 A
tiap menit. Uji disolusi serbuk dispersi padat dan serbuk campuran fisik
menggunakan metode rotating paddle method. Dispersi padat maupun campuran fisik
dimasukkan ke dalam kapsul ukuran 00 dan dilakukan uji pada medium cairan
lambung buatan tanpa pepsin. Menurut Farmakope IV cairan lambung buatan tanpa
pepsin dibuat dengan mencampur 2 g NaCl P dengan 7 mL HCl p.a kemudian di
tambah aquadest hingga 1000 mL. Medium disolusi yang digunakan sebanyak 900
mL dituang ke alat disolusi. Uji disolusi menggunakan metode rotating paddle
method karena diatur pada suhu ±37 o C dan dengan kecepatan 50 rpm. Pengujian
dilakukan selama 3 jam dengan pengambilan cuplikan dilakukan pada menit ke 5, 10,
20, 30, 45, 60, 90, 120, 150, dan 180 menit untuk setiap sampel. Cuplikan kemudian diukur kadarnya dengan Spektrofotometer Vis pada λ 421,6 nm dan dihitung persen
kurkumin yang terdisolusi.
G. Pengukuran Kadar Kurkumin
Pengukuran kadar kurkumin dilakukan dengan menggunakan
Spektrofotometer Visibel. Kadar kurkumin yang terukur kemudian dihitung persen
kurkumin terdisolusi. Dilakukan pengukuran terhadap dispersi padat dan campuran
fisik pada proporsi drug load 2, 1, dan 0,66% dan dilakukan replikasi tiga kali.
Dilakukan perbandingan persen kurkumin terdisolusi antara dispersi padat dengan
Data dari pengujian ditampilkan dalam grafik adalah sebagai berikut.
Gambar 8. Grafik Drug Load 0,66%
Untuk proporsi drug load 0,66% dari grafik terlihat adanya perbedaan
persen kurkumin terdisolusi antara dispersi padat dengan campuran fisik yang
signifikan. Hal ini terlihat dari tidak adanya nilai SD yang berhimpit baik dari 5 menit
hingga 180 menit. Menurut Srinarong (2009) dispersi padat akan memberikan
disolusi yang lebih besar karena dengan dispersi padat mengubah bentuk dari
kristalin menjadi amorphous yang menyebabkan peningkatan laju disolusi.
Dilakukan juga uji statistik antara disolusi dispersi padat dengan campuran
fisik. Uji statistik menggunakan Mann-Whitney karena data berdistribusi tidak
normal, dilihat dari nilai p <0,05. Uji normalitas dilakukan menggunakan
Saphiro-Wilk karena sampel yang diuji jumlahnya kurang dari 50. Dari uji T tidak
berpasangan dan uji diperoleh nilai signifikansi <0,05 maka dapat dikatakan ada
perbedaan yang bermakna antara disolusi dispersi padat dengan campuran fisik.
Gambar 9. Grafik Drug Load 1%
Untuk proporsi drug load 1% dari grafik terlihat adanya perbedaan persen
kurkumin terdisolusi antara dispersi padat dengan campuran fisik yang signifikan.
Hal ini terlihat dari tidak adanya nilai SD yang berhimpit, baik dari 5 menit hingga
180 menit.
Perbedaan disolusi dispersi padat dengan campuran fisik juga dilakukan
dengan statistik untuk melihat perbedaan disolusi dari keduanya . Uji statistik
menggunakan uji Mann-Whitney karena data berdistribusi tidak normal. Uji
normalitas dilakukan menggunakan Saphiro-Wilk. Dari uji Mann-Whitney diperoleh
nilai signifikansi <0,05 maka dapat dikatakan terdapat perbedaan yang bermakna
antara disolusi dispersi padat dengan campuran fisik.
Gambar 10. Grafik Drug Load 2%
Dari grafik diatas juga terlihat adanya perbedaan persen kurkumin
terdisolusi antara dispersi padat dengan campuran fisik pada drug load 2%. Dari
grafik terlihat bahwa dengan dispersi padat dapat meningkatkan persen terdisolusi
yang signifikan dibanding dengan campuran fisik. Hal ini terlihat dari tidak adanya
nilai SD yang berhimpit.
Dilakukan juga uji statistik antara disolusi dispersi padat dengan campuran
fisik. Uji statistik menggunakan uji T tidak berpasangan karena data berdistribusi
normal dilihat dari nilai p>0,05. Uji normalitas dilakukan menggunakan
Saphiro-Wilk. Dari hasil uji T tidak berpasangan diperoleh nilai signifikansi >0,05 maka
dapat dikatakan tidak terdapat perbedaan yang bermakna antara disolusi dispersi
padat dengan campuran fisik pada menit awal disolusi dikarenakan belum semua
kurkumin terdisolusi sempurna pada drug load 2 % di menit awal sehingga antara
dispersi padat maupun campuran fisik memberikan disolusi yang tidak bermakna.
Gambar 11. Grafik Drug Load 0,66%, 1%, dan 2%
Menurut Srinarong (2009) dengan menurunnya proporsi drug load maka
persen disolusi akan meningkat . Hal ini sesuai dengan teori karena dari grafik dapat
dilihat dengan menurunnya proporsi drug load maka persen kurkumin terdisolusi
semakin besar. Untuk proporsi drug load 0,66% tidak menunjukkan persen kurkumin
terdisolusi meningkat secara signifikan dibandingkan dengan drug load 1% karena
kurva berhimpit satu sama lain.
Dilakukan pula uji statistik untuk melihat korelasi antara proporsi drug
load dengan persen kurkumin terdisolusi pada menit tertentu. Waktu yang dipilih
adalah 60 menit untuk melihat ada tidaknya korelasi antara proporsi drug load
dengan persen kurkumin terdisolusi pada waktu 60 menit.
Uji korelasi yang dilakukan menggunakan uji korelasi Spearman karena
distribusi data tidak normal. Menurut Dahlan (2009), data dikatakan berdistribusi
0
normal jika nilai p > 0,05 dan sebaliknya jika p < 0.05 maka data dikatakan
berdistribusi tidak normal. Uji normalitas data menggunakan Shapiro-Wilk karena
sampel yang diuji kurang dari 50.
Tabel XIV. Korelasi Spearman 60 menit
Correlations
proporsidrugloa
d persendisolusi
Spearman's rho proporsidrugload Correlation Coefficient 1,000 -,422
Sig. (2-tailed) . ,258
N 9 9
persendisolusi Correlation Coefficient -,422 1,000
Sig. (2-tailed) ,258 .
N 9 9
Berdasar data di atas terdapat korelasi tidak bermakna antara proporsi drug
load dengan disolusi kurkumin, yang dapat dilihat dari nilai p 0,258. Hal ini terjadi
karena PVP merupakan contoh polisakarida dengan tingkat kelarutan yang tinggi
sehingga dispersi padat yang dihasilkan pun memiliki kelarutan yang tinggi.
Sehingga saat menit ke-60 baik proporsi 0,66%, 1% maupun 2% sudah sebagian
besar terdisolusi.
Nilai koefisien korelasi yang diperoleh adalah -0,422. Nilai negatif
menunjukkan bahwa korelasi antara proporsi drug load dengan persen kurkumin
terdisolusi adalah berbanding terbalik, dimana dengan meningkatnya proporsi drug
Tabel XV. Data ANOVA
Model Summaryb
Model
R R Square
Adjusted R
Square
Std. Error of the
Estimate Durbin-Watson
1 ,598a ,358 ,266 6,90730 1,468
a. Predictors: (Constant), proporsidrugload
b. Dependent Variable: persendisolusi
ANOVA
Model
b
Sum of Squares df Mean Square F Sig.
1 Regression 186,033 1 186,033 3,899 ,089a
Residual 333,975 7 47,711
Total 520,009 8
a. Predictors: (Constant), proporsidrugload
Gambar 12. Regresi linier
Dari regresi linear didapat persamaan yaitu y=-7,721x + 56,89. Persamaan
tersebut memiliki nilai signifikansi pada ANOVA diperoleh nilai 0,089 yang berarti >
0,05 yang menandakan persamaan tersebut tidak layak digunakan untuk meramalkan
pengaruh drug load terhadap disolusi kurkumin. Selain itu nilai adjusted R Square
yang diperoleh 0,266 menunjukan bahwa proporsi drug load mempengaruhi disolusi
sebesar 26,6% dan sisanya 73,4% dipengaruhi faktor lain yang tidak diteliti.
y = -7,721x + 56,89
45
Dispersi padat dapat meningkatkan disolusi kurkumin secara signifikan
dibandingkan dengan campuran fisik bila dibandingkan pada proporsi drug load
yang sama, namun tidak terdapat korelasi yang bermakna antara proporsi drug
load dengan disolusi kurkumin.
B. Saran
1. Pembuatan dispersi padat isolat ekstrak rimpang kunyit (Curcuma domestica
C-95)-PVP K-25 dengan proporsi drug load tidak dapat meningkatan disolusi
kurkumin, sehingga sebagai saran dapat digunakan PVP jenis yang lain.
2. Dapat dilakukan pula pembuatan dispersi padat isolate ekstrak rimpang kunyit
46
Anonim. 2010, Penerapan Nanotechnology Dalam Bidang Formulasi Sediaan Obat,
Anonim , 2010, UV-Vis Absorption Spectroscopy , http://teaching.shu.ac.uk
/hwb/chemistry/tutorials/molspec/uvvisab3.htm, diakses tanggal 21 November 2010.
Banakar, U. V., 1992, Pharmaceutical Dissolution Testing, Marcel Dekker Inc., New York, United States of America, pp. 15-17, 53.
Chan, C.C., Lam, N., Lee, Y.C., Zhang, X., 2004, Analytical Method Validation and Instrument Performance Verification, John Wiley & Sons, Inc., USA,16.
Chiou W.L., Riegelman S, 1971, Pharmaceutical Applications of Solid Dispersion System. J. of Pharm. Sci 60(9), 1281-1302.
Dahlan, M. S., 2009, Statistik untuk Kedokteran dan Kesehatan, Salemba Medika, 60-66, 163-170.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia, jilid III, Departemen Kesehatan Republik Indonesia, Jakarta.
Folttmann dan Quadir, 2008, Polyvinylpirrolidone(PVP)-One of the Most Widely Used Excipient in Pharmaceutical: An Overview, Drug Delivery Technology Vol 8 No 6, pp. 22-27.
Guideline, 2004, Guidelines for the Validation of Analytical Methods Active Constituen, Agriculture and Veterinary Chemical Product, Australian Pesticides & Veterinary Medicines Authority, 1-9.
Hadi, 2007, Spektrofotometri UV/VIS,
20 November 2010.
International Specialty Product , 2010,
Kaewnopparat, N., Kaewnopparat, S., Jangwang, A., and Mannenaun, D., 2009, Increased Solubility, Dissolution and Physicochemical Studies of Curcumin-Polyvinylpyrrolidone K-30 Solid Dispersion, World Academy Of Science, Engineering and technology 55, 229.
Li , D.X., Jang, K.J., Kang, W., Bae, K., Lee, M.H., Oh, Y.K., et al , 2009, Enhanced Solubility and Bioavaibility of Sibutramine Base by Solid Dispersion System with Aqueous Medium, Pharmaceutical Society of Japan, pp. 279.
Martono, S., 1996, Penentuan Kadar Kurkumin secara Kromatografi Lapis Tipis-Densitometri, Buletin ISFI Yogyakarta, Vol.2 No.4.
Mulja, H.M., dan Suharman, 1995, Analisis Instrumental, Airlangga University Press, Surabaya, pp. 102.
Paradkar, A., Ambike, A.A., Jadhav, B.K., dan Mahadik, K.R., 2004, Characterization of curcumin-PVP solid dispersion obtained by spray drying, International Journal of Pharmaceutics 271, 281.
Parinussa, T. M. S. dan Timotius, K. H., 2010, Pengaruh Penambahan Asam Terhadap Aktivitas Antioksidan Kurkumin, BSS, 194(1), 1-6.
Peakchem , 2010, 21 November 2010.
Prasetyo, Y, 2010,
diakses tanggal 16 September 2010.
Riwan, 2008, Kunyit (Curcuma domestica),
Rohman, A., 2009, Kromatografi untuk Analisis Obat, Graha Ilmu, Yogyakarta, pp.230-232.
Rohman, S, 2008, Teknologi Pengeringan Bahan Makanan ,
Shargel, L. dan Yu, A., 1999, Applied Biopharmaceutics & Pharmacokinetics, fourth edition, Medical Publishing Division, Mc Graw-Hill, pp.132
Sastrohamidjojo, H., 1991, Spektroskopi, Liberty, Yogyakarta, pp.1-15.
Srinarong, P., Kouwen, S.,Visser, M. K., Hinrichs, W. L. J., dan Frijlink, H. W., 2009, Effect of Drug-Carrier Interaction on dissolution Behavior of Solid Dispersion Tablets, Pharmaceutical Development and Technolog, 1-9.
Sutriyo, Rosmaladewi, dan Filosane Febrian Hevike, 2005, Pengaruh polivinilpirolidon terhadap laju disolusi furosemid dalam sistem dispersi padat, Majalah Ilmu Farmasi Vol.II No.1, 30-42.
Tonnesen, H.H., Karlsen , J. 1985, Studies on curcumin and curcuminoid . IV . Kinetics of curcumin degradation in aqueous solution, Z. Lebensm. Unters. Forch. 180, 402-404.
Traub, D.A, 2008, Spray Dryer Guide ,
United States Pharmacopeia Convention, 2005, The United State Pharmacopeia , 28th edition, United State Pharmacopeia Convention Inc., Rockville pp.2748-2751.
Waard, de. H, Hinrichs, W.L.J., Visser, M.R., Bologna, C., dan Frijlink H.W., 2007, Unexpected differences in dissolution behavior of tablets prepared from solid dispersions with a surfactant physically mixed or incorporated, International Journal of Pharmaceutics, 349.
Lampiran 3. Pembuatan kurva baku kurkumin
1. Pembuatan larutan stok kurkumin a. Penimbangan kurkumin baku
berat kertas = 0,1332 g berat kertas + zat = 0,1433 g berat kerta + sisa = 0,1334 g
berat zat = 0,0990 g = 9,9 mg
Kurkumin dilarutkan dengan methanol p.a lalu di add methanol p.a hingga 25 ml.
Konsentrasi larutan stok kurkumin = 9,9 mg / 25 ml = 0,3960 mg / ml 2. Pembuatan larutan intermediet kurkumin
1 ml larutan stok kurkumin di pipet , di add dengan methanol p.a 10,0 ml Konsentrasi larutan intermediet kurkumin = 0,3960 mg/ml x 1,0 ml / 10,0 ml
= 0,0396 mg/ml
Lampiran 4. Data orientasi PVP K-25
Penimbangan PVP K-25 ( 1 gram)
berat aluminium foil = 0,3142 g
Penimbangan hasil dispersi padat
berat aluminium foil = 0,2920 g berat aluminium foil + zat = 0,5580 g berat zat = 0,2660 g
0,2660 g = 266 mg / 4 = 66,5 mg dalam I kapsul
Formula Dispersi Padat Kurkumin- PVP K 25
PVP K 25 ( mg) Serbuk kunyit (mg)
4000 350,8772 40/(4000+40)
=0,99 % ≈ 1 %
6000 350,8772 40/(6000+40)
Perhitungan
Dari orientasi diperoleh persen kehilangan 80 % , agar setara dengan kurkumin 40 mg tiap kapsul maka serbuk kunyit yang ditimbang
= (100%-80%). X = 40 mg = 0,2 X = 40 mg = 200 mg
Lampiran 5. Perhitungan dispersi padat dan campuran fisik
Penimbangan hasil dispersi padat
Penimbangan serbuk kunyit
berat aluminium foil = 0,3306 g berat aluminium foil + zat = 1,7314 g berat aluminium foil + sisa = 0,3312 g berat zat = 1,4002 g
Penimbangan hasil dispersi padat
berat aluminium foil = 0,4572 g
Penimbangan hasil dispersi padat
berat aluminium foil = 0,4667 g berat aluminium foil + zat = 1,2670 g berat zat = 0,8003 g
% kehilangan yang diperoleh : ( 8,0080 + 1,4020) – 0.8003 8,0080+ 1,40020
= 91,50 %
NB : perhitungan untuk drugload 1 % dan 0,66 % sama.
Perhitungan campuran fisik
Jumlah serbuk kunyit yang ada dalam dispersi padat :
= Jumlah serbuk kunyit yang ditimbang – (Jumlah serbuk kunyit yang hilang )
Jumlah kurkumin yang ada dalam dispersi padat :
=( Jumlah serbuk kunyit yang ada dalam dispersi padat) x 0,9720 x 0,60
Jumlah kurkumin yang ada dalam dispersi padat ( dalam 1 kapsul) : =
4
( Jumlah serbuk kunyit yang ada dalam dispersi padat) x 0,9720 x 0,60
Contoh perhitungan
Drug load 2% Replikasi 1
Jumlah serbuk kunyit yang ada dalam dispersi padat
= jumlah serbuk kunyit yang ditimbang - jumlah serbuk kunyit yang hilang = 1,4004 g – (1,4004 g x 90,18 %)
= 1,4004 g – 1,2629 g = 0,1375 g = 137,5 mg
Jumlah kurkumin yang ada dalam tiap formula = 𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗 ℎ𝑘𝑘𝑗𝑗𝑘𝑘𝑘𝑘𝑗𝑗𝑗𝑗𝑘𝑘𝑘𝑘 𝑑𝑑𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗 ℎ𝑗𝑗𝑎𝑎𝑘𝑘𝑗𝑗𝑎𝑎𝑠𝑠𝑘𝑘𝑗𝑗𝑠𝑠
𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗 ℎ𝑏𝑏𝑗𝑗𝑘𝑘𝑠𝑠𝑗𝑗𝑘𝑘𝑘𝑘𝑠𝑠𝑗𝑗 𝑓𝑓𝑓𝑓𝑘𝑘𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗 𝑠𝑠𝑗𝑗𝑘𝑘𝑦𝑦 𝑑𝑑𝑘𝑘𝑏𝑏𝑗𝑗𝑗𝑗𝑑𝑑
= 78,375 𝑗𝑗𝑦𝑦
4 = 19,59375 mg ≈ 19,5938 mg
Jumlah serbuk yang dimasukan dalam kapsul sebanyak 190 mg Jumlah kurkumin dalam 190 mg
= 190 𝑗𝑗𝑦𝑦
𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗 ℎ𝑎𝑎𝑠𝑠𝑘𝑘𝑏𝑏𝑗𝑗𝑘𝑘 𝑠𝑠𝑗𝑗𝑘𝑘𝑦𝑦 𝑑𝑑𝑘𝑘ℎ𝑗𝑗𝑎𝑎𝑘𝑘𝑗𝑗𝑘𝑘𝑗𝑗𝑘𝑘 𝑑𝑑𝑘𝑘𝑗𝑗𝑠𝑠 𝑓𝑓𝑓𝑓𝑘𝑘𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗 x jumlah kurkumin dalam tiap formula
= 190 𝑗𝑗𝑦𝑦
230 ,875 𝑗𝑗𝑦𝑦 x 19,5938 = 16,4982 mg
Jumlah serbuk kunyit yang harus ditimbang
= jumlah serbuk kunyit dalam 190 mg : 97,20 % : 60 % = 16,4982 mg : 97,20 % : 60 %
= 28,2891 mg
Jumlah pembawa yang ditambahkan = 190 mg – jumlah serbuk kunyit ditimbang = 190 mg – 28,2891 mg
= 161,7109 mg
Jadi untuk campuran fisik, serbuk kunyit yang ditimbang sebanyak 28,2891 mg dan PVP K25 sebanyak 161,7109 mg.
Drug load 2% Replikasi 2
Jumlah serbuk kunyit yang ada dalam dispersi padat
= jumlah serbuk kunyit yang ditimbang - jumlah serbuk kunyit yang hilang = 1,4002 g – (1,4002 g x 89,58 %)