PENAPISAN BAKTERIOSIN PENGHAMBAT
PERTUMBUHAN ESCHERICHIA COLI
ENTEROTOKSIGENIK
(Screening of Bacteria Producing Bacteriocin as a
Growth Inhibitors of Enterotoksigenik Escherichia coli)
Siti Chotiah Balai Besar Penelitian Veteriner Jl. RE Martadinata No. 30, Bogor 16114
sitichoti@yahoo.co.id
ABSTRACT
Bacteriocins are antimicrobial peptides that are synthesized ribosomlly by many species of bacteria, and in general just showed bactericidal or bacteriostatic activity against other bacteria that are closely related to the producing strain. The purpose of this study was to determine the barriers to the growth of bacteria producing bacteriocins against local isolates of enterotoxigenic E. coli (ETEC) that cause neonatal diarrhea in calves. One hundred ninety-two samples consisting of 101 rectal swabs and 91 row milk from cows at the farm have been isolated, identified and conducted screening for bacteriocin-producing bacteria using agar diffusion test against strains of ETEC as indicator bacteria. Results showed that 12 isolates of bacteria producing bacteriocins isolated 151 bacterial isolates showed growth inhibition activity with inhibition zone diameter of 15 mm shown by Enterobacter cloacae SRUT, Enterobacter cloacae SRNU and Enterococcus faecalis SK39. Thus, this study indicated that three bacteria producing bacteriocins have the capacity to inhibit ETEC strains would be possible to design new biocontrol of this pathogen in calves.
Key Words: Bacteriocin Producing Bacteria, Enterobacter cloacae, Enterococcus faecalis, Enterotoxigenic
E. coli
ABSTRAK
Bakteriosin adalah peptida antimikroba yang disintesis secara ribosom oleh spesies bakteri, dan pada umumnya hanya menunjukkan aktivitas bakterisidal atau bakteriostatik terhadap bakteri. Tujuan dari penelitian ini adalah untuk mengetahui hambatan pertumbuhan bakteri penghasil bakteriosin terhadap isolat lokal galur E. Coli enterotoksigenik (ETEC) yang menyebabkan diare neonatal pada anak sapi. Seratus sembilan puluh dua sampel yang terdiri dari 101 swab rektal dan 91 susu dari sapi peternak telah diisolasi, diidentifikasi dan dilakukan penapisan terhadap bakteri penghasil bakteriosin menggunakan uji difusi agar terhadap galur ETEC sebagai bakteri indikator. Hasil penelitian menunjukkan bahwa 12 isolat bakteri penghasil bakteriosin dari 151 isolat bakteri yang terisolasi menunjukkan aktifitas hambatan pertumbuhan dengan diameter zona hambat sebesar 15 mm ditunjukkan oleh Enterobacter cloacae SRUT, Enterobacter
cloacae SRNU dan Enterococcus faecalis SK39. Studi ini mengindikasikan bahwa tiga bakteri penghasil
bakteriosin tersebut potensial untuk digunakan sebagai kontrol biologi pada sapi.
Kata Kunci: Bakteri Penghasil Bakteriosin, Enterobacter cloacae, Enterococcus faecalis, Enterotoksigenik
E. coli
PENDAHULUAN
Escherichia coli patogenik yang dapat menimbulkan penyakit pada saluran
pencernaan diantaranya E. coli
enterotoksigenik (ETEC) menyebabkan diare
pada anak babi, sapi dan kambing dan E. coli verotoksigenik (VTEC) menyebabkan hemoragik enterokolitis pada anak sapi, diare pada anak babi baru disapih dan hemoragik kolitis dan hemolitik uremik sindroma pada manusia (Quin et al. 2002). Salah satu agen
bakteri patogen penyebab diare yang banyak ditemukan adalah bakteri ETEC serotipe K99
dan enterohemoragik E. coli (EHEC).
Di Indonesia kasus diare neonatal pada sapi perah di Sukabumi dan Bandung berkisar antara 19,3-36% (Supar dan Hirst 1985) dan aplikasi vaksin ETEC terhadap induk sapi perah pada tingkat akhir kebuntingan dapat menurunkan kematian dari rata-rata 13% per bulan menjadi 0,7%. (Supar et al. 1998). Angka kesakitan (morbiditas) dan kematian (mortalitas) pada anak sapi sangat beragam tergantung pada faktor penyebabnya. Menurut Wudu et al. (2008) melaporkan bahwa angka kesakitan dan kematian pada anak sapi masing-masing dapat mencapai 62 dan 22%, kejadian tertinggi sebanyak 39% disebabkan oleh kasus diare. Anak sapi penderita diare akan mengalami kekurangan cairan yang mengandung garam mineral atau elektrolit sehingga terjadi dehidrasi dan asidosis yang dapat menyebabkan kematian. Kerugian ekonomi yang dirasakan oleh peternak akibat biaya obat dan tenaga pengobatan, kematian dan gangguan pertumbuhan pada penderita yang masih bertahan hidup (Anderson et al. 2003; Swift et al. 1996).
Tujuan dari studi ini adalah untuk mengisolasi dan karakterisasi bakteri penghasil bakteriosin hasil isolasi dari sapi yang dapat menghambat pertumbuhan bakteri ETEC pada bahan pangan asal ternak.
MATERI DAN METODE Isolasi bakteri
Sebanyak 192 sampel yang terdiri dari 101 sampel swab rektal dan 91 susu dari sapi yang diambil di peternakan di Jawa Barat. Sampel diambil seaseptis mungkin, dikumpulkan ke dalam boks berisi pendingin dan dibawa ke laboratorium Bbalitvet. Sampai di laboratorium masing-masing sampel disebarkan kedalam medium penumbuh bakteri Gram negatif dan Gram positif masing-masing berurutan adalah
Chromo ID Coli agar (Biomerieux, Perancis) dan De Mean Rogosa Shape (MRS) agar (Oxoid, Inggris). Selanjutnya diinkubasikan selama 24 jam pada suhu 37C kondisi aerob dan anaerob. Koloni bakteri yang tumbuh
dimurnikan dan disimpan dalam medium semi solid untuk dikerjakan lebih lanjut.
Isolat bakteri indikator
Isolat lokal ETEC serotipe K99
menghasilkan enterotoksin tahan panas dan dapat menyebabkan diare neonatal pada anak sapi perah digunakan sebagai indikator. Isolat diperoleh dari koleksi BB Litvet Culture Collection dengan nomor BCC B2422, digunakan pada penelitian ini sebagai indikator bakteri patogen. Ampul yang berisi isolat tersebut dibuka menggunakan alat pembuka didalam biosavety cabinet (BSC) kelas II. Selanjutnya disuspensikan dalam medium kaldu Brain Hart Inffusion (BHI), diinkubasikan pada suhu 37oC selama 24 jam. Biakan dipindahkan kedalam medium padat
Chromo ID Coli dan diinkubasikan pada suhu 37oC selama 24 jam. Isolat E. coli tersebur dilakukan identifikasi ulang, dan berdasarkan karakteristik biokemik menggunakan perangkat identifikasi API 20 E (Biomereux, Perancis). Selanjutnya E. coli yang teridentifikasi di uji terhadap antigen perlekatan K99, dan antigen
flagela F41 dengan metode standar slide
agglutination (Sojka 1965) menggunakan anti
serum K99 dan F41 (buatan Bbalitvet).
Aktifitas antibakteri terhadap indikator bakteri patogen
Pengujian aktifitas antibakteri dikelompokkan menjadi dua kelompok yaitu kelompok bakteri Gram negatif dan kelompok bakteri Gram positif menggunakan metode
agar spot tests masing-masing mengacu pada
Kumar et al. (2009) dan Herreros et al. (2005) dan dimodifikasi.
Setiap isolat bakteri Gram negatif yang akan diuji ditumbuhkan dahulu di dalam medium cair Luria Bertani Miller (LBM) (Diffco, Inggris) selama satu malam pada suhu 37oC sambil digoyang kurang lebih 100 rpm. Sebanyak 1 ml biakan tersebut ditambahkan ke dalam 10 ml medium yang sama dan diinkubasikan selama 1 jam, kemudian ditambahkan mitomycin C (200 ng/ml) dan inkubasi dilanjutkan selama 4 jam. Kultur di sentrifuge dengan kecepatan 10.000 x g selama 5 menit pada suhu 4oC. Filtrat yang diperoleh
disaring menggunakan filter 0,45 um dan disimpan pada suhu 5C untuk digunakan lebih lanjut. Masing-masing bakteri patogen sebagai indikator atau tantang ditumbuhkan dalam medium kaldu BHI, diinkubasi pada suhu 37oC selama 1 malam. Sebanyak 0,5 ml suspensi biakan tersebut pada konsentrasi sekitar 107 cfu (Mc.Farland nomor 0,5) dicampurkan kedalam 5 ml medium padat lunak LBM (47oC). Selanjutnya dituangkan ke dalam cawan petri yang berisikan 5 ml medium padat LBM dan didiamkan pada suhu 5oC selama 1 jam. Kemudian teteskan 10 l filtrat yang akan diuji diatas medium padat lunak tersebut dan didiamkan pada suhu 4oC selama 1 jam. Selanjutnya diinkubasikan pada suhu 37oC selama 18-24 jam. Amati zona jernih yang terjadi sekitar tetesan dan diukur diameternya.
Dengan perlakuan yang sama seperti tersebut diatas dilakukan pula pada semua isolat bakteri Gram positif yang akan diuji. Hanya disini bedanya adalah medium yang dipakai kaldu MRS dan tidak menggunakan
starter maupun penambahan mitomycin C dan
inkubasi selama 18-24 jam. Medium padat dan lunak yang dipakai adalah BHI.
Identifikasi bakteri penghasil bakteriosin (BPB)
Identifikasi BPB menggunakan metode standar menurut (Quin et al. 2002; Barrow dan
Feltham 2003) dan dimodifikasi dengan menggunakan medium spesifik untuk masing-masing bakteri. Masing-masing-masing isolat yang berpotensi memproduksi bakteriosin hasil dari penapisan tersebut diatas dalam keadaan murni umur 24 jam diwarnai dengan pewarnaan Gram dan dilakukan pemeriksaan morfologi secara mikroskopik. Kemudian uji biokimia dilakukan dengan API 20 E (Biomereux, Perancis), sedangkan kelompok bakteri Gram positif dengan API 50 CHL (Biomereux, Perancis), BBL Crystal ANR dan BBL Crystal GP (Becton Dickinson, Amerika).
HASIL DAN PEMBAHASAN Isolasi bakteri dari 192 sampel yang diperiksa diperoleh 151 isolat bakteri yang terdiri dari 73 isolat kelompok Gram negatif dan 78 isolat kelompok Gram positif. Setelah dipelajari lebih lanjut melalui penapisan terhadap bakteri penghasil bakteriosin yang memiliki aktifitas antibakteri terhadap isolat lokal ETEC serotipe K99, hasilnya dipaparkan
di dalam Tabel 1.
Pada studi ini, dari 151 isolat bakteri yang ditapis diperoleh 12 isolat BPB yang menunjukkan aktifitas antibakteri terhadap ETEC serotipe K99 yang dapat menyebabkan
diare pada anak sapi perah (Supar 1996), isolat selebihnya negatif. Setelah dilakukan identifikasi terhadap 12 isolat BPB, diperoleh 7
Tabel 1. Aktifitas antibakteri terhadap isolat lokal E. coli enterotoksigenik (ETEC) serotipe K99 produksi
toksin tahan panas nonor BCC B2422
Kelompok Gram Spesies ETEC serotipe K99 Diameter zona (mm)
Negatif E. coli membentuk zona bening 8
E. coli membentuk zona bening 8
E. coli membentuk zona bening 8
E. coli membentuk zona bening 8
E. coli membentuk zona bening 8
E. coli membentuk zona bening 8
E. coli membentuk zona bening 8
E. coli membentuk zona bening 8
E. cloacae membentuk zona bening 15
E. cloacae membentuk zona bening 15 Bakteri lainnya sebanyak 64
isolat
tidak membentuk zona bening
0 Positif E. faecalis membentuk zona bening 15
Bifidobacterium dentium membentuk zona bening 8
Streptococcus uberis membentuk zona bening 11 Bakteri lainnya sebanyak 75
isolat
tidak membentuk zona bening
isolat E. coli, 2 isolat E. cloacae, 1 isolat E.
faecalis, 1 isolat Bifidobacterium dentium dan
1 isolat Streptococcus uberis. E. coli dan E.
cloacae adalah bakteri Gram positif termasuk
dalam kelompok Enterobacteria dan diperoleh dari sampel swab rektal.
E. faecalis, B. dentium dan Streptococcus
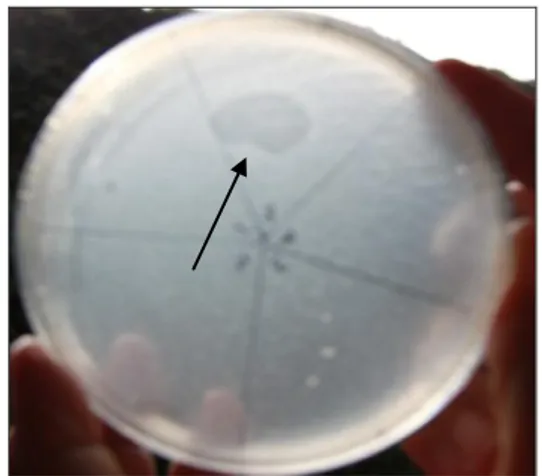
adalah bakteri Gram positif dan termasuk dalam kelompok bakteri asam laktat diperoleh dari sampel susu. Aktifitas anti bakteri dicirikan dengan terbentuknya zona bening, dan dalam pengamatan diperoleh zona terlebar sebesar 15 mm dibentuk oleh E. cloacae SRUT, E. cloacae SRNU dan E. faecalis SK39 Tabel 1 dan Gambar 1.
Gambar 1. Zona hambat yang dibentuk oleh E.
faecalis SK39 terhadap E.coli K99
enterotoksigenik BCC B2422
Bakteri penghsil bakteriosin galur Nissle 1917 telah digunakan untuk mengobati diare neonatal anak sapi (Von et al. 2005). Di Jerman, galur Nissle 1917 telah disetujui sebagai persiapan probiotik untuk anak sapi sejak tahun 2001 dan saat ini dikomersialisasikan dengan merek "Ponsocol." Hasil studi mengindikasikan bahwa tiga galur BPB ini memiliki kapasitas untuk menghambat pertumbuhan ETEC serotipe K99 yang dapat
menyebabkan diare neonatal pada anak sapi. Oleh karena itu, memungkinkan untuk digunakan sebagai kontrol biologi terhadap bakteri enterotoksigenik tersebut baik antar ternak maupun lingkungannya.
KESIMPULAN DAN SARAN Tiga galur isolat lokal bakteri penghasil bakteriosin yang terdiri dari E. cloacae SRUT,
E. cloacae SRNU dan E. faecalis SK39
potensial penghambat pertumbuhan ETEC serotipe K99 yang dapat menyebabkan diare
neonatal pada anak sapi.
Perlu penelitian lebih lanjut secara komprehensif dalam aplikasinya sebagai kontrol biologi pada ternak dan lingkungannya.
DAFTAR PUSTAKA
Anderson DC, Kress DD, Bernardini MM, Davis KC, Boss DL, Doornbos DE. 2003. The effect of scours on calf weaning weight. The
Professional Animal Scientist. 19:399-403.
Barrow GI, Feltham RKA, Cowan,Steel`S. 2003. Manual for the identification of medical bacteria. 3rd Ed. Cambridge University Press, UK. p. 118-119.
Herreros MA, Sandoval H, González L, Castro JM, Fresno JM, Tornadijo ME. 2005. Antimicrobial activity and antibiotic resistance of lactic acid bacteria isolated from Armada cheese (a Spanish goats’ milk cheese). Food Microbiol. 22:455-459.
Kumar P, Ferzin S, Chintan S, Kumar GN. 2009. Isolation and characterization of potential probiotic Escherichia coli strains from rat faecal samples. Am J Infect Dis. 5:112-117. Sojka WJ. 1965. Escherichia coli in domestic
animals and poultry. Commonwealth Agricultural Bureaux. Farnham Royal, Bucks, England. p. 195-196.
Supar, Hirst R. 1985. Detection of enteropathogenic
Escherichia coli in calves and pigs. In:
Proceedinga of the fourth national congress of Indonesian Society for Mycrobiology and the first meeting of Asean Microbiology. Jakarta, 2-4 December 1985. Jakarta, Indonesia. Supar. 1996. Kolibasilosis pada anak sapi perah di
Indonesia. Wartazoa. 5:26-32.
Supar, Kusmiyati, Poerwadikarta MB. 1998. Aplikasi vaksin enterotoksigenik Echerichia
coli (ETEC) K99, F41 polivalen pada induk
sapi perah bunting dalam upaya pengendalian kolibasilosis dan kematian pedet neonatal. JITV. 3:27-33.
Swift BL, Nelms GE, Coles R. 1996. The effect of neonatal diare on subsequent weight gains in beef calves. Vet Med Small Anim Clin. 71:1269-1272.
Von B, Jaekel RI, Schubotz E, Schwarz S, Stroff T, Krueger M. 2005. Escherichia coli strain Nissle 1917: significant reduction of neonatal calf diarrhae. J Dairy Sci. 88:317-323.
Wudu T, Kelay B, Mekonnen HM, Tesfu K. 2008. Calf morbidity and mortality in small holder dairy farm in Ada`a Liben district of Oromia, Ethiophia. Tropical Animal Health Production. 40:369-376.
Quinn PJ, Markey BK, Carter ME, Donnelly JW, Leonard FC. 2002. Veterinary microbiology and mycrobial disease: enterobacteriaceae. Blackwell Press, Oxford, UK. p. 84-123.