UJI AKTIVITAS ANTIOKSIDAN MINYAK MAKADAMIA (Macadamia integrifolia Maiden & Betche) FOOD GRADE DAN THERAPEUTIC GRADE DENGAN METODE DPPH (1,1-difenil-
2-pikrilhidrazil) SKRIPSI
OLEH:
RIANA RIBKA MANURUNG NIM 171501194
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2022
UJI AKTIVITAS ANTIOKSIDAN MINYAK MAKADAMIA (Macadamia integrifolia Maiden & Betche) FOOD GRADE DAN THERAPEUTIC GRADE DENGAN METODE DPPH (1,1-difenil-
2-pikrilhidrazil)
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara
OLEH:
RIANA RIBKA MANURUNG NIM 171501194
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2022
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Esa karena kasih, karunia dan penyertaan-Nya, penulis dapat menyelesaikan skripsi yang berjudul Uji Aktivitas Antioksidan Minyak Makadamia (Macadamia integrifolia Maiden & Betche) Food Grade dan Therapeutic Grade dengan Metode DPPH (1,1-difenil-2-pikrilhidrazil).
Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Selama proses penyusunan skripsi ini, penulis mendapatkan dukungan, doa, bantuan dan bimbingan dari berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih kepada yang terhormat Dekan Fakultas Farmasi Universitas Sumatera Utara, ibu Khairunnisa, S.Si., M.Pharm., Ph.D., Apt., yang telah memberikan bantuan dan fasilitas selama masa Pendidikan, juga bapak Prof. Dr. Ginda Haro, M.Sc., Apt., selaku pembimbing yang telah memberikan bimbingan dan nasehat yang baik selama penelitian dan penulisan skripsi ini berlangsung, bapak Prof. Dr.
Jansen Silalahi, M.App.Sc., Apt., dan Ibu Henny Sri Wahyuni, S.Farm., M.Si., Apt., selaku dosen penguji. Penulis juga ingin menyampaikan rasa terima kasih kepada ibu Lia Laila, S.Farm., M.Sc., Apt., selaku penasihat akademik yang telah membimbing selama masa perkuliahan.
Penulis juga mengucapkan terima kasih yang teristimewa kepada ayah Sahat Manurung dan ibu Rotua Nainggolan, serta kakak Ekaristi Manurung dan adik Immanuel Manurung dan Aryo Manurung yang telah memberikan dukungan, semangat dan doa setiap harinya. Terima kasih juga kepada teman-teman Dantob Batal, Natasha Adina, Asriana Saragih, dan No Kasih Lase serta teman-teman yang
tidak bisa disebutkan satu persatu atas bantuan yang tulus selama proses penelitian hingga selesainya penyusunan skripsi penulis.
Semoga Tuhan Yang Maha Esa senantiasa melimpahkan berkat dan penyertaan-Nya selalu. Akhir kata, penulis memohon maaf apabila masih ditemukan banyak kekurangan pada penyusunan skripsi ini. Penulis berharap semoga skripsi ini dapat memberikan manfaat bagi penulis, para pembaca dan rekan-rekan yang hendak melakukan penelitian berikutnya.
Medan, 12 Januari 2022 Penulis,
Riana Ribka Manurung NIM 171501194
UJI AKTIVITAS ANTIOKSIDAN MINYAK MAKADAMIA (Macadamia integrifolia Maiden & Betche) FOOD GRADE DAN THERAPEUTIC GRADE
DENGAN METODE DPPH (1,1-difenil-2-pikrilhidrazil)
ABSTRAK
Latar Belakang: Minyak makadamia merupakan minyak yang dapat digunakan baik secara topikal maupun dikonsumsi langsung. Minyak makadamia mengandung vitamin E yang merupakan zat antioksidan yang bermanfaat melindungi tubuh dari kerusakan akibat radikal bebas. Banyak faktor yang memengaruhi aktivitas antioksidan minyak makadamia seperti sumber tanaman, penambahan komponen campuran lain dan metode ekstraksi.
Tujuan: Untuk membandingkan aktivitas antioksidan dari minyak makadamia food grade dengan minyak makadamia therapeutic grade
Metode: Sampel yang digunakan adalah minyak makadamia food grade dan minyak makadamia therapeutic grade dengan vitamin C sebagai pembanding.
Pengujian aktivitas antioksidan dilakukan secara deskriptif menggunakan metode 1,1-difenil-2-pikrilhidrazil (DPPH) dengan alat spektrofotometer sinar tampak pada panjang gelombang 515,5 nm. Uji aktivitas antioksidan minyak makadamia dilakukan pada konsentrasi 50 µg/ml, 100 µg/ml, 150 µg/ml dan 200 µg/ml. Rata- rata persentase peredaman radikal bebas diperoleh untuk menentukan IC50
Hasil: Hasil penelitian menunjukkan bahwa kedua minyak makadamia memiliki aktivitas antioksidan dalam kategori sedang. Minyak makadamia therapeutic grade memiliki IC50 119,29 µg/ml dan minyak makadamia food grade memiliki IC50
130,52 µg/ml. Hasil pengukuran IC50 dari vitamin C sangat kuat yaitu sebesar 6,74 µg/ml.
Kesimpulan: Berdasarkan hasil penelitian dapat disimpulkan bahwa aktivitas antioksidan minyak makadamia therapeutic grade lebih kuat dibandingkan minyak makadamia food grade dan lebih lemah dibandingkan vitamin C.
Kata Kunci: antioksidan, radikal bebas, DPPH, minyak makadamia, IC50
ANTIOXIDANT ACTIVITY TEST OF MACADAMIA OIL (Macadamia integrifolia Maiden & Betche) FOOD GRADE AND THERAPEUTIC
GRADE USING DPPH METHOD (1,1-diphenyl-2-picrylhydrazyl)
ABSTRACT
Background: Macadamia oil is an oil that can be used both topically and consumed directly. Macadamia oil contains vitamin E, which is an antioxidant that protects the body from free radical damage. Many factors affect the antioxidant activity of macadamia oil such as plant source, addition of other mixed components and extraction method
Objective: To compare the antioxidant activity of food grade macadamia oil with therapeutic grade macadamia oil
Method: The samples used were food grade macadamia oil and therapeutic grade macadamia oil with vitamin C as a comparison. The antioxidant activity test was carried out descriptively using the 1,1-diphenyl-2-picrylhydrazyl (DPPH) method with a visible spectrophotometer at 515,5 nm wavelength. The antioxidant activity test of macadamia oil was carried out at concentrations of 50 µg/ml, 100 µg/ml, 150 µg/ml and 200 µg/ml. The average percentage of free radical scavenging was obtained to determine IC50
Results: The results showed that both macadamia oils had antioxidant activity in the moderate category. Therapeutic grade macadamia oil has an IC50 of 119,29 µg/ml and food grade macadamia oil has an IC50 of 130,52 µg/ml. The IC50
measurement result of vitamin C is very strong, which is 6,74 µg/ml.
Conclusion: Based on the result of study, it can be concluded that the antioxidant activity of therapeutic grade macadamia oil is stronger than food grade macadamia oil and weaker than vitamin C.
Keywords: antioxidant, free radicals, DPPH, macadamia oil, IC50
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
HALAMAN PERNYATAAN ORISINALITAS ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 5
1.3 Hipotesis ... 5
1.4 Tujuan Penelitian ... 5
1.5 Manfaat Penelitian ... 5
1.6 Kerangka Pikir Penelitian ... 6
BAB II TINJAUAN PUSTAKA ... 7
2.1 Makadamia ... 7
2.1.1 Taksonomi tanaman makadamia ... 8
2.1.2 Minyak makadamia ... 9
2.2 Radikal Bebas ... 12
2.3 Antioksidan ... 14
2.4 Vitamin C ... 16
2.5 Pengukuran Aktivitas Antioksidan ... 17
2.6 Spektrofotometri Ultraviolet Dan Sinar Tampak ... 20
2.6.1 Aspek kuantitatif spektrofotometri ultraviolet dan sinar tampak ... 20
2.6.2 Hal-hal yang harus diperhatikan dalam analisis spektrofotometri ultraviolet dan sinar tampak ... 21
BAB III METODE PENELITIAN ... 23
3.1 Alat dan Bahan ... 23
3.1.1 Alat ... 23
3.1.2 Bahan ... 23
3.2 Pengumpulan Bahan ... 23
3.3 Pengujian Aktivitas Antioksidan dengan Metode Peredaman DPPH ... 24
3.3.1 Pembuatan larutan induk DPPH (0,5 mM) ... 24
3.3.2 Pembuatan larutan blanko ... 24
3.3.3 Pembuatan kurva absorbansi maksimum DPPH ... 24
3.3.4 Penentuan waktu kerja ... 24
3.3.5 Pembuatan larutan induk sampel ... 24
3.3.6 Pembuatan larutan uji sampel ... 25
3.3.7 Pembuatan larutan induk vitamin C ... 25
3.3.8 Pembuatan larutan uji vitamin C ... 25
3.3.9 Penentuan persen peredaman ... 26
3.3.10 Penentuan nilai IC50 sampel uji dan vitamin C ... 26
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Hasil Pengukuran Absorbansi Maksimum Larutan DPPH ... 28
4.2 Waktu Operasional ... 28
4.3 Persamaan Regresi ... 29
4.4 Aktivitas Antioksidan Sampel Uji dan Vitamin C ... 29
4.5 Nilai IC50 (Inhibitory Concentration) ... 32
BAB V KESIMPULAN DAN SARAN ... 35
5.1 Kesimpulan ... 35
5.2 Saran ... 35
DAFTAR PUSTAKA ... 36
LAMPIRAN ... 37
DAFTAR TABEL
2.1 Kategori Nilai IC50 Sebagai Antioksidan ... 19 4.1 Aktivitas Antioksidan (IC50 dari Sampel Uji dan Pembanding) ... 32
DAFTAR GAMBAR
1.1 Kerangka Pikir Penelitian ... 6 2.1 Pohon Makadamia ... 9 2.2 Struktur Kimia 1,1,2,2-diphenyl picrylhydrazyl (DPPH) ... 18 4.1 Kurva Absorbansi Maksimum Larutan DPPH Menggunakan Spektrofotometer Sinar Tampak ... 28 4.2 Kurva Kalibrasi Peredaman DPPH oleh Sampel Minyak Makadamia Green
Tosca (Food Grade) ... 30 4.3 Kurva Kalibrasi Peredaman DPPH oleh Sampel Minyak Makadamia
Darjeeling (Food Grade) ... 30 4.4 Kurva Kalibrasi Peredaman DPPH oleh Vitamin C ... 30
DAFTAR LAMPIRAN
1. Sertifikat Analisis Minyak Makadamia Green Tosca (Food grade) ... 38
2. Sertifikat Analisis Minyak Makadamia Darjeeling (Therapeutic Grade) ... 39
3. Minyak Makadamia ... 40
4. Alat-alat Penelitian ... 41
5. Flowsheet Pengujian Aktivitas Antioksidan dengan Metode Peredaman DPPH ... 42
6. Pengujian Aktivitas Antioksidan dengan Spektrofotometer Sinar Tampak ... 46
7. Persentase Peredaman DPPH Terhadap Sampel dan Vitamin C ... 52
BAB I PENDAHULUAN 1.1 Latar Belakang
Makadamia (Macadamia integrifolia Maiden & Betche) adalah penghasil biji berkadar lemak tinggi. Biji makadamia rasanya lezat dan manis, mengandung lemak 70% atau lebih, dapat dimakan mentah, digongseng atau digoreng terlebih dahulu. Makadamia berasal dari timur benua Australia (Direktorat Jenderal Perkebunan, 2006). Minyak makadamia di ekstrak dari biji kacang makadamia yang sudah matang karena bagian biji makadamia mengandung minyak yang tinggi (Tan, 2020)
.
Minyak makadamia dengan pengepresan dingin biasa digunakan sebagai campuran salad dan menumis karena rasa dan aromanya yang enak. Industri farmasi menggunakan minyak makadamia pengepresan dingin untuk memproduksi berbagai produk suplemen makanan dan nutraseutikal yang dijual secara komersial dengan manfaat kesehatan jantung. Pada proses pengepresan minyak makadamia dihasilkan minyak makadamia murni dan ampas. Ampas yang dihasilkan dapat dilakukan pengepresan kedua dengan dan/atau ekstraksi pelarut untuk mendapatkan minyak tambahan untuk proses pemurnian kedua (Navarro dan Rodrigues, 2016)
.
Menurut Gustavheess (2010), minyak makadamia dengan olahan memiliki warna kuning pucat, bau dan rasa yang kurang kuat daripada minyak makadamia tanpa olahan dan dapat digunakan dalam pembuatan produk kosmetik. Karena sifat emolien dan penetrasi kulit yang cepat, minyak makadamia mentah dan halus telah banyak digunakan dalam produk kosmetik dan produk perawatan kulit (Tan, 2020)
.
Minyak esensial merupakan hasil ekstraksi dari suatu bagian tanaman di mana
merupakan sumber alami komponen fenolik dan menarik peneliti untuk mengevaluasi aktivitasnya sebagai antioksidan atau penangkal radikal bebas.
Beberapa minyak esensial telah terbukti menangkal radikal bebas dan sifat antioksidan diuji dengan radikal DPPH pada suhu kamar (Edris, 2007)
.
Minyak esensial sudah lama digunakan sebagai agen terapi (therapeutic agents). Menurut Shutes, istilah therapeutic grade dalam tingkatan minyak esensial digunakan oleh pabrik produksi minyak esensial untuk meningkatkan penjualan. Selain itu, beberapa minyak esensial telah terbukti secara ilmiah memiliki khasiat sebagai obat termasuk antiinflamasi, antivirus, antitumor, antihiperglikemik dan antikarsinogenik (Wei dan Shibamoto, 2007).
Kacang makadamia mengandung minyak lebih dari 75% beratnya, 9,0%
protein, 9,3% karbohidrat, 1,5% kadar air, 1,6% mineral lainnya dan 2,0% serat (Akhtar dkk., 2006). Minyak kacang makadamia kaya akan asam lemak tak jenuh tunggal (MUFA), didominasi oleh oleat (60%) dan asam palmitoleat (20%).
Kacang makadamia juga mengandung MUFA yang tinggi dibandingkan sumber makanan lainnya. Pola makan yang tinggi akan MUFA menurunkan kadar kolesterol plasma, dimana efek dari penurunan kolesterol dan perlindungan koroner ini mungkin disebabkan oleh tingginya persentase asam lemak tak jenuh, serta komponen penting bioaktif seperti tokoferol, fitosterol dan squalene (Wall, 2010)
.
Konsentrasi asam palmitoleat yang tinggi membuat minyak ini sangat bermanfaat untuk kulit kering atau dewasa (Barratt, 2010). Vitamin E dalam minyak makadamia (tokotrienol dan tokoferol) merupakan antioksidan alami.Minyak ini juga mengandung squalene yang memberi manfaat dalam meregenerasi sel dan bermanfaat sebagai antioksidan dengan melindungi kulit dari UV-induced
lipid peroxidation (Wall, 2010). Kandungan vitamin E dikenal baik sebagai antioksidan alami yang larut dalam lemak, antioksidan pemecah rantai, dan melindungi membran sel dari kerusakan peroksidase (Abubaker dkk., 2017)
.
Antioksidan dibutuhkan tubuh untuk melindungi tubuh dari serangan radikal bebas. Antioksidan adalah suatu senyawa atau komponen kimia yang dalam kadar atau jumlah tertentu mampu menghambat atau memperlambat kerusakan akibat proses oksidasi. Tubuh manusia tidak mempunyai cadangan antioksidan dalam jumlah berlebih, sehingga apabila terbentuk banyak radikal maka tubuh membutuhkan antioksidan eksogen. Adanya kemungkinan efek samping yang belum diketahui dari antioksidan sintetik menyebabkan antioksidan alami menjadi alternatif yang sangat dibutuhkan (Sayuti dan Yenrina, 2015). Radikal bebas juga berperan dalam proses penuaan, di mana reaksi inisiasi radikal bebas pada mitokondria menyebabkan diproduksinya Reactive Oxygen Species (ROS) yang bersifat reaktif. Radikal bebas dapat dihasilkan dari hasil metabolisme tubuh dan faktor eksternal seperti asap rokok, hasil penyinaran ultraviolet, zat kimiawi dalam makanan dan polutan lain (Werdhasari, 2014)
.
Aktivitas antioksidan suatu senyawa atau ekstrak dapat diuji dengan mengukur daya tangkap terhadap radikal bebas (radical scavenging activity) menggunakan radikal sintetik 1,1,2,2-diphenyl picrylhydrazyl (DPPH) (Santoso, 2016). Aktivitas scavenging DPPH melalui delokalisasi elektron yang akan mengubah larutan dari warna kuning menjadi ungu. Metode DPPH ini merupakan metode yang sensitif untuk menguji aktivitas antioksidan (Yuniwarti dkk., 2018). Metode DPPH juga merupakan metode yang sering dipilih karena sederhana, mudah, peka dan memerlukan sedikit sampel. Metode ini hanya membutuhkan senyawa DPPH yang
bersifat stabil dan senyawa pembanding seperti vitamin C (Lung dan Destiani, 2017).
Minyak makadamia telah banyak digunakan pada sebagian besar industri makanan. Namun saat ini banyak industri kosmetik yang mulai memformulasikan minyak makadamia sebagai campuran kosmetik seperti produk perawatan kulit dan produk untuk rambut. Lavenia (2017) telah melakukan penelitian terhadap aktivitas antioksidan minyak makadamia jenis food grade menggunakan metode 1,1-difenil- 2-pikrilhidrazil (DPPH) dengan hasil penelitian berupa kekuatan antioksidan minyak makadamia dengan IC50 sebesar 100,4 µg/ml yang termasuk aktivitas antioksidan kuat. Kemudian minyak makadamia jenis food grade ini diformulasikan dalam bentuk sediaan masker gel peel off dengan berbagai konsentrasi sebagai antiaging.
Berdasarkan uraian di atas, maka dilakukan penelitian untuk mengetahui perbedaan aktivitas antioksidan dari minyak makadamia yang beredar di pasaran yaitu jenis food grade yang ditujukan untuk campuran makanan dan therapeutic grade yang ditujukan untuk penggunaan topikal atau campuran kosmetik, kemudian sampel diuji dengan metode pemerangkapan radikal bebas 1,1-difenil- 2-pikrilhidrazil (DPPH) menggunakan alat spektrofotometer sinar tampak.
1.2 Perumusan Masalah
- Apakah terdapat perbedaan aktivitas antioksidan antara minyak makadamia food grade dan therapeutic grade?
- Apa jenis minyak makadamia yang memiliki aktivitas antioksidan lebih tinggi?
1.3 Hipotesis
- Minyak makadamia food grade dan therapeutic grade memiliki perbedaan aktivitas antioksidan.
- Minyak makadamia therapeutic grade memberikan aktivitas antioksidan yang lebih tinggi dibandingkan dengan minyak makadamia food grade.
1.4 Tujuan Penelitian
- Untuk mengetahui apakah terdapat perbedaan aktivitas antioksidan antara minyak makadamia food grade dan therapeutic grade.
- Untuk mengetahui jenis minyak makadamia yang memiliki aktivitas antioksidan lebih tinggi.
1.5 Manfaat Penelitian
- Sebagai sumber informasi bagi peneliti selanjutnya yang akan melakukan penelitian terkait dengan aktivitas antioksidan pada minyak makadamia.
- Sebagai sumber informasi bagi masyarakat tentang aktivitas antioksidan dan manfaat penggunaan minyak makadamia bagi kesehatan.
1.6 Kerangka Pikir Penelitian
Gambar 1.1 Kerangka pikir penelitian - Sampel minyak
makadamia food grade dan
therapeutic grade - Pembanding vitamin C
Uji aktivitas antioksidan dengan metode DPPH
(1,1-Difenil-2- Pikrilhidrazil)
Aktivitas antioksidan
BAB II
TINJAUAN PUSTAKA 2.1 Makadamia
Tanaman makadamia termasuk famili Protaceae, berasal dari Australia. Jenis yang bisa dimakan bijinya adalah yang dikenal dengan nama Macadamia integrifolia dengan permukaan tempurung atau batok halus. Tinggi tanaman makadamia bisa mencapai 18 meter
.
Bunganya berwarna putih atau putih kekuningan, bentuknya berangkai. Marga dari makadamia memiliki sembilan spesies; Macadamia integrifolia, Macadamia tetraphylla, Macadamia ternifolia, Macadamia jansenii, Macadamia whelani, Macadamia claudiensis dan Macadamia grandis yang berasal dari Australia, Macadamia neurophylla yang berasal dari Kaledonia Baru dan Makadamia hildebrandii yang berasal dari Sulawesi di Indonesia (Suheryadi, 2002).
Di Indonesia, makadamia tumbuh di Cibodas, Lembang dan Belawan (Kawasan Pegunungan Ijen) yang memiliki ketinggian ±1.000 m dpl. Tanaman makadamia dapat tumbuh dengan baik dan berbuah banyak. Tetapi, makadamia yang ditanam di dataran rendah (±50 m dpl) dengan suhu yang tinggi dan di musim kemarau yang panjang seperti di Pasuruan (Jawa Timur), tanaman makadamia tidak berbuah (Puspitojati dkk., 2017). Di Hawaii, makadamia merupakan tanaman utama dalam pengusahaan kebun buah-buahan yang dibudidayakan (9000 hektar tanaman yang berproduksi), sedangkan di Australia tanaman makadamia yang dibudidayakan mencapai 6000 ha, yang mana kacangnya merupakan jenis kacang- kacangan yang terbaik dan termahal di dunia. Makadamia dapat dipergunakan dalam berbagai hal termasuk:
a) Sebagai hidangan dapat dimakan baik mentah maupun disangrai (digongseng) dan digarami
b) Perusahaan makanan menggunakan kacang makadamia di dalam coklat dan permen sebagai isian
c) Dipanggang dalam kue, biskuit atau roti berukuran kecil d) Dapat meningkatkan rasa pada ikan, sup dan salad
e) Kualitas minyak sangat baik, tinggi lemak tidak jenuh tunggal (Ditjen Perkebunan, 2006)
.
Kacang dari makadamia merupakan bagian yang dapat dimakan. Umumnya dimakan mentah, digoreng atau dipanggang dan diasinkan. Kacang digunakan untuk pelengkap makanan penutup dan sebagai bahan tambahan dalam biskuit, es krim dan coklat. Kacang makadamia juga diekstraksi untuk diambil minyaknya dan digunakan untuk salad. Kacang Macadamia integrifolia Maiden & Betche yang dibudidayakan di Mesir merupakan kualitas yang baik dan daun tanaman memiliki nilai gizi untuk limbah tanaman (Abubaker dkk., 2017)
.
2.1.1 Taksonomi Tanaman Makadamia
Sistematika (taksonomi) tumbuhan, kedudukan tanaman makadamia diklasifikasikan sebagai berikut (Ditjen Perkebunan, 2006)
.
Kingdom : Plantae
Divisio : Spermatophyta Subdivisio : Angiospermae Kelas : Dicotyledoneae Bangsa : Proteales Famili : Proteaceae
Marga : Macadamia
Spesies : Macadamia integrifolia Maiden & Betche
Pohon makadamia (Macadamia integrifolia Maiden & Betche) dapat dilihat pada Gambar 2.1
Gambar 2.1 Pohon makadamia 2.1.2 Minyak Makadamia
Ada beberapa jenis metode ekstraksi seperti, ekstraksi pelarut, ekstraksi dengan bantuan gelombang ultrasonik, ekstraksi soklet dan ekstraksi CO2 super kritis, digunakan untuk mengekstrak minyak dari kacang Macadamia integrifolia, yang juga disebut minyak kacang makadamia (Zhu, 2013). Minyak makadamia di ekstrak dari kacang makadamia yang sudah matang di mana kacang makadamia mengandung minyak yang tinggi. Langkah awal dari produksi minyak makadamia yaitu pengupasan cangkang kacang makadamia menggunakan mesin kemudian cangkang yang diperoleh di dehidrasi sampai kadar air mendekati 3.5% dasar kering. Salah satu teknik yang digunakan dalam ekstraksi ini adalah pengepresan dingin (cold pressed) dengan temperatur 30ºC menggunakan teknik mekanik.
Minyak makadamia dengan pengepresan dingin berwarna kuning emas jernih dengan aroma dan rasa kacang (Tan, 2020). Beberapa teknik juga dapat digunakan untuk mengekstrak minyak esensial dari berbagai bagian tanaman aromatik,
misalnya destilasi air atau uap, dan ekstraksi pelarut. Minyak esensial adalah minyak alami, kompleks dan multikomponen sistem yang terutama terdiri dari terpena di samping beberapa komponen non terpena lainnya (Edris, 2007)
.
Menurut Shutes, minyak kualitas terapi (therapeutic grade) merupakan istilah yang diadakan oleh perusahaan produksi minyak essential dan ditujukan untuk pemasaran. Terdapat empat jenis tingkatan essential oil yang beredar di pasaran:
1) Therapeutic Grade Essential Oil (Grade A). Merupakan minyak esensial murni yang dibuat dari bahan alami dengan 100% bagian tumbuhan yang diperlukan, 2) Food Grade (Grade B). Merupakan minyak esensial yang bisa digunakan untuk bahan tambahan dalam makanan,
3) Perfume Grade (Grade C). Merupakan minyak esensial yang dicampur dengan bahan tambahan lain yang bisa mencapai 50%,
4) Floral Water. Merupakan tingkatan terendah minyak esensial yang dibuat dengan proses destilasi dari therapeutic grade dan berfungsi memberikan wangi pada produk pakai sehari-hari (CNN Indonesia, 2020)
.
Minyak makadamia merupakan sumber yang kaya akan oleat (54.6%-63.4%), palmitoleat (12.5%-19.3%), dan asam palmitat (8.1%-9.4%) (Tan, 2020). Asam lemak merupakan asam karboksilat yang memiliki panjang karbon yang bervariasi, dan tidak memiliki rantai cabang. Berdasarkan kejenuhannya, asam lemak dikelompokkan atas asam lemak jenuh dan asam lemak tak jenuh. Asam lemak tak jenuh ada yang memiliki satu ikatan rangkap, yang disebut sebagai MUFA (monounsaturated fatty acid), contohnya asam oleat. Asam lemak yang memiliki ikatan rangkap lebih dari satu disebut PUFA (polyunsaturated fatty acid). Asam linoleat memiliki tiga ikatan rangkap
.
PUFA dan MUFA merupakan asam lemakesensial karena tidak diproduksi di dalam tubuh manusia, namun sangat dibutuhkan untuk memenuhi kebutuhan tubuh, asam-asam lemak tersebut diperoleh melalui makanan (Rauf, 2015)
.
Peroksidase lipid dapat merusak membran sel, namun keberadaan asam palmitoleat berperan dalam melindungi membran sel. Penggunaan minyak kacang makadamia dapat melindungi sel dengan cara yang sama, terutama pada kulit yang terpapar sinar matahari berlebihan
.
Minyak makadamia juga merupakan emolien yang sangat baik dan memiliki hasil akhir pada kulit yang baik, oleh karena itu minyak makadamia digunakan dalam berbagai produk kosmetik termasuk lipstik, pelembab kulit, tabir surya, sampo, dan sediaan kulit lainnya (Akhtar dkk., 2006).Minyak makadamia dengan cepat menembus kulit, menghaluskan kulit dan mempengaruhi kondisi dan fungsi dari kulit dengan tepat sehingga bisa digunakan dalam produk yang ditujukan untuk memutihkan bintik hitam, meregenerasi kulit setelah terpapar radiasi sinar UV secara berlebihan dan mengurangi kerutan (Michalak dan Dadasiewicz, 2019)
.
Minyak makadamia banyak digunakan dalam industri makanan seperti digunakan secara langsung dengan cara memerciknya di atas hidangan
.
Kacang makadamia mempunyai kandungan lemak sehat sekitar 70% dan protein sekitar 8%.
Kacang makadamia mengandung pati, kalsium, zat besi, fosfor, magnesium, dan tiamin.
Minyak makadamia sering digunakan sebagai penunjang terapi alami pemulihan kecanduan alkohol, pemulihan gangguan hati, mengatasi gangguan anemia, dan membersihkan saluran pembuluh nadi jantung. Hasil studi menunjukkan bahwa mengonsumsi sekitar 40 gram kacang makadamia (setaradengan 305 kalori) dapat menurunkan kolesterol jahat (LDL) hingga 9% dalam waktu 5 minggu (Puspitojati dkk., 2017)
.
Tokoferol, tokotrienol dan squalene terdapat dalam kacang makadamia dan memiliki sifat antioksidan, tetapi manfaat terhadap stabilitas oksidatifnya belum dapat didefinisikan. Kacang makadamia mengandung tokoferol yang rendah bila dibandingkan dengan kacang almond dan pecan. Kacang makadamia juga mengandung fitosterol dengan konsentrasi yang signifikan terutama β-fitosterol.
Squalene banyak terdapat dalam minyak zaitun, biji labu dan quinoa. Dalam kacang makadamia, konsentrasi squalene adalah 185 µg/g minyak makadamia (Wall, 2010)
.
Minyak esensial memiliki potensi terapi karena aroma menguap dari minyak esensial yang dapat digunakan dalam pencegahan atau terapi penyakit. Minyak esensial menunjukkan aktivitas bakterisida terhadap mikroorganisme patogen mulut dan gigi dan dapat dimasukkan ke dalam obat kumur untuk pengendalian infeksi awal atau sebagai rutinitas untuk mengontrol plak (Edris, 2007). Beberapa minyak esensial telah terbukti menangkal radikal bebas dan sifat antioksidan diuji dengan radikal DPPH pada suhu kamar. Aktivitas antioksidan minyak esensial tidak dapat hanya dikaitkan dengan adanya komponen fenolik; alkohol monoterpene, keton, aldehida, hidrokarbon dan eter juga berkontribusi terhadap aktivitas peredaman radikal bebas beberapa minyak esensial. Beberapa jenis minyak esensial yang dianggap memiliki aktivitas antioksidan memungkinkan untuk diformulasikan sebagai bagian dari suplemen atau zat tambahan untuk mencegah stress oksidatif yang berkontribusi pada banyak penyakit degeneratif (Edris, 2007)
.
2.2 Radikal Bebas
Secara fisiologi, sel akan membentuk radikal bebas sebagai produk reaksi biokimia yang memerlukan oksigen yang terjadi di dalam tubuh. Radikal bebas oksigen adalah hasil metabolisme normal yang dihasilkan sel untuk mengubah makanan dan oksigen menjadi energi (Sari, 2019). Tubuh manusia dapat menetralisir radikal bebas bila jumlahnya tidak berlebihan. Mekanisme pertahanan tubuh dari radikal bebas adalah berupa antioksidan di tingkat sel, membran, dan ekstra sel (Werdhasari, 2014)
.
Radikal bebas adalah molekul atau fragmen molekul yang memiliki satu atau lebih elektron tidak berpasangan dalam orbital atom atau molekul. Hal ini menyebabkan molekul tersebut berusaha mencari dan menangkap elektron dari zat lain untuk menetralisir diri mereka sendiri. Radikal yang lebih reaktif dan kurang stabil dari pasangan non-radikalnya. Derivat non radikalnya atau oksidan dapat diubah dengan mudah menjadi radikal bebas melalui berbagai reaksi pada organisme (Sari, 2019). Radikal bebas juga dapat didefinisikan sebagai setiap spesies yang mampu berada secara independen dan memiliki satu atau lebih elektron tak berpasangan (unpaired electrone), yaitu elektron yang sendirian dalam orbital. Lambang dot radikal (.) digunakan untuk menandai adanya satu atau lebih elektron tak berpasangan (Santoso, 2016)
.
Reaksi pembentukan radikal bebas dalam oksidasi asam lemak dibagi atas tiga tahap yaitu,
1) Inisiasi. Pada tahap ini, adanya panas atau cahaya akan melepas atom hidrogen dari asam lemak membentuk radikal alkil bebas dan radikal hidrogen. Selanjutnya oksigen bereaksi dengan radikal alkil membentuk radikal peroksil,
2) Propagansi. Terjadi reaksi berantai dari senyawa radikal peroksil dengan atom hidrogen dari asam lemak yang lain, membentuk komponen hidroperoksida dan radikal peroksil,
3) Terminasi. Komponen-komponen radikal saling bereaksi membentuk komponen non-radikal. Pada tahap ini terbentuk komponen rantai pendek dengan berat molekul yang kecil sehingga mudah menguap dan memberikan aroma tengik (Rauf, 2015)
.
Jalur terbentuknya radikal bebas dalam sel makhluk hidup berlangsung melalui reaksi enzimatik dan non enzimatik yaitu berasal dari sumber endogen maupun eksogen. Radikal bebas endogen dibentuk dari aktivasi sel imun, inflamasi, keadaan stres mental, olahraga berlebihan, iskemik, kanker dan penuaan. ROS/RNS eksogen berasal dari polusi udara dan air, asap rokok, alkohol, logam berat atau transisi, obat-obatan, pelarut industri, memasak (daging asap, minyak bekas, lemak), radiasi. Penelitian menunjukkan bahwa radikal bebas memiliki pengaruh yang signifikan terhadap penuaan, bahwa kerusakan akibat radikal bebas dapat di kontrol dengan pertahanan antioksidan yang memadai, dan bahwa asupan nutrisi antioksidan yang optimal dapat berkontribusi pada peningkatan kualitas hidup.
Pengurangan radikal bebas atau penurunan tingkat produksinya dapat menunda penuaan yang terlalu cepat. Beberapa antioksidan nutrisi akan memperlambat proses penuaan. Penelitian terbaru menunjukkan bahwa antioksidan bahkan dapat secara positif mempengaruhi rentang hidup (Sari, 2019)
.
2.3 Antioksidan
Secara kimia senyawa antioksidan adalah senyawa pemberi elektron (elektron donor). Secara biologis, pengertian antioksidan adalah senyawa yang dapat
menangkal atau meredam dampak negatif oksidan
.
Antioksidan bekerja dengan cara mendonorkan satu elektronnya kepada senyawa yang bersifat oksidan sehingga aktivitas senyawa oksidan tersebut dapat di hambat (Sayuti dan Yenrina, 2015).
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya cuma-cuma kepada molekul radikal bebas tanpa terganggu sama sekali fungsinya dan dapat memutus reaksi berantai dari radikal bebas (Ramadhan, 2015).
Antioksidan bermanfaat dalam mencegah kerusakan oksidatif yang disebabkan radikal bebas dan ROS sehingga mencegah terjadinya berbagai macam penyakit seperti kardiovaskuler, jantung koroner, kanker, serta penuaan dini
.
Penambahan antioksidan ke dalam formulasi makanan, juga efektif mengurangi oksidasi lemak yang menyebabkan ketengikan, toksisitas, dan destruksi biomolekul yang ada dalam makanan (Ramadhan, 2015)
.
Antioksidan dibentuk oleh tiga kelompok molekul yang berbeda. Antioksidan diklasifikasikan menjadi dua:
1) Enzim (superoksida dismutase, katalase, glutation peroksidase serta kelompok glutation transferase)
.
2) non enzim
a. Protein sekuestrasi logam (feritin dan seruloplasmin)
b. Molekul dengan berat yang rendah (vitamin C atau asam askorbat), vitamin E (α-tokoferol), dan lain-lain
c. Glutation, Flavonoid
Berdasarkan sumbernya antioksidan dapat dikelompokkan meliputi:
a) Antioksidan endogen: Bilirubin, tiol, misalnya: glutation, asam lipoat, N-asetil sistein, NADPH dan NADH, ubiquinone, asam urat, enzim SOD, katalase, glutation peroksidase
.
b) Antioksidan eksogen: Vitamin C, vitamin E, beta karoten dan karotenoid dan oksikarotenoid lainnya, misalnya: Likopen dan lutein, polifenol, misalnya flavonoid, flavon, flavonol, dan proantosianidin (Sari, 2019)
.
Vitamin E adalah nutrisi esensial yang berfungsi sebagai antioksidan di dalam tubuh manusia. Disebut esensial karena tubuh tidak dapat membuat sendiri, sehingga harus disediakan dari makanan. Tokoferol terdapat dalam minyak, kacang, gandum, padi. Absorpsi tokoferol di dalam usus berhubungan dengan absorpsi lemak. Lebih kurang 40% tokoferol yang dimakan akan diabsorpsi. Fungsi utama vitamin E adalah mencegah peroksidase membran fosfolipid. Karakterisasi vitamin E yang lipofilik memungkinkan tokoferol berada di lapisan dalam sel membran. Tokoferol OH dapat memindahkan atom hidrogen dengan satu elektron ke radikal bebas dan membersihkan radikal bebas sebelum radikal bebas bereaksi dengan protein membran sel atau bereaksi membentuk lipid peroksidase (Ramadhan, 2015)
.
2.4 Vitamin C
Vitamin C termasuk senyawa alami yang memiliki sifat antioksidan kuat dan pengikat radikal bebas, serta mencegah kerusakan yang ditimbulkan oleh molekul superoksida, peroksida, radikal hidroksil, dan oksigen singlet. Termasuk katalase dan peroksidase antioksidan pencegah dan antioksidan pemutus ikatan yang mengikat radikal untuk mencegah timbulnya radikal bebas dan reaksi propagansi berantai. Antioksidan pemotong ikatan yang larut dalam air, termasuk vitamin C,
asam urat, sistein, glutation, sementara antioksidan yang larut dalam lemak antara lain vitamin E yang berfungsi dalam membran sel. Vitamin C mengikat superoksida dan radikal hidroksil, juga bereaksi langsung dengan hidrogen peroksida, oleh karena itu mencegah terhadap berbagai radikal bebas yang toksik yang menyebabkan oksidasi lemak. Sebagai contoh, timbulnya jenis oksigen toksik karena fagosit berhubungan dengan sejumlah degenerasi kronis dan kondisi inflamasi, termasuk kanker, artritis, dan penyakit paru-paru. Penelitian laboratorium telah menunjukkan bahwa vitamin C menetralkan oksidan yang berbahaya tersebut yang ditimbulkan oleh fagosit (Goodman, 2000)
.
Vitamin C/asam askorbat, merupakan antioksidan penting karena bekerja di lingkungan tubuh dengan kadar air yang tinggi. Pasangan antioksidan utama vitamin C adalah vitamin E dan karotenoid serta bekerja dengan enzim antioksidan.
Vitamin C bekerja sama dengan vitamin E untuk meregenerasi α-tokoferol dari radikal α-tokoferol dalam membran dan lipoprotein, dan juga meningkatkan kadar glutation dalam sel, sehingga vitamin C berperan penting dalam perlindungan protein grup tiol terhadap oksidasi. Vitamin C adalah agen pereduksi dan demikian menetralkan ROS seperti hidrogen peroksida (Sari, 2019)
.
2.5 Pengukuran Aktivitas Antioksidan
Radikal bebas memiliki waktu paruh yang relatif singkat, dan karena itu pengukuran kadar radikal bebas sangat sulit. Data tentang radikal bebas dapat diperoleh dengan melihat hasil peroksidase lipid seperti malondialdehyde, dan dengan memonitor aktivitas enzim seperti superoksida dismutase (SOD), katalase, glutathione peroksidase (Sari, 2019). Struktur kimia dari radikal bebas DPPH dapat dilihat pada Gambar 2.2
Gambar 2.2 Struktur kimia 1,1,2,2-diphenyl picrylhydrazyl (DPPH) DPPH merupakan senyawa radikal organik nitrogen yang stabil
.
Senyawa radikal sintetik ini merupakan metode sederhana yang digunakan sebagai petunjuk awal bahwa suatu komponen atau ekstrak memiliki aktivitas antioksidan.
Pengujian didasarkan pada pengukuran kemampuan pereduksi terhadap radikal DPPH.Pengukuran dapat dilakukan dengan electron spin resonance (EPR) atau dengan pengukuran penurunan absorbansi (Rauf, 2015)
.
Semakin tajam penurunan absorbansi, semakin besar aktivitas antioksidannya (Santoso, 2016).
Metode DPPH (1,1-diphenyl-2-picrylhydrazyl) menggunakan radikal chrogen yang stabil dalam metanol yang memberikan warna ungu tua. Dengan penambahan DPPH, warna larutan memudar dan reduksi dimonitor oleh penurunan absorbansi
.
Ketika larutan DPPH dicampur dengan zat yang menyumbangkan atom hidrogen, akan diperoleh bentuk radikal tereduksi disertai warna ungu yang hilang (Sari, 2019)
.
Metode DPPH menggunakan IC50 sebagai parameter untuk menentukan konsentrasi senyawa antioksidan yang mampu menghambat 50% oksidasi.
Semakin kecil nilai IC50, maka semakin tinggi aktivitas antioksidan
.
Kemudian, dibuat kurva hubungan antara konsentrasi dan persen inhibisi untuk menentukan nilai IC50 (Inhibitory Concentration 50%).
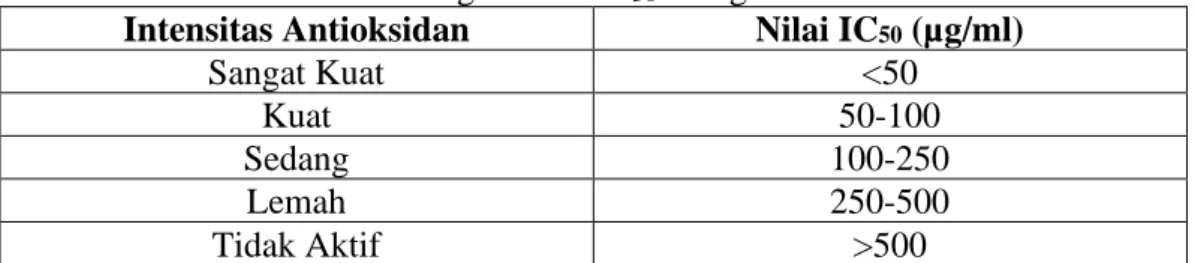
IC50 dijadikan parameter untukmembandingkan antioksidan. Kategori nilai IC50 sebagai antioksidan dapat dilihat pada Tabel 2.1
Tabel 2.1 Kategori nilai IC50 sebagai antioksidan Intensitas Antioksidan Nilai IC50 (µg/ml)
Sangat Kuat <50
Kuat 50-100
Sedang 100-250
Lemah 250-500
Tidak Aktif >500
(Lung dan Destiani, 2017).
Lavenia (2017) melakukan penelitian uji aktivitas antioksidan minyak makadamia dengan menggunakan metode DPPH, diukur pada panjang gelombang maksimum yaitu 516 nm. Hasil analisis menunjukkan bahwa semakin meningkat konsentrasi sampel, maka aktivitas peredaman DPPH semakin meningkat karena semakin banyak DPPH yang berpasangan dengan atom hidrogen dari minyak makadamia dan vitamin C sehingga serapan DPPH menurun. Pada penelitian yang dilakukan, hasil yang didapatkan berupa nilai IC50 minyak makadamia sebesar 100,4 µg/ml dan vitamin C sebesar 2,79 µg/ml. Hasil ini menunjukkan bahwa minyak makadamia memiliki aktivitas antioksidan yang kuat dan vitamin C sebagai pembanding memiliki aktivitas antioksidan yang sangat kuat (Lavenia, 2017).
Pengujian aktivitas antioksidan non enzimatis pada tanaman dan bahan pangan umumnya dapat dilakukan menggunakan metode yang berbasis air 2,2-difenil-1- pikrilhidrazil (DPPH) (reaksi dengan radikal bebas), Ferric Reducing Antioxidant Power (FRAP) (reaksi reduksi-oksidasi), Ferrous Ion Chelating (FIC) (reaksi kelat atau melalui pembentukan komplek), dan yang berbasis lemak biasanya dengan Thiobarbituric acid (TBA) (Maryam, dkk, 2015).
FRAP (Ferric Reducing Antioxidant Power) merupakan metode penentuan kandungan aktivitas antioksidan yang dilakukan secara spektrofotometri yang
berdasarkan pada reduksi analog ferroin, kompleks Fe3+ dari tripiridiltriazin Fe(TPTZ)3+ menjadi kompleks Fe2+, Fe(TPTZ)2+ yang berwarna biru intensif oleh antioksidan pada suasana asam. Kelebihan metode FRAP adalah metodenya murah, reagennya mudah disiapkan dan cukup sederhana dan cepat. Pada metode pengujian CUPRAC (Cupric Ion Reducing Antioxidant Capacity), reagen Cu(II)- neokuproin (Cu(II)-(Nc)2) digunakan sebagai agen pengoksidasi kromogenik karena reduksi ion Cu(II) dapat diukur. Pereaksi CUPRAC merupakan pereaksi yang selektif karena memiliki nilai potensial reduksi yang rendah. ABTS (2,2’- Azinobis (3-ethylbenzothiazoline-6-sulfonic acid-diammonium salt) merupakan metode pengukuran aktivitas antioksidan dengan prinsip pengujian adalah penghilangan warna kation ABTS untuk mengukur antioksidan yang langsung bereaksi dengan radikal kation ABTS (Maryam, dkk, 2015)
.
2.6 Spektrofotometri Ultraviolet Dan Sinar Tampak
2.6.1 Aspek Kuantitatif Spektrofotometri Ultraviolet Sinar Tampak
Spektroskopi merupakan kajian yang melibatkan interaksi antara radiasi elektromagnetik (REM) dengan sampel. Spektroskopi ultraviolet sinar tampak (UV-Vis) merupakan bagian dari REM yang mempunyai panjang gelombang 200- 800 nm (Rohman dkk., 2019)
.
Penyerapan (absorpsi) sinar UV dan sinar tampak pada umumnya dihasilkan oleh eksitasi elektron-elektron ikatan, akibatnya Panjang gelombang pita yang mengabsorpsi dapat dihubungkan dengan ikatan yang mungkin ada dalam suatu molekul. Dalam aspek kuantitatif, suatu berkas radiasi dikenakan pada cuplikan (larutan sampel) dan intensitas sinar radiasi yang diteruskan diukur besarnya.
Radiasi yang diserap oleh cuplikan ditentukan dengan membandingkan intensitas sinar yang diteruskan dengan intensitas sinar yangdiserap jika tidak ada spesies penyerap lainnya. Intensitas atau kekuatan radiasi cahaya sebanding dengan jumlah foton yang melalui satu satuan luas penampang per detik. Serapan dapat terjadi jika foton/radiasi yang mengenai cuplikan memiliki energi yang sama dengan energi yang dibutuhkan untuk menyebabkan terjadinya perubahan tenaga. Kekuatan radiasi juga mengalami penurunan dengan adanya penghamburan dan pemantulan cahaya, akan tetapi penurunan karena hal ini sangat kecil dibandingkan dengan proses penyerapannya (Gandjar dan Rohman, 2018).
2.6.2 Hal-hal Yang Harus Diperhatikan Dalam Analisis Spektrofotometri Ultraviolet dan Sinar Tampak
Pembentukan molekul yang dapat menyerap sinar ultraviolet dan sinar tampak dilakukan jika senyawa yang dianalisis tidak menyerap pada daerah tersebut. Cara yang digunakan adalah dengan mengubah menjadi senyawa lain atau direaksikan dengan pereaksi tertentu. Pereaksi yang digunakan harus memenuhi beberapa persyaratan yaitu:
- Reaksinya selektif dan sensitif
- Reaksinya cepat, kuantitatif, dan teratur
- Hasil reaksi stabil dalam jangka waktu yang lama
Keselektifan dapat dinaikkan dengan mengatur pH, pemakaian masking agent, atau penggunaan teknik ekstraksi (Gandjar dan Rohman, 2018).
Waktu operasional biasa digunakan untuk pengukuran hasil reaksi atau pembentukan warna. Tujuannya adalah untuk mengetahui waktu pengukuran yang stabil. Waktu operasional ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbansi larutan. Pada saat awal terjadi reaksi, absorbansi senyawa yang berwarna ini meningkat sampai waktu tertentu hingga diperoleh waktu absorbansi yang stabil. Semakin lama waktu pengukuran, maka ada
kemungkinan senyawa yang berwarna tersebut menjadi rusak atau terurai sehingga intensitas warnanya turun akibat absorbansinya juga turun (Gandjar dan Rohman, 2018).
Pemilihan panjang gelombang untuk analisis kuantitatif adalah Panjang gelombang yang mempunyai absorbansi maksimal. Untuk memilih panjang gelombang maksimal, dilakukan dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi tertentu. Ada beberapa variabel yang dapat mempengaruhi absorbansi yaitu: jenis pelarut, pH larutan, suhu, konsentrasi tinggi dan zat-zat pengganggu (Gandjar dan Rohman, 2018).
Pembuatan kurva baku dibuat seri larutan baku dari zat yang akan dianalisis dengan berbagai konsentrasi. Masing-masing absorbansi larutan dengan berbagai konsentrasi diukur, kemudian dibuat kurva yang merupakan hubungan antara absorbansi (y) dengan konsentrasi (x). Kurva baku sebaiknya sering diperiksa ulang (Gandjar dan Rohman, 2018). Pembacaan absorbansi sampel atau cuplikan yang terbaca pada spektrofotometer hendaknya antara 0,2 sampai 0,8 atau 15% sampai 70% jika dibaca sebagai transmitan. Anjuran ini berdasarkan anggapan bahwa kesalahan dalam pembacaan T adalah 0,005 atau 0,5% (kesalahan fotometrik) (Gandjar dan Rohman, 2018).
BAB III
METODE PENELITIAN 3.1 Alat dan Bahan
3.1.1 Alat
Alat-alat yang digunakan dalam penelitian ini meliputi aluminium foil, beaker glass, bola karet, kaca arloji, kuvet, labu tentukur, mikro pipet (Volac), neraca analitik (Sartorius), pipet volume, pipet tetes, spatula, spektrofotometer sinar tampak (Shimadzu UV–1800 Series), stopwatch, vortex (Boeco Germany). Contoh Gambar alat-alat penelitian dapat dilihat pada Lampiran 4 halaman 40.
3.1.2 Bahan
Bahan kimia yang digunakan pada penelitian ini adalah DPPH (PT. Smartlab Indonesia), metanol pro analisis, n-heksan pro analisis, vitamin C (Emsure ACS) dan sampel minyak makadamia food grade (Green Tosca) dan therapeutic grade (Darjeeling). Gambar minyak makadamia food grade (Green Tosca) dan therapeutic grade (Darjeeling) dapat dilihat pada Lampiran 3 halaman 39.
3.2 Pengumpulan Bahan
Sampel yang digunakan adalah minyak makadamia Green Tosca (Food grade) yang diperoleh dari Brastagi Supermarket, Jalan Gatot Subroto, Kota Medan, Provinsi Sumatera Utara dan minyak makadamia Darjeeling (Therapeutic Grade) yang diperoleh dari marketplace Shopee Darjeelingstore. Sertifikat analisis minyak makadamia food grade (Green Tosca) dan therapeutic grade (Darjeeling) masing- masing dapat dilihat pada Lampiran 1 dan 2 halaman 36 sampai 38.
3.3 Pengujian Aktivitas Antioksidan dengan Metode Peredaman DPPH 3.3.1 Pembuatan Larutan Induk DPPH (0,5 mM)
Sebanyak 10 mg DPPH ditimbang, kemudian dilarutkan dengan metanol dalam labu tentukur 50 ml, lalu volumenya dicukupkan dengan metanol sampai garis tanda (konsentrasi 200 µg/ml). Larutan dijaga pada suhu ruang, terlindung dari cahaya untuk segera digunakan (Molyneux, 2004). Bagan prosedur dapat dilihat pada Lampiran 5 halaman 41.
3.3.2 Pembuatan Larutan Blanko
Larutan DPPH 0,5 mM (konsentrasi 200 µg/ml) dipipet sebanyak 1 ml, kemudian dimasukkan ke dalam labu tentukur 5 ml, lalu dicukupkan volumenya dengan metanol sampai garis tanda (konsentrasi 40 µg/ml). Bagan prosedur dapat dilihat pada Lampiran 5 halaman 41.
3.3.3 Pembuatan Kurva Absorbansi Maksimum DPPH
Larutan DPPH konsentrasi 40 µg/ml dihomogenkan dan diukur serapannya pada panjang gelombang sinar tampak 400-800 nm, serta termasuk dalam rentang panjang gelombang DPPH yang berkisar antara 515-520 nm (Molyneux, 2004).
3.3.4 Penentuan Waktu Kerja
Lama pengukuran waktu kerja pada metode DPPH menurut beberapa literatur yang direkomendasikan adalah 30 menit (Molyneux, 2004; Wei dan Shibamoto, 2007).
3.3.5 Pembuatan Larutan Induk Sampel
Sebanyak 25 mg masing-masing sampel minyak makadamia Green Tosca (Food grade) dan Darjeeling (Therapeutic Grade) ditimbang kemudian dilarutkan dengan n-heksan dalam labu tentukur 25 ml dan dicukupkan volumenya dengan
metanol sampai garis tanda, lalu dihomogenkan dengan vortex selama 1 menit (konsentrasi 1000 µg/ml) (Lavenia, 2017)
.
3.3.6 Pembuatan Larutan Uji Sampel
Larutan induk dari sampel minyak makadamia Green Tosca (Food grade) dan Darjeeling (Therapeutic Grade) masing-masing dipipet sebanyak 0,25 ml; 0,5 ml;
0,75 ml; 1 ml, kemudian dimasukkan ke dalam labu tentukur 5 ml (untuk mendapatkan konsentrasi 50, 100, 150 dan 200 µg/ml), kemudian ke dalam masing- masing labu tentukur ditambahkan 1 ml larutan DPPH 0,5 mM (untuk mendapatkan konsentrasi DPPH 40 µg/ml) lalu volume dicukupkan dengan metanol sampai garis tanda, didiamkan di tempat gelap pada suhu ruang selama 30 menit, kemudian dihomogenkan dengan vortex selama 1 menit, lalu diukur serapannya menggunakan spektrofotometer sinar tampak pada panjang gelombang 515,5 nm (Lavenia, 2017). Bagan prosedur dapat dilihat pada Lampiran 5 halaman 43 3.3.7 Pembuatan Larutan Induk Vitamin C
Sebanyak 25 mg vitamin C ditimbang, kemudian dilarutkan dalam labu tentukur 50 ml dengan metanol lalu volumenya dicukupkan dengan metanol sampai garis tanda (konsentrasi 500 µg/ml)
.
3.3.8 Pembuatan Larutan Uji Vitamin C
Larutan induk vitamin C dipipet sebanyak 0,02 ml; 0,04 ml; 0,06 ml; 0,08 ml kemudian masing-masing dimasukkan ke dalam labu tentukur 5 ml (untuk mendapatkan konsentrasi 2 µg/ml, 4 µg/ml, 6 µg/ml, 8 µg/ml), kemudian dalam masing-masing labu tentukur ditambahkan 1 ml larutan DPPH 0,5 mM (untuk mendapatkan konsentrasi DPPH 40 µg/ml) lalu volume dicukupkan dengan metanol sampai garis tanda, didiamkan di tempat gelap pada suhu ruang selama 30
menit, kemudian dihomogenkan dengan vortex selama 1 menit, lalu diukur serapannya menggunakan spektrofotometer sinar tampak pada panjang gelombang 515,5 nm. Larutan uji vitamin C digunakan sebagai pembanding. Bagan prosedur dapat dilihat pada Lampiran 5 halaman 43.
3.3.9 Penentuan Persen Peredaman
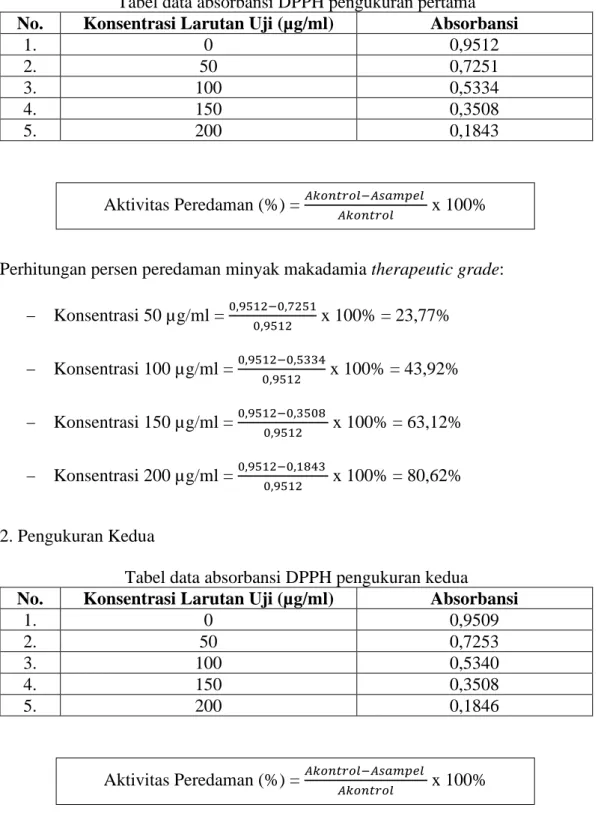
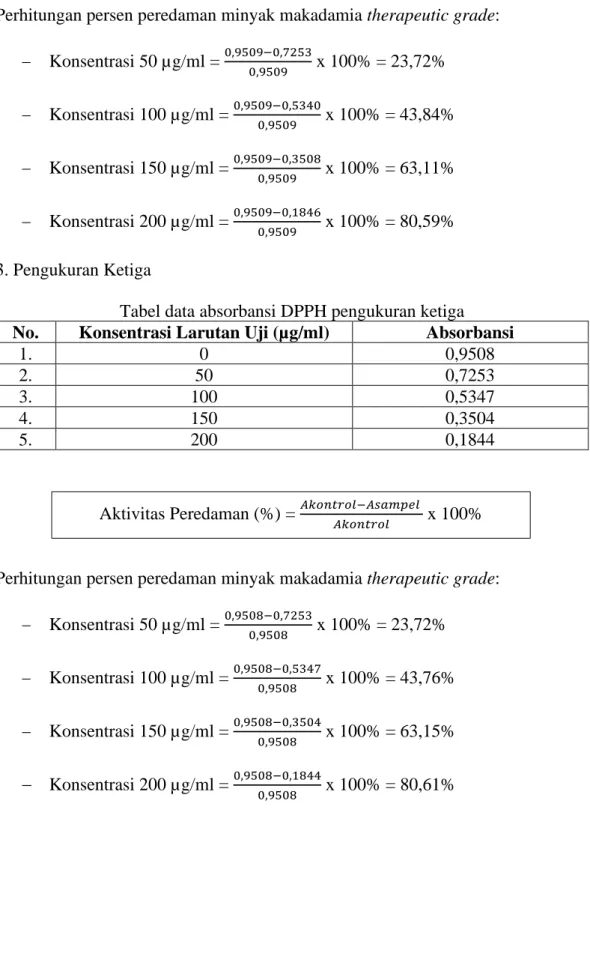
Kemampuan antioksidan diukur sebagai penurunan serapan larutan DPPH (peredaman warna ungu DPPH) akibat adanya penambahan larutan uji. Persentase peredaman dapat dihitung dengan menggunakan rumus:
% Peredaman = (A kontrol − A sampel
A kontrol ) x 100%
Keterangan:
A kontrol = Absorbansi tidak mengandung sampel A sampel = Absorbansi sampel
3.3.10 Penentuan Nilai IC50 Sampel Uji dan Vitamin C
Nilai IC50 merupakan bilangan yang menunjukkan konsentrasi sampel uji (µg/ml) yang memberikan peredaman DPPH sebesar 50% (mampu meredam proses oksidasi DPPH sebesar 50%). Nilai IC50 sampel uji dan vitamin C diperoleh dari kurva kalibrasi dengan analisis regresi linier dengan memplotkan antara volume sampel uji dengan persentase peredaman radikal bebas DPPH. Hasil yang diperoleh disubstitusikan ke dalam persamaan regresi di mana sumbu X adalah volume sampel uji dan sumbu Y adalah persentase peredaman radikal bebas DPPH.
Persentase peredaman yang diperoleh dapat digunakan dalam pembuatan kurva kalibrasi.
Penentuan nilai IC50 menggunakan persamaan regresi:
y = ax + b
Keterangan:
y = persentase aktivitas penangkapan radikal a = slope/gradien
x = volume sampel (ml)
b = intersep/koefisien regresi (Gandjar dan Rohman, 2007).
BAB IV
HASIL DAN PEMBAHASAN 4.1 Kurva Absorbansi Maksimum Larutan DPPH
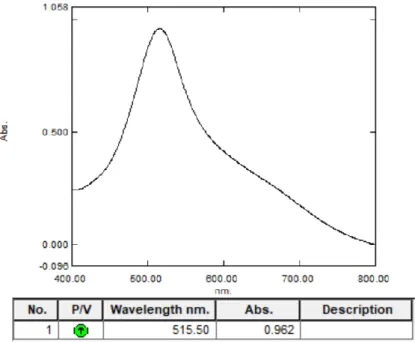
Kurva absorbansi maksimum larutan DPPH 40 µg/ml dalam pelarut metanol dengan menggunakan spektrofotometer sinar tampak menunjukkan serapan maksimum sebesar 0,9620 pada panjang gelombang 515,5 nm. Panjang gelombang 515,5 nm yang diperoleh sesuai secara teoritis di mana panjang gelombang pada serapan maksimum untuk larutan DPPH adalah 515-520 nm (Molyneux, 2004), dan termasuk salah satu dalam kisaran panjang gelombang sinar tampak yaitu 400-800 nm. Kurva absorbansi maksimum larutan DPPH dapat dilihat pada Gambar 4.1.
Gambar 4.1 Kurva absorbansi maksimum larutan DPPH menggunakan spektrofotometer sinar tampak
4.2 Waktu Operasional
Waktu operasional bertujuan untuk mengetahui waktu pengukuran yang stabil.
Waktu operasional ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbansi larutan. Menurut Molyneux (2004) dan Wei dan Shibamoto (2007), waktu reaksi yang direkomendasikan adalah 30 menit.
4.3 Persamaan Regresi
Persamaan regresi digunakan untuk mengukur IC50 dimana persamaan regresi didapatkan dari data pengukuran kurva kalibrasi larutan uji sampel dan vitamin C pada masing-masing konsentrasi sehingga diperoleh nilai absorbansi setiap sampel.
Perhitungan data hasil persamaan regresi setiap sampel dapat dilihat pada Lampiran 7 halaman 50 sampai 51 dan perhitungan data hasil persamaan regresi vitamin C yang menunjukkan aktivitas antioksidan dapat dilihat pada Lampiran 7 halaman 52.
4.4 Aktivitas Antioksidan Sampel Uji dan Vitamin C
Aktivitas antioksidan minyak makadamia Green Tosca (Food grade) dan Darjeeling (Therapeutic Grade) dengan penambahan larutan uji konsentrasi 50 µg/ml, 100 µg/ml, 150 µg/ml, dan 200 µg/ml. Untuk vitamin C dilakukan dengan penambahan larutan uji konsentrasi 2 µg/ml, 4 µg/ml, 6 µg/ml, dan 8 µg/ml. Hasil analisis aktivitas antioksidan sampel uji dan vitamin C menunjukkan bahwa kenaikan konsentrasi sampel menyebabkan terjadinya penurunan nilai absorbansi.
Adanya aktivitas antioksidan dari sampel mengakibatkan perubahan warna pada larutan DPPH dalam metanol yang semula berwarna violet pekat menjadi kuning pucat. Hasil persentase peredaman DPPH pada tiap sampel dan vitamin C dapat dilihat pada Lampiran 6 halaman 44 sampai 49.
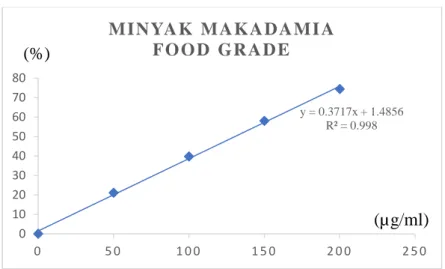
Setelah mendapatkan data persen peredaman, maka dibuat grafik antara konsentrasi larutan (x) dan persen peredaman (y) sehingga didapatkan persamaan regresi lainnya. Grafik hasil pengukuran peredaman DPPH terhadap kedua sampel dan vitamin C dapat dilihat pada Gambar 4.2 sampai dengan Gambar 4.4.
Gambar 4.2 Kurva kalibrasi peredaman DPPH oleh sampel minyak makadamia Green Tosca (Food grade)
Gambar 4.3 Kurva kalibrasi pengukuran peredaman DPPH oleh sampel minyak makadamia Darjeeling (Therapeutic Grade)
Gambar 4.4 Kurva kalibrasi peredaman DPPH oleh vitamin C
Dari gambar di atas, dapat dilihat bahwa terjadi peningkatan persentase peredaman dengan adanya peningkatan konsentrasi senyawa antioksidan. Hal ini
y = 0.3717x + 1.4856 R² = 0.998
0 10 20 30 40 50 60 70 80
0 5 0 1 0 0 1 5 0 2 0 0 2 5 0
M I N YA K M A K A D A M I A FO O D G R A D E
(%)
(µg/ml)
y = 0.4012x + 2.1424 R² = 0.9967
0 20 40 60 80 100
0 5 0 1 0 0 1 5 0 2 0 0 2 5 0
M I N YA K M A K A D A M I A T H E R A PE U T I C G R A D E
y = 7.2976x + 0.7819 R² = 0.9986
0 10 20 30 40 50 60 70
0 2 4 6 8 1 0
V I TA M I N C (%)
(µg/ml)
(%)
(µg/ml)
disebabkan karena terjadinya penurunan absorbansi yang membuktikan adanya aktivitas pemerangkapan radikal bebas DPPH oleh larutan uji yaitu minyak makadamia dan larutan pembanding vitamin C. Peredaman warna DPPH disebabkan oleh adanya senyawa yang bisa memberikan hidrogen kepada radikal DPPH sehingga tereduksi menjadi DPPH-H (1,1-difenil-2-pikrilhidrazin) (Sayuti dan Yenrina, 2015).
Dalam penelitian yang dilakukan Kornsteiner (2006), kenari, pistachio dan pecan mengandung total fenol dan total tokoferol tertinggi di antara semua jenis kacang, diikuti oleh kacang hazelnut dan almon dengan kulit. Antioksidan yang lebih rendah terdapat pada kacang mete dan pinus, sedangkan makadamia menduduki tempat terendah dalam penelitian ini.
Interaksi antioksidan dengan DPPH baik secara transfer elektron atau radikal hidrogen pada DPPH, akan menetralkan radikal bebas dari DPPH. Warna larutan berubah dari ungu tua menjadi kuning pucat dan absorbansi pada panjang gelombang 515,5 nm akan hilang jika semua elektron pada radikal bebas DPPH menjadi berpasangan (Molyneux, 2004).
Hukum Lambert-Beer terbatas karena sifat kimia dan faktor instrumen.
Penyebab non linearitas ini adalah :
- Deviasi koefisien ekstingsi pada konsentrasi tinggi (>0.01M), yang disebabkan oleh interaksi elektrostatik antara molekul karena jaraknya yang terlalu dekat
- Hamburan cahaya karena adanya partikel dalam sampel - Fluoresensi atau fosforesensi sampel
- Berubahnya indeks bias pada konsentrasi yang tinggi
- Pergeseran kesetimbangan kimia sebagai fungsi dari konsentrasi
- Radiasi non-monokromatik; deviasi bisa dikurangi dengan menggunakan bagian yang datar pada absorban yaitu pada panjang gelombang maksimum - Kehilangan cahaya (Dachriyanus, 2004).
Dalam analisis suatu unsur, sering terdapat keterbatasan yang menyebabkan penyimpangan hukum Lambert-Beer. Penyimpangan tersebut menyebabkan hubungan antara absorbansi dan konsentrasi menjadi tidak linear. Keterbatasan yang menyebabkan penyimpangan hukum Lambert-Beer bisa berasal dari gangguan kimia, gangguan instrumen dan gangguan latar (Skoog, 1996).
4.5 Nilai IC50 (Inhibitory Concentration)
Metode DPPH menggunakan IC50 sebagai parameter untuk menentukan konsentrasi senyawa antioksidan yang mampu menghambat 50% oksidasi.
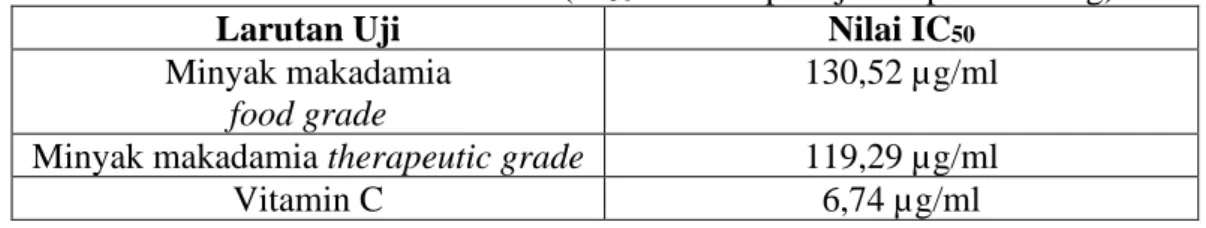
Semakin kecil nilai IC50, maka semakin tinggi aktivitas antioksidan (Lung dan Destiani, 2017). Nilai IC50 diperoleh berdasarkan perhitungan persamaan regresi menggunakan data kurva kalibrasi dengan cara memplot konsentrasi larutan uji dengan persen peredaman DPPH sebagai parameter aktivitas antioksidan, konsentrasi sampel (µg/ml) sebagai absis (sumbu X) dan nilai absorbansi sebagai ordinat (sumbu Y). Perhitungan hasil nilai IC50 pada kedua sampel dan pembanding dapat dilihat pada Lampiran 7 halaman 50 sampai 52. Hasil analisis nilai IC50 pada uji aktivitas antioksidan minyak makadamia dapat dilihat pada Tabel 4.1.
Tabel 4.1 Aktivitas antioksidan (IC50 dari sampel uji dan pembanding)
Larutan Uji Nilai IC50
Minyak makadamia food grade
130,52 µg/ml Minyak makadamia therapeutic grade 119,29 µg/ml
Vitamin C 6,74 µg/ml
Dari Tabel 4.1, diperoleh bahwa minyak makadamia Green Tosca (Food grade) dengan IC50 sebesar 130,52 µg/ml memiliki aktivitas antioksidan dalam kategori sedang dan minyak makadamia Darjeeling (Therapeutic Grade) dengan IC50 sebesar 119,29 µg/ml memiliki sifat antioksidan dalam kategori sedang.
Sedangkan vitamin C dengan IC50 sebesar 6,74 µg/ml memiliki sifat antioksidan dalam kategori sangat kuat. Hal ini dikarenakan vitamin C merupakan senyawa murni sedangkan sampel minyak merupakan senyawa hasil olahan dengan campuran komponen lain berdasarkan metode ekstraksi dan dari data di atas diketahui bahwa, kedua sampel minyak makadamia dan vitamin C mampu menetralisir DPPH. Nilai IC50 berbanding terbalik dengan aktivitas antioksidan, semakin tinggi aktivitas antioksidannya, maka nilai IC50 semakin rendah (Molyneux, 2004).
Senyawa yang memiliki aktivitas sebagai antioksidan bekerja dengan cara memberikan elektron kepada DPPH sehingga atom dengan elektron yang tidak berpasangan mendapat pasangan dan tidak lagi menjadi radikal. Hal ini ditandai dengan larutan berubah dari ungu tua menjadi kuning terang dan absorbansi pada panjang gelombang maksimumnya menurun (Molyneux, 2004). Pada penelitian ini didapatkan nilai IC50 yang berbeda antara dua jenis minyak makadamia dengan konsentrasi yang sama dapat disebabkan karena perbedaan metode ekstraksi minyak dan merek yang berbeda. Pada evaluasi yang dilakukan oleh Navarro dan Rodrigues (2016), dari beberapa metode ekstraksi minyak makadamia, menunjukkan bahwa ekstraksi soklet memberikan hasil minyak tertinggi (sekitar 74,6%) dan minyak ini terdiri dari asam lemak tak jenuh tunggal (sekitar 80%),
oleat dan asam palmitoleat. Komposisi asam lemak ini mendukung penggunaannya dalam formulasi kosmetik, terutama yang ditujukan untuk perawatan kulit.
Menurut Amorati dkk., (2013), perbedaan aktivitas antioksidan minyak juga dapat disebabkan oleh sumber tanaman juga faktor lingkungan yang dapat mempengaruhi komposisi minyak. Minyak dari tanaman yang sama tetapi diperoleh dengan cara ekstraksi yang berbeda juga dapat mempengaruhi aktivitas antioksidannya. Minyak makadamia jenis food grade yang digunakan sebagai sampel berasal dari Australia dan dibuat dengan metode pengepresan dingin dan ditujukan untuk penggunaan campuran pada makanan, sedangkan pada minyak therapeutic grade yang merupakan minyak esensial berasal dari Afrika dan ditujukan untuk penggunaan topikal atau bahan kosmetik biasanya dibuat dengan campuran komponen lain.
Menurut (Yuniwarti, dkk., 2018) minyak makan yang mempunyai aktivitas antioksidan paling tinggi adalah minyak zaitun, VCO (Virgin coconut oil), minyak wijen dan minyak buah merah. Jumlah fenol dalam minyak makan tersebut menunjukkan besarnya aktivitas, tetapi tergantung juga pada struktur fenol dan posisi cincin hidroksilnya. VCO mengandung fenol dan triacylglycerol sehingga mampu berperan sebagai antioksidan. Minyak zaitun juga mengandung fenol dan squalene yang berpotensi sebagai antioksidan. Minyak wijen juga berperan pada peningkatan kesehatan, minyak pandan merah juga berperan dalam menyembuhkan berbagai penyakit (Yuniwarti, dkk., 2018).
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
a. Terdapat perbedaan aktivitas antioksidan pada minyak makadamia food grade dan therapeutic grade yang dipengaruhi oleh beberapa faktor seperti metode ekstraksi, sumber tanaman dan pencampuran komponen lain dalam minyak makadamia.
b. Minyak makadamia therapeutic grade memiliki aktivitas antioksidan yang lebih tinggi dibandingkan dengan minyak makadamia food grade dengan IC50 masing-masing 119,29 µg/ml dan 130,52 µg/ml dengan kategori aktivitas antioksidan sedang dan dibanding dengan nilai IC50 vitamin C sebesar 6,74 µg/ml yang menunjukkan aktivitas antioksidan kategori sangat kuat.
5.2 Saran
Disarankan untuk peneliti selanjutnya untuk melakukan pengujian aktivitas antioksidan berdasarkan proses ekstraksi minyak makadamia yang berbeda seperti ekstraksi dengan bantuan ultrasound dan ekstraksi CO2 superkritis.
DAFTAR PUSTAKA
Abubaker, M., Hawary, S. E., Mahrous, E. A., dan El-Kader, E. M. A. 2017. Study of Nutritional Contents of Macadamia integrifolia Maiden & Betche Leaves, Kernel and Pericarp Cultivated in Egypt. International Journal of Pharmacognosy and Phytochemical Research. 9(12): 1444-1445.
Akhtar, N., Ahmad, M., Madni, A., dan Bakhsh, M. S. 2006. Evaluation of Basic Properties of Macadamia Nut Oil. Gomal University of Research. 22(1): 22- 23.
Barrat, W. 2010. The magic of macadamia uncovering its potential for the cosmetics industry. Oakbrook Terrace: Jindilli, Inc. Halaman 60.
CNN Indonesia. 2020. 4 Tingkatan essensial oil, therapeutic hingga floral water.
[online]. https://www.cnnindonesia.com/gaya-hidup/20200915162649- 260-546823/4-tingkatan-essential-oil-therapeutic-hingga-floral-water.
[diakses; 25 Oktober 2021].
Dachriyanus, D. 2004. Analisis struktur senyawa organik secara spektroskopi.
LPTIK Universitas Andalas.
Direktorat Jenderal Perkebunan. 2006. Pedoman budidaya makademia (Macademia integrifolia). Jakarta: Departemen Pertanian. Halaman 1-4.
Edris, A. E. 2007. Pharmaceutical and Therapeutic Potentials of Essential Oils and Their Individual Volatile Constituents: A Review. Phytotherapy Research.
21(4): 1-4.
Gandjar, I. G., dan Rohman, A. 2018. Kimia farmasi analisis. Yogyakarta: Pustaka Pelajar. Halaman 228-256.
Goodman, S. 2000. Ester-C® vitamin C generasi III. Jakarta: PT Gramedia Pustaka Utama. Halaman 30.
Kornsteiner, M., Wagner, K. H., dan Elmadfa, I. 2006. Tocopherols and Total Fenolic in 10 Different Nut Types. Food Chemistry. 98(2006): 381-387.
Lavenia, R. 2017. Formulasi dan uji efektivitas anti-aging masker gel peel-off yang mengandung minyak makadamia. Skripsi. Fakultas Farmasi. Universitas Sumatera Utara. Medan.
Lung, J. K. S., dan Destiani, D. P. 2017. Uji Aktivitas Antioksidan Vitamin A, C, E dengan Metode DPPH. Farmaka Suplemen. 15(1): 53-56.
Maryam, S., Baits, M., dan Nadia, A. 2015. Pengukuran Aktivitas Antioksidan Ekstrak Etanol Daun Kelor (Moringa oleifera Lam.) Menggunakan Metode FRAP (Ferric Reducing Antioxidant Power). Jurnal Fitofarmaka Indonesia. 2(2): 115-118.
Michalak, M. dan Dadasiewicz, A. K. 2019. Nut Oils and Their Dietic an Cosmetic Significance: A Review. Journal of Oleo Science. 68(2): 5-6.
Molyneux, P. 2004. The Use of The Stable Free Radical Diphenylpicrylhydrazyl (DPPH) For Estimating Antioxidant Activity. Songklanakarin J. Sci.
Technol. 26(2): 212-218.
Navarro, S. L. B., dan Rodrigues, C. E. C. 2016. Macadamia Oil Extraction Methods and Uses for The Defatted Meal Byproduct. Trends in Food Science & Technology. 54: 148.
Puspitojati, T., Siarudin, M., dan Widiyanto, A. 2017. Mengenal hasil hutan bukan kayu: 18 jenis tanaman penghasil minyak lemak. Bogor: Forda Press.
Halaman 41-43.
Ramadhan, P. 2015. Mengenal antioksidan. Yogyakarta: Graha Ilmu. Halaman 17- 20.
Rauf, R. 2015. Kimia pangan. Yogyakarta: Penerbit ANDI. Halaman 103, 107, 112.
Rohman, A., Riyanto, S., Lumakso, F. A., Windarsih, A., dan Indriyani, L. 2019.
Analisis autentikasi makanan: minyak dan lemak. Yogyakarta: Gadjah Mada University Press. Halaman 7.
Santoso, U. 2016. Antioksidan pangan. Yogyakarta: Gajah Mada University Press.
Halaman 11, 74.
Sari, M. I. 2019. Radikal bebas dan antioksidan. Medan: USU Press. Halaman 4- 5, 26, 35, 53, 60.
Sayuti, K., dan Yenrina, R. 2015. Antioksidan alami dan sintetik. Padang: Andalas University Press. Halaman 7.
Shutes, J. The quality of essential oils. [online]. https://naha.org/assets/uploads/
The_Quality_of_Essential_Oils_Journal.pdf. [diakses: 26 Mei 2021].
Skoog, D. 1985. Principles of instrumental analysis: Third edition. Japan: The Dryden Press. Halaman 728-730.
Sayuti, K. dan Yenrina, R. 2018. Antioksidan alami dan sintetik. Padang: Andalas University Press. Halaman 77-78.
Suheryadi, D. 2002. Teknik Perkecambahan Biji Makadamia. Buletin Teknik Pertanian. 7(1): 28.
Tan, C. X., Tan, S. S., dan Tan, S. T. 2020. Cold pressed oils: cold pressed macadamia oil. Malaysia: Academic Press. Halaman 588-592.
Wall, M. M. 2010. Functional Lipid Characteristics, Oxidative Stability, and Antioxidant Activity of Macadamia Nut (Macadamia integrifolia) Cultivars. Food Chemistry. 121(4): 1103.
Wei, A. dan Shibamoto, T. 2007. Antioxidant Activities and Volatile Constituents of Various Essential Oils. Journal of Agricultural and Food Chemistry.
55(5): 1738-1741.
Werdhasari, A. 2014. Peran Antioksidan Bagi Kesehatan. Jurnal Biotek Medisiana Indonesia. 3(2): 60.
Yuniwarti, E. Y. W., Saraswati, T. R., dan Kusdiyantini, E. 2018. Aktivitas Antioksidan Berbagai Minyak Edible Menggunakan Metode DPPH. Buletin Anatomi dan Fisiologi. 3(1): 86.
Zhu, B., Lin, L., Li, J., Lv, G., dan Huang, M. 2013. Comparison of Four Different Extraction Methods of Oil from Macadamia integrifolia. Advanced Materials Research. 160: 3382-3386.
Lampiran 1. Sertifikat Analisis Minyak Makadamia Green Tosca (Food grade)