PENGARUH HYDRAULIC RETENTION TIME (HRT)
DAN RASIO RECYCLE SLUDGE PADA PROSES
ASIDOGENESIS LIMBAH CAIR PABRIK KELAPA
SAWIT (LCPKS) PADA KEADAAN AMBIENT
SKRIPSI
Oleh
AIDIL SAPUTRA
110405066
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
SEPTEMBER 2015
PENGARUH HYDRAULIC RETENTION TIME (HRT)
DAN RASIO RECYCLE SLUDGE PADA PROSES
ASIDOGENESIS LIMBAH CAIR PABRIK KELAPA
SAWIT (LCPKS) PADA KEADAAN AMBIENT
SKRIPSI
Oleh
AIDIL SAPUTRA
110405066
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
SEPTEMBER 2015
Universitas Sumatera Utara
iii
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas limpahan rahmat dan
karunia-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan skripsi
dengan judul “Pengaruh Hydraulic Retention Time (HRT) dan Rasio Recycle Sludge pada Proses Asidogenesis Limbah Cair Pabrik Kelapa Sawit (LCPKS)
pada Keadaan Ambient”, berdasarkan hasil penelitian yang penulis lakukan di Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi
ini merupakan salah satu syarat untuk mendapatkan gelar sarjana teknik.
Hasil penelitian ini:
1. Penelitian ini memberikan informasi mengenai proses loading up dan variasi rasio recycle sludge dalam proses digestasi anaerobik tahapan asidogenesis.
2. Penelitian ini memanfaatkan limbah cair pabrik kelapa sawit dengan
menggunakan keadaan ambient sehingga lebih menghemat energi yang umumnya digunakan untuk pemanas.
3. Penelitian ini memberikan sumbangan ilmu pengetahuan mengenai
pengolahan limbah cair pabrik kelapa sawit.
Selama melakukan penelitian sampai penulisan skripsi ini, penulis banyak
mendapat bantuan dari berbagai pihak, untuk itu penulis mengucapkan
terimakasih dan penghargaan yang sebesar-besarnya kepada:
1. Dr. Eng. Ir. Irvan, M.Si selaku Ketua Jurusan Teknik Kimia USU.
2. Dr. Ir. Fatimah, MT selaku Sekretaris Jurusan Teknik Kimia USU dan
sebagai Dosen Penguji
3. Ir. Bambang Trisakti MT selaku Pembimbing
4. Ir. Seri Maulina, MSChe, PhD selaku Penguji
5. Ir. Renita Manurung, MT selaku Koordinator Skripsi
Penulis menyadari bahwa laporan hasil penelitian ini masih jauh dari sempurna,
oleh karena itu penulis mengharapkan saran dan masukan demi kesempurnaan
iv
skripsi ini. Semoga skripsi ini memberikan manfaat bagi pengembangan ilmu
pengetahuan.
Medan, September 2015
Penulis
Aidil Saputra
v
DEDIKASI
Penulis mendedikasikan skripsi ini kepada:
1. Orang tua penulis, Ayahanda Mayulis dan Ibunda Martina yang sangat
banyak memberikan dukungan moril maupun materil bagi penulis dalam
segala hal.
2. Saudara penulis Selvia Agustin, Ade Kurnia, Oki Dermawan, dan Marsya
Razita serta keluarga penulis yang telah memberikan saran dan semangat
dalam menyelesaikan studi.
3. Rekan penelitian M. Darul Nafis dan rekan-rekan LPPM yaitu Bg Zoeliadi,
Bg Basril Amirza Harahap, Bg Dedy Anwar, Bg Jeni Lubis, Intan Afrilia,
Ramlan, M. Darul Nafis, Rio Agung Prakoso, Ekuino Simanungkalit, Tri
Putra Pasaribu, Khairul Fahmi, Endah Hutabarat, Christianto Sitio dan
Muksalmina.
4. Teman sejawat, adik dan abang/kakak senior serta teman-teman stambuk
2011 terutama Yusrina Ika Putri, Yunasa Addien, Widya Gema Bestari,
Nadya Gema Bestari, Dwi Gita Ferani, Mutiara Mendopa, Rio Nazif,
Erlangga Wicaksana, Oktris Novali Gusti, William, Yos Pawer Ambarita,
Iloan Manalu, dan M. Fauzy Ramadhan Tarigan yang telah banyak
memberikan banyak dukungan, semangat, doa, pembelajaran hidup dan
kenangan tak terlupakan kepada penulis.
5. Seluruh Dosen/Staf Pengajar dan Pegawai Administrasi Departemen Teknik
Kimia yang telah memberikan banyak ilmu yang berharga dan bantuan
kepada penulis selama menjalankan perkuliahan.
vi
RIWAYAT HIDUP PENULIS
Nama : Aidil Saputra
NIM : 110405066
Tempat, tanggal lahir : Dumai / 26 Maret 1993 Nama Orang Tua : Mayulis dan Martina Alamat Orang Tua:
Jalan Ratu Sima No. 28, RT 005, Kelurahan Simpang Tetap Darul Ichsan, Kecamatan Dumai Barat, Kota Dumai, Riau
Asal Sekolah:
TK Aisyiah tahun 1998–1999
SD Negeri 010 Ratu Sima tahun 1999–2005 SMP Negeri 2 Dumai tahun 2005–2008 SMA Negeri Binaan Khusus tahun 2008–2011 Beasiswa yang pernah diperoleh:
1. Peningkatan Prestasi Akademik (PPA) tahun 2012 2. Beasiswa Data Print tahun 2012
Pengalaman Organisasi/Kerja:
1. Himpunan Mahasiswa Teknik Kimia (HIMATEK) FT USU periode 2014/2015 sebagai anggota Literatur dan Pengembangan.
2. Covalen Study Group (CSG) periode 2013/2014 sebagai anggota Peningkatan Akademik dan Literatur.
3. Asisten Laboratorium Proses Industri Kimia, Departemen Teknik Kimia, Universitas Sumatera Utara tahun 2013/2015 modul pulp, modul Resin Urea Formaldehid, dan Reaktor Fasa Cair.
vii
ABSTRAK
Proses asidogenesis merupakan tahap pertama dari digestasi anaeobik dua tahap yang menghasilkan produk intermediet berupa Volatile Fatty Acid (VFA). Penelitian ini bertujuan untuk mendapatkan pengaruh HRT dan recycle sludge pada proses asidogenesis LCPKS pada keadaan ambient. Proses loading-up dilakukan dengan variasi HRT mulai dari HRT 20 hari, 15 hari, 10 hari, 5 hari, dan 4 hari untuk mencapai operasi target. Operasi target dilakukan dengan variasi rasio recycle sludge 0%, 15%, 25% dan 35% dengan laju pengadukan 250 rpm dan temperatur ambient. Analisa padatan (TS, VS, TSS, dan VSS), COD dan VFA dilakukan untuk mengkaji perubahan senyawa organik yang berubah menjadi VFA. Konsentrasi VSS tertinggi dan Reduksi VS tertinggi diperoleh pada rasio recycle sludge 25% sebesar 21.280 mg/l dan 14,24 %. Reduksi COD pada rasio recycle sludge 25% sebesar 24,19%.
Kata kunci : asidogenesis, ambient, digestasi anaerobik, recycle sludge, Volatile FattyAcid(VFA).
viii
ABSTRACT
Acidogenesis process is the first stage of digestion anaeobik two stages that produce intermediate products in the form of Volatile Fatty Acids (VFA). This study aims to get the effect of HRT and recycle sludge at acidogenesis process LCPKS at ambient temperature. Loading-up process done with HRT variations ranging from 20 days of HRT, 15 days, 10 days, 5 days and 4 days to reach the target operation. The target operation performed by varying the ratio of the sludge recycle of 0%, 15%, 25% and 35% with a stirring rate of 250 rpm and ambient temperature. Analysis solids (TS, VS, TSS and VSS), COD and VFA conducted to review changes in the organic compounds that turn into VFA. The highest concentration of VSS and VS reduction obtained at ratio sludge recycle of 25% is 21 280 mg/l and 14,24%. COD reduction at ratio of sludge recycle of 25% is 24,19%
Keywords : acidogenesis, ambient, anaerobic digestion, recycle sludge, Volatile Fatty Acids (VFA).
ix
DAFTAR ISI
Halaman
PERNYATAAN KEASLIAN SKRIPSI i
PENGESAHAN UNTUK UJIAN SKRIPSI ii
PRAKATA ... iiiii iiii
DEDIKASI ... v
RIWAYAT HIDUP PENULIS ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR GAMBAR ... xii
DAFTAR TABEL ... xiv
DAFTAR LAMPIRAN ... xv
DAFTAR SINGKATAN ... xvi
BAB I PENDAHULUAN ... 1
1.1 LATAR BELAKANG ... 1
1.2 PERUMUSAN MASALAH ... 4
1.3 TUJUAN PENELITIAN ... 4
1.4 MANFAAT PENELITIAN ... 4
1.5 RUANG LINGKUP PENELITIAN ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 LIMBAH CAIR PABRIK KELAPA SAWIT ... 6
2.2 LIMBAH CAIR PABRIK KELAPA SAWIT SEBAGAI SUBSTRAT BIOGAS ... 10
2.3 DIGESTASI ANAEROBIK ... 11
2.3.1 Tahap Hidrolisis ... 12
2.3.2 Tahap Asidogenesis ... 13
2.3.3 Tahap Asetogenesis ... 14
2.3.4 Tahap Metanogenesis ... 15 2.4 DIGESTASI ANAEROBIK DENGAN SISTEM SATU TAHAP
DAN DUA TAHAP 15
x
2.5 FAKTOR-FAKTOR YANG MEMPENGARUHI DIGESTASI
ANAEROBIK 17
2.5.1 pH 17
2.5.2 Suhu 18
2.5.3 Mixing (Pencampuran) ... 19
2.5.4 Hidraulic Retention Time (HRT) ... 19
2.4.5 Solid Retention Time (SRT) ... 20
2.4.6 Organic Loading Rate(OLR)... 21
2.4.7 Volatile Fatty Acid (VFA) ... 21
2.5 ANALISIS EKONOMI ... 22
BAB III METODOLOGI PENELITIAN... 23
3.1 LOKASI PENELITIAN ... 23
3.2 BAHAN DAN PERALATAN ... 23
3.2.1 Bahan-bahan ... 23
3.2.2 Peralatan ... 23
3.3 TAHAPAN PENELITIAN ... 25
3.3.1 Analisis Bahan Baku Limbah Cair Pabrik Kelapa Sawit (LCPKS) ... 25
3.3.2 Loading Up dan Operasi Target ... 29
3.3.3 Prosedur Recycle... 29
3.3.4 Pengujian Sampel (Sampling) ... 29
3.4 FLOWCHART PENELITIAN ... 30
3.4.1 Flowchart Prosedur Analisis Bahan Baku Limbah Cair Pabrik Kelapa Sawit (LCPKS) dan Pengujian Sampel (Sampling) ... 30
3.4.2 Flowchart Prosedur Loading Up dan Operasi Target ... 36
3.4.3 Flowchart Prosedur Recycle ... 37
3.5 JADWAL PENELITIAN ... 37
BAB IV HASIL DAN PEMBAHASAN ... 39
4.1 KARAKTERISASI LIMBAH CAIR PABRIK KELAPA SAWIT ... 39
4.2 HASIL PENELITIAN VARIASI HRT (PROSES LOADING UP) ... 40
4.2.1 Profil pH dan Alkalinitas pada Proses Loading Up ... 40 4.2.2 Pengaruh Kondisi pH dan Alkalinitas terhadap Pertumbuhan
xi
Mikroba ... 41
4.2.3 Degradasi Chemical Oxygen Demand (COD) pada Proses Loading Up ... 43
4.2.4 Pembentukan Volatile Fatty Acid (VFA)Pada Proses Loading Up ... 44
4.3.5 Pengaruh pH terhadap Rasio VFA/Alkalinitas Pada Proses Loading Up ... 45
4.3 HASIL PENELITIAN PROSES OPERASI TARGET... 46
4.3.1 Pengaruh Recycle Sludge terhadap Alkalinitas ... 46
4.3.2 Pengaruh Recycle Sludge terhadap Profil Pertumbuhan Mikroba . 48 4.3.3 Pengaruh Recycle Sludge terhadap Reduksi Vollatile Solid (VS) . 49 4.3.4 Pengaruh Recycle Sludge terhadap Degradasi Chemical Oxygen Demand (COD) ... 51
BAB V KESIMPULAN DAN SARAN ... 53
5.1 Kesimpulan ... 53
5.2 Saran ... 53
DAFTAR PUSTAKA ... 54
xii
DAFTAR GAMBAR
Halaman
Gambar 2.1 Produksi Minyak Kelapa Sawit Dunia 7
Gambar 2.2 Pengolahan Minyak Kelapa Sawit yang Menghasilkan LCPKS 9
Gambar 2.3 Skema Proses Pengolahan Digestasi Anaerobik 12
Gambar 2.4 Pembentukan Monomer 13
Gambar 2.5 Klasifikasi Mikroorganisme Berdasarkan Suhu 19
Gambar 3.1 Rangkaian Peralatan 24
Gambar 3.2 Flowchart Prosedur Analisis pH 30 Gambar 3.3 Flowchart Prosedur Analisis M-Alkalinity 31 Gambar 3.4 Flowchart Prosedur Analisis Total Solids (TS) 32 Gambar 3.5 Flowchart Prosedur Analisis Volatile Solid (VS) 33 Gambar 3.6 Flowchart Prosedur Analisis Total Suspended Solid (TSS) 33 Gambar 3.7 Flowchart Prosedur Analisis Volatile Suspended Solid (VSS) 34 Gambar 3.8 Flowchart Prosedur Analisis Chemical Oxygen Demand (COD) 35 Gambar 3.9 Flowchart Prosedur Loading Up dan Operasi Target 36
Gambar 3.10 Flowchart Prosedur Recycle 37
Gambar 4.1 Hubungan pH dan Alkalinitas pada Proses Loading Up 41 Gambar 4.2 Pengaruh Kondisi pH dan Alkalinitas terhadap Pertumbuhan Mikroba 42
Gambar 4.3 Pengaruh Reduksi HRT terhadap Reduksi COD 43
Gambar 4.4 Pengaruh Reduksi HRT terhadap Pembentukan VFA 44
Gambar 4.5 Pengaruh Reduksi HRT terhadap rasio VFA/Alkalinitas 43
Gambar 4.6 Pengaruh Rasio RecycleSludge terhadap pH dan Alkalinitas pada
Operasi Target 46
Gambar 4.7 Pengaruh Rasio RecycleSludge terhadap Rerata Alkalinitas (Error
Bar Menyatakan Standar Deviasi) 47
Gambar 4.8 Pengaruh Rasio RecycleSludge terhadap Konsentrasi VSS pada
Operasi Target 48
Gambar 4.9 Pengaruh RecycleSludge terhadap Rata-rata Konsentrasi VSS
(Error Bar Menyatakan Standar Deviasi) 49
Gambar 4.10 Pengaruh Rasio RecycleSludge terhadap Reduksi VS 50
xiii
Gambar 4.11 Pengaruh Rasio RecycleSludge terhadap Rata-rata Reduksi VS (Error
Bar Menyatakan Standar Deviasi) 50
Gambar 4.12 Pengaruh Rasio RecycleSludge terhadap Degradasi Chemical
Oxygen Demand (COD) 51
Gambar C.1 Tangki Umpan 66
Gambar C.2 Fermentor 66
Gambar C.3 Botol Keluaran Fermentor (discharge) 67
Gambar C.4 Botol Penampung Biogas (Gas Collector) 67
Gambar C.5 Gas Meter 67
Gambar C.6 Rangkaian Peralatan 68
Gambar C.7 LCPKS Segar pada Temperatur Ambient 68
Gambar C.8 Effluent Fermentor untuk Proses Pengendapan 69
Gambar C.9 Peralatan Analisis M-Alkalinity 69
Gambar C.10 Detecting Tube Hasil Analisis Gas H2S dan CO2 70 Gambar C.11 Peralatan Analisis Padatan Tersuspensi (Vacuum Pump) 70 Gambar C.12 Peralatan Analisis Chemical Oxygen Demand (COD) 71
Gambar C.13 Timbangan Analitik 71
Gambar C.14 Desikator 72
Gambar C.15 Oven 72
Gambar C.16 Furnace 73
Gambar D.1 Hasil Uji Laboratorium untuk Analisis Lemak dalam LCPKS ... 74
Gambar D.2 Hasil Uji Laboratorium untuk Analisis Protein dalam LCPKS ... 74
Gambar D.3 Hasil Uji Laboratorium untuk Analisis Karbohidrat dalam LCPKS ... 75
Gambar D.4 Hasil Uji Laboratorium untuk Analisis VFA ... 76
Gambar D.5 Hasil Uji Laboratorium untuk Analisis VFA (lanjutan) ... 77
xiv
DAFTAR TABEL
Halaman
Tabel 1.1 Berbagai Penelitian Mengenai Pengolahan Anaerobik 3
Tabel 2.1 Produksi dan Ekspor Minyak Kelapa Sawit Indonesia, Malaysia dan
Thailand 7
Tabel 2.2 Karakteristik Limbah Cair Kelapa Sawit 10
Tabel 2.3 Baku Mutu Limbah Cair untuk Industri Minyak Sawit 10
Tabel 2.4 Produksi Biogas dan Metana Teoritis dari Karbohidrat,
Lemak dan Protein 11
Tabel 2.5 Beberapa Kelompok Enzim Hidrolisis dan Fungsinya 13
Tabel 2.6 Degradasi pada Tahap Metanogenesis 15
Tabel 2.7 Bahan Kimia yang Sering digunakan sebagai Sistem Penyangga 18 Tabel 3.1 Jadwal Analisis Influent dan Effluent 30 Tabel 3.2 Jenis Kegiatan dan Jadwal Pelaksanaan Penelitian 38 Tabel 4.1 Karakteristik POME dari PTPN IV PKS Adolina 39
Tabel A.1 Karakteristik POME dari PTPN IV PKS Adolina 59
Tabel A.2 Data Hasil Analisis pH, Alkalinitas, TS, VS, TSS, dan VSS pada
Variasi Hydraulic Retention Time (HRT) 59 Tabel A.3 Data Hasil Analisis Chemical Oxygen Demand (COD) pada
Variasi Hydraulic Retention Time (HRT) 61 Tabel A.4 Data Hasil Analisis Pembentukan Volatile Fatty Acid (VFA) pada
Variasi Hydraulic Retention Time (HRT) 61 Tabel A.5 Data Hasil Analisis pH, Alkalinitas, TS, VS, TSS, dan VSS pada
Variasi Recycle Sludge 62
Tabel A.6 Data Hasil Analisis Chemical Oxygen Demand (COD) pada
Variasi Recycle Sludge 63 Tabel B.1 Data Alkalinitas untuk Variasi Recycle Sludge 0% (HRT 4 hari) 65
xv
DAFTAR LAMPIRAN
Halaman
LAMPIRAN A DATA HASIL ANALISIS 59
A.1 KARAKTERISTIK LIMBAH CAIR PABRIK KELAPA SAWIT 59
A.2 DATA HASIL PENELITIAN 59
LAMPIRAN B CONTOH PERHITUNGAN 65
B.1 PERHITUNGAN REDUKSI COD 65
B.2 PERHITUNGAN STANDAR DEVIASI 65
LAMPIRAN C DOKUMENTASI 66
LAMPIRAN D HASIL UJI LABORATORIUM 73
D.1 HASIL UJI LABORATORIUM UNTUK ANALISIS LEMAK
DALAM LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS) 73
D.2 HASIL UJI LABORATORIUM UNTUK ANALISIS
PROTEIN DALAM LIMBAH CAIR PABRIK KELAPA
SAWIT (LCPKS) 73
D.3 HASIL UJI LABORATORIUM UNTUK ANALISIS
KARBOHIDRAT DALAM LIMBAH CAIR PABRIK
KELAPA SAWIT (LCPKS) 73
D.4 HASIL UJI LABORATORIUM UNTUK ANALISIS VOLATILE
FATTY ACID (VFA) 73
xvi
DAFTAR SINGKATAN
BOD Biological Oxygen Demand
COD Chemical Oxygen Demand
CPO Crude Palm Oil
CSTR Continous Stirred Tank Reactor
FAS Ferro Amonium Sulfat
HRT Hydraulic Retention Time
LCPKS Limbah Cair Pabrik Kelapa Sawit
OLR Organic Loading Rate
PKS Pabrik Kelapa Sawit
POME Palm Oil Mill Effluent
PTPN PT Perkebunan Nusantara
SRT Sludge Retention Time
TBS Tandan Buah Segar
TKKS Tandan Kosong Kelapa Sawit
TS Total Solid
TSS Total Suspended Solid
VFA Volatile Fatty Acid
VS Volatile Solid
VSS Volatile Suspended Solid
vii
ABSTRAK
Proses asidogenesis merupakan tahap pertama dari digestasi anaeobik dua tahap yang menghasilkan produk intermediet berupa Volatile Fatty Acid (VFA). Penelitian ini bertujuan untuk mendapatkan pengaruh HRT dan recycle sludge pada proses asidogenesis LCPKS pada keadaan ambient. Proses loading-up dilakukan dengan variasi HRT mulai dari HRT 20 hari, 15 hari, 10 hari, 5 hari, dan 4 hari untuk mencapai operasi target. Operasi target dilakukan dengan variasi rasio recycle sludge 0%, 15%, 25% dan 35% dengan laju pengadukan 250 rpm dan temperatur ambient. Analisa padatan (TS, VS, TSS, dan VSS), COD dan VFA dilakukan untuk mengkaji perubahan senyawa organik yang berubah menjadi VFA. Konsentrasi VSS tertinggi dan Reduksi VS tertinggi diperoleh pada rasio recycle sludge 25% sebesar 21.280 mg/l dan 14,24 %. Reduksi COD pada rasio recycle sludge 25% sebesar 24,19%.
Kata kunci : asidogenesis, ambient, digestasi anaerobik, recycle sludge, Volatile FattyAcid(VFA).
viii
ABSTRACT
Acidogenesis process is the first stage of digestion anaeobik two stages that produce intermediate products in the form of Volatile Fatty Acids (VFA). This study aims to get the effect of HRT and recycle sludge at acidogenesis process LCPKS at ambient temperature. Loading-up process done with HRT variations ranging from 20 days of HRT, 15 days, 10 days, 5 days and 4 days to reach the target operation. The target operation performed by varying the ratio of the sludge recycle of 0%, 15%, 25% and 35% with a stirring rate of 250 rpm and ambient temperature. Analysis solids (TS, VS, TSS and VSS), COD and VFA conducted to review changes in the organic compounds that turn into VFA. The highest concentration of VSS and VS reduction obtained at ratio sludge recycle of 25% is 21 280 mg/l and 14,24%. COD reduction at ratio of sludge recycle of 25% is 24,19%
Keywords : acidogenesis, ambient, anaerobic digestion, recycle sludge, Volatile Fatty Acids (VFA).
1
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Industri kelapa sawit telah berkembang pesat dalam beberapa tahun terakhir
dan menyumbang persentase terbesar produksi minyak dan lemak di dunia pada
tahun 2011 [1]. Melampaui Malaysia pada tahun 2008, Indonesia saat ini
merupakan produsen terbesar minyak sawit di dunia dengan total produksi pada
tahun 2012 mencapai 27 miliar ton yang dihasilkan dari sekitar 6 juta hektar
perkebunan. Malaysia dan Indonesia bersama-sama menghasilkan sekitar 87%
dari total minyak sawit dunia [2].
Meskipun ekspansi industri kelapa sawit telah mendorong perekonomian
nasional, juga secara bersamaan menghasilkan produk samping berlimpah seperti
limbah cair pabrik kelapa sawit limbah (LCPKS) atau palm oil mill effluent (POME) (60%), tandan kosong (23%), cangkang sawit (5%), dan serat mesocarp (12%) untuk setiap ton tandan buah segar diproses di pabrik [1,3]. Satu ton buah
kelapa sawit menghasilkan sekitar 0,87 m3 LCPKS atau 2,5 ton limbah per ton
minyak yang diproduksi. [3].
Indonesia memproduksi hampir 25 juta metrik ton kelapa sawit di
2011/2012 [4]. Diperkirakan bahwa sekitar 28 m3 biogas yang dihasilkan untuk
setiap m3 LCPKS dari pabrik pengolahan limbah dari pabrik kelapa sawit. Dalam
pabrik kelapa sawit, limbah padat dibakar langsung di boiler untuk menghasilkan
uap [5].
LCPKS adalah cairan cokelat kental yang mengandung konsentrasi asam
organik yang tinggi dengan tingkat COD yang lebih tinggi dari 20.000 mg/l.
Pengolahan anaerobik lebih menguntungkan untuk pengolahan LCPKS karena
dapat menghilangkan lebih banyak bahan organik bahkan dengan nutrisi yang
tersedia terbatas[6].
LCPKS mengandung bahan organik yang tinggi [7], serta memiliki
konstituen biodegradable dengan rasio BOD/COD sebesar 0,5 dan ini berarti bahwa LCPKS dapat diolah dengan mudah menggunakan cara biologis [1].
2
Pengolahan anaerobik adalah suatu proses degradasi multi-tahap senyawa
organik melalui berbagai intermediet menjadi metana dan karbon dioksida [8].
Langkah pertama dari degradasi anaerobik adalah hidrolisis bahan organik
kompleks menjadi monomer dasar oleh enzim hidrolitik. Senyawa organik yang
lebih sederhana kemudian difermentasi menjadi asam organik dan hidrogen oleh
bakteri fermentasi (acidogens). Asam organik volatil diubah menjadi asetat dan hidrogen oleh bakteri acetogenic. Bakteri metanogen menggunakan hidrogen dan asam asetat yang diproduksi oleh bakteri acetogenic untuk mengubahnya menjadi metana [9].
Dalam proses digestasi anaerobik konvensional, asidogenesis dan
metanogenesis berlangsung dalam sistem reaktor tunggal (single-stage)[10]. Sistem dua tahap dapat dioperasikan untuk memberikan kondisi yang optimal bagi
mikroorganisme dalam setiap tahap untuk lebih efisien dalam pengolahan [11].
Konsentrasi asam lemak volatil (VFA) dianggap sebagai Indikator yang
baik pada proses anaerobik, khususnya bagi aktivitas bakteri asetogenesis dan
metanogenesis [12]. Konsentrasi asam propinoat dapat menghambat proses
pembentukan metana dan efek inhibisi asam propionat juga berdampak negatif
baik terhadap mikroorganisme yang menghasilkan VFA maupun terhadap
mikroorganisme yang mengolah VFA [13]. Wijekoon et al, 2011 [12] melaporkan
bahwa konsentrasi asam propionat lebih dari 1-2 g/l terbukti dapat menghambat
bakteri metanogenesis.
Berikut beberapa penelitian terdahulu yang telah dilakukan mengenai
digestasi anaerobik:
Tabel 1.1 Berbagai Penelitian Mengenai Digestasi Anaerobik
Peneliti Tahun Penelitian Yang Dilakukan
Bambang Trisakti, Veronica Manalu, Irvan, Taslim,
Muhammad Turmuzi (2015) [3]
2015 Proses asidogenesis dengan bahan baku LCPKS menggunakan reaktor Continous Stirred Tank Reactor, variasi HRT menggunakan HRT 6,7; 5 dan 4 hari dengan laju pengadukan 50 rpm, pH 6 dan sedangkan variasi pH menggunakan pH 5; 5,5; 6, dengan laju pengadukan 100-110 rpm pada temperatur 55°C. VFA terdiri dari asam asetat, asam propionat dan asam butirat. Konsentrasi VFA maksimum (5.622,72 mg/L) pada HRT 4 hari dan pH 6
3
Tabel 1.1 Berbagai Penelitian Mengenai Digestasi Anaerobik (lanjutan)
Peneliti Tahun Penelitian Yang Dilakukan
Sergio Ponsa, Ivet Ferrer, Felicitas Vazquez, dan Xavier Font [14]
2008 Kondisi optimal pada pengolahan anaerobik sewage sludge pada tahap hidrolisis-asidogenesis pada 55oC dan 65oC dengan menggunakan reaktor CSTR Volume 4 l, HRT 1-4 hari. Maksimum VFA diperoleh pada HRT 4 hari dan 3 hari
Wee Shen Lee, Adeline Seak May Chua, Hak Koon Yeoh, dan Gek Cheng Ngoh [15]
2013 Produksi VFA dari LCPKS pada temperatur kamar (30 oC), 40 oC, dan 55 oC pada tiga reaktor anaerobik volume 1,5 L. Diperoleh bahwa pada temperatur mesofilik produksi VFA lebih baik dibandingkan dengan temperatur termofilik, sehingga dapat disarankan untuk menjalankan operasi tanpa pengontrolan suhu (temperatur ambient)
Sim Kean Hong [16] 2003 Fermentasi dua tahap LCPKS untuk produksi VFA dengan reaktor CSTR volume 50 l dengan dan tanpa recycle sludge. Diperoleh hasil VFA yang maksimum pada pH 6,5, suhu 30 oC, 100 rpm, sludge/LCPKS 1:1dengan HRT 4 hari yaitu 15,36 g/l
Umumnya LCPKS segar memiliki suhu 60-70oC, hal ini memungkinkan
LCPKS untuk diolah dengan proses asidogenesis pada kondisi mesofilik dan
termofilik tanpa memerlukan energi panas yang tinggi [15]. Apabila proses
dijalankan pada keadaan termofilik 55oC, panas yang dibutuhkan belum tentu
tercapai, terutama pada musim paceklik (musim trek) dimana LCPKS yang
dihasilkan juga menurun dari biasanya. Menurut Wee Shen Lee et al, Proses asidogenesis suhu mesofilik 30oC dan 40oC lebih baik dibandingkan termofilik.
Hal ini didukung oleh keadaan geografis Indonesia yang merupakan negara tropis
dengan suhu ambient antara 25-32oC[15].
Adapun setiap desain sistem pengolahan anaerobik, selalu diinginkan untuk
mempertahankan tingkat optimal dari pertumbuhan mikroorganisme di dalam
digester yang menghasilkan sebuah proses biokonversi efisien. Dalam rangka
mempertahankan konsentrasi biomassa yang optimal dalam digester, beberapa
strategi telah diadopsi oleh banyak peneliti. Di antara dengan recyclesludge, yang merupakan strategi sederhana untuk meningkatkan konsentrasi biomassa dalam
digester
4
Oleh sebab itu penelitian ini dilakukan untuk mempelajari pengaruh
Hidraulic Retention Time (HRT) dan rasio recycle sludge pada proses asidogenesis limbah cair kelapa sawit pada temperatur ambient. Proses ini menggunakan reaktor Continous Stirred Tank Reactor (CSTR) bervolume 2 liter.
1.2 PERUMUSAN MASALAH
Salah satu upaya dalam mengoptimalkan proses digestasi anaerobik adalah
dengan mendaur ulang lumpur (recycle sludge). Recycle sludge dilakukan agar dapat meningkatkan degradasi zat organik dengan menambah waktu tinggal
padatan dalam reaktor anaerobik.
Adapun beberapa masalah yang perlu diselesaikan dalam penelitian ini
adalah: (i) Berapa HRT terbaik pada proses asidogenesis LCPKS pada keadaan
ambient; dan (ii) Berapa rasio recycle sludge terbaik pada proses asidogenesis LCPKS pada keadaan ambient.
1.3 TUJUAN PENELITIAN
Adapun yang menjadi tujuan dari penelitian ini adalah:
1.Mendapatkan HRT terbaik pada proses asidogenesis LCPKS pada keadaan
ambient
2.Mendapatkan rasio recycle sludge terbaik pada proses asidogenesis LCPKS pada keadaan ambient.
1.4 MANFAAT PENELITIAN
Manfaat dari penelitian ini antara lain yaitu :
1. Memberikan informasi mengenai pengaruh variasi HRT dan HRT terbaik pada
proses asidogenesis LCPKS pada keadaan ambient.
2. Memberikan informasi mengenai pengaruh rasio recycle sludge dan rasio recycle sludge pada proses asidogenesis LCPKS pada keadaan ambient.
1.5 RUANG LINGKUP PENELITIAN
Penelitian ini dilaksanakan di Laboratorium Ekologi, Departemen Teknik
Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan. Penelitian dilakukan
menggunakan proses asidogenesis digestasi anaerobik menggunakan digester jenis
5
Continous Stirred Tank Reactor (CSTR) dengan volume 2 liter. Adapun variabel-variabel dari penelitian ini adalah sebagai berikut:
1. Variabel tetap:
a. Starter yang digunakan berasal dari hasil olahan penelitian sebelumnya yaitu proses digestasi anaerobik tahapan asidogenesis, dimana starter yang digunakan paling awal berasal dari kolam pengasaman Pabrik Kelapa Sawit
Torgamba PTPN III.
b. Jenis bahan baku atau umpan yang digunakan: LCPKS dari Pabrik Kelapa
Sawit Adolina PTPN IV.
c. pH fermentor: 6 ± 0,2
d. Temperatur fermentor: temperatur ambient e. Kecepatan pengadukan fermentor: 250 rpm.
f. Kecepatan pengadukan tangki umpan: 150 rpm.
2. Variabel divariasikan:
a. HidraulicRetentionTime (HRT) 20 hari, 15 hari, 10 hari, 5 hari, 4 hari.
Variasi HRT merupakan proses loading up untuk mencapai operasi target pada HRT terkecil yaitu HRT 4 hari
b. Rasio recycle 15 %, 25 %, 35%, dan tanpa recycle
3. Parameter analisa:
Analisa yang akan dilakukan di dalam penelitian ini meliputi analisa pada
bahan baku yang digunakan yaitu POME dengan influent limbah dan effluent limbah. Adapun analisa cairan ini terdiri dari :
1. Analisa M-Alkalinity (Metode Titrasi)
2. Analisa kadar total solid (TS) (Metode Analisa Proksimat) 3. Analisa volatile solid (VS) (Metode Analisa Proksimat)
4. Analisa kadar total suspended solid (TSS) (Metode Analisa Proksimat) 5. Analisa volatile suspended solid (VSS) (Metode Analisa Proksimat) 6. Analisa COD (Chemical Oxygen Demand) (Metode Reflux Terbuka) 7. Analisa volatile fatty acid (VFA) (Metode Kromatografi)
8. Analisa pH
Adapun analisa gas dilakukan jika pada penelitian ada terbentuk gas yaitu
gas CO2 dan H2S.
6
BAB II
TINJAUAN PUSTAKA
2.1 LIMBAH CAIR PABRIK KELAPA SAWIT
Minyak kelapa sawit adalah salah satu tanaman khatulistiwa yang paling
cepat berkembang dunia. Indonesia dan Malaysia adalah dua produsen kelapa
sawit terbesar di dunia [17]. Melampaui Malaysia pada tahun 2008, Indonesia saat
ini merupakan produsen terbesar minyak sawit di dunia dengan total produksi
pada tahun 2012 mencapai 27 miliar ton yang dihasilkan dari sekitar 6 juta hektar
perkebunan. Malaysia dan Indonesia bersama-sama menghasilkan sekitar 87%
dari total minyak sawit dunia[2].
Gambar 2.1 Produksi Minyak Kelapa Sawit Dunia [4]
Tabel 2.1 Produksi dan Ekspor Minyak Kelapa Sawit Indonesia, Malaysia dan
Thailand (dalam kiloton) [2]
Negara 2007/08 2008/09 2009/10 2010/11 2011/12 Juli 2012/13 Indonesia -Produksi
-Ekspor 18.000 13.969 20.500 15.964 21.000 16.200 23.600 16.422 25.400 18.000 27.000 19.100 Malaysia Produksi
-Ekspor 17.567 14.644 17.259 15.485 17.763 15.530 18.211 16.307 18.300 16.600 18.500 16.700 Thailand -Produksi
-Ekspor 1.050 360 1.540 114 1.345 130 1.288 382 1.546 500 1.700 520
7
Budidaya kelapa sawit telah menjadi salah satu kegiatan pertanian yang
dominan di Indonesia sejak akhir tahun 1990-an. Antara 1998 dan 2007 total luas
ditanami dengan kelapa sawit meningkat dari 3,9 juta hektar hingga lebih dari 7,9
juta hektar [1]. Minyak kelapa sawit berasal dari mesocarp berdaging buah kelapa sawit (Elaeis gunineensis). Satu hektar kelapa sawit menghasilkan 10 sampai 35 ton tandan buah segar (TBS) per tahun[17].
Kelapa sawit memiliki umur lebih dari 200 tahun, sementara umur
ekonomisnya adalah sekitar 20-25 tahun. Periode pembibitan adalah 11-15 bulan
dan panen pertama dilakukan setelah 32-38 bulan setelah penanaman. Dibutuhkan
5-10 tahun untuk pabrik kelapa sawit untuk mencapai hasil puncak. Dari 5,8 ton
tandan buah segar sekitar 1 ton minyak sawit mentah (CPO) dihasilkan [17]
Meskipun ekspansi industri kelapa sawit telah mendorong perekonomian
nasional, Namun dihasilkan pula limbah yang berlimpah seperti limbah cair
kelapa sawit atau POME (Palm Oil Mill Effluent), Tandan Kosong Kelapa Sawit (TKKS), cangkang, dan serat mesocarp selama pengolahan minyak kelapa sawit dari tandan buah segar (TBS)[1].
2,5 ton limbah cair kelapa sawit (LCPKS) (60 %) dihasilkan untuk setiap
ton minyak yang diproduksi. Pabrik kelapa sawit juga menghasilkan sejumlah
besar limbah padat seperti Tandan Kosong Kelapa Sawit (TKKS) (23%) , serat
mesocarp (fiber) (12%) ,dan cangkang (shell) (5%) untuk setiap ton tandan buah
segar (TBS) diproses di pabrik [3]. Dari limbah-limbah tersebut, LCPKS masih
relatif belum dimanfaatkan dan akan menjadi ancaman bagi lingkungan jika
langsung dibuang ke aliran air [1].
LCPKS adalah suspensi koloid yang mengandung 95-96% air, minyak
0,6-0,7% dan 4-5% total padatan termasuk 2-4% padatan tersuspensi. Padatan
tersuspensi yang terutama terdiri dari puing-puing mesocarp buah sawit dihasilkan dari tiga sumber utama, (1) sterilisasi kondensat, (2) pemisah lumpur
dan (3) limbah hydrocyclone [18].
LCPKS umumnya mengandung limbah padat, minyak dan air limbah yang
tinggi yang bersifat asam karena jumlah zat terlarutnya "protein, karbohidrat,
senyawa nitrogen, lipid dan mineral yang mungkin diubah menjadi bahan yang
bermanfaat menggunakan proses mikroba" [2].
8
LCPKS terdiri dari kombinasi dari air limbah yang terutama dihasilkan dan
dikeluarkan dari operasi pengolahan utama, seperti yang terlihat pada Gambar2.2
[19]:
• Sterilisasi Tandan Buah Segar - kondensat dari proses sterilisasi sekitar 36% dari total LCPKS;
• Klarifikasi dari CPO - air limbah klarifikasi adalah sekitar 60% dari total LCPKS;
• Clay bath Separation (Hydrocyclone) pemisahan campuran kernel dan cangkang - air limbah hidrosiklon adalah sekitar 4% dari total LCPKS
pabrik kelapa sawit.
Gambar 2.2 Pengolahan Minyak Kelapa sawit yang Menghasilkan LCPKS [5]
9
Tabel 2.2 Karakteristik Limbah Cair Kelapa Sawit [20]
Parameter LCPKS (Range) LCPKS (Rata-rata)
Temperatur (oC) 80-90 85
pH 3,4 – 5,2 4,2
Minyak dan Lemak 130 –18.000 mg/l 6.000 mg/l
BOD3 10.250 – 43.750 mg/l 25.000 mg/l
COD 15.000 – 100.000 mg/l 51.000 mg/l
Total Solid 11.500 – 79.000 mg/l 40.000 mg/l Suspended Solid 5.000 – 54.000 mg/l 18.000 mg/l Total Volatile Solid 9.000 – 72.000 mg/l 34.000 mg/l
Total Nitrogen 180 – 1.400 mg/l 750 mg/l
Ammoniacal nitrogen 4 – 80 mg/l 35 mg/l
Tabel 2.3 Baku Mutu Limbah Cair untuk Industri Minyak Sawit [21]
Parameter Kadar
Maksimum (mg/l)
Beban Pencemaran Maksimum
(kg/ton)
BOD5 250 1,5
COD 500 3,0
TSS 300 1,8
Minyak dan Lemak 30 0,18
Amonia Total (sebagai NH3-N) 20 0,12
pH 6,0 – 9,0
Debit Limbah Maksimum 6 m3 ton bahan baku
Kandungan organik yang tinggi pada limbah cair kelapa sawit (LCPKS)
membuat limbah cair tersebut menjadi sumber yang baik untuk menghasilkan gas
metana melalui digestasi anaerobik. Selain itu, LCPKS mengandung konstituen
biodegradable dengan rasio BOD / COD sebesar 0,5 dan ini berarti bahwa LCPKS dapat diolah dengan mudah menggunakan cara biologis [1].
2.2 LIMBAH CAIR PABRIK KELAPA SAWIT SEBAGAI SUBTRAT
BIOGAS
Bahan yang ditambahkan ke proses biogas adalah substrat (makanan) untuk
mikroba dan sifat-sifatnya memiliki pengaruh besar pada stabilitas dan efisiensi
proses. Komposisi substrat sangat penting baik untuk jumlah gas yang terbentuk
dan kualitas gas. Komposisi akhirnya juga mempengaruhi kualitas residu
digestasi, baik dari segi kandungan gizi tanaman dan potensi kontaminasi (logam,
senyawa organik, organisme penyebab penyakit, dan lain-lain). Memilih bahan
10
yang tepat mempengaruhi hasil dari proses, memaksimalkan output energi dan menghasilkan pupuk hayati berkualitas baik [22]. Bahan baku yang berbeda akan
menghasilkan jumlah biogas dan metana yang berbeda tergantung pada
kandungan karbohidrat, lemak dan protein. Secara teori, semua bahan
[image:30.595.106.516.251.322.2]biodegradable dengan kadar lignin yang wajar (bukan kayu) adalah bahan baku yang cocok untuk proses biogas [23].
Tabel 2.4 Produksi Biogas dan Metana Teoritis dari Karbohidrat,
Lemak dan Protein [24]
Substrat Biogas
(m3/ton)
Metana (m3/ton)
Kandungan Metana (%)
Karbohidrat 830 415 50,0
Lemak 1444 1014 70,2
Protein 793 504 63,6
2.3 DIGESTASI ANAEROBIK
Pengolahan anaerobik adalah proses menghasilkan energi, berbeda dengan
sistem aerobik yang umumnya memerlukan input energi yang tinggi untuk tujuan
aerasi. Pengolahan anaerobik merupakan teknologi yang relatif murah yang
mengkonsumsi lebih sedikit energi, ruang dan menghasilkan sedikit kelebihan
lumpur dibandingkan dengan teknologi pengolahan aerobik konvensional.
Produksi energi dari biogas membuat teknologi pengolahan anaerobik menjadi
pilihan yang lebih menarik daripada metode pengolahan lainnya [9].
Digestasi anaerobik adalah sebuah proses yang kompleks yang melibatkan
penguraian senyawa organik tanpa adanya molekul oksigen untuk menghasilkan
gas metana (CH4) dan gas karbon dioksida (CO2). Proses degradasi terjadi oleh
aksi dari berbagai jenis bakteri anaerobik. Proses degradasi ini meliputi hidrolisis,
asidogenesis (termasuk asetogenesis) dan metanogenesis. Gas metana merupakan
salah satu komponen yang diproduksi Melalui proses degradasi methanogenesis
anaerobik [24]. Effluent dari digestasi anaerobik akan menjadi pupuk yang baik karena mengandung hampir semua zat makro dan mikro yang dibutuhkan untuk
pertumbuhan tanaman [25].
Proses pengolahan anaerobik sangat stabil, asalkan sistem dioperasikan
dalam kondisi yang tepat. Ini mungkin diperlukan bahwa kondisi operasional
optimum ditentukan untuk setiap jenis tertentu air limbah dan yang lebih penting,
11
proses tersebut harus cukup dipahami oleh para insinyur dan operator [19].
Efisiensi operasional dari sistem digestasi anaerobik terutama tergantung pada
struktur komunitas mikroba dalam sistem. Selain itu, faktor lingkungan seperti
suhu dan pH memainkan peran penting dalam menentukan kinerja dan nasib
komunitas mikroba dalam digestasi anaerobik [18].
Proses digestasi anaerobik berlangsung dalam beberapa tahap yaitu
hidrolisis, asidogenesis (termasuk asetogenesis), dan metanogenesis. Skema
[image:31.595.118.541.253.601.2]proses digestasi anaerobik dapat dilihat pada Gambar 2.3 dibawah ini:
Gambar 2.3 Skema Proses Pengolahan Digestasi Anerobik [18]
2.3.1 Tahap Hidrolisis
Pada tahap pertama (hidrolisis), senyawa yang tidak terlarut seperti
selulosa, protein dan lemak dipecah menjadi monomer-monomer (fragmen larut
dalam air) oleh exoenzymes (hydrolase) dari bakteri anaerobik fakultatif dan
12
obligat. Sebenarnya, ikatan kovalen terputus oleh reaksi kimia dengan air, seperti
pada gambar 2.4 [26]. Semakin besar luas permukaan bahan baku, lebih efisien
enzim hidrolitik dapat menyerang materi. Kondisi operasional proses
mempengaruhi hidrolisis, misalnya suhu yang lebih tinggi meningkatkan
hidrolisis. pH optimal adalah sekitar 6,0, meskipun hidrolisis terjadi juga pada pH
yang lebih tinggi. Laju beban organik (OLR) yang terlalu tinggi dapat
menghambat hidrolisis melalui akumulasi degradasi intermediet [22].
[image:32.595.185.462.245.362.2]R – C – C – R
Gambar 2.4 Pembentukan monomer [26]
Proses hidrolisis dari karbohidrat membutuhkan waktu beberapa jam,
hidrolisis protein dan lemak membutuhkan waktu beberapa hari. Lignoselulosa
dan lignin didegradasi sangat lambat dan tidak sempurna [26].
Tabel 2.5 Beberapa Kelompok Enzim Hidrolisis dan Fungsinya [22]
Enzim Substrat Produk pemecahan
Proteinase Protein Asam amino
Cellulase Selulosa Cellobiose and glucose
Hemicellulase Hemicellulose Gula, seperti glukosa, xylose, mannose dan arabinose
Amylase Pati Glukosa
Lipase Lemak Asam lemak dan gliserol
Pectinase Pektin Gula seperti galaktosa, arabinose, dan polygalacticuronicacid
2.3.2 Tahap Asidogenesis
Langkah kedua adalah asidogenesis (juga disebut sebagai fermentasi),
Setelah bahan baku terdegradasi menjadi molekul yang lebih kecil, yaitu asam
lemak rantai panjang (Long Chain Fatty Acids), alkohol, gula sederhana dan asam amino, selama hidrolisis, bakteri Acidogenic mampu menyerap molekul tersebut dan memfasilitasi degradasi lebih lanjut menjadi asam lemak volatil (VFA) [23].
H2O
R – C – H
OH – C – R
monomer
[image:32.595.107.514.472.600.2]13
Sama seperti tahap hidrolisis, tahap ini terdiri bukan hanya dari satu reaksi.
Kecepatan reaksi yang terjadi tergantung pada organisme yang hadir dan substrat
selama proses. Banyak organisme yang berbeda aktif selama tahap ini, lebih
banyak dari pada tahap lain [22]. Konsentrasi ion hidrogen intermediet yang
terbentuk mempengaruhi jenis produk fermentasi. Tekanan parsial hidrogen yang
tinggi menyebabkan senyawa yang sedikit tereduksi, seperti asetat, terbentuk [26].
Asam lemak volatil dengan rantai lebih dari empat-karbon tidak dapat
digunakan langsung oleh metanogen. Asam organik ini selanjutnya dioksidasi
menjadi asam asetat dan hidrogen oleh bakteri acetogenic obligat hidrogen melalui proses yang disebut asetogenesis. Asetogenesis juga mencakup produksi
asetat dari hidrogen dan karbon dioksida oleh acetogens dan homoacetogens. Kadang-kadang asidogenesis dan asetogenesis tahap digabungkan bersama
sebagai satu tahap [10].
2.3.3 Tahap Asetogenesis
Selama proses asidogenesis, tidak hanya asetat, H2 dan CO2 yang
dihasilkan, namun produk intermediet kompleks seperti propionat, butirat, laktat
dan etanol akan diproduksi secara bersamaan. Produk intermediet tersebut akan
dikonversi menjadi asam organik sederhana, CO2 dan H2 oleh bakteri acetogenic [18]
Pada tahap asetogenesis, mikroorganisme homoacetogenic secara konstan terus mengurangi eksergonik H2 dan CO2 menjadi asam asetat.
2CO2 + 4H2→ CH3COOH+ 2H2O [26]
2.3.4 Tahap Metanogenesis
Metanogenesis merupakan tahap akhir dari proses biogas. Pada tahap ini,
metana dan karbon dioksida (biogas) yang dibentuk oleh berbagai
mikroorganisme yang memproduksi metana disebut metanogen. Substrat yang
paling penting bagi organisme ini adalah gas hidrogen, karbon dioksida, dan
asetat, yang terbentuk selama oksidasi anaerobik. Namun substrat lain seperti
metil amina, beberapa alkohol, dan format juga dapat digunakan untuk produksi
metana [26]. Bakteri metanogens sangat sensitif terhadap oksigen. oksigen
14
merupakan racun mematikan yang membunuh semua metanogens bahkan pada konsentrasi rendah [18]
Gas metana diproduksi dalam dua cara. Salah satunya adalah konversi
asetat menjadi karbon dioksida dan metana oleh organisme acetotrophic dan melalui reduksi karbon dioksida dengan hidrogen oleh organisme
hydrogenotrophic. Metanogen dominan dalam reaktor biogas terbatas pada Methanobacterium, methanothermobacter, methanobrevibacter, methanosarcina dan methanosaeta (sebelumnya methanothrix) [10]. Reaksi metanogenesis dapat dinyatakan sebagai berikut:
CH3COOH → CH4 + CO2
CO2 + 4H2→ CH4 + 2H2O
[image:34.595.106.486.350.459.2][10]
Tabel 2.6 Degradasi pada Tahap Metanogenesis [26]
Jenis Substrat Reaksi Kimia ∆Gf (kJ mol
-1 )
CO2 4H2 + HCO3
-
+ H+→ CH4 + 3H2O -135,4
CO2 + 4H2→ CH4 + 2H2O -131,0
4HCOO- + H2O + H
+ → CH
4 + 3HCO3
--130,4
Asetat CH3COO
+ H2O → CH4 + HCO3 -30,9
Metil 4CH3OH → 3CH4 + HCO3
+ H+ + H2O -314,3 CH3OH + H2→ CH4 + H2O -113,0 Etanol 2CH3CH2OH + CO2→ CH4 + 2CH3COOH -116,3
Produsen metana umumnya tumbuh sangat lambat, hal ini membatasi
proses pembentukan biogas. Waktu generasi, yaitu waktu yang dibutuhkan untuk
mikroorganisme untuk membagi dirinya dalam dua, adalah antara 1 hingga 12
hari bagi produsen metana. Waktu retensi yang terlalu pendek (kurang dari 12
hari) meningkatkan risiko bahwa organisme ini akan tercuci keluar dari proses,
karena mereka tidak memiliki waktu yang cukup untuk meningkatkan jumlah
pada tingkat yang sama dengan bahan yang dipompa ke dalam dan keluar dari
tangki pencernaan [26].
2.4 DIGESTASI ANAEROBIK DENGAN SISTEM SATU TAHAP DAN
DUA TAHAP
Dalam proses digestasi anaerobik konvensional, asidifikasi dan
metanogenesis berlangsung dalam sistem reaktor tunggal (single-stage) dan ada
15
keseimbangan antara acidogens dan metanogens karena kedua kelompok berbeda dalam hal fisiologi, kebutuhan nutrisi, kinetika pertumbuhan dan kepekaan
terhadap kondisi lingkungan [10]. Pada umumnya digestasi anaerobik satu tahap
dilakukan dengan pencampuran total (total mixed) dengan menggunakan reaktor CSTR (Continous Stirred Tank Reactor). Substrat harus benar-benar tercampur dengan pengaduk yang bervariasi. Proses satu tahap ini biasanya digunakan untuk
mengolah lumpur, sisa makanan, kotoran, dan lain-lain, Kadang-kadang beberapa
cairan residu / proses dikembalikan ke proses. Hal ini meningkatkan waktu retensi
bahan dan membantu lebih banyak mikroorganisme untuk tetap dalam proses
[22].
Sebuah alternatif untuk proses satu tahap adalah untuk membagi proses
menjadi dua bagian, yang disebut digestasti dua tahap. Dalam digestasi dua tahap,
langkah pertama adalah untuk memuat bahan baku ke dalam tangki digestasi
dimana proses difokuskan pada hidrolisis dan asidogenesis. Pada proses ini
menghasilkan asam, namun sejumlah biogas biasanya juga diproduksi, karena
sulit untuk benar-benar membagi proses. Kemudian cairan proses dari proses ini
dipisahkan dan ditambahkan ke tangki digestasi lain yang khusus disesuaikan
untuk metanogenesis. Jenis proses mungkin cocok ketika substrat mengandung
bahan yang mudah didegradasi dan tahap hidrolisis yang cepat [11].
Sistem dua fase dapat dioperasikan untuk memberikan kondisi yang optimal
bagi mikroorganisme dalam setiap tahap untuk lebih efisien dalam pencernaan.
Pada tahap pertama dari sistem dua fase, fase fermentasi asam, organisme
Acidogenic mencerna padatan organik dan organik terlarut yang kompleks, mengkonversi mereka ke VFA. Pada tahap kedua, metana yang memproduksi
mikroorganisme (metanogen) memanfaatkan VFA untuk menghasilkan metana
dan karbon dioksida [11].
pH selama fase asidogenesis biasanya dipertahankan pada 5,5-6,0 dan HRT
kurang dari 5 hari sementara di fase metanogen pH dipertahankan pada pH lebih
besar dari 7,0. Akibatnya, efisiensi pengolahan yang lebih tinggi dan stabilitas
proses yang lebih baik dapat dicapai dengan proses dua tahap dengan
penghilangan bahan organik secara keseluruhan lebih besar dari 87% pada HRT
17 hari, 96% dari total COD diubah untuk biomassa dan biogas [10].
16
2.5 FAKTOR-FAKTOR YANG MEMPENGARUHI DIGESTASI
ANAEROBIK
Proses digestasi anaerobik sangat sensitif terhadap kondisi operasional
dibanding proses aerob [10]. Berikut merupakan faktor-faktor penting dalam
proses digestasi anerob:
2.5.1 pH
pH adalah logaritma negatif untuk basis 10 dari konsentrasi ion hidrogen.
pH pada sebuah biogas plant bekerja normalnya terletak di antara 7 dan 8 dan
produksi biogas optimum dicapai untuk input digester dengan pH yang terletak
diantara 6 dan 7 [27].
Kebanyakan mikroorganisme lebih memilih rentang pH netral, yaitu sekitar
pH 7,0-7,5. Namun, beberapa organisme aktif pada nilai pH lebih rendah dan
lebih tinggi. Ada beberapa organisme yang berbeda dalam proses biogas, dan
persyaratan pH mereka untuk pertumbuhan yang optimal sangat bervariasi. Pada
fermentasi, mikroorganisme penghasil asam berhasil hidup dalam kondisi yang
relatif asam, pH dibawah 5.0, sebagian besar produsen metana umumnya
memerlukan nilai pH netral menjadi aktif. Meskipun sebagian besar produsen
metana berkembang terbaik pada nilai pH netral, mereka tetap aktif di luar ini
[22].
Nilai pH pada proses anaerobik akan mengalami penurunan dengan
diproduksinya asam volatil dan akan meningkat dengan dikonsumsinya asam
[image:36.595.122.505.559.703.2]volatil oleh bakteri pembentuk metana [28].
Tabel 2.7 Bahan kimia yang sering digunakan sebagai sistem penyangga [26]
Bahan Kimia Formula Kation Penyangga
Sodium bikarbonat NaHCO3 Na+
Potassium bikarbonat KHCO3 K+
Sodium karbonat Na2CO3 Na+
Potassium karbonat K2CO3 K+
Kalsium karbonat CaCO3 Ca2+
Kalsium hidroksida Ca(OH)2 Ca2+
Anhydrous ammonia
(gas) NH3 NH
4+
Sodium nitrat NaNO3 Na+
Aktivitas bakteri metanogens mulai terhambat pada pH 6,6 dan pH nilai di bawah 6 adalah indikasi yang jelas bahwa terlalu banyak asam yang terbentuk
17
sebagai hasil dari terlalu sedikit bakteri metanogens. nilai pH di atas 5 meskipun rendah dapat diperbaiki dengan penambahan kapur atau pengenceran umpan
digester. Nilai pH di bawah 5 akan mengarah pada penghentian digester dan
penggantian umpan [27].
2.5.2 Suhu
Suhu optimum, yaitu suhu di mana organisme tumbuh tercepat dan bekerja
paling efisien, memiliki nilai bervariasi untuk setiap spesies. Mikroorganisme
dapat dibagi menjadi kelompok-kelompok yang berbeda tergantung pada suhu di
mana mereka terbaik berkembang dan tumbuh: psychrophilic, mesofilik, termofilik, dan extremophilic/hyperthermophilic. Biasanya, Suhu optimum untuk organisme tertentu sangat terkait dengan lingkungan dari mana ia berasal [22].
Tingkat metabolisme dan pertumbuhan reaksi kimia dan biokimia
cenderung meningkat dengan suhu, sampai toleransi suhu mikroorganisme
terpenuhi. Jika suhu ekstrim, denaturasi sel akan terjadi mengakhiri kehidupan
efektif sel. Mikroorganisme menunjukkan pertumbuhan yang optimal dan tingkat
metabolisme dalam kisaran yang didefinisikan dengan suhu, yang spesifik untuk
masing-masing spesies. Organisme Psychrophilic berkembang dalam suhu di bawah 25 oC, mesofilik antara 25 oC dan 40oC dan thermophilic lebih tinggi dari
[image:37.595.126.500.512.694.2]45oC [29].
Gambar 2.5 Klasifikasi mikroorganisme berdasarkan suhu [22]
18
Secara umum, suhu terendah di mana mikroorganisme tumbuh, adalah -11
°C. Dibawah -25 °C, aktivitas enzim berhenti. Metanogens sensitif terhadap perubahan suhu yang cepat. Metanogen termofilik lebih sesitif suhu dibandingkan
mesofilik. Bahkan variasi kecil suhu menyebabkan penurunan substansial dalam
aktivitas. Oleh karena itu, suhu harus dijaga dengan tepat dalam jarak kurang
lebih 2 °C, Jika tidak, terjadi kehilangan gas hingga 30%. Terutama penting untuk
mesofilik adalah suhu di kisaran 40-45 °C, karena dalam rentang tersebut mereka
kehilangan aktivitas irreversibel [26].
2.5.3 Mixing (Pencampuran)
Pencampuran yang memadai sangat penting untuk mencapai keberhasilan
pengolahan anaerobik limbah cair organik. Dengan kata lain, pencampuran
meningkatkan proses anaerobik dengan mencegah stratifikasi substrat, mencegah
pembentukan permukaan kerak, memastikan sisa partikel padat dalam suspensi,
perpindahan panas seluruh digester, mengurangi ukuran partikel selama proses
pencernaan dan melepaskan biogas dari isi digester [30].
Pencampuran akan memberikan kontak yang baik antara substrat dan
mikroba memastikan suhu seragam, mengurangi resistensi terhadap perpindahan
massa, diminimalkan membangun kondisi lingkungan hambat menengah dan
menstabilkan [31]. Pencampuran juga meningkatkan produksi gas dibandingkan
dengan digester tidak mengalami pengadukan. Namun, pencampuran selama start
up tidak menguntungkan karena pH digester akan diturunkan menyebabkan
ketidakstabilan kinerja serta mengarah ke periode start-up yang lama [32].
2.5.4 Hydraulic Retention Time (HRT)
Hydraulic Retention Time (HRT) adalah periode waktu untuk volume tertentu cairan untuk dipertahankan dalam volume kerja reaktor [33]. HRT sama
dengan volume tangki (V) dibagi dengan aliran harian (Q) (HRT = V / Q). Waktu
retensi hidrolik penting karena menetapkan jumlah waktu yang tersedia untuk
pertumbuhan bakteri terutama untuk pertumbuhan bakteri Acidogenic hidrolitik dan konversi berikutnya dari bahan organik ke gas [32].
19
HRT juga memberlakukan peran penting untuk meningkatkan retensi sel
pada HRT tinggi atau rendah. Karena sistem dapat mempertahankan kandungan
biomassa yang tinggi dalam HRT yang berbeda [34].
Semakin lama HRT, semakin banyak bahan organik yang terdegradasi.
Namun, bahan organik yang paling rentan terhadap degradasi anaerobik biasanya
terdegradasi dalam waktu 14-50 hari (dalam reaktor biogas saja), tergantung pada
bahan baku, dan HRT yang tinggi hanya memerlukan volume reaktor yang lebih
besar dengan manfaat yang sedikit [23].
2.5.4 Solid Retention Time (SRT)
Solids Retention Time (SRT) adalah waktu rata-rata padatan lumpur (sludge) berada dalam sistem. SRT merupakan parameter operasi yang penting untuk proses anaerobik dan biasanya dinyatakan dalam hari [32]. Meskipun
perhitungan waktu retensi padatan sering dinyatakan dengan tidak tepat, SRT
merupakan jumlah padatan yang dipertahankan dalam digester dibagi dengan
jumlah padatan terbuang setiap hari seperti yang ditunjukkan pada persamaan di
bawah ini:
Qw CwCd V
SRT [32]
Dimana : V = Volume digester
Cd= Konsentrasi padatan dalam digester
Cw= Konsentrasi padatan yang dibuang
Qw = volume limbah yang dibuang setiap hari
Waktu retensi padatan (SRT) digunakan untuk mengendalikan laju
pertumbuhan mikroba dalam reaktor dan waktu rata-rata partikel padat, seperti
mikroba, dalam reaktor. Hal ini dihitung dengan membagi massa padatan dalam
reaktor dengan massa padatan yang dihilangkan dari sistem setiap hari [13].
Pada SRT yang rendah waktu yang tersedia tidak bagi bakteri untuk tumbuh
dan menggantikan bakteri yang hilang dalam limbah. Jika laju kehilangan bakteri
melebihi laju pertumbuhan bakteri,maka akan terjadi "wash-out". SRT di mana mulai terjadi "wash-out" adalah "critical SRT" [32].
20 2.5.5 Organic Loading Rate (OLR)
Organic loading rate (OLR) merupakan salah satu parameter yang paling penting dipelajari secara ekstensif untuk menyelidiki efek dari berbagai beban
substrat ketika salah satu limbah organik atau sintetis digunakan sebagai substrat
[33]. Semakin tinggi OLR tidak selalu mengarah pada hasil yang lebih tinggi
hidrogen. Oleh karena itu, optimasi variabel operasional sangat penting untuk
mendapatkan efisiensi produksi yang lebih tinggi. Namun demikian, optimalisasi
OLR hanya dapat dilaksanakan bila mikroba menyesuaikan diri dengan baik
terhadap OLR yang diterapkan terhadap substrat. [33]
2.6 VOLATILE FATTY ACID (VFA)
Volatile fatty acids (VFA) merupakan produk intermediet yang penting dalam produksi metana, dan konsentrasinya mempengaruhi efisiensi fermentasi.
VFA digunakan sebagai indikator keseimbangan proses [12]. Pada prinsipnya
produk akhir dari proses asidogenesis adalah VFA yang umumnya terdiri dari
asam asetat, asam propionat, asam n-butirat, asam iso-butirat, asam n-valerat, dan
asam iso-valerat [35].
Perubahan tingkat VFA yang terbukti menjadi parameter yang baik, di
bawah operasi tidak stabil, produk intermediet seperti asam volatil dan alkohol
terakumulasi pada laju yang berbeda tergantung pada substrat dan jenis gangguan
yang menyebabkan ketidakstabilan. Akumulasi asam lemak volatil
menggambarkan kinetika hubungan antara produsen dan konsumen asam. [32].
Pada kondisi termofilik, konsentrasi asam propionat sangat penting
daripada kondisi mesofilik. Selain itu, asam propionat merupakan senyawa yang
paling sulit untuk dikonversi ke intermediet lain karena persyaratan tekanan
parsial H2 rendah. Asam propionat memainkan peran penting dalam startup proses anaerobik serta kestabilan proses. Namun, asam propionat dianggap
sebagai VFA paling beracun yang ditemukan dalam digester anaerobik[13].
Wijekoon et al, 2011 melaporkan bahwa konsentrasi asam propionat lebih dari 1-2 g/l terbukti dapat menghambat bakteri metanogenesis[11-2].
21
2.7 ANALISA EKONOMI
Pada penelitian ini dilakukan analisa ekonomi yang sederhana terhadap
proses asidogenesis LCPKS pada keadaan ambient dengan produk yang diharapkan berupa VFA yang pada tahapan berikutnya dapat dikonversi menjadi
biogas. Kondisi yang digunakan adalah keadaan ambient sehingga tidak diperlukan pemanas dalam penelitian ini. Maka pada penelitian ini yang dikaji
adalah jumlah VFA yang akan dikonversi menjadi biogas pada proses digestasi
anaerobik dua tahap. Beberapa penelitian yang berhasil menghitung volume
[image:41.595.137.490.291.371.2]pembentukan biogas dari VFA disajikan pada Tabel 2.9.
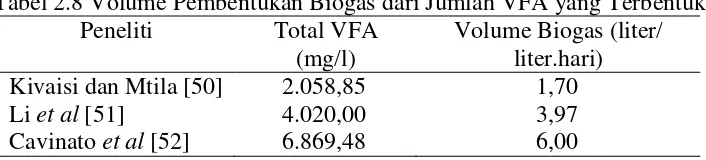
Tabel 2.8 Volume Pembentukan Biogas dari Jumlah VFA yang Terbentuk
Peneliti Total VFA
(mg/l)
Volume Biogas (liter/ liter.hari) Kivaisi dan Mtila [50]
Li et al [51] Cavinato et al [52]
2.058,85 4.020,00 6.869,48 1,70 3,97 6,00
Pada penelitian ini, total pembentukan VFA diperoleh pada variasi HRT 4
[image:41.595.154.462.475.623.2]hari (tanpa Recycle Sludge) dengan jumlah 5.583 mg/L. Menurut A.K. Kivaisi, et al konversi VFA menjadi biogas adalah 100%. Melalui Tabel 2.9 dapat digambarkan grafik linear seperti ditunjukkan pada Gambar 2.8 berikut.
Gambar 2.6 Konversi Total VFA menjadi Biogas [50, 51, 52]
Gambar 2.6 menunjukkan grafik linearisasi pembentukkan biogas dari
VFA dengan persamaan garis lurus: y = 0,0009 x + 0,104 dengan y merupakan
produksi biogas dan x merupakan VFA yang terbentuk. Berdasarkan persamaan y = 0,0009x + 0,104
0 2 4 6 8
0 1000 2000 3000 4000 5000 6000 7000 8000
P ro du k si B io g a s (lite r/lit er ·ha ri)
Total VFA (mg/l) Produksi Biogas
Linear (Produksi Biogas)
22
tersebut maka jumlah biogas yang dapat dihasilkan dari total VFA pada penelitian
ini adalah:
y = 0,0009 x + 0,104
= (0,0009) (5.583) + 0,104
= 5,13 liter biogas/liter LCPKS.hari
= 5,13 m3 biogas/m3 LCPKS hari
Ekivalensi 1 m3 biogas terhadap solar adalah sebesar 0,52 liter [53]. Sehingga
=
×
= 2,67 liter solar/m3 LCPKS
Harga solar industri adalah Rp 10.448,85/liter [54], sehingga untuk biogas yang
dihasilkan pada proses satu tahap diperoleh keuntungan sebesar:
Harga biogas yang dihasilkan =
×
= Rp. 27.898/m3 LCPKS
Jika LCPKS yang diolah sebesar 450 m3/ hari, maka keuntungan yang akan
diperoleh perhari adalah:
Keuntunan yang diperoleh =
×
= Rp. 12.554.100/hari
23
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI PENELITIAN
Penelitian ini dilakukan di Laboratorium Ekologi, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara (USU), Medan.
3.2 BAHAN DAN PERALATAN
3.2.1 Bahan-Bahan
1. Starter dari penelitian sebelumnya
2. Sampel LCPKS dari fat pit PKS Adolina 3. Asam klorida (HCl) 0,1 N
4. Aquadest (H2O)
5. Natrium Bikarbonat (NaHCO3)
3.2.2 Peralatan
3.2.2.1 Peralatan Utama
1. Fermentor tangki berpengaduk/jar fermentor (EYELA model No: MBF
300ME)
2. Pompa sludge/slurry pump (HEISHIN, model No.:3NY06F) 3. Gas meter (SHINAGAWA, model No.:W-NK-0.5B)
4. Tangki umpan (service tank) 5. Pengaduk
6. Sensor temperatur
7. pH elektroda
8. Timer (OMRON, model No.:H5F)
9. Botol penampungan keluaran fermentor 10.Gascollector
24 3.2.2.2 Peralatan Analisis
1. Buret 25 ml
2. Timbangan analitik
3. Oven
4. Desikator
5. Pipet volumetrik
6. Karet penghisap
7. Pengaduk magnetic 8. Furnace
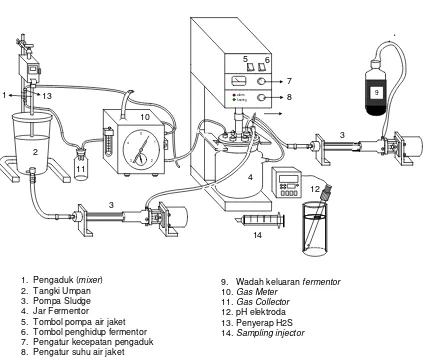
1. Pengaduk (mixer) 2. Tangki Umpan 3. Pompa Sludge 4. Jar Fermentor
5. Tombol pompa air jaket 6. Tombol penghidup fermentor 7. Pengatur kecepatan pengaduk 8. Pengatur suhu air jaket
1 0
2 4
3
1
11
7 5
3
10
8 6
4 2
3
alarm heating
13
12
14
9
9. Wadah keluaran fermentor
10. Gas Meter
11. Gas Collector
12. pH elektroda 13. Penyerap H2S
[image:44.595.117.542.285.648.2]14. Sampling injector
Gambar 3.1 Rangkaian Peralatan
25 3.3 TAHAPAN PENELITIAN
3.3.1 Analisis Bahan Baku Limbah Cair Pabrik Kelapa Sawit (LCPKS)
3.3.1.1 Analisis pH
Adapun prosedur analisis pH adalah [36]:
1) Kalibrasi pH meter dilakukan ke dalam pH 4, pH 7, dan pH 10. 2) Bagian elektroda dari pH meter dicuci dengan aquadest.
3) Elektoda dimasukkan ke dalam sampel yang akan diukur pH-nya.
4) Nilai bacaan pH meter ditunggu sampai konstan lalu dicatat nilai bacaannya.
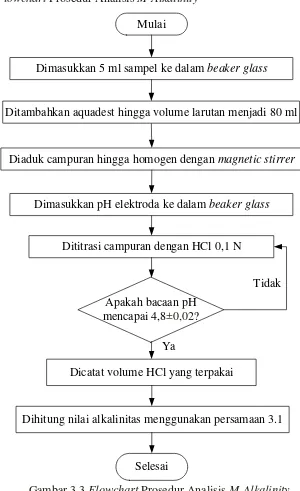
3.3.1.2 Analisis M-Alkalinity
Adapun prosedur analisis M-alkalinity adalah [36]:
1) Sampel dimasukkan sebanyak 5 ml ke dalam beaker glass lalu ditambahkan
dengan aquadest hingga volume larutan 80 ml.
2) Beaker glass diletakkan di atas magnetic stirrer, dan diletakkan pH elektroda
di dalam beaker gelas, kemudian stirrer dihidupkan dan kecepatan diatur sedemikian rupa hingga sampel tercampur sempurna dengan aquadest.
3) Campuran dititrasi dengan larutan HCl 0,1 N hingga pH mencapai 4,8 ± 0,02. 4) Analisis M-Alkalinity dilakukan untuk Limbah Cair Pabrik Kelapa Sawit
(LCPKS) dan limbah fermentasi pada Jar fermentor.
5) M-Alkalinity dapat dihitung berdasarkan rumus sebagai berikut:
M-Alkalinity mg NaHCO3 /L =
Sampel Vol
50000 x M x terpakai yang
Vol.HCl HCl
3.3.1.3 Analisis Total Solids (TS)
Adapun prosedur analisis Total Solids (TS) adalah [36]:
1) Cawan penguap kosong yang telah dibersihkan, dipanaskan pada 105oC di
dalam oven selama 1 jam. Apabila akan dilanjutkan untuk analisis zat tersuspensi organik, cawan dipanaskan pada 550oC, selama 1 jam.
2) Cawan didinginkan selama 15 menit di dalam desikator, lalu ditimbang. 3) Sampel dikocok merata, lalu dituangkan ke dalam cawan. Volume sampel
diatur sehingga berat residu antara 2,5-200 mg.
(3.1)
26
4) Cawan berisi sampel dimasukkan ke dalam oven, suhu 98oC untuk mencegah
percikan akibat didihan air di dalam cawan. Namun bila volum sampel kecil dan dinding cawan cukup tinggi maka langkah ini tidak perlu.
5) Pengeringan diteruskan di dalam oven dengan suhu 103-105oC selama 1 jam. 6) Cawan yang berisi residu zat padat tersebut didinginkan di dalam desikator
sebelum ditimbang.
7) Langkah 5 dan 6 diulang sampai didapat berat yang konstan atau berkurang
berat lebih kecil 4% berat semula atau 0,5 mg, biasanya pemanasan 1-2 jam sudah cukup. Penimbangan harus dikerjakan dengan cepat untuk mengurangi galat.
8) Kandungan TS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume
1000 B) -(A tal/L
padatan to
mg
Keterangan: A = berat residu kering + cawan porselen, mg B = berat cawan porselen, mg
3.3.1.4 Analisis Volatile Solids (VS)
Adapun prosedur analisis Volatile solids (VS) adalah [36]:
1) Cawan penguap setelah dari TS dipanaskan dengan menggunakan muffle
furnace pada suhu 550oC selama 1 jam.
2) Setelah itu cawan penguap didinginkan di dalam desikator hingga mencapai
suhu kamar.
3) Berat cawan penguap ditimbang.
4) Kandungan VS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume
1000 B) -(A latil/L
padatan vo
mg
Keterangan: A = berat residu+cawan porselen sebelum pembakaran, mg B = berat residu + cawan porselen setelah pembakaran, mg
3.3.1.5 Analisis Total Suspended Solids (TSS)
Adapun prosedur analisis Total Suspended Solids (TSS) adalah [36]: 1) Berat kertas saring kering yang digunakan ditimbang.
2) Kertas saring dibasahi dengan sedikit air suling.
(3.2)
(3.3)
27
3) Sampel diaduk dengan magnetic stirrer untuk memperoleh sampel yang
lebih homogen.
4) Sampel dipipetkan ke penyaringan dengan volume tertentu pada waktu
contoh diaduk dengan magnetic stirer.
5) Kertas saring dicuci atau disaring dengan 3 x 10 ml aquadest.
6) Kertas saring dipindahkan secara hati-hati dari peralatan penyaring ke wadah
timbang dengan aluminium sebagai penyangga.
7) Dikeringkan di dalam oven setidaknya selama 1 jam pada suhu 103ºC
sampai dengan 105ºC, didinginkan dalam desikator untuk menyeimbangkan suhu dan massanya.
8) Tahapan pengeringan, pendinginan dalam desikator, dan penimbangan
diulangi sampai diperoleh berat konstan atau sampai perubahan berat lebih kecil dari 4% terhadap penimbangan sebelumnya atau 0,5 mg.
9) Kandungan TSS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume 1000 B) -(A total/L rsuspensi padatan te
mg
Keterangan: A = berat kertas saring + berat residu, mg B = berat kertas saring, mg
3.3.1.6 Analisis Volatile Suspended Solids (VSS)
Adapun prosedur analisis Volatile Solids (VSS) adalah [36]:
1) Sampel residu hasil analisis TSS dibakar mengunakan api bunsen di dalam
cawan porselen yang telah dikering dan diketahui beratnya.
2) Setelah terbakar sempurna atau bebas asap, selanjutnya sampel diabukan
di dalam furnace pada suhu 550oC selama 1 jam.
3) Setelah 1 jam, furnace dimatikan dan sampel diambil setelah suhu furnace
sekitar 100oC dan disimpan di dalam desikator selama 15 menit lalu ditimbang.

![Gambar 2.3 Skema Proses Pengolahan Digestasi Anerobik [18]](https://thumb-ap.123doks.com/thumbv2/123dok/105622.8799/31.595.118.541.253.601/gambar-skema-proses-pengolahan-digestasi-anerobik.webp)
![Gambar 2.4 Pembentukan monomer [26]](https://thumb-ap.123doks.com/thumbv2/123dok/105622.8799/32.595.107.514.472.600/gambar-pembentukan-monomer.webp)
![Tabel 2.6 Degradasi pada Tahap Metanogenesis [26]](https://thumb-ap.123doks.com/thumbv2/123dok/105622.8799/34.595.106.486.350.459/tabel-degradasi-pada-tahap-metanogenesis.webp)
![Tabel 2.7 Bahan kimia yang sering digunakan sebagai sistem penyangga [26]](https://thumb-ap.123doks.com/thumbv2/123dok/105622.8799/36.595.122.505.559.703/tabel-bahan-kimia-digunakan-sistem-penyangga.webp)
![Gambar 2.5 Klasifikasi mikroorganisme berdasarkan suhu [22]](https://thumb-ap.123doks.com/thumbv2/123dok/105622.8799/37.595.126.500.512.694/gambar-klasifikasi-mikroorganisme-berdasarkan-suhu.webp)