!
"
! " #
$ "
! " # " $ % !# $ $
&' " (
$ ) * + *
,
- " .
+ "
/ . " 0 " %
"
1 " "
" 0 " %
' "
" " " ' 0
" " ,
- " "
/ 1
2 $
3 ! " $ ! " 4
$
5 ( 6 . % (
$ " " " "
! " #
$ % & % ' ' ( ( )
' * ' + # ' + *
%
• ' %# ,
• $ ' + #
,-• & -
,-• -
,-. % %/ # "
) & & % % " 0&& 1 -
-,-& % % 2' 3
) 4 % %/ ' 04 5'1 6 7 7 "
- 2- % + 4 + %#
-) 8 "# 9 08 91 " - :2- % +
4 + %#
:) % % ( + + $ '
7 % % 7 - :2- " 6 %
% & " " % %
& % % % " % % % % " " % % +
# % 0;6 1 % + "
" " % 3 " + % " % 3 # ) &
+ 3 " % 04! 1
" 4 % " " % 4 + " % % % " % %
( + 8 & + ' / 0(8&' 1 " " )
& % % " " % 4! " %
" " % 4
08 !1 # 4 < = = " " " % " - )
% % " 0 ; " ; 1 8 $ " ;6 "
3 + % # / # " " " % 3 " ;6 )
+ ;6 " * " % 4 # % + % )- > 2(
" % % % % % " % + % ? %
% + % :) - = )>< " -)< 2() ! " % ; " " % 8 $ % ?
% % + % - " - @ % % ;6 2 % % + % )
' * ( + 8 & + ' / % " % %
4
* " % % * %% % * %% + * " % % %
" " * ; 6 # * " 0;6 1 % " " * + * "
+ % A % %) % % * % * %
4#" * ! 04! 1 " 4 % / % + % 4 * " %
* %% % " % % % & 5 0& 51 + )
* %% " % " +# # 4!
" +# # 4 8 % " ! * 08 !1
4 <) = ) = ) " ) / % * " - ) #% % % "%
0 ; " ; 1 8 $ " ;6 * " * " %% %% * % *
* "% " " " ;6 ) % ;6 * "
% 4 ) % B - > 2( / * * * * * "
* * " " + # * * " % * # : - = >< " - < 2() ;
" * " " * 8 $ % * # -) " - ) @ "
;6 2 # ) )
' #/ "% & 5 * " % % + 4#" * !
4 ; 6 # * "
A
4
&5! C '5 ( '! &
&5 95 4 &! '
$5$ ' ;
! D C 4 $7& &5 7( ;
. ! ' . ! 8
$ 6 !
$ 6 ! 9 . !
$ 6 ! .5(
$ 6 ! ( & !
$ 6 ! 9'
$ 6 ! . (
A A A A A
A A . . &5 $ 47(7
) ( ! .5( ' 9
)- &5!7 7 ( 4
): 7E7 &5 5(
) 6 &5 5(
) !7 9 ( 9'7& &5 5(
:
. . E 7 &7 '
-) &5!'5 . 9 '5( & D $ $ 5
-)- ( . 4 8 ! & .! ' '5( & D 0(8&' 1
-)-) + ( + 8 & + ' / 0(8&' 1
-)-)- ' % ( + 8 & + ' / 0(8&' 1
-): &5 6 ( . 4 8 ! & .! ' '5( & D
0(8&' 1 5. 9 7. ! $ ( &! 5
$ 95 5! . '
-) &! 5 $ 95 5! . '
> >
-:
A
A
A
4
9 + -) ( % ( / 0" :4 1 " -
-9 + -)- $ & % % 5 % % # / "
( + # $ %
9 + -): ( + 8 & + ' /
9 + -) $ % % + 0 1, " 0.1 '
9 + -) & % % $ % % +
9 + -)< $ % % + $
9 + -)> & + ! %
9 + -) ' % ;6 3 " . %
9 + :) ! &
9 + ) & 4! " & 4 " %
9 + )- & 4! "
0; 1
9 + ): & 4! " ! " % -1
2 08 $1
9 + ) & 4! " & +
0;6 1
9 + ) & 4! " ;6 2 %
9 + )< & % "
9 + )> & ! ?! % " 4
9 + ) & 4 " ;
9 + ) & " ! ?! ;
9 + ) & 4 " 0; 1
9 + ) & 4 " ! ?! 0; 1
9 + ) - & 4 " ! " % -1
2 08 $1
9 + ) : & 4 " & +
0;6 1
-: -> : :
-:
< >
-:
A
A
A
" ; % 4
+ .) $ 4 % % % & +
0;6 1 " ; % 4
+ .) $ & ! % ;6 2 % " ; % 4
>
> >
A
A
( & ! $ $ '7 5
( & ! 5 4 ( 7E ( . ! ! 7
5) 4 ( 7E ( . ! ! 7 7 7' ( (5 '
$ ( ( . 4 8 ! & .! ' '5( & D 0(8&' 1
5)- 4 ( 7E ( . ! ! 7 7 7' ( &! 5
$ ( ( . 4 8 ! & .! ' '5( & D 0(8&' 1
5): 4 ( 7E ( . ! ! 7 7 7' (
' !. 4 $! $ ( ( . 4 8 ! & .! '
'5( & D 0(8&' 1
5) 4 ( 7E ( . ! ! 7 7 7' (
-% 3%7 320;6 1
<
<
>
>
A . $
8 $ 8& 8&' 8 ! 82 4! (8&' (&9 &'
& 5
8 .! . ''
7 . ;6 ; ;
, -1 2
-1 2
#
-# (
-9)
( + 8 & + ' /
% : 6 # 4
& + ' /
# - / 766
,
" . %
" ' % ' /
. 6 5 ,
A A
! "
.! *
4! ; ;!
. +
%% % +% % /
' % % +
D
; % +% % /
; " %
2 ) :
@ 2
: 2
:
& % % % " % % % % " " % % +
# % 0;6 1 % + "
" " % 3 " + % " % 3 # ) &
+ 3 " % 04! 1
" 4 % " " % 4 + " % % % " % %
( + 8 & + ' / 0(8&' 1 " " )
& % % " " % 4! " %
" " % 4
08 !1 # 4 < = = " " " % " - )
% % " 0 ; " ; 1 8 $ " ;6 "
3 + % # / # " " " % 3 " ;6 )
+ ;6 " * " % 4 # % + % )- > 2(
" % % % % % " % + % ? %
% + % :) - = )>< " -)< 2() ! " % ; " " % 8 $ % ?
% % + % - " - @ % % ;6 2 % % + % )
' * ( + 8 & + ' / % " % %
4
* " % % * %% % * %% + * " % % %
" " * ; 6 # * " 0;6 1 % " " * + * "
+ % A % %) % % * % * %
4#" * ! 04! 1 " 4 % / % + % 4 * " %
* %% % " % % % & 5 0& 51 + )
* %% " % " +# # 4!
" +# # 4 8 % " ! * 08 !1
4 <) = ) = ) " ) / % * " - ) #% % % "%
0 ; " ; 1 8 $ " ;6 * " * " %% %% * % *
* "% " " " ;6 ) % ;6 * "
% 4 ) % B - > 2( / * * * * * "
* * " " + # * * " % * # : - = >< " - < 2() ;
" * " " * 8 $ % * # -) " - ) @ "
;6 2 # ) )
' #/ "% & 5 * " % % + 4#" * !
4 ; 6 # * "
!
"
#$%&'(
" ) $ #")$ ( * ")$ +
,-+ ./ -0/
#)% ( 1+ +++ 2
#3% ( 1 +++ 2 0-1/ 0 1 "
!
")$ 4
! ")$ 4
3
-4 #1+-.1/(
#*+-0+/(
-! - 3
# (
5
0
,
5 !
.
3
' 6 ++* .
7)
+ * 8
! -!
! #9:;( 2 #)2<( ) %=
=
9:;
# (
# ( =>5 =
=>5
? =
4 , %
=>5 =
")$
9:; 5
9:;
*
0
4 =>5 $
! ! =>5
=>5 $
9:;
=
4 =
9:;
%
H # ( 3 =>5
")$ # ( 3 =
")$
=>5
; H
& =>5 ")$
&
& = ")$
=>5
; ! H
& ! 4 =>5 =>5
")$
& ! 4 = =
")$
=>5
* & !
1
$ " ' 5
: 5 I 4 I & $
" # $ % #) 5>( 4 ; 4
-4 H
9 H
"
$
5 $5$<
B H ")$ $
; $5$< 9
! H 1+
H 1+
5 H
! = 4 =>5H = ,
=>5 4 =H =>5 0
7 4 H 1
9 4 H
=>5 +@ 1@ +@ 1 0
= ! 4 0 1@ 1@ 1 1 ,
;
")$
; H
; =
; '! $ #& 5 (
* ; # " #5 ( #& ; $ (
0 ; " #9 ( #& ; $ (
1 ; # " " #5 ( #& ; $ (
, ; " " #9 ( #& ; $ (
. ; #)% ( #& > ! G 5 (
,
8 ; ! #9:;( #& ! (
;
)% =
; = '! $ ( 5 9
5 9 )% 9:; 1
+ * 1
; - H
; ")$
)& *
4 =>5 =>5 + 1 + 1 0
* % 4 = = ,@ 1 1
1 0 1
0 $ !
7
Dibandingkan dengan komoditi lainnya pada sub sektor perkebunan,
kelapa sawit merupakan salah satu komoditas yang pertumbuhannya paling pesat
pada dua dekade terakhir [14]. Dari 240 juta jiwa penduduk Indonesia saat ini,
lebih dari 46% bekerja di sektor pertanian. Kelapa sawit pertama kali masuk ke
Indonesia tahun 1911, dibawa oleh Adrien Hallet yang berkebangsaan Belgia.
Empat pohon sawit pertama dibawa dari Kongo, untuk kemudian ditanam di
Kebun Raya Bogor untuk melihat kecocokannya dengan iklim dan tanah di
Indonesia. Hasil perkembangbiakan dari tanaman induk inilah yang kemudian
menjadi cikal bakal perkebunan sawit pertama di Sumatera [1].
Kelapa sawit merupakan tanaman pohon tropis yang terutama ditanam
untuk menghasilkan minyak. Ditanam dan dipanen di daerah yang luas (3.000
sampai 5.000 ha) disekitar pabrik minyak sentral untuk memungkinkan
penanganan industri yang pesat [15]. Seiring dengan berkembangnya industri
sawit di Indonesia, luas areal perkebunan sawit juga semakin bertambah yang
dirangkum dalam Tabel 2.1 berikut, mulai dari tahun 2009 sampai 2013.
Tabel 2.1 Luas Areal Perkebunan Kelapa Sawit di Indonesia [16]
Tahun Luas areal (ha) Total (ha)
Perkebunan Besar Perkebunan Rakyat
2009 4.888.000 3.061.400 7.949.400
2010 5.161.600 3.387.300 8.548.900
2011 5.349.800 3.752.500 9.102.300
2012 5.995.700 4.137.600 10.133.300
2013 6.170.700 4.415.800 10.586.500
Menurut data Badan Pusat Statistik, pada tahun 2012 perkebunan kelapa
sawit di Indonesia sebagian besar berada di Pulau Sumatera seluas 6.624.900 Ha
diikuti oleh Kalimantan seluas 3.483.700 Ha, Sulawesi seluas 336.700 Ha, Papua
seluas 108.500 Ha dan Jawa seluas 32.600 Ha [16, 17]. Gambar 2.1 berikut
merupakan luas lahan sawit berbagai provinsi di Indonesia.
8
Gambar 2.1 Luas Lahan Sawit (dalam 103 Ha) pada Tahun 2012 [16]
Industri kelapa sawit berpotensi menghasilkan perkembangan ekonomi
dan sosial yang signifikan di Indonesia untuk mengurangi kemiskinan dan
memajukan pembangunan ekonomi [2, 17]. Salah satu hasil olahan kelapa sawit
adalah Minyak Sawit Mentah (MSM) seperti Crude Palm Oil (CPO) dan Crude
Palm Kernel Oil (CPKO) [18]. Minyak sawit merupakan minyak yang berasal
dari proses ekstraksi tandan buah segar kelapa sawit. Dapat digunakan untuk
konsumsi makanan maupun non konsumsi. Peningkatan permintaan untuk minyak
sawit didorong oleh meningkatnya konsumsi minyak nabati karena perkembangan
populasi manusia [19]. Tabel 2.2 berikut merupakan produksi minyak kelapa
sawit dunia.
Tabel 2.2 Produksi Minyak Kelapa Sawit Dunia, dalam Jutaan Ton [20] 2010/11 2011/12 2012/13 2014/15 Nov
Perkembangan pesat pada industri kelapa sawit setiap tahunnya telah
memberikan kontribusi terhadap pencemaran lingkungan dengan dihasilkan 1222,9
sejumlah besar residu dar
ekstraksi minyak sawit
produksi pada industri sa
terdiri dari tandan kosong
digunakan sebagai bahan
5].
Limbah cair dihas
dekanter. Limbah cair ini
sterilizer yang disebut
diagram alir proses ekstra
dengan limbah yang dihas
Gambar 2.2 Diagram A
9
dari proses di pabrik kelapa sawit yang berasal da
dari tandan buah segar di pabrik kelapa sawi
stri sawit menghasilkan limbah padat dan cair. Limb
osong buah, serat mesocarp buah dan cangkang kela
bahan bakar untuk menghasilkan uap dan listrik di p
dihasilkan dari ekstraksi minyak sawit dari proses
ini dikombinasikan dengan limbah dari air pendi
ebut sebagai LCPKS [3]. Gambar 2.1 berikut m
ekstraksi minyak sawit pada industri kelapa sawit, d
dihasilkan beserta sumbernya.
gram Alir Proses Ekstraksi Minyak Sawit dan Limbah Dihasilkan [21]
dari proses
sawit. Proses
Limbah padat
g kelapa sawit,
di pabrik [3,
roses basah di
pendingin dan
ut merupakan
wit, dilengkapi
imbah yang
10
Berdasarkan gambar di atas, dapat diketahui bahwa terdapat tiga sumber
utama limbah cair yang dihasilkan dari pabrik kelapa sawit konvensional yaitu
sterilizer kondensat, pemisah lumpur dan limbah hidrosiklon dengan
perbandingan sekitar 0,9 : 1,5 : 0,1 m3 [22, 23]. Produksi 1 juta ton minyak sawit
mentah membutuhkan 5 juta ton tandan buah segar (TBS). Rata rata pengolahan 1
juta ton TBS di Pabrik Kelapa Sawit menghasilkan 230.000 ton tandan kosong
buah (TKS) dan 650.000 ton LCPKS sebagai residu [20].
! !#' (' # !" ! ! # $!%! !& '
LCPKS adalah suspensi koloid berwarna kecoklatan yang mengandung
95 96% air, 0,6% minyak dan 0,7% lemak, dan 4 5% dari total padatan, memiliki
konsentrasi COD yang tinggi karena memiliki jumlah karbon rendah (8 20) dari
asam amino dan asam lemak yang terlarut, mengandung padatan dan minyak,
bersifat asam, mengandung bahan organik tinggi yang tidak beracun karena tidak
ada bahan kimia yang ditambahkan selama proses ekstraksi minyak dan
mengandung zat hara yang cukup untuk tanaman [4, 24, 25]. Adanya kandungan
COD yang tinggi, menyebabkan LCPKS berpotensi menjadi polutan, namun
karena kandungan organiknya juga tinggi, maka LCPKS dapat diuraikan secara
biologis.
Gambar 2.3 Limbah Cair Pabrik Kelapa Sawit (LCPKS) [26]
Karakteristik LCPKS dapat berbeda untuk operasi yang berbeda setiap
harinya dari pabrik pabrik industri kelapa sawit, tergantung pada teknik
pengolahan, usia atau jenis buah, iklim dan kondisi pengolahan kelapa sawit [21].
Tabel 2.3 berikut merupakan karakteristik LCPKS secara umum.
11
Tabel 2.3 Karakteristik Limbah Cair Pabrik Kelapa Sawit (LCPKS) [23, 27]
Parameter Satuan Nilai
pH – 4 – 6
Suhu °C 60 – 80
Biochemical Oxygen Demand (BOD) mg/l 20.000 – 60.000
Chemical Oxygen Demand (COD) mg/l 40.000 120.000
Total Solids (TS) mg/l 30.000 – 70.000
Total Suspended Solids (TSS) mg/l 15.000 – 40.000
Volatile Solids (VS) mg/l 9.000 – 72.000
Sistem pengolahan LCPKS pada dasarnya terdiri dari proses anaerobik dan
proses aerobik. Tiga sistem pengolahan yang paling umum digunakan adalah
kolam stabilisasi, digester tangki terbuka dengan aerasi diperpanjang, dan digester
tangki tertutup yang menghasilkan biogas dan sistem aplikasi tanah [28]. Sistem
kolam stabilisasi adalah metode anaerob konvensional yang paling sering
digunakan untuk pengolahan LCPKS [4].
LCPKS merupakan limbah yang sangat polutan. Limbah cair yang tidak
ditangani dengan baik akan menyebabkan polusi berupa ancaman besar bagi
daerah sekitar aliran sungai dan badan air serta menimbulkan bau busuk pada
daerah sekitar pabrik, ditambah dengan nilai BOD yang tinggi dan pH yang
rendah, menyebabkan LCPKS sangat sulit untuk diolah dengan metode
konvensional [28]. Oleh karena itu, dibutuhkan pengolahan sebelum LCPKS
dibuang ke lingkungan. Tabel 2.4 berikut merupakan baku mutu limbah cair
industri minyak sawit yang diperbolehkan dibuang ke lingkungan.
Tabel 2.4 Baku Mutu Limbah Cair untuk Industri Minyak Sawit [29]
Parameter Kadar Maksimum
(mg/l)
Beban Pencemaran Maksimum (kg/ton)
12
) *
Limbah cair yang dihasilkan dari proses produksi diolah di instalasi
pengolahan air limbah. Untuk penanganannya perlu dibangun kolam limbah
dengan kapasitas yang dapat menampung limbah cair dengan kapasitas olah
pabrik brondolan sawit/jam. Tahapan proses pengolahan air limbah terdiri atas:
(1) eoling Pond, (2) Kolam Pendingin, (3) Primary Anoerbic Pond, (4)
Secondary Anaerobic Pond dan (5) Aeration Pond. Waktu tinggal limbah pada
kolam keseluruhan adalah 109 hari, maka perluasan kolam limbah harus
dilakukan sejalan dengan pengembangan kapasitas produksi [30].
Pengolahan secara konvensional ini membutuhkan waktu yang lama dan
lahan yang luas, sedangkan LCPKS merupakan sumber pencemar potensial yang
dapat memberikan dampak serius bagi lingkungan, sehingga pabrik kelapa sawit
dituntut untuk menangani limbah ini melalui peningkatan teknologi pengolahan
(end of pipe) [31]. Peningkatan permintaan konsumen minyak sawit berbanding
lurus dengan produksi pabrik kelapa sawit sehingga berakibat pada peningkatan
LCPKS yang mengandung konstituen biodegradable atau dapat diuraikan secara
biologis dengan rasio BOD/COD sebesar 0,5 [32].
Biogas atau biometana adalah pilihan yang efisien untuk mencegah dan
mengurangi polusi serta memberikan energi yang berkualitas tinggi untuk bahan
bakar kendaraan, pembangkit listrik, dan pemanas [33]. Komposisi biogas
bervariasi sangat tergantung pada bahan organik dan proses biologis yang
digunakan [34]. Tabel 2.5 berikut merupakan karakteristik biogas secara umum.
Tabel 2.5 Karakteristik Biogas [6, 35, 36]
Parameter Komposisi
Metana (CH4) 50 – 75%
Karbon dioksida (CO2) 30 – 40%
Nitrogen (N2) 0,4 – 1,2%
Oksigen (O2) 0 – 0,4%
Hidrogen Sulfida (H2S) 0,02 – 0,4%
Kandungan Energi 6,0 – 6,5 kWh/m3
Kesetaraan Bahan Bakar 0,60 – 0,65 liter minyak/m3 udara
Batas Ledakan 6 – 12% biogas di udara
Temperatur Nyala 650 – 750 °C
Tekanan Kritis 75 – 89 bar
13
Parameter Komposisi
Temperatur Kritis –82,5 °C
Densitas Normal 1,2 kg/m3
Massa Molar 16,043 kg/kmol1
Salah satu keuntungan utama dari produksi biogas adalah kemampuan
untuk mengubah limbah menjadi sumber daya yang berharga, dengan
menggunakannya sebagai substrat untuk proses digestasi anaerobik [9]. Secara
umum, bahan baku substrat untuk pembuatan biogas harus mengandung tiga jenis
makromolekul yaitu karbohidrat, protein dan lipid [37]. Kandungan karbohidrat,
protein, senyawa nitrogen, lipid dan mineral yang tinggi dalam LCPKS
menjadikan LCPKS sebagai substrat yang baik untuk biokonversi melalui
berbagai proses bioteknologi [38]. Jika substrat untuk proses digestasi anaerobik
terdiri atas campuran homogen dari dua atau lebih jenis bahan baku (misalnya
lumpur kotoran hewan dan limbah organik dari industri makanan), proses ini
disebut o digestion dan umum digunakan dalam pembuatan biogas [9]. Tabel 2.6
berikut merupakan potensi biogas yang dihasilkan oleh beberapa substrat.
Tabel 2.6 Potensi Biogas yang Dihasilkan oleh Beberapa Substrat [42]
Komponen Biogas (m3/kg VS)
Komposis Biogas (CH4 : CO2) Karbohidrat
Lemak Protein
0,38 1,00 0,53
50 : 50 70 : 30 60 : 40
+
Beberapa spesies mikroba telah dikenal karena kemampuan mereka untuk
memecah bahan organik yang ada dalam limbah dengan memproduksi suatu
produk bernilai tambah [38]. Biogas merupakan produk gas dari proses digestasi
anaerobik, yaitu proses biokimia dimana bahan organik yang kompleks terurai
dalam ketiadaan oksigen dengan memanfaatkan aktivitas berbagai jenis
mikroorganisme [39]. Selama proses tersebut, bahan organik diubah terutama
untuk menjadi metana (CH4), karbon dioksida (CO2), dan biomassa. Nitrogen
dilepaskan dari senyawa organik dan dikonversi menjadi amonia [40]. Proses
anaerobik digunakan untuk mengolah limbah cair dengan kandungan organik
yang tinggi (BOD>500mg/l), bertujuan untuk pengolahan lebih lanjut dari lumpur
14
primer dan sekunder dari pengolahan air limbah konvensional [41]. Gambar 2.4
berikut merupakan skema digester anaerobik dengan sistem atch dan kontinu.
Gambar 2.4 Skema Digester Anaerobik (A) Batch dan (B) Kontinu [42]
Terdapat beberapa keuntungan dari proses digestasi yaitu mampu
mengolah limbah dengan kandungan senyawa organik yang tinggi, tidak
membutuhkan peralatan aerasi, investasi energi rendah dan jumlah lumpur yang
dihasilkan jauh lebih rendah dari proses aerobik [43]. Gambar 2.5 berikut
merupakan tahapan proses digestasi anaerobik.
Gambar 2.5 Tahapan Proses Digestasi Anaerobik [44]
15
+ , -$ ( (
Hidrolisis adalah tahapan ekstraseluler enzim dimediasi yang melarutkan
partikulat dan substrat yang tidak dapat langsung dimanfaatkan oleh organisme
anaerobik [40]. Pada hidrolisis terjadi degradasi bahan organik dan senyawa
dengan berat molekul tinggi seperti lipid, polisakarida, dan protein menjadi
molekul kecil dan substrat organik terlarut (misalnya, glukosa asam lemak pasir,
asam amino), yang cocok untuk digunakan sebagai sumber energi dan sel karbon
[45]. Senyawa yang terbentuk selama hidrolisis digunakan selama tahapan
asidogenesis.
!"#"$"$%idrolisis Polisakarida
Reaksi yang terjadi adalah [9]:
Polisakarida enzimselulosa,selobiase,xilanase,amilase→ monosakarida
Polisakarida adalah senyawa yang mengandung rantai gula terkait.
Polisakarida yang umum adalah selulosa, hemiselulosa, pati, pektin, dan glikogen.
Hidrolisis selulosa hasil dalam pembentukan selobiosa (dua molekul glukosa yang
saling berhubungan) dan glukosa. Pati dan glikogen dipecah menjadi unit glukosa,
dan beberapa gula yang berbeda terbentuk dari hemiselulosa dan pektin.
Organisme yang aktif dalam proses biogas selama hidrolisis polisakarida
termasuk berbagai kelompok bakteri dalam, misalnya, Bacteriodes genera,
Clostridium, dan Acetivibrio [42].
2.4.1.2 Hidrolisis Protein
Reaksi yang terjadi adalah [9]:
Protein enzimprotease→ asam amino
Protein adalah rantai asam amino yang ditemukan dalam konsentrasi
tinggi. Asam amino adalah produk primer akhir hidrolisis protein dan peptida.
Selain asam amino, dekomposisi glikoprotein juga memproduksi berbagai
karbohidrat. Organisme proteolitik dalam proses biogas antara lain, genera
Clostridium, Peptostreptococcus, dan Bifidbacterium [42].
16 !"#"$") Hidrolisis Lemak
Reaksi yang terjadi adalah [9]:
Lemak enzimlipase→ asam lemak, gliserol
Umumnya lemak terdiri dari gliserol (alkohol) dan asam lemak yang
berbeda, yang semuanya dirilis oleh biodegradasi. Enzim yang memecah lemak
disebut lipase. Sebagian besar lipase diketahui diproduksi oleh mikroorganisme
aerobik aerobik atau fakultatif. Mikroorganisme anaerobik yang banyak
mengeluarkan lipase antara lain, genus Clostridium [42].
+ ( ,-. / ( (
Selama asidogenesis, produk hidrolisis diubah oleh bakteri asidogenik
menjadi substrat untuk metanogen [9]. Bahan molekul kecil dan substrat organik
terlarut didegradasi menjadi VFA (misalnya asam asetat, asam propionat, asam
butirat, asam suksinat, asam laktat dan lain lain), alkohol, ammonia, CO2 dan H2
[42]. Gula sederhana, asam amino dan asam lemak terdegradasi menjadi asetat,
karbon dioksida dan hidrogen (70%) serta menjadi VFA dan alkohol (30%) [9].
Pada tahapan ini, mikroorganisme asidogenesis menyediakan substrat yang
penting bagi mikroorganisme asetogenesis dan mikroorganisme metanogenesis.
Banyak mikroorganisme yang berbeda, aktif selama tahap ini lebih dari pada
tahap lain. Mikoorganisme pada tahap ini sama dengan tahap hidrolisis, namun
organisme lain juga aktif, misalnya Enterobacterium, Bacteriodes,
Acetobacterium, Eubacterium, Clostridium, Ruminococcus, Butyribacterium,
Propionibacterium, Lactobacillus, Streptococcus, Pseudomonas, Desulfobacter,
Micrococcus, Bacillus dan Escherichia. Para anggota fakultatif kelompok ini juga
membantu melindungi metanogen yang sensitive terhadap oksigen dengan
mengkonsumsi jejak oksigen yang dapat masuk dalam umpan [42, 46].
+ ) ( '-. / ( (
Produk dari asidogenesis, yang tidak dapat langsung diubah menjadi
metana oleh bakteri metanogen, diubah menjadi substrat metanogen selama
asetogenesis [9]. Asetogenesis merupakan tahapan dimana asam organik yang
lebih tinggi dan zat zat lain yang dihasilkan oleh asidogenesis selanjutnya dicerna
17
oleh asetogen untuk menghasilkan asam asetat, CO2 dan hidrogen yang dapat
digunakan oleh metanogen untuk produksi metana [46].
VFA dengan rantai karbon lebih panjang dari dua unit, dan alkohol dengan
rantai karbon lebih panjang dari satu unit, dioksidasi menjadi asetat dan hidrogen
[9]. Konversi substrat menjadi asetat mengikuti reaksi berikut [47]:
Reaksi sintrofik asetogenik:
• Propionat + 3H2O → asetat + HCO3 + H+ + 3H2
• Butirat + 2H2O → 2 asetat + H+ + 2H2
• Propionat + 2HCO3 → asetat + 3 format + H+
• Butirat + 2HCO3 → 2 asetat + 2 format + H+
Reaksi homoasetogenik:
• Laktat → 1 ½ asetat + ½ H+
• Etanol + HCO3 → 1 ½ asetat + H2O + ½ H+
• Metanol + ½ HCO3 → ¾ asetat + H2O
• 4H2 + 2HCO3 + H+ → asetat + 4H2O
yntrophomonas, Syntrophus, Clostridium, dan Syntrobacter adalah
contoh genus dari mikroorganisme yang dapat melakukan oksidasi anaerobik
yang bersintrofik dengan mikroorganisme untuk menguraikan gas hidrogen.
Banyak organisme ini dikenal sebagai asetogens, yaitu selain gas hidrogen dan
karbon dioksida mereka juga membentuk asetat sebagai produk utama [42].
+ + '!/-. / ( (
Metanogenesis adalah tahapan mengubah senyawa antara menjadi produk
akhir yang lebih sederhana, terutama CH4 dan CO2 oleh dua kelompok
mikroorganisme metanogen: kelompok pertama mengkonversi asetat menjadi
metana dan karbon dioksida (methanogen aceticlastic) dan kelompok kedua
menggunakan hidrogen sebagai donor elektron dan CO2 sebagai akseptor untuk
menghasilkan metana (methanogen hydrogenotrophic). Sekitar 72% dari metana
yang dihasilkan dalam pencernaan anaerobik adalah dari asetat; dan 28% dari
metana berasal dari hidrogen [6, 45]. Reaksi yang terjadi yaitu [47]:
• Hidrogen : 4 H2 + CO2 → CH4 + 2 H2O
• Asetat : CH3COOH → CH4 + CO2
18
• Metanol : 4 CH3OH → 3 CH4 + CO2 + 2 H2O
Metanogenesis merupakan tahapan kritis dalam seluruh proses pencernaan
anaerobik, karena merupakan reaksi biokimia yang paling lambat [9]. Saat ini
hanya ada dua kelompok yang diketahui dari metanogen yang memecah asetat
yaitu -ethanosaeta dan Methanosarcina, sementara yang memecah gas hidrogen
yaitu Methanobacterium, Methanococcus, Methanogenium dan
Methanobrevibacter [42].
0
Tiga kelompok bakteri yang berbeda (fermentasi, asetogenik dan
metanogen) terlibat dalam proses digestasi anaerobik dan bakteri ini secara luas
berbeda satu sama lain dalam fisiologi dan kebutuhan gizi. Ketika substrat mudah
terhidrolisis seperti pati terlarut diperlakukan anaerob, proses ini memiliki
masalah pada tingkat pembebanan yang tinggi karena ketidakseimbangan antara
asam dan pembentukan metana [48]. Untuk mengatasi masalah ini, banyak upaya
telah dilakukan untuk memisahkan proses menjadi dua tahap yang berbeda yang
pertama untuk tahap hidrolisis dan asidogenesis sedangkan tahap kedua untuk
metanogenesis. Proses digestasi anaerobik dua tahap dapat digambarkan sebagai
berikut:
Gambar 2.6 Digestasi Anaerobik Dua Tahap [46]
Ide dari proses digestasi anaerobik dua tahap pada awalnya diusulkan oleh
Pohland dan Ghosh (1971). Hal ini bertujuan untuk meningkatkan biodegradasi
anaerob melalui pemisahan yang terkendali dari reaksi utama [46]. Pada proses
19
digestasi dua tahap, substrat dimasukkan ke dalam reaktor tahap pertama, cairan
yang mengandung senyawa antara, terutama VFA secara terus menerus
dikeluarkan dan dimasukkan ke reaktor tahap kedua yaitu tahap metanogen.
Dengan cara ini, kondisi masing masing tahap dapat dioptimalkan, kemudian
senyawa antara seperti VFA yang dapat menghambat kelompok mikroorganisme
dalam konsentrasi tinggi, terus menerus dapat dicuci dari reaktor tahap pertama
[49]. Mikroorganisme yang terkait dengan hasil tahap pertama memiliki tingkat
pertumbuhan dan aktivitas tertinggi, maka reaktor asidogenik akan selalu lebih
kecil dari reaktor metanogen [46]. Tujuan dari proses digestasi anaerobik dua
tahap tidak hanya untuk lebih mendegradasi limbah, tetapi juga untuk
mengekstrak energi lebih bersih dari sistem [50].
Penelitian JE Hernandez dan RGJ Edyvean, 2011 [51] menggunakan .o stage (asidogenesis dan metanogenesis) anaerobic digestion (TSAD) yang
dibandingkan dengan single stage anaerobic digestion (SSD) untuk mengolah air
limbah sintetis yang terkontaminasi fenol. Kedua sistem dioperasikan dalam
batch dilution dan semi kontinu pada 35°C. TSAD memiliki produksi biogas
lebih besar, pada reaktor asidogenesis lebih mudah terjadi penguraian tanpa
hambatan oleh akumulasi fenol (sampai 1.450 mg/l). Reaktor asidogenesis juga
mencegah penghambatan pembentukan biogas di tahap kedua (metanogen),
dengan menghambat fenol dan dihasilkan asam organik dengan cepat. Sistem ini
meningkatkan produksi biogas dan memungkinkan kontrol yang lebih baik dari
tahap asidogenesis dan metanogen.
Penelitian Noha et al, 2012 [50] mengevaluasi proses digestasi anaerobik
satu tahap dan dua tahap untuk produksi biometana dan biohidrogen
menggunakan thin stillage, hal ini dilakukan untuk menilai dampak dari
memisahkan tahap asidogenesis dan metanogenenesis pada digestasi anaerobik.
Thin stillage merupakan produk sampingan dari produksi etanol, ditandai dengan
TCOD yang tinggi mulai dari 122 g/l dan TVFA mulai dari 12 g/l. Dihasilkan
metana maksimum sebesar 0,33 L CH4/g CODadded pada proses dua tahap
sementara proses satu tahap mencapai hasil maksimum hanya sebesar 0,26 L
CH4/g CODadded. Pemisahan tahap pengasaman meningkatkan TVFA untuk rasio
TCOD dari 10% pada thin stillage mentah menjadi 54% karena konversi
20
karbohidrat menjadi hidrogen dan VFAs. Perbandingan dari dua proses
berdasarkan hasil akhir energi menunjukkan bahwa peningkatan terbesar 18,5%
pada keseluruhan untuk menghasilkan energi dicapai dengan menggunakan
digestasi anaerobik dua tahap.
Penelitian Prawit et al, 2014 [52] menggunakan reaktor UASB yang
dioperasikan pada kondisi termofilik dan digunakan untuk menyelidiki proses
anaerobik dua tahap untuk memproduksi hidrogen dan metana secara kontinu dari
skim lateks serum (SLS). Reaktor tahap pertama untuk memproduksi hidrogen
dioperasikan dengan umpan 38 g VS/L SLS dengan variasi HRT dari 60, 48, 36,
dan 24 jam. Produksi yield hidrogen optimum adalah 2,25±0,09 L H2/L SLS
dicapai pada HRT 36 jam. Effluent yang mengandung asetat diumpankan ke
reaktor UASB kedua untuk produksi metana pada HRT 9 hari dan dihasilkan
konversi metana 6.41±0.52 L CH4/L SLS. Efisiensi removal bahan organik yang
diperoleh dari proses dua tahap ini adalah 62%. Penelitian ini menunjukkan bahan
bakar gas bernilai tinggi dalam bentuk hidrogen dan metana dapat berpotensi
dihasilkan dengan menggunakan proses anaerobik dua tahap terus menerus, di
mana bahan organik yang tersedia secara bersamaan terdegradasi.
1 2
Proses digestasi anaerobik harus dipantau untuk memastikan keberhasilan
dari proses ini. Beberapa parameter yang penting dalam proses digestasi
anaerobik yaitu:
1 ! ! ' . ('!( /! - #
2.6.1.1 pH
pH merupakan parameter penting dalam pemantauan dan pengendalian
digestasi anaerobik [6]. Proses anaerobik sangat sensitif terhadap pH. Dalam
kebanyakan kasus, degradasi anaerobik bahan organik dicapai paling efisien pada
pH netral. Namun, banyak juga yang dapat tumbuh pada pH yang lebih rendah
atau lebih tinggi [51]. Pembentukan metana berlangsung pada kisaran pH 5,5 8,5,
dengan pH optimum untuk metanogenik adalah 7,0 8,0 [9]. pH mengontrol fraksi
21
VFA terdisosiasi yang dianggap bebas menembus membran sel mikroorganisme.
Setelah menyerap membran, asam lemak internal terpisah sehingga menurunkan
pH sitoplasma dan mempengaruhi metabolisme bakteri [6]. Nilai pH pada proses
anaerobik akan mengalami penurunan dengan diproduksinya asam volatil dan
akan meningkat dengan dikonsumsinya asam volatil oleh bakteri pembentuk
metana [54]. Mikroorganisme asidogenik dapat tumbuh dan terus menghasilkan
asam pada pH rendah (5 6) [53]. Tingkat pH optimal untuk kelompok fungsional
biokimia pada proses anaerob yaitu [40]:
1) Hidrolisis, biasanya optimal di atas pH 6 tetapi memungkinkan hingga pH 5.
2) Asidogenesis, optimal antara pH 5,5 dan 8, tetapi memungkinkan hingga pH 4.
3) Asetogenesis/hidrogen memanfaatkan metanogen, optimal antara pH 6,5 dan 8
tetapi memungkinkan hingga pH 5.
4) Metanogenenesis, optimal antara pH 7 dan 8, tetapi memungkinkan hingga pH
6.
!"/"$"! &alinitas
Alkalinitas adalah ukuran dari jumlah alkali (dasar) zat dalam proses
biogas. Semakin tinggi alkalinitas, semakin besar kapasitas buffer dalam proses,
yang akan menstabilkan nilai pH. Alkalinitas terutama terdiri dari ion bikarbonat
yang berada dalam keseimbangan dengan karbon dioksida. Karbon dioksida dan
ion karbonat juga berkontribusi terhadap alkalinitas. Dekomposisi substrat kaya
nitrogen dengan proporsi yang tinggi protein dan asam amino dapat meningkatkan
alkalinitas, karena amonia dirilis dapat bereaksi dengan karbon dioksida terlarut
membentuk amonium bikarbonat. Berikut merupakan reaksi dari karbon dioksida
dalam kesetimbangan dengan asam karbonat dan karbonat [42]:
CO2 + H2O ↔ H2CO3 ↔ HCO3 + H+ ↔ CO32 + 2H+
Kapasitas buffer sering disebut sebagai alkalinitas. Kapasitas buffer
sebanding dengan konsentrasi bikarbonat. Kapasitas buffer adalah metode yang
dapat diandalkan untuk mengukur ketidakseimbangan digester. Peningkatan
kapasitas buffer yang rendah, paling baik dilakukan dengan mengurangi organic
loading rate, meskipun pendekatan yang lebih cepat adalah penambahan basa
kuat atau garam karbonat untuk menghilangkan karbon dioksida dari ruang gas
22
dan mengubahnya menjadi bikarbonat, atau bikarbonat dapat ditambahkan secara
langsung [6]. Nilai alkalinitas tinggi (2000 4000 mg/l menggunakan CaCO3)
sering diperlukan untuk memastikan pH mendekati netral selama kandungan CO2
tinggi (30 50%). Tingkat alkalinitas yang dibutuhkan jarang tersedia pada air
limbah influen, tetapi dapat dihasilkan oleh degradasi protein dan asam amino
[45] juga bisa ditingkatkan menggunakan penambahan senyawa kimia. Tabel 2.7
berikut merupakan bahan kimia yang biasa digunakan sebagai penyangga.
Tabel 2.7 Bahan Kimia yang Biasa Digunakan sebagai Penyangga [36]
Bahan Kimia Formula Kation Penyangga
Sodium bikarbonat NaHCO3 Na+
Potassium bikarbonat KHCO3 K+
Sodium karbonat Na2CO3 Na+
Potassium karbonat K2CO3 K+
Kalsium karbonat CaCO3 Ca2+
Kalsium hidroksida Ca(OH)2 Ca2+
Anhydrous ammonia (gas) NH3 NH4+
Sodium nitrat NaNO3 Na+
Parameter yang lebih sensitif untuk memantau digester dan mengukur
stabilitas proses adalah VFA/rasio alkalinitas, ketika rasio ini kurang dari 0,35
0,40 (setara asam asetat/setara CaCO3) proses ini dianggap beroperasi
menguntungkan tanpa resiko pengasaman [6].
!"/"$") emperatur
Temperatur merupakan salah satu faktor lingkungan yang paling
berpengaruh karena mengontrol aktivitas semua mikroorganisme. Umumnya,
kenaikan suhu menyebabkan peningkatan laju reaksi biokimia dan enzimatik
dalam sel menyebabkan tingkat pertumbuhan meningkat. Namun, di atas suhu
tertentu yang merupakan karakteristik dari masing masing spesies, hal ini menjadi
penghambat dan menjadi tahap kematian mikroorganisme seperti protein dan
komponen struktural sel menjadi denaturasi. Terdapat tiga kondisi temperatur
yang memungkinkan mikroorganisme anaerobik berkembang, yaitu mesofilik
dengan temperatur optimum pada 30 37°C, termofilik dengan temperatur
optimum 55 60°C dan psikropilik dengan temperatur optimum pada 15 20°C
23
(ambient) [46]. Gambar 2.7 berikut merupakan tingkat pertumbuhan relatif
mikroorganisme anaerobik.
Gambar 2.7 Tingkat Pertumbuhan Relatif Mikroorganisme Metanogen [9]
Kondisi psikropilik sebagian besar terdapat di lingkungan, sementara
kondisi mesofilik dan termofilik sebagian besar dalam sistem rekayasa [40].
Dalam prakteknya, temperatur operasi dipilih dengan mempertimbangkan bahan
baku yang digunakan dan temperatur proses yang diperlukan dapat disediakan
oleh ruangan atau menggunakan sistem pemanas pada digester [9]. Enzim
berkembang dalam mikroorganisme setelah penyesuaian yang dapat mentolerir
perubahan suhu. Akibatnya ada mikroorganisme yang dapat tumbuh di lebih dari
satu rentang suhu. Digestasi anaerobik mesofilik dan termofilik lebih banyak
digunakan daripada psikropilik karena laju reaksi tinggi pada rentang suhu
tersebut. Namun, suhu psikropilik sering terjadi berdasarkan kondisi iklim
setempat dan penting untuk meningkatkan proses dalam kondisi ini [53].
2.6.1.4 Pengadukan
Proses start up anaerobik sering berlangsung 2 4 bulan. Start up memiliki
potensi untuk gagal dimana bioreaktor tidak bekerja dengan baik dan biogas tidak
dapat diproduksi. Untuk menghindari masalah ini, ke dalam reaktor hidrolisis dan
reaktor metanogenesis sering diinokulasikan lumpur anaerobik dari reaktor
fermentasi lainnya. Pencampuran dalam reaktor harus dilakukan dengan sangat
hati hati [36]. Kontak antara bahan organik dan mikroorganisme dapat
ditingkatkan dengan meningkatkan pencampuran, yang menyebabkan kinerja
reaktor yang lebih tinggi [46]. Hal ini terutama penting bagi mikroorganisme
24
hidrolitik untuk membuat kontak yang baik dengan berbagai molekul bahwa
mereka harus mencerna dan enzim mereka dapat didistribusikan di seluruh area
permukaan besar dalam substrat. Pengadukan juga mencegah bahan dari
terakumulasi di bagian bawah tangki digestasi dan mengurangi risiko berbusa
[42].
!"/"$"0Kebutuhan Nutrisi
Nutrisi sangat dibutuhkan dalam proses anaerobik. Nutrisi yang paling
penting bagi bakteri adalah karbon dan nitrogen, tapi dua elemen ini harus
disediakan dalam rasio yang tepat. Jika tidak, amonia dapat terbentuk ke tingkat
yang dapat menghambat mikroorganisme. Rasio karbon/nitrogen (C/N)
tergantung pada daya cerna dari sumber karbon dan nitrogen [44]. Nutrisi yang
memadai tersedia apabila menggunakan limbah yang kompleks untuk diolah.
Penambahan nutrisi diperlukan ketika mengolah limbah industri yang kekurangan
unsur hara makro seperti nitrogen dan fosfor. Umumnya kebutuhan nutrisi untuk
nitrogen, fosfor, dan sulfur masing masing berada di kisaran 10 13; 2 2,6; dan 1 2
mg per 100 mg biomassa. Untuk mempertahankan aktivitas maksimum
metanogen, sangat diinginkan nilai konsentrasi fasa cair nitrogen, fosfor, dan
belerang masing masing 50, 10 dan 5 mg/l [45].
Kandungan metana dari campuran biogas tergantung pada keadaan
oksidatif karbon dalam senyawa yang terdapat dalam bahan baku. Bahan baku
juga harus seimbang terhadap rasio karbon dan nitrogen (C:N = 20:30), karena
mikroorganisme menggunakan karbon dan nitrogen pada kisaran rasio ini.
Terlepas dari C dan N, elemen lain juga penting untuk pertumbuhan
mikroorganisme anaerob. Sebagai contoh, Ni (terlibat dalam sintesis koenzim
F430), Fe (konstituen pembawa elektron), Mg (menstabilkan membran sel), Ca
(menstabilkan dinding sel dan memberikan kontribusi bagi stabilitas termal dari
endospora), Co (komponen vitamin B12), Zn (konstituen dari beberapa enzim) dan
sebagainya. Jika elemen ini tidak terkandung dalam bahan baku, mereka harus
diberikan karena ketidakhadiran mereka berkorelasi dengan penurunan efisiensi
[53].
25 !"/"$"/ olatile Fatty Acid (VFA4
VFA merupakan senyawa intermediet yang dihasilkan selama tahapan
asidogenesis dengan rantai karbon hingga enam atom [9]. VFA dapat digunakan
sebagai indikator stabilitas proses fermentasi metana [55]. Ketidakstabilan proses
digestasi anaerobik akan menyebabkan akumulasi VFA di dalam digester yang
menyebabkan penurunan nilai pH. Namun, akumulasi VFA akan tidak selalu
dinyatakan dengan penurunan nilai pH, karena terdapat kapasitas buffer pada
digester yang berasal dari biomassa yang terkandung di dalamnya [9]. Jika pH
tinggi, digester dapat bekerja dengan konsentrasi VFA yang tinggi hingga
beberapa g/l. Tetapi efisiensi pengolahan akan rendah [56]. Akumulasi VFA
mencerminkan pemisahan kinetik antara pembentuk asam dan konsumen serta ciri
khas yang disebabkan oleh hidrolik atau organik overloading, variasi suhu tiba
tiba, adanya senyawa toksik atau penghambat dan beberapa faktor lainnya. Asam
asetat biasanya terdapat dalam konsentrasi yang lebih tinggi dari yang lainnya
dalam VFA selama proses digestasi anaerobik, sedangkan asam propionat dan
butirat menjadi penghambat aktivitas metanogen [6]. VFA dengan konsentrasi
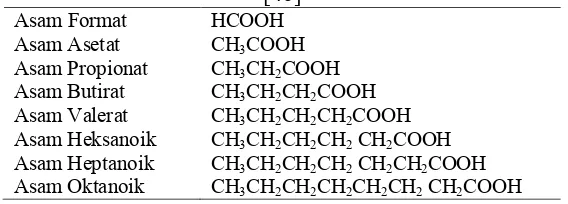
tinggi sering dikaitkan dengan efek toksisitas dan inhibisi [46]. Tabel 2.8 berikut
merupakan kandungan dari VFA pada proses digestasi anaerobik.
Tabel 2.8 Kandungan VFA yang Umum Terdapat pada Proses Digestasi Anaerobik [46]
Asam Format Asam Asetat Asam Propionat Asam Butirat Asam Valerat Asam Heksanoik Asam Heptanoik Asam Oktanoik
HCOOH CH3COOH CH3CH2COOH CH3CH2CH2COOH CH3CH2CH2CH2COOH CH3CH2CH2CH2 CH2COOH CH3CH2CH2CH2 CH2CH2COOH CH3CH2CH2CH2CH2CH2 CH2COOH
1 ! ! ' % !( -/!$
2.6.2.1 Beban Organik (Organic Loading Rate4
Beban organik merupakan parameter operasional yang penting, yang
menunjukkan berapa banyak bahan kering organik dapat dimasukkan ke dalam
digester, per volume dan satuan waktu, sesuai dengan persamaan [9]:
BR = m × c / VR (2.1)
26
Keterangan: BR = Beban organik (kg/hariRm3)
m = Massa substrat umpan per satuan waktu (kg/hari)
c = Konsentrasi bahan organik (%)
VR = Volume digester (m3)
Produksi gas akan meningkat dengan beban organik sampai tahap ketika
metanogen tidak bisa bekerja cukup cepat untuk mengkonversi asam asetat
menjadi metana. Beban oeganik berhubungan dengan konsentrasi substrat dan
HRT, sehingga keseimbangan yang baik antara kedua parameter harus diperoleh
untuk operasi digester yang baik. HRT pendek akan mengurangi waktu kontak
antara substrat dan biomassa [25].
!"/"!"! %ydraulic Retention Time (HRT4
HRT adalah rata rata interval waktu ketika substrat disimpan di dalam
tangki digester. HRT berkorelasi dengan volume digester dan volume substrat
umpan per satuan waktu, sesuai dengan persamaan:
HRT = VR / V (2.2)
Keterangan: HRT = Hydraulic Retention Time (hari)
VR = Volume digester (m3)
V = Volume substrat umpan per satuan waktu (m3/hari)
Menurut persamaan di atas, peningkatan beban organik akan mengurangi
HRT. Waktu retensi harus cukup panjang untuk memastikan bahwa jumlah
mikroorganisme yang mati pada proses pengolahan limbah cair tidak lebih tinggi
dari jumlah mikroorganisme direproduksi. Tingkat duplikasi bakteri anaerob
biasanya 10 hari atau lebih. Sebuah HRT singkat memberikan laju aliran substrat
yang baik, tapi hasil gas yang lebih rendah. Hal ini sangat penting untuk
menyesuaikan HRT dengan tingkat degradasi spesifik dari substrat yang
digunakan [9].
3
Pada penelitian ini dilakukan analisa ekonomi yang sederhana terhadap
proses asidogenesis LCPKS pada keadaan ambient dengan produk yang
diharapkan berupa VFA yang pada tahapan berikutnya dapat dikonversi menjadi
27
biogas. Maka pada penelitian ini yang dikaji adalah jumlah VFA yang akan
dikonversi menjadi biogas pada proses digestasi anaerobik dua tahap. Beberapa
penelitian yang berhasil menghitung volume biogas dari VFA ditunjukkan pada
Tabel 2.9.
Tabel 2.9 Volume Biogas dari Jumlah VFA yang Terbentuk
Pada penelitian ini, total pembentukan VFA tertinggi diperoleh pada
variasi pH 5,5 dengan jumlah 8.287 mg/L. Melalui Tabel 2.9 dapat digambarkan
grafik linear seperti ditunjukkan pada Gambar 2.8 berikut.
Gambar 2.8 Konversi Total VFA menjadi Biogas [57, 58, 59]
Gambar 2.8 menunjukkan grafik linearisasi pembentukkan biogas dari
VFA dengan persamaan garis lurus: y = 0,0009 x + 0,1043 dengan y merupakan
produksi biogas dan x merupakan VFA yang terbentuk. Berdasarkan persamaan
tersebut maka jumlah biogas yang dapat dihasilkan dari total VFA tertinggi pada
penelitian ini adalah:
y = 0,0009 x + 0,1043
= (0,0009) (8.287) + 0,1043
= 7,56 liter biogas/liter LCPKS hari = 7,56 m3 biogas/m3 LCPKS hari y = 0,0009x + 0,1043
0 2 4 6 8
0 2.000 4.000 6.000 8.000 10.000 Produksi Biogas
Linear (Produksi Biogas)
-'!$ 4* .5
-,
#
(
-.
!(
5
"
!
Peneliti Total VFA (mg/L) Volume Biogas (L/L·hari)
A.K Kivaisi dan M. Mtila [57] 2.058,85 1,70
Rongpin Li et al [58] 4.020,00 3,97
Cavinato et al [59] 6.896,48 6,00
28
Ekivalensi 1 m3 biogas terhadap *iquefied Petroleum Gas (LPG) adalah sebesar
0,465 kg. Sehingga
= ,
×
,= 3,52 kg LPG/m3 LCPKS
Harga LPG industri adalah Rp 11.767/kg [60] sehingga:
Harga biogas yang dihasilkan = ,
×
. .= Rp. 41.419,84/m3 LCPKS
! "
#" $ $ %
" & '
(" ' )& * # +
," '- ) .
/" + 0 + )&.(
#" 1 2 ' + 3
!0 (**!
" 1 ) 4 )4+ + "3(+2*5
(" 6 )4+'6'7' + "378+ 8*"/0
,"
/"
5"
9" )
:" .!;.+ + "3)/
" 0
#*"
(* #" 0 /
"
(" .
,"
/"
5" $
9" :"
6 ("# < %
& "
6 ("# ;
(#
! ! " #$ % $ & ' ( % )
' ) $ =5#>3
# ) ) , ) 9 ) #*"
0 ) ? ? - "
( % )8 % "
, + ? ) ?
? % "
!"
' !" $ =5 >3
# % /
$ - $ :* "
# )
$
? $ ?
- "
( & )& * # + $ ) ? , : @
* * "
, ' !" $ & A
& $ B $ "
/ !" $ 3
!" C
D
/ E #*** E ! E %
D ")& )&
% & '% (
' % & $ =5#>3
# & A % $ $ #*/ &
# < " ' < F
? A //* & # < "
& A #/ "
("#
(
( ? ? A " D
$ /8 /* "
, & A $ : &
? $ ? $ ? A " +
? ? A ? $ "
/ $ #*(8#*/ & #
< "
5 & A % F
"
9 $ / 5 %
$ ? ,G * / %
#8 < $ ? " $ <
? "
: $ 3
#*** 0 8 '
1 = ×
3 ' C H ? A
0 C ? A
) * & '* (
' * & D $ =5# 5 >3
# & A $
$ //* & # < "
$ ? A $
? $ "
( 0 ? A "
, D $ 3
#*** 0 8 '
1 = ×
3 ' C H? A
0 C H ? A $
("
("(
((
+ % & & & '% (
' % & & & $ =5#>3
# 0 % "
$ "
( $ %
$ $ "
, % A
? $ "
/ ? ? ( E #* - "
5 $ ? $ 8$ %
A $ % "
9 % # < $ #*(I&
#*/I&
% $ % "
: $
$ $ $
? ,G $ % * / "
$ 3
#*** 0 8 '
1 = ×
3 ' C H
0 C
, * & & & '* (
' * & D $ =5#>3
# $
? A % $ $ % "
$ < %
$ //* & # < "
( $ # < $ $
#** & #/
"
(",
(,
, D $ 3
#*** 0 8 '
1 = ×
3 ' C H ? A
0 C H ? A $
- ./ 01 2 & '.02(
' ./ 01 2 & &. $ =5(>3
# #* ? $ < % /* "
$ * 44 B ) ., $"
( $ / & .9 * / +"
, $ #/ B ) ., J B ' .,
$ 8 $ "
/ $ $ /
< "
5 ? ? $
? $ < < $ 9* "
9 $ B
( B B
' * # + A $ ? ? $ ' "
: $ # 9 $ "
$ ' ? " '
' &. "
&. $ 3
+ :*** 0
' .
1 = −
3 ' C '
0 C '
+ C + '
:*** C ×#*** 1
("/
("5
(/ * & !
' & $3
# % B "
0 $ & "
( ? & $ ?
#/* & ? "
, 0 $ & B "
/ $ B &
< $ ? /* "
5 ); A ); * $ $
? $ % $ "
9 $ #/ $ ? < ); #/ #* / ,"
); "
: ) B 5 & / /K / , /
$ + )&.( $ ) %
? " "
"+ #& ( )
' % < $
% $ $
D ' <
% &. ) "
("# L A ' 3 4
)
' # ( , / 5 9 : #* ## # #( #, #/
)
!8' %
D
D &. D ' 6
3 C '
C '
(5
, - .
? 9 < $ " L < A % $ (" "
(" L L A
+ "
0 # 0 8 0 8( 0 8, 0 8/ 0 85 0 89
# ( , # ( , # ( , # ( , # ( , # ( , # ( ,
#" "
$ ("
,"
/" %
$
5" %
$
! "!# $ !
"!#
% &$ ' &$
#! % ( )*+") % "*,,(%
-! C
. /01
2 "#!3#3 ,4+4535!#*+-,,"
! . 1 2 #4!,",+4#!,,, % -*",
"! . 1 2 #4!,4,+*-! 4, % -*",6
*!
. 1
2 -!5-,+-"! ,, % -*",0
4!
. 1
2 5!#,,+--!43, % -*",6
! 7 8 #)3, 6
3! 7 8 ,)#" $
5! 7 8 #)55 6
#,! ( ( (
2
#!*,3)53 *4,), , #!,33)4#
7 $
' % 9 6 +
*#2'6 %2#,2#55* '
: ; :
/0
( *,, 2 ,, 2 ) %
4+5 <-5=! "!# $
) /0 "#!3#3 2 -!5-,+
-"! ,, 2 % )*+") ! /0
$
3
! )
$ $ #4!,4,+
*-! 4, 2 ! / ) ; !
% /) ) -,#, <4 =
( > ( $
? )
!
' ; ) ) -,,5 <"-=) $
) ( # 2 )
,)* 2 ,) 3 2 ! % "!# $
)
)
! / ) ; ;
!
;
! $ )
; >
<4*=) %@ !
) A %@ %@ -,
$ %@ #*B #,B * %@ "
-*, % > $
4 .C,)-1 . % / 1
%! '
%)
) ) ) ) ) /0 ? !
! " #$%& " ! &' &% % (
' 0D ) ) -,## <",=)
% *)* 3! ! ) ) -,## <* =)
.*(41)
C !
"#
E "!- $ : %@ -, #* $
( ##!-4,+-"!,4, 2
##!54,+#5!3-, 2 ! %
:
> <-"=! %@ #,
* > (
##!*-,+# !*-, 2 #-!54,+#"! ", 2 )
$ ) %@ !
%@ "
#4!#-,+#5!,3,) : >
; > >
> !
) ) -,#* <#,=)
%@ " %@ )
F ( ) ) -,## <-"=) %@ )
$
!
>
$ ? $ $ <"-=!
' ; ) ) -,#" <4 =) "
$ @ %@ )
%@ ;
%@ !
/ )
) %@ >
) %@
!
, ! " ! '(%
-. /01 $ :
> ! ' ) ) -,#* <#,=)
/0)
-5)5 8) %@
""
E "!" $ : > ?
%@ -, %@ #,)
%@ * "! ? ( %@
? !#*3 2 :
$ ? ! '
%@ -,) ? %@
#,! % :
$ ? ! ?
> A $ $ !
)
A $ < #=)
) ) -,## < -=) :
A $ $
#!,,,+-!,,, 2
#,!,,, 2 !
% $
( 45-+#!5 4 2 5 5+#!4 " 2 ! /
) )
%@ !
1 ! " (%# / * &' &% % (
> $
? 2 <4=! )
? !
% $ ?
! ;
) ?
%! E "!* $ %@
? 2 !
E "!*
% >
% 4
/ )
# ! -, 2 ! ;
/ )
D (@) ) -,#" < *=)
-4!#, C"!"43 2
% *
% *)
% *)*!
*"
? ( A % ?
!#* )4 2 : A %
$ ? ! ? % *)*
/0
"! !" ; % !
?
) ) -,#* <#,= D D ) ) -,# <# = ;
% 4 ; %
% *)*! %
: % /
%! $ "! !# : $
% / A % (
%!
$ % / %
> ) % $ % /
$ !
(
$ "!-!"
M -!,,, 2
M #,!,,, 2 $ !
( 554+#!5 4 2 #!,3 +-!45* 2
! / )
A % )
% !
, 2 " ! " (%# / * &' &% % (
@ ? 2 $ "!-!*
$ ! E
"!#" $ % A %!
E "!#"
! "# $ % &
'( ! ) *+) ,
* ! # % - '(
! . *.) , - ' ! *- +/ 01
! *&- 2/
3 ' 4 ! !
- 4 ! 5 '(
! !
6 - ! !
* 6 !
7 ! !
'
! " # $ % & ! ' $ (
) * +$ ( , ' ( & )
! " # $ - . - &$ /
, 00 1 %0 0 )
/ 23 ( % % ( %2 ( 24 23 %
5 " & 6 & 7 # , 8, & , + $
9 " 8 & " & : ;"" ( ! % % & <
/ , /2=
(& 6, 8 ( > & (& !; , % - %
;"" " : ; + $ ?( % 7 , 9 # , :@
& 6 8 & 9 ( ! % %
, / < 2/ <=
< 9 7 A !7 % ( ! ' $ % $ %
% ( ($$ $ , = 2 .=
; @ $ , > B( $ $ )
* % 8, ($& , ' ( " , C (
, ?( D E # ( B )
= B6 & D (, && 3 ;% , 5+ & E %
, ;"" " +&$ 8 & ( 7 % C D % 6 #2-( % " &
+" 2F ( " 4 ( , 6 %! + , - .
% ;88 < = ) , / 2/ .
. 8 + / 7 % " ; ;(
= 7* . =2= 2.. .< 2 2
7 &$ % 8 G ( E 8 & (, && 8( &(@
5+ % " & : ;"" ( ( 7 % ;"" " 4 (
9 8 & 4! $ % " % ( % % .
, /<<2 / /
% + - + G E ( ,
F !;"" " 4 , + $ + % " +% (
B # " 1 & @ " 7 2, % ( > $2
=
;E ( D % 7 , 8 ! % % < / , =2
-, ,& E G E G !; % " & 7 & 2
6 & " 7 % ( +&$ 8 & ( ,
8 & ( & ( ( + $ - % D % G % $
B ! ) % % % <0 / , )/.2)
) %( % 3(A % H, % F & > I( B % C % 6, %1 (
% ( > ) !G ' + ( " & ' B ;"" "
4 8 & ( : % > % 9 ! % % /)
) , J )
/ B 9 ( $ $ + "
$ - , $ 0102 > &$ % 9 $( 7 %
=
B G , !C # , ( " : &! & $
) $ %
< 7 ( +
7 &$ % - A ! % )
> &$ % 9 $( *( 7 %
= ( ( 9 ($ & )0 2
*-0 ;90 0
. 4 @ , , ' ,( , % $
' $ # ( " +% ( (
8 , % 7 & ; % % C &
D - & " +% ( ( # "
- &$ /
8 3 % B( +$ ( B , $ , && & , , & *(
+ ( 5 ( 6 8 , % " , 8 & " & :
;"" ( : ; 8, (%, 2 "2 ! , - . (
. , /< 2 /.
+ * +(%( 4 : % 58 & " & :
6 $ + $ ! % & KK .== , = 2
.
) F & F 8 % > 59 # $ ( $ 7 %
( " & & : ;"" ( : ; B 2B % 8 #
7 ; E & ! % * ( % . , /2
/
.
/ 3 2 , B % 2+ : % F 2F > & 4 %26, >
5+ & @ " & ( " + % + $ - %
" & : ;"" ( ! + ) - % . (
+ + (
& , - E 7 % > ( % * & 5 & :
;"" ( : ; 8 & $ 6 &&( + $ - %
9 E #! + , - % - % % $ % / A(
/ * 2) )
< ( (& ) ! & $ ( &$ ( ( , F
> &$ , # ! - < ( C % , 00### A( (&
&0 /0 0 =0 & $2&( 2 &$ (2 ( , 2 2 &$ ,2 # 0
4 > 58 % % > &$ , ( F # !
, ) ) , / 2
= * & 8 3 6, # 3 @ @ 58 & " & :
;"" ( $ , + $ - % # , ' ( + ! $
, % % % / ..< , <)2 )
. F ( ( * % > % ( % 4 ( .. * & F; 2
0 ;*>40 0 ..
) 8, & 7 ' $ $ %
$ 3 4 ; E & E
% & +%( ( .
) ; # , A 7 $ B > ( A 4 ( A ,A #
5 > &$ , 6 $ F # ( ( ( 7 % !
( . = , /=2 * / 2 ))K
) 6, , , ; % 8 7 % 8 6, ; % % 6, F > %
57 % " & & : ;"" ( : ; : ( 6, % " &
L E ! . ( < )
, 2 <
)) H 8 % % ,( 6, % % B % K ,( >( 5- %
: & @ " 7 % 9 % + ! %
$ % ' ( . % 6, / / , ..2
)/
)/ G & , 7 , ( 5;1
7 % 4 $ # ! $ % . =/ / , .2
<
) +& 7 % 6 ( 5+ E % " E , '( E : , 7 %
D +% ( ( +- & ! ) - % + + )
)< - - ($ + % , ( =
-% 5 * + % % B >;32G64 G % C&$4
M 6 FC + B , & =
) + 4 @ ( 9 %( @ ( 3E + 5D "
6 "" ( % * # ($ " 4 % ( + $ 6 2
% # , # ( ! % % <= / , 2
=
)= + ( ,( H , % & 5 & : ;"" ( B
9 # ! , - * % % % = , /<<2/ )
* = .2 //K // ) , 2
). *9;> ) $ ! * > $ "
, D - & " ; %
/ - 7 - 5+ $ ! ($$ $ / ,
< 2<).
/ * C 5+ $ 8 & ! 6, . , =2 )/
/ + ,( + E % % / - $
E C 6 +7 G 7 , 6 (&$ 6 .
/) - 7( + , @ C 5' $ " 6 &$ D+ 7
79 & - B # 8 & +&$ 8 & ( !
) % . , ) ) , / 2/=
// ,( 9 9( , % H, % 7 9 $ 7 B &
) * % ' % ! - - %
# % 6 L 9 , 7 =
/ K H, % 5+ $ ! ) ( 6
$ - % G (& ) ($$ $ ) / , =2
/< F + ( D 5+ $ 8 & !
/ - % 6, / ) ,
). 2/ < 7* 2 2/ 2
/ + - E 7 (%, / *% - 7 '
.-- - $ % * 8, " "
; % % ; E & ; % % .
<
/= 23 ( % ( % %2 > %2F ( , 3( 26,( 6,( %
5;"" " 4 , + $ - % ! %
% . < , / <2/ .
/. - 6 6, 7 4 E F & 2+
C F @ 58, 9 " , " > % , > , 7
6 ( , % 9 " - % " ($
: & " 9 " & ! % % ) ,
<2<)
* , * ; ; $ ,$ , 4 , & 4 " @ C % * ,
4 , & ; * %% 56 & E + & " % 2 % 8# 2 %
+ $ - % " , 8 & " 8, % ! % %
, 2 <
; 4 @ 9C ; E 56 & 7 # 8# 2 %
% 2 % - % B, 8 % , B # 6 &
B , , ! * ) , 2) * = <J .
# F %A 9 $ & % :28, % 5+ $
- % " & > 1 (& > " 4 % , (
D % 8# 2 % " D 2' # + $ ( % 7
D+ 7 9 ! + , - / . ). / ,
.)/)2 .)/=
) F & ( C + ( ( C > $ 5 ( " 7 % G
+ $ - % ! / - - $ % 6, ,
<<2) /
/ , 4 C 58, $ % " + $ - % !
% , B * #
)
I %( * ( 8 , & 4 A B I 4 % I % 3(23 ( > !
6, @ " , % + % 4
8, & , , ' & " 6, ( ! ) % .
, // / , = J .<
< 9 * % ' )
> $ 7 , % L; E &
+ F F E ! ( " 7 % " & B 4 ,
. % % & 8# 2 % 7 ! ,
- % % / ..= , J )
= 9 % > ,( 6, K (A ( > !
![Tabel 2.1 Luas Areal Perkebunan Kelapa Sawit di Indonesia [16]](https://thumb-ap.123doks.com/thumbv2/123dok/112554.9132/30.612.160.478.488.582/tabel-luas-areal-perkebunan-kelapa-sawit-di-indonesia.webp)
![Gambar 2.1 Luas Lahan Sawit (dalam 103 Ha) pada Tahun 2012 [16]](https://thumb-ap.123doks.com/thumbv2/123dok/112554.9132/31.612.134.512.491.613/gambar-luas-lahan-sawit-dalam-ha-pada-tahun.webp)
![Gambar 2.2 Diagram Agram Alir Proses Ekstraksi Minyak Sawit dan LimbahDihasilkan [21] imbah yang](https://thumb-ap.123doks.com/thumbv2/123dok/112554.9132/32.612.173.475.293.675/gambar-diagram-agram-proses-ekstraksi-minyak-sawit-limbahdihasilkan.webp)

![Tabel 2.3 Karakteristik Limbah Cair Pabrik Kelapa Sawit (LCPKS) [23, 27] Parameter Satuan Nilai](https://thumb-ap.123doks.com/thumbv2/123dok/112554.9132/34.612.115.528.581.713/tabel-karakteristik-limbah-pabrik-kelapa-sawit-parameter-satuan.webp)
![Tabel 2.5 Karakteristik Biogas [6, 35, 36]](https://thumb-ap.123doks.com/thumbv2/123dok/112554.9132/35.612.169.472.558.708/tabel-karakteristik-biogas.webp)
![Tabel 2.6 Potensi Biogas yang Dihasilkan oleh Beberapa Substrat [42]](https://thumb-ap.123doks.com/thumbv2/123dok/112554.9132/36.612.187.472.398.468/tabel-potensi-biogas-yang-dihasilkan-oleh-beberapa-substrat.webp)
![Gambar 2.4 Skema Digester Anaerobik (A) Batch dan (B) Kontinu [42]](https://thumb-ap.123doks.com/thumbv2/123dok/112554.9132/37.612.163.479.350.691/gambar-skema-digester-anaerobik-a-batch-dan-kontinu.webp)
![Tabel 2.7 Bahan Kimia yang Biasa Digunakan sebagai Penyangga [36]](https://thumb-ap.123doks.com/thumbv2/123dok/112554.9132/45.612.151.491.221.355/tabel-bahan-kimia-digunakan-penyangga.webp)