PENGARUH HYDRAULIC RETENTION TIME (HRT) DAN pH
PADA PROSES ASIDOGENESIS LIMBAH CAIR PABRIK
KELAPA SAWIT (LCPKS) MENGGUNAKAN
TEMPERATUR 45
0C
SKRIPSI
Oleh
RAMLAN
110405017
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
PENGARUH HYDRAULIC RETENTION TIME (HRT) DAN pH
PADA PROSES ASIDOGENESIS LIMBAH CAIR PABRIK
KELAPA SAWIT (LCPKS) MENGGUNAKAN
TEMPERATUR 45
0C
SKRIPSI
Oleh
RAMLAN
110405017
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
PERNYATAAN KEASLIAN
SKRIPSI
s'ya menyatakan dengan sesungguhnya bahrva skripsi
denganjud,r:
PENGARLIH
HYDRAULIC RETENTIhN TIME (HRT)
DAIY
pH
I'ADA
PROSESESiPOCEI.{ESIS
LIMBAH
CAIR PABRIK
KELAPA
sAwIT
(tcpKs)
MIifr{cGtrNA
KANrTEMPERATUR
45OCDibuat untuk naelengkapi sebagran persyaratan menjadi sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik ljniversitas
Sumatera Utara. .tkripsi
ini
adalah hasil karya saya kecuari kutipan-kutipan yang terah saya sebutkan surnbernya.Dcmikian per .yataan ini ctiperbuat, apaL,la kemudian hari terbukti bahwa karya ini bukan karya saya ataurnerupakan hasil jiplakan
maka saya bersedia menerima sanksi sesuai uengan aturan yang berlaku
Medan, Septernber 2015
RAMLAN
PENGESAHAN
Skripsi dengan judul:
PENGARUH HYDRAULTC RETENTTON TIME (HRT) DAN pH PADA PROSES ASTDOGENESIS LIMBAH CAIR PABRIK KELAPA SAWIT
(LCPKS) PADA TEMPERATUR ,{s oC
dibuat untuk melengkapi persyaratan menjadi Sarjana Teknik pada Departemen
Teknik Kimia Fakulas Teknik Uruversitas Sumatera Utara. Skripsi
ini
telahdiujikan pada siding ujian skripsi pada 16 September 2015 dan dinyatakan memenuhi syarat/sah sebagai skripsi pada Departemen Teknik Kimia Fakultas Teknik Universitas Surnatera Utara.
Mengetahui, Medan, September 2015
Dosen Pembimbing
I 001
Dosen Pengrrji I Dosen Penguji II
,4rc
W
Prof Dr, Ir. Rosdanelli Hasibuan. MT
NrP. 19680808 199403 2 003
Dr. k. Fatimah. MT
NrP. 19640617 199403 2 001
ffi*Q
f(noonnrn,{ToR s
iN
Ir. Reniiii
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas limpahan rahmat dan karunia-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan skripsi dengan judul “Pengaruh Hydraulic Retention Time (HRT) dan pH pada Proses Asidogenesis Limbah Cair Pabrik Kelapa Sawit (LCPKS) pada Temperatur 45 oC”, berdasarkan hasil penelitian yang penulis lakukan di Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini merupakan salah satu syarat untuk mendapatkan gelar sarjana teknik.
Hasil penelitian ini:
1. Penelitian ini memberikan informasi mengenai proses loading up dan variasi pH dalam proses digestasi anaerobik tahapan asidogenesis menggunakan temperatur 45 oC sehingga lebih menghemat energi yang umumnya digunakan untuk pemanas.
2. Penelitian ini memberikan sumbangan ilmu pengetahuan mengenai pengolahan limbah cair pabrik kelapa sawit.
Selama melakukan penelitian sampai penulisan skripsi ini, penulis banyak mendapat bantuan dari berbagai pihak, untuk itu penulis mengucapkan terimakasih dan penghargaan yang sebesar-besarnya kepada:
1. Dr. Eng. Ir. Irvan, M.Si dan Ir. Bambang Trisakti, MT selaku Pembimbing
2. Prof. Dr. Ir. Rosdanelli Hasibuan, MT dan Dr. Ir. Fatimah, MT selaku Penguji
3. Ir. Renita Manurung, MT selaku Koordinator Skripsi
Penulis menyadari bahwa laporan hasil penelitian ini masih jauh dari sempurna, oleh karena itu penulis mengharapkan saran dan masukan demi kesempurnaan skripsi ini.
Medan, September 2015 Penulis
iv
DEDIKASI
Penulis mendedikasikan skripsi ini kepada:
1. Orang tua penulis, Ayahanda Mantari Mudo, Ibunda Khalimatussakdiah, Kak Kholidahanum, Kak Enna, Bang Basri, Bang Aman Nasir, Bang Abdi dan Anidah yang sangat banyak memberikan dukungan moril maupun materil bagi penulis dalam segala hal terkhusus untuk kakak tercinta Almarhumah Naimah meski beliau belum diizinkan merayakan apa yang diperjuangkannya pada skripsi ini.
2. Rekan penelitian Rio Agung Prakoso dan rekan-rekan LPPM yaitu Bg Zoeliadi, Bg Dedy Anwar, Aidil Saputra, M. Darul Nafis, Intan Afrilia, Yola Melida, Ekuino Simanungkalit, Tri Putra Pasaribu, Khairul Fahmi, Endah Hutabarat, Christianto Sitio dan Muksalmina.
3. Teman sejawat, adik dan abang/kakak senior serta teman-teman stambuk 2011 yang telah banyak memberikan banyak dukungan, semangat, doa, pembelajaran hidup dan kenangan tak terlupakan kepada penulis.
4. Seluruh Dosen/Staf Pengajar dan Pegawai Administrasi Departemen Teknik Kimia yang telah memberikan banyak ilmu yang berharga dan bantuan kepada penulis selama menjalankan perkuliahan.
v
RIWAYAT HIDUP PENULIS
Nama : Ramlan
NIM : 110405017
Tempat, tanggal lahir : Huta Gambir/ 10 Desember 1992 Nama Orang Tua : Mantari Mudo dan Khalimatussakdiah Alamat Orang Tua:
Pakantan Dolok, Kecamatan Pakantan, Mandailing Natal, Sumatera Utara
Asal Sekolah:
SD Negeri 1440062 tahun 1999–2005
SMP Negeri 1 Pakantan tahun 2005–2008
SMA Negeri 2 Plus Panyabungan tahun 2008–2011 Beasiswa yang pernah diperoleh:
1. Beasiswa Bidik Misi tahun 2011–2015 Pengalaman Organisasi/Kerja:
1. Himpunan Mahasiswa Teknik Kimia (HIMATEK) FT USU periode 2014/2015 sebagai anggota Hubungan Masyarakat
2. Covalen Study Group (CSG) periode 2013/2014 sebagai anggota Peningkatan Akademik dan Literatur
vi
ABSTRAK
Proses asidognesis merupakan tahap pertama dalam proses digestasi anaerobik. Proses asidognesis menghasilkan volatile fatty acid (VFA) yang menjadi substrat untuk tahap metanognesis dalam memproduksi biogas. Penelitian ini bertujuan untuk mendapatkan pengaruh variasi Hydraulic Retention Time (HRT) dan pH serta mendapatkan kondisi pH terbaik dalam proses asidogenesis menggunakan Limbah Cair Pabrik Kelapa sawit (LCPKS) pada temperatur 45 0C. Proses
loading-up dilakukan dengan memvariasikan HRT kemudian operasi target dilakukan dengan memvariasikan pH fermentor Continous Stirred Tank Reactor (CSTR), yaitu pH 6,0; 5,5; 5,0 dan 4,5 dengan kondisi pengadukan 150 rpm. Analisa padatan (TS, VS, TSS, dan VSS), COD dan VFA dilakukan untuk mengkaji perubahan senyawa organik yang berubah menjadi VFA pada asidogenesis. Pembentukkan VFA total tertinggi dicapai pada variasi pH 5,5 yakni 20.298,85 mg/L dengan konsentrasi asam asetat, asam propionat dan asam butirat masing-masing sebesar 8.503,90; 2.341,38 dan 9.453,55 mg/L, dengan degradasi VS dan COD masing-masing sebesar 28 % dan 39 % dan rasio VFA/Alkalinitas 12,793.
vii
ABSTRACT
Acidogenesis process is first step in anaerobic digestion process. Acidogenesis process produce volatile fatty acid (VFA) as a substrat in methanogenesis process to produce biogas. This research aimed to obtain effect of Hydraulic retention time (HRT) and pH also obtain the best pH in asidognesis process of palm oil mill effluent (POME) at temperature 45 oC. Loading up was done by varying the HRT 20,15,10,4 then followed by target operation by varying the pH (4,5;5,0; 5,5, and 6,0) of the CSTR fermentor with mixing of 150 rpm and temperature of 45 oC. Analysis for solids (TS, VS, TSS, and VSS), COD, and VFA are being done to study the conversion of organic compounds to VFA during acidogenesis. The highest VFA of 20.298,85 mg/L are formed at pH 5,5 with the concentrations of acetic acid, propionic acid, and butyric acid are 8.503,90; 2.341,38 and 9.453,55 mg/L, respectively through the VS and COD degradation of 28 and 39 %, respectively and VFA/Alkalinity ratio is 12,793.
viii
DAFTAR ISI
PERNYATAAN KEASLIAN SKRIPSI ... i
PENGESAHAN ... ii
PRAKATA ... iii
DEDIKASI ... iv
RIWAYAT HIDUP PENULIS ... v
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... vii
DAFTAR GAMBAR ... xi
DAFTAR TABEL ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Tujuan Penelitian ... 4
1.4 Manfaat Penelitian ... 4
1.5 Ruang Lingkup Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 7
2.1 Limbah Cair Pabrik Kelapa Sawit ... 7
2.2 Digestasi Anaerobik ... 10
2.2.1 Hidrolisis ... 12
2.2.2 Asidogenesis ... 12
2.2.3 Asetogenesis ... 13
2.2.4 Metanogenesis ... 13
2.3 Faktor Yang Mempengaruhi Digestasi Anaerobik ... 14
2.3.1 Temperatur ... 14
2.3..2 pH ... 15
2.3.3 Rasio Karbon-Nitrogen (C/N)... 15
2.3.4 Pengadukan ... 16
ix
2.4 Biogas ... 17
2.4 Analisa Ekonomi ... 17
BAB III METODOLOGI PENELITIAN... 19
3.1 Lokasi Penelitian ... 19
3.2 Bahan dan Peralatan ... 19
3.2.1 Bahan-bahan ... 19
3.2.2 Peralatan ... 19
A. Peralatan Utama ... 19
B. Peralatan Analisa ... 20
3.2.3 Rangkaian Peralatan ... 20
3.3 Prosedur Penelitian ... 21
3.3.1 Prosedur Loading Up dan Operasi Target ... 21
3.3.2 Prosedur Analisa Sampel ... 23
3.3.3 Jadwal Pengujian Sampel ... 32
3.4 Jadwal Penelitian ... 32
BAB IV HASIL DAN PEMBAHASAN ... 33
4.1 Karakterisasi Limbah Cair Pabrik Kelapa Sawit atau Palm Oil Mill Effluent (POME) ... 34
4.2 Hasil Penelitian Proses Loading Up (VAriasi HRT)... 35
4.2.1 Korelasi pH dan Alkalinitas pada Proses Loading Up ... 35
4.2.2 Pengaruh HRT terhadap Pertumbuhan Mikroba ... 37
4.2.3 Degradasi Chemical Oxygen Demand (COD) pada Proses Loading Up ... 38
4.2.4 Pembentukan Volatile Fatty Acid (VFA)Pada Proses Loading Up39 4.2.5 Pengaruh HRT terhadap Rasio VFA/Alkalinitas ... 40
4.3 Hasil Penelitian Proses Operasi Target ... 43
4.3.1 Pengaruh pH terhadap Alkalinitas pada Operasi Target ... 43
4.3.2 Pengaruh pH terhadap Padatan Tersuspensi pada Operasi Target . 44 4.3.3 Pengaruh pH terhadap Reduksi Vollatile Solid (VS) ... 45
x
4.3.6 Pengaruh pH terhadap Rasio VFA/Alkalinitas ... 50
BAB V KESIMPULAN DAN SARAN... 51
5.1 Kesimpulan ... 51
5.2 Saran ... 51
DAFTAR PUSTAKA ... 52
xi
DAFTAR GAMBAR
Gambar 2.1 Tahapan Proses Digestasi Anaerobik 11
Gambar 2.2 Reaksi Hidrolisis...12
Gambar 2.3 Reaksi Asidognesis ...12
Gambar 2.4 Reaksi Asetognesis ...13
Gambar 2.5 Reaksi Metanognesis Dari Asam Asetat ...13
Gambar 2.6 Reaksi Metanognesis Dari Karbondioksida ...14
Gambar 2.7 Konversi Total VFA menjadi Biogas... ...18
Gambar 3.1 Rangkaian Peralatan 20
Gambar 3.2 Flowchart Prosedur Penelitian...22
Gambar 3.3 Flowchart Prosedur Analisa pH... 23
Gambar 3.4 Flowchart Prosedur Analisa Alkalinitas ... 25
Gambar 3.5 Flowchart Prosedur Analisa Total Solid ... 26
Gambar 3.6 Flowchart Prosedur Analisa Volatile Solid ... 27
Gambar 3.7 Flowchart Prosedur Analisa Total Suspended Solid ... 30
Gambar 3.8 Flowchart Prosedur Analisa Volatile Suspended Solid ... 31
Gambar 4.1 Hubungan pH dan Alkalinitas pada Proses Loading Up 36
Gambar 4.2 Pengaruh HRT terhadap Pertumbuhan Mikroba 37
Gambar 4.3 Reduksi COD pada Proses loading up 38
Gambar 4.4 Pembentukan Volatile Fatty Acid (VFA) Pada Proses Loading Up 39 Gambar 4.5 Pengaruh pH terhadap Alkalinitas pada Operasi Target 41
Gambar 4.6 Pengaruh pH terhadap Rerata Alkalinitas (Error Bar Menyatakan Standar Deviasi) 42
Gambar 4.7 Pengaruh pH terhadap Padatan Tersuspensi pada Operasi Target 44
Gambar 4.8 Pengaruh pH terhadap Rerata Padatan Tersuspensi (Error Bar Menyatakan Standar Deviasi) 44
Gambar 4.9 Pengaruh pH terhadap Reduksi VS pada Operasi Target 46
Gambar 4.10 Pengaruh pH terhadap Rerata Reduksi VS (Error Bar Menyatakan Standar Deviasi) 46
xii
Gambar 4.13 Pengaruh pH terhadap Rasio VFA/Alkalinitas 50
Gambar C.1 Tangki Umpan LD-1
Gambar C.2 Fermentor LD-1
Gambar C.3 Gas Meter LD-2
Gambar C.4 Botol Keluaran Fermentor (discharge) LD-2
Gambar C.5 Botol Biogas (Gas Collector) LD-2
Gambar C.6 Rangkaian Peralatan LD-3
Gambar C.7 Peralatan Analisa M-Alkalinity LD-3
Gambar C.8 Detecting Tube Hasil Analisa Gas H2S dan CO2 LD-3 Gambar C.9 Peralatan Analisa Padatan Tersuspensi (Vacuum Pump) LD-4
Gambar C.10 Furnace LD-4
Gambar C.11 Oven LD-4
Gambar D1 Hasil Uji Laboratorium untuk Analisa Karbohidrat, Protein dan
xiii
DAFTAR TABEL
Tabel 1.1 Komposisi Limbah Cair Pabrik Kelapa Sawit 1 Tabel 1.2 Berbagai Penelitian Biogas ... 3 Tabel 2.1 Pertumbuhan Produksi Kelapa Sawit Indonesia ... 6 Tabel 2.2 Komposisi Limbah Cair Pabrik Kelapa Sawit 7 Tabel 2.3 Potensi Biogas Yang Dihasilkan Oleh Beberapa Substrat 7 Tabel 2.4 Baku Mutu Limbah Pengolahan Kelapa Sawit 8 Tabel 2.5 Karakteristik Limbah Cair Pabrik Kelapa Sawit 8 Tabel 2.7 Pengaruh Komponen-Komponen dalam Biogas dan Pengaruhnya 17
Tabel 3.1 Jadwal Analisis Influent dan Effluent ... 31
Tabel 3.2 Jenis Kegiatan dan Jadwal Pelaksanaan Penelitian 32 Tabel A.1 Karakteristik POME dari PTPN IV PKS Kebun Adolina LA-1
Tabel A.2 Data hasil pengukuran pH dan alkalinitas fermentor LA-1
Tabel A.3 Data hasil pengukuran konsentrasi padatan fermentor LA-3
Tabel A.6 Data hasil pengukuran konsentrasi padatan tersuspensi fermentor LA-5
Tabel A.9 Data hasil degradasi COD LA-6 Tabel A.10 Data hasil pengukuran konsentrasi VFA LA-7 Tabel A.11 Data perhitungan ratio VFA/alkalinitas LA-8
xiv
DAFTAR LAMPIRAN
vi
ABSTRAK
Proses asidognesis merupakan tahap pertama dalam proses digestasi anaerobik. Proses asidognesis menghasilkan volatile fatty acid (VFA) yang menjadi substrat untuk tahap metanognesis dalam memproduksi biogas. Penelitian ini bertujuan untuk mendapatkan pengaruh variasi Hydraulic Retention Time (HRT) dan pH serta mendapatkan kondisi pH terbaik dalam proses asidogenesis menggunakan Limbah Cair Pabrik Kelapa sawit (LCPKS) pada temperatur 45 0C. Proses
loading-up dilakukan dengan memvariasikan HRT kemudian operasi target dilakukan dengan memvariasikan pH fermentor Continous Stirred Tank Reactor (CSTR), yaitu pH 6,0; 5,5; 5,0 dan 4,5 dengan kondisi pengadukan 150 rpm. Analisa padatan (TS, VS, TSS, dan VSS), COD dan VFA dilakukan untuk mengkaji perubahan senyawa organik yang berubah menjadi VFA pada asidogenesis. Pembentukkan VFA total tertinggi dicapai pada variasi pH 5,5 yakni 20.298,85 mg/L dengan konsentrasi asam asetat, asam propionat dan asam butirat masing-masing sebesar 8.503,90; 2.341,38 dan 9.453,55 mg/L, dengan degradasi VS dan COD masing-masing sebesar 28 % dan 39 % dan rasio VFA/Alkalinitas 12,793.
vii
ABSTRACT
Acidogenesis process is first step in anaerobic digestion process. Acidogenesis process produce volatile fatty acid (VFA) as a substrat in methanogenesis process to produce biogas. This research aimed to obtain effect of Hydraulic retention time (HRT) and pH also obtain the best pH in asidognesis process of palm oil mill effluent (POME) at temperature 45 oC. Loading up was done by varying the HRT 20,15,10,4 then followed by target operation by varying the pH (4,5;5,0; 5,5, and 6,0) of the CSTR fermentor with mixing of 150 rpm and temperature of 45 oC. Analysis for solids (TS, VS, TSS, and VSS), COD, and VFA are being done to study the conversion of organic compounds to VFA during acidogenesis. The highest VFA of 20.298,85 mg/L are formed at pH 5,5 with the concentrations of acetic acid, propionic acid, and butyric acid are 8.503,90; 2.341,38 and 9.453,55 mg/L, respectively through the VS and COD degradation of 28 and 39 %, respectively and VFA/Alkalinity ratio is 12,793.
1
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Indonesia tahun 2014 memproduksi 29,34 juta ton minyak sawit kasar [1], tiap ton minyak sawit menghasilkan 2,5 ton limbah cair [2]. Limbah cair pabrik kelapa sawit atau palm oil mill effluent (POME) mentah sebagai padatan tersuspensi terdiri dari 95 – 95 % air, 0,6-0,7 % minyak dan 4-5 % padatan [3]. POME mengandung bahan organik yang tinggi dengan 113.000 ppm COD, 35.000 ppm BOD [4], temperatur tinggi berkisar 80-90 oC atau 50 – 60 oC, bersifat asam dengan pH berkisar 4 – 5 [5]. Pembuangan POME ke lingkungan menjadi masalah sehingga perlu dilakukan penelitian untuk memanfaatkannya. Minyak dan lemak merupakan komponen pencemar utama yang terdapat pada POME sehingga perlu penanganan terlebih dahulu sebelum dibuang ke badan air atau perairan . POME memiliki potensi untuk diproduksi menjadi biogas. Komposisi POME ditunjukkan pada Table 1.1
Tabel 1.1 Komposisi Limbah Cair Pabrik Kelapa Sawit [6]
Komponen Komposisi (%)
Protein Mentah 12,5
Lemak dan minyak 10,2
Abu 14,6
Karbohidrat 29,5
Nitrogen 26,3
Karoten 0,019
Air 6,9
2
Pemanfaatan teknologi digestasi anaerobik dapat meminimalisasi dampak dari gas ini [8].
Proses digestasi anaerobik merupakan proses fermentasi bahan organik oleh aktivitas bakteri anaerob pada kondisi tanpa oksigen bebas dan merubahnya dari bentuk tersuspensi menjadi terlarut dan biogas [9]. Digestasi anaerobik dianggap efektif untuk proses pengolahan limbah pabrik kelapa sawit (POME) karena melibatkan mikroorganisme dengan serangkaian reaksi biokimia kompleks dari bahan organik menghasilkan metana dan karbondioksida [10]. Secara umum digestasi anaerobik memiliki 4 tahapan yaitu : hidrolisis, asidogenesis, asetogenesis dan metanogenesis [11] dan dilakukan pada kondisi mesofilik (30 – 37 oC ) dan termofilik (50 - 60 oC) 0C [12] serta dalam kondisi intermediet 45 0C [13] serta terjadi dalam berbagai variasi reaktor seperti seperti up-flow anaerobic
sludge blanket (UASB) reactor, up-flow anaerobic sludge fixed-film (UASFF)
reactor, modified anaerobic baffled reactor (MABR), continuous stirred tank
reactor (CSTR), anaerobic pond, anaerobic digester, expanded granular sludge
bed (EGSB) reactor [14]. Beberapa penelitian yang telah dilakukan untuk menghasilkan biogas diperlihatkan pada table 1.2.
Dalam rangka meningkatkan kinerja digestasi anaerobik, metode baru seperti metode dua tahap meunjukkan tingginya tingkat produksi [15]. Digestasi anaerobik dengan dua tahap dapat meningkatkan yield CH4 sampai 23 % [16].
Ada rentang suhu yang memberikan kondisi pencernaan yang optimal untuk produksi metana yaitu rentang mesofilik dan termofilik. Rentang mesofilik optimum untuk produksi metana 30°C - 35°C dan suhu termofilik antara 50°C - 65°C. Biogas juga dapat diproduksi pada temperatur intermedit 45 0C [13]. Produksi biogas dipengaruhi oleh hydraulic retention time (HRT) yang digunakan. Proses Hidrolisis, asidognesis dan metanognesis memiliki memiliki pH optimum yang berbeda[17].
3
mesofilik (37 oC) menunjukkan hasil yang lebih baik pada suhu termofilik. Hasil ini menunjukkan peningkatan suhu dapat meningkatkan produksi digestasi anaerobik dua tahap Pada penelitian ini temperatur yang digunakan adalah diantara mesofilik dan termofilik yaitu 45 oC. Pemilihan suhu 45 0C ini dapat menghemat energi yang digunakan daripada suhu termofilik. Untuk meningkatkan proses digestasi anaerobik dua tahap kondisi optimum operasi seperti pH, pengadukan dan HRT harus diketahui. Oleh sebab itu, penelitian ini dilakukan pada suhu intermedit (45 0C) dengan menvariasikan pH dan HRT dari reaktor. Proses ini dilakukan dalam reaktor digestasi anaerobik dua tahap menggunakan reaktor continuous stirred tank reactor (CSTR) dengan bervolume 2 liter dengan umpan adalah palm oil mill effluent (POME).
Tabel 1.2 Berbagai Penelitian Biogas Nama Peneliti (Tahun) Hasil Penelitian Yee-Shian Wonga et al
(2013) [20]
Asidognesis palm oil mill effluent (POME) pada suspended closed anaerobic bioreaktor dengan volume 4,5 L pada suhu mesofilik (35 0C) dan pH 5,2 dengan variasi HRT (12, 10, 8, 4, 2) hari. Diperoleh peningkatan VFA sesuai dengan penurunan HRT. VFA terendah pada HRT 12 hari adalah 11569.71 mg CH3COOH/L dan VFA
tertinggi pada HRT 2 yaitu 16956.00 mg CH3COOH/L
Solmaz Aslanzadeh et al (2014) [21]
Penelitian tentang digestasi anaerobik satu tahap dan dua tahap dengan bahan baku limbah makanan. Diperoleh hasil bahwa dengan menggunakan proses dua tahap yield yang diperoleh lebih tinggi dan ukuran reaktor yang digunakan bisa lebih kecil
Kun Wang et al (2014) [22]
Penelitian menggunakan limbah makanan pada reaktor Batch bervolume 500 mL. Reaktor dijalankan pada suhu 32 0C, pengadukan 120 rpm,
dengan variasi pH yaitu 4,5,6 dan pH tidak dikontrol. Diperoleh VFA terbanyak dengan pH 6 yaitu 918,23 mg
Yee-Shian Wonga et al [2013] [23]
4 1.2 PERUMUSAN MASALAH
Menurut Anna Schnurer et al, 2009 [13] proses digestasi anaerobik dapat dilangsungkan pada kondisi ambient, mesofilik dan termofilik. Proses digestasi anaerobik yang dilakukan oleh Sridevi V et al, 2014 [18] pada suhu ambient dan mesofilik (35 oC) memberikan hasil yang lebih baik pada suhu mesofilik. Sedangkan penelitian oleh Jeong et al, 2014 [19] pada suhu termofilik (550C) dan mesofilik (37 oC) menunjukkan hasil yang lebih baik pada suhu termofilik. Dari penelitian diatas menunjukkan hasil yang lebih baik pada suhu yang lebih tinggi, sehingga pada penelitian ini temperatur yang digunakan adalah diantara mesofilik dan termofilik yaitu 45 oC. Pemilihan suhu 45 0C ini dapat menghemat energi yang digunakan daripada suhu termofilik. Untuk meningkatkan proses digestasi anaerobik dua tahap pada suhu 45 oC kondisi optimum operasi seperti pH dan HRT harus diketahui.
Oleh karena itu, beberapa masalah yang perlu diselesaikan dalam penelitian ini adalah: (i) Bagaimana pengaruh variasi HRT pada proses asidognesis LCPKS untuk pada temperatur 45 oC (ii) Bagaimana pengaruh variasi pH dan pH terbaik
pada proses asidognesis LCPKS pada temperatur 45 oC.
1.3 TUJUAN PENELITIAN
Adapun yang menjadi tujuan dari penelitian ini adalah :
1. Mendapatkan pengaruh variasi HRT dan mendapatkan HRT target untuk proses asidognesis LCPKS pada temperatur 45 0C.
2. Mendapatkan pengaruh pH dan pH terbaik pada proses asidognesis LCPKS pada temperatur 45 0C.
1.4 MANFAAT PENELITIAN
Adapun Manfaat dari penelitian yang akan dilakukan antara lain yaitu : 1. Memberikan informasi mengenai pengaruh variasi HRT pada proses
asidognesis LCPKS pada temperatur 45 0C.
5
3. Memberikan informasi bagi peneliti yang ingin melakukan penelitian sejenis atau yang berhubungan.
1.4 RUANG LINGKUP PENELITIAN
Penelitian ini dilaksanakan di Laboratorium Ekologi, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan. Penelitian dilakukan menggunakan proses asidogenesis digestasi anaerobik menggunakan digester jenis
continous stirred tank reactor (CSTR) dengan volume 2 liter. Adapun variabel-variabel dari penelitian ini adalah sebagai berikut:
1. Variabel konstan:
a. Starter yang digunakan berasal dari kolam pengasaman torgamba.
b. Jenis bahan baku atau umpan yang digunakan : Limbah cair kelapa sawit dari Pabrik Kelapa Sawit Adolina PTPN IV
c. Kecepatan pengadukan tangki umpan: 250 rpm d. Temperatur fermentor: 45oC
e. Kecepatan pengadukan fermentor: 150 rpm 2. Variabel divariasikan:
a. pH dari fermentor divariasikan pada 4,5; 5; 5,5 dan 6.
b. HRT dari fermentor divariasikan 20 hari, 15 hari, 10 hari dan 4 hari. 3. Parameter analisa: Analisa cairan berupa M-alkalinity, kadar padatan (TS,
VS, TSS, dan VSS), kandungan Chemical Oxygen Demand (COD), kandungan Volatile Fatty Acid (VFA), dan pH.
Analisa yang akan dilakukan di dalam penelitian ini meliputi analisa pada bahan baku yang digunakan yaitu POME dengan influent limbah dan effluent limbah.
Adapun analisa cairan ini terdiri dari : 1. Analisa M-Alkalinity (Metode Titrasi)
2. Analisa kadar total solid (TS) (Metode Analisa Proksimat) 3. Analisa volatile solid (VS) (Metode Analisa Proksimat)
6
7. Analisa volatile fatty acid (VFA) (Metode Kromatografi) 8. Analisa pH
.
7
BAB II
TINJAUAN PUSTAKA
2.1 Limbah Cair Pabrik Kelapa Sawit (LCPKS)
[image:25.595.111.527.363.569.2]Kelapa sawit merupakan salah satu sumber minyak nabati yang paling banyak diproduksi di dunia saat ini, pertumbuhan produksinya ini di dorong dengan perluasan penggunaannya dalam pembuatan biodiesel. Tetapi, produksi ini juga menjadi ancaman karena sejumlah besar residu biomassa dari pengolahannya menjadi ancaman bagi lingkungan. Secara khusus limbah cair pabrik kelapa sawit memberikan dampak yang lebih besar [24]. Indonesia pada tahun 2014 memproduksi 29,35 juta ton minyak sawit kasar [1], tiap ton sawit akan menghasilkan 2,5 m3 limbah cair[2].
Tabel 2.1 Pertumbuhan Produksi Kelapa Sawit Indonesia [1]
Tahun Luas Areal (Ha) Produksi Minyak Sawit
(Ton)
2005 5.453.817 10.375.792
2006 6594.914 10471.915
2007 6.66.836 11.875.418
2008 7.363.847 14.290.687
2009 7.873.294 16.829.205
2010 8.385.394 16.291.856
2011 8.992.824 16.436.202
2012 9.572.715 18.850.836
2013 10.465.020 20.577.976
2014 10.956.231 29.340.000
8
sumber polusi terhadap biota air dengan mengurangi kandungan oksigen terlarut dalam air ketika dibuang langsung tanpa pengolahan [27]. Lemak adalah polutan organik terbesar dalam POME. Lemak berupa senyawa gliserol, alkohol, dan beberapa jenis lain dengan ikatan ester . Komposisi limbah cair pabrik kelapa sawit ditunjukkan pada Tabel 2.1
Tabel 2.2 Komposisi Limbah Cair Pabrik Kelapa Sawit [6]
Komponen Komposisi (%)
Protein
Minyak dan Lemak
12,5 10,2
Abu 14,6
Karbohidrat 29,5
Nitrogen 26,3
Karoten 0,019
Air 6,9
Potensi biogas yang dihasilkan oleh beberapa substrat ditunjukkan pada table 2.3 Tabel 2.3 Potensi Biogas Yang Dihasilkan Oleh Beberapa Substrat [4]
Komponen Reaksi Metanogenik Biogas (lg-1) CH4 (%)
Lemak C50H90O6 + 24,5 H2O 34,75 CH4 +
15,25 CO2 1,425 69,5
Karbohidrat C6H10O5 + H2O 3 CH4 + 3 CO2 0,830 50,0
Protein C16H24O5N4 + 14,5 H2O 8,25 CH4 +
3,75 CO2 + 4NH4+ + 4HCO3- 0,921 68,8
9
Tabel 2.4 Baku Mutu Limbah Pengolahan Kelapa Sawit [28]
No Parameter Kadar Maksimum
(Mg/L)
Beban Pencemaran Maksimum (Kg/Ton)
1 BOD 100 1,5
2 COD 350 3,0
3 TSS 300 1,8
4 Minyak dan lemak 30 0,18
5 Ammonia total 20 0,12
6 Ph 6,0-9,0 6,0-9,0
Adapun karakteristik limbah cair pabrik kelapa sawit mentah diperlihatkan pada table 2.5
Tabel 2.5 Karakteristik Limbah Cair Pabrik Kelapa Sawit [6]
No. Parameter Satuan Nilai
1. Suhu 0C 80-90
2. pH - 4,7
3. BOD mg/L 25.000
4. COD mg/L 50.000
5. TS mg/L 40.000
6. TSS mg/L 18.000
7. TVS mg/L 34.000
8. Minyak Dan Lemak mg/L 4.000
9. Amonia-Nitrogen mg/L 35
10. Total Nitogen mg/L 750
Ada beberapa inovasi metode yang telah dikembangkan dan diaplikasikan pada pengolahan limbah cair kelapa sawit . Digestasi anaerobik dianggap menjadi proses yang efektif untuk pengolahan limbah cair kelapa sawit (POME). Proses ini melibatkan mikroorganisme yang menguraikan bahan organik menjadi metana dan karbondioksida .
10 2.2 Digestasi anaerobik
Digestasi anaerobik adalah serangkaian proses dimana mikroorganisme memecah bahan biodegradable tanpa oksigen. Proses digestasi anaerobik mengubahnya dari bentuk tersuspensi menjadi terlarut dan biogas [29]. Proses ini menghasilkan campuran metana dan karbondioksida sebagai sumber energi terbarukan. Digestasi anaerobik telah menjadi salah satu teknologi pilihan untuk mengurangi gas rumah kaca. Digestasi anaerobik pada umumnya dilakukan pada dua kondisi suhu yaitu mesofilik (30-37) 0C dan temofilik (50-60) 0C [10]. Proses digestasi anaerobik dapat dgunakan untuk mengolah berbagai limbah organik dan mengubahnya menjadi bioenergi dalam bentuk biogas [30]. Digestasi anaerobik dapat digunakan untuk limbah dengan kandungan organik tinggi yang lebih efisisen disbanding proses lain. Selain itu produk dari proses ini dapat digunakan. Jumlah gas yang diproduksi bevariasi sesuai dengan jumlah bahan organik yang diumpankan ke digester dan temperatur mempengaruhi laju penguraian dan produksi gas. Digestasi anaerobik sangat menguntungkan karna merupakan proses yang alami dimana teknologinya menggunakan mikroorganisme, dengan kebutuhan energi yang kecil dan polusi yang di sebabkannya terhadap atmosfer lebih sedikit dibandingkan dengan teknologi lain seperti insenerasi dan pirolisis. Sumber bahan bakunya yang dapat diperbaharui dan dapat mengurangi emisi gas karbon [8].
Digestasi anaerobik telah dilakukan di beberapa jeis rektor untuk menghasilkan biogas seperti flow anaerobik sludge blanket (UASB) reaktor,
up-flow anaerobik sludge fixed-film (UASFF) reaktor, modified anaerobik baffled
reaktor (MABR), continuous stirred tank reaktor (CSTR), anaerobik pond, anaerobik
11
reaktor yag sama. Sedangkan pada proses dua tahap hidrolisis dan asidognesis dilakukan pada reaktor pertama dan asam dimanfaatkan pada tahap metanognesis didalam reaktor lain. Berdasarkan hasil yang telah ditemukan bahwa kinerja digestasi anaerobik dengan dua tahap lebih efisien daripada satu tahap [12]. Digestasi anaerobik dua tahap memungkinkan pertumbuhan dari bakteri yang berbeda dalam reaktor yang berbeda yang akan meningkatkan kestabilan proses diikuti peningkatan organic loading rate dan hydraulic retention time yang semakin singkat. Beberapa penelitian menunjukkan penggunaan digestasi anaerob dua tahap dapat meningkatkan yield CH4 sampai 23%. [16].
[image:29.595.227.441.344.616.2]Proses anaerobik sangat kompleks dengan melalui tahapan proses hidrolisis, asidogenesis, asetogenesis dan metanognesis. Proses penguraian ini terjadi dengan bantuan bakteri anaerobik. Tahapan ini ditunjukkan pada gambar 2.1
12 2.2.1 Hidrolisis
Pada tahap hidrolisis molekul besar seperti protein, polisakarida, dan lemak dikonversi oleh mikroorganisme menjadi molekul yang lebih kecil yang terlarut dalam air seperti peptida, sakarida dan asam lemak [12]. Pada umumnya lemak dihidrolisis lebih cepat daripada protein atau karbohidrat [2]. Proses hidolisis pada umumnya berjalan lambat dan menjadi laju pembatas pada keseluruhan proses digestasi anaerobik. Polimer diubah menjadi monomer terlarut melalui mikroorganisme hidrolisis. Proses ini ditunjukkan oleh gambar 2.2
nC6H10O5 + nH2O Hidrolisis nC6H12O6 Gambar 2.2 Reaksi Hidrolisis [12]
Kelompok terbesar dari bakteri yang mendegradasi selulosa dalam proses hidrolisis termasuk Bacterioides succinogenes,Clostridium lochhadii, Clostridium
cellobioporus, Ruminococcus flavefaciens, Ruminococcus albus, Butyrivibrio
fibrosolvens, Clostridium thermocellum, Clostridium stercorarium dan
Micromonospora bispora [12].
2.2.2 Asidogenesis
Proses asidognesis mengkonversi produk hidrolisis menjadi molekul kecil dengan berat molekul rendah seperti asam lemak volatil, alkohol, aldehid dan gas seperti CO2, H2, dan NH3 dan poduk samping lain [32]. Bakteri asidognesis dapat menurunkan pH bahan organik menjadi sangat rendah sekitar 4 [12], penurunan ini disebabkan karna banyaknya senyawa asam yang dihasilkan dan sangat berbahaya jika terakumulasi terlalu banyak sehingga harus dilanjutkan langsung oleh proses berikutnya [8]. Monomer dari reaksi ini akan menjadi substrat pada reaksi asetognesis [12]. Reaksi asidogenesis ditunjukkan pada gambar 2.3
C6H12O6 CH3CH2CH2COOH + 2 CO2 + 2 H2 (glukosa) (asam butirat)
C6H12O6 + 2 H2 CH3CH2COOH + 2 H2O (glukosa) (asam propionat)
Gambar 2.3 Reaksi asidogenesis [15]
13
gula produksi hidrogen akan bertambah lebih banyak sehingga memungkinkan bisa digunakan sebagai pengganti energi [8]. Pada proses digestasi anaerobik, tahap asidognesis pome terlebih dahulu diubah menjadi VFA kemudian diubah menjadi metana dan karbondiosida. VFA merupakan senyawa intermediet yang sangat penting dalam kelangsungan proses pembentukan metana [20] Konsentrasi VFA yang terlalu banyak dapat menurunkan pH sehingga bisa menghambat proses metanognesis [33]. VFA menentukan kestabilan proses digestasi anaerobik. VFA yang terlalu bayak pada dasarnya tidak menghambat proses digestasi anaerobik [34]
2.2.3 Asetognesis
Pada proses ini produk asidognesis di konversi menjadi asam asetat, hidrogen, dan CO2 oleh bakteri asetognesis [12]. Reaksi asetogenesis ditunjukkan pada gambar 2.4
CH3CH2COOH CH3COOH + CO2 + 3 H2 (asam propionat) (asam asetat)
CH3CH2CH2COOH 2CH3COOH + 2 H2 (asam butirat) (asam asetat)
Gambar 2.4 Reaksi asetogenesis [15]
2.2.4 Metanognesis
Pada proses metanognesis , asam asetat dari proses asetognesis dikenversi menjadi CO2 dan CH4. Pada proses ini produksi CH4 dapat diagi menjadi dua cara. Pertama asam asetat dikonversi menjadi CO2 dan CH4 oleh bakteri acetoclastik. Kedua menggunakan CO2 sebagai sumber karbon dan hidrogen sebagai agen pereduksi oleh bakteri hydrognetropic atau dihasilkan bentuk lain oleh bakteri jenis lain. Genus bakteri paling besar dalam proses metanognesis adalah
Methanobacterium, Methanothermobacter (formerly Methanobacterium),
Methanobrevibacter, Methanosarcina, and Methanosaeta. Reaksinya ditunjukkan pada gambar 2.5
CH3COOH Metanognesis CH4 + CO2 CO2 + 4H2 Reduksi CH4 + 3H2O
14
Atau CO2 dapat di hidrolisis menjadi asam karbonik dan metana ditunjukkan pada gambar 2.6
CO2 + H2O Hidrolisis H3CO3 4H2 + H2CO3 Reduksi CH4 + 3H2O
Gambar 2.6 Reaksi Metanognesis Dari Karbondioksida [12]
Kehadiran gas CO2 tidak diinginkan. Gas ini harus dihilangkan untuk memaksimalkan kualitas biogas sebagai bahan bakar [12].
2.3 Faktor Yang Mempengaruhi Digestasi Anaerob
Proses digestasi anaerobik berhubungan satu sama lain. Jika aktivitas dari salah satu grup mikroorganisme terhambat maka akan mempengaruhi laju dari mikroorganisme lain, mengubah kesetimbangan populasinya dan menurunkan efektifitas proses [8]. Faktor yang mempengaruhi aktifitas tersebut antara lain :
2.3.1 Temperatur
Proses anaerobik sensitif terhadap suhu, pengubahan asam asetat menjadi metana sangat dipengaruhi temperatur. Suhu yang biasa digunakan dalam proses anaerobik yaitu suhu psychrophilic (10-20) 0C [17] suhu mesofilik (35-40 ) 0C dan suhu termofilik (50-65) 0C [12] . Temperatur mesofilik yang biasa digunakan adalah 35 0C dan termofilik adalah 55 0C [17]. Pada temperatur antara 40-50 0C mikroba mesofilik tidak aktif lagi, temperatur ini disebut dengan temperatur intermediet [13]. Suhu menjadi salah satu faktor penting yang mempengaruhi efisiensi penggurangan COD pada percobaan anaerobik. Pada umumnya, diketahui bahwa digester termofilik menghasilkan biogas lebih banyak daripada digester mesofilik [19]
15 2.3.2 pH
pH menunjukkan konsentrasi asam dalam larutan. pH dari reaktor anaerobik mempengaruhi efisiensi proses penguraian. Proses Hidrolisis, asidognesis dan metanognesis memiliki pH optimum masing masing [17]. Metanogenesis bekerja efektif pada pH 6,5 – 8,2 [12]. pH untuk proses hidrolisis dan asidognesis masing masing adalah 5,5 dan 6,5 [17]. pH mempengaruhi fungsi dari enzim extraselular dan laju proses hidrolisis. Pada beberapa kasus digestasi anaerobik lebih efektif pada pH yang netral. Karna beberapa mikroorganisme mengalami pertumbuhan yang lamban dalam pH yang tinggi atau rendah [8]. pH akan sangat berpengaruh terhadap produksi biogas jika mencapai 5. Hal ini disebabkan karna pada pH yang rendah aktivitas dari bakteri metanognesis akan menurun. Menjaga pH yang konstan sangat penting untuk mengontrol hubungan antara VFA dan konsentrasi bikarbonat. Untuk mengontrol pH, NaHCO3 ditambahkan kedalam saat mulai dijalankan [12]. Nilai pH dari substrat mempengaruhi pertumbuhan dari mikroorganisme dan mempengaruhui penguraian beberapa komponen yang sangat penting dalam proses digestasi anaerobik [34].
2.3.3 Rasio Karbon – Nitrogen (C/N)
Nitrogen adalah nutrisi terbesar dalam pertumbuhan mikroba. Karbon digunakan sebagai sumber energi dan Nitrogen digunakan sebagai pembangun struktur sel [40]. Untuk penguraian yang baik rasio dari karbon dan nitrogen sekitar 25-30 pada substrat. Jika kandungan nitrogen rendah populasi mikroba yang tersisa kan menurun dan waktu yang diperlukan untuk mencerna kabon yang tersedia akan semakin lama. Kelebihan nitrogen juga menyebabkan masalah pada pembentukan ammonia dimana mempengaruhi proses anaerobik. Konsentrasi karbon dan nitrogen menunjukkan kinerja proses digestasi anaerobik [12].
Untuk mencapai rasio C/N pada sebagian kasus digunakan pencampuran dua bahan (Co-Digestasion) seperti kotoran lembu dan limbah kota [8]. Pada penelitian yang dilakukan O-Thong et al [42], pencampuran anatara POME dan palm empty
16 2.3.4 Pengadukan
Pengadukan dilakukan menghomogenkan padatan terlarut dalam digester dengan mikroba yang aktif [46]. Pengadukan selama proses dekomposisi untuk mencegah terjadinya benda-benda mengapung pada permukaan cairan dan berfungsi mencampur metanogen dengan substrat. Tujuan dari proses pengadukan adalah agar seluruh mikroorganisme menerima asupan nutrisi yang menyeluruh dan seimbang dan produk hasil metabolismenya dapat dipisahkan secara maksimal. Pencampuran Substrat yang segar dengan substrat yang telah tergradasi diperlukan agar substrat segarnya berinokulasi dengan mikroorganisme yang aktif [7]
2.3.5 Hydraulic Retention Time (HRT)
Parameter yang penting untuk ukuran dari digester biogas adalah waktu tinggal (HRT). HRT adalah interval waktu rata-rata selama substrat tinggal di dalam tangki digester. HRT adalah korelasi dari volume digester dan volume umpan substrat per unti waktu yang dituliskan dalam persamaan berikut :
HRT = VR/V [37]
Dimana :
HRT = Waktu tinggal hidraulik ( hari) VR = Volume digester (m3)
V = Volume substrat umpan per unit waktu (m3/ hari)
HRT untuk digestasi anaerobik dipengaruhi oleh temperatur dan komposis dari limbah yang digunakan. Pada keadaan mesofilik HRT berkisar antara 10 sampai 40 hari. HRT untuk thermofilik biasanya lebih rendah [17].
17 2.4 Biogas
Biogas adalah campuran gas yang terdiri dari 40 – 60 % CH4, 30-50 % CO2, dan mengandung sebagian kecil SO2 dan NH3. Biogas telah digunakan sebagai bahan bakar sejak 100 tahun yang lalu. Karna komponen yang bermanfaat pada biogas adalah metana, dibeberapa daerah biogas telah ditingkatkan menjadi biometana dimana mengandung metana lebih dari 97 %. Biogas dapat diproduksi dari berbagai limbah tumbuhan, limbah makanan dan limbah perkotaan [40]. Biogas merupakan alternatif sebagai energi terbarukan untk menggantikan energi fosil [41]. Biogas merupakan energi alternatif yang dapat digunakan untuk bahan bakar pembangkit listrik, bahan bakar kendaraan dan lain lain. Biogas memberikan dampak buruk yang lebih sedikit dibandingkan dengan bahan bakar fosil. Bahan baku biogas juga dari limbah sehingga mengurangi volume limbah yang dibuang ke tanah dan air [6].
2.1 ANALISA EKONOMI
Pada penelitian ini dilakukan analisa ekonomi yang sederhana terhadap proses asidogenesis LCPKS pada temperatur 45 0C dengan produk yang diharapkan berupa VFA yang pada tahapan berikutnya dapat dikonversi menjadi biogas. Kondisi yang digunakan tidak memerlukan pemanas dalam penelitian ini. Maka pada penelitian ini yang dikaji adalah jumlah VFA yang akan dikonversi menjadi biogas pada proses digestasi anaerobik dua tahap. Beberapa penelitian yang berhasil menghitung volume pembentukan biogas dari VFA ditunjukkan pada Tabel 2.9.
Tabel 2.9 Volume Pembentukan Biogas dari Jumlah VFA yang Terbentuk
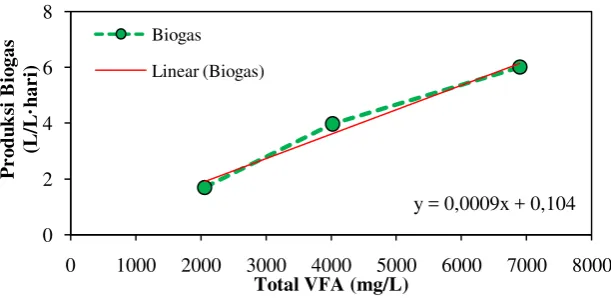
Pada penelitian ini, total pembentukan VFA tertinggi diperoleh pada variasi pH 5,5 dengan jumlah 20.298 mg/L. Menurut A.K. Kivaisi, et al konversi VFA menjadi biogas adalah 100%. Melalui Tabel 2.9 dapat digambarkan grafik linear seperti ditunjukkan pada Gambar 2.8 berikut.
Peneliti Total VFA (mg/L) Volume Biogas (L/L·hari)
Kivaisi dan Mtila 2.058,85 1,70
Li et al. 4.020,00 3,97
18
Gambar 2.7 Konversi Total VFA menjadi Biogas
Gambar 2.9 menunjukkan grafik linearisasi pembentukkan biogas dari VFA dengan persamaan garis lurus: y = 0,062 x + 907 dengan y merupakan produksi biogas dan x merupakan VFA yang terbentuk. Berdasarkan persamaan tersebut maka jumlah biogas yang dapat dihasilkan dari total VFA tertinggi pada penelitian ini adalah: y = 0,0009 x+ 0,1043
= 0,0009 x 20.298 + 0,1043 = 18,3725 L/ L LCPKS
Produksi Biogas tertinggi = 18,3725 L biogas/L LCPKS
= 18,3725 m3 biogas /m3 LCPKS Perbandingan 1m3 biogas terhadap solar adalah 0,52 liter solar
Sehingga 18,3725 m3 biogas / m3 LCPKS hari setara dengan 9,5537 Liter Solar / m3 LCPKS
Harga solar industri = 10.400/liter
Maka produksi perhari setara dengan = 10.448 x 9,5537 L solar/ m3 LCPKS = Rp. 99.817 / m3 LCPKS
Harga solar industri = 10.400/liter
Maka produksi perhari setara dengan = 10.448 x 9,5537 L solar/ m3 LCPKS = Rp. 99.817 / m3 LCPKS
y = 0,0009x + 0,104 0
2 4 6 8
0 1000 2000 3000 4000 5000 6000 7000 8000
P r o d u k si B io gas (L/ L· h ar i)
Total VFA (mg/L)
Biogas
19
BAB III
METODOLOGI PENELITIAN
3.1 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Ekologi, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara (USU), Medan.
3.2 Bahan dan Peralatan
3.2.1 Bahan-bahan
1. Starter yang digunakan berasal dari hasil olahan penelitian sebelumnya 2. Sampel Limbah Cair Pabrik Kelapa Sawit (LCPKS) dari fat pit PKS
Adolina
3. Asam klorida (HCl) 0,1 N 4. Aquadest (H2O)
5. Natrium Bikarbonat (NaHCO3)
3.2.2 Peralatan
A. Peralatan Utama
1. Fermentor tangki berpengaduk/jar fermentor (EYELA model No: MBF 300ME)
2. Pompa sludge/slurry pump (HEISHIN, model No.:3NY06F) 3. Gas meter (SHINAGAWA, model No.:W-NK-0.5B)
4. Tangki umpan (service tank) 5. Pengaduk
6. Sensor temperatur
7. Timer (OMRON, model No.:H5F)
8. Data logger (KEYENCE, model No.:NR-250) 9. Botol penampungan keluaran fermentor
20 B. Peralatan Analisa
1. Buret 25 ml
2. Timbangan analitik 3. Oven
4. Desikator
5. Pipet volumetrik 6. Karet penghisap
7. Pengaduk magnetic 8. Furnace
9. pH elektroda
3.2.2 Rangkaian Peralatan
Gambar 3.1 merupakan rangkaian peralatan yang dilakukan dalam asidognesis limbah cair kelapa sawit menjadi volatile fatty acid.
1. Pengaduk (mixer) 2. Tangki Umpan 3. Pompa Sludge 4. Jar Fermentor
5. Tombol pompa air jaket 6. Tombol penghidup fermentor 7. Pengatur kecepatan pengaduk 8. Pengatur suhu air jaket
1 0 2 4 3 1 11 7 5 3 10 8 6 4 2 3 alarm heating 13 12 14 9
9. Wadah keluaran fermentor
10. Gas Meter
11. Gas Collector
[image:38.595.159.563.402.736.2]12. pH elektroda 13. Penyerap H2S 14. Sampling injector
21 3.3 PROSEDUR PENELITIAN
3.3.1 Prosedur Loading Up dan Operasi Target
1. Starter asidogenesis sebanyak 2 L dimasukkan ke dalam fermentor.
2. Bahan baku LCPKS dimasukkan ke dalam tangki umpan.
3. Kecepatan di dalam tangki umpan LCPKS segar diatur hingga kecepatan 150 rpm agar larutan LCPKS tercampur dengan baik.
4. Suhu di dalam fermentor selama proses loading up dijaga pada suhu 45 0C
dengan kecepatan pengadukan pada 150 rpm dan pH 6.
5. HRT awal dimulai dengan HRT 20 hari dengan umpan dimasukkan secara bertahap yaitu 2 kali sehari.
6. Lakukan analisa selama 15 hari, kemudian percobaan dilanjutkan untuk HRT 15, 10, dan 4. Lakukan analisis untuk tiap HRT.
7. pH di dalam fermentor diturunkan menjadi 5,5 dengan HRT 4 dan suhu 45 0C
22
Flowchart percobaan ditunjukkan pada gambar 3.2
Selesai
Diatur kecepatan pengadukan tangki pengumpanan pada 150 rpm
Dilakukan variasi pH fermentor dari pH 6; 5,5; 5 dan 4,5 dengan penambahan NaHCO3
Dilakukan variasi HRT mulai dari HRT 20; 15; 10; dan 4 hari
Dilakukan analisa pH, M-Alkalinity, ,TS,VS,TSS,
VSS, COD dan VFA untuk setiap run
Apakah masih ada variasi pH?
Tidak
Ya
Diatur kecepatan pengadukan fermentor pada 150 rpm Dimasukkan LCPKS ke dalam tangki pengumpanan Dimasukkan starter sebanyak 2 L ke dalam fermentor
Mulai
Apakah masih ada variasi HRT?
Ya
[image:40.595.150.489.89.670.2]Tidak
23 3.3.2 Prosedur Analisa Sampel
3.3.2.1 Analisa Konsentrasi Chemical Oxygen Demand (COD) Prosedur analisa COD adalah sebagai berikut [43]: 1) Dimasukkan 10 ml contoh uji ke dalam erlenmeyer 250 ml.
2) Ditambahkan 0,2 g serbuk raksa (II) sulfat (HgSO4) dan beberapa batu didih. 3) Ditambahkan 5 ml larutan kalium dikromat, (K2Cr2O7) 0,25 N.
4) Ditambahkan 15 ml pereaksi asam sulfat (H2SO4) – perak sulfat (Ag2SO4) perlahan-lahan sambil didinginkan dalam air pendingin.
5) Dihubungkan dengan pendingin Liebig dan dididihkan di atas hot plate selama 2 jam.
6) Didinginkan dan dicuci bagian dalam dari pendingin dengan air suling hingga volume contoh uji menjadi lebih kurang 70 ml.
7) Didinginkan sampai temperatur kamar, ditambahkan indikator ferroin 2 sampai dengan 3 tetes, dititrasi dengan larutan ferro ammonium sulfat atau FAS 0,1 N sampai warna merah kecoklatan, dicatat kebutuhan larutan FAS. 8) Langkah 1 sampai dengan 7 dilakukan terhadap air suling sebagai blanko.
Kebutuhan larutan FAS dicatat. Analisis blanko ini sekaligus melakukan pembakuan larutan FAS dan dilakukan setiap penentuan COD.
9) Kandungan COD dapat dihitung berdasarkan rumus sebagai berikut:
sampel ml
N)8000 )(
B A ( O
mg/l 2
Keterangan: A = ml FAS untuk titrasi blanko B = ml FAS untuk titrasi sampel N = Normalitas FAS
8000 = berat miliekivalen oksigen 1000 ml/l
3.3.2.3 Analisia pH
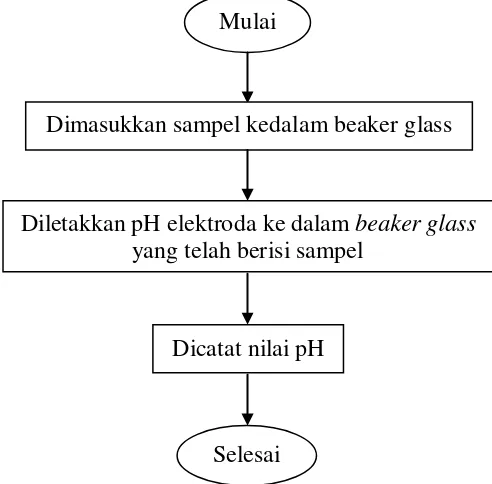
Prosedur analisa pH adalah sebagai berikut: 1. Sampel diambil melalui injektor.
2. Masukkan sampel ke dalam beaker glass.
24
[image:42.595.191.437.131.373.2]Flowchart percobaan ditunjukkan pada gambar 3.3 [43]
Gambar 3.3 Flowchart Prosedur Analisa pH
3.3.2.4 Analisa Alkalinitas
Adapun prosedurnya adalah sebagai berikut : 1. Rotating Magnet dimasukkan kedalam beaker glass.
2. Sampel sebanyak 5 ml ditambahkan dengan aquadest hingga volume larutan 80 ml dimasukkan kedalam beaker glass tersebut.
3. Beaker glass diletakkan diatas magnetic stirrer, dan pH elektroda diletakkan di dalam beaker glass, kemudian stirrer dihidupkan dan kecepatan diatur sedemikian rupa hingga sampel tercampur sempurna dengan aquadest.
4. Campuran dititrasi dengan larutan HCl 0,1 N hingga pH mencapai 4,8± 0,02. 5. Dicatat volume HCl yang di gunakan
6. Data yang diperoleh di hitung dengan rumus :
M-Alkalinity =
Sampel Vol
x x M x terpakai yang
HCl
Vol. HCl 1000 5
Mulai
Dimasukkan sampel kedalam beaker glass
Diletakkan pH elektroda ke dalam beaker glass yang telah berisi sampel
Dicatat nilai pH
Selesai
25
Flowchart percobaan ditunjukkan pada gambar 3.4[43]
Mulai
Dimasukkan 5 ml sampel ke dalam beaker glass
Selesai
Dicatat volume HCl yang terpakai
Ditambahkan aquadest hingga volume larutan menjadi 80 ml
Diaduk campuran hingga homogen dengan magnetic stirrer
Dimasukkan pH elektroda ke dalam beaker glass
Apakah bacaan pH
mencapai 4,8±0,02?
Dititrasi campuran dengan HCl 0,1 N
Tidak
Ya
[image:43.595.152.454.89.580.2]Dihitung nilai alkalinitas menggunakan persamaan 3.1
26 3.3.2.5 Analisa Total Solids (TS)
Prosedur analisa Total Solid adalah sebagai berikut :
1. Cawan penguap kosong yang telah dibersihkan, dipanaskan pada suhu 105oC dalam oven selama 1 jam. Apabila akan dilanjutkan untuk analisa zat tersuspensi organik, cawan dipanaskan pada 550oC, selama 1 jam. 2. Cawan didinginkan selama 15 menit dalam desikator, lalu ditimbang
cawan yang keluar dari furnace pada 550oC diturunkan dulu panasnya dalam oven pada 105oC sebelum didinginkan dalam desikator.
3. Sampel sebanyak 5 ml diletakkan ke dalam cawan yang telah di dinginkan. 4. Cawan yang berisi sampel ditimbang.
5. Masukkan cawan berisi sampel ke oven, suhu 103 – 105oC selama 1 jam. 6. Setelah 1 jam dinginkan cawan yang berisi residu zat padat tersebut dalam
desikator sebelum ditimbang.
7. Ulangi langkah 5 dan 6, sampai didapat berat yang konstan atau berkurang berat lebih kecil 4% berat semula atau 0,5 mg, biasanya pemanasan 1-2 jam sudah cukup. Penimbangan harus dikerjakan dengan cepat untuk mengurangi galat.
8. Kandungan TS dapat dihitung berdasarkan rumus sebagai berikut :
(mL) sampel volume
1000 B) -(A tal/L
padatan to
mg
Keterangan :
A = berat residu kering + cawan porselen, mg B = berat cawan porselen, mg
27
Flowchart percobaan ditunjukkan pada gambar 3.5 [43]
Mulai
Dipanaskan cawan penguap selama 2 jam pada suhu 105 oC
Diambil sampel dan masukkan ke dalam cawan
Selesai
Didinginkan cawan penguap selama 15 menit di dalam desikator
Ditimbang berat cawan
Didinginkan cawan penguap selama 15 menit di dalam desikator
Dimasukkan cawan berisi sampel ke oven pada suhu 103-105oC selama 1 jam
Didinginkan cawan penguap selama 15 menit di dalam desikator
Ditimbang berat cawan
Apakah berat cawan
sudah konstan? Tidak
Ya
[image:45.595.160.497.88.638.2]Dihitung nilai total solids (TS) menggunakan persamaan 3.2
28 3.3.2.6 Analisa Volatile Solid (VS)
Adapun prosedur analisa VS adalah sebagai berikut :
1. Cawan yang berisi residu dari analisa Total Solid dimasukkan kedalam furnace pada suhu 550oC selama 1 jam.
2. Setelah 1 jam ditimbang berat cawan dengan residu yang telah menguap menjadi abu.
3. Kandungan VS dapat dihitung berdasarkan rumus sebagai berikut:
(mL) sampel volume
1000 B) -(A latil/L
padatan vo
mg
Keterangan :
A = berat residu + cawan porselen sebelum pembakaran, mg B = berat residu + cawan porselen setelah pembakaran, mg Flowchart percobaan ditunjukkan pada gambar 3.6 [43]
Mulai
Dimasukkan cawan hasil analisis TS ke dalam furnace
Selesai
Dipanaskan pada suhu 550 oC selama 1 jam
Didinginkan cawan penguap di dalam desikator hingga suhunya mencapai suhu kamar
Ditimbang berat cawan
[image:46.595.153.458.302.649.2]Dihitung nilai volatile solids (VS) menggunakan persamaan 3.3
Gambar 3.6 Flowchart Prosedur Analisa Volatile Solid
29 3.3.2.7Analisa Total Suspended Solid (TSS)
Adapun prosedur analisa Total Suspended Solid adalah sebagai berikut : 1. Kertas saring kosong dipanaskan pada suhu 105oC dalam oven selama 1 jam,
setelah 1 jam didinginkan didalam desikator lalu ditimbang sebagai berat kertas saring.
2. Kertas saring dicuci dengan air aquadest sebanyak 10 ml lalu di letakkan di atas vacuump filter selama waktu tertentu.
3. Sampel yang telah dihomogenkan diletakkan di atas kertas saring yang telah diletakkan diatas vacuump filter selama waktu tertentu.
4. Kemudian residu yang tertahan diatas kertas saring tersebut dicuci dengan air suling sebanyak 3 x 10 ml.
5. Cawan kosong yang telah dipanaskan seperti prosedur analisa Total Solid ditimbang beratnya.
6. Residu yang tertahan diatas kertas saring diletakkan di atas cawan kosong yang telah ditimbang berat nya.
7. Timbang berat cawan kosong yang berisi residu yang tertahan di atas kertas saring.
8. Cawan tersebut dipanaskan di dalam oven pada suhu suhu 103 – 105oC selama 1 jam.
9. Setelah 1 jam cawan tersebut didinginkan sampai suhu kamar di dalam desikator.
10. Lalu ditimbang berat cawan tersebut.
Kandungan TSS dapat dihitung berdasarkan rumus sebagai berikut
(mL) sampel volume
1000 B) -(A L
rsuspensi/ padatan te
total
mg
Keterangan :
A = berat residu yang tertahan diatas kertas saring + cawan porselen, mg B = berat cawan porselen kosong, mg
30
Flowchart percobaan ditunjukkan pada gambar 3.7 [43]
Selesai
Dimasukkan sampel ke dalam oven pada suhu 103-105oC selama 1 jam
Didinginkan cawan penguap selama 15 menit di dalam desikator
Ditimbang berat cawan
Apakah berat cawan sudah konstan?
Tidak
Ya
Dipindahkan kertas saring secara hati-hati ke wadah timbang aluminium
Dihitung nilai total suspended solids (TSS) menggunakan persamaan 3.4
Mulai
Ditimbang kertas saring kering yang digunakan
Dibasahi kertas saring dengan sedikit air suling
Diaduk sampel dengan magnetic stirrer
hingga homogen
Dipipetkan sampel ke penyaringan
[image:48.595.117.499.107.632.2]Dicuci kertas saring atau saringan dengan 3 x 10 mL aquadest
31 3.3.2.8Analisa Volatile Suspended Solid (VSS)
Adapun prosedur analisa VSS adalah sebagai berikut [43]
1. Cawan yang berisi residu yang tertahan di kertas saring dari analisa TSS dimasukkan kedalam furnace pada suhu 550oC selama 1 jam.
2. Setelah 1 jam didinginkan didalam desikator cawan yang berisi abu tersebut. 3. Ditimbang berat cawan dengan kertas saring berisi residu yang telah menguap
menjadi abu.
4. Kandungan VSS dapat dihitung berdasarkan rumus sebagai berikut:
(mL) sampel volume
1000 B) -(A si/L
tersuspen latil
padatan vo
mg
Keterangan :
A = berat residu yang tertahan diatas kertas saring kering + cawan porselen, mg
B = berat cawan porselen + abu, mg
Flowchart percobaan ditunjukkan pada gambar 3.8 [43]
Mulai
Dimasukkan cawan hasil analisis TSS ke dalam furnace
Selesai
Dipanaskan pada suhu 550 oC selama 1 jam
Didinginkan cawan penguap di dalam desikator hingga suhunya mencapai suhu kamar
Ditimbang berat cawan
[image:49.595.134.489.365.643.2]Dihitung nilai volatile suspended solids (VSS) menggunakan persamaan 3.5
Gambar 3.9 Flowchart Prosedur Analisa Volatile Suspended Solid
3.3.2.9Analisis Volatile Fatty Acid (VFA)
Analisis VFA dilakukan dengan menggunakan Gas
Chromatographics/Mass Spectrometric (GC/MS) sesuai prosedur standar APHA
[43].
32 3.3.3 Jadwal Pengujian Sampel (Sampling)
[image:50.595.105.543.204.423.2]Adapun prosedur yang dilakukan untuk pengujian sampel adalah sama seperti prosedur yang dilakukan untuk analisis bahan baku, ditambah dengan analisis VFA, sedangkan analisis gas dilakukan jika pada penelitian ada terbentuk gas yaitu gas CO2 dan H2S. Jadwal penelitian ditunjukkan pada tabel 3.1
Tabel 3.1 Jadwal Analisis Influent dan Effluent
Hari ke
Analisis 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 pH M-Alkalinity TS VS TSS VSS COD SCOD VFA Gas Keterangan: = Analisis influent
= Analisis effluent
3.4 JADWAL PENELITIAN
32
32
Tabel 3.2 Jenis Kegiatan dan Jadwal Pelaksanaan Penelitian No
.
Kegiatan Bulan ke 1 Bulan ke-2 Bulan ke-3 Bulan ke-4 Bulan ke-5 Bulan ke-6 Bulan ke-7 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1. Persiapan penelitian
2. Survei dan pembelian bahan
3. Pelaksanaan penelitian dan pengumpulan data 4. Kompilasi data dan
penarikan kesimpulan 5. Penulisan karya
ilmiah 6. Penulisan karya
34
BAB IV
HASIL DAN PEMBAHASAN
4.1 KARAKTERISASI LIMBAH CAIR PABRIK KELAPA SAWIT
ATAU PALM OIL MILL EFFLUENT (POME)
[image:52.595.113.515.273.546.2]Bahan baku yang digunakan dalam penelitian ini berasal dari PTPN VI PKS Adolina. Adapun hasil analisis karakteristik dari bahan baku yang digunakan dapat dilihat pada Tabel 4.1.
Tabel 4.1 Hasil Analisis Karakteristik LCPKS dari PTPN IV PKS Adolina No. Parameter Satuan Hasil Uji Metode Uji
1. pH - 3,50-4,7 APHA 4500-H
2. Chemical Oxygen Demand (COD)
mg/L 41.818 SNI
3. Total Solid (TS) mg/L 16.040-61.000 APHA 2540B 4. Volatile Solid (VS) mg/L 16.060-52.360 APHA 2540E 5.
6.
Total Suspended Solid (TSS) Total Suspended Solid (TSS)
mg/L mg/L 2.920-24.700 1.920-25.800 APHA 2540D APHA 2540E 7. 8. 9. 10.
Volatile fatty acids -Asam asetat -Asam propionat -Asam butirat
Lemak Protein Karbohidrat mg/L % % % 1.508,987 560,0297 1.088,613 31,8 0,14 1,99 APHA 2540E Ekstraksi Sokletasi Kjeldah Lane Eynon
Tabel 4.1 menunjukkan hasil analisis karakteristik LCPKS dari PKS Adolina dimana terdapat beberapa parameter di atas ambang baku mutu limbah buangan.
35
Dari table 4.1 tersebut menunjukkan LCPKS PKS Adolina memiliki kandungan COD yang tinggi yaitu 41.818. kandungan COD ini mennjukkan jumlah bahan organik yang ada dalam limbah. Nilai COD yang diperoleh telah melewati batas yang diizinkan oleh Kementerian Lingkungan Hidup dalam Keputusan Menteri Negara Lingkungan Hidup Nomor: KEP 51-/MENLH/10/1995 yaitu sebesar 500 mg/L [28]. Tingginya nilai COD ini menunjukkan tingginya kandungan bahan organik yang ada dalam LCPKS sehingga dapat dimanfaatkan sebagai bahan baku pembuatan VFA.
Pada Tabel 4.1 juga menunjukkan konsentrasi lemak yang tinggi pada POME. Lemak merupakan substart yang dapat diubah menjadi VFA yang kemudian diubah menjadi biogas dalam digestasi anaerobik. Selain lemak, karbohidrat dan protein juga merupakn senyawa kompleks yang dapat diubah menjadi VFA. Sehingga POME ini merupakan substarat yang bisa digunakan untuk penelitian ini.
4.2 HASIL PENELITIAN VARIASI HRT (PROSES LOADING UP) Variasi HRT yang dilakukan dimulai dari HRT 20,15,10, dan 4 hari. Proses loading up dilakukan untuk membantu proses adaptasi dan pertumbuhan mikroba pada starter yang diambil dari kolam pengasaman PTPN III PKS Torgamba agar proses asidogenesis dapat berlangsung pada HRT operasi target. Selama proses loading up, fermentor dioperasikan dengan penurunan HRT dari 20,15, 10 dan 4 pada kondisi temperatur 45 0C, pengadukan sebesar 150 rpm dan pH dijaga konstan pada 6 (±0,2) dengan penambahan natrium bikarbonat (NaHCO3). Analisis pH, alkalinitas, TS, VS, TSS, VSS, COD serta VFA dilakukan untuk melihat metabolisme dan pertumbuhan mikroba selama proses
loading up.
4.2.1 Korelasi pH dan Alkalinitas Pada Proses Loading Up
36
Gambar 4.1 Hubungan pH dan Alkalinitas pada Proses Loading Up
Pada Gambar 4.1, menunjukkan grafik pH diantara 5,8-6,2. pH dari umpan berkisar antara 3,5 - 4,5, sehingga untuk menjaga pH fermentor tetap berada antara 5,8-6,2 dilakukan penambahan NaHCO3. Senyawa NaHCO3 ditambahkan untuk menetralkan sejumlah asam-asam yang terkandung di dalam POME dan meningkatkan kemampuan penyangganya sehingga tidak berdampak signifikan terhadap kondisi pH dan alkalinitas ketika diumpankan ke dalam fermentor [39].
Proses asidognesis pada umumnya berlangsung pada pH yang rendah.. Nilai alkalinitas yang diperoleh pada HRT 20 berfluktuasi antara 2.200 – 4.200 mg/L, pada HRT 15 alkalinitas berfluktuasi antara 2.250 - 3.800 mg/L, pada HRT 10 alkalinitas berfluktuasi antara 1.500 - 3.000 mg/L, pada HRT 4 alkalinitas berfluktuasi antara 1.300 - 3.000 mg/L. Nilai alkalinitas yang diperoleh antara 1.300 - 4.200. Nilai Alkalinitas yang diperoleh masih dalam rentang yang diizinkan yaitu 700 – 6.000 mg/L [20,45]. Penelitian Shentil Khumar et al [45] dan Aslanzadeh et al [21] memberikan nilai alkalinitas masing masing 738-746 mg/L dan 16.000 – 31.000 mg/L.
Pada proses loading up penurunan HRT tidak memberikan dampak yang signifikan pada perubahan alkalinitas. Grafik alkalinitas berfluktuasi pada kisaran pH dan alkalinitas asidognesis.
0 1 2 3 4 5 6 7 0 2000 4000 6000
0 5 10 15 20 25 30 35 40 45 50 55 60
pH A lk al in itas (m g/ L) Hari ke-Alkalinitas pH HRT 4
HRT 15 HRT 10
37
4.2.2 Pengaruh HRT Terhadap Pertumbuhan Mikroba
[image:55.595.115.529.210.420.2]Pertumbuhan mikroba dipengaruhi oleh beberapa faktor antara lain suhu, pH, HRT dan alkalinitas [8] . Konsentrasi mikroorganisme yang terbentuk dinyatakan dalam volatile suspended solid (VSS) [46]. Pengaruh pH dan alkalinitas terhadap pertumbuhan mikroba ditunjukkan pada Gambar 4.2.
Gambar 4.2 Pengaruh HRT terhadap Pertumbuhan Mikroba
Pada gambar 4.2 menunjukkan konsentrasi VSS yang berfluktuasi pada semua HRT mengalami kestabilan pada HRT 4. Perubahan HRT menyebabkan penurunan konsentrasi mikroba dan kembali mengalami peningkatan setelah hari ke 13 pada setiap HRT. Keadaan ini menunjukkan mikroba melakukan adaptasi ketika HRT dari fermentor diubah. Setelah proses adaptasi konsentrasi mikroba kemudian meningkat.
Pada gambar 4.2 pertumbuhan mikroorganisme pada HRT 4 menunjukkan hasil yang lebih baik. HRT juga merupakan faktor yang mempengaruhi pertumbuhan mikroorganisme karena HRT mempengaruhi ketersediaan nutrisi bagi mikroorganisme untuk melakukan metabolisme. Setelah mengalami fluktuasi pada HRT 20,15 dan 10, mikroba mengalami pertumbuhan yang stabil pada HRT 4. Konsentrasi mikroba yang semakin banyak ini menunjukkan mikroba telah siap melakukan penguraian bahan organik [47]. Dari hasil ini menunjukkan HRT 4 sudah siap untuk proses digestasi anaerobik operasi target. Penelitian Yee shian
0 1 2 3 4 5 6 7 0 5.000 10.000 15.000 20.000 25.000
0 5 10 15 20 25 30 35 40 45 50 55 60
pH V S S (m g/ L) Hari ke-VSS Alkalinity HRT 4
HRT 15 HRT 10
38
wong et al , 2013[20] dengan sampel limbah cair kelapa sawit juga memberikan HRT 4 sebagai HRT terbaik dalam proses digestasi anaerobik.
4.2.3 Reduksi Chemical Oxygen Demand (COD) Pada Proses Loading Up
[image:56.595.131.494.264.483.2]Parameter Chemical Oxygen Demand (COD) menunjukkan jumlah oksigen total yang dibutuhkan untuk mengoksidasi materi organik. COD menunjukkan jumlah bahan organik yang ada dalam bahan baku. Reduksi nilai COD menunjukkan berkurangnya jumlah bahan organik yang ada dalam bahan baku [48]. Gambar 4.3 menunjukkan tingkat reduksi COD selama loading up
Gambar 4.3 pengaruh HRT terhadap reduksi nilai COD
39
lebih rendah [49]. Sehingga untuk operasi target digunakan HRT 4 dengan reduksi COD yang tidak jauh berbeda dari HRT 15 dan 10.
4.2.4 Pembentukkan Volatile Fatty Acid (VFA) Pada Proses Loading Up
[image:57.595.129.493.310.529.2]Proses asidognesis merupakan konversi bahan organik komplek menjadi asam lemak volatil, alkohol, aldehid dan gas seperti CO2, H2, dan NH3 dan poduk samping lain. VFA merupakan asam lemak dengan atom karbon 2 sampai 5 (asam asetat, asam propionat, asam butirat dan lain lain). VFA dapat digunakan untuk memproduksi biogas, biohidrogen. Grafik 4.4 menunjukkan pengaruh HRT terhadap pembentukan VFA yang dinyatakan dalam bentuk asam asetat, asam propionat, asam butirat.
Gambar 4.4 Pengaruh variasi HRT terhadap pembentukan VFA
Pada proses asidognesis, VFA merupakan produk utama yang ingin dihasilkan. Komposisi dari VFA mempengaruhi keberlangsungan proses digestasi anaerobik. Terbentuknya asam propionat melebihi 3000 mg/L dapat menghambat proses digestasi anaerobik [50]. Metabolisme asam propionat menjadi asam asetat relatif lama sehingga menyebabkan akumulasi yang berakibat pada kegagalan proses digestasi anaerobik.
Dari grafik 4.4 diatas menunjukkan VFA pada HRT 20 adalah 15.975,9 mg/L dengan asam asetat, asam propionat dan asam butirat masing masing adalah 8.274685 mg/L, 3.456,628 mg/L, 4.244,586 mg/L. VFA yang dihasilkan pada
0 2000 4000 6000 8000 10000 12000 14000 16000 18000
20 15 10 4
V
F
A
(m
g/L
)
HRT
Asam Asetat
Asam Propionat
Asam Butirat
40
HRT 15 adalah 12.118,38 mg/L dengan asam asetat, asam propionat dan asam butirat masing masing adalah 6.080,505 mg/L, 3.082,163 mg/L, 2.955,713 mg/L. VFA yang dihasilkan pada HRT 10 adalah 10.805,27 mg/L dengan asam asetat, asam propionat dan asam butirat masing masing adalah 4.762,664 mg/L, 3.009,715 mg/L, 3.032,892 mg/L. VFA yang dihasilkan pada HRT 4 adalah 14.984,32 mg/L dengan asam asetat, asam propionat dan asam butirat masing masing adalah 7.279,023 mg/L , 2.122,409 mg/L, 5.582,886 mg/L.
Total VFA yang lebih banyak terbentuk pada HRT 20 yaitu 15.975,9 mg/L . Tetapi pada HRT ini terbentuk asam propionat yang tinggi yaitu 3.456,628 mg/L. Jumlah as
![Tabel 1.1 Komposisi Limbah Cair Pabrik Kelapa Sawit [6]](https://thumb-ap.123doks.com/thumbv2/123dok/112568.9134/19.595.164.461.434.614/tabel-komposisi-limbah-cair-pabrik-kelapa-sawit.webp)

![Tabel 2.1 Pertumbuhan Produksi Kelapa Sawit Indonesia [1]](https://thumb-ap.123doks.com/thumbv2/123dok/112568.9134/25.595.111.527.363.569/tabel-pertumbuhan-produksi-kelapa-sawit-indonesia.webp)
![Tabel 2.4 Baku Mutu Limbah Pengolahan Kelapa Sawit [28]](https://thumb-ap.123doks.com/thumbv2/123dok/112568.9134/27.595.142.499.353.596/tabel-baku-mutu-limbah-pengolahan-kelapa-sawit.webp)
![Gambar 2.1 Tahapan Proses Digestasi Anaerobik [2]](https://thumb-ap.123doks.com/thumbv2/123dok/112568.9134/29.595.227.441.344.616/gambar-tahapan-proses-digestasi-anaerobik.webp)