PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH JAKARTA
2019 M/1441 H
ELUSIDASI STRUKTUR SENYAWA TAXININE E DARI DAUN CEMARA SUMATRA (Taxus sumatrana) MENGGUNAKAN EKSTRAKSI SUBKRITIK HFC-134a
SKRIPSI
AFRIANA AWDADY
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH JAKARTA
2019 M/1441 H
ELUSIDASI STRUKTUR SENYAWA TAXININE E DARI DAUN CEMARA SUMATRA (Taxus sumatrana) MENGGUNAKAN EKSTRAKSI SUBKRITIK HFC-134a
SKRIPSI
Sebagai Salah Satu Syarat Memperoleh Gelar Sarjana Sains Program Studi Kimia
Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
Oleh :
AFRIANA AWDADY
11140960000050
ABSTRAK
AFRIANA AWDADY, Elusidasi Struktur Senyawa Taxinine E dari Daun Cemara Sumatra (Taxus sumatrana) menggunakan Ekstraksi Subkritik HFC-134a.
Di bawah bimbingan SANDRA HERMANTO dan R. ARTHUR ARIO LELONO
Indonesia memiliki sumber daya hayati yang berlimpah dengan tumbuhan atau pohon yang memiliki potensi sebagai sumber senyawa aktif obat-obatan.
Salah satu kelompok tanaman tersebut adalah tanaman Taxus sumatrana yang tumbuh di Hutan Lindung Dolok Sibuaton. Penelitian ini bertujuan untuk menapis senyawa aktif menggunakan teknik ekstraksi HFC-134a yang dilanjutkan dengan kromatografi kolom gravitasi dan TLC. Hasil fraksinasi kemudian dikarakterisasi dengan FTIR, LC-MS/MS dan NMR. Ekstraksi subkritik HFC-134a dilakukan sebanyak 7 batch dengan masing-masing batch sebanyak 3 siklus dan setiap siklus dilakukan selama 1 jam. Ekstrak pada batch 2, 3, 4, 6 dan 7 selanjutnya dilakukan kromatografi kolom gravitasi menggunakan eluen heksan dan etil asetat dengan perbandingan yaitu 10:0, 9:1, 8:2, 6:4, 5:5 dan 3:7 menghasilkan 305 fraksi. Fraksi-fraksi yang memiliki pola noda yang sama disatukan dan didapatkan 39 fraksi. Fraksi 8 diuji lebih lanjut didasarkan pada bentuk fraksi yang menyerupai kristal. Kemudian fraksi tersebut dikarakterisasi menggunakan FTIR, LC-MS/MS dan NMR. Analisa FTIR menunjukkan vibrasi C=C (1.641,42 cm-1), C=O (1.728,22 cm-1), C-O (1.240,23 cm-1 dan 1.159,22 cm-1), C-H ulur (2.949,16 cm-1), C-H tekuk (1.448,54 cm-1). Analisa LC-MS/MS menghasilkan puncak m/z [M+Na+] 673,2991 (BM=650,3099) dengan rumus molekul C37H46O10 diduga merupakan senyawa taxinine E. Analisa 1H NMR dan 13C NMR menunjukkan sinyal khas taxinine E yaitu C=C δC 146,54 (C-4), C=C δC 116,17 (C-20), gugus cinnamoyl δC 70,25 (C-5), gugus asetiloksi pada δC 75,01 (C-2), δC 70,25 (C-9), δC
71,92 (C-10), δC 70,81 (C-13). Isolasi senyawa Taxinine E dari Taxus sumatrana yang telah berhasil diisolasi merupakan senyawa yang diduga aktif sebagai antitumor, antiinflamasi dan antibakteri, dengan rendemen sebesar 0,0047%
merupakan yang pertama kali dilaporkan.
Kata kunci : Ekstraksi subkritik HFC-134a, FTIR, LC-MS/MS, NMR, taxinine E, Taxus sumatrana
ABSTRACT
AFRIANA AWDADY, Structure Elucidation of Taxinine E Compound from Sumatran Pine Cones (Taxus sumatrana) using HFC-134a Subcritical Extraction.
Under the guidance of SANDRA HERMANTO and R. ARTHUR ARIO LELONO
Indonesia has abundant biological resources with plants or trees that have the potential as a source of active compounds of medicines. One such group of plants is the Taxus sumatrana plant that grows in the Dolok Sibuaton Protection Forest. This study aims to screen the active compound using HFC-134a extraction technique followed by gravity column chromatography and TLC. The fractionation results were then characterized by FTIR, LC-MS/MS and NMR. The subcritical extraction of HFC-134a was done in 7 batches with 3 batches in each batch and each cycle was carried out for 1 hour. Extraction results showed greenish yellow paste. Extracts in batches 2, 3, 4, 6 and 7 were then carried out by gravity column chromatography using hexane and ethyl acetate eluents in a ratio of 10:0, 9:1, 8:2, 6:4, 5:5 and 3:7 produce 305 fractions. The fractions that have the same stain pattern are put together and 39 fractions are obtained. Fraction 8 was further tested based on the shape of the crystal-like fraction. Then the fraction was characterized using FTIR, LC-MS/MS and NMR. FTIR analysis shows vibrations of C=C (1.641,42 cm-1), C=O (1728.22 cm-1), CO (1.240,23 cm-1 and 1.159,22 cm-1), stretching CH (2,949.16 cm-1), CH bend (1,448.54 cm-1). LC- MS/MS analysis yields the peak m/z [M+Na+] 673.2991 (BM = 650.3099) with the molecular formula C37H46O10 thought to be a taxinine E compound. Analysis of 1H NMR and 13C NMR shows a typical signal of taxinine E namely C=C δC
146.54 (C-4), C=C δC 116.17 (C-20), cinnamoyl group 70,25 (C-5), the acetiloxy group at δC 75,01 (C-2), δC 70,25 (C-9), δC 71,92 (C-10), δC 70,81 (C-13).
Isolation of taxinine E compound from Taxus sumatrana which has been successfully isolated is a compound that is suspected to be active as an antitumor, anti-inflammatory and antibacterial, with a yield of 0,0047% which was first reported.
Keywords : HFC-134a subcritical extraction, FTIR, LC-MS/MS, NMR, taxinine E, Taxus sumatrana
KATA PENGANTAR
Puji syukur penulis panjatkan kepada Allah SWT yang telah melimpahkan rahmat, taufik, serta hidayah-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul Elusidasi Struktur Senyawa Taxinine E dari Daun Cemara Sumatra (Taxus sumatrana) menggunakan Ekstraksi Subkritik HFC-134a. Shalawat serta salam senantiasa tercurahkan kepada Nabi Muhammad Shollallahu ‘Alayhi wa Sallam beserta keluarga, sahabat dan kita selaku umatnya. Dalam pelaksanaan penyusunan skripsi ini, penulis mendapat banyak bantuan, bimbingan dan arahan dari berbagai pihak. Oleh sebab itu dalam kesempatan ini penulis ingin mengucapkan terima kasih yang tulus kepada :
1. Dr. Sandra Hermanto, M.Si selaku Pembimbing I yang telah memberikan pengarahan serta bimbingannya sehingga banyak membantu penulis dalam menyelesaikan skripsi ini;
2. R. Arthur Ario Lelono, Ph.D selaku Pembimbing II yang telah memberikan pengarahan serta bimbingannya baik dalam diskusi ilmiah serta arahan teknis rancangan penelitian sehingga banyak membantu penulis dalam menyelesaikan skripsi ini;
3. Dr. Siti Nurbayti, M.Si sebagai penguji I yang telah memberikan saran serta masukan yang bermanfaat;
4. Nurhasni, M.Si sebagai penguji II yang telah memberikan saran serta masukan yang bermanfaat;
5. Dr. La Ode Sumarlin, M.Si selaku Ketua Program Studi Kimia, Fakultas Sains dan Teknologi, UIN Syarif Hidayatullah Jakarta;
viii
6. Prof. Dr. Lily Surayya Eka Putri, M.Env. Stud. Selaku Dekan Fakultas Sains dan Teknologi UIN Syarif Hidayatullah Jakarta;
7. Dr. Sofa Fajriah dan Dr. Ahmad Darmawan selaku peneliti di bidang kimia bahan alam beserta pengoperasional NMR LIPI Kimia yang telah membantu dalam penelitian ini;
8. Ibu Kartinah, Bapak Alm. Surjadi dan Kakak Fayyadhah Awdady tercinta atas segala doa, pengorbanan, nasihat dan motivasinya kepada penulis;
9. Kak Ibnu dan Kak Herlan selaku teknisi yang telah membantu dan memberikan banyak masukan serta solusi dalam penelitian ini;
10. Segenap dosen Program Studi Kimia atas ilmu pengetahuan dan pegalaman hidup yang dengan ikhlas diajarkan dan diberikan kepada penulis;
11. Sahabat seperjuangan Nur Fauziyah, Nurlathifah, Lucyta Sari, Ambar Ilafah, Chinta Permatasari, Isni Putri yang selalu memberi bantuan dan semangat;
12. Tri, Eka, Nadya sahabat yang selalu memberikan motivasi;
13. Bayhaqi, Aldi, Dewi, Roy, Anggi, Humairah, Rosty, Alfi dan teman-teman PSM UIN Jakarta yang selalu memberi semangat dan keceriaan;
14. Teman–teman kimia angkatan 2014 yang senantiasa memberi dukungan, motivasi dan keceriaan kepada penulis;
15. Dan semua pihak yang telah membantu secara langsung dan tidak langsung, yang tidak dapat disebutkan satu persatu.
Semoga arahan, motivasi dan bantuan yang telah diberikan menjadi amal ibadah bagi keluarga, Bapak dan Ibu, sehingga memperoleh balasan yang lebih baik dari Allah SWT. Akhir kata penulis berharap, semoga skripsi ini dapat
bermanfaat bagi rekan-rekan mahasiswa-mahasiswi dan pembaca sekaligus demi menambah pengetahuan tentang kimia bahan alam.
Jakarta, Oktober 2019
Penulis
DAFTAR ISI
Halaman
KATA PENGANTAR viii
DAFTAR ISI xi
DAFTAR GAMBAR xiii
DAFTAR TABEL xiv
DAFTAR LAMPIRAN xv
BAB I PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Rumusan Masalah 5
1.3 Hipotesis Penelitian 5
1.4 Tujuan Penelitian 5
1.5 Manfaat Penelitian 6
BAB II TINJAUAN PUSTAKA 7
2.1 Tanaman Taxus sumatrana 7
2.2 Metabolit Sekunder Taxus sumatrana 10
2.3 Ekstraksi 14
2.4 TLC (Thin Layer Chromatorgraphy) 14
2.5 Ekstraksi Subkritik HFC-134a 16
2.6 Metode Penentuan Struktur Kimia 17
2.6.1 Fourier Transform Infra Red (FTIR) 18
2.6.2 LC-MS/MS 19
2.6.3 Spektroskopi 1H NMR dan 13C NMR 20
BAB III METODE PENELITIAN 23
3.1 Waktu dan Tempat Pelaksanaan 23
3.2 Alat dan Bahan 23
3.2.1 Alat 23
3.2.2 Bahan 23
3.3 Diagram Alir Penelitian 24
3.4 Prosedur Kerja 25
3.4.1 Preparasi Sampel 25
xi
3.4.2 Ekstraksi Daun Taxus sumatrana dengan Ekstraksi Subkritik
HFC-134a (Lelono et al., 2018) 25
3.4.3 Kromatografi Kolom Gravitasi (Aksara et al., 2013) 27
3.4.4 TLC (Marliana et al., 2005) 27
3.4.5 Penentuan Struktur Kimia 28
3.4.5.1 LC-MS/MS (Stachniuk et al., 2017) 28
3.4.5.2 FTIR (Widowati et al., 2003) 28
3.4.5.3 Analisis dengan Spektroskopi NMR (Tamela et al.,
2004) 28
BAB IV HASIL DAN PEMBAHASAN 29
4.1 Hasil Ekstraksi HFC-134a 29
4.2 Hasil Kromatografi Kolom Gravitasi dari Ekstrak HFC-134a Daun
Taxus sumatrana 33
4.3 Hasil Analisis Data FTIR 42
4.4 Hasil Analisis Data LC-MS/MS 43
4.5 Hasil Analisis Data 1H NMR 47
4.6 Analisis Data 13C NMR dan DEPT 135 53
4.7 Analisis Data HMBC (Heteronuclear Multiple Bond Connectivity) 58
BAB V PENUTUP 63
5.1 Simpulan 63
5.2 Saran 63
DAFTAR PUSTAKA 64
LAMPIRAN 70
xii
GAMBAR
Halaman
Gambar 1. Pohon Taxus sumatrana (Mingiweng, 2009) ... 8
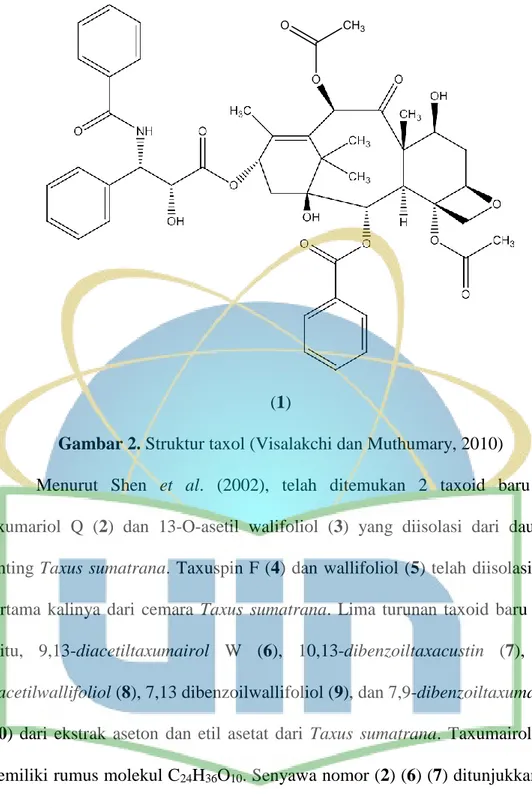
Gambar 2. Struktur taxol (Visalakchi dan Muthumary, 2010) ... 11
Gambar 3. (2) Struktur taxumairol Q, (6) 9,13-diacetiltaxumairol W dan (7) 10,13-dibenzoiltaxacustin (Shen et al., 2002) ... 12
Gambar 4. (3) Struktur 13-O-acetilwallifoliol, (8) 7,13- diacetilwallifoliol dan (9) 7,13-dibenzoilwallifoliol (Shen et al., 2002) ... 12
Gambar 5. Struktur tasumatrol H (Shen et al., 2002) ... 13
Gambar 6. Diagram alir penelitian ... 24
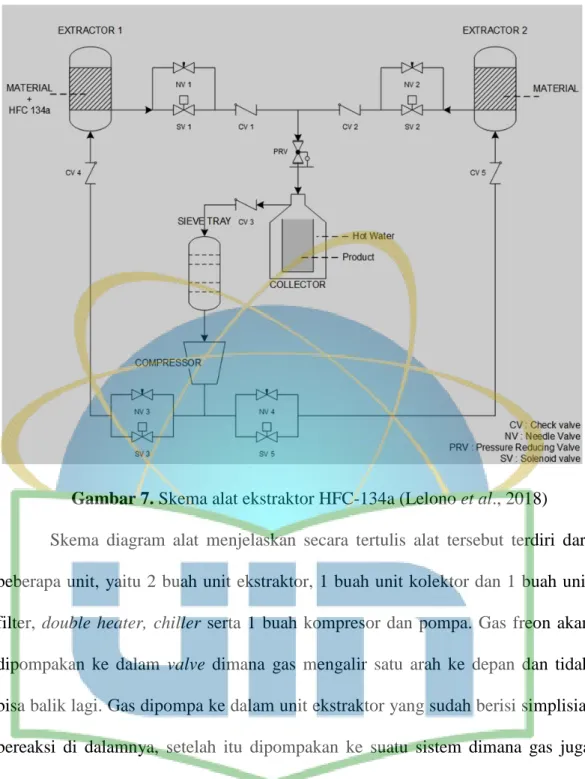
Gambar 7. Skema alat ekstraktor HFC-134a (Lelono et al., 2018) ... 26
Gambar 8. (a) Hasil KLT 39 fraksi dari kolom kromatografi gravitasi di bawah sinar UV dengan panjang gelombang 254 nm, (b) 365 nm dan (c) hasil pewarnaan dengan larutan H2SO4 ... 37
Gambar 9. Bentuk fraksi 6, 8, 9, 11, 12 dan 14 ... 38
Gambar 10. a) DCM : Ea (9:1), (b) n-heksan : Ea (7:3), (c) DCM : n- heksan (5:5), (d) DCM : Ea (9:1) dengan penyemprotan H2SO4, (e) n-heksan : Ea (7:3) dengan penyemprotan H2SO4, (f) DCM : n-heksan (5:5) dengan penyemprotan H2SO4 ... 40
Gambar 11. Hasil KLT 2 dimensi fraksi 8 dengan eluen n-heksan : etil asetat (8 : 2) dan eluen klororform : aseton (9 : 1) ... 41
Gambar 12. Hasil spektrum FTIR fraksi 8 ... 42
Gambar 13. (a) Kromatogram LC-MS/MS blanko, (b) Kromatogram LC-MS/MS fraksi 8 ... 44
Gambar 14. (a) Kromatogram LC-MS/MS pada waktu retensi 9,77 (b) Spektrum massa pada waktu retensi 9,77 menit ... 46
Gambar 15. Spektrum 1H NMR dari fraksi 8 perbesaran pada δH 0,8-7,7 ppm (CDCl3, 500 MHz) ... 48
Gambar 16. Senyawa 2-deacetyltaxinine E ... 53
Gambar 17. Spektrum 13C NMR dari fraksi 8 (CDCl3, 125 MHz) ... 54
Gambar 18. Spektrum NMR DEPT 135 dari fraksi 8 (CDCl3, 125 MHz) ... 55
Gambar 19. (a) struktur taxinine E dengan pergeseran kimia δH, (b) struktur taxinine E dengan pergeseran kimia δC dan penomoran pada karbon ... 60
Gambar 20. struktur taxinine E dengan korelasi HMBC ... 61
DAFTAR TABEL
Halaman
Tabel 1. Senyawa dalam Daun Taxus sumatrana ... 13
Tabel 2. Serapan khas beberapa gugus ... 19
Tabel 3. Pergeseran kimia 1H NMR dan 13C NMR ... 22
Tabel 4. Waktu, Tekanan ,Suhu dan Berat Hasil Ekstraksi Subkritik HFC-134a ... 30
Tabel 5. Berat ekstrak pada batch 2, 4, 5, 6 dan batch 7 ... 33
Tabel 6. Berat fraksi hasil kromatografi kolom gravitasi ... 35
Tabel 7. Hasil analisa gugus fungsi fraksi 8 berdasarkan spektrum FTIR ... 43
Tabel 8. Dugaan senyawa pada fraksi 8 ... 45
Tabel 9. Geseran kimia dan jenis proton dari data spektrum 1H NMR, 13C NMR, DEPT 135 serta HMBC ... 49
Tabel 10. Geseran Kimia 1H dan 13C NMR dari daun Taxus baccata L. ...51
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Alat ekstraktor sistem subkritik HFC-34a ... 70
Lampiran 2. Instumen karakterisasi ... 70
Lampiran 3. Spektrum FTIR Fraksi 8 ... 71
Lampiran 4. Spektrum LC-MS/MS Fraksi 8 ... 72
Lampiran 5. Spektrum 1H NMR Fraksi 8 ... 73
Lampiran 6. Spektrum 13C NMR Fraksi 8 ... 77
Lampiran 7. Spektrum HMBC ... 81
Lampiran 8. Perhitungan Rendemen ... 85
Lampiran 9. Gambar Ekstrak Hasil Ekstraksi Subkritik HFC-134a ... 86
Lampiran 10. Hasil TLC Pemisahan Kromatografi Kolom Gravitasi Awal ... 87
BAB I PENDAHULUAN
1.1 Latar Belakang
Indonesia merupakan negara dengan wilayah sumber daya hayati yang berlimpah yang telah sekian lama terfokus pada produk kayu, sehingga ketertarikan dan perhatian terhadap produk bukan kayu terabaikan. Diantara sekian banyak pengelompokan jenis hasil hutan bukan kayu, tumbuhan atau pohon yang memiliki potensi sebagai sumber senyawa aktif obat-obatan merupakan salah satu kelompok yang sangat menjanjikan. Salah satu kelompok tersebut adalah tanaman Taxus sumatrana (Hidayat et al., 2014).
Di Indonesia, Taxus sumatrana tumbuh secara alami di hutan pegunungan ataupun punggung pegunungan di Sumatra : Gunung Kerinci, Jambi, Kawasan Hutan Lindung Dolok Sibuaton, Sumatra Utara, dan Gunung Dempo, Sumatra Selatan. Genus Taxus merupakan satu-satunya pohon cemara yang penting secara ekonomi. Selama berabad-abad, masyarakat di dunia menggunakan Taxus sebagai bahan baku obat-obatan. Genus Taxus menjadi jenis yang sangat fenomenal mulai tahun 1990-an dengan berhasil diidentifikasinya taxane, senyawa unik yang termasuk golongan diterpenoid.
Taxus sumatrana telah banyak diteliti dalam kemampuannya menghasilkan senyawa taxol yang bersifat sebagai antikanker (Sukiman, 2010).
Tanaman Taxus sumatrana yang dapat menghasilkan senyawa yang bermanfaat untuk obat antikanker ini sesuai dengan firman Allah yang terdapat dalam ayat suci Al.quran yang menjelaskan tentang tumbuhan yang dapat
dimanfaatkan, sebagaimana telah dijelaskan dalam ayat suci Al.quran Surah As.Syu’araa’ ayat 7-8 :
(٧ ) ِ ر م ي ك
جوز ل ك ن م اه ي ف ان ت نب أ م ك ضرلأا ىلا ور ي ا م لو ا
Artinya :
(۸ ) ن ي مؤم هر م
ثك أ ناك مو ا
ِ ي ة
لأ
ن ذ ي كل
“Dan apakah mereka tidak memperhatikan bumi, berapakah banyaknya Kami tumbuhkan di bumi itu berbagai macam tumbuh-tumbuhan yang baik?
Sesungguhnya pada yang demikian itu benar-benar terdapat suatu tanda kekuasaan Allah, dan kebanyakan mereka tidak beriman” (Asy-Syu'araa': 7-8).
Shihab (2002) menafsirkan Surat Asy-Syu’araa’ ayat 7-8: “Adakah mereka akan terus mempertahankan kekufuran dan pendustaan serta tidak merenungi dan mengamati sebagian ciptaan Allah di bumi ini? Sebenarnya, jika mereka bersedia merenungi dan mengamati hal itu, niscaya mereka akan mendapatkan petunjuk.
Kamilah yang mengeluarkan dari bumi ini beraneka ragam tumbuh-tumbuhan yang mendatangkan manfaat. Dan itu semua hanya dapat dilakukan oleh Tuhan yang Maha Esa dan Maha Kuasa (7). Sesungguhnya adanya beraneka ragam tumbuh-tumbuhan di bumi merupakan bukti yang jelas akan adanya Sang Pencipta Yang Maha Kuasa. Tetapi kebanyakan kaum tidak mau beriman (8)”.
Sebagaimana telah dijelaskan dalam firman Allah SWT, maka salah satu tanaman yang memiliki manfaat yaitu Taxus sumatrana. Diyakini bahwa semua bagian tanaman ini, baik daun, ranting, maupun akarnya merupakan sumber taxane atau paclitaxel yang dapat diekstraksi sebagai obat yang sangat mujarab untuk kemoterapi berbagai jenis kanker seperti aktivitas anti kanker payudara
De Castro (1994) menjelaskan bahwa pelarut non polar dan hampir tidak polar memiliki suhu kritis sedang (misalnya N2O, CO2, etana, propana, pentana, xenon, SF6, dan beberapa freon) memiliki daya larut yang terbatas untuk zat terlarut yang memiliki polaritas tinggi. Dengan demikian, dilakukan modifikasi untuk meningkatkan daya larutnya dengan menambahkan senyawa polar ke dalam CO2 yang merupakan pelarut non polar. Namun, penambahan pelarut polar seperti metanol dapat meningkatkan suhu kritis yang efektif, dan ini dapat merusak produk yang labil terhadap termal.
HFC-134a adalah pelarut non polar, HFC-134a juga memiliki tekanan kritis yang relatif lebih rendah dibandingkan pelarut lainnya (Mustapa et al., 2004). Oleh karena itu, hal ini dapat meminimalkan biaya operasi karena tekanan yang diperlukan lebih rendah selama proses SFE (Supercritical fluid extraction).
Ekstraksi fluida superkritis merupakan alternatif ekstraksi yang potensial untuk mengambil bahan bioaktif dari tanaman herbal bila dibandingkan dengan ekstraksi cair menggunakan pelarut organik. Ekstraksi fluida superkitis mempunyai kelebihan yaitu lebih efisien karena waktu ekstraksi lebih pendek, tidak beracun dan alternatif ramah lingkungan. Sedangkan kerugian utama dari ekstraksi CO2 fluida superkitik adalah daya larutnya yang terbatas (Sondari et al., 2017).
HFC (Hydrofluorocarbon) merupakan molekul yang terdiri dari hidrogen, florin dan karbon. HFC telah digunakan terutama sebagai pendingin sejak tahun 1980-an. HFC-134a juga dapat digunakan untuk mengekstrak berbagai bahan alam (Lapkinet al., 2006).
Lembaga Ilmu Pengetahuan Indonesia (LIPI) telah melakukan penelitian tentang ekstraksi bahan alam dengan menggunakan ekstraksi subrkritik menggunakan HFC-134a. Penelitian tersebut berjudul Aklimitasi dan Kenampakan Agronomi dari Klon Poliploid Artemisia annua L. oleh Rahman et al. (2017). Ekstraksi dengan sistem subkritik HFC-134a adalah dengan memanfaatkan selektifitas HFC-134a, yang telah dilaporkan mampu mengisolasi senyawa artemisinin secara selektif dari Artemisia annua (Lelono et al., 2018).
Metode ekstraksi subkritik ini merupakan inovasi metode ekstraksi yang selektif, efisien dan ekonomis.
Penelitian ini dilakukan untuk mengisolasi senyawa dari Taxus sumatrana menggunakan sistem subritik HFC-134a yang dilaporkan mampu mengisolasi senyawa artemisinin secara selektif dari Artemisia annua. Menurut Shen et al.
(2002), telah ditemukan senyawa taxumairol Q (1) dan 13-O-asetilwallifoliol (2) yang berhasil diisolasi dari ekstrak aseton dan etil asetat tanaman Taxus sumatrana. Senyawa baru golongan diterpenoid juga berhasil diisolasi dari ranting Taxus sumatrana yaitu tasumatrol H-L dari ekstrak aseton (Shen et al., 2005).
Senyawa tasumatrol P-T juga berhasil diisolasi dari ekstrak aseton daun dan ranting Taxus sumatrana oleh (Shen et al., 2007). Isolasi senyawa tasumatrol U-Z berhasil ditemukan dalam ekstrak aseton daun Taxus sumatrana oleh (Shen et al., 2008). Senyawa taxol juga berhasil diisolasi dari Taxus brevifolia menggunakan metode ekstraksi superkritik dengan ekstrak sebesar 0,27% (Jennings et al., 1992).
Penelitian tentang ekstraksi senyawa dari daun Taxus sumatrana menggunakan metode ekstraksi subkritik HFC-134a belum pernah dilakukan. Hal inilah yang mendasari dilakukannya penelitian ini. Pemisahan dan analisis
senyawa dilakukan dengan menggunakan TLC dengan pewarna, dan kromatografi kolom gravitasi, sedangkan elusidasi struktur menggunakan LC-MS/MS, FTIR dan NMR.
1.2 Rumusan Masalah
Rumusan masalah dalam penelitian ini adalah :
1. Apakah metode ekstraksi subkritik HFC-134a mampu mengisolasi senyawa aktif pada daun Taxus sumatrana?
2. Senyawa apakah yang terdapat dalam isolat daun Taxus sumatrana berdasarkan hasil analisis FTIR, LC-MS/MS dan NMR?
1.3 Hipotesis Penelitian
Hipotesis dari penelitian ini adalah metode ekstraksi HFC-134a dapat mengekstraksi senyawa yang spesifik dari tanaman Taxus sumatrana dan dapat ditentukan struktur kimianya menggunakan spektroskopi FTIR, LC-MS/MS dan NMR.
1.4 Tujuan Penelitian
Tujuan dari penelitian ini dipaparkan sebagai berikut :
1. Mengisolasi senyawa aktif daun Taxus sumatrana menggunakan metode ekstraksi subkritik HFC-134a.
2. Mengetahui prediksi struktur senyawa aktif dalam fraksi daun Taxus sumatrana hasil ekstraksi subkritik HFC-134a menggunakan FTIR, LC- MS/MS, dan NMR.
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi tentang senyawa aktif yang terdapat dalam fraksi daun Taxus sumatrana dengan metode ekstraksi subkritik HFC-134a dan mengembangkan pengetahuan tentang kimia bahan alam serta untuk memanfaatkan potensi sumber daya hayati Indonesia.
BAB II
TINJAUAN PUSTAKA
2.1 Tanaman Taxus sumatrana
Taxus sumatrana merupakan jenis tumbuhan yang tumbuh pada dataran tinggi, termasuk dalam kelompok famili Taxaceae dan sub-divisi Gymnospermae.
Taxus sumatrana lebih dikenal dengan nama lokal yaitu cemara sumatra. Tinggi tanaman Taxus sumatrana berkisar antara 11-30 m dengan diameter mencapai 20- 230 cm (Frianto dan Novriyanti, 2017). Taxus sumatrana mengandung taxol yang mampu melawan sel kanker. Sebanyak 1 kg taxol membutuhkan bahan sebanyak 7.270-10.000 kg kulit batang pohon. Untuk mendapatkan 1 kg taxol dibutuhkan sekitar 2000 pohon Taxus. Padahal seorang penderita kanker memerlukan 2-2,5 gram taxol (Malik et al., 2011). Di Asia, hanya sedikit negara yang memiliki sebaran alami genus Taxus, antara lain Taxus cuspidata (ditemukan di Jepang), Taxus chinensis (ditemukan di Cina), dan Taxus sumatrana (ditemukan di Indonesia, Taiwan, Vietnam, Nepal, dan Tibet), yang kondisi populasinya terancam punah (Frianto dan Novriyanti, 2016).
Baru-baru ini, diterpenoid yang ditemukan dari Taxus sumatrana telah menunjukkan potensi penggunaan sebagai senyawa kemoterapi antikanker (Shen et al., 2005). Belum ada kesepakatan ahli botani mengenai jumlah spesies yang termasuk dalam genus Taxus. Taxus sumatrana merupakan tanaman yang mengandung taxane diterpenoid atau paclitaxel (taxol) yang bersifat antikanker (Iszkulo et al., 2013) serta 10-deacetylbaccatin III dan baccatin III (Hidayat dan Tachibana, 2013). Kedua senyawa tersebut merupakan produk antara (precursor)
7
dari biosintesistaxol. 10-deacetylbaccatin III dan baccatin III juga ditemukan pada daun dan batang muda Taxus sumatrana (Shen et al., 2005). Kulit, daun, cabang, ranting, dan akar dari jenis taxus merupakan sumber taxane, dimana paclitaxel diekstraksi sebagai obat yang sangat sukses digunakan dalam mengobati berbagai jenis kanker (Hendalastuti et al., 2010).
Menurut Database (2017) klasifikasi tanaman Taxus sumatrana:
Kingdom : Plantae Kelas : Pinopsida Ordo : Taxales Family : Taxaceae Genus : Taxus
Spesies : Taxus sumatrana Tanaman Taxus sumatrana ditunjukkan pada Gambar 1.
Gambar 1. Pohon Taxus sumatrana (Mingiweng, 2009)
Morfologi tanaman Taxus sumatrana yaitu bunga berukuran kecil, kuncup bunga mengelompok di sepanjang bagian bawah percabangan. Pohon memiliki daun seperti jarum (Hidayat et al., 2014). Taxus merupakan tanaman berupa pohon dengan daun berbentuk linear dan berwarna hijau tua pada permukaan atas sedang permukaan daun bagian bawah berwarna hijau kekuningan (Huang et al., 2008).
Hasil survei langsung di lapangan yang dilakukan Rachmat (2008) menunjukkan bahwa habitat alami cemara Sumatra di Indonesia saat ini terdapat di wilayah Gunung Kerinci, Jambi. Jenis ini tumbuh alami di hutan pegunungan pada bagian punggung bukit, lereng-lereng yang terjal dan tepian jurang pada ketinggian 1.700 - 2.200 mdpl. Pola penyebaran cemara Sumatra yang tumbuh di Gunung Kerinci juga memiliki kesamaan dengan pola penyebaran cemara Sumatra yang tumbuh di Taiwan, yaitu terpencar mengelompok (clustering). Berdasarkan kondisi tempat tumbuh alaminya yang hanya dijumpai di wilayah punggung bukit, lereng, dan tepian jurang, cemara Sumatra diketahui menyukai tempat yang berdrainase baik (well drainage) dan tidak pernah tergenang. Jumlah benih Taxus per kilogram sangat bervariasi menurut jenisnya.
Populasi Taxus di dunia telah menurun secara drastis seiring dengan tingginya tingkat eksploitasi yang dilakukan untuk memperoleh bahan aktif kelompok taxane di dunia farmasi. Ancaman tersebut akibat penebangan pohon dan pengulitan total batang, serta strategi manajemen yang minim. Namun demikian, Taxus sumatrana yang tumbuh di Indonesia sampai saat ini masih belum tereksploitasi sebagai alternatif sumber taxol. Status keterancaman jenis ini
dalam IUCN red list termasuk dalam kategori memiliki risiko keterancaman yang masih rendah least concern (LC) (IUCN, 2014). Penurunan populasi dan habitat yang terfragmentasi dapat menyebabkan terjadinya kepunahan pada Taxus sumatrana. Oleh karena itu diperlukan upaya konservasi dalam penyelamatan jenis tanaman ini (Frianto dan Novriyanti, 2017).
2.2 Metabolit Sekunder Taxus Sumatrana
Sejarah perkembangan penelitian dan penggunaan genus Taxus di wilayah bumi bagian Utara telah tercatat dengan baik. Sejarah ini dimulai dari penemuan genus Taxus sebagai sumber taxol. Taxol hanya dihasilkan dari genus Taxus (Court dan Hardman, 2006). Merek dagang taxol dan hak pemasarannya dipegang oleh Bristol-Myers Squibb sejak tahun 1991. Semenjak itu, permintaan fenomenal terhadap taxol terus meningkat dan diprediksi akan tetap tinggi karena sampai sekarang diyakini bahwa taxol adalah obat antikanker yang paling dicari di dunia, selain obat antikanker lainnya, seperti camptothecin, topotecan, irinotecan dan lain-lain (Cragg et al., 2006).
Taxol (1) berbentuk kristal putih dengan rumus empiris C47H51NO14 (berat molekul 853,9), sangat lipofilik, tidak larut dalam air dan meleleh di sekitar 216- 217ºC. Secara struktural, bisa dilihat sebagai N-benzoyl-β-phenylisoserin ester dari diterpenoid bacentia III dengan cincin oksetan yang sangat khas, taxol merupakan kelompok kecil dari campuran dengan empat cincin oksetan dan rantai samping komplek ester dalam struktur Taxus (Visalakchi dan Muthumary, 2010).
Struktur taxol dapat dilihat pada Gambar 2.
(1)
Gambar 2. Struktur taxol (Visalakchi dan Muthumary, 2010)
Menurut Shen et al. (2002), telah ditemukan 2 taxoid baru yaitu taxumariol Q (2) dan 13-O-asetil walifoliol (3) yang diisolasi dari daun dan ranting Taxus sumatrana. Taxuspin F (4) dan wallifoliol (5) telah diisolasi untuk pertama kalinya dari cemara Taxus sumatrana. Lima turunan taxoid baru (6-10) yaitu, 9,13-diacetiltaxumairol W (6), 10,13-dibenzoiltaxacustin (7), 7,13- diacetilwallifoliol (8), 7,13 dibenzoilwallifoliol (9), dan 7,9-dibenzoiltaxumairol P (10) dari ekstrak aseton dan etil asetat dari Taxus sumatrana. Taxumairol Q (2) memiliki rumus molekul C24H36O10. Senyawa nomor (2) (6) (7) ditunjukkan pada Gambar 3.
(2) (6)
(7)
Gambar 3. (2) Struktur taxumairol Q, (6) 9,13-diacetiltaxumairol W dan (7) 10,13-dibenzoiltaxacustin (Shen et al., 2002)
Struktur senyawa (3) (8) dan (9) ditunjukkan pada Gambar 4.
(3) (8)
(9)
Gambar 4. (3) Struktur 13-O-acetilwallifoliol, (8) 7,13-diacetilwallifoliol dan (9) 7,13-dibenzoilwallifoliol (Shen et al., 2002)
Menurut Shen et al. (2005), investigasi fitokimia dari ekstrak aseton daun dan ranting muda Taxus sumatrana (Taxaceae) telah menghasilkan isolasi lima taxane diterpen ester baru, tasumatrol H-L (11-15), bersama dengan 12 taxanes yang dikenal (16-26). Senyawa yang dikenal diidentifikasi sebagai 10-deasetil-13- oxobaccatin III (16), 10-deasetilbakatin III (17), taxacin (18), yunnanxana (19), 5α-hidroksi-2α,7β,9α,10β,13α-tetraasetoksi-4(20),11 taxadiena (20), taxuspine F (21), baccatin IV (22), 20-deacetyltaxachitriene A (23), taxinine M (24), 7-epi- 10-deasetiltaksol (25) dan baccatin III (26) Struktur taxane yang terisolasi diitetapkan berdasarkan analisis spektral, terutama MS serta 1-dan 2D NMR.
Struktur kimia senyawa Tasumatrol H dapat dilihat pada Gambar 5.
(11)
Gambar 5. Struktur tasumatrol H (Shen et al., 2002) Tabel 1. Senyawa dalam Daun Taxus sumatrana
No Nama Senyawa No Nama Senyawa
1 Taxol 14 Tasumatrol K
2 Taxumariol Q 15 Tasumatrol L
3 13-O-asetil walifoliol 16 10-deasetil-13-oxobaccatin III 4 Taxuspin F 17 10-deasetilbakatin III
5 Wallifoliol 18 Taxacin
6 9,13-diacetiltaxumairol W 19 Yunnanxana
7 10,13-dibenzoiltaxacustin 20 5α-hidroksi-2α,7β,9α,10β,13α- tetraasetoksi-4(20),11 taxadiena 8 7,13-diacetilwallifoliol 21 Taxuspine F
9 7,13 dibenzoilwallifoliol 22 Baccatin IV
10 7,9-dibenzoiltaxumairol P 23 20-deacetyltaxachitriene A
11 Tasumatrol H 24 Taxinine M
12 Tasumatrol I 25 7-epi-10-deasetiltaksol
13 Tasumatrol J 26 Baccatin III
(Shen et al., 2002; Shen et al., 2005)
Tabel 1 memperlihatkan secara ringkas beberapa senyawa yang telah ditemukan dari daun Taxus sumatrana menggunakan ekstraksi pelarut aseton dan etil asetat yang dilakukan oleh (Shen et al., 2002; Shen et al., 2005).
2.3 Ekstraksi
Ekstraksi merupakan proses pemisahan satu atau lebih senyawa atau bahan dari campurannya baik cair maupun padatan dengan menggunakan pelarut yang sesuai. Proses ekstraksi dihentikan ketika tercapai kesetimbangan antara konsentrasi senyawa dalam pelarut dengan konsentrasi dalam sel tanaman (Mukhriani, 2014). Setelah proses ekstraksi, pelarut dipisahkan dari sampel dengan penyaringan. Pemilihan metode ekstraksi tergantung pada sifat bahan dan senyawa yang akan diisolasi.
Proses ekstraksi khususnya untuk bahan yang berasal dari tumbuhan adalah sebagai berikut : Pengelompokan bagian tumbuhan (daun, bunga dan lain- lain), pengeringan dan penggilingan bagian tumbuhan; pemilihan pelarut; pelarut polar: air, etanol, metanol, dan sebagainya; pelarut semipolar: etil asetat, diklorometan, dan sebagainya; pelarut nonpolar: n-heksan, petroleum eter, kloroform, dan sebagainya (Sarker et al., 2007).
2.4 Thin Layer Chromatography (TLC)
Thin layer chromatography (TLC) menggunakan pelat kaca tipis yang dilapisi dengan aluminium oksida atau silika gel sebagai fasa padat. Fase gerak adalah pelarut yang dipilih sesuai dengan sifat komponen dalam campuran.
Prinsip TLC adalah distribusi senyawa antara fasa padat (lapisan tipis) yang
diaplikasikan pada gelas atau pelat plastik dan fasa gerak cair yang bergerak di atas fasa padat. Sejumlah kecil senyawa atau campuran diaplikasikan ke titik awal tepat di atas dasar pelat TLC (Belle et al., 2011).
Thin layer chromatography (TLC) adalah proses pemisahan campuran senyawa berdasarkan perbedaan dua fase, yaitu fase diam (silika gel atau alumina) dan fase gerak (pelarut). Proses isolasi terjadi berdasarkan perbedaan daya serap dan daya partisi serta kelarutan dari komponen-komponen kimia yang akan bergerak mengikuti kepolaran eluen. Oleh karena daya serap adsorben terhadap komponen kimia tidak sama, maka komponen bergerak dengan kecepatan yang berbeda sehingga hal inilah yang menyebabkan pemisahan (Clark, 2007).
Pelat dimasukkan ke dalam chamber yang telah berisi pelarut tepat di bawah tingkat di mana sampel diaplikasikan. Pelarut bergerak melalui gaya kapiler dan bergerak naik ke atas campuran, masing-masing senyawa tetap berada dalam fase padat atau larut dalam pelarut dan naik ke atas pelat. Senyawa tersebut bergerak ke atas pelat atau tetap berada di bawah tergantung pada sifat fisik senyawa tersebut dan karenanya bergantung pada struktur molekulernya. Semakin mirip sifat fisik senyawa dengan fase gerak, semakin lama akan tinggal di fase gerak. Fase gerak akan membawa senyawa terlarut ke atas pelat TLC. Senyawa yang kurang larut dalam fase gerak dan memiliki afinitas yang lebih tinggi terhadap partikel pada pelat TLC akan tetap tertinggal (Kumar et al., 2013).
Senyawa dalam TLC ditandai oleh suatu kuantitas dikenal sebagai Rƒ dan dinyatakan sebagai pecahan desimal. Rƒ dihitung dengan membagi jarak yang ditempuh dari posisi semula dengan jarak pelarut yang dilewati dari posisi semula (pelarut yang naik) (Belle et al., 2011).
Rƒ = 𝐽𝑎𝑟𝑎𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑡𝑒𝑚𝑝𝑢ℎ 𝑜𝑙𝑒ℎ 𝑧𝑎𝑡 𝑦𝑎𝑛𝑔 𝑑𝑖𝑡𝑒𝑙𝑖𝑡𝑖 𝐽𝑎𝑟𝑎𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑡𝑒𝑚𝑝𝑢ℎ 𝑜𝑙𝑒ℎ 𝑝𝑒𝑙𝑎𝑟𝑢𝑡
2.5 Ekstraksi Subkritik HFC-134a
Hydroflourocarbons (HFCs) adalah molekul yang hanya mengandung atom hidrogen, fluorin dan karbon. Di industri otomotif, HFC-I34a telah digunakan dalam sistem pendingin udara di kendaraan, dan pada saat bersamaan juga telah diaplikasikan sebagai bahan bakar aerosol. Sebenarnya, HFC-134a disetujui untuk penggunaan makanan di Eropa, di sistem regulator dan berbagai macam ekstrak HFC-134a disetujui di Jepang. Selain itu, Ineos Fluor telah memperoleh penegasan secara umum yang dianggap aman generally recognize as safe (GRAS) untuk penggunaan HFC-134a dalam makanan di Amerika Serikat (Corr, 2002).
HFC-134a (1,1,1,2-tetrafluoroetana) tidak beracun, tidak reaktif, tidak mudah terbakar. HFC-134a adalah cairan halogen yang tidak mudah terbakar, stabil terhadap asam dan basa, mudah larut dalam air pada 200C. HFC-134a berbentuk gas pada suhu kamar dan tekanan normal dengan titik didih 247 K (Mustapa et al., 2004).
HFC-134a telah ditemukan sebagai pelarut untuk mengekstrak berbagai bahan alam. Produk itu dapat diekstrak termasuk rasa alami dan wewangian.
Ekstrak yang diperoleh dengan menggunakan HFC-134a umumnya rendah warnanya dan kandungan lipida rendah. Ekstraksi bisa dilakukan di manapun dalam bentuk cairan HFC-134a namun umumnya dilakukan sekitar suhu kamar yaitu di 25-32°C (Corr, 2002). Karena volatilitas HFC-134a yang tinggi, meminimalkan hilangnya komponen dari ekstrak mudah menguap residu pelarut
yang minimal dalam produk yang terisolasi. Meski cairan superkritik menawarkan kemampuan untuk selektivitas pelarut, namun memerlukan kontrol suhu dan tekanan untuk menghasilkan produk dalam pemrosesan dengan menjadi cairan jenuh, HFC-134a hanya membutuhkan kontrol suhu atau tekanannya untuk mengendalikan kondisi ekstraksi atau isolasi produk. Ini memungkinkan proses kontrol yang jauh lebih sederhana (Corr, 2002).
Dalam perspektif ekonomi, pelarut HFC-l34a nampaknya lebih menjanjikan, tekanan ekstraksi yang digunakan jauh lebih rendah daripada CO2
dan dengan demikian biaya modal menggunakan HFC-l34a jauh lebih rendah daripada CO2, walaupun selektivitas lipid (squalene) jauh lebih rendah daripada SC-CO2 (Simoes et al., 2002).
2.6 Metode Penentuan Struktur Kimia
Pada abad 20, penentuan struktur senyawa organik didasarkan atas perbandingan dengan senyawa yang strukturnya telah diketahui sebelum dikenalkan teknik spektroskopi. Bila semua sifat fisik dan kimia senyawa identik dengan senyawa yang telah dideskripsikan di literatur, dapat disimpulkan bahwa senyawa yang sedang dipelajari identik dengan senyawa yang strukturnya telah diketahui. Kriteria ini masih diadopsi hingga kini walaupun perbandingan yang dilakukan mungkin berbeda (Takeuchi, 2006).
Bila sifat fisik dan kimia senyawa yang diselidiki tidak tepat dengan senyawa apapun yang sudah dikenal di literatur, besar kemungkinan senyawa ini adalah senyawa baru, belum pernah disintesis atau belum pernah dilaporkan.
Sehingga muuncul masalah baru untuk mengetahui senyawa apakah yang
ditemukan. Metoda penentuan struktur berubah drastis pada pertengahan abad 20.
Metoda tradisional, walaupun sederhana, sangat memakan waktu dan sukar dalam praktek, jadi, pertama struktur senyawa yang baru disintesis diasumsikan, kemudian suatu rute tertentu didesain untuk mengubah senyawa ini menjadi senyawa yang telah diketahui. Pengubahan itu mungkin memerlukan beberapa tahap. Sepanjang perubahan struktur yang disebabkan oleh tiap tahap teridentifikasi, pengubahan yang berhasil sampai senyawa yang diketahui merupakan bukti struktur yang diasumsikan. Harus ditambahkan bahwa reaksi untuk pengubahan ini dipilih dari reaksi yang hanya melibatkan gugus fungsi dan bukan kerangka molekulnya. Kini penentuan struktur terutama dilakukan dengan metoda spektroskopik dan difraksi. Berikut ini beberapa metoda penentuan struktur kimia (Takeuchi, 2006).
2.6.1 Fourier Transform Infra Red (FTIR)
Fourier transform infra red (FTIR) merupakan suatu metode analisis yang dipakai untuk analisis gugus fungsi, pengenalan senyawa, dan analisa campuran.
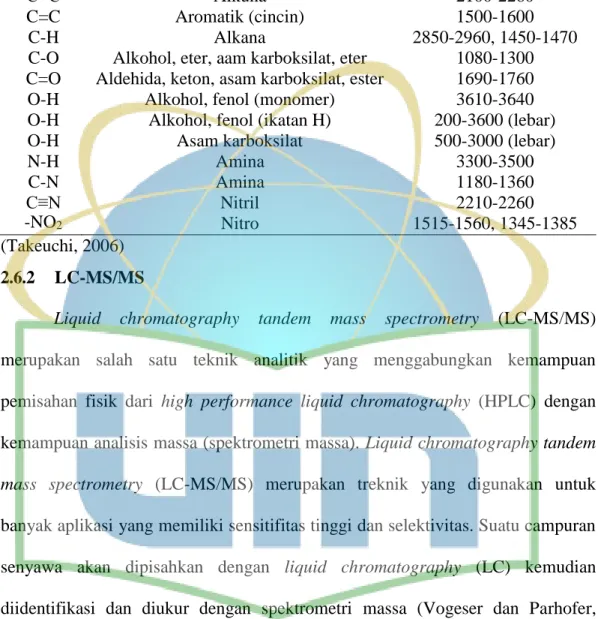
Penemuan gugus fungsional diperoleh berdasarkan bilangan gelombang yang dibutuhkan untuk suatu molekul bervibrasi pada suatu ikatan baik berupa rentangan (streaching) maupun berupa bengkokan (bending) dimana setiap ikatan mempunyai bilangan gelombang yang spesifik sehingga setiap molekul mempunyai spektra infra merah yang spesifik atau sidik jari (fingerprint) tertentu (Ibrahim et al., 2013). Tabel 2 menunjukkan serapan khas beberapa senyawa :
Tabel 2. Serapan khas beberapa gugus
Gugus Jenis Senyawa Daerah Serapan (cm-1)
C-H Alkana 2850-2960, 1350-1470
C-H Alkena 3020-3080, 675-1000
C-H Aromatik 3000-3100, 675-870
C-H Alkuna 3300
C=C Alkena 1640-1680
C≡C Alkuna 2100-2260
C=C Aromatik (cincin) 1500-1600
C-H Alkana 2850-2960, 1450-1470
C-O Alkohol, eter, aam karboksilat, eter 1080-1300 C=O Aldehida, keton, asam karboksilat, ester 1690-1760
O-H Alkohol, fenol (monomer) 3610-3640
O-H Alkohol, fenol (ikatan H) 200-3600 (lebar)
O-H Asam karboksilat 500-3000 (lebar)
N-H Amina 3300-3500
C-N Amina 1180-1360
C≡N Nitril 2210-2260
-NO2 Nitro 1515-1560, 1345-1385
(Takeuchi, 2006) 2.6.2 LC-MS/MS
Liquid chromatography tandem mass spectrometry (LC-MS/MS) merupakan salah satu teknik analitik yang menggabungkan kemampuan pemisahan fisik dari high performance liquid chromatography (HPLC) dengan kemampuan analisis massa (spektrometri massa). Liquid chromatography tandem mass spectrometry (LC-MS/MS) merupakan treknik yang digunakan untuk banyak aplikasi yang memiliki sensitifitas tinggi dan selektivitas. Suatu campuran senyawa akan dipisahkan dengan liquid chromatography (LC) kemudian diidentifikasi dan diukur dengan spektrometri massa (Vogeser dan Parhofer, 2007).
Kromatografi adalah suatu teknik pemisahan campuran berdasarkan perbedaan kecepatan perambatan komponen dalam medium tertentu. Pada kromatografi, komponen-komponen akan dipisahkan antara dua buah fase yaitu fase diam dan fase gerak. Fase diam akan menahan komponen campuran
sedangkan fase gerak akan melarutkan zat komponen campuran. Komponen yang mudah tertahan pada fase diam akan tertinggal. Sedangkan komponen yang mudah larut dalam fase gerak akan bergerak lebih cepat. Prinsip kerja HPLC yaitu pemisahan komponen-komponen sampel dengan cara melewatkan sampel pada suatu kolom, yang selanjutnya dilakukan pengukuran kadar masing-masing komponen-komponen tersebut dengan suatu detektor (Vogeser dan Parhofer, 2007).
Mass spectrometer (MS) adalah instrumen yang menyusun molekul gas (ion) berdasarkan massanya. Ada beberapa jenis masss pectrometer, tetapi semuanya harus memiliki komponen yang berfungsi mengionisasi sampel.
Penghubung (interface) antara kromatografi cair dan spektrometri massa merupakan bagian yang sangat vital. Alat penghubung (interface) mengggunakan teknik atmospheric pressure ionization (API) (Vogeser dan Parhofer, 2007).
2.6.3 Spektroskopi 1H NMR dan 13C NMR
Spektrometri nuclear magnetic resonance (NMR) atau resonansi magnetik inti merupakan metode yang sering dipakai dalam mempelajari struktur molekul.
Untuk melengkapi bagian-bagian lain dari suatu molekul organik yang tidak diketahui (unknown) dapat digunakan NMR yang memberikan informasi yang berguna dalam penentuan struktur yaitu NMR 1 dimensi terdiri dari NMR proton (1H), NMR karbon (13C), Distortionless enhancement by polarization transfer (DEPT). Prinsip NMR proton adalah inti atom hidrogen mempunyai sifat-sifat magnet, bila suatu senyawa mengandung hidrogen diletakkan dalam bidang magnet yang sangat kuat dan diradiasi menggunakan radiasi elektromagnetik maka inti atom hidrogen dari senyawa tersebut akan menyerap energi melalui
suatu proses absorpsi yang dikenal dengan resonansi magnet (Silverstein et al., 2014).
Spektrum 1H-NMR dapat memberikan informasi seperti adanya gugus- gugus fungsi yang dinyatakan dalam bentuk khas seperti jumlah dan posisi gugus fungsi (ortho, meta, para) dengan melihat nilai pergeseran kimia (δ) dan konstanta koplingnya (J), jumlah proton dapat dilihat dari hasil integrasinya, dan dapat menentukan bentuk konformasinya seperti cis atau trans, axial atau equatorial.
Untuk senyawa yang sudah diketahui, dapat dengan mudah dikonfirmasi struktur molekulnya tanpa adanya senyawa pembanding (standard). Pengukuran spektrum
13C-NMR dan DEPT dapat memberikan jenis karbon primer, sekunder, tersier dan kuartener (CH3, CH2, CH, C, O-C, C=O, H-C=O, -CONH, -COOH dan –COOR) dengan melihat nilai pergeseran kimianya (Jenie et al., 2014).
Spektroskopi NMR proton memberikan informasi mengenai atom-atom hidrogen dalam molekul organik. Beberapa hal yang perlu diperhatikan dalam mengintepretasikan spektrum 1H NMR adalah luas puncak (peak area) yang menunjukkan jumlah inti 1H pada puncak tersebut, pemecahan puncak (splitting) yang menjelaskan lingkungan dari sebuah proton dengan proton tetangganya, serta geseran kimia (chemical shift) yang menunjukkan jenis proton tersebut.
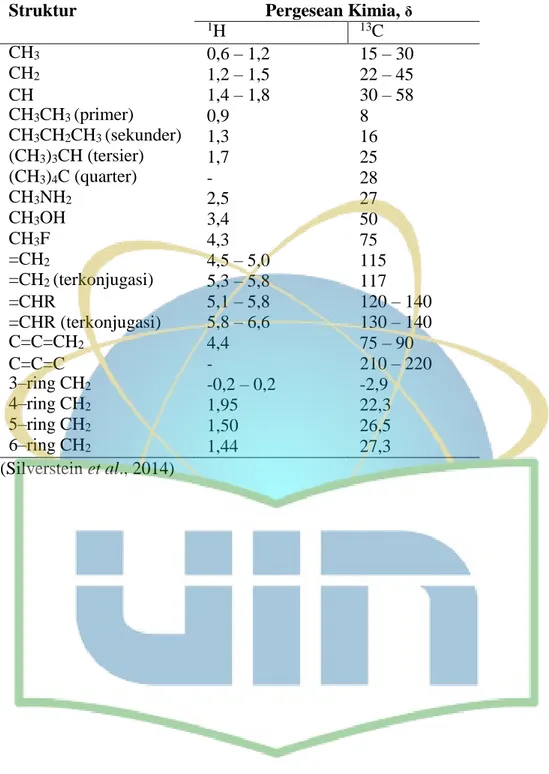
Spektrum 1H NMR biasanya diperoleh dengan cara sampel senyawa yang akan dianalisis dilarutkan dalam pelarut inert yang tidak memiliki inti 1H. Sebagai contoh CCl4 atau pelarut dengan hidrogen yang digantikan oleh deuterium, seperti CDCl3 (deuteri kloroform) dan CD3COCD3 (heksa-deuterioaseton) (Hart et al., 2003). Nilai berbagai pergeseran kimia 1H NMR dan 13C NMR ditampilkan pada Tabel 3.
Tabel 3. Pergeseran kimia 1H NMR dan 13C NMR
Struktur Pergesean Kimia, δ
1H 13C
CH3 0,6 – 1,2 15 – 30
CH2 1,2 – 1,5 22 – 45
CH 1,4 – 1,8 30 – 58
CH3CH3 (primer) 0,9 8
CH3CH2CH3 (sekunder) 1,3 16
(CH3)3CH (tersier) 1,7 25
(CH3)4C (quarter) - 28
CH3NH2 2,5 27
CH3OH 3,4 50
CH3F 4,3 75
=CH2 4,5 – 5,0 115
=CH2 (terkonjugasi) 5,3 – 5,8 117
=CHR 5,1 – 5,8 120 – 140
=CHR (terkonjugasi) 5,8 – 6,6 130 – 140
C=C=CH2 4,4 75 – 90
C=C=C - 210 – 220
3–ring CH2 -0,2 – 0,2 -2,9
4–ring CH2 1,95 22,3
5–ring CH2 1,50 26,5
6–ring CH2 1,44 27,3
(Silverstein et al., 2014)
BAB III
METODE PENELITIAN
3.1 Waktu dan Tempat Pelaksanaan
Penelitian ini dilaksanakan dari bulan Januari 2018 sampai dengan Februari 2019 dan dilaksanakan di Laboratorium Kimia Bahan Alam, Pusat Penelitian Kimia, Lembaga Ilmu Pengetahuan Indonesia (LIPI) kompleks PUSPIPTEK Serpong, Tangerang Selatan.
3.2 Alat dan Bahan 3.2.1 Alat
Alat yang digunakan untuk penelitian ini antara lain ekstraktor HFC- 134a,timbangan analitik KERN, TLC silica gel 60 F254, LC-MS/MSXevo G2-XS QTOF, FTIR Shimadzu dan NMR Jeol 500 MHz.
3.2.2 Bahan
Bahan yang digunakan untuk penelitian ini antara lain tanaman Taxus sumatrana dari Hutan Sibuaton, Sumatra Utara, metanol, heksan, etil asetat, HFC- 134a, asam sulfat, kloroform, diklorometan (DCM), aseton, kromtografi lapis tipis (KLT) menggunakan alumunium berlapis Si-gel Kiesegel 60 F254 0,25 mm (Merck).
23
Tanaman Taxus sumatrana
Daun
Dihaluskan
Serbuk ditimbang masing-masing 250 gram sebanyak 7 batch
1 250g
2 250g
3 250g
4 250g
5 250g
6 250g
7 250g
Kromatgrafi kolom gravitasi Ekstraksi HFC -134a - 3 siklus @ 1 jam
F8
LCMS/MS, FTIR, NMR TLC
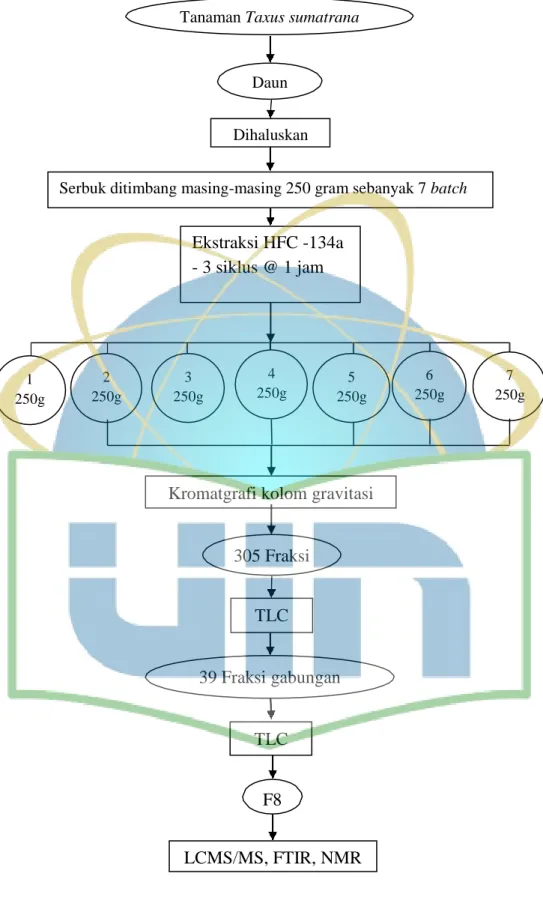
3.3 Diagram Alir Penelitian
Gambar 6. Diagram alir penelitian 305 Fraksi
TLC
39 Fraksi gabungan
3.4 Prosedur Kerja 3.4.1 Preparasi Sampel
Sampel daun Taxus sumatrana dipisahkan antra daun dan rantingnya kemudian diperoleh berat daun sebesar 1,8 kg. Daun yang telah dipisahkan tersebut dikeringkan menggunakan oven dengan suhu 50oC dan diblender atau digiling hingga menjadi serbuk dan ditimbang sebanyak 250 gram sebanyak 7 batch.
3.4.2 Ekstraksi Daun Taxus sumatrana dengan Ekstraksi Subkritik HFC- 134a (Lelono et al., 2018)
Sampel daun 250 gram diekstraksi dengan menggunakan ekstraktor HFC- 134a. Sampel yang diekstraksi sebanyak 7 batch, dengan masing-masing batch dilakukan ekstraksi sebanyak 3 siklus, total sampel yang diekstraksi sebanyak 1750 gram. HFC-134a yang dialirkan sebanyak 2500 gram tiap siklus yaitu dengan perbandingan serbuk dengan HFC-134a adalah 1:10. Suhu dan tekanan saat proses dalam ekstraktor dicatat. Kemudian ekstrak hasil menggunakan HFC- 134a dilarutkan dengan metanol. Skema alat ekstraktor HFC-134a dapat dilihat pada Gambar 7.
Gambar 7. Skema alat ekstraktor HFC-134a (Lelono et al., 2018) Skema diagram alat menjelaskan secara tertulis alat tersebut terdiri dari beberapa unit, yaitu 2 buah unit ekstraktor, 1 buah unit kolektor dan 1 buah unit filter, double heater, chiller serta 1 buah kompresor dan pompa. Gas freon akan dipompakan ke dalam valve dimana gas mengalir satu arah ke depan dan tidak bisa balik lagi. Gas dipompa ke dalam unit ekstraktor yang sudah berisi simplisia, bereaksi di dalamnya, setelah itu dipompakan ke suatu sistem dimana gas juga hanya bisa mengalir satu arah dan masuk ke dalam unit kolektor. Di dalam unit kolektor freon cair bersama ekstrak akan berubah fase menjadi gas masuk ke dalam kolektor dipanaskan dengan double heater berubah menjadi gas dan filtrat akan tertahan di dalam unit kolektor.
3.4.3 Kromatografi Kolom Gravitasi (Aksara et al., 2013)
Kromatografi kolom gravitasi digunakan untuk melakukan pemisahan fraksi daun. Silika gel G 60 dilarutkan dalam pelarut n-heksana kemudian dimasukkan ke dalam kolom dengan diameter kolom dan tinggi silika disesuaikan dengan massa sampel sehingga diperoleh bubur. Bubur silika dimasukkan ke dalam kolom setinggi 2/3 dari panjang kolom. Kemudian sampel sebanyak 2,4106 gram dilarutkan dalam metanol dan diimpregnasi dengan silika gel G 60 dengan perbandingan massa 1:1 (sampel : silika). Selanjutnya sampel dimasukkan ke dalam kolom dan dielusi menggunakan pelarut heksan dan etil asetat. Hasil pemisahan berupa fraksi ditampung dalam botol vial. Kemudian hasil pemisahan dianalisis dengan kromatografi lapis tipis untuk melihat pola noda yang sama untuk digabungkan. Hasil kromatografi kolom yanng memiliki noda yang sama dikumpulkan sehingga diperoleh fraksi-fraksi utama.
3.4.4 TLC (Marliana et al., 2005)
Masing-masing ekstrak hasil ekstraksi menggunakan HFC-134a yang telah dielusi melalui kromatografi kolom gravitasi kemudian dilihat pola noda pemisahannya melalui TLC dengan eluen heksan dan etil asetat. Masing-masing fraksi ditotolkan pada plat silika gel 254. Elusi dilakukan dengan heksan : etil asetat dengan perbandingan (8:2). Plat dikeringkan dan diamati pada cahaya tampak UV (ultraviolet) dengan panjang gelombang 254 nm dan 366 nm lalu disemprotkan dengan asam sulfat 5%.
3.4.5 Penentuan Struktur Kimia
3.4.5.1 LC-MS/MS (Stachniuk et al., 2017)
Fraksi daun Taxus sumatrana hasil kromatografi kolom gravitasi dianalisis menggunakan menggunakan LCMS Xevo G2-XS QTOF untuk mengetahui komponen senyawa yang terdapat pada ekstrak tersebut. Berdasarkan metode yang dilakukan oleh Stachniuk et al. (2017) kolom analisis Zorbax Plus C18 dengan fase gerak amonium format dan asam format dalam metanol dengan volume injeksi 5 ml dengan kecepatan alir 0,2 mL/menit. Analisis kromatogram dan spektrofotometer massa menggunakan software Norman Mass Bank.
3.4.5.2 FTIR (Widowati et al., 2003)
Analisa spektroskopi infra merah dilakukan dengan menggunakan peralatan spektrofotometer IR Shimadzu. Lebih kurang 1 mg sampel digerus dengan 200 mg kalium bromida yang telah dikeringkan sampai homogen. Campuran dimasukkan ke dalam cetakan, diratakan dan dikompresi. Kemudian dianalisis pada bilangan gelombang 4000 cm-1 sampai 600 cm-1.
3.4.5.3 Analisis dengan Spektroskopi NMR (Tamaela et al., 2014)
Fraksi 8 yang diperoleh diambil sebanyak 15 mg dan dilarutkan dalam 0,5 mL pelarut bebas proton yaitu (CDCl3) yang dapat melarutkan dengan sempurna.
Larutan sampel dimasukkan dalam tabung injeksi kemudian diletakkan dalam alat NMR untuk mengukur 1H NMR pada 500 MHz dan 13C NMR pada 125 MHz.
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Ekstraksi HFC-134a
Ekstraksi merupakan langkah pertama yang penting dalam menganalisis tanaman. Preparasi bahan seperti pengeringan bahan tanaman dan penggilingan untuk mendapatkan sampel yang homogen dilakukan untuk mempermudah proses ekstraksi dan juga meningkatkan kontak permukaan sampel dengan sistem pelarut (Fabricant & Franswort, 2001). Metode ekstraksi tradisional yang digunakan untuk memperoleh produk atau senyawa dalam bahan alam ini memiliki beberapa kelemahan yaitu memakan waktu, tenaga, memiliki selektivitas rendah dan / atau hasil ekstraksi rendah. Saat ini metode ekstraksi yang sedang dipelajari yaitu di antaranya ekstraksi cairan superkritis atau Supercritical Fluid Extraction (SFE) dan subkritis atau Subcritical Water Extraction (SWE). Teknik ekstraksi ini memberikan selektivitas yang lebih tinggi dan waktu ekstraksi yang lebih pendek (King, 2000).
Ekstraksi yang digunakan dalam penelitian ini adalah menggunakan sistem subkritik HFC-134a, teknik ini dapat memberikan hasil ekstraksi yang lebih tinggi, pada teknik ini menggunakan tekanan di bawah tekanan tinggi biasanya dari 10 hingga 60 bar (Herrero et al., 2006). Ekstraksi dengan HFC-134a memberikan ekstrak yang lebih spesifik (tidak terlalu banyak pengotor) bila dibandingkan dengan pelarut heksan dan metanol. Prosesnya yang ekonomis dan memiliki dampak lingkungan yang rendah dengan perhatian utama adalah kebutuhan akan persediaan pelarut (Lapkin et al., 2006). Hidrofluorokarbon
29
adalah gas dalam kondisi normal dan dicairkan pada tekanan yang relatif rendah.
Karena tekanan sederhana dan suhu operasi yang rendah, maka biaya energi dan biaya operasinya juga rendah.
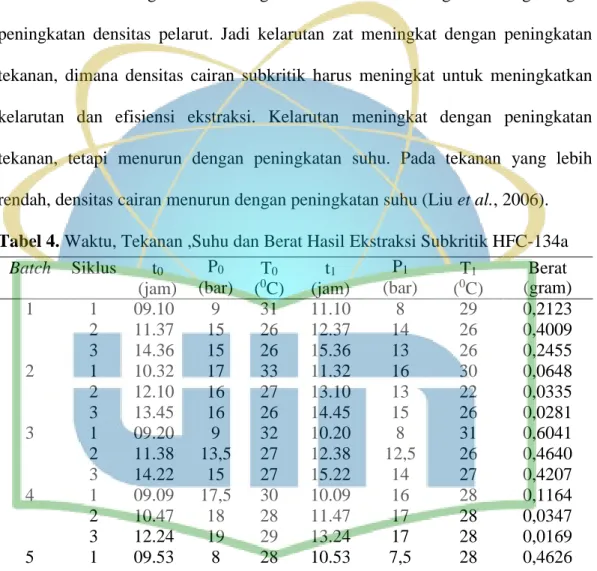
Tekanan adalah faktor utama pada densitas cairan subkritik, ketika tekanan lebih tinggi densitas cairan subkritik lebih besar. Kelarutan zat terlarut dalam cairan subkritik sangat terkait dengan densitas dan meningkat seiring dengan peningkatan densitas pelarut. Jadi kelarutan zat meningkat dengan peningkatan tekanan, dimana densitas cairan subkritik harus meningkat untuk meningkatkan kelarutan dan efisiensi ekstraksi. Kelarutan meningkat dengan peningkatan tekanan, tetapi menurun dengan peningkatan suhu. Pada tekanan yang lebih rendah, densitas cairan menurun dengan peningkatan suhu (Liu et al., 2006).
Tabel 4. Waktu, Tekanan ,Suhu dan Berat Hasil Ekstraksi Subkritik HFC-134a Batch Siklus t0
(jam) P0
(bar) T0
(0C) t1
(jam)
P1
(bar)
T1
(0C)
Berat (gram)
1 1 09.10 9 31 11.10 8 29 0,2123
2 11.37 15 26 12.37 14 26 0,4009
3 14.36 15 26 15.36 13 26 0,2455
2 1 10.32 17 33 11.32 16 30 0,0648
2 12.10 16 27 13.10 13 22 0,0335
3 13.45 16 26 14.45 15 26 0,0281
3 1 09.20 9 32 10.20 8 31 0,6041
2 11.38 13,5 27 12.38 12,5 26 0,4640
3 14.22 15 27 15.22 14 27 0,4207
4 1 09.09 17,5 30 10.09 16 28 0,1164
2 10.47 18 28 11.47 17 28 0,0347
3 12.24 19 29 13.24 17 28 0,0169
5 1 09.53 8 28 10.53 7,5 28 0,4626
2 12.06 15,5 28 13.06 13 23 0,2721
3 14.09 17,5 27 15.09 16 27 0,3488
6 1 10.19 17,5 32 11.19 15,5 29 0,0400
2 11.51 17 29 12.51 14 22 0,0321
3 13.40 17 26 14.40 25 27 0,0103
7 1 09.30 10 32 10.30 9 30 0,2020
2 11.36 14 28 12.36 3 27 0,4348
3 13.30 6 27 14.30 16 28 0,3135
Total 4,7581
Pada Tabel 4, disajikan kondisi suhu dan tekanan saat ekstraksi serta berat ekstrak pada ke-7 batch masing-masing 3 siklus dengan waktu 1 jam setiap siklusnya. Berat ekstrak yang didapatkan sebanyak 4,7581 gram dari 1.750 gram simplisia sehingga diperoleh rendemen sebesar 0,2719%. Suhu dan tekanan dalam sistem ekstraktor tidak dapat diubah, melainkan sudah diatur dalam sistem. HFC- 134a digunakan sebagai pelarut subkritik karena memiliki volatilitas tinggi dan titik didih 26,20C pada tekanan atmosfer (Babu et al., 2014). Ketika gas dipompakan dengan tekanan dan suhu tertentu maka akan cair sehingga dapat mengekstraksi bahan.
Ekstraksi daun Taxus sumatrana dalam penelitian ini menggunakan HFC- 134a sebagai pelarut serta sistem ekstraktor yang terdiri dari kompresor, kolektor, water chiller, pompa dan kondensor. Kompresor berfungsi mengalirkan refrigeran ke seluruh sistem pendingin. Sistem kerjanya adalah dengan mengubah tekanan dari yang bertekanan rendah ke sisi yang bertekanan tinggi. Ketika kompresor bekerja, refrigeran yang dihisap dari evaporator dengan suhu dan tekanan rendah dimampatkan, sehingga suhu dan tekanannya naik. Gas yang dimampatkan ini ditekan keluar dari kompresor lalu dialirkan ke kondensor. Kondensor merupakan suatu alat sebagai kondensasi refrigeran, berfungsi untuk membuang kalor yang diserap dari evaporator dan panas yang diperoleh dari kompresor, serta mengubah wujud gas menjadi cair (Widagdo, 2010).
Evaporator merupakan komponen pada sistem pendingin yang berfungsi sebagai penukar kalor dan menguapkan refrigeran dalam sistem sebelum dihisap oleh kompresor. HFC-134a mengalami perubahan fase dari gas menjadi cair, pada saat berubah menjadi fase cair, maka dapat mengekstrak bahan alam dalam sistem
ekstraktor. Kemudian fase cair dari HFC-134a berubah kembali menjadi fase gas setelah mengesktraksi bahan alam dengan membawa dan meninggalkan ekstrak pada kolektor. Perubahan fase pada evaporator terjadi karena suhu lingkungan lebih tinggi dari pada suhu evaporator. Water chiller juga merupakan mesin refrigerasi, dimana suhu dingin evaporator digunakan untuk mendinginkan air yang kemudian air ini disirkulasi untuk mendinginkan komponen-komponen sistem yang lain (Cholil, 2015).
Water chiller digunakan untuk memampatkan fluida (refrigeran).
Refrigeran merupakan jenis zat yang mudah diubah wujudnya dari gas menjadi cair atau sebaliknya. Cairan refrigeran dipompa dengan kompresor dan akan menjadi uap basah dengan tekanan dan suhu rendah kemudian mengalir ke evaporator. Refrigeran uap basah yang mengalir di evaporator mengambil panas dari udara di dalam ruangan pada permukaan evaporator. Refrigeran diuapkan kemudian dikirim ke kondensor dengan tekanan dan suhu tinggi, di dalam kondensor, gas refrigeran didinginkan dan akan menjadi cair lagi (Wibowo &
Subri, 2006).
Refrigeran cair ini dapat mengekstrak bahan alam yang terdapat dalam thimble (tempat sampel yang akan diekstraksi berupa tabung). Kemudian refrigeran cair ini dialirkan menuju kolektor dengan membawa ekstrak, lalu refrigeran cair akan diubah kembali menjadi gas untuk dibuang ke lingkungan.
Karena HFC (hydrofluorocarbon) tidak mempunyai unsur klor sehingga tidak merusak lapisan ozon.
Sehingga ekstrak yang akan dimasukan ke dalam kromatografi kolom gravitasi hanya pada batch 2, 4, 5, 6 dan batch 7, hal ini karena pada batch 1 dan
3 terjadi kesalahan dalam proses ektraksi, yaitu terjadi kebocoran pada tabung sampel (thimble) akibat kesalahan dalam teknis ketika memasukan serbuk ke dalam thimble, sehingga sampel masuk melalui evaporator dan terbawa oleh ekstrak yang menyebabkan ekstrak tercampur oleh sampel yang dapat dilihat pada Tabel 5.
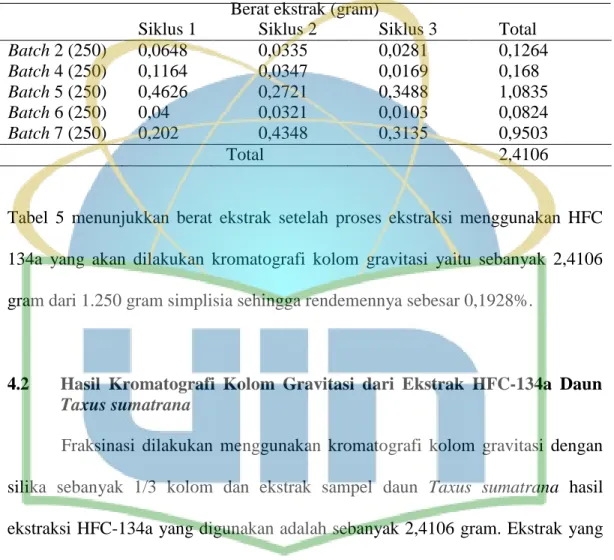
Tabel 5. Berat ekstrak pada batch 2, 4, 5, 6 dan batch 7 Berat ekstrak (gram)
Siklus 1 Siklus 2 Siklus 3 Total
Batch 2 (250) 0,0648 0,0335 0,0281 0,1264
Batch 4 (250) 0,1164 0,0347 0,0169 0,168
Batch 5 (250) 0,4626 0,2721 0,3488 1,0835
Batch 6 (250) 0,04 0,0321 0,0103 0,0824
Batch 7 (250) 0,202 0,4348 0,3135 0,9503
Total 2,4106
Tabel 5 menunjukkan berat ekstrak setelah proses ekstraksi menggunakan HFC 134a yang akan dilakukan kromatografi kolom gravitasi yaitu sebanyak 2,4106 gram dari 1.250 gram simplisia sehingga rendemennya sebesar 0,1928%.
4.2 Hasil Kromatografi Kolom Gravitasi dari Ekstrak HFC-134a Daun Taxus sumatrana
Fraksinasi dilakukan menggunakan kromatografi kolom gravitasi dengan silika sebanyak 1/3 kolom dan ekstrak sampel daun Taxus sumatrana hasil ekstraksi HFC-134a yang digunakan adalah sebanyak 2,4106 gram. Ekstrak yang digunakan hanya batch 2, 4, 5, 6 dan 7. Eluen yang digunakan adalah heksan dan etil asetat dengan berbagai perbandingan yaitu 10:0; 9:1; 8:2; 6:4; 5:5 dan 3:7 dengan masing-masing perbandingan yang digunakan sebanyak 500 sampai 1500 ml. Perbandingan eluen pada kolom dilakukan untuk memisahkan senyawa- senyawa sesuai dengan tingkat kepolarannya. Prinsip kerjanya adalah didasarkan
pada perbedaan afinitas absorbsi komponen-komponen campuran terhadap permukaan fase diam. Sampel yang memiliki afinitas besar terhadap absorben akan selektif tertahan dan yang afinitasnya paling kecil akan mengikuti aliran pelarut. Karena silika yang digunakan bersifat polar sehingga senyawa yang memiliki kepolaran yang tinggi akan tertahan di silika dan senyawa yang memiliki kepolaran yang lebih rendah serta senyawa yang nonpolar akan terelusi terlebih dahulu. Laju alir dari metode ini diperoleh dari gaya gravitasi. Fase gerak dimasukkan ke dalam kolom dengan cara dituangkan sedikit demi sedikit atau dialirkan dari bejana yang diletakkan di atas kolom sehingga fase gerak mengalir dengan sendirinya (Supriadin dan Kudus, 2017).
Elusi dihentikan jika sudah tidak ada lagi sampel yang dapat dibawa keluar lagi oleh fase gerak, bila digunakan elusi gradien sudah sampai pada fase gerak yang paling polar. Fraksi yang didapatkan sebanyak 305 fraksi dengan masing-masing fraksi yang ditampung sebanyak 8 ml. Fraksi-fraksi yang memiliki pola noda yang sama disatukan dalam satu fraksi dan didapatkan 39 fraksi. Fraksi- fraksi tersebut kemudian dikeringkan dan ditimbang bobotnya. Berikut ini berat masing-masing fraksi yang dapat dilihat pada Tabel 6.
Tabel 6. Berat fraksi hasil kromatografi kolom gravitasi
Fraksi Berat (g) Fraksi Berat (g)
F1 0.0017
F2 0.0831
F3 0.1121
F4 0.0449
F5 0.0553
F6 0.0293
F7 0.0175
F8 0.0597
F9 0.0538
F10 0.0258
F11 0.1344
F12 0.0188
F13 0.0298
F14 0.1639
F15 0.0986
F16 0.0109
F17 0.0118
F18 0.0574
F19 0.0090
F21 0.0062
F22 0.0158
F23 0.0096
F24 0.0037
F25 0.0060
F26 0.0111
F27 0.0051
F28 0.0038
F29 0.0073
F30 0.0032
F31 0.0398
F32 0.0027
F33 0.0020
F34 0.0063
F35 0.0016
F36 0.0026
F37 0.0051
F38 0.0025
F39 0.0104
F20 0.0154 Total 1,1780
Tabel 6 menunjukkan berat fraksi hasil kromatografi kolom gravitasi, didapatkan berat fraksi sebesar 1,1780 gram dari 2,4106 gram ekstrak yang dikolom. Masing-masing fraksi diidentifikasi dengan kromatografi lapis tipis (KLT) dengan menggunakan fase gerak yaitu n-heksana : etil asetat 8 : 2. Hal ini dilakukan agar menghasilkan pola pemisahan yang baik sesuai dengan kepolaran eluennya. Pola noda yang dihasilkan dilihat dengan menggunakan metode kromatografi lapis tipis (KLT) silika gel GF254.
Elusi yang dilakukan menggunakan fase gerak dengan gradien polaritas dari polaritas paling rendah sampai polaritas paling tinggi sehingga dapat memisahkan senyawa-senyawa yang memiliki polaritas yang berbeda. Dari hasil kromatografi kolom gravitasi dilihat pola nodanya melalui tahap kromatografi lapis tipis dengan tujuan mencari pelarut dan menganalisis fraksi yang sesuai