BAB II
TINJAUAN PUSTAKA
2.1. Aluminium
Aluminium adalah logam ringan yang cukup penting peranannya dalam
kehidupan manusia. Aluminium merupakan unsur kimia golongan IIIA dalam sistem
periodik unsur. Aluminium memiliki nomor atom 13 dan berat atom 26,9815 sma.
Dalam udara bebas aluminium mudah teroksidasi membentuk lapisan tipis oksida
yaitu Al2O3 yang tahan karat. Aluminium bersifat amfoter yang terkorosi dalam
larutan asam maupun basa, tetapi pada pH 4-8 bersifat stabil (Anton J Hartono,1992).
Di dalam dunia usaha logam, ada dua logam ringan yang digunakan secara
tersendiri : aluminium dan magnesium. Aluminium adalah logam yang paling banyak
digunakan setelah baja. Logam ini ditemukan pada tahun 1827 oleh seorang kimiawan
Jerman Friedrich Wohler. Aluminium umumnya ditemukan di atas bumi dalam bentuk
Bahan dasar terpenting untuk pembuatan aluminium ialah bauksit, Bauksit
ditemukan dalam bermacam-macam warna, antara lain putih, merah, kuning dan
lain-lain. Di Eropa, bauksit banyak ditemukan di Prancis Italia, Rusia dan Hongaria.
Bauksit juga banyak ditemukan di Afrika, Amerika, Asia, dan Australia. Melalui
proses elektrolisa diperoleh derajat kemurnian sebesar 99,8%. Dari aluminium murni
ini dihasilkan aluminium 99,998% melalui suatu elektrolisa khusus (elektrolisa tiga
lapis).
Beberapa sifat dari aluminium murni yaitu berat jenisnya rendah sekitar 2,7
kg/dm3, berwarna putih seperti perak, mengkilap, memiliki daya hantar panas listrik
yang baik, ketahanan karatnya tinggi. Aluminium menyelaputi diri di udara dengan
sebuah lapisan oksida (pelindung) yang tidak mudah dirusak. Aluminium tidak tahan
terhadap alkali dan asam. Karena kekerasannya rendah, aluminium kurang baik untuk
diubah bentuk dengan penyerpihan dan cederung untuk melumas. Untuk ini
diperlukan sudut serpih yang besar, kecepatan sayat yang tinggi dan bahan pelumas
yang cocok.
Aluminium sangat lunak dan mudah diregangkan sehingga mudah diubah
bentuk dalam keadaan dingin dan panas. Dengan penggilingan dapat dihasilkan
selaput setebal 0,004mm. Melalui pemartilan bahkan dapat dicapai ketebalan
0,0005mm. aluminium dapat disolder dan dilas begitu saja. Untuk ini diperlukan
Aluminium tidak beracun dan tidak magnetis, merupakan reflektor (pemantul
balik) yang baik untuk panas, cahaya dan gelombang-gelombang elektromagnetis. Di
dalam elektroteknik, disamping berbagai macam paduan aluminium dalam bentuk
lembaran, pipa, batang, benda tuangan, dan profil untuk bahan konstruksi dan
sambungan, aluminium dipakai pula dalam jumlah besar sebagai bahan penghantar
aluminium. Dalam bentuk tali baja-aluminium digunakan untuk transmisi tegangan
tinggi dengan pembebanan mekanis tertinggi. Kawat baja yang dilapis seng dan
dipersatukan secara kokoh dengan aluminium dapat menghasilkan penghantar arus
yang memiliki ketahanan yang tinggi.
2.1.1. Sejarah Aluminium
Aluminium adalah logam yang terbanyak di dunia. Logam 8 % dari bagian
pada kerak bumi. Boleh dikatakan setiap negara mempunyai persediaan bahan yang
mengandung aluminium, tetapi proses untuk mendapatkan aluminium logam dari
kebanyakan bahan itu masih belum ekonomis. Logam aluminium pertama kali dibuat
dalam bentuk murni oleh Oersted, pada tahun 1825, yang memanaskan ammonium
Pada tahun 1854, Henri Sainte-Claire Deville membuat aluminium dari
natrium-aluminium klorida dengan jalan memanaskan dengan logam natrium. Proses
ini beroperasi selama 35 tahun dan logamnya dijual dengan harga $ 220 per kilogram.
Pada tahun 1886 Charles Hall mulai memproduksi aluminium dengan skala besar
seperti sekarang, yaitu melalui elektrolisis alumina didalam kriolit (Na AlF ) lebur. Pada tahun itu pula, Paul Heroult mendapat hak paten dar Prancis untuk proses serupa
dengan proses Hall. Hingga pada tahun 1893, produksi aluminium menurut cara Hall
ini sudah sedemikian meningkat, sehingga harganya sudah jatuh menjadi $ 4,40 per
kilogram. Industri ini berkembang dengan baik, berdasarkan suatu pasaran yang sehat
dan berkembang atas dasar penelitian mengenai sifat-sifat aluminium dan cara-cara
pemakaian yang ekonomis bagi bahan itu (Austin, G.T., 1990).
2.1.2. Sifat-sifat Aluminium
Dalam tiga dasawarsa terakhir ini aluminium telah menjadi salah satu logam
industri yang paling luas penggunaannya di dunia. Aluminium banyak digunakan
didalam semua sektor utama industri seperti angkutan, konstruksi, listrik, peti kemas
dan kemasan, alat rumah tangga serta peralatan mekanis.
Penggunaan aluminium yang luas disebabkan aluminium memiliki sifat-sifat yang
a. Ringan : memiliki bobot sekitar 1/3 dari bobot besi dan baja, atau tembaga dan
karenanya banyak digunakan dalam industri transportasi seperti angkutan udara.
b. Kuat : terutama bila dipadu dengan logam lain. Digunakan untuk pembuatan
produk yang memerlukan kekuatan tinggi seperti pesawat terbang, kapal laut,
bejana tekan, kendaraan dan lain-lain.
c. Mudah dibentuk dengan semua proses pengerjaan logam. Mudah dirakit karena
dapat disambung dengan logam/material lainnya melalui pengelasan, brazing,
solder, adhesive bonding, sambungan mekanis, atau dengan teknik
penyambungan lainnya.
d. Tahan korosi : sifatnya durabel sehingga baik dipakai untuk lingkungan yang
dipengaruhi oleh unsur-unsur seperti air, udara, suhu dan unsur-unsur kimia
lainnya, baik di ruang angkasa atau bahkan sampai ke dasar laut.
e. Konduktor listrik : setiap satu kilogram aluminium dapat menghantarkan arus
listrik dua kali lebih besar jika dibandingkan dengan tembaga. Karena aluminium
relatif tidak mahal dan ringan, maka aluminium sangat baik untuk kabel-kabel
f. Konduktor panas : sifat ini sangat baik untuk penggunaan pada
mesin-mesin/alat-alat pemindah panas sehingga dapat memberikan penghematan energi.
g. Memantulkan sinar dan panas : Dapat dibuat sedemikian rupa sehingga
memiliki kemampuan pantul yang tinggi yaitu sekitar 95% dibandingkan dengan
kekuatan pantul sebuah cermin. Sifat pantul ini menjadikan aluminium sangat
baik untuk peralatan penahan radiasi panas.
h. Non magnetik : dan karenanya sangat baik untuk penggunaan pada peralatan
listrik atau elektronik, pemancar radio atau TV. dan lain-lain, dimana diperlukan
faktor magnetisasi negatif.
i. Tak beracun : dan karenanya sangat baik untuk penggunaan pada industri
makanan, minuman, dan obat-obatan, yaitu untuik peti kemas dan pembungkus.
j. Memiliki ketangguhan yang baik : dalam keadaan dingin dan tidak seperti
logam lainnya yang menjadi getas bila didinginkan. Sifat ini sangat baik untuk
penggunaan pada pemrosesan maupun transportasi LNG dimana suhu gas cair
k. Menarik : dan karena itu aluminium sering digunakan tanpa diberi proses
pengerjaan akhir. Tampak permukaan aluminium sangat menarik dan karena itu
cocok untuk perabot rumah (hiasan), bahan bangunan dan mobil. Disamping itu
aluminium dapat diberi surface treatment, dapat dikilapkan, disikat atau dicat
dengan berbagai warna, dan juga diberi proses anodisasi. Proses ini menghasilkan
lapisan yang juga dapat melindungi logam dari goresan dan jenis abrasi lainnya.
l. Mampu diproses ulang-guna yaitu dengan mengolahnya kembali melalui proses
peleburan dan selanjutnya dibentuk menjadi produk seperti yang diinginkan
Proses ulang-guna ini dapat menghemat energi, modal dan bahan baku yang
berharga (Daryus, A., 2008).
2.1.3. Kegunaan Aluminium
Aluminium banyak digunakan sebagai peralatan dapur, bahan konstruksi
bangunan dan ribuan aplikasi lainnya dimanan logam yang mudah dibuat, kuat dan
ringan diperlukan. Walaupun konduktivitas listriknya hanya 60% dari tembaga, tetapi
ia digunakan sebagai bahan transmisi karena ringan. Aluminium murni sangat lunak
dan tidak kuat. Tetapi dapat dicampur dengan tembaga, magnesium, silikon, mangan,
Campuran logam ini penting kegunaannya dalam konstruksi pesawat modern dan
roket. Logam ini jika diuapkan di vakum membentuk lapisan yang memiliki
reflektivitas tinggi untuk cahaya yang tampak dan radiasi panas. Lapisan ini menjaga
logam dibawahnya dari proses oksidasi sehingga tidak menurunkan nilai logam yang
dilapisi. Lapisan ini digunakan untuk memproteksi kaca teleskop dan kegunaan
lainnya.
1. Senyawa
Senyawa yang memiliki kegunaan besar adalah aluminium oksida,sulfat, dan
larutan sulfat dalam kalium. Oksida aluminium, alumina muncul secara alami sebagai
ruby, safir, corundum dan emery dan digunakan dalam pembuatan kaca dan tungku
pemanas.
Aluminium oksida adalah sebuah senyawa kimia dari aluminium dan oksigen,
dengan rumus kimia Al O Nama mineralnya adalah alumina, dan dalam bidang pertambangan, keramik dan teknik material senyawa ini lebih banyak disebut dengan
nama alumina.
Aluminium oksida adalah insulator (penghambat) panas dan listrik yang baik.
Aluminium oksida berperan penting dalam ketahanan logam aluminium
terhadap perkaratan dengan udara. Logam aluminium sebenarnya amat mudah
bereaksi dengan oksigen di udara. Aluminium bereaksi dengan oksigen membentuk
aluminium oksida, yang terbentuk sebagai lapisan tipis yang dengan cepat menutupi
permukaan aluminium. Lapisan ini melindungi logam aluminium dari oksidasi lebih
lanjut Ketebalan lapisan ini dapat ditingkatkan melalui proses anodisasi. Beberapa
alloy (paduan logam), seperti perunggu aluminium, memanfaatkan sifat ini dengan
menambahkan aluminium pada alloy untuk meningkatkan ketahanan terhadap korosi.
Al O yang dihasilkan melalui anodisasi bersifat amorf, namun beberapa proses oksidasi seperti plasma electrolytic oxidation menghasilkan sebagian besar
Al O dalam bentuk kristalin, yang meningkatkan kekerasannya. Secara alami, aluminium oksida terdapat dalam bentuk kristal corundum. Batu mulia rubi dan
sapphire tersusun atas corundum dengan warna-warna khas yang disebabkan kadar
ketidakmurnian dalam struktur corundum.
Aluminium oksida, atau alumina, merupakan komponen utama dalam bauksit
bijih aluminium yang utama. Pabrik alumina terbesar di dunia adalah Alcoa, Alcan,
dan Rusal. Perusahaan yang memiliki spesialisasi dalam produksi dari aluminium
terdiri dari Al O , Fe O , and SiO yang tidak murni. Campuran ini dimurnikan terlebih dahulu melalui Proses Bayer:
Al O + 3 H O + 2 NaOH + panas → 2 NaAl( OH)
Fe O tidak larut dalam basa yang dihasilkan, sehingga bisa dipisahkan melalui penyaringan. SiO larut dalam bentuk silikat Si( ) . Ketika cairan yang dihasilkan didinginkan, terjadi endapan Al( OH) , sedangkan silikat masih larut dalam cairan tersebut. Al( OH) yang dihasilkan kemudian dipanaskan, dan yang terbentuk adalah alumina.
2Al( OH) + panas → Al O + 3 H O
Setiap tahunnya, 65 juta ton alumina digunakan, lebih dari 90%-nya digunakan
dalam produksi logam aluminium. Aluminium hidroksida digunakan dalam
pembuatan bahan kimia pengelolaan air seperti aluminium sulfat, polialuminium
klorida, dan natrium aluminat. Bertonton alumina juga digunakan dalam pembuatan
zeolit, pelapisan pigmen titania dan pemadam api. Aluminium oksida memiliki
kekerasan 9 dalam skala Mohr. Hal ini menyebabkannya banyak digunakan sebagai
abrasif untuk menggantikan intan yang jauh lebih mahal. Beberapa jenis ampelas, dan
2. Senyawa organo-aluminum
Senyawa-senyawa organo-aluminum digunakan dalam jumlah besar untuk
polimerisasi olefin, dan di industri dihasilkan dari logam aluminum, hidrogen, dan
olefin seperti reaksi berikut:
2Al + 3H + 6CH =CHR → Al ( CH = CHR)
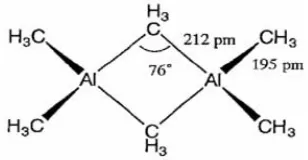
Senyawa ini berupa dimer kecuali yang mengandung gugushidrokarbon yang meruah.
Misalnya, trimetilaluminum, Al2( CH )6, adalah dimer dengan gugus metil menjembatani
atom aluminum dengan ikatan tuna elektron (Gambar 2.1). Senyawa organoaluminum
sangat reaktif dan terbakar secara spontan di udara. Senyawa-senyawa ini bereaksi
dengan hebat dengan air dan membentuk hidrokarbon jenuh, dengan aluminium
berubah menjadi aluminium hidroksida sesuai reaksi berikut:
Al ( CH CH ) + 3 H O → Al( OH) + 3C H
Oleh karena itu, senyawa-senyawa ini harus ditangani di laboratorium dalam
atmosfer yang inert sempurna.
Katalis Ziegler-Natta, yang terdiri atas senyawa organoaluminium dan
senyawa logam transisi membuat fenomena dalam katalisis polimerisasi, katalis ini
dikembangkan tahun 1950-an, dan dianugerahi Nobel tahun 1963. Senyawa alkil
logam transisi terbentuk bila senyawa organoaluminum bereaksi dengan senyawa
logam transisi. Senyawa alkil logam transisi yang terbentuk dapat diisolasi bila ligan
penstabil terkordinasi dengan atom logam pusat.
2.2. Alumina
Alumina merupakan persenyawaan kimia antara logam aluminium dengan
oksigen (Al O ). Alumina ditemukan dialam dalam bentuk bauksit. Alumina merupakan bahan baku utama dalam proses elektrolisa aluminium. Alumina
mempunyai morfologi sebagai bubuk berwarna putih dengan berat molekul 102, titik
leleh pada 2050˚C dan spesifikasi grafity 3,4 - 4,0.
Dalam industri peleburan aluminium, alumina memegang 3 fungsi penting
yaitu :
2. sebagai insulasi termal untuk mengurangi kehilangan panas dari atas tungku
reduksi, dan untuk mempertahankan temperatur operasi
3. melindungi anoda dari oksidasi udara
Dalam pembuatannya, alumina dapat di buat dengan beberapa proses salah
satunya dengan proses bayer. Proses pembuatan alumina (Al O ) dari bijih bauksit dengan proses bayer. Proses bayer terdiri dari tiga tahap reaksi yaitu :
a. Proses Ekstraksi
Al O . xH O + 2NaOH → 2NaAlO + (x+1)H O b. Proses Dekomposisi
2NaAlO + 4H O → 2NaOH + Al O .3H O c. Proses Kalsinasi
Al O .3H O + Kalor Al O + H O
Pada proses kalsinasi akan dihasilkan 2 jenis alumina, yaitu :
1. Alumina Sandy, yaitu alumina yang diperoleh dengan kalsinasi jika operasi
berlangsung pada temperatur rendah.
2. Alumina Fluory, yaitu alumina yang diperoleh dengan proses kalsinasi jika operasi
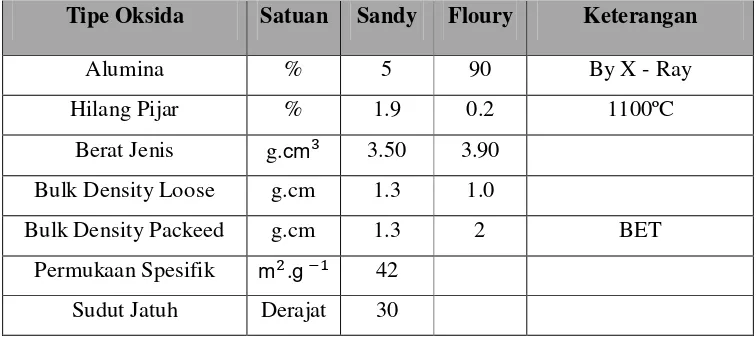
Tabel 2.1 Perbedaan Sifat Alumina Sandy dan Floury
Tipe Oksida Satuan Sandy Floury Keterangan
Alumina % 5 90 By X - Ray
Spesific Surface Area m2/g 40-80
Particle Size
+ 150 mesh % 25 min
- 325 mesh % 12,0 maks
Angle of Refuse Deg 30-34
2.3. Proses Elektrolisis
Elektrolisis adalah peristiwa kimia yang melibatkan dua atau lebih spesies
kimia yang berbeda, yang terjadi pada kedua elektroda (Anoda dan katoda) dan
berlangsung bila aliran listrik searah, DC (Direct Current) dialirkan kedalam suatu
pelarut elektrolit. Produksi aluminium dibuat didalam elektrolit cell atau disebut
“pot”. Alumina tidak bisa dilarutkan di dalam larutan kriolit (Na AlF ) pada suhu ± 960ºC. ampere tinggi, volt rendah dan listrik aktif di aliri melelui wadah berisi anoda
karbon yang terendam dalam larutan alaktrolit.
Elektrolisis Al O yang terjadi dalam larutan (antara lapisan anoda dan larutan logam). Ion-ion aluminium didalam Al O dikurangi tujuannya untuk membentuk larutan aluminium yang berkumpul dibawah cell katoda. Ion-ion oxide bereaksi
dengan anoda karbon hingga memproduksi karbon dioksida. Proses ini dikenal dengan
2 Al O (solution) + 3C (s) → 4 Al (l) + 3CO (g)
Mekanisme yang terjadi dalam proses tersebut adalah alumina diumpankan
kedalam elektrolit dan terpisah menjadi ion aluminium yang bermuatan positif (Al ) dan ion oksigen yang bermuatan negatif (O ). Arus searah dialirkan ke dalam tiap-tiap sel, sehingga menggerakkan ion-ion menuju arah yang berlawanan. Ion oksigen
bergerak ke arah anoda, lalu bereaksi dengan karbon membentuk karbondioksida,
sedangkan ion aluminium bergerak kearah katoda, lalu akan kehilangan muatannya
membentuk aluminium.
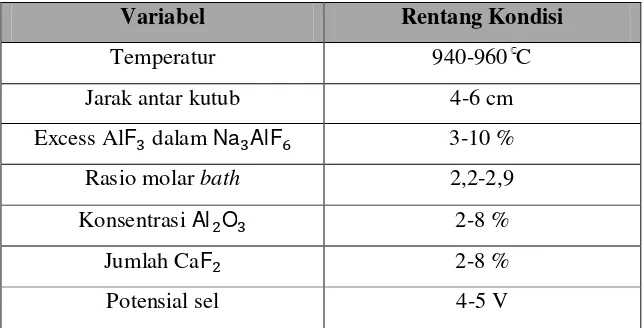
Kondisi operasi sel elektrolisis di industri pada umumnya dapat dilihat pada
tabel 2.3. Kondisi operasi ini meliputi temperature bath, komposisi bath, jarak antara
anoda dan katoda, tegangan sel, rapat arus, dan kedalaman logam cair.
Bahan baku dalam proses Hall-Heroult terdiri dari alumina, elektrolit, katoda
dan anoda. Proses hall-Heroult memproduksi aluminium dengan cara mereduksi
aluminium dari bahan baku alumina dalam proses elektrolisis yang digerakkan oleh
arus searah yang mengalir dari anoda ke katoda dengan kriolit sebagai elektrolit.
Kedua elektroda yang digunakan terbuat dari bahan karbon (Grjotheim, K., 1988).
2.3.1. Mekanisme Elektrolisa Hall-Heroult
Produksi aluminium dilakukan dalam sel elektrolisis atau pot. Alumina
(Al O ) dipisahkan dalam elektrolit cair (bath) pada temperatur 960 C di dalam sel baja segiempat yang besar yang saling berjajar dengan katoda blok karbon dan dilapisi
bricks. Aliran listrik searah (direct current, DC) dengan arus yang tinggi dan tegangan
yang rendah dilewatkan melalui blok karbon (anoda) yang dicelupkan dalam elektrolit
cair (bath), kemudian melewati lapisan aluminium cair (molten) yang mengumpul
diatas katoda karbon pada bagian bawah sel, lalu selanjutnya menuju ke katoda.
Batang baja dalam blok katoda membawa aliran listrik ke sel selanjutnya melalui
sistem busbar aluminium.
Rapat arus 0,7-1,2 A/cm
Elektrolisis Al O terjadi dalam lapisan elektrolit cair (bath) yaitu lapisan diantara anoda dan metal cair. Ion aluminium dalam Al O direduksi untuk membentuk aluminium cair, yang kemudian mengumpul diatas katoda pada bagian
bawah sel. Ion oksida bereaksi dengan anoda karbon dan menghasilkan
karbondioksida. Ini dikenal sebagai proses Hall-Heroult yang ditunjukkan oleh reaksi:
2Al O + 3C → 4Al + 3CO
Aluminium cair dihisap (tapping) dari sel kedalam “ceret” raksasa dan di bawa
ke pabrik pencetakan (casthouse) dimana, aluminium cair itu akan dibentuk menjadi
ingot untuk diproses lebih lanjut
Dalam industri peleburan aluminium, ada terdapat dua jenis tungku reduksi
yang dipergunakan yaitu Prebaked Anode Furnace (PAF) dan Soderberg Anode
Furnace (SAF). Perbedaan kedua tipe tungku tersebut terletak pada cara
pemanggangan anodanya, dalam sistem PAF anoda dipanggang terlebih dahulu
(prebaked) sebelum dipergunakan. Sedangkan pada sistem SAF tidak dilakukan
pemanggangan pendahuluan, melainkan dimasukkan langsung ke dalam tungku
reduksi. Pabrik peleburan aluminium di Kuala Tanjung menggunakan sistem PAF
yang telah dikembangkan oleh Sumitomo Aluminium Smelting Co.Ltd (Siahaan,B.,
1985).
Tipe pot (tungku reduksi)yang menggunakan tekhnologi Sumitomo
Pre Baked (CWPB). Arus listrik searah (DC) yang digunakan sebesar 188-200 kA
(sekarang ini kapasitas terpasang di INALUM adalah 190,3 kA), dengan tegangan tiap
pot (tungku reduksi) sekitar 4,2-4,4 volt. Pot satu dengan pot lainnya dihubungkan
secara listrik seri dan diletakkan bersisian (Side by Side). Daya yang digunakan untuk
satu pot kira-kira setara dengan 1600 rumah berdaya listrik 500 watt.
Reaksi keseluruhan pada industri elektrolisis alumina menggunakan anoda
karbon adalah sebagai berikut:
2Al O( ) + 3C( ) → 4Al( ) + 3CO( )
Mekanisme reaksi yang paling sering terjadi adalah reduksi Al O secara langsung dengan reaksi:
Al O →AlO + Al O Al O →Al + 2O
Dari reaksi diatas terbukti bahwa Al akan bergerak ke katoda, sedangkan O akan bergerak menuju anoda.
Reaksi pada katoda : Al + 3e→Al( l)
Reaksi pada anoda : 2O → O + 4e
Lalu selanjutnya O akan bereaksi dengan karbon anoda:
Dari proses peleburan aluminium ini, selain menghasilkan gas CO dan CO, dihasilkan pula gas HF yang diketahui sangat berbahaya bagi kesehatan, melalui
reaksi:
2AlF + 3H O→ Al O + 6HF, dan
2Na AlF ( )+ 3H O( ) → 2Al O ( ) + 6NaF( ) + HF( )
Gas-gas yang dihasilkan selanjutnya akan dihisap oleh main exhaust fan dan masuk ke
dalam DSS (Dry Scrubbing System), dimana sistem ini berfungsi menyaring debu dan
mengadsorbsi gas flourida yang berasal dari pot reduksi (gas HF akan bereaksi dengan
fresh alumina yang berasal dari silo dan menghasilkan reacted alumina). Selanjutnya
gas-gas yang sudah bersih tersebut dibuang ke atmosfer melalui exhaust stack
(PT.INALUM, 2011).
2.3.2. Jenis Sel yang digunakan dalam proses Hall-Heroult
Ada dua jenis sel yang digunakan dalam proses Hall-Heroult, yaitu sel yang
menggunakan seperangkat anoda yang telah dipanggang terlebih dahulu
(prapanggang) dan anoda yag memanggang sendiri (swapanggang) atau sering disebut
anoda Soderberg. Pada kedua jenis anoda ini, anodanya disuspensi dari superstruktur
penghantar anoda yang dapat bergerak sehingga sisi vertikalnya dapat diukur.
Blok-blok anoda yang prapanggangg dibuat dari campuran kokas migas kalsinasi berkadar
abu rendah dengan pitch atau ter dan dicetak dalam press hidraulik,kemudian
dipanggang sampai suhu 1100ºC.
Sel anoda soderberg mempunyai anoda tunggal yang besar yangmengisi
sebagian besar lubang sel. Anoda itu ditempatkan di dalam rumahan baja yang
terbuka, yang mempunyai dinding vertical.Anoda itu dipasangkan melalui rumahan
tersebut ke dalam kriolit. Pada waktu sel itu dioperasikan untuk pertama kali, suhunya
dinaikkan dengan menggunakan pemanasan tahanan listrik sampai mencapai suhu
operasi., anoda itu kemudian dihubungkan dengan lapisan partikel kokas pada dasar
lubang sel. Arus listrik kemudian dilewatkan melalui sel yang mengalami hubungan
singkat itu sampai mencapai suhu yang dikehendaki.
Bahan elektrolit ditambahkan melalui lubang sel disekitar anoda. Pada waktu
bahan ini berangsur-angsur melebur, anoda itu dinaikkan sehingga selnya beroperasi.
Biasanya jarak anoda dan katoda kira-kira 5cm. Elektrolit lebur itu terdiri terutama
dari kriolit (3NaF.AlF ) dan sisanya AlF serta CaF 6% sampai 10% berat dan Al O
2% sampai 6%. Sebagian kriolit diimpor ke Amerika serikat dari Greenland, tetapi
2.4. Kebutuhan Alumina
Selama beroperasinya sel, terjadi pembentukan kerak di atas permukaan
penangas lebur. Alumina ditambahkan ke atas kerak ini dan alumina akan mengalami
pemanasan selanjutnya melepaskan kandungan airnya. Kerak itu dipecahkan secara
berkala dan alumina itu diaduk ke dalam penangas agar konsentrasinya tetap berada di
sekitar 2% sampai 6%. Kebutuhan teoritis alumina adalah 1,89 per kilogram
aluminium. Tetapi dalam prakteknya, angkanya kira-kira 1,91. bila kadar alumina di
dalam penangas itu sudah berkurang dan efek anoda berlangsung pada anoda itu
terbentuk suatu lapisan tipis karbon tetrafluorida di penangas itu tidak dapat lagi
membatasi permukaan anoda. Dalam hal ini voltase sel akan naik dan ini terlihat dari
lampu peringatan atau lonceng yang dihubungkan dengan sel dan hanya bekerja jika
sel beroperasi tidak normal. Bila ini terjadi, alumina kemudian diadukkan ke dalam
sel, walaupun waktunya bukanlah waktu penambahan berkala yang direncanakan.
Mengenai mekanisme yang sebenarnya dari pelarutan alumina di dalam penangas dan
bagaimana mekanisme dekomposisi elektrolitnya masih belum jelas. Tetapi pada
akhirnya ialah pembebasan oksigen pada anoda dan pengendapan logam aluminium
pada katoda. Oksigen itu bergabung dengan anoda karbon menghasilkan CO dan CO
2.5. Pengelolaan Material Alumina
Bahan-bahan untuk keperluan produksi aluminium pertama sekali didatangkan
menggunakan kapal melalui pelabuhan. Bahan-bahan tersebut adalah fresh alumina,
kokas (coke) dan hard pitch. Fresh alumina akan dimasukkan ke dalam silo alumina,
kokas ke dalam silo kokas dan pitch ke dalam pitch storage house.
Bahan baku untuk keperluan di gedung reduksi berupa fresh alumina dibawa
menggunakan belt conveyor ke dalam silo alumina yang berjumlah 3 unit dan
masing-masing silo berkapasitas 20.000 ton, kemudian dibawa ke Dry ScrubbingSystem
(DSS) yang berjumlah 27 unit (namun yang beroperasi sekarang 24 unit) yang
masing-masing berkapasitas 13 ton dengan menggunakan air slide untuk direaksikan
dengan gas HF yang berasal dari pot. Hasil dari reaksi ini adalah reacted alumina
yang disimpan dalam alumina bin yang berjumlah 3 unit yang masing-masing
berkapasitas 12.000 ton. Alumina dimasukkan ke daybin yang berjumlah 6 unit dan
masing-masing berkapasitas 600 ton dengan menggunakan belt conveyor kemudian
dari daybin dimasukkan kedalam distribusi bin yang berjumlah 12 unit yang
masing-masing berkapasitas 60 ton dengan menggunakan air slide selanjutnya akan
dimasukkan ke dalam hopper pot yang berjumlah 510 unit (namun yang beroperasi
sekarang 470 unit) yang masing-masing berkapasitas 5 ton dengan menggunakan
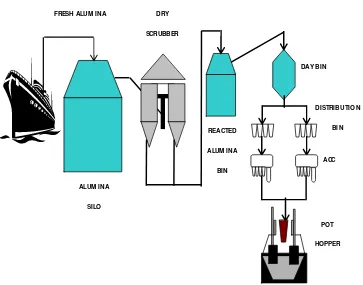
Flowsheet aliran material alumina dapat dilihat pada Gambar 2.2 sebagai
berikut :
Gambar 2.2 Flowsheet Aliran Material Alumina
ALUM INA
SILO
DRY
SCRUBBER FRESH ALUM I NA
REACTED
ALUM I NA
BIN
DAY BIN
DISTRIBU TION
BI N
ACC
POT
2.5.1. Pemasukan Alumina
Alumina feeding sebagian besar biasanya terdapat dalam prosedur sel
Hall-Heroult. Jadi, ini dilakukan dengan pengisian dan bentuk yang sangat berbeda dari
operasi yang strategis.
Grjotheim telah menjelaskan beberapa karakteristik dan konsekuensi termal untuk tipe
aluminium yang berbeda, gambarannya sangat berbeda untuk karakteristik break and
feed, kebutuhan panas dan kecenderungan endapannya (sludge), awalnya
menunjukkan keuntungan dari teknik feeding tersebut. Keuntungan-keuntungan ini
mungkin secara ringkas yang terdapat dibawah ini :
a. Dalam pembentukan lumpur atau endapan (sludge) dapat diperkecil
b. Konsentrasi alumina (Al O ) di dalam bath dapat dijaga konstan c. Bilangan dari anode effect (AE) dapat menurun secara drastis
Aplikasi dari proses pengontrolan alumina (Al O ) adalah bentuk dari asumsi bahwa kehabisan dari alumina (Al O ) dengan waktu tertentu. Strategi pengontrolan digunakan untuk menjaga konsentrasi alumina (Al O ) di dalam bath dibagian sempit dengan konsentrasi (± 0,5 % massa) dalam alumina (Al O ) yang rendah pada sisi sel yang minimum.
Aliran atau kecepatan feeding cocok dengan pertambahan berat unit per waktu,
mempunyai waktu interval yang berlainan. Pada waktu periode tertentu alumina
(Al O ) yang masuk ke dalam interval waktu yang singkat kepada aliran normal dari pemakaian alumina (Al O ) dalam sel dan pada periode alumina (Al O ) yang lain pemasukan alumina (Al O ) pada interval yang lama (underfeeding) (Grjotheim, K., 1988).
2.5.2. Metode Pemasukan Alumina
Pemasukan Alumina (Al O ) pada PT. Inalum memiliki dua metode, yaitu Regular Feeding dan Demand Feeding. Regular Feeding adalah metode pemasukan
alumina secara berkala dengan jumlah alumina (Al O ) per waktu yang telah ditentukan. Regular Feeding secara otomatis teah diatur pemasukannya oleh sistem
komputer yaitu rata – rata 20kg per 15 menit sekali, di mana pada saat alumina
(Al O ) akan masuk kerak tengah akan dipecah oleh teeth blade dan alumina (Al O ) akan masuk ke dalam tungku reduksi. Demand Feeding adalah metode pemasukan
Metode Demand Feeding memeiliki pembagian pada waktu dan takaran pada
pemasukkan alumina (Al O ) untuk mengetahui kapan kondisi pot lapar dan kelebihan alumina (Al O ) . Siklus pembagian metode Demand Feeding dapat dilihat pada tabel 2.4.
Alumina (Al O ) sebelum masuk ke dalam pot kerak tengah akan dipecah oleh teeth blade agar alumina (Al O ) dapat masuk dan tidak menumpuk dibagian anoda.
Gambar 2.3 Teeth Blade Memecah Kerak Tengah
2.6. Anode Effect (AE)
Anode effect adalah peristiwa naiknya tegangan listrik pot secara tiba-tiba
karena kandungan alumina di dalam elektrolit sangat rendah. Anode effect dapat
dihentikan dengan menambahkan alumina ke dalam elektrolit sambil menaik turunkan
anoda sehingga gas-gas di bawah anoda dapat keluar. Pekerjaan seperti ini dapat
dilakukan dengan kompoter maupun secara manual bila program kompoter tidak
menyebabkan kriolit berhenti membasahi anoda dan gelembung gas akan berkumpul
di permukaan anoda., dan bila lapisan ini pecah, maka akan menimbulkan percikan
bungan api atau funkenentladung (bahasa German), sehingga anode effect disebut
para operatur juga sebagai funken.
Anode effect dapat menyebabkan terhambatnya aliran arus dari anoda ke
katoda. Anosda effect dapat menyebabkan peningkatkan tegangan permukaan pada
anoda atau lapisan elektrolit yang berada pada kerapatan arus kritis. Selain itu
kekntalan juga mempengaruhi terjadinya Anode effect karena gelembung gas pada
anoda sulit bergerak ke luar. Kekentalan yang tinggi terjadi karena rendahnya
temperatur operasi.
Jika selama proses elektrolisa kandungan alumina dalam kriolit rendah, maka
akan menyebabkan sudut pembasahan anoda oleh kriolit besar. Akibatnya
gelembung-gelembung gas mudah berkumpul pada permukaan anoda yang berada dalam kriolit.
Jika hal tersebut sering terjadi dalam pot, maka operasi tidak akan stabil dan akan
mempengaruhi produksi dan CE (Current Efficiency) akan rendah.
Anode effect dihasilkan jika kandungan alumina yang terlarut dalam kriolit
rendah atau sekitar 1-1,5% dari kriolit.. selama berlangsungnya anode effect tegangan
sel meningkat karena intensitas arus listrik dijaga konstan dalam sel-sel yang
terhubung dalam satu rangkaian. Tegangan dapat bervariasi dari 10-50 volt,
memberikan banyak dampak negatif terhadap proses elektrolisa maupun kondisi pot,
namun anode effect juga sangat penting untuk operasi tungku reduksi. Semua alumina
yang ditambahkan terkonsumsi dan pot tersebut tidak mengalami overfeeding atau