BAB II
TINJAUAN PUSTAKA
2.1 Bakteri Extended Spectrum Beta Lactamase (ESBL)
Antibiotik pertama ditemukan oleh Sir Alexander Fleming pada tahun 1927 dan
dinamakan penisilin, yang merupakan beta laktam, yang mempunyai empat cincin beta laktam;
tiga cincin karbon dan satu nitrogen. Pada awal 1940an, Florey, Chain dan Heatley dari
Universitas Oxford menyempurnakan penisilin dan mulai digunakan untuk mengobati infeksi
bakteri secara luas. Antibiotik ini bekerja dengan cara menghambat sintesa dinding sel bakteri,
dimana cincin beta laktam meniru komponen dinding sel tempat ikatan transpeptidase, dan
secara kompetitif menghambat ikatan dari transpeptidase. Akibatnya, bakteri tidak lagi dapat
memproduksi dinding sel, sehingga pecah dan mati.2,11
Untuk mengatasi kerja dari antibiotik beta laktam ini, bakteri menghasilkan enzim, yang
disebut dengan beta laktamase, yang dapat merusak cincin beta laktam dari penisilin dengan
hidrolisis, dan tanpa cincin beta laktam, penisilin menjadi tidak efektif melawan bakteri (gambar
Gambar 2.1. Mekanisme Resistensi terhadap Beta laktam. Dikutip dari: John Wiley & sons, Inc, Bacterial Drug Resistance, 2004.2
Enzim beta laktamase yang pertama ditemukan pada bakteri gram negatif, diperantarai
oleh plasmid di Yunani pada tahun 1960an. Enzim ini dinamai dengan TEM, sesuai dengan
nama pasien asal isolat bakteri penghasil enzim ini, Temoniera. Kemudian TEM-2 ditemukan
dan sangat identik strukturnya secara biokimiawi dengan TEM-1, hanya berbeda pada satu asam
amino yang menyebabkan perbedaan titik isoelektris dari kedua enzim ini.3 Kedua enzim ini adalah enzim beta laktamase-diperantarai plasmid yang paling lazim ditemukan pada bakteri
gram negatif, termasuk Enterobacteriaceae, Pseudomonas aeruginosa, Haemophilus influenza,
dan Neisseria gonnorhoeae. TEM-1 dan TEM-2 menghidrolisis penisilin dan sefalosporin
spektrum sempit, seperti sefalotin atau sefazolin. Namun, mereka tidak efektif terhadap
sefalosporin generasi yang lebih tinggi dengan rantai samping oxyimino, seperti sefotaksim,
seftazidim, seftriakson, atau sefepim.3,5,12 Enzim beta laktamase yang berhubungan dengan enzim-enzim tadi, tetapi lebih jarang ditemukan, dinamai SHV, karena reagen sulfhydryl
memiliki efek spesifik terhadap substrat ini. SHV merupakan hasil dari mutasi serin menjadi
glisin pada posisi 238 enzim beta laktamase TEM.3
Saat bakteri menemukan mekanisme resistensi terhadap golongan beta laktam ini, banyak
obat-obatan baru yang dikembangkan dari penisilin untuk menandingi resistensi yang muncul
pada bakteri. Turunan dari antibiotik ini disebut dengan beta laktam spektrum luas (extended spectrum beta-lactams), termasuk di dalamnya sefalosporin, monobaktam.11
Penggunaan antibiotik sefalosporin spektrum luas semakin intensif digunakan dalam dua
dekade terakhir. Penggunaan obat ini secara luas dan tidak tepat mengakibatkan munculnya
strain bakteri yang resisten terhadap antibiotik, dengan menghasilkan enzim-enzim extended spectrum beta lactamase (ESBL).4 ESBL adalah enzim yang dapat menyebabkan resistensi terhadap hampir seluruh antibiotik beta laktam, termasuk penisilin, sefalosporin, dan
monobaktam aztreonam.3
Pada tahun 1983, sebuah enzim beta laktamase yang mampu menghidrolisis sefalosporin
spektrum luas ditemukan pada suatu strain Klebsiella pneumonia di Jerman. Kemampuan untuk menghidrolisis sefalosporin spektrum luas ini muncul akibat adanya mutasi pada satu nukleotide
(dibandingkan dengan gen yang menghasilkan SHV), dan diberi nama SHV-2. Enzim beta
TEM-2. Laporan serupa bermunculan secara cepat di Amerika Serikat (1988) dan Perancis
(1984). Distribusi yang cepat ini disebabkan oleh ekspansi klonal dari bakteri ESBL, dan transfer
horizontal dari gen ESBL. Karena spektrum aktivitasnya mencakup oxyiminocephalosporins, enzim ini kemudian dikenal dengan extended spectrum beta laktamase (ESBL).3,6,13,14
Kelompok dari enzim-enzim ESBL ini heterogenus. Enzim tipe SHV dan TEM muncul
dari pergantian asam amino yang memungkinkan enzim dengan spektrum yang lebih sempit
untuk menyerang beta laktam oxyimino baru. Kelompok lainnya, dari keluarga CTX-M,
mempunyai kemampuan menyerang beta laktam dengan spektrum luas, yang didapat dari
plasmid, yang ditentukan oleh gen-gen kromosom. Famili enzim ESBL yang lain yang telah
cukup lama dikenal adalah OXA beta laktamase, agak jarang ditemukan dan dimediasi oleh
plasmid juga. OXA beta laktamase dapat menghidrolisis oksasilin dan berhubungan dengan
penisilin anti stafilokokus. Enzim beta laktamase yang lain, seperti PER, VEB, dan GES telah
dilaporkan tetapi sangat jarang dan terutama ditemukan pada P. aeruginosa dan hanya didapati pada daerah geografis tertentu. Enzim ESBL lainnya, yang juga cukup jarang, dan ditemukan di
Enterobacteriaceae antara lain BES, SFO, dan TLA.3
Enzim-enzim ESBL mempunyai kemampuan yang bervariasi terhadap berbagai substrat
beta laktam oxyimino, tetapi tidak dapat menyerang sefamisin (sefoksitin, sefotetan dan
sefmetazole) dan karbapenem (imipenem, meropenem, doripenem, dan ertapenem).
Enzim-enzim ini juga sensitif terhadap inhibitor-inibitor beta laktamase, seperti klavulanat, sulbaktam,
dan tazobaktam, sehingga dapat digabungkan dengan substrat beta laktam untuk menguji apakah
ada mekanisme resistensi ini. Enzim-enzim ESBL ini ditemukan secara khusus pada bakteri
gram negatif, terutama Klebsiella pneumonia, Klebsiella oxytoca, dan Eschericia coli. Tetapi dapat juga ditemukan pada Acinetobacter, Burkhlorderia, Citobacter, Enterobacter, Morganella, Proteus, Pseudomonas, Salmonella, dan Seratia spp.3
Strain Enterobacteriaceae di atas, yang memiliki kemampuan menghasilkan enzim ESBL menjadi sangat penting, karena kebanyakan dari kelompok bakteri ini adalah flora normal pada
saluran cerna manusia dan hewan, dan juga tersebar luas di lingkungan bebas. Lebih jauh,
bakteri-bakteri ini dapat menyebabkan infeksi-infeksi yang berbeda, seperti septikaemia, infeksi
saluran kemih, pneumonia, kolesistitis, kolangitis, peritonitis, infeksi luka, meningitis, dan
2.2 Epidemiologi Infeksi Bakteri ESBL
Strain bakteri ESBL ini tersebar luas di seluruh dunia, lebih sering didapati pada
spesimen yang berasal dari rumah sakit tetapi juga dapat dijumpai di masyarakat. Prevalensi dan
fenotipnya berbeda dari satu daerah dengan daerah yang lain.4
Seperti disebutkan di atas, bakteri ESBL pertama sekali ditemukan di Jerman, tetapi
kebanyakan laporan tentang ditemukannya ESBL pada dekade pertama berasal dari Perancis.
Wabah pertama dilaporkan terjadi di Perancis pada tahun 1986; dimana 54 pasien di tiga ruang
rawat intensif terinfeksi bakteri ESBL dan menyebarkannya ke empat bangsal lainnya. Namun,
pada beberapa tahun terakhir, dengan gencarnya tindakan pengendalian infeksi, terjadi
penurunan insidensi infeksi bakteri ESBL. Di Perancis utara, proporsi isolat Klebsiella
pneumonia menurun dari 19,7% pada 1996 menjadi 7,9% pada tahun 2000. Terdapat perbedaan prevalensi secara geografis di Negara-negara Eropa. Di dalam suatu negara juga terjadi
perbedaan antara satu rumah sakit dengan rumah sakit lainnya. Di Swedia, bakteri ESBL dapat
ditemukan di masyarakat maupun di rumah sakit. Swedia telah melaporkan ke EARSS, the
European surveillance system, bahwa pada tahun 2006, 1,1% dari seluruh E.coli dan 0,8% dari
K. pneumoniae pada kultur darah ditemukan menghasilkan ESBL. Jumlah isolat ESBL telah meningkat secara tajam di Swedia dalam beberapa tahun, dan beberapa wabah telah dilaporkan.
Sejak Februari 2007, dalam enam bulan berikutnya, lebih dari 1000 kasus dilaporkan, yang
tersebar di seluruh wilayah. Artinya di Swedia, kasus ESBL berjumlah dua kali lipat daripada
MRSA.16 Kejadian di Eropa bervariasi mulai dari 3% di Swedia sampai 34% di Portugal. Secara keseluruhan di Eropa, penelitian Meropenem Yearly Susceptibility Test Information Collection
(Mystic Study) tahun 2008 melibatkan 12 negara diperoleh kejadian ESBL 5,6%.17
Di USA, National Nosocomial Infection Surveillance (NNIS) menemukan sejak Januari 1998 sampai Juni 2002 didapati 6,1% dari 6.101 isolat Klebsiella pneumonia dari 110 ruang rawat inap intensif resiten terhadap sefalosporin generasi ke-tiga.6
Di Asia sendiri, pada tahun 1988, isolat Klebsiella pneumonia dari China yang mengandung ESBL untuk pertama kali dilaporkan. Dalam suatu laporan yang mengumpulkan
Kariadi Semarang, selama kurun waktu 2004-2005 didapatkan proporsi bakteri penghasil ESBL
sebesar 50,6% berdasarkan tes skrining awal.7 Hasil penelitian Antimicrobial Resistance in
Indonesia: prevalence and prevention (AMRIN Study) tahun 2010-2011 menemukan bahwa
kejadian ESBL cukup tinggi yakni 29% pada E. coli dan 36% pada K. pneumoniae.18
Penelitian di Medan, tahun 2012 oleh Mayasari melaporkan dari 282 sampel urin dengan
kultur positif, diperoleh kejadian ESBL E.coli 18,7%.8 Dari data di bagian Mikrobiologi RS H Adam Malik Medan, dijumpai kejadian infeksi ESBL yang cukup tinggi. Pada tahun 2012
kejadian ESBL 16,9% (12% ESBL K. pneumoniae dan 4,9% ESBL E.coli) meningkat menjadi 19,51% (12,24% ESBL K. pneumoniae dan 7,17% ESBL E.coli) pada tahun 2013. Disamping itu, dari tahun 2013 diketahui bahwa 67,81% isolate K. pneumoniae dan 61,83% isolate E. coli
merupakan ESBL E. coli.
2.3 Faktor Risiko Infeksi Bakteri ESBL
Patogen-patogen yang memiliki resistensi terhadap berbagai macam obat ini
menyebabkan meningkatnya kemunculan dari kejadian infeksi baik yang didapatkan di fasilitas
kesehatan maupun yang didapatkan di masyarakat. Keterlambatan dalam pemberian antibiotik
yang tepat sebagai akibat dari resistensi menyebabkan meningkatnya morbiditas, mortalitas,
lamanya rawatan, dan biaya rawatan. Angka mortalitas pada pasien-pasien yang terinfeksi oleh
kuman yang multi resisten ini apabila diobati dengan antibiotik yang tidak tepat, berkisar
42-100%. Untuk memulai terapi yang tepat dengan cepat, klinisi harus mengenali faktor-faktor
risiko seorang pasien untuk terinfeksi bakteri yang menghasilkan ESBL.5,10
Demirdag dkk, tahun 2010, telah mengidentifikasi beberapa faktor risiko yang secara
signifikan berhubungan dengan meningkatnya risiko infeksi bakteri ESBL di Firat University Hospital, Turki. Masa rawat inap diatas tujuh hari sebelum terjadinya infeksi, pemakaian antibiotik sebelumnya, penggunaan kateter, dan intervensi bedah adalah beberapa faktor risiko
tersebut.19
Rupp dkk, dari departemen penyakit dalam di University of Nebraska Medical Centre, tahun 2003 mencoba merumuskan beberapa populasi yang pernah mengalami wabah dari bakteri
ESBL, faktor-faktor risiko untuk terinfeksi bakteri yang menghasilkan ESBL, dan beberapa
Tabel 2.1. Populasi wabah, faktor-faktor risiko, dan vektor/reservoir bakteri ESBL 5.
Dikutip dari: Rupp, ME, Drugs,2003
2.4 Sistem Skoring Duke Model Score
Untuk memulai terapi antibiotik secara tepat waktu, beberapa institusi kesehatan
memahami pentingnya untuk memiliki sebuah alat stratifikasi faktor risiko untuk
mengidentifikasi pasien-pasien yang memiliki risiko tinggi untuk mendapatkan infeksi bakteri
penghasil ESBL pada saat masuk RS. Walaupun beberapa peneliti telah mengidentifikasi
faktor-faktor risiko infeksi ESBL, namun penulis hanya menemukan dua sistem skoring yang berisikan
faktor-faktor risiko tersebut. Namun kedua sistem skoring ini dibuat dalam populasi spesifik
pertama yang ditemukan oleh Tumbarello dkk tahun 2011 di Italia, dengan cara mengidentifikasi
faktor-faktor risiko dengan model regresi logistik yang kemudian diubah ke sebuah aturan yang
berdasarkan nilai yang memberikan skor untuk tiap-tiap faktor risiko.4 Sistem skoring ini dikenal dengan Italian Score. (table 2.2)
Italian Model Score4
Kriteria penilaian Skor
Mendapat antibiotik beta laktam dan atau fluorokuinolon dalam 3 bulan terakhir
2
Riwayat dirawat sebelumnya dalam 12 bulan terakhir 3
Pasien rujukan dari fasilitas kesehatan lain 3
Charlson Comorbidity Score≥ 4 2
Penggunaan kateter urin dalam 30 hari terakhir 2
Usia ≥ 70 tahun 2
Dikutip dari: Tumbarello dkk, Antimicrob Agents Chemoter, 2011
Pada penelitian itu, Tumbarello dkk menggunakan cutoff skor 8 atau lebih untuk mendapatkan spesifisitas yang tinggi (96%) dan positive predictive value 80%, namun hanya memiliki sensitivitas 50%. Namun pada saat divalidasi di institusi lain, yaitu di Duke University
Hospital, maka pada tahun 2013, Steven dkk mengusulkan suatu sistem skoring baru yang lebih
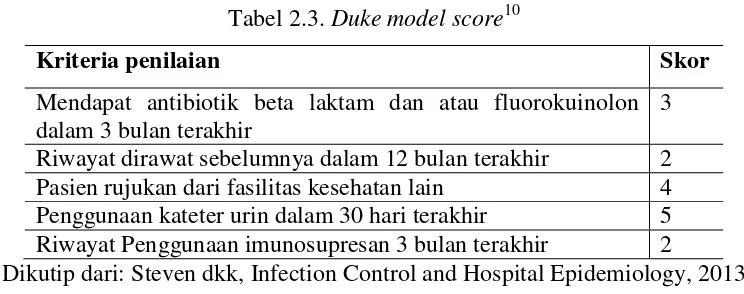
Tabel 2.3. Duke model score10
Kriteria penilaian Skor
Mendapat antibiotik beta laktam dan atau fluorokuinolon dalam 3 bulan terakhir
3
Riwayat dirawat sebelumnya dalam 12 bulan terakhir 2
Pasien rujukan dari fasilitas kesehatan lain 4
Penggunaan kateter urin dalam 30 hari terakhir 5 Riwayat Penggunaan imunosupresan 3 bulan terakhir 2
Dikutip dari: Steven dkk, Infection Control and Hospital Epidemiology, 2013
Penggunaan antibiotik empirik untuk ESBL membutuhkan spesifisitas dan positive
predictive value yang tinggi. Dan dengan cutoff sama dengan atau lebih dari 8, maka pada Duke model score memiliki spesifisitas 95% dan positive predictive value 79%.10 Namun sekali lagi, sistem skoring ini belum diuji pada populasi dan organisme lain, seperti di Indonesia, khususnya
di RS. H. Adam Malik, Medan.
2.5 Manajemen Infeksi Bakteri ESBL
Adanya sistem skoring yang valid akan sangat membantu klinisi dalam menghadapi
infeksi bakteri ESBL. Keputusan dalam bagaimana menghadapi bakteri ESBL ini semestinya
tidak hanya berdasarkan laporan mikrobiologis saja. Pemahaman menyeluruh terhadap kondisi
klinis pasien dan pertimbangan praktis seperti biaya, kenyamanan dalam pemberian obat,
kepatuhan pasien, efek samping obat, efikasi antibiotik yang dipilih harus menjadi unsur-unsur
penting dalam pembentukan keputusan dalam pemilihan intervensi klinis yang paling cocok.
Pertanyaan yang juga harus dijawab sebelum memutuskan terapi yaitu apakah isolat bakteri
menunjukkan suatu infeksi atau kolonisasi.
Untuk membedakan suatu infeksi dari kolonisasi, dapat dilihat dari berbagai hal, a) asal
spesimen (isolat dari spesimen yang secara fisiologis steril seperti darah, cairan bronko alveolar,
biopsi jaringan harus dipertimbangkan secara serius; namun isolat dari lokasi yang tidak steril,
seperti apusan dari luka kronis, sputum sepertinya lebih mengarah ke kolonisasi; isolat dari
spesimen kateter dari urin biasanya menampilkan suatu kolonisasi dibandingkan isolat dari urin
porsi tengah; namun, isolat dari kateter intravena meskipun dapat berupa kolonisasi tetapi harus
dianggap sebagai sumber potensial untuk infeksi sistemik), b) parameter inflamasi dari pasien-
adanya gangguan dari parameter ini, c) keadaan umum pasien, seperti temperatur, tekanan darah,
frekuensi nadi, saturasi oksigen, kebutuhan akan inotropik, dan alat penyokong hidup.
Faktor-faktor ini harus dilihat secara menyeluruh, dan tidak terpisah-pisah, dan perubahan dari
parameter diagnostik lebih signifikan daripada suatu nilai tunggal.
A. Pendekatan non farmakologis
Pendekatan tanpa antibiotik dalam manajemen infeksi ESBL merupakan suatu langkah
kritis dalam terapi. Eliminasi dari sumber infeksi adalah manajemen penting dari infeksi, tidak
terkecuali infeksi ESBL. Jika sumber infeksi merupakan benda asing seperti alat prostetik,
penggantian atau pengeluaran alat prostetik itu menjadi sangat penting. Hal ini disebabkan
karena infeksi ESBL dihubungkan dengan tindakan operasi implan atau alat-alat lainnya, dengan
terbentuknya biofilm. Pertumbuhan bakteri yang lambat, yang diikuti dengan penetrasi antibiotik
yang terhalang oleh biofilm ini menyebabkan eradikasi dan terapi dari infeksi yang berhubungan
dengan implan ini menjadi sulit.20 Pendekatan non farmakologis dalam manajemen infeksi ESBL termasuk penggantian jalur intravaskular yang terkolonisasi (central venous catheter, peripheral venous catheter), kateter urin yang terkolonisasi, drainase dari abses intra abdominal maupun intra viseral lainnya, dan pengeluaran dari katup jantung atau sendi buatan. Hal ini menunjukkan
bahwa pemberian antibiotik saja dalam infeksi ESBL yang terkait dengan alat-alat implan tidak
memberikan hasil klinis yang baik.21
B. Pendekatan Farmakologis
Pilihan antibiotik pada pasien dengan infeksi ESBL menjadi berkurang dengan adanya
kemampuan bakteri tersebut menghidrolisis beberapa antibiotik. Infeksi ESBL umumnya resisten
terhadap antibiotik beta laktam termasuk sefalosforin, aztreonam dan penisilin. Selain itu
resistensi terhadap antibiotik lain juga terjadi seperti trimetroprim-sulfametoksazol,
aminogikosida khususnya gentamisin.
Pilihan antibiotik idealnya adalah berdasarkan hasil kultur, tetapi seperti yang disebutkan
sebelumnya hasil kultur memerlukan waktu dan tidak semua fasilitas kesehatan memilikinya.
Pada hasil kultur umumnya diperoleh beberapa jenis antibiotik yang sensitif terhadap bakteri
Tabel 2.4 Rekomendasi pengobatan22
Tipe infeksi Pilihan terapi Terapi second-line Infeksi traktus urinarius
Dikutip dari: Rishi dkk, Critical Care Research and Practice, 2012
Berikut ini dipaparkan kemampuan beberapa golongan antibiotik terhadap infeksi bakteri
ESBL:
2.5.1 Karbapenem
Karbapenem merupakan antibiotik pilihan pada infeksi ESBL, yang termasuk dalam
golongan karbapenem adalah imepenem, meropenem, erapenem, dan doripenem. Pemilihan
antara imipenem dan meropenem sukar dilakukan karena memiliki profil yang hampir sama.
Pada meningitis meropenem merupakan pilihannya. Ertapenem pada beberapa penelitian lebih
baik dari pada meropenem dan imipenem dan penggunaannya hanya sekali sehari.4 Doripenem merupakan golongan karbapenem terbaru yang lebih poten dan dapat digunakan untuk infeksi
Pseudomonas aeruginosa. Penelitian yang membandingkan kombinasi karbapenem dengan
antibitik golongan lain dibandingkan karbapenem tunggal diperoleh hasil yang tidak berbeda.
Penelitian oleh Paterson, penggunaan karbapenem sebagai terapi inisial untuk ESBL selama 5
hari memiliki angka mortalitas yang lebih rendah.23
Dari penelitian oleh Muharrmi dkk, diperoleh karbepenem (imipenem dan meropenem)
100% sensitif terhadap ESBL.24 Hasil serupa juga diperoleh pada penelitian oleh Kulkarni dkk, Aminzadeh dkk, imepenem 100% sensitif terhadap ESBL.23,25 Chien Lye dkk meneliti pada 47 pasien ESBL dengan sumber infeksinya saluran kemih, hepatobilier dan akses vaskular yang
diterapi dengan ertapenem, memiliki respon yang baik pada 96% pasien.26 Penelitian Auer dkk, ertapenem 100% sensitif terhadap infeksi saluran kemih ESBL E.coli.27 Adapun dosis standar pada dewasa meropenem 1 gram setiap 8 jam intravena, imipenem 500 mg 4 kali sehari
muncul dengan nama Klebsiella Producing Carbapenemases (KPC) dan New Delhi Metalo Beta Lactamase (NDM) sehingga penggunaannya haruslah rasional.29
2.5.2 Βeta lactam/Βeta lactamase inhibitor
Βeta lactamase inhibitor merupakan antibiotik yang ideal untuk ESBL karena memiliki kemampuan menghambat enzim beta laktamase, namun banyaknya mutasi yang terjadi pada
enzim beta laktamase mengakibatkan berkurangnya efektivitas antibiotik beta lactamase inhibitor ini. Oleh karena itu, antibiotik beta lactam/beta lactamase inhibitor dapat digunakan untuk ESBL yang tidak berat. Amoksisilin/Klavulanat efektif untuk infeksi saluran kemih
komunitas akibat ESBL. Tazobaktam lebih efektif terhadap ESBL CTX-M dibandingkan beta
lactam lainnya dan sulbaktam lebih baik terhadap SHV dan TEM, namun pada labolatorium
sederhana pemeriksaan fenotif ini sulit dilakukan.6,29 Penelitian Rodriquez-Bano dkk, penggunaan amoxicillin/clavulanat selama 5-7 hari pada indeksi saluran kemih tanpa komplikasi
memiliki angka kesembuhan 84%.30 Adapun dosis standar pada dewasa amoxicillin-clavulanat 625 mg/1,2 mg /8 jam baik oral maupun intravena.28
Piperasilin-tazobactam memiliki kerentanan yang bervariasi terhadap ESBL. Penelitian
Muharrmi dkk memperoleh 64,4% sensitif terhadap ESBL E.coli dan 43,6% terhadap ESBL
K.pneumonia.31 DiAmerika Serikat dari hasil MYSTIC Study diperoleh 72,5% sensitif ESBL
E.coli dan 38,5% terhadap ESBL K.pneumonia, sedangkan di Eropa 80% ESBL E.coli dan 42,1 % terhadap ESBL K.pneumonia.31 Kemampuan eradikasinya meningkat dengan mengkombinasi-kannya dengan obat lain seperti dengan amikasin atau gentamisin. Piperasilin-tazobactam
dikombinasikan dengan amikasin 98,1% sensitif terhadap ESBL E.coli dan 93,1 % terhadap ESBL K.pneumonia. Sedangkan kombinasi Piperasilin-tazobactam dengan gentamisin 73,1% sensitif terhadap ESBL E.coli dan 61,4% terhadap ESBL K.pneumonia.26Penelitian Aminzadeh dkk, Piperasilin-tazobactam 100% sensitif terhadap ESBL.23 Adapun dosis standar pada dewasa 4,5 gr setiap 8jam intravena.28
2.5.3 Aminoglikosida
Aminoglikosida yang sering digunakan untuk indeksi bakteri ESBL adalah gentamisin
Muharrmi dkk, memperoleh 38,3% sensitif terhadap ESBL E.coli dan 37,6% terhadap ESBL
K.pneumonia.25 Penelitian Kulkarni dkk, gentamisin 19,4% sensitif terhadap ESBL.25 Penelitian Aminzadeh dkk, gentamisin 85,2% resisten terhadap ESBL.23 Adapun dosis standar pada dewasa 5 mg/KgBB perhari intravena.28
Amikasin memiliki kerentanan yang bervasriasi. Penelitian Muharrmi dkk memperoleh
kerentanan 94% terhadap ESBL (95,2% sensitif terhadap ESBL E.coli dan 90,1% terhadap ESBL K.pneumonia).24 Penelitian Kulkarni dkk, amikasin 70,4% sensitif terhadap ESBL.26Penelitian Aminzadeh dkk, amikasin 81,1% sensitif terhadap ESBL.23 Adapun dosis standar pada dewasa 15 mg/KgBB perhari terbagi dalam dua dosis intravena.28
2.5.4 Kuinolon
Bakteri ESBL yang sensitif terhadap kuinolon dapat menggunakannya. Namun
belakangan semakin banyak dilaporkan adanya resistensi terhadap kuinolon pada bakteri ESBL
dengan penyebab yang belum sepenuhnya dipahami. Resistensi ini diduga akibat hilangnya porin
bakteri untuk masuknya kuionolon dan aktifnya efluks kuinolon keluar sel.10,29 Siprofloksasin memiliki kemampuan eradikasi ESBL yang rendah. Dari penelitian Muharrmi dkk, diperoleh
hanya 29,6% sensitif terhadap ESBL ( 24,9% E.Coli dan 39% K.Pneumonia).24MYSTIC Study di Amerika Serikat Siprofloksasin 20% sensitif terhadap ESBL E.coli dan 36,8% terhadap ESBL
K.pneumonia, sedangkan di Eropa 20,2% sensitif ESBL E.coli dan 57,5% ESBL
K.pneumonia.31 Kemampuan eradikasinya meningkat dengan mengkombinasikannya dengan
obat lain seperti dengan amikasin atau gentamisin. Siprofloksasin dikombinasikan dengan
amikasin memiliki 96,7% sensitif terhadap ESBL E.coli dan 91,1% terhadap ESBL
K.pneumonia. Sedangkan kombinasi siprofloksasin dengan gentamisin memiliki 41,2% sensitif ESBL E.Coli dan 51,5% ESBL K.Pneumonia.26Penelitian Kulkarni dkk, siprofloksasin 30,2% sensitif terhadap ESBL.25
2.5.5 Sefalosporin
Secara umum sefalosporin tidak direkomendasikan sebagai pengobatan ESBL. Antibiotik
golongan ini yang masi mungkin digunakan adalah cefepime, tetapi data klinis tidak mendukung
sefalosporin generasi 3 untuk infeksi ESBL memberikan hasil yang buruk walaupun hasil kultur
masih sensitif, sehingga tidak direkomendasikan digunakan sebagai pilihan pertama. Penelitian
Kulkarni dkk, cepefime hanya 17,2% sensitif terhadap ESBL.27
2.5.6 Nitrofurantoin
Nitrofurantoin dapat digunakan untuk infeksi saluran kemih yang tidak komplikasi.
Penelitian Kulkarni dkk, Nitrofurantoin 75% sensitif terhadap ESBL. Penelitian Aminzadeh
dkk, Nitrofurantoin 71,3% sensitif terhadap ESBL.21Penelitian Auer dkk, Nitrofurantoin 94% sensitif terhadap infeksi saluran kemih ESBL E.coli.24 Adapun dosis standar pada dewasa 50 mg setiap 6 jam oral.28
2.5.7 Fosfomisin
Fosfomisin merupakan antibiotik yang bekerja dengan menghambat UDP N Acetylglucosamine yang merupakan enzim pada proses pembentukan dinding bakteri. Falagas dkk melakukan suatu sistematik review dengan total sampel 4448 infeksi ESBL ditemukan bahwa fosfomisin sensitif pada 90% kasus. Penelitian Rodriquez-Bano dkk, penggunaan