PENGARUH PERBANDINGAN SURFAKTAN TWEEN 80 DAN KOSURFAKTAN PEG 400 DALAM FORMULASI SEDIAAN
MIKROEMULSI ASKORBIL PALMITAT DAN ALFA
TOKOFEROL UNTUK ANTIAGING
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh:
Elizabeth Sita Permata Sari Sucipto Putri
NIM : 108114165
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH PERBANDINGAN SURFAKTAN TWEEN 80 DAN KOSURFAKTAN PEG 400 DALAM FORMULASI SEDIAAN
MIKROEMULSI ASKORBIL PALMITAT DAN ALFA
TOKOFEROL UNTUK ANTIAGING
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh:
Elizabeth Sita Permata Sari Sucipto Putri
NIM : 108114165
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Jangan mencari apa yang kamu takutkan melainkan carilah harapan dan impianmu. Jangan
berpikir tentang frustasimu, tetapi tentang potensi yang belum kamu kembangkan.
Perhatikan dirimu bukan pada apa yang telah kamu coba dan ternyata gagal, tetapi pada
segala sesuatu yang masih mungkin bagimu untuk melalukannya.
~ Paus Yohanes XXIII ~
Sebab rancangan-Ku bukanlah rancanganmu, dan jalanmu bukanlah jalan-Ku, demikianlah
firman Tuhan.
~ Yesaya 55:8 ~
Karya ini kupersembahkan untuk :
Tuhan Yesus Kristus,
Bapak dan Ibu tercinta,
Kedua Kakakku, Tia dan Vera
Kedua Keponakanku tersayang, Nathan dan Nolan
Sahabat-sahabatku,
vii PRAKATA
Puji dan syukur kepada Tuhan Yang Maha Esa atas kasih, berkat, dan
penyertaan-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul
“Pengaruh Perbandingan Surfaktan Tween 80 dan Kosurfaktan PEG 400 dalam
Formulasi Sediaan Mikroemulsi Askorbil Palmitat dan Alfa Tokoferol untuk
Antiaging” dengan baik. Skripsi ini disusun sebagai salah satu syarat untuk
memperoleh gelar Sarjana Farmasi (S.Farm.) di Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
Selama proses perkuliahan, penelitian, penyusunan dan penyelesaian
skripsi ini, penulis telah mendapatkan bantuan doa, dukungan, semangat, saran
dan kritik dari berbagai pihak. Oleh karena itu, penulis ingin mengucapkan terima
kasih kepada:
1. Orang tua atas doa, cinta, kasih sayang, perhatian, kebersamaan, kesabaran,
inspirasi, motivasi, saran, dan kritik yang diberikan kepada penulis.
2. Ibu Aris Widayati, M.Si., Ph.D., Apt, selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
3. Bapak Dr. T. N. Saifullah S., M.Si., Apt., selaku dosen pembimbing yang
telah banyak memberikan waktu, bimbingan, diskusi, kritik, dan saran kepada
penulis mulai dari proposal, penelitian, penyusunan hingga penyelesaian
skripsi ini.
4. Ibu C.M. Ratna Rini Nastiti, M. Pharm., Apt., selaku dosen penguji atas
kesediaannya meluangkan waktu untuk menjadi dosen penguji, serta
viii
5. Ibu Melania Perwitasari, M.Sc., Apt., selaku dosen penguji atas kesediaannya
meluangkan waktu untuk menjadi dosen penguji, serta memberikan
pengarahan, saran, dan kritik kepada penulis.
6. Segenap Dosen Fakultas Farmasi Universitas Sanata Dharma yang telah
mengajar dan membimbing Penulis selama perkuliahan.
7. Fransisca Kristi Astuti, dan Agrifina Akardias Mahalalita sebagai teman satu
tim penelitian atas kerja sama, bantuan, dan kebersamaan selama proses
skripsi ini.
8. Hendrika Putra Hastama atas perhatian, semangat, dukungan, saran dan kritik
yang diberikan kepada penulis.
9. Sahabat-sahabatku : Astuti Malyawati Susesanto, Marcelina Widani Amanda
Rompas, Rosalia Suryaningtyas, Eva Cristiana, Ayu Listiana, Rizki
Nugrahanto dan Candra Widiantoro atas semangat, dukungan, dan doa yang
diberikan kepada penulis.
10.Puspita Sari, Cindy Tiara Sari, Nita Rahayu dan teman-teman seperjuangan
atas kebersamaan dan motivasi yang diberikan kepada penulis selama proses
skripsi ini.
11.Pak Musrifin, Pak Suparlan, Mas Agung, Mas Kunto, Pak Wagiran, Mas
Ottok, Bapak-bapak satpam dan seluruh laboran serta karyawan lain di
Fakultas Farmasi Universitas Sanata Dharma yang telah banyak membantu
penulis selama penelitian.
12.Teman-teman FST 2010 atas kebersamaannya baik selama proses perkuliahan
ix
13.Semua pihak yang telah banyak membantu selama proses skripsi ini yang
tidak dapat disebutkan satu per satu.
Penulis sadar bahwa memiliki keterbatasan kemampuan dan pengetahuan
pada skripsi ini. Oleh karena itu, penulis sangat mengharapkan kritik dan saran
yang membangun dari berbagai pihak. Akhir kata, penulis berharap semoga
skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan, khususnya di
bidang farmasi.
x DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
HALAMAN PERNYATAAN KEASLIAN KARYA ... v
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvii
INTISARI ... xix
ABSTRACT ... xx
BAB I. PENGANTAR ... 1
A.Latar Belakang ... 1
B. Perumusan masalah ... 4
C.Keaslian penelitian... 4
D.Manfaat penelitian ... 5
E. Tujuan Penelitian ... 6
BAB II. PENELAAHAN PUSTAKA... 7
xi
B. Antioksidan ... 11
1. Definisi Antioksidan ... 11
2. Askorbil Palmitat Sebagai Antioksidan ... 12
3. Alfa Tokoferol Sebagai Antioksidan ... 14
4. Interaksi Askorbil palmitat dan Alfa tokoferol sebagai Antioksidan 15 C.Mikroemulsi ... 16
1. Definisi Mikroemulsi ... 16
2. Teori Pembentukan Mikroemulsi ... 17
3. Komponen Penyusun Mikroemulsi ... 19
4. Kontrol Kualitas Mikroemulsi ... 21
BAB III. METODE PENELITIAN... 33
xii
B. Variabel Penelitian dan Definisi Operasional... 33
1. Variabel penelitian ... 33
4. Evaluasi Sifat Fisik Sediaan Mikroemulsi Hasil Percobaan Utama .. 41
5. Uji Stabilitas Fisik ... 44
6. Uji Aktivitas Antioksidan ... 45
7. Uji Iritasi ... 50
F. Analisis Hasil ... 51
BAB IV. HASIL DAN PEMBAHASAN ... 52
A.Percobaan Pendahuluan Basis Mikroemulsi ... 52
B. Evaluasi Sifat Fisik Sediaan Mikroemulsi Hasil Percobaan Utama ... 54
1. Pemeriksaan Organoleptis dan pH ... 55
2. Pemeriksaan Tipe Mikroemulsi ... 57
3. Pengukuran Indeks Bias ... 58
4. Pengukuran Bobot Jenis ... 59
5. Pengukuran Persen Transmitansi ... 60
xiii
7. Pengukuran Ukuran Droplet ... 62
C.Stabilitas Fisik Sediaan Mikroemulsi ... 63
1. Stabilitas Organoleptis Sediaan Mikroemulsi setelah Freeze Thaw .. 64
2. Stabilitas pH Sediaan Mikroemulsi setelah Freeze Thaw... 65
3. Stabilitas Transmitansi Sediaan Mikroemulsi setelah Freeze Thaw.. 66
4. Stabilitas Viskositas sediaan mikroemulsi setelah freeze thaw ... 66
5. Stabilitas Ukuran Droplet Sediaan Mikroemulsi setelah Freeze Thaw 67 D.Aktivitas Antioksidan Sediaan Mikroemulsi ... 68
1. Penentuan Panjang Gelombang Maksimum ... 68
2. Penentuan Operating Time (OT) ... 69
3. Aktivitas Antioksidan Sediaan Mikroemulsi ... 71
E. Uji Iritasi Sediaan Mikroemulsi ... 74
BAB V. KESIMPULAN DAN SARAN ... 76
A.Kesimpulan ... 76
B. Saran ... 76
DAFTAR PUSTAKA ... 77
LAMPIRAN ... 82
xiv
DAFTAR TABEL
Tabel I. Tingkat kekuatan aktivitas antioksidan dengan metode DPPH .. 26
Tabel II. Hubungan iritation score dengan kategori iritasi ... 27
Tabel III. Formula acuan mikroemulsi ... 36
Tabel IV. Formula orientasi basis mikroemulsi ... 36
Tabel V. Formula sediaan mikroemulsi ... 40
Tabel VI. Hasil uji pendahuluan ... 52
Tabel VII. Hasil pengamatan setelah uji heating and cooling ... 53
Tabel VIII. Hasil pengamatan organoleptis dan pH sediaan mikroemulsi .... 55
Tabel IX. Hasil pengamatan indeks bias sediaan mikroemulsi ... 58
Tabel X. Hasil pengukuran ukuran droplet mikroemulsi formula A pada siklus ke-0 ... 63
Tabel XI. Hasil pengukuran ukuran droplet mikroemulsi formula A pada siklus ke-0 dan siklus ke-3 ... 68
Tabel XII. Hasil uji aktivitas antioksidan ... 72
xv
DAFTAR GAMBAR
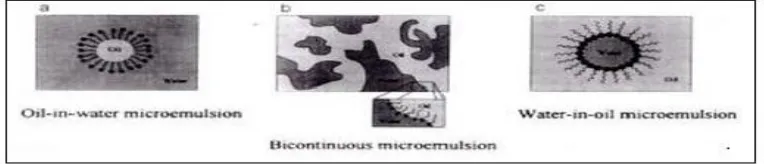
Gambar 1. Tipe sistem dispersi mikroemulsi ... 16
Gambar 2. Struktur DPPH radikal (1), struktur DPPH non radikal ... 25
Gambar 3. Struktur Ascorbyl Palmitate ... 27
Gambar 4. Struktur Alpha Tocopherol ... 28
Gambar 5. Struktur Polysorbate 80 (tween 80) ... 29
Gambar 6. Struktur PEG 400 ... 30
Gambar 7. Hasil uji viskositas uji pendahuluan ... 54
Gambar 8. a) Mikroemulsi yang dilarutkan dalam aquadest, (b) Mikroemulsi yang dilarutkan dalam minyak zaitun ... 57
Gambar 9. Hasil uji bobot jenis sediaan mikroemulsi ... 59
Gambar 10. Hasil uji persen transmitansi sediaan mikroemulsi ... 60
Gambar 11. Hasil uji viskositas sediaan mikroemulsi ... 61
Gambar 12. Grafik distribusi ukuran droplet sediaan mikroemulsi formula A 63 Gambar 13. Penampilan fisik seluruh formula sediaan mikroemulsi sesudah dan sebelum uji sentrifugasi ... 64
Gambar 14. Profil kurva pH sediaan mikroemulsi tiap siklus freeze thaw .... 65
Gambar 15. Profil kurva persen transmitansi sediaan mikroemulsi tiap siklus freeze thaw ... 66
xvi
Gambar 17. Grafik distribusi ukuran droplet sediaan mikroemulsi formula A
pada siklus ke-3 ... 68
Gambar 18. Profil kurva operating time askorbil palmitat, alfa tokoferol
serta campuran Askorbil Palmitat dan Alfa Tokoferol ... 70
Gambar 19. Profil kurva operating time formula A, formula B, formula C,
formula D, dan formula E ... 71
Gambar 20. Profil kurva operating time basis A, basis B, basis C, basis D,
xvii
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat analisis Askorbil Palmitat dari CV.Privat Equipment 83
Lampiran 2. Sertifikat analisis Alfa Tokoferol dari CV. Cipta Anugerah .... 84
Lampiran 3. Sertifikat analisis Minyak zaitun dari CV. Sofa Mediteranian . 85
Lampiran 4. Sertifikat analisis Tween 80 dari PT. Brataco Chemika ... 86
Lampiran 5. Sertifikat analisis PEG 400 dari PT. Brataco Chemika ... 87
Lampiran 6. Data Pengamatan Organoleptis Sediaan Mikroemulsi ... 88
Lampiran 7. Dokumentasi Pengamatan Organoleptis Sediaan Mikroemulsi 89
Lampiran 8. Data Sifat Fisik dan Stabilitas Fisik Sediaan Mikroemulsi ... 90
Lampiran 9. Hasil Pengamatan Ukuran Droplet Formula A ... 92
Lampiran 10. Analisis Statistika Sifat Fisik Mikroemulsi Menggunakan
Program R. 3.0.1 ... 94
Lampiran 11. Analisis Statistika Stabilitas Fisik Mikroemulsi Menggunakan
Program R. 3.0.1 ... 97
Lampiran 12. Perhitungan Irritation Score (IS)... 102
Lampiran 13. Pengamatan Uji Iritasi Mikroemulsi Menggunakan Metode
HET-CAM ... 103
Lampiran 14. Pengujian Aktivitas Antioksidan standar Askorbil palmitat .... 104
Lampiran 15. Pengujian Aktivitas Antioksidan standar Alfa tokoferol ... 107
Lampiran 16. Pengujian Aktivitas Antioksidan Campuran Askorbil palmitat
dan Alfa tokoferol ... 109
xviii
Lampiran 18. Pengujian Aktivitas Antioksidan Mikroemulsi Formula B ... 114
Lampiran 19. Pengujian Aktivitas Antioksidan Mikroemulsi Formula C ... 117
Lampiran 20. Pengujian Aktivitas Antioksidan Mikroemulsi Formula D ... 120
Lampiran 21. Pengujian Aktivitas Antioksidan Mikroemulsi Formula E ... 122
Lampiran 22. Aktivitas Antioksidan Basis Mikroemulsi Formula A ... 125
Lampiran 23. Aktivitas Antioksidan Basis Mikroemulsi Formula B ... 127
Lampiran 24. Aktivitas Antioksidan Basis Mikroemulsi Formula C ... 130
Lampiran 25. Aktivitas Antioksidan Basis Mikroemulsi Formula D ... 132
xix INTISARI
Sifat fisik dan stabilitas fisik mikroemulsi dipengaruhi oleh surfaktan dan kosurfaktan sebagai penyusunnya serta komposisi keduanya. Penelitian ini bertujuan untuk melihat pengaruh perbandingan komposisi surfaktan dan kosurfaktan terhadap sifat fisik dan stabilitas fisik mikroemulsi askorbil palmitat dan alfa tokoferol, serta daya antioksidan dan potensi iritasinya.
Pada penelitian ini dibuat lima formula tengan perbandingan antara tween 80 : PEG 400 yaitu : 2:1, 3:1, 4:1, 5:1, dan 6:1. Seluruh formula diuji sifat fisik meliputi organoleptis, tipe mikroemulsi, bobot jenis, indeks bias, pH, transmitansi, viskositas, dan ukuran droplet. Stabilitas fisik diuji dengan metode sentrifugasi dan freeze thaw, mengamati perubahan organoleptis, pH, transmitansi, viskositas, dan ukuran droplet sebelum dan sesudah freeze thaw. Data dianalisis secara statistik menggunakan menggunakan uji ANOVA satu arah dengan taraf kepercayaan 95% dengan software R3.0.1.. Sediaan diuji HET-CAM untuk mengamati potensi iritasi, sementara aktivitas antioksidan diuji menggunakan metode DPPH.
Hasil penelitian menunjukkan bahwa semakin tinggi perbandingan tween 80 dan PEG 400 berpengaruh signifikan pada viskositas dan pH, namun tidak berpengaruh signifikan terhadap organoleptis, bobot jenis, transmitansi, dan indeks bias sediaan mikroemulsi yang dihasilkan. Seluruh formula menghasilkan mikroemulsi yang stabil dan tidak mengiritasi. Sediaan mikroemulsi askorbil palmitat dan alfa tokoferol memiliki kemampuan antioksidan yang sangat kuat.
xx ABSTRACT
Physical properties and physical stability of microemulsion can be affected by the surfactant and the cosurfactant constituent and composition of both of them. This study aimed to investigate the effect of surfactant and cosurfactant ratio on the physical properties and physical stability of the microemulsion ascorbyl palmitate and alpha tocopherol. It also aimed to observe the antioxidants activity and irritation risk of the microemulsion.
In this study a comparison was made of five formulas between tween 80: PEG 400, the comparison are : 2: 1, 3: 1, 4: 1, 5: 1 and 6: 1. All formula were tested in terms of physical properties including organoleptic observation, microemulsion type, specific gravity, refractive index, pH, transmittance, viscosity, and droplet size. Physical stability was tested by using centrifugation and freeze thaw method, observing the changes in organoleptic parameter, pH, transmittance, viscosity, and droplet size before and after freeze thaw treatment. Data were statistically analyzed by one-way ANOVA with 95% level of confidence using the software of R3.0.1.. Irritation potential was tested by using HET-CAM method, while antioxidant activity by DPPH method.
The results showed that the increase of the ratio of tween 80 and PEG 400 increased the viscosity and pH, but gave no significant effect on the organoleptic, specific gravity, transmittance, and the refractive index of the resulting microemulsion preparation. All formulas produce stable microemulsion without any irritation risk. Moreover the microemulsion of ascorbyl palmitate and alpha tocopherol showed very strong antioxidant activity.
1 BAB I PENGANTAR
A. Latar Belakang
Penuaan atau aging merupakan suatu proses fisiologis yang pasti akan
dialami oleh setiap makhluk hidup dengan kecepatan yang berbeda, dikarenakan
oleh faktor fisiologis tiap individu yang berbeda. Namun, hal ini dapat dipicu oleh
hal-hal yang berasal dari luar yang dapat menyebabkan penuaan berjalan lebih
cepat, salah satunya radikal bebas. Untuk melawan radikal bebas ini diperlukan
suatu senyawa yang memiliki daya antioksidan, seperti askorbil palmitat and alfa
tokoferol.
Vitamin E atau alfa tokoferol merupakan salah satu antioksidan utama
yang bekerja dengan memecah rantai radikal bebas di dalam membran sehingga
mengakibatkan inaktivasi radikal peroksil di sekitar membran dan dengan
demikian menghambat peroksidasi lipid. Vitamin E memiliki fungsi lain, yaitu
fotoproteksi dan melembabkan kulit (Baumann, 2009). Askorbil palmitat
memiliki aktivitas sama seperti asam askorbat yaitu merupakan antioksidan kuat
karena dapat menyumbangkan atom hidrogen dan sebagai scavenger ROS dan
RNS, efektif melawan ion radikal superoksida, dan hidrogen peroksida (Padayatty
et al., 2003). Selain itu, juga berfungsi sebagai ko-faktor biosintesis kolagen
sehingga dapat mengembalikan elastisitas kulit dan menyamarkan keriput. Kedua
vitamin tersebut memiliki kerja yang saling mendukung dalam melawan radikal
topikal memiliki masalah kestabilan dan penetrasinya menembus barier kulit,
serta kelarutannya yang sedikit berbeda.
Sediaan yang sesuai untuk memformulasikan keduanya ialah sediaan
emulsi. Namun, emulsi memiliki beberapa kelemahan diantaranya kurang mampu
untuk menghantarkan zat aktif masuk kedalam lapisan kulit karena ukuran
dropletnya yang cukup besar, hal ini kurang efektif bila digunakan untuk sediaan
kosmetik yang ditujukan untuk anti penuaan dini serta sifatnya yang tidak stabil
secara termodinamika. Perkembangan ilmu pengetahuan telah didapat suatu
bentuk sediaan yang merupakan pengembangan dari bentuk emulsi itu sendiri
yaitu mikroemulsi.
Mikroemulsi memiliki sistem isotropik yang stabil secara
termodinamika, yang terdiri dari dua fase cairan air dan minyak membentuk fase
tunggal. Mikroemulsi memiliki kelebihan diantaranya adalah dapat meningkatkan
kelarutan suatu senyawa karena dapat berperan sebagai super solven, stabil secara
termodinamika, jernih dan dapat meningkatkan penetrasi suatu senyawa.
Mikroemulsi dapat mencapai kestabilannya dengan bantuan surfaktan dan
kosurfaktan. Surfaktan dalam mikroemulsi berperan dalam menurunkan tegangan
antar muka hingga sangat rendah dan membuat energi bebas permukaan
mendekati nol. Namun, dalam kebanyakan formulasi mikroemulsi, surfaktan saja
belum mampu untuk membentuk suatu sistem mikroemulsi sehingga perlu
ditambahkan suatu kosurfaktan. Kosurfaktan berperan membantu kerja surfaktan
dalam mengurangi tegangan permukaan dan meningkatkan entropi dari sistem
kosurfaktan yang sering dipakai adalah tween, span, PEG, propilen glikol, dan
alkohol rantai pendek.
Surfaktan dan kosurfaktan yang dipilih dalam penelitian ini adalah tween
80 dan PEG 400. Tween 80 merupakan surfaktan yang paling sering digunakan,
selain itu, tween 80 juga memiliki nilai toksisitas yang lebih rendah dari surfaktan
lain serta tidak bersifat iritatif terhadap kulit. Selain itu, tween 80 memiliki
kandungan asam oleat sama seperti minyak zaitun yang mengandung lebih dari
50% asam oleat, persamaan kandungan asam oleat ini membuat tween 80 dapat
membentuk sistem mikroemulsi (Mahdi et al., 2011). PEG 400 dipilih sebagai
kosurfakan karena senyawa ini mampu mengurangi teganggan permukaan,
meningkatkan entropi sistem serta dapat meningkatkan kelarutan zat yang sukar
larut dalam air. Kedua bahan tersebut sering digabungkan untuk membentuk suatu
sediaan mikroemulsi yang baik dan stabil.
Mikroemulsi sangatlah kompleks dengan sistem mikrostruktur yang
dapat berubah bila terjadi sedikit penyimpangan dari formulasi yang sesuai untuk
pembentukan mikroemulsi dapat menyebabkan perubahan yang drastis dari
karakteristik fisiknya (Pathan et al., 2012). Proporsi antara surfaktan, kosurfaktan,
minyak dan air dalam sediaan mikroemulsi sangat menentukan terbentuknya
mikroemulsi yang stabil. Oleh karena itu, diperlukan suatu penelitian untuk
mengetahui pengaruh komposisi tween 80 sebagai surfaktan dan PEG 400 sebagai
kosurfaktan terutama terhadap formulasi sediaan mikroemulsi untuk
menghasilkan sediaan mikroemulsi yang baik dan stabil. Penelitian pengaruh
mikroemulsi askorbil palmitat dan alfa tokoferol untuk antiaging diharapkan
dapat diketahui pengaruh dari perbandingan surfaktan (tween 80) dan kosurfaktan
(PEG 400) dalam menghasilkan sediaan mikroemulsi yang memenuhi syarat sifat
fisik dan stabilitas fisik dalam kondisi ekstrim penyimpanan yang baik.
B. Perumusan Masalah
Berdasarkan latar belakang tersebut, maka dirumuskan permasalahan
dalam penelitian sebagai berikut :
1) Apakah perbandingan tween 80 sebagai surfaktan dan PEG 400 sebagai
kosurfaktan berpengaruh terhadap sifat fisik sediaan mikroemulsi askorbil
palmitat dan alfa tokoferol serta bagaimanakah pengaruhnya ?
2) Apakah perbandingan tween 80 sebagai surfaktan dan PEG 400 sebagai
kosurfaktan berpengaruh terhadap stabilitas fisik sediaan mikroemulsi
askorbil palmitat dan alfa tokoferol dalam kondisi ekstrim penyimpanan
serta bagaimanakah pengaruhnya ?
3) Apakah sediaan mikroemulsi askorbil palmitat dan alfa tokoferol memiliki
aktivitas antioksidan ?
4) Apakah sediaan mikroemulsi askorbil palmitat dan alfa tokoferol memiliki
potensi mengiritasi ?
C. Keaslian Penelitian
Sejauh penelusuran pustaka dari beberapa sumber yang dilakukan
80 dan kosurfaktan PEG 400 dalam formulasi sediaan mikroemulsi askorbil
palmitat dan alfa tokoferol untuk angiaging “ belum pernah dilakukan.
Penelitian terkait mengenai vitamin C dan vitamin E yang
diformulasikan sebagai sediaan mikroemulsi yang pernah dilakukan dengan :
Temperature-Sensitive Microemulsion Gel: An Effective Topical Delivery
System for Simultaneous Delivery of Vitamins C and E (Rozman et al., 2008),
serta Simultaneous absorption of vitamins C and E from topical
microemulsions using reconstructed human epidermis as a skin model
(Rozman et al., 2009).
Penelitian terkait formulasi sediaan mikroemulsi dengan minyak
zaitun, tween 80 dan PEG 400 yang pernah dilakukan adalah Design and
Characterization of Self Emulsifying Drug Delivery System of Repaglinide
(Kundarapu et al, 2013), serta Formulation Development & Characterization
of Microemulsion Drug delivery systems Containing Antiulcer drug (Jha et al,
2010).
D. Manfaat Penelitian
1. Manfaat teoritis.
Penelitian ini diharapkan dapat memberikan sumbangan ilmiah terhadap
ilmu pengetahuan terutama mengenai pengaruh perbandingan tween 80
sebagai surfaktan dan PEG 400 sebagai kosurfaktan terhadap formulasi
dan evaluasi sediaan mikroemulsi askorbil palmitat dan alfa tokoferol
2. Manfaat praktis.
Penelitian ini diharapkan dapat menghasilkan sediaan mikroemulsi anti
aging dengan zat aktif askorbil palmitat dan alfa tokoferol yang memiliki
sifat fisik dan stabilitas yang baik serta memiliki kemampuan antioksidan
dan tidak bersifat iritatif yang bermanfaat bagi masyarakat.
E. Tujuan Penelitian
1. Untuk mengetahui pengaruh perbandingan tween 80 sebagai surfaktan dan
PEG 400 sebagai kosurfaktan terhadap sifat fisik sediaan mikroemulsi
askorbil palmitat dan alfa tokoferol.
2. Untuk mengetahui pengaruh perbandingan tween 80 sebagai surfaktan dan
PEG 400 sebagai kosurfaktan terhadap stabilitas fisik sediaan mikroemulsi
askorbil palmitat dan alfa tokoferol dalam kondisi ekstrim penyimpanan.
3. Untuk mengetahui kemampuan antioksidan dalam bentuk IC50 dari sediaan
mikroemulsi askorbil palmitat dan alfa tokoferol.
4. Untuk mengetahui sifat iritatif sediaan mikroemulsi askorbil palmitat dan alfa
7 BAB II
PENELAAHAN PUSTAKA
A. Penuaan (Aging)
Penuaan adalah suatu proses menjadi tua, yang merupakan proses
fisiologis yang pasti akan terjadi pada semua makhluk hidup dengan kecepatan
yang berbeda, dan terjadi setelah masa pertumbuhan berhenti. Pada orang tertentu
penuaan terjadi sesuai dengan usianya sedangkan pada orang lain datangnya lebih
cepat, keadaan ini disebut penuaan dini (premature aging) (Jusuf, 2005).
Cunnningham (2003) menjabarkan proses penuaan pada kulit terjadi
dengan dua macam proses yang saling berkaitan satu sama lain, yaitu :
a. Proses intrinsik (true aging, chronological aging)
Proses ini merupakan proses fisiologis yang berjalan alami seiring
dengan pertambahan usia seseorang yang disebabkan dan dipicu oleh
faktor-faktor dari dalam tubuh, seperti faktor genetik dan hormonal.
b. Proses ekstrinsik (entrinsic aging)
Merupakan proses penuaan yang berjalan lebih cepat dan
menjadikannya tidak sesuai dengan usia yang dipengaruhi oleh faktor dari
luar tubuh, seperti sinar matahari, kelembaban udara dan radikal bebas.
Proses serta mekanisme pasti terjadinya penuaan belum diketahui hingga
proses penuaan. Banyak teori penuaan yang berkembang seperti teori kerusakan
DNA, teori endokrin, teori telomer, dan teori radikal bebas.
a. Teori Kerusakan DNA
Teori ini mengemukakan bahwa proses penuaan merupakan akibat
akumulasi kesalahan pada replikasi DNA, sehingga mengakibatkan kematian
sel (Jusuf, 2005). Mitokondrial DNA (mtDNA) yang berperan dalam
mekanisme perbaikan DNA yang rusak banyak mengalami mutasi sehingga
mekanisme perbaikan DNA yang rusak menjadi berkurang. Paparan kronis
dari UVA dapat menyebabkan delesi pada mtDNA pada fibroblast dermis
yang merupakan salah satu penyebab photoaging (Murina et al., 2012).
b. Teori Telomer
Telomer membentuk ujung kromosom dan melindungi kromosom
serta membentuk cap dari protein. Pemendekan telomer pada setiap siklus
pembelahan sel menstimulasi respon perbaikan DNA dan menyebabkan
apoptosis. Radiasi UV meningkatkan gangguan telomer yang mengakibatkan
telomer tidak dapat mengalami pemendekan sehingga proses perbaikan DNA
dan apoptosis pada sel yang rusak terganggu seperti yang terjadi pada sel
kanker (Makrantonaki et al., 2010). Namun, Murina et al., (2012)
menyatakan bahwa hilangnya kemampuan telomer bukan faktor dominan
dalam penuaan kulit.
c. Teori Endokrin
Teori ini mengatakan bahwa bertambahnya usia menyebabkan
hormon-hormon tertentu yang bertugas untuk meregenerasi sel-sel, seperti hormon-hormon
pertumbuhan, hormon estrogen serta hormon progesteron (Jusuf, 2005).
d. Teori Radikal Bebas
Teori ini merupakan teori yang paling banyak diterima sebagai
penyebab penuaan dini, karena akumulasi kerusakan oleh radikal bebas dalam
sel. Radikal bebas adalah atom atau molekul yang mempunyai elektron yang
tidak berpasangan pada orbital terluarnya dan dapat berdiri sendiri. Bahan
radikal bebas dalam tubuh paling banyak berasal dari oksigen yang disebut
sebagai senyawa oksigen reaktif (reactive oxygen species/ROS). Sebagian
diantaranya berbentuk radikal seperti radikal hidroksil (●OH), radikal
peroksil (●OOH), dan ion superoksida (O2-●). Sebagian yang lain bukan
radikal, seperti singlet oksigen (1O2), hidrogen peroksida (H2O2) dan ion
hipoklorit (ClO-) (Clarkson et al., 2000).
Radikal bebas memiliki sifat reaktifitas tinggi dan dapat merubah
molekul menjadi suatu radikal, sehingga menyebabkan kerusakan sel,
gangguan fungsi sel, bahkan kematian sel. Radikal bebas ini akan merusak
enzim superoksida-dismutase (SOD) yang berfungsi mempertahankan fungsi
sel sehingga fungsi sel menurun dan menjadi rusak (Cunnningham, 2003).
tekanan oksidatif (oxidative stress) merupakan suatu keadaan dimana tingkat
oksigen reaktif yang toksik melebihi pertahanan antioksidan endogen.
Keadaan ini mengakibatkan kelebihan radikal bebas, yang akan bereaksi
dengan lemak, protein, asam nukleat dan transduksi sinyal. Lipid merupakan
poly unsaturated fatty acid (PUFA) (Birben et al., 2012). Proses peroksidasi
lipid dapat menghasilkan produk yang bersifat toksik, seperti 4-HNE
(4-hidroksi -2- nonenal) yang mampu menyerang dan merubah molekul biologis
penting seperti protein dan basa DNA yang dapat mengakibatkan berbagai
gangguan dan penyakit (Nikki, 2010).
Teori radikal bebas pada penuaan menunjukkan bahwa ROS
mengaktifkan sejumlah phosphorylase-mediated kinases, yang
mengakibatkan aktivasi jalur transduksi sinyal di seluruh epidermis. Jalur
transduksi sinyal ini salah satunya adalah mitogen-activated protein kinases,
seperti p38; c-jun N-terminal kinase; dan extracellular signal-regulated
kinases, yang mengakibatkan pengaktifan kompleks activator protein 1
(AP-1) nuklear transkripsi, yang merupakan heterodimer yang terdiri dari protein
c-jun dan c-fos. AP 1 bertanggung jawab dalam aktivasi gen
metalloproteinase matriks (MMP) (Murina et al., 2012).
Matriks metalloproteinase (MMP) adalah suatu zinc-dependent
endopeptidase yang terlibat dalam proses penyembuhan luka, turn over
matriks ekstraseluler, angiogenesis, dan kanker. Sejumlah MMP mampu
menimbulkan degradasi kolagen tipe I dan III, antara lain MMP-1, MMP-8,
MMP13, 14, 15, dan 16. Namun, pada kulit hanya
MMP-1 yang paling banyak dipicu pembentukannya oleh pajanan sinar UV dan
yang paling bertanggung jawab terhadap pemecahan kolagen akibat paparan
sinar matahari. Kolagenase ini memicu kejadian proteolitik yang
keseluruhan. Matriks metalloproteinase dapat dengan segera timbul hanya
dengan dosis minimal sinar UV. Ada suatu hubungan dosis dan respon yang
ditimbulkan antara paparan UV dan induksi MMP (Murina et al., 2012).
Sinar ultra violet juga mengaktifkan nuclear factor kappa B (NF -
kB), yaitu faktor transkripsi yang mempengaruhi ekspresi berbagai protein
serta memperburuk degradasi matriks kulit dengan cara meningkatkan kadar
1 dan 9. Degradasi matriks diperburuk dengan masuknya
MMP-8 (kolagenase) dari sumber neutrofil ke dalam kulit yang terpapar sinar UV
setelah infiltrasi neutrofil (Brennan, 2003).
Selain itu, radiasi sinar UV juga menganggu ekspresi gen dari
prokolagen jenis I dan III dalam dermal fibroblas dengan 2 mekanisme.
Pertama, radiasi UV menginduksi AP-1, sehingga menghambat transforming
growth factor β (TGF-β), suatu sitokin profibrotik yang meningkatkan
transkripsi gen-gen kolagen. Mekanisme kedua adalah membuat reseptor
TGF-β tidak dapat menanggapi TGF-β dengan demikian menghasilkan lebih
sedikit prokollagen tipe I (Murina et al., 2012).
B. Antioksidan 1. Definisi antioksidan
Antioksidan adalah zat yang dapat menetralkan radikal bebas dengan
mendonorkan elektron, dengan demikian dapat memperlambat atau bahkan
menghambat oksidasi dan melindungi tubuh dari beragam penyakit serta
kelompok, yaitu antioksidan enzimatik dan non-enzimatik. Antioksidan
enzimatik berperan untuk pertahanan tubuh terhadap radikal bebas dengan
menstabilkan atau deaktifasi radikal bebas, contoh dari antioksidan enzimatik
adalah superoksida dismutase (SOD), glutation peroksidase, glutation
reduktase, dan thioredoxin. Antioksidan non-enzimatik yang merupakan
scavangers ROS dan RNS, contoh dari antioksidan non enzimatik adalah
glutathione, vitamin A, C dan E (Birben et al., 2012).
Menurut Noori (2012), berdasarkan mekanisme kerjanya, antioksidan
dalam tubuh dikelompokkan menjadi 3 yakni:
1. Antioksidan primer, antioksidan ini bekerja untuk mencegah
pembentukan senyawa radikal baru, sebelum radikal bebas ini sempat
bereaksi. Contohnya: enzim SOD
2. Antioksidan sekunder, antioksidan ini bekerja menangkap senyawa serta
mencegah terjadinya reaksi berantai. Contoh: vitamin E, vitamin C,
betakaroten.
3. Antioksidan tersier, antioksidan ini berkerja memperbaiki kerusakan
sel-sel dan jaringan yang disebabkan radikal bebas. Contoh: enzim metionin
sulfoksidan reduktase untuk memperbaiki DNA pada inti sel.
2. Askorbil palmitat sebagai antioksidan
Aktivitas antioksidan dari askorbil palmitat merupakan aktivitas dari
asam askorbat itu sendiri, karena askorbil palmitat akan dimetabolisme tubuh
dan mengalami hidrolisis sehingga akan kembali menjadi bentuk semula yaitu
2012). Asam askorbat memiliki fungsi sebagai kofaktor enzim klasik
(hydroxylatingenzymes), agen protektif (sebagai hidroksilase pada biosintesis
kolagen), dan sebagai radikal askorbil dalam reaksi dengan metal ion transisi
(Padayatty et al., 2003). Asam askorbat juga sebagai kofaktor untuk aktivitas
enzimatik hidroksilase prolyl, sebuah enzim yang menghidrolisis residu prolyl
di prokolagen, elastin, dan protein lain sebelum pembentukan triple helix,
yang diperlukan untuk sintesis kolagen (Baumann, 2009).
Asam askorbat mampu bereaksi dengan radikal bebas, mengalami
oksidasi dengan kehilangan satu elektronnya. Oksidasi yang pertama
menghasilkan radikal bebas askorbil dan kemudian membentuk asam
dehidro-L-askorbid. Hidrolisis asam dehidroaskorbat menghasilkan asam
2,3-diketo-L-glukonat dimana akan mengalami dekarboksilasi menjadi CO2. Asam
askorbat dapat bereaksi dengan zat toksik, ROS anion superoksida (O2-) dan
radikal hidroksil (OH-). Reaksi inilah yang merupakan dasar dari sebagian
besar fungsi biologis esensial asam askorbat (Thiele et al., 2007). Radikal
askorbil dapat diregenerasi dengan beberapa jalur enzimatik dan NADPH
sebagai sumber energi. Tetapi, di dalam tubuh manusia, reduksinya hanya
terjadi secara parsial, sehingga asam askorbat yang terlah teroksidasi tidak
seluruhnya kembali (Padayatti, 2003).
Asam askorbat dapat menjadi antioksidan untuk lipid, protein, dan
DNA, dengan cara : (1) Untuk lipid, misalnya Low-Density Lipoprotein
(LDL), akan beraksi dengan oksigen sehingga menjadi lipid peroksida. Reaksi
proses radikal bebas. Asam askorbat akan bereaksi dengan oksigen sehingga
tidak terjadi interaksi antara lipid dan oksigen, dan akan mencegah terjadinya
pembentukan lipid hidroperoksida. (2) Untuk protein, asam askorbat
mencegah reaksi oksigen dan asam amino pembentuk peptida, atau reaksi
oksigen dan peptida pembentuk protein. (3) Untuk DNA, asam askorbat akan
mencegah reaksi DNA dengan oksigen akan menyebabkan kerusakan pada
DNA yang akhirnya menyebabkan mutasi (Padayatti, 2003).
3. Alfa tokoferol sebagai antioksidan
Vitamin E terdiri dari 2 jenis yaitu tokoferol dan tokotrineol.
Terdapat enam jenis tokoferol, α (alfa), ß (beta), γ (gama), δ (delta), ρ (eta), λ
(zeta) yang memiliki aktivitas bervariasi. Tokoferol yang memiliki aktifitas
terbesar adalah tokoferol alfa. Secara kimia, vitamin E (tokoferol) merupakan
turunan chromanol. Rantai hidrokarbon pada tokoferol berfungsi untuk
orientasi tokoferol di tempat aksinya, sedangkan bagian chromanol
memberikan sifat antioksidan dari tokoferol (Kretz et al., 2001).
Alfa tokoferol memiliki fungsi utama adalah sebagai antioksidan
alami pemecah rantai radikal bebas dan mencegah peroksidasi membran asam
lemak tak jenuh (PUFAs), karena alfa tokoferol dapat bersaing dengan radikal
peroksil lebih cepat dibanding PUFAs. Alfa tokoferol banyak digunakan untuk
mengatasi kulit kering, serta sebagai produk tabir surya (Baumann, 2009).
Riset membuktikan bahwa alfa tokoferol memberikan perlawanan terhadap
kekeringan pada kulit dengan menjadi pelembab natural pada kulit, namun
melembabkan dari vitamin E adalah dengan meningkatkan hidrasi pada kulit
atau sebagai humektan serta dengan membentuk barier lipid (Alencastre et al.,
2006).
Vitamin E dalam menjalankan fungsinya sebagai antioksidan
berubah bentuk menjadi suatu bentuk radikal semistabil, radikal tocopheroxyl.
Tidak seperti radikal bebas yang dibentuk dari PUFAs, radikal tocopheroxyl
relatif tidak reaktif sehingga dapat menghentikan proses penyebarluasan
perusakan oleh peroksidasi lipid (Fennema et al., 2004). Tocopheroxyl radikal
dapat mengalami beberapa kemungkinan reaksi, diantaranya : (1) radikal
tocopheroxyl dapat diubah kembali menjadi tokoferol melalui reaksi redoks
yang diperantarai oleh antioksidan lain seperti asam askorbat dan ubiquinon.
(2) Bereaksi dengan yang radikal tocopheroxyl lain untuk membentuk produk
non-reaktif seperti tokoferol dimer, (3) mengalami oksidasi lebih lanjut untuk
membentuk tocopherylquinone yang dapat tereduksi menjadi
α-tocopherylhydroquinone, yang dapat terkonjugasi dengan asam glukoronat
disekresikan dalam empedu, dan kemudian diekskresikan dalam feses
(eliminasi vitamin E), dan (4) bertindak sebagai prooksidan dan mengoksidasi
lipid lainnya (Rigel et al., 2004)
4. Interaksi askorbil palmitat dan alfa tokoferol sebagai antioksidan
Interaksi antar antioksidan bersifat sinergis dan mempunyai efek
saling memberi dimana satu antioksidan melindungi yang lain melawan
destruksi oksidatif. Askorbil palmitat mempunyai peran meregenerasi efek
mendonorkan atom hidrogen pada radikal tocopheroxyl yang akan membentuk
kembali bentuk aktif alfa tokoferol setelah berinteraksi dengan radikal bebas
(Fennema et al., 2004)
C. Mikroemulsi 1. Definisi Mikroemulsi
Mikroemulsi adalah sistem dispersi minyak dan air yang secara
termodinamika stabil, transparan atau jernih yang distabilkan oleh lapisan
antarmuka dari molekul surfaktan (Pathan et al., 2012). Mikroemulsi terdiri dari
empat komponen yaitu minyak, air, surfaktan dan kosurfaktan. Terdapat tiga tipe
sistem dispersi yang dibentuk oleh mikroemulsi yaitu tipe minyak dalam air (M/A
atau O/W), tipe air dalam minyak (A/M atau W/O) dan tipe bikontinu. Tipe sistem
dispersi mikroemulsi tersebut terbentuk dipengaruhi oleh komposisi dari
komponen mikroemulsi itu sendiri (Lawrence et al., 2000). Mikroemulsi memiliki
banyak kelebihan bila dibandingkan dengan emulsi, antara lain stabil secara
termodinamika (stabil dalam jangka waktu yang lama), jernih dan transparan,
dapat disterilkan secara filtrasi, biaya pembuatan murah, mempunyai kelarutan
yang tinggi serta dapat berpenetrasi dengan baik (Pathan et al., 2012).
Menurut Muzaffar et al. (2013) pembentukan mikroemulsi harus
memperhatikan tiga kondisi penting, yaitu :
a. Pemilihan surfaktan adalah hal yang sangat penting dalam mencapai tegangan
antar muka yang sangat rendah antara minyak dan air yang merupakan syarat
utama untuk menghasilkan mikroemulsi.
b. Konsentrasi surfaktan harus cukup tinggi untuk menyediakan jumlah molekul
surfaktan yang diperlukan untuk menstabilkan tetesan mikro yang akan
diproduksi oleh sistem mikroemulsi.
c. Sistem antarmuka harus cukup fleksibel untuk pembentukan mikroemulsi
2. Teori Pembentukan Mikroemulsi
Menurut Singh et al. (2014) terdapat tiga teori pembentukan
mikroemulsi, antara lain:
a. Teori bauran lapisan (Mixed film)
Teori ini menyatakan bahwa pembentukan mikroemulsi dapat
terjadi dengan penurunan tegangan lapisan antar muka hingga sangat
rendah (mendekati nol atau negatif). Pembentukan partikel mikroemulsi
yang spontan berhubungan dengan pembentukan suatu lapisan yang
kompleks pada antar muka minyak-air oleh surfaktan dan kosurfaktan. Hal
ini menyebabkan penurunan tegangan antar permukaan minyak-air hingga
nilai yang sangat rendah.
b. Teori kelarutan (solubilisasi)
Kelompok Shinoda dan Friberg menganggap mikroemulsi
terbentuk dari misel speris, air dan minyak. Karena surfaktan memiliki
kecenderungan untuk berkelompok membentuk misel dan konsentrasi
yang ditambahkan saat terbentuk kelompok misel yang disebut Criticall
Micell Concentration (CMC). Sifat terpenting misel adalah
kemampuannya untuk menaikkan kelarutan zat-zat yang biasanya sukar
larut atau sedikit larut dalam pelarut yang digunakan. Proses ini disebut
solubilisasi yang terbentuk antara molekul zat yang larut berasosiasi
dengan misel dari surfaktan membentuk larutan yang jernih dan stabil
secara termodinamika.
c. Teori termodinamika
Pembentukan Mikroemulsi bergantung kepada kemampuan
surfaktan dalam menurunkan tegangan antar muka antara tetesan minyak
dan perubahan entropi dari sistem. Teori termodinamika ini dapat dilihat
dari persamaan berikut :
∆ = ∆ − ∆
Dimana, Gf adalah energi bebas pada pembentukan mikroemulsi, γ adalah
tegangan permukaan antarmuka minyak-air, ΔA adalah perubahan luas
antarmuka pada mikroemulsifikasi, ΔS adalah perubahan entropi dari
sistem yang efektif dalam dispersi, dan T adalah temperatur.
Pada makroemulsi energi antarmuka lebih besar dari entropi
sistem dan proses pembentukannya tidak spontan, dibutuhkan energi
dalam pembentukannya yang didapat dari mixer dengan kecepatan tinggi.
meningkatkan entropi sistem dan menghasilkan nilai negatif pada energi
bebas permukaan.
3. Komponen Penyusun Mikroemulsi
a. Fase Minyak
Komponen minyak berpengaruh pada kemampuannya untuk
menembus wilayah ekor dari surfaktan. Kriteria utama untuk pemilihan
minyak adalah bahwa obat harus memiliki kelarutan yang tinggi di dalamnya
(Pathan et al., 2012).
b.Surfaktan
Surfaktan memiliki struktur bagian kepala bersifat hidrofilik dan
bagian ekor bersifat hidrofobik, menyebabkan surfaktan cenderung berada
pada antarmuka antara fase yang berbeda derajat polaritas dan membentuk
ikatan hidrogen dengan minyak dan air. Peran surfaktan dalam formulasi
mikroemulsi adalah untuk menurunkan tegangan antar muka yang akhirnya
akan memfasilitasi proses dispersi selama persiapan mikroemulsi.
Pembentukan suatu mikroemulsi dibutuhkan surfaktan dalam jumlah banyak
untuk dapat membentuk suatu mikroemulsi yang stabil, yaitu lebih dari 40%
dari total formula (Pathan et al., 2012).
Terdapat empat jenis surfaktan berdasarkan ionisasi dalam larutan
air yaitu anionik, kationik, nonionik, dan amfoterik (Nielloud et al, 2000).
1) Surfaktan Anionik
Surfaktan ini membawa muatan negatif pada bagian hidrofilik.
murah. Namun, surfaktan ini dapat menyebabkan iritasi dan toksik
sehingga hanya digunakan untuk sediaan luar. Surfaktan ini hanya
menghasilkan emulsi A/M. Contoh surfaktan ionik yaitu: Sodium lauril
sulfat; Triethanolamine; Sodium dioctylsulphosuccinate; dan sebagainya.
2) Surfaktan Kationik
Surfaktan ini mengandung muatan positif pada bagian hidrofilik.
Gugus terpenting pada surfaktan ini terdiri atas senyawa ammonium
kuartener. Surfaktan ini bersifat toksik sehingga cenderung digunakan
untuk formula krim antiseptik. Surfaktan kationik tidak dapat bercampur
dengan surfaktan anionik dan anion polivalen, serta tidak stabil pada pH
tinggi. Contoh surfaktan kationik yaitu: Cetrimide; Cetrimonium
bromida; Benzalkonium chlorida; dan Cetylpyridinium chlorida.
3) Surfaktan Amfoterik
Surfaktan ini memiliki dua sifat pada bagian hidrofiliknya,
tergantung pH sistem. Surfaktan ini bersifat kationik jika pH rendah dan
bersifat anionik jika pH tinggi. Contoh surfaktan amfoterik yaitu:
Lecithin.
4) Surfaktan Nonionik
Surfaktan nonionik tidak memiliki muatan pada bagian
hidrofiliknya. Surfaktan nonionik mempunyai kemampuan melarutkan
senyawa yang kurang larut dan memiliki toksisitas rendah. Contoh
surfaktan nonionik yaitu: Glikol dan gliserol ester; Sorbitan ester;
c.Kosurfaktan
Dalam kebanyakan kasus, surfaktan sendiri belum dapat
menurunkan tegangan antarmuka air-minyak hingga sangat rendah untuk
menghasilkan sebuah mikroemulsi. Dibutuhkan penambahan korsurfaktan
yang dapat berupa senyawa dengan molekul ampifiilik rantai pendek (seperti
etanol) ataupun surfaktan kedua (seperti polietilen glikol) untuk membuat
tegangan antarmuka mendekati nol. Kosurfaktan meningkatkan fluiditas
rantai hidrokarbon surfaktan primer, membantu untuk mengurangi tegangan
permukaan, yang meningkatkan entropi dari sistem yang mengarah ke
stabilitas termodinamika (Pathan et al., 2012). Secara luas molekul yang
dapat berfungsi sebagai kosurfaktan meliputi surfaktan nonionik, alkohol,
asam alkanoat, alkanediol dan alkil amina, etanol, butanol (Lawrence et al.,
2000).
4. Kontrol kualitas mikroemulsi
a. Karakteristik mikroemulsi
Menurut Muzaffar et al. (2013) terdapat beberapa uji untuk
mengetahui karakteristik mikroemulsi, antara lain:
1) Organoleptis : uji ini dilakukan untuk melihat fisik mikroemulsi secara
visual. Dalam uji ini yang diamati adalah warna, bau, pemisahan fase
dan kejernihan mikroemulsi.
2) Tipe mikroemulsi dapat diketahui dengan melakukan uji pengenceran
menggunakan fase minyak dan air yang digunakan, serta dapat
3) Ukuran droplet : pengukuran ini dilakukan untuk melihat apakah
ukuran droplet dari sediaan sudah memenuhi ukuran droplet
mikroemulsi sesuai dengan pustaka yang ada, yaitu kurang dari 100 nm.
4) Pengukuran pH : pengukuran pH dilakukan untuk melihat perubahan
pH saat awal dan akhir uji stabilitas. Pengujian ini juga dilakukan untuk
melihat apakah pH sediaan sesuai untuk kulit. Suatu sediaan topikal
harus didesain agar memiliki pH yang mirip dengan pH kulit yaitu 4,5 –
6,5, apabila melebihi batas tersebut sediaan dapat membuat kulit kering,
bila kurang dari rentang tersebut akan menimbulkan iritasi pada kulit.
5) Persen transmitansi : pengukuran persen transmitansi dilakukan untuk
mengukur kejernihan suatu mikroemulsi. Pengujian dilakukan dengan
spektrofotometer UV-Vis.
6) Indeks bias merupakan suatu nilai yang menunjukkan sifat isotropik
suatu cairan. Pengujiannya menggunakan refraktometer dan
dibandingkan dengan indeks bias aquadest (1,333).
7) Viskositas adalah suatu sifat dari fluida untuk mengalir serta dapat
untuk mengetahui jenis misel yang terbentuk. Makin kental suatu
cairan, makin besar kekuatan yang diperlukan untuk digunakan supaya
cairan tersebut mengalir dengan laju tertentu.
8) Potensial zeta berguna untuk menilai flokulasi yang terjadi karena
adanya muatan listrik pada partikel yang mempengaruhi laju flokulasi.
Nilai potensial zeta yang baik adalah netral, yang mengindikasikan
sistem tersebut stabil. Potensial zeta ditentukan dengan menggunakan
Zetasizer.
9) Bobot jenis berguna untuk mengetahui kerapatan partikel atau droplet
pada suatu sediaan mikroemulsi.
b. Stabilitas termodinamik
Uji stablitas adalah proses yang memakan waktu relatif lama,
sehingga uji stabilitas dipercepat lebih banyak dilakukan. Uji stabilitas
dipercepat pada mikroemulsi dapat dilakukan dengan uji sentrifugasi dan uji
freeze thaw seperti yang diungkapkan oleh Dawaba et al.(2010).
1) Uji sentrifugasi
Metode sentrifugasi digunakan untuk menginduksi dan
mempercepat ketidakstabilan yang disebabkan oleh gaya gravitasi.
kondisi penyimpanan normal dapat diprediksi dengan cepat dengan
mengamati pemisahan fase dispersi ketika mikroemulsi dikenakan
sentrifugasi. Uji sentrifugasi dilakukan dengan kecepatan 5000 rpm
selama 15 menit (Darole, et al., 2008).
2) Uji Heating-cooling
Uji Heating-cooling menginduksi stres dalam sistem
mikroemulsi dengan kondisi ekstrim suhu tinggi penyimpanan. Uji ini
dilakukan untuk mengamati perubahan dalam stabilitas seperti
pemisahan fase, inversi, agregasi, creaming dan cracking dari sampel
diikuti oleh 24 jam pada 40°C, siklus diulang tiga kali dan perubahan
yang terjadi dicatat.
3) Uji Freeze Thraw
Uji freeze thaw menginduksi stres dalam sistem mikroemulsi
dengan kondisi ekstrim suhu penyimpanan rendah. Uji ini dilakukan
untuk mengamati perubahan dalam stabilitas seperti pemisahan fase,
inversi, agregasi, creaming dan cracking dari sampel mikroemulsi.
Mikroemulsi disimpan pada -20°C selama 24 jam dan diikuti oleh 24
jam pada 25°C, siklus diulang tiga kali dan perubahan yang terjadi
dicatat.
D. Uji DPPH
Metode DPPH merupakan metode yang paling banyak digunakan dalam
mengevaluasi aktivitas antioksidan suatu senyawa. Metode ini mudah, cepat,
akurat dan murah untuk pengujian aktivitas antioksidan suatu senyawa. Metode
DPPH menggunakan 2,2difenil-1-pikrilhidrazil sebagai sumber radikal bebas,
yang dapat mendonorkan atom hidrogen (Marinova et al., 2011).
DPPH merupakan radikal bebas nitrogen organik yang memiliki sifat
sangat stabil, bereaksi dengan senyawa yang dapat menyumbangkan hidrogen
atom dan memiliki penyerapan maksimum UV-Vis pada 515 - 517nm. Metode ini
didasarkan pada penangkapan radikal DPPH oleh antioksidan melalui reaksi
reduksi, dan dekolorisasi dari larutan DPPH dalam metanol atau etanol (Ndhlala
menyumbangkan atom hidrogen, maka akan membuat warna violet pada larutan
DPPH berkurang atau hilang. Perubahan ini dapat diukur secara stoikiometri
sesuai dengan jumlah elektron atau atom hidrogen yang ditangkap oleh molekul
DPPH akibat adanya zat antioksidan dengan menggunakan spektrofotometer
UV-Vis (Molyneux, 2004).
Spektrofotometer UV-Vis memiliki prinsip kerja penyerapan radiasi
elektromagnetik pada panjang geombang UV-Vis oleh suatu molekul yang yang
dapat menyebabkan eksitasi elektron dalam orbital molekul tersebut dari tingkat
energi dasar ke tingkat energi yang lebih tinggi.Syarat senyawa yang dapat diukur
menggunakan spektrofotometer UV-Vis adalah mempunyai gugus kromofor dan
auksokrom dan memiliki serapan pada panjang gelombang UV-Vis
(Sastroamidjojo, 2001).
Gambar 2. Struktur DPPH radikal (1), struktur DPPH non radikal (Molyneux, 2004)
Aktivitas antioksidan merupakan kemampuan suatu senyawa untuk
menghambat reaksi oksidasi yang dapat dinyatakan dengan persen penghambatan.
Parameter yang dipakai untuk menunjukan aktivitas antioksidan adalah harga
konsentrasi efisien atau efficient concentration (EC50) atau Inhibition
Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat
menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat
aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50 yang rendah
(Molyneux, 2004).
Tabel I. Tingkat kekuatan aktivitas antioksidan dengan metode DPPH (Arianyo, 2006).
Nilai IC50 Aktivitas antioksidan
< 50 µg/mL Sangat Kuat
50-100 µg/mL Kuat
101-150µg/mL Sedang
> 150 µg/mL Lemah
E. Uji Iritasi
Iritasi kulit adalah proses peradangan pada kulit yang tidak dimediasi
oleh sistem imun dan bersifat reversibel. Pada iritasi akan terjadi perubahan kulit
yang dapat berupa eritema dan endema, dan disertai keluahan seperti gatal dan
rasa kulit seperti terbakar. Produk yang dapat mengiritasi kulit salah satunya
adalah kosmetik, dikarenakan kandungan bahan didalamnya. Uji iritasi menjadi
penting untuk menghindari terjadinya kemungkinan iritasi dari penggunaan
produk tersebut. Uji iritasi yang biasa digunakan menggunakan binatang sebagai
hewan uji, namun banyak pihak yang mengkritik dan menolaknya sehingga perlu
digunakan uji iritasi selain menggunakan hewan uji (Robinson et al., 2001).
Metode Hen’s Egg Test-Chroallontoic (HET-CAM) merupakan salah
satu uji iritasi alternatif yang mulai banyak digunakan sebagai penganti uji iritasi
dengan menggunakan binatang sebagai hewan uji. Uji HET-CAM biasa
digunakan dalam uji iritasi pada mata, namun uji ini dapat juga digunakan untuk
iritasi pada kulit pada beberapa kasus seperti penggunaan surfaktan pada kosmetik
(Bernardi et al., 2011). Kelebihan dari uji ini adalah mudah, dan dapat
CAM merupakan jaringan yang terdiri dari arteri, vena dan kapiler darah.
CAM akan memberikan respon berupa perdarahan, lisis atau koagulasi bila
terpapar bahan yang bersifat iritatif (Cazedey, et al., 2009).
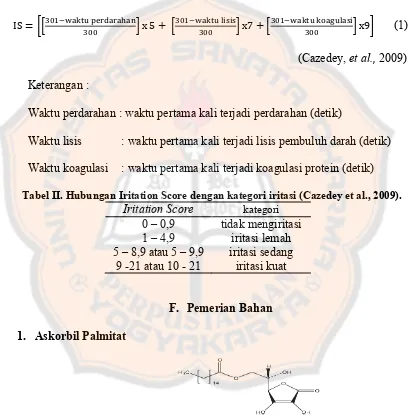
Iritation Score dihitung menggunakan persamaan :
IS = x 5 + x7 + x9 (1)
(Cazedey, et al., 2009).
Keterangan :
Waktu perdarahan : waktu pertama kali terjadi perdarahan (detik)
Waktu lisis : waktu pertama kali terjadi lisis pembuluh darah (detik)
Waktu koagulasi : waktu pertama kali terjadi koagulasi protein (detik)
Tabel II. Hubungan Iritation Score dengan kategori iritasi (Cazedey et al., 2009).
Iritation Score kategori
0 – 0,9 tidak mengiritasi 1 – 4,9 iritasi lemah 5 – 8,9 atau 5 – 9,9 iritasi sedang
9 -21 atau 10 - 21 iritasi kuat
F. Pemerian Bahan 1. Askorbil Palmitat
Gambar 3. Struktur Ascorbyl Palmitate (Rowe et al., 2009)
Pemerian askorbil palmitat adalah sebagai berikut rumus molekul :
C22H38O7, askorbil palmitat praktis tidak berbau, merupakan serbuk berwarna
1 dalam 8 bagian, dalam minyak zaitun 1 dalam 3300 bagain (Rowe et al.,
2009). Sangat sukar larut dalam air (≤ 1.8 g/L at 20oC) (Aquilina et al., 2013).
Asam askorbat sangat tidak stabil dan kurang diserap ke dalam kulit, askorbil
palmitat merupakan turunan dari asam askorbat dengan sifat lebih lipofilik,
lebih stabil serta lebih mudah diserap kulit karena memiliki bagian yang
hidrofil di satu sisi dan lipofil di sisi lain (Baumann, 2009).
2. Dl-alfa Tokoferol
Gambar 4. Struktur Alpha tocopherol (Rowe et al., 2009)
Pemerian alfa tokoferol adalah sebagai berikut rumus molekul :
C29H50O2, bobot molekul 430,72, alfa tokoferol merupakan larutan berminyak
berwarna kuning jernih, kental. Alfa tokoferol larut dalam etanol 95%,
miscible dengan aseton, kloroform, eter, dan minyak natural. Praktis tidak
larut dalam air. Alfa tokoferol dapat digunakan dalam formulasi sediaan oral
maupun topikal (Rowe et al., 2009).
3. Minyak Zaitun (Olea europaea)
Minyak zaitun adalah minyak yang diambil dari buah pohon Olea
europaea. Kandungan asam lemak dalam minyak zaitun berupa asam oleat
56-85%, asam palmitat 7,5-20%, asam linoleat 3,5-20%, asam palmitooleat
<3,6%, asam starat 0,5-5%, asam lemak jenuh dengan panjang rantai kurang
dari C16 <0,1% (Stuchlik et al., 2001). Minyak zaitun mengandung beberapa
vitamin A dan E sehingga dapat menstabilkan sediaan dan minyak zaitun
sendiri terhadap oksidasi dibandingkan dengan minyak nabati lainnya
(Waterman et al, 2007).
Minyak zaitun mengandung sejumlah besar asam oleat yang
merupakan asam lemak kuat yang dapat meningkatkan penetrasi. Asam oleat
juga berpengaruh terhadap proses metabolisme dalam kulit, meningkatkan
aktivitas vitamin A dan E dan memulihkan sifat perlindungan dari stratum
korneum serta memulihkan kondisi kulit yang kering. Minyak zaitun banyak
digunakan sebagai shampo dan kondisioner untuk rambut, produk pembersih,
serta krim dan lotion dalam bidang kosmetik (Alvarez et al., 2000).
4. Tween 80
Gambar 5. Struktur Polysorbate 80 (tween 80) (Mahdi et al., 2011)
Polysorbate merupakan surfaktan non-ionik hidrofilik yang
mengandung 20 unit oksietilena dan digunakan sebagai emulsifying agent pada
emulsi tipe minyak dalam air. Nama kimia untuk tween 80 adalah
polyoxyethylene 20 sorbitan monooleate dengan rumus kimia C64H124O26,
berbentuk cairan berminyak berwarna kuning. Tween 80 memiliki toksisitas
rendah sehingga dapat digunakan untuk penggunaan oral dan parenteral.
Tween 80 berbentuk cairan berwarna kuning dengan bau khas lemah. Tween
80 memiliki bobot jenis 1,08 g/cm3 dan nilai HLB 15. Tween 80 larut dalam
Dalam farmasetik tween 80 digunakan sebagai agen pengemulsi, solubilisator,
pembasah, dan agen pensuspensi atau pendispersi (Rowe et al., 2009).
5. PEG 400
Gambar 6. Struktur PEG 400 (Rowe et al., 2009)
Polietilenglikol 400 adalah polietilenglikol H(O-CH2-CH2)n OH
dimana harga n antara 8,2 dan 9,1. Pemerian : cairan kental jernih, tidak
berwarna atau praktis tidak berwarna, bau khas lemah, agak higroskopik.
Kelarutan : larut dalam air, dalam etanol (95%) P, dalam aseton P, dalam
glikol lain dan dalam hidrokarbon aromatik, praktis tidak larut dalam eter P
dan dalam hidrokarbon alifatik. Bobot molekul rata-rata : 380-420,
kandungan lembab : sangat higroskopis (sifat higroskopis turun dengan
meningkatnya bobot molekul), titik beku 4-80C (Raymond, 2006).
PEG merupakan salah satu jenis bahan pembawa yang sering
digunakan sebagai bahan tambahan dalam formulasi untuk meningkatkan
pelarutan obat yang sukar larut. Bahan ini merupakan salah satu jenis polimer
yang dapat membentuk komplek polimer pada molekul organik apabila
ditambahkan dalam formulasi untuk meningkatkan kecepatan pelarutan yang
dapat membentuk kompleks dengan berbagai obat (Sinko, 2006).
6. Aquadest
Menurut Farmakope Indonesia III, aquadest yaitu cairan jernih, tidak
air suling. Aquadest dibuat dengan menyuling air yang dapat diminum. Fungsi
aquadest sebagai pelarut. Rumus kimia dari aquadest adalah H2O dengan berat
molekul 18,02 (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1979).
G. Landasan Teori
Askorbil palmitat dapat berfungsi sebagai antioksidan, kofaktor dalam
sintesis kolagen, dan bersifat fotoprotektif. Askorbil palmitat merupakan asam
askorbat dengan penambahan ester yang menjadikannya lebih stabil terhadap
oksidasi dan lebih mudah terabsorbsi. Alfa tokoferol dapat berperan sebagai
antioksidan yang bekerja dengan memecah rantai pada radikal bebas dan
melembabkan kulit. Kedua vitamin dapat bekerja secara sinergis menangkap
radikal bebas sebagai antioksidan.
Mikroemulsi merupakan sediaan yang sesuai untuk memformulasikan
askorbil palmitat dan alfa tokoferol dalam suatu sediaan topikal, karena dalam
sediaan ini dapat dicampurkan antara fase air dan fase minyak, menjadi satu fase
yang stabil secara termodinamika. Mikroemulsi memiliki bebeberapa kelebihan
dibandingkan dengan emulsi, antara lain stabil secara termodinamika, dapat
meningkatkan kelarutan dan penetrasi suatu senyawa karena ukurannya yang
sangat kecil. Sistem mikroemulsi terdiri dari fase air, fase minyak, surfaktan dan
kosurfaktan. Surfaktan berperan untuk menurunkan teggangan permukaan,
sedangkan kosurfaktan berfungsi untuk membantu kerja surfaktan agar dapat
membentuk sediaan mikroemulsi dengan menurunkan teganggan permukaan
Dalam sistem mikroemulsi jumlah surfaktan dan kosurfaktan sangat
berperan dalam pembentukan sediaan mikroemulsi yang memiliki sifat fisik dan
stabilitas yang baik, sehingga jumlahnya harus cukup tinggi untuk memfasilitasi
terbentuknya sistem mikroemulsi yaitu lebih dari 40% dalam sistem mikroemulsi
tersebut. Tween 80 merupakan surfaktan non ionik sehingga cenderung akan
membentuk mikroemulsi M/A. Tween 80 dan PEG 400 bersifat tidak toksik dan
tidak iritatif sehingga aman digunakan sebagai sediaan topikal.
H. Hipotesis
1. Peningkatan perbandingan tween 80 sebagai surfaktan dan PEG 400
sebagai kosurfaktan akan mempengaruhi sifat fisik sediaan mikroemulsi
askorbil palmitat dan alfa tokoferol.
2. Semakin tinggi perbandingan tween 80 sebagai surfaktan dan PEG 400
sebagai kosurfaktan maka stabilitas fisik sediaan mikroemulsi askorbil
palmitat dan alfa tokoferol akan semakin baik.
3. Sediaan mikroemulsi askorbil palmitat dan alfa tokoferol memiliki
kemampuan antioksidan kuat.
4. Sediaan mikroemulsi askorbil palmitat dan alfa tokoferol tidak memiliki
33 BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dengan
rancangan acak pola searah.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas. Variabel bebas pada penelitian ini adalah variasi
perbandingan tween 80 sebagai surfaktan dan PEG 400 sebagai
kosurfaktan.
b. Variabel tergantung. Variabel tergantung pada penelitian ini adalah sifat
fisik dan stabilitas sediaan mikroemulsi, serta sifat iritatif (irritation
score) dan kemuampuan antioksidan sediaan mikroemulsi askorbil
palmitat dan alfa tokoferol (IC50).
c. Variabel pengacau terkendali. Variabel pengacau terkendali pada
penelitian ini adalah lama dan kecepatan pengadukan pada saat
pembuatan mikroemulsi serta suhu dan lama penyimpanan.
d. Variabel pengacau tidak terkendali. Variabel pengacau tak terkendali
2. Definisi operasional
a. Sediaan mikroemulsi adalah suatu sediaan mikroemulsi dengan
kandungan zat aktif askorbil palmitat dan dl-alfa-tokoferol yang dibuat
sesuai dengan formula yang tertera dalam penelitian ini.
b. Sifat fisik merupakan parameter yang digunakan untuk melihat kualitas
sediaan mikroemulsi askorbil palmitat dan alfa tokoferol yang meliputi
organoleptis, tipe mikroemulsi, pH, ukuran droplet, viskositas, indeks
bias, bobot jenis, dan persen transmitansi.
c. Stabilitas fisik adalah parameter yang digunakan utuk mengetahui tingkat
kestabilan sediaan mikroemulsi dengan melihat perubahan pH, ukuran
droplet, viskositas dan persen transmitansi yang diamati setelah sediaan
melewati setiap siklus dalam uji freeze thaw.
d. Surfactan Mix (Smix) adalah campuran tween 80 sebagai surfaktan dan
PEG 400 sebagai kosurfaktan dengan rasio perbandingan sesuai dengan
formula yang tertera dalam penelitian ini.
e. Inhibition Concentration 50 (IC50) adalah nilai konsentrasi larutan uji
yang menghasilkan penangkapan radikal DPPH hingga 50%. IC50
diperoleh dari persamaan regresi linear yang menyatakan hubungan
antara konsentrasi larutan uji (sumbu x) dengan persen penangkapan
C.Bahan Penelitian
Bahan yang digunakan adalah askorbil palmitat (CV. Privat Equipment
Pharmacy), dl-alfa-tokoferol (CV. Cipta anugrah), minyak zaitun (CV. Sofa
Mediteranean), Tween 80 (PT. Brataco Chemika), PEG 400 (PT. Brataco
Chemika), aquadestilata (PT. Brataco Chemika), Etanol p.a. (Merck Milipore),
(DPPH) (Laboratorium Chemix Pratama).
D. Alat Penelitian
Peralatan yang digunakan adalah alat – alat gelas (Pyrex), botol kaca,
cawan porselen, mortir dan stemper, timbangan analitik (OHAUS), magnetic
stirrer, pH meter (Hanna Instrument HI 9042 C), Piknometer, Hot plate
(Heidolph), Hand refractometer (Atago), Spektrofotometer UV-Vis (Shimadzu
1600), Viscotester Brookfield LVDV-II+P, Particle Size Analyzer Delta Nano C
Beckman Coulter, Sentrifugator (Benchtop Centrifuge PLC-05), Freezer
(Toshiba), Lemari Pendingin (Sanken Logic Cool), Oven (Memmert)
(Laboratorium Teknologi Semisolid-liquid).
E. Tata Cara Penelitian 1. Formula Acuan Mikroemulsi
Formula acuan yang digunakan dalam pembuatan mikroemulsi
askorbil palmitat dan dl-alfa-tokoferol dapat dilihat pada tabel III. Formula
yang digunakan adalah minyak zaitun, dengan surfaktan tween 80 dan
kosurfaktan PEG 400.
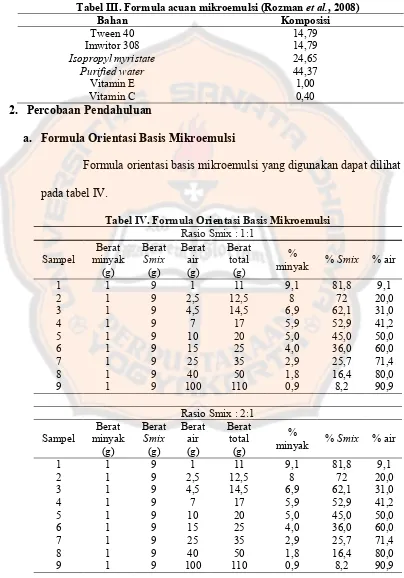
Tabel III. Formula acuan mikroemulsi (Rozman et al., 2008)
Bahan Komposisi
a. Formula Orientasi Basis Mikroemulsi
Formula orientasi basis mikroemulsi yang digunakan dapat dilihat
pada tabel IV.
Tabel IV. Formula Orientasi Basis Mikroemulsi