PENGARUH KOMBINASI SURFAKTAN TWEEN 80 DAN SPAN 80 TERHADAP SIFAT FISIK DAN STABILITAS FISIK MIKROEMULSI
ESTER VITAMIN C DAN VITAMIN E UNTUK ANTIAGING
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh: Fransisca Kristi Astuti
NIM : 108114160
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH KOMBINASI SURFAKTAN TWEEN 80 DAN SPAN 80 TERHADAP SIFAT FISIK DAN STABILITAS FISIK MIKROEMULSI
ESTER VITAMIN C DAN VITAMIN E UNTUK ANTIAGING
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh: Fransisca Kristi Astuti
NIM : 108114160
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Yesaya 41:10
“J
anganlah takut, sebab Aku menyertai engkau, janganlah bimbang, sebab Aku
ini Allahmu; Aku akan meneguhkan, bahkan akan menolong engkau; Aku akan
memegang engkau dengan tangan kanan-Ku yang
membawa kemenangan.”
Pengkhotbah 3:11
“Ia membuat segala sesuatu indah pada waktuNya, bahkan Ia memberi
kekekalan di dalam hati mereka”.
Amsal 2:10
“”Karena hikmat akan masuk ke dalam hatimu dan pengetahuan akan
Menyenangkan jiwamu”
.
Ketekunan bisa membuat yang tidak mungkin
menjadi mungkin, membuat kemungkinan kecil jadi
kemungkinan besar dan membuat kemungkinan menjadi pasti
(Robert Half)
Kupersembahkan skripsi ini untuk :
Tuhan Yesus Kristus, Bunda Maria dan Malaikat Gabriel
Papa dan mama tercinta
Dd Alisius Johan Affandi
Teman-teman Farmasi 2010
vii PRAKATA
Saya panjatkan puji dan syukur kepada Tuhan Yesus Kristus, Bunda Maria, Santo Tadeus dan Malaikat Gabriel atas curahan berkat dan kasih-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “PENGARUH KOMBINASI SURFAKTAN TWEEN 80 DAN SPAN 80 TERHADAP SIFAT FISIK DAN STABILITAS FISIK MIKROEMULSI ESTER VITAMIN C DAN VITAMIN E UNTUK ANTIAGING”. Penyusunan skripsi ini bertujuan untuk memenuhi salah satu syarat mendapatkan gelar Sarjana Strata Satu Program Studi Ilmu Farmasi (S.Farm).
Selama masa perkuliahan hingga penelitian dan penyusunan skripsi, penulis banyak mendapatkan bantuan dari berbagai pihak baik berupa bimbingan, perhatian, doa, dorongan, nasehat, sarana dan prasarana. Pada kesempatan ini penulis ingin menyampaikan ucapan terima kasih yang sebesar-besarnya kepada: 1. Papa Agustinus Suparyono dan mama Elizabeth Nuryati atas doa, perhatian
baik saat suka dan duka serta penyokong dana terhadap penulis selama berkuliah dan mengerjakan skripsi.
2. Aris Widayati, M.Si., Ph.D., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
3. Dr. Sri Hartati Yuliani, M.Si., Apt., selaku Ketua Program Studi Fakultas Farmasi Universitas Sanata Dharma.
viii
5. C. M. Ratna Rini Nastiti, M.Pharm., Apt. dan Melania Perwitasari, M.Sc., Apt. selaku dosen penguji yang telah memberikan saran kepada penulis dalam memperbaiki naskah skripsi.
6. Pak Musrifin, Mas Agung, Pak Parlan, Mas Otok, Mas bimo, Mas Kunto, Pak Wagiran, Pak Iswandi, Mas Sigit, Pak Pardjiman, Pak Heru, Pak Timbul, Mas Ketul dan segenap satpam dan karyawan atas bantuan dan kelancaran yang telah diberikan dalam pelaksanaan penelitian ini.
7. Elizabeth Sita dan Agrifina Akardias Mahalalita selaku teman seperjuangan dalam melakukan penelitian, serta atas masukan, saran, serta dukungannya selama ini.
8. Eveline Febrina dan Arfin dj, selaku sahabat sejati yang selalu memberikan semangat dikala suka dan duka.
9. Anggota Kwek-kwek Marcelina W. A. R, Rosalia Suryaningtyas, Astuti M. S, dan Eva Cristiana atas perhatian dan dukungannya kepada penulis.
10. Naomita Joice, Liliany Ludji, Nita Rahayu, Ricardo Kenny, Vivian hiu, Cindy, Eliza telamiana, Widya Agriani, Priskila Agnes, Ita (001), Olivia, Sita, dan Juliana atas tawa dan dukungannya yang diberikan kepada penulis.
11. Semua pihak dan teman-teman yang tidak dapat penulis sebutkan satu persatu, yang telah membantu terselesaikannya skripsi ini.
x INTISARI
Ester vitamin C dan vitamin E diketahui memiliki fungsi sebagai antioksidan. Campuran ester vitamin C dan vitamin E diformulasikan dalam bentuk mikroemulsi untuk meningkatkan absorpsi ke dalam lapisan kulit. Tujuan penelitian ini untuk mengetahui pengaruh campuran surfaktan tween 80 dan span 80 terhadap sifat fisik dan stabilitas fisik mikroemulsi ester vitamin C dan vitamin E.
Faktor dalam penelitian adalah tween 80 dan span 80 dengan perbandingan 5:1, 6:1, 7:1, 8:1. Parameter uji yang diamati meliputi organoleptis, ukuran partikel, persen transmitan, viskositas, indeks bias, pH, dilution test, uji aktivitas antioksidan menggunakan metode DPPH dan stabilitas sediaan menggunakan freeze thaw selama 3 siklus. Data yang diperoleh dianalisis secara statistik menggunakan Analysis of variance (ANOVA) dengan software R.3.0.2.
Hasil penelitian menunjukkan bahwa peningkatan tween 80 dalam kombinasi surfaktan tidak memberikan perubahan organoleptis, menyebabkan peningkatan pH, viskositas serta penurunan ukuran partikel dan persen transmitan sediaan mikroemulsi ester vitamin C dan vitamin E. Sediaan mikroemulsi ester vitamin C dan E memiliki aktivitas antioksidan yang termasuk dalam kategori sangat kuat dengan IC50 F5 0,012 mg/mL, F6 0,019 mg/mL, F7 0,022 mg/mL dan F8 0,040 mg/mL.
xi ABSTRACT
Ester vitamin C and vitamin E are known to have a function as an antioxidant. The mixture of ester vitamin C and E are formulated in the form of microemulsion to increase absorption in the skin surface. The purpose of this study was to determine the effect of surfactant tween 80 and span 80 on the physical properties and stability of microemulsion ester vitamin C and vitamin E.
Factors in the study were tween 80 and span 80 with a ratio of 5:1, 6:1, 7:1, 8:1. Parameters observed were organoleptic test, particle size, percent transmittance, viscosity, refractive index, pH, dilution test, Antioxidant activity test used DPPH method and freeze thaw stability of the microemulsion for 3 cycles. Data were analyzed statistically using analysis of variance (ANOVA) with software R.3.0.2.
The results showed that increasing of tween 80 on the surfactant mixture in this study did not provide organoleptic changes, causing increase in pH, viscosity and particle size and decreased in percent transmittance microemulsion ester vitamin C and E.Microemulsion ester vitamins C and E showed very strong antioxidant activity with an average IC50 F5 0,01200 mg/mL, F6 0,01857 mg/mL,
F7 0,02167 mg/mL, F8 0,04028 mg/ mL.
xii DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PERSETUJUAN SKRIPSI ... iii
HALAMAN PERSEMBAHAN ... iv
PERSETUJUAN PUBLIKASI ... v
PERNYATAAN KEASLIAN KARYA ... vi
PRAKATA ... vii
INTISARI ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ... xix
DAFTAR GAMBAR ... xxi
DAFTAR LAMPIRAN ... xxiii
BAB I. PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Perumusan Masalah ... 4
C. Keaslian Penelitian ... 4
D. Manfaat Penelitian ... 5
E. Tujuan Penelitian ... 6
BAB II. TINJAUAN PUSTAKA ... 7
A. Penuaan Dini ... 7
xiii
2. Penuaan dini akibat sinar UV ... 7
3. Pembentukkan Radikal Bebas pada Kulit ... 7
B. Antioksidan ... 8
1. Mekanisme Kerja Antioksidan ... 9
2. Vitamin E sebagai Antioksidan ... 10
3. Ester vitamin C atau Askorbil palmitat sebagai antioksidan ... 11
C. Mikroemulsi ... 12
1. Jenis Mikroemulsi ... 12
2. Teori Pembentukkan Mikroemulsi... 12
3. Surfaktan... 13
3.1. Tween 80 dan Span 80 sebagai Surfaktan... 14
4. Kontrol Kualitas dari Sediaan Mikroemulsi... 16
4.1. Uji Organoleptis... . 16
4.2. Uji pH... . 16
4.3. Uji Viskositas... . 16
4.4. Uji Ukuran Partikel Mikroemulsi... 18
4.5. Dilution Test... . 18
4.6. Uji Indeks Bias... . 19
4.7. Uji Persen Transmitan ... 19
5. Uji Stabilitas Mikroemulsi... . 20
D. Uji Iritasi Menggunakan Metode HET-CAM... 22
xiv
F. Pemerian Bahan... 24
1. Ester vitamin C atau Ascorbyl palmitate... ... 24
2. Vitamin E (alfa tokoferol)... 25
3. Sunflower oil... 25
4. Tween 80 ... 26
5. Span 80 ... 27
6. Aquadestilata ... 27
7. DPPH (2,2-dfenil 1-pikrilhidrazil) ... 27
8. Etanol ... 28
G. Analisis Data ... 29
H. Landasan Teori ... 29
I. Hipotesis Penelitian ... 30
BAB III. METODOLOGI PENELITIAN ... 31
A. Jenis Rancangan Penelitian ... 31
B. Variabel dan Definisi Operasional ... 31
1. Variabel Penelitian ... 31
2. Definisi Operasional... 31
C. Bahan Penelitian ... 32
D. Alat Penelitian ... 33
E. Tata Cara Penelitian ... 33
1. Orientasi Formula Sediaan Mikroemulsi Ester vitamin C dan vitamin E ... 33
xv
1.2. Pembuatan Sediaan Mikroemulsi Ester Vitamin C dan
Vitamin E Formula Orientasi ... 34
2. Evaluasi Sediaan Mikroemulsi saat orientasi ... 35
2.1. Uji organoleptis ... 35
2.2. Heating and Cooling Cycle ... 35
2.3. Uji Sentrifugasi ... 35
3. Pembuatan Mikroemulsi Ester vitamin C dan vitamin E dengan Formula Hasil Orientasi... 35
3.1. Formula Mikroemulsi Hasil Orientasi ... 35
3.2. Pembuatan Sediaan Mikroemulsi Ester Vitamin C dan Vitamin E ... 36
4. Uji Sifat Fisik Sediaan Mikroemulsi Ester vitamin C dan vitamin E ... 36
4.1. Uji Organoleptis ... 36
4.2. Uji pH menggunakan pH meter ... 36
4.3. Diluton Test ... 37
4.4. Persen Transmitan ... 37
4.5. Indeks Bias ... 38
4.6. Viskositas ... 39
4.7. Uji Ukuran partikel ... 39
5. Uji Stabilitas Dipercepat ... 39
5.1. Uji Freeze thaw ... 39
xvi
6.1. Penyiapan Telur ... 39
6.2. Kontrol Positif (NaOH 0,1 N) ... 40
6.3. Kontrol Negatif (0,9% NaCl) ... 40
6.4. Perlakuan ... 40
6.5. Pengamatan ... 40
7. Uji Aktivitas Antioksidan pada Sediaan Mikroemulsi... 41
7.1. Pembuatan Larutan DPPH ... 41
7.2. Penentuan Panjang Gelombang Maksimum DPPH ... 41
7.3. Penentuan Operating Time ... 42
7.4. Pembuatan Larutan uji ... 42
7.5. Pengukuran Absorbansi Larutan DPPH (kontrol)... 49
7.6. Penentuan Aktivitas Antioksidan ... 49
7.7. Penentuan Persamaan Regresi Linear ... 50
F. Analisis Data ... 50
BAB IV. HASIL DAN PEMBAHASAN ... 52
A. Uji Pendahuluan atau Orientasi Formula ... 52
B. Uji Sifat Fisik Sediaan Mikroemulsi Ester vitamin C dan vitamin E dengan Formula Hasil Orientasi ... 54
1. Uji Organoleptis dan pH ... 54
2. Dilution Test ... 55
3. Persen transmitan ... 56
4. Uji Indeks Bias ... 57
xvii
6. Uji Viskositas ... 60
C. Uji Stabilitas Fisik Sediaan Mikroemulsi Ester vitamin C dan vitamin E ... 62
1. Stabilitas organoleptis mikroemulsi ester vitamin C dan vitamin E setelah mengalami freeze thaw ... 63
2. Stabilitas pH mikroemulsi ester vitamin C dan vitamin E setelah mengalami freeze thaw... 64
3. Stabilitas persen transmitan mikroemulsi ester vitamin C dan vitamin E setelah mengalami freeze thaw ... 65
4. Stabilitas ukuran droplet mikroemulsi ester vitamin C dan vitamin E setelah mengalami freeze thaw ... 66
5. Stabilitas viskositas mikroemulsi ester vitamin C dan vitamin E setelah mengalami freeze thaw ... 66
D. General Discussion Antar Uji sifat Fisik Sediaan Mikroemulsi .... 67
E. Uji Aktivitas Antioksidan Basis Mikroemulsi dan Mikroemulsi Ester vitamin C dan vitamin E ... 70
1. Penentuan Panjang Gelombang Serapan Maksimum (λ maks) 70 2. Penentuan Operating Time (OT) ... 69
3. Hasil Aktivitas Antioksidan dengan Radikal DPPH ... 72
F. Uji Iritasi Menggunakan Metode HET-CAM ... 74
BAB V. KESIMPULAN DAN SARAN ... 76
A. Kesimpulan ... 76
xviii
xix
DAFTAR TABEL
Tabel I. Klasifikasi Skor Kumulatif dalam Chorioallantoic Membrane Test ... 23
Tabel II. Formula Mikroemulsi Acuan ...33
Tabel III. Orientasi Formula Mikroemulsi Ester vitamin C dan vitamin
E ...34 Tabel IV. Formula Mikroemulsi Hasil Orientasi ...35
Tabel V. Hasil Organoleptis Formula orientasi... 53 Tabel VI. Data Organoleptis dan pH Sediaan Mikroemulsi Formula
Hasil Orientasi ... 54 Tabel VII. pH Kombinasi Surfaktan Tween 80 dan Span 80 Setiap
Formula ... ... 55 Tabel VIII. Nilai HLB Kombinasi Surfaktan Tween 80 dan Span 80 pada
Setiap Formula Mikroemulsi Ester vitamin C dan vitamin E ... 56 Tabel IX. Hasil Ukuran Droplet (nm)... 58 Tabel X. Nilai Indeks Polidispersitas dan Koefisien Difusi (D) saat
Pengujian Ukuran Droplet... 60 Tabel XI. Hasil Organoleptis Selama Freeze Thaw Dengan 3 Siklus
xx
Tabel XII. Ukuran Droplet Mikroemulsi Ester Vitamin C Dan Vitamin E
Setelah Freeze Thaw ...65 Tabel XIII. Hasil Sifat Fisik Sediaan Mikroemulsi... 68
Tabel XIV Hasil Stabilitas Fisik Mikroemulsi... 68 Tabel XV IC50 Standar Ester vitamin C, Vitamin E, Campuran Ester
vitamin C dan vitamin E serta mikroemulsi Ester vitamin C dan vitamin E... 73 Tabel XVI. Data Hasil Pengujian Iritasi Mikroemulsi Ester vitamin C dan
vitamin E ... ...75 Tabel XVII. Data HLB Kombinasi Surfaktan Tween 80 dan Span 80
Setiap Formula Mikroemulsi ... 90 Tabel XVIII. Uji Statistik Sifat Fisik pH, Viskositas, Persen Transmitan,
Ukuran Partikel dan nilai IC50 Sediaan Mikroemulsi Ester vitamin C dan vitamin E ... 95 Tabel XIX. Uji Statistik Stabilitas pH, Viskositas, Persen Transmitan dan
Ukuran Droplet ... 98 Tabel XX. Waktu Saat Terjadi Iritasi dengan Perlakuan Kontrol Positif,
xxi
DAFTAR GAMBAR
Gambar 1. Reaksi Penangkapan Radikal oleh DPPH ... 24 Gambar 2. Struktur Kimia Ester vitamin C ...24 Gambar 3. Struktur Kimia Vitamin E ...25 Gambar 4. Struktur Kimia Tween 80 ...26 Gambar 5. Struktur Kimia Span 80...27 Gambar 6. Struktur Kimia DPPH ... 28 Gambar 7. Struktur Kimia Etanol... ...28 Gambar 8. Larutan Mikroemulsi yang dilarutkan dalam 100 mL
Akuades ...55 Gambar 9. Grafik Uji Persen Transmitan Sediaan Mikroemulsi Ester
ester vitamin C dan vitamin E formula 5 (5:1), formula 6
(6:1), formula 7 (7:1), formula 8 (8:1) ...56 Gambar 10. Grafik Uji Indeks Bias Sediaan Mikroemulsi Ester vitamin
C dan vitamin E formula 5 (5:1), formula 6 (6:1), formula 7 (7:1), formula 8 (8:1) ...57 Gambar 11. Hasil Grafik Uji Ukuran Droplet Sediaan Mikroemulsi
Ester vitamin C dan vitamin E formula 5 (5:1) sebelum
freeze thaw ... 58
Gambar 12. Hasil Grafik Uji Ukuran Droplet Sediaan Mikroemulsi
xxii
Gambar 13. Grafik Uji viskositas Sediaan Mikroemulsi Ester vitamin C dan vitamin E formula 5 (5:1), formula 6 (6:1), formula 7 (7:1), formula 8 (8:1) ... 61 Gambar 14. Grafik Uji Stabilitas pH Sediaan Mikroemulsi Ester
vitamin C dan vitamin E Selama Mengalami freeze thaw
selama 3 siklus ...63 Gambar 15. Grafik Uji Stabilitas Persen Transmitan Sediaan
Mikroemulsi Ester vitamin C dan vitamin E Selama
Mengalami freeze thaw 3 Siklus ...64 Gambar 16. Grafik Uji Stabilitas Viskositas Mikroemulsi Ester vitamin
C dan vitamin E Selama Mengalami freeze thaw 3 Siklus ...66 Gambar 17. Grafik Penentuan OT Standar Ester vitamin C 0,0015
mg/mL, Vitamin E 0,00075 mg/mL dan Campuran Ester
vitamin C dan vitamin E 0,0042 mg/mL ...71 Gambar 18. Grafik Penentuan OT Mikroemulsi formula 5 (5:1) 0,0084
mg/mL, formula 6 (6:1) 0,0196 mg/mL, formula 7 (7:1) 0,0168 mg/mL, formula 8 (8:1) 0,0196 mg/mL ...71 Gambar 19. Grafik Penentuan OT Basis Mikroemulsi formula 5 (5:1)
1,2 mg/mL, formula 6 (6:1) 1,4 mg/mL, formula 7 (7:1) 1,4
xxiii
DAFTAR LAMPIRAN
Lampiran 1. Certificate of Analysis (CoA) ester vitamin C (Askorbil palmitat) ... 84
Lampiran 2. Certificate of Analysis (CoA) vitamin E (Alfa-tokoferol)) ...85 Lampiran 3. Certificate of Analysis (CoA) Sunflower oil... 86
Lampiran 4 Certificate of Analysis (CoA) Tween 80 ...87 Lampiran 5. Certificate of Analysis (CoA) Span 80 ...88 Lampiran 6. Data Penimbangan Formula Orientasi ...89 Lampiran 7. Data Hasil Organoleptis Orientasi ...90 Lampiran 8. Data Pengamatan HLB ...90
Lampiran 9. Organoleptis Sediaan Mikroemulsi Ester vitamin C dan vitamin E... 90 Lampiran 10. Data Pengukuran pH Basis dan Sediaan Mikroemulsi
Vitamin C dan E ... 91 Lampiran 11. Data Pengukuran Viskositas (cP) Sediaan Mikroemulsi Ester
vitamin C dan vitamin E ...92 Lampiran 12. Data Pengukuran Persen Transmitan (% T) Sediaan
Mikroemulsi Ester vitamin C dan vitamin E ... 93 Lampiran 13. Data Pengukuran Indeks bias Sediaan Mikroemulsi Ester
vitamin C dan E ... 93
xxiv
Lampiran 15. Perhitungan Statistik Sifat Fisik Viskositas, pH, Persen Transmitan dan Ukuran partikel (24 Jam) Sediaan Mikroemulsi Ester vitamin C dan vitamin E Menggunakan Program R 3.0.2 open source... 94 Lampiran 16. Data Stabilitas pH, Viskositas, Persen Transmitan dan
Ukuran Partikel Sediaan Mikroemulsi Ester vitamin C dan vitamin E ... 97 Lampiran 17. Data Penimbangan Ester vitamin C, E, Campuran Ester
vitamin C dan E sebagai standar……... 100 Lampiran 18. Data Perhitungan DPPH, konsentrasi stok ester vitamin C,
seri konsentrasi ester vitamin C, Data Absorbansi Ester vitamin C, % IC dan IC50 ester vitamin C sebagai standar ... 100 Lampiran 19. Data Perhitungan DPPH, konsentrasi stok vitamin E, seri
konsentrasi vitamin E, Data Absorbansi Vitamin E, % IC dan IC50 vitamin E sebagai standar... 104 Lampiran 20. Data Perhitungan DPPH, konsentrasi stok campuran ester
vitamin C dan E, seri konsentrasi campuran ester vitamin C dan vitamin E, Data Absorbansi Ester vitamin C dan vitamin E, % IC dan IC50 ester vitamin C dan vitamin E sebagai standar... ...108 Lampiran 21. Uji Statistik Standar Ester vitamin C, E dan campuran Ester
xxv
Lampiran 22. Konsentrasi Stok dan Seri Konsentrasi Mikroemulsi Ester vitamin C dan E 5:1, Data Absorbansi Mikroemulsi Ester vitamin C dan vitamin E 5:1, % IC dan IC50 Mikroemulsi
Ester vitamin C dan vitamin E 5:1 ...113 Lampiran 23. Konsentrasi Stok dan Seri Konsentrasi Mikroemulsi Ester
vitamin C dan E 6:1, Data Absorbansi Mikroemulsi Ester vitamin C dan vitamin E 6:1, % IC dan IC50 Mikroemulsi
Ester vitamin C dan vitamin E 6:1 ...115 Lampiran 24. Konsentrasi Stok dan Seri Konsentrasi Mikroemulsi Ester
vitamin C dan E 7:1, Data Absorbansi Mikroemulsi Ester vitamin C dan vitamin E 7:1, % IC dan IC50 Mikroemulsi Ester vitamin C dan vitamin E 7:1 ... 117 Lampiran 25. Konsentrasi Stok dan Seri Konsentrasi Mikroemulsi Ester
vitamin C dan E 8:1, Data Absorbansi Mikroemulsi Ester vitamin C dan vitamin E 8:1,% IC dan IC50 Mikroemulsi Ester vitamin C dan vitamin E 8:1 ... 119 Lampiran 26. Konsentrasi Stok dan Seri Konsentrasi Basis Mikroemulsi
5:1, Data Absorbansi Basis Mikroemulsi 5:1, % IC ... 120 Lampiran 27. Konsentrasi Stok dan Seri Konsentrasi Basis Mikroemulsi
6:1, Data Absorbansi Basis Mikroemulsi 6:1 dan % IC ... 122 Lampiran 28. Konsentrasi Stok dan Seri Konsentrasi Basis Mikroemulsi
xxvi
1 BAB I
PENGANTAR
A. Latar Belakang
Kulit dianggap sebagai cermin penampilan seseorang sehingga tidak salah jika banyak orang terutama wanita berusaha merawat kulit wajah dan memperlambat proses penuaan dini. Radikal bebas merupakan faktor utama yang mempengaruhi atau mempercepat terjadinya proses penuaan dini. Radikal bebas menyebabkan kerusakan pada kulit, seperti kulit menebal, kaku, tidak elastis, keriput, pucat dan kering (Evawati, 2010). Peremajaan kulit merupakan salah satu upaya untuk membuat kulit tampak sehat dan muda kembali.
Salah satu cara peremajaan kulit adalah menggunakan antioksidan seperti ester vitamin C (Askorbil palmitat) dan vitamin E (alfa tokoferol) (Bauman, 2002). Ester vitamin C atau vitamin E sudah banyak digunakan oleh masyarakat dalam bentuk emulsi. Menurut Goncalves et al., (2009), emulsi ester vitamin C tidak stabil pada saat penyimpanan dengan suhu tinggi karena akan menyebabkan penurunan viskositas hingga pemisahan fase dengan adanya peningkatan motilitas partikel dan interaksi antar fase. Berdasarkan masalah tersebut maka pada penelitian ini ester vitamin C dan vitamin E diformulasikan dalam bentuk mikroemulsi.
diamati dengan uji DPPH berdasarkan parameter IC50. IC50 adalah ukuran efektivitas suatu senyawa murni atau senyawa dalam sediaan tertentu dalam menangkap radikal bebas (Dehpour et al., 2009).
Mikroemulsi mempunyai beberapa keunggulan, diantaranya transparan sehingga secara estetika lebih menarik, memiliki viskositas rendah sehingga saat diaplikasikan lebih mudah menyebar pada kulit dan stabil secara termodinamika atau energi bebas permukaan sistem lebih rendah dibanding energi bebas masing-masing bahan sehingga tidak mudah mengalami pemisahan fase (Gulati et al.,
1998). Selain itu, kapasitas solubilizing yang tinggi dari mikroemulsi dapat meningkatkan kelarutan dari suatu senyawa yang memiliki kelarutan rendah terhadap air (Cho et al., 2008).
Keunggulan dari tween 80 dan span 80 yaitu keduanya memiliki rantai polioksietilen yang menjadikan kombinasi kedua surfaktan ini sebagai halangan sterik bagi droplet–droplet fase minyak, sehingga kemungkinan untuk bergabungnya droplet-droplet fase minyak ini dapat diminimalkan dan membuat sediaan tetap stabil (Kim, 2005). Keunggulan lainnya, dilihat dari HLB yaitu bahan tween 80 memiliki HLB 15 dan span 80 memiliki HLB 4,3 sehingga dapat menurunkan tegangan permukaan antara fase minyak dan fase air lebih mudah dibanding dengan menggunakan satu surfaktan saja. Tween 80 bersifat lebih hidrofil akan sulit untuk menyatukan fase minyak dan fase air jika tidak dalam komposisi sangat besar. Pada span 80, dikarenakan sifatnya yang lebih lipofil dan memiliki karakteristik membentuk lapisan film yang kaku membuat span 80 lebih sulit dalam membentuk mikroemulsi jika tanpa kombinasi bahan lain (Radomska and Wojciechowska, 2005).
Penggunaan sediaan farmasi terutama kosmetik saat ini sudah merupakan kebutuhan bagi masyarakat dan digunakan secara terus-menerus pada kulit sehingga kosmetik harus memenuhi persyaratan keamanan. Pengujian keamanan dari suatu kosmetik seperti mikroemulsi dapat menggunakan metode HET-CAM. Menurut Bernardi et al., (2011), sediaan yang cocok diujikan menggunakan metode HET-CAM adalah sediaan liquid, solid dan semi solid.
tween 80 dan span 80, mengingat kombinasi kedua surfaktan yang mempengaruhi sifat fisik dan stabilitas fisik.
1. Perumusan Masalah
a. Bagaimanakah pengaruh variasi kombinasi surfaktan tween 80 dan span 80 terhadap sifat fisik dan stabilitas fisik mikroemulsi ester vitamin C dan vitamin E?
b. Apakah sediaan mikroemulsi ester vitamin C dan vitamin E dapat menangkap radikal bebas berdasarkan nilai IC50 yang dihasilkan melalui uji DPPH?
c. Apakah sediaan mikroemulsi ester vitamin C dan vitamin E bersifat aman (tidak iritatif) berdasarkan uji HET-CAM?
2. Keaslian Penelitian
Sejauh penelurusan pustaka dari beberapa sumber yang dilakukan peneliti, penelitian mengenai “Pengaruh kombinasi surfaktan tween 80 dan span 80 terhadap sifat fisik dan stabilitas fisik sediaan mikroemulsi ester vitamin C dan vitamin E untuk antiaging” belum pernah dilakukan. Adapun penelitian terkait yang pernah dilakukan yaitu :
a. Penelitian dengan judul Stability of Vitamins C and E In Topical Microemulsions for Combined Antioxidant Therapy, oleh Rozman et al.
(2007).
b. Penelitian dengan judul Dual Influence of Colloidal Silica on Skin Deposition of Vitamins C and E Simultaneously Incorporated in Topical
c. Penelitian dengan judul Temperature–Sensitive Microemulsion Gel: An Effective Topical Delivery System for Simultaneous Delivery of Vitamins
C and Vitamin E, oleh Rozman et al. (2009).
Ketiga penelitian di atas melihat sifat fisik dan stabilitas fisik dari mikroemulsi vitamin C dan E, namun pada penelitian Rozman et al. (2007) dilakukan dengan pengembangan konsentrasi pengental untuk mengubah viskositas sistem mikroemulsi ester vitamin C dan vitamin E, pada penelitian Rozman et al. (2007) dilakukan dengan optimasi silika koloid sebagai pengental untuk meningkatkan viskositas mikroemulsi baik hidrofilik maupun lipofilik dan pada penelitian Rozman et al. (2009) dilakukan dengan pengembangan suhu sensitif terhadap mikroemulsi gel ester vitamin C dan vitamin E.
3. Manfaat Penelitian
a. Manfaat Teoritis. Penelitian ini diharapkan dapat memberikan sumbangan ilmiah bagi perkembangan ilmu pengetahuan tentang formulasi, evaluasi sifat fisik dan kemampuan menghambat radikal bebas dari sediaan mikroemulsi Ester vitamin C dan vitamin E dengan kombinasi surfaktan tween 80 dan span 80 untuk antiaging.
B. Tujuan Penelitian
1. Mengamati pengaruh kombinasi surfaktan tween 80 dan span 80 terhadap sifat fisik dan stabilitas fisik mikroemulsi ester vitamin C dan vitamin E. 2. Menyelidiki kemampuan sediaan mikroemulsi ester vitamin C dan vitamin
E dalam menghambat radikal bebas berdasarkan nilai IC50 yang dihasilkan melalui uji DPPH.
7 BAB II
TINJAUAN PUSTAKA
A. Penuaan Dini
1. Pengertian
Menjadi tua atau aging adalah suatu proses menghilangnya kemampuan jaringan secara perlahan-lahan untuk memperbaiki atau mengganti diri dan mempertahankan struktur, serta fungsi normalnya. Proses penuaan terjadi pada seluruh organ tubuh meliputi organ dalam tubuh, seperti jantung, paru-paru, ginjal, dan lain-lain, juga organ terluar dan terluas tubuh, yaitu kulit (Cunnningham, 2003).
2. Penuaan dini akibat sinar UV
Efek fotobiologik sinar ultraviolet (UVA dan UVB) menghasilkan radikal bebas dan menimbulkan kerusakan pada DNA. Pejanan sinar UV pada kulit merupakan awal mula terbentuknya reaksi fotokimiawi yang dapat mengakibatkan penuaan kulit dini dan kanker. Reaksi fotokimiawi ini dapat menyebabkan perubahan pada DNA yang meliputi oksidasi asam nukleat. Reaksi oksidasi juga dapat mengubah protein dan lipid yang mengakibatkan fungsi sel terganggu. Akumulasi keduanya ini mengakibatkan penuaan jaringan (Dong et al., 2008).
3. Pembentukkan radikal bebas pada kulit
oksigen (O2) dalam kulit yang terdapat pada bagian bawah epidermis merupakan target utama gelombang sinar UV yang masuk ke dalam kulit (Fisher, 2002).
Molekul oksigen bersifat unik karena elektron yang terdapat pada lapisan luar tidak lengkap berada dalam orbit elektron sehingga mempunyai kecenderungan untuk menarik elektron dalam melengkapi pasangan elektronnya. Konsekuensinya adalah bahwa masuknya sinar UV dapat berperan sebagai donatur sebuah elektron kepada molekul oksigen di lapisan epidermis. Contoh radikal bebas pada kulit terbentuk dari interaksi sinar UV dengan molekul oksigen yang berada di dalam sel kulit adalah anion superoksida, hidrogen peroksida, hidroksi radikal, dan oksigen singlet (Fisher, 2002).
Faktor radikal bebas merupakan faktor utama yang mempengaruhi atau mempercepat terjadinya proses penuaan dini. Radikal bebas menyebabkan kerusakan pada kulit, seperti menurunkan kinerja zat-zat dalam tubuh, misalnya enzim yang bekerja mempertahankan fungsi sel (enzim protektif), menimbulkan kerusakan protein dan asam amino yang merupakan struktur utama kolagen dan jaringan elastin, kerusakan pembuluh darah kulit; dan mengganggu distribusi melanin (Evawati, 2010).
B. Antioksidan
Antioksidan bekerja dengan melindungi lipid dari proses peroksidasi oleh radikal bebas. Ketika radikal bebas mendapat elektron dari antioksidan, maka radikal bebas tersebut tidak lagi perlu menyerang sel dan reaksi rantai oksidasi akan terputus. Setelah memberikan elektron, antioksidan menjadi radikal bebas berdasarkan definisinya. Antioksidan pada keadaan ini berbahaya karena mereka mempunyai kemampuan untuk melakukan perubahan elektron tanpa menjadi reaktif (Frei, 2004).
Kulit sendiri memiliki kemampuan untuk membatasi kerusakan yang disebabkan oleh pajanan sinar UV misalnya melalui penghamburan cahaya oleh stratum korneum, penyerapan cahaya oleh melanin dan perbaikan DNA (DNA repair), dan melalui sistem antioksidan yang berfungsi mempertahankan keseimbangan antara prooksidan dan antioksidan (Dong et al., 2008).
1. Mekanisme Kerja Antioksidan
Mekanisme kerja antioksidan pada radikal bebas ada 3 macam, yaitu antioksidan primer, antioksidan sekunder dan antioksidan tersier.
Antioksidan primer mampu mengurangi pembentukan radikal bebas baru dengan cara memutus reaksi berantai dan mengubahnya menjadi produk yang lebih stabil. Contohnya adalah superoskida dismutase (SOD), glutation peroksidase, dan katalase yang dapat mengubah radikal superoksida menjadi molekul air (Frei, 2004).
vitamin A (betakaroten), ester vitamin C, vitamin E, dan senyawa fitokimia (Frei, 2004).
Antioksidan tersier berperan dalam mekanisme biomolekuler, seperti memperbaiki kerusakan sel dan jaringan yang disebabkan radikal bebas (Frei, 2004).
2. Vitamin E sebagai antioksidan
Fungsi utama vitamin E adalah sebagai antioksidan yang larut dalam lemak dan mudah memberikan atom hidrogen dari gugus hidroksil (OH) pada struktur cincin ke radikal bebas. Radikal bebas menjadi tidak reaktif setelah menerima atom hidrogen. Pembentukan oksigen secara bertahap direduksi menjadi air (Kathryn et al., 2004).
Berikut ini adalah inhibisi radikal bebas yang dilakukan oleh alfa tokoferol atau (α-TOH) :
α-TOH + ROO* α-TO* + ROOH,
α-TO* + ROO* produk inaktif (1) (Jishage et al., 2005).
3. Ester vitamin C atau Askorbil palmitat sebagai antioksidan
Askorbil palmitat paling efektif sebagai antioksidan sekunder atau sinergis yang bekerja dengan mempromosikan aktivitas antioksidan primer. Misalnya, Askorbil palmitat bekerja sinergis dengan antioksidan alfa tokoferol dengan regenerasi tokoferol yang hilang selama reaksi anti oksidasi (Meves et al., 2002).
Askorbil palmitat juga dapat bertindak sebagai rantai pemecah antioksidan, namun tindakan ini lemah dan tergantung pada jenis minyak yang teroksidasi. Pemecahan rantai antioksidan lambat atau oksidasi berhenti setelah itu sudah dimulai dengan mencegat peroksil radikal yang terbentuk ketika lipid dioksidasi. Radiasi peroksil akan memberi atom atau ion pada rantai oksidasi, sehingga antioksidan pemecah rantai memutus siklus reaksi oksidasi lanjutan (Meves et al., 2002).
C. Mikroemulsi
Mikroemulsi merupakan suatu sediaan yang transparan, isotropik, memiliki viskositas rendah dan stabil secara termodinamik yang terbuat dari surfaktan, minyak dan air dengan atau tanpa kosurfaktan. Kapasitas pelarutan obat yang tinggi dari mikroemulsi memungkinkan untuk meningkatkan kelarutan dari suatu senyawa yang memiliki kelarutan rendah dalam air. Mikroemulsi dibagi dalam tiga jenis yaitu mikroemulsi air dalam minyak (A/M), minyak dalam air (M/A) dan bicontinuous. Jenis mikroemulsi yang terbentuk tergantung pada komposisi pembentuknya (Lawrence and Ress, 2000).
1. Jenis Mikroemulsi
Mikroemulsi dibagi dalam tiga jenis yaitu mikroemulsi air dalam minyak (A/M), mikroemulsi minyak dalam air (M/A) dan mikroemulsi
bicontinuous. Jenis mikroemulsi yang terbentuk tergantung pada komposisi pembentuknya. Mikroemulsi minyak dalam air terbentuk karena fraksi dari minyak rendah. Sedangkan mikroemulsi air dalam minyak terjadi ketika fraksi dari air rendah. Sistem bicontinuous mungkin terjadi jika jumlah air dan minyak hampir sama (Lawrence and Rees, 2000).
2. Teori Pembentukan Mikroemulsi
karena adanya surfaktan dengan atau tanpa kosurfaktan. Surfaktan yang ada akan menyebabkan tegangan permukaan antara minyak dan air menurun (mendekati nol sampai negatif) (Surabhi et al., 2010).
Pernyataan terbentuknya lapisan interfasial pada mikroemulsi dijelaskan dengan persamaan (2) :
(2) Dimana γi menunjukkan tegangan antar permukaan, γm/a menunjukkan
tegangan antar permukaan antara minyak dan air tanpa adanya lapisan film dan πi menunjukkan tekanan yang menyebar pada sistem dua dimensi. Saat
surfaktan dengan atau tanpa kosurfaktan ditambahkan dan teradsorpsi pada lapisan antar permukaan, maka tekanan yang menyebar (πi) akan menjadi lebih besar daripada γm/a, sehingga dihasilkan tegangan antar permukaan yang negatif (Surabhi et al., 2010).
Mekanisme pembentukkan mikroemulsi berbeda dengan pembentukkan makroemulsi. Perbedaan yang paling signifikan terletak pada usaha makroemulsi atau peningkatan jumlah emulgator yang biasanya memperbaiki stabilitasnya, tidak terjadi pada mikroemulsi. Sistem dalam mikroemulsi dipengaruhi dari pembentukkannya yang spesifik melibatkan interaksinya antara molekul minyak, emulgator dan air (Date et al., 2008). 3. Surfaktan
untuk formulasi mikroemulsi. Surfaktan harus menyokong mikroemulsifikasi dari fase minyak dan harus memiliki potensi kelarutan yang baik untuk zat aktif. Lapisan tipis emulgator harus memiliki nilai hidrofilik-lipofilik yang sesuai pada daerah antarmuka supaya dihasilkan mikroemulsi. Pemilihan surfaktan harus diatur oleh tipe mikroemulsi yang akan diformulasikan. Surfaktan dengan HLB rendah seperti sorbitan monooleat lebih disukai untuk mikroemulsi A/M sedangkan surfaktan dengan HLB tinggi seperti tween 80 lebih disukai untuk mikroemulsi M/A (Date et al., 2008).
Ada tiga tipe surfaktan yaitu tipe ionik, non ionik dan amfoterik. Surfaktan tipe ionik terdiri dari tipe anionik dan kationik. Surfaktan tipe anionik dapat berdisosiasi dalam air dan bagian anionnya dapat berfungsi sebagai surfaktan, sebagai contoh Sodium lauril sulfat. Surfaktan tipe kationik dapat berdisosiasi dalam air dan bagian kationnya dapat berfungsi sebagai surfaktan, sebagai contoh setrimid. Surfaktan tipe non ionik tidak dapat berdisosiasi dalam air, sebagai contoh tween dan span. Surfaktan amfoterik mempunyai gugus kationik dan anionik dalam molekulnya dan dapat terionisasi dalam larutan air, namun gugus yang dilepaskan tergantung kondisi mediumnya. Contoh surfaktan amfoterik adalah protein dan lesitin (Sinko, 2011).
3.1. Tween 80 dan Span 80 sebagai surfaktan
etilena oksida untuk tiap molekul sorbitol dan anhidrida sorbitol. Tween 80 dapat bertindak baik sebagai reduktor dan stabilizer tanpa menambahkan agen pereduksi tambahan ke reaksi. Tween 80 sebagai agen stabilisasi yang diadsorpsi pada permukaan nanopartikel, sehingga memperlambat pertumbuhan fase kristal dengan mengurangi energi bebas permukaan. Konsentrasi tween 80 meningkat maka menurunkan energi bebas permukaan dan karenanya stabilisasi ukuran
droplet yang lebih kecil terbentuk (Rajaram and Natham, 2013). Span 80 adalah campuran ester sorbital dengan satu mol anhidrida asam oleat. Tween 80 bersama dengan span 80 akan berperan dalam menstabilkan sistem di mana semakin banyak tween 80 akan membuat medium dispers menjadi lebih rigid. Semakin rigid
4. Kontrol Kualitas dari Sediaan Mikroemulsi
Kontrol kualitas sediaan mikroemulsi yaitu : 4.1. Uji Organoleptis
Pengujian organoleptik adalah pengujian yang didasarkan pada proses pengindraan. Evaluasi organoleptis sediaan mikroemulsi atau emulsi dilakukan dengan mengamati terjadinya pemisahan fasa atau pecahnya emulsi atau mikroemulsi, bau tengik dan perubahan warna (Lawrence and Ress, 2000).
4.2. Uji pH
Sediaan kosmetik yang diaplikasikan pada kulit sebaiknya tidak mengiritasi kulit. Oleh karena itu sediaan harus mempunyai pH normal 4,5 – 6,5. pH yang terlalu basa dapat menyebabkan kulit bersisik, sementara jika pH terlalu asam maka membuat kulit iritasi atau berwarna merah (Ali and Yosipovitch, 2013).
4.3. Uji Viskositas
temperatur, gaya tarik antar molekul dan ukuran serta jumlah molekul terlarut (Martin et al., 2010).
Viskositas suatu bahan dipengaruhi oleh beberapa faktor yaitu :
4.3.1. Suhu
Viskositas berbanding terbalik dengan suhu. Jika suhu naik maka viskositas akan turun dan begitu pula sebaliknya. Hal ini disebabkan karena adanya gerakan partikel-partikel cairan yang semakin cepat apabila suhu ditingkatkan dan menurunkan kekentalannya (Martin et al., 2010).
4.3.2. Konsentrasi larutan
Viskositas berbanding lurus dengan konsentrasi larutan. Suatu larutan dengan konsentrasi tinggi akan memiliki viskositas yang tinggi pula, karena konsentrasi larutan menyatakan banyaknya partikel zat yang terlarut tiap satuan volume. Semakin banyak partikel yang terlarut, gesekan antar partikel semakin tinggi dan viskositasnya semakin tinggi pula (Martin et al., 2010).
4.3.3. Berat molekul solut
4.3.4. Tekanan
Tekanan akan bertambah jika nilai dari viskositas itu bertambah. Semakin tinggi tekanan maka semakin besar viskositas suatu zat cair (Martin et al., 2010).
4.4. Uji Ukuran droplet Mikroemulsi
Ukuran droplet dari suatu mikroemulsi umumnya dinyatakan sebagai diameter dari globul-globul dalam fase internal. Pengujian ukuran droplet menggunakan PSA (Particle Size Analyzer) dengan tipe Dynamic Light Scattering. Prinsip dasar alatnya yaitu sampel akan diterangi oleh sinar laser dan fluktuasi cahaya yang tersebar dideteksi pada hamburan sudut θ yang dikenal oleh detektor foton
secara cepat. DLS merupakan instrumen dengan pengukuran pada sudut tetap untuk menentukan ukuran droplet rata-rata dalam berbagai ukuran terbatas (Volker, 2009).
4.5. Dilution Test
mikroemulsi air dalam minyak dapat diencerkan dengan fase minyak yang digunakan (Firoz et al., 2012).
4.6. Uji Indeks Bias
Indeks bias suatu larutan dapat diukur dengan menggunakan refraktometer. Metode ini merupkan metode yang sederhana. Indeks bias adalah perbandingan kecepatan cahaya dalam udara dengan kecepatan cahaya dalam zat tersebut. Indeks bias berguna untuk identifikasi zat dan ketakmurnian. Perambatan cahaya dalam ruang hampa udara memiliki kelajuan c, kemudian setelah memasuki medium tertentu akan berubah kelajuannya menjadi v dengan v ≪ c. Ketika cahaya merambat di dalam suatu bahan, kelajuannya akan turun sebesar suatu faktor yang ditentukan oleh karakteristik bahan yang dinamakan indeks bias (n). Indeks bias merupakan perbandingan (rasio) antara kelajuan cahaya di ruang hampa terhadap kelajuan cahaya (Bhattacharjee, 2005).
4.7. Uji Persen Transmitan
Persen transmitan merupakan salah satu faktor penting dalam mikroemulsi. Persen transmitan diperiksa dengan akuades sebagai kontrol menggunakan spektrofotometer UV-vis. Pengujian ini dilakukan untuk melihat kelarutan dan transparansi. Sampel akan dilarutkan dalam 100 mL akuades dan diukur pada λ 650 nm. Jika hasil persen transmitan sampel mendekati persen transmitan air maka sampel tersebut memiliki kejernihan atau transparansi mirip air ( Thakkar et al., 2011).
5. Uji Stabilitas Mikroemulsi
Stabilitas menggambarkan ketahanan produk, waktu penyimpanan dan penggunaan. Stabilitas sediaan mikroemulsi diamati secara fisik yang meliputi bau, warna dan kejernihan. Kestabilan termodinamik dari tipe yang dipustulatkan secara umum untuk sistem terlarut atau mikroemulsi umumnya tergantung pada temperatur (Dawaba et al., 2010).
Accelerated stability dirancang untuk meningkatkan laju degradasi kimia dan atau perubahan fisik zat obat atau produk obat dengan menggunakan kondisi penyimpanan berlebihan dengan tujuan pemantauan reaksi degradasi dan memprediksi masa simpan di bawah kondisi penyimpanan normal. Desain studi stabilitas dipercepat termasuk suhu tinggi dan rendah, kelembaban tinggi dan rendah, dan cahaya yang kuat atau rendah (Dawaba et al., 2010).
mikroemulsi. Jika mikroemulsi masih stabil maka dilanjutkan dengan uji sentrifugasi dengan kecepatan 5000 rpm selama 15 menit (Darole, et al., 2008). Pada uji freeze thaw, mikroemulsi akan disimpan pada suhu -200C dan 350C selama 24 jam sebanyak 3 siklus. Sediaan mikroemulsi dinyatakan stabil jika tidak terjadi pemisahan (Darole et al., 2008).
Mikroemulsi yang stabil ditandai dengan dispersi globul yang seragam dalam fase kontinu, namun dapat terjadi penyimpangan dari kondisi tersebut. Seperti emulsi, ketidakstabilan mikroemulsi bisa digolongkan sebagai berikut : 5.1. Creaming
Agregat dan bulatan fase dalam mempunyai kecenderungan yang lebih besar untuk naik ke permukaan mikroemulsi atau jatuh ke dasar mikroemulsi tersebut daripada partikel-partikelnya sendiri.
5.2. Flokulasi
Flokulasi adalah agregasi globul menjadi kelompok besar. Gejala ini dapat meningkatkan creaming.
5.3. Coalescence (breaking, cracking)
Kerusakan yang lebih besar daripada creaming pada suatu mikroemulsi adalah penggabungan bulatan-bulatan fase dalam (coalescence) dan pemisahan fase tersebut menjadi suatu lapisan. Pemisahan fase dalam dari mikroemulsi tersebut disebut “pecah” atau
“retak” (cracked). Hal ini bersifat irreversible karena lapisan pelindung di sekitar bulatan-bulatan fase terdispersi tidak ada lagi (Dawaba et al.,
D. Uji Iritasi Menggunakan Metode HET-CAM
Uji HET-CAM (Hen’s Egg Test on the Chorioallantoic Membrane) bertujuan untuk mengevaluasi produk kosmetik dan melihat tingkat iritasi pada sediaan solid, semi solid atau liquid (Bernardi et al., 2011). Iritasi menyebabkan perubahan dalam sistem vaskular dari HET-CAM yang menghasilkan perubahan warna, pendarahan dan peningkatan perfusi pada membran. Setiap sampel diuji pada tiga telur berumur antara 9-10 hari sebelum pengujian. CAM dibilas dengan larutan NaCl 0,9 % setelah 30 detik pemaparan masing-masing substansi atau sampel, dan dilihat reaksi yang terjadi berupa hiperemi, perdarahan dan koagulasi. Pengamatan dilakukan secara semi-kuantitatif dinilai pada skala 0,5, 2 dan 5 menit setelah perlakuan. Skor numerik bergantung pada waktu saat terjadi hiperemi, perdarahan dan koagulasi yang selanjutnya dijumlahkan untuk memberikan skor numerik tunggal. Skor yang menunjukkan potensi iritasi bahan uji pada skala dengan nilai maksimal 21 (Tavaszi and Budai, 2007).
Hemorrhage time dimulai dalam detik reaksi hemoragi atau pendarahan pada CAM. Lysis time dimulai dalam detik lisis pembuluh darah hingga pembuluh darah hilang pada CAM. Coagulation time dimulai dalam detik pembentukan koagulan pada CAM. Rumus Irritation Score (IS) yaitu :
IS =
x 5 +
(3)
Tabel I. Klasifikasi Skor Kumulatif dalam Chorioallantoic Membrane Test (Bernardi et al., 2011)
Skor Kumulatif Penilaian Iritasi 0-0,9 Praktis tidak iritasi
1-4,9 Iritasi rendah
5-8,9 Iritasi sedang
9-21 Iritasi kuat
E. Uji Aktivitas Antioksidan Menggunakan Metode DPPH Terhadap Ester vitamin C dan vitamin E
DPPH (2,2-difenil 1-pikrilhidrazil) merupakan senyawa radikal bebas berbentuk prisma, berwarna ungu tua. Metode yang digunakan untuk menguji aktivitas antioksidan suatu senyawa adalah metode uji dengan menggunakan radikal bebas DPPH. Tujuan metode ini adalah mengetahui parameter konsentrasi yang ekuivalen memberikan 50% efek aktivitas antioksidan (IC50). DPPH merupakan radikal bebas yang dapat bereaksi dengan senyawa yang dapat mendonorkan atom hidrogen, dapat berguna untuk pengujian aktivitas antioksidan komponen tertentu (Dehpour et al., 2009).
Persentase peredaman =
x 100 % (4) Dimana A1 adalah absorbansi kontrol dan A2 adalah absorbansi sampel. Suatu senyawa dikatakan sebagai antioksidan sangat kuat apabila nilai IC50 kurang dari 0,05 mg/mL, kuat apabila nilai IC50 0,05-0,10 mg/mL, sedang apabila nilai IC50 berkisar antara 0,10-0,15 mg/mL, dan lemah apabila nilai IC50 berkisar antara 0,15-0,20 mg/mL (Prakash, 2001).
stokiometri sesuai jumlah elektron yang diambil. Keberadaan senyawa antioksidan dapat mengubah warna larutan DPPH dari ungu menjadi kuning. Perubahan absorbansi akibat reaksi ini telah digunakan secara luas untuk menguji kemampuan beberapa molekul sebagai penangkap radikal bebas (Dehpour et al., 2009).
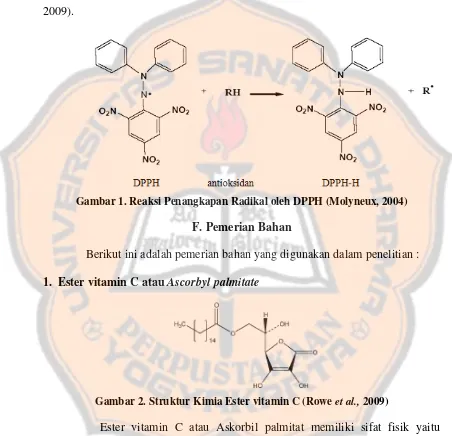
Gambar 1. Reaksi Penangkapan Radikal oleh DPPH (Molyneux, 2004)
F. Pemerian Bahan
Berikut ini adalah pemerian bahan yang digunakan dalam penelitian : 1. Ester vitamin C atau Ascorbyl palmitate
Gambar 2. Struktur Kimia Ester vitamin C (Rowe et al., 2009)
0,03-0,12%. Ester vitamin C dan vitamin E bekerja secara sinergis sebagai antioksidan (Rowe et al., 2009).
2. Vitamin E (α-tokoferol)
Alfa tokoferol merupakan senyawa yang sangat lipofilik, dan pelarut yang sangat baik untuk obat yang sukar larut. Secara umum, alfa tokoferol
merupakan produk farmasi yang berbasis lemak atau larut dalam minyak dan biasanya digunakan dalam rentang konsentrasi 0,001-0,05% v/V(Rowe et al.,
2009).
Gambar 3. Struktur Kimia Vitamin E (Rowe et al., 2009)
Vitamin E (Alfa Tokoferol) banyak terdapat dalam stratum corneum. α-tokoferol yang memiliki cincin aromatik tersubtitusi dan rantai panjang isoprenoid sebagai rantai samping. Sifat lipofilik alamiah alfa tokoferol
(vitamin E) menyebabkan ia mudah di aplikasikan dan di serap oleh kulit (Pinnell, 2003).
3. Sunflower Oil
Sunflower oil dengan stabilitas oksidasi yang baik dan bersifat emolien dapat digunakan dalam formulasi kosmetik. Sunflower oil dianggap sebagai bahan yang relatif tidak beracun dan tidak mengiritasi (Rowe et al., 2009).
Sifat fisik dari sunflower oil adalah titik didih pada 40–600C, densitas 0.915–0.919 g/cm3, melting point pada -180C, dan kelarutannya yaitu larut dengan benzena, kloroform, karbon tetraklorida, dietil eter, dan light petroleum, praktis tidak larut dalam etanol (95%) dan air (Rowe et al., 2009). 4. Tween 80
Sifat fisik dari Tween 80 yaitu dengan rumus molekul tween 80 C64H124O26, bobot molekul 1310 g/mol, warna dan bentuk pada suhu 250C yaitu cairan berminyak warna kuning, HLB yaitu 15, viskositas 42 mPa s, dan larut dalam etanol dan air, tidak larut dalam mineral oil dan vegetable oil
(Rowe et al., 2009).
Gambar 4. Struktur Kimia Tween 80 (Rowe et al., 2009)
Tween 80 bersifat stabil terhadap elektrolit, asam atau basa lemah, namun tidak cocok (incompatible) dengan basa kuat karena dapat terjadi saponifikasi. Selain itu dapat terjadi pengendapan atau perubahan warna dengan adanya fenol, tanin dan antimikroba golongan parabel (Rowe et al.,
5. Span 80
Sifat fisik span 80 yaitu cairan kuning bersifat lipofilik, larut dalam minyak dan mayoritas pelarut organik. Span 80 memiliki HLB 4,3; densitas 1,01; viskositas 970-1080 mPa s pada 250C, dan melting point 43-480 C (Rowe
et al., 2009).
Gambar 5. Struktur Kimia Span 80 (Rowe et al., 2009)
6. Aquadestilata
Aquadestilata secara luas digunakan sebagai pelarut dan pembawa pada formulasi farmasetika. Untuk aplikasi farmasi, air dimurnikan dengan caea destilasi, pertukaran ion, reverse osmosis (RO), atau beberapa proses lain yang sesuai untuk menghasilkan aquadestilata. Karakteristik aquadestilata
adalah cairan bening, tidak berwarna tidak berbau dan tidak berasa (Rowe et al., 2009).
7. DPPH (2,2-difenil 1-pikrilhidrazil)
DPPH merupakan senyawa radikal bebas berbentuk prisma, berwarna ungu tua. DPPH mempunyai berat molekul 394,3 g/mol. Titik leleh DPPH yaitu 132-1330C. DPPH dapat larut dalam air, etanol dan metanol (Pourmorad,
Gambar 6. Struktur Kimia DPPH (Pourmorad et al., 2002)
8. Etanol
Etanol merupakan cairan jernih, tidak berwarna, dan mudah menguap. Titik didih etanol sebesar 78,15oC. Etanol larut dalam kloroform, eter, gliserin dan air (Wade, 1994).
Gambar 7. Struktur Kimia Etanol (Wade, 1994)
G. Analisis Data
ANAVA merupakan salah satu jenis uji parametrik. Syarat dari uji parametrik adalah skala pengukuran variabel harus berupa variabel numerik, distribusi data yang dianalisis harus normal dapat dilakukan dengan Saphiro– Wilk, kesamaan variasi data tidak menjadi syarat mutlak untuk uji kelompok berpasangan dan untuk 2 kelompok tidak berpasangan, namun kesamaan variasi menjadi syarat yang harus dipenuhi untuk uji lebih dari 2 kelompok tidak berpasangan. Variasi data bisa dilakukan dengan uji Levene (Santoso, 2010).
parametrik yang bisa dilakukan. Alternatif uji ANAVA satu arah adalah Kruskal-Wallis (Santoso, 2010).
H. Landasan Teori
Mikroemulsi merupakan sediaan emulsi berukuran mikro yang transparan, isotropik dan stabil secara termodinamik. Sifat fisik seperti organoleptis, ukuran droplet, persen transmitan, pH, viskositas, indeks bias dan stabilitas mikroemulsi dipengaruhi oleh komponen surfaktan yang ada di dalamnya. Surfaktan tween 80 dan span 80 merupakan golongan turunan polioksietilen dan memiliki keseimbangan lipofilik dan hidrofilik dalam molekulnya. Peningkatan tween 80 akan menurunkan energi bebas permukaan dan meningkatkan luas permukaan globul sehingga ukuran globul dapat semakin diperkecil dengan ukuran mikrometer hingga nanometer serta menyebabkan organoleptis yang terbentuk jernih dan homogen (Rajaram and Natham, 2013). Tween 80 bersama dengan span 80 akan berperan dalam menstabilkan sistem di mana semakin banyak tween 80 akan membuat medium dispers menjadi lebih
rigid. Semakin rigid medium dispers akan mengakibatkan semakin meningkatnya viskositas sistem dari sediaan (Taylor, 2011).
Tingkat keamanan suatu sediaan dapat diamati berdasarkan metode HET-CAM. Skor numerik yang dihasilkan bergantung pada waktu saat terjadi hemoragi, lysis dan koagulasi yang selanjutnya dijumlahkan untuk memberikan skor numerik tunggal. Skor yang menunjukkan bahan uji tidak aman (iritatif) pada skala dengan nilai maksimal 21 (Tavaszi and Budai, 2007). Bahan-bahan yang digunakan dalam sediaan mikroemulsi diantaranya tween 80, span 80, sunflower oil, yang menurut Rowe et al., (2009) tidak bersifat mengiritasi kulit, namun pada ester vitamin C dan E bersifat mengiritasi jika digunakan berlebihan pada kulit berdasarkan MSDS.
I. Hipotesis Penelitian
1. Peningkatan tween 80 dan penurunan span 80 dalam kombinasinya tidak memberikan perubahan sifat fisik dan stabilitas fisik.
2. Sediaan mikroemulsi ester vitamin C dan vitamin E memiliki aktivitas dalam menangkap radikal bebas berdasarkan nilai IC50 melalui uji DPPH. 3. Sediaan mikroemulsi ester vitamin C dan vitamin E aman (tidak iritatif)
31 BAB III
METODOLOGI PENELITIAN
A. Jenis Rancangan Penelitian
Penelitian tentang pengaruh kombinasi surfaktan tween 80 dan span 80 terhadap sifat fisik dan stabilitas mikroemulsi ester vitamin C dan vitamin E termasuk jenis penelitian experimental murni dan rancangan acak lengkap pola searah.
B. Variabel dan Definisi Operasional
1. Variabel Penelitian
a. Variabel bebas. Variabel bebas pada penelitian ini adalah perbandingan tween 80 dan span 80 sebagai surfaktan dengan komposisi surfaktan dalam sediaan 70 %.
b. Variabel tergantung. Variabel tergantung pada penelitian ini adalah sifat fisik, stabilitas sediaan, nilai IC50 dan Irritation Score.
c. Variabel pengacau terkendali. Variabel pengacau terkendali pada penelitian ini adalah kecepatan pengadukan, lama pengadukan, suhu penyimpanan, lama penyimpanan, sifat dari wadah penyimpanan.
d. Variabel pengacau tak terkendali. Variabel pengacau terkendali pada penelitian ini adalah suhu dan kelembaban ruangan pembuatan sediaan. 2. Definisi Operasional
yang terbuat dari surfaktan, minyak dan air dengan atau tanpa kosurfaktan
b. Surfaktan. Surfaktan adalah suatu molekul yang memiliki gugus hidrofilik dan gugus lipofilik sehingga dapat mempersatukan campuran yang terdiri dari air dan minyak. Surfaktan yang digunakan yaitu kombinasi tween 80 dan span 80 dengan komposisi surfaktan dalam sediaan 70% dan perbandingan tween 80 dan span 80 yang berbeda-beda dalam sediaan mikroemulsi.
c. Ester vitamin C. Ester vitamin C yang digunakan dalam penelitian adalah Askorbil palmitat. Askorbil palmitat merupakan vitamin C (Asam askorbat) yang diesterifikasi dengan asam palmitat (asam lemak).
d. Vitamin E. Vitamin E yang digunakan dalam penelitian adalah α -tokoferol.
e. Faktor dan respon. Faktor adalah suatu hal yang dapat mempengaruhi hasil penelitian, sedangkan respon adalah hasil uji yang diamati untuk melihat besarnya pengaruh faktor. Faktor yang ada pada penelitian ini yaitu surfaktan, sedangkan respon yang tergantung berdasarkan faktor adalah organoleptis, pH, viskositas, indeks bias, ukuran droplet, persen transmitan, tipe mikroemulsi dengan dilution test, nilai IC50, stabilitas sediaan berupa freeze thaw serta uji HET-CAM.
C. Bahan Penelitian
Aquadest (Bratachem), Ester vitamin C atau Askorbil palmitat (CV. Privat Equipment Pharmacy), Vitamin E atau α-tokoferol (CV. Cipta Anugerah, Indonesia), Etanol p.a (Merck Milipore), DPPH (Laboratorium Chemmix Pratama).
D. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas (PYREX-GERMANY), viscometer Brookfield, Particle Size Analyzer tipe
Dynamic Light Scattering, Hotplate magnetic stitter, neraca analitik (OHAUS), cawan porselen, pengaduk magnetik, spektrofotometer UV (Shimadzu 1600, Jepang), pH meter (HANNA Instrument HI 9024 C), Sentrifugator (Benchtop Centrifuge PLC-05), Freezer (Toshiba), Kulkas (Sanken Logic Cool), Oven (Memmert) (Laboratorium Teknologi Semisolid-Liquid).
E. Tata Cara Penelitian
1. Orientasi Formula Sediaan Mikroemulsi Ester vitamin C dan vitamin E
a. Formula Orientasi
Formula acuan yang digunakan untuk membuat sediaan mikroemulsi minyak dalam air tertera pada tabel II yaitu :
Tabel II. Formula Mikroemulsi Acuan (Rozman et al., 2009)
Bahan (g) Formula Fungsi
Isopropol Myristate 24,65 Fase minyak
Tween 40 14,79 Surfaktan
Imwitor 308 14,79 Kosurfaktan
Ester vitamin C 0,4 Zat aktif
Zat aktif
Vitamin E 1
Berdasarkan formula di atas dilakukan modifikasi pada bagian fase minyak dan fase air, serta komponen surfaktan dibuat menjadi campuran 2 surfaktan dan kosurfaktan ditiadakan. Formula modifikasi yang dihasilkan tertera pada tabel III yaitu :
Tabel III. Orientasi Formula Mikroemulsi Ester vitamin C dan vitamin E
Bahan (g) Formula Fungsi
I II III IV V VI VII VIII
Sunflower oil 20 20 20 20 20 20 20 20 Fase minyak
Tween 80 35 46,9 52,5 56 59,99 61,25 62,23 63 Surfaktan I Span 80 35 23,1 17,5 14 10,01 8,75 7,77 7 Surfaktan II Ester vitamin
C
0,4 0,4 0,4 0,4 0,4 0,4 0,4 0,4 Zat aktif
Vitamin E 1 1 1 1 1 1 1 1 Zat aktif
Akuades 10 10 10 10 10 10 10 10 Fase air
b. Pembuatan Sediaan Mikroemulsi Ester Vitamin C dan Vitamin E Formula Orientasi
Tween 80 dan span 80 sebagai campuran surfaktan pada setiap formula dengan perbandingan 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, dan 8:1 masing-masing dicampurkan dan diaduk menggunakan magnetic stirrer
dengan kecepatan 1000 rpm selama 5-10 menit, setelah itu tambahkan 20 g
2. Evaluasi Sediaan Mikroemulsi Saat Orientasi
a. Uji Organoleptis
Pengamatan secara visual terhadap bau, bentuk, warna, homogenitas dan kejernihan sediaan mikroemulsi setelah 24 jam pembuatan.
a. Heating and Cooling Cycle
Sediaan mikroemulsi akan disimpan pada suhu 40C dan 450C selama 24 jam sebanyak 3 siklus. Pada akhir siklus diamati apakah terjadi pemisahan fase pada mikroemulsi (Darole et al., 2008).
b. Uji Sentrifugasi
Setelah sediaan mikroemulsi melalui proses Heating and Cooling Cycle, selanjutnya akan disentrifugasi dengan 5000 rpm selama 15 menit. Formula yang tidak mengalami pemisahan fase akan dipilih sebagai sampel (Darole et al., 2008).
3. Pembuatan Mikroemulsi Ester vitamin C dan vitamin E dengan Formula Hasil Orientasi
a. Formula Mikroemulsi Hasil Orientasi
Tabel IV. Formula Mikroemulsi Hasil Orientasi
Bahan (g) Formula Fungsi
V VI VII VIII
Sunflower oil 20 20 20 20 Fase minyak
Tween 80 59,99 61,62 61,25 63 Surfaktan I
Span 80 10,01 8,75 7,77 7 Surfaktan II
Ester vitamin C 0,4 0,4 0,4 0,4 Zat aktif Zat aktif
Vitamin E 1 1 1 1
b. Pembuatan Sediaan Mikroemulsi Ester Vitamin C dan Vitamin E
Tween 80 dan span 80 sebagai campuran surfaktan pada setiap formula dengan perbandingan 5:1, 6:1, 7:1, dan 8:1 masing-masing dicampurkan dan diaduk menggunakan magnetic stirrer dengan kecepatan 1000 rpm 5-10 menit, setelah itu tambahkan 20 g sunflower oil dan 1 g vitamin E sebagai fase minyak pada masing-masing formula dengan lama pengadukan 10 menit. Setelah surfaktan dan fase minyak tercampur ditambahkan 10 g aquadest sebagai fase air perlahan-lahan selama 15 menit pada setiap formula. Ester vitamin C sebanyak 0,4 g ditambahkan perlahan-lahan setelah fase air tercampur dengan fase minyak dengan pengadukan selama 15 menit. Empat formula sediaan mikroemulsi dibuat dengan tiga kali replikasi.
4. Uji Sifat Fisik Sediaan Mikroemulsi Ester vitamin C dan vitamin E
a. Uji organoleptis
Pengamatan secara visual terhadap bau, bentuk, dan warna sediaan mikroemulsi setelah 24 jam pembuatan.
b. Uji pH menggunakan pH meter
Kalibrasi pH meter dilakukan dengan cara menyalakan dan mengatur skalanya pada pH 7, kemudian menyiapkan buffer standar pH 4 dan pH 7 yang diperlukan untuk kalibrasi pH.
sampai pembacaan alat ukur itu cocok dengan pH larutan buffer yang diukur. Gabungan elektroda itu diambil dan dibilas dengan aquadest, kemudian dicelupkan dalam larutan buffer pH 4 yang ditaruh dalam
beaker glass.
Elektrode gabungan diambil dan dibilas dengan aquadest, kemudian diletakkan dalam larutan buffer yang pertama (pH 7) dan pastikan pembacaan alat menunjukkan nilai pH yang benar.
Elektrode dibilas dengan aquadest jika kalibrasi sudah selesai, selanjutnya dimasukkan ke dalam larutan uji yang ditaruh dalam beaker glass, dan selanjutnya pH larutan dibaca (Basset, 1994).
c. Dilution Test
Sampel mikroemulsi dilarutkan ke dalam fase air (1:100) dengan tujuan untuk mengetahui tipe sediaan mikroemulsi yang dihasilkan. Jika sampel mikroemulsi larut sempurna dalam akuades maka sampel tergolong dalam mikroemulsi minyak dalam air. Sampel dilarutkan dalam penyusun minyak yang ada dalam sampel yaitu
sunflower oil (1:100). Jika sampel mikroemulsi larut sempurna dalam fase minyak maka tergolong mikroemulsi tipe air dalam minyak (Firoz et al., 2012).
d. Persen transmitan
spektrofotometer uv-vis. Akuades digunakan sebagai blangko saat pengujian.
e. Indeks Bias
Penentuan indeks bias pada sampel mikroemulsi menggunakan alat Refraktometer ABBE dengan cara kerja sebagai berikut :
1) Kedua prisma dipisahkan dengan membuka klem (putar ke kanan sesuai dengan arah jarum jam) dan mengusahakan agar permukaan prisma yang bawah horizontal.
2) Prisma atau lensa dibersihkan dengan tissue lensa yang sudah dibasahi dengan etanol, lalu prisma didiamkan hingga kering. Sampel mikroemulsi yang akan diukur indeks biasnya diteteskan 1-2 tetes di atas permukaan prisma lalu dijepitkan lagi dengan prisma di atasnya.
3) Kaca cahaya diatur dengan memutar dasar prisma sehingga penglihatan sebelah atas terang dan sebelah bawah gelap, selanjutnya dasar prisma diputar perlahan-lahan (sekrup pada busur skala pembacaan 1, 2, 3) sampai batas terlihat jelas perpotongan gelap terang.
f. Viskositas
Pengukuran viskositas menggunakan alat Viscometer Brookfield. Sediaan mikroemulsi dimasukan ke dalam bekker glass 250 mL di pasang pada portable viscotester. Viscometer brookfield diatur dengan kecepatan 12 rpm dan 6 kali putaran selama 30 detik. Viskositas mikroemulsi diketahui dengan mengamati penunjuk viskositas secara analitis.
g. Uji ukuran droplet
Ukuran droplet mikroemulsi formula 5 dan 4 diuji menggunakan Particle Size Analyzer dengan tipe Dynamic light Scattering.
5. Uji Stabilitas Dipercepat menggunakan freeze thaw a. Uji Freeze thaw
Sediaan mikroemulsi akan disimpan pada suhu -200C dan 350C selama 24 jam sebanyak 3 siklus. Diakhir siklus diamati apakah terjadi pemisahan fase pada mikroemulsi. Pada sampel yang tidak mengalami pemisahan selanjutnya diuji organoleptis, ukuran droplet, pH, persen transmitan dan viskositas (Darole et al., 2008).
6. Uji HET-CAM
a. Penyiapan Telur.
udara yang selanjutnya akan digunakan untuk tempat meneteskan bahan. Penetesan dilakukan pada daerah membran yang dekat dengan pembuluh darah.
b. Kontrol Positif (NaOH 0,1 N).
0,4 gram NaOH padat ditimbang dan dilarutkan dengan aquadest
lalu dimasukkan ke dalam labu ukur 100 mL dan ditambahkan aquadest
hingga tanda.
c. Kontrol Negatif (0,9 % NaCl).
0,9 gram NaCl padat ditimbang dan dilarutkan dengan aquadest
lalu dimasukkan ke dalam labu ukur 100 mL dan ditambahkan aquadest
hingga tanda. d. Perlakuan.
Telur-telur yang telah dibuka cangkangnya diberi perlakuan sebagai berikut:
1. Diberi NaOH sebanyak 0,3 mL 2. Diberi NaCl sebanyak 0,3 mL
3. Diberi sampel mikroemulsi formula 5, 6, 7 dan 8 sebanyak 0,3 gram. Setiap perlakuan dilakukan sebanyak 3 kali replikasi, lalu diamati perubahannya hingga 300 detik.
e. Pengamatan.
diamati adalah hemoragi (pendarahan), vascular lysis (disintegrasi pembuluh darah) dan koagulasi (denaturasi protein ekstra dan intra vaskular).
Hemorrhage time dimulai dalam detik reaksi hemoragi atau pendarahan pada CAM. Lysis time dimulai dalam detik lisis pembuluh darah hingga pembuluh darah hilang pada CAM. Coagulation time dimulai dalam detik pembentukan koagulan pada CAM. Hasil yang diperoleh digambarkan dalam bentuk skoring dengan menggunakan rumus persamaan (3).
7. Uji Aktivitas Antioksidan pada Sedian Mikroemulsi
a. Pembuatan Larutan DPPH 0,4 mM atau 0,158 mg/mL
Sebanyak 15,8 mg serbuk DPPH dilarutkan dalam etanol p.a. pada labu takar 100 mL dengan konsentrasi 0,158 mg/mL.
b. Penentuan Panjang Gelombang Maksimum DPPH
Larutan DPPH sebanyak 0,5; 1,0; 1,5 mL dimasukkan ke dalam 3 labu ukur 10 mL, kemudian ditambah etanol p.a hingga tanda batas sehingga konsentrasi DPPH menjadi 0,0079; 0,0158; dan 0,0287 mg/mL. Larutan tersebut divortex selama 30 detik dan didiamkan selama