FORMULASI EMULGEL ANTI ACNE EKSTRAK KULIT BUAH MANGGIS (Garcinia mangostana L.): PENGARUH KECEPATAN PUTAR
PADA PROSES PENCAMPURAN TERHADAP SIFAT FISIK DAN STABILITAS FISIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Kristin Yunita NIM : 108114137
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
FORMULASI EMULGEL ANTI ACNE EKSTRAK KULIT BUAH MANGGIS (Garcinia mangostana L.): PENGARUH KECEPATAN PUTAR
PADA PROSES PENCAMPURAN TERHADAP SIFAT FISIK DAN STABILITAS FISIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Kristin Yunita NIM : 108114137
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Segala perkara dapat kutanggung
di dalam Dia yang memberi kekuatan
kepadaku (Filipi 4:13)
“Whatever you are, be a good one”
―
Abraham Lincoln
―
“What we know is a drop, what we don’t know is an ocean”
―
Isaac Newton
―
Kupersembahkan karya ini untuk:
vii PRAKATA
Puji syukur kepada Tuhan Yesus Kristus atas berkat dan penyertaan yang
telah diberikan kepada penulis sehingga penulis dapat menyelesaikan skripsi
dengan judul “Formulasi Emulgel Anti Acne Ekstrak Kulit Buah Manggis (Garcinia mangostana L.):Pengaruh Kecepatan Putar pada Proses Pencampuran
terhadap Sifat Fisik dan Stabilitas Fisik”ini dengan baik.
Penulis banyak mengalami kesulitan dan hambatan dalam proses
penyusunan skripsi ini. Namun, dengan adanya bantuan dan dukungan dari
perbagai pihak, akhirnya penulis dapat menyelesaikan penyusunan skripsi ini.
Oleh karena itu, dengan kerendahan hati penulis ingin mengucapkan terimakasih
kepada:
1. Kedua orang tua yang telah memberikan kasih sayang, semangat, dukungan,
dan perjuangan untuk membiayai selama penulis menempuh perkuliahan.
2. Ipang Djunarko, M.Sc., Apt., selaku dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
3. Dr. Sri Hartati Yuliani, M.Si., Apt., selaku dosen pembimbing atas bimbingan,
arahan, perhatian, semangat, dukungan dan kesabaran yang diberikan selama
penyusunan skripsi ini.
4. Melania Perwitasari M.Sc., Apt. selaku dosen penguji atas bimbingan, saran
dan pengarahannya selama penyusunan skripsi ini.
5. C. M. Ratna Rini Nastiti, M.Pharm., Apt. selaku dosen penguji sekaligus
viii
selama penyusunan skripsi ini serta segala perhatian yang diberikan kepada
penulis selama menempuh perkuliahan.
6. Maria Dwi Budi Jumpowati, S.Si., Enade Perdana Istyastono, Ph.D., serta
Prof. Dr. Sri Noegrohati, Apt., atas kesediaan untuk berkonsultasi dan
memberikan pengetahuan yang bermanfaat bagi penulis.
7. Dominikus Arif Budi Prasetyo, M.Si., dan Ir. Ignatius Aris Dwiatmoko,
M.Sc., atas kesediaan untuk berkonsultasi dan masukan-masukan yang
diberikan.
8. Segenap dosen atas kesabarannya dalam mengajar dan membimbing penulis
selama perkuliahan di Fakultas Farmasi Universitas Sanata Dharma.
9. Pak Musrifin, Mas Agung, Mas Bimo, Pak Mukminin dan laboran-laboran
lain atas bantuan yang diberikan selama penelitian dan menempuh
perkuliahan.
10.Oh Andri dan Nadya serta seluruh keluarga yang senantiasa mendoakan serta
memberikan dukungan dan semangat kepada penulis.
11.Rosi dan Vian selaku teman satu tim penelitian atas kerja sama, semangat,
dukungan dan suka duka yang telah dilewati bersama.
12.Sahabat-sahabatku Anggun, Stien, Neno, Kezia, Nover yang selalu
menguatkan, menghibur dan mendoakan selama ini serta canda tawa yang
telah dilewati bersama.
13.Ka Mey, Ka Windra, Gref, Kristy, Malindo, William, Niko, Kevin, Angel,
ix
Yogyakarta khususnya cell group Jehovah Immeka dan Christ Image untuk
semangat, doa, perhatian, dan pengertian yang diberikan selama ini.
14.Teman-teman kelompok PKM-M 3B (Istri, Shella, Remma) atas dukungan,
doa dan keceriaan selama ini.
15.Naomi, Bakti, Devina, Nia, Maria, Nita Go, Cindy, Lia, Nita Rahayu, Eliza,
Bella, Tora, Hans, Widya, Sisca, Sita, Agrif atas kebersamaan dalam proses
penelitian di lantai 1.
16.Semua teman-teman angkatan 2010, khususnya kelas FST-B atas
kebersamaan, semangat, dukungan dan keceriaan selama ini.
17.Semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah
membantu dalam menyelesaikan skripsi ini.
Penulis menyadari bahwa dalam penulisan skripsi ini terdapat banyak
kekurangan mengingat adanya keterbatasan kemampuan dan pengetahuan penulis.
Oleh karena itu, penulis mengharapkan saran dan kritik yang membangun dari
semua pihak. Semoga skripsi ini dapat bermanfaat bagi pembaca.
x
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN... iv
PERNYATAAN KEASLIAN KARYA ... v
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI UNTUK KEPENTINGAN AKADEMIS ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xviii
xi
BAB II. PENELAAHAN PUSTAKA... 8
A. Jerawat... 8
B. Manggis ... 10
1. Keterangan botani ... 10
2. Kandungan kimia dan kegunaan ... 11
C. Emulgel ... 13
H. Uji Potensi Antibakteri ... 30
I. Metode Kromatografi Lapis Tipis (KLT) - Densitometri ... 32
xii
K. Hipotesis ... 34
BAB III. METODOLOGI PENELITIAN... 35
A. Jenis dan Rancangan Penelitian ... 35
B. Variabel Penelitian dan Definisi Operasional ... 35
1. Variabel penelitian ... 35
2. Definisi operasional ... 36
C. Alat dan Bahan Penelitian ... 38
1. Alat penelitian ... 38
2. Bahan penelitian ... 38
D. Tata Cara Penelitian ... 39
1. Identifikasi bahan ... 39
2. Pembuatan emulgel anti acne ekstrak kulit buah manggis dengan variasi kecepatan putar ... 39
3. Uji pH emulgel ... 41
4. Uji sterilitas emulgel ... 42
5. Pengujian tipe emulsi dengan metode pengenceran... 43
6. Uji sifat fisik emulgel ... 43
7. Uji stabilitas fisik emulgel ... 44
8. Uji iritasi dengan HET-CAM ... 44
9. Uji daya antimikroba emulgel ekstak kulit buah manggis terhadap Staphylococcus epidermidis ... 45
xiii
E. Analisis Data ... 49
BAB IV. HASIL DAN PEMBAHASAN ... 52
A. Identifikasi Ekstrak Kulit Buah Manggis ... 52
B. Formulasi Emulgel dengan Variasi Kecepatan Putar Mixer ... 52
C. Pengamatan Organoleptis Emulgel ... 61
D. Uji pH Emulgel ... 62
E. Uji Sterilitas Emulgel ... 62
F. Uji Tipe Emulsi ... 64
G. Uji Sifat Fisik Emulgel... 65
H. Uji Stabilitas Fisik Sediaan Emulgel... 67
I. Pengaruh Kecepatan Putar terhadap Viskositas, Daya Sebar, dan Pergeseran Viskositas ... 70
1. Viskositas ... 70
2. Daya sebar ... 73
3. Pergeseran viskositas ... 74
J. Uji Iritasi dengan HET-CAM... 75
K. Uji Daya Antimikroba Emulgel terhadap Staphylococcus epidermidis ... 77
L. Penetapan Kadar Alfa Mangostin dalam Emulgel dengan KLT-Densitometri ... 81
1. Pembuatan kurva baku alfa mangostin ... 82
xiv
3. Penetapan kadar alfa mangostin dalam emulgel ekstrak kulit
buah manggis ... 84
BAB V. KESIMPULAN DAN SARAN ... 87
A. Kesimpulan ... 87
B. Saran ... 87
DAFTAR PUSTAKA ... 88
LAMPIRAN ... 93
xv
DAFTAR TABEL
Tabel I. Kategori iritasi berdasarkan skor iritasi pada HET-CAM... 30
Tabel II. Klasifikasi aktivitas antibakteri berdasarkan diameter zona
hambat ... 32
Tabel III. Formula emulgel chlorphenesin ... 40
Tabel IV. Formula emulgel ekstrak kulit buah manggis ... 40
Tabel V. Variasi kecepatan putar pada proses pembuatan emulgel
ekstrak kulit buah manggis... 41
Tabel VI. Hasil uji zona hambat formula orientasi emulgel terhadap
Staphylococcus epidermidis dengan variasi konsentrasi ekstrak kulit buah manggis... 54
Tabel VII. Hasil uji sifat fisik emulgel setelah sterilisasi ... 66
Tabel VIII. Hasil uji stabilitas fisik emulgel ... 69
Tabel IX. Hasil uji zona hambat tiap fomula, kontrol basis dan kontrol
positif... 79
Tabel X. Kadar alfa mangostin dalam emulgel ekstrak kulit buah
xvi
Gambar 5. Unit monomer asam akrilat dari polimer carbopol ... 17
Gambar 6. Propilen glikol ... 18
Gambar 13. Membran chorioallantoic pada telur ayam ... 29
Gambar 14. Skema droplet minyak pada emulsi minyak dalam air, menunjukkan arah molekul tween dan span pada antarmuka .. 57
Gambar 15. Gambaran skematis molekul carbopol dalam keadaan uncoil dengan ikatan hidrogen ... 58
Gambar 16. Cross-link polimer asam akrilat dalam bentuk coil (sebelum kontak dengan air) ... 59
xvii
Gambar 18. Cross-link polimer asam akrilat dalam bentuk uncoil setelah
netralisasi... 60
Gambar 19. Sediaan emulgel saat diaplikasikan di kulit ... 61
Gambar 20. Uji sterilitas emulgel dibandingkan dengan kontrol kontaminasi media ... 64
Gambar 21. Uji tipe emulsi ... 65
Gambar 22. Penampilan emulgel setelah pembuatan dan setelah penyimpanan satu bulan ... 68
Gambar 23. Profil kurva variasi kecepatan putar terhadap viskositas ... 71
Gambar 24. Perubahan bentuk polimer akibat shearing stress ... 72
Gambar 25. Profil kurva variasi kecepatan putar terhadap daya sebar ... 73
Gambar 26. Uji iritasi dengan HET-CAM: perlakuan NaOH 0,1 N dan perlakuan emulgel eksrak kulit buah manggis ... 77
Gambar 27. Uji zona hambat emulgel terhadap Staphylococcus epidermidis ... 79
xviii
DAFTAR LAMPIRAN
Lampiran 1. Certificate of Analysis ekstrak kulit buah manggis ... 93
Lampiran 2. MSDS ekstrak kulit buah manggis ... 94
Lampiran 3. Sertifikat hasil uji Staphylococcus epidermidis ... 96
Lampiran 4. Perhitungan HLB ... 97
Lampiran 5. Hasil uji zona hambat formula orientasi emulgel terhadap Staphylococcus epidermidis dengan variasi konsentrasi ekstrak kulit buah manggis... 97
Lampiran 6. Hasil uji sifat fisik dan stabilitas fisik emulgel ... 97
Lampiran 7. Analisis statistika sifat fisik dan stabilitas fisik emulgel menggunakan program R 2.13.2 ... 100
Lampiran 8. Hasil uji iritasi emulgel dengan HET-CAM ... 114
Lampiran 9. Hasil uji antimikroba emulgel terhadap Staphylococcus epidermidis ... 115
Lampiran 10. Analisis statistika uji antimikroba emulgel terhadap Staphylococcus epidermidis ... 116
Lampiran 11. Hasil penetapan kadar alfa mangostin dalam emulgel ekstrak kulit buah manggis ... 118
Lampiran 12. Analisis statistika penetapan kadar alfa mangostin dalam emulgel ekstrak kulit buah manggis ... 135
xix INTISARI
Sifat fisik dan stabilitas fisik emulgel dipengaruhi oleh proses pencampuran yaitu kecepatan putar. Penelitian ini bertujuan untuk mengetahui
signifikansi pengaruh kecepatan putar mixer terhadap sifat fisik dan stabilitas fisik
emulgel anti acne ekstrak kulit buah manggis.
Jenis penelitian adalah eksperimental murni dengan lima variasi kecepatan putar yaitu 100, 300, 500, 700, dan 900 rpm. Sifat fisik yang diamati meliputi viskositas dan daya sebar sedangkan stabilitas fisik berfokus pada pergeseran viskositas setelah satu bulan penyimpanan. Data dianalisis dengan menggunakan
program R 2.13.2 dengan uji ANOVA untuk data parametrik serta uji
Kruskal-wallis untuk data nonparametrik. Analisis statistik dilakukan dengan taraf kepercayaan 95%. Organoleptis, iritasi, aktivitas antimikroba emulgel terhadap
Staphylococcus epidermidis, bakteri penginduksi timbulnya jerawat juga diamati pada penelitian ini.
Hasil analisis data menunjukkan bahwa kecepatan putar berpengaruh signifikan terhadap viskositas dan daya sebar serta tidak berpengaruh signifikan terhadap pergeseran viskositas. Seluruh formula memenuhi persyaratan sifat fisik dan stabilitas fisik sesuai dengan kriteria.
xx
ABSTRACT
Physical properties and physical stability of emulgel are influenced by mixing process that is mixing rate. The aim of this study was to determine the effect of mixing rate on the physical properties and physical stability of anti acne emulgel of the mangosteen pericarp extract.
The study was pure experimental study with five variations of mixing rate, 100, 300, 500, 700, and 900 rpm. Physical properties observed were focused on viscosity and spreadabiliy while for physical stability was on viscosity shift after one month storage. Data were analyzed using R 2.13.2 program with ANOVA test for parametric data and Kruskal-wallis test for nonparametric data. Statistical analysis was performed at 95% confidence interval. Organoleptic, irritation, and antimicrobial activity of emulgel against Staphylococcus epidermidis, an acne inducing bacteria were also studied.
The result of this study showed that mixing rate was significantly affecting the viscosity and spreadability but not significantly affecting the viscosity shift. All of the formula was eligible the physical properties and physical stability in accordance with criteria.
1 BAB I PENGANTAR
A. Latar Belakang
Kulit terutama kulit wajah merupakan salah satu simbol penampilan yang
penting bagi pria dan wanita, oleh karenanya sangat penting untuk menjaga dan
merawat kulit wajah dengan baik agar selalu sehat. Salah satu masalah yang
paling sering dialami pada kulit wajah adalah jerawat. Munculnya jerawat menjadi
masalah yang penting karena menimbulkan kesan kurang menarik dalam
penampilan seseorang (Wirakusumah, 2007).
Jerawat adalah kondisi abnormal kulit akibat gangguan berlebihan
produksi kelenjar minyak (sebaceous gland) yang menyebabkan penyumbatan
saluran folikel rambut dan pori-pori kulit (Wirakusumah, 2007). Terdapat empat
faktor penting yang memicu terjadinya jerawat, yaitu tersumbatnya folikel rambut
oleh sel yang secara normal mengalami deskuamasi, hiperaktivitas kelenjar
minyak (sebaceous gland), proliferasi bakteri di dalam sebum, dan inflamasi
(Johnson and Nunley, 2000). Jerawat yang terjadi dengan adanya infeksi bakteri
bisa menyebabkan terjadinya inflamasi dan berakibat bertambah parahnya
jerawat. Propionibacterium acnes, Staphyloccocus epidermidis dan
Staphyloccocus aureus adalah tiga strain bakteri yang dapat menginduksi terjadinya jerawat (Sukatta, Rugthaworn, Pitpiangchan, Dilokkunanant, 2008).
Kulit buah manggis (Garcinia mangostana L.) merupakan bahan alam
pertumbuhan Staphyloccocus epidermidis (Sukatta, et al., 2008). Hal ini
dibuktikan oleh penelitian yang dilakukan oleh Pothitirat, Chomnawang,
Gritsanapan (2010), ekstrak etanol kulit buah manggis dengan kandungan alfa
mangostin 18,03 ± 80,71 % b/b dapat menghambat pertumbuhan bakteri
Staphylococcus epidermidis dengan nilai Kadar Hambat Minimum (KHM)
sebesar 7,81 g/ml serta memilki nilai Kadar Bunuh Minimum (KBM) sebesar
62,50 g/ml.
Berdasarkan Torrungruang, Vichienroj, Chutimaworapan (2007) aktivitas
antibakteri yang dihasilkan dari ekstrak kulit buah manggis berasal dari xanthone
dimana alfa mangostin merupakan turunan xanthone yang memiliki aktivitas
antibakteri paling poten. Alfa mangostin merupakan zat aktif yang bersifat
hidrofobik. Oleh karena itu ekstrak kulit buah manggis diformulasikan ke dalam
bentuk sediaan emulgel karena menurut Panwar, Upadhyay, Bairagi, Gujar,
Darwhekar, Jain (2011) bentuk sediaan emulgel bersifat lebih stabil dan
merupakan suatu pembawa dengan pelepasan yang lebih baik bagi obat yang
bersifat hidrofobik. Emulgel merupakan sistem gabungan antara emulsi dengan
gel dimana suatu senyawa hidrofobik dapat dengan mudah dimasukkan ke dalam
gel menggunakan emulsi dengan tipe obat/minyak/air.
Pencampuran merupakan suatu proses yang penting dalam pembuatan
suatu sediaan karena berperan untuk mencapai distribusi bahan yang homogen
dalam suatu sediaan (Voigt, 1995). Banyak faktor yang mempengaruhi proses
pencampuran pada sediaan dengan sistem non-Newtonian, antara lain suhu,
Marti-Mestres, 2000). Proses pencampuran memerlukan energi kinetik dimana
kecepatan putar mixer akan memberikan energi kinetik berupa gaya geser yang
mempengaruhi perubahan sifat fisik emulgel seperti viskositas. Hal ini karena
emulgel memiliki sistem reologi non-Newtonian sehingga reologi dan viskositas
sangat dipengaruhi oleh berbagai gaya geser yang dihasilkan oleh kecepatan putar
alat. Gaya geser yang diaplikasikan selama proses pencampuran tersebut dapat
menurunkan viskositas sehingga mempengaruhi sifat fisik emulgel dan
selanjutnya berpengaruh terhadap kualitas sediaan yang terbentuk (Amiji and
Sandmann, 2003). Penurunan viskositas emulgel menyebabkan emulgel semakin
encer dan dapat menyebabkan penurunan stabilitas fisik emulgel selama
penyimpanan.
Voigt (1995) menyatakan bahwa setiap alat pengemulsi memiliki
kecepatan pengadukan yang optimal. Sehingga pencampuran yang berlangsung
dengan kecepatan putar yang lebih tinggi belum tentu meningkatkan kualitasnya.
Selain itu, dalam skala industri, efisiensi jumlah energi yang digunakan
merupakan faktor penting yang perlu diperhatikan dimana semakin besar energi
yang digunakan, semakin besar pula biaya produksi yang diperlukan.
Berdasarkan latar belakang di atas, diketahui bahwa variasi kecepatan
putar pada proses pembuatan emulgel dimungkinkan memiliki pengaruh dalam
menghasilkan emulgel yang memenuhi persyaratan sifat fisik dan stabilitas fisik
yang baik. Oleh karena itu, perlu dilakukan penelitian untuk mengetahui pengaruh
buah manggis sehingga dapat dihasilkan sediaan emulgel yang memiliki sifat fisik
dan stabilitas fisik yang memenuhi kriteria.
1. Perumusan masalah
Berdasarkan latar belakang tersebut, permasalahan yang diangkat
penulis dalam penelitian ini adalah sebagai berikut:
a. Apakah diperoleh formula yang memenuhi persyaratan sifat fisik dan
stabilitas fisik yang sesuai dengan kriteria?
b. Apakah variasi kecepatan putar memberikan pengaruh yang signifikan
terhadap sifat fisik dan stabilitas fisik emulgel ekstrak kulit buah manggis
(Garcinia mangostana L.)?
2. Keaslian penelitian
Penelitian yang relevan pernah dilakukan oleh Pothitirat, et al. (2010)
yang meneliti tentang aktivitas antibakteri ekstrak etanol kulit buah manggis
terhadap bakteri penginduksi timbulnya jerawat, yaitu Propionibacterium
acnes dan Staphylococcus epidermidis. Hasilnya ekstrak etanol kulit buah
manggis dengan kandungan alfa mangostin 18,03 ± 80,71 % b/b memiliki
nilai KHM 7,81 g/ml terhadap Propionibacterium acnes dan Staphylococcus
epidermidis serta memilki nilai KBM 15,63 g/ml untuk Propionibacterium
acnes dan 62,50 g/ml tehadap Staphylococcus epidermidis.
Sukatta, et al. (2008) memformulasikan ekstrak etanol kulit buah
Carbopol Ultrez-10 dan konsentrasi ekstrak kulit buah manggis dengan aplikasi desain faktorial. Hasilnya diperoleh formula optimal dengan
konsentrasi Carbopol Ultrez-10 0,5% dan konsentrasi ekstrak kulit buah
manggis 0,5% berdasarkan hasil hedonic scale terhadap warna, viskositas,
absorpsi kulit, kemampuan melembabkan kulit dan penerimaan pasien.
Formula optimal gel yang dihasilkan memiliki aktivitas yang tinggi dalam
menghambat pertumbuhan bakteri penginduksi timbulnya jerawat yang
ditandai dengan adanya zona hambat terhadap Staphylococcus aureus sebesar
24,67 mm, Staphylococcus epidermidis sebesar 10,00 mm dan
Propionibacterium acnes sebesar 7,33 mm.
Penelitian tentang pengaruh proses pencampuran dalam formulasi
sediaan emulgel (kajian dari aspek suhu dan kecepatan pencampuran) pernah
dilakukan oleh Lestari (2012) dengan menggunakan zat aktif yang berbeda,
yaitu ekstrak teh hijau dengan menggunakan desain faktorial dua faktor dan
dua level. Hasil yang didapatkan adalah faktor suhu dan interaksi suhu dengan
kecepatan putar mixer berpengaruh terhadap respon pergeseran viskositas.
Sejauh penelusuran pustaka yang dilakukan oleh penulis, penelitian
tentang Formulasi Emulgel Anti Acne Ekstrak Kulit Buah Manggis (Garcinia
mangostana L.): Pengaruh Kecepatan Putar pada Proses Pencampuran
3. Manfaat penelitian a. Manfaat teoretis
Hasil penelitian diharapkan dapat menambah khasanah ilmu
pengetahuan tentang pengaruh kecepatan putar pada proses pencampuran
emulgel terhadap sifat fisik dan stabilitas fisik emulgel ekstrak kulit buah
manggis agar dapat dihasilkan emulgel dengan sifat yang diinginkan.
b. Manfaat praktis
Penelitian ini diharapkan dapat menghasilkan bentuk sediaan
kosmetik berupa obat jerawat ekstrak kulit buah manggis yang memenuhi
persyaratan sifat fisik dan stabilitas fisik dengan proses produksi yang
efisien.
c. Manfaat metodologis
Penelitian ini diharapkan dapat menambah informasi dalam bidang
kefarmasian mengenai contoh aplikasi penerapan uji statistika dalam
mengamati pengaruh kecepatan putar pada proses pencampuran emulgel
terhadap sifat fisik dan stabilitas fisik emulgel ekstrak kulit buah manggis.
B. Tujuan Penelitian 1. Tujuan umum
Secara umum, penelitian ini bertujuan untuk membuat sediaan emulgel
anti acne dari ekstrak kulit buah manggis dengan sifat fisik (viskositas dan
daya sebar) serta stabilitas fisik (pergeseran viskositas) yang memenuhi
2. Tujuan khusus
Secara khusus penelitian ini bertujuan untuk mengetahui signifikansi
pengaruh kecepatan putar pada proses pencampuran terhadap sifat fisik dan
8
menyebabkan penyumbatan saluran folikel rambut dan pori-pori kulit
(Wirakusumah, 2007). Terdapat empat faktor penting yang memicu terjadinya
jerawat, yaitu tersumbatnya folikel rambut oleh sel yang secara normal mengalami
deskuamasi, hiperaktivitas kelenjar sebasea (sebaceous gland), proliferasi bakteri
di dalam sebum, dan inflamasi (Johnson and Nunley, 2000). Propionibacterium
acnes, Staphyloccocus epidermidis dan Staphyloccocus aureus adalah tiga strain
bakteri yang dapat menginduksi terjadinya jerawat (Sukatta, et al., 2008).
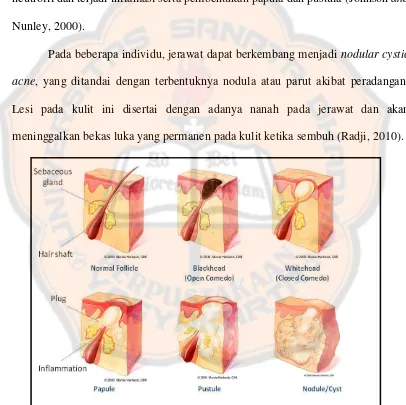
Jerawat atau acne dapat dibagi dalam tiga kategori yaitu komedo,
inflamasi dan nodular cystic acne. Jerawat terjadi apabila saluran ke permukaan
kulit untuk mengeluarkan sebum yang diproduksi oleh kelenjar minyak rambut
pada lapisan dermis tersumbat. Dalam keadaan normal, sel-sel folikel rambut
dapat keluar. Akan tetapi, jika terjadi jerawat, sel-sel folikel rambut bersama
dengan sebum akan menggumpal dan menyumbat saluran folikel rambut pada
lapisan epidermis kulit sehingga membentuk komedo yang menonjol di
permukaan kulit (Radji, 2010).
Komedo dapat berkembang menjadi inflamasi (inflammatory acne) apabila
menggunakan gliserol dalam sebum sebagai sumber nutrisi. (Radji, 2010).
Inflamasi yang terjadi timbul dari aksi enzim yang dihasilkan oleh bakteri. Enzim
ini menghidrolisis sebum menjadi asam lemak bebas, yang merangsang proses
inflamasi. Chemotactic factor dilepaskan pada reaksi ini sehingga menarik
neutrofil dan terjadi inflamasi serta pembentukan papula dan pustula (Johnson and
Nunley, 2000).
Pada beberapa individu, jerawat dapat berkembang menjadi nodular cystic
acne, yang ditandai dengan terbentuknya nodula atau parut akibat peradangan.
Lesi pada kulit ini disertai dengan adanya nanah pada jerawat dan akan
meninggalkan bekas luka yang permanen pada kulit ketika sembuh (Radji, 2010).
B. Manggis 1. Keterangan botani
Manggis (Garcinia mangostana L.) merupakan tanaman yang berasal
dari semenanjung Malaya kemudian menyebar ke seluruh daerah tropis di
Asia dan Australia. Di Indonesia, manggis dapat tumbuh mulai dari dataran
rendah hingga pegunungan dengan kisaran ketinggian 5-1.000 meter di atas
permukaan laut. Umumnya, tanaman manggis berbuah cukup baik di daerah
yang agak sejuk (Suhono dan LIPI, 2010).
Tanaman ini memiliki banyak nama daerah, antara lain: manggis
(Jawa, Melayu, Bali), manggu (Sunda), magi (Nias, Aceh), magisto (Batak),
kokapa (Mentawai), mangos (Kubu), sungkup (Dayak) dan kirasa (Makassar)
(Suhono dan LIPI, 2010). Klasifikasi tanaman manggis adalah sebagai berikut:
kingdom : Plantae (tumbuhan)
subkingdom : Tracheobionta (tumbuhan berpembuluh)
super divisi : Spermatophyta (menghasilkan biji)
divisi : Magnoliophyta (tumbuhan berbunga)
kelas : Magnoliopsida (berkeping dua/dikotil)
subkelas : Dilleniidae
ordo : Theales
famili : Clusiaceae
genus : Garcinia
spesies : Garcinia mangostana L. (Natural Resources Conservation
Morfologi tanaman manggis yaitu pohon memiliki tinggi 10-25 m,
batang berwarna cokelat keabu-abuan dan berdiameter 40-80 cm. Kayu batang
berwarna cokelat tua. Kulit batangnya mengeluarkan getah bila dilukai. Daun
berwarna hijau, kaku, mengilap, berbentuk lonjong, berujung lancip, terletak
berhadapan, dan berukuran 8 x 4 cm serta yang besar berukuran 12 x 5 cm
(Suhono dan LIPI, 2010).
Bunga manggis berwarna merah muda, terletak di ujung cabang daun.
Buah berdiameter 4-6,5 cm. Buah muda berwarna hijau dan bergetah kuning,
bila masak berwarna ungu kehitaman. Kulit buah bagian dalam tebal dan
berwarna merah. Biji ditutupi oleh aril berwarna putih. Setiap buah
mengandung 2-8 biji (Suhono dan LIPI, 2010).
2. Kandungan kimia dan kegunaan
Kulit buah manggis telah digunakan dalam obat-obatan tradisional
Asia untuk pengobatan luka, infeksi kulit, diare, disentri serta maag kronis.
Kulit buah manggis memiliki kandungan xanthone yang tinggi serta
mengandung zat bioaktif lainnya seperti tanin, flavonoid dan polifenol
(Pothitirat, et al., 2010).
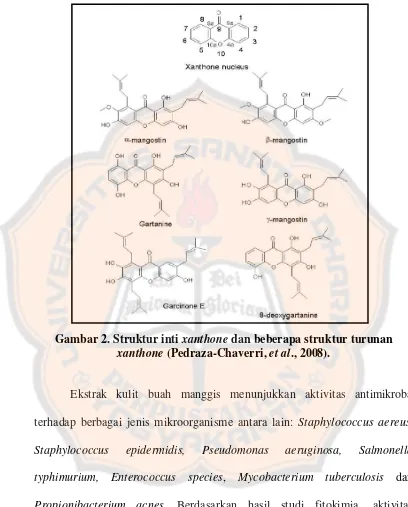
Xanthone memiliki aktivitas antioksidan, antitumor, antialergi,
antiinflamasi, antibakteri, antijamur dan antivirus. Beberapa turunan xanthone
yang paling banyak diteliti adalah α, β dan γ-mangostin, garcinone E,
8-deoxygartanin, dan gartanin (Pedraza-Chaverri, Cárdenas-Rodríguez,
Gambar 2. Struktur inti xanthone dan beberapa struktur turunan
xanthone (Pedraza-Chaverri, et al., 2008).
Ekstrak kulit buah manggis menunjukkan aktivitas antimikroba
terhadap berbagai jenis mikroorganisme antara lain: Staphylococcus aereus,
Staphylococcus epidermidis, Pseudomonas aeruginosa, Salmonella typhimurium, Enterococcus species, Mycobacterium tuberculosis dan
Propionibacterium acnes. Berdasarkan hasil studi fitokimia, aktivitas antimikroba yang dihasilkan berasal dari xanthone. Alfa mangostin merupakan
turunan xanthone yang memiliki aktivitas antibakteri paling poten
Ekstrak kulit buah manggis memiliki aktivitas antimikroba yang tinggi
terhadap bakteri penyebab timbulnya peradangan jerawat yaitu
Propionibacterium acnes dan Staphylococcus epidermidis. Ekstrak etanol kulit buah manggis dengan kandungan alfa mangostin 18,03 ± 0,71 % b/b
memiliki nilai KHM 7,81 g/ml untuk kedua strain bakteri serta memiliki nilai
KBM 15,63 g/ml untuk Propionibacterium acnes dan 62,50 g/ml untuk
Staphylococcus epidermidis (Pothitirat, et al., 2010).
C. Emulgel
Gel merupakan suatu bentuk sediaan semisolid yang mengandung
komposisi air dalam jumlah tinggi sehingga dapat meningkatkan disolusi obat dan
juga memudahkan migrasi obat melalui basis yang utamanya berbentuk cair,
dibandingkan dengan basis salep atau krim. Akan tetapi, karakteristik ini menjadi
keterbatasan bagi senyawa yang bersifat hidrofobik. Oleh karena itu, untuk
mengatasi keterbatasan ini digunakan emulgel sehingga senyawa hidrofobik bisa
disiapkan dengan memanfaatkan kelebihan gel (Panwar, et al., 2011).
Emulgel adalah emulsi, baik tipe minyak dalam air atau air dalam minyak
dimana dilakukan penambahan gelling agent untuk membentuk sistem gel.
Emulgel memiliki acceptability yang tinggi bagi pasien karena memiliki
kelebihan baik yang berasal dari emulsi maupun gel (Mohamed, 2004). Sediaan
emulgel untuk penggunaan secara topikal memiliki karakteristik yang
menguntungkan seperti sifat tiksotropi, tidak berminyak, daya sebarnya baik,
bentuk sediaan emulgel bersifat lebih stabil dan merupakan suatu pembawa
dengan pelepasan yang lebih baik bagi obat yang bersifat hidrofobik (Panwar, et
al., 2011).
Suatu senyawa hidrofobik dapat dengan mudah dimasukkan ke dalam gel
menggunakan emulsi dengan tipe obat/minyak/air. Kebanyakan obat hidrofobik
tidak dapat dimasukkan secara langsung ke dalam basis gel karena kelarutannya
menjadi penghalang serta dapat timbul masalah pada pelepasan obatnya. Emulgel
membantu memasukkan obat hidrofobik ke dalam fase minyak dan kemudian
globul-globul minyak terdispersi di dalam fase air menghasilkan emulsi tipe M/A.
Emulsi ini dapat dicampurkan dengan basis gel sehingga memberikan stabilitas
dan pelepasan obat yang lebih baik (Panwar, et al., 2011).
D. Bahan Formulasi 1. Emulsifying agent
Emulsifying agent adalah suatu molekul yang memiliki rantai hidrokarbon nonpolar dan polar pada tiap ujung rantai molekulnya.
Emulsifying agent memiliki kemampuan menarik fase air dan fase minyak sekaligus, serta dapat menempatkan diri di antara kedua fase tersebut sehingga
dapat menurunkan tegangan permukaan antara fase air dengan fase minyak
(Lieberman, Rieger and Banker, 1996).
Tipe emulsi yang diinginkan M/A atau A/M tergantung pada nilai
keseimbangan hidrofil-lipofil (hydrophile-lipophile balance), yakni sifat
dengan nilai HLB tertentu dapat menentukan apakah emulsi yang dihasilkan
merupakan tipe M/A atau A/M sesuai dengan jumlah yang digunakan.
Umumnya emulsi M/A terbentuk jika HLB 9-12 dan terbentuk emulsi A/M
jika HLB 3-6 (Martin, Swarbrick, Cammarata, 1993).
a. Polioksietilen 20 sorbitan monolaurat (Tween 20)
Gambar 3. Tween 20 (Iro, 2013).
Tween 20 berbentuk cairan minyak berwarna kuning yang
memiliki nilai HLB 16,7. Tween 20 larut dalam etanol dan air serta tidak
larut dalam minyak mineral. Tween digunakan sebagai emulsifying agent,
solubilizing agent, dan wetting agent. Tween merupakan surfaktan
non-ionik hidrofilik yang digunakan secara luas sebagai emulsifying agent
dalam pembuatan emulsi minyak dalam air yang stabil. Secara tunggal
digunakan sebagai emulsifying agent emulsi M/A dengan konsentrasi
1-15% dan secara kombinasi dengan surfaktan hidrofilik pada emulsi M/A
dengan konsentrasi 1-10%. Tween bersifat tidak toksik dan tidak
mengiritasi (Rowe, Sheskey, and Quinn, 2009).
b. Sorbitan monolaurat (Span 20)
Span 20 berbentuk cairan kental berwarna kuning yang memiliki
nilai HLB 8,6. Tween digunakan sebagai emulsifying agent, solubilizing
agent, dan wetting agent. Span 20 merupakan surfaktan non-ionik lipofilik yang larut dalam minyak dan pelarut organik serta tidak larut dalam air.
Span biasa digunakan sebagai emulsifying agent pada bentuk sediaan krim,
emulsi, salep untuk penggunaan secara topikal. Saat digunakan secara
tunggal span akan membentuk emulsi air dalam minyak yang stabil,
namun sering digunakan secara kombinasi dengan tween untuk
menghasilkan emulsi tipe A/M atau M/A dengan konsistensi yang
bervariasi tergantung proporsi yang digunakan. Span digunakan secara
tunggal pada emulsi A/M dengan konsentrasi 1-15% dan secara kombinasi
dengan surfaktan hidrofilik pada emulsi tipe M/A dengan konsentrasi
1-10%. Span bersifat tidak mengiritasi dan tidak toksik (Rowe, et al., 2009).
2. Gelling Agent
Gelling agent merupakan bahan yang digunakan untuk membentuk
gel. Secara umum gelling agent memiliki bobot molekul yang tinggi dan
diperoleh dari alam maupun sintetik. Gelling agent dapat terdispersi dalam air
dan dapat mengembang, serta meningkatkan viskositas. Gelling agent yang
ideal harus tidak berinteraksi dengan komponen lain dari formulasi, harus
bebas dari kontaminasi mikroba, perubahan suhu dan pH selama pembuatan
dan penggunaan preservative tidak boleh mengubah reologinya, ekonomis,
digunakan di tempat aplikasi, serta memiliki bau yang menyenangkan
(Mahalingam, Li, and Jasti, 2008).
Carbomer atau carbopol berbentuk serbuk putih yang higroskopis dan
merupakan suatu molekul asam. Carbopol merupakan polimer sintetik dari
asam akrilat dengan bobot molekul tinggi. Rantai polimernya terhubung
silang-menyilang (crosslinked) dengan alil sukrosa atau alil pentaeritritol.
Carbopol terdiri dari 52% – 68% gugus asam karboksilat (COOH). Secara teoritis bobot molekul carbopol diperkirakan antara 7 x 105sampai 4 x 109.
Carbopol dapat digunakan sebagai material bioadhesiv, controlled-release agent, emulsifying agent, rheology modifier, stabilizing agent, suspending agent, dan pengikat tablet. Sebagai gelling agent, carbopol digunakan pada
konsentrasi 0,5-2,0% (Rowe, et al., 2009).
Gambar 5. Unit monomer asam akrilat dari polimer carbopol (Rowe, et al., 2009).
Carbopol tersedia pada range bobot molekul yang luas yakni bobot
molekul rata-rata 450.000 (carbopol 907) hingga 4.000.000 (carbopol 940).
Bobot molekul berpengaruh pada tegangan permukaan dan viskositas produk
akhir. Oleh karena itu, carbopol 940 sangat efisien jika digunakan sebagai
Curteis (1991) menyatakan bahwa terdapat dua mekanisme
pengentalan carbopol, yaitu metode ikatan hidrogen (hanya dapat terjadi
dalam sistem pelarut polar) dan metode netralisasi (dapat terjadi baik pada
sistem pelarut polar maupun nonpolar).
a. Metode ikatan hidrogen
Sistem ini membutuhkan solvent yang dapat mendonorkan gugus
hidroksil. Hasil ikatan hidrogen antara gugus karboksil dari carbopol dan
gugus hidroksil dari solvent akan menyebabkan molekul carbopol yang
berbentuk coil menjadi uncoil dan terjadi kekentalan (Curteis, 1991).
b. Netralisasi
Carbopol yang didispersikan ke dalam air akan membentuk
dispersi koloid asam dengan viskositas yang rendah (Rowe, et al., 2009).
Pada metode ini carbopol yang bersifat asam dinetralkan oleh basa untuk
menghasilkan garam yang larut dalam pelarut. Selanjutnya molekul
carbopol berubah menjadi bentuk uncoil dan terjadi kekentalan pada gel (Walters, 2007). Bahan-bahan yang dapat digunakan dalam penetralan
polimer carbopol adalah borax, kalium hidroksida, natrium bikarbonat,
natrium hidroksida dan amin organik polar seperti trietanolamin (Rowe, et
al., 2009).
3. Propilen glikol
Propilen glikol berbentuk cairan kental, jernih, tidak berwarna, tidak
berbau. Propilen glikol dapat berfungsi sebagai antimicrobial preservative,
disinfectant, humectant, plasticizer, solvent, stabilizing agent dan water-miscible cosolvent. Pada formulasi sediaan topikal propilen glikol digunakan
sebagai humektan dengan konsentrasi ≈15%. Propilen glikol larut dalam
aseton, kloroform, etanol, gliserin, dan air. Propilen glikol bersifat
higroskopis (Rowe, et al., 2009).
4. Trietanolamin
Trietanolamin (TEA) berbentuk cairan kental, tidak berwarna sampai
kuning pucat dan berbau amoniak. TEA berperan sebagai alkalizing agent dan
emulsifying agent. TEA banyak digunakan dalam formulasi sediaan topikal terutama pembentukan emulsi. Konsentrasi yang digunakan dalam
emulsifikasi berkisar antara 2-4%. TEA bersifat sangat higroskopis dan larut
dalam air (Rowe, et al., 2009).
Trietanolamin yang bersifat basa dapat digunakan untuk netralisasi
carbopol. Penambahan trietanolamin pada carbopol akan menetralisasi gugus
asam karboksilat, membentuk garam yang larut. Sebelum netralisasi, carbopol
di dalam air akan ada dalam bentuk tak terion pada pH sekitar 3. Pada pH ini,
polimer sangat fleksibel dan strukturnya random coil. Penambahan
trietanolamin akan menggeser kesetimbangan ionik membentuk garam yang
larut. Hasilnya adalah ion yang saling tolak menolak dari gugus karboksilat
Viskositas dan kejernihan gel yang dapat diterima yaitu pada pH 4,5-5,0 dan
mencapai titik optimum pada pH 7 (Osborne and Amann, 1990).
Overnetralisasi dapat menyebabkan penurunan viskositas karena kation basa
yang berlebih akan melingkupi gugus karboksilat sehingga mengurangi
tolakan elektrostatik (Walters, 2007).
Gambar 7. Trietanolamin (Rowe, et al., 2009).
5. Parafin cair
Liquid paraffin atau mineral oil berbentuk cairan minyak kental, transparan, tidak berwarna, tidak berasa dan tidak berbau ketika dingin namun
memiliki bau samar minyak ketika dipanaskan. Parafin cair merupakan
campuran alifatik jenuh (C14-C18) dan hidrokarbon siklik dari hasil destilasi
minyak bumi. Parafin cair digunakan sebagai emolien, lubrikan, pelarut.
Parafin cair untuk emulsi topikal digunakan pada konsentrasi 1,0-32,0%.
Kelarutanmya yaitu praktis tidak larut dalam etanol 95%, gliserin, dan air,
larut dalam aseton, kloroform, eter, petroleum eter dan minyak atsiri (Rowe, et
6. Preservative
a. Metil paraben
Gambar 8. Metil paraben (Rowe, et al., 2009).
Metil paraben atau nipagin berfungsi sebagai antimicrobial
preservative yang secara luas digunakan pada sediaan farmasi, kosmetik dan makanan. Metil paraben berbentuk serbuk kristal putih, tidak berbau,
dan memiki rasa yang membakar. Paraben efektif pada rentang pH yang
luas (antara 4-8) dan memiliki spektrum aktivitas antimikroba yang luas
meskipun paraben paling efektif menghambat yeast dan fungi. Paraben
juga lebih aktif tehadap bakteri Gram positif dibandingkan bakteri Gram
negatif (Rowe, et al., 2009).
Metil paraben dapat digunakan secara tunggal maupun kombinasi
dengan paraben lain atau dengan agen antimikroba lain. Aktivitas
antimikroba paraben meningkat seiring dengan peningkatan rantai gugus
alkil, tetapi kelarutannya dalam air menjadi menurun. Oleh karena itu,
penggunaan kombinasi paraben sering digunakan untuk menghasilkan efek
antimikroba yang lebih efektif. Metil paraben untuk sediaan topikal
digunakan pada konsentrasi 0,02–0,3 (Rowe, et al., 2009).
Kelarutan metil paraben pada suhu 25°C yaitu 1 bagian metil
bagian air. Paraben bersifat nonmutagenik, nonteratogenik, dan
nonkarsinogenik (Rowe, et al., 2009).
b. Propil paraben
Propil paraben atau nipasol berbentuk serbuk kristal putih, tidak
berbau dan tidak berasa, yang berfungsi sebagai antimicrobial
preservative. Propil paraben untuk sediaan topikal digunakan pada
konsentrasi 0,01–0,6. Propil paraben dapat digunakan secara tunggal
maupun kombinasi dengan paraben lain atau dengan agen antimikroba lain
untuk meningkatkan aktivitasnya. Propil paraben digunakan secara
kombinasi dengan paraben lain pada formulasi sediaan topikal. Kelarutan
propil paraben pada suhu 20°C yaitu 1 bagian larut dalam 1,1 bagian
etanol 95%; 3,9 bagian propilen glikol; 2500 bagian air; 3330 bagian
minyak mineral (Rowe, et al., 2009).
Gambar 9. Propil paraben (Rowe, et al., 2009).
7. Etanol
Etanol atau etil alkohol merupakan cairan mudah menguap, jernih,
tidak berwarna, berbau khas dan memiliki rasa yang membakar. Utamanya
etanol digunakan sebagai solvent, namun dapat juga digunakan sebagai
disinfektan. Selain itu, etanol dalam larutan dapat berfungsi sebagai pengawet
enhancer. Kelarutannya yaitu larut dalam kloroform, eter, gliserin dan air
(Rowe, et al., 2009).
Gambar 10. Etanol (Rowe, et al., 2009).
8. Aquadest
Aqua destillata atau air suling merupakan air murni yang diperoleh
dengan penyulingan. Air murni berbentuk cairan jernih, tidak berwarna dan
tidak berbau dengan pH antara 5,0-7,0. Air murni dibuat dari air yang
memenuhi persyaratan air minum. Air murni digunakan untuk pembuatan
sediaan kecuali sediaan parenteral (Dirjen POM RI, 1995).
E. Pencampuran
Pencampuran adalah suatu proses yang bertujuan untuk menangani dua
atau lebih komponen yang belum bercampur atau sebagian bercampur, sehingga
setiap unit (partikel, molekul, dan lain-lain) dari komponen terletak sedekat
mungkin berinteraksi dengan unit lain dari komponen. Kapanpun jika suatu
produk mengandung lebih dari satu komponen maka tahap pencampuran
dibutuhkan dalam proses pembuatannya. Hal ini untuk menjamin distribusi yang
merata dari zat aktif, tampilan yang merata serta sediaan melepaskan obat pada
Faktor-faktor yang mempengaruhi pencampuran pada sistem non-Newton
yaitu suhu, kecepatan geser, tegangan geser, tekanan, dan waktu pencampuran
(Nielloud and Marti-Mestres, 2000). Kecepatan putar dapat mempengaruhi sifat
fisik sediaan dimana kecepatan putar memberikan energi kinetik yang
menghasilkan gaya geser dalam proses formulasi. Polimer memiliki tipe alir
pseudoplastis dimana dalam keadaan diam (tidak terdapat gaya geser) polimer
berada dalam keadaan coil karena adanya stabilisasi intramolekuler. Air yang
amobil bersama konformasi globular ini akan membentuk struktur tiga dimensi
dalam sistem sehingga menghasilkan viskositas yang lebih tinggi. Ketika sistem
tersebut mendapatkan gaya geser, maka rantai polimer akan terurai dan dapat
menurunkan viskositas sediaan (Amiji and Sandmann, 2003).
Masalah yang sering terjadi pada pencampuran sediaan semisolid adalah
sediaan semisolid tidak mudah mengalir sehingga bahan yang berada pada dead
spot tidak dapat bercampur dengan baik. Maka diperlukan mixer yang sesuai yang
memiliki rotating element dengan jarak yang sempit dengan dinding wadah.
Mixer yang dapat digunakan dalam pencampuran sediaan semisolid antara lain
planetary mixer dan sigma blade mixer (Aulton, 2007). 1. Planetary mixer
Jenis mixer ini umumnya ditemukan di dapur rumah tangga dan dalam
skala yang lebih besar digunakan di industri. Dayung pada mixer diletakkan di
tengah, pada rotating arm. Dayung akan berputar mengitari sekeliling
Gambar 11. Planetary mixer (Aulton, 2007). 2. Sigma blade mixer
Mesin ini digunakan untuk pencampuran bahan dengan viskositas
tinggi misalnya pasta yang kaku atau salep. Mekanisme pencampuran yang
terjadi didasarkan pada dua buah bladeberbentuk ‘Z’ yang akan berputar dan
bertemu satu sama lain sehingga bentuknya mirip seperti simbol Ʃ (Aulton,
2007). Berputarnya kedua blade memungkinkan produk dapat dipindahkan
dari satu blade ke blade yang lain. Jarak yang berdekatan antara blade dan
dinding menghasilkan campuran homogen sempurna (JEC, 2014).
F. Uji Sifat Fisik Emulgel 1. Viskositas
Pada pembuatan kosmetik, reologi berpengaruh pada penerimaan
pasien, stabilitas fisika dan ketersediaan hayati, salah satunya adalah
viskositas. Viskositas merupakan pernyataan tahanan untuk mengalir dari
suatu sistem di bawah stress yang digunakan. Makin kental suatu cairan,
makin besar kekuatan yang diperlukan supaya cairan tersebut dapat mengalir
dengan laju tertentu (Martin, et al., 1993). Peningkatan viskositas akan
meningkatkan waktu retensi pada tempat aplikasi, tetapi menurunkan daya
sebar (Garg, Aggarwal, Garg, and Singla, 2002).
Penggolongan bahan menurut tipe aliran dan deformasinya yaitu
sistem Newton dan sistem non-Newton (Martin, et al., 1993). Contoh bahan
dengan sistem Newton yaitu air, alkohol, gliserin dan larutan sejati.
Sedangkan untuk sediaan seperti emulsi, suspensi, dispersi, dan larutan
polimer umumnya termasuk tipe non-Newtonian (Lieberman, et al., 1996).
Viskositas (η) digambarkan dengan persamaan matematika:
η = =
dari persamaan tersebut dapat diketahui bahwa peningkatan gaya geser (shear
stress) sebanding dengan viskositas dan berbanding terbalik dengan kecepatan
geser (shear rate). Jika viskositas meningkat maka shear stress harus
ditingkatkan agar shear rate tetap konstan. Namun hal ini hanya berlaku untuk
senyawa dengan tipe Newtonian. Pada tipe non-Newtonian, viskositas tidak
hubungan antara shear stress dan shear rate tidak linier (Amiji and
Sandmann, 2003). Sistem non-Newtonian dibagi ke dalam tiga kelas aliran
yakni plastis, pseudoplastis dan dilatan (Martin, et al., 1993).
Banyak produk farmasi yang menunjukkan aliran pseudoplastis, antara
lain dispersi cair dari gom alam dan sintetis (misalnya tragakan, natrium
alginat, metil selulosa dan natrium karboksimetil selulosa). Secara umum,
aliran pseudoplastis diperlihatkan oleh polimer-polimer dalam larutan, yang
merupakan kebalikan dari sistem plastis, yang tersusun dari partikel-partikel
yang terflokulasi dalam suspensi. Viskositas zat pseudoplastis berkurang
dengan meningkatnya kecepatan geser (shear rate). Rheogram yang
melengkung pada bahan-bahan pseudoplastis diakibatkan karena kerja (aksi)
shearing terhadap molekul-molekul bahan yang berantai panjang seperti
polimer-polimer linier. Dengan meningkatnya shear stress (gaya geser),
molekul-molekul yang secara normal tidak beraturan mulai menyusun sumbu
yang panjang dalam arah aliran. Hal ini mengurangi tahanan internal dari
bahan tersebut dan mengakibatkan shear rate yang lebih besar pada setiap
shear stress berikutnya. Selain itu, sebagian dari pelarut yang berikatan dengan molekul kemungkinan dilepaskan, sehingga menyebabkan penurunan
efektif baik konsentrasi maupun ukuran molekul yang terdispersi. Hal ini juga
2. Daya sebar
Daya sebar adalah kemampuan dari suatu sediaan untuk menyebar di
tempat aplikasi. Hal ini berhubungan dengan sudut kontak dari sediaan dengan
tempat aplikasinya. Daya sebar merupakan salah satu karakteristik yang
bertanggung jawab dalam keefektifan dalam pelepasan zat aktif dan
penerimaan konsumen dalam menggunakan sediaan semisolid. Faktor-faktor
yang mempengaruhi daya sebar yaitu viskositas sediaan, lama tekanan,
temperatur tempat aksi (Garg, et al., 2002).
Metode plat sejajar adalah metode yang paling banyak digunakan
untuk menentukan dan mengukur daya sebar sediaan semi padat. Keuntungan
dari metode ini adalah sederhana dan relatif murah. Selain itu, peralatan dapat
didesain dan dibuat sesuai dengan kebutuhan tiap individu berdasarkan tipe
data yang dibutuhkan, rute administrasi, luas permukaan yang ditutupi, dan
pertimbangan model membran. Di sisi lain, metode ini kurang akurat dan
sensitif, serta data yang dihasilkan harus diinterpretasikan dan disajikan secara
manual (Garg, et al., 2002).
G. Uji Iritasi HET-CAM
Hen's Egg Test-Chorioallantoic Membrane (HET-CAM) merupakan salah satu metode uji iritasi menggunakan hewan uji yaitu telur ayam. Sebelum
dilakukan uji, telur ditempatkan dalam inkubator dan disimpan pada suhu 38,3°C
9-10 hari (Interagency Coordinating Committee on the Validation of Alternative Methods, 2006).
Metode HET-CAM menggunakan membran chorioallantoic (CAM),
merupakan membran pernapasan vaskuler yang mengelilingi embrio burung yang
sedang berkembang. CAM terdiri dari gabungan antara korion yang berbatasan
dengan allantois. Korion merupakan kantung terluar yang berisi embrio, amnion
dan kuning telur sedangkan allantois merupakan suatu organ respirasi bagi
embrio yang berisi pembuluh darah, berkembang dari usus kemudian keluar dari
usus embrio ayam pada inkubasi hari ke 4 atau 5. Seiring dengan meningkatnya
ukuran allantois antara inkubasi hari ke 4 hingga 10, allantois ini akan melingkupi
embrio dan bergabung dengan korion menjadi CAM. Penggabungan kedua
membran memungkinkan terjadinya pertukaran udara antara embrio dengan
lingkungan udara luar. Setelah terbentuknya CAM, maka terjadilah pertumbuhan
yang cepat pada luas permukaan CAM hingga inkubasi hari ke 9 (ICCVAM,
2006).
Gambar 13. Membran chorioallantoic pada telur ayam (Biology Learning Center The University of Arizona, 2007).
Pembuluh darah yang ada pada CAM adalah cabang dari arteri dan vena
dari allantois embrio yang berisi eritrosit dan leukosit yang terlibat dalam respon
disebabkan oleh zat uji pada pembuluh darah dan protein pada jaringan lunak
membran ini (ICCVAM, 2006).
Efek iritasi yang terjadi pada uji HET-CAM diamati selama 300 detik pada
bagian CAM setelah pemberian senyawa uji. Efek iritasi yang diamati yaitu waktu
awal terjadinya hemoragi (perdarahan pada pembuluh darah), lisis (pecahnya
pembuluh darah) dan koagulasi (denaturasi protein vaskuler) (ICCVAM, 2006).
Menurut ICCVAM (2006), efek iritasi yang terjadi diberi skor sesuai
dengan waktu terjadinya hemoragi, lisis dan koagulasi dengan menggunakan
rumus:
tingkat iritasi kemudian ditentukan dari nilai rata-rata skor ketiga telur dan dapat
diklasifikasikan sebagai berikut:
Tabel I. Kategori iritasi berdasarkan skor iritasi pada HET-CAM Skor HET-CAM Kategori Iritasi
0-0,9 Tidak mengiritasi
1-4,9 Iritasi lemah
5-8,9 atau 5-9,9 Iritasi sedang
9-21 atau 10-21 Iritasi kuat
H. Uji Potensi Antibakteri
Metode pengukuran potensi antibakteri dapat dilakukan dengan beberapa
metode, antara lain:
1. Metode difusi
Metode ini mengukur aktivitas antimikroba berdasarkan pengamatan
mikroba dimana agen antimikroba akan berdifusi pada media Agar. Contoh
metode difusi antara lain metode disc diffusion (Kirby & Bauer) dan dan
cup-plate technique (metode sumuran). Pada metode disc diffusion, disc yang berisi agen antimikroba diletakkan pada media Agar yang telah ditanami
mikroorganisme dimana agen antimikroba akan berdifusi pada media Agar
tersebut. Pada metode sumuran, Agar yang telah ditanami mikroorganisme uji
dibuat lubang sumuran kemudian ke dalam sumuran diberi agen antimikroba
yang akan diuji (Pratiwi, 2008).
2. Metode dilusi
Prinsip metode ini adalah larutan uji diencerkan sehingga diperoleh
beberapa konsentrasi. Metode dilusi dibedakan menjadi dua yaitu dilusi cair
dan dilusi padat. Pada dilusi cair, cara yang dilakukan adalah dengan membuat
seri pengenceran agen antimikroba pada medium cair yang masing-masing
ditambahkan mikroba uji. Pada dilusi padat dilakukan serupa dengan dilusi
cair namun menggunakan media padat. Masing-masing seri pengenceran yang
dibuat dicampurkan ke dalam media agar dan ditanami bakteri uji setelah
media telah memadat. Keuntungan metode ini dibandingkan dengan metode
difusi adalah dapat menentukan nilai KHM (kadar hambat minimum) dan
Berdasarkan Suryawiria (cit., Zahro dan Agustini, 2013), aktivitas antibakteri berdasarkan diameter zona hambat diklasifikasikan sebagai berikut:
Tabel II. Klasifikasi aktivitas antibakteri berdasarkan diameter zona hambat Aktivitas antibakteri Diameter zona hambat
(mm)
Lemah < 5
Sedang 5-10
Kuat 10-20
Sangat kuat > 20
I. Metode Kromatografi Lapis Tipis (KLT) – Densitometri
Kromatografi merupakan suatu teknik pemisahan yang menggunakan fase
diam (stationary phase) dan fase gerak (mobile phase). Kromatografi lapis tipis
(KLT) merupakan bentuk kromatografi planar, selain kromatografi kertas dan
elektroforesis. Pada KLT fase diamnya berupa lapisan yang seragam pada
permukaan bidang datar yang didukung oleh plat kaca, plat alumunium, atau plat
plastik (Gandjar dan Rohman, 2007). Pada KLT, sampel ditotolkan (berbentuk
spot) atau semprotkan (berntuk garis) pada plat. Sampel akan berjalan melintasi
plat bersama dengan fase gerak, didorong oleh gaya kapilaritas. Pemisahan
komponen terjadi melalui mekanisme adsorpsi, partisi, eksklusi atau pertukaran
ion atau kombinasi dari mekanisme tersebut (Patnaik, 2004).
Pelaksanaan KLT lebih mudah dan lebih murah dibandingkan dengan
kromatografi kolom. Peralatan yang digunakan pun sederhana sehingga dapat
dikatakan bahwa hampir semua laboratorium dapat melaksanakan setiap saat
KLT dapat digunakan untuk analisis kualitatif dan kuantitatif. Analisis
kualitatif dilakukan dengan cara membandingkan nilai Rf solut dengan Rf baku
sedangkan analisis kuantitatif dari suatu senyawa yang telah dipisahkan dengan
KLT biasanya dilakukan scanning dengan densitometer langsung pada permukaan
lempeng KLT. Prinsip densitometer yaitu pengukuran intensitas radiasi yang
direfleksikan dari permukaan lempeng ketika disinari dengan lampu UV atau sinar
tampak. Solut-solut yang mampu menyerap sinar akan dicatat sebagai puncak
(peak) dalam pencatat (recorder) (Gandjar dan Rohman, 2007).
J. Landasan Teori
Kulit buah manggis memiliki kandungan alfa mangostin, suatu derivat
xanthone yang memiliki aktivitas antibakteri. Ekstrak kulit buah manggis dapat diformulasikan menjadi obat jerawat karena alfa mangostin diketahui dapat
menghambat pertumbuhan Staphylococcus epidermidis, suatu bakteri penginduksi
terjadinya jerawat.
Emulgel merupakan sediaan topikal gabungan dari dua sistem, yaitu
sistem emulsi di dalam sistem gel. Alfa mangostin merupakan senyawa yang
bersifat hidrofobik sehingga bentuk sediaan emulgel cocok digunakan sebagai
pembawa karena emulgel bersifat lebih stabil dan merupakan suatu pembawa
dengan pelepasan yang lebih baik bagi obat yang bersifat hidrofobik.
Sifat fisik dan stabilitas fisik suatu sediaan sangat penting karena
berpengaruh terhadap acceptability pasien dan efektifitas terapetik suatu sediaan.
antara lain kecepatan putar. Kecepatan putar akan memberikan energi kinetik
yang akan menimbulkan gaya geser yang akan mempengaruhi viskositas sediaan
emulgel sehingga dapat mempengaruhi sifat fisik serta stabilitas fisiknya.
K. Hipotesis
Variasi kecepatan putar mixer memberikan pengaruh yang signifikan
terhadap sifat fisik dan stabilitas fisik emulgel anti acne ekstrak kulit buah
manggis (Garcinia mangostana L.) yang meliputi viskositas, daya sebar dan
35 BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan jenis penelitian eksperimental murni yang
bersifat eksploratif untuk mencari pengaruh kecepatan putar pada proses
pencampuran terhadap sifat fisik dan stabilitas fisik emulgel anti acne ekstrak
kulit buah manggis dengan rancangan penelitian acak lengkap pola searah.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas. Variabel bebas dalam penelitian ini adalah kecepatan putar
mixer.
b. Variabel tergantung.
1). Uji sifat fisik: viskositas, daya sebar.
2). Uji stabilitas fisik: pergeseran viskositas setelah penyimpanan selama
satu bulan.
3). Uji aktivitas antibakteri: diameter zona hambat.
c. Variabel pengacau terkendali.
1). Uji sifat fisik dan stabilitas fisik: jenis dan ukuran mixer, suhu
pencampuran, lama pencampuran, kondisi wadah dan penyimpanan,
2). Uji aktivitas antibakteri: kepadatan suspensi bakteri Staphylococcus epidermidis (setara dengan larutan standar Mac Farland 1), diameter lubang sumuran, dan lama inkubasi.
d. Variabel pengacau tak terkendali.
1). Uji sifat fisik dan stabilitas fisik: suhu ruangan saat proses pembuatan,
penyimpanan serta pengujian emulgel.
2). Uji aktivitas antibakteri: suhu inkubasi, suhu ruangan saat pengujian.
2. Definisi operasional
a. Ekstrak kulit buah manggis adalah ekstrak serbuk halus kering yang
berasal dari kulit buah tanaman manggis (GarciniamangostanaL.)dengan
kandungan alfa mangostin minimal 25% yang diperoleh dari PT
Borobudur, Semarang.
b. Emulgel anti acne ekstrak kulit buah manggis adalah sediaan topikal semisolid hasil emulsifikasi yang merupakan dispersi fase minyak dalam
air (M/A) yang dibuat dari bahan aktif ekstrak kulit buah manggis yang
digunakan untuk mengobati jerawat dengan formula yang tercantum dalam
penelitian ini.
c. Kecepatan putar adalah banyaknya putaran mixer per menit dalam proses
emulsifikasi, penambahan gelling agent (carbopol 940), dan netralisasi
carbopol 940 (penambahan trietanolamin).
d. Sifat fisik emulgel adalah parameter untuk mengetahui kualitas fisik
e. Stabilitas fisik emulgel adalah parameter yang digunakan untuk mengetahui ada tidaknya perubahan emulgel dalam penyimpanan yaitu
perubahan viskositas selama satu bulan penyimpanan.
f. Viskositas adalah suatu pertahanan dari emulgel untuk mengalir setelah adanya pemberian gaya. Semakin besar viskositas, maka emulgel akan
makin tidak mudah untuk mengalir. Kriteria viskositas optimum adalah
200-300 dPas.
g. Daya sebar adalah diameter penyebaran tiap 1 gram emulgel pada alat uji daya sebar yang diberi beban kaca dan pemberat hingga 125 gram dan
didiamkan selama 1 menit. Kriteria daya sebar optimum adalah 3-4 cm.
h. Pergeseran viskositas adalah presentase dari selisih viskositas emulgel setelah 1 bulan penyimpanan dengan viskositas emulgel setelah 48 jam
pembuatan. Kriteria pergeseran viskositas optimum adalah < 10%.
i. Iritasi adalah terjadinya hemoragi, lisis dan koagulasi pada bagian
Chorioallantoic Membrane (CAM) telur ayam yang mungkin timbul setelah pengaplikasian sediaan. Hemoragi merupakan perdarahan
pembuluh darah, lisis merupakan pecahnya pembuluh darah sedangkan
koagulasi merupakan denaturasi protein pada CAM.
j. Daya antibakteri emulgel ekstrak kulit buah manggis adalah kemampuan dari emulgel ekstrak kulit buah manggis dalam menghambat
atau membunuh bakteri Staphylococcus epidermidis penyebab jerawat,
k. Zona hambat adalah zona jernih di mana tidak dijumpai pertumbuhan
bakteri Staphylococcus epidermidis atau terdapat pertumbuhan sedikit
sekali dibandingkan dengan kontrol pertumbuhan.
l. Staphylococcus epidermidis adalah salah satu bakteri penyebab jerawat
yang berasal dari kultur murni Staphylococcus epidermidis ATCC 12228
yang diperoleh dari Balai Laboratorium Kesehatan Yogyakarta.
C. Alat dan Bahan Penelitian 1. Alat penelitian
Alat yang digunakan pada penelitian ini adalah alat-alat gelas (pipet
ukur, cawan petri, tabung reaksi, batang pengaduk, labu ukur, gelas ukur,
beaker glass, erlenmeyer) merk Pyrex-Japan, neraca digital, waterbath, mixer
merk Phillips modifikasi (Elecsa, USD), viscotester seri VT 04
(RION-JAPAN), alat pengukur daya sebar, stopwatch, vortex, hot plate, stirer, jarum
ose, pelubang sumuran nomor 2, autoklaf, mistar, pipet mikro 100-1000 μL,
autosampler (Camag Linomat 5 No. 170610) dan densitometer (Camag TLC scanner 3 CAT. No. 027.6485 SER. No. 160602).
2. Bahan penelitian
Bahan yang digunakan adalah ekstrak kulit buah manggis (Garcinia
Muller-Hinton Broth (Merck), Muller-Hinton Agar (Oxoid), media Nutrient
Agar (Oxoid), Cindala®, bakteri uji Staphylococcus epidermidis yang
diperoleh dari Balai Laboratorium Kesehatan Yogyakarta, HCl 1 M, NaCl 5%,
plat silica gel 60 F254, metanol p.a, kloroform p.a, etil asetat p.a, kertas saring, telur ayam, NaCl 0,9%, NaOH 0,1 N.
D. Tata Cara Penelitian 1. Identifikasi bahan
a. Ekstrak kulit buah manggis (GarciniamangostanaL.)yang diperoleh dari
PT Borobudur, Semarang dan telah diuji identitasnya, dibuktikan dengan
Certificate of Analysis.
b. Kultur murni bakteri uji Staphylococcus epidermidis yang diperoleh dari
Balai Kesehatan Yogyakarta dan telah diuji kemurniannya.
2. Pembuatan emulgel anti acne ekstrak kulit buah manggis dengan variasi kecepatan putar
Formula yang digunakan untuk pembuatan emulgel anti acne ekstrak
kulit buah manggis mengacu pada formula emulgel hasil penelitian Mohamed
Tabel III. Formula emulgel chlorphenesin
Bahan emulgel Satuan (g)
Chlorphenesin 0,5
Dilakukan modifikasi dengan mengganti zat aktif dan beberapa
eksipiennya. Formula hasil modifikasi adalah sebagai berikut:
Tabel IV. Formula emulgel ekstrak kulit buah manggis (100 g emulgel) Bahan emulgel Satuan (g)
Ekstrak kulit buah manggis 3
Carbopol 940 1
Cara pembuatan emulgel ekstrak kulit buah manggis:
Carbopol 940 dikembangkan dengan menggunakan sebagian aquadest dari formula (60 ml) selama 24 jam. Semua bahan yang termasuk dalam fase
minyak (parafin cair dan span 20) dicampur terlebih dahulu di atas waterbath