PENGARUH BEBERAPA KONSENTRASI SPERMIDIN TERHADAP
PERTUMBUHAN DAN KETAHANAN BIBIT MIKRO KENTANG
(Solanum tuberosum
L.) ENKAPSULASI
(The Effects of Spermidine Concentration to Maintain Microshoot Vigor on Potato
Seed Encapsulation)
Warnita, Tamsil Bustamam, dan Rida Putih
Program Studi Agroekoteknologi, Fakultas Pertanian, Universitas Andalas, Padang Kampus Unand Limau Manis, Padang 25163
ABSTRACT
An experiment was carried out at the plant Tissue Culture Lab. of Departement of Agronomy, Faculty of Agriculture, Andalas University Padang from August 2005 to January 2005. The objetive of the experiment is to obtain the best spermidine concentration to maintain microshoot vigor on seed encapsulation. The treatments were concentration of spermidine : 0.0 , 2.0 , 4.0 dan 6.0 mg/l. The experimental units aranged in Completely Randomized Design with 10 replications. Observation included explants with plantlet height , number of shoot, number of leaf, number of root, root height, percentage of live, and condition of capsul. Result indicated that 4.0 mg/l spermidin was the best to maintain the size of potato microshoot and support potato microshoot vigor.
Keyword : spermidine, microshoot, encapsulation, potato, alginate
PENDAHULUAN
ecara umum produksi kentang di Indonesia masih relatif rendah, yaitu 15.3 ton per hektar. Pada tahun yang sama produksi kentang Sumatera Barat adalah 12.7 ton per hektar (BPS, 2003). Sementara produktivitas kentang negara subtropis seperti USA dan Belanda sudah mencapai 37.4 ton/ha dan 45.1 ton/ha (Rubatsky dan Yamaguchi, 1995).
Masalah yang harus mendapat perhatian utama adalah penyediaan bibit kentang bermutu. Penyediaan benih bermutu dapat dilakukan dengan teknik kultur jaringan. Untuk mendapatkan bibit tanaman yang seragam dalam jumlah yang banyak dan bebas penyakit sistemik dapat dilakukan dengan metode kultur jaringan (Hwang, 1984).
Sukrosa sebagai sumber karbohidrat perlu ditambahkan ke dalam media untuk pertumbuhan bibit secara kultur jaringan. Penggunaan sukrosa di dalam pembibitan in
vitro ini adalah untuk menciptakan ketahanan
dari bibit mikro kentang itu sendiri. Konsentrasi sukrosa yang optimum untuk pertumbuhan in
vitro berkisar antara 2 – 5 % (Smith, 2000).
Selama ini bibit hasil kultur jaringan kentang mengalami kesulitan dalam hal pengemasan khususnya untuk distribusi jarak jauh. Penanganan masalah tersebut dapat dilakukan melalui teknik enkapsulasi.
Bibit mikro kentang (BMK) yang disiapkan untuk enkapsulasi merupakan plantlet kentang yang berasal dari tunas aksilar yang tumbuh pada ketiak dan stek buku tunggal kentang hasil tanaman in vitro. Selanjutnya bibit mikro kentang ditumbuhkan pada media MS yang ditambah 0,015 mg/l paclobutazol (Siahan, 1996).
Sudarmonowati dan Bachtiar (1994) menggunakan teknik enkapsulasi untuk perbanyakan secara in vitro. Tunas pucuk akasia (Accasia anangium) dienkapsulasi dengan 2 % natrium alginat yang mengandung media MS cair dan ditumbuhkan pada media MS yang mengandung 2 mg/l IBA dan 1 mg/l BAP dalam waktu 2 minggu tunas dalam kapsul tumbuh 80 %. Hasil penelitian Suliansyah dan Warnita (2001) menunjukkan konsentrasi alginat terbaik untuk enkapsulasi kentang adalah 2,5 %.
Enkapsulasi tunas pucuk atau tunas aksilar kerapkali memiliki kendala terhambatnya
S
sistem perakaran tanaman karena tidak memiliki primordial akar seperti halnya embrio somatik. Untuk mengatasi hal tersebut maka pada matrik kapsul perlu ditambahkan hormon untuk menginisiasi perakaranya (Picconi dan Standardi, 1995).
Enkapsulasi BMK kultivar RBB dengan 2,5 % Na alginat dalam media MS cair yang mengandung 0,015 mg/l paclobutrazol yang sebelumnya ditumbuhkan pada media MS padat mengandung 12 mg/l Ca-Pantotenat, 30 g/l sukrosa, menunjukkan daya tahan kapsul selama 8 – 10 hari dan persentase pertumbuhan kapsul 100 % (Siahan, 1996)
Hasil penelitian Moharia (2003) menun-jukkan bahwa perendaman BMK dengan GA3
belum mempengaruhi umur muncul tunas pertama, tinggi bibit dan persentase hidup bibit. Warnita (2004) menyatakan bahwa penambah-an paclobutrazol dengpenambah-an konsentrasi 0.025 mg/l baik untuk pertumbuhan BMK yang ke-kar dan 2.0 % natrium alginat terbaik pertum-buhan bibit mikro enkapsulasi. Bibit mikro enkapsulasi yang dihasilkan kurang dapat bertahan lama, diduga karena kekurangan oksigen.
Natrium alginat yang digunakan sebagai bahan untuk enkapsulasi mengandung kadar oksigen yang rendah. Kadar oksigen yang rendah menyebabkan stress pada BME yang mengakibatkan terbentuknya etilen. Etilen tersebut dapat menyebabkan penuaan pada BME dan mengurangi masa simpannya (Simajuntak, 1998).
Bibit mikro enkapsulasi yang dihasilkan kurang dapat bertahan lama, maka perlu usaha untuk meningkatkan ketahanannya. Masalah tersebut dapat diatasi dengan penambahan zat pengatur tumbuh seperti Poliamin. Poliamin dikenal 3 jenis, yaitu: putresin (di-amin), spermidin (tri-amin), dan spermin (tetra-amin) (Dundroff, 1990) Poliamin merupakan zat pengatur tumbuh yang berperan dalam pertumbuhan dan perkembangan tanaman (Galston dan Kaur – Sawhney, 1995).
Poliamin adalah zat pengatur tumbuh yang dapat meningkatkan perkembangan dan pertumbuhan jaringan tanaman, menurunkan stabilitas membran, menurunkan stres organ, mengatur kerja enzim dalam metabolisme tanaman, meningkatkan replikasi dan transakasi DNA, serta menunda penuaan
(senescence). Selain itu poliamin juga berguna
dalam pembelahan sel, embriogenesis kultur jaringan, meningkatkan pembentukan akar,
inisiasi bunga dan perkembangannya, serta untuk pembetukan buah dan pembentukan polen (Evan dan Mamberg, 1989 cit Simanjuntak, 1998).
Untuk itu telah dilakukan penelitian mengenai konsentrasi spermidin untuk menyokong pertumbuhan bibit mikro kentang. Penelitian ini bertujuan untuk mendapatkan konsentrasi spermidin yang sesuai pada enkapsulasi dalam menyokong pertumbuhan propagul mikro kentang.
BAHAN DAN METODA
Percobaan ini dilaksanakan di laboratorium Kultur Jaringan Tumbuhan Jurusan Budidaya Pertanian, Fakultas Pertanian Universitas Andalas Padang, mulai bulan Agustus 2004 sampai dengan Januari 2005. Varietas kentang yang digunakan adalah Atlantik. Percobaan ini disusun menurut Rancangan Acak Lengkap. Perlakuannya adalah spermidin yang terdiri dari empat taraf yaitu : 0.0, 2.0, 4.0 dan 6.0 mg/l. Data hasil pengamatan dianalisis dengan sidik ragam bila berbeda nyata dilanjutkan dengan uji BNJ pada taraf nyata 5 %.
Bibit mikro kentang diperoleh dengan cara menanam setek buku tunggal plantlet kentang secara in vitro. Setek buku tunggal kentang ditanam pada media MS yang ditambah paclobutrazol 0.025 mg/l selama 6 minggu.
Sebelum dilakukan enkapsulasi BMK direndam dengan spermidin sesuai perlakuan. Enkapsulasi dilakukan dengan meneteskan sebanyak 2 tetes natrium alginat pada satu setek mikrro hasil panenan dalam tabung reaksi yang berfungsi sebagai pencetak kapsul. Untuk mengeraskan alginat menjadi gel kapsul maka diberikan 2 g/150 ml CaCl2 2 H2O sebanyak 5
tetes, selanjutnya tabung reaksi digoyang perlahan sehingga terbentuk kapsul bibit mikro.
Biji sintetik yang diperoleh dari percobaan sebelumnya ditanam pada media arang sekam. Pengamatan dilakukan setiap tiga hari sekali untuk melihat kemampuan tumbuh dan ketahanan hidup bibit mikro, bersamaan dengan itu dilakukan pula penyiraan nutrisi (1/2 MS).
Peubah yang diamati antara lain : tinggi tanaman, jumlah tunas, jumlah daun, jumlah akar, panjang akar, persentse tumbuh, saat muncul tunas.
HASIL DAN PEMBAHASAN
Umumnya pertumbuhan enkapsulasi mikro kentang pada media yang ditambah spermidin cukup baik, dari hasil percobaandapat dilihat bahwa pertumbuhannya cukup bagus. Hal ini sesuai dengan peranan dari spermidin sebagai antioksidan yang dapat menyokong pertumbuhan bibit enkapsulasi.
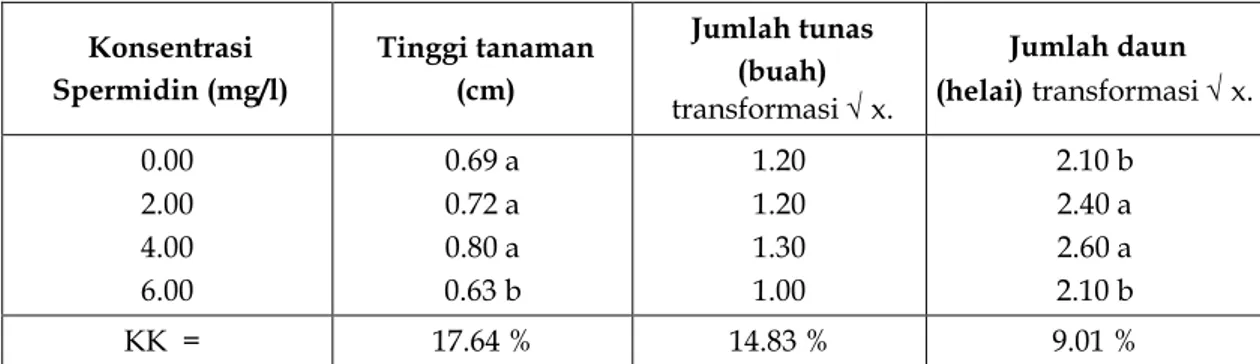
Tabel 1. Tinggi tanaman, jumlah tunas dan jumlah daun tanaman kentang pada beberapa konsentrasi spermidin
Konsentrasi Spermidin (mg/l) Tinggi tanaman (cm) Jumlah tunas (buah) transformasi x. Jumlah daun (helai) transformasi x. 0.00 2.00 4.00 6.00 0.69 a 0.72 a 0.80 a 0.63 b 1.20 1.20 1.30 1.00 2.10 b 2.40 a 2.60 a 2.10 b KK = 17.64 % 14.83 % 9.01 %
Angka-angka pada lajur yang sama yang diikuti oleh kecil yang sama adalah berbeda tidaak nyata menurut BNJ pada taraf nyata 5 %
Spermidin meningkatkan pertumbuhan tinggi tanaman dan jumlah daun. Sementara jumlah tunas belum dipengaruhi karena pertumbuhannya lambat. Spermidin mampu meningkatkan tinggi tanaman dan jumlah daun, dapat mengatur pertumbuhaan tanaman. Spermidin yang termasuk poliamin merupakan zat pengatur tumbuh yang berperan dalam pertumbuhan dan perkembangan tanaman (Galston dan Kaur – Sawhney, 1995). Dengan demikian spermidin akan merangsang pertumbuhan sehingga akan meningkatkan tinggi tanaman.
Jumlah dan ukuran daun dipengaruhi oleh genotipe dan lingkungan seperti suhu, cahaya
dan faktor-faktor lainnya, namun lebih dikendalikan oleh genetik (Gardner, 1991). Meristem apical batang merupakan tempat dimana daun, cabang, dan organ generatif terbentuk (Lakitan, 1995). Laju pembentukan daun relatif konstan jika tanaman ditumbuhkan pada suhu dan intensitas cahaya yang konstan.
Jumlah tunas pada semua pemberian spermidin menunjukkan hasil yang sama. Hal ini mungkin disebabkan oleh pertumbuhan tunas yang lambat. Meskipun spermidin berperan dalam pertumbuhan dan perkembangan tanaman, untuk pertumbuhan tunas pengaruh belum tampak.
Tabel 2. Saat muncul tunas, jumlah akar dan panjang akar tanaman kentang pada beberapa konsentrasi spermidin
Konsentrasi Spermidin (mg/l)
Saat inisiasi tunas (hari) Jumlah akar (buah) transformasi x.) Panjang akar (cm) 0.00 2.00 4.00 6.00 4.70 4.60 4.30 4.30 3.90 3.90 4.20 3.90 1.73 1.80 1.83 1.67 KK 14.27 % 9.59 % 9.30 %
Angka-angka pada lajur yang sama yang diikuti oleh kecil yang sama adalah berbeda tidaak nyata menurut BNJ pada taraf nyata 5 %
Data pada Tabel 2 menunjukkan bahwa saat inisiasi tunas pada setiap taraf spermidin adalah hampir sama. Pertumbuhan akar baik
panjang maupun jumlahnya belum dipengaruhi oleh penambahan spermidin sehingga pertumbuhan akar pada media yang
ditambah spermidin pertumbuhannya hampir sama. Meskipun poliamin juga berguna dalam pembelahan sel, embriogenesis kultur jaringan, meningkatkan pembentukan akar, inisiasi bunga dan perkembangannya, serta untuk pembetukan buah dan pembentukan polen (Evan dan Mamberg, 1989 cit Simanjuntak, 1998). Pada percobaan ini peningkatan konsentrasi spermidin belum memberikan pengaruh untuk meningkatkan jumlah dan panjang akar.
Keseragaman pertumbuhan BME dapat kita lihat melalui persentase tumbuh dari BME itu sendiri. Persentase tumbuh BME dapat dilihat pada Tabel 3 di bawah ini., dimana persentase tumbuh berkisar antara 70 % - 100 %. Tabel 3. Persentase tumbuh tunas BME
kentang pada beberapa konsentrasi Spermidin Konsentrasi Spermidin (mg/l) Persentase tumbuh (%) 0.00 2.00 4.00 6.00 70 100 100 100
Data tidak diolah secara statistika tetapi hanya dibandingkan dari 10 bobol
Dari hasil percobaan dapat dilihat bahwa pertumbuhan BME cukup seragam dengan yang berkisar antara 70 % - 100 %. Variasi persentase hidup terjadi karena penambahan spermidin. Pada tanpa pemberian spermidin persentase hidup lebih rendah daripada yang lainnya. Penyalutan BME dengan natrium alginat menyebabkan kadar oksigen yang rendah. Kadar oksigen yang rendah menyebabkan stress pada BME yang mengakibatkan terbentuknya etilen. Etilen tersebut dapat menyebabkan penuaan pada BME dan mengurangi masa simpannya (Simajuntak, 1998).
Penambahan spermidin dapat menyokong pertumbuhan bibit dalam kapsul sehingga lebih bertahan hidup. Sesuai dengan fungsi poliamin (spermidin) dapat meningkatkan ketahanan hidup BME kentang. Sesuai dengan pendapat Simanjuntak (1998) spermidin dapat meningkatkan daya tahan BMK.
KESIMPULAN DAN SARAN
Dari percobaaan yang telah dilaksanakan dapat ditarik kesimpulan sebagai berikut: 1. Penambahan spermidin dapat menyokongpertumbuhan Bibit Mikro Enkapsulasi kentang
2. Pemberian spermidin dengan konsentrasi 4.0 mg/l terbaik dalam meningkatkan tinggi tanaman dan jumlah daun.
UCAPAN TERIMA KASIH
Rasa terima kasih disampaikan kepada Pimpinan Proyek SP4 Jurusan Budidaya Pertanian Fakultas Pertanian Universitas Andalas Padang atas bantuan dana yang telah diberikan demi terlaksananya penelitian ini. Ucapan yang sama juga disampaikan kepada semua pihak yang telah membantu pelaksanaan penelitian ini terutama di Fakultas Pertanian Universitas Andalas Padang.
DAFTAR PUSTAKA
Biro Pusat Statistika. 2000. Survei Pertanian. Produksi Tanaman Sayuran di Indonesia. http//www.bps.go.id. Dumbroff, E.B., 1990, Polyamines-Functions
and Relationships with Ethylene and Cytokinins, P.256-266. In Flores, H.E., R.N. Arteca, and J.C. Shannon (Eds.) Polyamines and Ethylene: Biochemistry, Physiology, andInteractions, Amer. Soc. Plant-Physiol, Rockvile.
Galston, A.W. and R. Kaur-Sawhney, 1987, Polyamines and Senescence in Plants. pp. 167 - 181. In Thompson, W., E.A. Nothnagel and R.C. Huffaker (eds). Plant Senescense: Its Biochemistry and Physiology, American Society of Plant Physiologist, Rockville.
Gardner, F.P. 1991. Fisiologi tanaman budidaya. Penerbit Universitas Indonesia (UI. Press). Jakarta . 428 hal. Lakitan, B. 1996. Fisiologi pertumbuhan dan
perkembangan tanaman. PT. Raja Grafindo. Jakarta . 218 hal.
Moharia, E. 2003. Kemampuan tumbuh dan ketahanan hidup bibit mikro enkapsulasi kentang (Solanum tuberosum
L) dengan perendaman pada berbagai konsentrasi GA3 dan IBA. Skripsi
Fakultas Pertanian Unand Padang. Piccioni, E. and Standardi. 1995, Encapsulation
of micropropagated buds of six woody species. Plant cell tissue and delivery system. Info musa 2 (2) : 4 – 5.
Siahan, F. 1996. Enkaapsulasi bibit kentang
(Solanum tuberosum L.) dengan natrium
alginat. Karya ilmiah. Jurusan BDP. IPB. Bogor.
Simanjuntak, D. R. 1998. Pengaruh perlakuan poliamin terhadap daya tahan bibit mikro enkapsulasi system alginasi sekam dari beberapa kultivar kentang
(Solanum tuberosum L.). Karya ilmiah
Jurusan Budidaya Pertanian Fakultas Pertanian Bogor . 49 hal.
Sudarmonowati, E. dan A.S Bachtiar. 1994. produksi biji buatan enkapsulasi tunas pucuk pucuk Accasia mmanngium. Hal 25 – 30. Dalam Proseding Seminar Nasional Hasil-hasil penelitian dan pengembangan Bioteknologi II. Cibinong. Bogor.
Suliansyah, I dan Warnita. 2001. Teknologi pembuatan biji sintetik melalui enkapsulasi bibit mikro kentang
(Solanum tuberosum L.)
Warnita. 2004. Pengaruh paclobutrazol terhadap produksi dan ketahanan bibit mikro kentang (Solanum tuberosum L.) siap enkapsulasi. Jurnal Stigma. XII (2) : 214 – 218.