INTISARI
Gula merupakan salah satu kebutuhan pokok bagi manusia, selama ini kebutuhan gula dipenuhi oleh industri gula (penggiling tebu) dan beberapa industri kecil seperti gula merah dan gula aren. Glukosa dapat dibuat dengan jalan fermentasi dan hidrolisa. Hidrolisa pati dilakukan untuk memecah pati menjadi glukosa yang memiliki nilai guna dan nilai ekonomis tinggi. Untuk memenuhi kebutuhan gula yang terus meningkat, dilakukan hidrolisis pati sebagai alternatif sumber glukosa. Tujuan dari percobaan hidrolisa pati yaitu mempelajari pengaruh suhu terhadap reaksi hidrolisa pati dan menghitung konstanta kecepatan reaksi dan menganalisa pengaruh suhu terhadap konstanta kecepatan reaksi.
Hidrolisa merupakan reaksi pengikatan gugus hidroksil (-OH) oleh suatu senyawa. Gugus OH dapat diperoleh dari senyawa air. Hidrolisis pati terjadi antara suatu reaktan pati dengan reaktan air. Reaksi ini adalah orde satu, karena reaktan air yang dibuat berlebih, sehingga perubahan reaktan dapat diabaikan. Reaksi hidrolisis pati dapat dilakukan menggunakan katalisator H+ yang dapat diambil dari asam. Variabel-variabel yang berpengaruh terhadap reaksi hidrolisa yaitu katalisator, suhu dan tekanan, pengadukan, perbandingan zat pereaksi.
Pati yang kami gunakan pada percobaan ini yaitu tepung tapioka dengan katalis H2SO4 0,5 N dengan variabel suhu 700C dan 800C. Langkah awal yang kami lakukan yaitu
menghitung densitas pati dan H2SO4, membuat glukosa standar, dan menghitung kebutuhan
gram pati. Kemudian melakukan standarisasi larutan gula standart. Setelah itu penentuan kadar pati awal dan hidrolisa pati.
Hasil percobaan kami, konversi hidrolisa pati pada suhu 700C lebih besar dibandingkan suhu 800C. Hal ini dapat terjadi karena pati mengalami penggumpalan dimana karakteristik pati tapioka yang akan mengental dan mengeras pada suhu diatas 680C. Karena reaksi berjalan lambat, maka konversi yang didapat kecil. Nilai konstanta kecepatan reaksi suhu 700C yaitu 0,062/menit dan pada suhu 800C yaitu 0,059/menit. Gula reduksi adalah semua gula yang memiliki kemampuan untuk mereduksi dikarenakan adanya gugus aldehid atau keton bebas. Karbohidrat jenis monosakarida dan sebagian besar disakarida termasuk pada jenis gula reduksi.
Saran untuk percobaan hidrolisa pati adalah suhu operasi dijaga konstan 700C dan 800C, gunakan motor pengaduk supaya pati dapat terdispersi dengan baik, dan titrasi dilakukan diatas kompor dalam keadaan mendidih.
BAB I PENDAHULUAN
1.1 Latar Belakang
Gula merupakan salah satu kebutuhan pokok bagi manusia, selama ini kebutuhan gula dipenuhi oleh industri dula (penggiling tebu). Industri kecil seperti gula merah dan gula aren. Gula dapat berupa glukosa, sukrosa, fraktosa, sakrosa dll. Glukosa dapat digunakan sebagai pemanis dalam makanan, minuman, es krim dll.
Glukosa dapat dibuat dengan jalan fermentasi dan hidrolisa. Pada reaksi hidrolisa biasanya dilakukan dengan menggunakan katalisator asam seperti HCl (asam klorida). Bahan yang digunakan untuk proses hidrolisis adalah pati. Hidrolisa pati dilakukan untuk memecah pati menjadi glukosa yang memiliki nilai guna dan nilai ekonomis tinggi. Untuk memenuhi kebutuhan gula yang terus meningkat, dilakukan hidrolisis pati sebagai alternatif sumber glukosa. Di Indonesia banyak dijumpai tanaman yang menghasilkan pati. Tanaman-tanaman itu seperti seperti padi, jagung, ketela pohon, umbi-umbian, aren dan sebagainya.
1.2 Tujuan Percobaan
1. Mempelajari pengaruh suhu terhadap reaksi hidrolisa pati.
2. Menghitung konstanta kecepatan reaksi dan menganalisa pengaruh suhu terhadap konstanta kecepatan reaksi.
1.3 Manfaat Percobaan
1. Mahasiswa dapat mengetahui pengaruh suhu terhadap reaksi hidrolisa pati.
2. Mahasiswa dapat menghitung konstanta kecepatan reaksi dan menganalisa pengaruh suhu terhadap konstanta kecepatan reaksi.
BAB II
TINJAUAN PUSTAKA
Hidrolisa merupakan reaksi pengikatan gugus hidroksil (-OH) oleh suatu senyawa. Gugus OH dapat diperoleh dari senyawa air. Hidrolisis dapat digolongkan menjadi hidrolisis murni, hidrolisis katalis asam, hidrolisis katalis basa, hidrolisis gabungan alkali dengan air dan hidrolisis dengan katalis enzim. Sedangkan berdaasarkan fase reaksi yang terjadi diklasifikasikan menjadi hidrolisis fase cair dan hidrolisis fase uap.
Hidrolisis pati terjadi antara suatu reaktan pati dengan reaktan air. Reaksi ini adalah orde satu, karena reaktan air yang dibuat berlebih, sehingga perubahan reaktan dapat diabaikan. Reaksi hidrolisis pati dapat dilakukan menggunakan katalisator H+ yang dapat diambil dari asam. Reaksi yang terjadi pada hidrolisis pati adalah sebagai berikut :
(C6H10O5)X + H2O x C6H12O6
Berdasarkan teori kecepatan reaksi :
-rA = k. C pati. C air ...(1)
karena volume air cukup besar, maka dapat dianggap konsentrasi air selama perubahan reaksi sama dengan k’, dengan besarnya k’ :
k’ = k . Cair ...(2)
sehingga persamaan 1 dapat ditulis sebagai berikut -rA = k’. C pati dari persamaan kecepatan
reaksi ini, reaksi hidroisis merupakan reaksi orde satu. Jika harga –rA = -dCA/dt maka
persamaan 2 menjadi :
...(3)
Apabila CA = CA0 (1-xA) dan diselesaikan dengan integral dan batas kondisi t1, CA0 dan t2 : C-A akan diperoleh persamaan :
∫
∫
( )
( ) ( ) ...(4) Dimana xA = konversi reaksi setelah satu detik.
Persamaan 4 dapat diselesaikan dengan menggunakan pendekatan regresi y = mx + c, dengan
Variabel- variabel yang berpengaruh terhadap reaksi hidrolsa : 1. Katalisator
Hampir sama semua reaksi hidrolisa membutuhkan katalisator untuk mempercepat jalannya reaksi. Katalisator yang dipakai dapat berupa enzim atau asam karena kinerjanya lebih cepat. Asam yang dipakai beraneka jenisnya mulai dari HCl (Agra dkk, 1973; Stout & Rydberg Jr, 1939), H2SO4 sampai HNO3. Yang
mempengaruhi kecapatan reaksi adalah konsentrasi ion H+, bukan jenis asamnya. Meskipun demikian, didalam industri umumnya diakai asam klorida (HCl).
Pemilihan ini didasarkan atas sifat garam yang terbentuk pada penetralan tidak menimbulkan gangguan apa-apa selain rasa asin jika konsentrasinya tinggi. Oleh karena itu, konsentrasi asam dalam air penghidrolisa ditekan sekecil mungkin. Umumnya dipergunakan larutan asam yang mempunya konsentrasi asam yang lebih tinggi daripada pembuatan sirup. Hidrolisa pada tekanan 1 atm memerlukan asam yang jauh lebih pekat.
2. Suhu dan Tekanan
Pengaruh suhu terhadap kecepatan reaksi mengikuti persamaan Arrhenius, dimana semakin tinggi suhu maka semakin cepat laju reaksinya. Untuk mencapai konversi tertentu, diperlukan waktu sekitar 3 jam untuk menghidrolisa pati ketela rambat pada suhu 1000C. Tetapi jika suhunya dinaikkan hingga 1350C, konversi yang sama dapat dicapai dalam waktu 40 menit (Agra dkk, 1973). Hidrolisis pati gandum dan jagung dengan katalisator H2SO4 memerlukan suhu 1600C. Karena panas reaksi
mendekati nol dan reaksi berjalan dalam fase cair maka suhu dan tekanan tidak banyak mempengaruhi keseimbangan.
3. Pencampuran (pengadukan)
Supaya zat pereaksi dapat saling bertumbukan dengan sebaik-baiknya perlu adanya pencampuran. Untuk proses Batch, hal ini dapat dicapai dengan bantuan pengaduk atau alat pengocok (Agra dkk, 1973). Apabila prosesnya berupa proses alir (kontinyu), maka pecampuran dilakukan dengan cara mengatur aliran didalam reaktor supaya terbentuk olakan.
4. Perbandingan zat pereaksi
Jika salah satu zat pereaksi dibuat berlebihan jumlahnya maka keseimbangan dapat bergeser kearah kanan dengan baik. Oleh karena itu, suspensi pati yang kadarnya rendah memberi hasil yang lebih baik dibandingkan dengan yang kadarnya tinggi. Bila kadar suspensi pati diturunkan dari 40% menjadi 20% atau 1% maka konversi akan bertambah dari 80% menjadi 87 atau 99 % (Groggis, 1958). Pada permukaan, kadar suspensi pati yang tinggi sehingga molekul-molekul zat pereaksi akan sulit bergerak. Untuk menghasilkan glukosa biasanya dipergunakan suspensi pati sekitar 20%.
PATI TERMODIFIKASI
Pati termodifikasi adalah pati yang gugus hidroksilnya telah diubah lewat suatu reaksi kimia atau dengan mengganggu struktur asalnya. Pati diberi perlakuan tertentu dengan tujuan menghasilkan sifat yang lebih baik untuk memperbaiki sifat sebelumnya atau untuk merubah beberapa sifat sebelumnya atau sifat lainnya. Perlakuan ini dapat mencakup penggunaan panas, asam, alkali, zat pengolsidasi atau bahan kimia lainnya yang akan menghasilkan gugus kimia baru atau perubahan bentuk, ukuran serta struktur molekul pati. Pati dapat dimodifikasi melalui cara hidrolisis, oksidasi, cross-linking atau cross bonding dan subtitusi (Koswara, 2006).
Pati Termodifikasi Asam
Pati termodifikasi asam dibuat dengan menghidrolisis pati dengan asam dibawah suhu gelatinisasi, pada suhu sekitar 52oC. Reaksi dasar meliputi pemotongan ikatan a-1,4-glukosidik
dari amilosa a-1,6-D-glukosidik dari amilopektin, sehingga ukuran molekul pati menjadi lebih rendah dan meningkatkan kecenderungan pasta untuk membentuk gel. Thin-boiling Starch adalah pati termodifikasi yang diperoleh dengan cara hidrolisis dengan mengasamkan suspensi pati sampai pH tertentu dan memanaskan pada suhu tertentu sampai diperoleh derajat konversi yang diinginkan. Kegunaan utama thin-boiling starch adalah dalam larutan pembuatan gypsum wallboard, gum candies dan sizing tekstil (Atichokudomchaia dkk., 2000).
Pati Termodifikasi Hidrolisis Enzim
Hal-hal yang mempengaruhi hidrolisa enzim antara lain konsentrasi asam, temperatur, dan waktu pemasakan (O.S Azeez, 2002). Hidrolisis disini adalah dengan memecah rantai pada pati baik amilosa maupun amilopektin. Enzim yang memecah yaitu α - amilase. terdapat pada tanaman, jaringan mamalia, jaringan mikroba. Dapat juga diisolasi dari Aspergillus oryzae dan Bacillus subtilis. Laju hidrolisis akan meningkat bila tingkat polimerisasi menurun, dan laju hidrolisis akan lebih cepat pada rantai lurus. Hidrolisis amilosa lebih cepat dibanding hidrolisis terhadap amilopektin (Niba L.L dkk, 2002).
Cara kerja enzim α - amilase terjadi melalui dua tahap, yaitu : pertama, degradasi amilosa menjadi maltosa dan amiltrotriosa yang terjadi secara acak. Degradasi ini terjadi sangat cepat dan diikuti dengan menurunnya viskositas yang cepat pula. Kedua, relatif sangat lambat yaitu pembentukan glukosa dan maltosa sebagai hasil akhir dan caranya tidak acak. Keduanya merupakan kerja enzim α - amilase pada molekul amilosa (Koswara, 2006).
Pati Termodifikasi Ikatan Silang (Cross-Linking)
Pati termodifikasi ini diperoleh dengan cara mereaksikan pati dengan reagen bi atau polifungsional seperti sodium trimetaphosphate, phosphorus oxychloride, epichlorohydrin sehingga dapat membentuk ikatan silang pada molekul pati. Reagen tersebut juga dapat digabung dengan asetat anhidrat dan asam dikarboksilat membentuk pati modifikasi ganda. Karakteristik dari pati cross-linking adalah suhu gelatinisasi pati menjadi meningkat, pati tahan pada pH rendah dan pengadukan (Miyazaki, 2006).
Metode cross-linking bertujuan menghasilkan pati yang tahan tekanan mekanis, tahan asam dan mencegah penurunan viskositas pati selama pemasakan sedangkan metode esterifikasi-asetat bertujuan menstabilkan viskositas pati, menjernihkan pasta pati, mengurangi retrogradasi dan menstabilkan pati pada suhu rendah (Atichokudomchaia dkk, 2000).
Oksidasi Pati
Pati dapat dioksidasi dengan aktivitas dari beberapa zat pengoksidasi dalam suasana asam, netral atau larutan alkali. Menurut FDA (Food and Drugs Administration) zat pengoksidasi diklasifikasikan sebagai pemutih dan oksidan untuk pemutih yang diizinkan adalah oksigen aktif dari peroksida atau khlorin dari natrium hipokhlorida, kalium permanganat, ammonium persulfat (Koswara, 2006).
Zulaidah, Agustien. PENINGKATAN NILAI GUNA PATI ALAMI MELALUI PROSES MODIFIKASI PATI. Jurusan Teknik Kimia FT Universitas Pandanaran.
BAB III
PELAKSANAAN PERCOBAAN
3.1 Bahan dan Alat yang digunakan
3.1.1 Bahan
Glukosa 2 gram
Tepung tapioka 124 gram
NaOH H2SO4 0,5 N Indikator MB Fehling A dan B Aquades 3.1.2Alat Gelas ukur Termometer Erlenmeyer
Statif dan klem
Buret
Labu leher tiga
Labu takar
3.2 Gambar Alat Utama
Gambar 1.
Rangkaian alat hidrolisa
Keterangan:
1. Magnetic stirer + heater 2. Waterbatch
3. Labu leher tiga 4. Termometer 5. Pendingin balik 6. Klem 7. Statif 1 4 5 6 3 2 7
3.3 Prosedur percobaan 1. Persiapan awal
a. Menghitung densitas pati
Kedalam gelas ukur, 5 ml aquades dimasukkan 1 gr pati, catat penambahan volume.
b. Menghitung densitas H2SO4
Timbang berat picnometer kosong (m1), masukkan H2SO4 kedalam picnometer yang telah diketahui volumenya (v), timbang beratnya (m2), hitung densitas H2SO4.
c. Membuat glukosa standar
Glukosa anhidrit sebanyak 2 gram dilarutkan dalam 1000 ml aquades. 2. Penentuan kadar pati awal
a. Standarisasi larutan fehling
5 ml fehling A + 5 ml fehling B + 15 ml glukosa standar, dipanaskan sampai mendidih. Setelah mendidih ditambahkan 3 tetes MB, kemudian larutan dititrasi dengan glukosa standard hingga warna berubah menjadi merah bata. Catat Volume titran (F) yang diperlukan, proses titrasi dilakukan dalam keadaan mendidih (diatas kompor).
b. Penentuan kadar pati awal
Sebanyak 31 gram pati, 5 ml katalis H2SO4 0,5 N dan 313 ml aquadest dimasukkan ke dalam labu leher tiga dan dipanaskan hingga 700C dan 800C, selama 1 jam. Setelah itu larutan didinginkan, diencerkan dengan aquades sampai 500 ml lalu diambil 20 ml dan dinetralkan dengan NaOH (PH = 7). Larutan diambil 5 ml diencerkan sampai 100 ml, diambil 5 ml. Kedalam Erlenmeyer dimasukkan 5 ml larutan + 5 ml Fehling A + 5 ml fehling B + 5 ml glukosa standard, kemudian dipanaskan sampai mendidih. Lalu ditambahkan 3 tetes indikator MB. Kemudian larutan dititrasi dengan glukosa standard sehingga berubah warna menjadi warna merah bata. Catat volum titran yang dibutuhkan (M). Yang perlu diperhatikan, proses titrasi dilakukan dalam keadaan mendidih diatas kompor.
c. Hidrolisa pati
Sebanyak 31 gram pati, 5 ml katalis H2SO4 0,5 N dan 313 ml aquadest dimasukkan dalam labu leher tiga. Dipanaskan. Pada saat suhu operasi tercapai (700C dan 800C) anggap sebagai t0 diambil sampel sebanyak 20 ml. Kemudian sampel dinetralkan dengan NaOH (PH=7). Larutan diambil 5 ml diencerkan sampai 100 ml, diambil 5 ml. Kedalam Erlenmeyer dimasukkan 5 ml larutan + 5 ml fehling A + 5 ml fehling B + 5 ml glukosa standard, kemudian dipanaskan sampai mendidih. Lalu ditambahkan 3 tetes indikator MB. Kemudian larutan dititrasi dengan glukosa standard sehingga berubah warna menjadi warna merah bata. Catat V titran yang dibutuhkan (M). Yang perlu diperhatikan, proses titrasi dilakukan dalam keadaan mendidih diatas kompor. Pengambilan
sampel dilakukan setiap selang waktu 5 menit sebanyak 5 kali yaitu 20 menit. (t0=menit ke- , t1=menit ke-5, t2=menit ke-10, t3=menit ke-15, t4=menit ke-20)
Rumus penentuan kadar pati awal =
( )
Dimana : Nglukosa = 0,002 gr/ml W = 10 gram
Perhitungan kebutuhan reagen
a) Menghitung kebutuhan HCl/H2SO4 Dimana : kadar HCl = 0,25 untuk 25% 0,37 untuk 37% grek HCl = 1 kadar H2SO4 = 0,98 untuk 98% grek H2SO4 = 2
b) Menghitung kebutuhan pati
Dimana : ( ) ( )
Prosedur titrasi
5 ml fehling A + 5 ml fehling B + 15 ml glukosa standar
(jika ada hasil hidrolisa, prosedur diatas ditambah 5 ml sampel hasil hidrolisa) ↓
Dipanaskan sampai mendidih ↓
100 detik dari mendidih ditambah 3 tetes indikator MB
↓
2 menit kemudian dititrasi dengan glukosa standar, catat volume titran (titrasi dijalankan maks 1 menit)
BAB IV
HASIL PERCOBAAN DAN PEMBAHASAN 4.1 Hasil Percobaan
Tabel 4.1.1 Variabel suhu 700C
t (menit) M Xp XA -ln(1-XA) 0 12,5 0,0037 0,4625 0.620827 5 11,6 0,0048 0,6 0.916291 10 11,8 0,0045 0,5625 0.826679 15 10,7 0,0058 0,725 1.290984 20 9,8 0,0069 0,8625 1.984131 y = 0,062x + 0,507 k = 0,062/menit
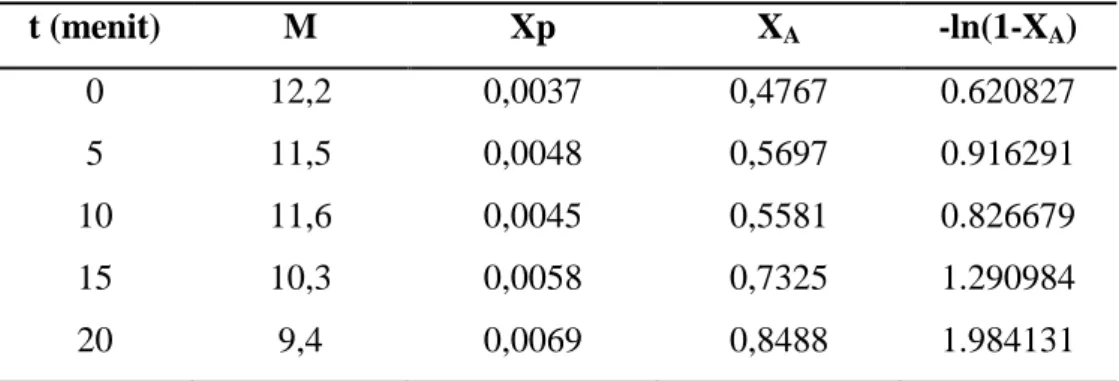
Tabel 4.1.2 Variabel suhu 800C
t (menit) M Xp XA -ln(1-XA) 0 12,2 0,0037 0,4767 0.620827 5 11,5 0,0048 0,5697 0.916291 10 11,6 0,0045 0,5581 0.826679 15 10,3 0,0058 0,7325 1.290984 20 9,4 0,0069 0,8488 1.984131 y = 0,059x + 0,856 k = 0,059/menit
0 0,2 0,4 0,6 0,8 1 1,2 0 10 20 30 40 50 60 70 Kon ve rs i (xp /xp 0) t (menit) temp hidrolisa pati 70C temp hidrolisa pati 80C BAB IV
HASIL PERCOBAAN DAN PEMBAHASAN 4.2 Pembahasan
4.2.1 Pengaruh suhu terhadap konversi hidrolisa pati
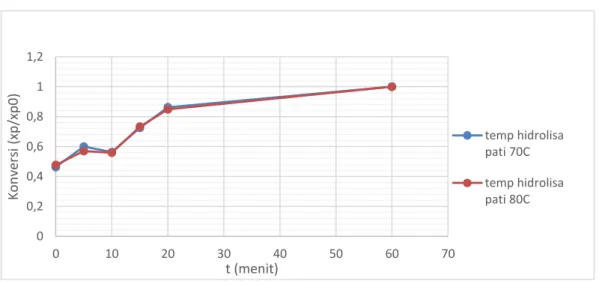
Grafik 4.2.1.1 Hubungan t (menit) vs konversi pada hidrolisa pati
Pada praktikum yang dilakukan, digunakan 1 variabel pembeda, yaitu suhu. Hidrolisa dilakukan pada suhu 700C dan 80⁰C untuk mengetahui perbedaan hasil konversi glukosa. Data yang didapat menunjukkan pada variabel waktu tetap, hidrolisa menggunakan suhu 80⁰C menghasilkan glukosa yang lebih banyak dibandingkan hidrolisa pada suhu 70⁰C. Hal ini sesuai persamaan Arrhenius :
k = Ae-Ea/RT di mana, k = Konstanta laju reaksi (mol jam-1) A = Faktor tumbukan
Ea = Energi aktivasi ( J mole -1) R = Konstanta gas (8.314 J K mole-1) T = Suhu (Kelvin)
dimana semakin tinggi suhu menyebabkan energi gerak partikel semakin besar sehingga laju reaksinya juga semakin besar. Semakin cepat laju reaksi berakibat pada konversi yang didapat semakin tinggi (pembentukan glukosa).
Berdasarkan grafik 4.2.1.1 perbandingan konversi hidrolisa pati pada suhu 70⁰C dengan 80⁰C bersifat fluktuatif. Pada menit ke- 0, 10, 15, hidrolisa pada suhu 80⁰C memiliki konversi yang lebih besar dibandingkan hidrolisa pada suhu 70⁰C. Sedangkan
pada menit ke- 5 dan 20 konversi terbesar didapat pada suhu operasi 70⁰C. Hal ini dapat terjadi karena pati mengalami penggumpalan dimana karakteristik pati tapioka yang akan mengental dan mengeras pada suhu diatas 680C (Nwokocha, 2009). Semakin tinggi suhu, pati akan lebih mengental sehingga pergerakan molekul-molekul zat pereaksi akan sulit bergerak yang menyebabkan hidrolisa tidak berjalan secara maksimal dan reaksi berjalan lambat. Karena reaksi berjalan lambat, maka konversi yang didapat kecil. Hal ini sesuai dengan fenomena praktikum yang terjadi dimana pada suhu 800C memiliki konversi yang lebih kecil dari 700C.
(Mastuti, Endang, Setyawardhani, Dwi Ardiana. 2010. Pengaruh Variasi Temperatur dan Konsentrasi Katalis pada Kinetika Reaksi Hidrolisis Tepung Kulit Ketela Pohon. Surakarta: Universitas Sebelas Maret)
(Adity. 2009. Skripsi Hidrolisa Pati Tapioka dengan Minyak Jahe Modifikasi Cross Linking. Teknik Kimia Fakultas Teknik Universitas Diponegoro)
4.2.2 Pengaruh suhu terhadap konstanta kecepatan reaksi
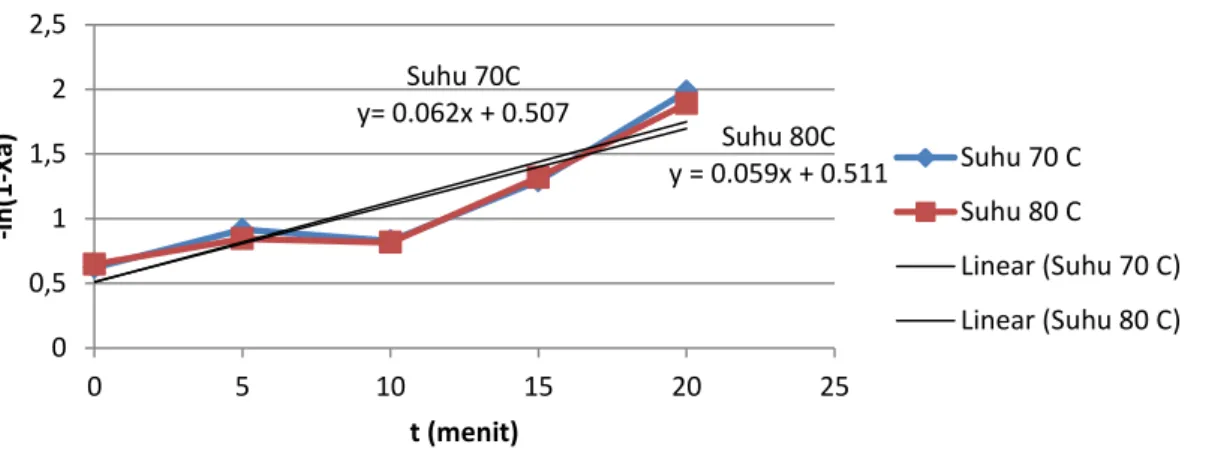
Gambar 4.2.2.2 Grafik t(menit) vs –ln(1-Xa) pada hidrolisa pati
Pada percobaan hidrolisa pati variabel yang digunakan adalah suhu 700C dan 800C. Pada hasil percobaan, variabel suhu 700C menghasilkan k=0,062/menit lebih besar dibandingkan variabel suhu 800C dengan k = 0,059/menit. Nilai k menunjukan seberapa cepat reaksi tersebut berlangsung. Hal ini berbanding terbalik dengan persamaan Arrhenius dimana semakin tinggi suhu maka konstanta kecepatan reaksi semakin besar.
Suhu 70C y= 0.062x + 0.507 Suhu 80C y = 0.059x + 0.511 0 0,5 1 1,5 2 2,5 0 5 10 15 20 25 -l n (1 -X a) t (menit) Suhu 70 C Suhu 80 C Linear (Suhu 70 C) Linear (Suhu 80 C)
k = Ae-Ea/RT di mana, k = Konstanta laju reaksi (mol jam-1) A = Faktor tumbukan
Ea = Energi aktivasi ( J mole -1) R = Konstanta gas (8.314 J K mole-1) T = Suhu (Kelvin)
Pada percobaan kami, nilai konstanta kecepatan reaksi suhu 800C lebih kecil dari pada suhu 700C karena pati mengalami penggumpalan dimana karakteristik pati tapioka yang akan mengental dan mengeras pada suhu diatas 680C (Nwokocha, 2009). Semakin tinggi suhu, pati akan lebih mengental sehingga pergerakan molekul-molekul zat pereaksi akan sulit bergerak yang menyebabkan hidrolisa tidak berjalan secara maksimal dan reaksi berjalan lebih lambat. Oleh karena itu diperlukan adanya pengadukan. Namun pengaduk yang digunakan yaitu magnetic stirer, dimana magnetic stirer hanya mengaduk pada bagian bawah larutan sehingga pengadukan kurang merata. Sebaiknya digunakan motor pengaduk sehingga pati dapat terdispersi dengan baik.
(Adity. 2009. Skripsi Hidrolisa Pati Tapioka dengan Minyak Jahe Modifikasi Cross Linking. Teknik Kimia Fakultas Teknik Universitas Diponegoro)
4.2.3 Gula Pereduksi
Gula reduksi adalah semua gula yang memiliki kemampuan untuk mereduksi dikarenakan adanya gugus aldehid atau keton bebas. Aldehid dapat teroksidasi langsung melalui reaksi redoks. Namun, gugus keton tidak dapat teroksidasi secara langsung, gugus keton, tetapi harus diubah menjadi aldehid dengan perpindahan tautomerik yang memindahkan gugus karbonil ke bagian akhir rantai.
Karbohidrat jenis monosakarida dan sebagian besar disakarida termasuk pada jenis gula reduksi. Gula Reduksi mempunyai kemampuan untuk mereduksi terutama dalam suasana basa karena adanya gugus aldehida atau keton yang bebas. Sifat sebagai reduktor ini dapat digunakan untuk keperluan indentifikasi kabohidratmaupun analisis kuantitatif.Sifat ini tampak pada reaksi ion-ion logam seperti ion Cu2+ dan Ag+ yang terdapat pada reaksi-reaksi tertentu. Contoh Gula reduksi dalam karbohidrat adalah
glukosa, galaktosa, fruktosa, laktosa, dan maltose sedangkan yang tidak termasuk didalam gula reduksi adalah sukrosa.
Fruktosa Glukosa
Wahed.2012. Laporan Resmi Analisa Gula Reduksi dan Pati.UPN Jawa Timur: LABORATORIUM TEKNOLOGI PANGANFAKULTAS TEKNOLOGI INDUSTRI UPN“VETERAN”JAWA TIMUR
Anonim.2012. Gula Reduksi danMetode Deteksinya .bisakimia.com/2012/11/24/gula-reduksi-dan-metode-deteksinya/
BAB V PENUTUP
5.1 Kesimpulan
1. Pada variabel suhu 700C menghasilkan konversi hidrolisa pati lebih besar dari suhu 800C.
2. Nilai konstanta kecepatan reaksi suhu 700C yaitu 0,062/menit dan pada suhu 800C yaitu 0,059/menit.
3. Gula reduksi adalah semua gula yang memiliki kemampuan untuk mereduksi dikarenakan adanya gugus aldehid atau keton bebas. Karbohidrat jenis monosakarida dan sebagian besar disakarida termasuk padajenis gula reduksi.
5.2 Saran
1. Suhu operasi dijaga konstan 700C dan 800C
2. Gunakan motor pengaduk supaya pati dapat terdispersi dengan baik. 3. Titrasi dilakukan diatas kompor dalam keadaan mendidih.
DAFTAR PUSTAKA
Anonim. 2012. Gula Reduksi dan Metode Deteksinya. Bisakimia.com/2012/11/24/gula-reduksi-dan-metode-deteksinya/
Abu Khalaf, A.M., “Chemical Engineering Education”, 28 (1), 48. 1994
Adity. 2009. Skripsi Hidrolisa Pati Tapioka dengan Minyak Jahe Modifikasi Cross Linking. Teknik Kimia Fakultas Teknik Universitas Diponegoro
Bej, Barnali, RK Basu and S N Ash.2008.Journal of Scientific &Indusrtial Research “Kinetic studies on acid catalysed hydrolysis of starch”. Departement of Chemical Engineering. University of Calcutta.
Charles, E. R, Harold, SM and Thomas K.S., “Applied Mathematics in Chemical Engineering” 2nd end., Mc. Graw Hill Book Ltd. 1987, New York
Hill, G.C., “An Introduction to Chemical Engineering Kinetika and Reactor Design”. 1nd ed, John Willey, New York, N.Y, 1977
Levenspiel. O., “Chemical Reaction Engineering” 2nd ed, Mc. Graw Hill Book Kogakusha Ltd, Tokyo, 1970
Mastuti, Endang, Setyawardhani, Dwi Ardiana. 2010. Pengaruh Variasi Temperatur dan Konsentrasi Katalis pada Kinetika Reaksi Hidrolisis Tepung Kulit Ketela Pohon. Surakarta: Universitas Sebelas Maret
Nur Ifah,Andi. 2013. Analisa Karbohidrat. http://organiksmakma3c03.blogspot.com/2013/03/ analisa-karbohidrat.html.Diakses 26 Maret 2013 08.00 WIB
Wahed. 2012. Laporan Resmi Analisa Gula Reduksi dan Pati. UPN Jawa Timur : LABORATORIUM TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI INDUSTRI. UPN “VETERAN” JAWA TIMUR.
Zulaidah, Agustien. Peningkatan Nilai Guna Pati Alami Melalui Proses Modifikasi Pati. Jurusan Teknik Kimia FT Universitas Pandanaran
LEMBAR PERHITUNGAN Basis : 350 ml 1. Persiapan awal a. Densitas Pati
pati =
=
= 1 gr/ml b. Densitas H2SO4 H2SO4 =
=
=
1,73 gr/ml2. Perhitungan kebutuhan reagen a. Menghitung kebutuhan H2SO4 V H2SO4= = = 5 ml
b. Menghitung kebutuhan pati (1:10) Vlarutan-VH2SO4 = Vair +Vpati
350-5 = Vair +Vpati
345 = Vair +Vpati
Vair = x 345 = 313 ml Vpati = x 345 = 31 ml mpati = x V = 1 x 31 = 31 gr
3. Penentuan Kadar Pati
a. Penentuan kadar pati awal Suhu 700C xp0 = ( ) = ( ) = 0,008 Suhu 800C xp0 = ( ) = 0,0086 b. Hidrolisa pati Suhu 700C t = 0 menit xp= ( ) = ( ) t = 5 menit xp = ( ) t = 10 menit xp = ( ) t = 15 menit xp = ( ) t = 20 menit xp = ( ) Suhu 800C t = 0 menit xp= ( ) = ( ) t = 5 menit xp = ( ) t = 10 menit xp = ( )
t = 15 menit xp = ( ) t = 20 menit xp = ( )
4. Penentuan Harga Konstanta Laju Reaksi -rA = kCA = kCA ∫ = k∫ -ln = kt + c CA = CAO (1 – xA) -ln (1–xA) = kt + c y = mx + c Suhu 700C t (x) -ln(1-XA) (y) x2 xy 0 0.620827 0 0 5 0.916291 25 4.581454 10 0.826679 100 8.266786 15 1.290984 225 19.36476 20 1.984131 400 39.68263 Σ = 50 Σ = 5.638911 Σ = 750 Σ = 71.89563 y = mx + c = ( ) ( ) ( ) = 0,062 = ( ) ( ) ( ) = 0,507
y = 0,062x + 0,507 k = 0,062 Suhu 800C t (x) -ln(1-XA) (y) x2 xy 0 0.6476 0 0 5 0.843273 25 4.216363 10 0.816672 100 8.166717 15 1.318636 225 19.77954 20 1.889152 400 37.78304 Σ = 50 Σ = 5.515332 Σ = 750 Σ = 69.94565 y = mx + c = ( ) ( ) ( ) = 0,059 = ( ) ( ) ( ) = 0,856 y = 0,059x + 0,856 k = 0,059
Faktor-faktor yang berpengaruh terhadap proses modifikasi pati secara umum
Proses Modifikasi Pati dipengaruhi oleh beberapa faktor yaitu ukuran partikel, temperatur, waktu reaksi, dan perbandingan berat air terhadap pati.
1. Ukuran Partikel
Dalam proses modifikasi pati, ukuran partikel berpengaruh terhadap laju reaksi. Semakin kecil ukuran pati maka semakin cepat reaksi berlangsung karena ukuran partikel yang kecil akan meningkatkan luas permukaan serta meningkatkan kelarutan dalam air (Saraswati, 2006).
2. Temperatur
Secara umum temperatur berhubungan dengan laju reaksi. Makin tinggi temperatur, maka reaksi akan berlangsung lebih cepat. Hal ini disebabkan konstanta laju reaksi meningkat dengan meningkatnya temperatur operasi. Hal ini sesuai dengan persamaan Arhenius berikut
k = Konstanta laju reaksi (mol jam-1) A = Faktor tumbukan
Ea = Energi aktivasi ( J mole -1) R = Konstanta gas (8.314 J K mole-1) T = Suhu (Kelvin)
(Hill, 1977)
Semakin tinggi tenperatur maka reaksi akan berjalan semakin cepat, namun kondisi ini dibatasi oleh minyak jahe yang akan terdegradasi pada suhu 60oC. (Battharai, 2001) dan karakteristik pati tapioka yang akan mengental dan mengeras pada suhu diatas 68oC (Nwokocha, 2009)
3. Waktu reaksi
Waktu reaksi berpengaruh terhadap tekstur pati yang dihasilkan. Waktu reaksi yang terlalu cepat mengakibatkan reaksi belum berjalan sempurna sedangkan jika waktu reaksi terlalu lama mengakibatkan terkstur yang kasar. Hal ini terjadi karena semakin lama waktu reaksi maka semakin banyak dinding sel singkong yang pecah sehingga terjadi pelubangan dari granula pati termodifikasi, hal ini menyebabkan permukaan yang tidak rata pada granula pati tersebut sehingga tekstur yang dihasilkan kasar (Subagio, 2008). Waktu reaksi yang optimum adalah 30 menit pada penelitian modifikasi pati tapioka menggunakan jahe (Daramola, 2006). 4. Perbandingan Berat Air Terhadap pati
Perbandingan berat air terhadap pati harus tepat agar pati dapat sempurna terlarut. Perbandingan yang terlalu besar akan menimbulkan pemborosan penggunaan pelarut, sedangkan perbandingan yang terlalu kecil dapat menyebabkan pengendapan pati. Perbandingan pati yang digunakan adalah 150 gram pati dilarutkan ke dalam 200 gram air pada penelitian modifikasi pati tapioka menggunakan jahe (Daramola, 2006).
Adity. 2009. Skripsi Hidrolisa Pati Tapioka dengan Minyak Jahe Modifikasi Cross Linking. Teknik Kimia Fakultas Teknik Universitas Diponegoro