LAPORAN PRAKTIKUM KIMIA FARMASI ANALISIS II
ANALISIS KUANTITATIF ASAM SALISILAT DENGAN METODE SPEKTROFOTOMETRI UV-VIS
Dosen Pengampu :
Dra. Apt. Hj. Lilis Tuslinah, M.Si., Apt. Ade Yeni Aprillia, M.Si.
Disusun oleh : Kelompok 1 / 3A Farmasi Najwa Agnia Cuandana 31121019 Arryza Azriel Pratama 31121033 Wildan Aulia Rahman 31121010
PROGRAM STUDI FARMASI FAKULTAS FARMASI
UNIVERSITAS BAKTI TUNAS HUSADA TASIKMALAYA
2024
i
KATA PENGANTAR
Syukur alhamdulillah penulis ucapkan kehadiran Allah SWT, karena dengan rahmat dan karunia-Nya penulis dapat menyelesaikan pembuatan Laporan Praktikum Kimia Farmasi Analisis II mengenai Analisis Kuantitatif Asam Salisilat dengan Metode Spektrofotometri UV-Vis. Penulisan Laporan Praktikum Kimia Farmasi Analisis II merupakan salah satu tugas dan persyaratan untuk menyelesaikan tugas mata kuliah Kimia Farmasi Analisis II di Universitas Bakti Tunas Husada Tasikmalaya.
Dalam hal ini penulis ingin mengucapkan terima kasih kepada dosen selaku pembimbing dan pembina mata kuliah Kimia Farmasi Analisis II. Keluarga tercinta yang selalu memberikan dukungan baik berupa moral maupun materil, rekan-rekan yang telah memberikan motivasi dan dorongan semangat sehingga penulis dapat menyelesaikan laporan ini.
Penulis menyadari sepenuhnya laporan ini jauh dari kesempurnaan. Dalam menyusun laporan ini masih banyak terdapat kesalahan dan kekurangan baik dari segi isi maupun cara penulisannya. Untuk itu penulis mengharapkan kritikan dan saran yang sifatnya membangun demi kesempurnaan makalah ini. Akhir kata penulis berharap mudah-mudahan laporan yang penulis susun ini ada manfaatnya bagi pembaca yang khususnya bagi penulis.
Tasikmalaya, 1 April 2024 Penulis
ii DAFTAR ISI
KATA PENGANTAR ... i
DAFTAR ISI ... ii
BAB I PENDAHULUAN ...1
1.1 Latar Belakang...1
1.2 Rumusan Masalah ...2
1.3 Tujuan ...2
BAB II TINJAUAN PUSTAKA ...3
2.1 Dasar Teori ...3
2.2 Sifat Fisikokimia Sampel ...4
2.3 Prinsip Percobaan ...4
2.4 Formula...5
BAB III METODOLOGI ...6
3.1 Alat dan Bahan ...6
3.1.1 Alat...6
3.1.2 Bahan ...6
3.2 Prosedur Kerja ...7
3.2.1 Isolasi Sampel ...7
3.2.2 Analisis Sampel ...8
3.3 Perhitungan ...8
3.3.1 Larutan Baku Asam Salisilat ...8
3.3.2 Penentuan Batas Deret Kurva ...8
3.3.3 Pembuatan Seri Pengenceran ...9
3.3.4 Pembuatan HCl 0,1 N 500 mL...9
3.3.5 Pembuatan FeCl3 1% 100 mL ...9
BAB IV DATA HASIL DAN PEMBAHASAN ...10
4.1 Data Hasil ...10
4.2 Pembahasan ...11
BAB V KESIMPULAN...15
DAFTAR PUSTAKA ...16
LAMPIRAN ...18
1 BAB I PENDAHULUAN
1.1 Latar Belakang
Ilmu kimia merupakan cabang dari ilmu pengetahuan alam, yang mendeskripsikan komposisi materi dan struktur, dan fenomena-fenomena lain yang mengalami perubahan materi (Brojonegoro, 2015). Ilmu kimia ini memiliki konsep sangat luas mulai dari konsep yang sederhana sampai konsep yang kompleks dan abstrak (Sari & Hidayat, R. Y., 2017). Diperlukan media pembelajaran untuk membantu mahasiswa dalam memvisualisasikan konsep-konsep yang kompleks dan abstrak menjadi konkrit (Gusbandono, dkk., 2013). Selain media pembelajaran diperlukan juga praktikum untuk mengetahui hasil yang lebih konkrit dalam sebuah pokok materi dalam ilmu kimia (Halimah & Hadiyati, 2017). Kegiatan praktikum bisa memudahkan mahasiswa dalam memahami konsep-konsep yang kompleks dan abstrak serta dapat meningkatkan keterampilan proses sains, karena mahasiswa melakukan pengamatan secara langsung (Pramesty, L. I., 2013).
Salah satu materi kimia yang dapat di integrasikan dengan praktikum yaitu pada materi pokok analisis spektrofotometri dengan sub bahasan hukum LambertBeer (Opstal & Fitch, 2018). Analisis spektrofotometri merupakan salah satu metode dalam kimia analitik yang dapat digunakan untuk mengetahui kandungan atau komposisi suatu sampel dengan cara kualitatif atau kuantitatif dan didasarkan pada serapan cahaya (Priyanto & Dwiyanto, 2008). Materi analisis spektrofotometri ini ada dalam mata kuliah kimia farmasi analisis dengan capaian pembelajaran yaitu mahasiswa mampu mendeskripsikan konsep dasar analisis spektrofotometri dan menginterpretasikan data yang diperoleh dari eksperimen spektrofotometri menggunakan spetrofotmeter (Williams et al., 2017). Berdasarkan hasil analisis capaian pembelajaran dari materi analisis spektrofotometri menunjukan bahwa materi analisis spetrofotometri harus dilakukan praktikum dengan menggunakan alat praktikum (Pratikta, 2017).
Asam salisilat merupakan salah satu bahan kimia obat yang sering ditambahkan didalam sediaan kosmetik. Asam salisilat sering ditambahkan dalam sediaan kosmetik karena bermanfaat sebagai pengobatan jerawat, psoriasis,
2
kapalan, kutil, ketombe, keratolitik, anti inflamasi, analgesik, dantabir surya (Choi et al., 2012; Sulistyaningrum et al., 2012). Pemakaian asam salisilat dalam kosmetik dengan kadar yang tinggi dapat mengakibatkan iritasi lokal, peradangan akut, ulserasi, iritasi mukosa lambung bahkan kematian (Hadisoebroto & Budiman, 2019;Lenggana, 2010).
Metode yang sering digunakan dalam menganalisa kadar asam salisilat adalah spektrofotometri UV-Vis. Kelebihan dari metode spektrofotometri UV-Vis ini, karena memiliki sensitivitas yang tinggi, memberikan hasil yang akurat, proses pengerjaannya lebih cepat dan dapat mendeteksi senyawa dengan zat yang sangat kecil (Nofita et al., 2018).
Banyak metode analisis yang telah dikembangkan untuk penetapan kadar asam salisilat, dan agar diperoleh suatu metode analisis yang akurat, spesifik dan reprodusibel maka perlu dilakukan validasi terhadap metodeanalisis tersebut.
Validasi metode merupakan konfirmasi bahwa metode analisis yang digunakan sesuai dengan tujuan yang diinginkan (Susanti &Dachriyanus, 2014). Validasi metode adalah suatu percobaan laboratoriumuntuk membuktikan bahwa parameter tersebut memenuhi persyaratan dalam penggunaannya (Harmita, 2004).IValidasi metode analisis dapat dinyatakan melalui analytical performance parameter, seperti akurasi, presisi, spesifitas, limits of detection (LOD), limits of quantitation (LOQ), linieritas dan rentang (Susanti & Dachriyanus, 2014).
Berdasarkan latar belakang tersebut, penulis melakukan praktikum terkait analisis asam salisilat dalam bentuk sediaan farmasi yang beredar di pasaran dengan metode Spektrofotometri UV-Vis.
1.2 Rumusan Masalah
1. Bagaimana cara menentukan kadar asam salisilat dengan metode Spektrofotometri UV-Vis?
2. Berapa kadar asam salisilat yang terkandung dalam sampel sediaan farmasi yang diberikan?
1.3 Tujuan
1. Untuk mengetahui cara menentukan kadar asam salisilat dengan metode Spektrofotometri UV-Vis
2. Untuk mengetahui kadar salisilat dalam sediaan farmasi
3 BAB II
TINJAUAN PUSTAKA
2.1 Dasar Teori
Asam salisilat dikenal juga dengan Asam 2,hidroksi-benzoat merupakan senyawa golongan fenol (Warrier, 2013). Pemerian hablur, biasanya berbentuk jarum halus atau serbuk halus; putih; rasa agak manis, tajam dan stabil di udara.
Bentuk sintetis warna putih dan tidak berbau. Kelarutannya sukar larut dalam air dan dalam benzena. Mudah larut dalam etanol dan dalam eter. Larut dalam air mendidih dan agak sukar larut dalam kloroform. Khasiat dan penggunaan sebagai keratolitikum (menipiskan selaput kulit/meratakan kulit) dan antifungi yang berkhasiat sebagai fungisidal dan bakteriostatis lemah. Asam salisilat bekerja keratolitik sehingga digunakan dalam sediaan obat luar terhadap infeksi jamur yang ringan (Astuti, 2007).
Asam salisilat sebagai zat aktif utama maupun tambahan tersedia dalam berbagai produk dengan beragam vehikulum. Penggunaan asam salisilat harus tetap berhati-hati dan tidak boleh diberikan pada area yang luas dalam jangka panjang (Sulistyaningrum, 2012). Panjang gelombang (λ) maksimum ditentukan dengan cara memindai serapan standar dalam spektro UV-Vis pada kisaran panjang gelombang 200-400 nm (Fatmawati & Herlina, 2017).
Spektrofotometri UV-Vis merupakan metode analisis yang menggunakan panjang gelombang UV dan Visible sebagai area serapan untuk mendeteksi senyawa. Pada umumnya senyawa yang dapat diidentifikasi menggunakan Spektrofotometri UV-Vis adalah senyawa yang memiliki gugus gugus kromofor dan gugus auksokrom . Pengujian dengan Spektrofotometri UV-Vis tergolong dan cepat cepat jika dibandingkan dengan metode lain (Handoyo Sahumena et al., 2020).
Validasi metode merupakan elemen penting dari kontrol kualitas. Validasi adalah konfirmasi melalui pemeriksaan dan penyediaan bukti objektif bahwa persyaratan tertentu untuk penggunaan yang dimaksudkan tertentu terpenuhi.
Parameter validasi metode analisis meliputi akurasi, presisi, spesifisitas, batas
4
deteksi (Limit of Detection) dan batas kuantifikasi (Limit of Quantification) (Handoyo Sahumena et al., 2020).
2.2 Sifat Fisikokimia Sampel
Gambar 2.2 Struktur Kimia Asam Salisilat
▪ Nama : Asam Salisilat, Asam 1,2-Hidroksibenzoat, O-asam Hidroksibenzoat
▪ Rumus kimia : C7H6O3
▪ BM : 138,12
▪ Pemerian : Hablur putih; biasanya berbentuk jarum halus atau serbuk halus putih; rasa agak manis, tajam dan stabil di udara. Bentuk sintetis warna putih dan tidak berbau. Jika dibuat dari metil salisilat alami dapat berwarna kekuningan atau merah muda dan berbau lemah mirip mint.
▪ Kelarutan : Sukar larut dalam air dan dalam benzen, larut dalam air mendidih;
mudah larut dalam etanol dan dalam eter; agak sukar larut dalam kloroform (Farmakope Indonesia Ed VI, 2020 halaman 193)
▪ Absorptivitas Molar : 260,04% (Spektrofotometri UV-Vis panjang gelombang max = 303 nm dalam etanol) (Analytical Profiles of Drug Substances Vol. 23 halaman 427)
▪ Identifikasi : Menggunakan larutan FeCl3 menghasilkan warna ungu (Analytical Profiles of Drug Substances Vol. 23 halaman 447)
2.3 Prinsip Percobaan
Metode spektrofotometri UV-Vis ini merupakan teknik analisis yang menggunakan sinar UV pada panjang gelombang sebesar 100-400 nm dan sinar tampak pada panjang gelombang 400-750 nm. Prinsip spektrofotometri UV-Vis adalah sinar yang datang akan diteruskan diserap. Sinar yang diserap intensitasnya berbanding lurus dengan besarnya konsentrasi zat yang menyerap sinar (Suhartati, 2017).
5 2.4 Formula
(Handbook of Pharmaceutical Manufacturing Formulations Volume 4)
6 BAB III METODOLOGI
3.1 Alat dan Bahan 3.1.1 Alat
1. Spektrofotometer UV-Vis 2. Pipet tetes
3. Mikropipet 1000 µL 4. Beaker glass
5. Ball pipet 6. Erlenmayer 7. Pipet Volume 8. Plat tetes
9. Cawan Penguap 10. Plastik warp 11. Tissue 12. Spatel
13. Corong pisah 50 dan 100 ml 14. Botol
15. Statif 16. Vial 17. Klem bulat 18. Batang Pengaduk 19. Tip Biru
20. Waterbath 21. Manice 22. Kaca arloji
23. Labu ukur 25 ml dan 10 ml 24. Timbangan analitik
3.1.2 Bahan
1. Asam Salisilat p.a 2. Etanol 95% p.a 3. Etanol 95%
4. Eter
5. NaOH 0,1 N 6. HCl 0,1 N 7. FeCl3 1%
8. Sampel Asam Salisilat
7 3.2 Prosedur Kerja
3.2.1 Isolasi Sampel
Metode Ekstraksi Cair-Cair Timbang Sampel
sebanyak 800 mg
Sampel dilarutkan dengan eter
Masukkan kedalam corong pisah
Tambahkan NaOH 0,1 N lalu kocok Diamkan sampai
terbentuk dua fase Pisahkan Fase eter
dengan Fase NaOH
Fase NaOH ditambahkan HCl
0,1 sampai pH 2 Sampai Ph 2
Tambahkan eter kemudian kocok
Diamkan sampai terbentuk dua fase Fase eter diambil
dan diuapkan sampai membentuk kristal asam salisilat
Ambil beberapa tetes Fase Eter dan uji dengan FeCl3 1% jika terbentuk warna ungu menunjukkan
hasil positif masih mengandung asam salisilat, lakukan ekstraksi Kembali sampai hasil negatif
8 3.2.2 Analisis Sampel
Metode Spektofotometri Uv-Vis
3.3 Perhitungan
3.3.1 Larutan Baku Asam Salisilat
Dibuat larutan asam salisilat 50 ppm dan dimasukan ke dalam labu ukur 25 mL, setelah itu ditambahkan etanol p.a hingga tanda batas.
▪ 50 ppm = mg / 0,025 L mg = 50 x 0,025 mg = 1,25 mg
▪ 1,25 mg Asam Salisilat p.a dilarutkan dalam etanol p.a hingga tanda batas labu ukur 25mL.
3.3.2 Penentuan Batas Deret Kurva
▪ Batas Bawah A = a x b x c 0,2 = 395,811 x 1 x c c = 0,2
395,811
c = 0,0005052917%
c = 5,052917 ppm
= 5 ppm
▪ Batas Atas
A = a x b x c 0,2 = 395,811 x 1 x c c = 0,8
395,811
c = 0,00202211667%
c = 20,211667 ppm = 20 ppm
Kurva kalibrasi dibuat dari 6 seri pengenceran yaitu : 6, 8, 10, 12, 14 dan 16 ppm Analit hasil ECC
dilarutkan pada labu ukur 25 ml ad
etanol pa sampai tanda batas
Tentukan konsentrasi dalam bentuk ppm
Lakukan pengecekan pada Panjang gelombang
234 nm
Apabila absorbansi >0,8, lakukan pengenceran hingga didapatkan absorbansi pada rentang 0,2 – 0,8 Hitung kadar asam salisilat pada
sampel dengan menggunakan multi point method
9 3.3.3 Pembuatan Seri Pengenceran
▪ 6 ppm
V1 x ppm1 = V2 x ppm2
V1 x 50 = 5 x 6 V1 x 50 = 30 V1 = 30
50
V1 = 0,6 ml
▪ 8 ppm
V1 x ppm1 = V2 x ppm2
V1 x 50 = 5 x 8 V1 x 50 = 40 V1 = 40
50
V1 = 0,8 ml
▪ 10 ppm
V1 x ppm1 = V2 x ppm2
V1 x 50 = 5 x 10 V1 x 50 = 50 V1 = 50
50
V1 = 1 ml
▪ 12 ppm
V1 x ppm1 = V2 x ppm2
V1 x 50 = 5 x 12 V1 x 50 = 60 V1 = 60
50
V1 = 1,2 ml
▪ 14 ppm
V1 x ppm1 = V2 x ppm2
V1 x 50 = 5 x 14 V1 x 50 = 120 V1 = 70
50
V1 = 1,4 ml
▪ 16 ppm
V1 x ppm1 = V2 x ppm2
V1 x 50 = 5 x 16 V1 x 50 = 80 V1 = 80
50
V1 = 1,6 ml 3.3.4 Pembuatan HCl 0,1 N 500 mL
V1 x N1 = V2 x N2 (Standar 12 N) V1 x 12 = 500 x 0,1
V1 x 12 = 50 V1 = 4,16 ml
3.3.4 Pembuatan NaOH 0,1 N 500 mL N = 𝑔𝑟
𝐵𝐸 𝑥 𝑉
0,1 = 𝑔𝑟
40 𝑥 0,5
gr = 0,1 x 40 x 0,5 = 2 gram 3.3.5 Pembuatan FeCl3 1% 100 mL
gr = 1
100 x 100 mL = 1 gram
10 BAB IV
DATA HASIL DAN PEMBAHASAN
4.1 Data Hasil
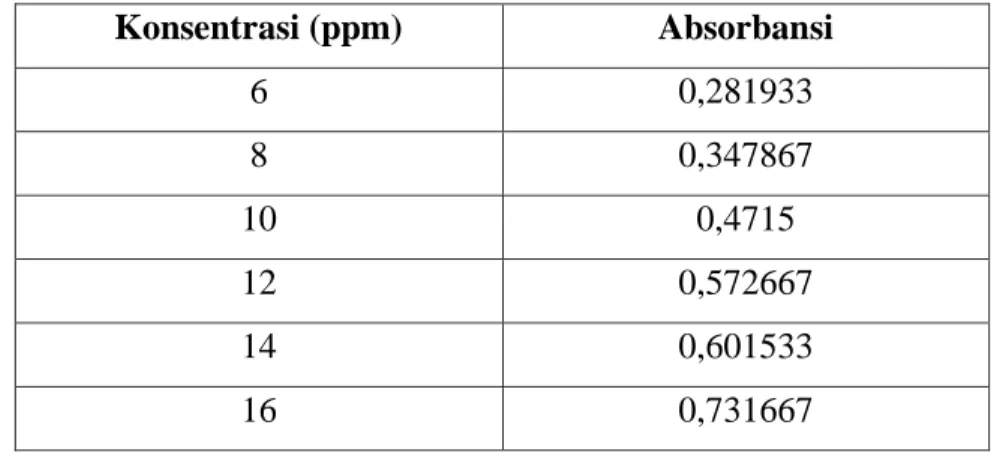
Dari 6 seri konsentrasi didapatkan nilai absorbansi seperti pada tabel 1.
Tabel 1. Nilai Absorbansi Larutan Standar Asam Salisilat
Konsentrasi (ppm) Absorbansi
6 0,281933
8 0,347867
10 0,4715
12 0,572667
14 0,601533
16 0,731667
Kurva kalibrasi Linear Larutan Standar Asam Salisilat dapat dilihat pada kurva 1.
Kurva 1. Regresi Linear Larutan Standar Asam Salisilat
▪ Perhitungan Konsentrasi Sampel
Berdasarkan hasil percobaan, didapatkan persamaan regresi linear standar asam salilisat yaitu: y = 0,0444x + 0,0123, dengan absorbansi sampel asam salisilat sebesar0,5036 serta faktor pengenceran sebanyak 10x. Maka dari itu, dapat diketahui konsentrasi sampel dengan cara mensubstitusi absorbansi sampel (0,5036) ke dalampersamaan regeresi linear standar asam salisilat:
0.281933 0.347867
0.4715 0.572667
0.601533 0.731667 y = 0.0444x + 0.0123
R² = 0.9821
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8
0 2 4 6 8 10 12 14 16 18
Absorbansi
Konsentrasi (ppm)
11 y = 0,0444x + 0,0123
0,5036 = 0,0444x + 0,0123 0,5036 - 0,0123 = 0,0444x 0,4913 = 0,0444x
x = 0,4913
0,0444
x = 11,06 ppm
Sehingga, kadar sebenarnya dari asam salisilat yaitu:
Kadar sebenarnya = 11,06 ppm x Faktor Pengenceran Kadar sebenarnya = 11,06 ppm x 10
Kadar sebenarnya = 110,6 ppm
▪ Konversi ppm → massa (mg) 110,6 ppm = 110,6 mg/1000 ml
Dikarenakan sampel asam salisilat yang telah mengkristal dilarutkan etanol p.a ad 25 ml, maka bobot asam salisilat pada analit dapat dihitung sebagai berikut:
Massa asam salisilat = 110,6 𝑚𝑔
1000 𝑚𝑙 x 25 ml Massa asam salisilat = 2,765 mg
▪ Perhitungan Kadar (%) Asam Salisilat pada Sampel
Diketahui bobot sampel yang ditimbang yaitu 800 mg dan bobot asam salisilat hasil analisis menggunakan spektrofotometri UV-Vis yaitu 2,765 mg.
Sehingga dapat dihitung persentase asam salisilat pada sampel yaitu sebagai berikut:
% Kadar Asam salisilat = 𝑏𝑜𝑏𝑜𝑡 𝐴𝑠𝑎𝑚 𝑆𝑎𝑙𝑖𝑠𝑖𝑙𝑎𝑡
𝐵𝑜𝑏𝑜𝑡 𝑆𝑎𝑚𝑝𝑒𝑙 x 100%
% Kadar Asam alisilat = 2,765 𝑚𝑔
800 𝑚𝑔 x 100%
% Kadar Asam alisilat = 𝟎, 𝟑𝟒𝟔%
4.2 Pembahasan
Pada praktikum kali ini dilakukan percobaan mengenai analisis kuantitatif sampel asam salisilat dalam sediaan farmasi menggunakan metode instrumental yaitu spektrofotometri UV-Vis. Metode ini dapat digunakan untuk menganalisis senyawa asam salisilat dikarenakan pada strukturnya terdapat gugus kromofor dan ausokrom yang dapat berinteraksi dengan cahaya. Gugus kromofor tersebut yaitu
12
ikatan C=C pada gugus aromatik dan ikatan C=O pada gugus karboksilat, sedangkan gugus ausokromnya merupakan gugus hidroksil (O-H) yang terikat langsung pada gugus aromatik. Selain itu, asam salisilat juga dapat dianalisis dengan menggunakan metode konvensional yaitu metode titrasi asam-basa dikarenakan senyawa ini memiliki gugus karboksilat yang menyebabkan senyawa ini bersifat asam.
Sampel asam salisilat yang akan dianalisis yaitu sampel dengan nomor 239 dengan bentuk sediaan berupa krim. Secara umum, formulakrim asam salisilat terdiri dari asam salisilat sebagai zat aktif yang dapat larut di dalam etanol, eter, dan kloroform; serta eksipien berupa basis yaitu vaseline yang tidak dapat larut di dalam etanol, namun dapatlarut di dalam eter atau kloroform.
Berdasarkan kelarutannya, isolasi sampel yang digunakan untuk memisahkan analit dari matriks yaitu dengan metode ekstraksi cair-cair. Prinsip dari metode ini yaitu pemisahan senyawa berdasarkan perbedaan kelarutan dalam dua pelarut yang berbeda kepolaran. Metode ini lebih dipilih daripada ekstraksi cair- padat dikarenakan basis dan zat aktif dapat larut sempurna dalam eter atau kloroform sehingga proses ekstraksi akan lebih sempurna ketimbang metode ekstraksi cair-padat.
Sebelum ekstraksi dilakukan, sampel ditimbang seberat 800 mg. Kemudian sampel dilarutkan di dalam pelarut eter dan dimasukan ke dalam corong pisah.
Setelah itu ditambahkan larutan NaOH 0,1 N agar terjadi reaksi pembentukan garam natrium salisilat, sehingga asam salisilat yang larut di dalam eter dapat terekstrak ke dalam fase air atau NaOH. Kemudian dilakukan pengocokan dan pemisahan antara fase eter dan NaOH. Untuk memastikan seluruh senyawa asam salisilat telah terekstrak ke dalam fase NaOH, maka dilakukan uji kualitatif pada fase eter dengan menggunakan reagen FeCl3 1% dengan cara menguapkan 1-2 tetes eter tersebut di atas plat tetes dan ditetesi reagen FeCl3 1%. Adanya pembentukan warna ungu-biru menunjukkan keberadaan senyawa asam salisilat pada fase eter sehingga proses ekstraksi harus diulang kembali dengan menggunakan larutan NaOH baru. Dikarenakan tidak terbentuk warna ungu-biru, maka tidak dilakukan pengulangan ekstrak kembali.
13
Proses selanjutnya yaitu mencampurkan fase garam salisilat dengan HCl hingga pH berada pada rentang 2. Hal tersebut bertujuan untuk mereaksikan natrium salisilat dengan HCl sehingga akan terbentuk garam natrium klorida dan asam salisilat yang terbebas dari bentuk garamnya. Tahap selanjutnya yaitu menambahkan eter pada campuran tersebut untuk mengekstrak senyawa asam salisilat, kemudian memisahkan fase eter dan garam natrium klorida di dalam corong pisah. Tahap terakhir yaitu menguapkan fase eter pada cawan penguap sehingga terbentuk senyawa asam salisilat dalam bentuk padatan berupa kristal asam salisilat.
Tahap selanjutnya yaitu menganalisis senyawa asam salisilat secara kuantitatif menggunakan metode spektrofotometri UV-Vis. Pada metode ini dibutuhkan tiga jenis larutan, yaitu larutan blanko, larutan standar, dan larutan sampel. Larutan blanko merupakan pelarut yang digunakan untuk melarutkan sampel dan standar. Larutan sampel merupakan senyawa asam salisilat hasil ekstraksi yang dilarutkan di dalam pelarut tertentu, sedangkan larutan standar merupakan senyawa asam salisilat murni yang dilarutkan didalam pelarut tertentu.
Berdasarkan literatur, asam salisilat memiliki panjang gelombang maksimum 234 nm apabila dilarutkan di dalam pelarut etanol 95%. Oleh karena itu, pelarut yang digunakan untuk membuat larutan standar dan sampel adalah etanol 95%.
Metode analisis spektrofotometri yang digunakan yaitu multi point method sehingga dibuat deret konsentrasi pada larutan standar dengan absorbansi yang terbaca pada spektrofotometer hendaknya berada pada rentang 0,2-0,8. Anjuran ini digunakan berdasarkan anggapan bahwa kesalahan dalam pembacaan T adalah 0,005 atau 0,5%. Untuk memudahkan pembuatan larutan standar, maka digunakan persamaan Lambert-Beer yang menyatakan bahwa absorbansi berbanding lurus dengan absortivitas, tebal kuvet, dan konsentrasi yang dinyatakan sebagai A = a.b.c. Berdasarkan hasil perhitungan tersebut, maka dibuatlah enam deret konsentrasi larutan standar dengan absorbansi pada rentang 0,2-0,8 yaitu 6 ppm, 8 ppm, 10 ppm, 12 ppm, 14 ppm, dan 16 ppm.
Setelah larutan standar dibuat dan dianalisis dengan menggunakan spektrofotometer, selanjutnya kristal asam salisilat dilarutkan di dalam pelarut etanol 95% ad 25 ml dan dianalisis absorbansinya pada spektrofotometer. Hasil
14
menunjukkan bahwa pada pengenceran 10x dari larutan induk sampel (25 ml) memiliki absorbansi berada pada rentang 0,2-0,8 yaitu 0,5036. Selanjutnya kadar asam salisilat dari sampel dianalisis dengan mensubstitusi absorbansi sampel terhadap persamaan regresi linear dari larutan standar. Hasil perhitungan menunjukkan bahwa kadar asam salisilat yang terkandung di dalamsampel nomor 239 adalah 0,346%
15 BAB V KESIMPULAN
Berdasarkan data hasil praktikum dapat disimpulkan bahwa :
1. Asam Salisilat dapat dianalisis kuantitatif dengan metode spektrofotometri UV- Vis karena pada strukturnya terdapat gugus kromofor dan ausokrom yang dapat berinteraksi dengan cahaya. Gugus kromofor tersebut yaitu ikatan C=C pada gugus aromatik dan ikatan C=O pada gugus karboksilat, sedangkan gugus ausokromnya merupakan gugus hidroksil (O-H) yang terikat langsung pada gugus aromatik.
2. Kadar asam salisilat pada sampel krim dengan nomor 239 adalah sebesar 0,346%.
16
DAFTAR PUSTAKA
Astuti. 2007. Petunjuk Praktikum Analisis Bahan Biologi. Yogyakarta : Jurdik.
Biologi FMIPA UNY
Brittain, H.G. (1999). Analytical profiles of drugs substances and excipients.
(Volume 23).
Brojonegoro, S. (2015). LKS Materi Larutan Elektrolit dan Non Elektrolit Bernasis Multiple Representasi Menggunakan Model Simayang. Jurnal Pendidikan Dan Pembelajaran Kimia, 4(1), 236–247.
Depkes RI. 2020. Farmakope Indonesia edisi VI. Departemen Kesehatan. Republik Indonesia. Jakarta: Kementrian Kesehatan Republik Indonesia
Fatmawati, F.; Herlina, L. Validasi Metode Dan Penentuan Kadar Asam Salisilat Bedak Tabur Dari Pasar Majalaya. EduChemia (Jurnal Kimia. dan Pendidikan) 2017, 2 (2), 141.
G. Hadisoebroto and S. Budiman, “Penetapan Kadar Asam Salisilat pada Krim Anti Jerawat yang Beredar di Kota Bandung dengan Metode Spektrotometri Ultra Violet,” J. Kartika Kim., vol. 2, no. 1, pp. 51–56, 2019.
Gusbandono Toto, Sukardjo, JS, dan U. B. S. (2013). Pengaruh Metode Pembelajaran Kooperatif Stdent Team Achievment (STAD) Dilengkapi Media Flash dan Plastisin Terhadap Representasi Belajar Siswa Pada Pokok Bahsan Ikatan Kimia Kelas X Semester 1 sma Negeri 1 Sambungmacan Tahun Pelajaran 2012/2013. Jurnal Pendidikan Kimia, 2(4), 102–109.
Halimah, M., Ayuni, N. D., & Hadiyati, Y. (2017). Uji Kelayakan KIT Praktikum Pengujian Kepolaran Senyawa dari Material Sederhana. Jurnal Riset Pendidikan Kimia, 7(1), 52–58.
Handoyo Sahumena, M., Ruslin, R., Asriyanti, A., & Nurrohwinta Djuwarno, E.
(2020). Identifikasi Jamu Yang Beredar Di Kota Kendari Menggunakan Metode Spektrofotometri Uv-Vis. Journal Syifa Sciences and Clinical Research, 2(2), 65–72. https://doi.org/10.37311/jsscr.v2i2.6977.
Opstal, M. T. Van, Nahlik, P., Daubenmire, P. L., & Fitch, A. (2018). Physicians as the First Analytical Chemists: Gall Nut Extract Determination of Iron Ion (Fe 2+ ) Concentration. Journal of Chemical Education, 93(4), 148–152.
https://doi.org/10.1021/acs.jchemed.7b00524
17
Niazi, S.K., 2009, Handbook of Pharmaceutical Manufacturing Formulations, 2nd.
Ed., Vol. 4: Semisolid Products, CRC Press,
Pramesty, L. I., & P. (2013). Pengembangan Alat Peraga KIT Fluida Statis Seagai Media Pembelajaran Pada Sub Materi Fluida Statis di Kelas XI IPA SMA Negeri 1 Mojosari , Rosalina Indah Pramesty , Prabowo. Jurnal Inovasi Pendidikan Fisika, 02(03), 70–74.
Pratikta, M. L. (2017). Studi Penggunaan Spektrofotometer Sederhana untuk Mendeteksi Logam Berat Kromium dalam Limbah Pabrik Tekstil. Journal Studi Fisika, 1(3), 110–112
Priyanto Nandang, Dwiyanto, & A. F. (2008). Analisis Kandungan Logam Berat ( Hg , Pb , Cd , dan Cu ) Pada Ikan dan Air Menggunakan Metode Spektrofotmetri. Jurnal Pascapanen Dan Bioteknologi Kelautan Dan Perikanan, 3(1), 69–78.
Sari & Hidayat Resti Yulianti. (2017). Pengembangan Keterampilan Berpikir Kreatif Siswa Pada Praktikum Jenis-Jenis Koloid: Pendekatan Saintifik.
Jurnal Tadri Kimiya, 1(1), 32–37.
Sulistyaningrum, K.S., Nilasari, H., dan Effendi, H.E. (2012): Penggunaan Asam Salisilat dalam Dermatologi, J Indon Med Assoc, Vol.62, No.7
Susanti, M., Dachriyanus. 2014. Kromatografi cair kinerja tinggi. Padang : Andalas. University Press.
Williams, J. L., Miller, M. E., Avitabile, B. C., Burrow, D. L., Schmittou, A. N., Mann, M. K., & Hiatt, L. A. (2017). Teaching Students To Be Instrumental in Analysis: Peer-Led Team Learning in the Instrumental Laboratory.
Juornal of Chemical Education, 8(4), 3–4.
https://doi.org/10.1021/acs.jchemed.7b00285.
18 LAMPIRAN
Alat yang digunakan dalam praktikum
Sampel Asam Salisilat yang akan dianalisis
Sampel dilarutkan dengan eter
Sampel yang telah dilarutkan dimasukkan
kedalam corong pisah
Penambahan NaOH 0,1 N kedalam corong pisah
yang berisi sampel
Corong pisah yang berisi sampel digojog selama
beberapa menit
Corong pisah berisi sampel didiamkan hingga terbentuk 2 fase
Memisahkan fase eter dengan fase NaOH
Pengujian Identifikasi as. Salisilat pada Fase NaOH dengan FeCl3 1%
19 Penambahan HCl 0,1 N
Pada Fase NaOH
Pengecekan pH Fase NaOH dengan indicator
universal
Penambahan eter Fase NaOH pada corong
pisah
Corong pisah digojog selama beberapa menit
Corong pisah didiamkan hingga terbentuk 2 fase
Fase eter diambil kemudian diuapkan
Pembuatan seri larutan
baku Pengenceran analit Pengecekan Panjang gelombang analit