ANALISIS SECARA GC-MS KOMPONEN MINYAK ATSIRI
DARI RIMPANG TANAMAN JERANGAU
(Acorus calamus)
HASIL ISOLASI MENGGUNAKAN METODE
HIDRODESTILASI DIBANDINGKAN
DENGAN DESTILASI UAP
SKRIPSI
DIAN ARINI SEMBIRING
070802034
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
ANALISIS SECARA GC-MS KOMPONEN MINYAK ATSIRI DARI RIMPANG TANAMAN JERANGAU (Acorus calamus)
HASIL ISOLASI MENGGUNAKAN METODE HIDRODESTILASI DIBANDINGKAN
DENGAN DESTILASI UAP
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
DIAN ARINI SEMBIRING 070802034
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : ANALISIS SECARA GC-MS KOMPONEN MINYAK
ATSIRI DARI RIMPANG TANAMAN JERANGAU
(Acoruscalamus) MENGGUNAKAN METODE
HIDRODESTILASI DIBANDINGKAN DENGAN DESTILASI UAP
Kategori : SKRIPSI
Nama : DIAN ARINI SEMBIRING
NomorIndukMahasiswa : 070802034
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (MIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Juni 2012
KomisiPembimbing :
Pembimbing 2, Pembimbing 1,
Drs. DarwisSurbakti, MS Dr.MimpinGinting, MS NIP. 195307071983031001 NIP. 195510131986011001
Diketahui/Disetujuioleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
ANALISIS SECARA GC-MS KOMPONEN MINYAK ATSIRI DARI RIMPANG TANAMAN JERANGAU (Acoruscalamus) HASIL ISOLASI
MENGGUNAKAN METODE HIDRODESTILASI DIBANDINGKAN DENGAN DESTILASI UAP
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2012
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Kristus atas limpah kasih dan karunia-Nya yang senantiasa menyertai sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini.
ABSTRAK
Telah dilakukan studi perbandingan komposisi minyak atsiri dari rimpang jerangau yang diperoleh dari hasil isolasi menggunakan metode hidrodestilasi dan destilasi uap air. Minyak atsiri yang dihasilkan dengan menggunakan metode hidrodestilasi maupun destilasi uap digunakan rimpang jerangau yang basah. Selanjutnya minyak atsiri yang diperoleh dianalisis komposisinya dengan menggunakan GC-MS. Melalui metode hidrodestilasi, diperoleh rendemen minyak atsiri sebanyak 0,325% v/w, yang terdiri dari 13 jenis senyawa dimana diantaranya sebanyak 11 senyawa yang dapat
diidentifikasi, yaitu : Kamfen (1,87%), β-Ocimen (1,42%), Kamfor (1,12%), Metil Isoeugenol (12,97%), Euasaron (1,87%), Asaron (60,34%), Cis-Calamenen (1,75%), Trans-Isoelemicin (1,14%), β-Ionon (1,97%) dan Aristolon (2,43%). Selanjutnya melalui metode destilasi uap diperoleh rendemen minyak atsiri sebanyak 0,35% v/w, yang terdiri dari 18 jenis senyawa dimana sebanyak 14 senyawa yang dapat
diidentifikasi, yaitu : α-Pinen (0,37%), Kamfen (1,69%), β-Ocimen (1,33%), Linalool (0,45%), Kamfor (1,04%), Aristolen (0,17%), Metil Isoeugenol (14,91%), Euasaron
ANALYSIS GC – MS THE COMPONENT ESSENTIAL OILS FROM JERANGAU RHIZOMES (Acorus calamus ) RESULTED
WITH USING HYDRODISTILLATION COMPARATIED TO STEAM
DISTILLATION METHOD
ABSTRACT
It had been studied ratio the composistion essential oils from Jerangau rhizomes obtained from isolation using the method of hidrodistillation and steam distillation. Essential oils was yielded using hidrodistillation method and steam distilation with fresh rhizome. And then, composition of essential oils that yielded were analyzed using GC-MS. Through hydrodistilation method, essential oil yield obtained a number of 0,325%, v/w, which consists of 13 types compounds which include a total of 11
compounds that can be identified, there are : Camphene (1,87%), β-Ocimene (1,42%), Camphor (1,12%), Methyl Isoeugenol 12,97%), Euasarone (1,87%), Asarone (60,34%), Cis-Calamenene (1,75%), Trans-Isoelemicin (1,14%), β-Ionone (1,97%), and Aristolone (2,43%). And then, by steam distilations obtained essential oils a number of 0,35%, v/w, which consists of 18 types compounds which include a total
of 14 compounds that can be indetified, there are : α-Pinene (0,37%), Camphene
DAFTAR ISI
Halaman
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak v
Abstract vi
Daftar Isi vii
Daftar Gambar ix
Daftar Lampiran xi
Daftar Tabel xii
BAB 1 PENDAHULUAN
1.1. Latar Belakang 1
1.2. Permasalahan 3
1.3. Batasan Masalah 3
1.4. Tujuan Penelitian 3
1.5. Manfaat Penelitian 4
1.6. Lokasi Penelitian 4
1.7. Metodologi Penelitian 4
BAB 2 TINJAUAN PUSTAKA
2.1. Tanaman Jerangau (Acorus calamus) 5
2.1.1. Manfaat Jerangau 7
2.1.2. Komposisi Minyak Atsiri Jerangau 8
2.2. Minyak Atsiri 9
2.2.1. Komposisi Kimia Minyak Atsiri 11
2.2.2. Sumber Minyak Atsiri 12
2.2.3. Biosintesa Pembentukan Minyak Atsiri 12
2.2.4. Kegunaan Minyak Atsiri 18
2.3. Rendemen 19
2.3.1. Faktor yang Mempengaruhi Rendemen Minyak Atsiri 20
2.4. Cara Memperoleh Minyak Atsiri 21
2.4.1. Penyulingan 21
2.4.1.1. Kelebihan dan Kekurangan Metode Penyulingan 23 2.4.1.2. Pengaruh Metode Penyulingan Terhadap Mutu
Minyak Atsiri 25
2.4.2. Ekstraksi Dengan Pelarut Menguap 25
2.4.3. Ekstraksi Dengan Lemak Dingin (Enfleurasi) 25
2.4.4. Pengepresan 26
2.5. Analisis Komponen Minyak Atsiri 27
2.5.2. Spektrometri Massa 28
BAB 3 BAHAN DAN METODOLOGI PENELITIAN
3.1. Alat-Alat 30
3.2. Bahan 31
3.3. Prosedur Penelitian 31
3.3.1. Penyediaan Sampel 31
3.3.2. Penyulingan Rimpang Jerangau 31
3.4. Bagan Penelitian 34
3.4.1. Bagan Penelitian Isolasi Minyak Atsiri Dengan Alat Stahl 34 3.4.2. Bagan Penelitian Isolasi Minyak Atsiri Dengan Destilasi Uap 35
BAB 4 HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian 36
4.1.1. Isolasi Minyak Atsiri Dari Rimpang Tanaman Jerangau 36 4.1.2. Hasil Analisis Kromatografi Gas-Spektra Massa 37
4.2. Pembahasan 40
4.2.1. Hasil Isolasi Minyak Atsiri Melalui Metode Hidrodestilasi
Menggunakan Alat Stahl 40
4.2.2. Hasil Isolasi Minyak Atsiri Menggunakan Destilasi Uap 60
BAB 5 KESIMPULAN DAN SARAN
5.1. Kesimpulan 79
5.2. Saran 80
DAFTAR GAMBAR
Gambar 2.1. Tanaman Jerangau 5
Gambar 2.2. Struktur α-Asaron dan β-Asaron 9
Gambar 2.3. Pembentukan Asam Mevalonat Sebagai Zat Antara Dalam
Biosintesis Terpenoid. 14
Gambar 2.4. Reaksi Biosintesa Terpenoid 15
Gambar 2.5. Biosintesa Fenil Propanoid 17
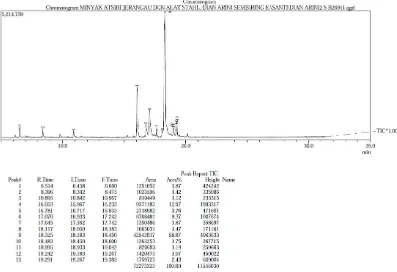
Gambar 4.1. Kromatogram Minyak Atsiri Dari Rimpang Jerangau Yang Diperoleh
Secara Hidrodestilasi Dengan Alat Stahl 37
Gambar 4.2. Kromatogram Minyak Atsiri Dari Rimpang Jerangau Yang Diperoleh Secara Hidrodestilasi Dengan Destilasi Ua 39 Gambar 4.3.Spektrum GC-MS Senyawa Kamfen Dari Minyak Atsiri Rimpang
Jerangau Dengan Menggunakan Alat 41
Gambar 4.4. Pola Fragmentasi Senyawa Kamfen 42
Gambar 4.5. Spektrum GC-MS Senyawa β-Ocimen Dari Minyak Atsiri Rimpang Jerangau Dengan Menggunakan Alat Stahl 43 Gambar 4.6. Pola Fragmentasi Senyawa β-Ocimen 44 Gambar 4.7. Spektrum GC-MS Senyawa Kamfor Dari Minyak Atsiri Rimpang
Jerangau Dengan Menggunakan Alat Stahl 45
Gambar 4.8. Pola Fragmentasi Senyawa Kamfor 46
Gambar 4.9. Spektrum GC-MS Senyawa Metil Isoeugenol Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 47 Gambar 4.10. Pola Fragmentasi Senyawa Metil Isoeugenol 48 Gambar 4.11. Struktur α-Asaron, β-Asaron, dan Euasaron 49 Gambar 4.12. Spektrum GC-MS Senyawa α-Asaron Dari Minyak Atsiri Rimpang
Jerangau Dengan Menggunakan Alat Stahl 50 Gambar 4.13. Spektrum GC-MS Senyawa β-Asaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 50 Gambar 4.14. Spektrum GC-MS Senyawa Euasaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 51 Gambar 4.15. Pola Fragmentasi Senyawa Asaron 51 Gambar 4.16. Pola Fragmentasi Senyawa Euasaron 52 Gambar 4.17. Spektrum GC-MS Senyawa Cis-Kalamen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 53 Gambar 4.18. Pola Fragmentasi Senyawa Cis-Kalamenen 54 Gambar 4.19. Spektrum GC-MS Senyawa Trans-Isoelemicin Dari
Minyak Atsiri Rimpang Jerangau Dengan Menggunakan Alat Stahl 55 Gambar 4.20. Pola Fragmentasi Senyawa Trans-Isoelemicin 57 Gambar 4.21. Spektrum GC-MS Senyawa β-Ionon Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 58
Gambar 4.22. Pola Fragmentasi Senyawa β-Ionon 59
Gambar 4.23. Spektrum GC-MS Senyawa Aristolen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 62
Gambar 4.26. Pola Fragmentasi Senyawa α-Pinen 63
Gambar 4.27. Spektrum GC-MS Senyawa Kamfene Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 64 Gambar 4.28. Spektrum GC-MS Senyawa β-Ocimen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 65 Gambar 4.29. Spektrum GC-MS Senyawa β-Ocimen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 66 Gambar 4.30. Pola Fragmentasi Senyawa L-Linalool 67 Gambar 4.31. Spektrum GC-MS Senyawa Kamfor Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 68 Gambar 4.32. Spektrum GC-MS Senyawa Aristolen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 69 Gambar 4.33. Pola Fragmentasi Senyawa Aristolen 70 Gambar 4.34. Spektrum GC-MS Senyawa Metil Isoeugenol Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 71 Gambar 4.35. Spektrum GC-MS Senyawa α-Asaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 72 Gambar 4.36. Spektrum GC-MS Senyawa β-Asaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 72 Gambar 4.37. Spektrum GC-MS Senyawa Euasaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 72 Gambar 4.38. Spektrum GC-MS Senyawa β-Ionon Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 73 Gambar 4.39. Spektrum GC-MS Senyawa β-Ionon Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 74 Gambar 4.40. Pola Fragmentasi Senyawa 2-Propanon,1-[dihidro-4-4-dimetil] 76 Gambar 4.41. Spektrum GC-MS Senyawa Aristolen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 76 Gambar 4.42. Spektrum GC-MS Senyawa Isokalamendiol Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 77 Gambar 4.43. Pola Fragmentasi Senyawa Isokalamendiol 77
DAFTAR GAMBAR
Gambar 2.1. Tanaman Jerangau 5
Gambar 2.2. Struktur α-Asaron dan β-Asaron 9
Gambar 2.3. Pembentukan Asam Mevalonat Sebagai Zat Antara Dalam
Biosintesis Terpenoid. 14
Gambar 2.4. Reaksi Biosintesa Terpenoid 15
Gambar 2.5. Biosintesa Fenil Propanoid 17
Gambar 4.1. Kromatogram Minyak Atsiri Dari Rimpang Jerangau Yang Diperoleh
Secara Hidrodestilasi Dengan Alat Stahl 37
Gambar 4.2. Kromatogram Minyak Atsiri Dari Rimpang Jerangau Yang Diperoleh Secara Hidrodestilasi Dengan Destilasi Ua 39 Gambar 4.3.Spektrum GC-MS Senyawa Kamfen Dari Minyak Atsiri Rimpang
Jerangau Dengan Menggunakan Alat 41
Gambar 4.4. Pola Fragmentasi Senyawa Kamfen 42
Gambar 4.5. Spektrum GC-MS Senyawa β-Ocimen Dari Minyak Atsiri Rimpang Jerangau Dengan Menggunakan Alat Stahl 43 Gambar 4.6. Pola Fragmentasi Senyawa β-Ocimen 44 Gambar 4.7. Spektrum GC-MS Senyawa Kamfor Dari Minyak Atsiri Rimpang
Jerangau Dengan Menggunakan Alat Stahl 45
Gambar 4.8. Pola Fragmentasi Senyawa Kamfor 46
Gambar 4.9. Spektrum GC-MS Senyawa Metil Isoeugenol Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 47 Gambar 4.10. Pola Fragmentasi Senyawa Metil Isoeugenol 48 Gambar 4.11. Struktur α-Asaron, β-Asaron, dan Euasaron 49 Gambar 4.12. Spektrum GC-MS Senyawa α-Asaron Dari Minyak Atsiri Rimpang
Jerangau Dengan Menggunakan Alat Stahl 50 Gambar 4.13. Spektrum GC-MS Senyawa β-Asaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 50 Gambar 4.14. Spektrum GC-MS Senyawa Euasaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 51 Gambar 4.15. Pola Fragmentasi Senyawa Asaron 51 Gambar 4.16. Pola Fragmentasi Senyawa Euasaron 52 Gambar 4.17. Spektrum GC-MS Senyawa Cis-Kalamen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 53 Gambar 4.18. Pola Fragmentasi Senyawa Cis-Kalamenen 54 Gambar 4.19. Spektrum GC-MS Senyawa Trans-Isoelemicin Dari
Minyak Atsiri Rimpang Jerangau Dengan Menggunakan Alat Stahl 55 Gambar 4.20. Pola Fragmentasi Senyawa Trans-Isoelemicin 57 Gambar 4.21. Spektrum GC-MS Senyawa β-Ionon Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Alat Stahl 58 Gambar 4.22. Pola Fragmentasi Senyawa β-Ionon 59 Gambar 4.23. Spektrum GC-MS Senyawa Aristolen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 62
Gambar 4.26. Pola Fragmentasi Senyawa α-Pinen 63
Gambar 4.27. Spektrum GC-MS Senyawa Kamfene Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 64 Gambar 4.28. Spektrum GC-MS Senyawa β-Ocimen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 65 Gambar 4.29. Spektrum GC-MS Senyawa β-Ocimen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 66 Gambar 4.30. Pola Fragmentasi Senyawa L-Linalool 67 Gambar 4.31. Spektrum GC-MS Senyawa Kamfor Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 68 Gambar 4.32. Spektrum GC-MS Senyawa Aristolen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 69 Gambar 4.33. Pola Fragmentasi Senyawa Aristolen 70 Gambar 4.34. Spektrum GC-MS Senyawa Metil Isoeugenol Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 71 Gambar 4.35. Spektrum GC-MS Senyawa α-Asaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 72 Gambar 4.36. Spektrum GC-MS Senyawa β-Asaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 72 Gambar 4.37. Spektrum GC-MS Senyawa Euasaron Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 72 Gambar 4.38. Spektrum GC-MS Senyawa β-Ionon Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 73 Gambar 4.39. Spektrum GC-MS Senyawa β-Ionon Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 74 Gambar 4.40. Pola Fragmentasi Senyawa 2-Propanon,1-[dihidro-4-4-dimetil] 76 Gambar 4.41. Spektrum GC-MS Senyawa Aristolen Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 76 Gambar 4.42. Spektrum GC-MS Senyawa Isokalamendiol Dari Minyak Atsiri
Rimpang Jerangau Dengan Menggunakan Destilasi Uap 77 Gambar 4.43. Pola Fragmentasi Senyawa Isokalamendiol 77
DAFTAR LAMPIRAN
Lampiran 1. Spektrum GC-MS dari Senyawa Kamfen dengan Alat Stahl 84 Lampiran 2. Spektrum GC-MS dari Senyawa β-Ocimen dengan Alat Stahl 85 Lampiran 3. Spektrum GC-MS dari Senyawa Kamfor dengan Alat Stahl 86 Lampiran 4. Spektrum GC-MS dari Senyawa Metil Isoeugenol dengan Alat Stahl 87 Lampiran 5. Spektrum GC-MS dari Senyawa Euasaron dengan Alat Stahl 88 Lampiran 6. Spektrum GC-MS dari Senyawa β-Asaron dengan Alat Stahl 89 Lampiran 7. Spektrum GC-MS dari Senyawa α-Asaron dengan Alat Stahl 90 Lampiran 8. Spektrum GC-MS dari Senyawa Cis-Kalamenen dengan Alat Stahl 91 Lampiran 9. Spektrum GC-MS dari Senyawa Trans-Isoelemicin dengan
Alat Stahl 92
Lampiran 10. Spektrum GC-MS dari Senyawa β-Ionon dengan Alat Stahl 93 Lampiran 11. Spektrum GC-MS dari Senyawa Aristolon dengan Alat Stahl 94 Lampiran 12. Spektrum GC-MS dari Senyawa α-Pinen dengan Destilasi Uap 95 Lampiran 13. Spektrum GC-MS dari Senyawa Kamfene dengan Destilasi Uap 96 Lampiran 14. Spektrum GC-MS dari Senyawa β-Ocimen dengan Destilasi Uap 97 Lampiran 15. Spektrum GC-MS dari Senyawa Linalool dengan Destilasi Uap 98 Lampiran 16. Spektrum GC-MS dari Senyawa Kamfor dengan Destilasi Uap 99 Lampiran 17. Spektrum GC-MS dari Senyawa Aristolen dengan Destilasi Uap 100 Lampiran 18. Spektrum GC-MS dari Senyawa Metil Isoeugenoldengan
Destilasi Uap 101
Lampiran 19. Spektrum GC-MS dari Senyawa Euasaron dengan Destilasi Uap 102 Lampiran 20. Spektrum GC-MS dari Senyawa α-Asaron dengan Destilasi Uap 103 Lampiran 21. Spektrum GC-MS dari Senyawa β-Asaron dengan Destilasi Uap 104 Lampiran 22. Spektrum GC-MS dari Senyawa β-Ionon dengan Destilasi Uap 105 Lampiran 23. Spektrum GC-MS dari Senyawa
2-Propanon,1-[dihidro-4-4-dimetil] dengan Destilasi Uap 106 Lampiran 24. Spektrum GC-MS dari Senyawa Aristolon dengan Destilasi Uap 107 Lampiran 25. Spektrum GC-MS dari Senyawa Isokalamendiol dengan Destilasi
Uap 108
Lampiran 26. Gambar alat Stahl 109
DAFTAR SINGKATAN
IPP = Isopentenil Piroposfat DMAPP = Dimetil Alil Piroposfat GPP = Geranil Piroposfat FPP = Farnesil Piroposfat
GGPP = Geranil-Geranil Piroposfat
DAFTAR TABEL
Tabel 2.1. Komposisi Minyak Atsiri Jerangau 8
Tabel 4.1. Hasil Isolasi Minyak Atsiri Melalui Hidrodestilasi 36 Tabel 4.2. Hasil Isolasi Minyak Atsiri Melalui Destilasi Uap 37 Tabel 4.3. Komponen Senyawa Minyak Atsiri Pada Rimpang Jerangau Yang
Diperoleh Melalui Metode Hidrodestilasi Menggunakan
Alat Stahl 38
Tabel 4.4. Komponen Senyawa Minyak Atsiri Pada Rimpang Jerangau
ABSTRAK
Telah dilakukan studi perbandingan komposisi minyak atsiri dari rimpang jerangau yang diperoleh dari hasil isolasi menggunakan metode hidrodestilasi dan destilasi uap air. Minyak atsiri yang dihasilkan dengan menggunakan metode hidrodestilasi maupun destilasi uap digunakan rimpang jerangau yang basah. Selanjutnya minyak atsiri yang diperoleh dianalisis komposisinya dengan menggunakan GC-MS. Melalui metode hidrodestilasi, diperoleh rendemen minyak atsiri sebanyak 0,325% v/w, yang terdiri dari 13 jenis senyawa dimana diantaranya sebanyak 11 senyawa yang dapat
diidentifikasi, yaitu : Kamfen (1,87%), β-Ocimen (1,42%), Kamfor (1,12%), Metil Isoeugenol (12,97%), Euasaron (1,87%), Asaron (60,34%), Cis-Calamenen (1,75%), Trans-Isoelemicin (1,14%), β-Ionon (1,97%) dan Aristolon (2,43%). Selanjutnya melalui metode destilasi uap diperoleh rendemen minyak atsiri sebanyak 0,35% v/w, yang terdiri dari 18 jenis senyawa dimana sebanyak 14 senyawa yang dapat
diidentifikasi, yaitu : α-Pinen (0,37%), Kamfen (1,69%), β-Ocimen (1,33%), Linalool (0,45%), Kamfor (1,04%), Aristolen (0,17%), Metil Isoeugenol (14,91%), Euasaron
ANALYSIS GC – MS THE COMPONENT ESSENTIAL OILS FROM JERANGAU RHIZOMES (Acorus calamus ) RESULTED
WITH USING HYDRODISTILLATION COMPARATIED TO STEAM
DISTILLATION METHOD
ABSTRACT
It had been studied ratio the composistion essential oils from Jerangau rhizomes obtained from isolation using the method of hidrodistillation and steam distillation. Essential oils was yielded using hidrodistillation method and steam distilation with fresh rhizome. And then, composition of essential oils that yielded were analyzed using GC-MS. Through hydrodistilation method, essential oil yield obtained a number of 0,325%, v/w, which consists of 13 types compounds which include a total of 11
compounds that can be identified, there are : Camphene (1,87%), β-Ocimene (1,42%), Camphor (1,12%), Methyl Isoeugenol 12,97%), Euasarone (1,87%), Asarone (60,34%), Cis-Calamenene (1,75%), Trans-Isoelemicin (1,14%), β-Ionone (1,97%), and Aristolone (2,43%). And then, by steam distilations obtained essential oils a number of 0,35%, v/w, which consists of 18 types compounds which include a total
of 14 compounds that can be indetified, there are : α-Pinene (0,37%), Camphene
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Di Indonesia, bahan-bahan tanaman yang mengandung minyak atsiri sejak dulu telah digunakan secara turun temurun dalam ramuan obat-obatan tradisional. Sumber bahan-bahan tanaman tersebut dewasa ini digunakan untuk keperluan bahan pangan, bahan obat-obatan, cita rasa (penyedap), kosmetika, dan wangi- wangian (parfum). Berbagai tanaman dapat menghasilkan minyak atsiri yang merupakan minyak yang dapat menguap dan mengandung aroma atau wangi yang khas baik bersumber dari daun, batang, bunga maupun akar tumbuhan (Guenther, 1987).
Minyak atsiri dikenal dengan nama minyak eteris atau minyak terbang merupakan bahan yang bersifat mudah menguap (volatile), mempunyai rasa getir, dan bau mirip tanaman asalnya yang diambil dari bagian- bagian tanaman seperti daun, buah, biji, bunga, akar, rimpang, kulit kayu, bahkan seluruh bagian tanaman. Minyak atsiri selain dihasilkan oleh tanaman, dapat juga sebagai bentuk dari hasil degradasi oleh enzim atau dibuat secara sintetis (Sastrohamidjojo, 1987).
Beberapa perusahaan farmasi sampai saat ini masih mengimpor calamus oil. Dalam industri parfum, calamus oil hanya akan dipakai untuk jenis-jenis produk parfum maupun kosmetika (Anonim I, 2006).
Penelitian tentang komponen minyak rimpang jerangau sudah pernah dilakukan oleh Dorna Sihite dimana mengetahui karakteristik dasar dari minyak atsiri jerangau dari bagian rimpang dan batang. Metode yang digunakan adalah metode uap dan air. Minyak atsiri yang diperoleh diuji kandungan sifat fisis dan kimianya (Sihite,2009).
Isolasi minyak atsiri dari bahan alam dapat bersumber dari akar, batang, dan daun. Menurut Dewan Atsiri Indonesia, proses produksi minyak atsiri dapat ditempuh melalui 3 cara, yaitu (1) pengempaan (pressing), (2) ekstraksi menggunakan pelarut
(solvent extraction), dan (3) penyulingan (distillation) (Anonimous II, 2009). Penyulingan merupakan metode yang paling banyak digunakan untuk mendapatkan minyak atsiri. Penyulingan dilakukan dengan mendidihkan bahan baku di dalam ketel suling sehingga terdapat uap yang diperlukan untuk memisahkan minyak atsiri dengan cara mengalirkan uap jenuh dari ketel pendidih air (boiler) ke dalam ketel penyulingan. Proses ini berdasarkan perbedaan titik uapnya dan dilakukan terhadap minyak yang tidak larut dalam air. Ada tiga sistem penyulingan minyak atsiri, yaitu penyulingan dengan air, penyulingan dengan air dan uap dan penyulingan dengan uap.
dibandingkan dengan metode penyulingan air karena dalam penyulingan air komponen minyak yang memiliki titik didih tinggi dan bersifat larut dalam air tidak dapat menguap secara sempurna sehingga banyak minyak yang hilang atau tidak tersuling (Sastrohamidjojo, 2004).
Berdasarkan hal diatas, penulis tertarik untuk membandingkan komposisi minyak atsiri yang diperoleh dari rimpang jerangau dengan menggunakan metode hidrodestilasi menggunakan alat stahl dan destilasi uap. Analisis komponen minyak atsiri dari tumbuhan Jerangau (Acorus calamus) dilakukan melalui pemeriksaan dengan GC-MS.
1.2. Permasalahan
1. Apakah minyak atsiri yang terdapat pada rimpang tanaman Jerangau (Acorus calamus) dapat diperoleh melalui hidrodestilasi atau dengan destilasi uap
2. Sejauh mana adanya perbedaan komponen kimia minyak atsiri yang diperoleh dari rimpang tanaman Jerangau (Acorus calamus) dapat diidentifikasi melalui analisis GC-MS bila dibandingkan antara hasil isolasi secara hidrodestilasi dengan destilasi uap.
1.3. Batasan Masalah
Penelitian ini dibatasi pada penentuan komponen minyak atsiri yang diperoleh dari metode hidrodestilasi dan destilasi uap, serta analisis kandungan atsirinya dengan menggunakan GC-MS.
1.4. Tujuan Penelitian
1. Untuk mendapatkan minyak atsiri dari rimpang tanaman Jerangau (Acorus calamus) secara hidrodestilasi atau dengan destilasi uap.
3. Untuk mrengetahui perbedaan komposisi senyawa dalam minyak atsiri yang diperoleh melalui isolasi secara hidrodestilasi dengan destilasi uap
1.5. Manfaat Penelitian
Penelitian ini diharapkan dapat menambah informasi tentang tanaman penghasil minyak atsiri sebagai hasil hutan bukan kayu dan mengenai komponen kimia minyak atsiri jerangau yang kemudian dapat diaplikasikan dalam industri oleh masyarakat.
1.6. Lokasi Penelitian
Penelitian untuk hidrodestilasi dan destilasi uap dilakukan di Laboratorium Kimia Organik FMIPA USU Medan dan analisis GC-MS dilakukan di Laboratorium Kimia Organik FMIPA UGM Yogyakarta.
1.7. Metodologi Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1. Tanaman Jerangau (Acorus calamus)
Jerangau merupakan tumbuhan spora air yang banyak dijumpai di kawasan tepi sungai. Tumbuhan ini berasal dari Eropa, Asia dan Amerika. Di Indonesia didapati tumbuh liar di hutan-hutan.
Taksonomi Tanaman Jerangau
Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Liliopsida
Ordo : Acorales
Famili : Acoraceae
Genus : Acorus
Spesies : Acorus calamus
Nama Inggris : Sweet Flag, Sweet root, Calamus
Nama Indonesia : Dringo, Jerangau
Nama Daerah : Jeurunger (Aceh), Jerango (Gayo), Jarango
(Batak), Daringo (Sunda), Dlingo (Jawa Tengah),
jarianggu (Minangkabau), Ai wahu(Ambon) (Balakumbahan, 2010).
Jerangau mempunyai rimpang yang berbau wangi. Penampang rimpang sekitar 1 cm sampai dengan 1,5 cm, sementara akarnya sekitar 3 mm sampai dengan 4 mm. Rimpang beruas-ruas dengan tunas pada tiap ruas. Panjang rimpang tergantung pada umur tanaman serta tingkat kegemburan lumpur. Jerangau tumbuh merumpun membentuk satu koloni tanaman yang makin lama akan semakin melebar. Jerangau memiliki rimpang yang berbau wangi. Kulit rimpangnya berwarna coklat muda dengan warna putih di dalamnya. Daunnya tebal dan keras berbentuk seperti pedang. Apabila daunnya dikoyakkan akan menghasilkan bau yang wangi. Jerangau merupakan tanaman yang mengandung minyak atsiri. Tanaman jerangau berkembang biak melalui tunas rimpang yang akan tumbuh menjadi sulur serta individu tanaman baru (Anonim I, 2006).
berasal dari β-asaron, dimana senyawa ini dapat menyebabkan kanker hati.Perbedaan
jenis Jerangau yang digunakan akan membedakan jumlah β-asaron yang terdapat di dalamnya. Tingkat racun dan karsinogenitas pada hewan dapat ditunjukkan dengan berbagai penelitian dan Jerangau banyak digunakan pada obat-obatan tradisional (Staden, 2002). Konsentrasi rendah dari β-asaron tidak mempengaruhi metabolisme manusia, namun sangat mempengaruhi kehidupan metabolisme tikus dengan atau tanpa aktivasi, dimana β-asaron dapat merusak hati dan menyebabkan kanker. Kanker diidentifikasi sebagai Leiomyosarcomas. Kandungan β-asaron yang tinggi (5000 ppm atau 5%) menunjukkan tanda positif berbahaya bagi manusia
2.1.1. Manfaat Jerangau
Rimpang Acorus calamus berkhasiat sebagai obat penenang, lambung dan obat limpa. Jerangau juga dapat digunakan dalam ramuan yang digunakan oleh wanita selepas bersalin bersama cekur. Ia mempunyai ciri-ciri anti oksidan . Selain itu, jerangau juga bermanfaat sebagai perangsang, menghilangkan sakit, menambah nafsu makan, dan tonik. Kegunaannya cukup banyak terutama untuk meredakan radang. Contoh penyakit yang dapat diatasi jerangau antara lain bengkak, kudis, limpa bengkak, cacar sapi, mimisan, demam, dan lainnya (Anonim I, 2006).
2.1.2 Komposisi Minyak Atsiri Jerangau
Rimpang (kering angin) mengandung sekitar 27% minyak atsiri dengan komposisi seperti tabel 2.1
Tabel 2.1 Komposisi minyak atsiri jerangau menurut Agusta (2000)
No. Senyawa Kandungan (%)
1. Metil eugenol 1,25
2. α-Kurkuinina 1,05
3. α-Zingiberena 3,41
4. β-Farnesena 1,07
5. 7,11-Dimetil-3-metilena-1,6,10 dodekatriena 1,57 6. 4a,5,6,7,8a-Heksahidro-7α-isopropil 4αβ, 8αβ-dimetil
2(1H)-naftalena
0,59
7. β-Asaron 2,70
8. α-Asaron 79,70
9. Asaron 4,29
O CH3
O CH3
CH3 O
H3C
O CH3
O CH3
CH3
O H3C
α-Asaron β-Asaron
Gambar 2.2. Struktur α-Asaron dan β-Asaron
Beberapa jenis minyak atsiri dikenal dapat meningkatkan aktivitas mental penggunanya atau memiliki aktivitas sebagai psikoaktif. Minyak atsiri dari Jerangau memiliki kandungan asaron berikut dua isomer alpha dan beta yang sangat tinggi (sekitar 85%). Asaron salah satu prazat alami dalam sintesis obat Psychedelic TMA-2 (Trimetoksiamphetamin) (Agusta, 2000).
2.2. Minyak Atsiri
Minyak atsiri dihasilkan dari bagian jaringan tanaman tertentu seperti akar, batang, kulit, daun, buah, atau biji. Sifat minyak atsiri yang menonjol antara lain mudah menguap pada suhu kamar, mempunyai rasa getir, berbau wangi sesuai aroma tanaman yang menghasilkannya dan umumnya larut dalam pelarut organik (Lutony dan Rahmayati, 2000).
Minyak atsiri dihasilkan di dalam tubuh tanaman dan disimpan dalam kelenjar minyak atsiri. Kelenjar minyak atsiri dalam tanaman disebut kelenjar internal dan di luar tanaman disebut dengan kelenjar eksternal (Koensoemardiyah, 2010).
1. Minyak atsiri yang dengan mudah dapat dipisahkan menjadi komponen- komponen atau penyusun murninya. Komponen-komponen ini dapat menjadi bahan dasar untuk diproses menjadi produk- produk lain, contoh : minyak sereh, minyak daun cengkeh, minyak permai, dan minyak terpentin.
2. Minyak atsiri yang sukar dipisahkan menjadi komponen murninya, contoh : minyak akar wangi, minyak nilam, dan minyak kenanga. Biasanya minyak atsiri tersebut langsung dapat digunakan tanpa diisolasi komponen-komponennya sebagai pewangi berbagai produk (Sastrohamidjojo, 2004).
Minyak atsiri mengandung campuran pelik dari bahan-bahan hayati, termasuk didalamnya adalah aldehid, alkohol, ester, keton, dan terpen. Bahan-bahan ini kemungkinan merupakan sisa metabolisme tumbuh-tumbuhan yang digunakan untuk menjalankan peran ganda, seperti menarik serangga perusak. Minyak atsiri dari beraneka ragam tanaman menghasilkan aroma yang berbeda, bahkan satu jenis tumbuhan yang sama bila ditanam di tempat yang berlainan mampu menghasilkan aroma yang berbeda. Iklim, keberadaan tanah, sinar matahari, cara pengolahan tidak hanya mempengaruhi rendemen minyak atsiri tetapi berpengaruh pula pada aromanya (Harris, 1990).
Minyak atsiri merupakan salah satu komoditas ekspor agroindustri potensial yang dapat menjadi andalan bagi Indonesia untuk mendapatkan devisa. Data statistik ekspor-impor dunia menunjukkan bahwa konsumsi minyak atsiri dan turunannya naik sekitar 10% dari tahun ke tahun. Kenaikan tersebut didorong oleh perkembangan kebutuhan untuk industri food flavouring, indutrsi kosmetik dan wewangian (Anonim II, 2009).
2.2.1. Komposisi Kimia Minyak Atsiri
Pada umumnya perbedaan komposisi minyak atsiri disebabkan perbedaan jenis tanaman penghasil, kondisi iklim, tanah tempat tumbuh, umur panenan, metode ekstraksi yang digunakan dan cara penyimpanan minyak.
Minyak atsiri biasanya terdiri dari berbagai campuran persenyawaan kimia yang terbentuk dari unsur karbon (C), Hidrogen (H), dan Oksigen (O). Pada umumnya komponen kimia minyak atsiri dibagai menjadi dua golongan, yaitu:
1. Hidrokarbon yang terutama terdiri dari persenyawaan terpen 2. Hidrokarbon teroksigenasi
A. Golongan Hidrokarbon
Persenyawaan yang termasuk golongan ini terbentuk dari unsur Karbon (C), dan Hidrogen (H). jenis Hidrokarbon yang terdapat dalam minyak atsiri sebagian besar terdiri dari monoterpen (unit isopren), sesquiterpen (3 unit isopren), diterpen (4 unit isopren), dan politerpen.
B. Golongan Hidrokarbon Teroksigenasi
Komponen kimia dari golongan ini terbentuk dari unsur Karbon (C), Hidrogen (H), dan Oksigen (O). persenyawaan yang termasuk dalam golongan ini adalah persenyawaan alkohol, aldehid, ester. Fenol. Ikatan Karbon yang terdapat dalam molekulnya dapat terdiri dari ikatan tunggal, ikatan rangkap dua dan ikatan rangkap tiga. Terpen mengandung ikatan tunggal dan ikatan rangkap dua. Senyawa terpen memiliki aroma kurang wangi, skar larut dalam alkohol encer dan jika disimpan dalam waktu lama akan membentuk resin. Golongan hidrokarbon teroksigenasi merupakan senyawa yang penting dalam minyak atsiri karena umumnya aroma yang lebih wangi. Fraksi terpen perlu dipisahkan untuk tujuan tertentu, misalnya untuk pembuatan parfum, sehingga didapatkan minyak atsiri yang bebas terpen (Ketaren, 1985).
karbon dan hidrogen atau karbon, hidrogen dan oksigen yang tidak bersifat aromatik ataupun bersifat aromatik. Senyawa-senyawa yang tidak bersifat aromatik biasanya termasuk ke dalam golongan senyawa terpenoid. Senyawa terpenoid dalam minyak atsiri terdiri dari senyawa dengan jumlah atom C berjumlah 10 atau disebut dengan monoterpen dan atom C yang berjumlah 15 atau disebut dengan sesquiterpen. Fraksi yang paling mudah menguap dari hasil destilasi fraksinasi biasanya terdiri dari senyawa-senyawa monoterpen dengan jumlah atom C berjumlah 10. Sedangkan fraksi yang mempunyai titik didih lebih tinggi biasanya senyawa-senyawa sesquiterpen.
Pada minyak atsiri yang bagian utamanya terpenoid, biasanya terpenoid itu terdapat pada fraksi minyak atsiri yang tersuling uap. Zat inilah penyebab wangi, harum atau bau yang khas pada banyak tumbuhan. Secara ekonomi senyawa tersebut penting sebagai dasar wewangian alam dan juga untuk rempah-rempah serta sebagai senyawa citarasa dalam industri makanan (Harborne, 1987).
2.2.2. Sumber Minyak Atsiri
Minyak atsiri merupakan salah satu akhir proses metabolisme sekunder dalam tumbuhan. Tumbuhan penghasil minyak atsiri antara lain termasuk famili Pinaceae, Labiatae, Compositae, Lauraceae, Myrtaceae, Rutaceae, Piperaceae, Zingiberaceae,
Umbelliferae, dan Gramineae. Minyak atsiri terdapat pada setiap bagian tumbuhan, yaitu di daun, bunga, buah, biji, batang, kulit, akar, dan rimpang (Ketaren, 1985).
2.2.3. Biosintesa Pembentukan Minyak Atsiri
Minyak atsiri pada umumnya mengandung persenyawaan terpena dalam jumlah yang besar, dimana terpena merupakan persenyawaan hidrokarbon tidak jenuh dan unit terkecil dalam molekulnya disebut dengan isoprene (C5H8) (Agusta,2000)
mengacu khusus ke hidrokarbon. Dengan kata lain, senyawa terpenoida dapat digambarkan sebagai sebuah terpena yang telah mengalami modifikasi, di mana kelompok-kelompok metil dipindahkan atau dihapus, atau ditambahkan atom oksigen. Sebaliknya, beberapa penulis menggunakan istilah "terpena" lebih luas untuk menyertakan terpenoida (Robinson, 1995).
Secara umum biosintesa terpenoida dengan terjadinya 3 reaksi dasar yaitu:
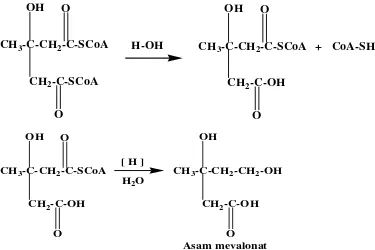
1. Pembentukan isoprena aktif berasal dari asam asetat melalui asam mevalonat. Asam asetat setelah diaktifkan oleh koenzim A (Ko-A) melakukan kondensasi jenis Claisen menghasilkan Asetoasetil Ko-A. Senyawa ini dengan Asetil Ko-A melakukan kondensasi jenis Aldol menghasilkan rantai karbon bercabang sebagaimana ditemukan pada asam mevalonat (Gambar 2.3)
CH3COOH Asam asetat
CoA-SH
CH3C-SHCoA
O
Asetil Koenzim A
CH3-C-CH2-C-SCoA
O O
CH3-C-SCoA O
CH3-C-SCoA O
+
Asetoasetil Ko-A
+ CoA-SH
CH3-C-CH2-C-SCoA
O O
Asetoasetil Ko-A
+ CH3-C-SCoA O
Asetil Ko-A
CH3-C-CH2-C-SCoA
CH2-C-SCoA
CH3-C-CH2-C-SCoA
CH2-C-SCoA
O
OH O
H-OH CH3-C-CH2-C-SCoA
O
OH O
CH2-C-OH
+ CoA-SH
CH3-C-CH2-C-SCoA
O OH O
CH2-C-OH
[ H ]
H2O
O OH
CH2-C-OH CH3-C-CH2-CH2-OH
[image:32.595.110.485.85.335.2]Asam mevalonat
Gambar 2.3. Pembentukan asam mevalonat sebagai zat antara dalam biosintesis terpenoid
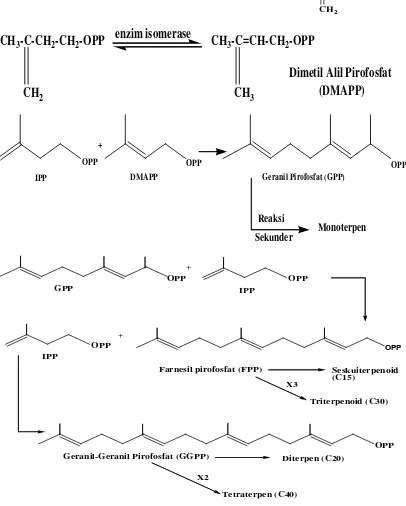
2. Penggabungan kepala dan ekor dua unit isoprena akan membentuk mono-, seskui-, di-, tri-, tetra-, dan poli- terpenoida.
CH3-C-CH2-C-O
-O OP
CH2-CH2-OPP
O OH
CH2-C-OH
CH3-C-CH2-CH2-OH
Asam mevalonat
ATP 3 tahap
dekarboksilasi CH
2=C-CH2-CH2-OPP
CH3
CH3-C-CH2-CH2-OPP
CH2
Isopentenil Pirofosfat (IPP)
CH
3-C-CH
2-CH
2-OPP
CH
2enzim isomerase
CH
3-C=CH-CH
2-OPP
CH
3Dimetil Alil Pirofosfat
(DMAPP)
OPP IPP + OPP DMAPP OPP Geranil Pirofosfat (GPP)Reaksi Sekunder Monoterpen GPP OPP + IPP OPP OPP
Farnesil pirofosfat (FPP) Seskuiterpenoid (C15) X3 Triterpenoid (C30) IPP OPP +
Geranil-Geranil Pirofosfat (GGPP)
OPP Diterpen (C20)
[image:33.595.110.516.206.712.2]Tetraterpen (C40) X2
3. Dalam pembentukan senyawa terpenoid, GPP, FPP, dan GGPP satu persatu hanya melibatkan beberapa jenis reaksi sekunder. Reaksi-reaksi sekunder ini lazimnya adalah hidrolisa, siklisasi, oksidasi, reduksi, dan reaksi-reaksi spontan yang dapat berlangsung dengan mudah dalam suasana netral dan suhu kamar seperti isomerisasi, dehidrasi, dekarboksilasi, dan sebagainya (Pinder, 1960).
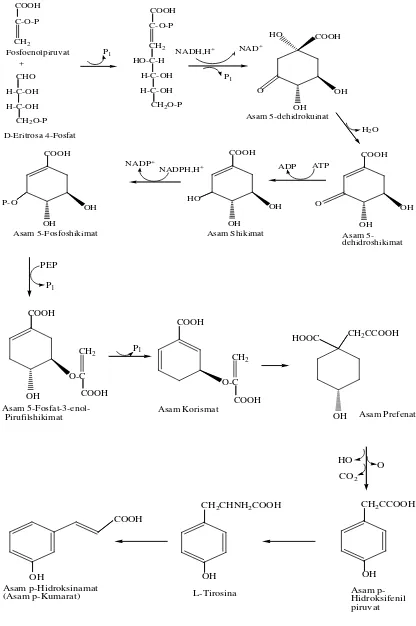
Kelompok komponen besar lainnya dalam minyak atsiri adalah senyawa fenilpropena(C6-C3) sebagai rantai samping. Kelompok senyawa ini dalam minyak
COOH C-O-P CH2 Fosfoenolpiruvat + CHO H-C-OH
CH2O-P
H-C-OH
D-Eritrosa 4-Fosfat
P1
HO-C-H H-C-OH
CH2O-P
H-C-OH CH2
C-O-P COOH
NADH,H+ NAD+
P1 O OH OH COOH HO OH OH COOH O Asam 5-dehidrokuinat Asam 5-dehidroshikimat
H2O
OH OH COOH Asam Shikimat HO NADP+
NADPH,H+ ADP ATP
OH OH COOH Asam 5-Fosfoshikimat P-O PEP P1 OH O-C COOH Asam Pirufilshikimat CH2 COOH P1 O-C COOH Asam Korismat CH2 COOH
CH2CCOOH
HOOC
OH Asam Prefenat
HO CO2
O
CH2CCOOH
OH Asam p-Hidroksifenil piruvat CH2CHNH2COOH
[image:35.595.107.523.84.710.2]OH L-Tirosina COOH Asam p-Hidroksinamat (Asam p-Kumarat) OH
2.2.4. Kegunaan Minyak Atsiri
Menurut Rochim (2009), kegunaan minyak atsiri sangat luas dan spesifik, khususnya dalam berbagai bidang industri, seperti :
1. Farmasi dan Kesehatan
Bidang kesehatan, minyak atsiri digunakan sebagai aroma terapi. Aroma yang muncul dari minyak atsiri dapat menimbulkan efek menenangkan yang pada akhirnya dapat digunakan sebagai terapi psikis. Minyak atsiri ini selain memberikan aroma wangi yang menyenangkan juga dapat membantu pencernaan dengan merangsang sistem saraf, sehingga akan meningkatkan sekresi getah lambung yang mengandung enzim hanya oleh stimulus aroma dan rasa bahan pangan. Selain itu juga dapat merangsang keluar cairan getah sehingga rongga mulut dan lambung menjadi basah.
Beberapa jenis minyak atsiri digunakan sebagai bahan antiseptik internal atau eksternal, bahan analgesik, haelitik atau sebagai antizimatik sebagai sedatif dan stimulan untuk obat sakit perut. Minyak atsiri mempunyai sifat membius atau merangsang. Dengan memanfaatkan aroma terapi, psikis dibuat lebih tenang dan rileks. Selain menenangkan, zat aktif dalam minyak atsiri juga sangat membantu proses penyembuhan karena memiliki sifat anti radang, antifungi, antiserangga, afrodisiak, anti-inflamasi, antiflogistik dan dekongestan.
2. Kosmetik
3. Makanan
Pada makanan, minyak atsiri ditambahkan sebagai penambah aroma dan penambah rasa. Dalam pembuatan makanan olahan, tak jarang bahan yang digunakan hanya sedikit menggunakan bahan utama. Oleh sebab itu, kehadiran minyak atsiri dapat memperkuat aroma dan rasa sehingga produk makanan serasa memiliki cita rasa yang tak kalah dengan produk aslinya. Minyak atsiri merupakan sumber dari aroma kimia alami yang dapat digunakan sebagai komponen flavor dan fragrance alami dan sebagai sumber yang penting dari struktur stereospesifik enansiomer murni yang biosintesisnya lebih murah dibandingkan dengan proses sintesis.
2.3. Rendemen
Rendemen adalah perbandingan antara output dengan input dinyatakan dalam persen. Jumlah minyak yang menguap bersama-sama air ditentukan oleh tiga faktor, yaitu besarnya tekanan uap yang dipakai, berat molekul dari masing- masing komponen dalam minyak dan kecepatan minyak yang keluar dari bahan (Maulana, 2007).
2.3.1. Faktor Yang Mempengaruhi Rendemen Minyak Atsiri
Ada perlakuan yang harus diperhatikan terhadap bahan tanaman yang mengandung minyak atsiri, yaitu :
1. Perajangan/ Pemotongan
Minyak atsiri dalam tanaman aromatik dikelilingi oleh kelenjar minyak pembuluh- pembuluh, kantung minyak atau rambut glandular. Minyak atsiri hanya dapat diekstraksi apabila uap air berhasil melalui jaringan tanaman dan mendesaknya permukaan.
Proses ini adalah peristiwa hidrodifusi dan prosesnya berlangsung lambat bila tanaman dibiarkan dalam keadaan utuh. Oleh karena itu dalam proses penyulingan terlebih dahulu dilakukan perajangan yang bertujuan agar kelenjar minyak dapat terbuka sebanyak mungkin.
2. Penyimpanan Bahan Tanaman
Tempat penyimpanan bahan tanaman sebelum perajangan juga mempengaruhi penyusutan minyak atsiri, namun pengaruhnya tidak begitu besar seperti pada perajangan. Penyimpanan ini dilakukan apabila tidak langsung dilakukan proses penyulingan. Jika harus disimpan sebelum diproses maka penyimpanan dilakukan pada udara kering yang bersuhu rendah dan bebas terhadap sirkulasi udara, jika mungkin disimpan pada ruangan ber-AC
3. Kehilangan Minyak Atsiri Dari Bahan Tanaman Sebelum Penyulingan
Minyak atsiri yang terdapat dalam tanaman sering hilang oleh proses pengeringan setelah panen. Beberapa macam tanaman yang masih segar dengan kadar air tinggi akan kehilangan sebagian minyak atsiri selama pengeringan udara, sedangkan pada beberapa jenis yang lain besarnya minyak yang hilang relative kecil. Kehilangan minyak terutama disebabkan oleh penguapan dan oksidasi.
4. Perubahan Sifat Fisika-Kimia Minyak Atsiri Tanaman Selama Pengeringan
membran sel berangsur-angsur akan pecah, cairan bebas melakukan penetrasi dari satu sel ke sel yang lain hingga membentuk senyawa-senyawa yang mudah menguap (Guenther, 1987).
2.4. Cara Memperoleh Minyak Atsiri
Minyak atsiri dapat diproduksi melalui beberapa metode, namun sebagian besar minyak atsiri diperoleh melalui penyulingan, ekstraksi dengan pelarut menguap
(solvent extraction), ekstraksi dengan lemak dingin (enfleurasi), ekstraksi dengan lemak panas (maserasi), dan pengepresan (pressing).
2.4.1. Penyulingan
Dalam tanaman minyak atsiri, terdapat dalam kelenjar minyak atau pada bulu-bulu kelenjar. Minyak atsiri hanya akan keluar setelah uap menerobos jaringan-jaringan tanaman yang terdapat dalam permukaan. Biasanya proses difusi berlangsung sangat lambat, maka untuk mempercepat proses difusi sebelum melakukan penyulingan terlebih dahulu bahan tanaman harus diperkecil dengan cara dipotong-potong atau digerus. Pemotongan atau penggerusan merupakan upaya untuk mengurangi ketebalan bahan hingga difusi terjadi. Peningkatan difusi akan mempercepat penguapan dan penyulingan minyak atsiri. Peristiwa terpenting yang terjadi dalam proses penyulingan dengan metode hidrodestilasi ini adalah terjadinya difusi minyak atsiri dan air panas melalui membran bahan yang disuling, terjadinya hidrolisa terhadap beberapa komponen minyak atsiri dan terjadinya dekomposisi yang disebabkan oleh panas.
Penyulingan dapat didefenisikan sebagai pemisahan komponen-komponen suatu campuran dari dua jenis cairan atau lebih berdasarkan perbedaan tekanan uap dari masing- masing zat tersebut. Dalam industri minyak atsiri dikenal 3 macam metode penyulingan, yaitu :
a. Penyulingan dengan air (Water distillation)
Tidak ada perbedaan yang mendasar dari ketiga jenis penyulingan diatas. Tetapi bagaimanapun juga perbedaan ini sangat berarti, karena tergantung pada metoda yang dipakai dan reaksi-reaksi kimia yang terjadi selama berlangsungnya penyulingan.
a. Penyulingan dengan Air
Pada metode ini bahan yang akan disuling kontak langsung dengan air mendidih. Bahan tersebut mengapung diatas air atau terendam secara sempurna tergantung dari bobot jenis dan jumlah bahan yang akan disuling. Air yang dipanaskan dengan metode pemanasan yang biasa dilakukan yaitu dengan panas langsung, mantel uap, pipa uap melingkar tertutup. Ciri khas metode ini ialah kontak langsung antara bahan dengan air mendidih. Oleh sebab itu sering disebut dengan penyulingan langsung. Beberapa jenis bahan (misalnya bubuk buah badam,bunga mawar, dan orange blossoms) harus disuling dengan metode ini.
b. Penyulingan dengan Air dan Uap
Pada metode penyulingan ini bahan olah diletakkan di atas rak-rak atau saringan berlubang. Ketel suling diisi dengan air sampai permukaan air berada tidak jauh dibawah saringan. Air dapat dipanaskan dengan berbagai cara yaitu dengan uap jenuh yang basah dan bertekanan rendah. Ciri khas metode ini adalah uap selalu dalam keadaan basah, jenuh dan tidak terlalu panas, bahan yang disuling hanya berhubungan dengan uap dan tidak dengan air panas. Hal-hal yang perlu diperhatikan adalah ukuran bahan olah harus seragam dan ruang antar bahan yang cukup, agar uap dapat berpenetrasi, pengisian dan kepadatan bahan harus merata di dalam ketel sehingga uap dapat menembus bahan tersebut secara merata dan menyeluruh.
c. Penyulingan dengan Uap
penyulingan berlangsung, suhu ketel diawasi agar jangan melampaui suhu ’’superheated steam”. Hal ini bertujuan untuk mendapatkan rendemen minyak yang lebih besar dan menghindarkan pengeringan bahan yang disuling (Ketaren, 1985).
2.4.1.1. Kelebihan dan Kekurangan Metode Penyulingan
1. Penyulingan dengan air
Meskipun proses pengerjaannya sangat mudah dan dapat menyuling minyak dari bahan yang berbentuk bubuk dan bunga-bungaan yang mudah membentuk gumpalan jika kena panas, tetapi penyulingan ini menyebabkan banyaknya rendemen yang hilang (tidak tersuling) dan terjadi pula penurunan mutu minyak yang diperoleh. Komponen yang bertitik didih tinggi dan bersifat larut dalam air tidak dapat menguap sempurna, sehingga minyak yang tersuling mengandung komponen yang tidak lengkap.Selain itu, juga menyebabkan terjadinya pengasaman (oksidasi) serta persenyawaan zat ester yang dikandung dengan air dan timbulnya berbagai hasil samping yang tidak dikhendaki. Penyulingan air memerlukan ketel suling yang lebih besar, ruangan yang lebih luas dan jumlah bahan bakar yang lebih banyak.
2. Penyulingan dengan uap
Proses produksi berlangsung lebih cepat karena ketel uap melayani beberapa buah ketel penyulingan yang dipasang seri. Mutu dan rendemen minyak yang dihasilkan sangat baik karena biasanya proses hidrolisa yang terjadi relatif kecil. Namun, proses ini memerlukan konstruksi ketel yang lebih kuat, alat-alat pengaman yang lebih baik dan lebih sempurna, serta biaya yang diperlukan pun lebih mahal. Penyulinan ini tidak baik dilakukian terhadap bahan yang mengandung minyak atsiri yang mudah rusak oleh pemanasan dan air.
3. Penyulingan dengan air dan uap
relatif singkat, rendemen minyak lebih besar dan mutunya lebih baik jika dibandingkan dengan minyak hasil penyulingan air, dan bahan yang disuling tidak dapat menjadi gosong. Kelemahan sistem ini adalah karena uap yang dibutuhkan cukup besar dan waktu penyulingan lebih lama. Dalam proses ini, sejumlah besar uap akan mengembun dalam jaringan tanaman, sehingga bahan bertambah basah, dan mengalami aglutinasi. Metode ini tidak dapat menghasilkan minyak dengan cepat karena tekanan uap yang dihasilkan relatif rendah. Untuk mendapatkan rendemen yang lebih tinggi diperlukan waktu penyulingan yang lama (Lutony dan Rahmayati, 2002).
2.4.1.2. Pengaruh Metode Penyulingan Terhadap Mutu Minyak Atsiri
Mutu maupun sifat-sifat fisika-kimia minyak atsiri dipengaruhi oleh keadaan bahan (umur, keadaan kering atau segar) dan cara penyulingan yang dilakukan. Faktor yang mempengaruhi yaitu metode penyulingan, tingkat perajangan bahan, jumlah bahan, lamanya penyulingan, besarnya tekanan yang dipakai, mutu uap, perlakuan pada air suling. Antara penyulingan air dan penyulingan uap perbedaan ini cukup besar. Jika bahan olah tidak cukup dirajang, maka komponen minyak atsiri yang bertitik didih tinggi tidak dapat diekstrak sebagian kecil dengan penyulingan air. Bahkan penyulingan dengan air terhadap daun menghasilkan komponen mudah menguap dan komponen bertitik didih tinggi yang tidak lengkap (Guenther, 1987).
2.4.2 Ekstraksi Dengan Pelarut Menguap
Dengan demikian sudah terjadi pemisahan dan eter dapat dibebaskan dengan penguapan.
Pelarut yang ideal harus memenuhi syarat sebagai berikut :
a. Harus dapat melarutkan semua zat wangi bunga dengan cepat dan sempurna, dan sempurna, dan sedikit mungkin melarutkan bahan seperti: lilin, pigmen, dan senyawa albumin
b. Harus mempunyai titik didih yang cukup rendah agar pelarut mudah diuapkan tanpa menggunakan suhu tinggi
c. Pelarut tidak boleh larut dalam air
d. Pelarut harus bersifat inert, sehingga tidak bereaksi dengan komponen minyak e. Pelarut harus mempunyai titik didih yang seragam dan jika diuapkan tidak
akan tertinggal dalam minyak
f. Harga pelarut harus serendah mungkin dan tidak mudah terbakar
Eter merupakan pelarut yang berkemampuan tinggi untuk melarutkan hidrokarbon dan senyawa yang mengandung oksigen. Eter mempunyai sifat menguap yang tinggi (titik didih 34,6oC) sehingga mudah dihilangkan dari suatu ekstrak, pada temperature rendah. Eter digunakan untuk isolasi produk alam yang terdapat pada binatang dan jaringan tumbuhan yang mempunyai kandungan air tinggi. Walaupun lebih sering digunakan untuk penelitian, namun eter dihindari penggunaannya di dunia industri karena bahaya kebakaran, kelarutannya dalam air, sulitnya diperoleh kembali karena mudahnya menguap dan pada keadaan kering mungkin meledak. Pelarut alternatif yang biasa digunakan adalah petroleum eter, ligroin, benzene, karbon tetra klorida, kloroform, diklorometana, 1-Butanol (Williamson,1987).
2.4.3. Ekstraksi Dengan Lemak Dingin (Enfleurasi)
diekstraksi dari lemak dengan menggunakan alkohol dan selanjutnya alkohol dipisahkan.
Berdasarkan pengalaman selama bertahun-tahun dapat dibuktikan bahwa campuran satu bagian lemak sapi dan dua bagian Lard (lemak babi) sangat baik untuk enfleurasi.
Banyak jenis bahan lain yang dapat digunakan sebagai absorben pada proses enfleurasi, tetapi belum ada yang diterapkan secara komersial. Keberhasilan proses enfleurasi tergantung pada kualitas lemak yang digunakan dan ketelitian serta keterampilan dalam mempersiapkan lemak. Lemak yang digunakan harus tidak berbau dan mempunyai konsistensi tertentu. Jika lemak terlalu keras kontak antara lemak dan minyak akan sulit sehingga akan mengurangi daya absorpsi dan rendemen minyak bunga yang dihasilkan (Guenther, 1987).
2.4.4. Pengepresan
Metode pengepresan merupakan metode penarikan minyak atsiri dengan pemberian tekanan untuk mengepres sampel, misal kulit buah sehingga minyak yang terkandung di dalamnya akan keluar. Cara ini sangat sederhana dan dalam hal tertentu memberikan hasil yang memuaskan seperti aroma yang alami.
2.5. Analisis Komponen Minyak Atsiri
Analisis dan karakterisasi komponen minyak atsiri merupakan masalah yang rumit karena kebanyakan mengandung campuran senyawa dengan berbagai tipe, ditambah dengan sifatnya yang mudah menguap pada suhu kamar. Kendala yang dihadapi pada saat menganalisis komponen minyak atsiri adalah hilangnya sebagian komponen selama proses preparative dan berlangsungnya proses analisis sejak ditemukannya kromatografi gas, kendala dalam analisis komponen minyak atsiri ini mulai dapat diatasi, efek penguapan dapat dihindari bahkan dihilangkan sama sekali. Perkembangan teknologi instrumentasi yang sangat pesat akhirnya dapat melahirkan gabungan dari dua system dengan prinsip dasar yang berbeda dan saling melengkapi yaitu gabungan dari kromatografi gas dan spektrometri massa (GC-MS).
Pada GC-MS, kedua alat dihubungkan dengan suatu interfase. Kromatografi gas disini berfungsi sebagai alat pemisah berbagai komponen campuran dalam sample, sedangkan spektrometri massa berfungsi untuk mendeteksi masing-masing molekul komponen yang telah dipisahkan pada system kromatografi gas. Analisis GC-MS merupakan metode yang cepat dan akurat untuk memisahkan campuran yang rumit (Agusta, 2000).
2.5.1 Kromatografi Gas
Kromatografi gas adalah suatu proses dengan mana suatu campuran menjadi komponen-komponennya oleh fase gas yang bergerak melewati suatu lapisan serapan yang stasioner (Vogel,1994). Dalam kromatografi gas, fase bergeraknya adalah gas dan zat terlarut terpisah sebagai uap. Pemisahan tercapai dengan partisi sampel antara fase bergerak dan fase diam berupa cairan dengan titik didih tinggi (tidak mudah menguap) yang terikat pada zat padat penunjangnya (Khopkar, 2003).
pada kondisi yang tepat. Waktu tambat adalah waktu yang menunjukkan berapa lama suatu senyawa tertahan dalam kolom. Kekurangan alat ini adalah tidak mudah memisahkan campuran dalam jumlah yang besar (Mc Nair, 1988).
Waktu yang menunjukkan berapa lama suatu senyawa tertahan di kolom disebut waktu tambat, yang diukur mulai saat penyuntikan sampai terjadi elusi (Gritter, 1991).
Hampir setiap campuran kimia, mulai dari bobot molekul rendah sampai tinggi, dapat dipisahkan menjadi komponen-komponennya dengan beberapa metode kromatografi. Sifat- sifat yang harus dimiliki cuplikan agar dapat dipisahkan dengan kromatografi, antara lain :
1. Kecenderungan molekul untuk melarut dalam cairan (kelarutan)
2. Kecenderungan molekul untuk melarut pada permukaan serbuk halus (adsorpsi) 3. Kecenderungan molekul untuk menguap atau berubah ke keadaan uap (keatsirian)
(Willet, 1987)
2.5.2. Spektrometri Massa
Penggunaan MS luas dalam kimia organik sejak 1960. Ada dua alasan utama penggunaan MS, pertama telah ditemukan alat yang dapat menguapkan hamper semua senyawa organik dan mengionkan uap; kedua, fragmen bermuatan yang dihasilkan dari ion molekul dapat dihubungkan dengan struktur molekulnya (Sudjadi, 1983).
Spektrometer massa menembaki bahan yang sedang diteliti dengan berkas elektron dan secara kuantitatif mencatat hasilnya sebagai suatu spektrum fragmen ion positif. Terpisahnya fragmen ion positif didasarkan pada massanya. Spektrometer massa biasa diambil pada energi berkas elektron sebesar 70 elektron volt. Kejadian tersederhana adalah tercampaknya satu elektron dari molekul dalam fasa gas oleh sebuah elektron dalam berkas elektron dan membentuk suatu kation radikal (M+.)
Satu proses yang disebabkan oleh tabrakan electron pada kamar pengion spektrometer massa adalah ionisasi dari molekul yang berupa uap dengan kehilangan satu elektron dan terbentuk ion molekul bermuatan positif, karena molekul senyawa organic mempunyai elektron berjumlah genap maka proses pelepasan satu electron menghasilkan ion radikal yang mengandung satu elektron tidak berpasangan.
M -e M+.
Proses lain, molekul yang berupa uap tersebut menangkap sebuah electron membentuk ion radikal bermuatan negatif dengan kemudian terjadi jauh lebih kecil (10-2) daripada ion radikal bermuatan positif (Sudjadi, 1985).
BAB 3
METODE PENELITIAN
3.1.Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah :
- Alat Stahl
- Alat Destilasi Uap
- Kompor Minyak hock
- Labu Alas pyrex
- Hot Plate cimarec 2
- Corong Pisah pyrex
- Labu Didih pyrex
- Beaker Glass pyrex
- Panci Aluminium - Aluminium Foil - Botol Aquadest - Statif dan Klem - Botol Vial
- Neraca Ohaus
- Syring - Teflon - Pipet Tetes - Pisau
- Kertas saring
- Spektrofotometer GC-MS Shimadzu
3.2. Bahan
Bahan-bahan yang digunakan dalam penelitian ini, antara lain :
- Rimpang Jerangau
- Natrium Sulfat Anhidrat p.a.(E.Merck)
- Natrium Klorida p.a.(E.Merck)
- Aquadest
- Dietil eter p.a.(E.Merck)
3.3. Prosedur Penelitian 3.3.1. Penyediaan Sampel
Bahan yang digunakan dalam penelitian adalah rimpang jerangau yang diperoleh dari desa Penen Kabupaten Deli Serdang Provinsi Sumatera Utara. Rimpang jerangau dibersihkan dan diperkecil ukuran dan ketebalannya dengan cara dirajang. Rimpang yang telah dirajang dibagi dua dengan berat yang sama.
3.3.2. Penyulingan Rimpang Jerangau
a. Penyulingan dengan menggunakan Alat Stahl (Hidrodestilasi)
Sebanyak 400 gram rimpang jerangau yang telah dirajang dimasukkan ke dalam labu Stahl volume 1 Liter. Kemudian ditambahkan air hingga bahan tersebut terendam. Dirangkai alat Stahl, didestilasi hingga keluar uap air bersama minyak. Lapisan minyak bagian atas didekantasi dengan menggunakan syring dan dimasukkan ke dalam botol vial I. Lapisan bawah dijenuhkan dengan NaCl dan ditambahkan dietil eter lalu diekstraksi. Lapisan atas yang diperoleh ditampung,kemudian dikeringkan dengan Na2SO4 anhidrous secukupnya, lalu disaring dan diuapkan eternya. Minyak
b. Penyulingan dengan Uap
Sebanyak 400 gram rimpang jerangau yang telah dirajang dimasukkan ke dalam labu didih. Dirangkai alat destilasi uap. Air pada ketel dipanaskan hingga menghasilkan uap yang kemudian masuk kedalam labu yang berisi jerangau lalu uap akan terkondensasi pada kondensor dan menghasilkan campuran air dan minyak sebagai destilat. Destilat ditampung pada corong pisah dan destilasi diakhiri setelah destilat yang keluar jernih. Lapisan atas pada corong pisah ditampung dan dimasukkan kedalam botol vial I. Lapisan bawahnya dijenuhkan dengan NaCl dan ditambahkan dietil eter lalu diekstraksi. Lapisan atas yang diperoleh ditampung, kemudian dikeringkan dengan Na2SO4 anhidrous secukupnya, lalu disaring dan diuapkan
eternya. Minyak yang diperoleh dimasukkan ke dalam botol vial minyak atsiri sebelumnya. Hasil yang diperoleh dianalisis dengan GC-MS.
c. Analisa GC-MS
Cuplikan dimasukkan ke dalam gerbang suntik pada sebuah alat GC-MS. Selanjutnya kondisi disesuaikan dengan kondisi dibawah ini kemudian diamati kromatogram yang dihasilkan oleh recorder serta mass spectra masing-masing senyawa.
Kondisi alat GC-MS, yaitu : GC-2010
Column Oven Temperature : 80.0OC
Injection Temperature : 310.00O
Injection Mode : Split
Flow Control Mode : Pressure
Pressure : 16.5 kPa
Total Flow : 80.0 mL/min
Column Flow : 0.50 mL/min
Linear Velocity : 26.1 cm/sec
Purge Flow : 0.3 Ml/MIN
Split Ratio : 158.4
High Pressure Injection : OFF
Carrier Gas Saver : OFF
Column Oven : Yes
SPLI : Yes
MS : Yes
SPLI Carrier : Yes
SPLI Purge : Yes
External Wait : No
Equilibrium : 0.5 min
[GC Program]
Ion Source Temperature : 250.00O
Interface Temperature : 310.00o
Solvent Cut Time : 2.80 min
Detector Gain Mode : Relative
Detector Gain : 0.00 kV
Threshold : 0
[MS Table]
Start Time : 3.00 min
End Time : 52.00 min
ACQ Mode : Scan
Event Time : 0.50 sec
Scan Speed : 1250
Start m/z : 28.00
End m/z : 600.00
Sample Inlet Unit : GC
[MS Program]
3.4. Bagan Penelitian
3.4.1. Bagan Penelitian Isolasi Minyak Atsiri Dengan Alat Stahl (Hidrodestilasi)
400 g Rimpang Jerangau Yang Telah Diiris
Dimasukkan ke dalam Labu Stahl volume 1 Liter
Ditambahkan air secukupnya
Didestilasi hingga keluar uap air bersama minyak
Residu Destilat
Lapisan Bawah Lapisan Atas
Didekantasi dengan Syring Dimasukkan kedalam botol Vial I
Dijenuhkan dengan NaCl
Ditambahkan dietil eter
Diekstraksi
Lapisan Bawah Lapisan Atas
Diuapkan eternya
Ditambahkan Na2SO4 anhidrous secukupnya
Dimasukkan kedalam botol Vial I
Minyak Atsiri
Analisis GC-MS
Dimasukkan ke dalam corong pisah
3.4.2. Bagan Penelitian Isolasi Minyak Atsiri Dengan Destilasi Uap
400 g Rimpang Jerangau yang telah diiris
Dirangkai alat destilasi uap
Dipanaskan ketel uap
Destilat
Dimasukkan kedalam corong pisah
Dijenuhkan dengan NaCl
Ditambahkan eter
Diekstraksi
Lapisan atas Lapisan bawah
Diuapkan eternya
Ditambahkan Na2SO4 anhidrous
Dimasukkan kedalam botol Vial I
Analisis GC-MS
Dimasukkan kedalam labu didih 3 Liter
Didekantasi dengan syring
Dimaukkan kedalam botol Vial I
Dijenuhkan dengan NaCl
Ditambahkan Dietil eter
Diekstraksi
Lapisan atas Lapisan bawah
Disaring
BAB 4
HASIL DAN PEMBAHASAN
4.1. HASIL PENELITIAN
4.1.1. Isolasi Minyak Atsiri Dari Rimpang Tanaman Jerangau
Hasil isolasi minyak atsiri dari rimpang tanaman jerangau melalui destilasi bersama
uap air (Hidrodestilasi) menggunakan alat Stahl dari masing-masing sebanyak 400 g
sampel rimpang basah yang digunakan diperoleh rata-rata sebanyak 1,3 mL (0,325%,
v/w) minyak atsiri atau 0,5%, v/w dari berat kering (Tabel 4.1). hasil isolasi melalui
destilasi uap dari 400 g sampel yang digunakan diperoleh rata-rata 1,41 mL (0,35 %,
v/w) minyak atsiri atau 0,54 %, v/w dari berat kering (Tabel 4.2).
Tabel 4.1. Hasil isolasi minyak atsiri rimpang tanaman jerangau melalui Hidrodestilasi dengan alat Stahl
No. Berat Sampel (g) Volume Minyak Atsiri (mL) Rata-rata Volume Minyak (mL) % (v/w) (berat basah) % (v/w) (berat kering) 1. 2. 3. 400 400 400 1,35 1,30 1,25
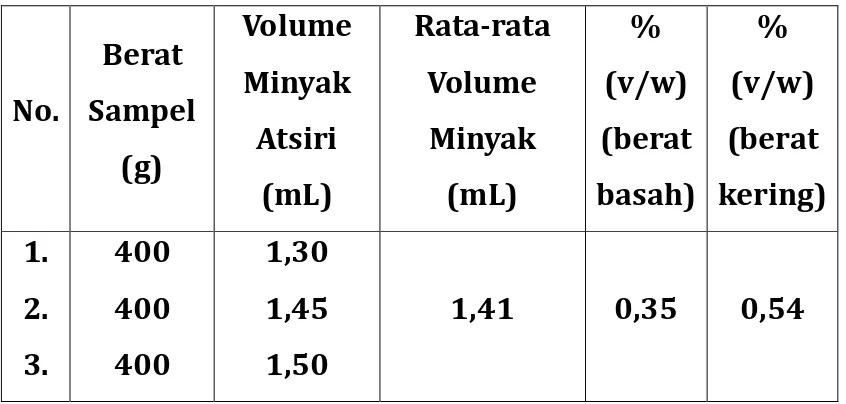
Table 4.2. Hasil isolasi minyak atsiri rimpang tanaman
jerangau melalui Destilasi uap
No.
Berat
Sampel
(g)
Volume
Minyak
Atsiri
(mL)
Rata-rata
Volume
Minyak
(mL)
%
(v/w)
(berat
basah)
%
(v/w)
(berat
kering)
1.
2.
3.
400
400
400
1,30
1,45
1,50
1,41
0,35
0,54
4.1.2. Hasil Analisis Kromatografi Gas- Spektra Massa
Hasil analisis melalui pemeriksaan GC-MS terhadap
minyak atsiri dari rimpang tanaman jerangau yang
dihasilkan melalui hidrodestilasi dengan alat Stahl
diperoleh kromatogram dengan memberikan puncak
Gambar 4.1. Kromatogram minyak atsiri dari rimpang
tanaman Jerangau yang diperoleh secara
Hidrodestilasi dengan alat Stahl
Dari 13 senyawa yang ditemukan ternyata berdasarkan
standard Library yang ada dapat diinterfretasi
spektrum massanya adalah sebanyak 11 senyawa
seperti pada (tabel 4.3.)
Tabel 4.3. Komponen Senyawa Minyak Atsiri Pada
Rimpang Jerangau Yang Diperoleh Melalui
Metode Hidrodestilasi Menggunakan Alat Stahl
Retensi (%) Molekul Mungkin
1. 6.517 1.87 C10H16 Kamfen
2. 8.400 1.42 C10H16 β-Ocimen
3. 10.892 1.12 C10H16O Kamfor
4. 16.050 12.97 C11H14O2 Metil Isoeugenol
5. 16.783 3.76 C12H20 -
6. 17.067 9.37 C15H26 -
7. 8. 9. 10. 11. 12. 13. 17.642 18.117 18.325 18.483 18.992 19.242 19.292 1.87 1.47 58.87 1.75 1.14 1.97 2.43
C12H16O3
C12H16O3
C12H16O3
C15H22
C12H16O3
C13H20O
C15H22O
Euasaron α,β-Asaron α,β-Asaron Cis-Kalamenen(*) Trans-Isoelemicin(*) β-Ionon Aristolon
Keterangan : (*) = Senyawa yang tidak ditemukan pada hasil dengan Metode Destilasi Uap
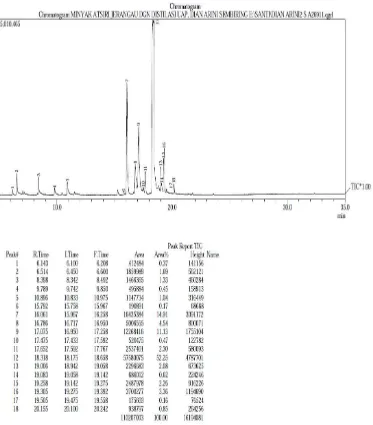
Gambar 4.2. Kromatogram minyak atsiri dari rimpang
tanaman Jerangau yang diperoleh secara
Destilasi Uap
Tabel 4.4. Komponen Senyawa Minyak Atsiri Pada Rimpang Jerangau Yang
Diperoleh Melalui Metode Destilasi Uap No. Waktu
Retensi
Kandungan (%)
Rumus
Keterangan: (*) = Senyawa yang tidak terdapat pada hasil dengan metode Hidrodestilasi dengan alat Stahl
4.2. Pembahasan
4.2.1. Hasil Isolasi Minyak Atsiri Melalui Metode Hidrodestilasi Menggunakan alat Stahl 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 6.142 6.517 8.400 9.792 10.892 15.792 16.058 16.783 17.075 17.475 17.650 18.317 19.008 19.083 19.258 19.308 19.508 20.158 0.37 1.69 1.33 0.45 1.04 0.17 14.91 4.54 11.13 0.47 2.30 52.25 2.08 0.62 2.26 3.36 0.16 0.85
C10H16
C10H16
C10H16
C10H18O
C10H16O
C15H24
C11H14O2
C12H20
C13H22
- C12H16O3
C12H16O3
C12H16O3
C13H20O
C14H20O2
C15H22O
- C10H18O
Hasil analisis spektroskopi GC-MS berdasarkan standar Library yang ada pada minyak atsiri rimpang jerangau dapat dideteksi sebanyak 13 senyawa (Tabel 4.3.), masing-masing senyawa tersebut dengan struktur serta memberikan spektrum MS dengan pola-pola fragmen adalah sebagai berikut :
1. Senyawa Kamfen
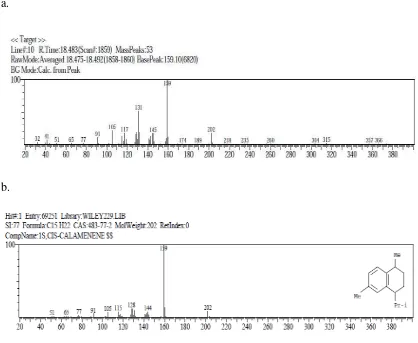
Senyawa ini memberikan waktu retensi 6,517 menit sebanyak 1,87%. Hasil MS memberikan spektrum dimana puncak ion molekul m/e = 136 (M+.), diikuti dengan fragmen-fragmen pada m/e = 121 (M-CH3)+., 107 (M-C2H5)+, 93 (121-C2H4)+, yang
merupakan puncak dasar, 79 (107-C2H2)+, 67(93-C2H2)+, , diikuti fragmen-fragmen
pada m/e = 41(67-C2H2)+ dan 27 (41-14)+ merupakan ciri khas hidrokarbon (Gambar
4.3). Berdasarkan standard Library bahwa senyawa tersebut memiliki rumus molekul C10H16 yang merupakan isomer monoterpen dengan pola fragmentasi secara hipotesis
seperti pada gambar 4.4.
a.
Gambar 4.3. Spektrum GC-MS senyawa Kamfen dari minyak atsiri rimpang Jerangau yang diperoleh dengan menggunakan alat Stahl (a = sampel; b = Standard library)
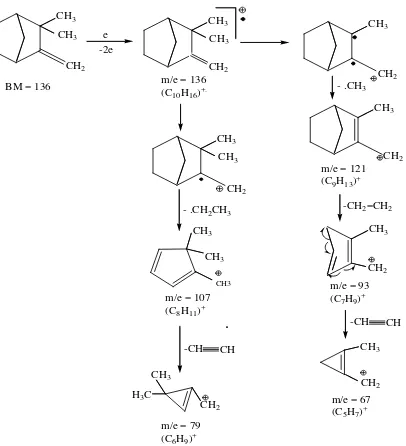
CH3 CH2 CH3 CH3 CH3 CH2 CH3 e -2e
m/e = 136
(C10H16)+. - .CH3
CH3
m/e = 121 (C9H13)+
-CH2=CH2
CH3 CH2
m/e = 67 (C5H7)+ - .CH2CH3
CH2 -CH CH CH3 CH2 CH2 CH3 CH2 CH3 CH3 CH3
m/e = 107 (C8H11)+
m/e = 93 (C7H9)+ CH3
-CH CH
CH3
H3C
CH2
m/e = 79 (C6H9)+ BM = 136
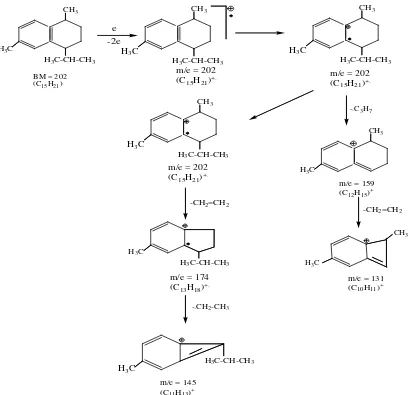
Senyawa ini memberikan waktu retensi 8,400 menit sebanyak 1,42%. Hasil MS memberikan spektrum dimanan puncak ion molekul m/e = 136 (M+.), diikuti fragmen-fragmen pada m/e = 121 (M-CH3)+, 93 (121-C2H4)+ yang merupakan
puncak dasar , 53 (79-C2H2)+ diikuti fragmen-fragmen pada m/e = 105 (121-CH4)+, 79
(105-C2H2)+ , 67 (93-C2H2)+, 41 (67-C2H2)+ dan 27 (53-C2H2)+ menunjukkan ciri
khas hidrokarbon (Gambar 4.5). Berdasarkan standard Library bahwa senyawa tersebut memiliki rumus molekul C10H16 yang merupakan isomer dari senyawa
monoterpen dengan pola fragmentasi secara hipotesis seperti pada gambar 4.6. a.
b.
H2C=CH-C=CH-CH2-CH=C-CH3 CH3 CH3
H2C=CH-C=CH-CH2-CH C-CH3
CH3
CH3
m/e = 136 (C10H16)+.
-.CH3
H2C=CH-C=CH-CH2-CH=C-CH3 CH3
m/e = 121 (C9H