PENATALAKSANAAN KUSTA DENGAN REGIMEN
RIFAMPISIN, OFLOKSASIN DAN MINOSIKLIN
DERYNE ANGGIA PARAMITA
198311112009122004
DEPARTEMEN ILMU KESEHATAN KULIT DAN KELAMIN
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
MEDAN
PENATALAKSANAAN KUSTA DENGAN REGIMEN ROM (RIFAMPISIN, OFLOKSASIN, MINOSIKLIN)
PENDAHULUAN
Kusta atau yang juga dikenal dengan penyakit Hansen’s adalah penyakit granulomatos kronik
yang menyerang saraf tepi dan kulit. Penyebabnya adalah bakteri tahan asam Mycobacterium
leprae yang pertama sekali ditemukan oleh peneliti dari Jerman, Gerhard Henrik Armauer
Hansen pada tahun 1873.1,2 Penyebarannya yang lambat dan terdapat hubungan kekeluargaan
pada penderitanya mengusulkan bahwa penyakit ini diturunkan.3 Sebagai konsekwensinya
beberapa kultur daerah setempat menganggap penderita kusta (dan seringnya anggota
keluarganya) sebagai “tidak bersih” atau sebagai “lepra” dan membuat peraturan bahwa mereka
tidak boleh berhubungan dengan masyarakat yang tidak menderita. Terkadang penderita
diwajibkan untuk memakai pakaian khusus dan membunyikan bel sehingga yang tidak menderita
dapat menghindari mereka.4
Kusta atau lepra berasal dari kata latin Lepros yang mengandung arti pengotoran. Faktanya kusta telah menjadi penyakit yang sukar disembuhkan yang juga menyebabkan deformitas parah
dan kelumpuhan, telah membuat stigmata yang buruk. Walaupun telah didokumentasikan sejak
jaman dahulu kala, kusta tetap menjadi endemis pada beberapa negara berkembang di dunia.2
WHO membagi kusta menjadi 2 klasifikasi untuk kepentingan pengobatan dan
pengontrolan penyebaran. Pada tahun 1981 oleh kelompok studi kusta di WHO, klasifikasi
dibagi 2 yaitu kusta tipe MB dan PB.1 Ini sejalan dengan obat yang diberikan yaitu MDT-PB dan
memperbaiki pengobatan kusta, dimana pengobatan MDT-MB durasi nya disingkatkan dari 24
bulan menjadi 12 bulan dan penggunaan regimen baru yaitu regimen dosis tunggal kombinasi
ROM untuk lesi tunggal PB. Menurut WHO dosis tunggal regimen kombinasi ROM dapat
diterima dengan baik dan sebagai alternatif yang efektif secara biaya untuk pengobatan lesi
tunggal kusta tipe PB.5
EPIDEMIOLOGI
Kusta endemis pada beberapa benua kecuali Antartika. Di Eropa insidensi sangat rendah,
sedangkan pada negara Pasifik insidensi lebih tinggi. Populasi terbanyak terdapat di India
dengan hampir duapertiga dari populasi kusta dunia. Menurut data regional WHO pada tahun
2007 prevalensi di Afrika adalah 29.548, di Asia Tenggara 116.663, di Pasifik Barat 9.805.1,6
Negara Kasus Baru yg Terdeteksi (n)
Tbl 1. Negara yang melaporkan ≥ 5.000 kasus pada tahun 2007 7
Pada semua penelitian populasi kusta, penyakit ini lebih umum pada pria dibandingkan
dibandingkan tipe lepromatous, tetapi pada kedua grup ini, kusta predominan pada usia muda
dengan umur rata rata adalah 35 tahun.1
Kusta adalah penyakit kronik dengan periode inkubasi yang panjang. Rata-rata masa
inkubasi adalah 2-5 tahun untuk kasus tuberkuloid, dan 8-12 tahun atau sampai 20 tahun untuk
kasus lepromatos. Seorang tentara amerika yang menderita kusta setelah bertugas di negara
tropis, klinis nya tampak 20 tahun setelah paparan pertama sekali.1,3
Walaupun kusta jarang sebagai penyebab utama kematian, pasien mempunyai rasio
kematian yang standar setidaknya 2 kali lebih tinggi dibandingkan populasi umum karena efek
sekunder yang tidak langsung dari penyakit ini. Diperkirakan 1 milyar penderita kehilangan
disability adjusted life year (DALY) secara global setiap tahunnya karena kusta, dengan 6,3 tahun kehidupan sehat yang hilang per pasien.3
ETIOLOGI
Kusta disebabkan Mycobacterium leprae bakteri dengan bentuk batang obligat intraseluler yang
hanya tumbuh pada manusia dan sel hewan. Bakteri M. leprae adalah bakteri tahan asam karena
karakteristik kimianya. Apabila dilakukan pewarnaan pada spesimen M. leprae akan terlihat
warna merah dengan latar belakang biru karena kandungan asam mikolik pada dinding selnya.4
Pada jaringan atau pewarnaan, M. leprae dinilai dengan indeks biopsi (BI), yaitu jumlah skala
logaritmik dari bakteri per lapangan minyak emersi/OIF: BI 6 adalah jika terdapat 1000 atau
lebih/OIF, BI 5 jika 100-1000/OIF, BI 4 10-100/OIF, BI 3 jika 10/OIF, BI 2 1/1-10 OIF, BI 1
jika 1/10-100 OIF dan BI 0 jika tidak ada bakteri dalam 100 OIF. Karena BI 6 mengindikasikan
109 bakteri per gram jaringan granuloma, maka jaringan dengan BI 0 mempunyai 103 organisme
M. leprae tumbuh pada suhu 30-33⁰C dengan waktu menggandakan adalah 12 hari, dan
akan tetap bertahan di lingkungan sampai 10 hari.3 Bakteri ini tumbuh sangat baik pada makrofag
tubuh dan sel Schwann.4
PATOGENESIS
Patogenesis dan gambaran klinis dari kusta disebabkan 4 prinsip dari kerusakan jaringan3
(Gbr 1):
1. Derajat dimana imunitas yang diperantarai sel (CMI) diekspresikan. Kusta lepromatos
menunjukkan kegagalan pada CMI terutama menuju M. leprae dengan multiplikasi
resultan basil, penyebaran dan akumulasi antigen pada jaringan yang terinfeksi. Tidak
dijumpainya limfosit yang teraktifasi dan makrofag menunjukkan bahwa kerusakan saraf
lambat dan muncul secara bertahap. Pada kusta tuberkuloid, CMI diekspresikan dengan
kuat sehingga infeksi terbatas pada satu atau beberapa tempat dikulit dan saraf perifer.
Infiltrasi limfositik secara cepat membuat kerusakan pada saraf. Diantara dua bentuk
penyakit terletak 2 bentuk borderline, dengan perluasan penyakit menggambarkan
keseimbangan antara CMI dengan muatan bakteri.
2. Peluasan penyebaran penyakit dan multiplikasi. Pada kusta lepromatos, pemyebaran
hematogen dari basil terjadi pada daerah dingin, superfisial termasuk mata, mukosa
pernafasan atas, testis, otot kecil dan tulang dari kaki, jari kaki dan wajah, juga pada saraf
perifer dan kulit. Pada kusta tuberkuloid, multiplikasi penyakit terbatas pada beberapa
daerah dan basil tidak dijumpai.
3. Gambaran kerusakan jaringan merupakan komplikasi imunologis: reaksi kusta. Pasien
4. Pembentukan kerusakan saraf dan komplikasinya. Kerusakan saraf terjadi dalam 2 bentuk,
pada lesi kulit dan saraf perifer batang tubuh. Pada lesi kulit, sensori dermal kecil dan
serabut saraf yang mensarafi kulit dan struktur kutaneus mengalami kerusakan,
menyebabkan hilangnya sensor lokal dan hilangnya keringat pada daerah lesi kulit. Saraf
perifer batang tubuh adalah daerah yang mudah diserang pada daerah perifernya atau
terowongan fibroseus. Pada titik ini, peningkatan diameter saraf yang hanya sedikit akan
membuat peningkatan tekanan intraneural, dengan akibatnya kompresi neural dan
iskemia. Kerusakan pada saraf perifer batang tubuh menyebabkan tanda karakteristik,
dengan hilangnya sensori dermatom dan disfungsi otot yang dipersarafi saraf perifer.
Gbr.1 Mekanisme kerusakan pada kusta dan jaringan yang terlibat. Mekanisme dibawah garis
utuh adalah menuju tuberkuloid. Terjadi tumpang tindih pada pertengahan garis, yang menjadi
predisposisi terjadinya reaksi tipe 1 (dikutip sesuai aslinya dari kepuastakaan 3).
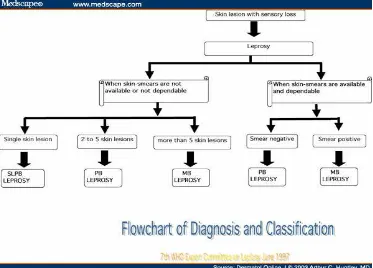
DIAGNOSIS DAN KLASIFIKASI
Diagnosis dari kusta berdasarkan gejala klinis dimana dijumpainya satu atau lebih dari satu atau
lebih tiga tanda kardinal : yaitu lesi kulit eritem atau hipopigmentasi yang anestesi; penebalan
saraf tepi dengan hilangnya sensasi pada daerah distribusi; dan pewarnaan kulit yang positif
untuk bakteri tahan asam.6,8 Petugas pemeriksa kusta yang biasa akan dapat menilai dan
mengenali gambaran klinis ini. Pada daerah endemis lesi kulit selalu konsisten dengan kusta jika
terdapat kehilangan sensori saraf dengan atau tanpa penebalan saraf dan pewarnaan slit kulit
yang positif.8
Terdapat banyak klasifikasi kusta, yang banyak dikenal adalah klasifikasi berdasarkan
WHO dan Ridley-jopling. Klasifikasi kusta menurut Ridley adalah berdasarkan klinis, perubahan
histopatologi dan status imunitas. Dibagi menjadi 5 bentuk yaitu kusta tipe TT (Tuberkuloid),
BT (Borderline tuberkuloid), BB (Borderline), BL (Borderline lepromatos), dan
LL(Lepromatos). Menurut konsepnya, tipe TT dan LL adalah stabil secara klinis, tetapi dapat
jatuh ke keadaan yang meningkat atau menurun sesuai status imunitasnya.1
Menurut WHO, kusta diklasifikasikan menjadi PB (pausibasiler) dan MB (multibasiler)
yang diperkenalkan pertama sekali pada tahun 1982 sebagai dasar untuk pengobatan dan
meminimalkan tingkat relaps.8 Klasifikasi ini berdasarkan manifestasi klinis dan pewarnaan
kulit. Dimana pada pasien dengan pewarnaan kulit yang negatif dimasukkan kedalam grup PB,
sedangkan pasien dengan pewarnaan kulit positif akan dimasukkan kedalam grup MB.8,9 Namun
didasarkan pada bentuk klinis dan jumlah saraf yang terlibat. Pada sistem ini, jika terdapat 1-5
lesi kulit dan keterlibatan saraf hanya satu akan dimasukkan kedalam lesi PB, sedangkan apabila
terdapat lesi kulit lebih dari 5 dan keterlibatan saraf lebih dari satu akan masuk kedalam lesi
MB.6,9
Pada tahun 1997, WHO menambah klasifikasi kusta menjadi tiga, juga untuk kepentingan
pengobatan. Klasifikasi baru ini dianggap tepat untuk kusta yang hanya mempunyai satu lesi
tunggal, selain tepat juga efektif secara biaya, yang kemudian dikenal dengan SLPB (Single
lesion Pausibasiler).5
Tbl 2. Pembagian klasifikasi kusta menurut WHO berdasarkan jumlah lesi, kerusakan saraf dan
pewarnaan kulit tidak berkontribusi pada klasifikasi ini
Gbr 2. Diagram pembagian kusta (dikutip sesuai aslinya dari kepustakaan 9).
GAMBARAN KLINIS
Terdapat berbagai bentuk kusta yang didasarkan atas respon imun seseorang terhadap M. leprae.
Respon imun yang baik akan membentuk lesi tuberkuloid, yang terbatas pada kulit dan
keterlibatan saraf yang asimetris. Respon imun yang buruk akan membentuk lesi lepromatos,
yang ditandai dengan lesi kulit dan keterlibatan saraf yang banyak. Beberapa pasien memiliki 2
bentuk secara bersamaan.4
Kusta tipe Tuberkuloid (TT)
Pada kusta tipe ini, imunitas penderita kuat sehingga terjadi kesembuhan yang cepat dan
tidak dijumpai penurunan kearah resistensi penjamu yang kurang. Akan dijumpai beberapa
makula hipopigmentasi, beberapa besar dan menjadi anestesia.4 Terdapat beberapa keterlibatan
tengah dan batas yang jelas. Lesi akan mengalami indurasi, tanpa rambut dan kering.1 Pada
pemeriksaan histopatologi akan dijumpai granuloma yang mengelilingi elemen vaskular,
granuloma menyerang zona papiler dan dapat mengikis epidermis, namun BTA tidak dijumpai.
Saraf kulit tidak seluruh nya rusak tampak bengkak karena sel granuloma epiteloid dan
dikelilingi oleh zona limfosit.3
Gbr 2. Gambaran klinis dan histopatologi kusta tipe Tuberkuloid (dikutip sesuai aslinya
dari kepustakaan 1,3)
Kusta tipe Borderline Tuberkuloid (BT)
Lesi akan tampak seperti kusta tipe tuberkuloid tetapi lebih kecil dan jumlah pembesaran
saraf menjadi lebih banyak, bentuk ini akan menetap atau menjadi bentuk yang lain.4 Pada tipe
ini imunitas penderita cukup kuat untuk menahan infeksi, sehingga penyakit hanya terbatas dan
pertumbuhan bakteri lemah, namun respon penjamu tidak cukup kuat untuk sembuh sendiri.Lesi
kulit berupa plak atau papul dengan batas yang jelas dengan pada beberapa orang akan dijumpai
lesi papul satelit. Secara histopatologi akan dijumpai jubah limfositik yang terbentuk agak
sempurna, sel Langhans tidak dijumpai atau dijumpai sedikit. BTA dan sel plasma adalah jarang.
Gbr 3. Lesi kusta tipe Bordeline Tuberkuloid (dikutip sesuai aslinya dari kepustakaan 1)
Kusta tipe Borderline (BB)
BB adalah titik tengah imunologik atau daerah pertengahan dari spektrum granulomatos,
merupakan bentuk yang sangat tidak stabil dimana pasien dapat menurun atau meningkat
menjadi bentuk granulomatos dengan atau tanpa reaksi klinis. Gambaran klinis berupa lesi anular
dengan bagian dalam yang berbatas tegas, plak lebar dengan pulau kulit yang sehat didalam plak
seperti gambaran “keju Swiss” atau lesi dimorfik klasik. Karena BB adalah bentuk yang tidak
stabil, lesi BB biasanya tidak bertahan lama dan pasien jarang dijumpai.1,4 Pada pemeriksaan
histopatologi akan dijumpai sel granuloma epiteloid akan terlihat lebih difus tetapi zona papiler
yang pendek. Sel raksasa cenderung menjadi badan asing dibandingkan Langhans dan sel saraf
bengkak sedang oleh infiltrat selular. BTA mungkin tidak dijumpai.3
Kusta tipe Borderline Lepromatos (BL)
Lesi kusta tipe BL akan dijumpai banyak makula, papul, plak dan nodul terkadang dengan
dan tanpa anestesia, bentuk akan menetap atau berubah menjadi bentuk LL.4 Pada tipe ini respon
imun sangat rendah sehingga tidak dapat menahan pertumbuhan bakteri, tetapi masih cukup
untuk merangsang kerusakan jaringan dnegan inflamasi terutama pada saraf. Lesi dapat berupa
bentuk anular dengan batas luar yang tidak jelas tetapi batas dalam yang jelas. Dapat juga
dijumpai lesi “punched out”. Pemeriksaan histologi akan tampak suatu respon yang klasik
dengan infiltrasi limfosit yang banyak yang mengelilingi makrofag. BTA akan mudah dijumpai.1
Gbr 5. Lesi kusta tipe BL (dikutip sesuai aslinya dari kepustakaan 1)
Kusta tipe Lepromatos Leprosy (LL)
Pada tipe LL, kurangnya CMI memyebabkan M. leprae replikasi bakteri tanpa hambatan
dan penyebaran kusta keseluruh organ. Infiltrasi dermal yang difus selalu terjadi subklinis dan
akan dijumpai bentuk pembesaran dari daun telinga, pelebaran dari hidung dan pembengkakan
jari yang akan menyerupai bentuk reumatik. Nodul dengan bentuk yang tidak jelas akan mudah
dijumpai dengan diameter 2 cm dan terdistribusi simetris.1 Pasien sering dijumpai tanpa alis mata
penebalan rete ridges. Dermis mengandung BTA yang banyak tunggal atau berkelompok
(clumps).3
Gbr 6. Lesi kulit tipe LL dan gambaran histopatologi (dikutip sesuai aslinya dari
kepustakaan 1,3)
PENGOBATAN KUSTA
Tujuan utama untuk program pengontrolan kusta adalah (1) deteksi pasien awal; (2) pengobatan
yang sesuai; dan (3) perawatan yang adekuat untuk pencegahan dari disabilitas dan rehabilitasi.
Karena kusta adalah penyakit infeksius, pengobatan antibiotik memegang peranan yang utama
pada manajemen pasien yang baru didiagnosis.9
Penemuan utama dalam pengobatan kusta adalah ditemukan dan diperkenalkannya MDT
(multidrug therapy) yang mengikuti rekomendasi WHO pada kemoterapi kusta untuk program
pengontrolan. MDT yang direkomendasikan WHO terdiri dari rifampisin, klofazimin dan
dapson. Ini sangat efektif dan telah lebih dari 18 milyar pasien sembuh, dan setidaknya 1 milyar
pasien kusta dicegah dari kelumpuhan. MDT terdiri dari 3 obat yaitu: dapson, rifampisin, dan
klofazimin. Pasien dengan pausibasiler diobati selama 6 bulan dengan regimen MDT PB. MDT
duluan). Ini kemudian diperbaiki hanya sampai 24 bulan pada tahun 1994 dan dipersingkat
menjadi 12 bulan pada 1998 tanpa terjadi pengurangan efikasinya.8
Pada pertemuan WHO tahun 1997 direkomendasikan penggunaan regimen ROM
(rifampisin, ofloksasin, minosiklin) untuk lesi tunggal PB. Pasien dengan lesi tunggal PB dapat
diobati dengan dosis tunggal regimen ROM. Penelitian eksperimental dan klinis telah
menunjukkan keefektifan bakterisidal dari obat ini, dalam kombinasi atau pun tunggal. Sehingga
untuk lesi tunggal PB (SLPB), WHO memberikan kebebasan dalam menentukan pilihan
pengobatan apakah menggunakan dosis tunggal regimen ROM atau MDT-PB selama 6 bulan.8,9
Pengobatan Kusta tipe PB
Pada pasien PB pemberian obat selama 6 bulan dengan rifampisin saja dapat membuat
pembersihan bakteri secara komplit. Namun, untuk mencegah resistensi rifampisin ditambahkan
dapson. Hasil yang dicapai dari inaktif penyakit secara klinis tidak seharusnya menjadi patokan
kelanjutan dari pengobatan MDT pada pasien PB, karena pada pasien ini biasanya selalu bebas
dari bakteri hidup dalam 6 bulan pengobatan MDT. Namun harus selalu diingat bahwa aktivitas
kusta PB tidak selalu berkorelasi dengan multiplikasi bakteri. Pada sebagian besar pasien,
inaktifitas klinis tidak dicapai dalam 6 bulan bahkan setelah hilangnya bakteri. Penelitian lebih
lanjut pada pasien PB yang menggunakan pengobatan MDT, telah menunjukkan bahwa
hilangnya lesi secara komplit dijumpai setelah 1-2 tahun setelah pemutusan obat. Insidensi relaps
pada pasien PB adalah sangat rendah dan sampai saat ini korelasi antara status aktivitas penyakit
dengan waktu dimana obat dihentikan dan relaps tidak ada didokumentasikan. Lebih lanjut,
Tbl 3. Regimen MDT-PB (dikutip sesuai aslinya dari kepustakaan 8)
Pengobatan kusta tipe MB
Rifampisin tetapmenajdi komponen utama dari regimen MDT, yang membersihkan
kebanyakan strain M. leprae pada beberapa bulan pengobatan. Baru-baru ini telah ditemukan
bahwa kombinasi dapson dan klofazimin sanhgat bakterisidal. Kombinasi ni sangat efektif pada
pasien kusta MB yang tidak diobati yang mengalami mutasi resisten-rifampisin dalam 3-6 bulan.
Untuk pengoabatan kusta MB, percobaan klinis yang terkontrol dan dapat dipercaya telah
menunjukkan bahwa MDT secara umum efektif dalam 24 bulan atau kurang. Penelitian ini
membawa rekomendasiWHO untuk mempersingkat pemakaian selaam 12 bulan untuk kusta
MB.9
Beberapa ahli khawatir bahwa pemberian regimen selama 12 bulan untuk pengobatan pada
pasien dengan indeks bakterial yang tinggi. Pengamatan telah menunjukkan bahwa indeks
bakterial yang tinggi pada saat awal pemberian regimen pengobatan telah berkorelasi dengan
tingginya risiko tidak hanya dengan lambatnya penghilangan lesi kulit juga indeks yang tinggi
pada akhir pemeberian regimen 12 bulan dibandingkan dengan pasien yang memulai dengan
indeks bakterial yang lebih rendah. Namun, telah ditemukan bahwa indeks bakterial yang tinggi
akan terus membaik setelah selesai regimen 12 bulan. Lebih lanjut, tambahan 12 bulan MDT
Tbl 4. Regimen pengobatan MDT-MB (dikutip sesuai aslinya dari kepustakaan 8)
Pengobatan kusta tipe SLPB
WHO pada tahun 1997 merekomendasikan dosis tunggal rifampisin-ofloksasin-minosiklin
(ROM) sebagai terapi lesi tunggal pausibasiler (SLPB), dan kemudian National Leprosy
Elimination Program di India mengadopsi ini dan menggunakannya pada seluruh negeri.10
Dosis tunggal kemoterapi ini telah digunakan pada pengobatan kusta, selain karena efikasi
nya secara klinis, regimen ini mempunyai keuntungan tambahan yaitu dalam penghematan
sumber daya manusia dan meningkatkan kepatuhan pasien. Respon klinis pada terapi regimen
ROM ditemukan sama efektifnya dengan MDT-PB untuk lesi tunggal kusta PB. Dari
pengamatan jangka panjang, manajemen dan problem klinis, dan implikasi lapangan didapati
hasil yang memuaskan.10
REGIMEN ROM
Pengobatan kusta utamanya terdiri dari rifampisin, dimana rifampisin adalah obat dengan efek
bakterisidal yang paling poten untuk M. leprae. Karena pengobatan pada kusta dirancang efektif untuk semua keadaan, yaitu pasien baru dan pasien yang relaps dari pengobatan sebelumnya
maka penggunaan rifampisin yang hanya dengan satu obat lain tidak direkomendasikan.
Rifampisin sebaiknya ditambah dengan dua agen obat lainnya yang harus memenuhi komponen
(i) dosis tunggal harus menunjukkan aktivitas bakterisidal melawan M. leprae (ii) obat lainnya
tidak sebagai antagonis dari rifampisin (iii) obat harus dapat ditoleransi apabila diberikan pada
dosis efektif.11
Ofloksasin dan minosiklin telah menunjukkan hasil yang memuaskan dalam melawan M.
leprae pada tikus dan manusia. Pemberian ofloksasin 400 mg dan minosiklin 100 mg menunjukkan aktivitas bakterisidal yang sama dengan pemberian DDS selama 30 hari untuk
pasien MDT-MB. Sehingga ofloksasin dan minosiklin dapat digunakan bersama dengan
rifampisin untuk pengobatan kusta.11
Rifampisin
Rifampisin adalah derivat dari rifamisin, suatu antibiotik makrosilik kompleks yang
menghambat DNA-dependent RNA polimerase pada patogen mikrobial yang luas.8 Rifampisin
adalah larut lemak, dengan pemberian secara oral akan cepat diabsorbsi dan didistribusikan
melalui jaringan seluler dan cairan tubuh. Apabila meningen mengalami inflamasi maka
beberapa jumlah yang signifikan akan masuk kedalam cairan serebrospinal. Dosis tunggal 600
mg akan mencapai puncak konsentrasi serum sekitar 10 mcg/ml dalam 2-4 jam, yang akan
didaur ulang pada sirkulasi enterohepatik, dan metabolitnya membentuk deasetilasi pada hati dan
kemudian akan diekresikan pada feses.12,13
Karena gampang terjadi resistensi maka rifampisin harus selalu diberikan kombinasi
dengan agen antimikrobial lainnya.12
Rifampisin adalah obat anti kusta yang sangat efektif dan menurunkan indeks morfologi
pada pasien lepromatos sampai 0 dalam 5 minggu. Diberikan secara oral 600 mg sekali untuk
dewasa dan 300 mg untuk anak-anak. Walaupun bakteri cepat dibunuh, rasio indeks bakterial
yang menurun, dan kecepatan perbaikan klinis dan insidensi reaksi kusta tipe 2 pada pasien
lepromatos adalah sama dengan dapson. Rifampisin memiliki kekurangan dimana ia dapat
memproduksi sindrom toksik. Toksisitasnya tergantung dosis (gagal ginjal dan hepatitis lebih
sering dengan dosis yang luas) dan interval diantara dosis (demam, anemia hemolotik dan
trombositopenia lebih sering jika obat diberikan dengan interval mingguan).8,13
Kontraindikasi pada penderita yang mengalami hipersensitivitas pada rifamisin dan
disfungsi hepar. Rifampisin merangsang enzim hati sehingga diperlukan peningkatkan dosis
yang diperlukan untuk memetabolisme obat pada hati. Ini termasuk kortikosteroid, kontrasepsi
steroid, agen hipoglikemik oral, antikoagulan oral, fenitoin, cimetidine, quinidin, siklosporin dan
glikosida digitalis. Apabila menggunakan rifampisin, pasien yang menggunakan kontrasepsi
sebaiknya menggunakan KB dalam bentuk nonsteroid selama pengobatan dan setidaknya 1 bulan
setelahnya. Ekskresi bilier dari media radiokontras dan sodium sulfobromopthalein dapat
berkurang dan kadar mikrobiologi dari asam folat dan vitamin B12 terganggu.12,14
Efek samping dari rifampisin biasanya dapat ditoleransi pada sebagian besar pasien dengan
dosis yang direkomendasikan, walaupun intoleransi gastrointestinal dapat parah. Efek samping
intermitten daripada harian. Peningkatan konsentrasi serum bilirubin dan transaminase yang
umum dijumpai pada saat pengobatan tapi tanpa manifestasi klinis. Namun hepatitis yang
tergantung dosis dapat terjadi yang biasanya fatal. Penting untuk diketahui bahwa maksimum
dosis perhari adalah 10 mg/kg (600 mg).8,12
Minosiklin
Minosiklin adalah tetrasiklin semisintetik. Merangsang bakteriostatik dengan menghambat
sintesis protein dan secara selektif terkonsentrasi pada organisme. Absorpsi terutama terjadi pada
lambung dan usus kecil. Konsentrasi puncak plasma terjadi dalam 1-4 jam dan waktu paruh
12-30 jam. Dimetabolisme pada hati dan diekskresi pada feses dan urin. Obat bertahan pada tubuh
setelah pemberian dihentikan karena retensi pada jaringan lemak.8,12
Minosiklin dikontraindikasikan pada pasien dengan gangguan ginjal, kehamilan dan
anak-anak. Dan pemberiannya tidak boleh diberikan bersamaan dengan garam besi dan antasida.12
Dalam pemberiannya sebaiknya hati hati dengan fungsi hati, pada gangguan fungsi hati
minosiklin akan diekskresikan lebih lama dari yang diharapkan. Susu atau garam alumunium
aluminium dan magnesium akan mnegurangi absorpsi dari minosiklin.12
Diberikan dengan kombinasi dengan ofloksasin dan rifampisin, minosiklin sebaiknya tidak
diberikan pda wanita hamil dan pada awal kehidupan. Karena terdeposit pada gigi dan tulang dan
mengganggu kalsifikasi tulang, dimana akan menyebabkan osteogenesis abnormal dan
pewarnaan gigi dan hipoplasia dari enamel gigi.12
Efek samping yang dapat terjadi antara lain berupa mual dan vertigo yang lebih sering
dibandingkan tetrasiklin lainnya. Iritasi gastrointestinal umum terjadi karena minosiklin
yang resisten. Reaksi fototoksik dapat terjadi dengan gambaran seperti perubahan kulit
porfiria.8,12
Dosis tunggal minosiklin digunakan pada anak-anak dengan lesi tunggal PB, penelitian di
lapangan telah menunjukkan bahwa dosis tunggal minosiklin dapat dtoleransi pada anak-anak
dan tidak terlihat adanya efek samping yang merugikan karenanya.12
Minosiklin apabila diberikan bersama dengan obat antikoagulan akan dapat mempotensiasi
kerja obat tersebut, gagal ginjal parah dilaporkan pada pasien yang dianestesi dengan agen
halogen yang sebelumnya memakan tetrasiklin. Antasida, garam kalsium, dan obat-obat lambung
akna mengurangi absorpsi minosiklin. Antiepilepsi meningkatkan metabolisme minosiklin yang
akan menurunkan kadar minosiklin plasma.12
Ofloksasin
Ofloksasin adalah florokuinolon sintetik yang bekerja secara spesifik sebagai penghambat
DNA girase bakterial. Ofloksasin ditemukan efektif pada pengobatan M. leprae. Resistensi
kromosom telah dilaporkan tetapi hanya sedikit yang signifikan secara klinis.8,12
Ofloksasin diabsorbsi cepat pada saluran cerna. Kadar plasma puncak terjadi dalam 0.5-1.5
jam setelah pemberian dan terdistribusi pada jaringan tubuh dan terkonsentrasi pada bilier.
Waktu paruh 4 jam dan dieksresikan pada urin dalam bentuk yang tidak berubah.12
Pemberiannya harus diperhatikan pada pasien dengan gangguan hepar atau ginjal sehingga
perlu pengurangan dosis. Dan hati-hati penggunaannya pda pasien dengan epilepsi karena dapat
merangsang kejang. Pastikan cairan cukup selama penggunaan karena dapat terbentuk
kristaluria. Pada wanita hamil, wanita menyusui, anak-anak dan dewasa muda penggunaan
artropati. Pasien sebaiknya menghindari paparan dengan sinar matahari dan berikan jeda selama
4 jam sebelum memakan agen yang mengandung aluminium, besi, dan garam magnesium.12
Ofloksasin biasanya gampang ditoleransi, efek samping yang paling sering biasanya mual,
diare, muntah, dispepsia, nyeri perut, sakit kepala, mual dan pruritus.8,12
Ofloksasin dapat berinteraksi dengan obat antiinflamasi nonsteroid yang dapat merangsang
konvulsi. Antasida mengurangi absorpsi dari ofloksasin, efek antikoagulan koumarin dan
warfarin ditingkatkan oleh ofloksasin. Besi oral dan sukralfat menurunkan absorpsi ofloksasin.12
REGIMEN ROM PADA SLPB
Telah banyak diketahui keuntungan penggunaan dosis tunggal regimen ROM pada lesi tunggal
PB, namun WHO hanya merekomendasikan penggunaan regimen ini pada negara yang
mempunyai program nasional untuk itu dengan pasien yang memiliki lesi tunggal 1000
pertahunnya. Ada ketakutan WHO apabila regimen ROM ini digunakan tanpa perhatian yang
kuat maka pekerja lapangan akan mempunyai kecendrungan untuk salah mengkategorikan pasien
dan salah mendiagnosis.5
Hal-hal yang patut diperhatikan dari regimen ROM5 :
1. Kebenaran dari diagnosis lesi tunggal
Pada pasien yagn dicurigai dengan lesi tunggal, pekerja lapangan sebaiknya memeriksa
permukaan tubuh secraa lengkap dan menilai keterlibatan saraf. Dikhawatirkan apabila
petugas tidak memeriksa secara lengkap dan ternyata lesi terdapat lebih dari satu maka
pasien akan menerima pengobatan yang insufisien. Sama halnya juga pada keterlibatan
saraf.
‐ Pemeriksaan tubuh lengkap telah dilakukan
‐ Pemeriksaan keterlibatan saraf tepi telah dilakukan
‐ Apabila memungkinkan dilakukan pemeriksaan pewarnaan kulit, untuk mengeluarkan
pasien yang positif dari pengobatan dosis tunggal
2. Kontraindikasi penggunaan regimen ROM
Tetrasiklin diketahui terdeposit pada tulang dan gigi, dimana agen obat ini dapat tembus
pada barier plasenta dan diekskresikan pada air susu. Namun hal ini belum dapat
dipastikan apabila minosiklin diberikan dalam dosis tunggal, tetapi untuk mencegah hal
yang tidak diinginkan sebaiknya minosiklin tidak diberikan pada wanita hamil. Efek
teratogenik dari ofloksasin juga sebaiknya tidak dilupakan, sehingga regimen ROM
dikontraindikasikan pada wanita hamil. Dan pada anak-anakdibawah 5 tahun. Untuk
keadaan ini pengobtaan kusta yang tepat adalah pemberian MDT-PB
Pemeriksaan lanjutan (follow up) pada pasien yang diberikan regimen ROM adalah tidak
perlu, namun pasien dapat dianjurkan untuk melaporkan diri secara sukarela apabila terdapat lesi
baru setelah pemakaian regimen ROM. Pasien yang tidak menunjukkan perubahan klinis setelah
1 tahun pemberian regimen ROM maka dianggap pasien tersebut mengalami kegagalan
pengobatan, dan untuk hal ini pasien diberikan pengobatan MDT-PB selama 6 bulan.5
Dosis tunggal regimen ROM telah diterima dengan baik dan kasus relaps dan problem
klinis yang dilaporkan sangat sedikit, kemajuan penelitian sekarang adalah penggunaan regimen
ROM pada PB lesi 2-5.14 Penelitian awal yang menilai efikasi regimen ROM pada PB dengan
lesi 2 mempunyai hasil yang sama dnegan pemberian MDT-PB.8 Untuk lesi PB lebih dari 3-5
penelitian sedang dilakukan, dan dari data awal diketahui adanya pasien yang relaps namun hasil
penelitian lebih lanjut dan pengamatan yang lebih panjang diperlukan untuk mengetahui
DAFTAR RUJUKAN
1. Rea TH, Modlin RL. Leprosy. In: Wolff K, Goldsmith LA, Katz SI, Gilchrest BA, Paller
AS, Leffell DJ, eds. Fitzpatrick’s Dermatology in General Medicine 7th ed. New York:
McGraw-Hill; 2008. p. 1786-96
2. Zulkifli. Penyakit Kusta Dan Masalah Yang Ditimbulkannya. Available from :
http://library.usu.ac.id/download/fkm/fkm-zulkifli2.pdf
3. Lockwood DNJ. Leprosy. In: Burns T, Breathnach S, Cox N, Griffiths C. Rook’s
Textbook of Dermatology 7th ed. Italy: Blackwell Science; 2004. p. 29.1-29.21
4. Charles D, Stoppler MC. Leprosy (Hansen’s Disease). Available from :
http://www.medicinenet.com/script/main/art.asp?articlekey=101078. Last update :
6/11/2009
5. ILEP. International Guidelines For The Introduction of New MDT Regimens for The
Treatment of Leprosy. ILEP Technical bulletin 1998;14:1-4
6. Depkes RI. Buku Pedoman Nasional Pengendalian Penyakit Kusta. 2007
7. Gautam VP. Treatment of Leprosy in India. J Postgrad Med July 2009;55:3:220-224
8. Sehgal NV, Sardana K, Dogra S. The Imperative of Leprosy Treatment in The Pre- and
Post- Global Leprosy Elimination Era: Appraisal of Changing The Scenario To Current
Status. Journal of Dermatological Treatment 2008;19:82-91
9. Ishii N. Recent Advances In The Treatment of Leprosy. Dermatology Online Journal
2003;9:2
10.Shinde A, Khopkar U, Ganapati R, Pai VV. Single-Dose Treatment for Single Lesion
11.Ji B, Sow S, Perani E, et al. Bactericidal Activity of a Single-Dose Combination of
Ofloxacin Plus Minocycline, With or Without Rifampin, Against Mycobacterium Leprae
in Mice and In Lepromatous Patients. Antimicrobial Agents and Chemotherapy
1998;42:5:1115-1120
12.WHO. Drug Used In Leprosy. Available from :
http://apps.who.int/medicinedocs/en/d/Jh2988e/13.1.html
13.Bryceson A, Pfaltzgraff RE. Treatment. In: Leprosy 3rd ed. Singapore: Longman; 1990.
p. 77-91
14.Revankar CR, Bulchand HO, Pai VV, Ganapati R. Single-Dose ROM Treatment for
Multilesion Leprosy-Further Observations. International Journal of Leprosy and Other