PENETAPAN KADAR KALSIUM, KALIUM, DAN
MAGNESIUM PADA AIR TEBU MERAH DAN AIR TEBU
HIJAU SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
NOVEN PRISSILIA
NIM 091501064
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR KALSIUM, KALIUM, DAN
MAGNESIUM PADA AIR TEBU MERAH DAN AIR TEBU
HIJAU SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
NOVEN PRISSILIA
NIM 091501064
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALSIUM, KALIUM, DAN
MAGNESIUM PADA AIR TEBU MERAH DAN AIR TEBU
HIJAU SECARA SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
NOVEN PRISSILIA
NIM 091501064
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 7 Februari 2014
Pembimbing I, Panitia Penguji,
Dra. Masria L. Tambunan, M.Si., Apt. Dr. Ginda Haro, M.Sc., Apt. NIP 195005081977022001 NIP 195108161980031002
Pembimbing II, Dra. Masria L. Tambunan, M.Si., Apt. NIP 195005081977022001
Dra. Tuty Roida Pardede, M.Si., Apt. Drs. Immanuel S. Meliala, M.Si., Apt.
NIP 195401101980032001 NIP 195001261983031002
Dra. Siti Nurbaya, M.Si., Apt. NIP 195008261974122001
Medan, 17 Februari 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur penulis ucapkan ke Hadirat Tuhan Yang Maha Esa atas berkat dan rahmatNya penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini. Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul Penetapan kadar kalsium, kalium, dan magnesium secara Spektrofotometri
Serapan Atom.
Pada kesempatan ini dengan kerendahan hati dan hormat, penulis mengucapkan terimakasih kepada
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU Medan, yang telah yang telah memberikan bimbingan dan
penyediaan fasilitas sehingga penulis dapat menyelesaikan pendidikan. 2. Ibu Dra.Masria Lasma Tambunan, M.Si., Apt., dan Ibu Dra. Tuty Roida
Pardede, M.Si., Apt., yang telah membimbing penulis dalam penelitian
dan penyusunan skripsi ini.
3. Bapak Dr. Ginda Haro, M.Sc., Apt., Bapak Drs. Immanuel S. Meliala,
M.Si., Apt., dan Ibu Dra. Siti Nurbaya, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini.
4. Orangtua dan saudara penulis yang telah banyak memberikan dukungan moril dan materil kepada penulis
6. Bapak dan Ibu staf pengajar Fakultas Farmasi USU Medan, serta seluruh pihak yang telah ikut membantu penulis namun tidak tercantum namanya.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis
berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Januari 2014 Penulis,
PENETAPAN KADAR KALSIUM, KALIUM, DAN MAGNESIUM DALAM AIR TEBU MERAH DAN AIR TEBU HIJAU SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Air tebu merupakan salah satu jenis minuman yang paling digemari masyarakat, umumnya dikemas dalam plastik dan dijual di jalanan. Kandungan kadar kalsium, kalium, dan magnesium pada air tebu merah dan air tebu hijau berbeda. Kondisi yang mempengaruhi perbedaan kandungan pada air tebu merah dan air tebu hijau adalah kondisi lingkungan tanah tempat penanaman tebu tersebut. Tujuan penelitian ini adalah untuk membandingkan kadar kalsium, kalium, dan magnesium dalam air tebu merah dan air tebu hijau.
Air tebu merah yang digunakan diperoleh dari Berastagi dan air tebu hijau diperoleh dari Medan.
Analisis kuantitatif kalsium, kalium, dan magnesium dilakukan pada panjang gelombang 422,7 nm, 769,9 nm, dan 285,2 nm. Hasil menunjukkan kadar rata-rata kalsium pada air tebu merah adalah 19,1088 ± 0,1032 mcg/ml; 59,0587 ± 0.2688 mcg/ml untuk kalium; dan 17,502 ± 0,3730 untuk magnesium. Sedangkan kadar rata-rata kalsium pada air tebu hijau adalah 10,516 ± 0,1367mcg/ml; 54,7287 ± 0,6920 mcg/ml untuk kalium; 5,7333 ± 0,1976 mcg/ml untuk magnesium. Dimana LOD kalsium yang diperoleh adalah 0,0646 mcg/ml, dan LOQ 0,2515 mcg/ml sedangkan LOD untuk kalium adalah 0,949 mcg/ml dan LOQ 0,3164 mcg/ml. Kemudian LOD untuk magnesium adalah 0,0568 mcg/ml dan LOQ 0,1893 mcg/ml.
Dari hasil yang diperoleh menunjukkan bahwa air tebu merah
mengandung kalsium, kalium, dan magnesium lebih tinggi dibandingkan dengan air tebu hijau dengan tingkat kepercayaan 95%.
DETERMINATION OF CALCIUM, POTASSIUM, AND MAGNESIUM IN RED AND GREEN SUGARCANE JUICE WITH ATOMIC ABSORPTION
SPECTROPHOTOMETRY
ABSTRACT
Sugarcane juice is one of the most favourite drink in community, usually packaged in plastic and sold by street vendors. The content level of calcium, potassium, and magnesium in red sugarcane and green sugarcane are different. Factors that affecting the level differences is the ground environment where the sugarcanes is planted.The purpose of this study is to compare the amount of calcium, potassium, and magnesium in the red and green sugarcane juice.
The red sugarcane juice was gotten from Berastagi and the green sugarcane juice was gotten from Medan.
Quantitative analysis of calcium, potassium, and magnesium was perfomed at a wavelength of 422.7 nm, 769.9 nm, and 285.2 nm, respectively. The results showed that the average level of calcium in red sugarcane juice was 19.1088 ± 0.1032 mcg/ml; 59.0587 ± 0.2688 mcg/ml for potassium; and 17.502 ± 0.3730 for magnesium. While the average level of calcium in green sugarcane juice was 10.516 ± 0.1367 mcg/ml; 54.7287 ± 0.6920 mcg/ml for potassium; and 5.7333 ± 0.1976 mcg/ml for magnesium. Whereas the LOD and LOQ of calcium was 0.0646 mcg/ml and 0.2515 mcg/ml, respectively. LOD and LOQ for potassium was 0.949 mcg/ml; and 0.3164 mcg/ml, respectively. And the last, LOD and LOQ for magnesium was 0.0568 mcg/ml; and LOQ 0.1893 mcg/ml, respectively.
The results showed that the red sugarcane juice contained calcium, potassium, and magnesium level higher than of the green sugarcane juice by confidency interval 95%.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Tebu ... 4
2.2 Mineral ... 6
2.2.1 Kalsium ... 5
2.2.2 Kalium ... 6
2.3 Penentuan Kadar Kalsium, Kalium, dan Magnesium ... 7
2.4 Spektrofotometri ... 7
2.5 Spektrofotometri Serapan Atom ... 8
2.5.1 Analisis Kuantitatif dengan Spektrofotometri Serapan Atom ... 11
2.6 Validasi Metode Analisis ... 12
2.6.1 Kecermatan (accuracy) ... 12
2.6.2 Keseksamaan / Ketelitian (precision) ... 12
2.6.3 Batas Deteksi dan Batas Kuantitasi... 13
BAB III METODE PENELITIAN ... 14
3.1 Tempat dan Waktu Penelitian ... 14
3.2 Bahan-bahan ... 14
3.2.1 Sampel ... 14
3.2.2 Bahan ... 14
3.3 Alat-alat ... 14
3.4 Pembuatan Pereaksi ... 15
3.4.1 Larutan Standar Kalsium ... 15
3.4.2 Larutan Standar Kalium ... 15
3.4.3 Larutan Standar Magnesium ... 15
3.4.4 Kuning Titan 0,1% ... 15
3.4.5 NaOH 2N ... 15
3.4.6 H2SO4 2N ... 16
3.5 Prosedur Penelitian ... 16
3.5.2 Destruksi Sampel ... 16
3.5.3 Pemeriksaan Kualitatif ... 17
3.5.3.1 Kalsium ... 17
3.5.3.2 Kalium ... 17
3.5.3.2 Magnesium ... 17
3.5.4 Pemeriksaan Kuantitatif ... 17
3.5.4.1 Pembuatan Kurva Kalibrasi Kalsium, Kalium Magnesium ... 17
3.5.4.2 Penetapan kadar Kalsium, Kalium, dan Magnesium Dalam Sampel ... 18
3.5.4.2.1 Penetapan Kadar Kalsium dalam Air Tebu Merah ... 18
3.5.4.2.2 Penetapan Kadar Kalsium dalam Air Tebu Hijau ... 18
3.5.4.2.3 Penetapan Kadar Kalium dalam Air Tebu Merah ... 18
3.5.4.2.4 Penetapan Kadar Kalium dalam Air Tebu Hijau ... 19
3.5.4.2.5 Penetapan Kadar Magnesium dalam Air Tebu Merah ... 19
3.5.4.2.6 Penetapan Kadar Magnesium dalam Air Tebu Hijau ... 19
3.5.5 Analisis Data Secara Statistik ... 20
3.5.5.1 Penolakan Hasil Pengamatan ... 20
3.5.5.2 Pengujian Beda Nilai Rata-rata Antar Sampel ... 21
3.5.7 Penentuan Batas Deteksi (Limit of Detection) dan
Batas Kuantitasi (Limit of Quantitation) ... 23
BAB IV HASIL DAN PEMBAHASAN ... 24
4.1 Analisis Kualitatif ... 24
4.2 Analisis Kuantitatif ... 25
4.2.1 Kurva Kalibrasi Kalium, Kalsium, dan Magnesium ... 25
4.2.2 Analisis Kadar Kalsium, Kalium, dan Magnesium dalam Air Tebu Merah dan Air Tebu Hijau ... 27
4.2.3 Uji Perolehan Kembali (Recovery) ... 29
4.2.4 Batas Deteksi dan Batas Kuantitasi ... 30
BAB V KESIMPULAN DAN SARAN ... 31
5.1 Kesimpulan ... 31
5.2 Saran ... 31
DAFTAR PUSTAKA ... 32
DAFTAR TABEL
Halaman
Tabel 1. Nilai Qkritis pada Taraf Kepercayaan 95% ... 20 Tabel 2. Hasil Analisis Kualitatif dalam Sampel Air Tebu merah dan
Air Tebu Hijau ... 24
Tabel 3. Hasil Analisis Kuantitatif Kadar Kalsium, Kalium. dan
Magnesium dalam Sampel ... 27 Tabel 4. Hasil Uji Beda Nilai Rata-rata kadar Kalsium, Kalium, dan
Magnesium antar Sampel ... 28 Tabel 5. Persen Uji Perolehan Kembali (recovery) kadar Kalsium,
DAFTAR GAMBAR
Halaman
Gambar 1. Komponen Spektrofotometer Serapan Atom ... 12
Gambar 2. Kurva Kalibrasi Seri (0,2; 0,4; 0,6; 0,8; dan 1 ppm) Larutan Standar Kalsium untuk Penetapan Kadar Kalsium ... 25
Gambar 3. Kurva Kalibrasi Seri (0,2; 0,4; 0,6; 0,8; dan 1 ppm) Larutan Standar Kalium untuk Penetapan Kadar Kalium ... 26
Gambar 4. Kurva Kalibrasi Seri (0,2; 0,4; 0,6; 0,8; dan 1 ppm) Larutan Standar Magnesium untuk Penetapan Kadar Magnesium ... 26
Gambar 5. Tebu Merah ... 84
Gambar 6. Tebu Hijau ... 84
Gambar 7. Uji Mikroskop Ca pada Sampel ... 85
Gambar 8. Uji Mikroskop K pada Sampel ... 85
Gambar 9. Blanko Sampel ... 86
Gambar 10. Uji Kualitatif Mg pada Sampel ... 86
Gambar 11. Uji Kualitatif K pada Sampel ... 87
DAFTAR LAMPIRAN
Halaman Lampiran 1. Data Kalibrasi Kalsium dengan Spektrofotometer
Serapan Atom, Perhitungan Persamaan Garis Regresi
dan Koefisien Korelasi (r) ... 34
Lampiran 2. Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) ... 36
Lampiran 3. Data Kalibrasi Magnesium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) ... 38
Lampiran 4. Contoh Perhitungan Kalsium dalam Sampel ... 40
Lampiran 5. Data Hasil Analisis Kadar Kalsium dalam Sampel ... 41
Lampiran 6. Contoh Perhitungan Kalium dalam Sampel ... 42
Lampiran 7. Data Hasil Analisis Kadar Kalium dalam Sampel ... 43
Lampiran 8. Contoh Perhitungan Magnesium dalam Sampel ... 44
Lampiran 9. Data Hasil Analisis Kadar Magnesium dalam Sampel ... 45
Lampiran 10. Perhitungan Kadar Kalsium dalam Sampel ... 46
Lampiran 11. Perhitungan Kadar Kalium dalam Sampel ... 49
Lampiran 12. Perhitungan Kadar Magnesium dalam Sampel ... 52
Lampiran 13. Perhitungan Statistik Kadar Kalsium dalam Sampel ... 55
Lampiran 14. Perhitungan Statistik Kadar Kalium dalam Sampel ... 58
Lampiran 15. Perhitungan Statistik Kadar Magnesium dalam Sampel .... 61
Tebu Merah dan Air Tebu Hijau (mcg/ml) ... 64
Lampiran 17. Pengujian Beda Nilai Rata-rata Kalium Antara Air Tebu Merah dan Air Tebu Hijau (mcg/ml) ... 66
Lampiran 18. Pengujian Beda Nilai Rata-rata Magnesium Antara Air Tebu Merah dan Air Tebu Hijau (mcg/ml) ... 68
Lampiran 19. Data % Recovery Ca ... 70
Lampiran 20. Data % Recovery K ... 71
Lampiran 21. Data % Recovery Mg ... 72
Lampiran 22. Contoh Perhitungan Pengenceran Larutan Standar 0,01 mcg/ml ... 73
Lampiran 23. Perhitungan Perolehan uji kembali untuk Ca ... 74
Lampiran 24. Perhitungan Perolehan uji kembali untuk K ... 75
Lampiran 25. Perhitungan Perolehan uji kembali untuk Mg ... 76
Lampiran 26. Perhitungan Batas Deteksidan Batas Kuantitasi Ca Persamaan Garis Regresi Y = 0,0554X + 0,000167 ... 77
Lampiran 27. Perhitungan Batas Deteksidan Batas Kuantitasi K Persamaan Garis Regresi Y = 0,0726X + 0,00247 ... 78
Lampiran 28. Perhitungan Batas Deteksidan Batas Kuantitasi Mg Persamaan Garis Regresi Y = 0,544X + 0,0011657 ... 79
Lampiran 29. Bagan Alir Proses Destruksi Basah ... 80
Lampiran 30. Bagan Alir Pembuatan Larutan Sampel ... 81
Lampiran 31. Tabel Nilai Kritik Distribusi t ... 82
Lampiran 32. Tabel Nilai Kritik Distribusi F ... 83
Lampiran 33. Gambar Tebu ... 84
Lampiran 34. Uji Kualitatif Kalsium, Kalium, dan Magnesium ... 85
PENETAPAN KADAR KALSIUM, KALIUM, DAN MAGNESIUM DALAM AIR TEBU MERAH DAN AIR TEBU HIJAU SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Air tebu merupakan salah satu jenis minuman yang paling digemari masyarakat, umumnya dikemas dalam plastik dan dijual di jalanan. Kandungan kadar kalsium, kalium, dan magnesium pada air tebu merah dan air tebu hijau berbeda. Kondisi yang mempengaruhi perbedaan kandungan pada air tebu merah dan air tebu hijau adalah kondisi lingkungan tanah tempat penanaman tebu tersebut. Tujuan penelitian ini adalah untuk membandingkan kadar kalsium, kalium, dan magnesium dalam air tebu merah dan air tebu hijau.
Air tebu merah yang digunakan diperoleh dari Berastagi dan air tebu hijau diperoleh dari Medan.
Analisis kuantitatif kalsium, kalium, dan magnesium dilakukan pada panjang gelombang 422,7 nm, 769,9 nm, dan 285,2 nm. Hasil menunjukkan kadar rata-rata kalsium pada air tebu merah adalah 19,1088 ± 0,1032 mcg/ml; 59,0587 ± 0.2688 mcg/ml untuk kalium; dan 17,502 ± 0,3730 untuk magnesium. Sedangkan kadar rata-rata kalsium pada air tebu hijau adalah 10,516 ± 0,1367mcg/ml; 54,7287 ± 0,6920 mcg/ml untuk kalium; 5,7333 ± 0,1976 mcg/ml untuk magnesium. Dimana LOD kalsium yang diperoleh adalah 0,0646 mcg/ml, dan LOQ 0,2515 mcg/ml sedangkan LOD untuk kalium adalah 0,949 mcg/ml dan LOQ 0,3164 mcg/ml. Kemudian LOD untuk magnesium adalah 0,0568 mcg/ml dan LOQ 0,1893 mcg/ml.
Dari hasil yang diperoleh menunjukkan bahwa air tebu merah
mengandung kalsium, kalium, dan magnesium lebih tinggi dibandingkan dengan air tebu hijau dengan tingkat kepercayaan 95%.
DETERMINATION OF CALCIUM, POTASSIUM, AND MAGNESIUM IN RED AND GREEN SUGARCANE JUICE WITH ATOMIC ABSORPTION
SPECTROPHOTOMETRY
ABSTRACT
Sugarcane juice is one of the most favourite drink in community, usually packaged in plastic and sold by street vendors. The content level of calcium, potassium, and magnesium in red sugarcane and green sugarcane are different. Factors that affecting the level differences is the ground environment where the sugarcanes is planted.The purpose of this study is to compare the amount of calcium, potassium, and magnesium in the red and green sugarcane juice.
The red sugarcane juice was gotten from Berastagi and the green sugarcane juice was gotten from Medan.
Quantitative analysis of calcium, potassium, and magnesium was perfomed at a wavelength of 422.7 nm, 769.9 nm, and 285.2 nm, respectively. The results showed that the average level of calcium in red sugarcane juice was 19.1088 ± 0.1032 mcg/ml; 59.0587 ± 0.2688 mcg/ml for potassium; and 17.502 ± 0.3730 for magnesium. While the average level of calcium in green sugarcane juice was 10.516 ± 0.1367 mcg/ml; 54.7287 ± 0.6920 mcg/ml for potassium; and 5.7333 ± 0.1976 mcg/ml for magnesium. Whereas the LOD and LOQ of calcium was 0.0646 mcg/ml and 0.2515 mcg/ml, respectively. LOD and LOQ for potassium was 0.949 mcg/ml; and 0.3164 mcg/ml, respectively. And the last, LOD and LOQ for magnesium was 0.0568 mcg/ml; and LOQ 0.1893 mcg/ml, respectively.
The results showed that the red sugarcane juice contained calcium, potassium, and magnesium level higher than of the green sugarcane juice by confidency interval 95%.
BAB I PENDAHULUAN 1.1Latar Belakang
Tebu termasuk keluarga Graminae atau rumput-rumputan dan berkembang biak di daerah beriklim udara sedang sampai panas. Gula putih adalah salah
satu hasil dari pengolahan batang tumbuhan tebu. Tinggi tanaman tebu berkisar 2 - 4 meter (Prasetyono, 2012).
Tebu terutama bermanfaat untuk rehidrasi karena tebu tidak hanya mendinginkan tubuh tetapi juga meningkatkan energi tubuh dalam bentuk Protein dan Karbohidrat. Nutrisi dalam Tebu menguntungkan terhadap organ
dalam tubuh seperti ginjal, jantung, otak dan organ kelamin (McCaffrey, 2011).
Air tebu mengandung banyak vitamin dan mineral yang baik untuk tubuh. Air tebu kaya akan fosfor, zat besi, kalsium, kalium, dan magnesium. Penelitian sebelumnya telah menunjukkan bahwa mengkonsumsi air tebu
dapat membantu memulihkan kehilangan vitamin yang terjadi akibat gangguan demam (Anonim, 2012).
Mineral alami dan vitamin terdapat dalam air tebu sangat berharga seperti Fosfor, Kalsium, Besi, Magnesium dan Kalium. Air tebu bersifat alkalis sehingga bermanfaat untuk melawan penyakit kanker. Studi telah
menunjukkan bahwa tebu telah terbukti secara efektif melawan sel kanker prostat dan kanker payudara (McCaffrey, 2011).
Penetapan kadar kandungan pada air tebu masih jarang dilakukan sehingga dilakukan penelitian ini dalam skala laboratorium menggunakan
Spektrofotometri Serapan Atom (AAS).
Penelitian ini menggunakan metode spektrofotometri serapan atom karena Spektrometri serapan atom merupakan metode analisis kuantitatif logam yang
paling banyak digunakan (0,1 sampai 100 ppm) dengan ketelitian relatif 0,5 sampai 2%. Spektrofotometri digunakan terutama untuk penetapan kandungan
metal, alkali, dan alkali tanah. Penetapan yang paling banyak dilakukan adalah penetapan Ca, Na, K, dan Mg (Fifield, 1983). Selain itu, Metode spektrofotometri serapan atom adalah salah satu metode yang selektif, sensitif,
mudah, dan cepat untuk analisis kandungan logam dan mineral (Haswell, 1991).
Analisis kuantitatif merupakan penetapan banyaknya suatu zat tertentu yang ada dalam suatu sampel. Spektrofotometri serapan atom merupakan salah satu metode analisis kuantitatif yang sering digunakan. Segi utama dari
spektrometri serapan atom yaitu kepekaan dimana batas konsentrasi sebesar sekian bagian per juta atau milyar (Day dan Underwood, 1986).
1.2Perumusan Masalah
1. Apakah air tebu merah dan hijau mengandung kalium, kalsium, dan magnesium?
2. Berapakah kadar kalsium, kalium, dan magnesium yang terdapat dalam air tebu merah dan hijau?
3. Apakah air tebu merah dan air tebu hijau mempunyai perbedaan
kandungan kalsium, kalium, dan magnesium?
1.3Hipotesis
1. Air tebu merah dan hijau mengandung kalium, kalsium, dan magnesium.
2. kalsium, kalium, dan magnesium dalam air tebu merah dan hijau terdapat dalam kadar tertentu.
3. Air tebu merah dan hijau mempunyai perbedaan kandungan kalsium, kalium, dan magnesium.
1.4Tujuan Penelitian
1. Menentukan kadar kalsium, kalium, dan magnesium yang terdapat dalam
air tebu merah dan air tebu hijau dengan menggunakan spektrofotometri serapan atom (AAS).
2. Menentukan validitas dari metode analisis yang digunakan.
1.5 Manfaat Penelitian
Melalui penelitian ini dapat diketahui kadar kalsium, kalium, magnesium
BAB II
TINJAUAN PUSTAKA
2.1 Tebu
Tebusugar cane) adalah tanaman yang ditanam untuk
bahan baku
tropis. Tanaman ini termasuk jenis rumput-rumputan. Umur tanaman sejak
ditanam sampai bisa dipanen mencapai kurang lebih 1 tahun. Di Indonesia tebu
banyak dibudidayakan di pula
Tanaman tebu mempunyai banyak manfaat mulai dari daunnya dan
batangnya (masih ada airnya maupun sudah menjadi ampas). Daunnya cocok untuk pakan ternak, sedangkan batangnya dapat dimanfaatkan untuk dikonsumsi
langsung atau dibuat tebu dan vetsin. Setelah menjadi ampas pun batang tebu masih bermanfaat bagi manusia, diantaranya sebagai pakan ternak. Hal ini sangat memungkinkan karena tebu memiliki serat kasar dengan kandungan lignin yang
tinggi yaitu 19,7 % (Anonim, 2013).
Air tebu mempunyai banyak manfaat yaitu:
1. Oleh karena mudah dikonsumsi, air tebu memberikan energi pada tubuh dalam waktu yang singkat.
2. Air tebu juga bermanfaat mencegah dan mengobati sakit tenggorokan, batuk,
dan flu.
3. Air tebu mengandung beberapa nutrisi esensial, seperti kalsium, kalium, besi,
Menurut Anonim (2013), klasifikasi ilmiah tebu, yaitu :
Kerajaan:
Divisi:
Kelas:
Ordo:
Famili:
Genus: Saccharum
Spesies: Sacharum officinarum
Tebu diklasifikasikan ke dalam genus Saccharum, dimana dalam genus Saccharum tersebut, terbagi menjadi tiga spesies tanaman tebu yang dibudidayakan yaitu S. officinarum L., S. barberi Jesw., dan S. sinense Roxb.) dan
dua spesies tanaman tebu liar yaitu S. robustum Brandes, dan S. spontaneum L (Sleper dan Poehlman, 2006).
Spesies Sacharum officinarum termasuk ke dalam golongan tanaman tropis, dan dibudidayakan sehingga tidak ditemukan tumbuh secara liar. Tanaman tebu dikarakterisasikan mempunyai akar yang kuat, kandungan serat yang rendah,
serta kandungan sukrosa murni yang tinggi (Sleper dan Poehlman, 2006).
2.2 Mineral 2.2.1 Kalsium
Kalsium merupakan mineral yang paling banyak teradapat dalam tubuh, yaitu
jumlah ini, 99% berada di dalam jaringan keras, yaitu tulang dan gigi (Almatsier, 2001).
Menurut Almatsier (2001), kalsium mempunyai berbagai fungsi dalam tubuh, yaitu:
1. Pembentukan tulang dan gigi
2. Mengatur pembekuan darah 3. Kontraksi otot
4. Katalisator reaksi-reaksi biologik
2.2.2 Kalium
Kalium bersama dengan natrium, memegang peranan dalam pemeliharaan keseimbangan cairan dan elektrolit serta keseimbangan asam basa. Bersama
Kalsium, kalium berperan dalam transmmisi saraf dan relaksasi otot. Di dalam sel, kalium berfungsi sebagai katalisator dalam banyak reaksi biologik, terutama dalam metabolisme energi dan sintesis glikogen dan protein. Kalium berperan
dalam pertumbuhan sel (Almatsier, 2001).
2.2.3 Magnesium
Magnesium adalah salah satu mineral terbanyak di dalam tubuh. Sekitar 50% dari magnesium total yang terdapat dalam tubuh berada dalam tulang. Sisanya
terdapat dalam sel-sel jaringan dan organ. Hanya 1% magnesium tubuh yang berada dalam darah. Tubuh kita selalu bekerja keras untuk mempertahankan kadar
Kebanyakan pangan, terutama pangan nabati seperti kentang, padi-padian, dan buah-buahan, mengandung magnesium. Magnesium juga esensial dalam
metabolisme terutama reaksi yang melibatkan ATP (Montgomery dkk, 1983).
2.3 Penentuan Kadar Kalsium, Kalium, dan Magnesium
Penentuan kadar kalsium, kalium, dan magnesium dapat dilakukan dengan metode spektrofotometri serapan atom. Metode spektrofotometri serapan atom
berdasarkan pada prinsip absorpsi cahaya oleh atom. Atom-atom akan menyerap radiasi pada panjang gelombang tertentu tergantung pada sifat unsurnya (Rohman, 2007).
Penentuan kadar kalsium, kalium, dan magnesium dapat juga dilakukan dengan metode titrasi kompleksometri menggunakan reaksi zat-zat pengkompleks organik
dengan ion logam. Titrasi ini berdasarkan pembentukan senyawa kompleks antara logam dengan zat pengkompleks (Rohman, 2007).
2.4 Spektrofotometri
Benda-benda bercahaya seperti matahari atau bola lampu listrik
memancarkan suatu spektrum luas terdiri dari banyak panjang gelombang. Panjang gelombang itu berhubungan dengan cahaya tampak yang dapat mempengaruhi retina mata manusia dan karenanya dapat menyebabkan
kesan-kesan subjektif pada penglihatan, tetapi banyak dari radiasi yang dipancarkan oleh benda-benda panas terletak di luar daerah dimana mata peka, dan kita
Spektrofotometri serapan merupakan pengukuran suatu interaksi antara radiasi elektromagnetik dengan molekul atau atom dari suatu zaat kimia
(Ditjen POM, 1995).
2.5 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom lebih cenderung digunakan untuk pengujian kuantitatif dibandingkan kualitatif. Panjang gelombang dibaca
melalui rentang yang diinginkan dan spektrum yang tercatat. Panjang gelombang yang absortif dibandingkan dengan nilai panjang gelombang yang diketahui untuk elemen – elemen yang diperkirakan (Braun, 1987).
Prinsip dasar spektrofotometri serapan atom adalah interaksi antara radiasi elektromagnetik dengan sampel. Spektrofotometri serapan atom merupakan
metode yang sangat tepat untuk analisis zat pada konsentrasi rendah (Khopkar, 1990).
Teknik ini digunakan untuk menetapkan kadar ion logam dan mineral
tertentu dengan jalan mengukur intensitas emisi atau serapan cahaya pada panjang gelombang tertentu oleh uap atom unsur yang ditimbulkan dari bahan,
misalnya dengan mengalirkan larutan zat ke dalam api (Ditjen POM, 1995). Menurut Vogel (1991), pembentukan atom – atom logam dan mineral dalam nyala dapat terjadi bila suatu larutan sampel yang mengandung logam
dan mineral dimasukkan ke dalam nyala. Peristiwa yang terjadi secara singkat setelah sampel dimasukkan ke dalam nyala adalah:
2. Penguapan zat padat dengan dissosiasi menjadi atom – atom penyusunnya, yang mula – mula akan berada dalam keadaan dasar.
3. Beberapa atom dapat tereksitasi oleh energi panas nyala ke tingkatan-tingkatan energi yang lebih tinggi, dan mencapai kondisi dimana atom-atom tersebut akan memancarkan energi,
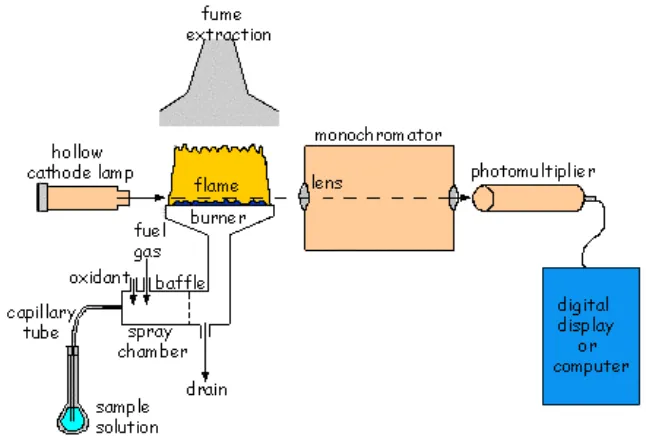
Adapun instrumentasi spektrofotometer serapan atom adalah sebagai berikut:
a. Sumber Radiasi
Sumber radiasi yang digunakan adalah lampu katoda berongga (hallow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup
yang mengandung suatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi dengan logam tertentu (Rohman, 2007).
b. Tempat Sampel
Sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan azas. Ada berbagai macam alat yang
digunakan untuk mengubah sampel menjadi uap atom-atomnya, yaitu: 1. Dengan Nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh nyala tergantung pada gas yang digunakan,
misalnya untuk gas asetilen – udara suhunya sebesar 2200°C (Rohman, 2007).
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil sedikit (hanya beberapa µl), lalu diletakkan dalam
tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom –
atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda sehingga terjadilah proses penyerapan
energi sinar yang memenuhi kaidah analisis kuantitatif (Rohman, 2007).
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih spektrum sesuai dengan panjang gelombang yang digunakan dalam
analisis dari sekian banyak spektrum yang dihasilkan lampu katoda (Rohman, 2007).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman (Rohman, 2007).
e. Amplifier
Amplifier merupakan suatu alat untuk memperkuat signal yang diterima dari detektor sehingga dapat dibaca sebagai alat pencatat hasil
(Readout) (Rohman, 2007). f. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan
berupa kurva yang menggambarkan absorbansi atau intensitas emisi (Rohman, 2007).
Gambar 1. Komponen Spektrofotometer Serapan Atom
2.5.1 Analisis Kuantitatif dengan Spektrofotometri Serapan Atom
Untuk keperluan analisis kuantitatif dengan spektrofotometri serapan atom, maka sampel harus dalam bentuk larutan. Yang penting untuk diingat adalah bahwa larutan yang akan dianalisis haruslah sangat encer. Menurut
Rohman (2007), ada beberapa cara untuk melarutkan sampel, yaitu: 1. Langsung dilarutkan dengan pelarut yang sesuai
2. Sampel dilarutkan dengan suatu asam
2.6 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya.
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis diuraikan dan didefinisikan sebagaimana cara penentuannya
(Harmita, 2004).
2.6.1 Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan (Harmita,
2004).
Perolehan kembali dapat ditentukan dengan metode adisi. Metode adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi
tertentu pada sampel yang diperiksa, lalu dianalisa dengan metode tersebut (Harmita, 2004).
2.6.2 Keseksamaan / Ketelitian (precision)
Ketelitian adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata – rata
jika prosedur ditetapkan secara berulang-ulang pada sampel-sampel yang diambil dari campuran yang homogen. Ketelitian diukur sebagai keterulangan
ketelitian metode jika dilakukan berulang kali oleh analisis yag sama pada kondisi yang sama dan dalam waktu interval yang pendek (Harmita, 2004).
2.6.3 Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan
blanko. Batas deteksi merupakan parameter uji batas. Batas kuantitasi merupakan parameter pada analisa renik dan diartikan sebagai kuantitasi
BAB III
METODE PENELITIAN
Penelitian ini merupakan penelitian deskriptif. Penelitian ini bertujuan untuk mengetahui kadar kalsium, kalium, dan magnesium pada air tebu merah dan hijau secara spektrofotometri serapan atom.
3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di laboratorium Penelitian, dan laboratorium Kimia
Farmasi Kualitatif Fakultas Farmasi USU. Penelitian dilakukan pada bulan April 2013 – Juli 2013.
3.2 Bahan-Bahan 3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah Air Tebu Hijau
(Saccharum officinarum L.) yang tumbuh di daerah kota Medan dan Air Tebu Merah yang tumbuh di Berastagi.
3.2.2 Bahan
Semua bahan yang digunakan dalam penelitian ini mempunyai kualitas pro analisis produksi E. Merck yaitu CaCO3, KCl, MgSo4, kuning titan 0,1%,
NaOH 2N, H2SO4 2N, asam pikrat dan asam nitrat pekat, kecuali dinyatakan lain yaitu akuabides.
3.3 Alat-Alat
saring Whatman No.42, krus porselen, spatula, dan alat-alat gelas (Pyrex dan Oberol).
3.4 Pembuatan Pereaksi
3.4.1 Larutan Standar Kalsium 1000 ppm
Larutan standar kalsium dibuat dengan melarutkan 250 mg CaCO3 dalam
campuran 20 ml air dan 5 ml HCl encer. Setelah larut sempurna, diencerkan dengan air hingga 100 ml (Ditjen POM, 1995).
3.4.2 Larutan Standar Kalium 1000 ppm
Larutan standar kalium dibuat dengan melarutkan 191 mg KCl dalam beberapa ml air dan diencerkan hingga 10 ml. Diencerkan sebagian dari larutan ini
dengan air dalam perbandingan 1 sampai 10 hingga kadar 1 mg kalium per ml (Ditjen POM, 1995).
3.4.3 Larutan Standar Magnesium 1000 ppm
Larutan standar magnesium dibuat dengan mengencerkan 1,014 g MgSO4 dengan air hingga 1000 ml (Ditjen POM, 1995).
3.4.4 Kuning Titan 0,1% (b/v)
Larutan kuning titan 0,1% dibuat dengan cara melarutkan 0,1 g Titan Yellow dalam 100 ml akuades (Vogel, 1979).
3.4.5 NaOH 2N
Larutan natrium hidroksida 2N dibuat dengan melarutkan 8,002 g natrium
3.4.6 H2SO4 1N
Larutan H2SO4 1N dibuat dengan ditambahkan secara hati-hati 57 ml asam
sulfat pekat ke dalam lebih kurang 100 ml air, dinginkan hingga suhu kamar dan encerkan dengan air hingga 1000 ml.
3.5 Prosedur Penelitian 3.5.1 Penyiapan Bahan
Pengambilan sampel dilakukan secara purposif yaitu tanpa membandingkan antara satu sampel dengan sampel yang lain karena sampel
dianggap homogen.
Tebu yang telah dikuliti, dicuci bersih dengan air mengalir, diperas airnya yang kemudian ditampung dalam wadah.
3.5.2 Destruksi Sampel
Sebanyak 1,25; 2,5; dan 5 ml air tebu dimasukkan ke dalam erlenmeyer
lalu ditambahkan 15 ml HNO3(p) dibiarkan selama ± 24 jam. Kemudian didestruksi dengan menggunakan hot plate sampai larutan berubah menjadi jernih dan uap nitrat habis pada suhu 100°C, didinginkan, dimasukkan ke dalam labu
tentukur 100 ml, dibilas erlenmeyer dengan akuabides sebanyak tiga kali, hasil pembilasan disatukan dengan larutan dalam labu tentukur ditepatkan dengan
akuabides sampai garis tanda. Disaring dengan kertas saring Whatman No. 42, dan ± 10% larutan pertama dibuang untuk menjenuhkan kertas saring kemudian larutan selanjutnya ditampung ke dalam botol. Larutan ini digunakan untuk uji
3.5.3 Pemeriksaan Kualitatif 3.5.3.1 Kalsium
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel dan ditambahkan 3 tetes H2SO4 2N akan segera menghasilkan endapan kristal putih (bila dilihat di mikroskop berbentuk seperti jarum) (Vogel,1979).
3.5.3.2 Kalium
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel, ditambahkan 3
tetes larutan asam pikrat akan menghasilkan endapan kuning (jika dilihat di mikroskop berbentuk jarum panjang) (Vogel, 1979).
3.5.3.3 Magnesium
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel, dan ditambahkan 3 tetes reagensia kuning titan dan 3 tetes NaOH 2N menghasilkan warna merah atau cherry merah (Vogel, 1979).
3.5.4 Pemeriksaan Kuantitatif
3.5.4.1 Pembuatan Kurva Kalibrasi Kalsium, Kalium, dan Magnesium
a. Masing–masing absorbansi larutan seri standar kalsium 0,2; 0,4; 0,6; 0,8 dan 1,0 mcg/ml diukur dengan spektrofotometer serapan atom pada panjang gelombang (λ)= 422,7 nm.
c. Masing–masing absorbansi larutan seri standar magnesium 0,2; 0,4; 0,6; 0,8 dan 1,0 mcg/ml diukur dengan spektrofotometer serapan atom pada panjang gelombang (λ)= 285,2 nm.
3.5.4.2 Penetapan Kadar Kalsium, Kalium, dan Magnesium dalam Sampel 3.5.4.2.1 Penetapan Kadar Kalsium dalam Air Tebu Merah
Larutan sampel hasil destruksi diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm
dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan standar kalsium. Konsetrasi kalsium dalam sampel ditentukan berdasarkan garis regresi dari kurva kalibrasi.
3.5.4.2.2 Penetapan Kadar Kalsium dalam Air Tebu Hijau
Larutan sampel hasil destruksi diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm
dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan standar kalsium. Konsetrasi kalsium dalam sampel
ditentukan berdasarkan garis regresi dari kurva kalibrasi.
3.5.4.2.3 Penetapan Kadar Kalium dalam Air Tebu Merah
Larutan sampel hasil destruksi diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 769,9 nm dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam
3.5.4.2.4 Penetapan Kadar Kalium dalam Air Tebu Hijau
Larutan sampel hasil destruksi diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 769,9 nm dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam
rentang kurva kalibrasi larutan standar kalium. Konsetrasi kalium dalam sampel ditentukan berdasarkan garis regresi dari kurva kalibrasi.
3.5.4.2.5 Penetapan Kadar Magnesium dalam Air Tebu Merah
Larutan sampel hasil destruksi diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 285,2 nm
dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan standar magnesium. Konsetrasi magnesium dalam sampel ditentukan berdasarkan garis regresi dari kurva kalibrasi.
3.5.4.2.6 Penetapan Kadar Magnesium dalam Air Tebu Hijau
Larutan sampel hasil destruksi diukur absorbansinya dengan
menggunakan spektrofotometer serapan atom pada panjang gelombang 285,2 nm dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada dalam
rentang kurva kalibrasi larutan standar magnesium. Konsetrasi magnesium dalam sampel ditentukan berdasarkan garis regresi dari kurva kalibrasi.
Kadar kalsium, kalium, dan magnesium dalam sampel dapat dihitung
(g) Sampel Berat n pengencera Faktor x (ml) Volume x (mcg/ml) i Konsentras (mcg/ml) Mineral
Kadar =
(Rohman, 2007)
3.5.5 Analisis Data Secara Statistik 3.5.5.1 Penolakan Hasil Pengamatan
Kadar Kalsium, Kalium, magnesium yang diperoleh dari hasil pengukuran
masing-masing larutan sampel dianalisis secara statistik. Menurut Sudjana (2005), standar deviasi dapat dihitung dengan rumus:
SD =
(
)
1 -n X -Xi 2
∑
Keterangan : Xi = Kadar sampel
−
X= Kadar rata-rata sampel
n = Jumlah pengulangan
Kadar Kalsium, Kalium, dan Magnesium yang diperoleh dari hasil pengukuran masing-masing ke enam larutan sampel, diuji secara statistik dengan uji Q. Q = terendah Nilai tertinggi Nilai terdekat yang Nilai dicurigai yang Nilai − −
[image:37.595.105.518.611.728.2]Hasil pengujian atau nilai Q yang diperoleh ditinjau terhadap daftar harga Q pada Tabel 1, apabila Q>Qkritis maka data tersebut ditolak (Rohman, 2007).
Tabel 1. Nilai Qkritis pada Taraf Kepercayaan 95%
Banyak data Nilai Qkritis
4 0,831
5 0,717
6 0,621
7 0,570
Menurut Sudjana (2005), untuk menentukan kadar kalsium, kalium, dan Magnesium di dalam sampel dengan taraf kepercayaan 95%, α = 0.05, dk = n-1,
dapat digunakan rumus:
Kadar Logam = µ= X ± (t(α/2, dk) x SD/√n Keterangan :
−
X = Kadar rata-rata sampel SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1) α = Tingkat kepercayaan
n = Jumlah pengulangan
3.5.5.2 Pengujian Beda Nilai Rata-Rata Antar Sampel
Sampel yang dibandingkan adalah independen dan jumlah pengamatan
masing-masing lebih kecil dari 30 dan variansi (σ) tidak diketahui sehingga dilakukan uji F. Menurut Sudjana (2005), untuk mengetahui apakah variasi kedua populasi sama (σ1 = σ2)atau berbeda (σ1≠ σ2) digunakan rumus:
Fo = 2
2 2 1 S S
Keterangan : Fo = Beda nilai yang dihitung S1 = Standar deviasi terbesar
S2 = Standar deviasi terkecil
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F maka
dilanjutkan uji dengan distribusi t dengan rumus:
) n ( + ) n ( S ) X X ( t
p 1 2
2 1 0 / 1 / 1 − =
Keterangan : X1 = kadar rata-rata sampel 1 n 1 = Jumlah perlakuan sampel 1 X2 = kadar rata-rata sampel 2 n 2 = Jumlah perlakuan sampel 2 Sp = Simpangan baku
jika Fo melewati nilai kritis F, dilanjutkan uji dengan distribusi t dengan rumus :
√S12/n1 + S22/n2
Keterangan : X1 = kadar rata-rata sampel 1 S1 = Standar deviasi sampel 1
X2 = kadar rata-rata sampel 2 S2 = Standar deviasi sampel 2 n 1 = Jumlah perlakuan sampel 1 n 2 = Jumlah perlakuan sampel 2
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai kritis t, dan sebaliknya (Sudjana, 2005).
3.5.6 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode
penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel setelah penambahan larutan standar
dengan konsentrasi tertentu (Ermer dan Miller, 2005).
Air tebu merah dan air tebu hijau diukur secara seksama sebanyak 2,5 ml
lalu ditambahkan 0,05 ml larutan standar kalsium 0,1 mcg/ml; 0,025 ml larutan standar kalium 0,1 mcg/ml; dan 0,02 ml larutan stadar magnesium 0,1 mcg/ml, kemudian dilanjutkan dengan prosedur destruksi seperti yang telah dilakukan
sebelumnya.
Persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
% Perolehan Kembali
= 100%
n ditambahka yang
baku mineral jumlah
awal sampel dalam
mineral jumlah
-sampel dalam
mineral l
Kadar tota ×
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat
diperoleh dari kalibrasi standar yang diukur sebanyak 6 sampai 10 kali, dan dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku (SB) =
(
)
2
2
− −
∑
n Yi Y
Batas deteksi (LOD) = slope
SB x 3
Batas kuantitasi (LOQ) = slope
SB x 10
BAB IV
HASIL DAN PEMBAHASAN 4.1 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk mengetahui ada atau tidaknya ion-ion kalium, kalsium, dan magnesium dalam
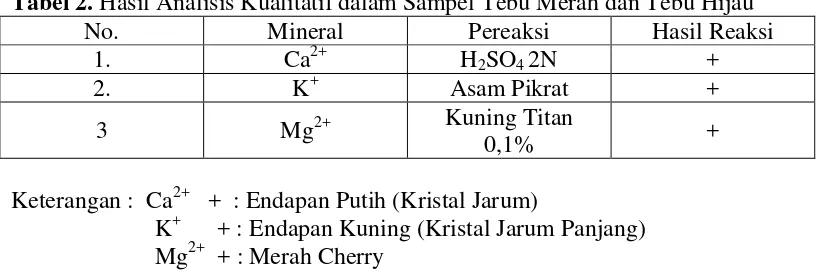
[image:41.595.108.521.284.420.2]sampel yang akan dianalisis secara kuantitatif dengan spektrofotometer serapan atom. Data dapat dilihat pada Tabel 2.
Tabel 2. Hasil Analisis Kualitatif dalam Sampel Tebu Merah dan Tebu Hijau
No. Mineral Pereaksi Hasil Reaksi
1. Ca2+ H2SO4 2N +
2. K+ Asam Pikrat +
3 Mg2+ Kuning Titan
0,1% +
Keterangan : Ca2+ + : Endapan Putih (Kristal Jarum)
K+ + : Endapan Kuning (Kristal Jarum Panjang) Mg2+ + : Merah Cherry
Tabel di atas menunjukkan bahwa larutan sampel yang diperiksa mengandung ion kalsium, kalium dan magnesium. Reaksi dengan penambahan
H2SO4 2N menghasilkan endapan putih dan kristal jarum apabila diamati di bawah mikroskop (Gambar dapat dilihat pada Lampiran 34, halaman 85). Reaksi dengan
penambahan Asam Pikrat menghasilkan endapan kuning dan kristal jarum panjang apabila diamati dibawah mikroskop (Gambar dapat dilihat pada Lampiran 34, halaman 85). Dan terakhir, reaksi dengan penambahan kuning titan
4.2 Pemeriksaan Kuantitatif
4.2.1 Kurva Kalibrasi Kalsium, Kalium, dan Magnesium
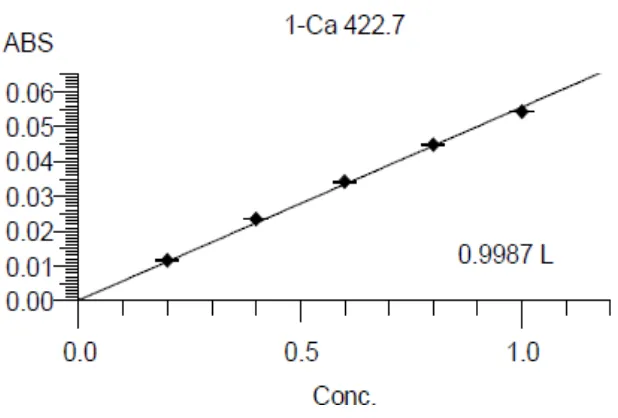
Kurva kalibrasi kalsium, kalium dan magnesium diperoleh dengan cara mengukur absorbansi dari larutan standar pada panjang gelombang masing-masing. Dari pengukuran kurva kalibrasi diperoleh persamaan garis regresi yaitu
Y = 0.0554X + 0,000167 untuk kalsium, Y= 0,0726X + 0,00247 untuk kalium, dan Y = 0,543886X + 0,011657 untuk magnesium.
[image:42.595.176.485.344.553.2]Kurva kalibrasi larutan standar kalsium, kalium, dan magnesium dapat dilihat pada Gambar 2 sampai dengan Gambar 4.
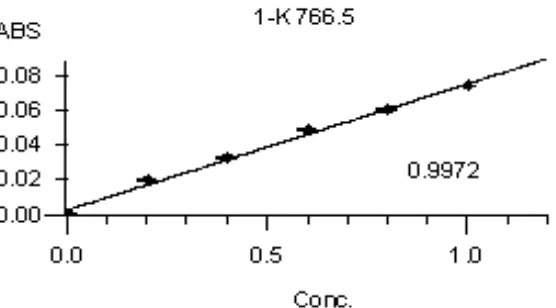
Gambar 3. Kurva Kalibrasi Seri (0,2; 0,4; 0,6; 0,8; 1 mcg/ml) Larutan Standar Kalium untuk Penetapan Kadar Kalium
Gambar 4. Kurva Kalibrasi Seri (0,2; 0,4; 0,6; 0,8; 1 mcg/ml) Larutan Standar Magnesium untuk Penetapan Kadar Magnesium
Berdasarkan kurva di atas diperoleh hubungan yang linear antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) kalsium sebesar 0,9987, kalium sebesar 0,9968 dan magnesium sebesar 0,9990. Nilai r ≥ 0,97 menunjukkan
adanya korelasi linier yang menyatakan adanya hubungan antara X (Konsentrasi) dan Y (Absorbansi) (Ermer dan Miller, 2005). Data hasil pengukuran absorbansi
larutan standar kalsium, kalium, dan magnesium dan perhitungan persamaan garis regresi dapat dilihat pada Lampiran 1 – 3, halaman 34 - 38.
[image:43.595.156.452.297.457.2]Penentuan kadar kalsium, kalium, dan magnesium dilakukan secara spektrofotometri serapan atom dimana sampel terlebih dulu didestruksi basah
dengan HNO3 kemudian dilarutkan dan diukur pada spektrofotometri serapan atom. Konsentrasi mineral kalsium, kalium, dan magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan standar
masing-masing mineral. Data dan contoh perhitungan dapat dilihat pada Lampiran 4 - 9, halaman 40 - 45.
[image:44.595.105.516.402.499.2]Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat dilihat pada Lampiran 10 - 12, halaman 46 - 52). Hasil analisis kuantitatif kadar kalsium, kalium, dan magnesium dalam sampel dapat dilihat pada Tabel 3.
Tabel 3. Hasil Analisis Kuantitatif Kadar Kalsium, Kalium, dan Magnesium dalam Sampel
No. Sampel Kadar Kalsium (mcg/ml)
Kadar Kalium (mcg/ml)
Kadar Magnesium
(mcg/ml) 1. Air Tebu
Merah 10,5160 ± 0,1032 59,0587 ± 0,2688 17,5020 ± 0,3730 2. Air Tebu
Hijau 19,1088 ± 0,1367 54,7287 ± 0,6920 5,7333 ± 0,1976 Keterangan: Hasil yang diperoleh merupakan rata-rata dari 6 kali pengulangan
Hasil di atas menunjukkan bahwa sampel air tebu merah memiliki kadar kalsium, kalium, dan magnesium yang lebih tinggi dibandingkan air tebu hijau.
Salah satu faktor penyebab terjadinya perbedaan kandungan kalsium, kalium, dan magnesium pada air tebu adalah tanah tempat penanaman tebu yang
kalsium, kalium, dan magnesium pada air tebu merah lebih tinggi dibandingkan dengan air tebu hijau.
Data yang diperoleh kemudian diuji kembali secara statistik untuk mengetahui beda nilai kadar rata-rata logam antar kedua sampel (Perhitungan dapat dilihat pada Lampiran 16 - 18, halaman 64 - 68). Hasil perhitungan uji
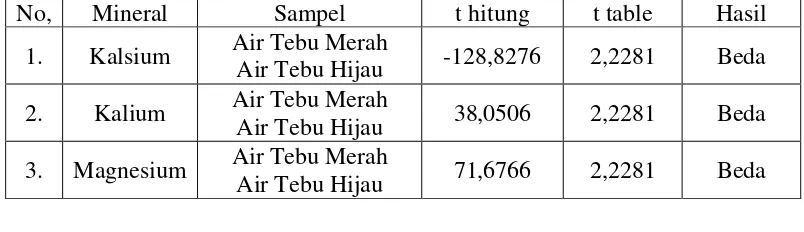
[image:45.595.115.517.293.409.2]statistik dapat dilihat pada Tabel 4.
Tabel 4. Hasil Uji Beda Nilai Rata-rata Kadar Kalsium, Kalium, dan Magnesium antar Sampel
No, Mineral Sampel t hitung t table Hasil 1. Kalsium Air Tebu Merah
Air Tebu Hijau -128,8276 2,2281 Beda 2. Kalium Air Tebu Merah
Air Tebu Hijau 38,0506 2,2281 Beda 3. Magnesium Air Tebu Merah
Air Tebu Hijau 71,6766 2,2281 Beda
. Berdasarkan Tabel 4 di atas dapat diketahui bahwa kadar rata-rata Kalsium, Kalium, dan Magnesium pada air tebu merah lebih besar dibandingkan
dengan air tebu hijau. Hasil uji statistik, ternyata kandungan kalsium, kalium dan magnesium antara air tebu merah dan air tebu hijau terdapat perbedaan yang signifikan. Hal ini dapat disebabkan beberapa faktor antara lain kondisi tanah,
unsur kimia tanah, kandungan mineral, jenis mineral dan kerusakan tanah akibat pencemaran baik oleh bahan pupuk (pestisida) atau logam berat serta industri
(Darmono, 1995).
Hasil uji perolehan kembali (recovery) kadar kalsium, kalium, dan magnesium setelah penambahan masing-masing larutan standar kalsium, kalium,
dan magnesium dalam sampel dapat dilihat pada Lampiran 19 - 21, halaman 70 - 72. Persen recovery kalsium, kalium, dan magnesium dalam sampel dapat dilihat pada Tabel 5.
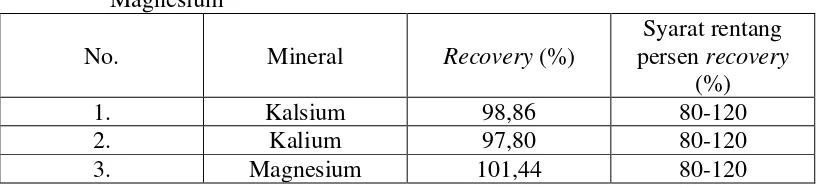
Tabel 5. Persen Uji Perolehan Kembali (recovery) Kadar Kalsium, Kalium, dan Magnesium
No. Mineral Recovery (%)
Syarat rentang persen recovery
(%)
1. Kalsium 98,86 80-120
2. Kalium 97,80 80-120
3. Magnesium 101,44 80-120
Berdasarkan Tabel 5 di atas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali (recovery) untuk kandungan kalsium adalah 98,86 %, untuk
kandungan kalium adalah 97,80%, dan untuk kandungan magnesium adalah 101,44%. Persen recovery tersebut menunjukkan kecermatan kerja yang baik pada saat pemeriksaan kadar kalsium, kalium dan magnesium dalam sampel. Hasil uji
perolehan kembali (recovery) ini memenuhi syarat akurasi yang telah ditetapkan, rata-rata hasil perolehan kembali (recovery) berada pada rentang 80-120% (Ermer
dan Miller, 2005).
4.2.4 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalsium, kalium, dan magnesium
diperoleh batas deteksi dan batas kuantitasi untuk mineral tersebut. Dari hasil perhitungan diperoleh batas deteksi untuk pengukuran kalsium sebesar 0,06464
[image:46.595.108.516.244.337.2]sedangkan batas kuantitasi sebesar 0,2515 mcg/ml untuk kalsium, 0,3164
mcg/ml untuk kalium dan 018934 mcg/ml untuk magnesium.
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
1. Air tebu merah dan air tebu hijau yang diperiksa mengandung mineral kalsium, kalium dan magnesium.
2. Hasil penetapan kadar dengan menggunakan spektrofotometri serapan atom menunjukkan bahwa kadar kalsium, kalium, dan magnesium pada air tebu
merah adalah 19,1088 mcg/ml untuk kalsium; 59,0587 mcg/ml untuk kalium; 17,502 mcg/ml untuk magnesium. Sedangkan kadar kalsium, kalium dan magnesium pada air tebu hijau adalah 10,516 mcg/ml untuk kalsium; 54,7287
mcg/ml untuk kalium; 5,7333 mcg/ml untuk magnesium.
3. Hasil uji statistik yaitu uji beda rata-rata kadar kalsium, kalium dan magnesium
antara air tebu merah dan hijau, menyimpulkan bahwa kadar kalsium, kalium, dan mgnesium pada air tebu merah lebih tinggi dari air tebu hijau dengan tingkat kepercayaan 95%.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk melakukan analisis
DAFTAR PUSTAKA
Almatsier, S. (2001). Prinsip Dasar Ilmu Gizi. Jakarta: PT Gramedia Pustaka Utama. Hal. 233 - 243.
Anonim. (2012). Khasiat Tebu dan Kandungan Gizinya.
Diakses pada tanggal 20 Agustus 2013.
Anonim. (2013). Tebu
Januari 2013.
Darmono. (1995). Logam dalam Sistem Biologi Makhluk Hidup. Jakarta: UI Press. Hal. 14.
Day, R.A., dan Underwood, A.L. (1986). Quantitative Analysis. Edisi Kelima. Penerjemah: Hadyana Pudjaatmaka. (1996). Analisis Kimia Kuantitatif. Jakarta: Penerbit Erlangga. Hal. 3.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Departemen Kesehatan RI. Jakarta. Hal. 748.
Ditjen POM. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Departemen Kesehatan RI. Hal. 1122, 1173.
Emer, J., dan Miller, J.H.M. (2005). Method Validation in Pharmaceutical Analysis. A Guide to Best Pratice. Weinheim: Wiley-VCH. Hal. 89.
Fifield, F.W. (1983). Principles and practice of Analytical Chemistry. Edisi Kedua. London: International Textbook Company Limited. Hal. 271, 276. Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara
Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 1(3): 117-122, 127-131.
Haswell, S.J. (1991). Atomic Absorption Spectrophotometry. Amsterdam: Elsevier. Hal. 202, 207-208.
Khopkar, S.M. (1990). Basic Concepts of Official Analytical Chemistry. India: New Age International Publisher. Hal. 189-191, 194-196.
McCaffrey, D. (2011). Raw Sugarcane Juice’s Nature perfect Wonder Food.
22 Agustus 2013.
Penerjemah: M. Ismadi. Biokimia: Suatu Pendekatan Berorientasi-kasus. (1993). Yogyakarta: Gadjah Mada University Press. Hal. 38.
Prasetyono, D.S. (2012). A-Z Daftar Tanaman Obat Ampuh di Sekitar Kita. Jogjakarta: Flashbooks. Hal. 67-68.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar Universitas Islam Indonesia. Hal. 298.
Sleper, D.A., dan Poehlman, J.M. (2006). Breeding Field Crops. Edisi Kelima. USA: Blackwell Publishing Professional. Hal. 377.
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Hal. 168-169.
Vogel, A.I. (1979). Textbook of Macro and Semimicro Qualitative Inorganic analysis. Edisi Kelima. Bagian I. Penerjemah: Setiono, Latief, dan Hadyana Pudjaatmaka. (1990). Analisis Anorganik Kualitatif Makro dan Semimikro. Jakarta: PT. Kalman Media Pustaka. Hal. 212.
Lampiran 1. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) No. Konsentrasi (mcg/ml)
(X)
Absorbansi (Y)
1. 0,0000 -0,0012
2. 0,2000 0,0116
3. 0,4000 0,0235
4. 0,6000 0,0342
5. 0,8000 0,0448
6. 1,0000 0,0543
No. X Y XY X2 Y2 x10-4
1. 0,0000 -0,0012 0,0000 0,0000 0,0144
2. 0,2000 0,0116 0,0023 0,0400 1,3456
3. 0,4000 0,0235 0,0094 0,1600 5,5225
4. 0,6000 0,0342 0,0205 0,3600 11,6964
5. 0,8000 0,0448 0,0358 0,6400 20,0704
6. 1,0000 0,0543 0,0543 1,0000 29,4849
∑ 3,0000
X = 0,5000
0,1672 Y= 0,0279
0,1224 2,2000 68,1342
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)(
)
(
3,0000)
/6 2000 , 2 6 / 1672 , 0 0000 , 3 1224 , 0 2 − − = 0,0554 Y = a X + b b = Y − aX= 0,0279 – (0,0554)(0,5000) = 0,000167
Maka persamaan garis regresinya adalah: Y = 0,0554X + 0,000167
=
(
)(
)
(
)
Lampiran 2. Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r). No. Konsentrasi (mcg/ml)
(X)
Absorbansi (Y)
1. 0,0000 -0,0005
2. 0,2000 0,0193
3. 0,4000 0,0323
4. 0,6000 0,0480
5. 0,8000 0,0598
6. 1,0000 0,0737
No. X Y XY X2 Y2 x10-4
1. 0,0000 -0,0005 0,0000 0,0000 0,0025
2. 0,2000 0,0193 0,0039 0,4000 3,725
3. 0,4000 0,0323 0,0129 0,1600 10,4330
4. 0,6000 0,0480 0,0288 0,3600 23,0400
5. 0,8000 0,0598 0,0478 0,6400 35,7600
6. 1,0000 0,0737 0,0737 1,0000 54,3200
∑ 3,0000
X = 0,5000
0,2326 Y = 0,0388
0,1671 2,2000 127,3000
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)
= 0,0388 – (0,0726)(0,5000) = 0,00247
Maka persamaan garis regresinya adalah: Y = 0,0726X + 0,000247
=
(
)
(
)
{
2,2000 3,0000 /6}
{
0127,3000 x10(
0,2326)
/6}
6 / ) 2326 , 0 ( 0000 , 3 1672 , 0 2 4 -2 − − − = 0509 , 0 0508 , 0 = 0,9968Lampiran 3. Data Kalibrasi Magnesium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r).
No. Konsentrasi (mcg/ml) (X)
Absorbansi (Y)
1. 0,0000 -0,0004
2. 0,2000 0,1248
3. 0,4000 0,2390
4. 0,6000 0,3449
5. 0,8000 0,4494
6. 1,0000 0,5451
No. X Y XY X2 Y2
1. 0,0000 -0,0004 0,0000 0,0000 0,0000
2. 0,2000 0,1248 0,0249 0,4000 0,0156
3. 0,4000 0,2390 0,0956 0,1600 0,0571
4. 0,6000 0,3449 0,2069 0,3600 0,1189
5. 0,8000 0,4494 0,3595 0,6400 0,2019
6. 1,0000 0,5451 0,5451 1,0000 0,2971
∑ 3,0000 X = 0,5000
1,7028 Y= 0,2838
1,2321 2,2000 0,6907
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)
(
3,0000)
/6 2000 , 2 6 / ) 7028 , 1 ( 0000 , 3 2321 , 01 2 − − = 0,5439Y = a X + b b = Y − aX
= 0,2386 – (0,5439)(0,5000) = 0,011657
Maka persamaan garis regresinya adalah: Y = 0,5439X + 0,011657
=
(
)
(
)
{
2,2000 3,0000 /6}
{
0,6907(
1,7208)
/6}
6 / ) 7208 , 1 ( 0000 , 3 2321 , 1 2 2 − − − = 3811 , 0 3807 , 0 = 0,9990Lampiran 4. Contoh Perhitungan Kadar Kalsium dalam Sampel
Dengan menggunakan Persamaan Garis Regresi
Contoh Perhitungan konsentrasi Ca dalam sampel yang absorbansi = 0,0148. X = Konsemtrasi sampel
Y = Absorbansi sampel
Persamaan garis regresi diperoleh dari kurva kalibrasi adalah Y = 0,0554X + 0,167 x10-3
X =
0,0554 x10 0,1670
0,0269− -3
X = 0,4826 mcg/ml
Maka konsentrasi sampel tersebut adalah 0,4826 mcg/ml
W F x V x C (mcg/ml)
Kadar = p
Keterangan : C= Konsentrasi larutan sampel (mcg/ml) V = Volume larutan sampel (ml)
Fp= Faktor pengenceran
W = Volume pemipetan sampel (ml)
Kadar =
ml mlx x 5 , 2 ) 1 ( 100 ml 0,4826mcg/
= 19,304 mcg/ml
Maka kadar Ca yang terkandung dalam sampel adalah 19,304 mcg/ml
Lampiran 5. Data Hasil Analisis Kadar Kalsium dalam Sampel
Sampel No. Volume Sampel (ml) Absorbansi (A) Konsentrasi (mcg/ml) Kadar (mcg/ml) TM
1 2,50 0,0269 0,4826 19,304
2 2,50 0,0264 0,4735 18,9408
3 2,50 0,0265 0,4753 19,012
4 2,50 0,0266 0,4771 19,084
5 2,50 0,0267 0,4789 19,156
6 2,50 0,0267 0,4789 19,156
TH
1 2,50 0,0148 0,2702 10,8080
2 2,50 0,0147 0,2623 10,4920
3 2,50 0,0148 0,2641 10,5640
4 2,50 0,0149 0,2659 10,6360
5 2,50 0,0147 0,2623 10,4920
Keterangan : TM : Air Tebu Merah TH : Air Tebu Hijau
Lampiran 6. Contoh Perhitungan Kadar Kalium dalam Sampel Dengan menggunakan Persamaan Garis Regresi
Contoh Perhitungan konsentrasi K dalam sampel yang absorbansi = 0,0562. X = Konsemtrasi sampel
Y = Absorbansi sampel
Persamaan garis regresi diperoleh dari kurva kalibrasi adalah Y = 0,0726X + 0,00247
X =
0,0726 0,00247 0,0562−
= 0,7402 mcg/ml
Maka konsentrasi sampel tersebut adalah 07402 mcg/ml
W F x V x C (mcg/ml)
Kadar = p
Keterangan : C= Konsentrasi larutan sampel (mcg/ml) V = Volume larutan sampel (ml)
Fp= Faktor pengenceran
W = Volume pemipetan sampel
Kadar =
ml
mlx x
25 , 1
) 1 ( 100 mcg/ml
0,7402
= 59,216 mcg/ml
Maka kadar K yang terkandung dalam sampel adalah 59,216 mcg/ml
Sampel No. Volume Sampel
(ml)
Absorbansi (A)
Konsentrasi (mcg/ml)
Kadar (mcg/ml)
TM
1 1,25 0,0562 0,7402 59,2160
2 1,25 0,0560 0,7374 58,9920
3 1,25 0,0559 0,7353 58,8240
4 1,25 0,0558 0,7346 58,7680
5 1,25 0,0561 0,7387 59,0960
6 1,25 0,0565 0,7432 59,4560
TH
1 1,25 0,0522 0,6844 54,7520
2 1,25 0,0521 0,6836 54,6888
3 1,25 0,0523 0,6864 54,9120
4 1,25 0,0522 0,6844 54,7520
5 1,25 0,0520 0,6822 54,5785
6 1,25 0,0521 0,6836 54,6888
Keterangan : TM : Air Tebu Merah TH : Air Tebu Hijau
Lampiran 8. Contoh Perhitungan Kadar Magnesium dalam Sampel Dengan menggunakan Persamaan Garis Regresi
Contoh Perhitungan konsentrasi Mg dalam sampel yang absorbansi = 0,2437. X = Konsemtrasi sampel
Y = Absorbansi sampel
Persamaan garis regresi diperoleh dari kurva kalibrasi adalah Y = 0,5439X + 0,011657
X =
0,5439 0,011657
-0,2437
X = 0,4263 mcg/ml
W F x V x C (mcg/ml)
Kadar = p
Keterangan : C= Konsentrasi larutan sampel (mcg/ml) V = Volume larutan sampel (ml)
Fp= Faktor pengenceran
W = Volume pemipetan sampel
Kadar =
ml
mlx x
5 , 2
1 100 mcg/ml
0,4263
= 17,052 mcg/ml
Lampiran 9. Data Hasil Analisis Kadar Magnesium dalam Sampel Sampel No. Volume
Sampel (ml)
Absorbansi (A)
Konsentrasi (mcg/ml)
Kadar (mcg/ml)
TM
1 5,0000 0,2437 0,4263 17,0520
2 5,0000 0,2476 0,4314 17,2560
3 5,0000 0,2496 0,4335 17,3400
4 5,0000 0,2563 0,4495 17,9800
5 5,0000 0,2544 0,4459 17,8360
6 5,0000 0,2505 0,4387 17,5480
TH
1 2,500 0,1667 0,2851 5,7020
2 2,500 0,1654 0,2822 5,6440
3 2,500 0,1722 0,2949 5,8980
4 2,500 0,1665 0,2847 5,6940
5 2,500 0,1682 0,2878 5,7565
6 2,500 0,1668 0,2853 5,7050
Lampiran 10. Perhitungan Kadar Kalsium dalam Sampel 1.Air Tebu Merah
A.Konsentrasi Ca dalam sampel Y = 0,0554X + 0,000167
Y = Absorbansi, X= Konsentrasi
1) 0,0269 = 0,0554X + 0,000167 X =0,4826 mcg/ml
2) 0,0264 = 0,0554X + 0,000167 X =0,4735 mcg/ml 3) 0,0265 = 0,0554X + 0,000167
X =0,4753 mcg/ml 4) 0,0266 = 0,0554X + 0,000167
X =0,4771 mcg/ml 5) 0,0267 = 0,0554X + 0,000167
X =0,4789 mcg/ml
6) 0,0267 = 0,0554X + 0,000167 X =0,4789 mcg/ml
B.Kadar Ca dalam sampel
W F x V x C (mcg/ml)
Kadar = p
Keterangan : C= Konsentrasi larutan sampel (mcg/ml) V = Volume larutan sampel (ml)
Fp= Faktor pengenceran
W = Volume pemipetan sampel 1) Kadar 1 = 0,4826���/���100���1
2) Kadar 1 = 0,4735���/���100���1
2,5�� = 18,9408 mcg/ml
3) Kadar 1 = 0,4753���/���100���1
2,5�� = 19,012 mcg/ml
4) Kadar 1 = 0,4771���/���100���1
2,5�� = 19,084 mcg/ml
5) Kadar 1 = 0,4789���/���100���1
2,5�� = 19,156 mcg/ml
6) Kadar 1 = 0,4789���/���100���1
2,5�� = 19,156 mcg/ml
2.Air Tebu Hijau
A.Konsentrasi Ca dalam sampel Y = 0,0554X + 0,000167
Y = Absorbansi, X= Konsentrasi 1) 0,0148 = 0,0554X + 0,000167
X =0,2641 mcg/ml 2) 0,0147 = 0,0554X + 0,000167
X =0,2623 mcg/ml
3) 0,0148 = 0,0554X + 0,000167 X =0,2641 mcg/ml
4) 0,0149 = 0,0554X + 0,000167 X =0,2659 mcg/ml 5) 0,0147 = 0,0554X + 0,000167
6) 0,0145 = 0,0554X + 0,000167 X =0,2587 mcg/ml
B.Kadar Ca dalam sampel
W F x V x C (mcg/ml)
Kadar = p
Keterangan : C= Konsentrasi larutan sampel (mcg/ml) V = Volume larutan sampel (ml)
Fp= Faktor pengenceran
W = Volume pemipetan sampel 1) Kadar 1 = 0,2641���/���100���1
2,5�� = 10,564 mcg/ml
2) Kadar 1 = 0,2623���/���100���1
2,5�� = 10,492 mcg/ml
3) Kadar 1 = 0,2641���/���100���1
2,5�� = 10,564 mcg/ml
4) Kadar 1 = 0,2659���/���100���1
2,5�� = 10,636 mcg/ml
5) Kadar 1 = 0,2623���/���100���1
2,5�� = 10,492 mcg/ml
6) Kadar 1 = 0,2587���/���100���1
2,5�� = 10,548 mcg/ml
Lampiran 11. Perhitungan Kadar Kalium dalam Sampel 1.Air Tebu Merah
Y = Absorbansi, X= Konsentrasi 1) 0,0562 = 0,0726X + 0,00247
X =0,7402 mcg/ml 2) 0,0560 = 0,0726X + 0,00247
X =0,7374 mcg/ml
3) 0,0559 = 0,0726X + 0,00247 X =0,7353 mcg/ml
4) 0,0558 = 0,0726X + 0,00247 X =0,7346 mcg/ml 5) 0,0561 = 0,0726X + 0,00247
X =0,7387 mcg/ml 6) 0,0565 = 0,0726X + 0,00247
X =0,7432 mcg/ml B.Kadar K dalam sampel
W F x V x C (mcg/ml)
Kadar = p
Keterangan : C= Konsentrasi larutan sampel (mcg/ml) V = Volume larutan sampel (ml)
Fp= Faktor pengenceran
W = Volume pemipetan sampel 1) Kadar 1 = 0,7402���/���100���1
1,25�� = 59,216 mcg/ml
2) Kadar 1 = 0,7374���/���100���1
1,25�� = 58,992 mcg/ml
3) Kadar 1 = 0,7353���/���100���1
4) Kadar 1 = 0,7346���/���100���1
1,25�� = 58,768 mcg/ml
5) Kadar 1 = 0,7387���/���100���1
1,25�� = 59,096 mcg/ml
6) Kadar 1 = 0,7432���/���100���1
1,25�� = 59,456 mcg/ml
2.Air Tebu Hijau
A.Konsentrasi K dalam sampel Y = 0,0726X + 0,00247
Y = Absorbansi, X= Konsentrasi 1) 0,0522 = 0,0726X + 0,00247
X =0,6844 mcg/ml 2) 0,0513 = 0,0726X + 0,00247
X =0,6836 mcg/ml
3) 0,0523 = 0,0726X + 0,00247 X =0,6864 mcg/ml
4) 0,0522 = 0,0726X + 0,00247 X =0,6844 mcg/ml 5) 0,0520 = 0,0726X + 0,00247
X =0,6822 mcg/ml 6) 0,0521 = 0,0726X + 0,00247
W F x V x C (mcg/ml)
Kadar = p
Keterangan : C= Konsentrasi larutan sampel (mcg/ml) V = Volume larutan sampel (ml)
Fp= Faktor pengenceran
W = Volume pemipetan sampel
1) Kadar 1 = 0,6844���/���100���1
1,25�� = 54,752 mcg/ml
2) Kadar 1 = 0,6836���/���100���1
1,25�� = 54,6888 mcg/ml
3) Kadar 1 = 0,6864���/���100���1
1,25�� = 54,912 mcg/ml
4) Kadar 1 = 0,6844���/���100���1
1,25�� = 54,752 mcg/ml
5) Kadar 1 = 0,6822���/���100���1
1,25�� = 54,5785 mcg/ml
6) Kadar 1 = 0,6836���/���100���1
1,25�� = 54,6888 mcg/ml
Lampiran 12. Perhitungan Kadar Magnesium dalam Sampel 1. Air Tebu Merah
A.Konsentrasi Mg dalam sampel Y = 0,543886X + 0,011657 Y = Absorbansi, X= Konsentrasi
X =0,4313 mcg/ml 3) 0,2496 = 0,543886X + 0,011657
X =0,4335 mcg/ml 4) 0,2563 = 0,543886X + 0,011657
X =0,4495 mcg/ml
5) 0,2544 = 0,543886X + 0,011657 X =0,4459 mcg/ml
6) 0,2505 = 0,543886X + 0,011657 X =0,4387 mcg/ml
B.Kadar Mg dalam sampel
W F x V x C (mcg/ml)
Kadar = p
Keterangan : C= Konsentrasi larutan sampel (mcg/ml) V = Volume larutan sampel (ml)
Fp= Faktor pengen