Lampiran 2. Gambar Tumbuhan Gaharu, Serbuk Simplisia Daun Gaharu (Aquilaria malacensis)
Pohon Gaharu
Lampiran 5. Perhitungan Pemberian Dosisi
Dosis pemberian seduhan teh pada mencit yaitu 130 mg/kgbb, di dapat dari 1 gram simplisia dengan konversi 0,0026 pada mencit, maka di dapat dosis 130 mg/kgbb
1 gram simplisia = 1000 mg simplisia 1000 mg x 0,0026 = 2,6 mg
Dengan berat badan mencit 20 gram
2,6 ��
20 �1000 = 130 ��
Dosis yang diberikan pada masing-masing mencit berbeda, sehingga pemberian dosisnya menggunakan 1 % berat badan mencit.
Oral sonde dan squite
Mencit
Mencit yang telah di bedah
Kontrol Dosis 130 mg/kgbb
Dosis 260mg/kgbb Dosis 390mg/kgbb
Gambar Organ ginjal
kontrol 130 mg/kgbb
260 mg/kgbb
390 mg/kgbb
Lampiran 10. Berat Badan Mencit Betina
Multiple Comparisons Tukey HSD
Dependent Variable (I) dosis (J) dosis
Mean Difference
(I-J) Std. Error Sig.
1.000 -.90000 2.23338 .994 -8.2502 6.4502 3.000 -.16667 2.23338 1.000 -7.5169 7.1836 4.000 -2.06667 2.23338 .881 -9.4169 5.2836 3.000 0 7.76667* 2.23338 .037 .4164 15.1169 1.000 -.73333 2.23338 .997 -8.0836 6.6169 2.000 .16667 2.23338 1.000 -7.1836 7.5169 4.000 -1.90000 2.23338 .908 -9.2502 5.4502 4.000 0 9.66667* 2.23338 .010 2.3164 17.0169 1.000 1.16667 2.23338 .983 -6.1836 8.5169 2.000 2.06667 2.23338 .881 -5.2836 9.4169 3.000 1.90000 2.23338 .908 -5.4502 9.2502
ANOVA
Sum of Squares df Mean Square F Sig. BBharike0 Between Groups 26.444 4 6.611 .838 .531
Within Groups 78.873 10 7.887
Total 105.317 14
BBharike7 Between Groups 52.623 4 13.156 1.913 .185
Within Groups 68.767 10 6.877
Total 121.389 14
BBharike14 Between Groups 176.636 4 44.159 5.902 .011
Within Groups 74.820 10 7.482
BBharike0 Between Groups 183.978 4 45.994 4.137 .019
Data Awal Berat Badan
Lampiran Ginjal Kanan Mencit Betina
Lampiran Berat Organ Hati Mencit Betina
Lampiran Organ Ginjal Kiri Mencit Betina
Berat Awal Organ Mencit Betina
Kelompok Hati Ginjal kanan Ginjal kiri
Lampiran Organ Hati Mencit Jantan
ANOVA hati
Sum of Squares df Mean Square F Sig.
Between Groups .130 4 .033 . .
Within Groups .000 0 .
Total .130 4
Lampiran Organ Ginjal Kiri Mencit Jantan
Descriptive Statistics
N Minimum Maximum Mean Std. Deviation
dosis 5 .00 4.00 2.0000 1.58114
ginjalkiri 5 .12 .16 .1400 .01871
Valid N (listwise) 5
Descriptive Statistics
N Minimum Maximum Mean Std. Deviation
dosis 5 .00 4.00 2.0000 1.58114
hati 5 1.12 1.55 1.3680 .18061
ANOVA
Kelompok Hati Ginjal kanan Ginjal kiri
DATAR PUSTAKA
Akbar, B. 2010. Tumbuhan Dengan Kandungan Senyawa Aktif Yang Berpotensi Sebagai Bahan Antifertilisasi.
Anonim. 2013. Teh gaharu dan manfaatnya bagi kesehatan. http://www.bibitgaharu.com [11 Mei 2014].
Aziz, F., dkk., 2008. Panduan Pelayanan Medik: Model Interdisiplin Penatalaksanaan Kanker Serviks dan Gangguan Ginjal. Penerbit Buku Kedokteran EGC, Jakarta
Batrisyiahherbal. 2012. Cara cepat aman dan alami menurunkan berat badan dengan teh daun gaharu. http://www.batrisyiaherbal.com. [29 mei 2014].
Cambridge Communication Limited, 1999. Anatomi Fisiologi, Sistem Perkemihan dan Sistem Pencernaan. Penerbit Buku Kedokteran EGC,
Jakarta.
Cheville, N. F. 2006. Introduction to Veterinary Pathology. 3rd Ed. Blackwell Publishing. USA.
Departemen Kesehatan RI, Pedoman Pelaksanaan Uji Klinik Obat Tradisional, Jakarta, Departemen Kesehatan RI, 2002, p.17.
Ditjen POM. 2000. Parameter Standar Umum Ekstrak Tumbuhan Obat. Cetakan P ertama. DepartemenKesehatan RI. Jakarta. Hal.9-11.
Ditjen POM. 2014. Peraturan Kepala Badan Pengawas Obat Dan MakananRepublik IndonesiaNomor 7 Tahun 2014TentangPedoman Uji Toksisitas Nonklinik Secara In Vivo.Jakarta: Badan Pengawasan Obat dan Makanan RI. Halaman 3-4, 9,11-12,28-32.
Elya, B., Amin, J., dan Emiyanah. 2010. Toksisitas Akut Daun Justicia gendarussa Burm. Makara Sains. 14(2): 129-134
Gupa,D., dan Bhardwaj, S. 20012. Study of Acute, Subacute and Chronic Toxiciy Test. Internasionak Journal of Advanced Research in Pharmaceutical and Bio Sciences (IJARPB). 1(2): 103-110.
Hernani dan Rahardjo, M. 2006. Tanaman Berkhasiat Antioksidan: Berbagai Jenis Tanaman Penangkal Racun. Penebar Swadaya. Jakarta.
Iwuanyanwu K.C.V., Amadi, U., Charles, I.A., dan Ayalogu, E.O. 2012. Evaluation of Acute and Subcronic Oral Toxicity Suti of Baker Cleancer Bitters A Polyherbal Drug on Exprimental Rat. EXCLI Journal11(1): 632-640.
Junqueira,L.C., dan Corneiro,J.2005. Basic Histology Text and Atlas Edisi XI. Jakarta: EGC. Halaman 71-75.
Kumalaningsih, S. 2006. Antioksida danAlami, PenangkalRadikalBebas: Sumber, Manfaat, Cara PenyediaandanPengolahan. TrubusAgrisana. Surabaya. Hal.4-5, 24, 43.
Lu, F. C., 1995, Toksikologi Dasar. Asas, Organ Sasaran, dan Penilaian Resiko. Edisi Kedua, UI Press, Jakarta.
MacFarlane PS, Robin R, Robin C. 2000. Pathology Illustrated. 5th ed. United Kingdom: Churchill Livingstone
Misra, H., D. Mehta, B.K. Mehta, M. soni, D.C dan Jain. 2008. Study Of Extraction and HPTLC-UVMethod for Estimation Of Caffeine in Marketed Tea (Camellia sinensis) Granules. International Journal of Green Pharmacy: 47-51.
OECD. 2001. Acute Oral Toxicity – Acute Toxic Class Method. OECD Guidelines for Testing Chemicals. 423(1) : 1-6
Prasta, B, P. 2010. Pengaruh Pemberian Dekstrometorfan Dosis Bertingkat Per Oral Terhadap Gambaran Histopatologi Ginjal Tikus Wistar. Fakultas Kedokteran Universitas Diponegoro.
Price S.A dan Wilson, Lorraine M.C, 2005. Patofisiologi Clinical Concept Of Desiace Procces, Edisi 6, Vol 2, Alih Bahasa Brahm U. Jakarta: EGC.
Retnomurti, D. Anggraini. 2008. Gambaran Makroskopik dan Makroskopik Hati dan Ginjal Mencit Akibat Pemberian Plumbum Asetat. Tesis. Medan: Pascasarjana Universitas Sumatra Utara.
Santoso, H.B., dan Nurliani, A. 2006. Efek Doksisiklin Selama Masa Organogenesis Pada Struktur Histology Organ Hati Dan Ginjal Fetus Mencit. Bioscientiae
Silaban, S. 2014. Skrining Fitokimia dan Uji Aktivitas Antioksi dan Ekstrak Etanol Daun G aharu (Aquilaria malaccensis Lamk). Skripsi. USU Press. Medan
Soehartono,T. 2001. Gaharu, Kegunaan dan Pemanfaatan. Proseding LokakaryaPengembangan Gaharu, Mataram 4-5 September 2001. Direktorat Bina UsahaPerhutanan Rakyat. Ditjen RLPS. Jakarta.
Sumarna, Y. 2002. BudidayaGaharu. Cet. Ke-1.PenebarSwadaya. Jakarta. Hal. 80.
Sumarna, Y.2007. Budidaya dan Rekayasa Produksi Gaharu. Temu Pakar Pengem bangan Gaharu. Direktorat Jendral RLPS. Jakarta.
Tarigan, K. 2004. Profil Pengusahaan (Budidaya) Gaharu. Pusat Bina Penyuluhan Kehutanan. Departemen Kehutanan. Jakarta.
Wicaksono, S. 2002. Efek Toksik dan Cara Menentukan Toksisitas Bahan Kimia. Jakarta: Departemen Kesehatan RI. Cermin Dunia Kesehatan No 135. Halaman 33.
Wirasuta, M.A.G., dan Niruri, R. 2006. Toksikologi Umum. Jurusan Farmasi Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Udayana. Halaman 22, 60. Bali
METODOLOGI PENELITIAN
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Juli hingga bulan Oktober 2016.
Pengambilan sampel dilakukan di Langkat, Sumatra Utara. Pembuatan teh, dan
pengujian akut oral dilakukan di Laboratorium Farmakologi di Laboratorium
Penelitian Fakultas Farmasi Universitas Sumatra Utara, Histopatologi Organ
dilakukan di Labolatorium Histopatologi Fakultas Kedokteran, Universitas
Sumatra Utara.
Bahan dan Alat Penelitian
Bahan yang digunakan adalah daun gaharu (A.malaccensis Lamk.) segar
non induksi yang telah dikeringkan selama 1 bulan, mencit (M. Musculus ),Histo
organ hati dan ginjal, akuades, dan air panas. Bahan kimia yang digunakan adalah
adalah etanol 96% dan air suling (akuades), Na2HPO4, NaH2PO4, dan
Formaldehyd, infus NaCl.
Alat yang digunakan adalah kandang mencit, dot, botol vial, oral sonde,
spuit, kaca arloji, batang pengaduk, tisu, kertas saring, kertas perkamen, lemari
pengering, lemari penyimpan, desikator, kamera digital dan lemari pengering,
mikroskop, timbangan, alat tulis, pot, gelas ukur, baker glass, plastikpolietilen.
Prosedur Penelitian
Pengambilan Sampel Tanaman
Pengambilan sample dilakukan secara purposive tanpa membandingkan dengan
tanaman yang sama dari daerah yang lain. Pengambilan sampel ini dilakukan berdasarkan
pohon yang belum diinduksi. Sampel yang digunakan dalam penelitian ini adalah daun
Pembuatan Teh
1. Dibersihkan sampel daun gaharu dari kotoran yang menempel dengan air
mengalir
2. Dilayukan dengan disebarkan di atas kertas perkamen hingga airnya
terserap
3. Dilakukan pengeringan di lemari pengering pada temperatur ± 40°C
sampai kering (ditandai bila diremas rapuh)
4. Diblender daun yang sudah kering
5. Dimasukkan ke dalam plastikpolietilen
6. Diseduh teh daun gaharu menjadi minuman teh dengan ukuran teh
sebanyak 2 g dan air panas 150 ml
Pembuatan Ekstrak Etanol Daun Gaharu
Pembuatan ekstrak dilakukan secara maserasi dengan pelarut etanol 96%,
sebanyak 100 g serbuk simplisia dimasukkan kedalam wadah kaca, di tuangi
dengan 1000 ml etanol 96%, ditutup, dibiarkan selama 5 hari terlindungi dari
cahaya dan sesekali diaduk, setelah 5 hari campuran tersebut diserkai (saring).
Ampas dicuci dengan etanol 96% secukupnya sehingga diperoleh 1000 ml, lalu
dipindahkan dalam bejana tertutup dan dibiarkan ditempat sejuk terlindung dari
cahaya selama 2 hari, kemudian dituangkan lalu disaring. Maserat dipekatkan
menggunakan alat rotary evaporator pada suhu 40°C sampai diperoleh maserat
pekat kemudian dikeringkan menggunakan freeze dryer sehingga dapat diperoleh
ekstrak kering (Ditjen POM, 1979).
Hewan uji toksik oral yang digunakan adalah mencit jantan dan betina
galur ddY berumur lebih kurang dua bulan dengan berat badan 20-30 g
masing-masing 50 ekor yang diperoleh dari Bagian Nonruminansia Fakultas Farmasi,
Universitas Sumatra Utara.
Persiapan Hewan Uji
Mencit diaklimatisasi selama dua minggu dengan tujuan untuk
mengadaptasikan terhadap lingkungan kandang percobaan. Pada tahap ini
dilakukan pengamatan keadaan umum hewan uji. Penelitian ini menggunakan 25
ekor mencit jantan dan 25 ekor mencit betina yang dibagi menjadi 5 kelompok
perlakuan. Pengelompokan hewan coba dilakukan secara acak lengkap yaitu
masing-masing terdiri dari 5 ekor.
Penetapan Dosis.
Dosis teh gaharu adalah 1 g. Faktor konversi dari manusia ke mencit, yaitu
0,0026, maka dosis sediaan uji untuk mencit adalah = 2,6 g/20 g bb mencit=
0,13g/kg bb mencit. Dosis ini ditetapkan sebagai dosis terendah yang akan
diberikan. Penentuan dosis terbesar dilakukan dengan uji pendahuluan untuk
mengetahui dosis terbesar yang dapat disondekan kepada mencit, diperoleh dosis
0,52g/kg bb mencit. Untuk mendapatkan hasil yang baik digunakan dosis secara
berturut-turut yang akan mengikuti progresi geometris yaitu :
YN = Y1 x RN-1
dengan
Y1 = Dosis pertama,
R = Faktor geometris ≠ 0 atau 1 kelipatan dosis. Dengan memasukkan dosis
terendah (dosis ke-1) dan dosis tertinggi (dosis ke-4) ke dalam persamaan, maka
diperoleh faktor geometris 0,52 = 0,13 x R4-1, sehingga diperoleh R = 2.
Berdasarkan perhitungan tersebut, untuk mendapatkan 4 dosis digunakan
kelipatan antar dosis sebesar 2, sehingga perhitungan dosis yang akan diberikan
sebagai
Untuk penentuan nilai LD50, digunakan dosis bertingkat yang terdiri dari
empat variasi dosis. Pemberian ekstrak dilakukan dalam satu kali pemberian
secara oral menggunakan sonde, mencit diamati selama 4 jam untuk melihat
apakah ada gejala toksik yang muncul atau tidak. Pengamatan pada
mencit kembali dilakukan pada 24 jam setelah pemberian larutan uji dengan
menghitung jumlah mencit yang mati dari tiap kelompok. Nilai LD50 dihitung
dengan menggunakan rumus Weil.
Pemberian Sediaan uji
Hewan harus dipuasakan sebelum di berikan perlakuan (mencit
dipuasakan selama 14-18 jam, mencit dipuasakan selama 3-4 jam, air boleh
diberikan), setelah dipuasakan, hewan ditimbang dan di berikan sediaan uji.
keadaan yang tidak memungkinkan untuk diberikan dosis dengan satu kali
pemberian, sediaan uji dapat di berikan dalam beberapa kali dalam jangka waktu
pemberiaan zat tidak lebih dari 24 jam, setelah di berikan perlakuan, pakan boleh
di berikan kembali setelah 3-4 jam untuk tikus dan 1-2 jam untuk mencit. Bila
sediaan uji diberikan beberapa kali, maka pakan boleh di berikan setelah
perlakuan tergantung pada lama periode pemberian sediaan uji tersebut.
Pada umumnya sediaan uji diberikan dalam volume yang tetap selama
pengujian (konsentrasi berbeda), akan tetapi jika bahan sediaan uji berupa cairan
atau campuran cairan, sebaiknya digunakan dalam bentuk tidak diencerkan
(konsentrasi tetap).
Pembuatan Preparat Hepar
Hepar direndam dalam larutanfiksatif yaitu formalin 10%.
Kemudiandirendam lagi dalam etanol 70%, dilanjutkandengan perendaman dalam
etanol 80% yangmasing-masing perlakuan berlangsungselama 2 jam. Perendaman
kembali dalametanol 90%, lalu etanol 95%, dilanjutkandalam etanol absolut yang
masing-masingperendaman dilakukan selama 20 menit.Selanjutnya, hepar
dicelupkan dalam paraffin cair yang dituang dalam wadah. Setelahbeberapa saat,
parafin akan memadat danhepar berada dalam blok parafin (embeding).Hasil
embeding hepar dipotong denganketebalan irisan 5-10 mikrometer. Irisan tersebut
diambil dengan kuas dan dimasukkan dalam air hangat untuk membuka lipatan
yang mungkin terjadi pada preparat, direntangkan sempurna pada object glass.
Potongan dikeringkan dan diletakkan di atas hot plate (38 – 40ºC). Preparat
Pengamatan
Pengamatan dilakukan tiap hari selama sekurang-kurangnya 14 hari
terhadap sistem kardiovaskular, pernafasan, somatomotor, kulit, dan bulu,
mukosa, mata dan sebagainya. Perhatian khusus diberikan akan adanya tremor,
kejang, salvias, diare, alergi, lemah, tidur dan koma. Hewan coba yang sekarat
dikorbankan dan dimasukkan dalam perhitungan sebagai hewan yang mati.
Hewan ditimbang sedikitnya 2 kali dalam seminggu.
Analisis Data
Data jumlah hewan uji dianalisa secara statistic menggunakan SPSS
dengan metode One Way Analisis Of Variance (ANOVA) dilanjutkan dengan uji
Post Hoc Tukaey untuk mengetahui perbedaan signifikan berat badan, berat organ
HASIL DAN PEMBAHASAN
Hasil Ekstraksi Daun Gaharu
Pembuatan ekstrak dilakukan dengan metode maserasi menggunakan
pelarut etanol 90% yang bertujuan untuk menarik senyawa metabolit skunder
yang terdapat dalam serbuk daun gaharu. Hasil masrasi dari 100 gram serbuk
simplisia diperoleh ekstrak kental 11,97 gram
Hasil Pengujian Toksisitas Akut
Hasil uji pendahuluan selama 14 hari tidak di temukan adanya gejala
toksik dan kematian pada kelompok kontrol maupun kelompok perlakuan dosis
130, 260, 390, 520 mg/kgbb.
Penelitian ini dilakukan berdasarkan metode Thomson dan Weil dengan
menggunakan kelipatan dosis. Hasil uji pendahuluan dari seduhan teh 1 gram
maka didapatkan dosis untuk pengujian toksisitas akut yaitu dosis 130, 260, 390
dan 520 mg/kg bb. Pengamatan dilakukan selama 14 hari meliputi gejala klinis,
kematian hewan, berat badan dan makropatologi.
Hasil Pengamatan Gejala Toksik
Hasil pengamatan yang dilakukan setiap hari selama 14 hari terhadap
adanya kejang, diare, salvias, lemas, tidur, dan koma (OECD, 2001) dapat dilihat
pada Tabel 1 dan 2
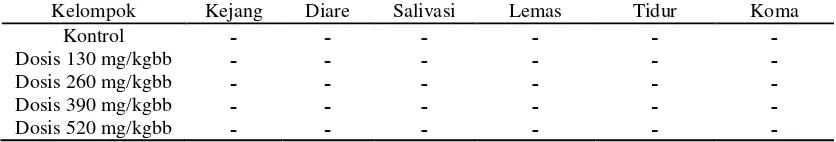
Tabel 1. Hasil Pengamatan Gejala Toksis Pada Mencit Betina
Kelompok Kejang Diare Salivasi Lemas Tidur Koma
Tabel 2. Hasil Pengamatan Gejala Toksis Pada Mencit Jantan
Keterangan : (-) = tidak menunjukkan gejala; (+) = menunjukkan adanya gejala
Berdasarkan tabel 1 dan 2 terlihat bahwa pemberian seduhan the tidak
ditemukan adanya gejala toksik yang menyerang sistem saraf pusat dan sistem
pencernaan, ditandai dengan tidak terjadinya tremor dan diare pada kelompok
kontrol dan perlakuan pada dosis 130, 260, 390 dan 520 mg/kgbb. Dari hasil
pengamatan yang dilakukan terlihat bahwa mencit jantan dan mencit betina yang
diberi seduhan teh terlihat lebih aktif dibandingkan dengan mencit yang tidak di
beri seduhan teh.
Evaluasi toksisitas akut tidak hanya mengenai LD50, tetapi juga terhadap
kelainan tingkah laku, stimulasi dan aktivitas motorik hewan uji untuk
mendapatkan gambaran tentang sebab kematian (Retnomurti, 2008).
Hasil Pengamatan Kematian
Hasil pengamatan uji kuantitatif selama 14 hari, berupa jumlah mencit
yang mati ditunjukkan pada Tabel 3 dan 4
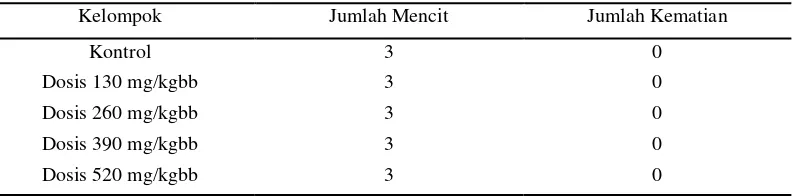
Tabel 3.Jumlah Mencit Betina Yang Mati Setelah Diberi Seduhan Teh Selama 14 Hari
Kelompok Jumlah Mencit Jumlah Kematian
Kontrol 3 0
Dosis 130 mg/kgbb 3 0
Dosis 260 mg/kgbb 3 0
Dosis 390 mg/kgbb 3 0
Tabel 4.Jumlah Mencit Jantan Yang Mati Setelah Diberi Seduhan Teh Selama 14 Hari
Kelompok Jumlah Mencit Jumlah Kematian
Kontrol 3 0
Dosis 130 mg/kgbb 3 0
Dosis 260 mg/kgbb 3 0
Dosis 390 mg/kgbb 3 0
Dosis 520 mg/kgbb 3 0
Keterangan P = perlakuan; 1,2,3, dan 4 = dosis 130,260,390 dan 520 mg/kgbb; bb = berat badan
Berdasarkan tabel 3 dan 4 menunjukkan bahwa pemberian seduhan teh
pada kelompok kontrol, dosis 130, 260, 390 dan 520 mg/kgbb tidak terdapat
mencit jantan dan mencit betina yang mati. Bila toksisitas akutnya rendah LD50
tidak perlu ditentukan secara tepat dan suatu angka perkiraan sudah dapat
memberi manfaat (Retnomurti, 2008). Berdasarkan kesepakatan para ahli, bila
pada dosis maksimal tidak ada kematian pada hewan coba, maka jelas senyawa
tersebut termasuk dalam kriteria “praktis tidak toksik” (Jenova, 2009;
Iwuanyanwu, et al., 2012).
Hasil Pengamatan Berat Badan
Hasil rata-rata berat badan tiap kelompok mencit sebelum dan sesudah
diberi seduhan teh di tunjukkan pada Tabel 5 dan 6
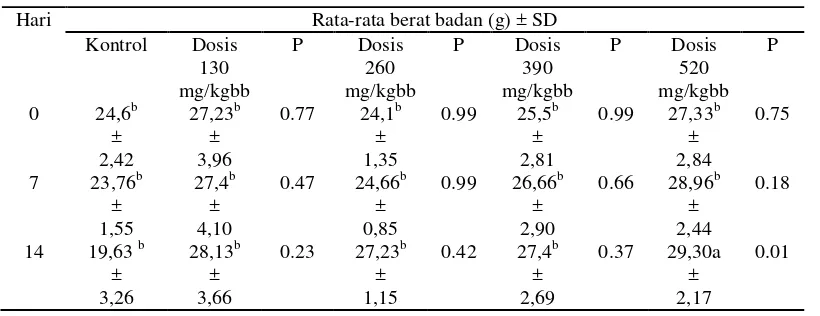
Tabel 5. Hasil Rata-Rata Berat Badan Mencit Betina
Tabel 6. Hasil Rata-Rata Berat Badan Mencit Jantan
Keterangan : bb = berat badan, SD = standart deviasi, P = angka kebermaknaan, a= signifikan, b= tidak signifikan
Berdasarkan tabel 5 dan 6 terlihat bahwa hasil uji statistic menunjukkan
tidak ada perbedaan yang signifikan antara kenaikan berat badan mencit jantan
dan betina dengan pemberian seduhan teh (p > 0.05). hal ini dapat dinyatakan
bahwa pemberian seduhan teh tidak berpengaruh terhadap perkembangan berat
badan mencit jantan dan mencit betina. Tetapi pada dosis 520 mg/kgbb pada hari
ke 14 terdapat perbedaan berat badan mencit betina yang signifikan pada
pemberian seduhan teh (p < 0.05). Hewan uji diamati setiap hari untuk gejala
klinis dan berat badan diukur skala berkala (Gupta dan Bhardwaj, 2012).
Pengamatan Berat Organ Relatif
Hasil berat organ relative hati, ginjal kanan, dan ginjal kiri dapat dilihat
pada Tabel 7 dan 8
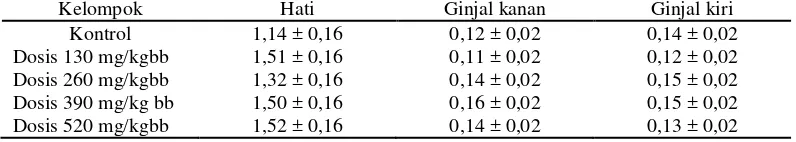
Tabel 7. Hasil Rata-Rata Berat Organ Relatif Mencit Betina
Kelompok Hati Ginjal kanan Ginjal kiri
Kontrol 1,14 ± 0,16 0,12 ± 0,02 0,14 ± 0,02
Dosis 130 mg/kgbb 1,51 ± 0,16 0,11 ± 0,02 0,12 ± 0,02
Dosis 260 mg/kgbb 1,32 ± 0,16 0,14 ± 0,02 0,15 ± 0,02
Dosis 390 mg/kg bb 1,50 ± 0,16 0,16 ± 0,02 0,15 ± 0,02
Berdasarkan tabel 7 terlihat bahwa pemberian seduhan teh berpengaruh
terhadap perubahan berat organ. Pada organ hati mengalami kenaikan pada semua
perlakuan dibandingkan control. Sedangkan pada organ ginjal kanan dan ginjal
kiri pada perlakuan 260 mg/kgbb mengalami penurunan dibandingkan dengan
kontrol.
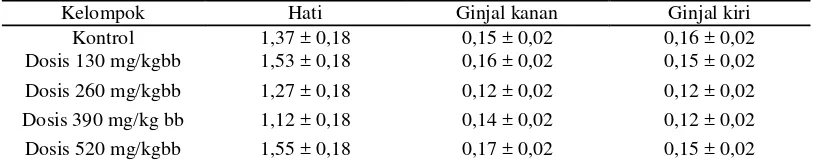
Tabel 8. Hasil Rata-Rata Berat Organ Relatif Mencit Jantan
Kelompok Hati Ginjal kanan Ginjal kiri
Kontrol 1,37 ± 0,18 0,15 ± 0,02 0,16 ± 0,02
Dosis 130 mg/kgbb 1,53 ± 0,18 0,16 ± 0,02 0,15 ± 0,02
Dosis 260 mg/kgbb 1,27 ± 0,18 0,12 ± 0,02 0,12 ± 0,02
Dosis 390 mg/kg bb 1,12 ± 0,18 0,14 ± 0,02 0,12 ± 0,02
Dosis 520 mg/kgbb 1,55 ± 0,18 0,17 ± 0,02 0,15 ± 0,02
Berdasarkan tabel 8 terlihat bahwa pemberian seduhan teh berpengaruh
terhadap perubahan berat organ. Pada kelompok dosis 130 mg/kgbb dan
kelompok dosis 520 mg/kgbb, organ hati mengalami kenaikan dari hati pada
perlakuan kontrol. Sedangkan perlakuan dosis 260 mg/kgbb dang 390 mg/kgbb,
organ hati mengalami penurunan dari hati pada perlakuan control. Pada kelompok
dosis 130 mg/kgbb dan kelompok dosis 520 mg/kgbb, organ ginjal kanan
mengalami kenaikan dari organ ginjal kanan pada perlakuan kontrol. Sedangkan
perlakuan dosis 260 mg/kgbb dang 390 mg/kgbb, organ ginjal kanan mengalami
penurunan dari organ ginjal kanan pada perlakuan kontrol. Sedangkan pada organ
ginjal kiri pada semua perlakuan mengalami penurunan dibandingkan dengan
kontrol.
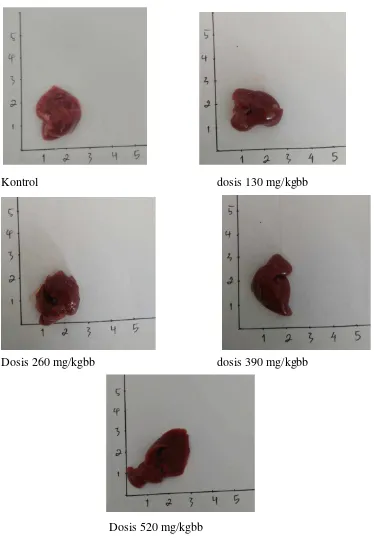
Hasil Pengamatan Makropatologi
Hasil pengamatan makropatologi meliputi pengamatan warna dan
Tabel 9. Hasil Pengamatan Warna Organ Mencit Jantan
Organ
Warna Organ
Kontrol Dosis 130
mg/kgbb
Hati Kecoklatan Merah Kecoklatan Merah Kecoklatan Merah KecoklatanMerah Kecoklatan Merah
Ginjal Kecoklatan Merah Kecoklatan Merah Kecoklatan Merah Kecoklatan Merah Kecoklatan Merah
Tabel 10. Hasil Pengamatan Warna Organ Mencit Betina
Organ Warna Organ
Kontrol Dosis 130
mg/kgbb
Berdasarkan tabel 9 dan 10 menunjukkan bahwa organ hati dan ginjal
setelah diberi seduhan teh pada kelompok kontrol, dosis 130, 260, 390 dan 520
mg/kgbb masih dalam keadaan normal yang bewarna merah kecoklatan. Hasil
dari pengamatan permukaan dan konsistensi organ hati dan ginjal mencit jantan
dan betina tidak terjadi perubahan, struktur permukaan terlihat licin dan
konsistensi kenyal pada semua kelompok.
Warna dan penampilan sering dapat menunjukkan sifat toksisitas seperti
perlemakan hati, atau sirosis. Biasanya berat organ merupakan petunjuk yang
sangat peka dari efek pada hati. Meski suatu efek tidak selalu menunjukkan
toksisitas, dalam kasus tertentu peningkatan berat hati merupakan criteria paling
peka untuk toksisitas (Lu, 1995).
Efek toksik segera terjadi setelah senyawa toksis mencapai organ hati dan
ginjal pada konsentrasi yang tinggi (Wirasuta dan Niruri, 2006). Oleh sebab itu,
hati menjadi organ yang sangat potensial menderita keracunan terlebih dahulu
dapat menjadi petunjuk apakah suatu zat yang diberikan bersifat toksik atau tidak
(Elya, dkk, 2010).
Kontrol dosis 130 mg/kgbb
Dosis 260 mg/kgbb dosis 390 mg/kgbb
Dosis 520 mg/kgbb
Kontrol Dosis 130 Mg/Kgbb
Dosis 260 Mg/Kgbb Dosis 390 Mg/Kgbb
Dosis 520 mg/kgbb
Histopatologi Hati dan Ginjal Mencit
Pengamatan histopatologi dilakukan pada akhir masa uji, yaitu pada hari
ke-15. Mencit yang masih hidup dibedah untuk diambil organ vitalnya yaitu
hati.Hasil pengamatan ini digunakan untuk menentukan spektrum efek toksik
pada mencit setelah pemberian sediaan uji. Melalui pengamatan histopatologi ini
dapatdilihat kerusakan organ yang tidak terlihat bila hanya diamati secara
makroskopik.
Salah satu organ yang sering menderita karena adanya zat-zat toksik
adalah hati, bahan kimia kebanyakan mengalami metabolisme dalam hati dan oleh
karenanya maka banyak bahan kimia yang berpotensi merusak sel-sel hati. Bahan
kimia yang dapat mempengaruhi hati disebut hipotoksik (Wicaksono, 2002).
Dalam setiap ginjalterdapat sekitar 1 juta nefron yang pada dasarnya
mempunyai struktur dan fungsi yang sama. Dengan demikian, kerja ginjal dapat
dianggap sebagai jumlah total dari fungsi semua nefron tersebut (Price dan
Wilson, 2006). Setiap nefron terdiri atas bagian yang melebaryakni korpuskel
renalis, tubulus kontortus proksimal, segmen tipis, dan tebal ansa henle, tubulus
Betina
Jantan
Gambar 3. Histopatologi Organ Hati Kontrol Keterangan : 1 = Vena Centralis
2 = Sinosoid
1
1
2
1
Betina
Jantan
Gambar 4. Histopatologi histopatologiorgan hati perlakuan dosis 130 mg/kgbb Keterangan : 1 = Vena Centralis
2 = Vena Porta
2 1
Betina
Jantan
Gambar 5. Histopatologi histopatologiorgan hati perlakuan dosis 260 mg/kgbb Keterangan : 1 = Vena Centralis
2 = Vena Porta
2
1
1
Betina
Jantan
Gambar 6. Histopatologi histopatologiorgan hati perlakuan dosis 390 mg/kgbb Keterangan : 1 = Vena Centralis
2 = Sinosoid
2
Betina
Jantan
Gambar 7. Histopatologi histopatologi organ hati perlakuan dosis 520 mg/kgbb Keterangan : 1 = Vena Centralis
2 = Hepatosit 3 = Limfosit
2
1
Kanan Betina Kiri
Kanan Jantan Kiri
Gambar 8. Histopatologi ginjal mencit kontrol Keterangan : 1 = Glumerulus
2 = Pembuluh darah 3 = Tubulus
1
1
2
3 1
Kanan Betina Kiri
Kanan Jantan Kiri
Gambar 9. Histopatologi ginjal mencit dosis 130 mg/kgbb Keterangan : 1 = Glumerulus
2 = Pembuluh darah 1
2
1
1
1
Kanan Betina Kiri
Kanan Jantan Kiri
Gambar 9. Histopatologi ginjal mencit dosis 260 mg/kgbb Keterangan : 1 = Glumerulus
2
3 1
2
1
Kanan Betina Kiri
Kanan Jantan Kiri
Gambar 10. Histopatologi ginjal mencit dosis 390 mg/kgbb Keterangan : 1 = Glumerulus
2 1 1
1
Kanan Betina Kiri
Kanan Jantan Kiri
Gambar 11. Histopatologi Ginjal Dosis 590 mg/kgbb keterangan : 1 = glumerulus
1 1
1
Berdasarkan gambar histologi hati mencit betina dan mencit jantan di
dapatkan hasil hepatosit yang normal menunjukkan susunan sel secara radie
terhadap vena sentralis, bentuk sel bulat danoval, dan terdapat lempeng-lempeng
hepatosit.Sel terlihat memiliki satu nukleus, namun adajuga yang memiliki lebih
dari satu nucleus(binukleat) yang terdapat di tengah sel. Hepatosit merupakan
sebagian besar organ yang bertanggung jawab terhadap peran sentral hati dalam
metabolisme.
Vena centralis pada gambar mengalami dilatasi dan hemorhage.
Hemorhage adalah terjadinya bendungan darah pada glomerulus.Hal ini
disebabkan adanya kerusakan pada badan malpghi sehingga sel-sel darah merah
dapat menembus glomerulus. Berdasarkan gambar histologi hati mencit jantan
yang di beri dosis 520 mg/kgbb mengalami limfosit atau peradangan.
Berdasarkan gambar histologi hati mencit jantan yang diberi dosis 390
mg/kgbb sinusoid mengalami pelebaran. Sinusoid hati adalah saluran yang
berliku-liku dan melebar diameternya. Aliran darah sinusoid berasal dari cabang
terminal vena porta dan arteri hepatik, membawa darah kaya nutrisi dari saluran
pencernaan dan juga kaya oksigen dari jantung.
Pengamatan yang dilakukan dari semua perlakuan didapat bahwa
pemberian ekstrak daun gaharu pada histologi ginjal kanan mencit betina pada
pemberian dosis 130 mg/kg bb Glomerulus mengalami atropi yaitu menurunnya
ukuran jaringan yang disebabkan oleh berkurangnya jumlah sel atau berkurangnya
ukuran sel. Salah satu bentuk kerusakan pada ginjal terlihat adanya penyempitan
pada ruang bowman. Penyempitan ruang bowman disebabkan terjadinya
Pembuluh darah vena centralis dan vena porta banyak mengalami
hemorhage dan dilatasi yaitu pembuluh darah mengalami pembesaran dan
peningkatan pembuluh darah pada daerah tertentu. Hal tersebut dikarenakan pada
proses pembedahan dan pembuatan preparat yang merusak pembuluh darah.
Secara keseluruhan pemberian ekstrak daun gaharu pada semua kelompok
perlakuan tidak mengalami toksik baik pada organ ginjal dan organ hati.
Fungsi utama ginjal adalah menyingkirkan buangan metabolism normal
dan mengkekskresi xenobiotik dan metabolitnya. Hal ini dipengaruhi oleh
produksi urin, suatu proses yang juga berperan dalam pemeliharaan status
homeostasis tubuh. Selain itu, ginjal mempunyai beberapa fungsi non-ekskretori
(Lu, 1995). Beberapa obatatau zat kimia yang beredar dalam sirkulasi sistematik
akan dibawa ke ginjal dalam kadar yang cukup tinggi, akan terjadi proses
perubahan struktur ginjal itu sendiri terutama di tubulus ginjal (Wirasuta dan
Niruri, 2006).
Tubulus proksimal merupakan bagian yang paling banyak dan mudah
mengalami kerusakan pada kasus nefrotoksik. Hal ini dapat terjadi karena adanya
akumulasi bahan-bahan toksik dan karakter tubulus proksimal yang memiliki
epitel yang lemah serta mudah bocor. Sama halnya dengan glomerulus, tubulus
paada penelitian ini tidak ada yang mengalami masalah, tubulus masih terlihat
normal dan berfungsi dengan baik. Kerusakan tubulus proksimal merupakan suatu
hasil korelasi yang sangat penting antara transpor segmental tubulus dengan
akumulasi, toksisitas, serta reaksi obat pada sel-sel target tubulus proksimal
KESIMPULAN DAN SARAN
Kesimpulan
Pada pemberian seduhan teh gaharu (A. malaccensis Lamk), tidak
ditemukan gejala toksik pada perilaku, berat badan, berat organ dan pengamatan
makropatologi organ mencit jantan dan mencit betina. Pemberian seduhan teh
pada organ hati mencit jantan yang di beri dosis 520 mg/kgbb mengalami dilatasi
dan hemorhage pada pembuluh darah vena porta dan vena centralis dan
mengalami peradangan.
Saran
Berdasarkan penelitian yang telah dilakukan, maka disarankan kepada
penelitian selanjutnya untuk menguji toksisitas subkronik pada organ hati, ginjal,
jantung, darah dan organ lain, menguji toksisitas khusus seperti teratogenetik dan
TINJAUAN PUSTAKA
Deskripsi Tanaman Gaharu (A. Malaccensis Lamk.)
Daun gaharu (A. malaccensis Lamk.) merupakan pohon dari suku
Thymeleaceae (Tarigan, 2004), sudah mulai populer dimanfaatkan masyarakat
petani gaharu di Langkat sebagai minuman yang diseduh. Hasil wawancara
terhadap petani gaharu menjelaskan bahwa mengkonsumsi daun gaharu dari jenis
ini memiliki banyak manfaat diantaranya memperbaiki pencernaan.
Taksonomi tanaman gaharu (A. malaccensis Lamk.) menurut Tarigan
(2004), yaitu: Kingdom : Plantae, Divisi : Spermatophyta, Sub Divisi :
Angiospermae, Kelas : Dicotyledonae, Sub Kelas : Dialypetale, Ordo : Myrtales
Famili : Thymeleaceae, Genus : Aquilaria, Spesies : Aquilaria malaccensis
Lamk.
Teh Daun Gaharu (Aquilaria malaccensis Lamk)
Daun gaharu yang dijadikan teh ternyata memiliki manfaat bagi orang
yang mengonsumsinya. Manfaat dari mengonsumsi teh gaharu yaitu sebagai
peluruh lemak, tidak membakar lemak yang aktif sehingga tidak menurunkan
berat badan bagi pemilik tubuh ideal, membantu mengobati keputihan, sebagai
deodoran alami sehingga membantu mengurangi bau badan, sebagai antioksidan
yang dapat membantu membuang racun dari tubuh, mencegah insomnia karena
teh daun gaharu menekan sistem syaraf pusat sehingga menimbulkan efek
menenangkan sebagai obat anti mabuk, membantu menurunkan kadar kolestrol
jahat, membantu meredakan ketegangan/hipertensi/stress dan mengurangi kadar
gula dalam darah sehingga dapat membantu mengobati diabetes melitus
Bagian tanaman gaharu yang dapat digunakan untuk tujuan pengobatan
yaitu pada daun yang telah dikeringkan, gubal gaharu, serbuk kayu, akar gaharu
dan kandungan minyak atsirinya. Di Cina dan Jepang gaharu dikenal sebagai obat
reumatik, obat untuk meredakan stress, liver, radang lambung dan kanker. Di
Indonesia, secara tradisional masyarakat Papua telah menggunakan daun, kulit
dan akar gaharu sebagai obat malaria dan perawatan kulit. Kini sudah
dikembangkan daun gaharu dari genusAquilaria dan Gyrinops yang diolah
menjadi bahan baku pembuatan produk minuman herbal (teh dan sirup) karena
kandungan zat antioksidan dalam daun yang cukup tinggi (Sumarna, 2002).
Sejumlah kandungan metabolit sekunder pada daun gaharu yang telah
diketahui dari penelitian sebelumnya adalah flavonoid, glikosida, tanin dan
steroid/triterpenoid (Silaban, 2014). Steroid/triterpenoid merupakan senyawa aktif
dalam tumbuhan obat yang telah digunakan untuk penanganan penyakit termasuk
diabetes mellitus, gangguan menstruasi, kontrasepsi, patukan ular, gangguan kulit,
kerusakan hati dan malaria. Salah satu fungsi penting triterpenoid tipe steroid
pada manusia dan mamalia terutama sebagai peningkatan ataupun pengendalian
hormon seks, misalnya estradiol, progesteron dan testosteron. Tipe sterol dan
triterpen pentasiklik digunakan sebagai obat anti radang dan anti lebam serta
pengobatan ulser lambung.
Hewan Uji
Adapun klasifikasinya adalah sebagai berikut : Phylum : Chordata, Sub
phylum : Vertebrata, Class : Mammalia, Ordo : Rodentia, Family: Muridae,
Mencit (M. musculus L.) memiliki ciri-ciri berupa bentuk tubuh kecil,
berwarna putih, memiliki siklus estrus teratur yaitu 4-5 hari. Kondisi ruang untuk
pemeliharaan mencit (M. musculus L.) harus senantiasa bersih, kering dan jauh
dari kebisingan. Suhu ruang pemeliharaan juga harus dijaga kisarannya antara
18-19ºC serta kelembaban udara antara 30-70%. Mencit betina dewasa dengan umur
35-60 hari memiliki berat badan 18-35 g. Lama hidupnya 1-2 tahun, dapat
mencapai 3 tahun. Masa reproduksi mencit betina berlangsung 1,5 tahun. Mencit
betina ataupun jantan dapat dikawinkan pada umur 8 minggu. Lama kebuntingan
19-20 hari. Jumlah anak mencit rata-rata 6-15 ekor dengan berat lahir antara
0,5-1,5 g (Akbar, 2010).
Antioksidan Alami
Antioksidan alami merupakan hasil ekstraksi dari bahan alami.
Sayur-sayuran dan buah-buahan kaya akan zat gizi (vitamin, mineral, serat pangan) serta
berbagai kelompok zat bioaktif lain yang disebut zat antioksidan.Antioksidan atau
reduktor berfungsi untuk mencegah terjadinya oksidasi atau menetralkan senyawa
yang telah teroksidasi dengan cara menyumbangkan hidrogen dan atau elektron
(Silalahi, 2006).
Senyawa antioksidan alami tumbuhan umumnya adalah senyawa fenolik
atau polifenolik yang dapat berupa golongan flavonoid, turunan asam sinamat,
kumarin dan tokoferol. Golongan flavonoid yang memiliki aktivitas antioksidan
meliputi flavon, flavonol, isoflavon, katekin, flavanon dan kalkon. Senyawa
antioksidan alami polifenolik dapat bereaksi sebagai pereduksi, penangkap radikal
bebas, pengkelat logam dan peredam terbentuknya singlet oksigen
Tanaman yang berkhasiat sebagai antioksidan menurut (Hernani dan
Rahardjo,2006) dikelompokkan atas 4 golongan yaitu:
1. Kelompok tanaman sayuran
Brokoli, kubis, lobak, wortel, tomat, bayam, cabai, buncis, pare dan
mentimun.
2. Kelompok tanaman buah
Anggur, alpukat, jeruk, semangka, markisa, apel, belimbing, pepaya dan
kelapa.
3. Kelompok tanaman rempah
Jahe, temulawak, kunyit, lengkuas, temu putih, kencur, kapulaga, temu
ireng, lada, cengkeh, pala dan asam jawa.
4. Kelompok tanaman lain
Teh, ubi jalar, kedelai, kentang, labu kuning dan petai cina.
Ekstraksi Daun Gaharu
Ekstraksi adalah proses penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan pelarut
cair. Diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah
pemilihan pelarut dan cara ekstraksi yang tepat. Senyawa aktif yang terdapat
dalam berbagai simplisia dapat digolongkan ke dalam golongan minyak atsiri,
alkaloid, flavonoid dan lain-lain (Ditjen POM, 2000).
Beberapa metode ekstraksi yang sering digunakan dalam berbagai
penelitian menurut Departemen Kesehatan Republik Indonesia (Ditjen POM
A. Cara dingin
1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman
menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada
suhu kamar. Maserasi kinetik dilakukan dengan pengadukan yang kontinu.
Remaserasi dilakukan dengan pengulangan penambahan pelarut setelah dilakukan
penyarian maserat pertama dan seterusnya. Prinsip metode ini adalah pencapaian
konsentrasi pada keseimbangan,cairan penyari akan menembus dinding sel dan
masuk ke dalam rongga sel yang mengandung zat aktif.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu
baru sampai sempurna yang umumnya dilakukan pada temperatur ruangan. Proses
perkolasi terdiri dari tahap pengembangan bahan, tahap maserasi antara, tahap
perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai
diperoleh ekstrak (perkolat) yang jumlahnya 1 - 5 kali bahan (Depkes, 2000).
B. Cara panas
1. Refluksi
Refluks adalah ekstraksi dengan menggunakan pelarut pada temperatur
titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif
konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada
temperatur lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan alat soklet dengan
pelarutyang selalu baru sehingga terjadi ekstraksi kontinu dengan jumlah pelarut
yang relatif konstan dengan adanya pendingin balik.
Toksisitas
Uji toksisitas adalah suatu uji untuk mendeteksi efek toksik suatu zat pada
sistem biologi dan untuk memperoleh data dosis-respon yang khas dari sediaan
uji. Data yang diperoleh dapat digunakan untuk memberi informasimengenai
derajat bahaya sediaan uji tersebut bila terjadi pemaparan padamanusia, sehingga
dapat ditentukan dosis penggunaannya demi keamananmanusia. Uji toksisitas
menggunakan hewan uji sebagai model berguna untukmelihat adanya reaksi
biokimia, fisiologik dan patologik pada manusiaterhadap suatu sediaan uji. Hasil
uji toksisitas tidak dapat digunakan secaramutlak untuk membuktikan keamanan
suatu bahan/ sediaan pada manusia,namun dapat memberikan petunjuk adanya
toksisitas relatif dan membantu identifikasi efek toksik bila terjadi pemaparan
pada manusia (Ditjen, POM., 2014).
1.Uji toksisitas akut oral
Uji toksisitas akut oral adalah suatu pengujian untuk mendeteksi
efektoksik yang muncul dalam waktu singkat setelah pemberian sediaan uji
yangdiberikan secara oral dalam dosis tunggal atau dosis berulang yang
diberikandalam waktu 24 jam.Prinsip uji toksisitas akut oral yaitu, sediaan uji
dalam beberapa tingkatdosis diberikan pada beberapa kelompok hewan uji dengan
satu dosis perkelompok, kemudian dilakukan pengamatan terhadap adanya
sampai akhirpercobaan diotopsi untuk dievaluasi adanya
gejala-gejala toksisitas.Tujuan uji toksisitas akut oral adalah untuk mendeteksi toksisitas
intrinsik suatu zat, menentukan organ sasaran, kepekaan spesies, memperoleh
informasi bahaya setelah pemaparan suatu zat secara akut, memperolehinformasi
awal yang dapat digunakan untuk menetapkan tingkat dosis,merancang uji
toksisitas selanjutnya, memperoleh nilai LD50 suatu bahan/sediaan, serta
penentuan penggolongan bahan/sediaan dan pelabelan (Ditjen, POM., 2014).
2. Uji toksisitas subkronis oral
Uji toksisitas subkronis oral adalah suatu pengujian untuk mendeteksi efek
toksik yang muncul setelah pemberian sediaan uji dengan dosis berulang
yangdiberikan secara oral pada hewan uji selama sebagian umur hewan,
tetapitidak lebih dari 10% seluruh umur hewan.
Prinsip dari uji toksisitas subkronis oral adalah sediaan uji dalam beberapa
tingkat dosis diberikan setiap hari pada beberapa kelompok hewan uji dengansatu
dosis per kelompok selama 28 atau 90 hari, bila diperlukanditambahkan kelompok
satelit untuk melihat adanya efek tertunda atau efekyang bersifat reversibel.
Selama waktu pemberian sediaan uji, hewan harusdiamati setiap hari untuk
menentukan adanya toksisitas. Hewan yang matiselama periode pemberian
sediaan uji, bila belum melewati periode rigor mortis(kaku) segera diotopsi,dan
organ serta jaringan diamati secara makropatologidan histopatologi.
Pada akhir periode pemberian sediaan uji, semua hewanyang masih hidup
diotopsi selanjutnya dilakukan pengamatan secaramakropatologi pada setiap
organ dan jaringan,pemeriksaan hematologi, biokimia klinis dan histopatologi.
efek toksik zat yang tidak terdeteksi pada uji toksisitas akut,
informasikemungkinan adanya efek toksik setelah pemaparan sediaan uji
secaraberulangdalam jangka waktu tertentu; informasi dosis yang
tidakmenimbulkan efek toksik (No Observed Adverse Effect Level / NOAEL);
danmempelajari adanya efek kumulatif dan efek reversibilitas zat tersebut (Ditjen,
POM., 2014).
Anatomi Ginjal
Ginjal merupakan organ berbentuk seperti kacang yang terletak di kedua
sisi kolumna vertebralis. Ginjal kanan sedikit lebih rendah dibandingkan ginjal
kiri karena tertekan kebawah oleh hati. Kutub atasnya terletak setinggi iga
keduabelas, sedangkan kutub atas ginjal kiri terletak setinggi iga kesebelas.Ginjal
terletak di bagian belakang abdomen atas, di belakang peritoneum, di depan dua
iga terakhir, dan tiga otot besar-transversus abdominis, kuadratus lumborum, dan
psoas mayor. Ginjal dipertahankan dalam posisi tersebut oleh bantalan lemak
yang tebal. Ginjal terlindung dengan baik dari trauma langsung, disebelah
posterior (atas) dilindungi oleh iga dan otot-otot yang meliputi iga, Ginjal kanan
dikelilingi oleh hepar, kolon, dan duodenum, sedangkan ginjal kiridikelilingi oleh
lien, lambung, pankreas, jejunum dan kolonsedangkan di anterior (bawah)
dilindungi oleh bantalan usus yang tebal (Aziz, 2008).
Pada orang dewasa, panjang ginjal adalah sekitar 12 cm sampai 13 cm
(4,7hingga 5,1 inci), lebarnya 6 cm (2,4 inci), tebalnya 2,5 cm (1 inci)
danberatnya sekitar 150 g. Ukurannya tidak berbeda menurut bentuk danukuran
tubuh. Perbedaan panjang dari kutub ke kutub kedua ginjal yanglebih dari 1,5 cm
besar manifestasi penyakit ginjal adalah perubahanstruktur (Price dan Wilson,
2006).
Unit kerja fungsional ginjal disebut sebagai nefron. Didalam setiap ginjal
terdapat sekitar 1 juta nefron yang pada dasarnya mempunyai struktur dan fungsi
yang sama. Setiap nefron terdiri dari kapsula bowman, tubulus kontraktus
proksimal, lengkung henle dan tubulus kontraktus distal yang mengosongkan diri
ke duktus pengumpul. Glomerulus bersama Kapsul Bowman juga disebut badan
Malpigi. Jalinan glomerulus merupakan kapiler-kapiler khusus yang berfungsi
sebagai penyaring. Kapiler glomerulus dibatasi oleh sel-sel endotel mempunyai
sitoplasma yang sangat tipis, yang mengandung banyak lubang disebut fenestra
dengan diameter 500-1000A0 (Alatas et al., 2002).
Lengkung henle adalah struktur berbentuk U terdiri atas ruas tebal
descenden dengan struktur yang sangat mirip tubulus kontraktus proksimal; ruas
tipis descenden dan ruas tebal ascenden strukturnya sangat mirip dengan tubulus
korteks-medula yang disebut dengan nefronjukstamedula. Nefron lainnya disebut
nefron kortikal. Semua nefron turut serta dalam proses filtrasi, absorpsi dan
sekresi.
Fungsi utama ginjal adalah menyingkirkan buangan metabolism normal
dan mengkekskresi xenobiotik dan metabolitnya. Hal ini dipengaruhi oleh
produksi urin, suatu proses yang juga berperan dalam pemeliharaan status
homeostasis tubuh. Selain itu, ginjal mempunyai beberapa fungsi non-ekskretori
(Lu, 1995). Beberapa obatatau zat kimia yang beredar dalam sirkulasi sistematik
akan dibawa ke ginjal dalam kadar yang cukup tinggi, akan terjadi proses
perubahan struktur ginjal itu sendiri terutama di tubulus ginjal (Wirasuta dan
Niruri, 2006).
Anatomi hati
Secara anatomi hati terdiri dari beberapa lobus, tergantung pada
spesiesnya. Hepar mencit (Mus musculus L.) memiliki empat lobus utama yang
saling berhubungan satu sama lain dan dapat tampak keseluruhannya pada bagian
dorsal organ ini. Keempat lobus tersebut dapat dibedakan, yakni: sebuah lobus
median, dua lobus lateral (kiri dan kanan), dan satu lobus caudal yang terbagi
setengah dibagian dorsal dan setengah lainnya di bagian ventral (Covelli, 1972).
Hati merupakan organ tubuh terbesar kedua di tubuh dan kelenjar terbesar
dalam tubuh, dengan berat rata-rata sekitar 1,5 kg. Organ ini terletak dalam
rongga perut di bawah diafragma (Junqueira dan Carneiro, 2005). Salah satu
organ yang sering menderita karena adanya zat-zat toksik adalah hati, bahan kimia
bahan kimia yang berpotensi merusak sel-sel hati. Bahan kimia yang dapat
mempengaruhi hati disebut hipotoksik (Wicaksono, 2002).
Fisiologi hati
Organ hati terlibat dalam metabolisme zat makanan serta sebagian besar
obat dan toksikan (Lu, 1994). Hati mempunyai fungsi yang sangat banyak dan
kompleks yang penting untuk mempertahankan hidup (Husada, 1996) yaitu :
a. Fungsi pembentukan dan ekskresi empedu
Hal ini merupakan fungsi utama hati. Hati mengekskresikan sekitar satu
liter empedu setiap hari. Garam empedu penting untuk pencernaan dan absorbsi
lemak dalam usus halus.
b. Fungsi metabolik
Hati berperaan penting dalam metabolisme karbohidrat, lemak, protein,
vitamin dan juga memproduksi energi. Hati mengubah ammonia menjadi urea,
untuk dikeluarkan melalui ginjal dan usus.
c. Fungsi pertahanan tubuh
Hati mempunyai fungsi detoksifikasi dan fungsi perlindungan. Fungsi
detoksifikasi dilakukan oleh enzim- enzim hati yang melakukan oksidasi, reduksi,
hidrolisis, atau konjugasi zat yang kemungkinan membahayakan dan
mengubahnya menjadi zat yang secara fisiologis tidak aktif. Fungsi perlindungan
dilakukan oleh sel kupfer yang terdapat di dinding sinusoid hati.
d. Fungsi vaskuler hati
Pada orang dewasa jumlah aliran darah ke hati diperkirakan mencapai
1500 cc tiap menit. Hati berfungsi sebagai ruang penampung dan bekerja sebagai
Histologi hati
Sel–sel yang terdapat di hati antara lain: hepatosit, sel endotel, dan sel
makrofag yang disebut sebagai sel kuppfer, dan sel ito (sel penimbun lemak). Sel
hepatosit berderet secara radial dalam lobulus hati dan membentuk lapisan
sebesar1-2 sel serupa dengan susunan bata. Lempeng sel ini mengarah dari tepian
lobulus ke pusatnya dan beranastomosis secara bebas membentuk struktur seperti
labirin dan busa. Celah diantara lempeng-lempeng ini mengandung kapiler yang
disebut sinusoid hati (Junquiera dan Carneiro, 2007).
Sinusoid hati adalah saluran yang berliku–liku dan melebar, diameternya
tidak teratur, dilapisi sel endotel bertingkat yang tidak utuh. Sinusoid dibatasi oleh
3 macam sel, yaitu sel endotel (mayoritas) dengan inti pipih gelap, sel kupfferyang
fagositik dengan inti ovoid, dan sel stelat atau sel Ito atau liposit hepatik yang
berfungsi untuk menyimpan vitamin A dan memproduksi matriks ekstraseluler
serta kolagen.
Aliran darah di sinusoid berasal dari cabang terminal vena portal dan arteri
oksigen dari jantung (Eroschenko, 2010; Junqueira and Carneiro, 2005).Darah
yang mengandung toksin dibawa dari usus, masuk ke hati melalui vena porta
PENDAHULUAN
Latar Belakang
Gaharu merupakan salah satu komoditi hasil hutan bukan kayu (HHBK)
yangmengandung resin atau damar wangi dan mengeluarkan aroma dengan
keharuman yang khas, sehingga diperlukan sebagai bahan baku industri parfum,
obat-obatan, kosmetik, dupa,pengawet serta untuk keperluan kegiatan agama
(Suhartono, 2001). Di Indonesia, terutama di Papua, gaharu sudah digunakan
secara tradisional oleh masyarakat setempat untuk pengobatan. Bahagian pohon
yang dimanfaatkan seperti daun, kulit batang dan akar digunakan sebagai bahan
pengobatan penyakit malaria. Air limbah dari proses penyulingan minyak gaharu
juga digunakan karena bermanfaat untuk merawat wajah dan menghaluskan kulit.
Daun gaharu (Aquilaria malaccensis Lamk) merupakan pohon dari suku
Thymeleaceae (Tarigan, 2004) sudah mulai popular dimanfaatkan masyarakat
petani gaharu di Langkat sebagai minuman yang di seduh. Hasil wawancara
terhadap petani gaharu menjelaskan bahwa mengkonsumsi daun gaharu dari jenis
ini memiliki banyak manfaat diantaranya memperbaiki pencernaan.
Teh merupakan minuman yang sudah dikenal dengan luas di Indonesia
dan di dunia. Minuman berwarna coklat ini umumnya menjadi minuman penjamu
tamu. Aromanya yang harum serta rasanya yang khas membuat minuman ini
banyak dikonsumsi (Misra,et al., 2008).
Teh telah menjadi minuman favorit yang dikenal sejak dulu. Teh biasanya
diminum pagi hari dan sore hari untuk menghangatkan dan menyegarkan tubuh.
Teh yang sering dikenal saat ini adalah teh yang berasal dari daun pohon teh tetapi
kesehatan. Salah satunya yaitu teh daun gaharu. Daun yang digunakan adalah
daun yang masih muda dari pohon penghasil gaharu (Anonim, 2013).
Berdasarkan uraian di atas penulis tertarik untuk mengetahui kandungan
dan senyawa kimia toksik yang terdapat pada teh gaharu. Daun yang digunakan
adalah pohon non-induksi.
Tujuan Penelitian
Mengetahui adanya gejala toksik yang ditimbulkan produk teh gaharu
(A. malaccencis Lamk) yang berasal dari pohon non induksi.
Hipotesis
Tidak terdapat gejala toksik yang terkandung dalam produk teh gaharu (A.
malaccencis Lamk) yang berasal dari pohon non induksi.
Manfaat Penelitian
1) Sebagai bahan informasi untuk mengetahui bahan kimia yang terkandung
dalam teh daun gaharu (A. malaccensis Lamk) berdasarkan pohon
non-induksi.
2) Sebagai acuan bagi masyarakat maupun petani gaharu manfaat produk teh
gaharu yang berasal dari pohon non induksi untuk dikonsumsi oleh
ABSTRACT
DINI HARDIANI HAS.“The Sefty Of Tea Aloes (Aquilaria malaccensis Lamk) ThroughAcute Oral Toxicity Test”. Under Academic Supervision of RIDWANTI BATUBARA and HERAWATI GINTING.
Aloes wood (Aquilaria malaccensis Lamk) is a tree of the tribe Thymeleaceae, has gaining popularity farming communities aloes used in Langkat as the drink is brewed. The results of interviews with farmers aloes explained that tea from the leaves of aloes of this kind has many benefits including improving digestion. For that conducted safety studies on tea leaves non-induction aloes taken from planting gaharu in Langkat, North Sumatra through oral toxic test. This study aims to determine the toxic symptoms arising from non-tea products gaharu induction.The observation of toxic symptoms showed no effect of steeping tea to their health and behavior of mice, administration of steeping is also not result in death of the entire dose, administration steeping tea also has no effect on body weight changes, observations makropatologi organs of mice was normal that is colored brownish red, surface slippery and chewy consistency. Histopathological results showed hemorhage and dilation of the blood vessels, at a dose of 520 mg/kgbw there is an inflammation of the liver, at a dose of 130 mg / kgbw of female mice experienced Bowmen space narrowing and atrophy of the right kidney. Results showed mice given steeping tea aloes non-induction starting dose of 130mg/kgbw, 260 mg/kgbw, 390 mg/kgbw and 520 mg/kgbw there are no mice died after given tea aloes non-induction into indicators of toxicity.
ABSTRAK
DINI HARDIANI HAS. “Keamanan Teh Gaharu (Aquilaria malaccensis Lamk) Melalui Uji Toksik Oral”. Dibimbing oleh RIDWANTI BATUBARA dan HERAWATI GINTING.
Daun gaharu (Aquilaria malaccensis Lamk) merupakan pohon dari suku Thymeleaceae, sudah mulai popular dimanfaatkan masyarakat petani gaharu di Langkat sebagai minuman yang di seduh.Hasil wawancara terhadap petani gaharu menjelaskan bahwa mengkonsumsi teh dari daun gaharu dari jenis ini memiliki banyak manfaat diantaranya memperbaiki pencernaan. Untuk itu dilakukan penelitian keamanan terhadap teh daun gaharu non-induksi yang diambil dari pertanaman gaharu di Langkat, Sumatra Utara melalui uji toksik oral. Penelitian ini bertujuan untuk mengetahui adanya gejala toksik yang ditimbulkan dari produk teh gaharu non-induksi. Hasil pengamatan gejala toksik menunjukkan tidak ada pengaruh pemberian seduhan teh terhadap kondisi kesehatan dan perilaku mencit, pemberian seduhan juga tidak mengakibatkan kematian terhadap keseluruhan dosis, pemberian seduhan teh juga tidak berpengaruh terhadap perubahan berat badan, pengamatan makropatologi organ mencit masih normal yaitu bewarna merah kecoklatan, permukaan licin dan konsistensi kenyal. Hasil histopatologi menunjukkan adanya hemorhage dan dilatasi pada pembuluh darah, pada dosis 520 mg/kgbb terdapat peradangan pada hati,pada dosis 130 mg/kgbb mencit betina mengalami penyempitan ruang bowmen dan atropi pada ginjal kanan. Hasil penelitian menunjukkan mencit yang diberikan seduhan teh gaharu non-induksi mulai dari dosis 130 mg/kgbb, 260 mg/kgbb, 390 mg/kg bb dan 520 mg/kgbb tidak terdapat mencit yang mati setelah di beri teh gaharu non-induksi yang menjadi indikator toksisitas.
KEAMANAN TEH GAHARU (Aquilaria malaccensis Lamk)
MELALUI UJI TOKSISITAS AKUT ORAL
SKRIPSI
DINI HARDIANI HAS 121201103
PROGRAM STUDI KEHUTANAN
FAKULTAS KEHUTANAN
UNIVERSITAS SUMATERA UTARA
KEAMANAN TEH GAHARU (Aquilaria malaccensis Lamk)
MELALUI UJI TOKSISITAS AKUT ORAL
SKRIPSI
DINI HARDIANI HAS 121201103
Skripsi sebagai salah satu syaratuntukmemperoleh GelarsarjanaKehutanan di FakultasKehutanan
Universitas Sumatera Utara
PROGRAM STUDI KEHUTANAN
FAKULTAS KEHUTANAN
UNIVERSITAS SUMATERA UTARA
LEMBAR PENGESAHAN
Judul : Keamanan Teh Gaharu (Aquilaria Malaccensis Lamk)
Melalui Uji Toksisitas Akut Oral
Nama : Dini Hardiani HAS
NIM : 121201103
Program Studi : Kehutanan
Minat : Teknologi Hasil Hutan
Disetujui oleh Komisi Pembimbing
Ridwanti Batubara, S,Hut, MP
Ketua Anggota
Dra. Herawati Ginting, M.Si.,Apt
Mengetahui,
ABSTRACT
DINI HARDIANI HAS.“The Sefty Of Tea Aloes (Aquilaria malaccensis Lamk) ThroughAcute Oral Toxicity Test”. Under Academic Supervision of RIDWANTI BATUBARA and HERAWATI GINTING.
Aloes wood (Aquilaria malaccensis Lamk) is a tree of the tribe Thymeleaceae, has gaining popularity farming communities aloes used in Langkat as the drink is brewed. The results of interviews with farmers aloes explained that tea from the leaves of aloes of this kind has many benefits including improving digestion. For that conducted safety studies on tea leaves non-induction aloes taken from planting gaharu in Langkat, North Sumatra through oral toxic test. This study aims to determine the toxic symptoms arising from non-tea products gaharu induction.The observation of toxic symptoms showed no effect of steeping tea to their health and behavior of mice, administration of steeping is also not result in death of the entire dose, administration steeping tea also has no effect on body weight changes, observations makropatologi organs of mice was normal that is colored brownish red, surface slippery and chewy consistency. Histopathological results showed hemorhage and dilation of the blood vessels, at a dose of 520 mg/kgbw there is an inflammation of the liver, at a dose of 130 mg / kgbw of female mice experienced Bowmen space narrowing and atrophy of the right kidney. Results showed mice given steeping tea aloes non-induction starting dose of 130mg/kgbw, 260 mg/kgbw, 390 mg/kgbw and 520 mg/kgbw there are no mice died after given tea aloes non-induction into indicators of toxicity.
ABSTRAK
DINI HARDIANI HAS. “Keamanan Teh Gaharu (Aquilaria malaccensis Lamk) Melalui Uji Toksik Oral”. Dibimbing oleh RIDWANTI BATUBARA dan HERAWATI GINTING.
Daun gaharu (Aquilaria malaccensis Lamk) merupakan pohon dari suku Thymeleaceae, sudah mulai popular dimanfaatkan masyarakat petani gaharu di Langkat sebagai minuman yang di seduh.Hasil wawancara terhadap petani gaharu menjelaskan bahwa mengkonsumsi teh dari daun gaharu dari jenis ini memiliki banyak manfaat diantaranya memperbaiki pencernaan. Untuk itu dilakukan penelitian keamanan terhadap teh daun gaharu non-induksi yang diambil dari pertanaman gaharu di Langkat, Sumatra Utara melalui uji toksik oral. Penelitian ini bertujuan untuk mengetahui adanya gejala toksik yang ditimbulkan dari produk teh gaharu non-induksi. Hasil pengamatan gejala toksik menunjukkan tidak ada pengaruh pemberian seduhan teh terhadap kondisi kesehatan dan perilaku mencit, pemberian seduhan juga tidak mengakibatkan kematian terhadap keseluruhan dosis, pemberian seduhan teh juga tidak berpengaruh terhadap perubahan berat badan, pengamatan makropatologi organ mencit masih normal yaitu bewarna merah kecoklatan, permukaan licin dan konsistensi kenyal. Hasil histopatologi menunjukkan adanya hemorhage dan dilatasi pada pembuluh darah, pada dosis 520 mg/kgbb terdapat peradangan pada hati,pada dosis 130 mg/kgbb mencit betina mengalami penyempitan ruang bowmen dan atropi pada ginjal kanan. Hasil penelitian menunjukkan mencit yang diberikan seduhan teh gaharu non-induksi mulai dari dosis 130 mg/kgbb, 260 mg/kgbb, 390 mg/kg bb dan 520 mg/kgbb tidak terdapat mencit yang mati setelah di beri teh gaharu non-induksi yang menjadi indikator toksisitas.
RIWAYAT HIDUP
Penulis dilahirkan di Tanjung Balai, 23 September 1994 dari ayah Hairun
Sibarani dan ibu Suarni Simanjuntak. Penulis merupakan putri tunggal.
Tahun 2006 penulis lulus dari MIN Kisaran.Tahun 2009 penulis lulus dari
SMP Negeri 1 Kisaran. Tahun 2012 penulis lulus dari SMA Negeri 1 Kisaran,
pada tahun yang sama masuk ke Fakultas Kehutanan Universitas Sumatera Utara
melaluli jalur Uian Masuk Bersama. Penulis memilih Fakultas Kehutanan
Selain mengikuti perkulihan, penulis juga aktif sebagai anggota Rain
Forest Community. Penulis mengikuti Praktik Pengenalan Ekosisten Hutan
(P2EH) pada tahun 2014 di pulau Sembilan, Kecamatan Pangkalan Susu,
Kabupaten Sumatera Utara. Penulis melakukan Praktek Kerja Lapang (PKL) di
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Allah SWT, yang telah
melimpahkan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan
skripsi yang berjudul “Keamanan Teh Gaharu (Aquilaria malaccensis Lamk)
Melalui Uji Toksik Oral” Skripsi ini merupakan salah satu syarat untuk
memperoleh gelar Sarjana Kehutanan di Fakultas Kehutanan, Universitas
Sumatera Utara.
Keberhasilan penulis dalam menyelesaikan skripsi ini tentunya tidak
terlepas dari dukungan berbagai pihak. Pada kesempatan ini penulis ingin
mengucapkan terima kasih kepada :
1. Ayahanda Hairun Sibarani dan Ibunda Suarni Simanjuntak yang telah
memberikan kasih sayang, dukungan, doa dan harapan kepada penulis, serta
membesarkan dan mendidik penulis segingga penulis dapat menyelesaikan
program sarjana ini.
2. Ridwanti Batubara, S.Hut.,MP dan Dra. Herwati Ginting, M.Si.,Apt selaku
ketua dan anggota komisi pembimbing yang telah membimbing dan
memberikan berbagai masukan serta kesabaran dalam proses penyusunan
skripsi.
3. dr. Radita Ginting, dr. Nafiah dan Tiwi, Friska yang telah membanntu kami
dalam menyelesaikan penelitian saya di laboratorium farmakologi dan
laboratorium histopatologi
3. Rekan Tim penelitian dan rekan mahasiswa/i Fakultas Kehutanan USU Tahan
Nurlan, Dilla Ersyahdes Riski, Lucky Swetta Sinulingga, Fatma Safira, Horas
Simanjuntak serta semua pihak yang tidak dapat disebutkan satu persatu yang
turut memberikan sumbangsihnya yang tidak ternilai.
Penulis berharap semoga skripsi ini dapat berkontribusi dalam
pengembangan ilmu pengetahuan.
Medan, Januari 2017
DAFTAR ISI
ProsedurPenelitian ... 16
Pengambilan Sample Tanaman ... 16
DAFTAR TABEL
No. Teks Halaman
1. Hasil Pengamatan Gejala Toksik Pada Mencit Betina. ... 22
2. Hasil Pengamatan Gejala Toksik Pada Mencit Jantan ... 23
3. Jumlah Mencit Betina Yang Mati Setelah Pemberian Seduhan Teh Gaharu Selama 14 Hari ... 23
4. Jumlah Mencit Jantan Yang Mati Setelah Pemberian Seduhan Teh Gaharu Selama 14 Hari ... 24
5. Hasil Rata-Rata Berat Badan Mencit Betina ... 24
6. Hasil Rata-Rata Berat Badan Mencit Jantan ... 25
7. Hasil Rata-Rata Berat Organ Relative Mencit Betina... 25
8. Hasil Rata-Rata Berat Organ Relative Mencit Jantan ... 26
9. Hasil Pengamatan Warna Organ Mencit Betina ... 27
DAFTAR GAMBAR
No. Teks Halaman
1. Anatomi Ginjal ... 11
2. Anatomi Hati ... 14
3. Makropatologi Organ Hati ... 28
4. Makropatologi Orgn Ginjal ... 29
5. Histopatologi Organ Hati Kontrol ... 31
6. Histopatologi Organ Hati Dosis 130 Mg/Kgbb ... 32
7.Histopatologi Organ Hati Dosis 260 Mg/Kgbb ... 33
8. Histopatologi Organ Hati Dosis 390 Mg/Kgbb ... 34
7.Histopatologi Organ Hati Dosis 520 Mg/Kgbb ... 35
8. Histopatologi Organ Ginjal Kontrol ... 36
9. Histopatologi Organ Ginjal Dosis 130 Mg/Kgbb ... 37
10.Histopatologi Organ Ginjal Dosis 260 Mg/Kgbb ... 38
11.Histopatologi Organ Ginjal Dosis 390 Mg/Kgbb ... 39
DAFTAR LAMPIRAN
No. Teks Halaman
1. Surat Izin Penelitian Di Fakultas Farmasi Universitas
Sumatra Utara ... 46
2. Gambar Tumbuhan Gaharu, Serbuk Simplisis Daun Gaharu ... 47
3. Bagan Pembuatan Ekstrak Etanol Dauan Gaharu ... 48
4. Bagan Alur Penelitian Uji Toksisitas Akut Oral ... 49
5. Perhitungan Pemberian Dosis ... 50
6. Alat Yang Digunakan Dalam Pemberian Seduhan Teh ... 51
7. Hewan Percobaan Yang Digunakan ... 52
8. Gambar Perbandingan Organ Antar Kelompok ... 53