PENETAPAN KESERAGAMAN KANDUNGAN DEKSKLORFENIRAMIN MALEAT PADA TABLET DEKSTAMIN SECARA KROMATOGRAFI
CAIR KINERJA TINGGI
TUGAS AKHIR
Oleh:
GUNTUR PERJUANGAN NIM 072410009
PROGRAM DIPLOMA III ANALIS FARMASI DAN MAKANAN FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN
PENETAPAN KESERAGAMAN KANDUNGAN DEKSKLORFENIRAMIN MALEAT PADA TABLET DEKSTAMIN SECARA KROMATOGRAFI
CAIR KINERJA TINGGI TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Untuk Memperoleh Gelar Ahli Madya Pada Program Diploma III Analis Farmasi dan Makanan
Fakultas Farmasi Universitas Sumatera Utara
Oleh:
Guntur Perjuangan NIM 072410009
Medan, Mei 2010 Disetujui Oleh: Dosen Pembimbing
Drs. Syafruddin , M.S., Apt NIP 194811111976031003
Disahkan Oleh: Dekan,
KATA PENGANTAR
Segala puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah
melimpahkan Rahmat dan Karunia-Nya sehingga penulis dapat menyelesaikan
tugas akhir ini.
Adapun judul dari tugas akhir ini adalah ”Penetapan Keragaman
Kandungan Deksklorfeniramin Maleat Pada Tablet Dextamin Secara
Kromatografi Cair Kinerja Tinggi” yang dibuat sebagai salah satu syarat untuk
menyelesaikan Program Studi Diploma III Analis Farmasi dan Makanan Fakultas
Farmasi Universitas Sumatera Utara. Tugas Akhir ini disusun berdasarkan praktek
kerja lapangan di Balai Besar POM di Medan.
Tidak lupa penulis mengucapkan banyak terima kasih kepada semua pihak
yang telah memberi dorongan, bantuan dan dukungan moril maupun secara
spritual kepada penulis, sehingga penulis dapat menyelesaikan tugas akhir ini
dengan baik dan pada kesempatan ini penulis juga ingin mengucapkan terima
kasih kepada :
1. Ayahanda St. HR Sihombing dan Ibunda Tj. Purba tercinta serta seluruh
keluarga yang telah memberikan doa restu dan motivasi sehingga Tugas
Akhir ini selesai.
2. Bapak Drs. Syafruddin, M.S., Apt., yang telah membimbing dan
mengarahkan penulis dalam menyusun Tugas Akhir ini.
3. Bapak Prof. Dr. Sumadio Hadisahputra., Apt. selaku Dekan Fakultas
4. Bapak Prof. Dr. Jansen Silalahi M.App.Sc., Apt selaku koordinator
program Diploma III Analis Farmasi dan Makanan Fakultas Farmasi
Universitas Sumatera Utara.
5. Ibu Zakiah Kurniati, S. Farm, Apt. selaku Koordinator Pembimbing PKL
di Balai Besar POM di Medan.
6. Seluruh staf dan karyawan Balai Besar POM di Medan yang telah
membantu penulis selama Praktek Kerja Lapangan (PKL).
7. Bapak dan Ibu dosen beserta seluruh staf Program Studi Diploma III
Analis Farmasi dan Makanan Universitas Sumatera Utara.
8. Teman-temanku YESUA HAMASIA yang selalu memberikan dukungan
dan doa kepada penulis.
9. Seluruh rekan-rekan mahasiswa Analis Farmasi dan Makanan Angkatan
2007 yang telah memberikan saran dan dukungan dalam menyelesaikan
tugas akhir ini.
Penulis menyadari bahwa tugas akhir ini tidak luput dari kekurangan dan
kelemahan, oleh karena itu penulis mengharapkan kritik dan saran yang bersifat
membangun dari semua pihak yang membaca karya ilmiah ini demi
kesempurnaan penulisan dimasa yang akan datang. Akhir kata penulis berharap
semoga karya ilmiah ini dapat bermanfaat bagi kita semua.
Medan, Mei 2010
Penulis
DAFTAR ISI
Halaman
Lembar Judul……… i
Lembar Pengesahan……….. ii
Kata Pengantar……….. iii
BAB I PENDAHULUAN……… 1
1.1 Latar Belakang………. 1
1.2 Tujuan dan Manfaat………. 3
1.2.1 Tujuan……… 3
1.2.2 Manfaat………. 3
BAB II TINJAUAN PUSTAKA………... 4
2.1 Tablet……….... 4
2.2 Antihistamin-antialergi……….. 6
2.3 Evaluasi Tablet……….. 8
2.4 Kromatografi………. 11
2.4.1 Kromatografi Kolom……….. 12
2.4.2 Kromatografi Kertas………... 12
2.4.3 Kromatografi Lapis Tipis……… 13
2.5 Pembagian Kromatografi……….. 13
2.5.1 Kromatografi Adsorpsi……….... 14
2.5.2 Kromatografi Partisi………. 14
2.5.3 Pertukaran Ion……….. 14
2.5.4 Kromatografi Eksklusi………. 15
2.6 Kromatografi Cair Kinerja Tinggi……….. 15
2.6.1 Pompa……….. 16
2.6.2 Kolom………... 16
2.6.3 Wadah fase gerak pada KCKT………. 16
2.6.4 Fase gerak pada KCKT………. 17
2.6.5 Detektor………. 17
2.6.6 Perekam………. 17
2.7 Dekskloefeniramin maleat……….. 18
2.7.1 Sifat Fisika Kimia………. 18
2.7.2 Mekanisme Kerja……….. 19
2.7.3 Farmakokinetik Deksklorfeniramin maleat……….. 19
2.7.4 Efek Samping……… 20
2.8 Metode Penetapan Deksklorfeniramin maleat……… 20
2.8.1 Secara Spektrofotometri……… 20
2.8.2 Secara Volumetri……….. 20
BAB III METODOLOGI………. 21
3.1 Sampel yang diperiksa……… 21
3.2 Alat dan Bahan……… 21
3.2.1 Alat……… 21
3.2.2 Bahan……… 21
3.3.1 Fase gerak………. 22
3.3.2 Pembuatan Larutan Uji………. 22
3.3.3 Pembuatan Larutan Baku………. 22
3.4 Cara Penetapan secara KCKT……… 23
BAB IV HASIL DAN PEMBAHASAN………. 24
4.1 Hasil……… 24
4.2 Pembahasan……… 26
BAB V KESIMPULAN DAN SARAN………... 27
5.1 Kesimpulan………. 27
5.2 Saran………... 27 DAFTAR PUSTAKA
BAB I PENDAHULUAN
1.1. Latar Belakang
Obat memiliki cakupan makna yang cukup luas, bukan hanya terbatas
pada zat-zat yang digunakan untuk menyembuhkan seseorang dari sakit. Zat-zat
yang berfungsi untuk menetapkan diagnosa (mengetahui penyakit), mencegah,
mengurangi, menghilangkan penyakit atau gejala penyakit, luka atau kelainan,
baik jasmani maupun rohani pada manusia dan hewan juga disebut obat(Widodo,
2004).
Tablet merupakan bahan obat dalam bentuk sediaan padat yang
biasanya dibuat dengan penambahan bahan tambahan farmasetika yang sesuai.
Tablet-tablet dapat berbeda dalam ukuran, bentuk, berat, kekerasan, ketebalan,
daya hancurnya, dan dalam aspek lainnya tergantung pada cara pemakaian tablet
dan metode pembuatannya. Kebanyakan tablet digunakan pada pemberian obat
secara oral, dan kebanyakan dari tablet ini dibuat dengan penambahan zat warna,
zat pemberi rasa, dan lapisan-lapisan dalam berbagai jenis(Ansel, 1989).
Deksklorfeniramin maleat adalah antihistamin derivat propilamin.
Deksklorfeniramin maleat menghambat aksi farmakologis histamin secara
kompetitif(antagonis histamin reseptor H1). Deksklorfeniramin maleat merupakan
suatu antihistamin yang dapat mencegah gejala-gejala alergi, yang disebabkan
sebagian besar oleh histamin (H1). Deksklorfeniramin maleat bekerja dengan
Selain itu juga dapat mengatasi reaksi hipersensitivitas atau keadaan lain yang
disertai penglepasan histamine endogen yang berlebihan(Anonim, 2009).
Penetapan kadar deksklorfeniramin maleat dapat dilakukan secara titrasi
bebas air-basa (TBA-Basa), spektrofotometri, dan kromatografi cair kinerja tinggi
(KCKT). Pada titrasi bebas air-basa penetapan kadar deksklorfeiramin maleat
menggunakan pelarut asam asetat dan pentiter asam perklorat. Asam asetat
merupakan penerima proton yang sangat lemah sehingga tidak berkompetisi
secara efektif dengan basa-basa lemah dalam hal menerima proton. Asam
perklorat dalam larutan asam asetat merupakan asam yang paling kuat diantara
asam-asam umum yang digunakan untuk titrasi basa lemah dalam medium bebas
air. Dalam TBA biasanya ditambah dengan asam asetat anhidra dengan tujuan
untuk menghilangkan air yang ada dalam asam perklorat(Rohman, 2007).
Sedangkan pada spektrofotometri deksklorfeniramin maleat penetapan
kadar dilakukan secara spektrum ultraviolet, diukur pada panjang gelombang 265
nm : A¦ 320a.
Penetapan kadar deksklorfeniramin maleat dalam tablet campuran dengan
deksametason dapat dilakukan dengan metode kromatografi cair kinerja
tinggi(KCKT) fase balik dengan kolom Larutan A dan B disuntikkan secara
terpisah dan dilakukan kromatografi cair kinerja tinggi dengan menggunakan
kolom baja tahan karat C18/L1 diameter 3 – 6 mm panjang antara 150- 400 mm,
isi gugus oktadesilsilan pada penyangga silica dengan ukuran partikel 3 – 10 mm,
semua penetapan dilakukan pada UV-Vis pada absorbansi detector dengan
20 µL dengan fase gerak Kalium Dihidrogen Pospat (KH2PO4 ) 0,05 M : Metanol
(85:15), disaring menggunakan membran filter 0,45 µm(Metode analisa, 2001).
1.2. Tujuan dan Manfaat 1.2.1. Tujuan
Adapun tujuan dari penetapan kadar Deksklorfeniramin Maleat adalah
untuk mengetahui apakah kadar Deksklorfeniramin Maleat yang terdapat dalam
sediaan tablet secara kromatografi cair kinerja tinggi memenuhi persyaratan sesuai
dengan Farmakope Indonesia yaitu berada pada rentang 85-115 dengan
simpangan baku relatif ≤ 6,0 % .
1.2.2. Manfaat
Adapun manfaat dari penetapan kadar Deksklorfeniramin Maleat adalah
untuk mengetahui apakah kadar Deksklorfeniramin Maleat memenuhi syarat yang
BAB II
TINJAUAN PUSTAKA
2.1 Tablet
Tablet adalah sediaan padat, dibuat secara kempa-cetak berbentuk rata
atau cembung rangkap, umumnya bulat, mengandung satu jenis obat atau lebih
dengan atau tanpa zat tambahan. Zat tambahan yang digunakan dapat berfungsi
sebagai:
a. Zat pengisi, yaitu untuk memperbesar volume tablet. Biasanya yang
digunakan Amilum Manihot, Kalsium fosfat, Kalsium Karbonat dan zat lain
yang cocok.
b. Zat pengikat, yaitu agar tablet tidak pecah atau retak, dapat merekat. Biasanya
yang digunakan adalah musilago 10-20%, larutan Metil cellulosum 5%.
c. Zat penghancur, yaitu agar tablet dapat hancur dalam saluran pencernaan.
Biasanya yang digunakan Amilum manihot kering, Gelatin, Natrium Alginat.
d. Zat pelicin, yaitu agar tablet tidak melekat pada cetakan. Biasanya yang
digunakan Talkum 5%, Magnesium stearat, asam stearat.
Menurut Ansel, (1989) berdasarkan penggunaannya tablet
diklasifikasikan sebagai berikut :
a. Tablet kunyah
Tablet ini harus lembut (segera hancur ketika dikunyah) atau mudah
melarut dalam mulut. Pengunyahan dapat mempercepat penghancuran tablet dan
tablet antasida. Tablet kunyah diberikan pada pasien yang mengalami gangguan
menelan tablet. Tablet ini digunakan dalam formulasi tablet untuk anak-anak
(dalam sediaan multivitamin). Sediaan ini juga memungkinkan untuk digunakan
ditempat yang tidak tersedia air. Contohnya: Acitral, Vitacimin, Promag
b. Tablet Sublingual
Tablet yang disisipkan dibawah lidah. Biasanya berbentuk datar,
ditujukan untuk obat-obat yang diabsorbsi melalui mukosa oral. Cara ini berguna
untuk penyerapan obat yang rusak oleh cairan lambung dan sedikit sekali
diabsorpsi oleh saluran pencernaan. Tablet ini dibuat segera melarut untuk
memberikan efek yang cepat. Contohnya: Bodrexin tablet
c. Tablet bukal
Tablet yang disisipkan di pipi. Tablet ini dibuat agar hancur dan melarut
perlahan-lahan. Contohnya: Promag tablet
d. Tablet triturat
Tablet ini bentuknya kecil dan biasanya silinder. Tablet triturat harus cepat
dan mudah larut seutuhnya didalam air. Contohnya: Supradyn, Bevitram.
e. Tablet hipodermik
Tablet ini digunakan melalui bawah kulit, dibuat dari bahan yang mudah
larut. Contohnya: Andantol, sagalon, Confortin.
e. Tablet efervesen
Tablet yang menghasilkan gas, dibuat dengan cara kompresi granul yang
mengandung garam efervesen atau bahan-bahan lain yang mampu menghasilkan
bikarbonat dengan tatrat menghasilkan gas CO2 di dalam air. Tablet bentuk ini
mempercepat pelarutan sediaan dan meningkatkan rasa, contohnya: tablet CDR,
Redoxon.
f. Tablet Sistemik; Per Oral
Tablet yang bekerja sistemik dapat dibedakan menjadi:
- yang bekerja short acting (jangka pendek ): dalam satu hari memerlukan
beberapa kali menelan tablet. Contohnya: Dextamin tablet, Dermasolon.
- yang bekerja long acting (jangka panjang): dalam satu hari cukup satu kali
menelan tablet, contohnya: Pharmaton tablet, Hemaviton Formula.
2.2 Antihistamin-antialergi
Antihistamin (antagonis histamin) adalah zat yang mampu mencegah
penglepasan atau kerj
menjelaskan antagonis histamin yang mana pun, namun seringkali istilah ini
digunakan untuk merujuk kepada antihistamin klasik yang bekerja pada reseptor
histamin H1. Antihistamin ini biasanya digunakan untuk mengobati reaksi alergi,
yang disebabkan oleh tanggapan berlebihan tubuh terhadap alergen (penyebab
alergi), seperti serbuk sari tanaman. Reaksi alergi ini menunjukkan penglepasan
histamin dalam jumlah signifikan di tubuh.
Terdapat beberapa jenis antihistamin, yang dikelompokkan berdasarkan
sasaran kerjanya terhadap reseptor histamin. Antagonis Reseptor Histamin H1
secara klinis digunakan untuk mengobati alergi. Contoh obatnya adalah:
difenhidramina, loratadina, desloratadina, meclizine, quetiapine (khasiat
Deksklorfeniramin maleat merupakan suatu antihistamin yang dapat mencegah
gejala-gejala alergi, yang disebabkan sebagian besar oleh histamin (H1).
Deksklorfeniramin maleat bekerja dengan menghambat reseptor H1, pada
pembuluh darah, bronkus, dan berbagai otot polos. Selain itu juga dapat mengatasi
reaksi hipersensitivitas atau keadaan lain yang disertai penglepasan histamin
endogen yang berlebihan.
Klorfeniramin merupakan antihistamin derivat propilamin.
Deksklorfeniramin maleat merupakan bentuk dextro isomer, memiliki aktivitas
2X lipat dibanding klorfeniramin berbentuk rasematnya.
Obat-obat anti alergi yang bisa dijumpai secara bebas di apotek atau toko
obat adalah golongan antihistamin. Obat ini bekerja dengan cara memblokir
reseptor histamin sehingga histamin tidak bisa bekerja lagi menyebabkan
reaksi-reaksi alergi. Obat ini hanya bisa menyembuhkan gejala alergi, tetapi tidak bisa
menyembuhkan alergi. Artinya, walaupun sekarang sudah hilang gatal-gatalnya,
tetapi jika suatu saat terjadi kontak lagi dengan alergen, maka reaksi alergi bisa
timbul lagi. Obat antihistamin yang paling banyak digunakan adalah
klorfeniramin maleas atau CTM (chlor tri methon). Obat ini bisa diperoleh dalam
bentuk tunggal atau kombinasi dengan obat-obat lain. Pada komposisi obat flu
atau obat batuk, sering sekali dijumpai adanya CTM, mungkin karena sebagian
kejadian flu atau batuk dapat dipicu oleh reaksi alergi. Obat antihistamin lain
adalah : prometazin, difenhidramin, dan deksklorfeniramin. Obat-obat ini
termasuk antihistamin generasi pertama yang memiliki efek samping mengantuk.
menjalankan mesin-mesin berat. Obat ini dapat dibeli secara bebas di apotek atau
toko obat. Antihistamin generasi yang lebih baru adalah antihistamin yang tidak
berefek sedatif (mengantuk), contohnya : loratadin, terfenadin, triprolidin,
setirizin, dan ketotifen. Obat-obat ini biasanya harus diperoleh dengan resep
dokter.
Semua obat-obat antihistamin ini aksinya mirip satu sama lain, tetapi
berbeda lama aksinya. Loratadin dan terfenadin misalnya, lama aksinya lebih dari
12 jam, sehingga cukup diminum sehari sekali atau dua kali, sedangkan
prometazin dan difenhidramin aksinya hanya 4-6 jam, sehingga harus diminum
3-4 kali sehari. Obat-obat antihistamin bisa diperoleh dalam bentuk tablet, sirup,
atau salep. Penggunaannya disesuaikan dengan macam alerginya dan kemudahan
pasien menggunakannya. Jika reaksi alerginya hanya bersifat lokal di permukaan
kulit, penggunaan salep cukup efektif. Tetapi jika reaksinya luas di seluruh tubuh,
penggunaan obat per-oral (yang diminum) lebih disarankan(Zulliesikawati, 2010).
2.3 Evaluasi tablet
Untuk menjamin mutu tablet maka dilakukan beberapa pengujian yaitu sebagai berikut:
a. Uji keseragaman bobot
Tablet harus memenuhi uji keseragaman bobot. Keseragaman bobot ini
ditetapkan untuk menjamin keseragaman bobot tiap tablet yang dibuat.
Tablet-tablet yang bobotnya seragam diharapkan akan memiliki kandungan bahan obat
dapat ditetapkan sebagai berikut: ditimbang 20 tablet, lalu dihitung bobot rata-rata
tiap tablet. Kemudian timbang tablet satu persatu, tidak boleh lebih dari 2 tablet
bobotnya menyimpang dari bobot rata-rata lebih besar dari yang ditetapkan pada
kolom A dan tidak boleh satu tablet pun bobotnya menyimpang dari rata-rata
lebih besar dari yang ditetapkan pada kolom B. jika perlu gunakan 10 tablet yang
lain dan tidak satu tablet yang bobotnya menyimpang lebih besar dari bobot
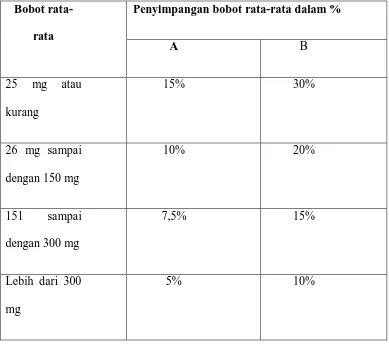
[image:15.595.122.511.333.677.2]rata-rata yang ditetapkan dalam kolom A maupun kolom B (Dirjen POM,1979).
Tabel 1 : Penyimpangan bobot rata-rata
Bobot rata-rata
Penyimpangan bobot rata-rata dalam %
A B
25 mg atau
kurang
15% 30%
26 mg sampai
dengan 150 mg
10% 20%
151 sampai
dengan 300 mg
7,5% 15%
Lebih dari 300
mg
b. Uji kekerasan
Kekerasan tablet dan ketebalannya berhubungan dengan isi die dan gaya
kompresi yang diberikan. Bila tekanan ditambahkan, maka kekerasan tablet
meningkat sedangkan ketebalan tablet berkurang. Selain itu metode granulasi juga
menentukan kekerasan tablet. Umumnya kekuatan tablet berkisar 4 - 8 kg, bobot
tersebut dianggap sebagai batas minimum untuk menghasilkan tablet yang
memuaskan. Alat yang di gunakan untuk uji ini adalah hardness tester, alat ini
diharapkan dapat mengukur berat yang diperlukan untuk memecahkan tablet
(Lachman,1994).
c. Uji keregasan
Cara lain untuk menentukan kekuatan tablet ialah dengan mengukur
keregasannya. Gesekan dan goncangan merupakan penyebab tablet menjadi
hancur. Untuk menguji keregasan tablet digunakan alat Roche friabilator.
Sebelum tablet dimasukkan ke alat friabilator, tablet ditimbang terlebih dahulu.
Kemudian tablet dimasukkan kedalam alat, lalu alat dioperasikan selama empat
menit atau 100 kali putaran. Tablet ditimbang kembali dan dibandingkan dengan
berat mula-mula. Selisih berat dihitung sebagai keregasan tablet. Persyaratan
keregasan harus lebih kecil dari 0,8 %(Ansel,1989).
d. Uji waktu hancur
Peralatan uji waktu hancur terdiri dari rak keranjang yang mempunyai enam
lubang yang terletak vertikal diatas ayakan mesh nomor 10 selama percobaan,
tablet diletakkan pada tiap lubang keranjang. Kemudian keranjang tersebut
permenit. Interval waktu hancur adalah 5 – 30 menit. Tablet dikatakan hancur bila
bentuk sisa tablet (kecuali bagian penyalut) merupakan massa dengan inti yang
tidak jelas(Ansel,1989).
e. Uji penetapan kadar zat berkhasiat
Uji penetapan kadar berkhasiat dilakukan untuk mengetahui apakah tablet
tersebut memenuhi syarat sesuai dengan etiket. Bila kadar obat tersebut tidak
memenuhi syarat maka obat tersebut tidak memiliki efek terapi yang baik dan
tidak layak dikonsumsi. Uji penetapan kadar dilakukan dengan menggunakan
cara-cara yang sesuai pada masing-masing monografi antara lain di Farmakope
Indonesia Edisi IV 1995.
f. Uji disolusi
Obat yang telah memenuhi persyaratan kekerasan, waktu hancur, keregasan,
keseragaman bobot, dan penetapan kadar, belum dapat menjamin bahwa suatu
obat memenuhi efek terapi, karena itu uji disolusi harus dilakukan pada setiap
produksi tablet. Disolusi adalah proses pemindahan molekul obat dari bentuk
padat kedalam larutan pada suatu medium. Disolusi menunjukan jumlah bahan
obat yang terlarut dalam waktu tertentu. Disolusi menggambarkan efek obat
secara invitro, jika disolusi memenuhi syarat maka diharapkan obat akan
memberikan khasiat secara invivo.
2.4 Kromatografi
Kromatografi pertama kali dikembangkan oleh seorang ahli botani Rusia
Michael Tsweet pada tahun 1903 untuk memisahkan pigmen berwarna dalam
berisi kalsium karbonat (CaCo3). Saat ini kromatografi merupakan teknik
pemisahan yang paling umum dan paling sering digunakan dalam bidang kimia
analisis dan dapat dimanfaatkan untuk melakukan analisis, baik analisis kualitatif,
kuantitatif, atau preparative dalam bidang farmasi, lingkungan, industri, dan
sebagainya. Kromatografi suatu teknik pemisahan yang menggunakan fase diam
(stationary phase) dan fase gerak (mobile phase)(Rohman, 2007).
Jenis kromatografi yang bermanfaat dalam analisa kualitatif dan kuantitatif
yang digunakan dalam penetapan kadar dan pengujian Farmakope Indonesia
adalah kromatografi Kolom, Kromatografi Gas, Kromatografi Kertas,
Kromatografi Lapis Tipis dan KCKT.
2.4.1 Kromatografi Kolom
Kromatografi kolom terbagi atas kromatografi kolom adsorpsi dan
kromatografi kolom partisi. Pada kromatografi kolom adsorpsi zat uji dilarutkan
dalam sejumlah kecil pelarut, dituangkan kedalam kolom dan dibiarkan mengalir
kedalam penjerap, sedangkan pada kromatografi kolom partisi, zat yang harus
dipisahkan terbagi antara dua cairan yang tidak saling bercampur. Salah satu
campuran. Salah satu cairan, yaitu fase diam, umumnya diadsorpsikan pada
penyangga padat.
2.4.2 Kromatografi Kertas
Pada kromatografi kertas sebagai penjerap digunakan sehelai kertas dengan
susunan serabut dan tebal yang sesuai. Sebagai alternatif dapat juga digunakan
menjadi fase diam (umumnya fase yang lebih polar dalam hal kertas yang
dimodifikasi). Kromatogram dilakukan dengan merambatkan fase gerak, melalui
kertas. Dapat dilakukan kromatografi menaik, pelarut merambat naik pada kertas
ditarik oleh gaya kapiler ataupun kromatografi menurun, pelarutnya mengalir
oleh gaya gravitasi.
2.4.3 Kromatografi Lapis Tipis
Pada KLT, zat penjerap merupakan lapis tipis serbuk halus yang dilapiskan pada
lempeng kaca. Plastik atau logam secara merata, umumnya digunakan lempeng
kaca. Pemisahan yang tercapai dapat didasarkan pada adsorpsi, partisi atau
kombinasi dari kedua efek, tergantung jenis penyangga, cara pembuatan, dan jenis
pelarut yang digunakan. Perkiraan identifikasi diperoleh dengan pengamatan
bercak dengan harga Rf yang identik dan ukuran yang hamper sama. Dengan
menotolkan zat uji dan baku pembanding pada lempeng yang sama. Bercak dapat
dikerok dari lempeng, kemudian diekstraksi dengan pelarut yang sesuai dan
diukur secara spektrofotometri.
2.5 Pembagian Kromatografi
Kromatografi dapat dibedakan atas berbagai macam tergantung pada
pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi
dapat dibedakan menjadi: (a) kromatografi adsorpsi; (b) kromatografi partisi; (c)
kromatografi pasangan ion; (d) kromatografi penukar ion; (e) kromatografi
2.5.1 Kromatografi Adsorpsi
Adsorpsi merupakan penyerapan pada permukaannya saja dan jangan
sekali-kali dikacaukan dengan proses absorpsi yang berarti penyerapan
keseluruhan. Adsorpsi pada permukaan melibatkan interaksi-interaksi
elektrostatik seperti ikatan hidrogen, penarikan dipol-dipol, dan penarikan yang
diinduksi oleh dipole. Silika gel merupakan jenis absorben (fase diam) yang
penggunaannya paling luas. Permukaan silika gel terdiri atas gugus Si-O-Si dan
gugus silanol (Si-OH).
2.5.2 Kromatografi Partisi
Partisi merupakan analog dengan ekstraksi pelarut. Fase diam diikatkan
pada padatan lapis tipis yang lembam (inert). Karena fase diam cair diikatkan
pada padatan pendukung maka masih diperdebatkan apakah proses adsorpsinya
merupakan partisi murni atau partisi yang dimodifikasi karena absorpsi juga
mungkin terjadi(Rohman,2007).
Cara ini didasarkan pada partisi linarut antara dua pelarut yang tak
bercampur, salah satunya diam (fase diam) dan yang lainnya bergerak (fase
gerak). Pada tahap awal KC, fase diam dibuat dengan cara yang sama seperti
membuat penyangga kromatografi gas(Johnson, Stevenson,1991).
2.5.3 Pertukaran Ion
Cara ini didasarkan pada pertukaran (penjerapan) ion antara fase gerak dan
titik ion pada kemasan. Banyak dammar diperoleh dari kopolimer stirena
divinilbenzena yang telah ditambahi gugus fungsi. Dammar jenis asam sulfonat
pemakaian. Baik fase terikat maupun dammar telah digunakan. Cara tersebut
banyak dipakai dalam ilmu hayat, contohnya pemisahan asam amino, dan dapat
pula dipakai untuk pemisahan kation dan anion (Jonhson, Stevenson,1991)
2.5.4 Kromatografi Eksklusi
Eksklusi berbeda dari mekanisme sorpsi yang lain, yakni dalam eksklusi
tidak ada interaksi spesifik antara solute dengan fase diam. Teknik ini unik karena
dalam pemisahan didasarkan pada ukuran molekul dari zat padat pengepak (fase
diam). Pengepak adalah suatu gel dengan permukaan berlubang-lubang sangat
kecil (porous) yang inert. Sebagai fase gerak digunakan cairan. Kromatografi
jenis ini sangat dipengaruhi oleh perbedaan bentuk struktur dan ukuran molekul
(Rohman,2007)
.
2.6 Kromatografi Cair Kinerja Tinggi
Kromatografi cair kinerja tinggi atau KCKT atau biasa juga disebut
dengan HPLC (High Performance Liquid Chromatography) dikembangkan pada
akhir tahun 1960an dan awal tahun 1970an. Saat ini, KCKT merupakan teknik
pemisahan yang diterima secara luas untuk analisis dan pemurnian senyawa
tertentu dalam suatu sampel tertentu seperti asam-asam amino, asam-asam
nukleat, dan protein-protein dalam cairan fisiologis; menentukan kadar
senyawa-senyawa aktif obat, produk hasil samping proses sintesis, atau produk-produk
Instrumentasi KCKT pada dasarnya terdiri atas delapan komponen pokok
yaitu : (1) wadah fase gerak, (2) sistem penghantaran fase gerak, (3) alat untuk
memasukkan sampel, (4) kolom, (5) detektor, (6) wadah penampung buangan fase
gerak, (7) tabung penghubung, dan (8) suatu computer atau integrator atau
perekam.
2.6.1 Pompa
fase gerak dalam KCKT sudah tentu cair, dan untuk menggerakkannya
melalui kolom diperlukan alat. Ada dua jenis utama pompa yang digunakan :
tekanan-tetap dan pendesakan-tetap. Pompa pendesakan tetap dapat dibagi
menjadi pompa torak dan pompa semprit. Pompa torak menghasilkan aliran yang
berdenyut, jadi memerlukan peredam denyut atau peredam elektronik untuk
menghasilkan garis alas detector yang stabil jika detector peka terhadap aliran.
Kelebihan utamanya tidak terbatas. Pompa semprit menghasilkan aliran yang tak
berdenyut, tetapi tandonnya terbatas(Johnson, Stevenson 1991).
2.6.2 Kolom
Kolom merupakan jantung kromatografi, keberhasilan atau kegagalan
analisis bergantung pada pilihan kolom dan kondisi kerja yang tepat. Dianjurkan
untuk memasang penyaring 2 µ m di jalur antara penyuntik dan kolom, untuk
menahan partikel yang dibawa fase gerak dan cuplikan. Hal ini dapat
memperpanjang umur kolom(Munson, 1991).
2.6.3 Wadah Fase Gerak pada KCKT
Wadah fase gerak harus bersih dan lembam (inert). Wadah pelarut kosong
gerak biasanya dapat menampung fase gerak antara 1 sampai 2 liter pelarut. Fase
gerak sebelum digunakan dilakukan degassing (penghilangan gas) yang ada pada
fase gerak, sebab adanya gas akan berkumpul dengan komponen lain terutama di
pompa detektor sehingga akan mengacaukan analisis.(Rohman, 2007)
2.6.4 Fase Gerak pada KCKT
Pada kromatografi cair, susunan pelarut atau fase gerak merupakan salah
satu peubah yang mempengaruhi pemisahan. Berbagai macam pelarut dipakai
dalam semua ragam KCKT, tetapi ada beberapa sifat yang diinginkan yang
berlaku umum. Fase gerak haruslah : (a) murni, tanpa cemaran; (b) tidak bereaksi
dengan kemasan; (c) sesuai dengan detektor; (d) dapat melarutkan cuplikan; (e)
mempunyai viskositas rendah; (f) memungkinkan memperoleh kembali cuplikan
dengan mudah, jika diperlukan; (g) harganya wajar ( Johnson & Stevenson,1991).
2.6.5 Detektor
Detektor harus memberi tanggapan pada cuplikan, tanggapan yang dapat
diramal, peka, hasil yang efisien dan tidak terpengaruh oleh perubahan suhu atau
komposisi fase gerak. Detektor yang dipakai pada KCKT biasanya adalah UV 254
nm. Bila tanggapan detektor lebih lambat dari elusi sample timbullah pelebaran
pita yang memperburuk pemisahan. Pemilihan detektor KCKT tergantung pada
sifat sample, fase gerak dan kepekaan yang tinggi dicapai.
2.6.6 Perekam
Perekam merupakan salah satu dari bagian peralatan yang berfungsi untuk
merekam atau menunjukkan hasil pemeriksaan suatu senyawa berupa peak
mengetahui senyawa apa yang diperiksa, luas dan tinggi puncak berbanding lurus
dengan konsentrasi. Dari data ini dapat pula dipakai untuk memperoleh secara
kuantitatif. Sebagai perekam biasanya dipakai bersama-sama dengan
integrator(Munson, 1991).
2.7 Deksklorfeniramin Maleat 2.7.1 Sifat Fisika Kimia
Nama kimia : (+)-2-[p-Kloro α-[(Dimetilamino)etil]benzil] piridina
maleat
Rumus molekul : C16H19ClN2. C4H4O6
Berat molekul : 390,87
Pemerian : Serbuk hablur putih tidak berbau
Susut pengeringan : Lakukan pengeringan pada suhu 65oC selama 4 jam
sebelum digunakan.
pKb : 4-5
Kelarutan : Mudah larut dalam air, larut dalam etanol dan dalam
kloroform, sukar larut dalam benzene dan dalam eter
Aqueous acid 265 nm : A¦ 320a
Deksklorfeniramin Maleat mengandung tidak kurang dari 98,0% dan tidak
lebih dari 100,5% C16H19ClN2. C4H4O6, dihitung terhadap zat yang telah
dikeringkan(Ditjen POM,1995).
2.7.2 Mekanisme Kerja
Memblokir reseptor-H1 dengan menyaingi histamine pada reseptornya
diotot licin dinding pembuluh dan dengan demikian menghindarkan timbulnya
reaksi alergi. Khasiat lainnya menciutkan bronchi, saluran cerna, kandung kemih
dan rahim(Tjay dan Rahardja, 2002).
Obat yang menentang kerja histamin pada H1 reseptor histamin berguna
dalam menekan alergi yang disebabkan oleh timbulnya simptom karena
histamin(ISO, 2007).
2.7.3 Farmakokinetik Deksklorfeniramin Maleat
Proses mulai dari masuknya obat ke dalam tubuh sampai dikeluarkan
kembali disebut farmakokinetik. Termasuk dalam proses farmakokinetik ialah
absorpsi, distribusi, biotransformasi, dan ekskresi obat. Untuk menghasilkan efek,
sesuatu obat harus terdapat dalam kadar yang tepat pada tempat obat itu bekerja
( Sutomo,1991).
Setelah pemberian oral atau parenteral, AH1 diapsorsi secara baik.
Efeknya timbul 15-30 menit setelah pemberian oral dan dan maksimal 1-2 jam.
Lama kerja AH1 setelah pemberian dosis tunggal kira-kira 4-6 jam. Kadar
tertinggi terdapat pada paru-paru, sedangkan pada limpa, ginjal, otak, otot dan
2.7.4 Efek samping
Efek samping yang umum terjadi adalah sedasi (2-50% kasus). Efek sedasi
ini bersifat individual, tergantung pada individu, dosis, dan jenis antihistamin
yang diberikan. Efek samping lain berupa perasaan lemas dan pusing.
Jarang-jarang dapat pula terjadi gejala stimulasi SSP (gelisah, gugup, insomnia), gejala
efek antikolinergik berupa retensi urin (terutama pada orang tua), palpitasi, mulut
kering, dan konstipasi. Umumnya efek samping ini timbul pada dosis tinggi
(Sjamsuir,1991).
2.8 Metode Penetapan Deksklorfeniramin maleat
2.8.1 Secara Spektrofotometri UV
Spektrum serapan ultraviolet larutan 0,002% b/v dalam asam sulfat 0,1 N
setebal 2 cm pada daerah panjang delombang antara 230 nm dan 350 nm menun-
jukkan maksimum hanya pada 265 nm.
2.8.2 Secara Volumetri
Pada titrasi bebas air-basa penetapan kadar deksklorfeiramin maleat
menggunakan pelarut asam asetat dan pentiter asam perklorat. Asam asetat
merupakan penerima proton yang sangat lemah sehingga tidak berkompetisi
secara efektif dengan basa-basa lemah dalam hal menerima proton. Asam
perklorat dalam larutan asam asetat merupakan asam yang paling kuat diantara
asam-asam umum yang digunakan untuk titrasi basa lemah dalam medium bebas
air. Dalam TBA biasanya ditambah dengan asam asetat anhidra dengan tujuan
BAB III METODOLOGI
3.1 Sampel yang Diperiksa
Nama Dagang : Dextamine
Komposisi : Deksametason 0,5 mg, dan Deksklorfeniramin Maleat
2 mg.
No.Batch : D/201813
No.Reg : 15014013
Kadaluarsa : Sep 2012
Nama Industri : PT. PHAPROS tbk Semarang-Indonesia
3.2 Alat dan Bahan 3.2.1 Alat
HPLC (High Performance Liquid Chromatography) Shimadzu Seri
LC20AD,labu ukur 10ml; 25ml, branson Ultrasonic, gelas ukur 1000ml, beaker
glas, pipet tetes, membran filter ukuran 0,45µ m, timbangan analitik.
3.2.2. Bahan
Aquadest, kalium Dihidrogen Pospat (KH2PO4 ) 0,05 M, metanol,
3.3 Pembuatan Pereaksi 3.3.1 Fase gerak
Ditimbang seksama Kalium Dihidrogen Pospat (KH2PO4 ) sebanyak
6,8096 g, diencerkan dengan aquadest, masukkan kedalam labu tentukur 1000 ml,
dicukupkan dengan aquadest ( Larutan A), dari Larutan A diambil sebanyak 850
ml dan dicampur dengan 150 ml metanol, kocok hingga homogen dan pindahkan
kedalam beaker glass.
3.3.2 Pembuatan Larutan Uji
Ambil 10 tablet Dextamin masukkan masing-masing kedalam 10 buah
labu tentukur 10 ml, larutkan dengan FG, sonikasi selama 15 menit dicukupkan
sampai garis tanda dengan FG, Saring dengan kertas whatman.
3.3.3 Pembuatan Larutan Baku
Ditimbang seksama Deksklorfeniramin BPFI sebanyak 2,082 mg
masukkan kedalam labu tentukur 10 ml, larutkan dengan FG, sonikasi selama 15
3.4 Cara Penetapan secara KCKT
Larutan A dan B disuntikkan secara terpisah dan dilakukan kromatografi cair kinerja tinggi dengan menggunakan kolom baja tahan karat C18/L1 diameter 3
– 6 mm panjang antara 150- 400 mm, isi gugus oktadesilsilan pada penyangga
silica dengan ukuran partikel 3 – 10 mm, semua penetapan dilakukan pada
UV-Vis pada absorbansi detector dengan panjang gelombang 254 nm, kecepatan aliran
1,0 ml/menit, Volume penyuntikan 20 µL dengan fase gerak Kalium Dihidrogen
Pospat (KH2PO4 ) 0,05 M : Metanol (85:15), disaring menggunakan membran
filter 0,45 µm.
Hasil yang diperoleh dapat dilihat dari bentuk puncak yang direkam oleh
CBM ( Communication Bus Mobile) yaitu sejenis penghubung dengan komputer
yang dilengkapi dengan pencetak kromatogram.
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil
Penetapan kadar Deksklorfeniramin Maleat pada tablet dextamin secara
Kromatografi Cair Kinerja Tinggi (KCKT) memenuhi syarat yaitu berada pada
rentang antara 85-115 %, dengan simpangan baku relatif ≤ 6,0 % .
Rumus Perhitungan kadar
Bobot = xkandbaku Fu Fb x Bu Bb x Lb Lu
Dimana : Lu : Luas Area Uji
Lb : Luas Area Baku
Bb : Bobot Baku
Bu : Bobot Uji
Fu : Faktor Uji
Fb : Faktor Baku
Perhitungan :
Bobot 1 = 99,5703
10 10 2 082 , 2 532616 517074 x x x
= 100,6260%
Bobot 2 = 99,5703
10 10 2 082 , 2 532616 508947 x x x
Bobot 3 = 99,5703 10 10 2 082 , 2 532616 545443 x x x
= 106,1489%
Bobot 4 = 99,5703
10 10 2 082 , 2 532616 498050 x x x
= 96,0134%
Bobot 5 = 99,5703
10 10 2 082 , 2 532616 513480 x x x
= 99,9286%
Bobot 6 = 99,5703
10 10 2 082 , 2 532616 533079 x x x
= 103,7427%
Bobot 7 = 99,5703
10 10 2 082 , 2 532616 511237 x x x
= 99,4921%
Bobot 8 = 99,5703
10 10 2 082 , 2 532616 580175 x x x
Bobot 9 = 99,5703 10 10 2 082 , 2 532616 526312 x x x
= 102,4258%
Bobot 10 = 99,5703
10 10 2 082 , 2 532616 519938 x x x
= 101,1854%
% RSD = 4,451 ( Memenuhi Syarat )
4.2 Pembahasan
Dari hasil percobaan dengan menggunakan Kromatografi Cair Kinerja
Tinggi (KCKT), diketahui bahwa kadar keragaman kandungan Deksklorfeniramin
Maleat memenuhi syarat berada pada rentang antara 85-115 %, dengan simpangan
baku relatif ≤ 6 % .
Metode KCKT yang digunakan adalah dengan kolom fase terbalik.
Kromatografi ini fase diamnya bersifat non polar sedangkan fase geraknya
bersifat polar yaitu campuran metanol dan dapar pospat dimana akan terjadi
pemisahan yang berdasarkan kompetisi antara fase gerak dengan sampel yang
berikatan didalam kolom. Oleh karena itu molekul-molekul polar akan lebih cepat
keluar dari kolom sedangkan molekul-molekul yang non polar akan tertahan lebih
lama didalam kolom. Penetapan kadar deksklorfeniramin dapat dilakukan dengan
metode titrasi Titrasi Bebas Air (TBA) dengan pentiter asam perklorat 0,1 N dan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
• Metoda Kromatogarfi Cair Kinerja Tinggi (KCKT) dapat digunakan
untuk menetapkan kadar Deksklorfeniramin Maleat dalam sedian
tablet
• Penetapan kadar yang diperoleh dari hasil percobaan pada
Deksklorfeiramin Maleat memenuhi syarat karena berada pada rentang
antara 85-115%, dengan simpangan baku relatif ≤ 6 % .
5.2 Saran
• Diharapkan agar dilakukan penetapan kadar Deksklorfeniramin
Maleat dalam sediaan lain.
• Diharapkan kepada PT PHAPROS untuk mempertahankan kadar
produksinya dalam rentang yang telah ditetapkan khususnya dalam
DAFTAR PUSTAKA
Anonim. (2006). Optilimasi Terapi Antihistamin. Ulas Obat Edisi Desember 2006 (vol. 6 No.5)
Ansel, H.C., (1989). Pengantar Bentuk Sediaan Farmasi. Edisi 4. Jakarta. Universitas Indonesia Press. Hal 244
Dr. Munaf S. (1991). Catatan Kuliah Farmakologi. Bagian I. Palembang. Buku Kedokteran EGC. Hal 106
Ditjen, POM Departemen Kesehatan RI. (1995). Farmakope Indonesia. Edisi 4. Jakarta. Departemen RI. Hal 293
Ditjen, POM Departemen Kesehatan RI. (1995). Farmakope Indonesia. Edisi 4. Jakarta. Departemen RI. Hal 1001-1012
ISO. (2007). Informasi Spesialite Obat. Volume 42. Jakarta. Ikatan Sarjana Farmasi Indonesia.
Johnson. E.L, dan Stevenson, R., (1991). Dasar Kromatografi Cair. Bandung. ITB. Hal 4,7-8
Lachman, L dan Lieberman Herbert A. (1994). Teori dan Praktek Farmasi Industri II. Edisi 2. Jakarta. Universitas Indonesia. Hal 1091-1092
Munson, J.W., (1991). Analis Farmasi Metode Modern, Parwa B. Surabaya. University Press. Hal 26-33
Rohman, Abdul. (2007). Kimia Farmasi Analis. Yogyakarta. Pustaka Pelajar. Hal 378-379
Sastrohamidjojo, H. (1985). Kromatografi. Edisi pertama. Cetakan pertama. Yogyakarta. Penerbit Liberty. Hal 46
Tjay, T.H., dan Rahardja, K. (2002). Obat-Obat Penting. Edisi IV. Cetakan ke 2. Jakarta. PT. Gramedia. Hal 685,777
Widodo, Rahayu, S.Si., Apt., (2004). Panduan Keluarga Memilih dan Menggunakan Obat. Yogyakarta. Penerbit Kreasi Wacana. Hal 1;95
Zulliesikawati. (2010). Alergi dan Pengobatannya. Tanggal akses 14 Mei 2010 http:// zulliesikawati.wordpress.com