PENERAPAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI (KCKT) PADA PENETAPAN KADAR
DEKSKLORFENIRAMIN MALEAT DALAM TABLET
CAMPURAN DENGAN DEKSAMETASON
SKRIPSI
OLEH:
JAYA PRAMANA SEMBIRING
NIM 081524015
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
PENERAPAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI (KCKT) PADA PENETAPAN KADAR
DEKSKLORFENIRAMIN MALEAT DALAM TABLET
CAMPURAN DENGAN DEKSAMETASON
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
JAYA PRAMANA SEMBIRING
NIM 081524015
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
Lembar Pengesahan Skripsi
PENERAPAN METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) PADA PENETAPAN KADAR DEKSKLORFENIRAMIN MALEAT DALAM TABLET CAMPURAN DENGAN DEKSAMETASON
OLEH:
JAYA PRAMANA SEMBIRING NIM 081524015
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: Juli 2011
Pembimbing I, Panitia Penguji,
Dra. Salbiah, M.Si., Apt NIP 194810131987012001 NIP 194809041974122001
Dra. Salbiah, M.Si., Apt NIP 194810131987012001 Pembimbing II,
Drs. Fathur Rahman Harun, M.Si., Apt. Drs. Syafruddin, M.S., Apt
NIP 195201041980031002 NIP 194811111976031003
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
Dekan,
KATA PENGANTAR
Puji serta syukur saya panjatkan atas kehadirat Tuhan Yang Maha Esa
karena atas Rahmat dan karunia-Nya lah, sehingga penulis dapat menyusun dan
menyelesaikan Skripsi ini sebagaimana mestinya. Skripsi ini berjudul
“PENERAPAN METODE KROMATOGRAFI CAIR KINERJA TINGGI
(KCKT) PADA PENETAPAN KADAR DEKSKLORFENIRAMIN MALEAT DALAM TABLET CAMPURAN DENGAN DEKSAMETASON”
Penulis menyadari bahwa dalam penulisan skripsi ini masih terdapat berbagai
kekurangan dan kesalahan, maka untuk itu penulis membuka hati untuk menerima
segala macam kritik dan saran yang bersifat membangun demi penyempurnaan
skripsi ini.
Skripsi ini merupakan syarat untuk menyelesaikan pendidikan program S-1 Ekstensi Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan banyak terima kasih kepada
Ibu Dra.Salbiah, MSi.,Apt dan Bapak Drs. Fathur Rahman Harun, M.Si., Apt
Selaku pembimbing yang telah membimbing penulis dengan kesabaran dari awal
penelitian hingga menyelesaikan penyusunan skripsi ini. Penulis juga
menyampaikan rasa terima kasih yang tulus kepada :
1. Ayahanda dan ibunda tercinta, serta seluruh keluarga tercinta atas doa
restu dan dorongan yang telah diberikan kepada penulis, hingga skripsi ini
selesai.
2. Bapak Prof.Dr. Sumadio Hadisahputra, Apt selaku dekan Fakultas Farmasi
3. Bapak Prof. Dr. Hakim Bangun, Apt., selaku penasehat akademik yang
telah memberikan motivasi dan bimbingan selama perkuliahan.
4. Ibu Dra. Nurmadjuzita, M.Si., Apt., Bapak Drs. Syafruddin, M.S., Apt.,
dan Ibu Dra. Sudarmi, M.Si., Apt., selaku penguji yang telah
memberikan kritik dan saran demi kesempurnaan skripsi ini.
5. Bapak atau Ibu Dosen yang mengajar di Program S-1 Ekstensi Farmasi
Fakultas Farmasi USU
6. Abang, kakak, dan adik-adik Fakultas Farmasi yang memberi dukungan
dan semangat kepada penulis.
Akhir kata penulis berharap semoga Skripsi ini bermanfaat bagi ilmu
pengetahuan pada umumnya dan ilmu farmasi pada khususnya.. Dan semoga
Tuhan yang Maha Kuasa senantiasa melimpahkan rahmat-Nya pada kita semua,
amin.
Medan, Juli 2011
Penulis
PENERAPAN METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) PADA PENETAPAN KADAR DEKSKLORFENIRAMIN MALEAT DALAM TABLET CAMPURAN DENGAN DEKSAMETASON
ABSTRAK
Sediaan obat yang mengandung deksklorfeniramin maleat dan deksametason banyak digunakan untuk berbagai penyakit. Hal ini dikarenakan deksametason memiliki kemampuan mengatasi peradangan serta alergi dan sifat antihistamin yang dimiliki oleh deksklorfeniramin maleat.
Menurut undang-undang no.36 tahun 2009 pasal 105 ayat 1 tentang kesehatan bahwa sediaan farmasi yang berupa obat dan bahan baku obat harus memenuhi syarat Farmakope Indonesia atau buku standar lainnya. Salah satu parameter obat tersebut dikatakan memenuhi standar apabila kadar zat berkhasiat yang terkandung di dalamnya memenuhi persyaratan Farmakope Indonesia.
Penetapan kadar deksklorfeniramin maleat dalam tablet campuran dengan deksametason dilakukan dengan menggunakan Kromatografi Cair Kinerja Tinggi (KCKT) fase balik dengan kolom Agilent TC-18 (4,6 x 250 mm), fase gerak campuran larutan Kalium Dihidrogen Fosfat 0,05M : Metanol, laju aliran 1 ml/menit, Sensifitas 1,000 AUFS pada panjang gelombang 254 nm. Hasil uji identifikasi terhadap sampel yang ditentukan dengan parameter waktu retensi, menunjukkan bahwa sampel mengandung deksklorfeniramin maleat. Uji validasi dari tablet Dextamine (PT Phapros) secara statistik diperoleh persen recovery sebesar 100,5%, relative standar deviasi (RSD) = 1,5274 dan batas deteksi (LOD) = 4,1784 µg/ml dan batas kuantitasi (LOQ) = 13,9281 µg/ml. Ini menunjukkan bahwa metode yang digunakan memiliki ketepatan dan ketelitian yang baik.
Dari hasil penelitian diperoleh kadar deksklorfeniramin maleat dalam sediaan tablet Proxona (PT Harsen) = 95,96% ± 2,60, Pritacort (PT Molex ayus) = 107,58% ± 0,99, Omegtamine (PT Mutifa) = 95,52% ± 3,37, Dextamine (PT Phapros) = 95,88% ± 1,20. Ini menunjukkan bahwa semua sediaan tablet yang dianalisa memenuhi pesyaratan kadar yang tercantum dalam Farmakope Indonesia Edisi IV (1995), yaitu mengandung deksklorfeniramin maleat tidak kurang dari 90 dan tidak lebih dari 110% dari jumlah yang tertera pada etiket.
APPLICATION OF HIGH PERFORMANCE LIQUID
CHROMATOGRAPHY (HPLC) METHOD IN DETERMINATION OF CONCENTRATION DEXCHLORPHENIRAMINE MALEATE ON THE
TABLET MIXED WITH DEXAMETHASONE ABSTRACT
Medicinal preparations containing dexchlorpheniramine maleate and dexamethasone is widely used for various diseases. This is because dexamethasone has the ability to resolve inflammation and allergy and antihistamine properties owned by dexchlorpheniramine maleate.
According to undang-undang no.36 of 2009 Article 105 paragraph 1 concerning health that the pharmaceutical form of medicines and pharmaceutical raw materials must meet the Farmakope Indonesia or other standard books. One of the parameters of the drug is said to meet the standards if the levels of active ingredient contained in them meet the requirements of Farmakope Indonesia.
Determination of dexchlorpheniramine maleate levels within the tablet mix with dexamethasone performed by means of High Performance Liquid Chromatography (HPLC) with reversed phase with Agilent TC-18 column (4,6 x 250 mm), mobile phase mixture of Potassium Dihydrogen Phosphate 0,05M : Methanol, flow rate 1 ml/minute, sensitivity 1.000 AUFS at a wavelength of 254 nm. Identification test results on samples that are determined by the retention time parameter indicates that the sample contains dexchlorpheniramine maleate. Validation test of the tablets Dextamine (PT Phapros) is statistically obtained percent recovery of 100,5%, relative standard deviation (RSD) = 1,5274 and the limit of detection (LOD) = 4,1784 µg/ml and limit of quantitation (LOQ) = 13.9281 µg/ml. This shows that the method used has good accuracy and precision.
The results were obtained dexchlorpheniramine maleate levels in tablet dosage proxona (PT Harsen) = 95,96% ± 2,60 Pritacort (PT Molex Ayus) = 107,58% ± 0,99, Omegtamine (PT Mutifa) = 95, 52% ± 3,37, Dextamine (PT Phapros) = 95,88% ± 1,20 This shows that all the analyzed tablets meet the requirement levels specified in Farmakope Indonesia IV Edition (1995), which contains not less than dexamethasone 90% and not more than 110% of the amount listed on the label.
2.3.8 Pengolahan Data ... 16
2.3.9 Fase Gerak ... 16
2.4 Validasi... 18
BAB III METODOLOGI PENELITIAN... 20
3.1 Waktu dan Tempat Penelitian... 20
3.5.1.1 Pembuatan Fase Gerak Larutan Kalium Dihidrogen posfat 0,05M - Metanol ... 21
3.5.2.2 Pembuatan larutan Induk baku BPFI Deksklorfeniramin Maleat ... 22
3.5.2.3 Penentuan Perbandingan Fase Gerak dan Laju Alir yang Optimum ... 22
3.5.2.4 Analisis Kualitatif ... 22
3.5.2.4.1 Uji Identifikasi Deksklorfeniramin maleat Menggunakan KCKT ... 22
3.5.2.5 Analisis Kuantitatif ... 23
3.5.2.5.1 Pembuatan Kurva Kalibrasi Deksklorfeniramin maleat BPFI ... 23
3.5.2.5.2 Pembuatan Larutan uji ... 23
3.5.2.5.3 Penetapan Kadar Sampel ... 24
3.5.2.6 Analisa Data Penetapan Kadar Secara Statistik ... 24
3.5.3 Metode Validasi ... 25
3.5.3.2 Presisi ... 26
3.5.3.3 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) .... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
BAB V KESIMPULAN DAN SARAN... 37
5.1 Kesimpulan ... 37
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Halaman
Tabel 1. Hasil pengolahan data dari sediaan tablet
deksklorfeniramin maleat ... 33 Tabel 2. Hasil Penetapan kadar deksklorfeniramin maleat dalam
sediaan tablet dengan nama dagang ... 34 Tabel 3. Hasil pengujian % recovery deksklorfeniramin maleat dengan
Metode adisi standar ... 50 Tabel 4. Tabel. Data hasil penyuntikan larutan deksklorfeniramin maleat BPFI
berdasarkan luas area ... 50
Tabel 5. Konsenterasi (X) VS luas Area (Y) untuk deksklorfeniramin maleat . 50
DAFTAR GAMBAR
Halaman
Gambar 1. Kromatogram Hasil Penyuntikan Larutan Deksklorfeniramin maleat, dengan Fase gerak Larutan kalium dihidrogen posfat 0,05 M - Metanol (60:40), Laju
Alir 1 ml/menit ... 29
Gambar 2. Kromatogram Hasil Penyuntikan Larutan Tablet Proxona dengan Fase gerak Larutan kalium dihidrogen posfat 0,05 M - Metanol (60:40), Laju Alir 1 ml/menit ... 29
Gambar 3. Kromatogram Hasil Penyuntikan Larutan Tablet Omegtamine, dengan Fase gerak Larutan kalium dihidrogen posfat 0,05 M - Metanol (60:40), Laju Alir 1 ml/menit ... 30
Gambar 4. Kromatogram Hasil Penyuntikan Larutan Tablet Pritacort, dengan Fase gerak Larutan kalium dihidrogen posfat 0,05M - Metanol (60:40), Laju Alir 1 ml/menit ... 30
Gambar 5. Kromatogram Hasil Penyuntikan Larutan Tablet Dextamine, dengan Fase gerak Larutan kalium dihidrogen posfat 0,05 M - Metanol (60:40), Laju Alir 1 ml/menit ... 31
Gambar 6. Kurva Kalibrasi Deksklorfeniramin maleat BPFI ... 32
DAFTAR LAMPIRAN
Halaman Lampiran 1. Kromatogram Penyuntikan Deksklorfeniramin maleat Baku
Untuk mencari Perbandingan Fase Gerak larutan kalium dihidrogen posfat 0,05M - Metanol yang Optimal
untuk Analisis ... 39
Lampiran 2. Kromatogram Larutan Deksklorfeniramin maleat BPFI pada
pembuatan kurva kalibrasi ... 41
Lampiran 3. Perhitungan persamaan regresi dari kurva kalibrasi
deksklorfeniramin maleat BPFI yang diperoleh secara KCKT
pada panjang gelombagn 254 nm ... 50
Lampiran 4. Perhitungan Recovery dengan Metode Penambahan Bahan Baku Tablet Dextamine (PT Phapros) ... 52
Lampiran 5. Contoh Perhitungan Penimbangan Bahan Baku pada Persen
Perolehan Kembali ... 54
Lampiran 6. Contoh perhitungan kadar tablet Dextamine (PT Phapros)
sebelum penambahan bahan baku dari lampiran 4 berdasarkan luas area menggunakan persamaan garis regresi ... 55
Lampiran 7. Contoh perhitungan kadar tablet Dextamine (PT Phapros) setelah penambahan bahan baku dari lampiran 4 berdasarkan luas area menggunakan persamaan garis regresi ... 56
Lampiran 8. Kromatogram Hasil Recovery dari sampel Dextamine
(PT.Phapros) ... 57
Lampiran 9. Data Hasil % Recovery Deksametason pada tablet Dextamine (PT Phapros ) dengan menggunakan standar adisi... 69
Lampiran 10.Contoh Perhitungan % Recovery dengan Metode Adisi
standar ... 69
Lampiran 11. Perhitungan Batas Deteksi (LOD) dan Batas kuantitasi (LOQ) Persamaan Regresi : Y = ax + b ... 70
Lampiran 12. Kromatogram dari larutan tablet omegtamine (PT Mutifa) ... 71
Lampiran 13. Kromatogram Spike dari larutan tablet omegtamine
(PT Mutifa)... 74
Lampiran 14. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari
Lampiran 15. Kromatogram dari larutan tablet Pritacort (PT Molex Ayus) .... 77
Lampiran 16. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Pritacort (PT Molex Ayus) ... . 80
Lampiran 17. Kromatogram dari larutan tablet Dextaminee (PT Phapros) ... 82
Lampiran 18. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari Penyuntikkan Larutan tablet Dextamine (PT Phapros) ... 85
Lampiran 19. Kromatogram dari larutan tablet Proxona (PT Harsen) ... 87 Lampiran 20. Analisis Data Statistik untuk Mencari Kadar Sebenarnya dari
Penyuntikkan Larutan tablet Proxona (PT Harsen) ... 90
Lampiran 21. (Lanjutan) Analisis Data Statistik Larutan tablet
Proxona (PT Harsen) ... . 91
Lampiran 22. Perhitungan Penimbangan sampel ... . 93
Lampiran 23. Hasil Analisa Kadar Deksklorfeniramin Maleat dalam
sampel. ... 94 Lampiran 24.Contoh perhitungan untuk mencari kadar Deksklorfeniramin
maleat ... . 95
Lampiran 25. Daftar Spesifikasi Sampel ... . 96 Lampiran 26. Tabel Nilai Distribusi t ... . 98
Lampiran 27. Analisa Deksklorfeniramin maleat berdasarkan Clarke’s Analysis Of Drugs and Poisons (Bagian 1) ... . 99
Lampiran 28. Daftar Analisa Deksklorfeniramin maleat berdasarkan Clarke’s Analysis Of Drugs and Poisons (Bagian 2) ... 100 Lampiran 29. Sertifikat Deksklorfeniramin maleat BPFI ... 101 Lampiran 30. Prosedur Penetapan Kadar Deksklorfeniramin maleat dari
Metode Analisa BPOM (Bagian 1) ... 102
Lampiran 31. Prosedur Penetapan Kadar Deksklorfeniramin maleat
dari Metode Analisa BPOM (Bagian 2) ... 103
Lampiran 32. Gambar alat KCKT Shimadzu ... 104
PENERAPAN METODE KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) PADA PENETAPAN KADAR DEKSKLORFENIRAMIN MALEAT DALAM TABLET CAMPURAN DENGAN DEKSAMETASON
ABSTRAK
Sediaan obat yang mengandung deksklorfeniramin maleat dan deksametason banyak digunakan untuk berbagai penyakit. Hal ini dikarenakan deksametason memiliki kemampuan mengatasi peradangan serta alergi dan sifat antihistamin yang dimiliki oleh deksklorfeniramin maleat.
Menurut undang-undang no.36 tahun 2009 pasal 105 ayat 1 tentang kesehatan bahwa sediaan farmasi yang berupa obat dan bahan baku obat harus memenuhi syarat Farmakope Indonesia atau buku standar lainnya. Salah satu parameter obat tersebut dikatakan memenuhi standar apabila kadar zat berkhasiat yang terkandung di dalamnya memenuhi persyaratan Farmakope Indonesia.
Penetapan kadar deksklorfeniramin maleat dalam tablet campuran dengan deksametason dilakukan dengan menggunakan Kromatografi Cair Kinerja Tinggi (KCKT) fase balik dengan kolom Agilent TC-18 (4,6 x 250 mm), fase gerak campuran larutan Kalium Dihidrogen Fosfat 0,05M : Metanol, laju aliran 1 ml/menit, Sensifitas 1,000 AUFS pada panjang gelombang 254 nm. Hasil uji identifikasi terhadap sampel yang ditentukan dengan parameter waktu retensi, menunjukkan bahwa sampel mengandung deksklorfeniramin maleat. Uji validasi dari tablet Dextamine (PT Phapros) secara statistik diperoleh persen recovery sebesar 100,5%, relative standar deviasi (RSD) = 1,5274 dan batas deteksi (LOD) = 4,1784 µg/ml dan batas kuantitasi (LOQ) = 13,9281 µg/ml. Ini menunjukkan bahwa metode yang digunakan memiliki ketepatan dan ketelitian yang baik.
Dari hasil penelitian diperoleh kadar deksklorfeniramin maleat dalam sediaan tablet Proxona (PT Harsen) = 95,96% ± 2,60, Pritacort (PT Molex ayus) = 107,58% ± 0,99, Omegtamine (PT Mutifa) = 95,52% ± 3,37, Dextamine (PT Phapros) = 95,88% ± 1,20. Ini menunjukkan bahwa semua sediaan tablet yang dianalisa memenuhi pesyaratan kadar yang tercantum dalam Farmakope Indonesia Edisi IV (1995), yaitu mengandung deksklorfeniramin maleat tidak kurang dari 90 dan tidak lebih dari 110% dari jumlah yang tertera pada etiket.
APPLICATION OF HIGH PERFORMANCE LIQUID
CHROMATOGRAPHY (HPLC) METHOD IN DETERMINATION OF CONCENTRATION DEXCHLORPHENIRAMINE MALEATE ON THE
TABLET MIXED WITH DEXAMETHASONE ABSTRACT
Medicinal preparations containing dexchlorpheniramine maleate and dexamethasone is widely used for various diseases. This is because dexamethasone has the ability to resolve inflammation and allergy and antihistamine properties owned by dexchlorpheniramine maleate.
According to undang-undang no.36 of 2009 Article 105 paragraph 1 concerning health that the pharmaceutical form of medicines and pharmaceutical raw materials must meet the Farmakope Indonesia or other standard books. One of the parameters of the drug is said to meet the standards if the levels of active ingredient contained in them meet the requirements of Farmakope Indonesia.
Determination of dexchlorpheniramine maleate levels within the tablet mix with dexamethasone performed by means of High Performance Liquid Chromatography (HPLC) with reversed phase with Agilent TC-18 column (4,6 x 250 mm), mobile phase mixture of Potassium Dihydrogen Phosphate 0,05M : Methanol, flow rate 1 ml/minute, sensitivity 1.000 AUFS at a wavelength of 254 nm. Identification test results on samples that are determined by the retention time parameter indicates that the sample contains dexchlorpheniramine maleate. Validation test of the tablets Dextamine (PT Phapros) is statistically obtained percent recovery of 100,5%, relative standard deviation (RSD) = 1,5274 and the limit of detection (LOD) = 4,1784 µg/ml and limit of quantitation (LOQ) = 13.9281 µg/ml. This shows that the method used has good accuracy and precision.
The results were obtained dexchlorpheniramine maleate levels in tablet dosage proxona (PT Harsen) = 95,96% ± 2,60 Pritacort (PT Molex Ayus) = 107,58% ± 0,99, Omegtamine (PT Mutifa) = 95, 52% ± 3,37, Dextamine (PT Phapros) = 95,88% ± 1,20 This shows that all the analyzed tablets meet the requirement levels specified in Farmakope Indonesia IV Edition (1995), which contains not less than dexamethasone 90% and not more than 110% of the amount listed on the label.
BAB I PENDAHULUAN
1.1Latar Belakang
Analisis senyawa obat baik dalam bahan ruahan (bulk), dalam sediaan
farmasi, maupun dalam cairan biologis dengan metode kromatografi dapat dilihat
kembali pada awal tahun 1920-an. Pada tahun 1995-an, metode kromatografi
kertas secara menaik (ascending) dan menurun (descending) telah muncul pada
berbagai Farmakope untuk analisis produk-produk obat. Edisi Farmakope lanjut
mulai menggunakan metode kromatografi cair kinerja tinggi (KCKT) dan
kromatografi gas (KG) untuk analisis obat. Saat ini, metode kromatografi
merupakan metode utama yang digunakan untuk analisis obat dalam Farmakope
(Rohman, 2007).
Deksklorfeniramin maleat merupakan suatu antihistamin yang dapat
mencegah gejala-gejala alergi, yang disebabkan sebagian besar oleh histamin
(H1). Deksklorfeniramin maleat bekerja dengan menghambat reseptor H1, pada
pembuluh darah, bronkus, dan berbagai otot polos. Selain itu juga dapat mengatasi
reaksi hipersensitivitas atau keadaan lain yang disertai penglepasan histamin
endogen yang berlebihan (Anonym, 2010).
Histamin memegang peranan utama pada proses peradangan dan pada
sistem daya-tangkis. Kerjanya berlangsung melalui tiga jenis reseptor, yakni
reseptor-H1, -H2 dan –H3. Reseptor-H1 secara selektif diblok oleh antihistaminika
(H1-blockers), Reseptor-H2 oleh penghambat asam lambung (H2-blockers),
semua organ dan jaringan memiliki histamin dalam keadaan terikat dan inaktif,
yang terutama terdapat dalam sel-sel tertentu. ‘Mast Cells’ ini (ing.mast =
menimbun) menyerupai bola-bola kecil berisi gelembung yang penuh dengan
histamin dan zat-zat mediator lain. Di luar tubuh manusia histamin terdapat dalam
bakteri, tanaman (bayam, tomat) dan makanan (Tjay, 2007).
Sediaan obat yang mengandung deksametason dan deksklorfeniramin
maleat banyak digunakan untuk berbagai penyakit, bahkan sering disebut life
saving drugs. Hal ini dilatarbelakangi kemampuan menanggulangi peradangan
serta alergi yang dimiliki deksametason dan sifat antihistamin yang ada pada
deksklorfeniramin maleat (Suherman, 2007).
Kedua komponen ini berbeda sifat kepolarannya dimana
deksklorfeniramin maleat lebih polar daripada deksametason, sehingga
kemungkinan dapat dipisahkan dengan menggunakan kromatografi fase balik
(C18) dan deksklorfeniramin maleat akan terelusi lebih dahulu dibandingkan
deksametason.
Dekslorfeniramin dapat ditentukan kadarnya dengan beberapa cara
diantaranya dengan Kromatografi Cair Kinerja Tinggi (KCKT), Spektrofotometri
UV dan Titrasi Asam Basa.
Menurut Gritter Roy.J (1991), Dalam beberapa tahun terakhir ini teknologi
KCKT telah menjadi metode analisis rutin dan bahkan preparatif pada banyak
laboratorium. Kolom yang tersedia mempunyai banyak sekali pelat teori (lebih
dari 10.000 untuk kolom 100cm), dan kromatografi dilakukan dalam kondisi
yang sangat baik; seringkali, hasil dapat diperoleh dalam waktu beberapa menit
dan ditafsirkan secara kuantitatif dengan ketepatan yang lumayan.
Metode Kromatografi Cair Kinerja Tinggi (KCKT) memiliki keuntungan
antara lain dapat digunakan untuk analisa suatu zat dalam jumlah kecil,
Resolusinya baik, kecepatan analisis dan kepekaannya tinggi, ideal untuk molekul
besar dan ion, serta kolom dapat dipakai kembali.
Berdasarkan hal tersebut diatas, penulis mencoba menetapkan kadar
Deksklorfeniramin maleat dalam tablet campuran dengan Deksametason
menggunakan Kromatografi Cair Kinerja Tinggi (KCKT). Selain itu juga ingin
mengetahui apakah kadar Deksklorfeniramin maleat dalam sediaan tablet
campuran dengan Deksametason yang beredar di pasaran memenuhi syarat
Farmakope Indonesia.
Dalam penelitian ini penulis menggunakan metode penelitian dari BPOM
yaitu dengan menggunakan kolom KCKT dengan fase gerak Kalium dhidrogen
fosfat 0,05 M – Metanol dan laju aliran 1 ml per menit dengan detektor pada
panjang gelombang 254 nm.
Pada penelitian ini juga dilakukan uji validasi metode dengan metode
standar adisi yang meliputi uji akurasi dengan parameter % recovery dan uji
presisi dengan parameter RSD (Relative Standar Deviasi), LOD (Limite of
Detection), dan LOQ (Limite of Quantitation)
1.2Perumusan Masalah
- Apakah penetapan kadar Deksklorfeniramin maleat dalam sediaan tablet
dengan metode KCKT menggunakan fase gerak Kalium Dihidrogen Posfat
0,05 M – Metanol?
- Apakah kadar Deksklorfeniramin maleat dalam sediaan tablet yang
mengandung deksklorfeniramin dan deksametason yang beredar di
pasaran yang ditetapkan dengan metode KCKT memenuhi persyaratan
yang ditetapkan Farmakope Indonesia Edisi IV (1995) ?
1.3Hipotesis
- Penetapan kadar Deksklorfeniramin maleat dalam sediaan tablet yang
mengandung deksklorfeniramin dan deksametason dapat ditentukan
dengan metode KCKT menggunakan fase gerak Kalium Dihidrogen Posfat
0,05 M - Metanol.
- Kadar Deksklorfeniramin maleat dalam sediaan tablet yang mengandung
deksklorfeniramin dan deksametason yang beredar di pasaran yang
ditetapkan secara KCKT memenuhi persyaratan yang ditetapkan
Farmakope Indonesia edisi IV (1995).
1.4Tujuan Penelitian
- Menerapkan metode KCKT pada penetapan kadar Deksklorfeniramin
maleat dalam sediaan tablet yang mengandung deksklorfeniramin dan
deksametason menggunakan fase gerak Kalium Dihidrogen Posfat 0,05 M
- Untuk mengetahui kadar Deksklorfeniramin maleat dalam sediaan tablet
yang mengandung deksklorfeniramin dan deksametason yang beredar di
pasaran yang ditetapkan secara KCKT sesuai atau tidak dengan
persyaratan yang ditetapkan Farmakope Indonesia edisi IV (1995).
1.5 Manfaat Penelitian
Sebagai metode analisa kuantitatif baru bagi industri farmasi pada
penetapan kadar Deksklorfeniramin maleat dalam sediaan tablet yang
mengandung deksklorfeniramin dan deksametason dengan metode Kromatografi
BAB II
TINJAUAN PUSTAKA
Analisis secara kromatografi yang berhasil baik berkaitan dengan
mengkompromikan daya pisah kromatografi, beban cuplikan, dan waktu analisis
atau kecepatan seperti digambarkan dalam segitiga kromatografiwan pada gambar
1 di bawah ini.
Daya Pisah
Kecepatan Kapasitas
Gambar 1 Hubungan antara daya pisah, kecepatan dan kapasitas
Gambar tersebut menunjukkan bahwa, dalam batas tertentu, mungkin saja kita
mengubah kondisi pemisahan untuk memperbaiki salah satu dari ketiga hal itu
dengan mengorbankan hal lain. pengalaman menunjukkan bahwa pemahaman
teori kromatografi secara kualitatif akan membantu kromatografiwan dalam
mengoptimumkan pemisahan secara cepat. Walaupun ada cara pengoptimuman
yang canggih, ternyata kondisi pemisahan yang optimum harus dicari dengan
hanya mengubah-ubah satu parameter pada suatu saat (Johnson, 1991).
2.1 Deksklorfeniramin maleat
Gambar 1. struktur Deksklorfeniramin maleat
Nama Kimia : (+) -2-[P-kloro-α-[2-(dimetilamino)etil]benzil]piridina maleat (1:1)
Rumus Molekul : C16H19ClN2.C4H4O4
Berat Molekul : 390,87 (Depkes RI, 1995)
Pemerian : Serbuk hablur, putih ; tidak berbau
Kelarutan : Mudah larut dalam air, larut dalam etanol dan dalam
kloroform, sukar larut dalam benzena dan dalam eter.
(Depkes RI, 1995).
2.2Kromatografi
Kromatografi merupakan suatu proses pemisahan yang mana analit-analit
dalam sampel terdistribusi antara 2 fase, yaitu fase diam dan fase gerak. Fase
diam dapat berupa bahan padat atau porus dalam bentuk molekul kecil, atau
dalam bentuk cairan yang dilapiskan pada pendukung padat atau dilapiskan pada
dinding kolom. Fase gerak dapat berupa gas atau cairan. Jika gas digunakan
sebagai fase gerak, maka prosesnya dikenal sebagai kromatografi gas. Dalam
kromatografi cair dan jiga kromatografi lapis tipis, fase gerak yang digunakan
Kromatografi dapat dibedakan atas berbagai macam tergantung pada
pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi
dibedakan menjadi :
a) Kromatografi adsorbsi
b) Kromatografi partisi
c) Kromatografi pasangan ion
d) Kromatografi penukar ion
e) Kromatografi eksklusi ukuran, dan
f) Kromatografi afinitas
Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas :
a) Kromatografi kertas
b) Kromatografi lapis tipis
c) Kromatografi cair kinerja tinggi (KCKT), dan
d) Kromatografi gas (Rohman, 2007).
2.2.1 Penggunaan Kromatografi
1. Pemakaian untuk tujuan kualitatif mengungkapkan ada atau tidak adanya
senyawa tertentu dalam cuplikan
2. Pemakaian untuk tujuan kuantitatif menunjukkan banyaknya masing-masing
komponen campuran
3. Pemakaian untuk tujuan preparatif untuk memperoleh komponen campuran
dalam jumlah memadai dalam keadaan murni.
Selama pemisahan kromatografi, solut individual akan membentuk profil
konsentrasi yang simetris atau dikenal juga dengan profil Gaussian dalam arah
aliran fase gerak. Profil dikenal juga dengan puncak atau pita, secara perlahan –
lahan akan melebar dan sering juga membentuk profil yang asimetrik karena solut
– solut melanjutkan migrasinya ke fase diam (Rohman, 2007).
2.2.3 Puncak asimetris
Profil konsentrasi solut yang bermigrasi akan simetris jika rasio
distribusi solut (D) konstan selama dikisaran konsentrasi keseluruhan puncak,
sebagaimana ditunjukkan oleh isoterm sorpsi yang linear yang merupakan plot
konsentrasi solut dalam fase diam (Cs) terhadap konsentrasi solut dalam fase
gerak(Cm). Meskipun demikian, kurva isot erm akan berubah menjadi 2 jenis
puncak asimetris yakni membentuk puncak yang berekor (tailing) dan adanya
puncak pendahulu (fronting) jika ada perubahan rasio distribusi solut yang lebih
besar.
Untuk kromatografi yang melibatkan kolom, kuantifikasi dapat
dilakukan dengan luas puncak atau tinggi puncak. Tinggi puncak atau luas puncak
berbanding langsung dengan banyaknya solut yang dikromatografi, jika dilakukan
pada kisaran detektor yang linier.
1. Metode tinggi puncak
Metode yang paling sederhana untuk pengukuran kuantitatif adalah
dengan tinggi puncak. Tinggi puncak diukur sebagai jarak dari garis dasar ke
puncak maksimum seperti puncak 1, 2, dan 3 pada gambar 3. Penyimpangan garis
Gambar 3. Pengukuran tinggi puncak
Metode tinggi puncak hanya digunakan jika perubahan tinggi puncak
linier dengan konsentrasi analit. Kesalahan akan terjadi jika metode ini digunakan
pada puncak yang mengalami penyimpangan (asimetris) atau jika kolom
mengalami kelebihan muatan.
2. Metode luas puncak
Prosedur penentuan luas puncak serupa dengan tinggi puncak. Suatu
teknik untuk mengukur luas puncak adalah dengan mengukur luas puncak sebagai
hasil kali tinggi puncak dan lebar pada setengah tinggi (W1/2). Teknik ini hanya
dapat digunakan untuk kromatografi yang simetris atau yang mempunyai bentuk
serupa (Johnson, 1991).
Saat ini integrator elektronik telah banyak digunakan untuk mengukur luas
puncak pada kromatografi cair kinerja tinggi dan pada kromatografi gas.
Integrator digital mengukur luas puncak dan mengubahnya dalam bentuk angka
(Rohman, 2007).
Baik tinggi puncak maupun luasnya dapat dihubungkan dengan
konsentrasi. Tinggi puncak mudah diukur, akan tetapi sangat dipengaruhi
pelarut. Oleh karena itu, luas puncak dianggap merupakan parameter yang lebih
akurat untuk pengukuran kuantitatif (Ditjen POM, 1995).
2.3 Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi cair kinerja tinggi (KCKT) merupakan sistem pemisahan
dengan kecepatan dan efisiensi yang tinggi. Hal ini karena didukung oleh
kemajuan dalam teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang
sangat sensitif dan beragam. KCKT mampu menganalisa berbagai cuplikan secara
kualitatif maupun kuantitatif, baik dalam komponen tunggal maupun campuran
(Ditjen POM, 1995).
KCKT merupakan teknik pemisahan yang diterima secara luas untuk
analisis dan pemurnian senyawa tertentu dalam suatu sampel pada sejumlah
bidang antara lain; farmasi, lingkungan dan industri-industri makanan.
Kegunaan umum KCKT adalah untuk pemisahan sejumlah senyawa
organik, anorganik, maupun senyawa biologis, analisis ketidakmurnian
(impurities) dan analisis senyawa-senyawa yang tidak mudah menguap
(nonvolatil). KCKT paling sering digunakan untuk: menetapkan kadar
senyawa-senyawa tertentu seperti asam-asam amino, asam-asam nukleat dan
protein-protein dalam cairan fisiologis, menentukan kadar senyawa-senyawa aktif obat
dan lain-lain.
Kelebihan KCKT antara lain:
− Mampu memisahkan molekul-molekul dari suatu campuran
− Resolusinya baik
− Mudah melaksanakannya
− Dapat dihindari terjadinya dekomposisi/kerusakan bahan yang dianalisis
− Dapat digunakan bermacam-macam detektor
− Kolom dapat digunakan kembali
− Mudah melakukan rekoveri cuplikan
− Tekniknya tidak begitu tergantung pada keahlian operator dan
reprodusibilitasnya lebih baik
− Instrumennya memungkinan untuk bekerja secara automatis dan kuantitatif
− Waktu analisis umumnya singkat
− Kromatografi cair preparatif memungkinkan dalam skala besar
− Ideal untuk molekul besar dan ion.
Keterbatasan metode KCKT adalah untuk identifikasi senyawa, kecuali
jika KCKT dihubungkan dengan spektrometer massa (MS). Keterbatasan lainnya
adalah jika sampelnya sangat kompleks, maka resolusi yang baik sulit diperoleh
(Munson, 1991).
2.3.1 Cara Kerja KCKT
Kromatografi merupakan teknik yang mana solut atau zat-zat terlarut
terpisah oleh perbedaan kecepatan elusi, dikarenakan solut-solut ini melewati
suatu kolom kromatografi. Pemisahan solut-solut ini diatur oleh distribusi dalam
fase gerak dan fase diam. Penggunaan kromatografi cair membutuhkan
penggabungan secara tepat dari berbagai macam kondisi operasional seperti jenis
kolom, fase gerak, panjang dan diameter kolom, kecepatan alir fase gerak, suhu
kolom, dan ukuran sampel (Rohman, 2007).
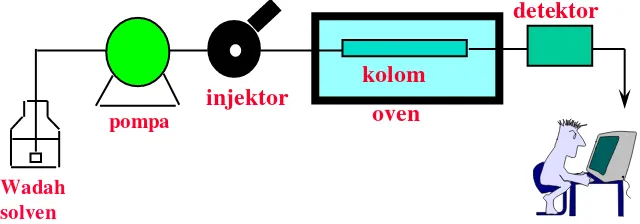
Gambar 4. Bagan alat KCKT
2.3.3 Wadah Fase Gerak
Wadah fase gerak harus bersih dan lembam (inert). Wadah pelarut kosong
ataupun labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini
biasanya dapat meampung fase gerak antara 1 sampai 2 liter pelarut. Fase gerak
sebelum digunakan harus dilakukan degassing (penghilangan gas) yang ada pada
fase gerak, sebab adanya gas akan berkumpul dengan komponen lain terutama
dipompa dan detektor sehingga akan mengacaukan analisis (Rohman, 2007).
2.3.4 Pompa
Pompa yang cocok digunakan untuk KCKT adalah pompa yang
mempunyai syarat sebagaimana syarat wadah pelarut yakni : pompa harus inert
terhadap fase gerak. Bahan yang umum dipakai untuk pompa adalah gelas, baja
tahan karat, teflon, dan batu nilam. Pompa yang digunakan sebaiknya mampu
memberikan tekanan sampai 5000 psi dan mampu mengalirkan fase gerak dengan
kecepatan alir 3 ml/menit. Untuk tujuan preparatif, pompa yang digunakan harus
mampu mengalirkan fase gerak dengan kecepatan 20 mL/ menit (Rohman, 2007).
2.3.5 Injektor
Ada 3 jenis injektor, yakni syringe injector, loop valve dan automatic
injector (autosampler). Syringe injector merupakan bentuk injektor yang paling
sederhana (Meyer, 2004).
Pada waktu sampel diinjeksikan ke dalam kolom, diharapkan agar aliran
pelarut tidak mengganggu masuknya keseluruhan sampel ke dalam kolom.
Sampel dapat langsung diinjeksikan ke dalam kolom (on column injection) atau
digunakan katup injeksi (Adnan, 1997).
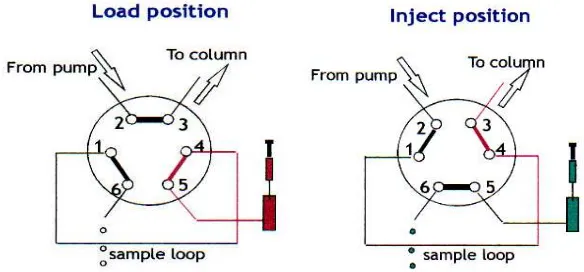
Katup putaran (loop valve) ditunjukkan secara skematik dalam Gambar 8,
tipe injektor ini umumnya digunakan untuk menginjeksi volume lebih besar
daripada 10 µl dan sekarang digunakan dengan cara otomatis (dengan adaptor
khusus, volume-volume lebih kecil dapat diinjeksikan secara manual). Pada posisi
LOAD, sampel loop (cuplikan dalam putaran) diisi pada tekanan atmosfir. Bila
katup difungsikan, maka cuplikan di dalam putaran akan bergerak ke dalam
kolom.
Automatic injector atau disebut juga autosampler memiliki prinsip yang mirip,
hanya saja sistem penyuntikannya bekerja secara otomatis (Meyer, 2004).
2.3.6 Kolom
Kolom merupakan jantung kromatografi. Keberhasilan atau kegagalan
analisis bergantung pada pemilihan kolom dan kondisi kerja yang tepat. Kolom
dapat dibagi menjadi dua kelompok :
a. Kolom analitik : garis tengah dalam 2 – 6 nm. Panjang bergantung pada
jenis kemasan,untuk kemasan pelikel biasanya panjang kolom 50 – 100
cm. Untuk kemasan mikropartikel berpori, biasanya 10 – 30 cm;
b. Kolom preparatif : umumnya bergaris tengah 6 mm atau lebih besar dan
panjang kolom 25 – 100 cm.
Kolom umumnya dibuat dari stainless steel dan biasanya dioperasikan pada
temperatur kamar, tetapi bisa juga digunakan temperatur lebih tinggi, terutama
untuk kromatografi penukar ion dan kromatografi eksklusi. Kemasan kolom
tergantung pada mode KCKT yang digunakan (Johnson, 1991).
2.3.7 Detektor
Suatu detektor dibutuhkan untuk mendeteksi adanya komponen cuplikan
dalam aliran yang keluar dari kolom. Detektor-detektor yang baik memiliki
sensitifitas yang tinggi, gangguan (noise) yang rendah, kisar respons linier yang
luas, dan memberi tanggapan/respon untuk semua tipe senyawa. Suatu kepekaan
yang rendah terhadap aliran dan fluktuasi temperatur sangat diinginkan, tetapi
tidak selalu dapat diperoleh.
Detektor yang paling banyak digunakan dalam kromatografi cair modern
detektor dengan variasi panjang gelombang UV-Vis sekarang menjadi populer
karena mereka dapat digunakan untuk mendeteksi senyawa-senyawa dalam
rentang yang luas. Detektor indeks refraksi juga secara luas digunakan, terutama
dalam kromatografi eksklusi, tetapi umumnya kurang sensitif dari pada detektor
spektrofotometer UV. Detektor lainnya, antara lain: detektor fluometer, detektor
ionisasi nyala, detektor elektrokimia dan lain-lain juga telah digunakan.
2.3.8 Pengolahan Data
Komponen yang terelusi mengalir ke detektor dan dicatat sebagai
puncak-puncak yang secara keseluruhan disebut sebagai kromatogram
Guna kromatogram:
1. Kualitatif
Waktu retensi selalu konstan dalam setiap kondisi kromatografi yang sama
dapat digunakan untuk identifikasi.
2. Kuantitatif
Luas puncak proporsional dengan jumlah sampel yang diinjeksikan dan
dapat digunakan untuk menghitung konsentrasi.
3. Kromatogram dapat digunakan untuk mengevaluasi efisiensi pemisahan
dan kinerja kolom (kapasitas ‘k’, selektifitas ‘α’, jumlah pelat teoritis
‘N’, jarak setara dengan pelat teoritis ‘HETP’ dan resolusi ‘R’).
2.3.9 Fase Gerak
Fase gerak atau eluen biasanya terdiri atas campuran pelarut yang dapat
bercampur yang secara keseluruhan berperan dalam daya elusi dan resolusi. Daya
elusi dan resolusi ini ditentukan oleh polaritas keseluruhan pelarut, polaritas fase
Dalam kromatografi cair komposisi pelarut atau fase gerak adalah satu
variabel yang mempengaruhi pemisahan. Terdapat keragaman yang luas dari fase
gerak yang digunakan dalam semua mode KCKT, tetapi ada beberapa sifat-sifat
yang diinginkan yang mana umumnya harus dipenuhi oleh semua fase gerak.
Fase gerak harus:
• Murni; tidak ada pencemar/kontaminan
• Tidak bereaksi dengan pengemas
• Sesuai dengan detektor
• Melarutkan cuplikan
• Mempunyai viskositas rendah
• Mudah rekoveri cuplikan, bila diinginkan
• Tersedia diperdagangan dengan harga yang pantas
Umumnya, pelarut-pelarut dibuang setelah digunakan karena prosedur
pemurnian kembali membosankan dan mahal. Dari semua persyaratan di atas, 4
persyaratan pertama adalah yang paling penting.
Gelembung udara (degassing) yang ada harus dihilangkan dari pelarut,
karena udara yang terlarut keluar melewati detektor dapat menghasilkan banyak
noise sehingga data tidak dapat digunakan (Johnson, 1991).
Elusi Gradien dan Isokratik
Elusi dapat dilakukan dengan cara isokratik (komposisi fase gerak tetap
selama elusi) atau dengan cara bergradien (komposisi fase gerak berubah – ubah
selama elusi). Elusi bergradien digunakan untuk meningkatkan resolusi campuran
yang kompleks terutama jika sampel mempunyai kisaran polaritas yang luas
Jenis Pemisahan Kromatografi Cair Kinerja Tinggi
Berdasarkan jenis fase gerak dan fase diamnya, jenis pemisahan KCKT
dibedakan atas :
a. Kromatografi Fase Normal
Kromatografi dengan kolom yang fase diamnya bersifat polar, misalnya silika
gel, alumina, sedangkan fase geraknya bersifat non polar seperti heksan.
b. Kromatografi Fase Terbalik
Pada kromatografi fase terbalik, fase diamnya bersifat non polar, yang banyak
dipakai adalah oktadesilsilan (ODS atau C18) dan oktilsilan (C8). Sedangkan fase
geraknya bersifat polar, seperti air, metanol dan asetonitril (Mulja dan Suharman,
1995).
2.4 Validasi
Validasi adalah suatu tindakan terhadap parameter tertentu pada prosedur
penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi
persyaratan untuk penggunaannya (WHO, 1992).
Validasi metode menurut United States Pharmacopeia (USP) dilakukan
untuk menjamin bahwa metode analisis akurat, spesifik, reprodusibel dan tahan
pada kisaran analit yang akan dianalisis. Suatu metode analis harus divalidasi
untuk verifikasi bahwa parameter-parameter kinerjanya cukup mampu untuk
mengatasi masalah dalam analisis. Parameter analisis yang ditentukan pada
validasi adalah akurasi, presisi, batas deteksi, batas kuantitasi, spesifikasi,
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
diekspresikan sebagai relatif standar deviasi (RSD) dari sejumlah sampel yang
berbeda secara signifikan secara statistik.
Batas deteksi (limit of detection, LOD) didefinisikan sebagai konsentrasi
analit terendah dalam sampel yang masih dapat terdeteksi.
Batas kuantitasi (limit of quantitation, LOQ) didefinisikan sebagai
konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi
dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan.
Linieritas merupakan kemampuan suatu metode untuk memperoleh
hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran
BAB III
METODE PENELITIAN
3.1 Waktu dan tempat penelitian
Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi
Universitas Sumatera Utara pada bulan November sampai Januari 2011.
3.2 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah satu unit alat KCKT
(Shimadzu) yang terdiri dari Vacum degasser, pompa, detektor UV/Vis, printer,
wadah fase gerak, penyuntik mikroliter (100 µl), Kolom agilent TC-18, neraca
analitik (mettler Toledo), sonifikator (Branson 1510), Pompa vakum (Gast DOA -
membran filter PTFE 0,5 µm dan 0,2 µm, cellulose nitrat membran filter 0,45 µm.
3.3 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian yaitu Kalium Dihidrogen
Fosfat 0,05 M, Metanol HPLC solvent (Merck), Deksklorfeniramin maleat BPFI
(Badan POM RI), Deksklorfeniramin maleat baku pabrik (PT Phapros), tablet
Proxona (PT Harsen), tablet Omegtamine (PT Mutifa), tablet Pritacort (Molex
Ayus), tablet Dextamine (PT Phapros), Aquabidestilata (PT Ikapharmindo
Putramas)
3.4 Pengambilan sampel
Pengambilan sampel secara purposif yaitu tanpa membandingkan antara
satu tempat dengan tempat yang lain, karena tempat pengambilan sampel
tablet Omegtamine (PT Mutifa), tablet Pritacort (PT Molex Ayus), tablet
Dextamine (PT Phapros).
3.5 Prosedur penelitian 3.5.1 Penyiapan Bahan
3.5.1.1 Pembuatan fase gerak Kalium Dihidrogen Fosfat 0,05 M – Metanol
3.5.1.2 Pembuatan Larutan Kalium Dihidrogen Fosfat 0,05 M
Ditimbang 6,8045 g Kalium Dihidrogen Fosfat kemudian
dimasukkan ke dalam labu tentukur 1000 ml lalu tambahkan sedikit aquabides,
homogenkan. Setelah itu add kan sampai garis tanda.
Larutan Kalium Dihidrogen Fosfat dan metanol disaring dengan
membran selulosa 0,45 µm kemudian di campur dengan perbandingan
perbandingan (60 : 40), (70 : 30), (85 : 15), dan (80 : 20). diawaudarakan selama
20 menit.
3.5.1.3 Pembuatan pelarut
Pelarut dibuat secara kuantitatif dari larutan Kalium dihidrogen Fosfat 0,05 M dan
Metanol dengan perbandingan yang sama seperti perbandingan fase gerak hasil
optimasi. Pelarut lalu disaring dengan penyaring membran Cellulose Nitrate 0,45
µm dan diawaudarakan selama ± 20 menit.
3.5.2 Prosedur Analisis
3.5.2.1 Penyiapan Alat Kromatografi Cair Kinerja Tinggi
Masing-masing unit diatur, kolom yang digunakan agilent T-C18 (250 mm
x 4,60 mm), detektor UV-Vis pada panjang gelombang analisis yang diperoleh
dengan sensitifitas 1,000 AUFS. Pompa menggunakan mode aliran tetap dengan
Setelah alat KCKT dihidupkan, maka pompa dijalankan dan fase gerak
dibiarkan mengalir selama 30 menit sampai diperoleh garis alas yang datar,
menandakan sistem tersebut telah stabil.
3.5.2.2 Pembuatan larutan Induk baku BPFI Deksklorfeniramin Maleat
Sejumlah lebih kurang 50 mg Deksklorfeniramin Maleat BPFI ditimbang
seksama, dilarutkan ke dalam labu tentukur 50 ml dengan 15 ml fase gerak,
disonikasi selama 15 menit dan diencerkan dengan fase gerak sampai tanda.
Sehingga diperoleh larutan dengan konsentrasi 1000 mcg/ml, Larutan Induk Baku
(LIB)
3.5.2.3 Penentuan Perbandingan Fase Gerak yang Optimum
Dipipet 5 ml Larutan Induk Baku Deksklorfeniramin maleat konsentrasi
5000 µg/ml masukkan dalam labu tentukur 50 ml, dicukupkan dengan pelarut
hingga garis tanda, kocok sehingga diperoleh larutan Deksklorfeniramin maleat
dengan konsentrasi 100 µg/ml, disaring dengan membran filter PTFE 0,2 µm,
Disonikasi selama 15 menit kemudian diinjeksikan ke dalam sistem KCKT
sebanyak 20 µl, menggunakan fase gerak Larutan Kalium Dihidrogen posfat 0,05
M - metanol, dengan perbandingan (60 : 40), (70 : 30), (85 : 15), dan (80 : 20)
dengan laju alir 1 ml/menit, dan dideteksi pada panjang gelombang 254 nm.
Kemudian dipilih perbandingan fase gerak yang memberikan data yang terbaik.
3.5.2.4 Analisis Kualitatif
3.5.2.4.1 Uji Identifikasi Deksklorfeniramin Maleat Menggunakan KCKT
Larutan Induk Baku Deksklorfeniramin Maleat dipipet 5 ml masukkan
dikocok sehingga diperoleh larutan Deksklorfeniramin maleat dengan konsentrasi
100 µg/ml.
larutan disaring dengan membran filter PTFE 0,2 µm dan disonikasi
selama 15 menit, diinjeksikan ke dalam sistem KCKT sebanyak 20 µl,
menggunakan perbandingan fase gerak dan laju alir yang memberikan pemisahan
yang terbaik, kemudian dicatat waktu tambatnya. Kemudian waktu tambat
Deksklorfeniramin Maleat BPFI dibandingkan dengan waktu tambat
masing-masing sampel. Apabila waktu tambat sampel hampir sama dengan waktu tambat
BPFI, maka sampel mengandung Deksklorfeniramin maleat.
3.5.2.5 Analisis Kuantitatif
3.5.2.5.1 Pembuatan Kurva Kalibrasi Deksklorfeniramin Maleat BPFI
Larutan Induk Baku Deksklorfeniramin Maleat dipipet sebanyak 1 ml, 1,5
ml, 2 ml, 2,5 ml, 3 ml, dan 3,5 ml dimasukkan dalam labu tentukur 25 ml,
diencerkan dengan pelarut hingga garis tanda. Kocok sehingga diperoleh
konsentrasi 40 µg/ml, 60 µg/ml, 80 µg/ml, 100 µg/ml, 120 µg/ml dan 140 µg/ml
Kemudian masing-masing larutan disaring dengan membran filter PTFE 0,2 µm,
disonikasi selama 15 menit dan diinjeksikan ke sistem KCKT dengan volume
penyuntikan 20 µl dideteksi pada panjang gelombang 254 nm dengan laju alir 1,0
ml/menit. Selanjutnya dari luas area yang diperoleh pada kromatogram dibuat
kurva kalibrasi dihitung persamaan garis regresi dan faktor korelasinya.
3.5.2.5.2 Pembuatan Larutan Uji
Sejumlah 20 tablet ditimbang seksama dan diserbukkan homogen.
Sejumlah serbuk setara dengan lebih kurang 2 mg Deksklorfeniramin Maleat
fase gerak, di sonikasi selama 15 menit, diencerkan dengan fase gerak sampai
tanda dan disaring.
3.5.2.5.3 Penetapan Kadar Sampel
Ditimbang 20 tablet mengandung Deksklorfeniramin Maleat kemudian
digerus, ditimbang sejumlah serbuk tablet setara dengan 4 mg deksklorfeniramin
maleat (sebanyak 6 kali pengulangan). Masing-masing dimasukkan kedalam labu
tentukur 50 ml, dilarutkan dengan pelarut, diencerkan dengan pelarut sampai garis
tanda, hingga diperoleh larutan dengan konsentrasi 80 µg/ml Deksklorfeniramin
maleat, kemudian saring larutan dengan kertas saring ke dalam labu tentukur,
Masing-masing larutan tersebut disaring dengan membran filter PTFE 0,2 µm dan
diawaudarakan selama 15 menit, kemudian diinjeksikan sebanyak 20 µl ke sistem
KCKT dan dideteksi pada panjang gelombang 254 nm dengan laju alir 1 ml/menit
kemudian hitung kadarnya.
Kadar dapat dihitung dengan mensubtitusikan luas area sampel pada Y
dari persamaan regresi :
Y = ax + b.
3.5.2.6 Analisis Data Penetapan Kadar Secara Statistik
Data perhitungan kadar dianalisis secara statistik menggunakan uji t.
Rumus yang digunakan adalah :
1
Kadar dapat dihitung dengan persamaan garis regresi dan untuk
t hitung
Dengan dasar penolakan apabila t hitung ≥ t tabel
Keterangan :
SD = Standard deviation/simpangan baku
X = Kadar dalam satu perlakuan
X = Kadar rata-rata dalam satu sampel
n = Jumlah perlakuan
n = Jumlah perlakuan
t = Harga ttabel sesuai dengan derajat kepercayaan
dk= Derajad kebebasan.
3.5.3 Metode Validasi 3.5.3.1 Akurasi
Pada senyawa obat metode yang umum untuk menentukan akurasi adalah
dengan melakukan prosedur analisis terhadap senyawa obat tersebut dan
menganalisisnya secara kuantitatif lalu membandingkan hasilnya dengan senyawa
standar rujukan dengan kemurnian yang sudah diketahui. Untuk produk obat,
campuran sintetik yang merupakan komponen produk obat atau suatu plasebo
yang di tambah dengan zat aktif senyawa obat dengan tingkat kemurnian yang
telah diketahui (Rohman, 2009).
Akurasi dinyatakan sebagai persen perolehan kembali dalam kaitannya dengan
jumlah analit yang ditambahkan kedalam sampel, atau sebagai perbedaan antara
jumlah yang diketahui dan jumlah yang ditentukan oleh analis. Uji akurasi dengan
parameter persen perolehan kembali dilakukan dengan membuat 3 konsentrasi
analit dengan rentang spesifik 80%, 100%, dan 120%, masing-masing dengan 3
replikasi dan setiap rentang spesifik mengandung 70% analit dan 30% bahan
baku, kemudian dianalisa dengan perlakuan yang sama seperti pada penetapan
kadar sampel. Persen perolehan kembali dapat dihitung dengan rumus:
% Perolehan kembali x100%
A = Konsentrasi sampel yang diperoleh setelah penambahan bahan baku
B = Konsentrasi sampel sebelum penambahan bahan baku
C = Konsentrasi baku yang ditambahkan
3.5.3.2 Presisi
Menurut Rohman (2009), presisi merupakan ukuran kedekatan antar serangkaian
hasil analisis yang diperoleh dari beberapa kali pengukuran pada sampel homogen
yang sama.
Presisi seringkali diekspresikan dengan SD atau Standar Deviasi Relative (RSD)
dari serangkaian data. Nilai RSD dirumuskan dengan :
Keterangan:
RSD = Standar Deviasi Relatif (%)
SD = Standar deviasi
X = Kadar rata-rata sampel
Sementara itu, nilai SD dihitung dengan :
SD =
(
(
)
)
X = nilai dari masing-masing pengukuran
X = rata-rata (mean) dari pengukuran
N = banyaknya data
N-1 = derajat kebebasan
3.5.3.3 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Menurut Miller (2005), Batas Deteksi (Limit Of Detection /LOD) dan
Batas Kuantitasi (Limit Of Quantitation/LOQ) dapat dihitung dengan
menggunakan rumus sebagai berikut :
2
SY = simpangan baku residual
BAB IV
HASIL DAN PEMBAHASAN
Pada penelitian ini sampel yang ditentukan merupakan sediaan tablet yang
mengandung campuran deksklorfeniramin maleat 2 mg dan deksametason 0,5 mg.
Tetapi yang ditentukan kadarnya hanya deksklorfeniramin maleat dengan metode
KCKT menggunakan kolom Agilent TC-18 4,6 x 250 mm dengan fase gerak
campuran larutan Kalium Dihidrogen Posfat 0,05 M dan Metanol. Dan detektor
yang digunakan adalah detektor UV-Vis. Panjang gelombang yang dipilih adalah
254 nm karena kebanyakan senyawa obat menyerap di 254 nm.
Dari hasil orientasi pada penentuan kondisi kromatografi yang terbaik
untuk deksklorfeniramin maleat diperoleh komposisi fase gerak larutan Kalium
Dihidrogen Posfat 0,05 M – Metanol 60 : 40, laju alir 1 ml/menit dan tekanan 180
kgf/cm2.
Pemisahan deksklorfeniramin maleat dan deksametason dengan
menggunakan kromatografi fase balik terjadi karena kedua komponen ini berbeda
sifat kepolarannya, dimana deksklorfeniramin maleat lebih bersifat polar daripada
deksametason sehingga deksklorfeniramin maleat akan terelusi lebih dahulu
dibandingkan deksametason.
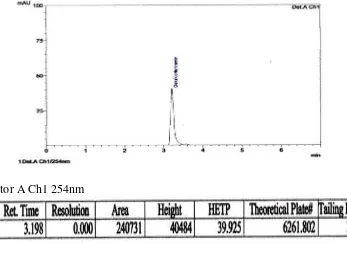
Hasil identifikasi deksklorfeniramin maleat BPFI diperoleh kromatogram
dengan waktu retensi pada menit ke-3,27.
Hasil pengujian untuk sampel diperoleh waktu retensi yang hampir sama
dengan Deksklorfeniramin maleat BPFI. Hal ini berarti sampel yang digunakan
Detector A Ch1 254nm
Gambar 1. Kromatogram deksklorfeniramin maleat BPFI secara KCKT
menggunakan kolom Agilent TC-18 (4,6 x 250 mm) dengan fase gerak larutan kalium dihidrogen posfat – metanol (60:40) dan laju alir 1 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 254 nm.
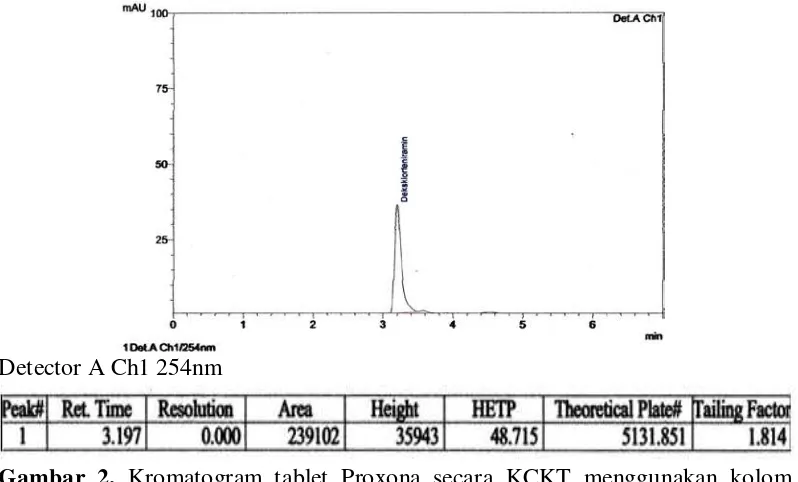
Detector A Ch1 254nm
Gambar 2. Kromatogram tablet Proxona secara KCKT menggunakan kolom
Detector A Ch1 254nm
Gambar 3. Kromatogram tablet Omegtamine secara KCKT menggunakan kolom
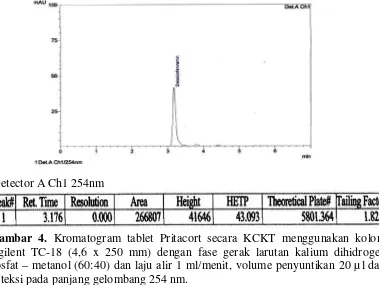
Agilent TC-18 (4,6 x 250 mm) dengan fase gerak larutan kalium dihidrogen posfat – metanol (60:40) dan laju alir 1 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 254 nm.
Detector A Ch1 254nm
Gambar 4. Kromatogram tablet Pritacort secara KCKT menggunakan kolom
Detector A Ch1 254nm
Gambar 5. Kromatogram tablet Dextamine secara KCKT menggunakan kolom
Agilent TC-18 (4,6 x 250 mm) dengan fase gerak larutan Kalium Dihidrogen Posfat – metanol (60:40) dan laju alir 1 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 254 nm.
Dari keempat sampel yang diuji ditemukan adanya satu sampel yaitu
sampel tablet omegtamine (PT Mutifa) yang memiliki 2 kromatogram, dimana 1
kromatogram dengan waktu retensi yang sama dengan deksklorfeniramin maleat
dan 1 dengan waktu retensi yang berbeda. Ini kemungkinan sampel tablet
Omegtamine (PT Mutifa) mengandung bahan selain deksklorfeniramin maleat.
Penentuan kurva kalibrasi deksklorfeniramin maleat BPFI ditentukan
berdasarkan luas area pada rentang konsentrasi 40 µg/ml, 60 µg/ml , 80 µg/ml ,
100 µg/ml ,120 µg/ml dan 140 µg/ml, diperoleh hubungan yang linier dengan
koefisien korelasi, r = 0,9991 dan persamaan regresi Y = 3144,18X – 3323,58.
Nilai koefisien korelasi yang diperoleh ini dapat diterima karena lebih besar dari
Gambar 6. Kurva kalibrasi deksklorfeniramin maleat BPFI secara KCKT
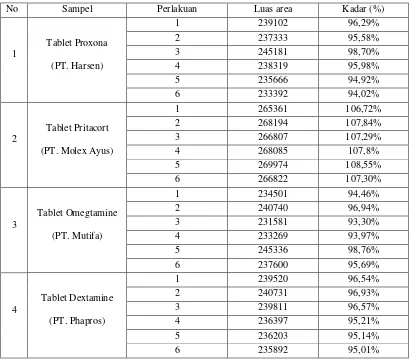
Hasil pengolahan data dari sediaan tablet deksklorfeniramin maleat yang
ada di perdagangan dapat dilihat pada Tabel 1 di bawah ini.
Tabel 1 : Hasil pengolahan data dari sediaan tablet deksklorfeniramin maleat
No Sampel Perlakuan Luas area Kadar (%)
4 Tablet Dextamine (PT. Phapros)
Berdasarkan data pada tabel di atas yang diolah menggunakan perhitungan
statistik diperoleh kadar deksklorfeniramin maleat dalam sediaan tablet dengan
Tabel 2. Hasil penetapan kadar deksklorfeniramin maleat dalam sediaan tablet
dengan nama dagang
No Nama Sediaan Kadar Deksklorfeniramin maleat 1 Tablet Proxona (PT. Harsen) 95,96 % ±2,60 %
2 Tablet Pritacort (PT. Molex Ayus) 107,58 % ± 0,99 % 3 Tablet omegtamine (PT. Mutifa) 95,52 % ± 3,37 % 4 Tablet Dextamine (PT. Phapros) 95,88 % ± 1,20 %
Sediaan tablet deksklorfeniramin maleat dengan nama dagang yang
ditentukan kadarnya berdasarkan luas area keseluruhannya memenuhi persyaratan
yang ditetapkan Farmakope Indonesia edisi IV (1995) yaitu mengandung
deksklorfeniramin maleat tidak kurang dari 90,0 % dan tidak lebih dari 110,0 %
dari jumlah yang tertera pada etiket.
Pada penelitian ini dilakukan uji validasi metode dengan metode standar
adisi terhadap sampel tablet Dextamine (PT Phapros) yang meliputi ujji akurasi
dengan parameter % recovery dan uji presisi dengan parameter RSD (Relative
Standard Deviasi), LOD (Limite of Detection) dan LOQ (Limite of quantitation).
Uji akurasi dengan parameter % recovery dilakukan dengan membuat 3
konsentrasi analit dengan rentang spesifik 80 %, 100 %, dan 120 %, masing –
masing dengan 3 replikasi dan setiap rentang spesifik mengandung 70 % analit
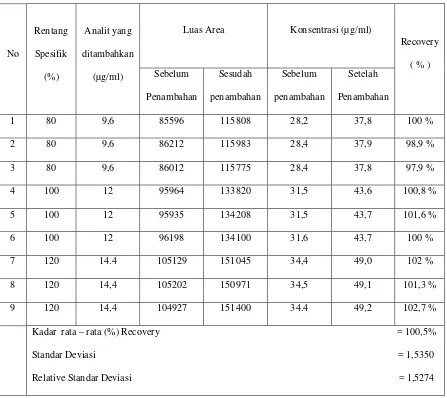
Data hasil pengujian % recovery deksklorfeniramin maleat dengan metode
adisi standar dapat dilihat pada Tabel 3.
Tabel 3. Hasil pengujian % recovery deksklorfeniramin maleat dengan metode
adisi standar
Dari tabel di atas diperoleh hasil pengujian akurasi dengan kadar rata-rata %
recovery 100,5 %. Persen recovery ini dapat diterima karena memenuhi syarat
akurasi, bahwa rentang rata-rata hasil recovery ialah 97-103 %. Maka dapat
disimpulkan bahwa metode ini mempunyai akurasi yang baik (Epshteiin, N.A.,
2004).
Luas Area Konsentrasi (µg/ml)
Hasil uji presisi dengan dengan parameter Relative Standar Deviasi (RSD)
diperoleh 1,5274 %, nilai RSD yang diinginkan adalah ≤ 2 % maka dapat
disimpulkan bahwa metode analisis mempunyai presisi yang baik. Batas deteksi
dan batas kuantitasi yang diperoleh dari penelitian ini berturut-turut 4,1784 µg/ml
dan 13,9281 µg/ml.
Dari hasil pengujian akurasi dan presisi yang diperoleh ini dapat
disimpulkan bahwa metode analisis dengan metode kromatogtrafi cair kinerja
tinggi memenuhi persyaratan validasi metode sehingga dapat digunakan untuk
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Penetapan kadar Deksklorfeniramin maleat dalam sediaan tablet dapat
dilakukan secara Kromatografi Cair Kinerja Tinggi (KCKT) menggunakan kolom
agilent TC-18 (250 mm x 4,60 mm). Dari hasil optimasi diperoleh kondisi
kromatografi yang baik dengan perbandingan fase gerak Larutan Kalium
dihidrogen posfat 0,05 M – metanol (60 : 40), laju alir 1 ml/menit, panjang
gelombang 254 nm.
Kadar deksklorfeniramin maleat dalam campuran yang dianalisis dari 4
sediaan tablet di pasaran dengan kondisi kromatografi yang terpilih diperoleh
hasil yang memenuhi persyaratan kadar umum untuk sediaan tablet yaitu
mengandung Deksklorfeniramin maleat tidak kurang dari 90,0% dan tidak lebih
dari 110,0% dari jumlah yang tertera pada etiket. Hasil uji validasi yang dilakukan
memberikan hasil akurasi dan presisi yang baik.
5.2 Saran
Disarankan agar dilakukan penelitian lebih lanjut terhadap penetapan
DAFTAR PUSTAKA
Anonym. (2010). Dextina.www.indofarma.co.id
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen
Kesehatan Republik Indonesia. Hal 649, 1133.
Épshtein, N.A. (2004). Validation of HPLC Techniques for Pharmaceutical Analysis. Pharmaceutical Chemistry Journal. Page 212-228.
Johnson, L. Edward. (1991). Dasar Kromatografi Cair. Diterjemahkan oleh:
Kosasih Padmawinata. Bandung. Penerbit ITB Bandung. Hal 4, 6, 7, 9 dan 16.
Gunawan. (2007). Farmakologi dan Terapi. Jakarta. Gaya Baru. Hal 63 & 74.
Gritter, R.J. (1991). Pengantar Kromatografi. Diterjemahkan oleh: Kosasih
Padmawinata. Bandung. Penerbit ITB Bandung. Hal 186.
Harkness, R. (1989). Interaksi Obat. Diterjemahkan oleh: Goeswin agoes.
Bandung. Penerbit ITB. Hal 9.
Meyer, V.R. (2004). Practical High-Performance Liquid Chromatography.
Fourth Edition. Chichester: John Wiley and Sons Inc. Page 4.
Miller, J.N. and J.C. miller. (2005). Statistics and Chemometric for Analytical Chemistry. 5th Edition. Pearson Education, Ltd. Page 116.
Mulja, M, Suharman. 1995. Analisis Instrumental. Surabaya: Airlangga University Press.
Munson, J. W. (1991). Analisis Farmasi Metode Modern. Diterjemahkan oleh:
Harjana Penerbit Air langga University Press. Surabaya. Hal. 46.
Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan Pertama.
Yogyakarta: Pustaka Pelajar. Hal 381-382.
Rohman, A. (2009). Kromatografi untuk Analisis Obat. Edisi Pertama.
Yogyakarta: Graha Ilmu. Hal 225-226.
Tjay, Tan Hoan. (2007). Obat-Obat Penting. Jakarta.Penerbit PT Elex Media
Komputindo. Hal 819 & 822.
WHO. (1992). The International Pharmacopeia. Fourth Edition. Electronic
Lampiran 1. Kromatogram Penyuntikan Deksklorfeniramin maleat Baku untuk
Mencari Perbandingan Fase Gerak larutan kalium dihidrogen posfat 0,05 M - Metanol yang Optimal untuk Analisis.
A
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit
B
C
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (85:15) dengan laju alir 1 ml/menit
D
Lampiran 2 Kromatogram Larutan Deksklorfeniramin maleat BPFI pada
pembuatan kurva kalibrasi
A
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit konsentrasi 40 µg/ml
B
C
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit konsentrasi 40 µg/ml
D
E
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit, konsentrasi 60 µg/ml
F
G
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit, konsentrasi 80 µg/ml
H
I
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit, konsentrasi 80 µg/ml
J
K
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit, konsentrasi 100 µg/ml
L
M
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit, konsentrasi 120 µg/ml
N
O
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit, konsentrasi 120 µg/ml
P
Q
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit, konsentrasi 140 µg/ml
R
Perbandingan fase gerak Larutan kalium dihidrogen posfat 0,05 M-metanol (60:40) dengan laju alir 1 ml/menit, konsentrasi 140
Lampiran 3 Perhitungan persamaan regresi dari kurva kalibrasi
deksklorfeniramin maleat BPFI yang diperoleh secara KCKT pada panjang gelombang 254 nm
Tabel 4. Tabel data hasil penyuntikan larutan Deksklorfeniramin BPFI
berdasarkan luas area
Tabel 5. Konsenterasi (X) VS luas Area (Y) untuk Deksklorfeniramin maleat
No.
4 100 319234,1 31923410 10000 101910410600
5 120 371884,1 44626092 14400 138297783800
6 140 432725,5 60581570 19600 187251358400
∑ 540 1677915,67 173021606 55600 538549242900
Rata2 90 279652,6111 28836934,33 9266,666667 89758207150
Y = ax + b
No Konsentrasi (µg/ml) Luas Area
Sehingga diperoleh persamaan regresi Y = 3144,18X – 3323,58
Untuk mencari hubungan kadar (X) dengan luas area (Y) digunakan pengujian koefisien korelasi (r)
Lampiran 4. Perhitungan Recovery dengan Metode Penambahan Bahan Baku
Tablet Dextamine (PT Phapros)
Berat 20 tablet = 3012,6
Kandungan zat berkhasiat :
- Deksklorfeniramin = 2 mg
- Deksametason = 0,5 mg
Rentang spesifik : 80%, 100% 120% dan setiap rentang mengandung 70% analit dan 30% baku pembanding.
Rentang 80% :
Deksklorfeniramin maleat =
Analit 70% :
= mg
Sampel yang ditimbang = x 3012,6 = 84,35 mg
Baku Pembanding 30% :
=
Rentang 100% :
Deksklorfeniramin maleat =
Analit 70% :
=
Sampel yang ditimbang =
Baku pembanding 30% :
= g
Konsentrasi Bahan Baku =
Rentang 120% :
Dekslorfeniramin maleat =
Analit 70% :
Sampel yang ditimbang = mg
Baku pembanding 30% :
Lampiran 5 Contoh Perhitungan Penimbangan Bahan Baku pada Persen
Perolehan Kembali - Rentang 80%
Baku 30 % =
Pembuatan Larutan baku :
Cara : Timbang 150 mg bahan baku masukkan dalam labu 25 ml, larutkan dan cukupkan sampai garis tanda lalu pipet 8 ml dan masukkan ke dalam labu 100 ml dan cukupkan hingga garis tanda.
Kadar Larutan = 6 mg/ml kemudian pipet 8 ml ke dalam
labu 100 ml, maka kadar akhir larutan = = 0,48 mg/ml
Kemudian dari larutan ini dipipet sesuai kebutuhan untuk uji validasi
- Rentang 100%
Baku 30 % = g
Pembuatan Larutan baku :
Cara : Timbang 60 mg bahan baku kemudian masukkan ke dalam labu 100 ml. Larutkan dan cukupkan hingga garis tanda.
Kadar Larutan = = 0,6 mg/ml
Kemudian dari larutan ini dipipet sesuai kebutuhan untuk uji validasi
- Rentang 120%
Baku 30 % =
Pembuatan Larutan baku :
Cara : Timbang 72 mg bahan baku kemudian masukkan ke dalam labu 100 ml. Lalu larutkan dan cukupkan hingga garis tanda.
Kadar Larutan = = 0,72 mg/ml
Lampiran 6 Contoh perhitungan kadar tablet Dextamine (PT Phapros) sebelum
penambahan bahan baku dari lampiran 4 berdasarkan luas area menggunakan persamaan garis regresi
- Rentang 80%
Luas area (y) sebelum penambahan bahan baku : 85596 y = ax + b
y = 3144,18x – 3323,58 85596 = 3144,18x – 3323,58
x =
x = 28,2 µg/ml
- Rentang 100%
Luas Area (y) sebelum penambahan bahan baku : 95964 y = ax + b
y = 3144,18x – 3323,58 95964 = 3144,18x – 3323,58
x =
x = 31,5 µg/ml
- Rentang 120%
Luas area (y) sebelum penambahan bahan baku : 105129 y = ax + b
y = 3144,18x – 3323,58 105129 = 3144,18x – 3323,58
x =