PENGARUH TEMPERATUR TERHADAP KADAR TANIN PADA PEMBUATAN TEH BOTOL SOSRO
DI PT SINAR SOSRO KPB DELI SERDANG
TUGAS AKHIR
OLEH:
TRI WAHYUNI TAMPUBOLON NIM 082410007
PROGRAM STUDI DIPLOMA III ANALIS FARMASI DAN MAKANAN FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN
PENGARUH TEMPERATUR TERHADAP KADAR TANIN PADA PEMBUATAN TEH BOTOL SOSRO
DI PT SINAR SOSRO KPB DELI SERDANG
TUGAS AKHIR
Diajukan untuk Memenuhi Salah Satu Syarat untuk Memperoleh Gelar Ahli Madya Pada Program Diploma III Analis Farmasi dan Makanan
Fakultas Farmasi Universitas Sumatera Utara
OLEH:
TRI WAHYUNI TAMPUBOLON NIM 082410007
Medan, Juni 2011 Disetujui Oleh: Dosen Pembimbing,
Dra. Herawaty Ginting, M.Si., Apt. NIP 195112231980032002
Disahkan Oleh:
Dekan Fakultas Farmasi USU,
KATA PENGANTAR
Syukur yang tiada henti penulis ucapkan kepada Allah SWT, karena atas
limpahan rahmat dan pertolongan-Nya semata penulis dapat menyelesaikan tugas
akhir ini.
Adapun judul tugas akhir ini adalah : “ Pengaruh Temperatur Terhadap
Kadar Tanin Pada Pembuatan Teh Botol Sosro Di PT Sinar Sosro KPB Deli Serdang” yang dibuat sebagai salah satu syarat untuk menyelesaikan Program
Studi Diploma III Analis Farmasi dan Makanan di Fakultas Farmasi Universitas
Sumatera Utara.
Dalam penyelesaian tugas akhir ini, penulis menyadari bimbingan dan
dukungan dari berbagai pihak tidak terlepas dari penulis. Untuk itu izinkan penulis
dengan tulus hati dalam kesempatan ini menyampaikan ucapan terima kasih
kepada :
1. Kedua orang tua yang tercinta, ayahanda Imran Tampubolon dan ibunda
Tinuria br Manurung yang tak pernah melepaskan perhatiannya kepada
penulis selama meniti masa pendidikan sampai akhirrnya
terselesaikannya tugas akhir ini.
2. Kakanda Yunita Herniati Tpb, Tuty Hermayana Tpb serta adinda
Saifullah Tpb dan Elfri Rahayu Tpb dukungan dan motivasi yang kalian
berikan sangat luar biasa hingga terselesaikannya tugas akhir ini.
3. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagai dekan Fakultas
Farmasi Universitas Sumatera Utara.
4. Bapak Prof. Dr. Jansen Silalahi, M.Sc., Apt., sebagai kepala koordinator
Program Pendidikan Diploma III Analis Farmasi dan Makanan Fakultas
Farmasi Universitas Sumatera Utara.
5. Ibu Dra. Herawaty Ginting, M.Si., Apt., sebagai dosen pembimbing
yang dengan penuh kesabaran membimbing penulis hingga
6. Bapak dan ibu dosen beserta seluruh staf Program Studi Diploma III
Analis Farmasi dan Makanan Universitas Sumatera Utara.
7. Sahabat seperjuangan di HTI ( Hizbut Tahrir Indonesia), Mba Dew,
Ukhti Nur, Kak Mimi, Kak Wiji, Kak Dewi, Kak Hafni, Kak Khadijah,
ukhti Sinta dan yang belum disebutkan, semuanya telah memberikan
banyak inspirasi, motivasi, serta dukungan baik materi, dan doa.
8. Seluruh rekan – rekan mahasiswa/i Analis Farmasi dan Makanan
angkatan 2008 yang telah ikhlas berbagi ilmu dan pengalamannya.
Penulis menyadari sepenuhnya penulisan tugas akhir ini masih belum
sempurna, oleh karena itu dengan segala kerendahan hati, saran dan kritik yang
membangun sangat penulis harapkan dari berbagai pihak demi perbaikan di masa
yang akan datang.
Semoga Allah SWT memberikan rahmat-Nya bagi kita semua dan
diharapkan tugas akhir ini bermanfaat bagi pembaca dan penulis sendiri. Aamiin.
Medan, Juni 2011
Penulis
DAFTAR ISI
Halaman
Lembar Pengesahan ... i
Kata Pengantar ... ii
Daftar Isi ... iv
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Tujan dan Manfaat ... 2
1.2.1 Tujuan... 2
1.2.2 Manfaat ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1. Uraian Tumbuhan Teh ... 4
2.1.1 Tumbuhan Teh ... 4
2.1.2 Morfologi Tumbuhan Teh ... 5
2.1.3 Sistematika Penamaan Tumbuhan Teh ... 5
2.2. Perkembangan teh di Indonesia ... 6
2.3. Jenis Teh Berdasarkan Pengolahannya ... 7
2.3.1. Teh Oolong ... 7
2.3.3 Teh Hitam ... 10
2.3.4 White Tea ... 13
2.4 Kandungan Teh ... 14
2.4.1 Tanin ... 15
2.4.1.1 Klasifikasi Tanin ... 16
2.4.1.2 Sifat Umum Tanin ... 19
2.4.1.3 Cara Identifikasi Senyawa Tanin ... 20
BAB III METODOLOGI... 21
3.1. Alat ... 21
3.2 Bahan ... 21
3.3. Pereaksi ... 21
3.4 Prosedur ... 21
3.4.1 Larutan Uji ... 21
3.4.2 Larutan Blanko ... 22
BAB IV HASIL DAN PEMBAHASAN... 24
4.1 Hasil ... 24
4.1.1. KMnO4 yang Terpakai pada Percobaan Larutan Uji ... 24
4.1.2. KmnO4 yang Terpakai pada Percobaan Larutan Blanko ... 24
4.2. Pembahasan ... 26
BAB V KESIMPULAN DAN SARAN... 28
5.1. Kesimpulan ... 28
5.2 Saran ... 28
BAB I PENDAHULUAN
1.1 Latar Belakang
Tumbuhan teh, Camellia sinensis (L) O. Kuntze familia dari Theaceae,
umumnya telah dikenal penduduk Indonesia terutama sebagai minuman penyegar.
Selain di Indonesia, tumbuh pula di India, Srilanka dan Cina (Kartasapoetra, 1992).
Daun teh mengandung zat–zat yang berguna bagi tubuh. Diantaranya polifenol,
teofilin, teobromin, flavonoid, vitamin C, vitamin E, katekin, kafein, serta
beberapa mineral. Jadi, selain sebagai minuman penyegar, teh juga diminati karena
manfaatnya yang baik bagi tubuh. Seperti pada beberapa penelitian menyebutkan
bahwa kelompok polifenol memiliki peran sebagai
kesehatan. Mampu menetralisir radikal bebas, yaitu suatu produk sampingan dari
proses kimiawi dalam tubuh yang mengganggu. Kemampuan inilah yang mungkin
menjadi jawaban, mengapa teh kemudian juga bisa mencegah resiko serangan
jantung da
Tanin merupakan salah satu jenis senyawa kimia yang termasuk ke dalam
golongan polifenol yang terdapat pada tumbuhan teh. Tanin memiliki peranan
biologis yang kompleks. Hal ini dikarenakan sifat tanin yang sangat kompleks
mulai dari pengendap protein hingga pengkelat logam. Maka dari itu efek yang
disebabkan tanin tidak dapat diprediksi. Umumnya tanin digunakan untuk aplikasi
dibidang pengobatan, misalnya untuk pengobatan diare, hemostatik (menghentikan
Maka dari itu semua penelitian tentang senyawa tanin mulai dilirik para peneliti
sekarang (Fitri, 2009).
Tanin akan terurai menjadi pirogallol, pirokatekol dan floroglusinol, bila
dipanaskan sampai temperatur 99 oC-102 oC. Semua jenis tanin dapat larut dalam
air. Kelarutannya akan bertambah besar apabila dilarutkan dalam air panas. Begitu
juga tanin akan larut dalam pelarut organik, seperti metanol, etanol, aseton dan
pelarut organik lainnya. Maka, atas pertimbangan inilah perlu dilakukan penelitian
mengenai pengaruh temperatur terhadap kadar tanin, pada saat penyeduhan
pembuatan produk minuman teh. Hingga diketahui temperatur dan warna produk
minuman teh yang baik dalam hubungannya menjaga kandungan zat – zat
berkhasiat termasuk senyawa tanin dari kerusakan (Risnasari, 2001).
1.2 Tujuan dan Manfaat 1.2.1 Tujuan
- Untuk mengetahui apakah ada atau tidak pengaruh perbedaan
temperatur saat penyeduhan teh terhadap kadar tanin dalam teh.
- Untuk mengetahui temperatur yang baik yang dipakai dalam
perhatiannya terhadap kadar tanin pada penyeduhan teh sesuai hasil
analisa PT Sinar Sosro dan yang menjadi Standart Operational
Procedure (SOP) PT Sinar Sosro KPB Deli Serdang pada pembuatan
1.2.2 Manfaat
- Menambah pengetahuan tentang pengujian – pengujian yang
dilakukan untuk menjamin mutu dari produk teh dalam kemasan.
- Menambah pengalaman kerja di laboratorium Quality Control (QC)
pada pembuatan produk minuman.
- Menambah pengetahuan mengenai salah satu pengawasan mutu
BAB II
TINJAUAN PUSTAKA 2.1 Uraian Tumbuhan Teh
2.1.1 Tumbuhan Teh
Tumbuhan teh (Camellia sinensis) familia dari Theaceae, diperkirakan berasal
dari pegunungan Himalaya dan daerah – daerah pegunungan yang berbatasan
dengan Republik Rakyat Cina, India, dan Birma. Tanaman ini dapat tumbuh di
daerah tropis dan subtropis, dengan menuntut cukup sinar matahari dan hujan
sepanjang tahun (Spillane, 1992).
Tumbuhan teh dapat tumbuh sekitar 6 – 9 meter tingginya. Di perkebunan –
perkebunan, tanaman teh dipertahankan hanya sekitar 1 meter tingginya dengan
pemangkasan secara berkala. Hal ini adalah untuk memudahkan pemetikan daun
dan agar diperoleh tunas – tunas daun teh yang cukup banyak. Tumbuhan teh
umumnya mulai dapat dipetik daunnya secara terus – menerus setelah umur 5 tahun
dan dapat memberikan hasil daun teh cukup besar selama 40 tahun, baru kemudian
diadakan peremajaan. Tumbuhan ini dapat tumbuh dengan subur di daerah dengan
ketinggian 200 – 2000 meter di atas permukaan air laut. Semakin tinggi letak
daerahnya, semakin menghasilkan mutu teh yang baik. Misalnya, teh di Darjeeling
dari India, terletak di atas ketinggian 1500 meter. Di Indonesia perkebunan teh
banyak di daerah Jawa Barat, Jawa Tengah, Jawa Timur, juga di Sumatera Utara
dan Sumatera Selatan. Hasil teh diperoleh dari daun – daun pucuk tumbuhan teh
yang dipetik dengan selang 7 – 14 hari, tergantung dengan keadaan tumbuhan di
teh, juga sangat menentukan mutu teh yang dihasilkan. Pemetikan daun teh hingga
kini banyak dilakukan oleh tenaga – tenaga manusia dan sebagian besar adalah
tenaga – tenaga wanita (Spillane, 1996).
2.1.2 Morfologi Tumbuhan Teh
Daun teh berbau khas aromatik, rasanya agak sepet. Selain itu daun teh
mempunyai ciri–ciri ( morfologi ) sebagai berikut:
1. Helai–helai daun yang cukup tebal, kaku, berbentuk sudip melebar sampai
sudip memanjang, panjangnya tidak lebih dari 5 cm, bertangkai pendek.
2. Permukaan daun bagian atas mengkilat, pada daun muda permukaan
bawahnya berambut jika telah tua menjadi licin.
3. Tepi daun bergerigi, agak tergulung ke bawah, berkelenjar yang khas dan
terbenam (Kartasapoetra, 1992).
2.1.3 Sistematika Penamaan Tumbuhan Teh
Walaupun tumbuhan teh aslinya ditulis oleh Linnaeus di dalam sistem
binominalnya pada tahun 1753 sebagai Thea sinensis, sekarang teh dimasukkan di
Camellia sebagai C. Sinensis (keluarga Theaceae). Lalu Linnaeus mengakui dua
jenis yang sebelumnya digambarkan oleh John Hill, yaitu T. viridis dan T. bohea.
Secara keliru dianggap bahwa T. bohea adalah sumber teh hitam, sedangkan T.
viridis menghasilkan teh hijau. Namun, pada tahun 1843 Robert Fortune
menemukan bahwa teh hitam dan teh hijau dihasilkan dari daun tanaman yang
sama dengan proses produksi yang berbeda. Ada banyak nama yang mirip
termasuk Thea bohea, T. viridis, T. cantonensis, T. assamica, Camellia thea, C.
mengusulkan banyak variasi teh, tetapi banyak tidak berlaku dan tidak ada
kesepakatan antara ahli biologi atau hortikultura mengenai batas – batas variasi teh.
Hal ini dapat dijelaskan oleh fakta bahwa pengarang pada masa sekarang ini tidak
mempunyai koleksi buku referensi yang cukup. Juga tanaman teh, seperti banyak
tanaman lain yang diolah, bervariasi dalam beberapa cirinya khas dan hal ini
tergantung pada kondisi lokal dan pada kualitas pilihan bibitnya dan pembibitannya
(Spillane, 1992).
2.2 Perkembangan Teh di Indonesia
Tumbuhan teh pertama kali masuk ke Indonesia tahun 1686, berupa biji teh
dari Jepang yang dibawa oleh orang Belanda bernama Andreas Cleyer, dan
ditanam sebagai tanaman hias di Jakarta. Pada tahun 1694, seorang pendeta
bernama F. Valentijn melaporkan melihat perdu teh muda berasal dari Cina tumbuh
di Taman Istana Gubernur Jendral Champhuys di Jakarta, setelah pada tahun 1824
Dr.Van Siebold seorang ahli bedah tentara Hindia Belanda yang pernah melakukan
penelitian alam di Jepang mempromosikan usaha pembudidayaan dengan bibit teh
dari Jepang
Pada tahun 1826 tanaman teh berhasil ditanam melengkapi Kebun Raya
Bogor, dan pada tahun 1827 di Kebun Percobaan Cisurupan, Garut, Jawa Barat.
Usaha perkebunan teh pertama dipelopori oleh Jacobus Isidorus Loudewijk Levian
Jacobson, seorang ahli teh pada tahun 1828, yang kemudian digunakan sebagai
dasar bagi usaha perkebunan teh di Jawa dan sejak itu menjadi komoditas yang
menguntungkan pemerintah Hindia Belanda, sehingga pada masa pemerintahan
rakyat melalui politik Tanam Paksa (Culture Stelsel). Pada masa kemerdekaan,
usaha perkebunan dan perdagangan teh diambil alih oleh pemerintah RI. Sekarang
perkebunan dan perdagangan teh juga dilakukan oleh pihak swasta
2.3 Jenis Teh berdasarkan Pengolahannya
Ada 4 (empat) jenis teh yang sudah akrab bagi orang Indonesia: teh oolong
(oolong tea), teh hitam (black tea), teh hijau (green tea), teh putih (white tea).
Keempatnya dibedakan berdasarkan proses pengolahan. Kualitas teh tinggi apabila
dipetik dari lembar pucuk pertama sampai ketiga. Sebab dalam ketiga lembar daun
itu kandungan katekin penambah rasa segar dan kafein tinggi. Katekin sendiri
merupakan senyawa polifenol yang kaya antioksidan (Mulja, 1995).
2.3.1 Teh Oolong
Teh oolong adalah teh hasil semioksidasi enzimatis alias tidak bersentuhan
lama dengan udara saat diolah. Teh oolong terletak diantara teh hijau dan teh hitam.
Fermentasi terjadi namun hanya sebagian (30 – 70 %). Hasilnya, warna teh menjadi
cokelat kemerahan. Teh oolong biasa disajikan dalam upacara pernikahan dan
sebagai teman menyantap hidangan laut. Sebelum menjadi teh oolong yang kering
dan dapat dikonsumsi secara praktis, teh tersebut mengalami beberapa tahapan
proses yaitu:
Proses ini dilakukan dengan tangan agar lebih selektif. Kalau dengan alat
pemotong, misalnya ani-ani yang digunakan untuk memanen padi, batang
keras pun kemungkinan besar akan ikut terpotong.
2. Proses Pelayuan
Proses pelayuan ini dilakukan dengan menggunakan sinar matahari selama
90 menit. Kemudian dipaparkan di dalam ruangan untuk dilakukan
kembali proses pelayuan selama 4-8 jam.
3. Proses Pengeringan
Pada proses pengeringan dilakukan dengan Panning System, hal ini
bertujuan untuk inaktivasi enzim agar fermentasi tidak sempurna atau
fermentasinya parsial.
4. Proses Penggulungan
Proses peggulungan ini dilakukan dengan sistem open top roller selama
5-12 menit. Tujuannya adalah untuk memecah sel daun sehingga
menghasilkan rasa sepat. Tapi proses penggulungannya tidak sampai
hancur seperti pada proses teh hitam (pada bagian penggilingan)
(Sujayanto, 2008).
2.3.2 Teh Hijau
Teh hijau diolah tanpa mengalami oksidasi, tidak memberi kesempatan
terjadinya fermentasi. Setelah layu daun teh langsung digulung, dikeringkan, dan
siap untuk dikemas. Biasanya pucuk teh diproses langsung dengan uap panas
(steam) atau digoreng (pan frying) untuk menghentikan aktivitas enzim. Warna
menurunkan bobot tubuh. Hal ini disebabkan kandungan polifenolnya tinggi. Teh
hijau menjadi favorit masyarakat di Jepang dan Korea. Bahkan di Jepang terdapat
beragam teh hijau seperti gyokuro, sencha, kabusecha dan konacha masing-masing
dibedakan berdasarkan proses pembuatannya. Menurut Bambang Mukhtar, seorang
ahli teh dari Bogor Jawa Barat bahwa gyokuro yang paling istimewa karena
di-aging selama 5 tahun, rasanya gurih seperti kaldu. Aroma kaldu itu pun menguat
tajam. Teh hijau pas dinikmati saat banyak aktivitas karena dipercaya
meningkatkan konsentrasi, jadi tidak cocok diminum sebelum berangkat tidur
(Sujayanto, 2008).
Sebelum menjadi teh hijau yang kering, teh hijau ini juga mengalami beberapa
proses yaitu:
1. Proses Pemetikan
Proses ini dilakukan dengan tangan agar lebih selektif. Kalau dengan alat
pemotong misalnya ani-ani yang digunakan untuk memanen padi, batang
keras pun kemungkinan besar akan ikut terpotong.
2. Proses Pelayuan
Proses selanjutnya adalah pelayuan. Proses ini bertujuan untuk
inaktivasikan enzim polifenol oksidase dan mengurangi kadar air hingga
60-70 %. Proses ini dilakukan dengan system rotary panner dengan panas
80-100oC selama 2-4 menit.
Proses peggulungan ini dilakukan dengan sistem open top roller selama
15-17 menit. Tujuannya adalah untuk memecah sel daun sehingga
menghasilkan rasa sepet. Tapi proses penggulungannya tidak sampai
hancur seperti pada proses teh hitam (pada bagian penggilingan).
4. Proses Pengeringan
Proses selanjutnya adalah pengeringan yang dilakukan dalam dua tahap.
Tahap pertama dilakukan pada suhu 110-135oC selama 30 menit. Tahap
berikutnya pemanasan 70-90o C dalam waktu 60-90 menit, selanjutnya
proses sortasi dan pengemasan (Sujayanto, 2008).
2.3.3 Teh Hitam
Teh hitam didapat dari hasil penggilingan yang menyebabkan daun terluka dan
mengeluarkan getah. Getah itu bersentuhan dengan udara sehingga menghasilkan
senyawa tea flavin dan tearubigin. Artinya, daun teh mengalami perubahan kimiawi
sempurna sehingga hampir semua kandungan katekin terfermentasi menjadi tea
flavin dan tearubugin. Warna hijau bakal berubah menjadi kecoklatan dan selama
proses pengeringan menjadi hitam. Teh hitam paling dikenal luas dan banyak
dikonsumsi. Dadan, periset di pusat Penelitian Teh dan Kina Gambung,
menamakan reaksi itu oksidasi enzimatis. Tea flavin menurunkan warna merah
kekuning-kuningan dalam setiap seduhan, tearubigin memberi kombinasi warna
coklat kemerahan dan kuning. Soal rasa seperti katekin, tea flavin memberi
kesegaran (Sujayanto, 2008).
Sebelum menjadi teh hitam yang kering daun-daun teh tersebut telah melewati
1. Proses Pemetikan
Proses ini dilakukan dengan tangan agar lebih selektif. Kalau dengan alat
pemotong misalnya ani-ani yang digunakan untuk memanen padi, batang
keras pun kemungkinan besar akan ikut terpotong.
2. Proses Pelayuan
Proses selanjutnya adalah pelayuan. Proses ini bertujuan untuk
mengurangi kadar air sehingga kandungan enzim dalam pucuk teh lebih
kental. Proses ini dilakukan pada tempat pelayuan (withering trough)
berupa kotak persegi panjang beralaskan kawat kasa. Di bawah kawat kasa
ini terdapat blower penghembus udara kearah kasa. Pucuk daun teh
dibeberkan di atas withering trough dengan ketebalan 30 cm, bagian
permukaannya harus rata agar pelayuan merata. Hembusan udara tadi
dapat menerbangkan air dalam daun teh. Proses pelayuan berlangsung
7-24 jam. Untuk mencapai kadar air yang diinginkan maka dilakukan proes
pembalikan. Langkah ini juga supaya pucuk teh tidak terbang tertiup
blower. Kemudian hamparan pucuk teh dibongkar untuk dimasukkan ke
dalam conveyor (semacam corong yang dihubungkan dengan alat
penggiling). Lalu teh dimasukkan ke dalam tong plastik lantas diletakkan
ke ban berjalan untuk masuk ke ruang giling.
Setelah itu daun masuk ke mesin penggilingan. Yaitu Green Leaf Shifter,
pada proses ini pucuk teh masuk ke mesin getar. Dengan demikian pucuk
teh terpisahkan dari ulat, kerikil, pasir dan serpihan lain melalui perbedaan
berat jenisnya. Pucuk teh tersebut masuk ke conveyor untuk mengalami
proses penggilingan awal dengan mesin BLC (Barbora Leaf Conditioner),
dimana pucuk teh dipotong menjadi serpihan kecil-kecil sebagai
prakondisi untuk proses penggilingan selanjutnya menggunakan mesin
Crush Tear & Curl (CTC) dan agar fermentasi dapat berlangsung dengan
lancar. Out put yang dihasilkan adalah berupa bubuk teh basah berwarna
hijau.
4. Proses Fermentasi
Proses ini lebih tepat disebut oksidasi enzimatik. Mesin bekerja membeber
bubuk daun teh basah hingga terpapar oksigen sehingga terjadi perubahan
warna. Pada ujung fermentasi teh akan berwarna kecoklatan. Selain
perubahan warna juga terjadi perubahan aroma, dari bau daun menjadi
harum teh. Proses ini berlangsung selama 1-5 jam dengan suhu optimal 26
- 27oC .
5. Proses Pengeringan
Tujuan dari proses ini adalah untuk menghentikan reaksi oksidasi
enzimatik pada daun teh. Selain itu juga untuk membunuh
mikroorganisme yang beresiko terhadap kesehatan. Pengeringan ini juga
dapat membuat teh tahan lama disimpan karena kadar air yang rendah
menggunakan oven besar Fluid Bed Dryer (FBD), dengan suhu masuk
100 - 120oC dan suhu keluarnya 80 - 105oC selama 15 - 20 menit.
Sehingga kadar airnya hanya 2,5 - 3 % saja di dalam teh, selanjutnya
proses sortasi dan pengemasan (Sujayanto, 2008).
2.3.4 White tea
Teh lain yang tak kalah istimewa adalah white tea alias teh putih. Disebut
begitu karena saat diseduh warna air hanya sedikit berubah menjadi kekuningan.
White tea dipercaya memiliki lebih banyak manfaat daripada teh hijau. Dari teh ini
diambil dari pucuk daun yang masih menggulung yang memiliki kandungan
katekin dan kafein paling tinggi. Teh beraroma tajam seperti rempah-rempah ini
menjadi unggulan di cafe tea Addict di bilangan Gunawarman, Jakarta Selatan.
“white tea yang dicampur 20% teh hijau dinamakan pure nirvana,” kata Priyanto,
juru racik teh disana. Meneguk secangkir pure nirvana langsung menghangatkan
tubuh. Yang menarik sisa daun teh bisa dimakan sambil dicampur madu (Sujayanto,
2008).
Kenikmatan keempat teh itu maksimal jika diseduh dengan benar. Aroma dan
rasa seperti kaldu pada teh hijau dari varietas sinensis keluar saat diseduh air
bersuhu 70 atau saat dididihkan bergelembung kecil-kecil. Lebih dari itu daun
teh pecah dan mengeluarkan lendir sehingga rasanya lebih pahit dan warna hijau
kecoklatan (Sujayanto, 2008).
Dari 4 macam teh klasik itu kemudian berkembang berbagai macam variasi
dengan penambahan bahan lain seperti bunga melati sebagi penambah aroma dan
diramu untuk kepentingan kesehatan dan pengobatan. Buah umumnya memang
kaya vitamin C dan antioksidan. Pembuatan fruit tea menggunakan buah yang
dikeringkan. Selain bahan teh klasik, ada juga teh herba yang dibuat bukan dengan
bahan Camellia sinensis. Sama seperti teh buah, teh herba juga dibuat untuk
keperluan kesehatan dan pengobatan (Sujayanto, 2008).
2.4 Kandungan Teh
Secara umum, daun teh mengandung zat – zat yang berguna bagi tubuh. Di
antaranya polifenol, teofilin, teobromin, flavonoid, vitamin C, vitamin E, katekin,
kafein, serta beberapa mineral (Yellia, 2003).
Zat flavonoid berfungsi sebagai penangkal radikal bebas yang dapat
mengacaukan sistem keseimbangan tubuh dan memicu timbulnya kanker dan
tumor. Katekin pada daun teh dapat menurunkan kolesterol darah dan mengurangi
kemungkinan terserang kanker (Kartasapoetra, 1992).
Meskipun bermanfaat bagi kesehatan, meminum teh secara berlebihan tidak
baik. Hal ini disebabkan di dalam teh terkandung kafein meskipun tidak setinggi
yang terkandung dalam kopi. Terlalu tingginya jumlah kafein yang dikonsumsi
menyebabkan gangguan, seperti insomnia, dan ketidakteraturan kerja jantung.
Minum teh sebaiknya dilakukan 2 cangkir sehari (Yellia, 2003).
Kandungan kafein yang terdapat di dalam teh jumlahnya lebih sedikit
dibandingkan pada kopi. Meskipun demikian itu tidak mengurangi manfaat dari
kafein tersebut. Kafein bersifat sebagai mild stimulant pada sistem saraf pusat
akan meningkatkan daya ingat, memacu kecerdasan kognitif, dan perasaan senang
(Manitto, 1992).
2.4.1 Tanin
Tanin merupakan senyawa organik yang terdiri dari campuran senyawa
polifenol kompleks, dibangun dari elemen C, H, dan O serta sering membentuk
molekul besar dengan berat molekul lebih besar dari 2000 (Risnasari, 2001).
Senyawa-senyawa tanin termasuk suatu golongan senyawa yang berasal dari
tumbuhan yang sejak dahulu kala digunakan untuk merubah kulit hewan menjadi
kedap air, dan awet. Istilah tanin diperkenalkan oleh Seguil pada tahun 1796. Pada
waktu itu belum diketahui bahwa tanin tersusun dari campuran bermacam-macam
senyawa, bukan hanya satu golongan senyawa saja. Senyawa-senyawa tanin dapat
diartikan sebagai suatu senyawa-senyawa alami dengan bobot molekul antara 500
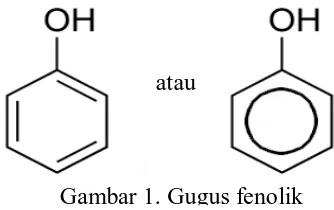
dan 3000, serta mempunyai sejumlah gugus hidroksi fenolik dan membentuk ikatan
silang yang stabil dengan protein dan biopolimer lain, misalnya selulosa dan pectin
(Manitto, 1992).
Tanin disebut juga asam tanat dan asam galotanat. Tanin dapat tidak berwarna
sampai berwarna kuning atau coklat. Asam tanat yang dapat dibeli di pasaran
mempunyai BM 1701 dan kemungkinan besar terdiri dari sembilan molekul asam
galat dan sebuah molekul glukosa. Beberapa ahli pangan berpendapat bahwa tanin atau
terdiri dari katekin, leukoantosianin, dan asam hidroksi yang masing-masing dapat
menimbulkan warna bila bereaksi dengan ion logam (Winarno, 1992).
Tanin secara umum didefinisikan sebagai senyawa polifenol yang memiliki
berat molekul cukup tinggi (lebih dari 1000) dan dapat membentuk kompleks
dengan protein. Berdasarkan strukturnya, tanin dibedakan menjadi dua kelas yaitu
tanin terkondensasi (condensed tannins) dan tanin-terhidrolisiskan (hydrolysable
tannins) (Manitto, 1992).
Tanin memiliki peranan biologis yang kompleks. Hal ini dikarenakan sifat
tanin yang sangat kompleks mulai dai pengendap protein hingga pengkhelat logam.
Maka dari itu efek yang disebabkan tanin tidak dapat diprediksi. Tanin juga dapat
berfungsi sebagai antioksidan biologis. Maka dari itu semua penelitian tentang
berbagai jenis senyawa tanin mulai dilirik para peneliti sekarang. Dalam makalah
ini akan dibahas berbagai hal tentang tanin yaitu klasifikasinya dan contoh
senyawanya, sifat umumnya, cara identifikasi serta contoh pemurnian senyawa
tanin (Shorgum Tanin) (Manitto, 1995).
2.4.1.1 Klasifikasi tanin
Senyawa tanin dibagi menjadi dua yaitu tanin yang terhidrolisis dan tanin
1. Tanin Terhidrolisis (hydrolysable tannins).
Tanin ini biasanya berikatan dengan karbohidrat dengan membentuk
jembatan oksigen, maka dari itu tanin ini dapat dihidrolisis dengan
menggunakan asam sulfat atau asam klorida. Salah satu contoh jenis tanin
ini adalah gallotanin yang merupakan senyawa gabungan dari karbohidrat
dengan asam galat. Selain membentuk gallotanin, dua asam galat akan
membentuk tanin terhidrolisis yang bisa disebut ellagitanin. Ellagitanin
sederhana disebut juga ester asam hexahydroxydiphenic (HHDP). Senyawa
ini dapat terpecah menjadi asam galik jika dilarutkan dalam air.
2. Tanin terkondensasi (condensed tannins).
Tanin jenis ini biasanya tidak dapat dihidrolisis, tetapi dapat terkondensasi
menghasilkan asam klorida. Tanin jenis ini kebanyakan terdiri dari polimer
flavonoid yang merupakan senyawa fenol. Nama lain dari tanin ini adalah
Proantosianidin. Proantosianidin merupakan polimer dari flavonoid yang
dihubungkan melalui C8 dengan C4. Salah satu contohnya adalah Sorghum
prosianidin, senyawa ini merupakan trimer yang tersusun dari epikatekin dan
katekin. Senyawa ini jika dikondensasi maka akan menghasilkan flavonoid
jenis flavan dengan bantuan nukleofil berupa floroglusinol (Manitto, 1995).
Sumber : Mamitto, 1995
Sifat fisika dari tanin adalah sebagai berikut :
a. Jika dilarutkan kedalam air akan membentuk koloid dan memiliki rasa
asam dan sepat.
b. Jika dicampur dengan alkaloid dan glatin akan terjadi endapan .
c. Tidak dapat mengkristal.
d. Mengendapkan protein dari larutannya dan bersenyawa dengan
protein tersebut sehingga tidak dipengaruhi oleh enzim protiolitik.
2. Sifat kimia
a. Merupakan senyawa kompleks dalam bentuk campuran polifenol
yang sukar dipisahkan sehingga sukar mengkristal.
b. Tanin dapat diidentifikasikan dengan kromotografi.
c. Senyawa fenol dari tanin mempunyai aksi astringensia, antiseptik dan
pemberi warna (Manitto, 1995).
3. Sifat tanin sebagai pengkhelat logam.
Senyawa fenol yang secara biologis dapat berperan sebagai khelat
logam. Proses pengkhelatan akan terjadi sesuai pola subtitusi dan pH
senyawa fenolik itu sendiri. Karena itulah tanin terhidrolisis memiliki
potensial untuk menjadi pengkhelat logam. Hasil khelat dari tanin ini
memiliki keuntungan yaitu kuatnya daya khelat dari senyawa tanin ini
membuat khelat logam menjadi stabil dan aman dalam tubuh. Tetapi jika
tubuh mengkonsumsi tanin berlebih maka akan mengalami anemia karena
zat besi dalam darah akan dikhelat oleh senyawa tanin tersebut (Manitto,
2.4.1.3 Cara Identifikasi Senyawa Tanin
Berdasarkan sifat-sifat diatas maka untuk menganalisis tanin dapat
dilakukan berbagai cara sesusai tujuannya. Untuk analisis secara kualitatif dapat
dilakukan dengan menggunakan metode :
a. Diberikan larutan FeCl3 berwarna biru tua / hitam kehijauan.
b. Ditambahkan Kalium Ferrisianida + amoniak berwarna coklat.
c. Diendapkan dengan garam Cu, Pb, Sn, dan larutan Kalium Bikromat
berwarna coklat (Manitto, 1995).
Sedangkan untuk menganalisis secara kuantitatif dapat dilakukan dengan
mengunakan metode :
a. Metode analisis umum fenolik, karena tanin merupakan senyawa fenolik
(Metode blue prussian dan Metode Folin).
b. Metode analisis berdasarkan gugus fungsinya
c. Dengan menggunakan HPLC, dan UV-Vis
d. Metode presipitasi menggunakan protein (Manitto, 1995).
3.1 Alat
- Beaker glass 2000 ml, botol sampel, hot plate, magnetic stirrer, bola
hisap, mat pipet 25 ml, termometer, pipet volum 10 ml, pipet volum
5 ml, spatula, timbangan analitik, corong, erlenmeyer 300 ml, buret,
gelas ukur 100 ml.
3.2 Bahan
- Serbuk teh
- Air Buffer III ( air dengan kesadahan nol)
3.3 Pereaksi
- Aquades
- KMnO4 0,05 N
- Serbuk Kaolin
- Indigo Carmin
- NaCl asam
- Gelatin
3.4 Prosedur
3.4.1 Larutan uji
1. Teh Cair Pahit (TCP) dibuat, dengan mencampurkan 6,5
gram serbuk teh ( black tea ) dengan 1 liter air buffer III.
2. Dimasukkan ke dalam beker glass 2000 ml.
3. Ke dalamnya dimasukkan magnetic stirrer sebagai pengaduk.
5. Diukur suhu secara berkala mulai dari 65 ºC, 70 ºC, 80 ºC,
dan 90 ºC dengan menggunakan termometer.
6. Diambil 25 ml masing – masing pada 4 (empat) kondisi
temperatur yang berbeda.
7. Dimasukkan ke dalam wadah botol secara terpisah antara 25
ml dari temperatur 65 ºC, 70 ºC, 80 ºC, dan 90 ºC.
8. Didiamkan hingga dingin.
9. Dipipet masing – masing 5 ml.
10. Dimasukkan masing – masing ke dalam erlenmeyer.
11. Ditambahkan 5 ml indigo carmin.
12. Ditambah 75 ml aquades.
13. Digoyang – goyang hingga terhomogenkan.
14. Dititrasi dengan KmnO4 0,05 N hingga warna kuning emas.
15. Dicatat volume KmnO4 yang terpakai untuk masing –masing
percobaan.
3.4.2 Larutan blanko
1. Ditimbang serbuk kaolin sebanyak 2,0 gram.
2. Dimasukkan ke dalam wadah gelas.
3. Diambil 20 ml larutan sampel dari larutan sampel yang
memiliki temperatur 90 ºC.
4. Dicampurkan ke dalam wadah gelas yang berisi serbuk
kaolin tadi.
6. Ditambah 20 ml NaCl asam.
7. Diaduk hingga rata
8. Disaring
9. Diambil filtratnya sebanyak 5 ml.
10. Dimasukkan ke dalam Erlenmeyer.
11. Ditambah 5 ml indigo carmin
12. Ditambah 75 ml aquades.
13. Dititrasi dengan KMnO4 0,05 N sampai kuning emas.
14. Dicatat volume KMnO4 yang terpakai.
BAB IV
4.1 Hasil
4.1.1 KMnO4 yang terpakai pada percobaan larutan uji
Keterangan :
Volume KMnO4 yang terpakai = A ml
4.1.2 KMnO4 yang terpakai pada percobaan larutan blanko
KMnO4 yang terpakai = 4,95 ml ( B ml )
4.1.3 Perhitungan
Rumus : Kadar tanin = A – B x Normalitas KMnO4
Normalitas KMnO4 = 415,468
1. Untuk temperatur 65 ºC :
Rumus Kadar tanin: A – B x Normalitas KMnO4
A = 6,45 ml
B = 4,95 ml
Kadar tanin = A – B x Normalitas KMnO4 Temperatur Volume KMnO4 yang terpakai (ml)
65 ºC 6,45 ml
70 ºC 6,5 ml
80 ºC 7,25 ml
= 1,5 x 415, 468
= 623, 202 ppm
2. Untuk temperatur 70 ºC :
Rumus kadar tanin: A – B x Normalitas KMnO4
A = 6,5 ml
B = 4,95 ml
Kadar tanin = A – B x Normalitas KMnO4
= ( 6,5 – 4,95 ) x 415,468
= 1,55 x 415,468
= 643, 9754 ppm
3. Untuk temperatur 80 ºC :
Rumus kadar tanin: A – B x Normalitas KMnO4
A = 7,25 ml
B = 4,95 ml
kadar tanin = A – B x Normalitas KMnO4
= ( 7,25 – 4,95 ) x 415,468
= 955, 1232 ppm
4. Untuk temperatur 90 ºC :
Rumus kadar tanin: A – B x Normalitas KMnO4
A = 7,35 ml
B = 4,95 ml
Kadar tanin = A – B x Normalitas KMnO4
= ( 7,35 – 4,95 ) x 415,468
= 2,4 x 415,468
= 997, 1232 ppm
4.2 Pembahasan
Percobaan dilakukan dengan menggunakan metode titrasi permanganometri.
Yaitu menggunakan KMnO4 sebagai pentiter. Dari hasil percobaan kandungan
tanin yang paling tinggi diperoleh pada penyeduhan untuk temperatur 90 ºC.
Diperoleh kadar tanin sebesar 997,1232 ppm. Temperatur 90 ºC adalah temperatur
yang baik yang digunakan untuk menyeduh teh pada pembuatan minuman teh.
Dimana dketahui bahwa semakin tinggi suhu maka semakin baik untuk tanin
terlarut. Kelarutan tanin akan mempengaruhi warna tampilan dari produk minuman
teh dan juga temperatur yang digunakan juga mempengaruhi kandungan zat – zat
lain dalam teh. Maka standar yang telah ditentukan PT Sinar Sosro untuk kadar
tanin adalah 900 ppm – 1150 ppm. Standar ini adalah standar dengan pemeriksaan
bahwa pada temperatur ini baik dalam menghasilkan warna minuman teh dan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
- Ada pengaruh perbedaan temperatur terhadap kadar tannin pada
penyeduhan teh.
- Temperatur yang baik yang dipakai pada penyeduhan teh guna
mempertahankan kandungan zat dalam teh adalah 90 ºC, dan ini yang
dijadikan Standart Operational Procedure ( SOP ) pada pembuatan teh
botol di PT Sinar Sosro KPB Deli Serdang.
5.2 Saran
- Hendaknya pemeriksaan dilakukan dengan metode lain yang
menghasilkan data yang akurat serta juga mudah dilakukan demi
perkembangan dalam pengujian – pengujian senyawa dalam tumbuhan
dalam hal ini senyawa tanin.
- Hendaknya pengujian terhadap senyawa tanin dilakukan berdasarkan
variabel yang lain, agar semakin berkembang pengetahuan mengenai
DAFTAR PUSTAKA
Alaerts, G., dan Santika, S, S. (1984). Metode Penelitian Air. Surabaya: Penerbit Usaha Nasional.
Belitz, H.D dan W. Grosch. (1987). Food Chemistry. New York : Library of Congress Cataloging in Publication Data.
Coultate, T.P. (1989). Food The Chemistry of Its Components. Second edition. London : Departement of Biotechnology South Bank Polytechnic.
Depkes RI. (2000). Penelitian Tanaman Obat di Beberapa Perguruan Tinggi di
Indonesia. Jakarta : Departemen Kesehatan RI.
Dewick, Paul M. (2001). Medicinal Natural Products A Biosynthetic Approach. Second edition. UK : School of Pharmaceutical Sciences University of Nottingham.
Fitri, N, S. 2009. Pengaruh Berat dan Waktu Perendaman Terhadap Kadar Kafein
dari Bubuk Teh di Medan. Skripsi. Medan: Universitas Sumatera Utara.
Hasibuan, D, B. 2005. Pengaruh Suhu Dan Lama Pengadukan Dalam Penentuan
Kadar Tanin Dari Biji Buah Pinang. Skripsi. Medan: Universitas Sumatera
Utara.
Kartasapoetra, G. 1992. Budidaya Tanaman Berkhasiat Obat. Jakarta: Penerbit Rineka Cipta.
Mangan, Yellia. (2003). Cara Bijak Menaklukkan Kanker. Cetakan Pertama. Depok : Penerbit PT Agromedia Pustaka.
Manitto, P. 1992. Biosintesis Produk Alami. Cetakan Pertama. Tejemahan Koensoemardiyah dan Sudarto. New York: Ellis Horwood Limited.
Mulja, M. 1995. Analisis Instrumenta. Bandung: Penerbit ITB.
Oktavia. R, W. 2009. Pengaruh Seduhan Teh Hijau (Camellia sinensis) Terhadap
Farmakokenetika Parasetamol yang Diberikan Bersama Secara Oral Kepada Kelinci Jantan. Skripsi. Surakarta: Universitas Muhammadiyah Surakarta.
Potter, N, N. 1986. Food Science. Fourth Edition. New York: Van Nostrand Reinhold.
Risnasari, I. 2001. Pemanfaatan Tanin Sebagai Bahan Pengawet Kayu. Skripsi.
Spillane, J, J. 1992. Komoditi Teh: Peranannya Dalam Perekonomian Indonesia. Cetakan I. Yogyakarta : Penerbit Kanisius.
Sujayanto, G. 2008. Khasiat Teh Untuk Kesehatan dan Kecantikan. Flona Serial hal. 34-38. Jakarta : ITB.
Winarno, F, G. 1992. Kimia Pangan Dan Gizi. Cetakan VI. Jakarta: PT Gramedia
Pustaka Utama.
http://www.Pusat Penelitian Teh dan Kina.com.