ABSTRACT
PEMBARUAN SIREGAR. The relationship among three populations of climbing perch fish (Anabas testudineus) based on analysis of Random Amplified Polymorphic DNA (RAPD) and morphometric characters. Supervised by Dinar Tri Soelistyowati dan Rudhy Gustiano
This research’s aimed is to evaluate three population of climbing perch fish collected from Java, Sumatera and South Kalimantan using Random Amplified Polymorphic DNA (RAPD) and morphometric characters. The results showed the moderate level of heterozygosity (0,088-0,109), while the genetic variability was highest in Kalimantan population. The genetic distance among populations showed that the populations from Java and Sumatera was closer (0,279) than Kalimantan (0,398-0,551). The UPGMA dendrogram analysis based on genetic distance performed the climbing perch populations into two groups that consisted of Java and Sumatera populations separated from South Kalimantan. The morphometric characters described that 3 type of characters duabled to separate into three different groups and about 10% of sharing component showed that the climbing perch populations from Sumatera consist of Java population.
1
I. PENDAHULUAN
1.1. Latar Belakang
Betok merupakan spesies ikan air tawar yang hidup liar di perairan tawar, payau, dan rawa. Pada umumnya berukuran kecil, panjang maksimal sekitar 25 cm, bersisik keras kaku, sisi atas tubuh (dorsal) gelap kehitaman agak kecoklatan atau kehijauan, sisi samping (lateral) kekuningan, terutama di sebelah bawah, dengan garis-garis gelap melintang yang samar dan tak beraturan, sisi belakang tutup insang bergerigi tajam seperti duri, dan berkepala besar (Anonim, 2011). Ikan betok dikenal dengan nama bethok atau bethik, puyu, pepuyu. Ikan betok dikenal juga sebagai climbing gouramy atau climbing perch, karena kemampuannya memanjat ke daratan. Nama ilmiahnya adalah Anabas testudineus. Distribusi populasi ikan betok (Anabas testudineus) yang hidup di air
tawar mulai langka. Pemangsa serangga yang juga menjadi musuh alami wereng ini makin susah ditemukan dalam ukuran besar. Berikut klasifikasi ilmiah ikan betok pada umumnya.
Suhu yang sesuai sebagai syarat hidup ikan betok adalah 15 – 31°C . Ikan betok merupakan ikan penghuni asli Asia Tenggara, India, Srilanka, Taiwan, Bangladesh, Afrika, Hindia Timur, Indo-Cina dan Cina bagian selatan serta menjadi ikan introduksi untuk Papua (daerah Merauke), kemudian menyebar ke arah timur Papua New Guinea (www.fishbase.org)
Klasifikasi ilmiah : Kerajaan : Animalia Filum : Chordata Kelas : Actinopterygii Ordo : Perciformes Famili : Anabantidae Genus : Anabas
Spesies : Anabas testudineus
2
Ikan ini mempunyai naluri yang kuat untuk mendeteksi di mana keberadaan sumber air. Banyak orang yang menyebutnya ikan gaib karena ikan ini dapat dengan cepat menghilang padahal ikan ini hanya kabur dari air dengan cara berjalan di darat (merayap). Saat berjalan ikan ini merayap dengan tutup insang sebagai kaki depannya, selain itu ikan ini mempunyai daya tahan kuat.
Ikan betok liar di Kalimantan, semula bisa mencapai sampai bobot 250 gram. Kini ikan betok hanya berbobot 70-100 gram per ekor dengan kisaran harga Rp 40.000-Rp 70.000 per kilogram. Selain itu produksi tangkapan ikan betok di provinsi Kalimantan Timur antara tahun 2002-2008 mengalami peningkatan tiap tahunnya yaitu 91 ton pada tahun 2004 menjadi 1505 ton pada tahun 2005 (DKP, 2006 dalam Pellokila, 2009). Semakin meningkatnya penangkapan terhadap ikan ini menimbulkan kekhawatiran akan menurunnya populasi ikan ini di kemudian hari. Berdasarkan hal tersebut maka pengelolaan perikanan berkelanjutan perlu secepatnya dilakukan untuk mencegah terjadinya penurunan populasi ikan betok. Beberapa informasi dasar dibutuhkan dalam upaya pengelolaan yaitu kajian mengenai informasi karakteristik genotip dan fenotipnya. Identifikasi genotip dapat dilakukan dengan beberapa teknik, diantaranya adalah Random Amplified Polymorphic DNA (RAPD) dengan teknik PCR (Polymerase Chain Reaction)
(Muladno, 2002). Sedangkan identifikasi fenotip dapat dilakukan dengan analisis karakter morfometrik.
1.2. Tujuan
3
II. BAHAN DAN METODE
2.1. Waktu dan Lokasi Penelitian
Penelitian ini dilaksanakan dari bulan Agustus sampai September tahun 2011. Sampel ikan berasal dari 3 lokasi yaitu Jawa (Jawa Barat), Sumatera (Jambi), dan Kalimantan (Kalimantan Tengah). Analisa genetik ikan dilakukan di Laboratorium Genetik Ikan, Balai Riset Perikanan Budidaya Air Tawar, Sempur, Bogor, sedangkan pengukuran karakter morfometrik dilakukan di Instalasi Riset Plasma Nutfah, Cijeruk, Bogor.
2.2. Materi Uji
Sampel ikan betok berasal dari 3 lokasi, yaitu dari Kalimantan Tengah (Pulang Pisau), Jawa Barat (Tasikmalaya), dan Sumatera (Jambi), masing masing 10 ekor. Kondisi lingkungan di lokasi sampling adalah perairan rawa (Kalimantan Tengah) dan kolam budidaya air tawar ( Jawa Barat dan Sumatera). Sampel ikan diambil siripnya dan dilarutkan dalam larutan alkohol 70%-90% untuk mengawetkan sirip ikan, selanjutnya dilakukan analisis DNA dengan teknik PCR. Untuk pengukuran karakter morfometrik, diambil masing masing 10 ekor dari populasi dan dihitung panjang yang mencakup seluruh bagian luar tubuh.
Gambar 1. Ikan betok (Anabas testudineus)
4
2.3. Metode Kerja
Profil genotip ikan dianalisis menggunakan metode RAPD yang diawali dengan proses ekstraksi DNA genom, amplifikasi DNA menggunakan teknik PCR dan elektroforesis. Sedangkan profil fenotip ikan betok dianalisis menggunakan metode pengukuran karakter morfometrik.
2.3.1. Ekstraksi DNA
Sampel ikan berupa sirip dorsal ditimbang sebanyak 5-10 mg dan dimasukan ke dalam tabung eppendorf 1,5 ml, kemudian dilisis dengan menambahkan TNES urea sebanyak 500 µl dan protein kinase 10 µl. Setelah itu dikocok menggunakan alat vortex dan diinkubasi pada suhu 37°C selama 24 jam atau sampai sirip hancur. Selanjutnya ditambahkan larutan phenolchloroform isoamilalkohol (PCL) dengan perbandingan 25:24:1 sebanyak 1000 µl dan disentrifuse dengan menggunakan kecepatan 10.000 rpm selama 10 menit. Supernatan lalu dipindahkan ke tabung baru dan ditambahkan etanol 90% sebanyak 1000 µl dan Na asetat sebanyak 10 µl lalu disentrifugasi pada kecepatan 10.000 rpm selama 10 menit. Supernatan dibuang dan pellet dikering anginkan sampai etanol menguap. DNA dilarutkan dengan menambahkan rehydration solution sebanyak 100 µl.
2.3.2. Amplifikasi DNA dengan teknik PCR
Sebelum amplifikasi DNA, maka dilakukan terlebih dahulu seleksi primer untuk mendapatkan jenis primer yang sesuai. Amplifikasi DNA dilakukan menggunakan metode PCR dengan komposisi bahan 1 unit dry taq produk Promega, 2 µl DNA template, 2 µl primer dan 21 µl air dengan volume total sebanyak 25 µl. Lalu dimasukkan ke dalam mesin PCR dengan 35 siklus, yaitu denaturasi awal pada 94°C selama 2 menit, denaturasi 94°C selama 1 menit. annealing 36°C selama 1 menit, elongasi 72°C selama 2 menit 30 detik, elongasi
5
Tabel 1. Sekuen primer RAPD yang diuji
No Primer Sekuen Nukleotida (5’Æ3’)
1 OPA-02 TGCCGAGCTG
2 OPC-02 GTGAGGCGTC
3 OPC-05 GATGACCGCC
Keterangan : T = deoksi Timidin 5’- monofosfat G = deoksi Guanosin 5’- monofosfat C = deoksi Sitidin 5’- monofosfat A = deoksi Adenosin 5’- monofosfat
2.3.3. Elektroforesis
Untuk mengetahui keberhasilan amplifikasi primer yang digunakan, campuran 9 µl hasil PCR dengan 2 µl loading die dielektroforesis pada gel agarose 2% (w/v) dalam larutan TBE dan tegangan 100 volt selama 30 menit. Kemudian, gel direndam agar pita DNA nya dapat terlihat pada cahaya ultraviolet. Selanjutnya, digunakan kamera untuk keperluan dokumentasi. Gene ruler 100bp DNA loader digunakan sebagai standar untuk menentukan ukuran fragmen hasil
amplifikasi.
2.3.4. Karakterisasi fenotip morfometrik
Ikan betok yang berasal dari Kalimantan Tengah, Jawa Barat, dan Jambi diambil dari akuarium masing masing 10 ekor. Metode karakteristik morfometrik dilakukan dengan cara mengukur jarak titik-titik tanda yang akan dibuat pada kerangka tubuh (Gambar 2). Skema dan 21 karakteristik morfometrik ikan betok dapat dilihat pada Gambar 2 dan Tabel 2 ( Brzesky and Doyle, 1988)
6
Tabel 2. Karakteristik morfometrik
No Kode Deskripsi Jarak
1 A1-2 Bawah mulut-ujung bagian atas insang 2 A1-3 Bawah mulut-operkulum
3 A1-4 Bawah mulut-awal sirip punggung 4 A1-5 Bawah mulut-awal sirip perut 5 A2-3 Ujung atas insang-operkulum
6 A2-4 Ujung atas insang-awal sirip punggung 7 A2-5 Ujung atas insang-awal sirip perut 8 A3-4 Operkulum-awal sirip punggung 9 A3-5 Operkulum-awal sirip perut
10 A4-5 Awal sirip punggung-awal sirip perut 11 B5-6 Awal sirip perut-awal sirip anal 12 B5-7 Awal sirip perut-akhir sirip anal 13 B6-4 Awal sirip anal-awal sirip punggung 14 B10-4 Akhir sirip punggung-awal sirip punggung 15 B10-6 Akhir sirip punggung-awal sirip anal 16 C7-8 Awal sirip ekor bawah-awal sirip ekor atas 17 C7-9 Awal sirip ekor bawah-akhir sirip ekor atas 18 C8-9 Akhir sirip ekor bawah-akhir sirip ekor atas 19 C10-7 Akhir sirip punggung-awal sirip ekor bawah 20 C10-8 Akhir sirip punggung-akhir sirip ekor bawah 21 C10-9 Awal sirip punggung-awal sirip ekor atas
Keterangan : A = bagian kepala 1-2, dst = jarak antar titik karakter B = bagian seluruh tubuh
C = bagian ekor
7
2.4. Analisis Data
Keragaman genetik yang meliputi tingkat polimorfisme, heterozigositas, uji perbandingan Fst dianalisa dengan descriptive statistics (Miller, 1997), exact test for population differentiation (Raymond & Rousset, 1995 dalam Miller, 1997)
dengan menggunakan program TFPGA (Tools for Population Genetic Analyses). Kekerabatan antar populasi berdasarkan jarak genetik yang disertai dengan dendrogram dianalisis menggunakan UPGMA (Unweighted Pair Group Method with Arithmetic Mean) Wright (1978) modifikasi Rogers (1972) dalam Miller
8
III. HASIL DAN PEMBAHASAN
3.1. Hasil
3.1.1. Profil RAPD
Keragaman profil penanda DNA meliputi jumlah dan ukuran fragmen DNA. Hasil amplifikasi dengan menggunakan primer OPA-02, OPC-02, OPC-05 selengkapnya disajikan pada Tabel 3. Amplifikasi DNA pada 3 populasi dapat dilihat pada Gambar 3-5. Profil DNA teramplifikasi dengan primer OPA-02, OPC-02, OPC-05 selengkapnya disajikan pada Lampiran 1.
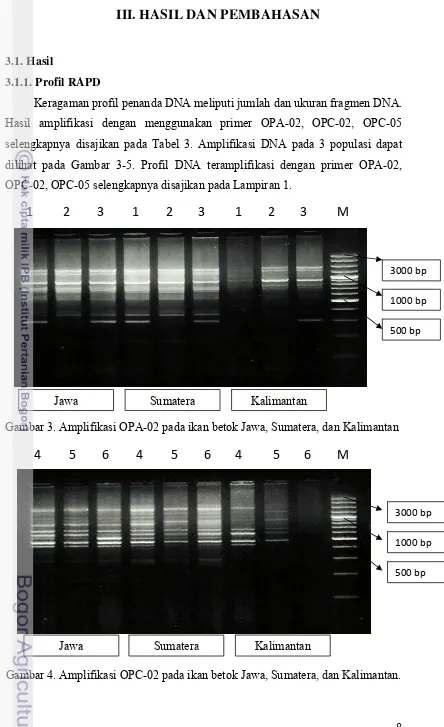
Gambar 3. Amplifikasi OPA-02 pada ikan betok Jawa, Sumatera, dan Kalimantan
1
2
3
1
2
3
1
2
3
M
3000 bp
1000 bp
500 bp
Jawa Sumatera Kalimantan
4
5
6
4
5
6
4
5
6
M
Jawa
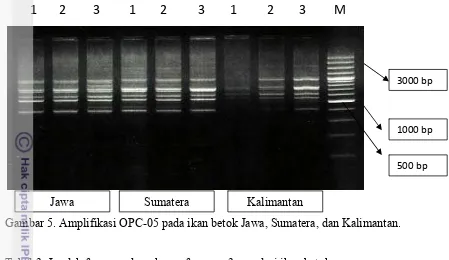
Gambar 4. Amplifikasi OPC-02 pada ikan betok Jawa, Sumatera, dan Kalimantan. 500 bp 1000 bp 3000 bp
9
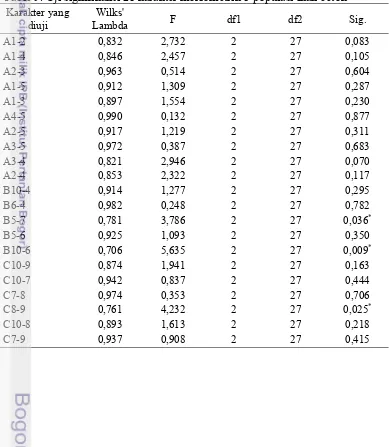
Gambar 5. Amplifikasi OPC-05 pada ikan betok Jawa, Sumatera, dan Kalimantan.
Tabel 3. Jumlah fragmen dan ukuran fragmen 3 populasi ikan betok
Populasi Betok Jumlah Fragmen Kisaran Ukuran Fragmen (bp)
Jawa 24-26 100-2000
Sumatera 23-27 100-2000
Kalimantan 18-20 275-1750
Jumlah fragmen teramplifikasi berkisar antara 18-27 pada kisaran 100-2000 bp. Jumlah fragmen terbanyak adalah populasi ikan betok Sumatera dengan kisaran 100-2000 bp. Sedangkan kisaran terendah adalah populasi ikan betok Kalimantan yaitu 275-1750 bp.
3.1.2. Polimorfisme
Tingkat keragaman genetik populasi meliputi derajat polimorfisme dan heterozigositas (Lampiran 2). Polimorfisme memberikan gambaran mengenai tingkat keragaman suatu populasi (Yuwono, 2006). Perbedaan jumlah dan polimorfisme pita DNA yang dihasilkan setiap primer menggambarkan keunikan genom yang diamati. Pita DNA hasil amplifikasi merupakan pasangan antara nukleotida primer dengan nukleotida sampel. Panjang ukuran fragmen pita DNA yang dihasilkan setelah amplifikasi berkisar 100 sampai 2000 bp (base pairs).
1
2
3
1
2
3
1
2
3
M
Jawa Sumatera Kalimantan
3000 bp
10
Tabel 4. Persentase polimorfisme 3 populasi ikan betok
Populasi Betok Polimorfisme (%)
Jawa 18.52 Sumatera 22.22 Kalimantan 25.93
Persentase polimorfisme berkisar antara 18,52% sampai 25,93%. Persentase polimorfisme tertinggi adalah populasi ikan betok Kalimantan yaitu sebesar 25,93%, sedangkan polimorfisme terendah adalah populasi ikan betok Jawa yaitu sebesar 18,52%.
3.1.3. Heterozigositas
Heterozigositas tiap populasi disajikan dalam Tabel 5 berikut:
Tabel 5. Nilai heterozigositas 3 populasi ikan betok
Populasi Betok Heterozigositas
Jawa 0,088
Sumatera 0,095
Kalimantan 0,109
Nilai rata rata heterozigositas terendah dimiliki ikan betok dari populasi Jawa yaitu sebesar 0,088, sedangkan heterozigositas ikan betok tertinggi adalah populasi ikan betok dari Kalimantan yaitu sebesar 0,109.
3.1.4. Uji perbandingan Fst
Secara statistik dengan menggunakan uji perbandingan Fst, menunjukkan ada perbedaan genetik secara nyata antara populasi ikan betok Kalimantan terhadap populasi betok Jawa dan Sumatera.
Tabel 6. Nilai uji perbandingan berpasangan Fst 3 populasi ikan betok
Populasi Betok Jawa Sumatera Kalimantan Jawa *****
Sumatera 0,9986ns *****
Kalimantan 0,0000 0,0000 *****
11
Berdasarkan Tabel 6 diatas dapat diketahui bahwa antara populasi ikan betok Kalimantan dengan Jawa dan Sumatera berbeda nyata. Sedangkan ikan betok Jawa dan Sumatera tidak berbeda nyata.
3.1.5. Jarak genetik
Pada Tabel 7 di bawah ini disajikan jarak genetik masing masing populasi ikan betok dari tiap tiap populasi.
Tabel 7. Jarak genetik 3 populasi ikan betok
Populasi Betok Jawa Sumatera Kalimantan Jawa *****
Sumatera 0,279 *****
Kalimantan 0,551 0,398 *****
Jarak genetik 3 populasi berkisar antara 0,279 sampai 0,551. Hubungan kekerabatan interpopulasi 3 populasi ikan betok dapat digambarkan dalam bentuk dendrogram. Dendrogram yang ditampilkan merupakan hasil analisis dengan menggunakan program TFPGA pada analisis UPGMA.
Berdasarkan dendrogram (Gambar 6) digambarkan bahwa hubungan kekerabatan genetik paling dekat adalah populasi ikan betok Jawa dengan
Gambar 6. Dendrogram hubungan genetik 3 populasi ikan betok
Jawa
Sumatera
12
populasi ikan betok Sumatera, yaitu sebesar 0,279 dan yang paling jauh adalah populasi ikan betok Kalimantan dengan populasi ikan betok Jawa.
3.1.6. Karakter morfometrik
Pengukuran karakter morfometrik dilakukan terhadap 21 karakter pada ikan betok Jawa, Sumatera, dan Kalimantan (Lampiran 3). Rata rata karakter morfometrik disajikan dalam Tabel 8 berikut.
Tabel 8. Rata rata 21 karakter morfometrik (cm) 3 populasi ikan betok
Karakter yang
13
3.1.7. Uji signifikansi
Uji signifikansi dilakukan untuk mengetahui karakter yang dapat digunakan sebagai penciri dari suatu jenis ikan. Berdasarkan hasil penelitian, bahwa 21 karakter yang diuji, 18 karakter tidak berbeda nyata (P>0,05) dan 3 karakter berbeda nyata (P<0,05) yaitu karakter B5-7 (awal sirip perut-akhir sirip anal), B10-6 (akhir sirip punggung-awal sirip anal) dan C8-9 (awal sirip ekor atas-awal sirip ekor bawah)
Tabel 9. Uji signifikansi 21 karakter morfometrik 3 populasi ikan betok Karakter yang
diuji
Wilks'
Lambda F df1 df2 Sig.
A1-2 0,832 2,732 2 27 0,083
A1-4 0,846 2,457 2 27 0,105
A2-3 0,963 0,514 2 27 0,604
A1-5 0,912 1,309 2 27 0,287
A1-3 0,897 1,554 2 27 0,230
A4-5 0,990 0,132 2 27 0,877
A2-5 0,917 1,219 2 27 0,311
A3-5 0,972 0,387 2 27 0,683
A3-4 0,821 2,946 2 27 0,070
A2-4 0,853 2,322 2 27 0,117
B10-4 0,914 1,277 2 27 0,295
B6-4 0,982 0,248 2 27 0,782
B5-7 0,781 3,786 2 27 0,036*
B5-6 0,925 1,093 2 27 0,350
B10-6 0,706 5,635 2 27 0,009*
C10-9 0,874 1,941 2 27 0,163
C10-7 0,942 0,837 2 27 0,444
C7-8 0,974 0,353 2 27 0,706
C8-9 0,761 4,232 2 27 0,025*
C10-8 0,893 1,613 2 27 0,218
14
3.1.8. Canonical discriminant function
Hasil analisis fungsi kanonikal (Gambar 7) memperlihatkan bahwa karakter morfologi ikan betok Jawa dan ikan betok Sumatera tidak bersinggungan dengan ikan betok Kalimantan. Karakter morfometrik ikan betok Jawa berada di kuadran 1. Sedangkan karakter morfometrik ikan betok Sumatera dan betok Kalimantan berada di kuadran 3 dan 4. Persinggungan yang terjadi antara ikan betok Jawa dan Sumatera menunjukkan adanya pencampuran diantara kedua populasi tersebut. Karakter ikan betok Jawa dan Sumatera hanya sedikit yang bersinggungan, sedangkan ikan betok Kalimantan sama sekali tidak bersinggungan dengan ikan betok Jawa dan betok Sumatera
Gambar 7. Peta kanonikal 3 populasi ikan betok Kuadran 1
15
3.1.9. Indeks kemiripan
Analisis kemiripan populasi berdasarkan karakter morfometrik (Tabel 10) menunjukkan tingkat homogenitas 100% pada populasi Sumatera dan Kalimantan, sedangkan karakter morfometrik populasi ikan betok Jawa memiliki indeks kemiripan dengan populasi ikan betok Sumatera sebesar 10% .
Tabel 10. Indeks kemiripan (sharing components) morfometrik (%)
Jawa Sumatera Kalimantan Total
Jawa 90,0 10,0 0,0 100,0
Sumatera 0,0 100,0 0,0 100,0 Kalimantan 0,0 0,0 100,0 100,0
3.2.0. Dendrogram penyebaran morfometrik
Analisis dendrogram karakter morfometrik ketiga populasi ikan betok menunjukkan kemiripan antara populasi Jawa dan Sumatera (Gambar 8).
16
3.2. Pembahasan
17
sesuai dengan kondisi alami populasi ikan betok di Kalimantan diduga menjadi penyebab terjadinya genetic drift karena beberapa populasi diduga terperangkap dalam area yang tertutup (sistem budidaya) sehingga mengakibatkan rendahnya variasi gen. Pengujian Fst keragaman genetik antar populasi menunjukkan perbedaan yang nyata antara populasi ikan betok Kalimantan dengan Sumatera dan Jawa. Sedangkan antara populasi ikan betok Sumatera dan ikan betok Jawa menunjukkan kesamaan populasi atau mencerminkan distribusi unsur genetik yang sama.
Keragaman genetik mempengaruhi kemampuan spesies untuk merespon perubahan lingkungan baik buatan maupun alami dalam proses adaptasi agar bertahan hidup. Setiap kombinasi gen memiliki respons yang berbeda terhadap perubahan lingkungan, dalam hal ini keberagaman gen memberikan peluang yang lebih baik untuk dapat merespon perubahan lingkungan tersebut. Reduksi variasi genetik yang berlangsung dalam waktu lama dapat mengarah pada penurunan produktifitas populasi yang berdampak pada penurunan profit. Untuk mengatasi hal tersebut perlu dilakukan revitalisasi stok induk dengan mengintroduksi ragam genetik di lingkungan budidaya maupun restocking di perairan umum (Tave, 1983)
Hubungan kekerabatan antar populasi yang digambarkan menurut jarak genetik menunjukkan bahwa semakin kecil jarak genetik maka semakin tinggi kemiripan populasi tersebut, dan sebaliknya. Jarak genetik antara ketiga populasi ikan betok berkisar antara 0,279-0,551 yang menunjukkan bahwa ikan betok Jawa dengan Sumatera memiliki kemiripan yang lebih tinggi dibandingkan dengan populasi dari Kalimantan. Selain itu, lingkungan perairan rawa di Kalimantan diduga mempengaruhi perbedaan variasi genetik tersebut terkait dengan parameter kualitas air, terutama alkalinitas dan pH yang lebih rendah dibandingkan dengan perairan lingkungan budidaya di Jawa dan Sumatera (Pellokila, 2009)
18
ovipar, memijah sepanjang tahun dengan puncak pemijahannya pada musim penghujan (musim banjir) di tepi tumbuhan air. Puncak pemijahan terjadi pada bulan Oktober-Desember, dengan telur telur mengapung bebas (egg layer). Suhu air yang cocok untuk pemijahan ikan betok adalah 28°C dengan pH 7. Pada musim kemarau, ikan ini membenamkan diri ke dalam lumpur dan muncul kembali saat musim penghujan (Pellokila, 2009). Selain itu, di perairan rawa, fluktuasi air tinggi dalam setahun sangat besar, hal ini terkait dengan siklus hidrologi. Akibat adanya peningkatan kedalaman dan penggenangan daratan, habitat berkembang sangat luas. Semakin luas habitat, semakin beragam pula sebaran makhluk hidup yang hidup di dalamnya karena semakin beragam pula ketersediaan makanan yang terdapat di sana. Hal ini sesuai dengan tangkapan ikan betok yang diperoleh (Setiadi dan Dewi 1989). Hasil tangkapan terbanyak terdapat pada bulan Desember saat kedalaman air tinggi. Pada populasi ikan betok dari Kalimantan, perubahan kondisi lingkungan diduga juga dipengaruhi oleh kerusakan lingkungan seperti kerusakan hutan, penebangan hutan bakau dan pencemaran lingkungan, sehingga mengakibatkan penurunan kualitas air yang berdampak pada semakin kritisnya peluang hidup ikan betok, dan memperkecil adanya migrasi maupun interaksi dengan populasi ikan betok dari tempat lain (Christanty, 2009)
19
lama, maka kemampuannya untuk bertahan hidup menjadi bergantung pada kelengkapan keragaman genetiknya dengan munculnya genotip-genotip baru yang memiliki toleransi baru sehingga memungkinkan spesies tersebut untuk bertahan hidup dan mengembangkan jenisnya (Stansfield, 1991)
Keragaman morfometrik ikan betok Kalimantan lebih rendah dibandingkan dengan populasi betok Jawa dan Sumatera. Berdasarkan uji signifikansi karakter morfometrik diketahui 3 fenotip, yaitu karakter B5-7 (awal sirip perut-akhir sirip anal), B10-6 (akhir sirip punggung-awal sirip anal) dan C8-9 (awal sirip ekor atas-awal sirip ekor bawah), menunjukkan perbedaan populasi betok Kalimantan dengan populasi Jawa dan Sumatera. Dalam hal ini, 18 karakter yang tidak berbeda nyata dapat digunakan sebagai penciri jenis ikan betok. Perbedaan habitat masing masing populasi dapat menjadi penyebab adanya perbedaan pada ketiga karakter tersebut. Selain perbedaan habitat, faktor ragam lingkungan seperti pakan, kepadatan populasi, ukuran dan umur induk, ukuran telur, dan teknik pendederan juga dapat mempengaruhi (Alawi et al, 2006).
20
IV. KESIMPULAN DAN SARAN
4.1. Kesimpulan
Populasi ikan betok dari Kalimantan memiliki tingkat polimorfisme yang paling tinggi (25,92%) dan hubungan kekerabatan genetik yang paling jauh terhadap populasi ikan betok dari Jawa (0,551) dan Sumatera (0,398). Karakter morfometrik populasi ikan betok Jawa memiliki indeks kemiripan dengan populasi ikan betok Sumatera sebesar 10%.
4.2. Saran
HUBUNGAN 3 POPULASI IKAN BETOK (Anabas testudineus)
BERDASARKAN ANALISIS RAPD (Random Amplified
Polymorphic DNA) DAN KARAKTER MORFOMETRIK
PEMBARUAN SIREGAR
SKRIPSI
DEPARTEMEN BUDIDAYA PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
ABSTRACT
PEMBARUAN SIREGAR. The relationship among three populations of climbing perch fish (Anabas testudineus) based on analysis of Random Amplified Polymorphic DNA (RAPD) and morphometric characters. Supervised by Dinar Tri Soelistyowati dan Rudhy Gustiano
This research’s aimed is to evaluate three population of climbing perch fish collected from Java, Sumatera and South Kalimantan using Random Amplified Polymorphic DNA (RAPD) and morphometric characters. The results showed the moderate level of heterozygosity (0,088-0,109), while the genetic variability was highest in Kalimantan population. The genetic distance among populations showed that the populations from Java and Sumatera was closer (0,279) than Kalimantan (0,398-0,551). The UPGMA dendrogram analysis based on genetic distance performed the climbing perch populations into two groups that consisted of Java and Sumatera populations separated from South Kalimantan. The morphometric characters described that 3 type of characters duabled to separate into three different groups and about 10% of sharing component showed that the climbing perch populations from Sumatera consist of Java population.
ABSTRAK
PEMBARUAN SIREGAR. Hubungan 3 populasi ikan betok (Anabas testudineus) berdasarkan analisis RAPD (Random Amplified Polymorphic DNA) dan karakter morfometrik. Dibimbing oleh Dinar Tri Soelistyowati dan Rudhy Gustiano.
Penelitian ini bertujuan untuk mengevaluasi hubungan 3 populasi ikan betok (Anabas testudineus) yang berasal dari Jawa, Sumatera, dan Kalimantan dengan metode RAPD (Random Amplified Polymorphic DNA) dan karakter morfometrik. Hasil penelitian menunjukkan bahwa tingkat heterozigositas populasi ikan betok berkisar antara 0,088-0,109, sedangkan polimorfisme genetik populasi ikan betok Kalimantan merupakan yang tertinggi (25,93%) dibandingkan dengan populasi dari Sumatera (22,22%) dan Jawa (18,52%). Hubungan kekerabatan ketiga populasi menunjukkan jarak genetik antara populasi ikan betok Jawa dan Sumatera (0,279) lebih dekat dibandingkan dengan Kalimantan terhadap Jawa (0,398) dan Sumatera (0,551). Berdasarkan analisis dendrogram UPGMA mengelompokkan populasi Jawa dan Sumatera terpisah dari populasi Kalimantan. Dalam hal ini, 3 karakter morfometrik menunjukkan perbedaan populasi dan 18 karakter kemiripan, serta terdapat indeks kemiripan antara Sumatera dan Jawa sebesar 10% .
HUBUNGAN 3 POPULASI IKAN BETOK (Anabas testudineus)
BERDASARKAN ANALISIS RAPD (Random Amplified
Polymorphic DNA) DAN KARAKTER MORFOMETRIK
PEMBARUAN SIREGAR
SKRIPSI
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Program Studi Teknologi & Manajemen Perikanan Budidaya
Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan,
Institut Pertanian Bogor
DEPARTEMEN BUDIDAYA PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
PERNYATAAN MENGENAI SKRIPSI
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa Skripsi yang berjudul :HUBUNGAN 3 POPULASI IKAN BETOK (Anabas testudineus)
BERDASARKAN ANALISIS RAPD (Random Amplified Polymorphic DNA)
DAN KARAKTER MORFOMETRIK
adalah benar merupakan hasil karya yang belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, November 2011
PEMBARUAN SIREGAR C14070074
Judul Skripsi : Hubungan 3 populasi ikan betok (Anabas testudineus) berdasarkan
analisis RAPD (Random AmplifiedPolymorphic DNA) dan
karakter morfometrik
Nama Mahasiswa : Pembaruan Siregar
Nomor Pokok : C14070074
Disetujui
Pembimbing I Pembimbing II
Dr.Ir.Dinar Tri Soelistyowati, DEA Dr.Ir.Rudhy Gustiano, M.Sc
NIP. 19611016 198403 2 001 NIP. 19610803 198903 1 006
Diketahui
Kepala Departemen Budidaya Perairan
Dr.Ir.Odang Carman, M.Sc NIP. 19591222 198601 1 001
DAFTAR RIWAYAT HIDUP
Penulis dilahirkan di Pandan, Tapanuli Tengah, Sumatera Utara tanggal 17
September 1989 dari Bapak MP. Siregar dan Ibu R. Manalu. Penulis merupakan anak
keempat dari lima bersaudara.
Pendidikan formal yang dilalui penulis adalah SD Negeri 158466 Aksara Indah,
Pandan, dan lulus pada tahun 2001, SMP Swasta St. Fransiskus, Aek Tolang, dan
lulus pada tahun 2004, kemudian SMA Swasta Tri Ratna, Sibolga dan lulus pada
tahun 2007. Pada tahun yang sama Penulis lulus seleksi masuk IPB melalui jalur
Seleksi Penerimaan Mahasiswa Baru (SPMB) dan memilih Program Studi Teknologi
dan Manajemen Perikanan Budidaya, Departemen Budidaya Perairan, Fakultas
Perikanan dan Ilmu Kelautan.
Selama mengikuti perkuliahan, penulis pernah magang di PT Semata,
Tasikmalaya. Penulis juga merupakan anggota dari Komisi Kesenian Persekutuan
Mahasiswa Kristen Institut Pertanian Bogor. Tugas akhir dalam pendidikan tinggi
diselesaikan dengan menulis skripsi yang berjudul “Hubungan 3 populasi ikan
betok (Anabas testudineus) berdasarkan analisis RAPD (Random Amplified
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan Yesus atas segala karunia dan
berkat-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam
penelitian yang dilaksanakan sejak bulan Agustus 2011 s.d September 2011 adalah
pengembangbiakan genetik ikan dengan judul Hubungan 3 populasi ikan betok
(Anabas testudineus) berdasarkan analisis RAPD (Random Amplified Polymorphic
DNA) dan karakter morfometrik.
Dalam kesempatan ini, penulis mengucapkan terimakasih kepada :
1. Ibu Dr.Ir.Dinar Tri Soelistyowati, DEA dan Bapak Dr.Ir.Rudhy Gustiano,
M.Sc sebagai dosen pembimbing yang telah banyak memberikan bimbingan,
arahan dan nasehat.
2. Ibu Iskandariah, Bang Glen, Bang Farid, Ibu Kusdiarti, Kak Vera yang telah
banyak membantu penulis selama penelitian.
3. Balai Riset Perikanan Budidaya Air Tawar, Sempur Bogor atas bantuannya
selama penelitian berlangsung
4. Intan dan Nova selaku teman seperjuangan penulis selama penelitian
5. Keluarga ku yang terkasih, Bapak, Mama, kak Gelora, bang Putra, bang
Tama, dek Mora dan Christini RA Lubis yang selalu memberikan doa,
dukungan dan semangat kepada penulis
6. Seluruh dosen serta staf karyawan Departemen Budidaya Perairan serta
Fakultas Perikanan dan Ilmu Kelautan atas bantuannya
7. Teman-teman terkasih di BDP 44, Baskom, dan Pondok Iona atas dukungan
dan doanya, serta semua pihak yang telah membantu dalam penulisan skripsi.
Semoga karya ilmiah ini bermanfaat.
Bogor, 24 November 2011
i
DAFTAR ISI
Halaman DAFTAR TABEL ... ii
DAFTAR GAMBAR... iii
DAFTAR LAMPIRAN... iv
I. PENDAHULUAN... 1 1.1 Latar Belakang... 1 1.2 Tujuan... 2
II. BAHAN DAN METODE... 3 2.1 Waktu dan Lokasi Penelitian ... 3 2.2 Materi Uji... ... 3 2.3 Metode Kerja... ... 4 2.3.1 Ekstraksi DNA... 4
2.3.2 Amplifikasi DNA dengan teknik PCR... 4
2.3.3 Elektroforesis... ... 5 2.3.4 Karakterisasi fenotip morfometrik... 5 2.4 Analisis data... 7
III. HASIL DAN PEMBAHASAN ... 8 3.1 Hasil... 8 3.1.1 Profil RAPD... 8 3.1.2 Polimorfisme... 9 3.1.3 Heterozigositas... ... 10 3.1.4 Uji perbandingan Fst... 10 3.1.5 Jarak genetik... 11
3.1.6 Karakter morfometrik... 12
3.1.7 Uji signifikansi... 13
3.1.8 Canonical discriminant function... 14
3.1.9 Indeks kesamaan……... 15
3.2.0 Dendrogram penyebaran morfometrik... 15
3.2 Pembahasan... 16
IV. KESIMPULAN DAN SARAN... 20 4.1 Kesimpulan... 20 4.2 Saran... 20
DAFTAR PUSTAKA ... 21
ii
DAFTAR TABEL
Halaman
1. Sekuen primer RAPD yang diuji... 5
2. Karakteristik morfometrik... 6
3. Jumlah fragmen dan ukuran fragmen 3 populasi ikan betok... 9
4. Persentase polimorfisme 3 populasi ikan betok... 10
5. Nilai heterozigositas 3 populasi ikan betok... 10
6. Nilai uji perbandingan berpasangan Fst 3 populasi ikan betok... 10
7. Jarak genetik 3 populasi ikan betok... 11
8. Rata rata 21 karakter morfometrik (cm) 3 populasi ikan betok... 12
9. Uji signifikansi 21 karakter morfometrik 3 populasi ikan betok... 13
10. Indeks kemiripan (sharing components) morfometrik (%)... 15
iii
DAFTAR GAMBAR
Halaman
1. Ikan betok (Anabas testudineus)... 3
2. Ikan betok beserta skema karakteristik morfometriknya... 5
3. Amplifikasi OPA-02 pada ikan betok Jawa, Sumatera, dan Kalimantan... 8
4. Amplifikasi OPC-02 pada ikan betok Jawa, Sumatera, dan Kalimantan... 8
5. Amplifikasi OPC-05 pada ikan betok Jawa, Sumatera, dan Kalimantan... 9
6. Dendrogram hubungan genetik 3 populasi ikan betok... 11
7. Peta kanonikal 3 populasi ikan betok... 14
8. Dendrogram hubungan morfometrik 3 populasi ikan betok ... 15
iv
DAFTAR LAMPIRAN
Halaman
1. Amplifikasi DNA pada 3 populasi ikan betok... 24
2. Uraian statistik... 25
3. Pengukuran 21 karakter morfometrik ikan betok Jawa, Sumatera, dan
Kalimantan (cm)... 40
4. Koefisien keragaman morfometrik 3 populasi ikan betok... 41
1
I. PENDAHULUAN
1.1. Latar Belakang
Betok merupakan spesies ikan air tawar yang hidup liar di perairan tawar, payau, dan rawa. Pada umumnya berukuran kecil, panjang maksimal sekitar 25 cm, bersisik keras kaku, sisi atas tubuh (dorsal) gelap kehitaman agak kecoklatan atau kehijauan, sisi samping (lateral) kekuningan, terutama di sebelah bawah, dengan garis-garis gelap melintang yang samar dan tak beraturan, sisi belakang tutup insang bergerigi tajam seperti duri, dan berkepala besar (Anonim, 2011). Ikan betok dikenal dengan nama bethok atau bethik, puyu, pepuyu. Ikan betok dikenal juga sebagai climbing gouramy atau climbing perch, karena kemampuannya memanjat ke daratan. Nama ilmiahnya adalah Anabas testudineus. Distribusi populasi ikan betok (Anabas testudineus) yang hidup di air
tawar mulai langka. Pemangsa serangga yang juga menjadi musuh alami wereng ini makin susah ditemukan dalam ukuran besar. Berikut klasifikasi ilmiah ikan betok pada umumnya.
Suhu yang sesuai sebagai syarat hidup ikan betok adalah 15 – 31°C . Ikan betok merupakan ikan penghuni asli Asia Tenggara, India, Srilanka, Taiwan, Bangladesh, Afrika, Hindia Timur, Indo-Cina dan Cina bagian selatan serta menjadi ikan introduksi untuk Papua (daerah Merauke), kemudian menyebar ke arah timur Papua New Guinea (www.fishbase.org)
Klasifikasi ilmiah : Kerajaan : Animalia Filum : Chordata Kelas : Actinopterygii Ordo : Perciformes Famili : Anabantidae Genus : Anabas
Spesies : Anabas testudineus
2
Ikan ini mempunyai naluri yang kuat untuk mendeteksi di mana keberadaan sumber air. Banyak orang yang menyebutnya ikan gaib karena ikan ini dapat dengan cepat menghilang padahal ikan ini hanya kabur dari air dengan cara berjalan di darat (merayap). Saat berjalan ikan ini merayap dengan tutup insang sebagai kaki depannya, selain itu ikan ini mempunyai daya tahan kuat.
Ikan betok liar di Kalimantan, semula bisa mencapai sampai bobot 250 gram. Kini ikan betok hanya berbobot 70-100 gram per ekor dengan kisaran harga Rp 40.000-Rp 70.000 per kilogram. Selain itu produksi tangkapan ikan betok di provinsi Kalimantan Timur antara tahun 2002-2008 mengalami peningkatan tiap tahunnya yaitu 91 ton pada tahun 2004 menjadi 1505 ton pada tahun 2005 (DKP, 2006 dalam Pellokila, 2009). Semakin meningkatnya penangkapan terhadap ikan ini menimbulkan kekhawatiran akan menurunnya populasi ikan ini di kemudian hari. Berdasarkan hal tersebut maka pengelolaan perikanan berkelanjutan perlu secepatnya dilakukan untuk mencegah terjadinya penurunan populasi ikan betok. Beberapa informasi dasar dibutuhkan dalam upaya pengelolaan yaitu kajian mengenai informasi karakteristik genotip dan fenotipnya. Identifikasi genotip dapat dilakukan dengan beberapa teknik, diantaranya adalah Random Amplified Polymorphic DNA (RAPD) dengan teknik PCR (Polymerase Chain Reaction)
(Muladno, 2002). Sedangkan identifikasi fenotip dapat dilakukan dengan analisis karakter morfometrik.
1.2. Tujuan
3
II. BAHAN DAN METODE
2.1. Waktu dan Lokasi Penelitian
Penelitian ini dilaksanakan dari bulan Agustus sampai September tahun 2011. Sampel ikan berasal dari 3 lokasi yaitu Jawa (Jawa Barat), Sumatera (Jambi), dan Kalimantan (Kalimantan Tengah). Analisa genetik ikan dilakukan di Laboratorium Genetik Ikan, Balai Riset Perikanan Budidaya Air Tawar, Sempur, Bogor, sedangkan pengukuran karakter morfometrik dilakukan di Instalasi Riset Plasma Nutfah, Cijeruk, Bogor.
2.2. Materi Uji
Sampel ikan betok berasal dari 3 lokasi, yaitu dari Kalimantan Tengah (Pulang Pisau), Jawa Barat (Tasikmalaya), dan Sumatera (Jambi), masing masing 10 ekor. Kondisi lingkungan di lokasi sampling adalah perairan rawa (Kalimantan Tengah) dan kolam budidaya air tawar ( Jawa Barat dan Sumatera). Sampel ikan diambil siripnya dan dilarutkan dalam larutan alkohol 70%-90% untuk mengawetkan sirip ikan, selanjutnya dilakukan analisis DNA dengan teknik PCR. Untuk pengukuran karakter morfometrik, diambil masing masing 10 ekor dari populasi dan dihitung panjang yang mencakup seluruh bagian luar tubuh.
Gambar 1. Ikan betok (Anabas testudineus)
4
2.3. Metode Kerja
Profil genotip ikan dianalisis menggunakan metode RAPD yang diawali dengan proses ekstraksi DNA genom, amplifikasi DNA menggunakan teknik PCR dan elektroforesis. Sedangkan profil fenotip ikan betok dianalisis menggunakan metode pengukuran karakter morfometrik.
2.3.1. Ekstraksi DNA
Sampel ikan berupa sirip dorsal ditimbang sebanyak 5-10 mg dan dimasukan ke dalam tabung eppendorf 1,5 ml, kemudian dilisis dengan menambahkan TNES urea sebanyak 500 µl dan protein kinase 10 µl. Setelah itu dikocok menggunakan alat vortex dan diinkubasi pada suhu 37°C selama 24 jam atau sampai sirip hancur. Selanjutnya ditambahkan larutan phenolchloroform isoamilalkohol (PCL) dengan perbandingan 25:24:1 sebanyak 1000 µl dan disentrifuse dengan menggunakan kecepatan 10.000 rpm selama 10 menit. Supernatan lalu dipindahkan ke tabung baru dan ditambahkan etanol 90% sebanyak 1000 µl dan Na asetat sebanyak 10 µl lalu disentrifugasi pada kecepatan 10.000 rpm selama 10 menit. Supernatan dibuang dan pellet dikering anginkan sampai etanol menguap. DNA dilarutkan dengan menambahkan rehydration solution sebanyak 100 µl.
2.3.2. Amplifikasi DNA dengan teknik PCR
Sebelum amplifikasi DNA, maka dilakukan terlebih dahulu seleksi primer untuk mendapatkan jenis primer yang sesuai. Amplifikasi DNA dilakukan menggunakan metode PCR dengan komposisi bahan 1 unit dry taq produk Promega, 2 µl DNA template, 2 µl primer dan 21 µl air dengan volume total sebanyak 25 µl. Lalu dimasukkan ke dalam mesin PCR dengan 35 siklus, yaitu denaturasi awal pada 94°C selama 2 menit, denaturasi 94°C selama 1 menit. annealing 36°C selama 1 menit, elongasi 72°C selama 2 menit 30 detik, elongasi
5
Tabel 1. Sekuen primer RAPD yang diuji
No Primer Sekuen Nukleotida (5’Æ3’)
1 OPA-02 TGCCGAGCTG
2 OPC-02 GTGAGGCGTC
3 OPC-05 GATGACCGCC
Keterangan : T = deoksi Timidin 5’- monofosfat G = deoksi Guanosin 5’- monofosfat C = deoksi Sitidin 5’- monofosfat A = deoksi Adenosin 5’- monofosfat
2.3.3. Elektroforesis
Untuk mengetahui keberhasilan amplifikasi primer yang digunakan, campuran 9 µl hasil PCR dengan 2 µl loading die dielektroforesis pada gel agarose 2% (w/v) dalam larutan TBE dan tegangan 100 volt selama 30 menit. Kemudian, gel direndam agar pita DNA nya dapat terlihat pada cahaya ultraviolet. Selanjutnya, digunakan kamera untuk keperluan dokumentasi. Gene ruler 100bp DNA loader digunakan sebagai standar untuk menentukan ukuran fragmen hasil
amplifikasi.
2.3.4. Karakterisasi fenotip morfometrik
Ikan betok yang berasal dari Kalimantan Tengah, Jawa Barat, dan Jambi diambil dari akuarium masing masing 10 ekor. Metode karakteristik morfometrik dilakukan dengan cara mengukur jarak titik-titik tanda yang akan dibuat pada kerangka tubuh (Gambar 2). Skema dan 21 karakteristik morfometrik ikan betok dapat dilihat pada Gambar 2 dan Tabel 2 ( Brzesky and Doyle, 1988)
[image:38.595.125.507.569.718.2]6
Tabel 2. Karakteristik morfometrik
No Kode Deskripsi Jarak
1 A1-2 Bawah mulut-ujung bagian atas insang 2 A1-3 Bawah mulut-operkulum
3 A1-4 Bawah mulut-awal sirip punggung 4 A1-5 Bawah mulut-awal sirip perut 5 A2-3 Ujung atas insang-operkulum
6 A2-4 Ujung atas insang-awal sirip punggung 7 A2-5 Ujung atas insang-awal sirip perut 8 A3-4 Operkulum-awal sirip punggung 9 A3-5 Operkulum-awal sirip perut
10 A4-5 Awal sirip punggung-awal sirip perut 11 B5-6 Awal sirip perut-awal sirip anal 12 B5-7 Awal sirip perut-akhir sirip anal 13 B6-4 Awal sirip anal-awal sirip punggung 14 B10-4 Akhir sirip punggung-awal sirip punggung 15 B10-6 Akhir sirip punggung-awal sirip anal 16 C7-8 Awal sirip ekor bawah-awal sirip ekor atas 17 C7-9 Awal sirip ekor bawah-akhir sirip ekor atas 18 C8-9 Akhir sirip ekor bawah-akhir sirip ekor atas 19 C10-7 Akhir sirip punggung-awal sirip ekor bawah 20 C10-8 Akhir sirip punggung-akhir sirip ekor bawah 21 C10-9 Awal sirip punggung-awal sirip ekor atas
Keterangan : A = bagian kepala 1-2, dst = jarak antar titik karakter B = bagian seluruh tubuh
C = bagian ekor
7
2.4. Analisis Data
Keragaman genetik yang meliputi tingkat polimorfisme, heterozigositas, uji perbandingan Fst dianalisa dengan descriptive statistics (Miller, 1997), exact test for population differentiation (Raymond & Rousset, 1995 dalam Miller, 1997)
dengan menggunakan program TFPGA (Tools for Population Genetic Analyses). Kekerabatan antar populasi berdasarkan jarak genetik yang disertai dengan dendrogram dianalisis menggunakan UPGMA (Unweighted Pair Group Method with Arithmetic Mean) Wright (1978) modifikasi Rogers (1972) dalam Miller
8
III. HASIL DAN PEMBAHASAN
3.1. Hasil
3.1.1. Profil RAPD
[image:41.595.108.552.79.806.2]Keragaman profil penanda DNA meliputi jumlah dan ukuran fragmen DNA. Hasil amplifikasi dengan menggunakan primer OPA-02, OPC-02, OPC-05 selengkapnya disajikan pada Tabel 3. Amplifikasi DNA pada 3 populasi dapat dilihat pada Gambar 3-5. Profil DNA teramplifikasi dengan primer OPA-02, OPC-02, OPC-05 selengkapnya disajikan pada Lampiran 1.
Gambar 3. Amplifikasi OPA-02 pada ikan betok Jawa, Sumatera, dan Kalimantan
1
2
3
1
2
3
1
2
3
M
3000 bp
1000 bp
500 bp
Jawa Sumatera Kalimantan
4
5
6
4
5
6
4
5
6
M
Jawa
Gambar 4. Amplifikasi OPC-02 pada ikan betok Jawa, Sumatera, dan Kalimantan. 500 bp 1000 bp 3000 bp
9
Gambar 5. Amplifikasi OPC-05 pada ikan betok Jawa, Sumatera, dan Kalimantan.
Tabel 3. Jumlah fragmen dan ukuran fragmen 3 populasi ikan betok
Populasi Betok Jumlah Fragmen Kisaran Ukuran Fragmen (bp)
Jawa 24-26 100-2000
Sumatera 23-27 100-2000
Kalimantan 18-20 275-1750
Jumlah fragmen teramplifikasi berkisar antara 18-27 pada kisaran 100-2000 bp. Jumlah fragmen terbanyak adalah populasi ikan betok Sumatera dengan kisaran 100-2000 bp. Sedangkan kisaran terendah adalah populasi ikan betok Kalimantan yaitu 275-1750 bp.
3.1.2. Polimorfisme
Tingkat keragaman genetik populasi meliputi derajat polimorfisme dan heterozigositas (Lampiran 2). Polimorfisme memberikan gambaran mengenai tingkat keragaman suatu populasi (Yuwono, 2006). Perbedaan jumlah dan polimorfisme pita DNA yang dihasilkan setiap primer menggambarkan keunikan genom yang diamati. Pita DNA hasil amplifikasi merupakan pasangan antara nukleotida primer dengan nukleotida sampel. Panjang ukuran fragmen pita DNA yang dihasilkan setelah amplifikasi berkisar 100 sampai 2000 bp (base pairs).
1
2
3
1
2
3
1
2
3
M
Jawa Sumatera Kalimantan
3000 bp
[image:42.595.108.557.97.357.2]10
Tabel 4. Persentase polimorfisme 3 populasi ikan betok
Populasi Betok Polimorfisme (%)
Jawa 18.52 Sumatera 22.22 Kalimantan 25.93
Persentase polimorfisme berkisar antara 18,52% sampai 25,93%. Persentase polimorfisme tertinggi adalah populasi ikan betok Kalimantan yaitu sebesar 25,93%, sedangkan polimorfisme terendah adalah populasi ikan betok Jawa yaitu sebesar 18,52%.
3.1.3. Heterozigositas
Heterozigositas tiap populasi disajikan dalam Tabel 5 berikut:
Tabel 5. Nilai heterozigositas 3 populasi ikan betok
Populasi Betok Heterozigositas
Jawa 0,088
Sumatera 0,095
Kalimantan 0,109
Nilai rata rata heterozigositas terendah dimiliki ikan betok dari populasi Jawa yaitu sebesar 0,088, sedangkan heterozigositas ikan betok tertinggi adalah populasi ikan betok dari Kalimantan yaitu sebesar 0,109.
3.1.4. Uji perbandingan Fst
Secara statistik dengan menggunakan uji perbandingan Fst, menunjukkan ada perbedaan genetik secara nyata antara populasi ikan betok Kalimantan terhadap populasi betok Jawa dan Sumatera.
Tabel 6. Nilai uji perbandingan berpasangan Fst 3 populasi ikan betok
Populasi Betok Jawa Sumatera Kalimantan Jawa *****
Sumatera 0,9986ns *****
Kalimantan 0,0000 0,0000 *****
11
Berdasarkan Tabel 6 diatas dapat diketahui bahwa antara populasi ikan betok Kalimantan dengan Jawa dan Sumatera berbeda nyata. Sedangkan ikan betok Jawa dan Sumatera tidak berbeda nyata.
3.1.5. Jarak genetik
[image:44.595.83.521.232.818.2]Pada Tabel 7 di bawah ini disajikan jarak genetik masing masing populasi ikan betok dari tiap tiap populasi.
Tabel 7. Jarak genetik 3 populasi ikan betok
Populasi Betok Jawa Sumatera Kalimantan Jawa *****
Sumatera 0,279 *****
Kalimantan 0,551 0,398 *****
Jarak genetik 3 populasi berkisar antara 0,279 sampai 0,551. Hubungan kekerabatan interpopulasi 3 populasi ikan betok dapat digambarkan dalam bentuk dendrogram. Dendrogram yang ditampilkan merupakan hasil analisis dengan menggunakan program TFPGA pada analisis UPGMA.
Berdasarkan dendrogram (Gambar 6) digambarkan bahwa hubungan kekerabatan genetik paling dekat adalah populasi ikan betok Jawa dengan
Gambar 6. Dendrogram hubungan genetik 3 populasi ikan betok
Jawa
Sumatera
12
populasi ikan betok Sumatera, yaitu sebesar 0,279 dan yang paling jauh adalah populasi ikan betok Kalimantan dengan populasi ikan betok Jawa.
3.1.6. Karakter morfometrik
[image:45.595.95.474.150.786.2]Pengukuran karakter morfometrik dilakukan terhadap 21 karakter pada ikan betok Jawa, Sumatera, dan Kalimantan (Lampiran 3). Rata rata karakter morfometrik disajikan dalam Tabel 8 berikut.
Tabel 8. Rata rata 21 karakter morfometrik (cm) 3 populasi ikan betok
Karakter yang
13
3.1.7. Uji signifikansi
[image:46.595.110.499.261.708.2]Uji signifikansi dilakukan untuk mengetahui karakter yang dapat digunakan sebagai penciri dari suatu jenis ikan. Berdasarkan hasil penelitian, bahwa 21 karakter yang diuji, 18 karakter tidak berbeda nyata (P>0,05) dan 3 karakter berbeda nyata (P<0,05) yaitu karakter B5-7 (awal sirip perut-akhir sirip anal), B10-6 (akhir sirip punggung-awal sirip anal) dan C8-9 (awal sirip ekor atas-awal sirip ekor bawah)
Tabel 9. Uji signifikansi 21 karakter morfometrik 3 populasi ikan betok Karakter yang
diuji
Wilks'
Lambda F df1 df2 Sig.
A1-2 0,832 2,732 2 27 0,083
A1-4 0,846 2,457 2 27 0,105
A2-3 0,963 0,514 2 27 0,604
A1-5 0,912 1,309 2 27 0,287
A1-3 0,897 1,554 2 27 0,230
A4-5 0,990 0,132 2 27 0,877
A2-5 0,917 1,219 2 27 0,311
A3-5 0,972 0,387 2 27 0,683
A3-4 0,821 2,946 2 27 0,070
A2-4 0,853 2,322 2 27 0,117
B10-4 0,914 1,277 2 27 0,295
B6-4 0,982 0,248 2 27 0,782
B5-7 0,781 3,786 2 27 0,036*
B5-6 0,925 1,093 2 27 0,350
B10-6 0,706 5,635 2 27 0,009*
C10-9 0,874 1,941 2 27 0,163
C10-7 0,942 0,837 2 27 0,444
C7-8 0,974 0,353 2 27 0,706
C8-9 0,761 4,232 2 27 0,025*
C10-8 0,893 1,613 2 27 0,218
14
3.1.8. Canonical discriminant function
[image:47.595.74.529.92.791.2]Hasil analisis fungsi kanonikal (Gambar 7) memperlihatkan bahwa karakter morfologi ikan betok Jawa dan ikan betok Sumatera tidak bersinggungan dengan ikan betok Kalimantan. Karakter morfometrik ikan betok Jawa berada di kuadran 1. Sedangkan karakter morfometrik ikan betok Sumatera dan betok Kalimantan berada di kuadran 3 dan 4. Persinggungan yang terjadi antara ikan betok Jawa dan Sumatera menunjukkan adanya pencampuran diantara kedua populasi tersebut. Karakter ikan betok Jawa dan Sumatera hanya sedikit yang bersinggungan, sedangkan ikan betok Kalimantan sama sekali tidak bersinggungan dengan ikan betok Jawa dan betok Sumatera
Gambar 7. Peta kanonikal 3 populasi ikan betok Kuadran 1
15
3.1.9. Indeks kemiripan
Analisis kemiripan populasi berdasarkan karakter morfometrik (Tabel 10) menunjukkan tingkat homogenitas 100% pada populasi Sumatera dan Kalimantan, sedangkan karakter morfometrik populasi ikan betok Jawa memiliki indeks kemiripan dengan populasi ikan betok Sumatera sebesar 10% .
Tabel 10. Indeks kemiripan (sharing components) morfometrik (%)
Jawa Sumatera Kalimantan Total
Jawa 90,0 10,0 0,0 100,0
Sumatera 0,0 100,0 0,0 100,0 Kalimantan 0,0 0,0 100,0 100,0
3.2.0. Dendrogram penyebaran morfometrik
Analisis dendrogram karakter morfometrik ketiga populasi ikan betok menunjukkan kemiripan antara populasi Jawa dan Sumatera (Gambar 8).
16
3.2. Pembahasan
17
sesuai dengan kondisi alami populasi ikan betok di Kalimantan diduga menjadi penyebab terjadinya genetic drift karena beberapa populasi diduga terperangkap dalam area yang tertutup (sistem budidaya) sehingga mengakibatkan rendahnya variasi gen. Pengujian Fst keragaman genetik antar populasi menunjukkan perbedaan yang nyata antara populasi ikan betok Kalimantan dengan Sumatera dan Jawa. Sedangkan antara populasi ikan betok Sumatera dan ikan betok Jawa menunjukkan kesamaan populasi atau mencerminkan distribusi unsur genetik yang sama.
Keragaman genetik mempengaruhi kemampuan spesies untuk merespon perubahan lingkungan baik buatan maupun alami dalam proses adaptasi agar bertahan hidup. Setiap kombinasi gen memiliki respons yang berbeda terhadap perubahan lingkungan, dalam hal ini keberagaman gen memberikan peluang yang lebih baik untuk dapat merespon perubahan lingkungan tersebut. Reduksi variasi genetik yang berlangsung dalam waktu lama dapat mengarah pada penurunan produktifitas populasi yang berdampak pada penurunan profit. Untuk mengatasi hal tersebut perlu dilakukan revitalisasi stok induk dengan mengintroduksi ragam genetik di lingkungan budidaya maupun restocking di perairan umum (Tave, 1983)
Hubungan kekerabatan antar populasi yang digambarkan menurut jarak genetik menunjukkan bahwa semakin kecil jarak genetik maka semakin tinggi kemiripan populasi tersebut, dan sebaliknya. Jarak genetik antara ketiga populasi ikan betok berkisar antara 0,279-0,551 yang menunjukkan bahwa ikan betok Jawa dengan Sumatera memiliki kemiripan yang lebih tinggi dibandingkan dengan populasi dari Kalimantan. Selain itu, lingkungan perairan rawa di Kalimantan diduga mempengaruhi perbedaan variasi genetik tersebut terkait dengan parameter kualitas air, terutama alkalinitas dan pH yang lebih rendah dibandingkan dengan perairan lingkungan budidaya di Jawa dan Sumatera (Pellokila, 2009)
18
ovipar, memijah sepanjang tahun dengan puncak pemijahannya pada musim penghujan (musim banjir) di tepi tumbuhan air. Puncak pemijahan terjadi pada bulan Oktober-Desember, dengan telur telur mengapung bebas (egg layer). Suhu air yang cocok untuk pemijahan ikan betok adalah 28°C dengan pH 7. Pada musim kemarau, ikan ini membenamkan diri ke dalam lumpur dan muncul kembali saat musim penghujan (Pellokila, 2009). Selain itu, di perairan rawa, fluktuasi air tinggi dalam setahun sangat besar, hal ini terkait dengan siklus hidrologi. Akibat adanya peningkatan kedalaman dan penggenangan daratan, habitat berkembang sangat luas. Semakin luas habitat, semakin beragam pula sebaran makhluk hidup yang hidup di dalamnya karena semakin beragam pula ketersediaan makanan yang terdapat di sana. Hal ini sesuai dengan tangkapan ikan betok yang diperoleh (Setiadi dan Dewi 1989). Hasil tangkapan terbanyak terdapat pada bulan Desember saat kedalaman air tinggi. Pada populasi ikan betok dari Kalimantan, perubahan kondisi lingkungan diduga juga dipengaruhi oleh kerusakan lingkungan seperti kerusakan hutan, penebangan hutan bakau dan pencemaran lingkungan, sehingga mengakibatkan penurunan kualitas air yang berdampak pada semakin kritisnya peluang hidup ikan betok, dan memperkecil adanya migrasi maupun interaksi dengan populasi ikan betok dari tempat lain (Christanty, 2009)
19
lama, maka kemampuannya untuk bertahan hidup menjadi bergantung pada kelengkapan keragaman genetiknya dengan munculnya genotip-genotip baru yang memiliki toleransi baru sehingga memungkinkan spesies tersebut untuk bertahan hidup dan mengembangkan jenisnya (Stansfield, 1991)
Keragaman morfometrik ikan betok Kalimantan lebih rendah dibandingkan dengan populasi betok Jawa dan Sumatera. Berdasarkan uji signifikansi karakter morfometrik diketahui 3 fenotip, yaitu karakter B5-7 (awal sirip perut-akhir sirip anal), B10-6 (akhir sirip punggung-awal sirip anal) dan C8-9 (awal sirip ekor atas-awal sirip ekor bawah), menunjukkan perbedaan populasi betok Kalimantan dengan populasi Jawa dan Sumatera. Dalam hal ini, 18 karakter yang tidak berbeda nyata dapat digunakan sebagai penciri jenis ikan betok. Perbedaan habitat masing masing populasi dapat menjadi penyebab adanya perbedaan pada ketiga karakter tersebut. Selain perbedaan habitat, faktor ragam lingkungan seperti pakan, kepadatan populasi, ukuran dan umur induk, ukuran telur, dan teknik pendederan juga dapat mempengaruhi (Alawi et al, 2006).
20
IV. KESIMPULAN DAN SARAN
4.1. Kesimpulan
Populasi ikan betok dari Kalimantan memiliki tingkat polimorfisme yang paling tinggi (25,92%) dan hubungan kekerabatan genetik yang paling jauh terhadap populasi ikan betok dari Jawa (0,551) dan Sumatera (0,398). Karakter morfometrik populasi ikan betok Jawa memiliki indeks kemiripan dengan populasi ikan betok Sumatera sebesar 10%.
4.2. Saran
21
DAFTAR PUSTAKA
Alawi H, Nuraini, Sukendi. 2006. Genetika dan Pemuliaan Ikan. Uni Press. Pekanbaru.
[Anonim]. 2011. Ikan Betok .www.wikipedia.com [7 Agustus 2011].
[Anonim]. 2011. Ilmuwan IPB Rekayasa Genetik Ikan Betok. www.kompas.com [5 Agustus 2011].
Brzesky VJ, Doyle RW. 1988. A morphometric criterion for sex discrimination in tilapia. In Pullin, R.S.V., T. Bukaswan, K. Tonguthai, and J.L. Maclan (Eds.). The Second ISTA, Bangkok, Thailand. ICLARM Conf. Proc. 15:439-444.
Christanty L. 2009. Sumber Daya Alam : Ciptaan Tuhan Yang Harus Dilestarikan. Coremap II-LIPI. Jakarta.
Kurniawirawan A. 2007. Analisis Keragaman Genetik Beberapa Populasi Ikan Batak (Tor soro) dengan Metode Random Amplified Polymorphism DNA (RAPD) [Skripsi]. Jurusan Manajemen Sumberdaya Perairan. Fakultas Perikanan dan Ilmu Kelautan. Institut Pertanian Bogor.
Miller MP. 1997. A Windows Program for the Analysis of Allozym and Molecular Population Genetic Data. Departmen of Biological Sciences Northern Arizona University Box 5640 Flagstaff, AZ 86011-5640.
Muladno. 2002. Seputar Teknologi Rekayasa Genetik. Pustaka Wirausaha Muda. Bogor.
Pellokila NAY. 2009. Biologi Reproduksi Ikan Betok (Anabas testudineus Bloch, 1792) di Rawa Banjiran Das Mahakam, Kalimantan Timur. [Skripsi]. Departemen Manajemen Sumberdaya Perairan, Institut Pertanian Bogor. Bogor.
Raymond ML, Rousset F. 1995. An exact test for population differentiation. Evolution 49: 1280-1283.
Rogers JS. 1972. Measures of genetic similarity and genetic distance. p. 145-154 in "Studies in Genetics VII". University of Texas Publication no. 7213, Austin.
22
Soewardi K. 2007. Pengelolaan Keragaman Genetik Sumberdaya Perikanan dan Kelautan.Departemen Manajemen Sumberdaya Perairan Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor. Bogor.
Stansfield WD. 1991. Genetika Edisi Kedua. Penerbit Erlangga, Jakarta.
Tave D. 1983. Genetics for Fish Managers. The AVI Publ. Comp. Inc. NY, USA.418. pp.
Wright S. 1978. Evolution and the Genetics of Populations, vol. 4. Variability Within and Among Natural Populations. University of Chicago Press, Chicago.
www.fishbase.org. Anabas testudineus Bloch 1792. [terhubung berkala]. www. Fishbase.com/PopDyn/PopCharList.php?ID=495&GenusName=Anabas&S peciesName=testudineus&fc=426. [14 November 2011].
23
24
Lampiran 1. Amplifikasi DNA pada 3 populasi ikan betok
Amplifikasi OPA-02 sampel ke 4,5,6 pada ikan betok Jawa,
Sumatera, Kalimantan
Amplifikasi OPA-02 sampel ke 7,8,9 pada ikan betok Jawa,
Sumatera, Kalimantan
Amplifikasi OPC-02 sampel ke 1,2,3 pada ikan betok Jawa,
Sumatera, Kalimantan
Amplifikasi OPC-02 sampel ke 7,8,9 pada ikan betok Jawa,
Sumatera, Kalimantan
Amplifikasi OPC-05 sampel ke 4,5,6 pada ikan betok Jawa,
Sumatera, Kalimantan
Amplifikasi OPC-05 sampel ke 7,8,9 pada ikan betok Jawa,
25
Lampiran 2. Uraian statistik
9/12/2011 4:47:15 AM
Analysis of C:\TFPGA\BETOK.DAT
Data set contains genotypes of individuals sampled from populations. Organism Type: Diploid
Marker Type: Dominant H-W Equilibrium Assumed.
Allele frequencies estimated based on the square root of the frequency of the null (recessive) genotype. DESCRIPTIVE STATISTICS
******************************************************** RESULTS FOR EACH POPULATION.
POPULATION 1
Locus 1 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 2 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
26
Locus 3 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 4 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.000
Locus 5 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 7 0.4523 4.9545 0.4954 2 3 0.5477 4.9545 0.4954 Heterozygosity: 0.4954
Heterozygosity (unbiased): 0.5215 Heterozygosity (direct count): 0.4954
Locus 6 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 7 0.4523 4.9545 0.4954 2 3 0.5477 4.9545 0.4954 Heterozygosity: 0.4954
Heterozygosity (unbiased): 0.5215 Heterozygosity (direct count): 0.4954
Locus 7 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 8 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
27
Locus 9 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 10 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 11 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 12 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 13 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 14 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
28
Locus 15 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 16 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 17 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 4 0.2254 3.4919 0.3492 2 6 0.7746 3.4919 0.3492 Heterozygosity: 0.3492
Heterozygosity (unbiased): 0.3676 Heterozygosity (direct count): 0.3492
Locus 18 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 19 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 20 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
29
Locus 21 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 22 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 8 0.5528 4.9443 0.4944 2 2 0.4472 4.9443 0.4944 Heterozygosity: 0.4944
Heterozygosity (unbiased): 0.5204 Heterozygosity (direct count): 0.4944
Locus 23 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 9 0.6838 4.3246 0.4325 2 1 0.3162 4.3246 0.4325 Heterozygosity: 0.4325
Heterozygosity (unbiased): 0.4552 Heterozygosity (direct count): 0.4325
Locus 24 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 25 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 26 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
30
Locus 27 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
--- Results over all loci
Ave. sample size: 10.0000 Ave. heterozygosity: 0.0840
Ave. heterozygosity (unbiased): 0.0884 Ave. heterozygosity (direct count): 0.0840 % polymorphic loci (no criterion): 18.5185 % polymorphic loci (99% criterion): 18.5185 % polymorphic loci (95% criterion): 18.518 POPULATION 2
Locus 1 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 9 0.6838 4.3246 0.4325 2 1 0.3162 4.3246 0.4325 Heterozygosity: 0.4325
Heterozygosity (unbiased): 0.4552 Heterozygosity (direct count): 0.4325
Locus 2 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 3 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 4 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
31
Locus 5 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000
Locus 6 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct count): 0.0000 Locus 7 # obs. at locus= 10
allele: # obs: allele freq: # hets: het freq: 1 10 1.0000 0.0000 0.0000 2 0 0.0000 0.0000 0.0000 Heterozygosity: 0.0000
Heterozygosity (unbiased): 0.0000 Heterozygosity (direct co