(Azadirachtaindica A.Juss) SEBAGAI LARVISIDA
TERHADAP NYAMUK Aedes aegypti
ARIEF HERU PRIANTO
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Eksplorasi dan Identifikasi Kulit Mimba
(Azadirachtaindica A.Juss) sebagai Larvisida terhadap Nyamuk Aedes aegypti
belum diajukan dalam bentuk apapun kepada perguruantinggi manapun. Sumber
informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak
diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam
Daftar Pustaka di bagian akhir tesis.
Bogor, juli 2012
(AzadirachtaindicaA.Juss) as Larvicide against AedesaegyptiMosquitoes.
Supervisors:WASRIN SYAFII, ARINANA,and SULAEMAN YUSUF.
Synthetic pesticide causes many negative side-effects. For insects, it causes
physiological resistances and can kill non-target insects. Resistant insects will need
more insecticide dose than before. To avoid the negative effect, World Health
Organization (WHO) recomends to use natural insecticide. Resistant mechanism is
combination of many factors which are biochemistry, physiology, andbehaviour.
The more specific insecticide is used, the easier it causes the resistant effect.Neem
is one of plants that has been extensively used to study its insecticidal and
medicinal activity. It has opportunity to become strong natural insectides to many
insects.
Aims of this research were to analysis of extractivecontens of neem bark,
toxicity test of bioactive against Aedesegyptilarvae, and isolate and identify
bioactive compounds of neems bark in against Ae.aegypti larvae. Neem bark
powder was extracted using methanol as a solvent. Obtained extract of this process
was separated by different polar solvent. Separation process obtains three fractions
that are ethyl acetatesoluble fraction, buthanolsolublefraction, and unsoluble
fraction. Each fraction was evaporated to get condensed extract. Effectiveness of
each fraction to Ae.aegypti larvae were tested with several concentrations that are
50, 100, 250, 500, and 1000 ppm.
This experiment showed that ethyl acetatesolublefraction was the most
effective fraction. Phytochemical analysis also confirmed that it contained many
compound such as; alkaloid, flavonoid, saponin, and triterpenoid. Then, ethyl
acetatesolublefraction was separated using chromatography column and yield 9
fractions. Second fraction (Ef-2) was the best larvicidal efficacy, and it also had
higher efficacy than ethyl acetate fraction before it was isolated. Furthermore,
magnetic resonance analysis (1H and 13C NMR) of Ef-2 was performed, and the
molecul structure of bioactive compound was identifiedas Glycerol
1,2-di-(9Z-octadecenoate) 3-tetradecanoate.
RINGKASAN
ARIEF HERU PRIANTO. Eksplorasi dan Identifikasi Kulit Mimba (Azadirachta indica A.Juss) sebagai Larvisida terhadap Nyamuk Aedes aegypti. Dibawah
bimbingan;WASRIN SYAFII, ARINANA, dan SULAEMAN YUSUF.
Penggunaan bahan kimia sintetis untuk pestisida menyebabkan pengaruh
negatif yaitu pencemaran lingkungan, gangguan kesehatan, membunuh musuh
alami dan serangga non target. Serangga yang resisten menuntut dosis yang lebih
besar untuk pengendaliannya. Untuk menghindari efek negatif tersebut, WHO
merekomendasikan insektisida nabati. Mekanisme resistensi umumnya
merupakan gabungan factor - faktor penyebab yaitu biokimia,
fisiologi, danperilaku. Semakin spesifik suatu insektisida, semakin mudah
menyebabkan terjadinya resistensi. Mimba merupakan tanaman yang telah banyak
diteliti aktifitas insektisida dan farmasinya. Mimba memiliki peluang yang besar
sebagai insektisida nabati yang kuat.
Penelitian ini bertujuan untuk menganalisisi kandungan ekstraktif dalam
kulit mimba, menguji tingkat toksisitas dari senyawa aktif terhadap larva nyamuk
Ae aegypti, mengisolasi dan mengidentifikasi senyawa aktif dari kulit mimba yang
efektif terhadap larva nyamuk Ae aegypti. Serbuk kulit mimba diekstraksi dengan
pelarut metanol. Ekstrak yang diperoleh dipartisi dengan pelarut yang berbeda
kepolarannya. Proses pemisahan menghasilkan tiga fraksi yaitu fraksi terlarut etil
asetat, terlarut butanol dan tidak terlarut. Pengujian efektivitas fraksi terhadap larva
Ae. aegypti dilakukan pada beberapa konsentrasi yaitu 0, 50, 100, 250, 500, and
1000 ppm.
Penelitian ini menunjukkan bahwa fraksi terlarut etil asetat merupakan
fraksi yang paling efektif. Analisis fitokimia juga menunjukkan fraksi terlarut etil
asetat memiliki bebrapa kelompok senyawa yaitu alkaloid, flavonoid, saponin, dan
triterpenoid. Fraksi terlarut etil asetat telah dipisahkan dengan kromatografi kolom
dan mendapatkan 9 sub fraksi. Sub fraksi kedua (Ef-2) menunjukkan aktivitas
larvasida yang paling baik, dan juga memiliki efikasi yang lebih tinggi dibanding
fraksi terlarut etil asetat sebelum dipisahkan. Analisis 1H NMR and 13C NMR)
telah dilakukan dan struktur molekul senyawa aktif teridentifikasi sebagaiGlycerol
© Hak cipta milik Institut Pertanian Bogor, tahun 2012 Hak Cipta dilindungi Undang – Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya tulis ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
EKSPLORASI DAN IDENTIFIKASI KULIT MIMBA
(Azadirachtaindica A.Juss) SEBAGAI LARVISIDA
TERHADAP NYAMUK Aedes aegypti
Arief Heru Prianto
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program StudiIlmudan Teknologi Hasil Hutan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji Luar Komisi Pada Ujian Tesis
Judul Skripsi : Eksplorasi dan Identifikasi Kulit Mimba (Azadirachtaindica
A.Juss) sebagai Larvisida terhadap Nyamuk Aedes aegypti
Nama : Arief Heru Prianto
NRP :E251090081
Disetujui,
Komisi Pembimbing
Ketua
Prof. Dr. Ir. Wasrin Syafii, M.Agr.
Arinana S.Hut., MSi
Anggota Anggota
Prof (R). Dr. Sulaeman Yusuf, M. Agr
Mengetahui:
Ketua Program Studi DekanSekolahPascasarjana
Dr. Ir. I Wayan Darmawan, M.Sc. Dr. Ir. Dahrul Syah, M.Sc, Agr.
yang telah melimpahkan rahmat dan karunia-Nya sehingga penulis dapat
menyelesaikan tesis dengan judul “Eksplorasi dan Identifikasi Kulit Mimba
(Azadirachta indica A.Juss) sebagai Larvisida terhadap Nyamuk Aedes aegypti”
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada program
studi Ilmu dan Teknologi Hasil Hutan, Fakultas Kehutanan, IPB. Shalawat dan
salam penulis panjatkan kepada Rasulullah Muhammad SAW beserta keluarga
dan para sahabatnya.
Penulis menyampaikan banyak terima kasih kepada semua pihak
yang telah membantu penulis dalam menyelesaikan tugas akhir ini, khususnya
kepada :
1. Prof. Dr. Ir. Wasrin Syafii, M.Agr. yang telah memberikan bimbingan dan arahan
kepada penulis.
2. Arinana, S.Hut., MSi yang telah memberikan bimbingan dan arahan kepada
penulis.
3. Prof (R). Dr. Sulaeman Yusuf, M.Agr yang telah memberikan bimbingan dan
arahan kepada penulis.
4. Dr.Sci Muhammad Hanafi, Prof (R). Dr Partomuan Simanjuntak dan Dr. Andrea
yang telah memberikan arahan kepada penulis.
5. Ibu dan Bapak tercinta yang telah dengan ikhlas berjuang dan berkorban demi
tercapainya cita-cita penulis.
6. Istri dan anakku tersayang yang telah dengan tulus memberikan dukungan moral
dan materil, serta doa restu kepada penulis.
7. Rekan-rekan di UPT. Balai Litbang Biomaterial, Laboratorium Farmakologi
Bioteknologi , Lembaga Ilmu Pengetahuan Indonesia dan rekan-rekan
Pascasarjana jurusan Ilmu dan Teknologi Hasil Hutan angkatan 2009 di Institut
Pertanian Bogor.
Bogor, Juli2012
RIWAYAT HIDUP
Penulis dilahirkan di Brebes pada tanggal 3 Mei 1978, merupakan
anak kedua dari tiga bersaudara, dari keluarga Soehardjo dan Farikha.
Penulis memasuki dunia pendidikan dasar di Madrasah Ibtidaiyah I
Jatibarang pada tahun 1984 - 1986 dan Sekolah Dasar Negeri I Janegara,
lulus pada tahun 1990. Pada tahun yang sama penulis melanjutkan
pendidikan menengah pertama di Sekolah Menengah Pertama Negeri I
Jatibarang, lulus pada tahun 1993. Pendidikan menengah atas dijalani penulis
di Sekolah Menengah Atas Negeri I Brebes pada tahun 1996.
Tahun 1997 penulis diterima di Jurusan Teknologi Hasil Hutan,
Fakultas Kehutanan, Institut Pertanian Bogor dan lulus sebagai Sarjana
Kehutanan pada tahun 2001. Tahun 2009 penulis diterima di programsarjana
IPB pada program studi Ilmu dan Teknologi Hasil Hutan Sebagai salah satu
syarat untuk memperoleh gelar Magister, penulis menyusun Tesis dengan
judul : “Eksplorasi dan Identifikasi Kulit Mimba (Azadirachtaindica A.Juss)
Halaman
Bioaktivitas Ekstrak Tumbuhan ... 8
Bioaktif sebagai Larvisida ... 11
Taksonomi Mimba . ... 12
Morfologi Tanaman Mimba. ... 12
Kandungan Kimia Tanaman Mimba. ... 12
Khasiat Tanaman Mimba. ... 13
Ekstraksi dan Fraksinasi ... 17
Kromatografi Lapis Tipis... 20
Kromatografi Kolom... 20
Persiapan Larva... 21
Uji Efikasi sebagai Larvisida... 21
Analisis Data... 22
HASIL DAN PEMBAHASAN Kandungan Ekstrak ... 22
Hasil Pegujian Larvisida terhadap Larva Ae.aegypti ... 24
Penentuan Nilai Lethal Concentration (LC) Ekstrak Kasar ... 26
Pemisahan Senyawa Aktif dengan Kromatografi Kolom ... 27
Aktivitas Larvisida Subfraksi Hasil Kromatografi Kolom ... 28
Penentuan Nilai Lethal Concentration (LC) Subfraksi F2... 30
Identifikasi Senyawa Aktif... 31
KESIMPULAN DAN SARAN ... 35
DAFTAR TABEL
Nomor Halaman
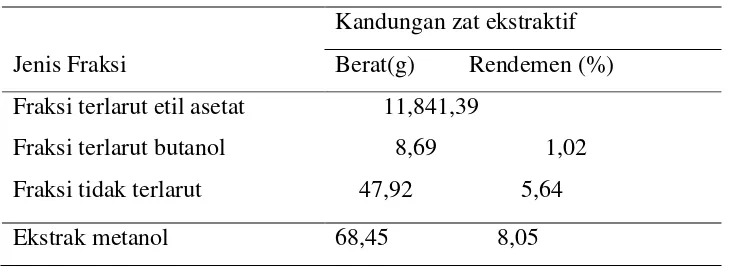
1. Kandungan ekstraktif kulit mimba... ………... 23
2. Hasil analisa fitokimia fraksi terlarut etil asetat…………... 26
3. Lethal Concentration fraksi terlarut etil asetat....………. 26
4. Rendemen bioaktif hasil kromatografi kolom... 28
5. Nilai LC50 dan LC90 Fraksi F2 6. Nilai Geseran Kimia ....…...…..………. 31
1 7. Nilai Geseran Kimia H-NMR Senyawa aktif....…….………. 31
DAFTAR GAMBAR
Nomor Halaman
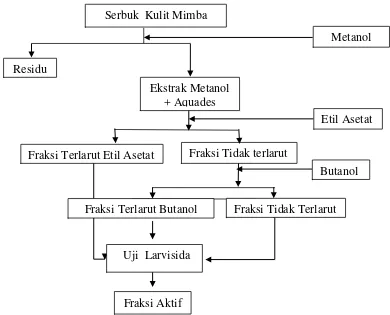
1. Diagram alir ekstraksi kulit mimba . ... 18
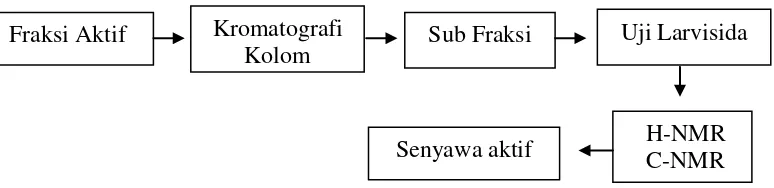
2. Diagram alir pemurnian senyawa aktif. ... 21
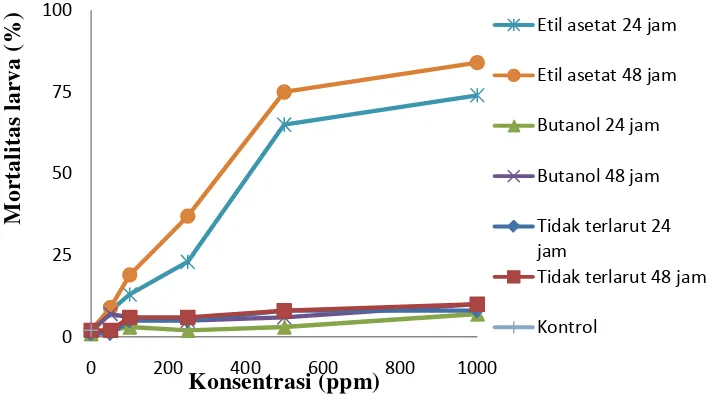
3. Mortalitas larva Ae. aegypti fraksi terlarut etil asetat. ... 24
4. Mortalitas larva Ae. aegypti Sub Fraksi F2
5. Mortalitas larva Ae.aegypti sub fraksi F
. ... 29
2
6. Struktur senyawa aktif. ... 33
DAFTAR LAMPIRAN
Nomor Halaman
1. Mortalitas larva fraksi tidak terlarut . ... 37
2. Mortalitas larva fraksi terlarut butanol. ... 38
3. Mortalitas larva fraksi terlarut etil asetat. ... 39
4. Mortalitas larva Sub Fraksi F2
5. Identifikasi sampel kulit mimba (Azadirachta indica). ... 41
. ... 40
6. Spektrum 1H-NMR senyawa aktif F2
7. Spektrum
. ... 42
13
PENDAHULUAN
Latar belakang
Penelitian mengenai pemanfaatan ekstraktif tumbuhan sudah lama
dilakukan banyak peneliti di berbagai negara. Ketertarikan para peneliti sangat
besar terhadap bahan aktif yang terkandung dalam ekstraktif. Pemanfaatan
bio-aktif untuk kebutuhan hidup manusia diantaranya sebagai bahan obat-obatan,
bahan pengawet, bahan kosmetik dan bahan insektisida. Menurut Sjostrom (1995)
ekstraktif merupakan konstituen kayu yang tidak struktural, hampir seluruhnya
terbentuk dari senyawa-senyawa ekstraseluler dengan berat molekul yang rendah.
Penggunaan bahan alam semakin diminati karena meningkatnya kesadaran
masyarakat terhadap masalah lingkungan yang sehat. Penggunaan bahan kimia
sintetis untuk pestisida menyebabkan pengaruh negatif yaitu pencemaran
lingkungan, gangguan kesehatan, membunuh musuh alami dan serangga non
target. Bahan kimia juga dapat menyebabkan serangga menjadi resisten, sehingga
serangga akan semakin tahan terhadap bahan kimia tersebut, sehingga menuntut
dosis yang lebih besar. Untuk mendapatkan pengendalian nyamuk yang efisien
dan menghindari terjadinya resistensi nyamuk, WHO merekomendasikan
pencampuran atau rotasi penggunaan insektisida (Andrandeet al.1991, WHO
2005, PMKRI 2010). Mekanisme resistensi umumnya merupakan
gabungan faktor-faktor penyebab yaitu biokimia, fisiologis dan perilaku.
Semakin spesifik suatu insektisida, semakin mudah menyebabkan terjadinya
resistensi (Martono 2011).
Pelarangan terhadap penggunaan beberapa jenis bahan kimia sudah mulai
diberlakukan dibanyak negara (Johannis dan Panut 2009). Hal tersebut
menyebabkan peluang penerimaan akan produk-produk bio-aktif semakin
meningkat, sehingga penelitian-penelitian yang menyangkut eksplorasi, isolasi
dan pemanfaatan bio-aktif masih sangat dibutuhkan.
Mimba merupakan tumbuhan yang telah banyak diteliti kandungan
senyawa aktifnya untuk penggunaannya sebagai pestisida nabati (Atawodi dan Joy
2009). Akan tetapi masih sedikit penelitian yang melaporkan senyawa yang
Pestisida nabati berbasis mimba mempunyai kisaran yang luas dalam
penggunaannya terhadap serangga hama. Mimba memiliki karakteristik sebagai
repelen, umpan, racun, pemandulan, dan pengatur tumbuh. Tumbuhan ini relatif
aman terhadap biota air yang bukan target (Dua et al. 2009). Semua bagian
Mimba memiliki aktivitas biopestisida atau farmakologi (Atawodidan Joy 2009).
Minyak dari biji mimba diketahui memiliki aktivitas larvisida yang baik terhadap
larva Anopheles gambiaepada konsentrasi yang rendah (Okumuet al. 2007, Dua et
al. 2009).
Dewasa ini telah banyak bahan pestisida yang telah dilarang
penggunaannya oleh WHO diantaranya; diklorofenol, dikloro difenil trikloroetan,
metil parathion, natrium klorat, formaldehida, dan klordan. Penggunaan pestisida
kimiawi lebih banyak merugikan daripada menguntungkan karena dampak
negatifnya yang sangat besar terhadap lingkungan dan mahluk hidup. Menurut
Mansyur (2012) Pestisida kimia dapat meninggalkan residu pada lingkungan dan
residu ini dapat bertahan hingga 100 tahun tergantung bahan aktifnya. Efek-efek
karsinogenik dari zat-zat kimia biasanya mempunyai satu masa latent yang
panjang yaitu 20 -30 tahun. Peracunan urat-urat syaraf yang ditimbulkan oleh
beberapa agent-agent antikoline esterase organo fosfat. Penyakit yang ditimbulkan
akibat pestisida diantaranya kanker, menurunnya kekebalan tubuh, kerusakan sel,
penuaan dini dan penyakit degenaratif lainnya.
Aedes aegypti merupakan vektor yang menyebarkan virus Dengeu yang
dapat menyebabkan penyakit demam berdarah (DBD). Jumlah kematian akibat
demam berdarah diIndonesia menduduki urutan tertinggi di ASEAN yaitu
mencapai 1.317 orang pada tahun 2010 (Kompas 2011).Penyebaran nyamuk Ae.
aegypti semakin luas, sehingga jutaan orang beresiko terinfeksi virus ini.
Pengendalian vektor yaitu nyamuk Ae. aegypti merupakan cara yang paling efektif
untuk mencegah penularan penyakit DBD ini. Pengendalian Ae. aegypti pra
dewasa dilakukan dengan bahan larvisida yang dapat membunuh larva Ae.
aegypti.
Larvisida utama yang digunakan untuk mengendalian larva nyamuk vektor
demam berdarah Dengeu adalah temephos (PMKRI 2010). Temephos beracun
3
(Cavalcanti et al. 2004). Ada kemungkinan resistensi dari larva Ae. aegypti
terhadap temephos yang ditunjukkan oleh survival ratenya setelah perlakuan
(Andrande et al. 1991, Georghiouet al. 1987). Menurut Agustinus (2010), sesuai
standar WHO populasi nyamuk Ae. aegypti di kota Surabaya menunjukkan sudah
toleran terhadap insektisida Malation pada konsentrasi 5%. Penggunaan bahan
yang lebih ramah lingkungan dan efektif untuk mengendalikan larva Ae. aegypti
akan mendukung program peningkatan penggunaan bahan non kimia untuk
pengendalian vektor demam berdarah Dengeu (PMKRI 2010). Oleh karena itu
mimba sebagai tanaman yang memiliki daya insektisida yang kuat diharapkan
dapat menyumbangkan suatu senyawaan yang efektif dan aman dalam membunuh
larva Ae. aegypti. Senyawa aktif tertentu memiliki inherent selectivitysehingga
aman bagi musuh alami hama (Johannis dan Panut 2009).
Identifikasi Masalah
Mimba merupakan tumbuhan yang telah banyak dimanfaatkan sebagai
insektisida nabati pada tanaman pertanian. Penggunaan bahan kimia dapat
menyebabkan resistensi serangga target, maka pemanfaatan insektisida nabati
semakin dibutuhkan. Temephos sebagai bahan aktif larvisida berbasis kimia
sintetik telah menunjukkan resistensi terhadap nyamuk Ae. aegypti. Penelitian
terhadap mimba banyak dilakukan terutama terhadap biji dan daunnya. Pada biji
telah ditemukan senyawa aktif yang bersifat toksik yang dikenal dengan nama
azadirachtin, namun diduga masih ada banyak senyawa lain yang bersifat toksik
yang belum teridentifikasi. Permasalahan yang ingin diungkap pada penelitian ini
adalah apakah kulit mimba memiliki senyawa aktif yang berpotensi sebagai
larvisida nabati? Bagaimana struktur molekul senyawa aktif tersebut?
Tujuan Penelitian
Berdasarkan permasalahan di atas, maka penelitian ini bertujuan untuk:
1. Mengetahui kandungan ekstraktif dalam kulit mimba
2. Menguji tingkat toksisitas dari senyawa aktif kulit mimbaterhadap larva
nyamuk Ae. aegypti.
3. Mengisolasi dan mengidentifikasi senyawa aktif dari kulit mimba yang efektif
Manfaat Penelitian Manfaat dari penelitian ini adalah:
1. Memberikan informasi ilmiah mengenai jenis senyawa aktif dari kulit mimba
dan tingkat toksisitasnya.
2. Memberikan informasi mengenai sifat senyawa aktif dari kulit mimba
terhadap larva Ae. aegypti untuk pemanfaatan ekstrak kulit mimba yang lebih
efektif dan efisien.
Hipotesis
Kulit mimba memiliki senyawa aktif yang bersifat toksik terhadap larva
TINJAUAN PUSTAKA
Zat Ekstraktif
Zat ekstraktif merupakan produk metabolisme sekunder. Metabolit
sekunder berperan pada kelangsungan hidup suatu spesies dalam perjuangan
menghadapi spesies – spesies lain, misalnya sebagai zat pertahanan dan zat
penarik bagi lawan jenisnya. Zat ekstraktif merupakan timbunan energi dan
makanan dalam tumbuhan. Jenis – jenis senyawa zat ekstraktif dan proses
pembentukannya telah banyak diketahui(Kristanti 2006).
Zat ektraktif merupakan zat-zat dalam kayu yang mudah larut dalam
pelarut netral atau pelarut organik dan memiliki berat molekul rendah. Zat
ekstraktif ini bukan merupakan bagian struktur dinding sel kayu, tetapi sebagai zat
pengisi rongga sel. Zat ekstraktif merupakan komponen kayu yang berjumlah
kecil, biasanya kurang dari 10 % bagian kayu dan larut dalam pelarut-pelarut
organik netral atau air (Sjostrom, 1995).Menurut Fengel dan Wegener (1995) dan
Sjostrom (1995), ekstraktif bersifat racun yang dapat mencegah bakteri, jamur,
dan rayap. Ekstraktif lainnya dapat memberikan warna dan bau pada kayu.
Daun-daunan juga mengandung zat ekstraktif. Selain mengandung senyawa-senyawa
yang juga terkandung di dalam kayu seperti: mono-terpena, diterpena, asam
lemak, fenol sederhana, lignan, flavonoid, gula, dan protein, juga terdapat
beberapa asam resin, asam siklis, dan berbagai siklitol.Menurut Sjostrom (1995)
dan Bowyer et al. (2003) kerugian adanya ekstraktif kayu antara lain;
1. Zat ekstraktifdapat mengganggu proses perekatan pada produk hasil hutan
2. Zat ekstraktif tertentu dapat bersifat korosif terhadap logam
3. Zat ektraktif dapat menghambat proses delignifikasi pada pembuatan pulp
Sedangkan, keuntungan adanya ekstraktif dalam kayu yaitu;
1. Meningkatkan keawetan alami kayu
2. Zat ekstraktif merupakan sumber bahan kimia alamiyang
selamainidigunakansebagaibahanbakuuntukberbagaiindustriantaralain;
Zat ekstraktif terdiri atas senyawa-senyawa tunggal fraksi lipofilik dan
fraksi hidrofilik. Fraksi lipofilik antara lain: lemak, lilin, terpena, terpenoid dan
alkohol alifatik tinggi, sedangkan fraksi hidrofilik meliputi senyawa fenolik
(tanin, lignan, stilbena), karbonat terlarut, protein, vitamin, dan garam anorganik.
Menurut Sjostrom (1995) komponen ekstraktif terdiri atas:
1. Lemak dan lilin contoh asam-asam lemak, arakhinol, behenol, dan
lignoserol
2. Terpenoiddan steroid contoh:monoterpen, diterpen, triterpen, sitosterol,
kampesterol
3. KomponenFenol terdiri atas fenoliksederhana (Gallic acid, Vanillin),
Stillben (pinosylvin), flavonoid (taxifolin, krisin, katekin), lignan
(inoresinol, konidendrin, asam plikatat, dan hidrosimatai-resinol), dan
tanin-tanin kondensasi
Cara pemisahan ekstraktif menggunakan pelarut yang memiliki angka
polaritas sama atau hampir sama (Achmadi 1990). Sedangkan menurut Fengel dan
Wegener (1995), isolasi ekstraktif dapat dilakukan dengan ekstraksi menggunakan
campuran pelarut netral dan atau dengan pelarut tunggal secara berurutan.
Kelarutan zat di dalam pelarut-pelarut itu tergantung dari ikatannya, apakah polar,
semi polar atau non polar. Pelarut polar misalnya : air, alkohol, dan metanol,
sedangkan yang non polar misalnya heksan dan karbon tetra klorida. Zat-zat yang
polar hanya larut dalam pelarut polar, sedangkan zat-zat non polar hanya larut
dalam pelarut non polar (Yuliani dan Rusli 2003).
Proses Ekstraksi
Ekstraksi adalah suatu cara untuk memisahkan campuran beberapa zat
menjadi komponen-komponen terpisah. Ragam ekstraksi yang tepat tergantung
pada tekstur dan kandungan air bahan tumbuhan yang diekstraksi dan pada jenis
senyawa yang diisolasi. Bila mengisolasi senyawa dari jaringan hijau,
keberhasilan ekstraksi dengan alkohol berkaitan langsung dengan seberapa jauh
klorofil tertarik oleh pelarut tersebut. Bila ampas jaringan pada ekstraksi ulang
sama sekali tak berwarna hijau kembali, dapat dianggap semua senyawa berbobot
7
(2006) berdasarkan bentuk campuran yang diekstraksi, dapat dibedakan dua
macam ekstraksi yaitu:
1. Ekstraksi padat-cair jika substansi yang diekstraksi terdapat didalam
campuran yang berbentuk padat. Proses ini paling banyak ditemukan
dalam usaha mengisolasi suatu substansi yang terkandung di dalam
suatu bahan alam
2. Ekstraksi cair-cair jika substansi yang diekstraksi terdapat didalam
campuran yang berbentuk cair
Sedangkan berdasarkan proses pelaksanaannya, ekstraksi dapat dibedakan sebagai
berikut:
1. Ekstraksi yang berkesinambungan (continous extraction)
Dalam ekstraksi ini pelarut yang sama dipakai berulang-ulang sampai
proses ekstraksi selesai
2. Ekstraksi bertahap (bath extraction)
Dalam ekstraksi ini setiap tahap ekstraksi selalu dipakai pelarut yang
baru sampai proses ekstraksi selesai
MenurutAchmadi (1990), ekstraksidapat dikerjakan dengan pelarut
organik seperti eter, aseton, benzena, etanol, diklorometana atau campuran larutan
tersebut. Menurut Kristanti et al. (2006) maserasi adalah suatu contoh metode
ekstraksi padat-cair bertahap yang dilakukan dengan jalan membiarkan padatan
terendam dalam suatu pelarut. Proses perendaman dalam usaha mengekstraksi
suatu substansi dari bahan alam ini bisa dilakukan tanpa pemanasan (suhu kamar),
dengan pemanasan atau bahkan pada titik didih. Sesudah disaring, tidak terlarut
dapat diekstraksi kembali menggunakan pelarut yang baru. Pelarut yang baru
dalam hal ini tidak berarti harus berbeda zat dengan pelarut yang terdahulu, tetapi
bisa berasal dari pelarut yang sama. Proses ini bisa diulang beberapa kali sesuai
kebutuhan.
Ragam ekstraksi yang tepat tergantung pada tekstur dan kandungan air
bahan tumbuhan yang diekstraksi dan pada jenis senyawa yang diisolasi. Bila
mengisolasi senyawa dari jaringan hijau, keberhasilan ekstraksi dengan alkohol
berkaitan langsung dengan seberapa jauh klorofil tertarik oleh pelarut itu. Bila
dianggap semua senyawa berbobot molekul rendah telah terekstraksi (Harborne
1987). Zat ekstraktif dapat diekstraksi dari kayu dengan menggunakan pelarut
polar dan non-polar (Fengel dan Wegener, 1995).
Faktor yang mempengaruhi keberhasilan proses ekstraksi menurut Yuliani
dan Rusli (2003) adalah sebagai berikut : persiapan bahan, pemilihan pelarut,
metode ekstraksi, proses penyaringan, dan proses pemekatan. Bahan yang akan
diekstraksi sebelumnya dikeringkan terlebih dahulu, pengeringan tanaman yang
digunakan untuk pestisida nabati sebaiknya sampai kadar air mencapai 10 %
dengan suhu kurang dari 50 ºC agar bahan aktif yang terkandung tidak rusak.
Sebelum ekstraksi bahan perlu dikeringkan agar tidak terlalu banyak terjadi
perubahan kimia dan suhu rendah bertujuan agar komponen tertentu yang
diinginkan tidak rusak selama ekstraksi.
Konstituen-konstituen kulit dapat dibagi menjadi konstituen lipofil dan
hidrofil. Bagian lipofil dapat diekstraksi dengan pelarut nonpolar yang terdiri atas
lemak, lilin, terpenoid, dan alkohol alifatik tinggi. Terpenoid, asam-asam resin,
dan sterol-sterol terdapat dalam saluran resin. Sitosterol terdapat dalam lilin
sebagai komponen alkohol (Sjostrom 1995). Alkaloid dapat ditemukan dalam
bagian tumbuhan seperti biji, daun, ranting, dan kulit kayu. Biasanya kandungan
alkaloid pada tumbuhan sekitar 1% tapi pada bagian kulit kayu dapat memiliki
kandungan 10-15% alkaloid (Suradi 1995 dalam Mulyana 2002).Senyawa
alkaloid tropana dapat menginhibisi syaraf parasimpatik pada sistem syaraf pusat
serangga (Batchelder 1995 dalam Mulyana 2002).
Bioaktifitas Ekstrak Tumbuhan
Eriksson et al. (2008) meneliti sepuluh jenis tanaman yaitu alder (Alnus
glutinosa), aspen (Populus tremula), beech (Fagus sylvatica), guelder rose
(Viburnum opulus), holly (Ilex aquifolium), horse chestnut (Aesculus
hippocastanum), lilac (Syringa vulgaris),spindle tree (Evonymus europaeus),
walnut (Juglans regia), dan yew (Taxus baccata). Hasil peneilitian menunjukkan
bahwa senyawa aktif dari ekstrak metanol kulit Aesculus yang difraksinasi
dengan liquid chromatography menunjukkan bahwa komponen senyawa
utamanya adalah golongan alkohol dan ester-ester dari hexanoic acid yang
9
Menurut Atmaka (2002), penambahan tepung daun sirsak ke dalam media
memiliki pengaruh nyata dalam penurunan serangga turunan pertamadengan
konsentrasi sebesar 2%. Menurut Putri (2004) biopestisida dari daun sirsak
memberikan pengaruh nyata pada konsentrasi 2% sebagai biopestisida, sedangkan
menurut Kulsum (1998) pertambahan 0,5% tepung biji sirsak pada media dapat
menghambat perkembangan Sitophilus zeamanis.Biji sirsak mengandung minyak
yang dapat digunakan untuk cat dan insektisida(Samson 1992 dalam Kulsum
1998). Biji sirsak mengandung 2 jenis alkaloid yang beracun bagi serangga yaitu
cytinine dan spartein (Fear 1987 dalam Kulsum 1998). Selain itu juga
mengandung flavonoid, senyawa berupa rotenon yang dapat bereaksi dengan
mengganggu proses produksi energi (Guenter & Jippson dalam Kulsum 1998).
Isoflavon rumit berupa senyawa rotenon merupakan insektisida alam yang kuat
(Harborne 1987).
Cengkeh digunakan untuk pengobatan, pemeliharaan gigi, dan sebagai
rempah-rempah. Paling banyak digunakan sebagai campuran dalam rokok kretek
(Hadiwijaya 1986). Bagian yang banyak dimanfaatkan adalah bunga, tangkai, dan
daunnya. Minyak cengkeh beraroma khas, biasa digunakan untuk campuran
farfum dan sabun. Terkadang minyak cengkeh juga digunakan untuk memberi
rasa pada berbagai jenis makanan (Guenther 1990).
Minyak atsiri yang terkandung pada tanaman cengkeh bersifat
bakteriostatik, bakterisida, antifungal, dan antiseptik. Salah satu komponen dari
minyak atsiri tanaman cengkeh adalah eugenol yang presentasenya bervariasi
pada setiap tanaman. Minyak bunga cengkeh mengandung eugenol 85-95%,
minyak gagang atau tangkai cengkeh mengandung 90-95%, dan minyak dari daun
cengkeh mengandung eugenol 80-88%. Selain itu minyak cengkeh juga
mengandung eugenol asetat yang sifatnya sama dengan eugenol namun dalam
jumlah yang lebih sedikit (Guenther 1988).
Menurut Syafii (2000) fraksi n-heksana dari kayu Sonokembang terdapat 3
komponen utama yaitu guaiacol, 2-napthalenemetanol, dan 9,12-octadekadienoat.
Fraksi n-heksana kayu Eboni dapat diidentifikasi lima komponen utama yaitu
2-metil-1-propoksi-propana, dan asam oktanoat. Pada fraksi tak terlarut kayu Torem terdapat asam
p-hidroksi benzoat, asam vanilat, dan asam siringat.
Menurut Prianto (2008) menyatakan bahwa uji fitokimia Picrasma
javanicamemiliki kandungan berupa saponin, flavonoid, triterpenoid dan
glikosida. Kandungan flavonoid berupa isoflavon rumit yaitu senyawa rotenon
merupakan insektisida alam yang kuat (Harborne 1987). Sedangkan menurut
Robinson (1995) rotenon berfungsi sebagai pestisida yang merupakan inhibitor
oksidasi mitokondria. Kandungan triterpenoid merupakan komponen aktif sebagai
anti fungus, insektisida, dan anti pemangsa, diduga berupa senyawa asam ursolat,
dan asam oleanolat. Kandungan glikosida merupakan senyawa perlindungan dari
gangguan serangga tertentu (Robinson 1995), sedangkan menurut Harborne
(1987) glikosida berkhasiat farmakologi dan senyawa fenolik menghambat kerja
enzim. Kandungan triterpenoid steroid mampu mempengaruhi hormon serangga
dalam proses ganti kulit (Harborne 1987).
Ekstrak D. AcutangulumdanP. retrofractum efektif terhadap hama sasaran
S.litura dan aman terhadap predatornya S. annulicornis (Fachry, 1995).
Penggunaan bahan tumbuhan liar rawa seperti rumput minjangan (Chromolaena
odorata), maya (Amorphophallus campanulatus), sirih hutan (Piper
sarmentosum), tumbuhan kayu lurus/sungkai (Peronema canescens), simpur
(Dellinea suffiruticosa), kalampan, suli tulang, binderang (Scleria oblata), bakung
(Crymum asiaticum), jengkol (Phitecellobium lobatum), tawar (Costus spec), dan
tumbuhan mercon dapat membunuh ulat grayak antara 75-95%. Dengan demikian
tumbuhan liar rawa tersebut perlu mendapat perhatian kelestariannya terutama
sebagai alternatif pengganti insektisida sintetik dalam pengendalian ulat grayak
(Asikin dan Thamrin 2009).
Sebagai penelitian awal, diketahui tiga jenis tumbuhan yang berpotensi
dijadikan bioinsektisida yaitu tumbuhan pegagan (Centella asiatical), kacang
parang (Canavalia ensiformis), dan mengkudu (Morinda citrifolia). Ketiga jenis
tumbuhan tersebut dapat membunuh ulat Plutella xylostella pada kubis dengan
11
Bioaktif sebagai Larvisida
Ektrak Lantana camara pada konsentrasi 1,0 mg/ml memberikan
mortalitas maksimum terhadap larva Ae. aegypti, sedangkanpada larvaCulex
quinquefasciatus mortalitas tertinggi terjadi pada konsentrasi 3,0mg/ml (Kumar
dan Maneemegalai 2008). Daun dan biji Sirsak dapat digunakan untuk ramuan
biopestisida, larvisida, repellent (penolak serangga), dan anti feedant (penghambat
makan dengan cara racun kontak), menanggulangi hama belalang dan hama
lainnya. Kandungan efektifnya biji, daun, dan akar berupa senyawa annonain.
Pada bagian bijinya mengandung minyak 42 % - 45% (Zuhud dan Haryanto
1994).Fraksi A1
Ekstrak etanol dari Cryptomeria japonica, memiliki aktivitas terbaik
terhadap larva Ae. aegypti dan Ae. albopictus dengan masing-masing nilai LC
dari ekstrak biji Sterculia guttata merupakan senyawa non-polar
yang mempunyai aktivitas biolarvisida (Katade et al. 2006).
50 63,2 dan 93,8 µg/ml,. Empat senyawa utama: ferruginol, epi-cubebol, cubebol,
dan isopimarol. Cubebol menunjukkan aktivitas terbaik terhadap Ae. aegypti dan
Ae. albopictus dengan masing-masing nilai LC50 nilai 60,1 dan 50,0 µg/ml.
Ekstrak C. japonica memiliki efek penghambatan yang sangat baik terhadap larva
Ae. aegypti dan Ae. albopictus dan nilai LC50-nya masing-masing adalah 2,4 dan
3,3 µg/ml. Hasil isolasi kayu C. japonica berupatectoquinoneLC50
Ekstrak methanol kulitCinnamomum cassia, buahIlliciumverum,
buahPiper nigrum, buahZanthoxylumpiperitum danKaempferia
galangamemilikipotensisebagailarvisida (Yang et al.
2004).EkstrakbenzenefraksidaunCitrullus vulgaris Schradlebihefektifterhadap
larva nyamukAe. stephensi daripadaAe. aegypti (Mulaiiet al. 2008).
EkstraketanoldaundanbuahMelia azedarach Lmenyebabkankematian yang
tinggiterhadap larva Ae.aegypti(Coria et al. 2008).Minyak kamandrah dan jarak
pagar berpengaruh terhadap peletakan telur Ae. aegypti. Minyak kamandrah
terdapat senyawa aktif jenis alkaloid golongan piperdine yg diduga sebagai
larvisida, kadar piperdine kamandrah 0,0385% dan jarak pagar 0,0054% (Astuti
2008).
dari
tectoquinone terhadap Ae. aegypti dan Ae. albopictus dalam 24 jam
Taksonomi Mimba
Menurut Sukrasno (2003) sistematika taksonomi tanaman mimba sebagai berikut:
Domain : Eukaryota
Kingdom : Plantae
Divisi : Spermatophytes
Subdivisi : Angiosperms
Class : Dicotyledonae
Order : Rutales
Suborder : Meliineae
Family : Meliaceae
Genus : Azadirachta
Specific epithet : indica – A.Juss
Botanical name : Azadirachta indica A. Juss
Nama daerah : nimba (jawa), surian bawang (Kalimantan), nibwak (Irian)
Morfologi Tanaman Mimba
Mimba merupakan pohon yang tinggi batangnya dapat mencapai 20 m.
Mimba dapat tumbuh pada pada dataran rendah sampai ketinggian 1.500 m diatas
permukaan laut. Kulit tebal, batang agak kasar, daun menyirip genap, dan
berbentuk lonjong dengan tepi bergerigi dan runcing, sedangkan buahnya
merupakan buah batu dengan panjang 1 cm. Buah mimba dapat dihasilkan dengan
baik pada ketinggian 0 – 200mdpl. Buah mimba dihasilkan dalam satu sampai dua
kali setahun, berbentuk oval, bila masak daging buahnya berwarna kuning, biji
ditutupi kulit keras berwarna coklat dan didalamnya melekat kulit buah berwarna
putih. Batangnya agak bengkok dan pendek, oleh karena itu kayunya tidak
13
Kandungan Kimia Tanaman Mimba
Menurut Atawodi dan Joy (2009) metabolit sekunder yang ditemukan dalam
Azadirachta indica antara lain;
1. DaunmengandungParaisin, suatu alkaloid
dankomponenminyakatsirimengandungsenyawasulfida
2. Bijimengandungazadirahtin, azadiron, azadiradion, epoksiazadiradion,
gedunin, 17-epiazadiradion, 17-hidroksi azadiradiondan alkaloid dan ester
asam lemak.
3. Kulitbatangdankulitakarmengandungnimbin, nimbinin, nimbidin,
nimbosterol, nimbosterin, sugiol, nimbiol, margosin, asam gallic,
polisakarida, polisakarida GIa, polisakarida GIb, polisakarida GIIa,
polisakarida GIIIa.
4. Hasilhidrolisisekstrakbungaditemukankuersetin, kaemferol,
dansedikitmirisetin. Dari bagiankayuditemukannimaton, 15%
zatsamakterkondensasi.
Khasiat Tanaman Mimba
Aktivitas farmakologi tanaman mimba telah banyak dibuktikan dalam
berbagai penelitian diantaranya sebagai antifertilitis, antiplasmodial, antiinflamasi,
antiteramatik, antipiretik, penurunan gula darah, antitukak lambung,
hepatoprotektor, imunopotensiasi, antifertilitas, antibakteri, antijamur, anti
kanker, antitripanosoma dan antivirus (Atawodi dan Joy 2009).
Taksonomi Aedes aegypti
Klasifikasi Aedes aegypti adalah sebagai berikut (Soedarto 1992) :
Subfamily : Culicinae
Genus : Aedes
Subgenus : Stegomya
Species : Aedes aegypti
Morfologi Aedes aegypti
Nyamuk Ae. aegypti mempunyai ciri-ciri sebagai berikut :
1. Terdiridaritigabagianyaitu : kepala, dada, danperut
2. Kepalaterdapatsepasangantena yang berbuludanmoncong yang panjang
(proboscis) untukmenghisapdarah
3. Pada dada ada 3 pasang kaki yang
beruassertasepasangsayapdepandansayapbelakang yang mengecil yang
berfungsisebagaipenyeimbang (halter).
Ae. aegypti dewasa berukuran kecil dengan warna dasar hitam. Pada bagian
dada, perut, dan kaki terdapat bercak-bercak putih yang dapat dilihat dengan mata
telanjang. Pada bagian kepala terdapat pula probocis yang pada nyamuk betina
berfungsi untuk menghisap darah, sementara pada nyamuk jantan berfungsi untuk
menghisap bunga. Terdapat pula palpus maksilaris yang terdiri dari 4 ruas yang
berujung hitam dengan sisik berwarna putih keperakan. Pada palpus maksilaris
Ae. aegypti tidak tampak tanda-tanda pembesaran, ukuran palpus maksilaris ini
lebih pendek dibandingkan dengan proboscis (Sudarto 1992).
Siklus Hidup Ae. aegypti
Ae. aegypti merupakan serangga yang aktif pada pagi hingga siang hari.
SiklushidupnyamukAe.aegyptimengalami metamorphosis sempurnayaitutelur,
larva, pupa dandewasa (HadidanKoesharto 2006). Larva dan pupa memerlukan air
untukkehidupannya, sedangkantelurtahanhiduptanpa airdalamwaktu lama,
meskipunharustetapdalamlingkungan yang lembab (Christoper 1960).
Telur
Nyamuk Ae. aegypti meletakkan telur pada permukaan air bersih. Telur berbentuk
elips berwarna hitam dan terpisah satu dengan yang lain. Telur bias tahan
15
menutupiseluruhbagiantelur,
makatelurakanmenetasmenjadijentik(HadidanKoesharto2006). Telur menetas
dalam 1 sampai 2 hari dengan tingkat fertilitas mencapai 98% pada suhu 24-250
Larva
C
dan menurun pada suhu yang lebih tinggi (Mohammed dan Cadee 2011).
Terdapat empat tahapan dalam perkembangan larva (instar). Perkembangan dari
instar 1 ke instar 4 memerlukan waktu sekitar 4-8 hari. Setelah mencapai instar
ke-4, larva berubah menjadi pupa di mana larva memasuki masa dorman.
Persentase larva menjadi pupa mencapai 87,7% pada suhu 24-250
Pupa
C, 98.5% dan
prosentase menurun dengan kenaikan suhu (Mohammed dan Cadee 2011).
Perubahan fase instar ditandai dengan proses pergantian kulit (Bates 1970).
Kepala larva berkembangbaikdengansepasang antenna danmatamajemuk,
sertasikatmulut yang menonjol.Perutnyaterdiriatas 9 ruas yang jelas,
danruasterakhirdilengkapidengantabungudara (sifon) yang bentuknyasilinder
(HadidanKoesharto 2006).
Pupa merupakan larva yang memasuki masa dorman.Larva cenderung berhenti
makan dan tetapsaat istirahat di permukaan. Pupa nyamuk berbentuk seperti
koma, kepala dan dadanya bersatu dilengkapi dengan sepasang trompet
pernapasan.Pupa nyamukbergerakaktiftifaksepertikebanyakan pupa
seranggalainnya (Bates 1970).Pupa bertahan selama 2 hari sebelum akhirnya
nyamuk dewasa keluar dari pupa (HadidanKoesharto 2006).
Dewasa
Nyamuk dewasa Ae. aegypti mudah dibedakan dari anggota sub-genus lainnya
dengan corak putih pada punggung dengan pola seperti siku yang berhadapan.
Probosis gelap, sedangkan palpi 1/5 panjang probosis dengan corak putih pada
ujungnya, clypeus bercorak putih lateral, dan pedicel dengan bercak putih di
bagian samping. Pada nyamuk jantan palpi sama panjang dengan probosis dengan
pita dasar putih pada palpomere II-IV. Dua segmen terakhir ramping dengan seta
yang pendek. (Becker et al. 2003). Nyamuk Aedes memiliki ujung abdomen yang
runcing, mempunyai cerci yang menonjol, dibagian lateral dada terdapat rambut
Waktu dan Tempat
Penelitian ini dilaksanakan daribulan April 2011 sampai dengan Maret
2012di Laboratorium Farmakologi Bioteknologi dan Laboratorium Pengendalian
Serangga Hama dan Biodegradasi, Lembaga Ilmu Pengetahuan Indonesia.
Bahan dan Alat
Bahan penelitian yang digunakan adalah kulit mimba (Azadirachta indica
A.Juss) yang diperoleh dari Situbondo Jawa Timur. Bahan pelarut yang digunakan
untuk ekstraksi antara lain: metanol, etil asetat, butanol dan aquadest, sedangkan
bahan untuk pengujian fitokimia antara lain: aquadest, pereaksi Dragendorf,
pereaksi Mayer, pereaksi Liebermann-Burchard, FECL3
Persiapan Bahan
dan natrium
hidroklorida,serta bahan untuk fraksinasi antara lain:lempeng silika gel, dan silika
gel 60. Alat yang digunakan antara lain, hammer mill, saringan 60 mesh, oven,
kertas saring whatman, tabung reaksi, neraca analitik, vacuumrotary evaporator,
Sonicator Branson, corong pisah, water bath,Column Cromatography (CC), dan
NMR.
Kulit batang mimba dibersihkan dan kemudian dipotong-potong dengan
ukuran + 2 cm. Potongan kulit mimba dikeringkan dalam suhu ruang selama 7
hari. Potongan kulit mimba kemudian dibuat serbuk dengan menggunakan
hammer mill dan disaring untuk memperoleh ukuran 40 – 60 mesh. Serbuk
kemudian dikering udarakan sampai Kadar Air 15%.
Penetapan Kadar Air
Pengukuran kadar air dilakukan dengan menimbang serbuk kulit mimba
sebanyak ± 2 gram.Serbuk diukur beratnya dan dimasukkan dalam oven pada
suhu 102±3oC sampai beratnya konstan (+ 3 jam).Serbuk didinginkan dalam
18
Perhitungan % kadar air sesuai denganrumus :
Kadar air (%) = –
dimana,
BKU = Bobot serbuk kering udara
BKT = Bobot serbuk kering anur
Ekstraksi dan Fraksinasi
Metode ekstraksi yang digunakan adalah metode maserasi menggunakan
pelarut metanol, etil asetat, danbutanol.Ekstraksi dilakukan secara bertingkat
dengan pelarut pertama metanol, kemudian dilanjutkan dengan pelarut etil asetat,
dan butanol. Serbuk kulit mimba sebanyak ± 1000 gram direndam dengan
metanol selama 24 jam dengan mengaduk sesering mungkin. Perendaman
dilakukan beberapa kali sampai diperoleh ekstrak yang bening. Ekstrak metanol
diperoleh dengan menyaring residu dengan ekstraknya dengan kertas saring
Whatman.
Ekstrak dievaporasi dengan rotari evaporator vakum pada suhu ± 40o
Tiap ekstrak kemudian dievaporasi dengan rotari evaporator vakum pada
suhu ± 40
C,
sampai diperoleh ekstrak pekat metanol ± 30 ml. Ekstrak pekat tersebutkemudian
ditambahkan aquades sampai diperoleh 300 ml ekstrak. Ekstrak kemudian
dimasukkan dalam corong pisah 1000 ml dan diekstraksi dengan pelarut
berikutnya yaitu etil asetat sebanyak 300 ml (1:1). Ekstrak dalam corong pisah
dikocok agar aquades dan etil asetat berinteraksi dan didiamkan beberapa saat
sampai ada pemisahan yang jelas antara kedua pelarut. Pada tahap ini diperoleh
fraksi terlarut etil asetat dan tidak terlarutnya. Fraksi tidak terlarut diekstraksi
kembali dengan pelarut berikutnya yaitu butanol. Tahap ini dilakukan beberapa
kali sampai diperoleh fraksi terlarut etil asetat dan butanol yang jernih.
o
C untuk memperoleh fraksi terlarut pekat etil asetat, butanol, dan
pelarut,ekstrak pekat hasil evaporasi kemudian dikeringkan pada suhu ruang
dengan bantuan kipas angin.Sedangkan padatan fraksi tidak terlarut diperoleh
dengan mengeringkannya dalam water bath.
Rendemen tiap ekstrak dihitung dengan rumus:
Rendemen (%) = x 100 %
dimana:
BKA = Berat kering ekstrak padat yang diperoleh (gram)
BKS = Berat kering serbuk yang diekstraksi (gram)
Ekstrak padat yang diperoleh kemudian diuji fitokimia sesuai dengan
metode Harborne (1987):Kelompok senyawa yang diamati antara lain alkaloid,
saponin, triterpenoid, steroid, phenol, dan flavonoid . Menurut Kristanti (2006) Serbuk Kulit Mimba
Residu
Fraksi Tidak terlarut
Metanol
Fraksi Terlarut Etil Asetat
Uji Larvisida Fraksi Terlarut Butanol
Etil Asetat
Butanol
Fraksi Tidak Terlarut
Fraksi Aktif
Ekstrak Metanol + Aquades
20
fitokimia merupakan langkah awal untuk mengetahui gambaran tentang golongan
senyawa yang terkandung dalam tanaman yang sedang diteliti, dimana metode
yang digunakan sebagian besar merupakan reaksi pengujian warna dengan suatu
pereaksi warna.
Penapisan Fitokimia
a. Identifikasi golongan alkaloid
Ekstrak sebanyak 10mg dilembabkan dengan amonia 30%, digerus dalam
mortir, ditambahkan 20 ml kloroform dan digerus kuat. Campuran disaring
dengan kertas saring, filtrat berupa larutan organik diambil (sebagai
larutan A), sebanyak 5 ml larutan A diekstraksi dengan 5 ml larutan HCL
1:10 dengan pengocokan tabung reaksi, diperoleh larutan bagian atas
(larutan B). Larutan A diteteskan pada kertas saring dan disemprot atau
ditetesi dengan pereaksi Dragendorff dan Mayer, terbentuk endapan merah
bata dengan pereaksi Dragendorff dan endapan putih dengan pereaksi
Meyer menunjukkan adanya asenyawa alkaloid.
b. Identifikasi golongan steroid dan triterpenoid
Ekstrak sebanyak 10 mg simplisia dimaserasi dengan 100 ml eter selama 2
jam dalam wadah dengan penutup wadah rapat, disaring dan diambil
filtratnya. Sebanyak 5 ml dari filtrat tersebut diuapkan dalam cawan
penguap hingga diperoleh residu, ke dalam residu ditambahkan 2 tetes
asam asetat anhidrat dan 1 tetes asam sulfat pekat (pereaksi
Liebernman-Buchard), terbentuknya warna hijau atau merah menunjukkan adanya
senyawa golongan steroid dan triterpenoid.
c. Identifikasi golongan flavonoid
Ekstrak sebanyak 20 mg simplisia ditambahkan 10 ml air panas,
dididihkan selama 10 menit, kemudian saring dengan kertas saring,
sehingga diperoleh filtrat yang selanjutnya digunakan sebagai larutan
percobaan. Sebanyak 5 ml larutan percobaan ditambahkan serbuk atau
lempeng magnesium secukupnya dan ditambah 1 ml asam klorida pekat
dan 5 ml amil alkohol, dikocok kuat dan dibiarkan memisah, terbentuknya
warna merah pada lapisan amil alkohol menunjukkan adanya senyawa
d. Identifikasi golongan saponin
Sebanyak 10 ml larutan percobaan yang diperoleh dari percobaan C,
dimasukkan ke dalam tabung reaksi dan dikocok selama 10 detik secara
vertikal, kemudian dibiarkan 10 menit, terbentuknya busa yang stabil
dalam tabung reaksi menunjukkan adanya senyawa golongan saponin, dan
bila ditambahkan 1 tetes asam klorida 1 % (encer) busa tetap stabil.
Kromatografi Lapis Tipis
Eluen yang digunakan dalam Kromatografi Lapis Tipis (KLT) sangat
menentukan keberhasilan pemisahan senyawa dalam ekstrak. Penentuan eluen
terbaik menggunakan kombinasi beberapa pelarut dengan sistem gradien. Eluen
disiapkan dengan mencampur sistem eluen yang diinginkan dalam bejana
kromatografi. Bejana dijenuhkan dengan eluen beberapa saat (+ 15 menit). Pelat
KLT yang digunakan adalah silika gel G 60 F254. Larutan ekstrak diteteskan pada
permukaan KLT dengan menggunakan pipa kapiler. Penetesan dilakukan sampai
diperoleh spot yang pekat. Pelat KLT dimasukkan dalam bejana kromatografi.
Setelah pelarut mencapai batas atas KLT (+ 1 cm dari tepi atas), pelat KLT
diangkat. Spot yang terbentuk diamati dengan sinar UV 254 nm. Eluen terbaik
digunakan pada kromatografi kolom.
Kromatografi Kolom
Kolom dipasang pada statif secara tegak lurus. Bagian dasar kolom
dimasukkan kapas secukupnya dan diatas kapas dimasukkan sea sand sebagai
penahan kapas. Eluen dimasukkan dalam kolom sebanyak 1/3 bagian kolom.
Silika dilarutkan dalam eluen hingga menjadi bubur silika. Bubur silika
dimasukkan dalam kolom sedikit demi sedikit. Cerat kolom dibuka dan dialirkan
eluen sampai diperoleh silika yang homogen di dalam kolom. Ekstrak
dihomogenkan dengan cellite dan dimasukkan dalam kolom. Ekstrak yang keluar
dari kolom ditampung tiap 20 ml dalam botol. Senyawa dalam tiap botol dilihat
spotnya dengan KLT. Senyawa yang memiliki nilai Rf yang sama disatukan
22
Persiapan Larva
Telur Ae. aegypti ditempatkan dalam wadah plastik (volume + 1 L) berisi
air sumur ±500 ml. Wadah plastik kemudian ditutup dengan kain kasa. Larva
yang menetas diberi makan pelet ikan. Larva- larva tersebut dipelihara sampai
instar IV, kurang lebih selama 6 hari, kemudian digunakan untuk penelitian.
Uji Efikasi sebagai Larvisida
Pengujian ekstrak terhadap larva nyamuk mengacu pada standar pengujian
laboratorium WHO terhadap larva nyamuk. Konsentrasi ekstrak yang digunakan
0, 50, 100, 250, 500, dan 1000 ppm, tiap konsentrasi ekstrak dimasukkan dalam
gelas dengan ditambahkan 1%DMSO sebagai surfaktan untuk mengurangi
tegangan permukaan, sehingga ekstrak dapat larut dalam air. Volume ekstrak
dalam gelas yang akan diujikan adalah 100 ml. Ekstrak dimasukkan dalam wadah
gelas 200 ml dan ditutup kain kasa setelah larva dimasukkan ke dalamnya. Tiap
gelas dimasukkan 25 ekor larva nyamuk instar IV. Kontrol negatif dilakukan
dengan menambahkan 1% DMSO dalam 100 ml air sumur sedangkan kontrol
positif dilakukan dengan menggunakan larvisida berbahan aktif temephos 1 ppm.
Untuk pengujian fraksi, pengamatan dilakukan setiap 24 jam setelah larva
dimasukkan, sedangkan pada pengujian sub fraksi aktif pengamatan dilakukan
setiap menit sampai diperoleh mortalitas larva 100%.
Mortalitas (%) = x 100%
dimana A = jumlah larva yang dimasukkan dalam gelas uji
B = jumlah larva yang hidup pada gelas uji.
Gambar 2 Diagram alir pemurnian senyawa aktif
Uji Larvisida Kromatografi
Kolom Sub Fraksi
Senyawa aktif H-NMR
Analisis Data
Rancangan percobaan yang digunakan adalah Rancangan Acak Kelompok
(RAK). Ada tiga kelompok berdasarkan fraksi yang diujikan yaitu fraksi terlarut
etil asetat, butanol, dan tidak terlarut. Konsentrasi tiap fraksi yang diujikan yang
terdiri atas 6 level yaitu 0, 50, 100, 250, 500, dan 1000 ppm. Pengujian dilakukan
dengan 4 ulangan untuk tiap konsentrasi. Analisis probit dilakukan untuk
mengetahui Lethal concentration yaitu LC50 dan LC90 dilakukan dengnan
HASIL DAN PEMBAHASAN
Kandungan Ekstrak
Ekstraksi kulit mimba dilakukan dengan pelarut awal metanol, pelarut ini
dapat melarutkan senyawa yang bersifat polar sampai non polar. Sehingga
diharapkan lebih banyak senyawa yang terekstraksi. Aktifitas insektisida,
larvisida, akarisida, nematisida yang berasal dari ekstrak bagian mimba telah
dilaporkan menggunakan pelarut metanol (Atawodi dan Joy 2009, Nicolettiet al.
2010). Partisi dilakukan dengan pelarut dengan kepolaran yang bertingkat, yaitu
etil asetat dankemudian butanol, sehingga diperoleh dua fraksi dan fraksi tidak
terlarutnya. Hasil ekstraksi 1000 gram kulit mimba dengan metanol mendapatkan
68,45 gram (8,1%) ekstrak, selanjutnya ekstrak metanoldipartisi dengan etil asetat
dan butanol mendapatkan rendemen ekstrak seperti pada Tabel 1.
Tabel 1Kandungan ekstraktif kulit mimba
Kandungan zat ekstraktif
Jenis Fraksi Berat(g) Rendemen (%)
Fraksi terlarut etil asetat
Fraksi terlarut butanol
Fraksi tidak terlarut
11,841,39
8,69 1,02
47,92 5,64
Ekstrak metanol 68,45 8,05
Keterangan: dihitung berdasarkan berat kering oven
Senyawa polar akan larut dalam pelarut polar dan sebaliknya pada
senyawa nonpolar. Dengan demikian, ekstraksi kulit mimba mendapatkan
senyawa yang lebih banyak bersifat polar. Hasil ekstrak yang diperoleh
dipengaruhi oleh sifat – sifat bahan alam dan bahan yang diekstraksi. Metode
ekstraksi padat-cair menghasilkan ekstraksi yang lebih sempurna (Kristanti et al.
Hasil Pengujian Larvisida terhadap Larva Ae.aegypti
Pengujian fraksi – fraksi dari ekstrak kulit mimba dilakukan sesuai dengan
standar WHO, hasil pengujian ditunjukkan pada Gambar 3. Fraksi terlarut butanol
dan tidak terlarut memberikan warna air menjadi kecoklatan, sedangkan fraksi
terlarut etil asetat agak keruh (air lebih jernih). Ketiga fraksi memberikan tingkat
mortalitas larva yang berbeda, fraksi terlarut butanol dan tidak terlarut
memberikan mortalitas larva Ae. aegypti yang rendah (<20%). Fraksi terlarut
n-heksan, butanol dan air dari ampas mimba memiliki efektivitas yang lebih rendah
terhadap larva Ae. aegypti dibanding fraksi terlarut etil asetat (Nicoletti et al.
2010). Kontrol negatif dilakukan dengan menambahkan air sumur dengan 1%
DMSO, dimana hasil pengamatan menunjukkan bahwa DMSO pada konsentrasi
ini tidak beracun yang ditunjukkan dengan rata-rata mortalitas larvanya yang kecil
yaitu 2%. Kontrol positif yang menggunakan bahan aktif temephos
(C16H20O6P2S3) menunjukkan efektivitas yang tinggi dengan mortalitas larva
100% pada konsentrasi 1 ppm. Temephos berbentuk granul dan tidak mewarnai
air (jernih). Temephos termasuk insektisida sintetik dalam golongan organofosfor.
Pengujian temephos pada konsentrasi 1, 10, 100, dan 1000 ppm juga
mengakibatkan mortalitas larva 100% dengan jangka waktu dua sampai empat
jam pengamatan (Astuti 2008).
Gambar 3 Mortalitas larva Ae. aegypti pada fraksi terlarut etil asetat,butanol dan
fraksi tidak terlarut Tidak terlarut 24 jam
26
Peningkatan konsentrasi dari 50 sampai 1000 ppm pada fraksi terlarut
butanol dan fraksi tidak terlarutnya tidak menunjukkan peningkatan mortalitas
larva yang signifikan. Hal ini menunjukkan fraksi terlarut butanol dan tidak
terlarut tidak bersifat toksik terhadap larva Ae.aegypti. Fraksi terlarut etil asetat
memberikan tingkat mortalitas larva Ae.aegypti yang paling tinggi yaitu 84%. Hal
ini menunjukkan adanya aktivitas larvisida yang tinggi pada fraksi ini. Fraksi
terlarut etil asetat dari ampas mimba memiliki efektivitas yang lebih tinggi
terhadap nyamuk Ae.aegypti daripada formula yang berbahan aktif azadirachtin
(Nicoletti et al. 2010). Aktivitas larvisida yang paling tinggi terjadi pada
konsentrasi 1000 ppm, dan terjadi penurunan aktivitas pada konsentrasi 500, 250,
100, dan 50 ppm. Pengamatan yang dilakukan pada 24 dan 48 jam menunjukkan
perbedaan yang berarti pada setiap konsentrasi dan setiap fraksinya. Peningkatan
mortalitas larva terjadi pada pengamatan kedua (48 jam). Peningkatan mortalitas
larva tertinggi terjadi pada fraksi terlarut etil asetat sebesar 28%, sedangkan pada
fraksi terlarut butanol dan tidak terlarut berturut-turut sebesar 12% dan 4%.
Adanya peningkatan mortalitas larva yang signifikan pada fraksi terlarut etil asetat
menunjukkan bahwa zak aktif pada fraksi ini bersifat toksik.
Fraksi yang memiliki efektivitas yang paling tinggi yaitu fraksi terlarut etil
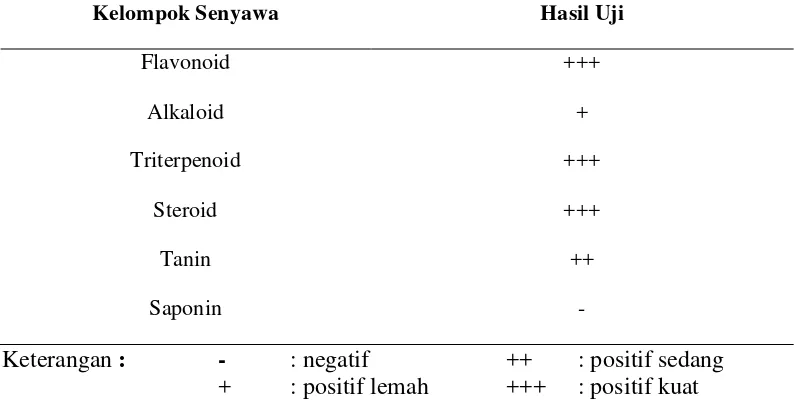
asetat dianalisa lanjut kandungan golongan senyawanya dengan uji fitokimia.
Analisis fitokimia pada Tabel 2 menunjukkan ekstrak etil asetat memiliki
kandungan flavonoid, triterpenoid, dan steroid yang kuat. Triterpenoid yang
diperoleh dari ekstrak metanol daun mimba memiliki aktifitas larvisida seperti
halnya senyawa aktif lain dalam tanaman mimba (Siddiqui et al. 2002). Flavonoid
merupakan pelindung dari serangan penyakit dan insektisida yang kuat (Harborne
1987). Flavonoid merupakan salah satu jenis golongan fenol yang banyak
ditemukan dalam tumbuh – tumbuhan. Flavonoid dapat menimbulkan kelayuan
pada syaraf dan kerusakan pada spirakel yang dapat mengakibatkan serangga
mati. Flavonoid pada Poncirus trifoliate memiliki pengaruh terhadap mortalitas
larva Ae. aegypti (Rajkumar dan Jebanesan 2008).Penelitian terhadap aktivitas
biologi menunjukkan bahwa aktivitas ekstrak biji terhadap serangga banyak
latifolia dan Calophyllum inophyllum yang memiliki alkaloid yang bersifat racun
(Katade et al. 2006).
Tabel 2 Hasil analisa fitokimia fraksi terlarut etil asetat
Kelompok Senyawa Hasil Uji
Flavonoid +++
Penentuan Nilai Lethal Concentration (LC) Ekstrak Kasar
Pengujian terhadap larva Ae.aegypti pada enam tingkat konsentrasi
dilakukan untuk mendapatkan nilai LC50 dan LC90. Nilai LC50 dan LC90
merupakan konsentrasi yang menyebabkan terjadinya kematian 50% dan 90%
larva. Nilai LC50 dan LC90 dihitung dengan analisis probit dengan menggunakan
software statistik SAS vers 9.2. Hasil perhitungan LC50 dan LC90
Tabel 3Lethal Concentrationfraksi terlarut etil asetat
28
Nilai tengah Lethal concentration setelah 24 jam perlakuan fraksi terlarut
etil asetat sebesar 567,6 ppm, sedangkan pada pengamatan 48 jam LC50 nya lebih
rendah yaitu 460,3 ppm. LC90pada pengamatan 24 jam sebesar 1.152 ppm dan
989,7 ppm pada pengamatan 48 jam. Lama perlakuan dapat menyebabkan
penurunan nilai LC50 dan LC90 berturut-turut sebesar 18,9% dan 14%. Hal ini
mengindikasikan bahwa konsentrasi dan waktu merupakan variabel yang
berhubungan untuk terjadinya kematian larva, dimana konsentrasi yang lebih kecil
membutuhkan waktu yang lebih lama untuk mencapai mortalitas larva yang sama.
Ekstrak C. japonica memiliki efek penghambatan yang sangat baik terhadap larva
Ae. aegypti dan Ae. albopictus dan nilai LC50-nya masing-masing adalah 2,4 dan
3,3 µg/ml. Hasil isolasi kayu C. japonica berupatectoquinone LC50
Pemisahan Senyawa Aktif dengan Kromatografi Kolom
dari
tectoquinone terhadap Ae. aegypti dan Ae. albopictus dalam 24 jam
masing-masing adalah 3,3 dan 5,4 µg /ml (Cheng et al. 2008).
Fraksi terlarut etil asetat merupakan fraksi yang menunjukkan efektivitas
yang paling tinggi terhadap larva Ae. aegypti, sehingga dilakukan kromatografi
kolom untuk mendapatkan senyawa tunggal yang paling bertanggungjawab
terhadap mortalitas larva. Ekstrak yang dipisahkan dengan teknik ini sebanyak 8
gram. Fase gerak yang digunakan adalah campuran n-heksan dan etil asetat
dengan elusi gradien yang telah ditentukan. Sedangkan fase diam yang digunakan
adalah silica gel dengan perbandingan antara ekstrak dan silica gel adalah 1: 30.
Diameter kolom yang digunakan adalah 3,5 cm dan panjang 100 cm. Elusi diawali
dengan pelarut yang lebih nonpolar yaitu n-heksan dan komposisi eluen
bertambah polar dengan menambahkan kepolaran pelarut secara gradien.
Perubahan komposisi eluen dilakukan setelah eluen yang telah dimasukkan dalam
kolom sebesar tiga kali volume silica gel. Eluen yang keluar ditampung dalam
botol dan dievaporasi dengan bantuan kipas angin. Setelah cukup pekat larutan
kemudian diperiksa dengan KLT untuk mendapatkan nilai Rfnya. Larutan yang
memiliki Rf yang sama disatukan menjadi satu fraksi. Proses kromatografi kolom
Tabel 4Rendemen bioaktif hasil kromatografi kolom
Sub Fraksi Rendemen (gram)
F1 1,01
Pemisahan dengan kromatografi kolom menghasilkan rendemen yang
bervariasi, sub fraksi pertama F1 merupakan sub fraksi yang memiliki rendemen
terbesar kedua yaitu 1,01 gram, sedangkan rendemen terbesar pada F2 yaitu 1,12
gram, sub fraksi F3 sampai F9 memiliki rendemen yang lebih rendah yaitu kurang
dari satu gram. Sub fraksi F1 sampai F3 memiliki warna putih keruh, sedangkan
F4 sampai F9
Aktivitas Larvisida Sub fraksi Hasil Kromatografi Kolom
berwarna kecoklatan sampai coklat. Untuk keperluan aplikasi
ekstrak pada air, maka warna ekstrak menjadi pertimbangan dalam
penggunaannya, dimana fraksi yang tidak mewarnai air akan lebih
menguntungkan.
Sub fraksi tersebut kemudian diujikan pada larva Ae. aegypti selama 24
jam, sub fraksi F1 dan F9 memberikan mortalitas larva 24% dan 96%, sedangkan
sub fraksi F2 sampai F8 memberikan mortalitas larva 100% dengan capaian waktu
yang berbeda. Karena beberapa sub fraksi memiliki rendemen yang kecil, maka
sub fraksi – sub fraksi tersebut diujikan hanya pada satu konsentrasi yaitu 1000
30
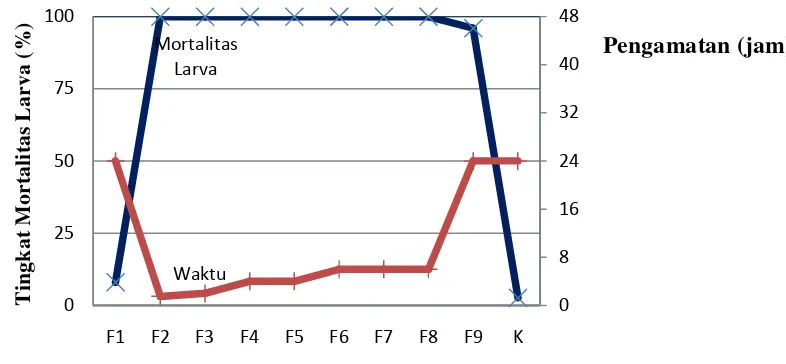
Gambar 4 Mortalitas larva Ae. aegypti pada sub fraksi hasil kromatografi kolom
Berdasarkan hasil uji larva, sub fraksi – sub fraksi tersebut memiliki
efektivitas terhadap mortalitas larva yang lebih tinggi daripada ekstrak kasarnya.
Hal ini menunjukkan bahwa senyawaan yang terkandung didalam fraksi tersebut
bersifat non-sinergi, sehingga bila senyawa tersebut berada bersama senyawaan
lain menjadi berkurang tingkat toksisitasnya. Peningkatan toksisitas sub fraksi
ditunjukkan oleh peningkatan prosentase mortalitas larva dan durasi aplikasi yang
lebih cepat. F2 merupakan sub fraksi yang paling cepat mencapai mortalitas 100%
yaitu 1,5 jam, sedangkan F1 dan F9 merupakan sub fraksi yang mortalitas
larvanya tidak mencapai 100%. Sub faksi lainnya yaitu F3, F4, F5, F6, F7 dan F8
berkisar antara 2- 6 jam untuk mendapatkan 100% mortalitas larva. Berdasarkan
pertimbangan kecepatan aplikasi, rendemen, kemurnian sub fraksi dan
pewarnaannya maka sub fraksi F2
Hasil pengujian sub fraksi F
merupakan sub fraksi yang potensial sebagai
kandidat senyawa aktif yang terpilih.
2 terhadap larva Ae.aegypti dengan beberapa
konsentrasi yaitu 0, 50, 100, 250, 500, dan 1000 ppm ditunjukkan gambar 5.
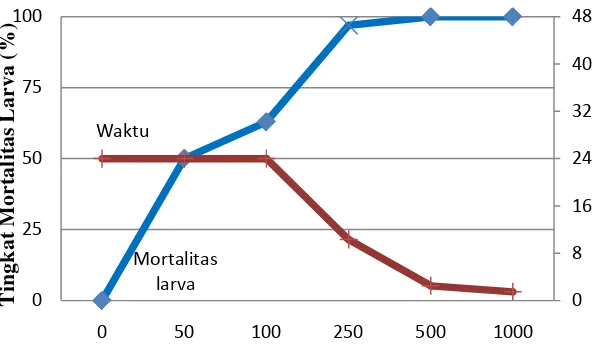
Gambar 5 Mortalitas larva Ae.aegypti pada beberapa konsentrasi sub fraksi F
Tingkat mortalitas larva meningkat dengan semakin bertambahnya
konsentrasi sub fraksi. `Pada konsentrasi 250 ppm 97% larva mati, sedangkan
pada 500 dan 1000 ppm semua larva mati dalam waktu yang cepat (< 2 jam).
Waktu yang dibutuhkan untuk mencapai mortalitas larva 100% semakin kecil
dengan meningkatnya konsentrasi sub fraksinya. Nilai perkalian antara
konsentrasi dan waktu (CT), merupakan ukuran yang sering digunakan pada
pengendalian serangga, dimana nilai CT ini dijadikan acuan kesuksesan
pengendalian serangga tersebut. Hal ini menyebabkan pada penggunaan
insektisida kimia akan menimbulkan pencemaran lingkungan yang lebih besar bila
menghendaki mortalitas serangga yang lebih cepat karena membutuhkan
konsentrasi yang lebih tinggi.
2
Penentuan Nilai Lethal Concentration (LC) Subfraksi F
Hasil analisis probit pada pengujian sub fraksi F
2
2 terhadap larvaAe.aegypti
dengan beberapa konsentrasi mendapatkan nilai LC50 dan LC90 seperti yang
ditunjukkan pada Tabel 5.
32
Tabel 5 Nilai LC50 dan LC90 Sub Fraksi F2
Lethal Concentration
LC 50 (ppm) LC 90 (ppm)
Sub Fraksi F2 57,8 180,7
Nilai LC50 sub fraksi F2 sebesar 57,8 ppm mendekati konsentrasi
terendah dari pengujian sub fraksi tersebut terhadap larva yaitu 50 ppm. Hal ini
menunjukkan bahwa LC50 dicapai konsentrasi yang hanya sedikit diatas
konsentrasi sub fraksi yang belum efektif membunuh larva. Sididiqui (2002)
melaporkan bahwa ekstrak daun mimba memiliki nilai LC50
Identifikasi Senyawa Aktif
sebesar 60 ppm
terhadap larva Anopheles stephensi.
Berdasarkan hasil pengukuran spektrum 1H-NMR memperlihatkan adanya asam
lemak dan gugus gliserol.Spektrum 1
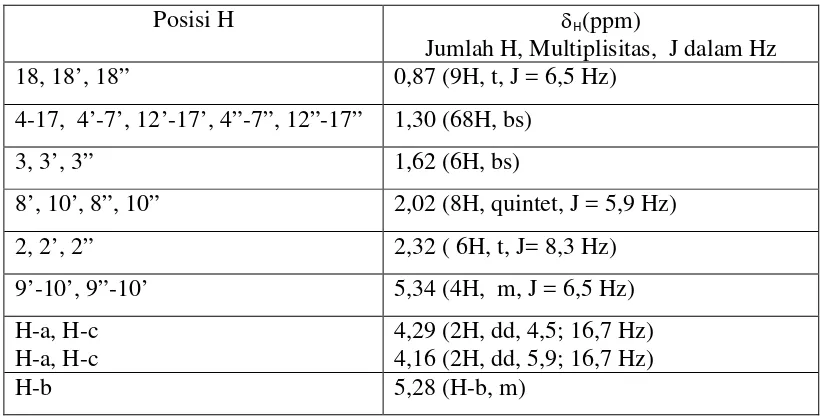
Tabel 6 Nilai Geseran Kimia Senyawa aktif (CDCl3, 500 MHz)
H-NMR ditampilkan pada Lampiran 6
sedangkannilai geseran kimia senyawa aktif ditunjukkan pada Tabel 6.
Posisi H δH
Jumlah H, Multiplisitas, J dalam Hz (ppm)
Adanya gugus metil (H-18, -CH3) suatu alifatik rantai panjang dengan
13 gugus metilen (-CH2-) muncul pada δH 1,30 (bs, 28 H), disamping 3 metilen
lain yang muncul pada daerah geseran kimia yaitu δH1,62 (bs, 2H), 2,02 (3 x 2H,
quintet, J = 5,9 Hz), dan 2,32 (3 x 2H, t, 8,3 Hz). Adanya 2 ikatan rangkap terlihat
padaδH 5,34 (4H, m, 6,5 Hz). Disamping itu adanya gugus gliserol ditunjukkan
pada δH
Spektrum
4,29 (H-a, 2H, dd, 4,5; 16,7 Hz) dan 4,16 (H-c, 2H, dd, 5,9; 16,7 Hz) serta
5,34 (H-b, 1H, m). Hal ini menunjukkan bahwa asam lemak yang terikat pada C-a
dan C-c mempunyai jenis asam lemak yang berbeda.
13
C-NMR pada Lampiran 3 menunjukkan kemungkinan jumlah
atom C sebanyak 57 buah yang tampak pada pergeseran 14,31 – 173,48 ppm.
Spektrum 13C-NMR juga menunjukkan ciri adanya asam lemak dan gugus
glicerol. Adanya gugus metil (C-18, -CH3) suatu alifatik rantai panjang dengan
melihat adanya gugus metilen (-CH2-) muncul padaδC 29,3 – 29,9. Ikatan
rangkap terlihat padaδC130,39. Disamping itu adanya gugus gliserol pada 62,26
dan 69,05 serta adanya ester padaδc173,48. Hal ini juga dipekuat dengan hasil
prediksi, seperti pada Tabel 7.
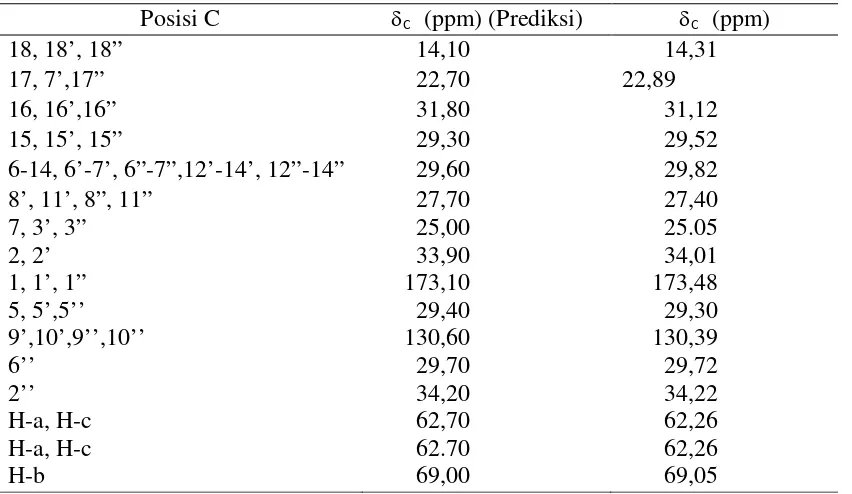
Tabel 7. Nilai Geserankimia senyawa aktif (13
34
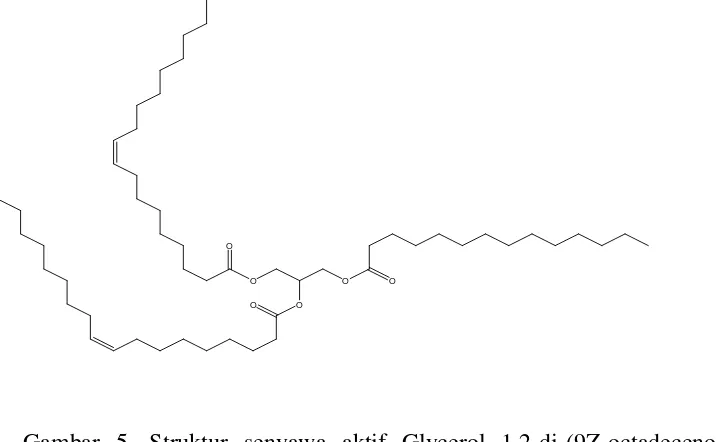
Berdasarkan analisa dari spektrum 1H-NMR dan 13C-NMR maka senyawa
aktif pada fraksi terlarut etil asetat tersebut adalah Glycerol
1,2-di-(9Z-octadecenoate) 3-tetradecanoate (C57H106O6) yang dikenal dengan nama
Dioleomyristin. Hal ini didukung dengan data nilai geseran kimia hasil prediksi
dengan menggunakan ChemDraw Ultra 10.0 seperti terlihat pada gambar 5.
O
O
O O
O O
Gambar 5. Struktur senyawa aktif Glycerol 1,2-di-(9Z-octadecenoate) 3-tetradecanoate
Hasil identifikasi dan pengujian terhadap larva menunjukkan bahwa
senyawa Glycerol 1,2-di-(9Z-octadecenoate) 3-tetradecanoate memiliki aktifitas
larvisida yang kuat terhadap larva Ae. aegypti. Senyawa ini termasuk senyawa non
polar karena terdapat bentuk ester dan trigliserid. Siddiqui (2002) melaporkan
bahwa 22, 23-dihydronimocinol dan desfurano-6a-hydroxyazadiradione
merupakan senyawa yang berhasil diisolasi dari daun mimba yang memiliki
aktifitas larvisida.
Penelitian terhadap tanaman mimba menunjukkan bahwa azadirachtin dan
minyak mimba secara bersama-sama memiliki efikasi yang lebih tinggi dalam
mengendalikan kutudaun dibandingkan efektivitas masing-masing senyawa
tersebut. Hal tersebut disebabkan karena minyak mimba membantu penyebaran
bahan aktif pada permukaan kulit serangga dan berpenetrasi. Senyawa – senyawa
aktif pada tanaman mimba bekerja melalui sistem pencernaan atau kontak