Alsade Santoso Sihotang
SKRIPSI
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
i
Dengan ini saya menyatakan skripsi yang berjudul :
Biologi Reproduksi Ikan Bilis Thryssa hamiltonii (Famili Engraulidae) yang Tertangkap di Teluk Palabuharatu
adalah benar merupakan hasil karya sendiri dan belum diajukan dalam bentuk
apapun kepada perguruan tinggi manapun. Semua sumber data dan informasi yang
berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari
penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di
bagian akhir skripsi ini.
Bogor, Februari 2011
Alsade Santoso Sihotang
ii
Alsade Santoso Sihotang. C24050963. Biologi Reproduksi Ikan Bilis, Thryssa hamiltonii (Famili Engraulidae) yang Tertangkap di Teluk Palabuhanratu. Dibimbing oleh Yunizar Ernawati dan M. Mukhlis Kamal
Sumberdaya ikan pelagis kecil di Indonesia merupakan sumberdaya yang sangat melimpah dan banyak ditangkap untuk dikonsumsi masyarakat bila dibandingkan dengan tuna yang sebagian besar diekspor. Ikan bilis termasuk pelagis kecil yang dapat punah jika mengalami eksploitasi yang berlebihan. Salah satu indikasi dari tingginya eksploitasi terhadap populasi ikan bilis adalah berubahnya keragaan reproduksi ikan. Penelitian ini diharapkan dapat melihat biologi reproduksi ikan bilis dengan mengetahui pola pemijahan dan puncak musim pemijahan.
Pengambilan ikan contoh dilakukan di tempat pelelangan ikan (TPI) satu kali dalam sebulan selama waktu penelitian, yaitu Mei, Juni dan Juli. Panjang dan berat diukur langsung di tempat; kemudian sebagian ikan contoh dianalisis di laboratorium. Analisis laboratorium dilakukan di Laboratorium Bio-Makro, Departemen Manajemen Sumberdaya Perairan. Analisis data meliputi panjang dan berat ikan, faktor kondisi, tingkat kematangan gonad (TKG), indeks kematangan gonad (IKG), fekunditas, dan ukuran diameter telur. Kemudian data yang diperoleh dianalisis untuk melihat sebaran variasi pertumbuhan dan keragaan reproduksi ikan tersebut.
iii
ALSADE SANTOSO SIHOTANG C24050963
Skripsi
sebagai salah satu syarat untuk memperoleh
gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
iv
Judul : Biologi Reproduksi Ikan Bilis Thryssa hamiltonii (Famili Engraulidae) yang Tertangkap di Teluk Palabuhanratu
Nama Mahasiswa : Alsade Santoso Sihotang
Nomor Pokok : C24050963
Program Studi : Manajemen Sumberdaya Perairan
Menyetujui,
Komisi Pembimbing
Dr. Ir. Yunizar Ernawati, MS Dr. Ir. M. Mukhlis Kamal, M.Sc NIP 19490617 197911 2 001 NIP 19680914 1994031 1 00
Mengetahui,
Ketua Departemen Manajemen Sumberdaya Perairan
Dr. Ir. Yusli Wardiatno, M.Sc NIP 19660728 199103 1 002
v
Puji dan syukur ke hadirat Tuhan YME yang telah memberikan berkatnya
sehingga penulis dapat menyelesaikan usulan penelitian yang berjudul “Pengaruh
Tingkat Eksploitasi terhadap Keragaan Reproduksi Ikan bilis, Thryssa hamiltonii (Famili Engraulidae).
Proposal ini dibuat sebagai salah satu syarat untuk dapat melaksanakan
penelitian dan tugas akhir di Departemen Manajemen Sumberdaya Perairan,
Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Pada proposal ini
terbagi menjadi tiga bagian yaitu pendahuluan, tinjauan pustaka, dan metode
penelitian.
Atas tersusunnya proposal ini penulis mengucapkan terima kasih kepada Ibu
Dr. Ir. Yunizar Ernawati, M.S dan Bapak Dr. Ir. M. Mukhlis Kamal, M.Sc sebagai
pembimbing yang telah memberikan bimbingan dan arahan serta motivasi kepada
penulis dalam penyelesaian proposal ini. Akhir kata penulis menyadari masih
banyak kekurangan pada penyusunan proposal ini. Oleh karena itu, penulis sangat
mengharapkan saran dan bantuan dari berbagai pihak, sehingga proposal ini dapat
bermanfaat bagi penulis khususnya dan pembaca pada umumnya.
Bogor, Februari 2011
vi
Pada kesempatan ini penulis mengucapkan terima kasih yang sebesar-besarnya
kepada :
1. Dr. Ir. Yunizar Ernawati, MS. dan Dr. Ir. M. Mukhlis Kamal, M.Sc.
masing-masing selaku ketua dan anggota pembimbing skripsi dan akademik yang telah
banyak memberikan bantuan berupa bimbingan, masukan dan dana dalam
penyelesaian skripsi ini.
2. Dr. Ir. H. Ridwan Affandi, DEA selaku dosen penguji dan Ir. Agustinus M.
Samosir, M.Phil selaku wakil komisi pendidikan program S1 atas saran dan
arahan dalam perbaikan skripsi ini.
3. Majariana Krisanti S.Pi, M.Si. selaku dosen pembimbing akademik atas
bimbingannya selama kuliah di MSP.
4. Papa dan Mama serta seluruh keluargaku tersayang atas segala doa dan perhatian
yang begitu kuat.
5. Para staff Tata usaha MSP, trutama mba widar atas kesabarannya dalam
membantu saya, staf Lab. Biologi Makro I (BIMA-I), Egg Team (Ega Rikky,
dan Anhar) dan teman-teman MSP42 terutama teman sekontrakan baut berkarat.
6. Tita Antari yang selalu setia menemani dan teman-teman Dragon yang selalu
memberikan hiburan dan kelucuan.
vii
Penulis dilahirkan di Bogor, pada tanggal 11 Agustus
1987. Penulis adalah anak keempat dari empat bersaudara dari
keluarga Bapak S. Sihotang dan Ibu Dasima Br Sinaga. Penulis
memulai masa pendidikannya di TK Harapan Putra Utama
Depok, kemudian bersekolah di SD Negeri Baktijaya 01
Cimanggis-Depok pada tahun 1993-1999, dilanjutkan ke jenjang
sekolah lanjutan di SLTPN 8 Depok, kemudian SMUN 88 Jakarta Timur pada tahun
2002-2005. Penulis diterima di Insitut Pertanian Bogor (IPB) melalui jalur SPMB
pada tahun 2005 dan masuk di Departemen Manajemen Sumberdaya Perairan,
Fakultas Perikanan Dan Ilmu Kelautan, Institut Pertanian Bogor (FPIK-IPB).
Penulis pernah menjadi pemain terbaik pada kejuaraan futsal tingkat TPB,
kemudian penulis juga terdaftar sebagai anggota Persekutuan Mahasiswa Kristen
(PMK) IPB tahun 2006, klub basket IPB, dan anggota Himpunan Mahasiswa
Manajemen Sumberdaya Perairan (HIMASPER) tahun 2007-2008.
Untuk menyelesaikan studi di Fakultas Perikanan dan Ilmu Kelautan dan
mendapatkan gelar Sarjana Perikanan, penulis melaksanakan penelitian yang
viii
2.3.2 Indeks kematangan gonad dan tingkat kematangan gonad ... ... 10
3.3.1 Pengambilan ikan contoh... 15
3.3.2 Pengamatan ikan contoh di laboratorium ... 15
3.3.2.1 Panjang dan berat total ...…… 15
3.3.2.2 Jenis kelamin dan tingkat kematangan gonad (TKG)...…… 15
3.3.2.3 Indeks kematangan gonad (IKG) ...……… 16
3.3.2.4 Fekunditas ...…… 16
3.3.2.5 Diameter telur ... 17
3.4 Analisis Data ... . 17
3.4.1 Aspek pertumbuhan ……… 17
3.4.1.1 Sebaran frekuensi panjang ...…... 17
3.4.1.2 Hubungan panjang-berat ...……….. 18
3.4.1.3 Faktor kondisi ………... 19
3.4.2 Aspek reproduksi ………. 20
ix
3.4.2.3 Nisbah kelamin... 22
3.4.2.4 Kadar protein (cara Kjeldahl in AOAC 2005)… 22 4. HASIL DAN PEMBAHASAN ... 23
4.1 Kondisi Lingkungan Teluk Palabuhanratu …………... 23
4.2 Aspek Pertumbuhan ... 23
4.2.1 Sebaran frekuensi panjang ikan bilis (Thryssa hamiltonii) hasil tangkapan ... 23
4.2.2Hubungan panjang berat... 25
4.2.3Faktor kondisi ……….. 26
4.3Aspek Reproduksi ... 30
4.3.1Nisbah kelamin ... 30
4.3.2 Tingkat kematangan gonad ... 30
4.3.3 Indeks kematangan gonad ... 34
4.3.4 Fekunditas ... 35
4.3.5 Diameter telur ... 40
4.3.6 Kandungan protein ... 41
4.4 Alternatif Pengelolaan ……… 42
5. KESIMPULAN DAN SARAN ... 44
DAFTAR PUSTAKA... 45
x
1. Klasifikasi tingkat kematangan gonad ikan tembang
(Clupea platygaster) menurut Ismail (2006) ... 16
2. Faktor kondisi ikan Bilis (T. hamiltonii) jantan dan betina yang tertangkap di Teluk Palabuhanratu ………….. 27
3. Hubungan faktor kondisi dengan tingkat kematangan gonad ikan bilis (T. hamiltonii) betina……….. 29
4. Rasio kelamin ... 30
5. Fekunditas T. hamiltonii pada bulan Mei ... 36
6. Fekunditas T. hamiltonii pada bulan Juni ... 37
7. Fekunditas T. hamiltonii pada bulan Juli ... 38
xi
1. Skema pendekatan masalah ... 2
2. Ikan bilis (T. hamiltonii, Gray 1835)... 5
3. Hubungan panjang dan berat pada ikan (Effendie, 2002)... 7
4. Peta lokasi pengambilan ikan contoh... 14
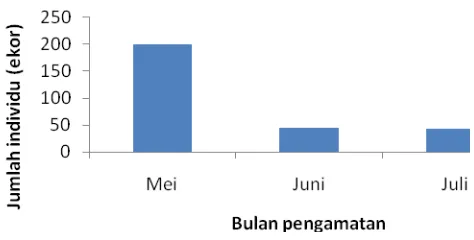
5. Sebaran jumlah ikan bilis selama bulan pengamatan (Mei-Juli) ……… 24
6. Sebaran frekuensi panjang ... 24
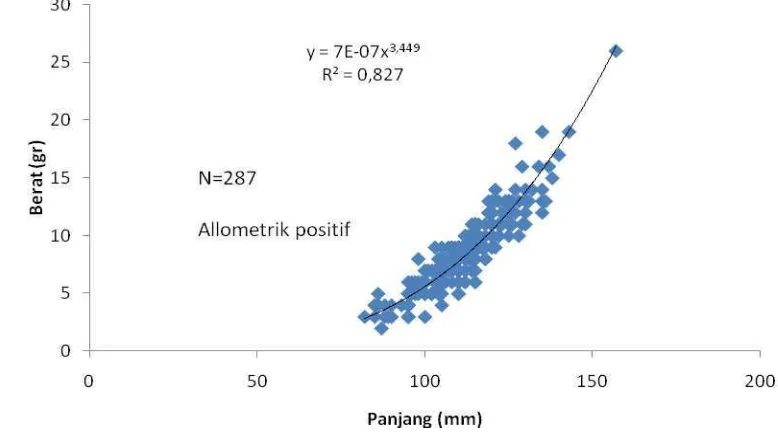
7. Hubungan panjang dan berat ... 26
8. Sebaran Faktor kondisi ikan Bilis (T. hamiltonii) betina... 27
9. Sebaran Faktor kondisi ikan Bilis (T. hamiltonii) jantan... 28
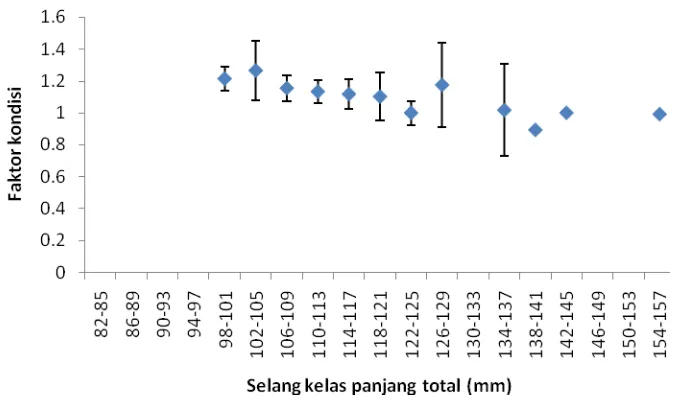
10. Nilai faktor kondisi berdasarkan selang kelas panjang betina.. 29
11. Histologis Gonad TKG I, II, III, dan IV ikan Bilis (T. hamiltonii) ... 32
12. TKG ikan bilis betina berdasarkan selang kelas panjang……. 33
13. Persentase TKG berdasarkan bulan pengamatan……….. 33
14. Indeks kematangan gonad ……….. 35
15. Grafik hubungan fekunditas dengan panjang dan berat (Mei 2009) …...… 36
16. Grafik hubungan fekunditas dengan panjang dan berat (Juni 2009) ………. 37
17. Grafik hubungan fekunditas dengan panjang dan berat (Juli 2009) ……….. 39
18. Grafik sebaran diameter telur ikan Bilis (T. hamiltonii) pada TKG IV ……….. 40
xii
1. Gambar alat dan bahan yang digunakan selama
melakukan penelitian ………. 50
2. Proses pembuatan preparat histologis gonad ikan kresek (Thryssa mystax) menurut
Banks (1986) in Fatimah (2006) ... 51 3. Metode penentuan kadar protein
berdasarkan AOAC (2005) ... 53
4. Tabel data frekuensi ikan bilis (T. hamiltonii)
setiap bulannya berdasarkan sebaran ukuran kelas panjang……… 54
5. Uji t hubungan panjang berat ikan bilis (T. hamiltonii)
pada bulan pengamatan (Mei-Juli)………... 55
6. Nilai-nilai faktor kondisi ikan bilis (T. hamiltonii)
pada setiap bulannya di Perairan teluk Palabuhanratu………. 56
7. Frekuensi Tingkat Kematangan Gonad berdasarkan selang kelas ukuran panjang ikan bilis (T. hamiltonii)
di Perairan teluk Palabuhanratu pada bulan pengamatan (Mei-Juli)... 57
8. Ukuran pertama kali matang gonad ikan bilis (T. hamiltonii) ……… 58 9. Nilai rata-rata indeks kematangan gonad (IKG) ikan bilis
(T. hamiltonii) pada setiap bulannya di Perairan teluk Palabuhanratu.. 59 10.Sebaran frekuensi diameter telur ikan bilis (T. hamiltonii)
selama bulan pengamatan (Mei-Juli) ……… 59
11.Perhitungan tinggi tubuh ikan bilis (T. hamiltonii)
pada ukuran pertama kali matang gonad ……… 60
12.Sebaran rata-rata diameter telur ikan bilis (T. hamiltonii)
I. PENDAHULUAN
1.1.Latar Belakang
Sumberdaya ikan pelagis kecil di Indonesia merupakan salah satu sumberdaya yang paling melimpah dan paling banyak ditangkap untuk konsumsi masyarakat bila
dibandingkan dengan tuna yang sebagian besar merupakan produk unggulan ekspor
sehingga hanya sebagian kelompok yang dapat menikmatinya. Ikan pelagis umumnya
hidup di daerah neritik dan membentuk schooling juga berfungsi sebagai konsumen
dalam food chain (antara produsen dengan ikan-ikan besar) sehingga perlu upaya
pelestarian (Merta, et al., 1988 in Widodo, 1998).
Ikan bilis yang juga termasuk ke dalam ikan pelagis kecil mampu
memperbaharui dirinya namun kemampuan ini bukan tidak terbatas, bahkan dapat
luruh bila dilakukan eksploitasi yang berlebihan. Sebagian sumberdaya yang
pemanfaatannya bersifat terbuka dan pemiliknya umum, diperlukan adanya usaha
pengelolaan yang mengatur pemanfaatan, pelestarian dan bila diperlukan juga
rehabilitasi. Sebab kelangkaan pengelolaan akan mengarah terjadinya "biological
overfishing", yaitu bila hasil penangkapan terhadap satu jenis ikan laut lebih besar dari
MSY (Maximum Sustainable Yield) untuk populasi ikan tersebut. Ikan – ikan yang
besar (dewasa) selalu ditangkap oleh nelayan. Penangkapan yang dilakukan juga
terlalu cepat sehingga ikan – ikan yang lain tidak diberi kesempatan untuk tumbuh
hingga usia yang optimal untuk melakukan reproduksi. Kejadian tersebut akan
memaksa ikan yang sudah dapat memijah untuk menghasilkan telur-telur dengan
kualitas kurang baik pada musim pemijahan dikarenakan ikan – ikan tersebut belum
mencapai usia optimum untuk melakukan pemijahan (Widodo, 1998).
Biologi reproduksi dapat dilihat pada ikan betina karena pengaruh dari betina
lebih tinggi terhadap keberhasilan reproduksi ikan. Penelitian ini diharapkan dapat
melihat biologi reproduksi ikan bilis dengan mengetahui pola pemijahan dan puncak
musim pemijahan sehingga diharapkan dapat menjadi dasar informasi dalam
1.2.Perumusan Masalah
Ikan bilis bukan merupakan target utama tangkapan pada daerah teluk
Palabuhanratu dan digolongkan ke dalam sumberdaya ikan ekonomis. Akan tetapi
apabila setiap upaya penangkapan selalu dijumpai ikan bilis dan tidak jarang pula pada
ikan yang matang gonad serta siap memijah juga ikut tertangkap, dikhawatirkan dapat
menyebabkan penurunan pertumbuhan populasi.
Hal ini dapat mempengaruhi pada masa yang akan datang kehidupan ikan bilis
akan terancam, baik berupa kepunahan maupun degradasi genetis. Oleh sebab itu jenis
ikan ini perlu dilestarikan melalui pengelolaan habitat dan populasi yang rasional.
Untuk hal tersebut diperlukan informasi dan data tentang keadaan reproduksinya,
karena dalam pengelolaan untuk menjamin kelestarian sumberdaya maka reproduksi
berperan untuk mengetahui ukuran pertama kali ikan matang gonad. Informasi hasil
dari penelitian ini diharapkan dapat digunakan sebagai dasar dan menjadi acuan dalam
upaya pengelolaan sumberdaya ikan bilis yang lestari dan berkelanjutan.
Gambar 1. Skema perumusan masalah
1.3.Tujuan dan Manfaat
Penelitian ini bertujuan untuk mendapatkan informasi mengenai biologi
reproduksi ikan bilis (T. hamiltonii) yang tertangkap di Teluk Palabuhanratu, seperti
nisbah kelamin, tingkat kematangan gonad, indeks kematangan gonad, fekunditas,
diameter telur dan kandungan protein.
Hasil penelitian ini diharapkan dapat menjadi sumber informasi mengenai
biologi reproduksi ikan bilis (T. hamiltonii) yang tertangkap di Teluk Palabuhanratu,
sehingga hasil penelitian ini juga dapat menjadi salah satu pertimbangan untuk
menetapkan strategi pengelolaan yang efektif.
2.1 Klasifikasi, Tata Nama dan Ciri-ciri Morfologi
Klasifikasi ikan bilis (Thryssa hamiltonii) berdasarkan tingkat sistematikanya
menurut Gray (1835):
Kingdom : Animalia
Filum : Chordata
Subfilum : Vertebrata
Kelas : Actinopterygii
Subkelas : Neopterygii
Ordo : Clupeiformes
Subordo : Clupeoidei
Famili : Engraulidae
Subfamili : Coilinae
Genus : Thryssa
Spesies : Thryssa hamiltonii
Sinonim : Engraulis grayi, Thryssa hamiltoni, Stolephorus hamiltoni, Engraulis
nasuta
Nama umum : Hamilton's thryssa, Hamilton's anchovy
Nama lokal : Bilis
Ikan-ikan jenis famili Engraulidae tersebar di perairan Atlantik, Hindia dan
Pasifik dan termasuk jenis ikan yang suka bergerombol (schooling). Beberapa spesies
dapat hidup di air tawar. Memiliki mulut inferior dengan tubuh yang tembus
cahaya/jernih. Sebagian besar ikan famili ini adalah filter feeding zooplankton. Famili
Engraulidae selanjutnya terdapat kelas Actinopterygii dan ordo Clupeiformes yang
Gambar 2. Ikan bilis (T. hamiltonii, Gray 1835)
Ciri-ciri Ikan bilis (T. hamiltonii) yaitu, memiliki bentuk badan memanjang dan
pipih. Badan bersifat fusiform, pipih, ukuran maksimum yang dapat dicapai hingga 27
cm SL dengan ukuran rata-rata yang sering tertangkap adalah sebesar 15,2-22,2 cm
SL. Ikan bilis tidak memiliki dorsal spine maupun anal spine namun terdapat 32-39
anal soft rays. Pada bagian perut meruncing dengan 23-26 scute yang terbalik hingga
anus (Gray, 1835).
Ikan merupakan organisme yang bersifat poikiloterm yaitu suhu tubuh ikan
sesuai dengan suhu perairan. Huet (1971) menyatakan fluktuasi harian suhu perairan
sangat mempengaruhi kehidupan organisme di dalamnya, fluktuasi suhu air yang
terlalu besar dapat mematikan organisme perairan. Bishop (1973) menyatakan suhu air
dapat merangsang dan mempengaruhi pertumbuhan organisme perairan serta
mempengaruhi oksigen terlarut untuk respirasi. Setiap organisme mempunyai suhu
maksimum, optimum dan minimum untuk kehidupannya, Menurut Boyd dan Kopler
(1979) suhu optimum untuk pertumbuhan ikan di daerah tropis adalah 25 oC- 30 oC.
Ikan Bilis biasa hidup pada perairan pelagis-neritik dengan kedalaman rata-rata
10-13 m. Iklim yang cocok adalah tropis. Ikan ini biasanya ditangkap dengan trawl
dan termasuk ikan ekonomis penting. Pemanfaatannya untuk ikan segar konsumsi,
kering, ikan asin. Makanan utamanya adalah zooplankton dan beberapa jenis
crustaceans. Ikan ini memiliki ciri-ciri telur yang berbentuk bola, transparan,
Distribusi ikan bilis secara ekologis terdapat di daerah tropis dan sub tropis,
hidup di laut pada kedalaman 40 m, estuaria dan sebagian masuk ke arah sungai.
Secara geografis penyebaran ikan tetet meliputi Sumatera (Sungai Rokan, Deli, Pulo
Weh, Simalur, Nias), Jawa (Jakarta, Jawa Barat), Kalimantan, Sulawesi, Papua Nugini,
Pantai India, Andamans, Malaysia, Laut Cina Selatan, Filipina, dan Australia
(www.fishbase.org).
2.2 Aspek Pertumbuhan
2.2.1 Hubungan panjang-berat
Panjang tubuh sangat berhubungan dengan berat tubuh. Hubungan panjang dan
berat seperti hukum kubik, berat merupakan pangkat tiga dari panjang (Effendie,
2002). Namun, hubungan yang terdapat pada ikan tidak demikian karena bentuknya
yang berbeda-beda. Menurut Moyle dan Cech (1988) pertumbuhan terjadi karena
adanya energi yang berlebih dari hasil metabolisme dalam tubuh. Proses metabolisme
ini dikontrol secara internal oleh hormon pertumbuhan dan hormon steroid. Selain itu,
pertumbuhan ikan dipengaruhi oleh faktor lingkungan seperti temperatur, tingkat
oksigen terlarut, ammonia, salinitas, dan periode sinar juga derajat kompetisi, jumlah
dan kualitas makanan yang dicerna.
Panjang dan berat ikan bila diplotkan dalam suatu gambar maka akan kita
dapatkan seperti Gambar 3. Terdapat dua jenis hubungan, yaitu pertambahan panjang
ikan atau udang yang seimbang dengan pertambahan beratnya, yang disebut
pertumbuhan isometrik. Apabila harga konstanta n lebih besar atau lebih kecil dari 3,0
dinamakan pertumbuhan allometrik. Harga konstanta n yang kurang dari 3,0
menunjukkan keadaan ikan yang kurus yaitu pertambahan panjangnya lebih depat dari
pertambahan beratnya, sedangkan harga konstanta n lebih besar dari 3,0 menunjukkan
2.2.2 Faktor kondisi
Faktor kondisi adalah keadaan yang menyatakan kemontokan ikan yang
dinyatakan dengan angka-angka berdasarkan data panjang dan berat (Lagler, 1961 in
Effendie, 2002). Faktor kondisi menunjukkan keadaan ikan baik dilihat dari segi
kapasitas fisik untuk bertahan hidup dan bereproduksi. Tingkat kematangan gonad dan
jenis kelamin mempengaruhi nilai faktor kondisi. Nilai faktor kondisi ikan betina lebih
besar dari ikan jantan, hal ini memperlihatkan bahwa ikan betina memiliki kondisi
yang baik dengan mengisi sel kelamin (cell sex) untuk proses reproduksinya
dibandingkan dengan ikan jantan. Nilai faktor kondisi antara 1-3 menunjukkan bahwa
tubuh ikan berbentuk kurang pipih (Effendie, 2002).
Faktor kondisi dapat dijadikan indikator kondisi pertumbuhan ikan dan dapat
menentukan kecocokan lingkungan serta membandingkan berbagai tempat hidup.
Variasi faktor kondisi tergantung pada kepadatan populasi, tingkat kematangan gonad,
makanan, jenis kelamin, dan umur (Le Cren, 1951 in Effendie, 2002). Sementara itu,
Lagler (1972) menyatakan bahwa dengan meningkatnya ukuran ikan maka nilai faktor
kondisinya akan bertambah dengan asumsi faktor lain tidak ada yang mempengaruhi.
Berat (gram)
Ketersediaan makanan akan mempengaruhi faktor kondisi. Pada saat makanan
berkurang jumlahnya, ikan akan menggunakan cadangan lemaknya sebagai sumber
energi selama proses pematangan gonad dan pemijahan sehingga faktor kondisi ikan
menurun (Rininta, 1988 in Saadah, 2000). Berdasarkan hasil penelitian Saadah (2000)
di perairan Teluk Labuan bahwa faktor kondisi ikan L. splendens betina lebih besar
dari ikan jantan. Sementara di perairan Pantai Mayangan, faktor kondisi ikan L.
equulus jantan lebih besar daripada ikan betina dan berfluktuatif berdasarkan bulan,
ukuran panjang, dan tingkat kematangan gonad (Novitriana, 2004).
2.3 Aspek Reproduksi
Pengelolaan sumberdaya perikanan untuk menjaga kelestariannya tidak hanya
terpusat pada aspek produksi ikannya, melainkan juga pada aspek biologi ikan dan
faktor lingkungan hidupnya (Samuel & Ondara 1987). Nikolsky (1963)
mengemukakan bahwa beberapa aspek biologi reproduksi diperlukan untuk
penelaahan frekwensi pemijahan, keberhasilan pemijahan, lama pemijahan dan ukuran
ikan pada saat pertama kali mencapai kematangan gonad.
2.3.1 Fekunditas
Fekunditas ikan merupakan aspek yang berhubungan dengan dinamika
populasi, sifat-sifat rasial, produksi dan stok rekruitmen (Bagenal 1978 in Effendie
2002). Fekunditas merupakan kemampuan reproduksi ikan yang ditunjukkan dengan
jumlah telur yang ada dalam ovarium ikan betina. Secara tidak langsung melalui
fekunditas ini kita dapat menaksir jumlah anak ikan yang akan dihasilkan dan akan
menentukan pula jumlah ikan dalam kelas umur yang bersangkutan. Menurut Nikolsky
(1963) jumlah telur yang terdapat dalam ovarium ikan dinamakan fekunditas individu.
Dalam hal ini ia memperhitungkan telur yang ukurannya berlain-lainan. Oleh karena
itu dalam memperhitungkannya harus diikutsertakan semua ukuran telur dan
masing-masing harus mendapatkan kesempatan yang sama. Bila ada telur yang jelas kelihatan
ukurannya berlainan dalam daerah yang berlainan dengan perlakuan yang sama harus
adalah jumlah telur dari generasi tahun itu yang akan dikeluarkan tahun itu pula.
Dalam ovari biasanya ada dua macam ukuran telur, yang besar dan yang kecil. Telur
yang besar akan dikeluarkan pada tahun itu dan yang kecil akan dikeluarkan pada
tahun berikutnya. Namun apabila kondisi baik, telur yang kecilpun akan dikeluarkan
menyusul telur yang besar. Sehubungan dengan hal ini maka perlu menentukan
fekunditas ikan apabila ovari ikan itu sedang dalam tahap kematangan yang ke-IV dan
yang paling baik sesaat sebelum terjadi pemijahan (Nikolsky, 1963).
Semakin banyak makanan tersedia, pertumbuhan ikan semakin cepat dan
fekunditas semakin besar. Fekunditas ikan berhubungan erat dengan lingkungan
dimana fekunditas spesies akan berubah bila keadaan lingkungan berubah (Nikolsky,
1963). Fekunditas cenderung meningkat dengan ukuran tubuh yang besar, sehingga
populasi dengan proporsi ikan berukuran besar memiliki potensi reproduksi yang lebih
besar dibandingkan dengan populasi dengan proporsi ikan yang berukuran kecil
(Walker et al.,1998 in Stevens et al., 2000). Fekunditas individu akan sukar diterapkan
untuk ikan-ikan yang mengadakan pemijahan beberapa kali dalam satu tahun, karena
mengandung telur dari berbagai tingkat dan akan lebih sulit lagi menentukan telur
yang benar-benar akan dikeluarkan pada tahun yang akan datang. Jadi fekunditas
individu ini baik diterapkan pada ikan-ikan yang mengadakan pemijahan tahunan atau
satu tahun sekali. Selanjutnya Royce (1984) menyatakan bahwa fekunditas total ialah
jumlah telur yang dihasilkan ikan selama hidupnya. Fekunditas relatif adalah jumlah
telur per satuan berat atau panjang. Fekunditas inipun sebenarnya mewakili fekunditas
individu kalau tidak diperhatikan berat atau panjang ikan. Status ikan betina dan
kualitas dari telur lebih terlihat kalau berat yang dipakai tanpa berat alat-alat
pencernaan makanannya. Ikan-ikan yang tua dan besar ukurannya mempunyai
fekunditas relatif lebih kecil. Umumnya fekunditas relatif lebih tinggi dibanding
dengan fekunditas individu. Fekunditas relatif akan menjadi maksimum pada golongan
ikan yang masih muda (Nikolsky, 1969 in Effendie, 2002).
Seperti contoh pada ikan L. equulus di perairan Mayangan. Ikan tersebut memiliki
fekunditas berkisar 1.496-157.845 butir dan dijumpai hubungan yang erat terhadap
(Novitriana, 2004). Sementara di perairan Barat Daya Taiwan rata-rata fekunditas ikan
L. equulus adalah 129.955 ± 79.343 (Fang Lee et al., 2005).
2.3.2 Indeks kematangan gonad dan tingkat kematangan gonad
Dalam proses reproduksi, sebelum terjadi pemijahan gonad semakin bertambah
besar dan berat. Berat gonad akan mencapai maksimum sesaat ikan memijah,
kemudian menurun dengan cepat selama pemijahan sampai selesai (Effendie, 2002).
Untuk mengetahui perubahan gonad tersebut secara kualitatif dapat dinyatakan dengan
index kematangan gonad (IKG). IKG adalah suatu nilai dalam persen sebagai hasil
perbandingan berat gonad dengan berat tubuh ikan termasuk gonad dikalikan 100 %
(Effendie, 2002). IKG ini akan bertambah besar sampai mencapai maksimum ketika
akan terjadi pemijahan (Effendie, 2002). Royce (1984), mencatat bahwa ikan dapat
memijah, jika nilai IKG betina berkisar antara 10%-25%. Nilai IKG jantan berkisar
antara 5 % - 10 %.
Salah satu aspek biologi reproduksi ialah tingkat kematangan gonad (TKG)
yaitu tahap-tahap tertentu perkembangan gonad sebelum dan sesudah ikan memijah.
Keterangan tentang TKG ikan diperlukan untuk mengetahui perbandingan antara ikan
yang berada diperairan, ukuran atau unsur ikan pertama kali matang gonadnya, dan
apakah ikan sudah memijah atau belum (Nikolsky, 1963 dan Effendie, 2002).
Marza (1938), Wallace dan Selman (1981) in Murua (2003) membagi tiga tipe
perkembangan oosit, yaitu :
1. Synchronous, yaitu semua oosit yang ada di dalam ovarium mengalami tingkat
kematangan yang sama.
2. Group-synchronos, yaitu ovarium memiliki dua kelompok oosit dengan
tingkat kematangan yang berbeda.
3. Asynchronous, yaitu ovarium yang menganduung oosit yang memiliki tingkat
kematangan yang berbeda dan proses oogenesis berlangsung setiap saat.
Semakin meningkat TKG ikan, umumnya garis tengah telur yang ada dalam
gonad semakin besar. Dengan kata lain ukuran dan berat gonad serta garis tengah telur
pula bahwa saat ikan pertama kali mencapai matang gonad dipengaruhi oleh beberapa
faktor luar seperti suhu, arus, adanya individu yang berjenis kelamin yang berbeda dan
faktor dalam seperti umur, ukuran dan perbedaan spesies. Seperti di perairan Barat
Daya Taiwan pada ikan L. equulus betina matang gonad pada saat panjang cagaknya
162 mm dan ikan jantan pada panjang cagak 158 mm (Fang Lee et al., 2005).
Menurut Weng et al. (2005), dari analisis makroskopik perkembangan ovarian
ikan Spratelloides gracilis dapat dibagi kedalam 4 fase :
• Fase sebelum matang gonad (immature) : indung telur kecil dan langsing, dan oocyte tidak terlihat dengan mata biasa. Diameter oocyte < 0,2 mm, dan model
tunggal ditemukan dalam distribusi frekuensi diameter telur. Distribusi oocyte
belum berkembang secara acak, dan oogonia jarang ditemukan.
• Fase menuju matang gonad (maturing) : indung telur menjadi lebih besar dan
kekuning-kuningan. Rata-rata diameter oocyte < 0,4 mm. Model tunggal juga
ditemukan dalam distribusi frekuensi diameter telur.
• Fase matang gonad (mature) : indung telur sangat gembung dan
kekuning-kuningan, dan telur tembus cahaya. Diameter oocyte meningkat secara pesat.
Umumnya diameter oocyte yang ditemukan 0,6 – 0,9 mm. Ada dua model
dalam distribusi frekuensi diameter telur, yang lebih kecil pada 0,2 mm dan
satunya lagi pada 0,7 mm.
• Fase setelah matang gonad (spent) : indung telur kecil dan lembut. Beberapa
oocyte yang besar tidak dikeluarkan, ditemukan dekat kloaka. Diameter oocyte
> 0,6 mm. Oocyte ini secara normal akan diserap kembali, indeks kematangan
gonad berkisar antara 0,022 – 0,0395.
2.3.3 Nisbah kelamin
Nisbah kelamin merupakan perbandingan ikan jantan dan ikan betina dalam
suatu populasi, dengan kondisi nisbah kelamin yang ideal yaitu rasio 1:1 (Bal dan Rao,
dapat berubah menjelang dan selama pemijahan. Pada ikan yang melakukan ruaya
untuk memijah terjadi perubahan nisbah jantan dan betina secara teratur, yaitu pada
awalnya ikan jantan lebih banyak kemudian nisbah kelamin berubah menjadi 1:1 lalu
diikuti ikan betina lebih banyak (Nikolsky, 1963).
2.3.4 Diameter telur
Diameter telur adalah garis tengah atau ukuran panjang sebuah telur yang
diukur dengan mikrometer berskala yang sudah ditera dan dilihat dibawah mikroskop.
Diameter telur semakin besar pada tingkat kematangan gonad yang lebih tinggi
terutama saat mendekati waktu pemijahan (Johnson in Effendie, 2002). Selain itu,
adanya ukuran diameter telur yang beragam setiap spesies ikan dipengaruhi oleh faktor
genetik, lingkungan, ketersediaan makanan dan umur (Chamber dan Leggett, 1996)
Menurut Effendie (2002) ukuran telur biasanya dipakai untuk menentukan
kualitas kandungan kuning telur, telur yang berukuran besar akan menghasilkan larva
yang berukuran yang lebih besar daripada telur yang berukuran kecil. Lama penijahan
dapat diduga dari frekuensi ukuran diameter telur. Diameter telur digunakan untuk
melihat frekuensi pemijahan dari ikan-ikan dengan TKG III dan IV.
2.3.5 Kualitas telur
Ada empat komponen dominan pada telur yaitu chorion, ruang perivetelin
(perivetelliene space/PVS), kuning telur (yolk) dan OML (ovoplasm minus lipid)
(Vestergaard, 2002). Perbandingan komposisi kualitas telur dapat dibandingkan
dengan kandungan lemak di jaringan tubuh. Definisi kualitas telur yang umum
digunakan adalah kemampuan telur untuk menghasilkan benih yang baik. Potensi telur
untuk menghasilkan benih yang baik ditentukan oleh beberapa faktor, yakni faktor
fisik, genetik dan kimia selama terjadi proses perkembangan telur. Jika satu dari faktor
esensial ini tidak ada maka telur tidak berkembang dalam beberapa stadia. Beberapa
indikator kualitas telur adalah pembuahan, morfologi, ukuran dan kandungan kimia
Kondisi telur sangat menentukan bagaimana keberhasilan suatu proses
rekrutmen. Watanabe (2009) menyatakan bahwa kegagalan rekrutmen disebabkan
tingginya laju kematian (mortalitas) setelah tahap awal memakan. Selain itu, tingkat
mortalitas larva disebabkan oleh adanya predator dan kondisi lingkungan yang buruk.
Chambers dan Leggett (1996) menyatakan ukuran telur ikan capelin (Malotus villosus)
dan kemampuan larva untuk tetap bertahan dari kelaparan berhubungan langsung
dengan kondisi dan kandungan lemak induk ikan betina.
Material yang diperlukan selama perkembangan secara umum dapat dibagi
menjadi 1) diperlukan secara langsung untuk sintesis jaringan embrionik, dan 2)
digunakan untuk energi metabolisme. Kadar protein, lipid dan karbohidrat berkorelasi
positif terhadap kelangsungan hidup larva. Protein merupakan komponen dominan
kuning telur, sedangkan jumlah dan komposisinya menentukan besar kecilnya ukuran
telur (Kamler, 1992 in Utiah, 2006).
III. METODE PENELITIAN
Penelitian ini dilaksanakan pada bulan Mei sampai dengan Juli 2009. Lokasi
pengambilan ikan contoh adalah tempat pendaratan ikan (TPI) Palabuhanratu. Analisis
contoh dilakukan di Laboratorium Ekobiologi, Fakultas Perikanan dan Ilmu Kelautan,
Institut Pertanian Bogor. Berikut ini disajikan peta lokasi pengambilan ikan contoh
pada Gambar 4.
Gambar 4. Peta lokasi pengambilan ikan contoh
3.2 Alat dan Bahan
Alat yang digunakan, yaitu alat bedah, botol sampel, penggaris dengan
ketelitian 1 mm, timbangan digital untuk menimbang berat ikan (ketelitian 0,01 g),
cawan petri dan pipet tetes, mikrometer okuler, mikrometer objektif, gelas objek, gelas
ukur kapasitas 10 ml. Preparat histologi menggunakan mikrotom, oven, gelas objek
dan gelas penutup.
Bahan yang digunakan adalah ikan Bilis (T. hamiltonii), larutan Bouin larutan
formalin dengan konsentrasi 10% untuk mengawetkan ikan contoh, sedangkan untuk
mengawetkan gonad menggunakan larutan formalin formalin 4%.
3.3 Metode Kerja
3.3.1 Pengambilan ikan contoh
Pengambilan ikan contoh dilakukan di tempat pelelangan ikan (TPI) satu kali
dalam sebulan selama waktu penelitian. Pengukuran panjang dan berat diukur
langsung di tempat. Kemudian ikan contoh dianalisis di laboratorium terutama pada
ikan betina, yang sebelumnya diawetkan terlebih dahulu dengan formalin 10% dan
diawet segar untuk analisis proximat.
3.3.2 Pengamatan ikan contoh di laboratorium
3.3.2.1 Panjang dan berat total
Panjang total ikan diukur dari ujung kepala terdepan sampai ujung sirip ekor
paling belakang menggunakan penggaris dengan ketelitian 0,1 mm. Berat total ikan
didapat dengan menimbang berat seluruh tubuh ikan pada timbangan digital (ketelitian
0,01 g).
3.3.2.2 Jenis kelamin dan tingkat kematangan gonad (TKG)
Jenis kelamin diduga berdasarkan pengamatan gonad ikan contoh (Tabel 1).
Tingkat kematangan gonad ditentukan menggunakan klasifikasi tingkat kematangan
gonad menurut penelitian yang dilakukan oleh Ismail (2006) (Tabel 1).
Tabel 1. Klasifikasi tingkat kematangan gonad ikan tembang (Clupea platygaster) menurut Ismail (2006).
TKG Jantan Betina
I Testis seperti benang dengan warna putih susu.
bervariasi antara – panjang rongga
tubuh.
II Ukuran testis lebih besar, bentuk lebih jelas dari TKG I.
Terdapat jaringan bewarma putih susu, telur masih menyatu dan belum dapat dipisahkan. Panjang gonad bervariasi antara – dari
panjang rongga tubuh.
III Ukuran testis semakin besar, bewarna putih kekuningan dan lebih jelas dibanding TKG III. Permukaan gonad tidak rata (berlekuk-lekuk), ujung posterior bergerigi.
Ukuran lebih besar, pada bagian anterior melebar dan bagian posterior meruncing, telur sudah dapat dipisahkan, bewarna lebih
gelap. Panjang gonad bervariasi antara –
dari panjang rongga tubuh.
IV Ukuran testis besar, warna testes putih, pejal dan gerigi semakin besar.
Diameter telur semakin besar dan jelas terlihat dibawah mikroskop, semua telur bewarna kuning. Panjang gonad bervariasi antara – dari panjang rongga tubuh.
V Permukaan testes berkerut, warna putih susu dan berbentuk kurang pejal dibanding dengan TKG IV.
Ovarium berkerut, butiran telur sisa terkumpul di posterior, ovarium bewarna kemerah-merahan.
3.3.2.3 Indeks kematangan gonad (IKG)
Untuk mengetahui perubahan yang terjadi pada gonad, tingkat perkembangan
ovarium, secara kuantitatif dapat dinyatakan dengan suatu Indeks Kematangan Gonad
(IKG) yaitu suatu nilai dalam persen sebagai hasil perbandingan berat gonad dengan
berat tubuh ikan dikalikan 100 persen (Effendie, 1979 in Hadiaty, 2000).
IKG = Wg / W x 100%
Wg = berat gonad ; W = berat tubuh
3.3.2.4 Fekunditas
Fekunditas dihitung hanya pada ovarium TKG III dan IV. Terlebih dahulu
ovarium dikeluarkan dari tubuh ikan, kemudian diawetkan dengan formalin
(konsentrasi 4%) dan dimasukan dalam larutan fisiologis. Dalam penghitungan, telur
diambil dari 3 bagian ovarium yaitu bagian anterior, median, dan posterior yang
dalam aquades 10 ml lalu telur diambil dengan pipet sebanyak 1 ml, tempatkan telur
dalam cawan petri kemudian hitung jumlah telur sebagai jumlah telur contoh.
3.3.2.5 Diameter telur
Diameter telur dilihat hanya dari ovarium TKG IV. Diambil 100 butir/ekor
ikan contoh dari fekunditasnya. Kemudian diamati menggunakan mikroskop dengan
perbesaran 10X10 yang dilengkapi dengan mikrometer okuler yang telah ditera dengan
mikrometer objektif, lalu dicatat diameter telurnya.
3.4 Analisis data
3.4.1 Aspek Pertumbuhan
3.4.1.1 Sebaran frekuensi panjang
Untuk mengetahui sebaran frekuensi panjang ikan (Walpole, 1995) diikuti
tahapan-tahapan :
a. Menentukan wilayah kelas, r = pb-pk (r = wilayah kelas, pb = panjang terbesar,
pk = panjang terkecil).
b. Menentukan jumlah kelas 1 + 3,32 log N (N = jumlah data).
c. Menghitung lebar kelas, L = r / jumlah kelas (L = lebar kelas, r = wilayah
kelas).
d. Memilih ujung bawah kelas interval
e. Menentukan frekuensi jumlah masing-masing selang kelas yaitu jumlah
frekuensi dibagi jumlah total dikalikan 100%.
Parameter pendugaan untuk mendapatkan nilai panjang maksimum (Linf) dan
koefisien pertumbuhan menggunakan perhitungan yang dilakukan dengan bantuan
program FISAT (FAO-ICLARM Stock Assesment Tools) II versi 1.2.2. Penentuan laju
eksploitasi (E) berdasarkan data ukuran panjang ikan yang dicatat di lapangan setiap
pengambilan contoh ikan. parameter-parameter laju mortalitas yang meliputi laju
mortalitas total (Z) digunakan model Beverton dan Holt berbasis data panjang dengan
)
K : koefisien pertumbuhan (per tahun) L∞ : panjang asimtotik (mm)
L’’ : panjang rata-rata ikan yang tertangkap (mm)
L’ : batas bawah dari interval kelas panjang tangkapan terbanyak (mm) Z : laju mortalitas total (pertahun)
3.4.1.2 Hubungan panjang-berat
Pola pertumbuhan ikan dapat diduga dengan melihat hubungan panjang dan
berat (Effendie, 1979). Analisis panjang dan berat bertujuan untuk mengetahui pola
pertumbuhan ikan di alam. Hubungan panjang berat digunakan persamaan
eksponensial sebagai berikut (Lagler, 1972) :
W = aL
bKeterangan :
W : berat total ikan (gram) L : panjang total ikan (mm) a dan b : konstanta hasil regresi
Untuk mempermudah perhitungan maka persamaan di atas dilogaritmakan
sehingga menjadi persamaan linear sebagai berikut :
log W = log a + b log L
Hubungan panjang berat dapat dilihat dari nilai konstanta b, bila b = 3 maka
hubungannya bersifat isometrik (pertambahan panjang sebanding dengan pertambahan
berat). Bila n ≠ 3 maka hubungan yang terbentuk adalah allometrik, jika b > 3 maka
hubungannya bersifat allometrik positif (pertambahan berat lebih dominan dari
bersifat allometrik negatif (pertambahan panjang lebih dominan dari pertambahan
beratnya).
Untuk menentukan bahwa nilai b = 3 atau tidak sama dengan 3, maka digunakan
uji-t, dengan rumus (Walpole, 1995) :
Thit =
Selanjutnya Thit yang didapat akan dibandingkan dengan Ttabel pada selang
kepercayaan 95%. Jika Thit > Ttabel, maka tolak Ho, dan sebaliknya jika Thit < Ttabel,
maka terima Ho.
3.4.1.3 Faktor kondisi
Menurut Effendie (2002) faktor kondisi dapat ditentukan berdasarkan panjang
dan berat ikan contoh. Rumus yang digunakan untuk mengetahui faktor kondisi
dibedakan berdasarkan pola pertumbuhan.
Apabila ikan memiliki pola pertumbuhan allometrik (b≠3), maka rumus yang
digunakan adalah :
b
aL W K =
Ikan yang memiliki pola pertumbuhan isometrik (b=3), maka rumus yang
L : panjang ikan (mm) W : berat ikan (gram) a dan b : konstanta hasil regresi
3.4.2 Aspek reproduksi
3.4.2.1 Fekunditas
Fekunditas ikan ditentukan dengan menggunakan metode gabungan antara metode
grafimetrik dan metode volumetrik dengan menggunakan rumus (Effendie, 1979) :
Keterangan :
Kemudian dilihat hubungan fekunditas dengan panjang total tubuh ikan dengan
rumus :
Keterangan :
F = fekunditas L = panjang total ikan (mm) a dan b = konstanta
Persamaan tersebut ditransformasikan kedalam persamaan logaritma sehingga
diperoleh bentuk linear atau persamaan garis lurus :
Log F = Log a + b Log L
Keterangan :
F = fekunditas Log a = y
Log b = x
Hubungan fekunditas dengan berat total tubuh ikan dilihat dengan rumus :
F = fekunditas
W = berat total ikan (g) a dan b = konstanta
Persamaan tersebut ditransformasikan ke dalam persamaan logaritma sehingga
diperoleh bentuk linear atau persamaan garis lurus :
Log F = Log a + b Log W
Keterangan :
F = fekunditas Log a = y
Log b = x
Keeratan hubungan antara panjang total ikan dan berat total ikan dengan
fekunditas diketahui dengan mencari koefisien korelasi (r).
3.4.2.2. Indeks kematangan gonad dan tingkat kematangan gonad
Nilai indeks kematangan gonad (IKG) dapat diketahui dengan menggunakan
rumus menurut Effendie (1979) :
Keterangan :
IKG = indeks kematangan gonad Bg = berat gonad (g)
Bt = berat tubuh total (g)
Penentuan tingkat kematangan gonad (TKG) dilakukan terhadap semua ikan
contoh yang diambil. Sementara untuk menduga ukuran pertama kali ikan matang
gonad berdasarkan selang kelas dimana terdapat ikan yang memiliki tingkat
kematangan gonad yang matang yakni gonad TKG IV dengan menggunakan rumus,
Rumus Spareman Karber :
Keterangan:
Xi = log nilai tengah pada saat ikan matang gonad X = selisih log nilai tengah kelas
Pi = Nb / Ni
Nb = jumlah ikan matang gonad pada kelas ke-i Ni = jumlah ikan pada kelas ke-i
Qi = 1 – Pi
3.4.2.3 Nisbah kelamin
Keterangan : M = jumlah ikan jantan (ekor) F = jumlah ikan betina (ekor)
Keseragaman sebaran nisbah kelamin dilakukan dengan uji “Chi-Square”
(Steel dan Torrie, 1980).
Keterangan : Oi = frekuensi ikan jantan dan betina yang diamati ke-i
ei = frekuensi harapan yaitu frekuensi ikan jantan + frekuensi ikan betina dibagi dua
X2 = nilai peubah acak X2 yang sebaran penarikan contohnya menghampiri sebaran Chi-square
3.4.2.4 Kadar protein (cara Kjeldahl in AOAC 2005)
Rumus menghitung kadar protein :
% N = vol.blanko- vol.titrasi NaOH sampel x N NaOH x 100% x 14.00
gram sampel x 1000
IV. HASIL DAN PEMBAHASAN
4.1. Kondisi Lingkungan Teluk Palabuhanratu
Perairan Palabuhanratu merupakan perairan berbentuk teluk yang terletak di
sebelah Selatan Jawa Barat. Secara geografis berada pada 6057’ – 7025’ LS dan 106049’
– 107000’ BT. Berdasarkan hasil wawancara dengan nelayan setempat, terdapat empat
periode musim penangkapan, yaitu musim barat (Desember-Februari), musim timur
(Juni-Agustus), dan dua periode musim peralihan (pancaroba). Musim peralihan terdiri
atas musim utara (Maret-Mei) merupakan peralihan dari musim barat ke musim timur
dan musim selatan (September-Nopember) yang merupakan musim peralihan dari
musim timur ke musim barat. Periode musim barat merupakan musim hujan dimana
kondisi perairan relatif buruk sehingga sebagian besar nelayan tidak melaut. Periode
musim timur merupakan musim kemarau dimana kondisi perairan relatif lebih tenang
sehingga nelayan banyak turun ke laut untuk melakukan penangkapan ikan.
Secara umum suhu permukaan air laut di Teluk Palabuhanratu berkisar antara 27 –
300C dan ini merupakan kisaran suhu yang optimum bagi pertumbuhan ikan tropis.
Arus di Teluk Palabuhanratu dipengaruhi oleh arus musim di pantai selatan Jawa
(Hartami, 2008). Berdasarkan hasil penelitian Atmadipoera et al. (1994) in Wiyono
(2001) bahwa kecepatan arus permukaan maksimum di Teluk Palabuhanratu adalah
sekitar 1,28 m/detik dengan arah timur-tenggara. Gelombang besar terjadi selama
musim Barat, sedangkan selama musim Timur kondisi perairan Palabuhanratu relatif
tenang. Menurut BLH Kabupaten Sukabumi dan PKSPL-IPB (2003) in Wahyudin
(2005) bahwa kondisi kualitas air di Teluk Palabuhanratu tergolong bagus tercermin
dari penampakan air yang bening dan kecerahan cahaya matahari dapat menembus
perairan mencapai 6-7 meter.
4.2 Aspek Pertumbuhan
4.2.1 Sebaran frekuensi panjang ikan bilis (T. hamiltonii) hasil tangkapan
Berdasarkan 3 kali pengambilan ikan contoh yang dilakukan per bulan selama
tiga bulan, dari bulan Mei - Juli. Pada Gambar 5 terlihat jumlah ikan contoh pada bulan
diambil sebanyak 45 ekor untuk dianalisis di laboratorium. Pada bulan Juni dan Juli
didapatkan sejumlah 44 ekor dan 43 ekor untuk diukur panjang dan beratnya, kemudian
masing-masing setiap bulannya diambil sebanyak 30 ekor untuk dianalisis di
laboratorium. Penurunan jumlah ikan bilis yang tertangkap disebabkan karena
sedikitnya jumlah nelayan yang melakukan aktivitas penangkapan pada bulan Juni-Juli.
Hal ini dikarenakan kondisi laut yang tidak memungkinkan nelayan untuk menangkap
ikan pada bulan tersebut. Keseluruhan ikan contoh yang didapatkan adalah sebesar 287
ekor untuk diukur panjang dan beratnya, dan 105 ekor untuk dianalisis di laboratorium.
Gambar 5. Sebaran jumlah ikan bilis selama bulan pengamatan (Mei-Juli)
Berdasarkan grafik sebaran frekuensi panjang (Gambar 6) ikan bilis (T.
hamiltonii) yang tertangkap memiliki kisaran panjang 82-157 mm. Pada bulan Mei
ukuran panjang minimum yang didapat adalah 82 mm dan ukuran panjang maksimum
130 mm. Pada bulan Juni dan Juli secara berturut-turut ukuran panjang terkecil yang
diperoleh adalah sebesar 108 mm dan 98 mm dan ukuran panjang terbesarnya adalah
157 mm dan 135 mm. Dengan bantuan program FISAT (FAO-ICLARM Stock
Assesment Tools) II versi 1.2.2. dengan berbasis data panjang didapat nilai panjang
maksimum yang mampu dicapai ikan bilis (T. hamiltonii) adalah sebesar (L∞) 161.7
mm dengan koefisien pertumbuhan (K) sebesar 0.55. Sedangkan menurut Gray (1835)
ikan Bilis dapat mencapai panjang maksimum hingga 222 mm. Hal ini dapat
mengidentifikasi bahwa ikan ini sudah mengalami perubahan struktur populasi.
Gambar 6 juga memperlihatkan adanya pergeseran modus kelas panjang dari
bulan Mei hingga Juli. Pada bulan Mei modus kelas panjang berada pada selang kelas
102-105 mm, kemudian pada bulan Juni modus bergeser ke kanan pada selang kelas
118-121 mm dan pada bulan Juli modus kelas panjang kembali bergeser ke kanan pada
selang kelas 122-125 mm. Pergeseran modus kelas panjang ini mengindikasikan adanya
pertumbuhan ikan bilis. Pertumbuhan tersebut diduga karena perbedaan musim yang
terjadi. Hal ini didukung oleh pernyataan Bishop (1973) bahwa suhu air dapat
merangsang dan mempengaruhi pertumbuhan organisme perairan serta mempengaruhi
oksigen terlarut untuk respirasi. Setiap organisme mempunyai suhu maksimum,
optimum dan minimum untuk kehidupannya. Sehingga dari pengamatan dapat
diindikasikan bahwa ikan Bilis memiliki waktu pertumbuhan optimum pada bulan Juli.
4.2.2. Hubungan panjang berat
Hubungan panjang-berat ikan bilis adalah W = 7x10-7 L3,449 dengan nilai
koefisien determinasi (R2) sebesar 0,827. Hal tersebut berarti bahwa model dugaan
mampu menjelaskan data sebesar 82,7% (Walpole, 1995). Dari nilai b yang diperoleh
dan setelah dilakukan uji t (α = 0,05) diketahui bahwa ikan bilis memiliki pola
pertumbuhan allometrik positif yang berarti bahwa pertambahan berat lebih cepat
pertumbuhan tersebut terkait erat dengan faktor lingkungan seperti suhu, jumlah dan
kualitas makanan yang dicerna, umur (Moyle dan Cech, 1988). Selain itu diperoleh
hubungan yang erat antara panjang-berat melalui nilai koefisien korelasi (r). Dengan
demikian dapat dikatakan bahwa pertambahan panjang ikan diikuti dengan pertambahan
bobotnya. Hal tersebut dipengaruhi oleh faktor musim (suhu) dan stok makanan yang
ada di daerah penangkapan ikan Bilis. Pernyataan tersebut didukung oleh Effendie
(2002) yang menyatakan pertumbuhan dipengaruhi oleh dua faktor yaitu faktor dalam
seperti keturunan, umur, jenis kelamin, hormon dan penyakit; serta faktor luar seperti
suhu perairan dan makanan.
Gambar 7. Hubungan panjang dan berat
4.2.3 Faktor kondisi
Penentuan nilai faktor kondisi didasarkan pada pola pertumbuhan. Pola
pertumbuhan ikan Bilis yang ditemukan selama waktu penelitian bersifat allometrik
positif. Kisaran nilai faktor kondisi ikan jantan dan betina ikan Bilis di tiap bulan
Tabel 2. Faktor kondisi ikan Bilis (T. hamiltonii) jantan dan betina yang tertangkap di Teluk Palabuhanratu
Bulan
Betina Jantan N Kisaran rata-rata Sb N Kisaran Rata-rata Sb
Mei 19 0.97-1.47 1.19 0.11 26 0.88-1.37 1.15 0.11
Juni 18 0.81-1.25 1.06 0.12 12 0.96-1.18 1.07 0.06 Juli 13 0.87-1.22 1.03 0.11 17 0.77-1.18 0.93 0.10
Ket : Sb = Simpangan baku
Nilai rata-rata faktor kondisi tertinggi ikan jantan dan betina terjadi pada bulan
Mei. Berdasarkan jenis kelamin ditemukan bahwa nilai faktor kondisi rata-rata ikan
betina pada bulan Mei dan Juli lebih besar dari ikan jantan. Hal ini menunjukkan bahwa
ikan bilis betina pada waktu tersebut lebih montok dari pada ikan jantan. Sementara
pada bulan Juni ditemukan hal yang sebaliknya. Nilai faktor kondisi rata-rata ikan
betina lebih besar dari ikan jantan. Hal ini dapat dipahami karena bobot gonad ikan
betina cenderung lebih berat dari pada gonad ikan jantan akibatnya bobot ikan betina
lebih besar dari bobot ikan jantan dan selanjutnya berpengaruh terhadap nilai faktor
kondisi. Nilai faktor kondisi ikan betina dan jantan yang tertangkap di Teluk
Palabuhanratu menurun setiap bulannya (Gambar 8 dan Gambar 9).
Gambar 9. Sebaran Faktor kondisi ikan Bilis (T. hamiltonii) jantan
Nilai faktor kondisi terbesar terdapat pada bulan Mei yaitu sebesar 1.19 (betina)
dan 1.15 (jantan). Perbedaan nilai faktor kondisi tiap bulannya dapat menggambarkan
faktor lingkungan mempengaruhi pertumbuhan ikan. Variasi faktor kondisi ini
dipengaruhi adanya kepadatan populasi, tingkat kematangan gonad, ketersediaan
makanan, jenis kelamin, dan umur (Effendi 1979). Faktor kondisi digunakan untuk
menentukan kecocokan lingkungan dan membandingkan berbagai tempat hidup ikan.
Kondisi dimana faktor kondisi ikan betina lebih besar dari ikan jantan ini dijumpai
pada ikan L. splendens di perairan Teluk Labuan (Saadah, 2000), ikan tunisi
Pristipomoides filamentosus, Valenciennes 1830 di Teluk Palabuhanratu (Susanto,
2006).
Berdasarkan Gambar 10 kita dapat melihat nilai faktor kondisi berdasarkan selang
kelas panjang total. Dari gambar tersebut didapat faktor kondisi terkecil sebesar 0.8924,
yaitu pada selang kelas panjang 138-141 mm sedangkan nilai terbesar ada pada selang
kelas panjang 102-105 mm sebesar 1.2649. Menurut Lagler (1972) dengan
meningkatnya ukuran ikan maka nilai faktor kondisinya akan bertambah. Namun pada
penelitian ini hasil yang didapatkan tidak sesuai dengan pernyataan tersebut. Hal ini
Gambar 10. Nilai faktor kondisi berdasarkan selang kelas panjang betina.
Tabel 3 menunjukkan hubungan faktor kondisi dengan tingkat kematangan gonad
pada ikan bilis (T. hamiltonii) betina. Terlihat bahwa nilai faktor kondisi rata-rata
meningkat seiring dengan perkembangan gonad (TKG). Dengan berkembangnya gonad
maka ukuran gonad juga akan semakin bertambah, sehingga akan mempengaruhi bobot
dari ikan. Hal ini menunjukkan bahwa meningkatnya bobot ikan maka nilai faktor
kondisinya akan bertambah dengan asumsi faktor lain tidak ada yang mempengaruhi
(Lagler,1972).
Tabel 3. Hubungan faktor kondisi dengan tingkat kematangan gonad ikan bilis (T. hamiltonii) betina.
TKG Jumlah Kisaran FK FK rata-rata Simpangan baku
I 1 - 0.9746 -
II 23 0.8133-1.2647 1.0712 0.123227
III 13 0.8956-1.4685 1.1405 0.139902
4.3 Aspek Reproduksi
4.3.1 Nisbah kelamin
Perbandingan ikan jantan dan ikan betina dalam suatu populasi, dengan kondisi
nisbah kelamin yang ideal yaitu rasio 1:1 (Bal dan Rao, 1984). Data perbedaan nisbah
kelamin ini selanjutnya digunakan untuk menduga tingkah laku pemijahan. Data nisbah
kelamin ikan bilis yang diamati dapat terlihat pada Tabel 4.
Tabel 4. Rasio kelamin
Berdasarkan Tabel 4 terlihat bahwa rasio kelamin ikan contoh yang di dapat
selama penelitian terjadi perubahan rasio, pada bulan Mei rasio kelamin yang diperoleh
sebesar 1,3684 (jantan lebih banyak dibandingkan betina), sedangkan pada bulan Juni
diperoleh rasio kelamin sebesar 0,6667 yang berarti betina lebih banyak dibandingkan
jantan, dan pada bulan Juli jumlah jantan kembali lebih banyak dibandingkan jumlah
betina dengan rasio kelamin sebesar 1,3077. Terjadi penyimpangan rasio kelamin dari
batas ideal (1:1), Selain itu penyimpangan rasio kelamin ditemukan juga pada ikan
kresek Thryssa mystax (Fatimah, 2006). Penyimpangan yang terjadi dari pola 1:1
disebabkan oleh pola tingkah laku bergerombol antara jantan dan betina, perbedaan
laju mortalitas dan pertumbuhan, pola distribusi yang disebabkan oleh ketersediaan
makanan, kepadatan populasi, tingkat kematangan gonad, dan keseimbangan rantai
makanan (Bal dan Rao, 1984; Effendie, 2002).
4.3.2 Tingkat Kematangan Gonad
Pengamatan tingkat kematangan gonad ikan betina dilakukan dengan dua cara
yaitu cara morfologi dan cara histologis. Sedangkan pada ikan jantan pengamatan hanya
penampakan luarnya seperti warna, bentuk dan ukuran. Hal ini dikarenakan penelitian
ini lebih difokuskan terhadap ikan betina.
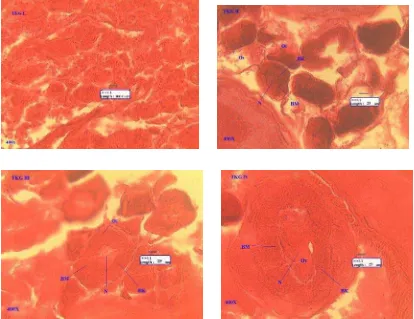
Tahap perkembangan kematangan gonad ikan betina baik secara morfologis
maupun secara histologis dapat terlihat pada Gambar 11, yaitu sebagai berikut :
Tahap I : Awal pertumbuhan (Tidak Masak)
Secara morfologi ovarium berbentuk memanjang. Ukuran sel telur relatif kecil
dan belum terlihat jelas oleh mata telanjang. Secara histologis, ovarium didominasi oleh
oogonium dan dijumpai telah adanya oosit primer hasil dari perkembangan oogonium.
Belum dilapisi selaput folikel. Inti sel (nukleus) terletak di tengah dan bentuknya bulat
serta dikelilingi oleh sitoplasma.
Tahap II : Berkembang (Tidak Masak)
Secara morfologi, ovarium berwarna merah jambu, pembuluh darah masih
belum terlihat jelas. Ovarium berwarna lebih kuning dari pada TKG I. Sel telur masih
belum terlihat jelas oleh mata telanjang. Secara histologis, Ovarium didominasi oleh
oosit primer, masih ditemukan oogonium, terlihat adanya lapisan folikel. Tahap awal
terjadinya proses vitellogenesis.
Tahap III : Dewasa (Hampir Masak)
Secara morfologi, ovarium berwarna merah jambu sampai kekuningan, butir
telur sudah dapat dilihat oleh mata telanjang namun diameternya lebih kecil dan
pembuluh darah mulai terlihat. Secara histologis, oogonium dan oosit sekunder masih
ditemukan dan oosit sekunder berkembang menjadi oosit. Butir kuning telur (yolk egg)
dan vakuola minyak terlihat jelas yang menyebar dari sekitar nukleus yang mengarah ke
tepi.
Tahap IV : Matang (Masak)
Secara morfologi, ovarium makin membesar berwarna kuning
kemerah-merahan, pembuluh darah jelas, telur terlihat jelas, keadaan telur masak berukuran besar
berwarna terang. Secara histologis, Ovarium didominasi oleh ovum, inti sel terlihat
Gambar 11. Histologis Gonad TKG I, II, III, dan IV ikan Bilis (T. hamiltonii)
Keterangan : N = Nukleus; Si = Sitoplasma; Os = oosit; Ot = Ootid; Ov = Ovum; Bm = Butir minyak; Bk = butir kuning telur
Berdasarkan perkembangan gonad betina secara histologis terlihat bahwa ikan T.
hamiltonii memiliki tipe perkembangan oosit group-synchronous yaitu ovarium
memiliki dua kelompok oosit dengan tingkat kematangan yang berbeda (Murua, 2003).
Secara keseluruhan dapat disimpulkan bahwa ikan bilis sedang dalam musim pemijahan
pada waktu penelitian dan mengalami puncak pemijahan pada bulan Mei. Hal ini
terlihat dari ikan hasil tangkapan pada bulan Mei yang didominasi oleh ikan yang
matang gonad (TKG IV).
Berdasarkan Gambar 12, yaitu frekuensi TKG ikan bilis betina yang tertangkap di
teluk Palabuhanratu bulan Mei - Juli dengan menggunakan kelompok ukuran panjang,
terlihat ikan Bilis betina TKG IV ditemukan pertama kali pada kelas ukuran 110-113
mm. Terlihat tingkat kematangan gonad yang lebih besar didapat pada ikan dengan
ukuran panjang yang juga makin besar. Dengan mengetahui TKG ikan, kita selanjutnya
dapat mengetahui perbandingan antara ikan yang berada diperairan, ukuran atau unsur
ikan pertama kali matang gonadnya, dan apakah ikan sudah memijah atau belum
(Nikolsky, 1963).
Gambar 12. TKG ikan bilis betina berdasarkan selang kelas panjang
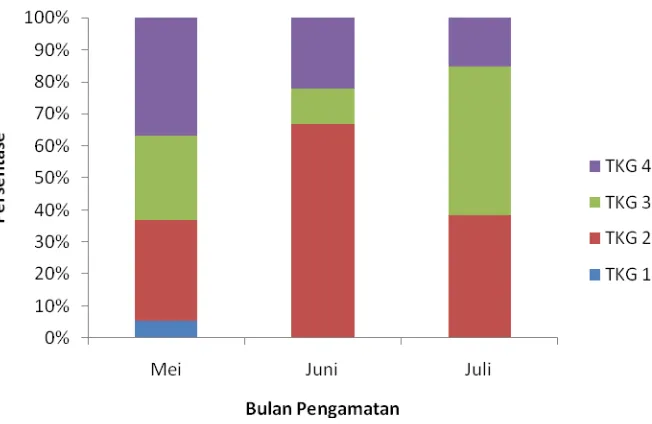
Persentase TKG ikan pada tiap bulan ditunjukan pada Gambar 13. Gambar
tersebut memperlihatkan bahwa selama penelitian, ikan bilis betina dengan TKG IV
ditemukan disetiap bulannya. Sehingga dapat dikatakan bahwa musim pemijahan ikan
bilis adalah sepanjang tahun. Jumlah ikan betina yang teridentifikasi tingkat
kematangan gonadnya sebanyak 50 ekor, yaitu TKG I ditemukan sebanyak 1 ekor ,
TKG II sebanyak 23 ekor, TKG III sebanyak 13 ekor, dan TKG IV sebanyak 13 ekor.
Persentase terbesar ditemukannya gonad betina TKG IV terdapat pada bulan Mei yaitu
sebesar 36.8421%, sebanyak 7 ekor dari 19 ekor ikan yang dibedah. Ada dua faktor
yang mempengaruhi perkembangan gonad, yaitu faktor lingkungan dan hormon
(Affandi dan Tang 2000).
Untuk mengetahui ukuran pertama kali matang gonad, data TKG diolah dengan
menggunakan rumus Spareman Karber (Lampiran 8). Sehingga didapatkan ukuran
pertama kali matang gonad pada selang kelas 126-129 mm yaitu pada ukuran
127.9875±0.0131. Hasil penelitian Juraida (2004) menunjukan ukuran pertama kali
matang gonad ikan tetet betina sebesar 86-100 mm. Perbedaan ukuran ikan pertama kali
matang gonad ini dipengaruhi beberapa faktor, yaitu faktor luar dan faktor dalam.
Beberapa faktor yang diduga dapat menjadi penyebab perbedaan pencapaian ukuran
pertama kali matang gonad, seperti sifat genetik populasi, perbedaan letak wilayah
(latitude), kualitas perairan, dan besarnya tekanan penangkapan. Selain itu kematangan
gonad berhubungan dengan pertumbuhan dan faktor lingkungan terutama ketersediaan
makanan baik secara kualitas maupun kuantitas (Toelihere 1985 in Affandi dan Tang
2000). Effendie (1997) menyatakan faktor yang mempengaruhi pertama kali ikan
matang gonad ada dua yaitu faktor luar seperti suhu dan arus serta faktor dari dalam
seperti umur, jenis kelamin, sifat-sifat fisologis ikan seperti kemampuan beradaptasi
dengan lingkungan serta ukuran.
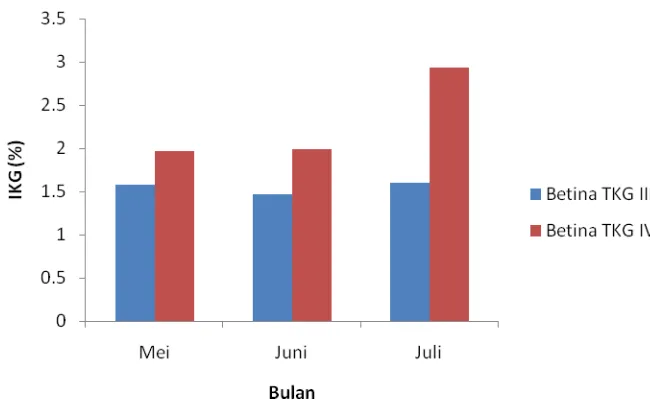
4.3.3 Indeks kematangan gonad
Indeks kematangan gonad (IKG) merupakan nilai yang memberikan informasi
mengenai perubahan yang terjadi dalam gonad. Nilai IKG ikan bilis betina TKG III di
pada bulan Juni adalah 1,2767% - 2,6667% dan pada bulan Juli berkisar antara 1,5% -
1,7%. Nilai IKG ikan bilis betina TKG IV di TPI Palabuhanratu pada bulan Mei
berkisar antara 1,75% - 2,3077%, sedangkan kisaran pada bulan Juni adalah 1,9231% -
2,1053% dan pada bulan Juli 2,9286% . Gambar 14 menunjukkan bahwa secara
keseluruhan rata-rata nilai IKG betina TKG IV lebih besar dari TKG III. Hal ini diduga
karena perubahan IKG berkaitan erat dengan tahap perkembangan telur. Effendie
(2002) mengatakan bahwa berat gonad akan mencapai maksimum saat ikan akan
memijah dan nilai tersebut akan menurun dengan cepat selama pemijahan berlangsung
sampai pemijahan selesai. Selain itu, meningkatnya tingkat kematangan gonad akan
menyebabkan ukuran diameter telur berat gonad meningkat sehingga nilai IKG juga
meningkat.
Gambar 14. Indeks kematangan gonad
4.3.4 Fekunditas
Fekunditas ikan bilis yang diamati didapat dari pengamatan ikan dengan TKG 3
dan TKG 4. Pada Tabel 5 terlihat bahwa fekunditas ikan bilis pada bulan Mei berkisar
dan berat 8 gram, sedangkan fekunditas maksimum terjadi pada ikan dengan panjang
12,5 dan berat 13. Hubungan fekunditas pada bulan Mei dengan panjang dan beratnya
disajikan pada Gambar 13.
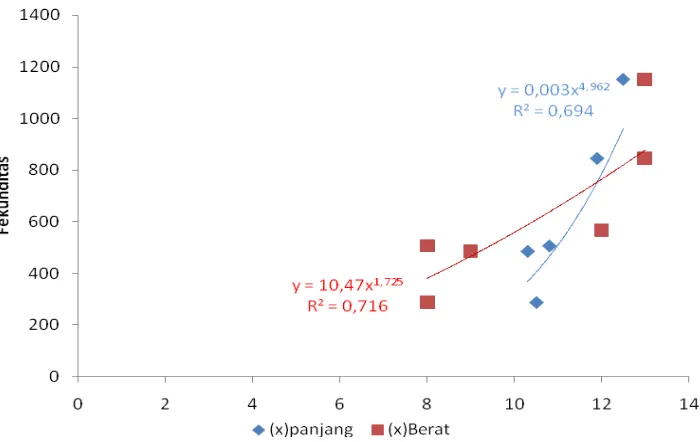
Tabel 5. Fekunditas T. hamiltonii pada bulan Mei
Panjang 10,5 10,3 10,8 12 12,5 11,9
Berat 8 9 8 12 13 13
fekunditas 288 486 507 567 1152 846
Berdasarkan hasil regresi pada bulan Mei fekunditas dengan panjang total
tubuhnya (Gambar 15) diperoleh koefisien determinasi sebesar 0,694 di TPI
Palabuhanratu, menunjukkan bahwa model tersebut dapat menjelaskan data sebesar
69,4%. Dari nilai koefisien determinasi tersebut didapat nilai koefisien korelasi sebesar
0,83 sehingga dapat disimpulkan bahwa hubungan antara fekunditas dengan panjang
tubuh di TPI Palabuhanratu sangat erat.
Dengan meregresikan fekunditas dengan berat tubuh ikan didapatkan koefisien
determinasi sebesar 0,716, hal ini menunjukkan bahwa model tersebut dapat
menjelaskan data sebesar 71,6%. Dari nilai koefisien determinasi tersebut didapat nilai
koefisien korelasi sebesar 0,84 sehingga dapat disimpulkan bahwa terdapat hubungan
yang sangat erat antara fekunditas dengan berat tubuhnya.
Berdasarkan Tabel 6 terlihat bahwa fekunditas ikan bilis pada bulan Juni
berkisar antara 899-2280 telur. Fekunditas minimum terjadi pada ikan dengan panjang
12,6 cm dan berat 11 gram, sedangkan fekunditas maksimum terjadi pada ikan dengan
panjang 15,7 dan berat 26. Hubungan fekunditas pada bulan Juni dengan panjang dan
beratnya akan disajikan pada Gambar 16.
Tabel 6. Fekunditas T. hamiltonii pada bulan Juni
Panjang 12,6 12,5 15,7 14,3 13,5
Berat 11 12 26 19 19
fekunditas 898,8 1140 2280 1176,6 1536
Gambar 16. Grafik hubungan fekunditas dengan panjang dan berat (Juni 2009)
Berdasarkan hasil regresi fekunditas dengan panjang total tubuh ikan (Gambar
16) diperoleh koefisien determinasi sebesar 0,735 yang menunjukkan bahwa model
didapat nilai koefisien korelasi sebesar 0,85 sehingga dapat disimpulkan bahwa
hubungan antara fekunditas dengan panjang tubuh di TPI Palabuhanratu sangat erat.
Dengan meregresikan fekunditas dengan berat tubuh ikan didapatkan nilai koefisien
determinasi yang sebesar 0,771 yang menunjukkan bahwa model tersebut dapat
menjelaskan data hingga sebesar 77,1%. Dari nilai koefisien determinasi tersebut
didapat nilai koefisien korelasi sebesar 0,88 sehingga dapat disimpulkan bahwa terdapat
hubungan yang sangat erat antara fekunditas dengan berat tubuhnya. Apabila
dibandingkan hasil – hasil regresi tersebut kita dapat menarik kesimpulan bahwa pada
bulan Juni fekunditas ikan bilis yang tertangkap di teluk Palabuhanratu lebih
dipengaruhi oleh berat tubuh daripada panjang total tubuhnya.
Berdasarkan Tabel 7 terlihat bahwa fekunditas ikan bilis pada bulan Juli berkisar
antara 1040-7339 telur. Fekunditas minimum terjadi pada ikan dengan panjang 11,6 cm
dan berat 10 gram, sedangkan fekunditas maksimum terjadi pada ikan dengan panjang
12,1 dan berat 14. Hubungan fekunditas pada bulan Juli dengan panjang dan beratnya
akan disajikan pada Gambar 17.
Tabel 7. Fekunditas T. hamiltonii pada bulan Juli
Panjang 11,6 12,1 12
Berat 10 14 10
fekunditas 1040,4 7339,2 1071
Berdasarkan hasil regresi fekunditas dengan panjang total tubuh ikan (Gambar
17) diperoleh koefisien determinasi sebesar 0,444 yang menunjukkan bahwa model
tersebut dapat menjelaskan data sebesar 44,4%. Dari nilai koefisien determinasi tersebut
didapat nilai koefisien korelasi sebesar 0,67 sehingga dapat disimpulkan bahwa
hubungan antara fekunditas dengan panjang tubuh di TPI Palabuhanratu cukup erat.
Dengan meregresikan fekunditas dengan berat tubuh ikan didapatkan nilai koefisien
determinasi yang sebesar 0,999 yang menunjukkan bahwa model tersebut dapat
didapat nilai koefisien korelasi sebesar 0,99 sehingga dapat disimpulkan bahwa terdapat
hubungan yang sangat erat antara fekunditas dengan berat tubuhnya.
Gambar 17. Grafik hubungan fekunditas dengan panjang dan berat (Juli 2009)
Apabila kita melihat hasil – hasil regresi tersebut kita dapat menyimpulkan
bahwa terdapat hubungan yang erat antara fekunditas ikan bilis yang tertangkap di teluk
Palabuhanratu dengan panjang total tubuhnya dan hubungan yang sangat erat dengan
berat tubuhnya. Sehingga kita dapat mengatakan bahwa fekunditas ikan Bilis (T.
Hamiltonii) yang tertangkap di teluk Palabuhanratu dipengaruhi oleh berat dan panjang
tubuhnya. Hal ini didukung oleh Walker et al. (1998) in Stevens et al. (2000) yang
menyatakan fekunditas cenderung meningkat dengan ukuran tubuh yang besar,
sehingga potensi reproduksi ikan berukuran besar lebih besar dibandingkan dengan ikan
yang berukuran kecil. Selanjutnya Bagenal (1978) in Syandri (1996) yang menyatakan
bahwa pertambahan berat tubuh dan panjang ikan meningkatkan fekunditas secara
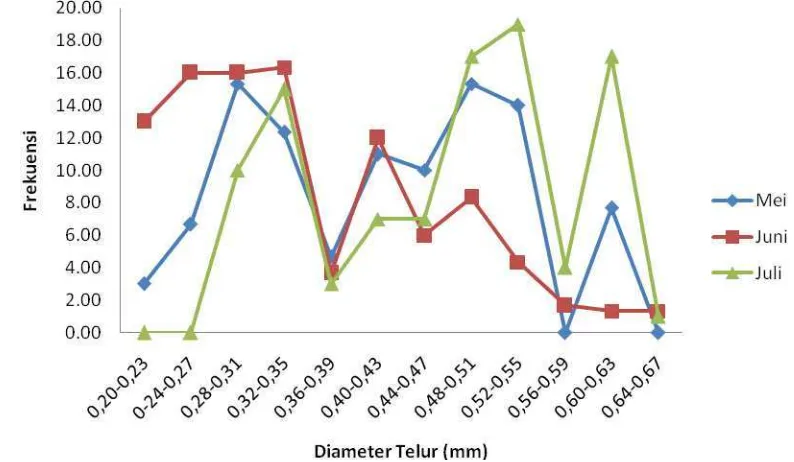
4.3.5 Diameter telur
Diameter telur pada ikan Bilis hasil tangkapan Mei-Juli di Teluk Palabuhanratu
memiliki nilai terkecil sebesar 0,2 mm dan nilai terbesarnya 0,67 mm. Berdasarkan
Gambar 18, terlihat beberapa puncak pada grafik sebaran diameter sehingga dapat
diduga bahwa ikan bilis mengeluarkan telur secara sebagian sewaktu memijah (partial
spawner) dengan waktu pemijahan yang panjang dan terus menerus. Hal ini didasarkan
oleh ukuran telur yang berbeda-beda di dalam ovarium (Prabu, 1956 in Liana, 2003).
Gambar 18. Grafik sebaran diameter telur ikan Bilis (T. hamiltonii) pada TKG IV
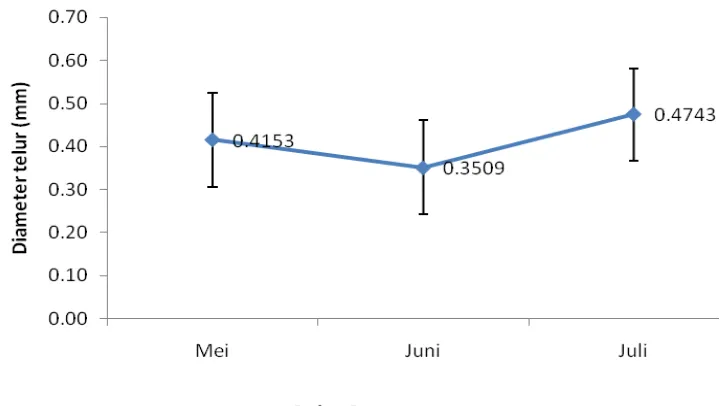
Berdasarkan Gambar 19 terlihat bahwa diameter rata-rata telur ikan bilis rata-rata
pada bulan Mei didapat sebesar 0.4153, sedangkan pada bulan Juni diameter rata-rata
telur sebesar 0.3509 dan pada bulan Juli diameter rata-rata telur didapat sebesar 0.4743.
Perkembangan diameter telur umumnya dikarenakan terjadinya akumulasi kuning telur
selama proses vitelogenesis yang menyebabkan telur dari ukuran kecil menjadi besar
(Utiah, 2006). Selain itu, adanya ukuran diameter telur yang beragam setiap spesies
ikan dipengaruhi oleh faktor genetik, lingkungan, ketersediaan makanan dan umur
Gambar 19. Nilai rata-rata diameter telur ikan bilis (T. hamiltonii) pada setiap bulan pengamatan
4.3.6 Kandungan protein
Rata-rata kandungan protein telur ikan bilis (T. hamiltonii) diperoleh dari
rata-rata panjang, berat tubuh dan berat gonad, pada tiap bulan penelitian disajikan pada
Tabel 8. Kadar protein tertinggi ditemukan pada bulan Mei (20,76%) dan yang terkecil
pada bulan Juni (14,44%). Rata-rata kandungan protein selama penelitian adalah
sebesar 17,74%.
Kadar protein yang terdapat pada ikan bilis (T. hamiltonii) dianalisis dari
telurnya yang memiliki TKG IV. Penghitungan analisis proksimat dari telur ikan ini
menggunakan berat basah telur karena berat keringnya menunjukkan nilai yang tidak
dapat dianalisis. Kandungan protein yang didapat selama waktu penelitian (Mei-Juli)
masih tergolong tinggi, yaitu sebesar 15%-20% (www.nbin.lipi.go.id). Tetapi pada