i
KARAKTERISTIK NANOEMULSI EKSTRAK JAHE
(
Zingiber officinale
var. Amarum)
FLENI AYU KENIA HAQUE
TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi berjudul Karakteristik Nanoemulsi Ekstrak Jahe (Zingiber officinale var. Amarum) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Agustus 2015
Fleni Ayu Kenia Haque
1
ABSTRAK
FLENI AYU KENIA HAQUE. Karakteristik Nanoemulsi Ekstrak Jahe (Zingiber officinale var. Amarum). Dibimbing oleh ERLIZA NOOR dan JUNIAWATI. Jahe merupakan salah satu tumbuhan yang digunakan sebagai obat herbal karena memiliki banyak khasiat untuk kesehatan. Namun, oleresin jahe yang mengandung senyawa aktif gingerol memiliki sifat hidrofobik sehingga sukar larut dalam air, sulit terdispersi, serta kecepatan dan daya serapnya dalam tubuh masih rendah. Salah satu solusi yang dapat diakukan adalah pengaplikasian nanoteknologi dengan menempatkan oleoresin jahe dalam sistem emulsi minyak dalam air (O/W) dan diputar dengan kecepatan tinggi sehingga diperoleh ukuran berskala nano. Tujuan dari penelitian ini adalah mempelajari karakteristik nanoemulsi ekstrak jahe meliputi stabilitas ukuran, bioavailabilitas dan kelarutan pada berbagai jenis pelarut. Bahan utama yang digunakan adalah jahe emprit yang dibuat dalam bentuk serbuk dan diekstrak dengan metode maserasi. Pembuatan nanoemulsi ekstrak jahe dilakukan dengan pencampuran ekstrak jahe dan larutan buffer fosfat ph 7 dengan perbandingan 3:7, kemudian diputar dengan alat ultra turrax kecepatan 22 000 rpm selama 20 menit pada suhu ruang. Pada uji stabilitas ukuran, nanoemulsi dibuat dengan dan tanpa penambahan antioksidan dan disimpan pada tiga variasi suhu, yaitu suhu rendah (4oC), suhu ruang, dan suhu tinggi (45-50oC). Ukuran droplet nanoemulsi paling stabil pada penyimpanan suhu rendah dan paling tidak stabil pada penyimpanan suhu tinggi. Namun, penambahan antioksidan tidak berpengaruh pada kestabilan ukuran nanoemusi. Nanoemulsi memiliki bioavailabilitas senyawa aktif yang lebih baik dibanding dengan emulsi. Persentase gingerol nanoemulsi terpenetrasi adalah 49,73%, sedangkan gingerol emulsi hanya terpenetrasi 17,68%. Kelarutan nanoemulsi menunjukkan nilai yang lebih baik dari pada emulsi pada pelarut semi polar dan polar. Nanoemulsi ekstrak jahe memiliki kelarutan tertinggi pada pelarut air, yaitu 94,0%.
ABSTRACT
FLENI AYU KENIA HAQUE. Characteristics of Ginger Extract Nanoemulsion (Zingiber officinale var. Amarum). Supervised by ERLIZA NOOR and JUNIAWATI.
Ginger is one of the plants that used as herbal medicine because it has many health benefits. However, oleoresin that containing gingerol active compounds are hydrophobic so it difficults to soluble in water, hard dispersed, speed and the absorption in the body is low. One solution that can be done is the application of nanotechnology to put ginger oleoresin in oil in water ( O / W) emulsion system and rotated at high speed to obtain nanoscale size. The purpose of this research is to study the characteristics of ginger extract nanoemulsion include size stability, bioavailability and solubility in various kinds of solvents. The main materials that used are ginger that made in powder form and extract by maceration method. Nanoemulsion are made by mixing ginger extract and phosphate buffer pH 7 with ratio 3:7, then rotated with ultra turrax, speed 22.000 rpm for 20 minutes at room temperature. In size stability test, nanoemulsion made with and without the addition of antioxidants and stored at three variations of temperature, those are low temperature (4°C), room temperature, and high temperature (45-50oC). Droplet size of nanoemulsion is most stable at low temperature storage and most unstable at high temperature storage. However, additional of antioxidants have no effect on the size stability of nanoemulsion. Nanoemulsion have better active compounds bioavailability than the emulsion. The percentage gingerol of nanoemulsion penetrated is 49.73%, while the gingerol of emulsion penetrated only 17.68%. Solubility of nanoemulsion shows a better value than emulsion on semi-polar and polar solvents. Nanoemulsion ginger extract has the highest solubility in aqueous solvent, that is 94.0%.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Ilmu dan Teknologi Pangan
KARAKTERISTIK NANOEMULSI EKSTRAK JAHE
(
Zingiber officinale
var. Amarum)
FLENI AYU KENIA HAQUE
TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Mei 2014 ialah Karakteristik Nanoemulsi Ekstrak Jahe (Zingiber officinale var. Amarum). Atas terselesaikannya kegiatan penelitian dan penulisan skripsi ini, penulis mengucapkan terima kasih kepada Prof. Dr. Ir. Eliza Noor dan Juniawati, STP, M,Si selaku pembimbing. Ungkapan terima kasih juga penulis sampaikan kepada ayah, ibu, adik serta seluruh keluarga atas segala doa, dukungan, pengertian dan kesabaran, serta Heri Supriadi yang selalu menjadi semangat dan banyak membantu dari awal hingga akhir.
Terima kasih kepada Sugar Group Companies yang telah memberikan beasiswa dan kesempatan sehingga penulis dapat menimba ilmu di Institut Pertanian Bogor melalui jalur USMI. Penulis juga mengucapkan terima kasih kepada seluruh staff IPB yang telah membantu terlaksananya penelitian ini. Fachrizal sebagai rekan satu bimbingan serta teman-teman TIN 47 yang tidak dapat saya sebutkan satu per satu yang telah terus-menerus memberikan semangat kepada penulis. Semoga karya ilmiah ini bermanfaat.
Bogor, Agustus 2015
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
PENDAHULUAN
Latar Belakang 1
Tujuan 2
Perumusahn Masalah 2
Manfaat Penelitian 2
Ruang Lingkup Penelitian 2
METODE
Waktu dan Tempat Penelitian 3
Bahan 3
Alat 3
Prosedur Penelitian 3
HASIL DAN PEMBAHASAN
Analisis Proksimat Serbuk Jahe 8
Rendemen dan Karakteristik Oleoresin 9
Nanoemulsi Ekstrak Jahe 11
Stabilitas Nanoemulsi Ekstrak Jahe 12
Bioavailabilitas Nanoemulsi Ekstrak Jahe 15
Kelarutan Nanoemusi Ekstrak Jahe 17
Implikasi Teknis 18
SIMPULAN DAN SARAN
Simpulan 19
Saran 19
DAFTAR PUSTAKA 20
LAMPIRAN 24
DAFTAR TABEL
1 Analisis proksimat serbuk jahe kering 8
2 Perbandingan produk oleoresin dengan standar oleoresin 10
3 Uji karateristik emulsi dan nanoemulsi 12
4 Kelarutan gingerol emulsi dan nanoemulsi pada berbagai pelarut 18
DAFTAR GAMBAR
1 Skema pembuatan serbuk jahe kering 4
2 Skema ekstraksi jahe 4
3 Skema pembuatan nanoemulsi ekstrak jahe 5
4 Alat uji bioavailabilitas 6
5 Rimpang jahe emprit 8
6 Oleoresin jahe hasil penelitian 9
7 Struktur gingerol 10
8 Ukuran droplet nanoemulsi dengan penambahan antioksidan 14 9 Ukuran droplet nanoemulsi tanpa penambahan antioksidan 14 10 Jumlah kumulatif gingerol terpenetrasi selama 8 jam 16
DAFTAR LAMPIRAN
1 Analisis Proksimat Serbuk Jahe Kering 24
2 Uji Karakteristik Ekstrak Jahe dan Nanoemulsi 26
3 Kurva Standar Gingerol 27
4 Emulsi dan Nanoemulsi Ekstrak Jahe 28
5 Distribusi Ukuran Nanoemulsi Ekstrak Jahe 29
1
PENDAHULUAN
Latar Belakang
Dewasa ini banyak masyarakat yang beralih dari mengkonsumsi obat kimia ke obat herbal yang berasal dari tanaman obat (biofarmaka) karena obat-obatan kimia diyakini menimbulkan dampak negatif, sedangkan obat herbal diyakini lebih aman tanpa efek samping. Seiring dengan meningkatnya konsumsi obat berbahan dasar herbal, perkembangan teknologi pengolahan obat herbal juga mengalami peningkatan guna mendapat obat-obatan dengan kualitas dan sediaan yang lebih baik.
Jahe merupakan salah satu tumbuhan yang berkhasiat sebagai obat herbal. Fungsi jahe sebagai obat antara lain memperbaiki pencernaan, mengobati masuk angin, merangsang pengeluaran getah lambung dan empedu, memperlancar menstruasi, anti pengerasan pembuluh darah dan mencegah infeksi (Tusilawati 2010). Jahe menjadi salah satu tumbuhan yang dibutuhkan dalam jumlah besar untuk industri kecil obat tradisional (IKOT) maupun industri obat tradisional (IOT) serta telah digunakan sebagai bahan baku lebih dari 40 produk obat (Kementerian Pertanian 2008).
Rimpang jahe memiliki kandungan minyak atsiri (2,58-3,90%) dan oleoresin (3%). Oleoresin jahe mengandung senyawa aktif utama yaitu gingerol yang berasal dari hasil metabolisme sekunder. Fungsi gingerol pada jahe adalah sebagai pembawa rasa pedas, tajam dan sensasi menyengat dalam mulut (pungent). Oleoresin telah diaplikasikan pada berbagai indutri, antara lain sebagai bahan baku obat, kosmetik, hingga industri bakery. Namun, zat pada jahe ini belum optimal dimanfaatkan karena sifatnya yang hidrofobik sehingga kurang larut dalam air, sulit terdispersi serta kecepatan dan daya serapnya dalam tubuh masih rendah (Harimurti dan Yuliani 2010).
Salah satu solusi yang dapat dilakukan adalah pengaplikasian nanoteknologi, yaitu dengan menempatkan oleoresin dalam sistem emulsi minyak dalam air (o/w), dimana oleoresin berada pada fase minyak dan air sebagai fase kontinyu dan diputar dengan kecepatan tinggi sehingga diperoleh ukuran berskala nano. Nanoemulsi memiliki ukuran droplet rata-rata 2 – 500 nm (Shah et al. 2010). Nanoemulsi sangat prospektif untuk meningkatkan efektifitas dan stabilitas serta biovailabilitas bahan aktif jahe yang terekstrak. Selain itu pula, penerapan nanoemulsi juga meningkatkan kelarutan sehingga ekstrak jahe lebih mudah untuk diaplikasikan dan digunakan untuk membuat produk berbasis jahe.
Tujuan
Tujuan dari penelitian ini adalah mempelajari karakteristik nanoemulsi ekstrak jahe meliputi stabilitas ukuran pada berbagai suhu simpan dengan dan tanpa penambahan antioksidan, bioavailabilitas senyawa aktif dan kelarutan pada berbagai jenis pelarut.
Perumusan Masalah
Oleoresin yang mengandung senyawa aktif gingerol memiliki sifat tidak larut dan sulit terdispersi. Kekurangan tersebut dapat diatasi dengan pembuatan nanoemulsi sehingga mudah diaplikasikan dalam produk obat dan makanan. Karakteristik nanoemulsi dapat berubah selama penyimpanan. Perubahan tersebut disebabkan oleh agregasi butiran nanoemulsi sehingga ukuran menjadi tidak stabil (Harimurti et al. 2012; Solanki 2012; Rachmawati et al. 2014). Perlu juga diketahui suhu simpan terbaik dan pengaruh penambahan antioksidan terhadap kestabilan ukuran nanoemulsi dan pengaruh ukuran partikel terhadap jumlah senyawa aktif yang dapat diserap dan kelarutannya.
Permasalahan yang akan dikaji dalam penelitian ini adalah:
1. Bagaimana perubahan ukuran nanoemulsi ekstrak jahe selama penyimpanan dengan dan tanpa penambahan antioksidan
2. Bagaimana perubahan ukuran nanoemulsi ekstrak jahe pada penyimpanan suhu rendah, suhu ruang, dan suhu tinggi
3. Bagaimana pengaruh ukuran nanoemulsi terhadap bioavailabilitas 4. Bagaimana kelarutan nanoemulsi dalam berbagai pelarut
Manfaat Penelitian
Pengetahuan dan informasi tentang karakteristik nanoemulsi ekstrak jahe dapat bermanfaat dalam pembuatan dan pengembangan obat-obatan herbal berbahan dasar jahe.
Ruang Lingkup Penelitian
METODE
Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada bulan Mei 2014 - Juni 2015 di Laboratorium Dasar Ilmu Terapan dan Laboratorium Pengawasan Mutu, Departemen Teknologi Industri Pertanian. Pembuatan nanoemulsi dilakukan di Laboratorium Nanoteknologi, Balai Besar Penelitian Dan Pengembangan Pascapanen Pertanian dan Laboratorium Farmasetika Non-Steril, Farmasi Universitas Indonesia. Pengujian ukuran nanoemulsi dilakukan di Laboratorium Fisika Departemen Fisika, dan analisis gingerol dilakukan di Laboratorium Uji Balai Penelitian Rempah dan Obat dan Laboratorium Pusat Studi Biofarmaka.
Bahan
Bahan yang digunakan dalam penelitian ini adalah jahe emprit (Zingiber officinale var. Amarum), akuades, heksan, etanol, metanol, etil asetat, aseton, Tween 80, NaOH, HCl, asam askorbat, reagen folin, larutan buffer fosfat pH 7, usus kambing atau sapi, dan kertas saring.
Alat
Peralatan yang digunakan adalah alat peralatan gelas, homogenizer Ultra Turrax, hammer mill, magnet stirer, rotary evaporator, spektrofotometer (Hach DR 2500), hot plate, oven, viskometer ostwald, Particle Size Analyzer (VASCO),
neraca analitik, pisau, kertas saring, piknometer, spatula dan alat uji difusi Franz.
Prosedur Penelitian
Penelitian dilakukan dalam empat tahap, yaitu tahap pendahuluan, tahap ekstraksi, tahap pembuatan nanoemulsi ekstrak jahe, dan tahap uji. Tahap pendahuluan merupakan tahap pengolahan jahe segar menjadi serbuk jahe sebagai sediaan proses ekstraksi. Tahap ekstraksi, merupakan tahap pengambilan bahan aktif jahe dengan metode maserasi menggunakan pelarut heksana. Tahap pembuatan nanoemulsi, merupakan tahap pembuatan nanoemulsi ekstrak jahe dengan menggunakan alat Ultra Turrax. Tahap uji, merupakan tahap pengujian kestabilan ukuran nanoemulsi ekstrak jahe yang disimpan pada suhu bervariasi, bioavailabilitas gingerol dalam emulsi dan nanoemulsi, serta uji kelarutan nanoemulsi di berbagai pelarut.
Tahap Pendahuluan
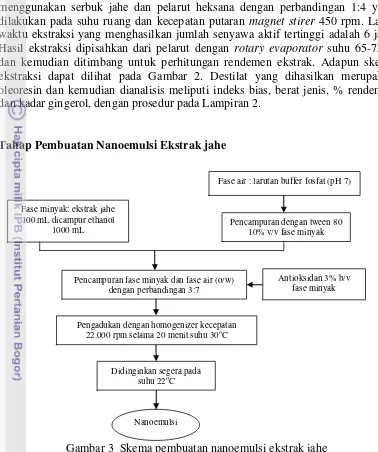
sampai benar-benar kering. Jahe kering dihaluskan dengan menggunakan hammer mill hingga menjadi serbuk dengan ukuran 40 mesh. Rendemen serbuk jahe kering dihitung berdasarkan pada persentase antara bobot serbuk jahe yang didapat dengan bobot rimpang jahe segar yang digunakan. Adapun tahap persiapan dilakukan seperti skema pada Gambar 1. Serbuk jahe kering kemudian dianalisis proksimat untuk mengetahui kandungan didalamnya, dengan prosedur yang dapat dilihat pada Lampiran 1.
Gambar 1 Skema pembuatan serbuk jahe kering
Tahap Ekstraksi
Gambar 2 Skema ekstraksi jahe
Pencucian
Pengirisan
Pengeringan
Penghalusan
Pengayakan 40 mesh
Serbuk jahe kering Rimpang jahe
segar
100 gram serbuk jahe
Maserasi 6 jam
Penyaringan
Filtrat
Pemekatan dengan rotary evaporator 65-75oC Ampas
Heksana 400 mL
Tahap ekstraksi mengacu pada penelitian yang telah dilakukan oleh Tririzqi (2013). Ekstraksi senyawa aktif jahe dilakukan dengan metode maserasi menggunakan serbuk jahe dan pelarut heksana dengan perbandingan 1:4 yang dilakukan pada suhu ruang dan kecepatan putaran magnet stirer 450 rpm. Lama waktu ekstraksi yang menghasilkan jumlah senyawa aktif tertinggi adalah 6 jam. Hasil ekstraksi dipisahkan dari pelarut dengan rotary evaporator suhu 65-75oC dan kemudian ditimbang untuk perhitungan rendemen ekstrak. Adapun skema ekstraksi dapat dilihat pada Gambar 2. Destilat yang dihasilkan merupakan oleoresin dan kemudian dianalisis meliputi indeks bias, berat jenis, % rendemen dan kadar gingerol, dengan prosedur pada Lampiran 2.
Tahap Pembuatan Nanoemulsi Ekstrak jahe
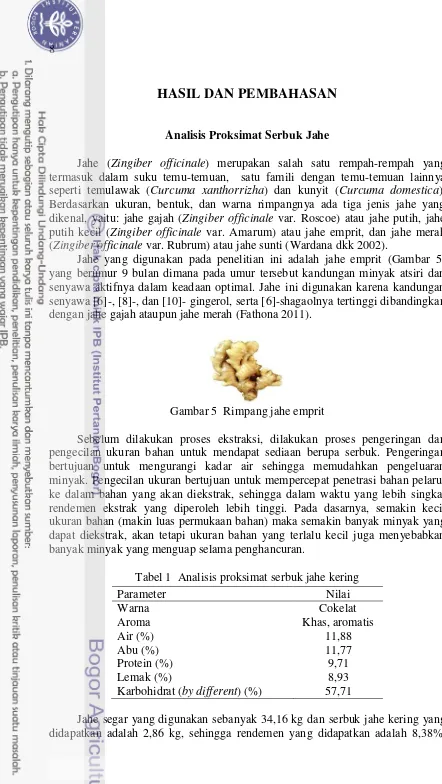
Gambar 3 Skema pembuatan nanoemulsi ekstrak jahe
Pembuatan nanoemulsi ekstrak jahe (Gambar 3) mengacu pada penelitian Harmi (2013). Ekstrak jahe yang diperoleh dari tahap ekstraksi dipersiapkan sebagai fase minyak dicampur dengan ko-surfaktan berupa etanol sehingga diperoleh konsentrasi 10%. Larutan buffer dibuat menggunakan NaOH dan atau HCl hingga pH 7. Tween 80 sebanyak 10% v/v fase minyak dilarutkan dalam larutan buffer. Sampel disiapkan dengan mencampurkan fase minyak dan fase air dengan perbandingan 3:7 dan diaduk dengan menggunakan homogenizer Ultra Turrax selama 20 menit dengan kecepatan 22.000 rpm pada suhu 30oC. Proses pembuatan nanoemulsi dilakukan dengan dan tanpa penambahan antioksidan untuk melihat pengaruh ontioksidan terhadap kestabilan ukuran nanoemulsi
Fase minyak: ekstrak jahe 100 mL dicampur ethanol
1000 mL
Fase air : larutan buffer fosfat (pH 7)
Pencampuran dengan tween 80 10% v/v fase minyak
Tahap Uji
Uji Stabilitas Ukuran
Stabilitas ukuran nanoemulsi diamati pada tiga kondisi suhu penyimpanan, yaitu suhu 4oC, suhu kamar, dan 50oC. Kemudian dilakukan pengamatan ukuran dengan dengan waktu pengamatan yaitu hari ke-0, 1, 2, 3, 5, dan 7. Analisis dispersi dan ukuran butiran nanoemulsi dilakukan dengan Particulate Sisteme –
Particle Size Analyzer yang dapat mengukur distribusi ukuran dengan kisaran 2-7.000 nm.
Uji Bioavailabilitas
Bioavailabilitas nanoemulsi ekstrak jahe diukur dengan alat uji difusi Franz
(Gambar 4). Tahap awal yang dilakukan yaitu mempersiapkan usus duabelas jari kambing atau sapi sebagai membran difusi. Usus disayat dengan ketebalan 0.10 ± 0.05 mm. Kemudian usus bagian dalam direndam pada larutan buffer fosfat pH 7 selama 30 menit. Usus kemudian disisipkan pada sebuah cincin diantara kompartemen reseptor dan kompartemen donor dari alat difusi Franz. Sambungan dirapatkan dan dilapisi dengan parafilm untuk mencegah kebocoran. Setelah dipastikan tidak ada kebocoran, larutan buffer fosfat pH 7 dimasukkan ke dalam kompartemen reseptor dengan dipastikan tidak ada gelembung udara dan larutan buffer menyentuh lapisan usus.
Cairan reseptor diaduk dengan kecepatan 200 rpm. Sampel sebanyak 10 ml diaplikasikan pada kompartemen donor. Gingerol yang terpenetrasi diamati dengan menggambil 0,5 ml larutan buffer dari kompartemen reseptor. Pengujian dilakukan pada jam ke-1, 2, 3, 4, 5, 6, 7, dan 8. Jumlah kuantitatif gingerol terpenetrasi di uji dengan metode spektrofometer Folin-Ciocalteau. Pertama, 0,1 ml sampel dimasukkan ke dalam gelas ukur 10 ml dan ditambahkan 2 ml sodium karbonat 2%. Sampel diaduk dan didiamkan selama 5 menit. Setelah itu ditambahkan 0,1 ml reagen folin yang telah diencerkan dengan perbadingan 1:1. Sampel ditera dengan akuades hingga 10 ml dan diduk dengan menggunakan vorteks, kemudian didiamkan selama 30 menit sampai 1 jam dan di analisis dengan panjang gelombang 765 nm. Adapun kurva standar gingerol terdapat pada Lampiran 3.
Gambar 4 Alat uji difusi Franz
Keterangan :
Q = Jumlah kumulatif gingerol yang terpenetrasi per luas area membran (µg cm-2)
C = Konsentrasi gingerol (µg/ml) pada sampling jam ke-n V = Volume difusi Franz (100 ml)
= Jumlah konsentrasi gingerol(µg ml-1) jam ke-0 hingga sebelum jam ke-n
S = Volume sampling (0,5 ml) A = Luas area membran (3.730 cm2)
Uji Kelarutan
Kelarutan nanoemulsi ekstrak jahe dilakukan dengan mencampur nanoemulsi dan pelarut dengan perbandingan 1:1. Pelarut yang digunakan dari berbagai tingkat polaritas yaitu heksan, aseton, etanol, metanol dan air dengan nilai polaritas berturut-turut : 0, 47, 68, 73 dan 90 dalam gelas ukur 10 ml. Masing-masing campuran diaduk dengan sudip selama 5 menit kemudian diamati kelarutannnya setelah 3 jam. Analisis kadar gingerol pada fasa pelarut dilakukan dengan spektrofotometer. Persentase kelarutan nanoemulsi dihitung dengan rumus:
Keterangan:
P : Persentase kelarutan gingerol (%)
HASIL DAN PEMBAHASAN
Analisis Proksimat Serbuk Jahe
Jahe (Zingiber officinale) merupakan salah satu rempah-rempah yang termasuk dalam suku temu-temuan, satu famili dengan temu-temuan lainnya seperti temulawak (Curcuma xanthorrizha) dan kunyit (Curcuma domestica). Berdasarkan ukuran, bentuk, dan warna rimpangnya ada tiga jenis jahe yang dikenal, yaitu: jahe gajah (Zingiber officinale var. Roscoe) atau jahe putih, jahe putih kecil (Zingiber officinale var. Amarum) atau jahe emprit, dan jahe merah (Zingiber officinale var. Rubrum) atau jahe sunti (Wardana dkk 2002).
Jahe yang digunakan pada penelitian ini adalah jahe emprit (Gambar 5) yang berumur 9 bulan dimana pada umur tersebut kandungan minyak atsiri dan senyawa aktifnya dalam keadaan optimal. Jahe ini digunakan karena kandungan senyawa [6]-, [8]-, dan [10]- gingerol, serta [6]-shagaolnya tertinggi dibandingkan dengan jahe gajah ataupun jahe merah (Fathona 2011).
Gambar 5 Rimpang jahe emprit
Sebelum dilakukan proses ekstraksi, dilakukan proses pengeringan dan pengecilan ukuran bahan untuk mendapat sediaan berupa serbuk. Pengeringan bertujuan untuk mengurangi kadar air sehingga memudahkan pengeluaran minyak. Pengecilan ukuran bertujuan untuk mempercepat penetrasi bahan pelarut ke dalam bahan yang akan diekstrak, sehingga dalam waktu yang lebih singkat rendemen ekstrak yang diperoleh lebih tinggi. Pada dasarnya, semakin kecil ukuran bahan (makin luas permukaan bahan) maka semakin banyak minyak yang dapat diekstrak, akan tetapi ukuran bahan yang terlalu kecil juga menyebabkan banyak minyak yang menguap selama penghancuran.
Tabel 1 Analisis proksimat serbuk jahe kering
Parameter Nilai
Warna Cokelat
Aroma Khas, aromatis
Air (%) 11,88
Abu (%) 11,77
Protein (%) 9,71
Lemak (%) 8,93
Karbohidrat (by different) (%) 57,71
Rendemen yang diperoleh dipengaruhi oleh jumlah air yang teruapkan selama pengeringan. Analisis proksimat dilakukan untuk mengetahui kandungan dalam serbuk jahe kering. Hasil analisis proksimat serbuk jahe kering dapat dilihat pada tabel 1.
Menurut menurut Eze dan Agbo (2011), jahe kering memiliki kadar air 7-12%, karbohidrat 50-55%, dan sejumlah kecil protein, serat, lemak sampai 7%. Perbedaan hasil analisis dan literatur dapat dipengaruhi oleh beberapa faktor yaitu iklim, curah hujan, varietas jahe, keadaan lahan dan faktor lain (Koswara 1995). Komposisi rimpang jahe dapat mengalami perubahan selama penanganan lepas panen dan selama penyimpanan.
Penentuan kadar air penting untuk dilakukan karena dapat mempengaruhi masa simpan serbuk kering sampel dan sebagai salah satu syarat bahan baku herbal. Dengan kadar air <12% maka sampel dapat disimpan dalam jangka waktu yang lebih lama. Hal ini disebabkan karena pada tingkat kadar air tersebut sampel dapat terhindar dari pertumbuhan mikroba yang cepat (Harjadi 1986).
Rendemen dan Karakterisasi Oleoresin
Ekstraksi jahe dilakukan dengan metode maserasi yang mengacu pada penelitian Tririzqi (2013). Serbuk jahe dengan ukuran 40 mesh diekstraksi menggunakan pelarut heksana dengan perbandingan 1:4 yang dilakukan pada suhu ruang, kecepatan putaran 450 rpm dan waktu 6 jam. Tririzqi (2013), mendapatkan rendemen ekstrak jahe sebesar 6,01%.
Maserasi adalah proses pengekstrakan simplisia menggunakan pelarut dengan beberapa kali pengadukan pada suhu ruang. Maserasi bertujuan untuk menarik zat-zat berkhasiat yang terkandung dalam suatu bahan karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dan di luar sel, sehingga larutan yang lebih pekat terdesak keluar. Prinsip metode maserasi yaitu terjadinya peristiwa leaching pada komponen aktif dalam bahan yang memiliki sifat kelarutan yang sama dengan pelarut yang digunakan (Singh 2008).
Rendemen oleoresin yang diperoleh pada penelitian ini adalah 7,99%. Ekstrak yang didapatkan tersebut tidak murni oleoresin, melainkan masih mengandung sedikit pelarut yang terikat bersama oleoresin, sehingga tidak terupakan. Menurut Ketaren dan Djatmiko (1980), jahe kering memiliki kandungan oleoresin yang terdiri dari gingerol, zingiberol, shagaol dan zingiberen sekitar 0,5 sampai 5,3 persen, tergantung umur panen dan tumbuhnya.
Oleoresin (Gambar 6) merupakan gabungan resin dan minyak atsiri (20-30%), berbentuk padat atau semi padat, berwarna kecoklatan dan biasanya lengket. Oleoresin jahe juga mengandung komponen-komponen minor seperti gingerdiol, paradol, heksahidrokurkumin, gingerdiasetat, lemak, lilin, karbohidrat, vitamin dan mineral (Kimura et al. 2005; Shukla dan Singh, 2006). Resin ekstrak jahe mengandung senyawa aktif utama jahe yang merupakan turunan fenol, yaitu gingerol. Fungsi gingerol pada jahe adalah sebagai pembawa rasa pedas. Gingerol dibedakan menjadi [6], [8] dan [10] gingerol berdasarkan rantai cabangnya, namun limpahan gingerol tertinggi adalah [6]-gingerol. Hal ini sesuai dengan hasil karakteristik oleoresin pada Tabel 2 yang menunjukkan kandungan bahan aktif jahe terdiri atas [6], [8], dan [10] gingerol dimana limpahan tertinggi adalah [6]-gingerol sebesar 89,071 mg/g.
Tabel 2 Perbandingan produk oleoresin dengan standar oleoresin Karakteristik Standar Oleoresin Indesso Produk Oleoresin
Warna Cokelat tua Cokelat tua
Bentuk Cairan pekat/kental Cairan pekat
Aroma Aroma khas jahe Aroma Khas jahe
Indek Bias 1,488-1,495 1,4872
Densitas (gr/ml) 1,063-1,150 0,8997
[6] Gingerol (mg/g) - 89,071
[8] Gingerol (mg/g) - 23,418
[10] Gingerol (mg/g) - 88,909
[6] Shagaol (mg/g) - 82,100
Gingerol (Gambar 7) terdapat pada jahe yang masih segar dan dalam pengolahannya apabila dikeringkan atau dipanaskan, gingerol dapat berubah menjadi shogaol (Wohlmuth et al. 2005). Kecepatan degradasi dari [6]-gingerol menjadi [6]-shogaol tergantung pada pH, stabilitas terbaik pada pH 4, sedangkan pada suhu 100°C dan pH 1, degradasi perubahan relatif cukup cepat (Bhattarai et al. 2001). Gingerol dapat terdegradasi lebih lanjut menjadi zingerone dan aldehid pada pemanasan di atas 200oC (Purseglove et al. 1981). Gingerol, shogaol dan zingerone memberi efek farmakologi dan fisiologi seperti antioksidan, antiimflammasi, analgesik, antikarsinogenik, non-toksik dan non-mutagenik meskipun pada konsentrasi tinggi (Surh et al. 1998; Masuda et al. 1995; Manju dan Nalini 2005; Stoilova et al. 2007).
Nanoemusi Ekstrak Jahe
Nanoemusi Ekstrak Jahe
Nanoemulsi adalah sistem emulsi transparan atau bening dengan ukuran sangat kecil, biasanya dalam kisaran 2-500 nm. Nanoemulsi terdiri atas nanoemulsi minyak dalam air (o/w) atau nanoemulsi air dalam minyak (w/o), di mana inti dari partikel dapat berupa minyak atau air. Nanoemulsi stabil secara kinetik membuat nanoemulsi menjadi unik (Tadros 2005; Solans 2003; Fast & Mecozzi 2009). Menurut Tadros (2005), nanoemulsi memiliki keuntungan sebagai berikut :
1. Butiran berukuran sangat kecil, sehingga dapat mencegah terjadinya creaming
atau sedimentasi selama penyimpanan.
2. Cocok untuk penghantaran bahan aktif melalui kulit. Sistem nanoemulsi memiliki luas permukaan yang besar, sehingga penetrasi zat aktif lebih cepat. 3. Ukuran butiran yang kecil memudahkan penyebaran dan penetrasi dapat
ditingkatkan karena tegangan permukaan dan tegangan antarmuka yang rendah.
4. Berwarna transparan yang dapat memberikan estetika yang menarik dan menyenangkan saat digunakan.
Pembuatan nanoemulsi ekstrak jahe dilakukan menggunakan alat Ultra Turrax kecepatan 22.000 rpm selama 20 menit. Penggunaan alat mekanis Ultra Turrax berfungsi untuk memecah molekul-molekul makroskopik secara intens, sehingga menghasilkan ukuran yang lebih kecil. Bahan utama yang digunakan adalah oleoresin dan buffer fosfat pH 7. Oleoresin jahe yang dicampur ko-surfaktan berfungsi sebagai fase minyak pembawa obat atau zat aktif. Buffer fosfat pH 7 berfungsi sebagai fase air yang mencegah reaksi penyabunan pada saat pencampuran Tween 80, dimana Tween 80 dapat mengalami reaksi penyabunan pada lingkungan asam kuat atau basa kuat (American Pharmaceutical Co. 1994).
Bahan tambahan yang digunakan pada penelitian ini adalah emulsifier dan ko-surfaktan. Emulsifier yang digunakan pada pembuatan nanoemulsi ekstrak jahe adalah Tween 80. Penggunaan emulsifier dapat menurunkan tegangan antarmuka dari kedua fase cairan yang tidak saling bercampur, mengurangi gaya tolak antara cairan-cairan tersebut dan mengurangi gaya tarik-menarik antar molekul sejenis, sehingga mencegah terjadinya koalesen (Ansel 1989 dan Tangsuphoom et al. 2005). Emulsifier bekerja dengan membentuk film di sekeliling butiran yang terdispersi sehingga mencegah koalesen dan terpisahnya fase terdispersi (Anief 1999).
Berdasarkan uji karakteristik yang dilakukan, pada Tabel 3 terlihat bahwa terdapat perbedaan warna antara emulsi dan nanoemulsi ekstrak jahe. Emulsi memiliki warna kuning keruh, sedangkan nanoemulsi memiliki warna kuning jernih seperti gambar pada Lampiran 4. Nanoemulsi berwarna kuning jernih karena memiliki ukuran droplet yang sangat kecil, lebih kecil dari panjang gelombang cahaya tampak sehingga terlihat transparan, dimana perbedaan indeks refraktif antara fase minyak dan air cukup besar. Panjang gelombang cahaya tampak berkisar antara 400-700 nm, sedangkan nanoemulsi ekstrak jahe memiliki ukuran <100 nm, sehingga cahaya yang melewati cairan tersebut tidak terpecah atau dipecah oleh dropet nanoemulsi yang menyebabkan nanoemulsi terlihat transparan.
Berat jenis antara emulsi dan nanoemulsi tidak berbeda secara signifikan, begitu pula dengan pH. Secara umum, pH emulsi dan nanoemulsi tersebut mendekati pH netral yaitu 6,98 dan 6,72. Hal ini menunjukkan bahwa ukuran partikel tidak berpengaruh terhadap berat jenis dan pH. Nilai pH nanoemulsi ekstrak jahe yang dihasilkan aman digunakan sebagai bahan dasar obat karena sesuai dengan pH usus halus (7-7.4), dimana usus halus merupakan organ utama penyerapan obat (Utami 2012). Selain itu, hal ini juga menunjukkan bahwa buffer fosfat dengan pH 7 sebagai fase air mampu menjaga pH nanoemulsi yang dihasilkan (Jusnita 2014).
Berdasarkan hasil pengukuran viskositas, emulsi memiliki viskositas lebih tinggi (2,82 cP) dibandingkan nanoemulsi (1,85 cP). Viskositas sediaan berpengaruh terhadap pelepasan bahan aktif dari basis menuju permukaan membran. Viskositas nanoemulsi yang lebih rendah membuat kecepatan penetrasi zat aktif menjadi lebih cepat dan mudah sehingga meningkatkan mobilitas bahan aktif.
Tabel 3 Uji karakteristik emulsi dan nanoemulsi
Parameter Emulsi Nanoemulsi
Warna Kuning keruh Kuning jernih
Bentuk Cair Cair
memiliki stabilitas yang lebih baik terhadap agregasi droplet dan pemisahan karena gravitasi.
Stabilitas, sifat fisikokimia, dan sifat fungsional dari nanoemulsi dipengaruhi oleh komposisi fase dan kondisi proses produksi nanoemulsi (McClement 2010). Ukuran droplet yang semakin kecil membuat nanoemulsi stabil secara kinetik sehingga dapat mencegah terjadinya sedimentasi dan agregasi selama penyimpanan. Berbagai gaya yang menarik antara droplet menurun seiring dengan penurunan ukuran droplet sedangkan tolakan antara droplet meningkat membuat tingkat agregasi dan sedimentasi relatif sangat lambat (Solans et al. 2005; McClement 2005).
Pada penelitian ini dilakukan uji stabilitas nanoemulsi berdasarkan perubahan ukuran droplet selama penyimpanan. Nanoemulsi dibuat dengan dan tanpa penambahan antioksidan dan di simpan pada tiga variasi suhu yaitu suhu rendah 4oC, suhu ruang, dan suhu tinggi 45-50oC. Berdasarkan aturan polar paradox, pada minyak utuh, antioksidan polar/hidrofilik lebih dapat melindungi oksidasi karena berorientasi pada udara dan minyak, sedangkan pada emulsi, antioksidan nonpolar/lipofilik akan bersifat cukup aktif pada permukaan dan berorientasi pada interfasa minyak dan air sehingga menghambat minyak dari oksidasi (Frangkel et al. 1994). Namun, berdasarkan penelitian yang telah dilakukan Fatimah (2005) tentang efektivitas antioksidan pada emulsi minyak jagung, hasil menunjukkan bahwa aturan polar paradox hanya berlaku pada kadar minyak 10%, sedangkan pada konsentrasi 30% dan 50% aturan polar paradox
tidak berlaku. Penggunaan antioksidan non-polar tidak efektif, sehingga pada penelitian ini digunakan antioksidan polar yaitu asam askorbat karena persentase fase minyak yang digunakan pada penelitian ini adalah 30%.
Droplet nanoemulsi diukur dengan menggunakan alat PSA (Particle size analyzer). Selain ukuran droplet, nilai indeks polidispersitas (PDI) juga memberikan informasi mengenai kestabilan emulsi. Indeks polidispersitas (PDI) adalah parameter yang digunakan untuk melihat keseragaman ukuran dropet pada nanoemulsi. Semakin rendah nilai indeks polidispersitas, maka menunjukkan ukuran yang semakin seragam. Ukuran yang seragam ditunjukkan dengan grafik yang cenderung lebih curam, distribusi ukuran partikelnya yang lebih sempit dengan titik puncak yang lebih tinggi (Lampiran 5). Menurut Ahmed et al. 2012, nanoemulsi terbentuk jika ukuran diameter partikel <200 nm dengan nilai indeks polidispersitas 0,2<PDI<0,6 yang akan stabil dari kemungkinan terjadinya pertumbukkan partikel dan pemisahan gravitasi. Nanoemulsi ekstrak jahe mempunyai ukuran yang relatif homogen dan dapat dikatakan stabil karena memiliki nilai 0,08<PDI<0,4 (Lampiran 6).
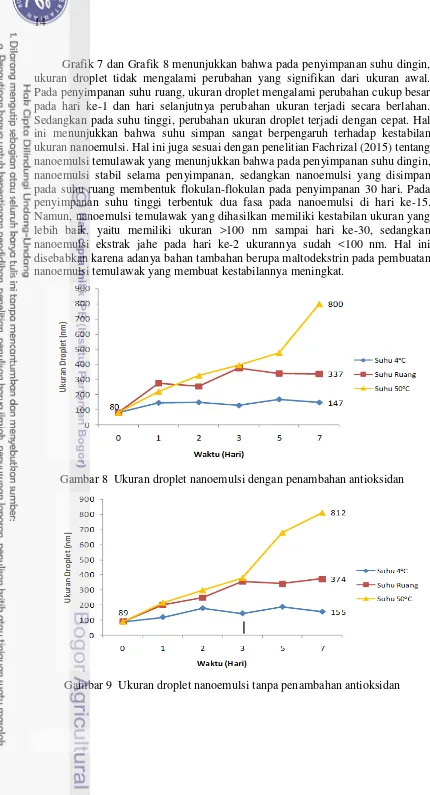
Grafik 7 dan Grafik 8 menunjukkan bahwa pada penyimpanan suhu dingin, ukuran droplet tidak mengalami perubahan yang signifikan dari ukuran awal. Pada penyimpanan suhu ruang, ukuran droplet mengalami perubahan cukup besar pada hari ke-1 dan hari selanjutnya perubahan ukuran terjadi secara berlahan. Sedangkan pada suhu tinggi, perubahan ukuran droplet terjadi dengan cepat. Hal ini menunjukkan bahwa suhu simpan sangat berpengaruh terhadap kestabilan ukuran nanoemulsi. Hal ini juga sesuai dengan penelitian Fachrizal (2015) tentang nanoemulsi temulawak yang menunjukkan bahwa pada penyimpanan suhu dingin, nanoemulsi stabil selama penyimpanan, sedangkan nanoemulsi yang disimpan pada suhu ruang membentuk flokulan-flokulan pada penyimpanan 30 hari. Pada penyimpanan suhu tinggi terbentuk dua fasa pada nanoemulsi di hari ke-15. Namun, nanoemulsi temulawak yang dihasilkan memiliki kestabilan ukuran yang lebih baik, yaitu memiliki ukuran >100 nm sampai hari ke-30, sedangkan nanoemulsi ekstrak jahe pada hari ke-2 ukurannya sudah <100 nm. Hal ini disebabkan karena adanya bahan tambahan berupa maltodekstrin pada pembuatan nanoemulsi temulawak yang membuat kestabilannya meningkat.
Gambar 8 Ukuran droplet nanoemulsi dengan penambahan antioksidan
Kenaikkan ukuran butiran nanoemulsi dipengaruhi oleh perbedaan suhu penyimpanan. Suhu penyimpanan yang tinggi berkaitan erat dengan perpindahan energi dari lingkungan ke fase air yang menyebabkan molekul-molekul air memperoleh energi. Energi yang diterima oleh air membuat molekul air bergerak dan tegangan antarmuka nanoemulsi naik (Shinoda dan Saitu 1969). Tegangan antarmuka fase air dan minyak yang naik dapat menyebabkan nanoemulsi cenderung tidak stabil (Hadiwiyoto 2011). Hal ini senada dengan McClements (2011) yang menyatakan bahwa pada kondisi suhu lingkungan yang berbeda menyebabkan interaksi yang kuat antara butiran fase terdispersi dengan fase pendispersi menurun sehingga menyebabkan ketidakstabilan emulsi. Adanya suhu yang tinggi menyebabkan droplet-droplet lebih sering berinteraksi sehingga beberapa droplet bergabung menjadi besar. Selain itu pula, besarnya ukuran droplet pada suhu tinggi juga disebabkan karena Tween 80 bersifat sangat tidak stabil dengan adanya panas. Tween 80 bersifat hidrofilik pada suhu rendah tetapi menjadi lipofilik dengan meningkatnya suhu karena dehidrasi rantai polyoxyethylene (Herrera 2012).
Penambahan asam askorbat sebagai antioksidan pada pembuatan nanoemulsi tidak berpengaruh terhadap kestabilan ukuran droplet. Hal ini ditunjukkan dari ukuran droplet nanoemulsi dengan penambahan asam askorbat memiliki ukuran tidak jauh berbeda dengan nanoemulsi tanpa penambahan asam askorbat (Lampiran 6). Nanoemulsi yang dibuat tanpa penambahan asam askorbat menunjukkan warna yang sedikit lebih cokelat, dibandingkan nanoemulsi yang dibuat dengan penambahan asam askorbat yang menunjukan warna kuning cerah. Hal disebabkan karena terjadi reaksi pencokelatan secara enzimatis pada nanoemulsi. Pembuatan nanoemulsi dengan kecepatan tinggi menghasilkan panas yang menyebabkan senyawa fenolat terdegrasi dan teroksidasi. Adanya panas (30oC-40oC) dan oksigen menyebabkan enzim polifenol oksidase atau enzim fenol hidroksidase yang bersifat reaktif akan bereaksi secara optimum dengan senyawa fenolat dalam oleoresin membentuk senyawa quinon yang berwarna cokelat karena adanya pigmen melanoidin (Feri 2010). Warna cerah pada nanoemulsi dengan penambahan antioksidan disebabkan karena asam askorbat dapat mereduksi kembali quinon menjadi senyawa fenolat. Pada penyimpanan suhu ruang dan suhu tinggi, terdapat endapan asam askorbat yang menunjukkan bahwa antioksidan ini tidak melarut sempurna pada sistem emulsi (Lampiran 7).
Bioavailabilitas Nanoemulsi Ekstrak Jahe
Bioavailabilitas adalah laju dan jumlah relatif obat yang mencapai sirkulasi umum tubuh atau sistem peredaran darah. Manfaat dari biovailabilitas diantaranya adalah dapat diketahui waktu yang dibutuhkan suatu obat agar dapat memberikan efek terapi dan seberapa banyak obat tersebut dapat terserap oleh tubuh. Bioavailabilitas dari nanoemulsi ekstra jahe dilakukan dengan studi penetrasi secara in vitro menggunakan alat difusi Franz. Studi penetrasi secara in vitro
Alat uji difusi Franz memiliki dua bagian utama, yaitu kompartemen donor dan kompartemen reseptor. Cairan kompartemen reseptor yang digunakan adalah buffer fosfat dengan pH 7. Larutan buffer digunakan karena pH cairan biologis manusia pada usus adalah 7-7.4 (Kuntarti 2010). Waktu yang digunakan pada uji ini adalah selama 8 jam. Pembentukan gelembung udara pada membran difusi harus dihindari karena gelembung udara di permukaan membran mengakibatkan pembentukan celah antara membran dengan cairan reseptor sehingga dapat menghalangi penetrasi zat aktif.
Hasil pengujian pada Gambar 9 menunjukkan bahwa kemampuan penetrasi sediaan nanoemulsi ekstrak jahe lebih cepat dan lebih besar dibandingkan dengan penetrasi emulsi. Pada gambar tersebut terlihat pada jam ke-8 hasil analisis cairan reseptor pada sediaan nanoemulsi mampu terpenetrasi 2,588 mg/cm2, sedangkan pada sediaan emulsi hanya mampu terpenetrasi 1,430 mg/cm2. Persentase gingerol terpenetrasi pada jam ke-8 pada sediaan nanoemulsi dan emulsi berturut-turut sebesar 49,50 % dan 17,58 % (Lampiran 8).
Gambar 10 Jumlah kumulatif gingerol terpenetrasi selama 8 jam
Kemampuan penetrasi dari sediaan nanoemulsi yang lebih baik dibandingkan dengan sediaan emulsi disebabkan karena ukuran droplet nanoemulsi yang lebih kecil dibandingkan dengan emulsi. Syukri (2002) menyatakan bahwa ukuran droplet suatu obat berpengaruh terhadap absorsi di dalam tubuh. Teori ini dibuktikan dengan penelitian yang dilakukan oleh Lanimarta (2012) yang membandingkan bioavailabilitas sediaan nanogel dan gel. Hasil menunjukkan bahwa kemampuan penetrasi nanogel lebih besar dibandingkan dengan gel.
Selain ukuran yang kecil, viskositas juga berpengaruh terhadap pelepasan bahan aktif dari basis menuju permukaan membran. Rendahnya viskositas nanoemulsi dibandingkan dengan emulsi akan meningkatkan kecepatan penetrasi, sehingga meningkatkan mobilitas zat aktif menuju permukaan membran. Berdasarkan hasil pengukuran viskositas, emulsi memiliki viskositas lebih tinggi (2,82 cP) dibandingkan nanoemulsi (1,85 cP).
Obat-obatan dalam ukuran nanometer mampu meningkatkan kelarutan dan penyerapan oleh tubuh. Selain itu pula, nanoemulsi memiliki energi bebas yang jauh lebih besar dibandingkan emulsi, sehingga menjadikannya suatu sistem transport yang efektif. Penggunaan obat-obatan dalam skala nano dapat mengurangi dosis obat yang dapat mengakibatkan efek samping pada beberapa pasien. Kemampuan penetrasi yang baik akan menghemat penggunaan bahan aktif suatu bahan.
Kelarutan Nanoemulsi Ekstrak Jahe
Pada penelitian ini, dibandingkan kelarutan nanoemulsi dan emulsi. Uji sifat kelarutan dilakukan dengan mencampur dalam gelas ukur 10 ml nanoemulsi atau emulsi dengan pelarut organik (1:1) dari berbagai tingkat polaritas yaitu heksan, aseton, etanol, metanol dan air dengan nilai polaritas berturut-turut : 0, 47, 68, 73 dan 90. Kelarutan suatu zat merupakan faktor yang sangat penting dalam suatu proses formulasi sediaan nanoemulsi untuk pemanfaatan lebih lanjut. Kelarutan suatu zat sebagian besar disebabkan oleh polaritas dari pelarut.
Ekstrak jahe dapat larut sempurna pada pelarut n-Heksan, etil asetat, aseton dan etanol tapi tidak dapat larut sempurna pada metanol dan air (Harmi 2013). Pada Tabel 4 terlihat bahwa emulsi sedikit larut pada pelarut non polar yaitu n-heksan, namun juga tidak terlarut sempurna pada pelarut lainnya yaitu aseton, air, methanol, dan ethanol. Emulsi memiliki kelarutan tertinggi pada pelarut ethanol, yaitu sebesar 57,7%. Campuran antara emulsi dan n-heksan menghasilkan larutan dua fasa yang tidak bercampur. Hal ini disebabkan karena emulsi sebagian besar terdiri dari air yang bersifat polar, sedangkan n-heksan bersifat non polar. Emulsi yang dicampurkan dengan aseton dan air menghasilkan larutan yang berwarna kuning keruh, sedangkan emulsi yang dicampur dengan ethanol dan methanol menghasilkan larutan yang berwarna kuning jernih (Lampiran 9).
Gingerol dalam nanoemulsi tidak larut pada n-heksan, namun terlarut sempurna pada pelarut lainnya. Campuran antara nanoemulsi dan n-heksan juga menghasilkan larutan dua fasa yang tidak bercampur, sedangkan campuran antara nanoemulsi dengan pelarut lainnya menghasilkan larutan yang homogen berwarna kuning jernih (Lampiran 9). Nanoemulsi ekstrak jahe memiliki kelarutan tertinggi pada pelarut air, yaitu 94,0%. Emulsi dan nanoemulsi yang digunakan memiliki komponen bahan penyusun yang sama, sehingga juga memiliki sifat kelarutan yang sama. Namun, nanoemulsi menunjukkan nilai kelarutan yang lebih baik pada pelarut semi-polar dan polar. Hal ini menunjukkan bahwa nanoemulsi dapat meningkatkan kelarutan zat dalam pelarut.
Tabel 4 Kelarutan gingerol emulsi dan nanoemulsi pada berbagai pelarut
Implikasi Teknis
Berdasarkan hasil penelitian, nanoemulsi sebaikanya disimpan dalam kondisi suhu yang rendah atau di dalam mesin pendingin. Nanoemulsi lebih stabil pada penyimpanan suhu dingin ditandai dengan ukuran droplet yang tidak berubah secara signifikan dari ukuran awalnya, sehingga mencegah terbentuknya agregasi dan terpisahnya fasa-fasa pembentuknya membuat nanoemulsi memiliki waktu simpan lebih lama. Selain itu pula, walaupun penambahan asam askorbat tidak berpengaruh terhadap kestabilan nanoemulsi, namun asam askorbat mampu mencegah terjadinya reaksi pencokelatan selama proses pembuatan dan penyimpanan.
Pembuatan nanoemulsi terbukti mampu meningkatkan karakteristik suatu zat yang memiliki kelarutan rendah, partikel besar, dan sulit diabsorpsi usus. Ukuran nanoemulsi <100 nm membuat kestabilan ukuran dan penyerapan zat aktif didalam usus lebih baik dibandingkan emulsi. Hal tersebut menyebabkan dosis obat yang mengakibatkan efek samping pada beberapa pasien dapat dikurangi. Kemampuan penetrasi yang baik akan menghemat penggunaan bahan aktif suatu bahan sehingga dengan jumlah bahan baku yang sama, produk yang dihasilkan akan lebih banyak dengan kata lain keuntungan akan meningkat. Kelarutan nanoemulsi yang lebih baik membuat proses pengaplikasiannya dalam produk akan lebih mudah dan lebih cepat karena tidak perlu adanya penambahan zat lain untuk meningkatkan kelarutan dan waktu pengadukan menjadi lebih singkat.
No Pelarut Kelarutan
Emulsi
Kelarutan Nanoemulsi
1 Heksana 24,7% 8,6%
2 Aseton 48,1 % 93,0%
3 Air 53,6 % 94,0%
4 Methanol 55,2 % 93,65
SIMPULAN DAN SARAN
Simpulan
Homogenizer Ultra Turrax kecepatan 22.000 rpm dengan waktu putar selama 20 menit dapat menghasilkan nanoemulsi ekstrak jahe dengan ukuran 80-89 nm. Nanoemulsi ekstrak jahe memiliki kestabilan ukuran paling baik pada penyimpanan suhu dingin 4oC. Penambahan asam askorbat pada nanoemulsi ekstrak jahe tidak menunjukkan pengaruh yang signifikan pada kestabilan ukuran droplet nanoemulsi. Nanoemulsi memiliki biovailabilitas zat aktif yang lebih besar dan menunjukkan persentase kelarutan yang lebih baik pada pelarut semi-polar dan semi-polar dibanding dengan emulsi. Hal ini menunjukkan bahwa nanoemulsi dapat meningkatkan penetrasi zat aktif dan kelarutan zat dalam pelarut.
Saran
DAFTAR PUSTAKA
Ahmed K, Y Li, DJ Mcclemments, H Xiao. 2012. Nanoemulsion and emulsion based delivevery systems for curcumin: encapsulation and release properties. Journal Food Chem. 132:799-807. doi: 10.1016/ j.foodchem.2011.11.039.
American Pharmaceutical Codex. 1994. Handbook of Pharmaceutical Exipients. London: Pharmaceutical Press.
Anief M. 1999. Sistem Dispersi, Formulasi Suspensi dan Emulsi. Yogyakarta: Gadjah Mada University Press. Hal: 56, 65-66, 71-79.
Ansel HC. 1989. Pengantar Bentuk Sediaan Farmasi. Ibrahim F, penerjemah. Jakarta (ID): UI-Pr. Terjemahan dari: Introduction to Pharmaceutical Dosage Forms.
Bhattarai S, VH Tran, CC Duke. 2001. The stability of gingerol and shogaol in aqueous solution. Journal Pharm. Sci. 90 : 1658–1664.
Bouchemal K, S Briancon, E Perrier, H Fessi. 2004. Nanoemulsion formulation using spontaneous emulsification: solvent, oil and surfactant optimisation.
International Journal of Pharmaceutics, 280: 241 – 251.
Debnath S, Satayanarayana, Kumar GV. 2011. Nanoemulsion a method to improve the solubility of lipophilic drugs. Journal of adv in Pharmaceutical Sci vol 2(2-3): 72-83.
Eze JI, KE Agbo. 2011. Comparative studies of sun and solar drying of peeled and unpeeled ginger. Am. Journal. Sci. Ind. Res. 2 : 136-143.
Fachrizal, Muhammad. 2015. Karakteristik Nanoemulsi Temulawak [skripsi]. Bogor: Institut Pertanian Bogor
Fast JP, Mecozzi S. 2009. Nanoemulsions for Intravenous drug delivery. Di dalam: Villiers MM, Aramwit P, Kwon GS, editor. Nanotechnology in Drug Delivery [internet]. New York: American Association of Pharmaceutical Scientist. hlm 461, 463-465; [diunduh 2015 April 20]. Tersedia pada: http://books.google.co.id.
Fathona D. 2011. Kandungan gingerol dan shogaol, intensitas kepedasan dan penerimaan panelis terhadap oleoresin jahe gajah (Zingiber officinale var. Roscoe), jahe emprit (Zingiber officinale var. Amarum), dan jahe merah (Zingiber officinale var. Rubrum)[skripsi]. Bogor: Institut Pertanian Bogor. Fatimah T. 2005. Efektivitas antioksidan dalam sistem emulsi oil in water (O/W)
[disertasi]. Bogor: Institut Pertanian Bogor.
Feri WAP. 2010. Penyimpanan Produk Pangan. Surabaya : Trubus Agrisarana. Frangkel EN, SW Huang, J Kenner, JB Bruce German. 1994. Interfacial
Hadiwiyoto S. 2011. Produk Meat Emulsion [Internet]. diunduh 2015 Jan 15. Tersedia pada: httpfoodreview.co.id.
Harimurti, Niken, Iceu A, Hoerudin. 2012. Pengaruh Konsentrasi Ekstrak dan Surfaktan (Tween 20 dan Tween 80) terhadap Karaketristik Nanoemulsi Ekstrak Temulawak dalam Pendispersi Minyak Sawit Merah. Seminar Bulanan. Balai Besar Penelitian dan Pengembangan Pascapanen Pertanian, Badan Penelitian dan Pengembangan Pertanian, Kementerian Pertanian RI. Harimurti, Sri Yuliani. 2010. Aplikasi Produk Mikrokapsul Oleoresin Jahe
Sebagai Bahan Perisaan Sirup. Prosiding Seminar Nasional Pascapanen Pertanian 2010.
Harmi L. 2013. Pembuatan nanogingerol dari ekstrak jahe (Zingiber officinale
Rosc) menggunakan homoginezer dengan kombinasi inversi komposisi dan suhu [tesis]. Bogor: Institut Pertanian Bogor.
Harjadi. 1986. Ilmu Kimia Analitik Dasar. Jakarta (ID): Erlangga.
Hartomo AJ, Widiatmoko MC. 1993. Emulsi dan Pangan Instant Berlesitin. Yogyakarta: Andi Oflset.
Herrera ML. 2012. Analytical Technique for Studying the Physical Properties of Lipid Emulsion ; Nano and Micro Food Emulsions. Springer.
Jusnita N. 2014. Produksi nanoemulsi ekstrak temulawak dengan metode homogenisasi [tesis]. Bogor: Institut Pertanian Bogor.
Kementretian Pertanian. 2008. Budidaya Organik Tanaman Jahe, Bogor: Balai Penelitian Tanaman Obat dan Aromatik Kementrian Pertanian.
Ketaren S, Djatmiko B. 1980. Minyak Atsiri Bersumber dari Batang dan Akar. Fakultas Teknologi Hasil Pertanian. Bogor: Institut Pertanian Bogor.
Kimura I, Pancho LR, Tsuneki H. 2005. Pharmacology of Ginger. Di dalam: Ravindran PN dan Babu KN (eds.). Ginger: The Genus Zingiber. Washington DC: CRC Press.
Koswara. 1995. Jahe dan Hasil Olahannya. Jakarta: Sinar Harapan.
Kuntarti. 2013. Kesetimbangan Cairan, Elektrolit, Asam, dan Basa [internet] . diunduh 20 Mei 2015 Tersedia pada: http://staff.ui.ac.id/system/files /users/kuntarti/publication/fluidbalance.pdf.
Lanimarta Y. 2012. Pembuatan dan uji penetrasi nanopartikel kurkumin-dendrimer poliamidoamin (Pamam) generasi 4 dalam sediaan gel dengan menggunakan sel difusi Franz [skripsi]. Depok (ID): Universitas Indonesia. Manju V, N Nalini. 2005. Chemopreventive efficacy of ginger, a naturally
occurring anticarcinogen during the initiation, post initiation stages of 1, 2 dimethyl hydrazine-induced colon cancer. Clin Chim Acta. 358: 60-67. Masuda T, A Jitoe, TJ Mabry. 1995. Isolation and structure determination of
McClement DJ. 2011. Edible Nanoemulsion: Fabrication, Properties and Functional Performance. Journal Soft Matter. 7(6); 2297-2316.
McClement DJ. 2010. Emulsion Design to Improve the Delivery of Funcional Liphophilic Component. An Rev of Food Sci and Tech. 1(1); 241-256. McClements DJ. 2005. Food Emultions: Principles, Practices and Techniques.
New York: CRC Press, pp 265-339.
Purseglove JW, Brown EG, Green CL dan Robbins SJR. 1981. Spices Volume II. New York (US): Longman Inc.
Rachmawati H, Budiputra DK, Mauludin R. 2014. Curcumin Nanoemulsion for Transdermal Application: Formulation and Evaluation. Bandung: ITB. Shah P, Bhalodia D, Shelat P. 2010. Nanoemulsioan: A Pharmaceutical review.
Sys Rev Pharm January – June Vol 1, Issue 1.
Shargel L, Yu ABC. 1999. Applied Biopharmaceutics. Edisi ke-4. Stanford. hlm 325-352.
Shinoda K, Saitu H. 1969. The stability of O/W type emulsions as function of temperature and the HLB of emulsifier: The emulsification by PIT-methode.
Journal Colloids and Interface Sci. 30; 258-263.
Shukla Y, Singh M. 2006. Cancer preventive properties of ginger: a brief review.
Journal Food and Chemical Toxicology 45: 683-690.
Sinko PJ. 2011. Farmasi Fisika dan Famarsetika 5th ed. Joshita Djajadisastra & Amalia H. Hadinata, Penerjemah. Jakarta: EGC.
Singh J. 2008. Maceration, percolation and infusion techniques for the extraction of medicinal and aromatic plants. Di dalam: S. K. Handa. Extraction Technologies for Medicinal and Aromatic Plants (hal 81). Trieste: International Centre for Science and High Technology.
Solanki KH. 2012. Incorporation of curcumin in lipid based delivery systems and assessment of its bioaccessibility [tesis]. New Jersey (US) : The State University of New Jersey.
Solans C, Izquerdo P, Nolla J, Azeman N, Ganca-Celma MJ. 2005. Nanoemulsions Curr.Opin. Journal Colloid Interface Sci.
Solans Conxita. 2003. Nanoemulsions Formation, Properties and Application. Mittal KL dan Shah DO, editor. Adsorption and Aggregation of Surfactants in Solution. New York: Marcel Dekker.
Surh YJ, E Loe, JM Lee.1998. Chemopreventive properties of some pungent ingredients present in red pepper and ginger. Mutat Res. 402:259-267. Stoilova I, A Krastanov, A Stoyanova, P Denev dan S Gargova. 2007.
Antioxidant activity of a ginger extract (Zingiber officinale). Food Chemistry.102: 764–770
Tadros, Tharwat F. (Ed.). (2005). Applied Surfactants: Surfactans in Nanoemulsions. Weinheim: Wiley-VCH. hlm 285-286.
Tangsuphoom N, JN Coupland. 2005. Effect of heating and homogenization on the stability of coconut milk emulsions. Journal Food Sci. 70 (8): 466-470. Thakker KD, Chern WH. 2003. Development and Validation of In Vitro Release
Test for Semisolid Dosage Forms-Case Study. Dissolution Technologies 2003, 10-15.
Tririzqi Fathia. 2013. Ekstraksi senyawa gingerol dari rimpang jahe dengan metode maserasi bertingkat [Skripsi]. Bogor: Institut Pertanian Bogor. Tusilawati Berliana. 2010. 15 Herbal Paling Ampuh. Yogyakarta: Aulia
Publishing.
Utami SS. 2012. Formulasi dan uji penetrasi in-vitro nanoemulsi, nanoemulsi gel dan gel kurkumin [skripsi]. Depok: Universitas Indonesia.
Wardana, Heru D, Barwa NS, Kongsjahju A, Iqbal A, Khalid M, dan Taryadi RR. 2002. Budi Daya secara Organik Tanaman Obat Rimpang. Jakarta: Penebar Swadaya.
Lampiran 1 Analisis Proksimat Serbuk Jahe Kering
a) Kadar Air (SNI 01-3181-1992 yang dimodifikasi)
Labu didih dan tabung Bidwell-Sterling dikeringkan dalam oven bersuhu 105°C dan didinginkan dalam desikator. Bubuk jahe ditimbang sebanyak 5 gram dan dimasukkan ke dalam labu didih yang telah dikeringkan dan ditambakan 60-80 ml toluena. Setelah alat dirangkai, refluks pada suhu rendah selama 45 menit kemudian suhunya dinaikkan dan dipanaskan selama 60-90 menit. Volume yang terdestilasi dibaca. Penetapan faktor destilasi diperoleh dengan mengganti sampel ekstrak jahe dengan air (4gram). Kadar air bahan dihitung dengan rumus sebagai berikut:
Kadar air (%) = x FD x 100% Keterangan:
Ws : Bobot contoh (g)
Vs : Volume air yang terdestilasi dari contoh (ml) FD : Faktor destilasi (g/ml)
Faktor destilasi dihitung dengan rumus sebagai berikut: FD =
W : Bobot air yang terdestilasi (g) V : Volume air yang terdetilasi (ml)
b) Kadar abu (SNI 01-3181-1992 yang dimodifikasi)
Cawan dikeringkan dalam oven bersuhu 105°C sebelum digunakan dan kemudian didinginkan dalam desikator selama 15 menit. Bubuk jahe ditimbang sebanyak 1.5 gram. Sebanyak 2 ml etanol dituang ke dalam cawan dan dibakar sampai etanol habis terbakar dan tidak mengeluarkan asap. Cawan dipanaskan menggunakan nyala api kecil lalu dipijarkan dalam tanur pada suhu 600°C selama 2 jam. Abu didinginkan dan dibasahi dengan beberapa tetes air, dikisatkan dan dipanaskan kembali dalam tanur selama satu jam pada suhu 600°C. Bila pada pembasahan ternyata abu telah bebas karbon, cawan dipindahkan ke dalam desikator dan dibiarkan dingin dan ditimbang. Kadar abu dapat dihitung dengan rumus sebagai berikut:
Kadar abu (%) = (M2-M0) x x
Keterangan:
M0 : Bobot cawan kosong (g)
M1 : Bobot cawan dan contoh (g)
c) Kadar Protein (AOAC 1995)
Penentuan kadar protein dilakukan dengan metode mikro-kjeldahl. Sampel dihomogenkan, kemudian sampel sebanyak 0.1 gram dimasukkan ke dalam labu kjeldahl 100 ml lalu ditambahkan katalis (CuSO4 dan Na2SO4) dan 2.5 ml H2SO4
pekat 98%. Selanjutnya sampel didekstruksi selama 30-40 menit sampai berwarna hijau bening. Setelah didinginkan, sampel ditambahkan dengan air suling hingga tanda tera. Sebanyak 5 ml larutan hasil pengenceran ditambahkan dengan 10 ml NaOH 40%, disuling selama 5 menit. Hasil penyulingan ditampung dalam erlenmeyer yang berisi 10 ml asam borat (2%) dan 0.1 ml campuran indikator hijau bromkresol 0,1% dengan merah metal 0,1% (5:1), kemudian dititrasi dengan larutan HCl 0.1 N sampai berwarna merah muda. Kadar protein dihitung dengan rumus sebagai berikut:
Kadar N (%) = x 100%
Keteerangan:
A : Selisih jumlah volume HCl titrasi blangko dan contoh (ml) N : Normalitas larutan HCl
Ws : Bobot contoh (mg) d) Kadar Lemak
Sebanyak 2 gram contoh bebas air diekstraksi dengan pelarut organik heksana dalam alat soxhlet selama 6 jam. Contoh hasil ekstraksi diuapkan dengan cara diangin-anginkan dalam over bersuhu 105°C. Contoh didinginkan dalam desikator dan ditimbang hingga diperoleh bobot tetap.
Kadar lemak (%) = x 100%
e) Kadar Karbohidrat (by difference)
Pada analisis bahan baku, kadar karbohidrat dihitung dengan cara by different, yaitu pengurangan jumlah komponen bahan total dengan jumlah kadar air, kadar abu, kadar lemak, kadar protein dan kadar serat. Kadar karbohidrat dihitung dengan rumus sebagai berikut:
Lampiran 2 Uji Karakterisasi Ekstrak Jahe dan Nanoemulsi
a) Indeks Bias
Ke dalam alat refraktometer yang telah dialirkan air pada suhu 25%, ditempatkan ekstrak jahe pada permukaan prisma dan tutup dengan memutar skrup. Sampel dibiarkan beberapa menit, kemudian dibaca.
b) Berat jenis
Piknometer dikosongkan hingga bebas dari air, kemudian didiamkan diatas neraca analitik selama 30 menit, kemudian timbang (berat piknometer kosong). Setelah itu, piknometer diisi oleoresin jahe secara berlahan hingga tidak terbentuk gelembung udara. Piknometer diletakkan dalam water bath yang mempunyai sikulasi air pada suhu 25oC, selama 30 menit. Piknometer diangkat diangkat dan dilap sampai bersih kemudian diletakkan di atas nerac analitik selama 30 menit dan ditimbang (berat piknometer + oleoresin). Dilakukan hal yang sama, namum sampel diganti dengan air akuades.
Berat Jenis =
c) Rendemen (%)
Oleoresin yang diperoleh dariproses ekstraksi ditimbang beratnya dengan menggunakan neraca analaitik.
Rendemen (%) = x 100%
d) Viskositas
Sampel diukur dengan viscosimeter ostwald pada suhu ruang (27 ± 0.2 0C) e) Derajat Keasamaan (pH) dengan menggunakan pH meter
Lampiran 3 Kurva Standar Gingerol
0
0,085 0,123 0,178
0,26 0,307
0,354 0,381 0,436
0,493 0,552
0 0,1 0,2 0,3 0,4 0,5 0,6
0 0,201 0,403 0,604 0,806 1,007 1,208 1,409 1,611 1,812 2,01
A
b
s
o
rb
a
n
s
i
Konsentrasi (mg/g)
Kurva Standar Gingerol
Lampiran 4 Emulsi dan Nanoemulsi Ekstrak Jahe
Lampiran 5 Distribusi ukuran nanoemulsi ekstrak jahe
Distribusi droplet nanoemulsi ukuran 80 nm
Distribusi droplet nanoemulsi ukuran 89 nm
Distribusi droplet nanoemulsi ukuran 476 nm
PDI : 0,2330
PDI : 0,2100
Lampiran 6 Perubahan ukuran droplet nanoemulsi selama penyimpanan
Stabilitas Ukuran Nanoemulsi Gingerol Dengan Penambahan Antioksidan
Hari Suhu 4oC Suhu Ruang Suhu 45-50oC
Stabilitas Ukuran Nanoemulsi Gingerol Tanpa Penambahan Antioksidan
80
800
89
812
0 100 200 300 400 500 600 700 800 900
0 1 2 3 5 7
U
k
u
ra
n
D
ro
p
le
t
(n
m
)
Waktu (Hari)
Perubahan Ukuran Droplet Suhu 45-
0ᵒC
Dengan Antioksidan
Lampiran 8 Hasil Uji Bioavailabilitas Emulsi dan Nanoemulsi Ekstrak Jahe
Jumlah gingerol rata-rata yang terpenetrasi tiap jam Waktu
(Jam)
Gingerol Terpenetrasi (mg/g)
Emulsi Nanoemulsi
0 0,000 0,000
1 0,000 0,000
2 0,000 0,007
3 0,000 0,038
4 0,007 0,042
5 0,011 0,049
6 0,023 0,079
7 0,034 0,091
8 0,053 0,095
Jumlah kumulatif gingerol terpenetrasi per luas membran setiap jam Waktu
(Jam)
Gingerol Terpenetrasi per luas membran (mg/cm2)
Emulsi Nanoemulsi
0 0,000 0,000
1 0,000 0,000
2 0,000 0,187
3 0,000 1,019
4 0,187 1,132
5 0,295 1,325
6 0,619 2,136
7 0,917 2,467
8 1,430 2,588
Perhitungan Jumlah Kumulatif Kurkumin yang terpenetrasi pada jam ke-8: Konsentrasi Emulsi = 3,033 mg/g 3,033 mg/ml Konsetrasi Nanoemulsi = 1,950 mg/g 1,950 mg/ml Jumlah emulsi yang diaplikasikan = 10 ml x 3,033 mg/ml = 30,33 mg Jumlah nanoemulsi yang diaplikasikan = 10 ml x 1,950 mg/ml = 19,50 mg Sediaan Emulsi:
Sediaan Nanoemulsi :
Persentase gingerol terpenetrasi selama 8 jam Waktu
(Jam)
Gingerol Terpenetrasi (%)
Emulsi Nanoemulsi
0 0,00 0,000
1 0,00 0,000
2 0,00 3,57
3 0,00 19,49
4 2,29 21,65
5 3,62 25,34
6 7,61 40,85
7 11,27 47,18
Lampiran 9 Kelarutan Emulsi dan Nanoemulsi pada Berbagai Pelarut Kelarutan emulsi :
Kelarutan nanoemulsi :
No Pelarut Gingerol Terlarut (mg/g) Emlusi Nanoemulsi
1 Heksana 0,374 0,083
2 Aseton 0,730 0,906
3 Air 0,813 0,916
4 Methanol 0,838 0,912
5 Ethanol 0,874 0,899
Heksana Aseton Air Methanol Ethanol
Bening
Keruh
Keruh Keruh
Bening
Bening
Heksana Aseton Air Methanol Ethanol
Bening Bening
Bening
Bening Bening
RIWAYAT HIDUP
Penulis memiliki nama lengkap Fleni Ayu Kenia Haque. Penulis dilahirkan di Menggala pada tanggal 19 Januari 1992 dari Ayah Sapriyadi dan Ibu Hujan Maningsih. Penulis merupakan putri pertama dari tiga bersaudara. Adik perempuan penulis bernama Dwi Dara Septi Putriani dan adik laki-laki bernama Anugrah Putra Sakti Oktavillano. Penulis menyelesaikan jenjang pendidikan mulai dari TK Angkasa (1996-1997), TK Abadi Perkasa (1997-1998), SD Abadi Perkasa (1998-2004), SMP Abadi Perkasa (2004-2007), SMA Sugar Group (2007-2010). Penulis kemudian melanjutkan studinya di Institut Pertanian Bogor (IPB), Departemen Teknologi Industri Pertanian (2010-2015) melalui jalur USMI.
Penulis pernah mengikuti program magang di Sugar Group Companies pada tahun 2011 dan 2012 pada divisi Workshop. Praktik lapang dilakukan di PT. Indolampung Perkasa pada tahun 2013 dengan judul Studi Manajemen Inventori Dan Database Komputer Werehouse PT. Indolampung Perkasa. Selama mengikuti perkuliahan, penulis cukup aktif dalam kepanitiaan yang diadakan oleh Himpunan Mahasiswa Teknologi Industri Pertanian (Himalogin) dan BEM Fateta, seperti
Agroindustrial Fair, Calistung BEM Fateta, Hari Warga Industri (Hagatri), One Step, dan Together. Penulis juga aktif pada Organisasi Mahasiswa antar Daerah (OMDA) dengan menjadi panitia dalam acara IPB Goes To Village dan menjadi Putri Provinsi Lampung di Gebyar Nusantara (2010).