DALAM TOLERANSI ASAM-ALUMINIUM PADA
Bradyrhizobium japonicum
DINI NURDIANI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER
INFORMASI
Dengan ini saya menyatakan bahwa tesis Analisis Fragmen DNA Genom yang Terlibat dalam Toleransi Asam-aluminium pada Bradyrhizobium japonicum adalah karya saya sendiri dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal dari atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
DINI NURDIANI. Analisis Fragmen DNA Genom yang Terlibat dalam Toleransi Asam-aluminium pada Bradyrhizobium japonicum melalui Mutagenesis dengan Transposon. Dibimbing oleh ANJA MERYANDINI dan ARIS TRI WAHYUDI.
Bradyrhizobium japonicum merupakan salah satu spesies bakteri dari kelompok Rhizobia yang umumnya dapat membentuk bintil akar pada tanaman Kedelai (Glycine max). Asosiasi antara bakteri bintil akar (BBA) dengan tanaman kelompok legum dapat menghasilkan fiksasi N2 atmosfer menjadi NH3 yang dapat digunakan untuk pertumbuhan tanaman.
Keasaman tanah merupakan salah satu masalah yang secara signifikan mempengaruhi produksi pertanian di banyak tempat di seluruh dunia. Penurunan pH tanah mempengaruhi organisme tanah termasuk mikroflora. Salah satu sistem biologi yang dipengaruhi oleh penurunan pH tanah adalah simbiosis antara BBA dan tanaman kelompok legum. Hal ini dapat mempengaruhi hasil asosiasi antara keduanya dalam fiksasi N2 menjadi NH3.
Beberapa galur B. japonicum telah dilaporkan memiliki toleransi yang tinggi terhadap asam-Al, diantaranya yaitu BJ11, BJ38, dan KDR15. Adanya galur-galur toleran tersebut dapat menjadi sumber eksplorasi materi genetik yang berperan dalam toleransi B. japonicum pada media asam-Al, yaitu dengan melakukan analisis gen penyandi ketahanan B. japonicum terhadap cekaman asam-Al di lingkungannya. Penelitian ini bertujuan untuk melakukan analisis fragmen DNA genom yang terlibat dalam toleransi B. japonicum terhadap cekaman asam-aluminium.
ABSTRACT
DINI NURDIANI. Analysis of Genomic DNA Fragment Involved in Acid-Aluminium Tolerance in Bradyrhizobium japonicum. Under the direction of ANJA MERYANDINI and ARIS TRI WAHYUDI.
Bradyrhizobium japonicum is one of Rhizobia species which generally form root nodule on soybean plant (Glycine max). In association with leguminous plant, root nodule bacteria (RNB) fix atmospheric nitrogen (N2) into NH3 which can be used for plant growth.
Soil acidity is a significant problem affecting agricultural production in many areas of the world. Lowering pH of the soil can affect soil organisms including the microflora. Among the biological system affected by the decrease in soil pH are those between RNB and leguminous plants. It could affect the association result between them in fixing nitrogen.
© Hak cipta milik Dini Nurdiani, tahun 2006
Hak cipta dilindungi
ANALISIS FRAGMEN DNA GENOM YANG TERLIBAT
DALAM TOLERANSI ASAM-ALUMINIUM PADA
Bradyrhizobium japonicum
DINI NURDIANI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Departemen Biologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Analisis Fragmen DNA Genom yang Terlibat dalam Toleransi Asam-aluminium pada Bradyrhizobium japonicum
Nama : Dini Nurdiani NIM : G351030021
Disetujui Komisi Pembimbing
Dr. Anja Meryandini, M.S. Dr. Aris Tri Wahyudi, M.Si.
Ketua Anggota
Diketahui
Ketua Program Studi Biologi Dekan Sekolah Pascasarjana
Dr. Ir. Dedy Duryadi S., DEA Prof. Dr. Ir. Syafrida Manuwoto, M.Sc.
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah yang berjudul Analisis Fragmen DNA genom yang Terlibat dalam Toleransi Asam-Aluminium pada Bradyrhizobium japonicum. Penelitian ini dibiayai oleh Hibah Bersaing No. XIII tahun 2005-2007.
Pada kesempatan ini penulis juga ingin mengucapkan terima kasih yang sebesar-besarnya kepada Dr. Anja Meryandini, MS. dan Dr. Aris Tri Wahyudi, MSi. selaku pembimbing atas saran, kritik, dan bimbingannya serta bantuan biaya dan fasilitas bahan-bahan yang digunakan selama penelitian.
Kepada Prof. Dr. Ir. Antonius Suwanto, selaku kepala Laboratorium Research Center for Microbial Diversity (RCMD), penulis mengucapkan terima kasih atas fasilitas laboratorium yang diberikan terutama dalam telaah genetika molekuler dari galur-galur mutan B. japonicum. Ucapan terima kasih juga penulis sampaikan kepada ibu Ani Fitriani atas saran, bantuan dan kerjasamanya terutama dalam menggunakan fasilitas di Laboratorium RCMD.
Ucapan terima kasih juga disampaikan kepada ayah, ibu, kakak-kakak dan adik-adik, atas segala doa dan kasih sayangnya, serta kepada laboran dan teman-teman di Laboratorium Mikrobiologi Rika, Elsie, Andini, Henry, Wulan, Risa, Prima dan juga kepada teman-teman yang namanya tidak dapat disebutkan satu persatu, atas bantuan dan kerjasamanya selama penelitian ini.
Akhir kata, penulis berharap semoga karya ilmiah ini bermanfaat.
Bogor, Januari 2006
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 17 Juli 1974 di Kuningan, Jawa Barat sebagai anak kelima dari pasangan bapak Drs. H. Mahmud (alm.) dan ibu E. Muthiah.
Tahun 1992 penulis lulus dari SMA Muhammadiyah Cirebon dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Jurusan Biologi, Fakultas Matematika dan Ilmu Pengeta-huan Alam, lulus pada tahun 1997. Sejak tahun 2000 penulis bekerja sebagai staf pengajar di Universitas Kuningan.
DAFTAR ISI
Halaman
DAFTAR TABEL ………. vi
DAFTAR GAMBAR ……… vii
DAFTAR LAMPIRAN ………. viii
PENDAHULUAN ……… 1
TINJAUAN PUSTAKA Bakteri Bintil Akar ………. 4
Toleransi Bakteri Bintil Akar terhadap Cekaman Lingkungan Asam ... 5
Mutagenesis dengan Transposon pada Bakteri ……….. 7
BAHAN DAN METODE Waktu dan Tempat ………….……… 11
Metode ………... 11
HASIL Penentuan Resistensi terhadap Antibiotik ……….. 22
Mutagenesis dengan Transposon dan Seleksi Mutan B. japonicum Sensitif Asam-Al ……… 23
Uji Pembentukan Bintil Akar ………. 25
Isolasi DNA Genom Pengapit Transposon dengan Inverse PCR dan Kloning Produk Inverse PCR ………. 26
Analisis Sekuen DNA Genom yang Terlibat dalam Toleransi Asam-Al 27
PEMBAHASAN ………... 29
SIMPULAN DAN SARAN ………... 36
DAFTAR PUSTAKA ………... 37
DALAM TOLERANSI ASAM-ALUMINIUM PADA
Bradyrhizobium japonicum
DINI NURDIANI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER
INFORMASI
Dengan ini saya menyatakan bahwa tesis Analisis Fragmen DNA Genom yang Terlibat dalam Toleransi Asam-aluminium pada Bradyrhizobium japonicum adalah karya saya sendiri dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal dari atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
DINI NURDIANI. Analisis Fragmen DNA Genom yang Terlibat dalam Toleransi Asam-aluminium pada Bradyrhizobium japonicum melalui Mutagenesis dengan Transposon. Dibimbing oleh ANJA MERYANDINI dan ARIS TRI WAHYUDI.
Bradyrhizobium japonicum merupakan salah satu spesies bakteri dari kelompok Rhizobia yang umumnya dapat membentuk bintil akar pada tanaman Kedelai (Glycine max). Asosiasi antara bakteri bintil akar (BBA) dengan tanaman kelompok legum dapat menghasilkan fiksasi N2 atmosfer menjadi NH3 yang dapat digunakan untuk pertumbuhan tanaman.
Keasaman tanah merupakan salah satu masalah yang secara signifikan mempengaruhi produksi pertanian di banyak tempat di seluruh dunia. Penurunan pH tanah mempengaruhi organisme tanah termasuk mikroflora. Salah satu sistem biologi yang dipengaruhi oleh penurunan pH tanah adalah simbiosis antara BBA dan tanaman kelompok legum. Hal ini dapat mempengaruhi hasil asosiasi antara keduanya dalam fiksasi N2 menjadi NH3.
Beberapa galur B. japonicum telah dilaporkan memiliki toleransi yang tinggi terhadap asam-Al, diantaranya yaitu BJ11, BJ38, dan KDR15. Adanya galur-galur toleran tersebut dapat menjadi sumber eksplorasi materi genetik yang berperan dalam toleransi B. japonicum pada media asam-Al, yaitu dengan melakukan analisis gen penyandi ketahanan B. japonicum terhadap cekaman asam-Al di lingkungannya. Penelitian ini bertujuan untuk melakukan analisis fragmen DNA genom yang terlibat dalam toleransi B. japonicum terhadap cekaman asam-aluminium.
ABSTRACT
DINI NURDIANI. Analysis of Genomic DNA Fragment Involved in Acid-Aluminium Tolerance in Bradyrhizobium japonicum. Under the direction of ANJA MERYANDINI and ARIS TRI WAHYUDI.
Bradyrhizobium japonicum is one of Rhizobia species which generally form root nodule on soybean plant (Glycine max). In association with leguminous plant, root nodule bacteria (RNB) fix atmospheric nitrogen (N2) into NH3 which can be used for plant growth.
Soil acidity is a significant problem affecting agricultural production in many areas of the world. Lowering pH of the soil can affect soil organisms including the microflora. Among the biological system affected by the decrease in soil pH are those between RNB and leguminous plants. It could affect the association result between them in fixing nitrogen.
© Hak cipta milik Dini Nurdiani, tahun 2006
Hak cipta dilindungi
ANALISIS FRAGMEN DNA GENOM YANG TERLIBAT
DALAM TOLERANSI ASAM-ALUMINIUM PADA
Bradyrhizobium japonicum
DINI NURDIANI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Departemen Biologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Analisis Fragmen DNA Genom yang Terlibat dalam Toleransi Asam-aluminium pada Bradyrhizobium japonicum
Nama : Dini Nurdiani NIM : G351030021
Disetujui Komisi Pembimbing
Dr. Anja Meryandini, M.S. Dr. Aris Tri Wahyudi, M.Si.
Ketua Anggota
Diketahui
Ketua Program Studi Biologi Dekan Sekolah Pascasarjana
Dr. Ir. Dedy Duryadi S., DEA Prof. Dr. Ir. Syafrida Manuwoto, M.Sc.
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah yang berjudul Analisis Fragmen DNA genom yang Terlibat dalam Toleransi Asam-Aluminium pada Bradyrhizobium japonicum. Penelitian ini dibiayai oleh Hibah Bersaing No. XIII tahun 2005-2007.
Pada kesempatan ini penulis juga ingin mengucapkan terima kasih yang sebesar-besarnya kepada Dr. Anja Meryandini, MS. dan Dr. Aris Tri Wahyudi, MSi. selaku pembimbing atas saran, kritik, dan bimbingannya serta bantuan biaya dan fasilitas bahan-bahan yang digunakan selama penelitian.
Kepada Prof. Dr. Ir. Antonius Suwanto, selaku kepala Laboratorium Research Center for Microbial Diversity (RCMD), penulis mengucapkan terima kasih atas fasilitas laboratorium yang diberikan terutama dalam telaah genetika molekuler dari galur-galur mutan B. japonicum. Ucapan terima kasih juga penulis sampaikan kepada ibu Ani Fitriani atas saran, bantuan dan kerjasamanya terutama dalam menggunakan fasilitas di Laboratorium RCMD.
Ucapan terima kasih juga disampaikan kepada ayah, ibu, kakak-kakak dan adik-adik, atas segala doa dan kasih sayangnya, serta kepada laboran dan teman-teman di Laboratorium Mikrobiologi Rika, Elsie, Andini, Henry, Wulan, Risa, Prima dan juga kepada teman-teman yang namanya tidak dapat disebutkan satu persatu, atas bantuan dan kerjasamanya selama penelitian ini.
Akhir kata, penulis berharap semoga karya ilmiah ini bermanfaat.
Bogor, Januari 2006
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 17 Juli 1974 di Kuningan, Jawa Barat sebagai anak kelima dari pasangan bapak Drs. H. Mahmud (alm.) dan ibu E. Muthiah.
Tahun 1992 penulis lulus dari SMA Muhammadiyah Cirebon dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Jurusan Biologi, Fakultas Matematika dan Ilmu Pengeta-huan Alam, lulus pada tahun 1997. Sejak tahun 2000 penulis bekerja sebagai staf pengajar di Universitas Kuningan.
DAFTAR ISI
Halaman
DAFTAR TABEL ………. vi
DAFTAR GAMBAR ……… vii
DAFTAR LAMPIRAN ………. viii
PENDAHULUAN ……… 1
TINJAUAN PUSTAKA Bakteri Bintil Akar ………. 4
Toleransi Bakteri Bintil Akar terhadap Cekaman Lingkungan Asam ... 5
Mutagenesis dengan Transposon pada Bakteri ……….. 7
BAHAN DAN METODE Waktu dan Tempat ………….……… 11
Metode ………... 11
HASIL Penentuan Resistensi terhadap Antibiotik ……….. 22
Mutagenesis dengan Transposon dan Seleksi Mutan B. japonicum Sensitif Asam-Al ……… 23
Uji Pembentukan Bintil Akar ………. 25
Isolasi DNA Genom Pengapit Transposon dengan Inverse PCR dan Kloning Produk Inverse PCR ………. 26
Analisis Sekuen DNA Genom yang Terlibat dalam Toleransi Asam-Al 27
PEMBAHASAN ………... 29
SIMPULAN DAN SARAN ………... 36
DAFTAR PUSTAKA ………... 37
Halaman 1 Pertumbuhan galur B. japonicum dan E.coli pada media agar yang
mengandung antibiotik ………... 22 2 Frekuensi Konjugasi pUTmini-Tn5Km1 dari E. coli S17-1 (λ pir)
ke B. japonicum pada tiga waktu inkubasi mating yang berbeda ………….. 24 3 Hasil uji pembentukan bintil akar pada tanaman siratro
DAFTAR GAMBAR
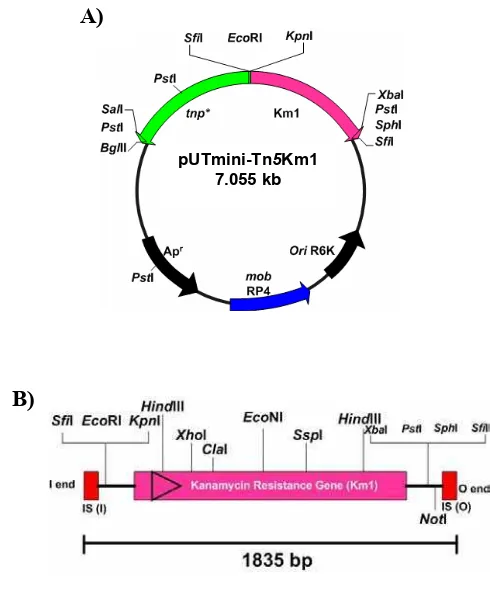
Halaman 1 A) Peta plasmid pUTmini-Tn5Km1. B) transposon mini-Tn5Km1 …… 9 2 Mutagenesis dengan transposon dari sel E. coli S17-1 (λ pir)
(pUTmini-Tn5Km1) ke sel B. japonicum melalui proses konjugasi …….. 13 3 Strategi amplifikasi DNA genom pengapit transposon dengan inverse
PCR ……… 18
4 Penampilan pertumbuhan B. japonicum toleran asam-Al galur BJ11, KDR15, dan BJ38 pada media YMA + CR 0.0025% + rifampisin
50 µg/ml setelah inkubasi selama 8 hari pada suhu ruang ……….... 23 5 A) Bintil akar tanaman siratro yang terbentuk hasil inokulasi dengan B.
japonicum KDR15 (WT), dengan B) akar tanaman siratro yang terbentuk hasil inokulasi dengan mutan AAS15.2 ………... 25 6 A) Elektroforesis gel agarosa DNA genom pengapit transposon yang
berhasil diamplifikasi dengan inverse PCR dari genom mutan B. japonicum sensitif asam-Al AAS11.2 (1) dan M= marker DNA 1 kb ladder plus. B) Peta plasmid rekombinan pGEMT-11 (∼3.8 kb) ………. 27 7 A) Hasil Elektroforesis gel agarosa plasmid rekombinan. M= Marker
DNA 1 kb ladder plus, 1 dan 2= pGEM-T11 yang dipotong dengan EcoRI. B) Hasil verifikasi DNA sisipan (insert) dalam plasmid rekombinan dengan PCR pada gel agarosa 1% ………... 27 8 Hasil pensejajaran (alignment) homologi antara sekuen fragmen DNA
Halaman 1 Tabel komposisi media agar Ayanaba (Ayanaba et al. 1983)……..………. 42 2 Komposisi larutan hara Ahmed dan Evans yang telah dimodifikasi
PENDAHULUAN
Latar Belakang
Kedelai merupakan sumber protein penting dan menjadi komponen utama sejumlah makanan yang biasa dikonsumsi masyarakat Indonesia. Nilai penting kedelai semakin meningkat dengan adanya program diversifikasi pangan dari pemerintah untuk mencapai kecukupan dan ketahanan dalam produksi pangan. Meskipun hasil produksi per hektar dan luasan pertanaman kedelai meningkat secara tetap, namun total produksi kedelai tidak mampu memenuhi kebutuhan di dalam negeri. Untuk meningkatkan produksi kedelai melalui perluasan lahan pertanian terdapat sejumlah kendala, karena pada lahan yang baru dibuka pada umumnya memiliki karakteristik tanah asam seperti tingginya kandungan Al dan Mn serta rendahnya kadar fosfat dan Ca (Saleh & Sumarno 1995).
perluasan pemanfaatan lahan asam untuk tanaman kedelai membutuhkan introduksi galur BBA yang toleran terhadap kondisi asam tersebut.
Bradyrhizobium japonicum merupakan salah satu spesies bakteri dari kelompok Rhizobia yang umumnya dapat membentuk bintil akar pada tanaman kedelai (Glycine max). pH optimum bagi pertumbuhan Bradyrhizobium berkisar antara 6-7 (Holt et al. 1994), akan tetapi isolat dari beberapa spesies Bradyrhizobium telah diidentifikasi memiliki kemampuan toleransi yang unggul terhadap cekaman pada tanah seperti pH rendah dan fosfat rendah (Bottomley 1992). Pada penelitian sebelumnya telah dilakukan seleksi terhadap galur-galur B. japonicum indigenus toleran media asam-Al dan diperoleh tiga galur toleran dengan nomor sandi galur BJ11 (Endarini et al. 1995), BJ38 (Fitri 1995), dan KDR15 (Imas et al. 1994). Kemampuan tumbuh dari galur toleran seperti BJ11 pada media kaldu Ayanaba (pH 4.5; Al 50 µM) menunjukkan bahwa galur
tersebut mampu mengakumulasi ammonium yang menyebabkan peningkatan pH media. Wahyudi et al. (1998) juga melaporkan bahwa galur BJ11 merupakan galur yang kompetitif dan berpotensi untuk dikembangkan sebagai galur introduksi (inokulan) pada lahan asam dengan menggunakan varietas kedelai yang juga toleran asam. Adanya galur-galur toleran tersebut dapat menjadi sumber eksplorasi materi genetik yang berperan dalam toleransi B. japonicum pada media asam-Al, yaitu dengan melakukan analisis gen penyandi ketahanan B. japonicum terhadap cekaman asam-Al di lingkungannya.
3
Transposon adalah elemen DNA yang dapat berpindah dari satu tempat ke tempat lain dalam suatu genom (Madigan et al. 2003). Insersi transposon biasanya akan menimbulkan suatu gen menjadi inaktif. Salah satu kegunaan penting dari transposon yaitu untuk mutagenesis, karena gen yang telah disisipi oleh transposon akan mengalami mutasi yaitu gen tersebut tidak dapat terekspresi. Kegunaan lain dari transposon yaitu dapat memudahkan untuk memetakan secara fisik maupun genetik dari suatu gen yang telah disisipi transposon dengan menggunakan enzim restriksi endonuklease (Snyder & Champness 1997). Transposon yang digunakan pada penelitian ini adalah transposon mini-Tn5Km1 yang membawa gen resistensi terhadap kanamisin yang telah dikonstruksi dalam plasmid pUT (didesain pUTmini-Tn5Km1). Penyisipan yang stabil pada kromosom dapat diperoleh ketika transposon mini-Tn5 berpindah tanpa membawa gen transposase (Herrero et al. 1990). Analisis gen dari mutan B. japonicum sensitif asam-Al dapat dilakukan dengan cara mengisolasi fragmen DNA yang mengapit transposon mini-Tn5 menggunakan teknik inverse PCR.
Tujuan
Penelitian ini bertujuan melakukan analisis fragmen DNA genom yang terlibat dalam toleransi B. japonicum terhadap cekaman asam-aluminium.
Bakteri Bintil Akar
Salah satu interaksi bakteri dengan tanaman yang paling penting dan
menarik adalah antara tanaman legum dan bakteri dari genus Rhizobium,
Bradyrhizobium, Shinorhizobium, Mesorhizobium dan Azorhizobium. Legum merupakan suatu kelompok besar tanaman yang memiliki nilai ekonomi penting
seperti kedelai, semanggi (clover), alfafa, buncis, dan kapri. Rhizobium,
Bradyrhizobium, Shinorhizobium, Mesorhizobium dan Azorhizobium adalah bakteri gram negatif motil yang berbentuk batang. Infeksi akar tanaman legum
oleh spesies yang cocok dengan salah satu genus tersebut mengarah pada
pembentukan bintil akar yang dapat mengubah nitrogen yang berupa gas menjadi
nitrogen terikat, dan proses ini dinamakan fiksasi nitrogen. Pada umumnya bintil
terbentuk pada akar tanaman, namun bintil juga dapat terbentuk pada batang,
misalnya pada legum tropis Sesbania yang dinodulasi oleh Azorhizobium caulinodans. Tanaman ini tersebar di daerah tropis yang tanahnya seringkali mengalami defisiensi nitrogen (Madigan et al. 2003).
Sekitar 90% dari seluruh spesies tanaman legum dapat mengalami
nodulasi. Namun, terdapat spesifisitas antara legum dan galur Rhizobium. Suatu galur Rhizobium umumnya dapat menginfeksi spesies legum tertentu dan tidak pada spesies lainnya. Sekelompok galur Rhizobium yang dapat menginfeksi kelompok legum yang berkerabat dinamakan kelompok inokulasi silang.
Walaupun galur Rhizobium mampu menginfeksi legum tertentu, tetapi tidak selalu dapat menghasilkan bintil yang memfiksasi nitrogen (Madigan et al. 2003).
Genus Bradyrhizobium hanya memiliki satu tipe spesies, yaitu
Bradyrhizobium japonicum (Holt et al. 1994). Menurut Perret et al. (2000), B. japonicum termasuk salah satu anggota famili Rhizobiaceae yang memiliki kisaran inang yang luas seperti pada tanaman anggota kelompok
Aeschynomeneae (Papilionoideae), Arachis spp., Phaseoleae (Papilionoideae),
Macroptilium, dan Vigna spp. Namun pada umumnya B. japonicum membentuk bintil akar pada jenis legum anggota kelompok Phaseoleae (Papilionoideae) dan
5
B. japonicum memiliki karakteristik antara lain berbentuk batang dengan ukuran 0.5-0.9 x 1.2-3.0 µm, tidak membentuk spora, dapat membentuk granul
poly-β-hidroksibutirat, motil dengan satu flagela polar atau subpolar, dan bersifat
aerobik. Temperatur optimum pertumbuhannya berkisar antara 25-30 oC sedang-kan pH optimumnya 6-7 meskipun demikian galur yang berasal dari tanah asam
dapat hidup di bawah pH optimum (Holt et al. 1994).
Toleransi Bakteri Bintil Akar terhadap Cekaman Lingkungan Asam
Simbiosis Rhizobium-legum dipengaruhi oleh penurunan pH tanah. Penurunan pH tanah tidak hanya menimbulkan peningkatan konsentrasi proton,
tetapi juga kelarutan logam seperti aluminium yang bersifat toksik terhadap BBA.
Respon BBA terhadap tanah asam tergantung pada interaksi sejumlah faktor
diantaranya konsentrasi H+, aktivitas Al3+ dan kemampuan kompetisi dan persistensi dari galur Rhizobium (Tiwari et al.1992).
Isolasi dan karakterisasi BBA dilakukan untuk memperoleh galur yang
toleran terhadap lingkungan asam. Adanya BBA yang toleran asam-Al menjadi
sumber eksplorasi materi genetik yang berperan dalam respon toleransi bakteri
tersebut pada lingkungan asam. Telaah molekuler dilakukan dengan
menggu-nakan mutan yang dihasilkan melalui mutagenesis dengan transposon seperti Tn5. Goss et al. (1990) melakukan karakterisasi mutan galur Rhizobium meliloti
WSM419 yang dihasilkan melalui mutagenesis dengan Tn5. Galur liar R. meliloti
WSM419 dapat bertahan hidup dan memiliki kemampuan nodulasi pada tanah
asam (pH 5.6). Sementara itu galur mutannya menjadi sensitif terhadap asam dan
tidak mampu tumbuh pada pH 5.6. Hal ini menunjukkan pada galur mutan telah
kehilangan kemampuan untuk memelihara pH intraselulernya (pHi). Hasil
analisis fragmen DNA yang membawa Tn5 dan klon sekuen pengapit dari mutan tersebut menunjukkan lokus act (untuk acid tolerance) berada pada 4.4 kb dari fragmen yang dipotong dengan EcoRI. Selanjutnya Tiwari et al. (1992) melakukan karakterisasi mutan yang diinduksi dengan Tn5 dari galur-galur R. meliloti WSM419 dan R. leguminosarum WSM710. Hasil pemetaan melalui pemotongan dengan enzim restriksi pada WSM419 menunjukkan bahwa gen yang
pemotongan dengan EcoRI. Pada galur mutan yang sensitif terhadap pH media di bawah 6.0 (TG2-6) dengan kandungan Ca 1 mM, dapat diperbaiki kemampuan
ketahanan hidupnya pada pH media 5.5 dengan penambahan Ca 50 mM. Pada
galur ini peningkatan konsentrasi Ca media dapat memperkecil penurunan pHi.
Sementara itu pada WSM710, dua gen yang berperan dalam toleransi terhadap
asam berada pada fragmen hasil pemotongan dengan EcoRI yang terpisah yaitu pada 12 kb dan 16 kb. Karena galur-galur R. leguminosarum lebih toleran terhadap asam daripada WSM419, maka terdapat kemungkinan untuk transfer
materi genetik dari galur yang lebih toleran ke galur yang kurang toleran.
Analisis sekuen DNA yang terlibat dalam respon toleransi BBA terhadap
lingkungan asam telah dipelajari pada R. tropici (Ricillo et al. 2000), R. leguminosarum bv. viciae, dan S. meliloti (Reeve et al. 2002). Hasil analisis gen yang mengalami penyisipan oleh Tn5-luxAB pada galur mutan R. tropici
CIAT899-13T2 yang tidak mampu tumbuh pada kondisi asam, menunjukkan
similaritas yang tinggi dengan gen gsh dari E. coli yang menyandikan enzim
glutathion synthetase. Kelimpahan Kalium dan pHi pada galur mutan tersebut lebih rendah dibandingkan tipe liarnya (Ricillo et al. 2000). Pada galur mutan R. leguminosarum bv. viciae, dan S. meliloti yang mengalami transposisi Tn5 pada gen actP mengalami hambatan ekspresi dari P-type ATPase yang termasuk subfamili CPx yang berperan dalam transport logam berat. Pada mutan yang
mengalami knockout pada gen actP tersebut menunjukkan sensitivitas terhadap Cu. Hal ini menunjukkan adanya keterlibatan logam berat tersebut dalam
mempertahankan pH media pada kondisi asam (Reeve et al. 2002).
Selain itu ketahanan terhadap pH juga dipelajari pada E. coli yang memiliki kemampuan adaptasi terhadap perubahan lingkungannya. E. coli dapat tumbuh pada kisaran pH eksternal yang luas yaitu antara 5-9. Pada E. coli
homeostasis pH tergantung pada konsentrasi K+ eksternal (White et al. 1992). Arginin dekarboksilase yang disandikan oleh gen adi mengalami induksi pada pH asam, anaerobiosis, dan media kaya. Hasil analisis sekuen DNA yang berukuran
3 kb dari kromosom E. coli yang menyandikan arginin dekarboksilase menunjukkan bahwa sekuen ini menyandikan protein yang terdiri atas 755 asam
7
lain dari E. coli yaitu CadA (lisin dekarboksilase), SpeC (ornitin dekarboksilase biosintetik) dan SpeF (ornitin dekarboksilase biodegradatif) (Stim & Bennet
1993).
Mutagenesis dengan Transposon pada Bakteri
Masing-masing tipe bakteri membawa transposon yang unik, berikut ini
adalah beberapa tipe transposon yang umum terdapat pada bakteri antara lain: (i)
insertion sequence elements (elemen IS), (ii) transposon komposit, dan (iii) transposon nonkomposit (Snyder & Champness 1997).
Elemen IS adalah transposon bakteri terkecil yang biasanya hanya
berukuran 750-2000 bp dan hanya mengkode enzim transposase yang dibutuhkan
dalam transposisinya. Elemen IS tidak membawa gen penanda seleksi dan
ditemukan hanya karena elemen ini menimbulkan inaktivasi dari gen yang
disisipinya. Pada E. coli secara alami ditemukan empat elemen IS yang berbeda yaitu IS1, IS2, IS3, dan IS4. Sampai saat ini telah ditemukan lebih dari 700 elemen IS pada bakteri, meskipun kebanyakan dapat digolongkan dalam 20
famili.
Kadang-kadang dua elemen IS dari tipe yang sama membentuk transposon
yang lebih besar, disebut tranposon komposit dengan membawa gen lain. Contoh
tipe transposon komposit yaitu Tn5, Tn9, dan Tn10. Untuk transposon komposit Tn5 misalnya terdiri atas gen untuk resistensi terhadap kanamisin (Kanr) dan resistensi streptomisin (Strr) yang diapit oleh elemen IS yang disebut IS50.
Transposon komposit bukan satu-satunya tipe transposon yang membawa
gen-gen resistensi terhadap antibiotik. Gen-gen tersebut juga dapat menjadi
bagian dari transposon nonkomposit. Gen-gen pada transposon nonkomposit
diapit oleh suatu inverted repeat dan tipe transposon ini minimal terdiri atas satu gen resistensi saja. Contoh transposon nonkomposit adalah Tn3 yang memiliki gen resistensi terhadap ampisilin.
Tidak semua tipe transposon dapat digunakan untuk mutagenesis. Suatu
transposon yang digunakan dalam mutagenesis harus memiliki kelengkapan
berikut ini: (i) memiliki kemampuan untuk berpindah dengan frekuensi yang
penanda seleksi sederhana, seperti resistensi terhadap antibiotik, dan (iv) dapat
digunakan untuk transposisi ke berbagai macam bakteri yang berbeda (broad host range). Tn5 ideal digunakan untuk mutagenesis acak pada bakteri gram negatif karena memiliki kelengkapan di atas. Tn5 tidak hanya berpindah dengan frekuensi yang relatif tinggi, tetapi juga transposon ini hampir tidak ada
spesifisitas dalam pemilihan targetnya dan mampu bertransposisi pada setiap
bakteri gram negatif. Tn5 juga membawa gen resistensi terhadap kanamisin yang dapat terekspresi pada hampir semua bakteri gram negatif (Snyder & Champness
1997).
Pada penelitian ini digunakan transposon mini-Tn5 yang merupakan turunan dari transposon Tn5. Keistimewaan transposon ini adalah tidak membawa gen transposase yang berperan dalam proses transposisinya. Untuk
proses transposisi dari mini-Tn5, gen transposase dikonstruksi pada plasmid yang membawanya yaitu pUT (pUTmini-Tn5) (Herrero et al. 1990). Setelah mini-Tn5
mengalami transposisi (berpindah) dalam hal ini dari plasmid ke kromosom, tidak
dapat melakukan transposisi kembali karena gen transposase-nya tetap berada di
dalam plasmid pUT.
Plasmid pUT merupakan turunan dari plasmid pGP704 dan memiliki
origin of replication dari plasmid R6K yang hanya dapat dipelihara pada bakteri penghasil π protein. Plasmid ini juga membawa origin of transfer (oriT) dari plasmid RP4, yang dapat menghasilkan transfer yang efisien ke sel resipien dari
galur donor yang mengekspresikan fungsi konjugatif dari RP4 seperti E. coli
SM10 (λ pir). pUT membawa gen tnp*, suatu mutan gen tnp dari IS50R yang tidak memiliki situs NotI dan menyandikan transposase yang dibutuhkan untuk transposisi dari elemen mini-Tn5 (Lorenzo et al. 1990). Penghilangan situs NotI tersebut tidak merubah struktur dari produk gen tnp. Gen transposase yang dimodifikasi (dengan menghilangkan situs NotI), dinamakan gen tnp* dan diklon pada situs SalI dari pGP704 derivatif dengan orientasi yang dapat mengatur proses transposisi secara optimal. Konstruksi ini dinamakan pUTKm. Plasmid
pUTKm mengendalikan donor minitransposon dengan penanda resistensi
9
pUT/Km terdiri atas tiga Kmr derivatif. Dua gen resistensi kanamisin berasal dari transposon Tn903 dengan orientasi yang berlawanan, sedangkan yang ketiga diisolasi dari Tn5 sendiri. Salah satu ciri penting dari elemen tersebut adalah hilangnya inhibitor transposase bersama dengan pUT setelah transposisi, sehingga
satu galur resipien dapat digunakan untuk proses insersi berulang dengan
menggunakan minitransposon yang memiliki penanda seleksi yang berbeda
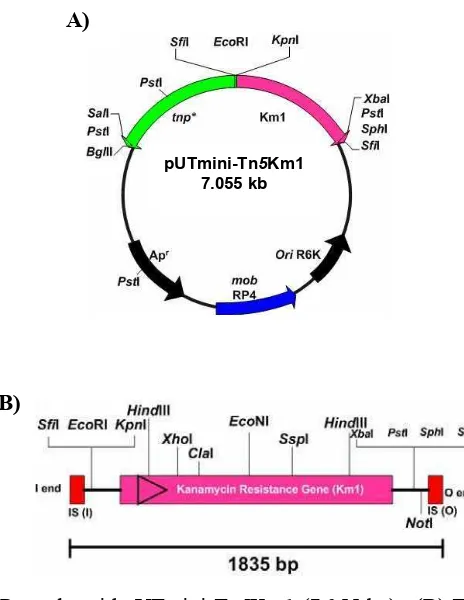
(Lorenzo et al. 1990). Gambar 1 menampilkan peta plasmid pUTmini-Tn5Km1 beserta transposon mini-Tn5Km1 yang digunakan dalam penelitian ini untuk melakukan mutagenesis dengan transposon melalui proses konjugasi.
Gambar 1 (A) Peta plasmid pUTmini-Tn5Km1 (7.055 bp). (B) Transposon mini-Tn5Km1.
Herrero et al. (1990) melaporkan hasil insersi transposon pada kromosom
melalui proses konjugasi antara E. coli SM10(λ pir) dengan Pseudomonas putida. Dari hasil analisis pada 8 koloni ekskonjugan menunjukkan bahwa terjadi insersi
tunggal pada masing-masing ekskonjugan, insersi transposon pada kromosom
ekskonjugan terjadi pada lokasi yang berbeda, dan gen transposase tidak terdapat
A)
B)
[image:32.612.193.438.272.568.2]pada ekskonjugan. Pada penelitian ini dilakukan mutagenesis dengan transposon
mini-Tn5Km1 dari E. coli S17-1 (λ pir) ke B. japonicum toleran asam-Al melalui proses konjugasi dan dari ekskonjugan yang diperoleh diharapkan terdapat mutan
sensitif asam-Al. Selanjutnya dari galur mutan sensitif dilakukan isolasi gen yang
BAHAN DAN METODE
Waktu dan Tempat
Penelitian ini dilakukan di Laboratorium Mikrobiologi dan Research
Center for Microbial Diversity (RCMD), Departemen Biologi, FMIPA, IPB dari
bulan Januari sampai dengan Nopember 2005.
Bahan
Bahan yang digunakan dalam penelitian ini adalah tiga galur B. japonicum
toleran asam-aluminium dengan nomor sandi galur BJ11, BJ38, dan KDR15.
Ketiga galur tersebut digunakan sebagai resipien dalam konjugasi dan Escherichia
coli S17-1 (λ pir) (pUTmini-Tn5Km1) digunakan sebagai donor dalam
mutagenesis dengan transposon. Galur E. coli DH5 α digunakan sebagai inang
dalam kloning fragmen DNA. Vektor plasmid pGEM-T Easy digunakan untuk
TA-cloning fragmen DNA genom yang terlibat dalam toleransi asam-Al.
Metode
Media dan Kondisi Pertumbuhan
E. coli DH5 α secara rutin ditumbuhkan pada media Luria Bertani broth
(LB) (tryptone 10.0 g/l, NaCl 10.0 g/l, yeast extract 5.0 g/l) tanpa antibiotik. E.
coli S17-1 λ pir (pUTmini-Tn5Km1) secara rutin ditumbuhkan pada media LB
yang mengandung ampisilin (100 µg/ml) dan kanamisin (50 µg/ml) pada suhu 37
o
C. E.coli DH5 α yang membawa plasmid rekombinan pGEM-T dikulturkan pada
media LB yang mengandung ampisilin (100 µg/ml) dan kanamisin (50 µg/ml)
pada suhu 37 oC. Galur BJ11, BJ38, dan KDR15 dikulturkan secara aerobik pada
media yeast extract mannitol agar (YMA) (manitol 10.0 g/l, K2HPO4 0.5 g/l,
MgSO4·7H2O 0.2 g/l, NaCl 0.2 g/l, yeast extract 1.0 g/l).
Penentuan Resistensi terhadap Antibiotik
Tiga galur B. japonicum yang digunakan dalam penelitian ini dengan sandi
beberapa antibiotik untuk menentukan penanda antibiotik yang akan dipakai
dalam seleksi transkonjugan.
Sebelum dilakukan pengujian pada media dengan antibiotik terlebih
dahulu ketiga galur tersebut diremajakan pada media agar cawan YMA selama
7-8 hari pada suhu ruang. Selanjutnya masing-masing biakan tersebut digoreskan
pada agar cawan YMA + Congo Red (CR) 0.0025% + antibiotik. Antibiotik yang
digunakan dalam pengujian ketiga galur tersebut yaitu ampisilin 50 µg/ml dan 100
µg/ml, kanamisin 25 µg/ml dan 50 µg/ml, rifampisin 25 µg/ml dan 50 µg/ml, serta
tetrasiklin 25 µg/ml dan 50 µg/ml. Inkubasi dilakukan pada suhu ruang selama
7-8 hari dan diamati pertumbuhannya. Biakan yang tumbuh berarti resisten,
sedangkan yang tidak tumbuh berarti sensitif terhadap antibiotik yang digunakan.
Pengujian resistensi terhadap antibiotik tersebut juga dilakukan pada E. coli S17-1
(λ pir) pada media agar cawan Luria agar (LA).
Penyiapan Kultur untuk Konjugasi
Galur BJ11, BJ38, dan KDR15 masing-masing ditumbuhkan pada 50 ml
media yeast extract mannitol broth (YMB) yang ditambah Rifampisin (50 µg/ml)
dan dikocok dengan mesin pengocok (shaker) kecepatan 200 rpm pada suhu
ruang dengan waktu inkubasi 60 jam sampai sel mencapai fase logaritmik (∼108 sel/ml). Galur E. coli S17-1 (λ pir) (pUTmini-Tn5Km1) ditumbuhkan pada 25 ml
LB yang ditambah dengan kanamisin (50 µg/ml). Pengocokan dilakukan dengan
kecepatan 200 rpm pada suhu 37 oC selama 18-20 jam.
Mutagenesis dengan Transposon
Introduksi transposon mini-Tn5Km1 (pUTmini-Tn5Km1, 7055 bp)
(Gambar 1) ke dalam sel B. japonicum dilakukan melalui konjugasi. Kultur B.
japonicum dan E. coli yang telah mencapai fase logaritmik disentrifugasi dengan
kecepatan 2300 g selama 3 menit dan peletnya dicuci sebanyak tiga kali dengan
NaCl 0.85% untuk membersihkan sel dari sisa antibiotik. Pelet sel donor
disuspensikan dalam 40 µl kaldu LB modifikasi (tryptone 5.0 g/l, NaCl 1.0 g/l,
yeast extract 5.0 g/l) dan dicampurkan dengan pelet sel resipien dengan
13
sel/ml. Campuran ini selanjutnya diletakkan di atas filter nitroselulosa steril
(ukuran pori 0.45 µm) pada media LA modifikasi. Pada media tersebut dibuat tiga juring sehingga pada tiap juring dapat diletakkan satu buah filter,
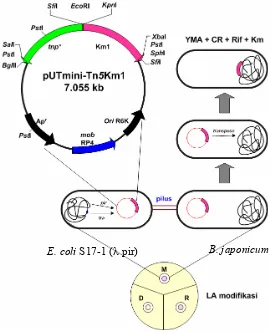
masing-masing untuk donor (D), resipien (R), dan campuran antara D dan R (M). Gambar
2 memperlihatkan diagram skematik dalam melakukan mutagenesis dengan
transposon. Mating dilakukan secara aerobik pada suhu ruang dengan tiga waktu
lama inkubasi yaitu 12, 18, dan 24 jam. Selanjutnya filter diangkat dan
dimasukkan ke dalam tabung mikro yang berisi 1 ml garam fisiologis (NaCl
0.85%) dan divorteks. Masing-masing suspensi sel sebanyak 100 µl disebarkan
pada media YMA ditambah kanamisin (50 µg/ml) dan rifampisin (50 µg/ml).
Inkubasi dilakukan pada suhu ruang selama 5-8 hari dan dihitung frekuensi
[image:36.612.165.436.317.650.2]transkonjugasinya.
Gambar 2 Mutagenesis dengan transposon dari sel E. coli S17-1 (λ pir) (pUTmini-Tn5Km1) ke sel B. japonicum melalui proses konjugasi.
Seleksi Mutan B. japonicum Sensitif asam-Al
Koloni transkonjugan hasil sebar yang telah tumbuh pada media YMA +
CR 0.0025% + rifampisin (50 µg/ml) + kanamisin (50 µg/ml) direplika pada media yang sama dan diseleksi sensitivitasnya terhadap asam-Al dengan
menggunakan media agar asam-Al Ayanaba (pH 4.5 ditambah 50 µM Al) yang komposisinya dibuat sesuai dengan komposisi Ayanaba et al. (1983) (Tabel
Lampiran 1). Transkonjugan yang tidak tumbuh pada media tersebut adalah
mutan dari B. japonicum yang sensitif asam-Al.
Uji Pembentukan Bintil Akar
Galur-galur mutan B. japonicum sensitif asam-Al hasil konjugasi,
masing-masing diuji kemampuannya untuk membentuk bintil akar. Uji pembentukan
bintil akar pada tanaman siratro (Macroptilium atropupureum) menggunakan
metode tabung sedangkan untuk pembentukan bintil akar pada tanaman kedelai
(Glycine max) digunakan botol Leonard berdasarkan metode Vincent yang
dimodifikasi seperti yang telah dilaporkan Wahyudi (1998).
Uji Pembentukan Bintil Akar pada Tanaman Siratro. Biji siratro yang
telah dipilih (tidak luka, tidak keriput, tidak terapung, dan memiliki ukuran
seragam) ditoreh kulit bijinya dengan silet untuk menghilangkan masa
dormansinya. Sterilisasi permukaan biji dilakukan dengan cara merendam biji
berturut-turut dalam alkohol 95% selama 10 detik, H2O2 5% selama 5 menit, dan
dibilas dengan akuades steril sebanyak 7 kali. Biji selanjutnya dikecambahkan
dalam cawan petri berisi kertas saring steril yang telah dibasahi akuades steril.
Perkecambahan dilakukan selama 2 hari pada suhu ruang dalam keadaan gelap.
Sementara itu media agar tegak (20 ml) disiapkan dalam tabung berukuran
25x200 mm. Media agar tersebut terdiri atas larutan hara yang komposisinya
dibuat berdasarkan komposisi Ahmed & Evans (Speidel & Wollum 1980) (Tabel
Lampiran 2) yang telah dimodifikasi dan ditambahkan agar Bacto 0.85%.
Kecambah siratro yang berumur 2 hari ditanam secara aseptik pada tabung agar
tegak tersebut masing-masing satu kecambah. Setelah kecambah berumur 2 hari
di dalam tabung (4 hari) dilakukan inokulasi B. japonicum mutan dan galur
15
media agar YMA miring selama 8 hari. Selanjutnya ke dalam biakan
ditambahkan 1 ml garam fisiologis steril untuk mendapatkan seluruh suspensi
dengan tingkat kekeruhan sekitar 109 sel/ml dan diinokulasikan ke dalam tabung
agar tegak yang telah ditumbuhi kecambah siratro. Tabung-tabung tersebut
kemudian dibenamkan kurang lebih setinggi media agar tegak dalam bak pasir
yang telah dibasahi air dan disimpan di rumah kaca. Suhu pasir dijaga agar tidak
lebih dari 30 oC dengan cara menyiram pasir setiap 2-3 hari sekali. Pengamatan
bintil akar yang terbentuk dilakukan mulai hari ke-5 sampai ke-30 setelah
inokulasi.
Uji Pembentukan Bintil Akar pada Tanaman Kedelai. Biji kedelai
dipilih, disterilisasi, dan dikecambahkan dengan perlakuan yang sama seperti
yang dilakukan pada biji siratro. Kecambah yang berumur dua hari selanjutnya
ditanam dalam botol Leonard. Media yang digunakan berupa pasir dan arang.
Pasir yang digunakan adalah yang tertahan ayakan yang berukuran 50 mesh (0.31
mm) dan lolos ayakan 30 mesh (0.52 mm), yang sebelumnya telah dicuci dengan
air bersih 10 kali dan dikeringkan. Arang yang digunakan adalah tumbukan arang
yang tertahan ayakan 28 mesh dan lolos ayakan 3 mm. Perbandingan pasir dan
arang 3:1 dan setiap botol diisi 480 gram. Botol Leonard modifikasi terdiri atas
dua botol kecap atau bir volume 700 ml. Salah satu botol dipotong dan pada
bagian dasarnya digunakan untuk media penumbuhan yang berisi pasir dan arang.
Botol lainnya dipotong pada bagian leher dan digunakan sebagai tandon untuk
larutan hara. Botol yang berisi campuran pasir dan arang diletakkan di atas botol
tandon yang berisi larutan hara. Masing-masing botol diisi 300 ml larutan hara
bebas N menurut Alva et al. (1988) (Tabel Lampiran 3) dan 100 ml disiramkan ke
atas campuran pasir dan arang. Botol bagian atas ditutup dengan aluminium foil.
Selanjutnya seluruh botol ditutup dengan kertas semen dan dilakukan sterilisasi
pada suhu 121 oC selama 2 jam. Biji kedelai yang dikecambahkan ditanam pada
media pasir-arang dengan tandon yang berisi larutan hara dalam botol Leonard.
Untuk tiap botol ditanam dua kecambah. Bersamaan dengan penanaman juga
diinokulasikan suspensi B. japonicum mutan dan tipe liarnya sebanyak 1 ml
(dengan menambahkan garam fisiologis pada biakan hingga kepekatan sel sekitar
dan diletakkan dalam ruangan pada suhu kamar 2-3 hari (sampai ujung atas
kecambah menyentuh aluminium foil). Permukaan aluminium foil dibuka dan
selanjutnya botol tersebut diletakkan di rumah kaca. Larutan hara bebas N
ditambahkan setiap dua hari sekali dan tanaman dipelihara hingga 30 hari setelah
inokulasi.
Isolasi DNA Genom Mutan B. japonicum Sensitif Asam-Al
Mutan B. japonicum dikulturkan pada media YMB (50 ml) yang ditambah
kanamisin (50 µg/ml) dan rifampisin (50 µg/ml), dan diinkubasi pada suhu ruang
sampai mencapai fase logaritmik. Selanjutnya isolasi DNA genom dilakukan
dengan menggunakan metode CTAB (Sambrook & Russel 2001).
Sel kemudian dipanen dengan mengambil sebanyak 50 ml kultur dan
disentrifugasi dengan kecepatan 9000 g selama 10 menit. Kemudian pelet
dipindahkan pada tabung eppendorf steril dan dicuci 2-3 kali dengan 250 µl buffer
TE 1x. Pelet diresuspensi dalam 250 µl buffer TE 1x, 50 µl SDS 10%, dan 10 µl
proteinase K (10 mg/ml), dan diinkubasi pada suhu 37 oC selama 1 jam.
Selan-jutnya suspensi ditambah dengan 80 µl NaCl 5 M dan 100 µl CTAB (suhu 65 oC),
dan diinkubasi selama 20 menit dalam penangas air pada suhu 65 oC. Suspensi
lalu ditambah dengan 600 µl fenol-kloroform-isoamilalkohol (25:24:1), dikocok
kuat dan disentrifugasi pada kecepatan 12900 g selama 15 menit. Fase cair
diambil dan dicampur kloroform-isoamilalkohol (24:1) dengan volume yang
sama, dan disentrifugasi dengan kecepatan 12900 g selama 15 menit. Selanjutnya
supernatan dipresipitasi dengan etanol absolut dingin sebanyak 2x volume
supernatan dan dicampur dengan hati-hati. DNA hasil presipitasi diinkubasi di es
selama 30 menit, dicuci dengan etanol 70% dan disentrifugasi dengan kecepatan
12900 g selama 10 menit. Pelet DNA dikeringudarakan dan dilarutkan dalam 20
µl ddH2O yang mengandung RNase 1% dan diinkubasi pada suhu 37 oC selama
17
Isolasi DNA Pengapit Transposon dengan Inverse Polymerase Chain Reaction
(Inverse PCR)
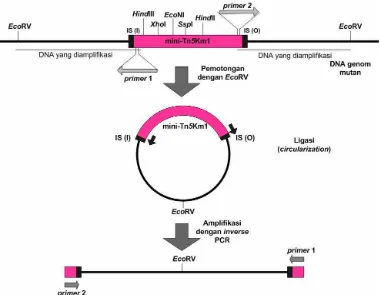
Untuk mengamplifikasi DNA genom yang mengapit transposon digunakan
metode seperti yang diterangkan Wahyudi et al. (2001) yang dimodifikasi
(Gambar 3), seperti diuraikan berikut ini.
Preparasi DNA Cetakan (Template). DNA cetakan untuk inverse PCR
disiapkan dari sekitar 1 µg DNA genom mutan B. japonicum sensitif asam-Al
yang dipotong dengan EcoRV (enzim restriksi ini tidak memotong
mini-Tn5Km1). DNA hasil pemotongan diekstrak dengan
fenol-kloroform-isoamilalkohol dan dipresipitasi dengan etanol absolut yang mengandung 0.1
volume Na-asetat 3 M pH 4.6. DNA selanjutnya dicuci dua kali dengan etanol
70% dan disentrifugasi dengan kecepatan 12900 g. Pelet DNA dilarutkan dalam 5
µl ddH2O steril dan seluruhnya diligasi menggunakan T4 DNA ligase sebanyak 3
Weiss unit (Promega, USA). Campuran ligasi diinkubasi semalam pada suhu 4
o
C. Selanjutnya DNA sirkuler digunakan sebagai cetakan dalam inverse PCR.
Kondisi Inverse PCR. Fragmen DNA genom yang mengapit transposon
mini-Tn5 (sekitar 0.5 µg) diamplifikasi menggunakan Gene Amp PCR 2400
(Perkin Elmer, USA) dalam campuran reaksi dengan volume total 50 µl yang
mengandung 2.5 mM dNTP mixture, GC buffer II, LA Taq DNA polimerase 2.5
unit dan primer yang didesain dari sekuen mini-Tn5Km1 yang diarahkan keluar
dari tranposon. Primer (P1: 5’-ACA CTG ATG AAT GTT CCG TTG-3’ dan P2:
5’-ACC TGC AGG CAT GCA AGC TTC-3’) masing-masing 100 pmol
digunakan untuk mengamplifikasi sekuen DNA yang mengapit transposon
upstream dan downstream. Denaturasi DNA sampel dilakukan pada suhu 95 oC
selama 2 menit, annealing pada suhu 58 oC selama 1 menit dan elongation pada
suhu 72 oC selama 1 menit dan 10 menit untuk siklus yang terakhir. DNA
diamplifikasi sebanyak 30 siklus (Gambar 3). Produk inverse PCR
dielektro-foresis pada gel agarosa 1% untuk mengetahui ukuran fragmen yang
Gambar 3 Strategi amplifikasi DNA genom pengapit transposon dengan inverse
PCR (Wahyudi et al. 2001).
Purifikasi Produk Inverse PCR
Produk inverse PCR dielektroforesis dan fragmen DNA diisolasi dari gel
agarosa 0.8%. Fragmen DNA diisolasi dan dipurifikasi dengan menggunakan
Wizard SV Gel & PCR Clean-up System (Promega, USA). Setelah elektroforesis,
gel yang berisi pita DNA yang dikehendaki dipotong dan hasil cacahan dari gel
tersebut dimasukkan ke dalam tabung mikro 1.5 ml. Kemudian ke dalam tabung
tersebut ditambahkan 10 µl membrane binding solution per 10 mg cacahan gel,
lalu divorteks dan diinkubasi pada suhu 50-65 oC sampai gel benar-benar larut.
Setelah melarutkan gel dilakukan pengikatan DNA dengan memasukkan
campuran gel ke dalam tabung penampung yang dilengkapi dengan minikolom
dan diinkubasi pada suhu ruang selama 1 menit. Selanjutnya tabung penampung
19
melewati minikolom dibuang dan minikolom dimasukkan kembali pada tabung
penampung. Proses pencucian dilakukan dengan menambahkan 700 µl membrane
wash solution yang mengandung etanol dan disentrifugasi pada kecepatan 10000
g selama 1 menit. Cairan dibuang dan minikolom dimasukkan kembali dalam
tabung penampung. Tahap pencucian diulang dengan menambahkan 500 µl
membrane wash solution dan disentrifugasi kembali pada kecepatan yang sama
selama 5 menit. Untuk proses elusi, minikolom dipindahkan dengan hati-hati
pada tabung mikro yang baru dan ditambahkan 50 µl air bebas nuklease pada
minikolom. Lalu diinkubasi pada suhu ruang selama 1 menit dan disentrifugasi
pada kecepatan 10000 g selama 1 menit. Minikolom dibuang dan DNA disimpan
pada suhu –20 oC.
Kloning Produk Inverse PCR
Produk inverse PCR yang telah dimurnikan diligasikan dengan vektor
plasmid pGEM-T Easy (TA-cloning, Promega, WI, USA) membentuk plasmid
rekombinan, pGEMT-11. Reaksi diinkubasi pada suhu 4 oC semalam. DNA hasil
ligasi ini kemudian ditransformasikan ke E. coli DH5 α dengan menggunakan
metode heat shock-CaCl2 dingin (Sambrook & Russel 2001).
Penyiapan Sel Kompeten. Sel E. coli DH5 α yang kompeten disiapkan
terlebih dahulu sebelum melakukan transformasi. E. coli DH5 α ditumbuhkan
pada media LB dan diinkubasi semalam pada suhu 37 oC, kemudian dilakukan
subkultur pada media LB (1% kultur diinokulasikan pada 25 ml LB) dengan suhu
yang sama selama 3 jam. Sebanyak 1.5 ml kultur disentrifugasi dengan kecepatan
2300 g selama 2 menit. Pelet yang diperoleh diresuspensi dengan 1 ml larutan
CaCl2 dingin (CaCl2 0.1 M, Tris HCl 5 mM, dan MgCl2 5 mM; pH 7.0) dan
diinkubasi di es selama 20 menit. Suspensi sel tersebut kemudian disentrifugasi
kembali dengan kecepatan 2300 g selama 2 menit. Selanjutnya pelet diresuspensi
kembali dalam 200 µl larutan CaCl2 dingin dan diinkubasi di es selama 10 menit.
Tranformasi Plasmid Rekombinan. Transformasi dilakukan dengan
menambahkan 3-5 µl DNA hasil ligasi ke dalam 200 µl sel kompeten dan
diinkubasi di es selama 30 menit (setiap 15 menit tabung eppendorf dijentik).
tabung eppendorf langsung dimasukkan kembali ke dalam es selama 2 menit. Sel
dipulihkan dengan menambahkan 250 µl LB dan dishaker dengan kecepatan 200
rpm pada suhu 37 oC selama 1 jam. Seluruh campuran disentrifugasi dengan
kecepatan 2300 g selama 2 menit. Pelet diresuspensi kembali dalam 200 µl LB
dan dicawankan pada media LA + ampisilin (100 µg/ml) + X-gal (40 µg/ml) dan
diinkubasi pada suhu 37 oC semalam. Seleksi transforman dilakukan pada media
LA + ampisilin (100 µg/ml) + X-gal (40 µg/ml) dan diinkubasi pada suhu 37 oC
semalam. Koloni putih diambil dan dikulturkan pada media LB yang ditambah
ampisilin (100 µg/ml) untuk verifikasi plasmid rekombinan. Plasmid rekombinan
pGEMT-11 diisolasi dengan metode lisis alkalin (Sambrook & Russel 2001) yang
dimodifikasi (Wahyudi, Komunikasi pribadi) seperti diterangkan berikut ini.
Plasmid rekombinan dipotong dengan EcoRI, kemudian hasilnya dipisahkan
dengan elektroforesis gel agarosa 1%. Fragmen DNA sisipan diamplifikasi
kembali dengan menggunakan plasmid rekombinan sebagai cetakan dan primer
yang sama dengan amplifikasi DNA pengapit transposon.
Isolasi DNA Plasmid Rekombinan
Plasmid rekombinan, pGEM-T membawa fragmen produk inverse PCR,
diekstrak dari E. coli DH5 α menggunakan metode alkalin lisis (Sambrook &
Russel 2001). Sel E. coli DH5 α yang membawa plasmid rekombinan dikulturkan
semalam pada suhu 37 oC. Kemudian 1.5 ml kultur disentrifugasi dengan
kecepatan 2300 g selama 2 menit. Pelet diresuspensi dengan 100 µl larutan 1 (10
mM Tris-Cl, 1 mM EDTA; pH 8.0 dan 50 mM glukosa). Selanjutnya
ditambahkan 125 µl larutan 2 (SDS 1% dalam 0.2 M NaOH) dan suspensi
dibolak-balik secara perlahan sampai terjadi lisis. Sebanyak 375 µl larutan 3
(K-asetat 5 M dan asam (K-asetat glasial) ditambahkan dan dibolak-balik secara
perlahan. Kemudian campuran tersebut disentrifugasi pada kecepatan 12900 g
selama 10 menit. Supernatan diekstraksi dengan menggunakan
fenol-kloroform-isoamilalkohol (25:24:1), dikocok kuat, dan disentrifugasi pada kecepatan 12900
g selama 10 menit. Fase cair dipindahkan ke tabung eppendorf yang baru dan
diendapkan dengan menambahkan etanol absolut dingin sebanyak 2x volume
21
diinkubasi di es selama 30 menit, dicuci dengan etanol 70% dan disentrifugasi
dengan kecepatan 12900 g selama 10 menit. Pelet DNA dikeringudarakan dan
dilarutkan dalam 20 µl ddH2O yang mengandung RNase 1% dan diinkubasi pada
suhu 37 oC selama 15 menit. Selanjutnya DNA disimpan pada suhu –20 oC.
Analisis Sekuen DNA Genom yang Terlibat dalam Toleransi Asam-Al
Sekuensing fragmen DNA genom yang terlibat dalam toleransi asam-Al
dilakukan pada kedua utas menggunakan metode dideoksi menggunakan primer
universal M13 (forward dan reverse) digunakan untuk cycle sequencing. Plasmid
rekombinan digunakan sebagai template untuk sekuensing yang dilakukan dengan
meggunakan DNA Sequencer ABI310 (Applied Biosystems, USA) yang
dilakukan di Fakultas Bioteknologi Universitas Atmajaya Jakarta. Analisis
sekuen DNA genom pengapit transposon dilakukan menggunakan program
BLASTX (Gish & States 1993) melalui situs European Bioinformatics Institute
Penentuan Resistensi terhadap Antibiotik
Ketiga galur B. japonicum BJ11, BJ38, dan KDR15 menunjukkan
kemampuannya tumbuh pada media YMA + CR 0.0025% yang mengandung
antibiotik ampisilin, rifampisin atau tetrasiklin (Tabel 1). Namun demikian ketiga
galur tersebut tidak mampu tumbuh pada media YMA + CR 0.0025% +
kanamisin (50 µg/ml). E. coli S17-1 (λ pir) dengan konsentrasi antibiotik yang
sama mampu tumbuh pada media LA yang mengandung ampisilin ataupun
kanamisin, tetapi tidak mampu tumbuh pada media LA yang mengandung
rifampisin ataupun tetrasiklin (Tabel 1). Hal ini disebabkan karena E. coli S17-1
(λ pir) membawa plasmid pUTmini-Tn5Km1 yang membawa gen resistensi
[image:45.612.133.506.397.515.2]terhadap kanamisin dan ampisilin (Gambar 1).
Tabel 1 Pertumbuhan galur B. japonicum dan E. coli pada media agar yang mengandung antibiotik
Ampisilin Kanamisin Rifampisin Tetrasiklin Sandi galur
50 100 25 50 25 50 25 50
BJ11
BJ38
KDR15
E.c S17-1 λpir
+ + + + + + + + - - - + - - - + + + + - + + + - + + + - + + + -
Keterangan : + = tumbuh; - = tidak tumbuh; konsentrasi antibiotik yang digunakan dalam µg/ml
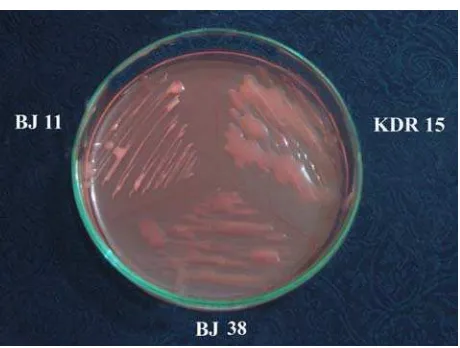
Gambar 4 memperlihatkan penampilan pertumbuhan ketiga galur B.
japonicum (BJ11, BJ38, dan KDR15) pada media YMA + CR 0.0025% +
rifampisin 50 µg/ml setelah diinkubasi selama 7 hari pada suhu ruang. Ketiga
galur tersebut memiliki tipe koloni Large Watery atau berair pada masa inkubasi 8
23
Gambar 4 Penampilan pertumbuhan B. japonicum toleran asam-Al galur BJ11, KDR15, dan BJ38 pada media YMA + CR 0.0025% + rifampisin 50 µg/ml setelah inkubasi selama 8 hari pada suhu ruang.
Berdasarkan kemampuan tumbuh galur-galur tersebut pada media agar
yang mengandung antibiotik, pada penelitian ini dapat ditentukan media YMA +
CR 0.0025% + kanamisin (50 µg/ml) + rifampisin (50 µg/ml) digunakan sebagai
media seleksi hasil konjugasi. Karena galur-galur B. japonicum sensitif terhadap
kanamisin tetapi resisten rifampisin, sedangkan E. coli resisten kanamisin tetapi
sensitif terhadap rifampisin, maka hasil seleksi pada proses konjugasi adalah
koloni B. japonicum yang tumbuh pada media seleksi tersebut.
Mutagenesis dengan Transposon dan Seleksi Mutan
B. japonicum Sensitif Asam-Al
Transposon mini-Tn5Km1 yang dibawa plasmid pUT dalam E. coli S17-1
(λ pir) telah berhasil ditransfer ke B. japonicum toleran asam-Al melalui
konjugasi. Konjugasi bakteri dilakukan pada tiga waktu inkubasi mating yaitu 12,
18, dan 24 jam. Frekuensi tertinggi dicapai oleh galur BJ11 pada waktu inkubasi
mating 24 jam sebesar 7.1x10-6 sel/resipien, sedangkan frekuensi terendah dicapai
oleh galur BJ38 sebesar 6.1x10-8 pada waktu inkubasi mating 12 jam (Tabel 2).
Frekuensi konjugasi dari galur BJ11 dan KDR15 cenderung meningkat
sampai waktu inkubasi mating 24 jam. Untuk galur BJ38 frekuensi konjugasinya
setelah waktu inkubasi 24 jam. Berdasarkan hasil konjugasi pada ketiga galur B.
japonicum tersebut dengan menggunakan donor E. coli S17-1 (λ pir) terlihat
bahwa penambahan lama waktu inkubasi mating dapat dilakukan antara 18-24
jam untuk mendapatkan frekuensi konjugasi yang lebih tinggi dibandingkan
waktu inkubasi 12 jam.
[image:47.612.134.508.237.334.2]
Tabel 2 Frekuensi konjugasi pUTmini-Tn5Km1 dari E. coli S17-1 (λ pir) ke B. japonicum pada tiga waktu inkubasi mating yang berbeda
Frekuensi konjugasi (sel/resipien) Konjugasi Bakterial
12 jam 18 jam 24 jam
BJ11 x E. coli S17-1 λpir
BJ38 x E. coli S17-1 λpir
KDR15 x E. coli S17-1 λpir
6.7x10-7 6.1x10-8 3.4x10-6 1.1x10-6 6.6x10-7 5.1x10-6 7.1x10-6 1.3x10-7 6.3x10-6
Koloni transkonjugan yang diperoleh dari hasil konjugasi diuji
sensitivitasnya pada media Ayanaba (pH 4.5; Al 50 µM) untuk menentukan
koloni B. japonicum transkonjugan yang sensitif asam-Al. Koloni transkonjugan
yang sensitif tidak mampu tumbuh atau terhambat pertumbuhannya pada media
asam-Al, sedangkan koloni transkonjugan yang tetap toleran mampu tumbuh pada
media tersebut. Koloni yang sensitif diduga telah mengalami penyisipan
transposon pada gen yang terlibat dalam toleransi asam-Al sehingga tidak mampu
tumbuh pada media asam-Al dan transkonjugan sensitif ini selanjutnya diberi
nama mutan sensitif asam-Al (acid-Al sensitive= AAS).
Hasil seleksi transkonjugan dari galur BJ11 dan BJ38 diperoleh
masing-masing tiga mutan sensitif asam-Al yaitu dengan sandi galur AAS11.1, AAS11.2,
dan AAS11.5 yang dihasilkan dari galur BJ11 serta AAS38.1, AAS38.2, dan
AAS38.3 yang dihasilkan dari galur BJ38. Hasil seleksi transkonjugan yang
dihasilkan dari galur KDR15 diperoleh satu mutan sensitif asam-Al dengan sandi
galur AAS15.2. Selanjutnya satu mutan yang dihasilkan dari galur BJ11, yang
didesain sebagai AAS11.2 digunakan sebagai model untuk analisis genetika
25
Uji Pembentukan Bintil Akar
B. japonicum termasuk spesies bakteri tumbuh lambat yang dapat
membentuk bintil akar baik pada tanaman dari genus Macroptilium maupun
Glycine (Perret et al. 2000). Ketiga galur B. japonicum BJ11, KDR15, dan BJ38
beserta mutannya dapat membentuk bintil pada tanaman siratro (Macroptilium
atropupureum) atau kedelai (Glycine max). Galur BJ11, BJ38, dan AAS38.3
tidak mampu membentuk bintil pada tanaman siratro, tetapi mampu membentuk
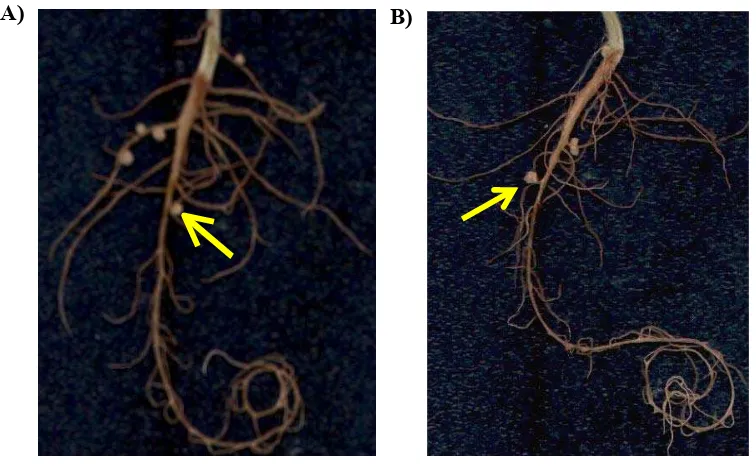
bintil pada tanaman kedelai. Gambar 5 menampilkan bintil akar yang terbentuk
pada tanaman siratro yang diinokulasi dengan galur liar (wild type= WT) KDR15
dan mutannya (AAS15.2). Waktu yang dibutuhkan untuk membentuk bintil pada
tanaman siratro lebih cepat (15 hari) dibandingkan pada tanaman kedelai (30
hari). Jumlah dan letak bintil yang terbentuk cenderung beragam pada
masing-masing galur yang diuji (Tabel 3).
Gambar 5 A) Bintil akar tanaman siratro yang terbentuk inokulasi dengan B. japonicum KDR15 (WT), dengan B) Bintil akar tanaman siratro yang terbentuk hasil inokulasi dengan mutan AAS15.2 (ditunjukkan dengan anak panah).
[image:48.612.131.509.365.598.2]Tabel 3 Hasil uji pembentukan bintil akar pada tanaman siratro (Macroptilium atropupureum) dan kedelai (Glycine max)
Bintil akar yang terbentuk Sandi galur Tanaman inang
yang digunakan Hari ke- Jumlah Letak Tipe liar
kedelai 30 4 3AU/1AS BJ11
siratro 15 0 -
kedelai 30 7 5AU/2AS BJ38
siratro 15 0 -
kedelai td - -
KDR15
siratro 15 4 3AU/1AS
Mutan
kedelai td - -
AAS11.2
siratro 15 3 AU
kedelai 30 7 AS
AAS38.3
siratro 15 0 -
kedelai td - -
AAS15.2
siratro 15 5 4AS/1AU
Keterangan: AU = akar utama; AS = akar sekunder; td = tidak dilakukan
Isolasi DNA Genom Pengapit Transposon dengan Inverse PCR
danKloning Produk Inverse PCR
Amplifikasi DNA genom pengapit transposon yang berukuran 0.8 kb
(Gambar 6A) dari galur mutan AAS11.2 telah berhasil diperoleh melalui inverse
PCR. Ligasi fragmen DNA genom pengapit transposon yang berukuran 0.8 kb ke
dalam pGEM-T Easy menghasilkan plasmid rekombinan pGEMT-11 (∼3.8 kb).
Peta plasmid rekombinan pGEMT-11 ditampilkan pada Gambar 6B.
Plasmid rekombinan pGEMT-11 telah berhasil dikonstruksi dan
diintro-duksikan ke dalam sel inang E. coli DH5 α. Hal ini ditunjukkan dengan hasil
verifikasi plasmid rekombinan yang dipotong dengan EcoRI menghasilkan dua
pita DNA yaitu pita berukuran ~3 kb (vektor pGEM-T) dan DNA sisipan
(fragmen DNA genom hasil inverse PCR) yang berukuran 0.8 kb (Gambar 7A).
Selain itu verifikasi dengan PCR pada plasmid rekombinan juga diperoleh pita
27
Gambar 6 A) Elektroforesis gel agarosa DNA genom pengapit transposon yang berhasil diamplifikasi dengan inverse PCR dari genom mutan B. japonicum sensitif asam-Al AAS11.2 (1) dan M= marker DNA 1 kb ladder plus. B) Peta plasmid rekombinan pGEMT-11 (∼3.8 kb).
Gambar 7 A) Hasil Elektroforesis gel agarosa plasmid rekombinan. M= Marker DNA 1 kb ladder plus, 1 dan 2= pGEM-T11 yang dipotong dengan
EcoRI. B) Hasil verifikasi DNA sisipan (insert) dalam plasmid rekombinan dengan PCR pada gel agarosa 1%. M= Marker DNA 1 kb ladder plus, 1 dan 2= pita DNA insert yang diamplifikasi dengan PCR.
Analisis SekuenDNA Genom yang Terlibat dalam Toleransi Asam-Al
Fragmen DNA pengapit tranposon dari mutan AAS11.2 (0.8 kb) pada
plasmid rekombinan pGEMT-11 telah disekuen dengan menggunakan primer
universal M13-R dan M13-F. Hasil sekuensing DNA diperoleh 764 nukleotida.
Analisis sekuen dengan menggunakan program BLASTX melalui situs European
Bioinformatics Institute (EBI) menunjukkan similaritas dengan putative inner B)
0.85 2.0 3.0 12
(kb) M 1
0.8 kb A)
pGEMT-11 (∼3.8 kb)
0.8 kb
12
3.0 2.0
0.85
(kb) M 1 2
B) 1 A) kb 12 3.0 2.0 0.85 M 2
[image:50.612.149.515.83.235.2] [image:50.612.137.519.331.483.2]membrane protein yang disandikan oleh gen yhfK (79% identity; 84% similarity,
E-value= 1.0xe-100) dari Salmonella typhimurium (nomor akses Q8ZLK8). Pada
Salmonella protein tersebut berfungsi sebagai efflux transporter. Hasil
pensejajaran (alignment) dari sekuen tersebut terlihat pada Gambar 8.
Gambar 8 Hasil pensejajaran (alignment) homologi antara sekuen fragmen DNA genom yang terlibat dalam toleransi asam-Al pada B. japonicum
PEMBAHASAN
Mutagenesis dengan transposon mini-Tn5Km1 melalui proses konjugasi
pada tiga galur B. japonicum toleran asam-Al (BJ11, BJ38, dan KDR15)
menghasilkan frekuensi konjugasi yang berkisar antara 10-8-10-6 sel/resipien
artinya untuk memperoleh satu koloni transkonjugan dibutuhkan sel B. japonicum
sebanyak 106-108 sel. Untuk mendapatkan koloni transkonjugan yang sensitif
asam-Al dari hasil mutagenesis dengan transposon dibutuhkan frekuensi
konjugasi yang tinggi, karena transposon mini-Tn5Km1 yang berukuran 1835 bp
menyisip secara acak pada kromosom B. japonicum, sehingga kemungkinan untuk
menyisip pada gen toleransi asam-Al sangat rendah. Frekuensi konjugasi
tertinggi yang dicapai galur BJ11 (7.1x10-6 sel/resipien) lebih tinggi bila
dibandingkan hasil konjugasi pada Magnetospirillum magneticum (2.7x10-7
sel/resipien) dengan menggunakan plasmid yang sama (Wahyudi et al. 2001),
ataupun pada Bartonella henselae (10-9 sel/resipien) menggunakan pUT/Km
(mini-Tn5 dengan Kmr) (Dehio & Meyer 1997). Frekuensi transkonjugasi dari
BJ11 tersebut cukup untuk menghasilkan B. japonicum sensitif asam-Al seperti
yang dilaporkan pada penelitian ini.
Plasmid pUT yang berperan sebagai pembawa transposon mini-Tn5Km1
diturunkan dari pGP704 dan memiliki origin of replication (ori) dari plasmid R6K
yang hanya dapat bereplikasi pada bakteri penghasil protein π seperti di dalam λ
pir lisogen dari E.coli K-12. Plasmid ini juga membawa oriT dari plasmid RP4
yang dapat menghasilkan proses transfer yang efisien ke sel resipien yang
diperantarai fungsi mobilisasi RP4 di dalam donor. Selain itu pUT membawa
tnp* yaitu mutan gen tnp dari IS50R yang menyandikan transposase yang
dibutuhkan untuk perpindahan (transposisi) mini-Tn5 (Lorenzo et al. 1990).
Setelah terjadi transfer pUTmini-Tn5Km1 dari E. coli S17-1 (λpir) ke sel B.
japonicum melalui konjugasi, transposon mini-Tn5Km1 menyisip secara acak
pada kromosom B. japonicum. Proses ini dapat menghasilkan insersi yang stabil,
karena gen transposase berada di luar transposon mini-Tn5Km1 (Herrero et al.
1990). Sementara itu pUT tidak dapat bereplikasi di dalam sel B. japonicum
initiation of replication) dari inangnya, sehingga setelah proses transfer plasmid
ini tidak dapat dipertahankan pada sel inang B. japonicum atau dinamakan suicide
vector.
Sebelumnya Wahyudi et al. (1998) melaporkan hasil konjugasi antara B.
japonicum 11, 33, dan 43 dengan E. coli S17-1 λ pir (pUTmini-Tn5Km1)
menggunakan perbandingan antara sel donor dan resipien (10:1) pada waktu
inkubasi mating 12 jam diperoleh frekuensi konjugasi ∼10-9 sel/resipien.
Penambahan waktu inkubasi 18-24 jam dan perbandingan yang sama antara sel
donor dan resipien (1:1) pada ketiga galur B. japonicum yaitu BJ11, BJ38, dan
KDR15 menghasilkan frekuensi konjugasi yang lebih tinggi dibandingkan waktu
inkubasi 12 jam. Galur BJ11 dan BJ38 frekuensi konjugasinya meningkat 10 kali
lipat setelah waktu inkubasi 18 dan 24 jam. Tetapi untuk galur KDR15
pening-katan frekuensi konjugasi pada tiga waktu inkubasi mating masih pada kisaran
yang sama yaitu 10-6 sel/ resipien.
Pada kondisi yang optimal, beberapa plasmid hampir 100% dapat
mentransfer dirinya sendiri ke sel lain setiap terjadi kontak antar sel. Sistem
transfer dari plasmid RP4 memungkinkan efisiensi transfer yang tinggi dari sel
donor ke sel resipien, karena plasmid ini bersifat promiscuous sehingga dapat
mentransfer dirinya sendiri ke berbagai bakteri gram negatif (Snyder &
Champness 1997). Namun frekuensi transposisi dari Tn5 sendiri secara in vivo
dipengaruhi oleh inangnya (Goryshin & Reznikoff 1998). Perbedaan frekuensi
konjugasi juga dapat dipengaruhi oleh perangkat sistem sel yang dimiliki bakteri
(Wahyudi 2004). Jadi kemungkinan waktu inkubasi merupakan salah satu faktor
yang dapat mempengaruhi efisiensi transfer plasmid dari sel donor ke sel resipien.
Namun sistem sel inang sendiri juga menentukan efisiensi transposisi dari Tn5,
sehingga terdapat perbedaan nilai frekuensi konjugasi diantara ketiga galur B.
japonicum ataupun diantara spesies bakteri yang menggunakan plasmid yang
sama.
Koloni B. japonicum tanskonjugan yang diperoleh dari hasil konjugasi
secara konsisten dapat tumbuh pada media YMA + CR 0.0025% + rifampisin +
kanamisin. Hal ini menunjukkan proses transfer transposon mini-Tn5Km1 telah
31
rifampisin tetapi juga resisten terhadap kanamisin. Mutan sensitif asam-Al
diperoleh dari hasil seleksi koloni mutan B. japonicum pada media Ayanaba (pH
4.5; Al 50 µM) yang diduga telah mengalami insersi pada gen yang menyandikan
toleransi asam-Al, sehingga tidak mampu tumbuh pada media Ayanaba pH 4.5
dan konsentrasi Al 50 µM. Menurut Ayanaba et al. (1983), setelah waktu
inkubasi 10 hari galur toleran dapat tumbuh dengan baik dan pada media yang
menggunakan indikator pH yaitu bromcresol purple (BCP) dan bromcresol green
(BCG). Hal ini menunjukkan adanya perubahan pH dengan adanya perubahan
warna media. Sedangkan galur yang sensitif tidak dapat tumbuh sampai waktu
inkubasi 25 hari. Tujuh mutan sensitif asam-Al diperoleh dari hasil seleksi koloni
transkonjugan galur BJ11, BJ38, dan KDR15 yang telah mengalami insersi
transposon pada kromosomnya. O’Hara et al. (1989) melaporkan bahwa galur
Rhizobium meliloti toleran pada media asam dikarenakan galur tersebut
mempunyai kemampuan untuk mempertahankan pH intraseluler (pHi) antara 7.2
dan 7.4 ketika pH eksternalnya rendah (pH 5.6). Sedangkan pada empat galur
mutan R. meliloti WSM419 yang genomnya disisipi dengan Tn5 tidak dapat
tumbuh pada pH 5.6. Hal ini menunjukkan galur mutan kehilangan kemampuan
untuk mempertahankan pHi-nya. Pada bakteri neutrofil, pemeliharaan pHi
membutuhkan sistem transport elektron, ATPase untuk translokasi proton, dan
antiporter pr