DAFTAR PUSTAKA
Ansel, G. H. 1989. Pengantar Bentuk Sediaan Farmasi. Edisis Keempat. UI Press. Jakarta
Azis, S., Supardi, S. dan Herman, M. J. 2004. Kembali Sehat dengan Obat (Mengenal Manfaat dan Bahaya Obat). Pustaka Populer Obat. Jakarta
Bull, E dan Archard, G. 2007. Simple Guide: Nyeri Punggung. Erlangga. Jakarta Cairns, D. 2004. Intisari Kimia Farmasi. Buku Kedokteran EGC. Jakarta
Davey, P. 2006. At a Glance Medicine. Erlangga. Jakarta
Dirjen POM. 1995. Farmakope Indonesia. Edisi IV. Departemen Kesehatan Republik Indonesia. Jakarta
Ganiswarna, S. G. 1995. Farmakologi dan Terapi. Edisi 5. UI Press. Jakarta
Gandjar, I. G dan Rohman, A. 2007. Kimia Farmasi Analisis. Pustaka Pelajar. Yogyakarta
Ikawati, Z. 2010. Cerdas Mengenali Obat. Kanisius. Jakarta
Insley, J. 1997. Vade-Vacum Pediatri. Buku Kedokteran EGC. Jakarta
Sugani, S dan Priandarini, L. 2010. Cara Cerdas untuk Sehat: Rahasia Hidup Sehat tanpa Dokter. Transmedia Pustaka. Jakarta
Tan, H. T dan Rahardja, K. 2010. Obat-Obat Sederhana untuk Gangguan Sehari-Hari. PT Alex Media Komputindo. Jakarta
Wallace, D. J. 2007. The Lupus Book. PT Benteng Pustaka. Jakarta Widjajanti, V. N. 1991. Obat-Obatan. Kanisius. Jakarta
BAB 3
METODOLOGI
3.1. Alat-Alat
Adapun alat-alat yang digunakan antara lain :
a. HPLC Waters Detector 2489 Pump 1525
b. Ultrasonic Bath Digitals Merk ELMA Type D-78224 c. Labu takar 250 ml : Pyrex
d. Labu takar 50 ml : Pyrex e. Gelas ukur 50 ml : Pyrex f. Beaker glass 250 ml : Pyrex g. Digital Balance Merk Sartorius h. Alu dan lumpang
i. Botol vial
j. Pipet volum 1 ml : Pyrex k. Bola karet
l. Filter 0,45µm Phenex NY m. Syringe injector
n. Pompa vakum
3.2. Bahan-bahan
Adapun bahan-bahan yang digunakan antara lain : a. Tablet parasetamol 500 mg
3.3. Prosedur
3.3.1 Pembuatan Larutan Fase Gerak
a. Dibuat campuran aquabides dan metanol dengan perbandingan 3 : 1 b. Disaring dengan penyaring filter berukuran 0,45 µm
3.3.2 Pembuatan Larutan Baku Pembanding Sekunder
a. Ditimbang kertas
b. Ditambahkan baku pembanding sekunder Acetaminophen 99,625 % sebanyak 50 mg di atas kertas yang sedang ditimbang
c. Dimasukkan ke dalam labu takar 100 ml
d. Ditambahkan 30 ml pelarut parasetamol yaitu Metanol : Aquabides (1 : 3) ke dalam labu takar
e. Di ultrasonic selama 15 menit f. Didiamkan hingga suhu kamar
g. Ditambahkan pelarut parasetamol hingga garis batas, dan dihomogenkan h. Dipipet 1 ml larutan ke dalam labu takar 50 ml
i. Ditambahkan pelarut parasetamol hingga garis batas, dan dihomogenkan
3.3.3 Prosedur Sampel
a. Digerus tablet parasetamol 500 mg sebanyak 10 butir dengan keseragaman bobot yang telah diketahui
b. Ditimbang kertas
c. Ditambahkan serbuk parasetamol sebanyak 50 mg di atas kertas yang sedang ditimbang
e. Ditambahkan 30 ml pelarut parasetamol yaitu Metanol : Aquabidest (1 : 3) ke dalam labu takar
f. Di ultrasonic selama 15 menit g. Didiamkan hingga suhu kamar
h. Ditambahkan pelarut parasetamol hingga garis batas, dan dihomogenkan j. Dipipet 1 ml larutan ke dalam labu takar 50 ml
i. Ditambahkan pelarut parasetamol hingga garis batas, dan dihomogenkan
3.3.4 Pemakaian Alat HPLC
3.3.4.1 Persiapan Analisa
1. Dihidupkan Power Detektor 2489, Manual Injector dan pompa 1525 2. Dihidupkan komputer
3. Double klik menu Breeze 2
4. Pada Windows Explorer Login dimasukkan :
a) User Name : Breeze (atau nama user lain jika sudah dibuat) b) Klik : OK atau Enter
5. Dipilih Project yang akan kita gunakan. Klik OK 6. Maka dilayar akan terlihat tampilan project
7. Dibuka Reverence Velve pada pump 1525 ke arah kanan, kemudian lakukan Purging dengan mengklik Control Panel pada menu Run
8. Diset flow rate dan komposisi fasa gerak sesuai kebutuhan analisa (langkah ini digunakan untuk conditioning column). Klik OK
3.3.4.2 Persiapan Injeksi
1. Sebelum diinjeksikan larutan baku pembanding sekunder dan larutan sampel disaring dengan filter 0,45 µm
2. Disuntikkan secara terpisah larutan baku pembanding sekunder dan larutan uji parasetamol ke dalam kromatografi cair kinerja tinggi dengan volume penyuntikan masing-masing 20 µm
3. Pemisahan zat aktif terjadi melalui mekanisme kromatografi
4. Hasil pemisahan dibaca oleh detektor dengan panjang gelombang 243 nm
5. Dicatat oleh rekorder
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil
Tabel 4.1 Larutan Baku Parasetamol
NO Nama Zat Berat (mg) Luas Area Puncak
Utama 1 Baku pembanding sekunder
Acetaminophen 99,625 %
Luas Area Rata-Rata 672070
Tabel 4.2 Larutan Sampel Parasetamol
NO Nama Zat Berat (mg) Luas Area Puncak
4.2 Perhitungan
Perhitungan Kadar Zat Aktif Parasetamol yang terdapat dalam sediaan tablet Parasetamol 500 mg dapat menggunakan rumus sebagai berikut :
Keterangan :
AU Csp : Luas area sampel AU Cst : Luas area baku standar
Bst : Berat baku pembanding parasetamol (mg) Bsp : Berat sampel (mg)
Dimana : Bsp = berat tablet
Bza : Berat zat aktif acetaminophen (500 mg) (sudah ketentuan) Bt : Berat tablet (600 mg) (sudah ketentuan)
Parasetamol (a) Bsp
Parasetamol (b) Bsp
Kst : Kadar standar acetaminophen (99,625 %) (sudah ketentuan) Kadar zat aktif :
Kadar Parasetamol (a)
Kadar Parasetamol (b)
4.3 Pembahasan
Telah dilakukan pengujian penetapan kadar Parasetamol tablet secara Kromatografi Cair Kinerja Tinggi (KCKT). Hasil pemeriksaan dapat dilihat dari tabel berikut : Tabel 4.3 Hasil penetapan kadar parasetamol tablet secara Kromatografi Cair
Kinerja Tinggi (KCKT)
Hasil pengujian kadar dengan menggunakan Kromatografi Cair Kinerja Tinggi (KCKT) dengan volume penyuntikan 20 µm dapat diperoleh kadar sampel parasetamol (a) 101,004 % dan parasetamol (b) 101,029 %.
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Penetapan kadar zat aktif pada tablet parasetamol 500 mg produksi PT Kimia Farma (Persero) Tbk. Plant Medan dengan menggunakan metode Kromatografi Cair Kinerja Tinggi (KCKT) pada sampel tablet parasetamol (a) didapatkan hasil 101,004 % dan parasetamol (b) 101,029 %. Kedua kadar tablet parasetamol tersebut telah memenuhi standar pada Farmakope Indonesia Edisi IV tidak kurang dari 90,00 % dan tidak lebih dari 110,00 %.
5.2. Saran
BAB 2
TINJAUAN PUSTAKA
2.1 Tablet
Tablet merupakan bahan obat dalam bentuk sediaan padat yang biasanya dibuat dengan penambahan bahan tambahan yang sesuai. Tablet dapat berbeda-beda dalam ukuran, bentuk, berat, kekerasan, ketebalan, daya hancurnya, dan dalam aspek lainnya tergantung pada cara pemakaian dan metode pembuatan tablet tersebut. Kebanyakan tablet digunakan pada pemberian obat secara oral. (Ansel, 1989)
2.1.1 Jenis-Jenis Tablet
Jenis-jenis tablet yang banyak digunakan adalah:
1. Tablet Isap: dimaksudkan bekerja setempat di mulut atau di tenggorok. Tablet hendaknya diisap dengan perlahan-lahan tanpa dikunyah. Banyak tablet isap mengandung suatu zat antiseptik untuk menghentikan pertumbuhan atau mematikan kuman.
2. Tablet Efervesen mengandung zat pembantu yang akan bereaksi dan mengeluarkan gas (karbondioksida) bila tablet dimasukkan ke dalam air. Dengan demikian obat akan melarut lebih cepat. Jenis tablet ini banyak digunakan untuk vitamin.
3. Tablet Kunyah: harus dikunyah sampai halus sekali untuk mencapai efek obat optimal sebelum diminum dengan air. Sering kali mengandung obat lambung.
dikunyah dan harus ditelan secara utuh dengan air. Hanya boleh dipecah dua, jika terdapat garis pembagi di atas tablet.
5. Tablet Tahan Asam (enteric coated) mengandung suatu lapisan tertentu yang tahan asam sehingga tablet tidak dipecah di lambung, tetapi di usus halus. Biasanya tablet demikian juga tersalut dengan suatu lapisan gula atau pop (dagree, sugar- atau film coated). Tablet jenis ini digunakan untuk obat yang meransang atau menimbulkan mual, misalnya obat sembelit bisakodil (Dulcolax). Jelas bahwa tablet ini tidak boleh dipecahkan sebelum ditelan.
2.1.2 Cara Penggunaan Tablet
Tablet harus selalu diminum dengan segelas air, sebaiknya dengan posisi tubuh tegak. Perhatian: tablet bergula (dragee) tidak boleh digigit atau dikunyah karena biasanya keras sekali dan mengandung obat yang berasa pahit. Disamping itu ada pula beberapa jenis tablet yang tidak boleh dipecahkan sebelum ditelan.
Bila tablet ditelan tanpa atau dengan terlampau sedikit air atau dalam posisi berbaring, terdapat resiko bersangkutnya tablet di kerongkongan. Obat-obat yang bersifat asam dan merangsangnya dapat menimbulkan kerusakan pada selaput lender setempat, misalnya tablet vitamin C dan zat antibiotika doksisiklin. (Tan & Rahardja, 2010)
2.2 Parasetamol
Rumus Bangun :
Gambar 2.1 Struktur Parasetamol Rumus Molekul : C8H9NO2
Nama Kimia : 4- Hidroksiasetanilida
Pemerian : Serbuk hablur, putih; tidak berbau; rasa sedikit pahit
Kelarutan : Larut dalam air mendidih dan dalam NaOH 1N; mudah larut dalam etanol
Sinonim : Asetaminofen (Ditjen POM, 1995)
Parasetamol dan obat-obat serupa aspirin secara umum memiliki efektivitas yang sama dalam meredakan nyeri, namun parasetamol tidak terlalu mengiritasi lambung. Karena alasan ini, maka parasetamol sering digunakan pada orang lanjut usia dan pada kelompok orang yang rentan seperti wanita hamil, orang dengan asma, dan orang dengan ulkus lambung. Overdosis parasetamol sangat berbahaya karena dapat menyebabkan kerusakan hati yang permanen dan ireversibel. Selalu gunakan parasetamol berdasarkan aturan pakai yang tercantum dalam kemasan (1-2 tablet 500 mg parasetamol, 3-4 kali sehari, maksimal 8 tabet dalam 24 jam, atau menurut petunjuk dokter) dan kolsultasikan dengan dokter bila nyeri asih berlangsung. Anda harus waspada bahwa parasetamol dapat tersembunyi dalam beberapa produk bermerek dan berikan perhatian ekstra sehingga tidak terjadi overdosis. (Bull & Archard, 2007)
2.2.1 Toksisitas Parasetamol
Kerusakan hati, sering kali belum muncul dalam beberapa hari setelah minum obat, merupakan komplikasi akibat dosis berlebihan yang mengancam jiwa, tetapi untungnya anak umur <10 tahun tahan terhadap efek hepatotoksik. Dapat terjadi muntah, pendarahan gastrointestinal, hiperglikemia atau hipoglikemia, kerusakan tubulus ginjal dan edema serebri. (Insley, 1997)
Hal yang harus diperhatian :
1. Dosis harus tepat, tidak berlebihan, karena dapat menimbulkan gangguan fungsi hati dan ginjal.
2. Hindari penggunaan campuran obat demam karena dapat menimbulkan overdosis.
3. Hindari penggunaan bersama dengan alkohol karena meningkatkan risiko gangguan hati.
4. Minta petunjuk dokter untuk penderita penyakit ginjal. 5. Tidak boleh digunakan pada :
a. Penderita gangguan fungsi hati b. Alergi terhadap obat ini
c. Pecandu berat alkohol (Azis dkk, 2004)
2.2.2 Farmakokinetik
Parasetamol diserap cepat dan sempurna melalui saluran cerna. Konsentrasi tertinggi dalam plasma dicapai dalam waktu setengah jam, masa paruh dalam plasma antara 1-3 jam. Obat ini tersebar ke seluruh cairan tubuh. Dalam plasma terikat 25% oleh protein plasma.
Menurunkan suhu tubuh dengan mekanisme yang diduga juga berdasarkan efek sentral. Efek anti-inflamasinya sangat lemah, oleh karena itu parasetamol tidak digunakan sebagai antireumatik. Parasetamol merupakan penghambat biosintesis prostaglandin yang lemah. Efek iritasi dan perdarahan lambung tidak terlihat pada obat ini, demikian juga gangguan pernapasan dan keseimbangan asam basa. (Ganiswarna dkk, 1995)
2.3 Kromatografi
2.3.1 Uraian Umum
Kromatografi pertama kali dikembangkan oleh seorang ahli botani Rusia Michael Tswett pada tahun 1903 untuk memisahkan pigmen berwarna dalam tanaman dengan cara perkolasi ekstrak petroleum eter dalam kolom gelas yang berisi kalsium karbonat (CaCO3). Saat ini kromatografi merupakan teknik pemisahan
yang paling umum dan paling sering digunakan dalam bidang kimia analis dan dapat dimanfaatkan untuk melakukan analisis, baik analisis kualitatif, kuantitatif, atau preparatif dalam bidang farmasi, lingkungan, industri dan sebagainya. Kromatografi merupakan suatu teknik pemisahan yang menggunakan fase diam (stationary phase) dan fase gerak (mobile phase).
Teknik kromatografi telah berkembang dan telah digunakan untuk memisahkan dan mengkuantifikasi berbagai macam komponen yang kompleks, baik komponen organik maupun komponen anorganik.
2.3.2 Pembagian Kromatografi
kromatografi pasangan ion; (d) kromatografi penukar ion; (e) kromatografi eksklusi ukuran; dan (f) kromatografi afinitas.
Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas: (a) kromatografi kertas; (b) kromatografi lapis tipis; (c) Kromatografi Cair Kinerja Tinggi (KCKT); dan (d) Kromatografi Gas (KG). Bentuk kromatografi yang paling awal adalah kromatografi kolom yang digunakan untuk pemisahan sampel dalam jumlah yang besar.
Kromatografi Gas (KG) dan Kromatografi Cair Kinerja Tinggi (KCKT) merupakan teknik kromatografi yang komplementer karena kromatografi gas dapat digunakan untuk memisahkan komponen-komponen yang mudah menguap, sementara KCKT dapat digunakan untuk memisahkan komponen-komponen yang tidak mudah menguap. Alat kedua kromatografi ini dapat dikendalikan dengan computer dengan software yang canggih dan berkemampuan untuk memisahkan sampai 100 komponen dalam campuran yang kompleks.
2.3.3 Kromatografi Cair Kinerja Tinggi (KCKT)
2.3.4 Kegunaan Kromatografi Cair Kinerja Tinggi (KCKT)
Kegunaan umum KCKT adalah untuk: pemisahan sejumlah senyawa organik anorganik, maupun senyawa biologis; analisis ketidakmurnian (impurities); analisis senyawa-senyawa tidak mudah menguap (non-volatil); penentuan molekul-molekul netral, ionik, maupun zwitter ion; isolasi dan pemurnian senyawa; pemisahan senyawa-senyawa yang strukturnya hampir sama; pemisahan senyawa-senyawa dalam jumlah sekelumit (trace elements), dalam jumlah banyak, dan dalam skala proses industri. Kromatografi Cair Kinerja Tinggi merupakan metode yang tidak destruktif dan dapat digunakan baik untuk analisis kualitatif maupun kuantitatif.
Kromatografi Cair Kinerja Tinggi paling sering digunakan untuk: menetapkan kadar senyawa-senyawa tertentu seperti asam-asam amino, asam-asam nukleat, dan protein-protein dalam cairan fisiologis; menentukan kadar senyawa-senyawa aktif obat, produk hasil samping proses sintetis, atau produk-produk degradasi dalam sediaan farmasi; memonitor sampel-sampel yang berasal dari lingkungan; memurnikan senyawa dalam suatu campuran; memisahkan polimer dan menentukan distribusi berat molekulnya dalam suatu campuran; control kualitas; dan mengikuti jalannya reaksi sintetis. Keterbatasan metode KCKT adalah untuk identifikasi senyawa kecuali jika KCKT dihubungkan dalam Spektrometer Massa (MS). Keterbatasan lainnya adalah jika sampelnya sangat kompleks, maka resolusi yang baik sulit diperoleh.
Kromatografi merupakan teknik yang mana solute atau zat-zat terlarut terpisah oleh perbedaan kecepatan elusi, dikarenakan solute-solut ini melewati suatu kolom kromatografi. Pemisahan solut-solut ini diatur oleh distribusi solut dalam fase gerak dan fase diam. Penggunaan kromatografi cair secara sukses terhadap suatu masalah yang dihadapi membutuhkan penggabungan secara tepat dari berbagai macam kondisi operasional seperti jenis kolom, fase gerak, panjang dan diameter kolom, kecepatan alir fase gerak, suhu kolom, dan ukuran sampel. Untuk tujuan memilih kombinasi kondisi kromatografi yang terbaik, maka dibutuhkan pemahaman yang mendasar tentang berbagai macam faktor yang mempengaruhi pemisahan pada kromatografi cair.
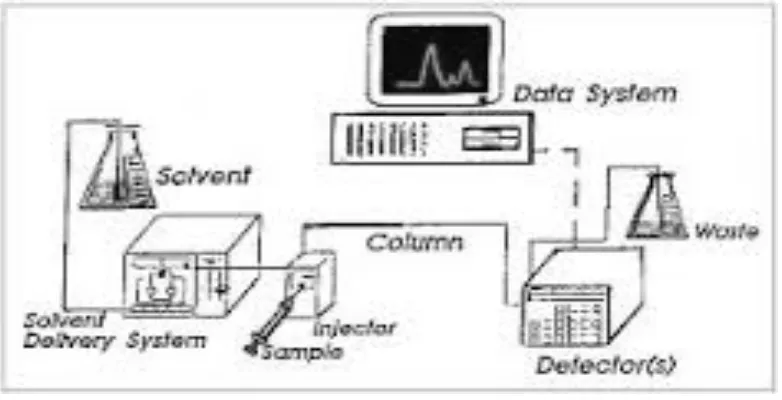
Instrumentasi KCKT pada dasarnya terdiri atas delapan komponen pokok yaitu: (1) wadah fase gerak, (2) sistem penghantaran fase gerak, (3) alat untuk memasukkan sampel, (4) kolom, (5) detektor, (6) wadah penampung buangan fase gerak, (7) tabung penghubung, (8) suatu komputer atau integrator atau perekam.
Gambar 2.2 Alat KCKT secara umum
2.3.5 Sistem Peralatan Kromatografi Cair Kinerja Tinggi (KCKT)
Wadah fase gerak harus bersih dan lembam (inert). Wadah pelarut kosong ataupun labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini biasanya dapat menampung fase gerak antara 1 sampai 2 liter pelarut. Fase gerak sebelum digunakan harus dilakukan degassing (penghilangan gas) yang ada pada fase gerak, sebab adanya gas akan berkumpul dengan komponen lain terutama di pompa dan detektor sehingga akan mengacaukan analisis. Pada saat membuat pelarut untuk fase gerak, maka sangat dianjurkan untuk menggunakan pelarut, buffer, dan reagen dengan kemurnian yang sangat tinggi, dan lebih terpilih lagi jika pelarut-pelarut yang akan digunakan untuk KCKT berderajat KCKT (HPLC grade). Adanya pengotor dalam reagen dapat menyebabkan gangguan pada sistem kromatografi. Adanya partikel yang kecil dapat terkumpul dalam kolom atau dalam tabung yang sempit, sehingga dapat mengakibatkan suatu kekosongan pada kolom atau tabung tersebut. Karenanya, fase gerak seblum digunakan harus disaring terlebih dahulu untuk menghindari partikel-partikel kecil ini.
2. Fase Gerak pada Kromatografi Cair Kinerja Tinggi
terbalik (fase diam kurang polar daripada fase gerak), kemampuan elusi menurun dengan meningkatnya polaritas pelarut.
Elusi dapat dilakukan dengan cara isokratik (komposisi fase gerak tetap selama elusi) atau dengan cara bergradien digunakan (komposisi fase gerak berubah-ubah selama elusi). Elusi bergradien digunakan untuk meningkatkan resolusi campuran yang kompleks terutama jika sampel mempunyai kisaran polaritas yang luas.
Fase gerak yang paling sering digunakan untuk pemisahan dengan fase terbalik adalah campuran larutan bufer dengan methanol atau campuran air dengan asetonitril. Untuk pemisahan dengan fase normal, fase gerak yang paling sering digunakan adalah campuran pelarut-pelarut hidrokarbon dengan pelarut yang terklorisasi atau menggunakan pelarut-pelarut jenis alkohol. Pemisahan dengan fase normal ini kurang umum dibanding dengan fase terbalik.
3. Pompa pada Kromatografi Cair Kinerja Tinggi
Tujuan penggunaan pompa atau sistem penghantaran fase gerak adalah untuk menjamin proses penghantaran fase gerak berlangsung secara tepat, reprodusibel, konstan, dan bebas dari gangguan. Ada 2 jenis pompa dalam KCKT yaitu: pompa dengan tekanan konstan, dan pompa dengan aliran fasse gerak yang konstan. Tipe pompa dengan aliran fase gerak yang konstan sejauh ini lebih umum dibandingkan dengan tipe pompa dengan tekanan konstan.
4. Penyuntikan Sampel pada Kromatografi Cair Kinerja Tinggi
Sampel-sampel cair dan larutan disuntikkan secara langsung ke dalam fase gerak yang mengalir di bawah tekanan menuju kolom menggunakan alat penyuntik yang terbuat dari tembaga tahan karat dan katup Teflon yang dilengkapi dengan keluk sampel (sample loop) internal atau eksternal. 5. Kolom pada Kromatografi Cair Kinerja Tinggi
Ada 2 jenis kolom pada KCKT yaitu kolom konvensional dan kolom mikrobor.
Kolom mikrobor mempunyai 3 keuntungan yang utama dibandingkan dengan kolom konvensional, yakni:
a. Konsumsi fase gerak kolom mikrobor hanya 80% atau lebih kecil dibanding dengan kolom konvensional karena pada kolom mikrobor kecepatan alur fase gerak leboh lambat (10-100µm/menit)
c. Sensitivitas kolom mikrobor ditingkatkan karena solute lebih pekat, karenanya jenis kolom ini sangat bermanfaat jika jumlah sampel terbatas misal sampel klinis
Meskipun demikian, dalam prakteknya, kolom mikrobor ini tidak setahan kolom konvensional dan kurang bermanfaat untuk analisis rutin.
6. Fase Diam pada Kromatografi Cair Kinerja Tinggi
Kebanyakan fase diam pada KCKT berupa silika yang dimodofikasi secara kimiawi, silika yang tidak dimodifikasi, atau polimer-polimer stiren dan divinil benzene. Permukaan silika adalah polar dan sedikit asam karena adanya residu gugus silanol (Si-OH).
7. Detektor UV-Vis
Detektor pada KCKT dikelompokkan menjadi 2 golongan yaitu: detektor universal (yang mampu mendeteksi zat secara umum, tidak bersifat spesifik, dan tidak bersifat selektif) seperti detektor indeks bias dan detektor spektrofotometri massa; golongan detektor yang spesisfik yang hanya akan mendeteksi analit secara spesisfik dan selektif, seperti detektor UV-Vis, detektor fluoresensi, dan elekrokimia. Idealnya, suatu detektor harus mempunyai karakteristik sebagai berikut:
a. Mempunyai respon terhadap solut yang cepat dan reprodusibel b. Mempunyai sensitifitas yang tinggi, yakni mampu mendeteksi solut
pada kadar yang sangat kecil c. Stabil dalam pengoperasiannya
atau lebih kecil, sementara kolom mikrobor selnya bervolume 1 µl atau lebih kecil lagi
e. Signal yang dihasilkan berbanding lurus dengan konsentrasi solut pada kisaran yang luas (kisaran dinamis linier)
f. Tidak peka terhadap perubahan suhu dan kecepatan alir fase gerak Detektor jenis ini merupakan detektor yang paling banyak digunakan dan sangat berguna untuk analisis di bidang farmasi karena kebanyakan senyawa obat mempunyai struktur yang dapat menyerap sinar UV-Vis. Detektor ini didasarkan pada adanya penyerapan radiasi ultraviolet (UV) dan sinar tampak (Vis) pada kisaran panjang gelombang 190-800 nm oleh spesies solut yang mempunyai struktur-struktur atau gugus-gugus kromoforik. Sel detektor umumnya berupa tabung dengan diameter 1 mm dan panjang celah optiknya 10 mm, serta diatur sedemikian rupa sehingga mampu menghilangkan pengaruh indeks bias yang dapat mengubah absorbansi yang terukur.
Detektor dengan panjang gelombang yang bervariasi lebih berguna dibanding dengan detektor pada panjang gelombang yang tetap karena seorang analis dapat memilih panjang gelombang yang memberikan sensitifitas yang paling tinggi.
8. Komputer, Integrator, atau Rekorder
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Demam adalah kondisi saat suhu tubuh di atas 38oC. Meski bisa merupakan gejala penyakit tertentu, pada umumnya demam menunjukkan bahwa tubuh sedang melawan infeksi. Saat melawan infeksi, ada zat dalam tubuh yang meningkatkan produksi panas sekaligus menahan pelepasan panas sehingga menyebabkan demam. Seseorang dikatakan demam jika ia merasa gejala-gejala berikut: menggigil, panas dan dingin bergantian, lemas, berkeringat, dan wajah kelihatan memerah.(Sugani & Priandarini, 2010)
Demam ringan tidak selalu berbahaya, sebaliknya mampu meningkatkan denyut nadi yang bisa menurunkan stamina. Dalam keadaan tertentu, demam merupakan tanda adanya infeksi dan menunjukkan perlunya diadakan pemeriksaan spesifik atau pemberian obat-obat antibiotik. Jika suhu tubuh naik hingga melebihi 40oC, tindakan-tindakan harus dilakukan untuk mencegah seizure (serangan penyakit tiba-tiba) atau dehidrasi. Pencegahannya antara lain dengan aspirin dan ibuprofen atau parasetamol secara bergantian setiap 2 jam. (Wallace, 2007)
Demam akan meletihkan/melemahkan penderita, maka harus ditekan/dikurangi dengan obat penurun panas (antipiretika). Yang perlu diperhatikan pada pemberian obat antipiretika pada penderita jangan sampai pemberian obat analgetik tersebut menutupi gejala-gejala penyakit penderita. (Widjajanti,1991)
Parasetamol merupakan analgesik bebas (“over the counter”) untuk orang dewasa dan anak-anak yang paling popular di Inggris dan benar-benar aman jika digunakan sesuai dengan dosis yang direkomendasikan (untuk orang dewasa, biasanya tidak lebih dari delapan tablet 500 mg dalam waktu 24 jam ). (Cairns, 2004)
Parasetamol termasuk obat lama yang bertahan lama sebagai analgesik, karena relatif aman terhadap lambung, juga merupakan analgesik pilihan untuk anak-anak maupun ibu hamil/menyusui. Ada sedikit perbedaan mekanisme aksi parasetamol sebagai analgesik dan antipiretik.
Tapi bukan berarti parasetamol tidak punya efek samping. Efek samping parasetamol larinya ke liver/hati. Ia bersifat toksik di hati jika digunakan dalam dosis besar. Karena itu dosis maksimal penggunaan parasetamol adalah 4 gram/sehari atau 8 tablet 500 mg/hari. Melebihi itu, akan berisiko terhadap hati. (Ikawati, 2010)
konjugasi di hati: bila jalur ini menjadi jenuh akan terbentuk metabolit toksik, biasanya diinaktivasi oleh glutation. Dosis yang lebih rendah menjadi toksik bagi orang yang menggunakan obat penginduksi enzim (seperti fenitoin, karbamazepin, rifampisin) dan orang dengan gizi buruk (anoreksia, alkoholisme, kelaparan). (Davey, 2006)
Atas dasar inilah penulis ingin membuat tugas akhir berjudul “Penetapan Kadar Zat Aktif pada Tablet Parasetamol 500 mg Di PT Kimia Farma (Persero) Tbk Plant Medan”, untuk mengetahui apakah kadar zat aktif dalam tablet parasetamol 500 mg sesuai dengan penetapan kadar dalam Farmakope Indonesia Edisi IV.
1.2 Permasalahan
Permasalahannya adalah apakah kadar zat aktif dalam tablet parasetamol 500 mg yang diproduksi oleh PT Kimia Farma (Persero) Tbk. Plant Medan telah memenuhi syarat sesuai dengan Farmakope Indonesia (FI) Edisi IV yang tidak kurang dari 90% tidak lebih dari 110,0%.
1.3 Tujuan
1.4 Manfaat
PENETAPAN KADAR ZAT AKTIF PADA TABLET PARASETAMOL 500 mg DI PT. KIMIA FARMA (PERSERO) Tbk. PLANT MEDAN
ABSTRAK
Parasetamol (C8H9NO2) memiliki karakteristik yaitu berbentuk serbuk hablur,
DETERMINATION OF ACTIVE MATTER IN PARACETAMOL TABLETS 500 mg IN PT. KIMIA FARMA (PERSERO) Tbk. PLANT MEDAN
ABSTRACT
Paracetamol (C8H9NO2) has characteristics that crystalline powder form, white,
PENETAPAN KADAR ZAT AKTIF PADA TABLET
PARASETAMOL 500 mg DI PT KIMIA FARMA
(PERSERO) Tbk. PLANT MEDAN
TUGAS AKHIR
JAUHARIA
122401015
PROGRAM STUDI D-3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENETAPAN KADAR ZAT AKTIF PADA TABLET
PARASETAMOL 500 mg DI PT KIMIA FARMA
(PERSERO) Tbk. PLANT MEDAN
TUGAS AKHIR
Diajukan untuk melengkapi tugas dan memenuhi syarat memperoleh gelar Ahli Madya
JAUHARIA
122401015
PROGRAM STUDI D-3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Penetapan Kadar Zat Aktif Pada Tablet Parasetamol 500 mg Di PT. Kimia Farma (Persero) Tbk. Plant Medan
Kategori : Tugas Akhir
Nama : Jauharia
Nomor Induk Mahasiswa : 122401015
Program studi : Diploma Tiga (D-3) Kimia
Departemen : Kimia
Fakultas : Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara NIP : 195509181987012001 NIP : 195504051983011002
Disetujui Oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENETAPAN KADAR ZAT AKTIF PADA TABLET PARASETAMOL 500 mg DI PT. KIMIA FARMA (PERSERO) Tbk. PLANT MEDAN
TUGAS AKHIR
Saya mengakui bahwa tugas akhir ini adalah hasil karya saya sendiri. Kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juli 2015
PENGHARGAAN
Puji dan syukur penulis sampaikan kehadirat Allah SWT atas segala rahmat dan hidayah-Nya yang telah diberikan kepada penulis, sehingga penulis dapat menyelesaikan tugas akhir ini tepat pada waktunya. Tugas Akhir ini disusun sebagai persyaratan untuk menyelesaikan pendidikan Program Studi D-3 Kimia Analis Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara dengan judul ”Penetapan Kadar Zat Aktif Pada Tablet Parasetamol 500 mg Di PT. Kimia Farma (Persero) Tbk. Plant Medan”
. Dalam penyusunan tugas akhir ini penulis banyak menemukan kendala. Namun berkat bantuan, bimbingan dan dukungan dari berbagai pihak, akhirnya penulis dapat mengatasi berbagai kendala tersebut dengan baik. Atas bantuan, bimbingan dan dukungan dari berbagai pihak maka pada kesempatan ini dengan segala ketulusan dan kerendahan hati, penulis mengucapkan terima kasih kepada :
1. Kedua orang tua tercinta, Ayahanda Syahrul D. dan Ibunda Ismawarni serta saudara penulis tersayang, Fazlul Rozi dan Muhammad Try Imran Yasin yang telah memberikan bantuan moril dan materil serta doa restu demi kesuksesan penulis.
2. Bapak Dr. Sutarman, M.Sc selaku Dekan FMIPA USU.
3. Ibu Dr. Rumondang Bulan, MS selaku Ketua Departemen Kimia FMIPA USU.
4. Ibu Dra. Emma Zaidar Nst, M.Si selaku Ketua Program Studi D-3 Kimia FMIPA USU.
5. Bapak Prof. Dr. Zul Alfian, M.Sc selaku Dosen Pembimbing yang telah dengan tulus memberikan bimbingan kepada penulis dan bersedia meluangkan waktu, tenaga, dan pikiran dalam membantu penulisan tugas akhir ini.
6. Bapak Prof. Dr. Tamrin, M.Sc selaku Dosen Pembimbing Akademik serta seluruh staff pengajar dan pegawai Departemen Kimia, FMIPA USU. 7. Bapak Drs. Beben Budiman, Apt. selaku Plant Manager PT. Kimia Farma
(Persero) Tbk. Plant Medan yang telah memberikan tempat untuk melaksanakan PKL.
8. Bapak Yogi Sugianto, S.Farm., Apt. selaku Apoteker Penanggung Jawab Quality Control yang telah memberikan pengarahan dan membimbing penulis selama pelaksanaan PKL di PT. Kimia Farma (Persero) Tbk. Plant Medan.
10.Teman-teman saya M. Deddy Harfiansyah, Drahenti Saragih, dan Maslin Samosir yang telah membantu saya selama mengikuti Praktik Kerja Lapangan (PKL) di PT Kimia Farma (Persero) Tbk. Plant Medan.
11.Teman-teman saya Ika Puteri, Sri Wulandari, Amelia, Anisya, Deby serta teman-teman seperjuangan D-3 Kimia stambuk 2012 dan seluruh pihak yang tidak dapt penulis sebutkan satu persatu yang turut andil dalam membantu penulis sehingga selesainya tugas akhir ini.
Penulis menyadari bahwa Tugas Akhir ini masih jauh dari kesempurnaan. Oleh karena itu penulis sangat mengharapkan kritik dan saran yang bersifat membangun dari para pembaca untuk kesempurnaan Tugas Akhir ini. Segala bentuk masukan yang diberikan akan penulis terima dengan senang hati dan penulis ucapkan terima kasih. Harapan penulis, semoga Tugas Akhir ini dapat bermanfaat bagi para pembaca umumnya dan bagi penulis khususnya.
Medan, Juli 2015
PENETAPAN KADAR ZAT AKTIF PADA TABLET PARASETAMOL 500 mg DI PT. KIMIA FARMA (PERSERO) Tbk. PLANT MEDAN
ABSTRAK
Parasetamol (C8H9NO2) memiliki karakteristik yaitu berbentuk serbuk hablur,
DETERMINATION OF ACTIVE MATTER IN PARACETAMOL TABLETS 500 mg IN PT. KIMIA FARMA (PERSERO) Tbk. PLANT MEDAN
ABSTRACT
Paracetamol (C8H9NO2) has characteristics that crystalline powder form, white,
DAFTAR ISI Bab 2. Tinjauan Pustaka 2.1 Tablet 5
2.1.1. Jenis-jenis Tablet 5
2.1.2. Cara Penggunaan Tablet 6 2.2. Parasetamol 6
2.2.1. Toksisitas Parasetamol 7 2.2.2. Farmakokinetik 8 2.2.3. Farmakodinamik 9 2.3. Kromatografi 9
2.3.2. Pembagian Kromatografi 9 2.3.3. Kromatografi Cair Kinerja Tinggi (KCKT) 10 2.3.4. Kegunaan Kromatografi Cair Kinerja Tinggi
(KCKT) 11
2.3.5. Cara Kerja Kromatografi Cair Kinerja Tinggi
(KCKT) 12
2.3.6. Sistem Peralatan Kromatografi Cair Kinerja
Tinggi 13
Bab 3. Metodologi
3.1. Alat-Alat 19
3.2. Bahan-Bahan 19
3.3. Prosedur 20
3.3.1. Pembuatan Larutan Fase Gerak 20 3.3.2. Pembuatan Larutan Baku Pembanding Sekunder 20
3.3.3. Prosedur Sampel 20
3.3.4. Pemakaian Alat HPLC 21
3.3.4.1. Persiapan Analisa 21
3.3.4.2. Persiapan Injeksi 22
Bab 4. Hasil dan Pembahasan
4.1. Hasil 23
4.2. Perhitungan 24
4.3. Pembahasan 25
Bab 5. Kesimpulan dan Saran
5.1 Kesimpulan 26
5.2. Saran 26
DAFTAR TABEL
Nomor Tabel Judul Halaman
4.1 Larutan Baku Parasetamol 23
4.2 Larutan Sampel Parasetamol 23
4.3 Hasil Penetapan Kadar Tablet Secara Kromatografi
DAFTAR GAMBAR
Nomor Gambar Judul Halaman
2.1 Struktur Parasetamol 6
2.2 Alat Kromatografi Cair Kinerja Tinggi (KCKT)
DAFTAR LAMPIRAN
Nomor Lampiran Judul Halaman
1 Kromatogram Larutan Baku Pembanding 28 2 Luas Area Larutan Baku Pembanding 29
3 Kromatogram Parasetamol 30
4 Luas Area Parasetamol 31