PENETAPAN KADAR BAHAN BAKU PARASETAMOL
YANG DIGUNAKAN PT. KIMIA FARMA (Persero) Tbk.
PLANT MEDAN SECARA HPLC
(High Performance Liquid Chromatography)
TUGAS AKHIR
OLEH:
HILVINA ANUGRAHWATI NIM 122410102
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Segala puji dan syukur penulis panjatkan kepada Allah SWT yang telah
melimpahkan rahmat dan hidayah-Nya serta menganugerahkan pengetahuan dan
kesempatan sehingga penulis dapat menyelesaikan tugas akhir yang berjudul
”penetapan kadar bahan baku parasetamol yang digunakan PT. Kimia Farma
(Persero) Tbk. Plant Medan secara HPLC (High Performance Liquid
Chromatography)”. Tugas akhir ini disusun untuk memenuhi salah satu syarat
dalam menyelesaikan Program Studi Diploma III Analis Farmasi dan Makanan di
Fakultas Farmasi Universitas Sumatera Utara.
Penulis menyadari bahwa tanpa bantuan dari berbagai pihak, penulis tidak
akan dapat menyelesaikan tugas akhir ini sebagaimana mestinya. Untuk itu
penulis juga mengucapkan terima kasih yang sebesar–besarnya kepada berbagai
pihak antara lain:
1. Ibu Dra. Anayanti Arianto, M.Si., Apt., sebagai Dosen Pembimbing yang
telah memberikan bimbingan dan pengarahan kepada penulis dalam
penyusunan tugas akhir ini.
2. Bapak Yogi Sugianto, S.Farm., Apt., sebagai Supervisor Quality Control
sekaligus Pembimbing II yang telah membimbing dan memberikan saran
serta petunjuk selama pelaksanaan PKL di PT. Kimia Farma (Persero) Tbk
Plant Medan hingga penyusunan tugas akhir ini.
3. Bapak Drs. Beben Budiman, Apt. selaku Plant Manager PT. Kimia Farma
(Persero) Tbk. Plant Medan yang telah memberikan tempat untuk
melaksanakan PKL ini.
4. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagai Dekan Fakultas
5. Ibu Prof. Dr. Julia Reveny, M.Si., Apt. selaku Wakil Dekan I Fakultas
Farmasi Universitas Sumatera Utara.
6. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., sebagai Ketua Program
Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas
Sumatera Utara.
7. Prof. Dr. Urip Harahap, Apt., sebagai Dosen Penasehat Akademis yang telah
memberikan nasehat dan pengarahan kepada penulis dalam hal akademis
setiap semester.
Terima kasih untuk kedua orang tua tercinta, abang serta adik yang telah
memberikan dukungan moril dan materil selama ini. Dan sahabat–sahabatku Try
Iga Septiawandari, Anggi Nulvi Siregar, Vanesia Atelya O. Manurung dan
Sherina Elvira Nasution yang telah saling membantu dalam penulisan tugas akhir
ini. Serta pihak–pihak yang telah ikut membantu penulis namun tidak tercantum
namanya.
Penulis menyadari bahwa penulisan tugas akhir ini masih belum sempurna.
Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun untuk
kesempurnaan tugas akhir ini. Akhir kata penulis berharap tugas akhir ini dapat
bermanfaat bagi semua pihak yang membaca.
Medan, Maret 2015
Penulis,
PENETAPAN KADAR BAHAN BAKU PARASETAMOL YANG
DIGUNAKAN PT. KIMIA FARMA (Persero) Tbk. PLANT
MEDAN SECARA HPLC (High Performance Liquid
Chromatography)
ABSTRAK
Pemeriksaan terhadap bahan baku yang akan digunakan dalam pembuatan sediaan farmasi dilakukan penetapan kadar bahan baku sebelum diformulasikan untuk menjadi suatu sediaan obat. Kualitas mutu dari bahan baku yang digunakan untuk produksi akan mempengaruhi produk jadi.
Sampel yang digunakan berasal dari bahan baku parasetamol yang digunakan untuk pembuatan sediaan tablet parasetamol produksi PT. Kimia Farma (Persero) Tbk. Plant Medan.
Metode yang digunakan dalam penetapan kadar bahan baku parasetamol adalah metode HPLC (High Performance Liquid Chromatography) atau biasa disebut juga dengan KCKT (Kromatografi Cair Kinerja Tinggi). Metode ini menggunakan pelarut dan fase gerak yang sama yaitu metanol : aquabidest (1:3) dengan panjang gelombang 243 nm.
Diperoleh hasil rata-rata kadar bahan baku parasetamol 100,47%. Dari hasil pengukuran menunjukkan masih memenuhi persyaratan kadar bahan baku Farmakope Indonesia Edisi IV yaitu tidak kurang dari 98,00% dan tidak lebih dari 101,00%.
Dengan demikian, bahan baku parasetamol yang digunakan oleh PT. Kimia Farma (Persero) Tbk. Plant Medan telah memenuhi persyaratan kadar yang ada di Farmakope Indonesia Edisi IV.
DAFTAR ISI
2.1Asetaminofen (Parasetamol) ... 3
2.1.1 Farmakodinamik ... 4
2.1.2 Farmakokinetik ... 4
2.1.3 Penetapan Kadar Parasetamol ... 5
2.2Bahan Baku Obat ... 9
2.3High Performance Liquid Chromatography (HPLC) ... 9
2.3.1 Alat Utama HPLC ... 11
3.1Tempat dan Waktu Percobaan ... 15
3.2Bahan-bahan ... 15
3.2.1 Sampel ... 15
3.2.2 Fase Gerak dan Pelarut ... 15
3.3Alat-alat ... 15
3.4Pembuatan Larutan Fase Gerak dan Pelarut ... 15
3.4.1 Larutan Metanol : Aquabidest (1:3) ... 15
3.5Prosedur Percobaan ... 16
3.5.1 Pengambilan Sampel ... 16
3.5.2 Larutan Standart ... 16
3.5.3 Larutan Sampel Uji... 16
3.5.4 Penetapan Kadar Menggunakan HPLC ... 17
BAB IV HASIL DAN PEMBAHASAN ... 18
4.1Hasil ... 18
4.2Pembahasan ... 18
BAB V KESIMPULAN DAN SARAN ... 20
5.1Kesimpulan ... 20
5.2Saran ... 20
DAFTAR TABEL
Halaman
Tabel 4.1 Hasil HPLC Untuk Standart Parasetamol (Baku Pembanding) ... 18
DAFTAR GAMBAR
Halaman
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Penetapan Kadar Bahan Baku Parasetamol ... 22
Lampiran 2. Hasil Print Our HPLC... 25
PENETAPAN KADAR BAHAN BAKU PARASETAMOL YANG
DIGUNAKAN PT. KIMIA FARMA (Persero) Tbk. PLANT
MEDAN SECARA HPLC (High Performance Liquid
Chromatography)
ABSTRAK
Pemeriksaan terhadap bahan baku yang akan digunakan dalam pembuatan sediaan farmasi dilakukan penetapan kadar bahan baku sebelum diformulasikan untuk menjadi suatu sediaan obat. Kualitas mutu dari bahan baku yang digunakan untuk produksi akan mempengaruhi produk jadi.
Sampel yang digunakan berasal dari bahan baku parasetamol yang digunakan untuk pembuatan sediaan tablet parasetamol produksi PT. Kimia Farma (Persero) Tbk. Plant Medan.
Metode yang digunakan dalam penetapan kadar bahan baku parasetamol adalah metode HPLC (High Performance Liquid Chromatography) atau biasa disebut juga dengan KCKT (Kromatografi Cair Kinerja Tinggi). Metode ini menggunakan pelarut dan fase gerak yang sama yaitu metanol : aquabidest (1:3) dengan panjang gelombang 243 nm.
Diperoleh hasil rata-rata kadar bahan baku parasetamol 100,47%. Dari hasil pengukuran menunjukkan masih memenuhi persyaratan kadar bahan baku Farmakope Indonesia Edisi IV yaitu tidak kurang dari 98,00% dan tidak lebih dari 101,00%.
Dengan demikian, bahan baku parasetamol yang digunakan oleh PT. Kimia Farma (Persero) Tbk. Plant Medan telah memenuhi persyaratan kadar yang ada di Farmakope Indonesia Edisi IV.
BAB I PENDAHULUAN
1.1Latar Belakang
Obat adalah unsur aktif secara fisiologi dipakai dalam diagnosis,
pencegahan, pengobatan atau penyembuhan suatu penyakit pada manusia atau
hewan (Ansel, 2005).
Pada jaminan mutu, setiap bahan baku yang diluluskan untuk dibawa
kebagian produksi harus dicek bahwa bahan memenuhi persyaratan resmi
farmakope atau oleh industri farmasi yang bersangkutan. Bahan baku adalah
semua bahan yang berkhasiat (zat aktif) yang digunakan dalam pengolahan obat
(Siregar, 2010).
Parasetamol (asetaminofen) merupakan salah satu obat
analgesik-antipiretik yang sangat populer. Parasetamol dapat tersedia dalam berbagai
macam sediaan seperti tablet, kapsul, tetes, eliksir, suspensi dan supositoria.
Parasetamol pada umumnya diberikan dalam bentuk tablet yang mengandung
bahan aktif. Parasetamol juga sering dikombinasikan dengan bahan obat lain
dalam satu formulasi (Sudjadi dan Abdul, 2008).
Menurut sudjadi dan abdul penetapan kadar bahan baku parasetamol dapat
ditetapkan kadarnya dengan cara yang hampir sama dengan asetofenetidin yakni
dengan titrimetri dengan metode diazotasi, spektrofotometri (baik UV maupun
dengan cara spektrofotometri visibel) dan dengan kromatografi. Penetapan kadar
bahan baku parasetamol yang ada di PT. Kimia Farma (Persero) Tbk. Plant
Medan menggunakan metode HPLC (High Performance Liquid
Berdasarkan hal ini, penulis tertarik untuk mengambil judul tugas akhir
sebagai berikut ”Penetapan Kadar Bahan Baku Parasetamol Yang Digunakan
PT. Kimia Farma (Persero) Tbk. Plant Medan Secara HPLC (High Performance Liquid Chromatography)”.
1.2Tujuan dan Manfaat 1.2.1 Tujuan
Tujuan dari tugas akhir ini adalah:
- Untuk mengetahui kadar dari bahan baku Parasetamol yang digunakan
oleh PT. Kimia Farma (Persero) Tbk. Plant Medan.
- Untuk mengetahui apakah kadar bahan baku Parasetamol yang digunakan oleh PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi persyaratan
menurut Farmakope Indonesia Edisi IV yang telah ditetapkan.
1.2.2 Manfaat
Untuk memberikan informasi tentang kadar bahan baku parasetamol yang
digunakan oleh PT. Kimia Farma (Persero) Tbk. Plant Medan apakah bahan baku
parasetamol memenuhi persyaratan Farmakope Indonesia Edisi IV yaitu tidak
BAB II
TINJAUAN PUSTAKA
2.1Asetaminofen (Parasetamol)
Gambar 2.1. Rumus Bangun Parasetamol
Sifat-sifat fisika : kristal putih tidak berbau atau serbuk kristalin dengan
rasa pahit. Jarak lebur 169o sampai 172oC.
Kelarutan : 1 g dapat larut dalam kira-kira 70 ml air pada suhu 25oC,
1 g larut dalam 20 ml air mendidih, dalam 7 ml alkohol,
dalam 13 ml aseton, dalam 50 ml kloroform, dalam 40 ml
gliserin, dan dalam 9 ml propilen glikol. Tidak larut dalam
benzen dan eter, dan larut dalam larutan alkali hidroksida.
Larutan jenuh mempunyai pH kira-kira 6 dimana pKa
adalah 9,51 (Connors dkk, 1986).
Parasetamol merupakan metabolit fenasetin dengan efek antipiretik yang
telah digunakan sejak tahun 1893. Efek antipiretik ditimbulkan oleh gugus
amino-benzen. Parasetamol di Indonesia dikenal sebagai antipiretik, dan tersedia sebagai
obat bebas. Efek anti-inflamasi parasetamol hampir tidak ada (Wilmana, 2007).
Analgetik non narkotik sering pula disebut analgetik-antipiretik atau Non
Steroidal Anti-Inflamantory Druds (NSAID). Analgetik non narkotik bekerja pada
perifer dan sentral sistem syaraf pusat. Obat golongan ini digunakan untuk
mengurangi rasa sakit yang ringan sampai moderat, untuk menurunkan suhu
pengobatan rematik. Analgetik-antipiretik digunakan untuk pengobatan
simptomatik, yaitu hanya meringankan gejala penyakit, tidak menyembuhkan atau
menghilangkan penyebab penyakit. Antipiretik non narkotik menimbulkan kerja
antipiretik dengan meningkatkan eliminasi panas, pada penderita dengan suhu
badan tinggi, dengan cara menimbulkan dilatasi pembuluh darah perifer dan
mobilisasi air hingga terjadi pengenceran darah dan pengeluaran keringat.
Pengaruh obat pada suhu badan normal relatif kecil (Siswandono dan Bambang,
2000).
Analgetik adalah obat yang menghilangkan rasa nyeri dengan cara
meningkatkan nilai ambang nyeri di sistem syaraf pusat tanpa menekan
kesadaran. Antipiretik adalah obat yang menekan suhu tubuh pada keadaan
demam. Analgetik-antipiretik adalah kelompok non narkotika, artinya obat ini
tidak menimbulkan adiksi pada penggunaan jangka panjang ( Djamhuri, 1990).
2.1.1 Farmakodinamik
Efek analgesik parasetamol serupa dengan salisilat yaitu menghilangkan
atau mengurangi nyeri ringan sampai radang. Menurunkan suhu tubuh dengan
mekanisme yang diduga juga berdasarkan efek sentral. Efek anti-inflamasinya
sangat lemah, oleh karena itu parasetamol tidak digunakan sebagai antireumatik.
Parasetamol merupakan penghambat biosintetis prostaglandin yang lemah. Efek
iritasi dan perdarahan lambung tidak terlihat pada obat ini, demikian juga
gangguan pernapasan dan keseimbangan asam basa (Wilmana, 2007).
2.1.2 Farmakokinetik
Parasetamol diserap cepat dan sempurna melalui saluran cerna.
paruh dalam plasma antara 1-3 jam. Obat ini tarsebar ke seluruh cairan tubuh.
Dalam plasma terikat 25% oleh protein plasma (Wilmana, 2007).
Obat ini mengalami metabolisme oleh enzim-enzim mikrosom dalam hati,
80% parasetamol dikonjugasi dengan asam glukuronat dan sebagian kecil dengan
asam sulfat dalam hati. Selain itu obat ini juga dapat mengalami hidroksilasi.
Metabolit hasil hidroksilasi ini dapat menimbulkan methemoglobinemia dan
hemolisis ertrosit. Obat ini diekskresi melalui ginjal, sebagian kecil sebagai
parasetamol dan sebagian besar dalam bentuk terkonjugasi (Wilmana, 2007).
2.1.3 Penetapan Kadar Parasetamol
Parasetamol dapat ditetapkan kadarnya dengan cara yang hampir sama
dengan asetofenetidin yakni dengan titrimetri dengan metode diazotasi,
spektrofotometri (baik UV maupun dengan cara spektrofotometri visibel) dan
dengan kromatografi (Sudjadi dan Abdul, 2008).
1. Metode titrimetri
a. Diazotasi
Metode analisis parasetamol dalam tablet dengan metode ini mirip
dengan penetapan kadar asetofenetidin (fenasetin) yakni melibatkan
hidrolisis parasetamol untuk menghasilkan amin aromatis primer lalu
diikuti dengan titrasi menggunakan larutan baku natrium nitrit dalam
suasana asam (Sudjadi dan Abdul, 2008).
b. Titrasi dengan N,N-dibromo dimetilhidantoin
Suatu metode titrimetri yang sederhana dan akurat telah
dikembangkan oleh Kumar dan Letha untuk analisis parasetamol baik
menggunakan titran dibromo dimetilhidantoin (DBH). Larutan
N,N-dibromo dimetilhidantoin (DBH) disiapkan dengan brominasi
dimetilhidantoin. Suatu larutan baku DBH dengan konsentrasi ± 0,01 M
disiapkan dalam air (Sudjadi dan Abdul, 2008).
Parasetamol murni disiapkan dalam larutam asam asetat 10 % dalam
air. Sebagai indikator digunakan larutan amaranth 0,2 % dalam etanol
lalu dititrasi dengan larutan baku DBH. Titik akhir titrasi ditandai dengan
hilangnya warna pink (Sudjadi dan Abdul, 2008).
2. Spektrofotometri UV
Parasetamol dapat ditetapkan kadarnya secara spektrofometri UV
karena parasetamol mempunyai kromofor yang mampu menyerap sinar UV.
Parasetamol dalam etanol mempunyai panjang gelombang maksimal 249
nm dengan nilai ∑1 %1 cm sebesar 900. Cara penetapan parasetamol dengan
spektrofotometri UV adalah 100 mg parasetamol ditimbang dengan cara
seksama lalu dilarutkan dalam etanol. Larutan dimasukkan dalam labu takar
100 mL dan ditambah etanol sampai tanda batas. Sebanyak 0,5 mL larutan
diatas diambil dan dimasukkan kedalam labu takar 100 mL, dan ditambah
etanol sampai tanda batas. Larutan ini selanjutnya dibaca absorbansinya
pada panjang gelombang 249 nm terhadap blanko yang berisi etanol
sehingga akan didapatkan absorbansi larutan blanko (Ab). Untuk sampel
dilakukan hal yang sama sehingga didapatkan absorbansi sampel (As)
(Sudjadi dan Abdul, 2008).
Parasetamol dapat ditetapkan kadarnya dengan spektrofometri
visibel menggunakan metode Bratton-Marshall dan metode amonium
molibdat (Sudjadi dan Abdul, 2008).
a. Metode Bratton-Marshall
Metode Bratton-Marshall untuk parasetamol dilakukan dengan cara
menghidrolisis parasetamol dengan asam sehingga terbentuk amin
aromatis primer yang selanjutnya didiazotasi dengan asam nitrit (berasal
dari natrium nitrit dalam suasana asam) membentuk garam diazonium,
lalu direaksikan dengan naftil etilen diamin (Sudjadi dan Abdul, 2008).
b. Metode Amonium molibdat
Metode spektrofotometri visible yang mendasarkan pada reaksi
antara parasetamol dengan amonium molibdat dengan medium asam kuat
menghasilkan molibdenum biru telah dikembangkan oleh Morelli.
Hukum Beer’s dipenuhi sampai pada konsentrasi parasetamol 6 µg/mL
dan nilai absorbtivitas molarnya pada panjang gelombang 670 nm
sebesar 2,6 x 104 L/mol (Sudjadi dan Abdul, 2008).
4. Metode spektrofluorometri
Metode spektrofluorometri dengan batas deteksi yang rendah telah
disusulkan untuk penetapan kadar parasetamol. Karena parasetamol bukan
suatu senyawa yang berfluoresensi maka parasetamol dapat ditetapkan
sacara tidak langsung dengan mereaksikannya menggunakan Ce (IV)
sebagai agen pengoksidasi dan mengukur intensitas fluoresensi relatif Ce
Penetapan kadar parasetamol dengan spektrofluometri secara
langsung sebelumnya membutuhkan tahap derivatisasi. Reagen-reagen
seperti fluoresamin dan dansil klorida telah diusulkan oleh Bosch dkk.
sebagai agen penderivat parasetamol (Sudjadi dan Abdul, 2008).
5. Metode Kromatografi
Dalam sediaan farmasi, parasetamol biasanya bercampur dengan
bahan obat lain sehingga membutuhkan teknik pemisahan, misal dengan
kromatografi lapis tipis, kromatografi cair kinerja tinggi, kromatografi gas
dan diikuti dengan kuantikasinya untuk menentukan berapa kadar
masing-masing bahan obat dalam sediaan farmasi (Sudjadi dan Abdul, 2008).
a. Kromatografi Lapis Tipis (KLT)
Metode KLT-Densitometri telah digunakan untuk analisis
parasetamol dan klorsoksazol secara simultan. Keuntungan
KLT-Densitometri dibandingkan dengan spektrofotometri adalah kemampuan
KLT untuk memisahkan komponen-komponen dalam sampel yang
dianalisis sehingga meghilangkan adanya kemungkinan saling
mengganggu antar komponen (Sudjadi dan Abdul, 2008).
b. Kromatografi Cair Kinerja Tinggi (KCKT)
Metode KCKT yang sederhana, cepat, dan sesuai telah
dikembangkan untuk penetapan kadar secara simultan parasetamol dan
senyawa-senyawa terkait (4-aminofenol dan 4-klorasetanilid) dalam
sediaan farmasi. Fase gerak yang digunakan adalah campuran
isokratik. Detektor yang digunakan adalah spektrofotometer UV pada
panjang gelombang 244 nm (Sudjadi dan Abdul, 2008).
2.2Bahan Baku Obat
Bahan (zat) aktif adalah tiap bahan atau campuran bahan yang akan
digunakan dalam pembuatan sediaan farmasi dan apabila digunakan dalam
pembuatan obat menjadi zat aktif obat tersebut. Dalam arti lain, bahan (zat) aktif
adalah bahan yang ditujukan untuk menciptakan khasiat farmakologi atau efek
langsung lain dalam diagnosis, penyembuhan, pengobatan atau pencegahan
penyakit, atau untuk memengaruhi struktur dan fungsi tubuh (Dirjen POM, 2006).
Semua bahan baku yang digunakan harus memenuhi persyaratan resmi
farmakope atau persyaratan lain yang disetujui oleh regulator atau oleh industri
farmasi yang bersangkutan. Selain itu, bahan–bahan yang dibeli harus sesuai
dengan spesifikasi hasil uji praformulasi agar diperoleh mutu obat yang konsisten
dan memenuhi persyaratan keamanan, khasiat, stabilitas, dan ketersediaan hayati
(Siregar, 2010).
Setiap bahan obat memiliki ciri-ciri kimiawi dan fisika tersendiri yang
menjadikannya unik. Ciri-ciri ini digunakan dalam menyusun standar identifikasi
bahan dan untuk pengujian (Ansel, 2005).
2.3High Performance Liquid Chromatography (HPLC)
Kromatografi adalah suatu nama yang diberikan untuk teknik pemisahan
tertentu. Pada dasarnya semua cara kromatografi menggunakan dua fase yaitu fase
tetap (stationary) dan fase bergerak (mobile), dimana pemisahan-pemisahan
tergantung pada gerakan relatif dari dua fase ini. Pemisahan dengan kromatografi
fase-fase bergerak dan tetap perbandingan yang sangat berbeda-beda dari satu
senyawa yang lain (Sastrohamidjojo, 1985).
Kemajuan teknologi kolom, sistem pompa tekanan tinggi, dan detektor
yang sensitif telah menyebabkan perubahan kromatografi kolom cair menjadi
suatu sistem pemisahan dengan kecepatan dan efisiensi yang tinggi. Metode ini
dikenal sebagai Kromatografi Cair Kinerja Tinggi (Ditjen, 1995).
Kromatografi Cair Kinerja Tinggi (KCKT) atau biasa disebut dengan
HPLC ( high perfomance liquid chromatography) dikembangkan pada akhir tahun
1960-an dan awal tahun 1970-an (Rohman, 2009).
Kegunaan umum Kromatografi Cair Kinerja Tinggi (KCKT) adalah untuk
pemisahan sejumlah senyawa organik, anorganik, maupun senyawa biologis;
analisis ketidakmurnian (impurities), analisis senyawa yang mudah menguap
(non-volatil), analisis senyawa yang tidak ionik maupun zwitter, isolasi dan
pemurnian senyawa, pemisahan senyawa-senyawa yang strukturnya hampir sama,
pemisahan senyawa-senyawa dalam jumlah sekelumit (trace elements), dalam
jumlah banyak, dan dalam skala proses industri. Kromatografi Cair Kinerja Tinggi
(KCKT) merupakan metode yang tidak destruktif dan dapat digunakan baik untuk
analisis kualitatif maupun kuantitatif (Rohman, 2009).
Salah satu konsep penting KCKT ialah mengusahakan volum pelarut
antara penjerap dan detektor atau fraksinator sekecil mungkin untuk mencegah
pencampuran kembali fraksi-fraksi setelah terpisahkan (Gritter dkk, 1991).
Tiga bentuk kromatografi cair kinerja tinggi yang paling banyak
digunakan penukar ion, partisi dan adsorbsi (Ditjen, 1995).
Kromatografi penukar ion terutama digunakan untuk pemisahan
zat-zat larut dalam air yang ionik atau yang dapat terionisasi dengan bobot
molekul kurang dari 1500 (Ditjen, 1995).
Kromatografi pertukaran ion menggunakan fase diam yang dapat
menukar kation atau anion yang berada dalam fase gerak. Pertukaran
ionnya bolak-balik dan terjadi antara fase diam penukaran ion dengan fase
gerak cair. Pemisahan terjadi karena perbedaan kekuatan interaksi
elektrostatik dari zat terlarut dengan fase diam (Munson, 1991).
b. Kromatografi Partisi
Pada kromatografi partisi digunakan fase gerak dan fase dengan
polaritas yang berbeda. Jika fase gerak bersifat polar dan fase diam
non-polar, dikenal sebagai kromatografi fase balik, maka senyawa nonpolar
yang larut dalam hodrokarbon, dengan bobot molekul kurang dari 1000,
dapat dipisahkan berdasarkan atas afinitasnya terhadap fase diam (Ditjen,
1995).
c. Kromatografi Adsorbsi
Pemisahan kromatografi adsorbsi biasanya menggunakan fase
normal dengan menggunakan fase diam silika gel dan alumina, meskipun
demikian sekitar 90% kromatografi ini memakai silika sebagai fase
diamnya (Rohman, 2009).
2.3.1 Alat Utama HPLC
Alat utama HPLC adalah tandon pelarut, pipa, pompa, suntikan, kolom,
detektor, penguat sinyal dan perekam.
Tandon pelarut atau fase gerak harus mempunyai beberapa ciri. Bahan
tandon harus tahan terhadap fase gerak berair dan tidak berair. Sehingga
baja anti karat dan gelas menjadi bahan terpilih. Daya tampung tandon harus
lebih besar dari 500 ml, yang dapat digunakan selama 4 jam untuk
kecepatan alir yang umumnya 1-2 ml/menit. Kecermatan harus
diperhatikan untuk menghindari pecahnya tandon gelas supaya tidak tumpah
(Munson, 1991).
b. Pipa
Sifat pipa penyambung seluruh bagian sistem harus diperhatikan. Garis
tengah dalam pipa sebelum penyuntikan tidak berpengaruh, dapat tahan
tekanan serta mampu dilewati pelarut dengan volume yang memadai
(Munson, 1991).
c. Pompa
Berdasarkan dari cara kerjanya pompa untuk HPLC dapat digolongkan
dalam dua kelompok yaitu pompa kecepatan tetap dan pompa tekanan tetap.
Masing-masing mempunyai kelebihan dan kelemahan dan tidak satu pun
dapat dipakai secara menyeluruh (Munson, 1991).
d. Penyuntik / Sistem Penyuntik Cuplikan
Teknik penyuntikan harus dilakukan dengan cepat untuk mencapai
ketelitian maksimum analisis kuantitatif. Yang terpenting sistem harus dapat
mengatasi tekanan balik yang tinggi tanpa kehilangan cuplikan. Pada saat
pengisian cuplikan, cuplikan dialirkan melewati lingkaran cuplikan dan
diputar sehingga fase gerak mengalir melewati lingkar cuplikan ke kolom
(Munson, 1991).
e. Kolom
Kolom merupakan jantung kromatografi, keberhasilan atau kegagalan
analisi bergantung pada pilihan kolom dan kondisi kerja yang tepat.
Dianjurkan untuk memasang penyaring 2 μm dianjurkan antara penyuntik
dan kolom, untuk menahan partikel yang dibawa fase gerak dan cuplikan.
Hal ini dapat memperpanjang umur kolom. (Munson, 1991).
Kolom kromatografi untuk pengaliran oleh gaya tarik bumi (Gravitasi)
atau sistem bertekanan rendah biasanya terbuat dari kaca yang dilengkapi
kran jenis tertentupada bagian bawahnya untuk mengatur aliran pelarut.
Salah satu konsep penting KCKT adalah mengusahakan volum pelarut
antara penjerap dan detektor atau farksinator sekecil mungkin untuk
mencegah pencampuran kembali fraksi-fraksi setelah terpisah. (Gritter,
1991).
f. Detektor
Detektor harus memberi tanggapan pada cuplikan, tanggapan yang
dapat diramal, peka, hasil yang efisien dan tidak terpengaruh oleh
perubahan suhu atau komposisi fasgerak. Detektor yang dipakai pada
Kromatografi Cair Kinerja Tinggi (KCKT) biasanya adalah UV 254 nm.
Bila tanggapan detektor lebih lambat dari elusi sampel timbullah pelebaran
jalan pita yang memburuk pemisahan. Pemilihan detektor Kromatografi
Cair Kinerja Tinggi (KCKT) tergantung pada sifat sampel, fase gerak dan
g. Penguat sinyal
Pada umunya sinyal yang berasal dari detektor diperkuat terlebih
dahulu sebelum disampaikan pada alat perekam potensiometrik. Dapat pula
sinyal dikirimkan kepada suatu integrator digital elektronik untuk mengukur
luas puncak kromatogram secara otomatik (Munson, 1991).
h. Perekam
Perekam merupakan salah satu dari bagian peralatan yang berfungsi
untuk merekam atau menunjukkan hasil pemeriksaan suatu senyawa berupa
peak (puncak). Dari daftar tersebut secara kualitatif kita dapat menentukan
atau mengetahui senyawa apa yang diperiksa, luas dan tinggi puncak
berbanding lurus dengan konsentrasi. Dari data ini dapat pula dipakai untuk
memperoleh secara kuantitatif. Sebagai perekam biasanya dipakai
BAB III
METODE PERCOBAAN
3.1 Tempat dan Waktu Percobaan
Percobaan ini dilakukan di Laboratorium Instrument yang terdapat di
industri PT. Kimia Farma (Persero) Tbk. Plant Medan yang beralamat di jl.
Sisingamaraja KM.9 No.59 Medan pada bulan Februari 2015.
3.2 Bahan-bahan
3.2.1 Sampel
Sampel yang digunakan dalam percobaan ini adalah bahan baku
parasetamol yang digunakan oleh PT. Kimia Farma (Persero) Tbk. Plant Medan.
3.2.2 Fase Gerak dan Pelarut
Fase gerak dan pelarut yang digunakan dalam percobaan ini adalah
metanol : aquabidest (1:3).
3.3 Alat-alat
Alat-alat yang digunakan dalam percobaan ini adalah alat-alat gelas (labu
erlenmeyer 250 mL, labu tentukur 50 mL dan 100 mL, gelas ukur 25 mL dan
pipet volum 1 mL), digital analytical balance, ultrasonic digital Merk ELMA
type D-78224 dan seperangkat alat HPLC Merk WATERS 510/486/746.
3.4 Pembuatan Larutan Fase Gerak dan Pelarut 3.4.1 Larutan Metanol : Aquabidest ( 1 : 3 )
Diambil metanol sebanyak 200 mL dan ditambahkan dengan aquabidest
sebanyak 600 mL. Sehingga diperoleh larutan sebanyak 800 mL. Lalu di saring
3.5 Prosedur percobaan 3.5.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan secara random (acak) yang dapat
mewakili semuanya dengan menggunakan rumus 1 + √�. Dari 16 kemasan
sampel bahan baku yang ada, terpilih 5 sampel bahan baku yang akan diambil dan
kemudian digerus menjadi satu untuk uji penetapan kadar bahan baku.
3.5.2 Larutan Standart
Timbang 50 mg baku pembanding (std) sebanyak 6 kali, masing-masing
dimasukkan kedalam labu tentukur 100 mL. Tambahkan pelarut metanol :
aquabidest (1:3) sebanyak 25 mL, utrasonic selama 15 menit pada masing-masing
labu tentukur agar homogen dan larut dengan sempurna. Diadd sampai tanda batas
dengan pelarut, kocok dan pipet 1 mL, masukkan ke dalam labu tentukur 50 mL.
Cukupkan sampai tanda batas dengan pelarut, lalu dikocok, lakukan hal yang
sama untuk labu tentukur berikutnya. Disaring dengan filter 0,45 µm. Larutan siap
untuk diinjeksikan.
3.5.3 Larutan Sampel Uji
Timbang 50 mg sampel (paracetamolum) sebanyak 2 kali (duplo) dan
masukkan masing-masing ke dalam labu tentukur 100 mL. Tambahkan pelarut
metanol : aquabidest (1:3) sebanyak 25 mL, ultrasonic selama 15 menit pada
masing-masing labu tentukur agar homogen dan larut dengan sempurna. Diadd
sampai tanda batas dengan pelarut, kocok dan pipet 1 mL labu tentukur dan
masukkan ke dalam labu tentukur 50 mL. Cukupkan sampai tanda batas dengan
pelarut, lalu dikocok, lakukan hal yang sama untuk labu tentukur berikutnya.
3.5.4 Penetapan Kadar Menggunakan HPLC
Hidupkan semua saklar yang menyambung ke alat HPLC. Atur panjang
gelombang 243 nm dengan flow rate 1,20 mL/menit. Cuci kolom dengan
menggunakan fase gerak yang akan digunakan metanol : aquabidest (1:3). Kolom
yang digunakan adalah kolom tipe bondapack C18. Pada proses injection atau
penyuntikan dimana untuk 1 kali penyuntikan diperlukan larutan yang telah
disiapkan masing-masing sebanyak 20 µl. Dimana penyuntikan dimulai dari
larutan standart sebanyak 6 kali dan dilanjutkan dengan larutan sampel uji
sebanyak 2 kali (duplo). Tunggu dan lihat grafik kromatogram yang terbentuk
dilayar komputer.
Perhitungan penetapan kadar bahan baku parasetamol dapat digunakan
rumus sebagai berikut:
AUC Std : Luas Area Standart (Baku Pembanding)
[Sp] : Konsentrasi Sampel
[St] : Konsentrasi Standart
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Penetapan kadar bahan baku parasetamol menggunakan HPLC, didapat
hasil sebagai berikut:
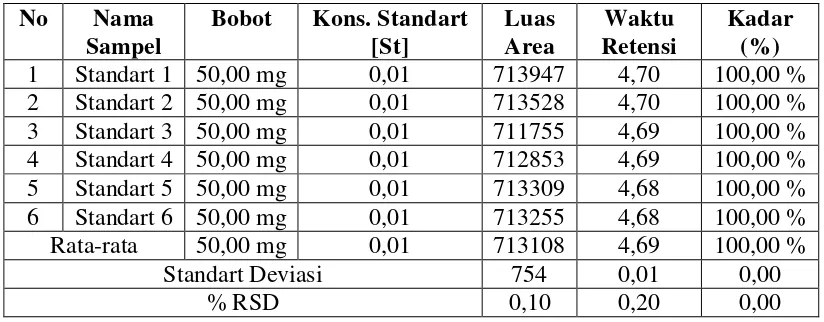
Tabel 4.1. Hasil HPLC Untuk Standart Parasetamol (Baku Pembanding)
No Nama Sampel
Bobot Kons. Standart [St]
Tabel 4.2. Hasil HPLC Untuk Bahan Baku Parasetamol
No Nama
Sehingga diperoleh kadar rata-rata dari bahan baku parasetamol adalah
100,47 %.
4.2 Pembahasan
Pada penetapan kadar bahan baku parasetamol diperoleh kadar rata-rata
yaitu 100,47%, menurut Farmakope Indonesia Edisi IV, rentang kadar
dari 101,00 %. Dengan demikian kadar bahan baku parasetamol yang digunakan
oleh PT. Kimia Farma (Persero) Tbk. Plant Medan yang telah ditetapkan kadarnya
memenuhi persyaratan dan dapat digunakan untuk produksi sediaan tablet
parasetamol.
Semua bahan baku yang digunakan harus memenuhi persyaratan resmi
farmakope atau persyaratan lain yang disetujui oleh regulator atau oleh industri
farmasi yang bersangkutan. Selain itu, bahan–bahan yang dibeli harus sesuai
dengan spesifikasi hasil uji praformulasi agar diperoleh mutu obat yang konsisten
dan memenuhi persyaratan keamanan, khasiat, stabilitas, dan ketersediaan hayati
(Siregar, 2010).
Penetapan kadar bahan baku sangat mempengaruhi kualitas sediaan obat
yang akan di produksi. Metode dan prosedur kerja yang digunakan sesuai dengan
Farmakope Edisi IV yang dimodifikasi oleh PT. Kimia Farma (Persero) Tbk.
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
- Kadar bahan baku parasetamol yang digunakan oleh PT. Kimia Farma (Persero) Tbk. Plant Medan adalah 100,47 %.
- Kadar bahan baku parasetamol yang digunakan oleh PT. Kimia Farma (Persero) Tbk. Plant Medan, memenuhi persyaratan yang tertera pada
Farmakope Indonesia edisi ke-IV yaitu tidak kurang dari 98,00 % dan
tidak ada yang lebih dari 101,00 %.
5.2Saran
Disarankan PT. Kimia Farma (Persero) Tbk. Plant Medan tetap
mempertahankan mutu dan kualitas bahan baku yang digunakan untuk produksi
DAFTAR PUSTAKA
Anief, M. (1994). Farmasetika. Yogyakarta: Gadjah Mada University Press. Hal. 17.
Ansel, H. C. (2005). Pengantar Bentuk Sediaan Farmasi. Edisi Keempat. Jakarta: UI Press. Hal. 50.
Connors, K. A., Gordon L. A., dan Valentino J. S. (1986). Stabilitas Kimiawi Sediaan Farmasi. Edisi kedua Jilid 1. Semarang: IKIP Semarang Press. Hal. 197.
Ditjen, POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan. Hal. 1009-1010.
Ditjen, POM. (2006). Cara Pembuatan Obat yang Baik. Jakarta: Badan POM. Hal. 5, 77, 98, 237.
Djamhuri, A. (1995). Sinopsis Farmakologi dengan Terapan Khusus di Klinik dan Perawatan. Jakarta: Hipokrates. Hal. 45.
Gritter, R. J., James, M. B., dan Arthur E. S. (1991). Pengantar Kromatografi. Bandung: ITB. Hal. 163.
Munson, J. W. (1991). Analisis Farmasi Metode Modern. Surabaya: Airlangga University Press. Hal. 14-15, 17, 26-32.
Rohman, A. (2009). Kromatografi Untuk Analisis Obat. Yogyakarta: Graha Ilmu. Hal. 117.
Sastrohamidjojo, H. (1985). Kromatografi. Yogyakarta: Liberty. Hal. 1-2.
Siregar, J. P. (2010). Teknologi Farmasi Sediaan Tablet Dasar-dasar Praktis.
Jakarta: EGC. Hal. 15-16, 123, 605, 647.
Siswandono, B. S. (2000). Kimia Medisinal. Edisi kedua. Surabaya: Airlangga University Press. Hal. 291-292.
Sudjadi., Abdul R. (2008). Analisis Kuantitatif Obat. Yogyakarta: Gadjah Mada University Press. Hal. 48-56.
Lampiran 1. Perhitungan Penetapan Kadar Bahan Baku Parasetamol
Kadar bahan baku parasetamol ditentukan dengan menggunakan rumus sebagai
berikut:
AUC Std : Luas Area Standart (Baku Pembanding)
[Sp] : Konsentrasi Sampel
[St] : Konsentrasi Standart
Kst : Kadar Standart (Baku Pembanding)
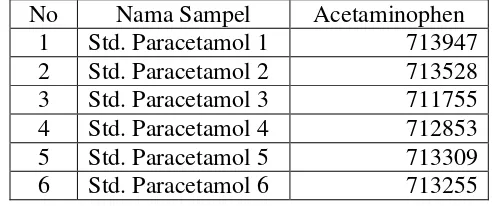
Tabel Luas Area Standart (Baku Pembanding)
No Nama Sampel Acetaminophen 1 Std. Paracetamol 1 713947
Luas area yang digunakan adalah luas area dari hasil rata-rata 6 kali pengukuran:
= 713947 + 713528 + 711755 + 712853 + 713309 + 713255 6
= 3565794 6
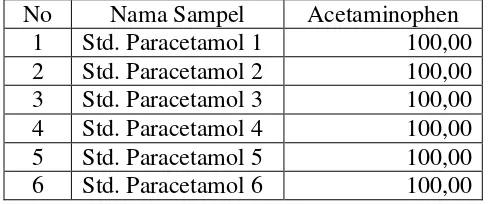
Tabel Kadar Larutan Standart (Baku Pembanding)
No Nama Sampel Acetaminophen 1 Std. Paracetamol 1 100,00
Rata-rata dari kadar larutan standart (Kst):
= 100 + 100 + 100 + 100 + 100 + 100
Luas Area Standart (AUC Std) adalah 713108 dan Kadar Standart (Kst) adalah
100,00 %. Pengukuran dilakukan dua kali dalam waktu yang berdekatan (duplo),
jadi Luas Area Sampel (AUC Sp) yang digunakan adalah:
Tabel Luas Area Bahan Baku Parasetamol
No Nama Sampel Acetaminophen
[St] = 50,00 100 ×
1
50= 0,01
Oleh sebab itu [Sp] = [St]. Maka rumus yang digunakan pada penetapan kadar
bahan baku parasetamol adalah:
Kadar = AUC Sp AUC Std× Kst
Kadar masing-masing Bahan Baku adalah sebagai berikut:
Kadar 1 = AUC Sp
Hasil penetapan kadar bahan baku parasetamol disajikan dalam bentuk tabel
dibawah ini.
Tabel Kadar Bahan Baku Parasetamol
No Nama Sampel Acetaminophen
1 Bahan Baku 1 100,43%
2 Bahan Baku 2 100,50%
Lampiran 2. Hasil Print Out HPLC