HUBUNGAN DEFISIENSI GLUKOSA 6 FOSFAT
DEHIDROGENASE (G6PD) DENGAN
INFEKSI MALARIA PADA
POPULASI NIAS DI KOTA
MEDAN
TESIS
Oleh
MUTIARA INDAH SARI
047008004/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
MEDAN
2008
Mutiara Indah Sari : Hubungan Defisiensi Glukosa 6 Fosfat Dehidrogenase (G6pd) Dengan Infeksi Malaria Pada Populasi Nias Di Kota Medan, 2008
HUBUNGAN DEFISIENSI GLUKOSA 6 FOSFAT
DEHIDROGENASE (G6PD) DENGAN
INFEKSI MALARIA PADA
POPULASI NIAS DI KOTA
MEDAN
TESIS
Untuk Memperoleh Gelar Magister Sains dalam Program Studi Biomedik
pada Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
MUTIARA INDAH SARI
047008004/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
Judul Tesis : HUBUNGAN DEFISIENSI
GLUKOSA 6 FOSFAT DEHIDROGENASE (G6PD) DENGAN INFEKSI MALARIA PADA
POPULASI NIAS DI KOTA MEDAN Nama Mahasiswa : Mutiara Indah Sari
Nomor Pokok : 047008004 Program Studi : Biomedik
Menyetujui Komisi Pembimbing
(Dr. Yahwardiah S, PhD) (Prof. Dr. Azmi S Kar, SpPD-KH) Ketua Anggota
Ketua Program Studi, Direktur,
(Dr. Yahwardiah S, PhD) (Prof. Dr. Ir. T. Chairun Nisa B, M.Sc)
Telah diuji pada
Tanggal, 30 Oktober 2008
PANITIA PENGUJI TESIS
Ketua : Dr. Yahwardiah S, PhD
Anggota : 1. Prof. Dr. Azmi S Kar, SpPD-KH
ABSTRAK
Seleksi natural terhadap infeksi malaria ditemukan berhubungan dengan defisiensi enzim glukosa 6 fosfat dehidrogenase(G6PD). Penemuan ini masih kontroversial. Penelitian ini dilakukan untuk melihat adanya hubungan defisiensi enzim glukosa 6 fosfat dehidrogenase dengan infeksi malaria pada populasi Nias di kota Medan. Metode: Penelitian ini dilakukan secara cross sectional study terhadap populasi Nias yang berada di kota Medan, laki-laki berumur 18-55 tahun.
Kriteria inklusi adalah populasi penelitian berasal dari salah satu daerah endemik malaria di Nias. Dilakukan pemeriksaan aktifitas enzim G6PD sel eritrosit, konsentrasi Hb dan anamnesa riwayat infeksi malaria. Test yang digunakan uji Kolmogorov-Smirnov dan uji koefisien korelasi pearson (r) dengan program komputer SPSS 12
Hasil: Hubungan defisiensi G6PD dengan infeksi malaria dengan uji Kolmogorov-Smirnov, didapati nilai p=0.692 (p>0,05) dan uji korelasi aktifitas G6PD dengan konsentrasi Hb dengan koefisien korelasi Pearson (r) didapati nilai r = -0.105, p = 0.560.
Kesimpulan: Tidak terdapat hubungan antara defisiensi G6PD dengan infeksi malaria pada populasi ini dan tidak ada korelasi antara aktifitas G6PD dengan konsentrasi Hb.
ABSTRACT
Natural Selection for malaria infection has been found to relate to glucose 6 phosphate dehydrogenase (G6Pd) deficiency. These findings however, are controversial. The aim of the present research is to test the association of G6Pd deficiency with malaria infection of a population of Nias in Medan.
Methods: The the research is a cross sectional study of a population Nias men living in Medan, 18-55 years of age.This population come from one of the endemic malaria areas of Nias. The activity of G6Pd erythrocytes was tested, as well as the Hb concentration and the patient history of malaria infection.
The Kolmogorov-Smirnov test and the Pearson correlation coefficient test (r) were evaluated with the SPSS 12 program.
Results: The Kolmogorov-Smirnov test result for the association of G6Pd deficiency and malaria infection was p=0.692 ( p>0,05). The Pearson correlation coefficient for the correlation of G6Pd and Hb concentration was r = - 0.105, p = 0.560
Conclusion: No significant association of G6Pd deficiency and malaria infection, nor G6Pd and Hb concentration was found in this population
KATA PENGANTAR
Puji dan syukur atas kehadirat Allah SWT karena atas berkat dan rahmatNya penulis dapat menyelesaikan penelitian tesis dengan judul Hubungan defisiensi enzim glukosa 6 fosfat dehidrogenase (G6PD) dengan infeksi malaria pada populasi Nias di kota Medan. Tesis ini merupakan salah satu syarat yang harus dilaksanakan penulis dalam rangka memenuhi persyaratan untuk meraih gelar Magister pada Sekolah Pascasarjana Universitas Sumatera Utara.
Dengan selesainya tesis ini perkenankanlah penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
Rektor Universitas Sumatera Utara, Prof. Chairuddin P. Lubis, DTM&H, Sp.A(K) dan seluruh jajarannya yang telah memberikan kesempatan pada penulis untuk mengikuti pendidikan di Sekolah Pascasarjana USU Medan.
Direktur Sekolah Pascasarjana USU Medan, Prof. Dr. Ir. T. Chairun Nisa B, M.Sc atas kesempatan yang diberikan kepada penulis untuk mengikuti pendidikan Program Magister di Sekolah Pascasarjana USU Medan.
Dekan Fakultas Kedokteran Universitas Sumatera Utara, Prof. dr. Gontar Siregar, SpPD, KGEH yang telah memberikan izin dan memfasilitasi penulis untuk mengikuti pendidikan magister di Sekolah Pascasarjana USU Medan.
dr. Yahwardiah Siregar, Ph.D (Ketua Program Studi Ilmu Biomedik dan sekaligus ketua komisi pembimbing), Prof. Dr. Azmi S Kar, SpPD-KH (sebagai anggota komisi pembimbing), atas semangat, bimbingan, dan dorongan yang diberikan untuk mengikuti dan menyelesaikan pendidikan program magíster di Sekolah Pascasarjana USU Medan.
Terima kasih yang tidak terhingga disampaikan kepada semua dosen yang telah membimbing dan membagi ilmu kepada penulis selama mengikuti program magister ini.
Ucapan terima kasih yang tulus dan bakti penulis sampaikan kepada kedua orang tua, ayahanda Amir Hamzah Hutagalung dan ibunda Mardianis, mertua saya, ayahanda Suhandoko dan ibunda Maisarah serta seluruh keluarga yang telah memberikan dukungan moril dan materil selama penulis menjalani pendidikan di Sekolah Pascasarjana.
Kepada suamiku tercinta, Dr. Dadik Wahyu Wijaya, SpAn, yang dengan penuh cinta kasih, semangat dan kesabaran yang terus memotivasi penulis dalam menyelesaikan penelitian dan pendidikan penulis.
Kepada seluruh pihak yang telah membantu selama penulis mengikuti pendidikan ini tak lupa penulis sampaikan rasa terima kasih yang tidak terhingga. Akhirnya penulis menyadari bahwa hasil penelitian ini masih jauh dari kesempurnaan. Oleh karena itu penulis berharap kritik dan saran yang membangun demi perbaikan tesis ini. Semoga tesis ini dapat bermanfaat bagi kita.
Medan, 20 Oktober 2008
Penulis,
RIWAYAT HIDUP
Data Pribadi:
Nama Lengkap : Dr. Mutiara Indah Sari
NIP : 132 296 973
Tempat/ Tanggal Lahir : Medan, 15 Oktober 1973 Pangkat/ golongan : Asisten ahli/ III b
Jabatan : Staf Biokimia FK USU
Agama : Islam
Alamat : Jl. Garuda No. 79 A Medan
Telp. : 061-8457487
Email : muthi_indah@yahoo.com Riwayat Pendidikan:
- S-1 Fakultas Kedokteran USU Tahun 1996
- Tamat dokter Tahun 1998
- S-2 PPS USU Tahun 2004 – sekarang
Riwayat Pekerjaan:
DAFTAR ISI
Halaman
ABSTRAK...i
ABSTRACT...ii
KATA PENGANTAR...iii
RIWAYAT HIDUP...v
DAFTAR ISI ...vi
DAFTAR TABEL...ix
DAFTAR GAMBAR...x
DAFTAR LAMPIRAN...xii
BAB I PENDAHULUAN...1
1. Latar Belakang...1
2. Perumusan Masalah...4
3. Kerangka Teori...4
4. Tujuan Penelitian...6
5. Hipotesis...6
6. Manfaat Penelitian...6
BAB II TINJAUAN PUSTAKA...7
1. Malaria...7
1.1. Distribusi daerah endemik malaria...7
1.2. Patofisiologi penyakit malaria...8
1.3. Manifestasi klinik penyakit malaria...10
2.1. Definisi...11
2.2. Biomolekul enzim G6PD...11
2.3. Mutasi gen G6PD...12
2.4. Klasifikasi varian G6PD...13
2.5. G6PD dan lintasan pentosa fosfat...14
2.6. Patofisiologi defisiensi G6PD pada eritrosit...17
2.7. Manifestasi klinik defisiensi G6PD pada eritrosit...19
2.8. Distribusi populasi defisiensi G6PD...20
3. Defisiensi G6PD dan Malaria...20
BAB III METODOLOGI PENELITIAN...22
1. Desain Penelitian...22
2. Tempat Penelitian...22
3. Populasi Penelitian...22
4. Sampel Penelitian...22
5. Pelaksanaan Penelitian...24
6. Prosedur Pemeriksaan ...24
7. Analisa Data ...28
BAB IV. HASIL DAN PEMBAHASAN...30
1. Hasil...30
A. Karakteristik Peserta Penelitian ...30
B. G6PD...31
C. Nilai Hb dan RBC ...34
D. Korelasi Aktifitas G6PD dengan Umur...38
E. Riwayat Penyakit ...39
F. Hubungan G6PD dan Malaria………...40
G. Defisiensi G6PD dan Riwayat Anemia...41
BAB V KESIMPULAN DAN SARAN...49
1. Kesimpulan...49
2. Saran...50
DAFTAR TABEL
Nomor Judul Halaman
1. Klasifikasi Varian Enzim G6PD...14
2. Distribusi Subjek Penelitian Berdasarkan Umur...30
3. Data statistik distribusi aktifitas G6PD pada sampel penelitian...31
4. Distribusi G6PD Normal dan Defisiensi...33
5. Distribusi Statistik Hb dan RBC...34
6. Uji Korelasi Aktifitas G6PD dan Hb...35
7. Uji Korelasi Aktifitas G6PD dan Nilai RBC...36
8. Distribusi Statistik Hb dan RBC pada G6PD Normal dan Defisiensi...37
9. Uji Korelasi Aktifitas G6PD dan Umur...38
10. Distribusi Riwayat Penyakit Peserta Penelitian……….39
11. Distribusi Aktifitas G6PD Normal dan Defisiensi dengan Riwayat Penyakit Malaria...40
DAFTAR GAMBAR
Nomor Judul Halaman
1. Bagan Kerangka teori hubungan defisiensi G6PD dan infeksi malaria ...5
2. Distribusi Daerah Endemik Malaria di Dunia Tahun 2003 ...7
3. Siklus hidup plasmodium ...10
4. Molekul G6PD ...11
5. Pola Penurunan Kelainan Gen Resesif Terangkai Kromosom X pada Penderita Defisiensi G6PD ...13
6. Lintasan Pentosa Fosfat ...15
7. NADPH dalam Reaksi Reduksi Glutation ...16
8. Patofisiologi Defisiensi G6PD pada Eritrosit ...17
9. Gambaran Heinz body pada Eritrosit ...18
10.Distribusi Populasi G6PD ...20
11.Kerangka Kerja Penelitian...29
12.Distribusi Peserta Penelitian Berdasarkan Umur...31
13.Distribusi Aktifitas G6PD...32
14.Frekuensi G6PD Normal dan Defisiensi...33
15.Karakteristik aktifitas G6PD Normal dan Defisiensi...34
16.Distribusi Hb...35
17.Distribusi RBC...35
19.Scater Plot Aktifitas G6PD dan RBC...37
20.Scater Plot Aktifitas G6PD dan Umur...38
21.Distribusi Riwayat Penyakit Peserta Penelitian...40
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Daftar Data Sampel Penelitian ...56
2. Lampiran Penjelasan Tentang Penelitian Kepada Awam ... ...59
3. Surat Persetujuan Ikut Penelitian (Lembar Wawancara 1) ...61
4. Lembar Wawancara...63
BAB I
PENDAHULUAN
1. Latar Belakang
Penyakit malaria adalah penyakit yang disebabkan oleh parasit
Plasmodium dan manusia dapat terinfeksi oleh Plasmodium ini melalui gigitan nyamuk Anopheles, yang melepaskan Plasmodium dari dalam salivanya sewaktu menggigit manusia. Plasmodium memasuki sel-sel hepatosit, dan kemudian melalui sirkulasi darah akan memasuki sel-sel eritrosit. Di dalam sel-sel eritrosit plasmodium selanjutnya berreplikasi. Replikasi ini merangsang sitolisis sel eritrosit dan menyebabkan lepasnya hasil metabolisme Plasmodium yang bersifat toksis ke sirkulasi darah. Hal ini mencetuskan sejumlah gejala klinik yang ringan sampai berat yang dapat menyebabkan kematian (Farmedia, 2005).
Di Nias, salah satu kabupaten di Propinsi Sumatera Utara, malaria merupakan masalah kesehatan yang penting. Kasus malaria di daerah ini dilaporkan cukup tinggi. Dari 27,448 kasus malaria yang ditemukan di Sumatera Utara sepanjang tahun 2005, 14,868 kasus berasal dari daerah Nias (Dinkes, 2005).
Seleksi natural terhadap infeksi malaria ditemukan berhubungan dengan defisiensi enzim glukosa 6 fosfat dehidrogenase (Glucose 6 Phosphate Dehydrogenase/ G6PD) (Tishkoff et al., 2001, Saunders et al., 2002, Beutler, 1996). Distribusi populasi penderita defisiensi G6PD banyak ditemukan pada populasi di daerah endemik malaria. Peninggian angka kejadian defisiensi G6PD di daerah endemik malaria ini menjelaskan teori hubungan defisiensi G6PD dengan infeksi malaria.Pada penderita defisiensi G6PD variant A- di daerah Afrika Timur dan Afrika Barat, didapati penurunan resiko terinfeksi malaria (Ruwende et al., 1995, Ruwende, 1998 ). Ini memberi kesan bahwa defisiensi tersebut menguntungkan pada keadaan lingkungan tertentu. Sebagai salah satu daerah endemik malaria, kemungkinan prevalensi penderita defisiensi G6PD di Indonesia adalah tinggi. Diperkirakan 2-6 % dari populasi di Indonesia sebagai carriers (Beutler, 1996).
pemberian obat-obatan tertentu, infeksi tertentu, diabetes asidosis dan memakan kacang fava (Frank, 2005)
Enzim G6PD berperan sebagai enzim utama pada lintasan pentosa fosfat (PMP shunt), yang menghasilkan ekuivalen pereduksi NADPH.Pada sel eritrosit, lintasan pentosa fosfat merupakan satu-satunya lintasan yang menghasilkan NADPH. NADPH berperan dalam reaksi reduksi disulfida dari glutation (GSSG) menjadi bentuk sulfhidril (GSH), suatu anti oksidan (Murray et al., 2000 ). Kurangnya pembentukan NADPH pada sel eritrosit defisiensi G6PD menyebabkan lingkungan sel eritrosit bersifat oksidatif oleh karena glutathione tidak tereduksi. Parasit
Plasmodium di duga rentan terhadap lingkungan sel eritrosit yang bersifat oksidatif (Kamchonwongoaisan et al., 1989 ).
Walaupun beberapa penelitian terdahulu menunjukkan penurunanan angka resiko terinfeksi malaria pada penderita defisiensi G6PD (Ruwende et al., 1995, Mockenhaupt et al., 2003), hubungan defisiensi G6PD dengan infeksi malaria masih menimbulkan kontroversi. Penelitian yang dilakukan pada daerah endemik malaria di Myamar dan Indonesia menunjukkan hasil tidak adanya hubungan antara defisiensi G6PD dan infeksi malaria. (Jalloh et al., 2004 ).
2. Perumusan Masalah
Telah dijelaskan di atas bahwa seleksi natural terhadap infeksi malaria dapat ditemukan pada penderita defisiensi G6PD. Pada penderita defisiensi G6PD ini diketahui terdapat penurunan resiko terinfeksi malaria.
Parasit malaria diduga tidak dapat hidup di lingkungan sel eritrosit penderita yang bersifat oksidatif akibat kurangnya pembentukan NADPH. Walaupun peninggian angka kejadian defisiensi G6PD di daerah endemik malaria mendukung teori hubungan defisiensi G6PD dengan infeksi malaria, beberapa penelitian mengenai menunjukkan hasil yang berbeda. Berdasarkan hal-hal tersebut, maka masalah dalam penelitian ini adalah bagaimana hubungan defisiensi G6PD dengan infeksi malaria pada populasi Nias di kota Medan.
3. Kerangka Teori
Ini karena di dalam sel eritrosit satu-satunya jalan untuk pembentukan NADPH adalah melalui lintasan pentosa fosfat.
Didapati penurunan resiko terinfeksi malaria pada penderita defisensi G6PD di daerah endemik malaria.
NADP GSH H2O2
NADPH GSSG H2O+O2
- defect membran eritosit - hemoglobin yang abnormal
- kerusakan autoimun eritrosit
- hypersplenism
Stress Oksidatif Lisis eritrosit Defisiensi G6PD
- anemia hemolitik akut
- anemia
hemolitik kronik non spherositik - hiperbilirubinemia neonatus - dll Tidak terinfeksi malaria Endemik malaria Mutasi Gen G6PD
4. Tujuan Penelitian
Tujuan umum penelitian ini adalah untuk mengetahui hubungan defisiensi G6PD dengan infeksi malaria pada populasi Nias di kota Medan.
Tujuan khusus penelitian ini adalah untuk:
1. Mengetahui gambaran aktifitas G6PD pada populasi penelitian
2. Mengetahui frekuensi penderita defisiensi G6PD pada populasi penelitian 3. Mengetahui korelasi konsentrasi Hb, RBC dan umur dengan aktifitas G6PD
pada populasi tersebut.
4. Mengetahui defisiensi G6PD pada populasi Nias di kota Medan dengan riwayat tidak terinfeksi malaria .
5. Mengetahui defisiensi G6PD dengan riwayat pernah terinfeksi malaria. 6. Mengetahui riwayat anemia pada populasi penelitian
5. Hipotesis
Yang menjadi hipotesis pada penelitian ini adalah ada hubungan antara defisiensi G6PD dengan infeksi malaria.
6. Manfaat Penelitian
Hasil penelitian diharapkan bermanfaat untuk:
1. Dunia pendidikan khususnya bidang kesehatan dan informasi tambahan bagi Dinas Kesehatan
BAB II
TINJAUAN PUSTAKA 1. Malaria
Malaria adalah salah satu penyakit infeksi, penyebab kematian sekitar 1-2 juta penduduk dunia pertahun terutama di daerah Afrika. Setiap tahun penyakit ini menyerang hampir 300-500 juta penduduk dunia. Manusia terserang penyakit ini akibat terinfeksi parasit Plasmodium yang ditularkan melalui gigitan nyamuk
Anopheles (Farmedia, 2005).
2.1.Distribusi daerah endemik malaria
Gambar 2. Distribusi Daerah Endemik Malaria di Dunia Tahun 2003 (Farmedia, 2005)
Penyakit malaria merupakan penyakit yang endemisitasnya terjadi di daerah tropis dan subtropis. Nyamuk Anopheles sebagai vektor pembawa Plasmodium
dalam penyebaran penyakit ini tidak dapat bertahan hidup di bawah suhu 20°C dan
Penyebaran Plasmodium dapat ditemukan di daerah Afrika Timur, Afrika Sahara, Asia Timur, Papua Nugini, Timur Tengah, Amerika Selatan, yang berhubungan dengan endemisitas malaria (Farmedia, 2005).
Indonesia, sebagai negara tropis yang dilalui garis khatulistiwa yang secara geografis terbentang dari 6°LU – 11°LS dan 95 °BT – 140°BT, endemisitas malaria terjadi hampir di seluruh wilayah Indonesia. Pada tahun 2003, dari 227,5 juta penduduk Indonesia, sekitar 89.8 juta tinggal daerah endemik malaria. Kasus malaria yang dilaporkan sepanjang tahun 2003 ini adalah 175,558 dari 2,898,698 kasus yang mungkin terjadi berdasarkan jumlah pendududuk yang tinggal di daerah endemik tersebut (WHO, 2003).
Nias, merupakan salah satu daerah endemik malaria di Indonesia. Kasus malaria di daerah ini dilaporkan cukup tinggi. Ditemukan 14,868 kasus malaria di daerah Nias sepanjang tahun 2005 (Dinkes, 2005).
1.2. Patofisiologi penyakit malaria
Di dalam sel-sel eritrosit merozoit-merozoit akan berkembang membentuk tropozoit dan berlanjut membentuk skizont. Proses ini berlangsung, secara periodik dan juga menyebakan pecahnya sel-sel eitrosit.
Gambar 3. Siklus Hidup Plasmodium
1.3. Manisfestasi klinik penyakit malaria
Gejala klinik malaria adalah (Farmedia, 2005) : 1. Demam
2. Berkeringat 3. Menggigil 4. Nyeri sendi 5. Muntah 6. Anemia 7. Splenomegali
2. Defisiensi G6PD
2.1. Definisi
Kelainan yang bersifat diturunkan dan terangkai kromosom X akibat mutasi
yang terjadi pada struktur tertier gen G6PD yang menurunkan aktivitas enzim, akibat penurunan kestabilan enzim dan kemampuannya berikatan dengan substrat
(Naylor et al., 1996).
2.2. Biomolekul enzim G6PD
Enzim G6PD (EC, 1.1.1.49) merupakan suatu protein monomer yang terdiri dari 516 asam amino, dengan BM 59,256 kD. Bentuk aktif enzim ini adalah suatu dimer yang mengikat kuat NADP. Sequencing dari gen ini telah diketahui pada sejumlah spesies termasuk pada manusia. Gen yang mengkode enzim glukosa 6 fosfat dehidrogenase ini terletak di daerah distal kromosom X (Xq28).
2.3. Mutasi gen G6PD
Mutasi pada gen G6PD menyebabkan perubahan sifat kinetika dari enzim G6PD, disebabkan pertukaran asam amino yang membentuk struktur tertier, tempat katalitik enzim untuk berikatan dengan substrat. Terjadi penurunan aktifitas katalitik enzim, penurunan stabilitas dan perubahan aktifitas untuk mengikat NADP, NADPH dan glukosa 6 fosfat. Perbedaan mutasi pada gen G6PD menyebabkan perbedaan tingkat defisiensi enzim. Jenis mutasi yang terjadi seluruhnya merupakan jenis mutasi noktah dan kebanyakan adalah mutasi noktah missense
yang dijumpai pada kelipatan dari tiga nukleotida (Beutler, 1994).
Gambar 5. Pola Penurunan Kelainan Gen Resesif Terangkai Kromosom X pada Penderita Defisiensi G6PD (Favismus)
2.4.Klasifikasi varian G6PD
Pada tahun 1967, komite di WHO mengusulkan prosedur baku biokimia untuk mengelompokkan varian dari G6PD dengan mengukur aktifitas enzim, Km untuk glukosa 6 fosfat dan NADP, stabilitas enzim terhadap pemanasan, efisiensi penggunaan glukosa 6 fosfat dan NADP, mobilitas elektroforetik dan pH optimun dari enzim.
Tabel 1. Klasifikasi Varian Enzim G6PD
Kelas Tingkat defisiensi dan gejala klinik Residu aktifitas
I Defisiensi enzim yang berat, dengan < 2%
anemia hemolitik kronik non spherositik II Defisiensi enzim yang berat, yang tidak
< 10%
berhubungan dengan anemia hemolitik kronik III Defisiensi enzim ringan sampai sedang, 10-60%
gejala hemolisis terjadi hanya jika ada terpapar obat atau infeksi tertentu
IV Aktifitas enzim normal
60-150%
V Peningkatan aktifitas enzim Di atas normal
2.5.G6PD dan lintasan pentosa fosfat
Enzim G6PD berperan sebagai enzim utama dalam lintasan pentosa fosfat, salah satu lintasan dalam metabolisme karbohidrat. Lintasan ini berlangsung di sitosol semua sel. Lintasan pentosa fosfat disebut juga sebagai lintasan heksosa monofosfat atau lintasan 6 fosfoglukonat, berjalan melalui dua fase yaitu: (McKee and McKee, 2003)
G6PD mengkatalisis reaksi pertama pada fase ini dengan mengoksidasi
G6PD menghasilkan 6 fosfoglukono δ-lakton, dan mereduksi NADP
menjadi NADPH.
6 fosfoglukono δ-lakton dengan cepat terhidrolisis menjadi 6 fosfoglukonat.
6 fosfoglukonat akan mengalami reaksi dekarboksilasi menggunakan koenzim NADP untuk direduksi menghasilkan molekul NADPH. Dalam fase ini dihasilkan 2 molekul NADPH untuk setiap satu molekul glukosa 6 fosfat
2. Fase nonoksidatif yang reversibel
Pada fase ini dihasilkan prekursor ribosa untuk sintesis nukleotida dan asam nukleat
NADPH yang dihasilkan pada lintasan pentosa fosfat ini merupakan koenzim tereduksi yang diperlukan dalam berbagai jalan reaksi dalam sel seperti: (Champe and Harvey, 1994)
1. Berperan dalam berbagai sintesis reduktif pada semua jaringan dimana lintasan pentosa fosfat ini aktif misalnya sintesis asam lemak, hormon steroid dan lain-lain
2. Berperan dalam reaksi yang dikatalisis oleh enzim mikrosom hepar sitokrom P-450 monooksidase.
3. Berperan dalam reaksi reduksi glutathion yang berfungsi sebagai antioksidan yang poten untuk melindungi sel dari kerusakan oksidatif akibat spesies oksigen reaktif (reactive oxygen species/ ROS) hidrogen peroksida (H2O2).
Gambar 7. NADPH dalam Reaksi Reduksi Glutation (Lippicont Williams & Wilkins, 1994)
4. Berperan dalam reaksi yang dikatalisis oleh enzim NADPH oksidase, jalan reaksi untuk menfagositosis mikroorganisme, partikel asing, debris oleh sel neutrofil dan makrofage.
2.6. Patofisiologi defisiensi G6PD pada eritrosit
NADPH yang dihasilkan dalam lintasan pentosa fosfat oleh aktifitas G6PD berperan dalam eritrosit untuk mereduksi bentuk disulfida dari GSSG menjadi bentuk sulfhidril/ GSH melalui reaksi yang dikatalisis oleh enzim glutation reduktase. GSH adalah suatu tripeptida dengan gugus sulfhidril bebas.
Gambar 8. Patofisiologi Defisiensi G6PD pada Eritrosit (Lippicont Williams & Wilkins, 1994)
Stres oksidatif tambahan yang menyebabkan peningkatan H2O2 mengakibatkan turunnya konsentrasi GSH di dalam sel ke tahap tertentu (Johnson et al., 1994). Ini menyebabkan gugus sulfhidril pada beberapa protein yang penting menjadi krisis dan tidak dapat dipertahankan dalam bentuk tereduksi. Terjadi peningkatan kecepatan oksidasi hemoglobin menjadi methemoglobin (Murray et al., 2000 ). Oksidasi ini menyebabkan hemoglobin terdenaturasi dan dilepaskan hemin ke permukaan membran eritrosit (Chiu and Liu, 1997) Hemoglobin yang teroksidasi mengalami pengikatan silang antara satu dengan yang lain oleh ikatan disulfida, menyebabkan terbentuknya suatu jembatan yang selanjutnya dioksidasi membentuk agregat, disebut sebagai badan Heinz (Heinz body) (Berg et al., 2002).
Ditemukannya Heinz body pada sel eritrosit dapat menegakkan diagnosa defisiensi G6PD (Oduola and Olayinka, 2004 ).
Pada apusan darah tepi, gambaran sel eritrosit terlihat seperti digigit (bite cel) atau berbentuk hemiblister.
Gambar 9. Gambaran Heinz body pada Eritrosit
Dengan terbentuknya Heinz body menyebabkan penurunan deformabilitas sel eritrosit (Chiu and Liu, 1997) .Dalam keadaan normal, eritrosit harus mengalami deformasi, menjadi lebih lentur untuk dapat mengalir dalam pembuluh darah yang halus Akibat semua hal ini, membran eritrosit menjadi kaku dan mudah lisis.
2.7. Manifestasi klinik defisiensi G6PD pada eritrosit
Defisiensi G6PD pada eritrosit dapat menimbulkan manisfestasi klinik berupa (Roos et al., 1999, Hundsdoerfer et al., 2002)
1. Anemia hemolitik akut 2. Anemia hemolitik kronik
Anemia hemolitik akut pada defisiensi G6PD dapat dicetuskan oleh stres oksidatif akibat setelah pemberian obat-obatan tertentu, infeksi tertentu dan setelah memakan kacang fava.
Golongan obat yang dapat menimbulkan keadaan anemia hemolisis akut ini seperti antibiotik sulfonamid, antimalaria primaquin dan antipiretik tertentu(Berg et al, 2002, Khan, 2004). Infeksi yang merangsang timbulnya hemolisis pada penderita diantaranya adalah hepatitis virus, pneumonia dan demam thypoid. (Beutler, 1994) Anemia hemolitik kronik non spherositik berhubungan dengan defisiensi G6PD jarang ditemukan dan dapat terjadi tanpa adanya faktor pencetus stress oksidatif.
2.8. Distribusi populasi defisiensi G6PD
Gambar 10. Distribusi Populasi G6PD (WHO, 1989)
3. Defisiensi G6PD dan Malaria
Defisiensi G6PD berhubungan dengan seleksi evolusi oleh infeksi malaria. Di daerah endemik malaria, defisiensi G6PD ini berhubungan dengan pertahanan terhadap infeksi malaria. Ini memberi kesan bahwa defisiensi tersebut menguntungkan pada keadaan lingkungan tertentu.(Beutler, 1996, McKee and McKee, 2003). Orang Persia yang bermigrasi kira-kira 1300 tahun yang lalu dari Iran, ke daerah endemik malaria di Bombay dan Gujrat India, memiliki insiden tinggi terhadap defisiensi G6PD. Sebaliknya insiden defisiensi G6PD rendah pada komunitas yang sama, yang tetap tinggal di Iran (Mohanty et al., 2004)
et al, 1995, Ruwende & Hill, 1998). Pada penelitian yang dilakukan terhadap populasi ibu hamil, didapati penurunan dari 66% terinfeksi malaria pada ibu hamil dengan G6PD normal menjadi 58% terinfeksi malaria pada penderita defisensi G6PD heterozygot dan 50% pada penderita defisiensi G6PD homozygot (Mockenhaupt et al., 2003) .
BAB III
METODOLOGI PENELITIAN 1. Desain Penelitian
Desain yang digunakan pada penelitian ini adalah cross sectional study terhadap populasi Nias yang berada di kota Medan.
2. Tempat Penelitian
Pengambilan sampel dilakukan pada sejumlah subjek penelitian, yaitu
populasi suku Nias yang bertempat tinggal di kota Medan dengan pemeriksaan aktifitas G6PD dilakukan di Laboratorium Spectrum Medan
3. Populasi Penelitian
Populasi penelitian adalah yang berjenis kelamin laki-laki karena laki-laki yang hanya mempunyai satu copy kromosom X akan lebih sering mendapat gangguan akibat kelainan resesif terangkai kromosom X ini dibandingkan perempuan. Populasi juga diambil yang berumur 18-55 tahun karena subjek penelitian berumur diatas 18 tahun sudah bisa menanda tangan informed consent sendiri dan subjek penelitian dibatasi pada umur 55 tahun, karena umur diatas 55 tahun sudah dikelompokkan sebagai tua (aging). Aktifitas enzim menurun pada kelompok ini.
4. Sampel penelitian
Kriteria ini diperoleh dengan metode wawancara dan pengisian kuesioner (Lembar Wawancara 2).
Pada peserta penelitian juga dilakukan anamnesa untuk mengetahui secara garis besar kesehatan subjek.
Kriteria Inklusi :
1. Laki-laki suku Nias yang berasal dari salah satu daerah endemik malaria di Nias yaitu : Awai, Lotu, Alasa, Lagundri, Amandraya, Gomo, Teluk dalam (Dinas Kesehatan Tk 1 Propinsi Sumatera Utara, 2005).
2. Pernah berdomisili atau berkunjung ke daerah endemik malaria paling sedikit selama 3 bulan.
3. Tiga garis keturunan ke atas harus suku Nias asli 4. Bersedia ikut penelitian
Kriteria Eksklusi:
1. Memakan obat-obatan yang dapat mengganggu sistem trombosis selama tiga hari sebelum penelitian
2. Sedang mengalami hemolisis eritrosit
3. Mengalami demam karena infeksi virus dan bakteri akut 4. Pemakai narkoba dengan jarum suntik
5. Mendapat transfusi darah 4 minggu sebelum penelitian berlangsung Besar sampel :
Besar sampel ditentukan dengan menggunakan Program EpiInfo 2000:
Z= confidence level = 95% D=worst acceptable=10%
P= expected frequency=25% (Sopacoa & Kar, 2003) N= jumlah sampel minimal=32
5. Pelaksanaan Penelitian
Kepada semua subjek yang ikut dalam penelitian sebelumnya diterangkan tujuan, prosedur, manfaat, resiko sebagai subjek dalam penelitian dan perasaan yang tidak menyenangkan yang mungkin ada akibat pelaksanaan prosedur penelitian. Kepada semua subjek penelitian dimintakan sewaktu datang untuk pengambilan sampel, untuk membawa rekam medik/ catatan kesehatan jika ada yang berhubungan dengan riwayat demam, malaria, penyakit kurang darah/ anemia. Semua subjek yang setuju ikut dalam penelitian, diminta menanda tangani persetujuan secara tertulis untuk mengikuti penelitian (informed consent).
Lembar Wawancara 1.
6. Prosedur Pemeriksaan
Diambil sampel darah dari semua subjek penelitian, kemudian diperiksa
aktifitas enzim G6PD sel eritrosit dan konsentrasi Hb untuk menentukan aktifitas G6PD dan defisensi G6PD.
Dengan menggunakan lembar wawancara 2, di anamnesa riwayat infeksi malaria pada subjek penelitian untuk mendapat kelompok penelitian yang pernah terinfeksi malaria, dan kelompok yang tidak pernah terinfeksi malaria.
Prinsip:
Aktifitas enzim G6PDH ditentukan dengan mengukur terbentuknya NADPH melalui peningkatan absorpsi sinar ultraviolet pada panjang gelombang 340 nm dengan metode UV spektrofotometer.
G6PDH
G6P + NADP 6 Fosfoglukonat + NADPH +H+ Alat :
1. Spuit 3 ml 7. Pipet effendorf 2. Tabung vakum EDTA 3 ml 8. Tips (steril) berbagai ukuran
3. Spektrofotometer 9. Centrifuge
4. Tabung reaksi 10. Waterbath
5. Tabung falcon centrifuge 11.Kulkas
6. Vortex
Reagensia:
A. Kit Glucose 6 Phosphate Dehydrogenase yang terdiri dari 1. Buffer (Triethanolamine Buffer) : 31,7 mmol/l, pH 7,6
EDTA : 3,2 mmol/l 2. NADP : 0.34 mmol/l 3. Glucose 6 phosphate : 0.34 mmol/l
4. Digitonin : 0.58 mmol/l B. NaCl 0,9 %
1. Dilakukan pengambilan 3 ml darah vena, masukkan ke dalam tabung vakum EDTA
2. 0,2 ml darah ini dicuci dengan 2 ml NaCl 0,9 %
3. Kemudian larutan di centrifuge selama 10 menit pada 3000 rpm, ulangi 3x 4. Selanjutnya eritrosit di suspensikan dengan 0,5 ml larutan digitonin
5. Larutan di simpan 15 menit pada suhu +4°C, kemudian di centrifuge
kembali
6. Pengukuran supernatant (haemolysate) dilakukan dalam waktu 2 jam 7. Ke dalam cuvette di pipetkan:
1. Buffer
3,00 ml
2. NADP
0,10 ml
3. Haemolysate
0,05 ml
8. Campur larutan, inkubasi 5 menit pada suhu 25°C, tambahkan Glucose 6
phosphate 0,05 ml
9. Pada panjang gelombang 340 nm baca absorbpsi awal, kemudian absorpsi dibaca kembali setiap 60 detik selama 3 menit.
Perhitungan
Untuk menghitung aktifitas enzim G6PDH menggunakan rumus:
Diukur aktifitas G6PD 3 kali, selisihnya /3*koefisiensi faktor dibg nilai RBC
RBC eritrosit ml
mU eritrosit
mU /10 9 = /
Hb eritrosit ml
mU gHb
mU / = / ×100
Hb= konsentrasin hemoglobin yang ditentukan untuk masing-masing sampel Nilai aktifitas G6PD dalam sel eritrosit normal
=118-144 mU/109 Ery
=6,97-20,5 U/gHb (37°) (Lohr and Waller, 1974)
Defisiensi G6PD = residu aktifitas G6PD < 118 mU/109 Ery atau <6,97-20,5 U/gHb Pemeriksaan Hb
Alat : 1. Tabung reaksi 2. Pipet Sahli
3. Pipet effendorf
4. Tips (steril) 5. Vortex
6. Spektrofotometer
Reagensia : Kit Hb dengan komposisi
1. Potassium Ferricyanide 0,61 mmol/l
2. Potassium Cyanide 0,77 mmol/l 3. Potassium Phosphate 1,03 mmol/l
Cara pemeriksaan:
1. Terhadap 20 μl darah , dicampur dengan anti koagulan EDTA
2. Darah yang mengandung antikoagulan dimaasukkan ke dalam tabung yang telah diisi dengan 5 ml larutan Hb
3. Dibiarkan lebih kurang selama 3 menit pada suhu kamar 4. Absorbsi larutan dibaca pada panjang gelombang 540 nm Nilai Hb: 14-18 g/dl (laki-laki)(Van Kampen and Zijlstra, 1961)
7. Analisa Data
Kerangka Kerja:
Populasi Laki-laki suku Nias di kota Medan
Berasal dari daerah endemik malaria
Pemeriksaan aktifitas G6PD
G6PD l
G6PD defisiensi
Pernah terinfeksi malaria
(
riwayat diagnosa dengan pemeriksaan menggunakan objek glass)
Tidak pernah terinfeksi malaria
Hubungan defisiensi dengan tidak terinfeksi malaria
BAB IV
HASIL DAN PEMBAHASAN 1. Hasil
Telah dilakukan penelitian cross sectional study terhadap 33 sukarelawan laki-laki, berusia antara18 sampai 47 tahun, suku Nias asli tiga garis keturunan ke atas, berasal dari daerah endemik malaria di Nias, pernah tinggal di daerah endemik tersebut lebih selama lebih dari 3 bulan dan saat penelitian berlangsung bertempat tinggal di kota Medan. Seluruh subjek terpilih memenuhi kriteria inklusi, mengikuti penelitian ini dengan sukarela dan menanda tangani pernyataan persetujuan (Informed Concent) setelah dijelaskan tujuan, prosedur dan resiko dari penelitian ini. Penelitian ini telah mendapat persetujuan dari Komite Etik Penelitian Bidang Kesehatan USU.
A. Karakteristik Peserta Penelitian
Dari hasil penelitian dapat dibuat karakteristik subjek penelitian berdasarkan umur sebagai berikut:
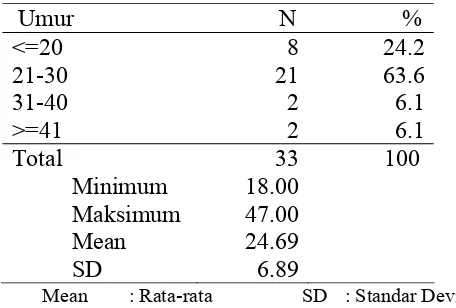
Tabel 2. Distribusi Subjek Penelitian Berdasarkan Umur
Umur N %
<=20 8 24.2
21-30 21 63.6
31-40 2 6.1
>=41 2 6.1
Total
Minimum Maksimum Mean SD
33 18.00 47.00 24.69 6.89
100
[image:47.604.159.387.553.707.2]Pada penelitian ini, subjek penelitian yang terbanyak adalah yang berumur antara 21 sampai 30 tahun yaitu sebanyak 21 orang (63,6 %) , yang paling sedikit pada kelompok umur 31 sampai 40 tahun dan di atas 40 tahun yaitu masing – masing sebanyak 2 orang (6,1 %). Umur subjek penelitian paling muda adalah 18 tahun dan yang paling tua berumur 47 tahun.
<=20 21-30 31-40 >=40 KelUmur 0 10 20 30 40 50 60 70 Pe rcent
Gambar 12. Distribusi Peserta Penelitian Berdasarkan Umur
B. G6PD
1. Karakteristik aktifitas G6PD pada seluruh sampel penelitian
Tabel 3. Data statistik distribusi aktifitas G6PD pada sampel penelitian
Aktifitas G6PD (mU/109 Ery) n: 33 Minimum Maksimum Mean Mean Mode Range
Hasil pemeriksaan aktifitas G6PD dalam satuan mU/109 Ery pada 33 sampel didapatkan, nilai aktifitas G6PD minimum adalah 86,00, aktifitas maksimum 162,00.
Nilai aktifitas rata-rata 124,8, median dan modus 260,00, standart deviasi 19,27 dan perbedaan nilai minimum dan maksimum adalah 76,00. Distribusi aktifitas G6PD terlihat pada grafik 2.
kadar g6pd 160.0 150.0 140.0 130.0 120.0 110.0 100.0 90.0
kadar g6pd
F req ue n c y 10 8 6 4 2 0Std. Dev = 19.27 Mean = 124.8 N = 33.00
Gambar 13. Distribusi Aktifitas G6PD
2. Kriteria G6PD
Tabel 4. Distribusi G6PD Normal dan Defisiensi
Kriteria
G6PD Frekuensi Aktifitas (mU/10
9 Ery)
N % Minimum Maksimum Mean Range SD Varians Defisiensi 11 33.3 86.00 115.00 102.81 29.00 11.42 130.56 Normal 22 66.7 121.00 162.00 135.63 41.00 11.28 127.38
[image:50.604.188.357.558.687.2]Dari hasil penelitian, yang terlihat pada table 4, didapat sampel dengan aktifitas G6PD defisiensi adalah 11 (33,3 %), sedangkan aktifitas G6PD normal terdapat pada 22 (66,7 %) sample. Distribusi aktifitas G6PD defisiensi dalam satuan mU/109 Ery didapatkan nilai terendah adalah 86,00 dan tertinggi adalah 115,00 dengan nilai rata-rata 102,81, standart deviasi 11,42, dan perbedaan nilai minimum dan maksimum adalah 29,00. Distribusi aktifitas G6PD normal dalam satuan mU/109 Ery didapatkan nilai terendah adalah 121,00 dan tertinggi adalah 162,00 dengan nilai rata-rata 135,63, standart deviasi 11,28, dan perbedaan nilai minimum dan maksimum adalah 41,00.
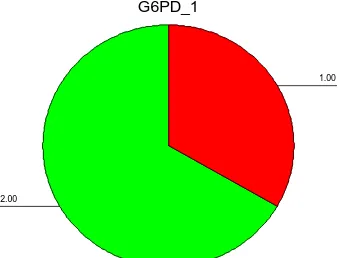
Grafik jumlah kasus dengan aktifitas G6PD Normal dan Defisiensi, serta dsitribusi aktifitas masing-masing kelompok dapat dilihat pada grafik 3 dan 4
G6PD_1
2.00
1.00
0 20 40 60 80 100 120 140 160 180
mU/10E9 Ery
Minimum Maksimum Mean Range SD Varians Karakteristik G6PD
Defisiensi Normal
Gambar 15. Karakteristik aktifitas G6PD Normal dan Defisiensi
C. Nilai Hb dan RBC
1. Distribusi Statistik Hb dan RBC
Tabel 5.Distribusi Statistik Hb dan RBC
Variabel N Minimum Maksimum Mean SD
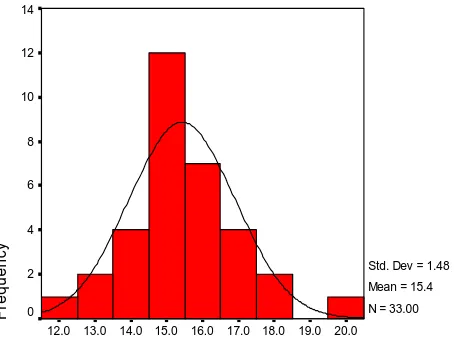
Hb (G/dl) 33 12.40 19.60 15.42 1.48
RBC
(count/ml*109) 33 4.10 6.50 5.13 .49
kadar hb 20.0 19.0 18.0 17.0 16.0 15.0 14.0 13.0 12.0 kadar hb F requenc y 14 12 10 8 6 4 2 0
Std. Dev = 1.48 Mean = 15.4 N = 33.00
Gambar 16. Distribusi Hb
4.00 4.50 5.00 5.50 6.00
RBC(count/ml*10E9) 0 2 4 6 8 10 12 Fr eku en si
Mean = 5.0591 Std. Dev. = 0.43387 N = 22
Gambar 17. Distribusi RBC
2. Korelasi Aktifitas G6PD dengan Hb dan RBC
Tabel 6. Uji Korelasi Aktifitas G6PD dan Hb
Aktifitas G6PD (mU/109 Ery)
Hb (G/dl) KonstG6PD Pearson
Correlation 1 -.105
Sig.
(2-tailed) . .560
[image:52.604.203.439.117.595.2] [image:52.604.209.436.139.318.2]Dari hasil pada table 6, pada penelitian ini didapatkan tidak ada korelasi antara aktifitas G6PD dengan Hb dengan nilai p = 0.560, r = -0.105 (r=koefisien korelasi
pearson)
12.00 14.00 16.00 18.00 20.00
Hb (G/dl) 80.00
100.00 120.00 140.00 160.00
Aktifitas G
6
PD (mU/10E
9
Er
y)
Gambar 18. Scater Plot Aktifitas G6PD dan Hb
Tabel 7. Uji Korelasi Aktifitas G6PD dan Nilai RBC
Aktifitas G6PD (mU/109Ery)
RBC (count/ml*109) KonstG6PD Pearson
Correlation 1 -.109
Sig. (2-tailed) . .544
N 33 33
4.00 4.50 5.00 5.50 6.00 6.50
RBC(count/ml*10E9) 80.00
100.00 120.00 140.00 160.00
Akt
ifit
as G6PD
(
m
U/10E9 Ery)
Gambar 19. Scater Plot Aktifitas G6PD dan RBC
Karakteristik Hb dan RBC pada kelompok aktifitas G6PD Normal dan Defisiensi dapat dilihat pada tabel 8.
Tabel 8. Distribusi Statistik Hb dan RBC pada G6PD Normal dan Defisiensi
Karakteristik Parameter Kriteria
G6PD Minimum Maksimum Mean SD Defisiensi 13.80 19.60 15.90 1.78 Konsentrasi Hb
(G/dl) Normal 12.40 18.00 15.18 1.28
Defisiensi 4.60 6.50 5.30 0.58
RBC
(count/ml*109) Normal 4.10 6.00 5.05 0.43
Hb 18,00, nilai rata-rata 15,18 dan standart deviasi 1,28. Karakteristik RBC dalam satuan count/ml*109 pada kelompok peserta penelitian dengan aktifitas G6PD defisiensi, nilai minimum 4,60, nilai maksimum 6,50 dan rata-rata nilai RBC sampel penelitian ini adalah 5,30, dengan standart deviasi 0,58. Pada Kelompok G6PD normal nilai RBC minimum 4,10, nilai maksimum 6,00 dan nilai rata-rata adalah 5,03, dengan standart deviasi 0,43.
D. Korelasi Aktifitas G6PD dengan Umur
Tabel 9. Uji Korelasi Aktifitas G6PD dan Umur
Aktifitas G6PD
Umur Aktifitas G6PD Pearson
Correlation 1 -.060
Sig. (2-tailed) . .739
N 33 33
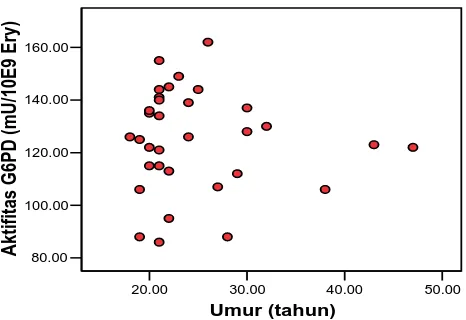
Korelasi aktifitas G6PD dan umur diuji dengan uji korelasi pearson dan didapat bahwa tidak ada hubungan antara aktifitas G6PD dengan umur pada penelitian ini karena didapatkan nilai p = 0.739, r = -0.060 (r=koefisien korelasi pearson)
20.00 30.00 40.00 50.00
Umur (tahun) 80.00
100.00 120.00 140.00 160.00
Aktifitas G6PD
(mU/10E9 Ery)
[image:55.604.160.448.323.396.2] [image:55.604.185.418.540.700.2]E. Riwayat Penyakit
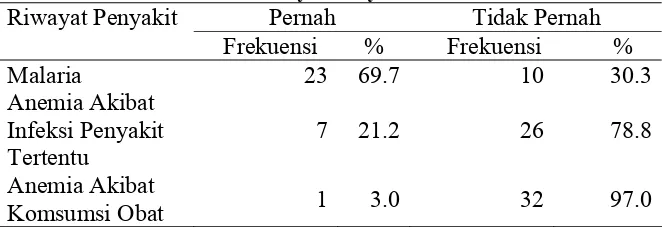
Riwayat penyakit yang pernah diderita pasien diperoleh data sebagai berikut: Tabel 10. Distribusi Riwayat Penyakit Peserta Penelitian
Pernah Tidak Pernah
Riwayat Penyakit
Frekuensi % Frekuensi %
Malaria 23 69.7 10 30.3
Anemia Akibat Infeksi Penyakit Tertentu
7 21.2 26 78.8
Anemia Akibat
Komsumsi Obat 1 3.0 32 97.0
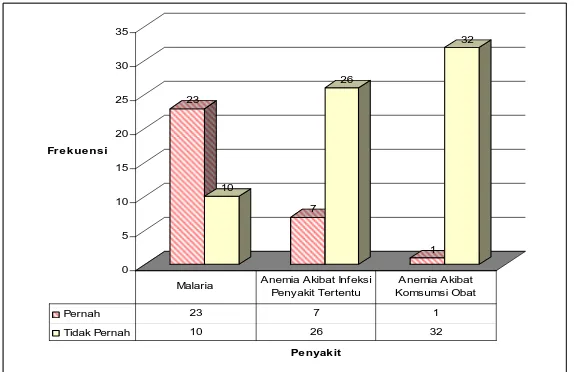
[image:56.604.135.466.182.297.2]23 10 7 26 1 32 0 5 10 15 20 25 30 35
Frek ue nsi
Pe nyak it
Pernah 23 7 1
Tidak Pernah 10 26 32
Malaria Anemia Akibat Infeksi Penyakit Tertentu
Anemia Akibat Komsumsi Obat
Gambar 21. Distribusi Riwayat Penyakit Peserta Penelitian
F. Hubungan G6PD dan Malaria
Pada penelitian ini, jumlah sampel penelitian dengan aktifitas G6PD normal dan defisiensi dengan riwayat pernah terinfeksi malaria dan tidak pernah
terinfeksi malaria dapat dilihat pada tabel 11.
Tabel 11. Distribusi Aktifitas G6PD Normal dan Defisiensi dengan
Riwayat Penyakit Malaria
G6PD Riwayat Malaria
Normal % Defisiensi %
Pernah terinfeksi 14 42.4 9 27.3
Tidak pernah terinfeksi 8 24.3 2 6
[image:57.604.170.457.116.302.2] [image:57.604.135.457.469.527.2]Setelah di uji secara statistik, dengan Kolmogorov-Smirnov Test ditemukan tidak terdapat hubungan antara defisiensi G6PD dengan infeksi malaria pada populasi ini dengan p=0.692 (p>0,05).
14 8 9 2 0 2 4 6 8 10 12 14 Frekuensi
Pernah terinfeksi 14 9
Tidak pernah terinfeksi 8 2 Normal Defisiensi
G6PD
Gambar 22. Aktifitas G6PD Normal dan Defisiensi Dengan Riwayat Malaria
G. Defisiensi G6PD dan Riwayat Anemia
Tabel 12. Distribusi Riwayat Anemia pada Peserta Penelitian dengan Aktifitas G6PD Normal dan Defisiensi
G6PD Riwayat Anemia
Normal Defisiensi Pernah
Akibat Infeksi
Penyakit Tertentu Tidak pernah Pernah Akibat Konsumsi
Obat Tidak pernah
5 17 0 22 2 9 1 10
Riwayat anemia akibat konsumsi pernah dialami oleh 1 orang penderita defisiensi G6PD, sedangkan pada peserta penelitian dengan aktifitas G6PD yang normal hal ini tidak terjadi.
2. Pembahasan
Nilai aktifitas G6PD minimum dalam satuan mU/109 Ery pada 33 sampel penelitian ini adalah 86,00, aktifitas maksimum 162,00, dengan nilai aktifitas
rata-rata 124,69. Aktifitas G6PD normal adalah 118-144 mU/109 Ery, pada suhu 25°C.
(Lohr and Waller, 1974). Penurunan aktifitas G6PD dari nilai normal dapat terjadi akibat mutasi pada gen yang mengkode enzim ini pada struktur tertier gen G6PD yang menurunkan kestabilan enzim dan kemampuannya berikatan dengan substrat sehingga menyebabkan turunnya aktifitas enzim. (Naylor et al., 1996)
Ditemukannya nilai aktiftas G6PD < 118 mU/109 Ery pada subjek penelitian ini, dikategorikan sebagai penyandang defisiensi G6PD. Jumlah sampel dengan aktifitas G6PD defisiensi pada populasi ini adalah 11 (33,3 %), sedangkan aktifitas G6PD normal terdapat pada 22 (66,7 %) sampel. Distribusi aktifitas G6PD defisiensi dalam satuan mU/109 Ery didapatkan nilai terendah adalah 86,00 dan tertinggi adalah 115,00 dengan nilai rata-rata 102,81. Distribusi aktifitas G6PD normal didapatkan nilai terendah adalah 121,00 dan tertinggi adalah 162,00 dengan nilai rata-rata 135,63.
paling banyak ditemukan dan mengenai sekitar 7 % atau lebih dari 400 juta populasi dunia (Beutler, 1996, Frank, 2005).
Walaupun defisiensi G6PD ini bisa terjadi pada pada populasi manapun, defisiensi G6PD banyak ditemukan pada populasi di daerah endemik malaria.
Angka kejadian defisensi G6PD pada populasi penelitian ini lebih tinggi dibandingkan hasil yang dilaporkan penelitian terdahulu menemukan frekuensi penyandang G6PD defisensi pada populasi Nias adalah 25%.(Sopacoa and Kar, 2003). Penelitian di daerah endemik malaria di Flores, didapati 4,4 % penderita defisiensi dari seluruh jumlah subjek yang diperiksa (Matsuoka et al., 2003). Skreening G6PD defisiensi di Maluku Tenggara, salah satu daerah endemik malaria di Indonesia, diperoleh 4.03 % subjek penelitian menderita G6PD defisiensi (Suhartati, 2005).
Tingginya angka kejadian G6PD defisensi pada populasi Nias di kota Medan ini, dimungkinkan karena Nias merupakan salah satu daerah endemik malaria di Indonesia serta seleksi populasi dilakukan pada suku Nias asli, 3 keturunan ke atas.
Pada peserta penelitian ini konsentrasi Hb minimum dalam satuan G/dl
penelitian lain yang juga mendapatkan tidak ada korelasi antara aktifitas G6PD dengan konsentasi Hb dan juga aktifitas G6PD dengan nilai RBC (Muller, 2003). Hasil yang berbeda pada penelitian lain, mendapatkan adanya korelasi yang kuat antara aktifitas G6PD dengan konsentrasi Hb (Jalloh et al., 2004 )
Untuk menghindarkan kesalahan tidak terdiagnosa G6PD defisiensi pada subjek penelitian ini, maka salah satu kriteria eksklusi pada penelitian adalah subjek penelitian sedang mengalami hemolisis eritrosit. Tidak adanya episode hemolitik yang menyebabkan penurunan nilai Hb pada subjek penelitian ini menyebabkan tidak ditemukannya korelasi antara aktifitas G6PD dengan konsentrasi Hb.
Uji korelasi aktifitas G6PD dan umur secara statistik didapat bahwa tidak ada korelasi antara aktifitas G6PD dengan umur pada penelitian ini.
Hal yang sama juga didapatkan pada dua penelitian terdahulu (Erbagci and Yilmac, 2002, Muller, 2003)
Penurunan aktifitas G6PD yang menyebabkan defisiensi dari enzim diketahui akibat terjadinya mutasi pada gen yang menyandi enzim ini. Mutasi yang terjadi menyebabkan perubahan sifat kinetika dari enzim, karena pertukaran asam amino terjadi pada asam amino yang membentuk struktur tertier, sehingga terjadi penurunan aktifitas katalitik, penurunan stabilitas dan perubahan aktifitas untuk mengikat substrat. (Mohanty et al., 2004).
pernah menderita malaria, 10 orang (30,3 %) tidak pernah menderita malaria.Dari 23 orang yang pernah menderita malaria terdapat 14 orang (42,4 %) mempunyai aktifitas G6PD normal dan 9 (27,3 %) orang G6PD defisiensi.
Pada 10 orang subjek penelitian yang tidak pernah menderita malaria, didapat 8 orang (24,3 %) aktifitas G6PD normal dan 2 orang (6 %) aktifitas G6PD defisiensi. Hasil uji secara satistik pada populasi penelitian ini didapatkan tidak ada hubungan antara defisiensi G6PD dengan infeksi malaria. Hasil ini sama dengan dengan hasil penelitian yang di dapat sebelumnya oleh peneliti lain ( Jalloh et al, 2004). Pada penelitian ini, tidak dilakukan pengelompokkan tingkat defisiensi yang diderita subjek penelitian apakah defisiensi yang diderita ringan, sedang atau berat serta tidak dilakukan pemeriksaan gen dari protein enzim untuk penentuan dari varian G6PD (WHO,1989). Kemungkinan jika subjek penelitian mengalami defisiensi G6PD yang ringan, kemampuan untuk bertahan dari infeksi malaria tidak optimal sehingga menjawab mengapa tidak ditemukan adanya hubungan defisiensi G6PD dengan infeksi malaria pada penelitian ini (Tishkoff et al, 2001). Varian dari G6PD juga berperan dalam menentukan hubungan defisiensi G6PD dengan infeksi malaria.
Walaupun riwayat anemia pada subjek penelitian bisa terjadi tanpa berhubungan dengan kelainan G6PD defisiensi-nya, episode anemia hemolitik pada G6PD defisiensi dapat dicetuskan oleh stres oksidatif yang timbul akibat infeksi tertentu ataupun mengkomsumsi makanan dan obat-obatan tertentu.
Pada penelitian pada populasi di daerah Turki, didapatkan adanya riwayat episode anemia hemolitik pada penderita G6PD defisensi (Keskin et al., 2000 ).
Penyakit hepatitis, malaria dan infeksi bakteri diketahui merupakan penyebab anemia pada penderita G6PD defisensi (Sarkar et al., 1993).
Riwayat krisis anemia hemolitik berdasarkan catatan medis yang dapat diterima pada penderita G6PD defisensi juga pernah dilaporkan dari penelitian terdahulu akibat demam tiphoid dan dan demam yang tidak diketahui sebabnya (Gupte et al, 2005).
Infeksi merupakan pencetus episode anemia hemolitik terbanyak pada penderita defisiensi G6PD. Respon inflamasi infeksi menghasilkan pembentukan radikal bebas yang berdifusi ke dalam sel darah merah menyebabkan kerusakan oksidatif (Champe and Harvey, 1994, Frank, 2005). Diperkirakan nitrit oksida mungkin ikut berperan dalam proses ini (Beutler, 1994).
timbul berupa urin menjadi hitam, timbul ikterus dan jumlah hemoglobin mengalami penurunan yang tajam. Pada sejumlah kasus dapat terjadi penghancuran sel darah merah secara besar besaran yang menyebabkan kematian. (Berg et al, 2002).
Pada sejumlah individu dengan defisiensi G6PD, dapat terjadi episode anemia hemolitik setelah memakan kacang fava.
Kerusakan oksidatif pada sel darah merah diduga terjadi melalui senyawa yang dikandungnya yaitu hidroksipirimidin glukosida: vicin, convicin ataupun isouramil. (Frank, 2005). Glukosida-glukosida ini bersifat sebagai pro oksidan setelah dihidrolisis oleh enzim beta glukosidase pada ikatan beta-O-glikosidiknya.
Dari hasil anamnesa, 6 orang (18,2 %) keluarga dari subjek penelitian pernah menderita anemia akibat infeksi penyakit tertentu, yaitu 2 orang (33.3 %)
BAB V
KESIMPULAN DAN SARAN 1. Kesimpulan
Pada penelitian Hubungan Defisiensi G6PD dengan Infeksi Malaria Pada Populasi Nias ini, berdasarkan analisa statistik dan pembahasan dapat disimpulkan bahwa:
a. Karakteristik aktifitas G6PD dalam satuan mUx10E9 Ery adalah pada rentang aktifitas 86,00, sampai 162,00, dengan nilai aktifitas rata-rata 124,69.
b. Frekuensi defisiensi G6PD pada populasi Nias 33,3 %. Hal ini menunjukkan tingginya angka kejadian kelainan yang bersifat diturunkan ini pada populasi Nias.
c. Tidak ditemukan adanya korelasi antara aktifitas G6PD konsentrasi Hb d. Tidak ditemukan adanya korelasi antara aktifitas G6PD dan nilai RBC e. Aktifitas G6PD tidak berkorelasi dengan umur secara statistik
f. Tidak ada hubungan antara defisiensi G6PD dengan infeksi malaria pada populasi Nias.
2. Saran
Dianjurkan untuk melakukan penelitian ini dengan jumlah sampel yang lebih besar dan defisensi G6PD ditegakkan dengan pemeriksaan genetik untuk melihat mutasi gen (varian) pada enzim G6PD tersebut. Dengan sampel yang lebih besar dan pemeriksaan gen dari G6PD dapat dilakukan pengelompokkan defisiensi G6PD ringan, sedang atau berat serta klasifikasi varian defisensi G6PD .
DAFTAR PUSTAKA
AINOON, O., YU, Y. H., MUHRIZ, A. L. A., BOO, N. Y., CHEONG, S. K. & HAMIDAH, N. H. (2003) Glucose-6-phosphate dehydrogenase (G6PD) variants in Malaysian Malays. Hum Mutat (Online), 21, 101-9.
BERG, J., TYMOCZKA, J. & STRYER, L. (2002) The Calvin Cycle and the Pentose Phosphate Pathway In: Biochemistry, New York, W.H Freeman and Company.Americas.
BEUTLER, E. (1994) G6PD Deficiency. Blood, 84, 3613-36.
BEUTLER, E. (1996) G6PD: population genetics and clinical manifestations.
Blood Review, 10, 45-52.
CHAMPE, P. C. & HARVEY, R. A. (1994) Hexose monophosphate pathway In:Biochemistry, Philadephia, Lippicont Williams & Wilkins.
CHIU, D. T. & LIU, T. Z. (1997) Free radical and oxidative damage in human blood cells. J Biomed, 4, 256-9.
DINKES (2005) Profil Kesehatan. Dinas Kesehatan Tk I Propinsi Sumatera Utara. ENCYCLOPEDIA (2005) Glucose 6 phosphate dehydrogenase-image.
laborlawtalk.
ERBAGCI, A. B. & YILMAC, N. (2002) Erythrocyte glucose-6-phosphate dehydrogenase deficiency in Gaziantep, turkey. Eastern Journal of Medicine, 7, 15-8.
FARMEDIA (2005) Malaria Update (from basic science to clinical practice). FAVISMUS Favismus image.
FRANK, J. E. (2005) Diagnosis and management of G6PD deficiency. Am Fam Physician, 72, 1277-82.
HUNDSDOERFER, P., VETTER, B. & KULOZIK, A. (2002) Chronic haemolytic anaemia and glucose-6-phosphate dehydrogenase deficiency. Case report and review of the literature. Acta Haematol. , 108, 102-5.
JALLOH, A., TANTULAR, I. S., PUSARAWATI, S., KAWILARANG, A. P., KERONG, H., LIN, K., FEREIRA, M. U., MATSUOKA, H., ARAI, M., KITA, K. & KAWAMOTO, F. (2004 ) Rapid epidemiologic assessment of glucose-6phosphate dehydrogenase deficiency in malaria-endemic areas in Southeast Asia using a novel diagnostic kit Tropical Medicine and
International Health 9, 615-25.
JOHNSON, R. M., RAVINDRANATH, Y., EL-ALFI, M. & GOYETTE, G.-J. (1994 ) Oxidant damage to erythrocyte membrane in of glucose-6-phosphate dehydrogenase deficiency: Correlation with in vivo reduced glutathione concentration and membrane protein oxidation. Blood, 83,
1117-1123.
KAMCHONWONGOAISAN, S., BUNYARATVEJ, A., WANACHIWANAWIN, W. & YUTHAVONG, Y. (1989 ) Susceptibility to hydrogen peroxide of Plasmodium falciparum infecting glucose-6-phosphate dehydrogenase-deficiencient erythrocytes. Parasitology 99, 171-4.
KAPLAN, M., BEUTLER, E., VREMAN, H. J., HAMMERMAN, C., LEVY-LAHAD, E., RENBAUM, P. & STEVENSON, D. K. (1999) Neonatal hyperbilirubinemia in glucose-6-phosphate dehydrogenase deficiency heterozygotes. Pediatrics 104, 68-74
KESKIN, N., OZDES, I., KESKIN, A., ACIKBAS, I. & BAGCI, H. (2000 ) Incidence and molecular analysis of glucose-6-phosphate dehydrogenase deficiency in the province of Denizli, Turkey. Med Sci Monit, 8, 453-6. KHAN, M. (2004) Glucose 6 phosphate dehydrogenase deficiency in adult. J Coll
Physicians Surg Pak, 14 400-3.
LOHR, G. W. & WALLER, H. D. (1974) Glucose-6-phosphate dehydrogenase. Methods of enzymatic analysis, Wehnheim, Varlag Chemie.
MCKEE, T. & MCKEE, J. R. (2003) Carbohydrate metabolism In: The molecular basis of Life, New York, McGraw-Hill. Americas.
MOCKENHAUPT, F. P., MANDELKOW, J., TILL, H., EHRHARDT, S., EGGELTE, T. A. & BIENZLE, U. (2003) Reduced prevalence of
Plasmodium falciparum infection and of concomitant anaemia in pregnant women with heterozygous G6PD deficiency. Tropical Medicine and International Health 8, 118-24.
MOHANTY, D., MUKHERJEE, M. B. & COLAH, R. B. (2004) Glucose-6-phosphate dehydrogenase deficiency in India. . India J Pediatr, 71, 525-9. MULLER, R. (2003) Use of a simplified spectrophotometric method for
quantitative determination of glucose-6-phosphate dehydrogenase activity in normal children from two day-care centers of the city of Sao Paulo.
Einstein, 1, 89-94.
MURRAY, R. K., GRANNER, D. K., MAYES, P. A. & RODWELL, V. W. (2000 ) The pentose phosphate pathway and other pathways of hexose metabolism In:Harper’s Biochemistry, New York, Appleton & Lange. America.
NAYLOR, C. E., ROWLAND, P., BASAK, A. K., MASON, P. J., BAUTISTA, J. M., VULLIAMY, T. J., LUZZATTO, L. & ADAMS, M. J. (1996) Glucose-6-phosphate dehydrogenase mutations causing enzyme deficiency in a model of the tertiary structure of the human enzyme. Blood, 7, 2974-82. NUCHPRAYOON, I., SANPAVAT, S. & NUCHPARYOON, S. (2002)
Glucose-6-phosphate dehydrogenase mutations in Thailand: G6PD Viangchan is the most common deficient variant in the Thai population. Hum Mutat (Online),
19 185-90.
ODUOLA, T. & OLAYINKA, A. A. (2004 ) Heinz body demonstration for glucose-6-phosphate-dehydrogenase (G6PD) screening; Our experience at Ife, Nigeria. Journal of Medical Laboratory Science, 13 45-7.
RUWENDE, C., KHOO, S. C., SNOW, A. W., YATES, S. N. R.,
KWIATKOWSKI, D., GUPTA, S., WARN, P., CEM, A., GILBERT, S. C., PESCHU, N., NEWBOLD, C. I., GREENWOOD, B. M., MARSH, K. & HILL, A. V. S. (1995) Natural-selection of hemizygotes and heterozygotes for G6PD deficiency in Africa by resistance to severe malaria. Nature 376,
246-9.
RUWENDE, C. H., A. (1998 ) Glucose 6 phosphate dehydrogenase and malaria. J Mol Med 76, 581-8.
SARKAR, S., PRAKASH, D., MARWAHA, R. K., GAREWAL, G., KUMAR, L., SINGH, S. & WADIA, B. N. (1993) Acute intravascular hemolysis in glucose 6-phosphate dehydrogenase deficiency. J Trop Pediatr 38, 139-40. SAUNDERS, M. A., HAMMER, M. F. & NACHMAN, M. W. (2002) Nucleotide
variability at G6pd and the signature of malarial selection in humans.
Genetics, 162:, 1849-61,62.
SOPACOA, E. & KAR, A. S. (2003) Prevalensi G6PD pada suku Nias KOPAPDI
Menado
SUHARTATI (2005) Analisa gen penyandi defisiensi glukosa 6 fosfat
dehidrogenase (G6PD) pada daerah endemic malaria di kepulauan Maluku Tenggara. Airlangga University Library.
TANTULAR, I. S., IWAI, K., LIN, K., BASUKI, S., HORIE, T., HTAY, H. H., MATSUOKA, H., MARWOTO, H., WONGSRICHANALAI, C., DACHLAN, Y. P., KOJIMA, S., ISHII, A. & KAWAMOTO, F. (1999) Field trials of a rapid test for G6PD deficiency in combination with a rapid diagnosis of malaria. Tropical Medicine and International Health, 4, 245-50.
TIAN, W., BRAUNSTEIN, L. D., APSE, K., PANG, J., ROSE, M. & TIAN, X. (1999) Importance of of glucose-6-phosphate dehydrogenase activity in cell death. Am J Physiol Cell Physiol, 276, 1121-31.
TISHKOFF, S. A., VARKONYI, R., CAHINHINAN, N., ABBES, S.,
ARGYROPOULOS, G. & DESTRO-BISOL, G. (2001) Haplotype diversity and linkage disequilibrium at human G6PD: recent origin of alleles that confer malarial resistance Science, 293, 455-462.
WENG, Y. H., CHOU, Y. H. & LIEN, R. I. (2003) Hyperbilirubinemia in healthy neonates with glucose-6-phosphate dehydrogenase deficiency. . Early Human Dev 71, 129-36.
WHO (1989) Glucose-6-phosphate dehydrogenase deficiency Bulletin of the World Health Organization. , 67, 601-11.
WHO (2003) Indonesia-Malaria Situation in SEAR Countries WIKIPEDIA (2006) Nias. Wikipedia, the free encyclopedia.
Lampiran 1. Daftar Data Sampel Penelitian
G6PD Hb RBC NO UMUR
mU/ery perml
mU/109
Ery G/dl count/ml*109
1 21 777.1 141 16.6 5.5
2 22 731.4 113 19.6 6.5
3 21 761.9 134 17.1 5.7
4 22 868.6 145 18.0 6.0
5 21 792.3 155 15.4 5.1
6 25 746.7 144 15.5 5.2
7 21 457.1 86 16.0 5.3
8 26 746.7 162 13.9 4.6
9 21 807.6 144 16.8 5.6
10 20 700.9 135 15.5 5.2
11 27 639.9 107 18.0 6.0
12 23 761.9 149 15.2 5.1
13 24 746.7 139 16.2 5.4
14 32 651.3 130 15.1 5.0
15 29 561.1 112 15.1 5.0
16 30 685.0 137 15.0 5.0
17 19 581.9 106 16.4 5.5
18 30 640.0 128 15.0 5.0
19 38 487.6 106 13.8 4.6
20 43 591.6 123 14.5 4.8
21 28 473.4 88 16.1 5.4
22 47 610.0 122 15.0 5.0
23 21 624.8 121 15.5 5.2
24 20 593.3 122 14.6 4.9
25 20 685.7 136 15.1 5.0
26 24 624.8 126 14.9 5.0
27 18 563.8 126 13.4 4.5
28 21 548.6 115 14.3 4.8
29 21 579.0 140 12.4 4.1
30 19 548.6 125 13.3 4.4
31 19 411.4 88 14.1 4.7
32 20 563.8 115 14.7 4.9
Lampiran 1. Lanjutan
Riyawat Penyakit Terinfeksi
malaria
Anemia akibat infeksi penyakit
Anemia akibat komsumsi obat
Pernah
Tidak
Pernah Pernah Tidak Pernah Pernah Tidak Pernah
Lampiran 1. Lanjutan
Riwayat Riwayat Penyakit dalam Keluarga Transfusi darah
Anemia akibat infeksi penyakit
Lampiran 2. Lampiran Penjelasan Tentang Penelitian Kepada Awam
PENJELASAN TENTANG PENELITIAN
HUBUNGAN DEFISIENSI
GLUKOSA 6 FOSFAT DEHIDROGENASE (G6PD)
DENGAN INFEKSI MALARIA
PADA POPULASI NIAS
Selamat pagi Bapak2/Saudara2 sekalianKami ucapkan terimakasih atas kehadiran Bapak2/Saudara2 sekalian di tempat ini sebagai sukarelawan dalam penelitian kami
Sebelumnya kami akan menjelaskan tentang hal-hal yang berkaitan dengan penelitian ini, sehingga Bapak2/Saudara2 dapat dapat mengerti tujuan dan manfat dari penelitian ini, serta nantinya dapat dengan sukarela menandatangani surat persetujuan Bersedia Ikut sebagai Sukarelawan dalam penelitian ini
Penelitian ini bertujuan melihat kelainan darah pada orang-orang yang tinggal/ pernah tinggal di suatu daerah yang penduduknya banyak terkena penyakit malaria. Orang yang mempunyai kelainan darah ini akan mudah terkena penyakit kurang darah jika dalam keadaan sakit demam memakan obat-obat penurunan penurunan panas tubuh ataupun obat-obat jenis lain sewaktu sakit. Selain obat ada makan-makanan terrtentu yang jika di makan dapat menyebabkan orang yang punya kelainan di darah ini menjadi kurang darah
Nanti Bapak2/Saudara2 akan kami wawancara untuk menentukan apakah Bapak2/Saudara2 memenuhi persyaratan sebagai sukarelawan dalam penelitian ini. Pertanyaan-pertanyaan yang kami tanyakan kami harap di jawab dengan sebenar-benarnya agar penelitian ini dapat berjalan dengan semestinya.
Dalam penelitian ini, darah Bapak2/Saudara2 akan di ambil sebanyak 3 ml atau sebanyak jarum suntik dengan menggunakan spuit berukuran 3 ml, dengan cara memasukkkan jarum suntik pada daerah lipatan siku. Akan terasa sedikit sakit, tetapi sakitnya hanya sementara. Selanjutnya daerah bekas suntik akan kami tutup dengan kapas mengandung alkohol, Bapak2/Saudara2 cukup menjaga kebersihan daerah tersebut. Satu jam setelahnya biasanya kapas tersebut sudah dapat dilepaskan.
Setelah menjalani prosedur tadi, berarti Bapak2/Saudara2 telah menyelesaikan tugas sebagai sukarelawan dalam penelitian ini. Kami akan memberikan obat penambah darah serta penggantian ongkos menuju dan kembali dari tempat kami ini.
Baiklah jika sudah tidak ada pertanyaan, kami persilahkan Bapak2/Saudara2 yang setuju ikut sebagai sukarelawan dalam penelitian kami ini untuk menandatangan surat pernyataan persetujuan ikut dalam penelitian kami ini
Jika ada hal-hal yang tak terduga terjadi beberapa hari setelah pengambilan darah Bapak2/ Saudara2, seperti pembengkakan ataupun infeksi di daerah tempat pengambilan darah , Bapak2/ Saudara2 dapat menghubungi kami pada alamat: Dr. Mutiara Indah Sari
Alamat Institusi
Departemen Biokimia Fakultas Kedokteran USU Jl. Dr. Mansyur No. 5 Medan
Telp: 061-8211045 Alamat Rumah
Jl. Garuda No. 79 A Medan Telp: 061-8457487
Hp : 061-77774099
Kami akhiri dengan ucapan terimakasih atas kesediaan Bapak2/Saudara2 menjadi sukarelawan.
Lampiran 3. Surat Persetujuan Ikut Penelitian (Lembar Wawancara 1)
SURAT PERNYATAAN
PERSETUJUAN KEIKUTSERTAAN DALAM PENELITIAN HUBUNGAN DEFISIENSI GLUKOSA 6 FOSFAT DEHIDROGENASE
DENGAN INFEKSI MALARIA PADA POPULASI NIAS
PENGESAHAN OLEH PENELITI
Bersama ini saya menyatakan telah memberi penjelasan tentang tujuan, prosedur, manfaat, resiko sebagai subjek dalam penelitian dan perasaan yang tidak menyenangkan yang mungkin ada akibat pelaksanaan prosedur penelitian
hubungan defisiensi G6PD dengan infeksi malaria pada populasi suku Nias, dan telah dimengerti oleh subjek yang ikut dalam penelitian.
Tanda tangan : ____________________________ Tanggal: _____________
(Hari/Bulan/Tahun) Nama peneliti : ____________________________
PERSETUJUAN INDIVIDU YANG DITELITI
Saya yang bertanda tangan di bawah ini:
Nama :
Umur :
Alama :
Pekerjaan :
No.KTP/lainnya :
- Telah memperoleh penjelasan sepenuhnya dan menyadari serta memahami tentang tujuan, manfaat serta resiko yang mungkin timbul dalam penelitian yang brejudul hubungan defisiensi G6PD dengan infeksi malaria pada populasi suku Nias
- Saya setuju bila diambil data pribadi, data fisik, serta sampel saya diambil (darah) untuk materi penelitian. Saya telah diberi tahu bahwa dalam pengambilan sampel darah akan sedikit terasa sakit.
- Selain itu saya juga mengijinkan semua data tersebut dan sampel saya dipergunakan untuk penelitian terkait, sepanjang penelitian ini bermanfaat bagi peningkatan kesehatan dan kesejahteraan manusia.
Medan, ...Juni 2006
Mengetahui
Yang menyatakan,
Penanggung jawab Penelitian
Peserta penelitian
(Dr. Mutiara Indah Sari) (...)
Disaksikan oleh :
(...)
Lampiran 4. Lembar Wawancara 2
Pewawancara
No. Sampel
KUESIONER PENELITIAN HUBUNGAN
DEFISIENSI GLUKOSA 6 FOSFAT DEHIDROGENASE
DENGAN INFEKSI MALARIA PADA POPULASI NIAS
Tanggal pengisian :
Waktu :
I. IDENTITAS
Nama :
………...….…
Umur/ Tgl Lahir : ………....…
Tempat Lahir :
………...……….… Alamat lengkap :
………....…
………..………..…
Kampung asal :
………
Lama menetap dikampung asal : ……….. Suku bangsa : Bapak...Kampung
asal………
Ibu...Kampung asal………...…. Berat Badan : ...
Tinggi Badan : ... Tekanan Darah : ...
Frekuensi Nafas : ...
Pertanyaan :
1. Apakah pernah mengunjungi daerah yang diketahui merupakan daerah endemik malaria ?
II. Riwayat Keluarga
SILSILAH 4 GENERASI ORANG NIAS
____________________________________________________________________________________________________________