EFEKTIVITAS DEKONTAMINAN
AMMONIUM IRON (III) HEXACYANOFERRATE
(NH
4Fe[Fe(CN)
6]) TERHADAP CESIUM-137 PADA MONYET
EKOR PANJANG (
Macaca fascicularis)
FITRI ROSIDAH
PROGRAM STUDI BIOLOGI
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
EFEKTIVITAS DEKONTAMINAN
AMMONIUM IRON (III) HEXACYANOFERRATE
(NH
4Fe[Fe(CN)
6]) TERHADAP CESIUM-137 PADA MONYET
EKOR PANJANG (
Macaca fascicularis)
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains
Pada Program Studi Biologi Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
FITRI ROSIDAH
105095003126
PROGRAM STUDI BIOLOGI
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
PERNYATAAN
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI BENAR- BENAR HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU LEMBAGA MANAPUN.
Jakarta, Oktober 2009
ABSTRAK
EFEKTIVITAS DEKONTAMINAN AMMONIUM IRON (III)
HEXACYANOFERRATE (NH4Fe[Fe(CN)6]) TERHADAP CESIUM-137
PADA MONYET EKOR PANJANG (Macaca fascicularis)
Cs-137 adalah unsur kimia yang bersifat radioaktif dengan memancarkan sinar gamma yang dapat mengkontaminasi lingkungan setelah kecelakaan nuklir seperti reaktor Chernobyl. Zat radioaktif cesium yang masuk ke dalam tubuh
dapat diekskresikan dengan dekontaminan Ammonium Iron (III)
Hexacyanoferrate (AFCF) dengan cara mengikat cesium sehingga mempercepat pengeluaran dari dalam tubuh. Penelitian dilakukan pada bulan April sampai Juni 2009 dengan menggunakan monyet ekor panjang (M. fascicularis) yang diberi kontaminan Cs-137 1 µ Ci/ml secara oral kemudian diberikan AFCF melalui oral tiga kali sehari selama 3 hari berturut-turut dengan dosis total 3000, 4500 dan 6000 mg/ekor. Monyet tidak diberi AFCF bertindak sebagai kontrol. Pengamatan ekskresi Cs-137 dilakukan pada feces dan urin pada hari-hari ke 1, 2, 3, 7, 9, 14, 21, 28 dan 35 pasca kontaminasi dan aktivitas AFCF dalam menekan akumulasi radionuklida dievaluasi dengan menentukan aktivitas dalam darah pada hari ke 3, 7, 14, 21, 28, 35 dan organ pada hari ke 35. Sampel karkas direndam dalam asam nitrat, kemudian aktivitas Cs-137 di cacah dengan spektrometer gamma menggunakan detektor NaITl pada energi 661,65 keV. Hasil penelitian menunjukkan bahwa ketiga dosis AFCF mampu menekan aktivitas Cs-137 dalam darah dan organ, serta dapat meningkatkan pengeluaran Cs-137 melalui feses dan urin sampai hari ke-35 masing-masing sebesar 46,32% untuk dosis 3000 mg, 44,20 % untuk dosis 4500 mg dan 45,39% untuk dosis 6000 mg, sedangkan kontrol hanya sebesar 34,27%. Dengan demikian pemberian AFCF secara oral terbukti efektif dan dosis 3000 mg paling efektif mengekskresikan Cs-137 dari dalam tubuh monyet ekor panjang .
Kata Kunci : Dekontaminan AFCF, Radionuklida Cs-137, Monyet ekor
panjang (Macaca fascicularis)
ABSTRACT
EFFECTIVITY OF AMMONIUM IRON (III) HEXACYANOFERRATE (NH4Fe[Fe(CN)6]) DEKONTAMINANT ON CESIUM-137 IN LONG TAIL
MONKEY(Macaca fascicularis).
Cs-137 is a chemical radioactive element with emit gamma rays which could contaminate the environment after the nuclear accident such as Chernobyl reactor. Radioactive Cesium agent that entered to the body can be excreted by AFCF decontaminant by binding them and then excreted from the body. The research was done from April to Juni 2009 with using long tail monkey (M. fascicularis) which injected with contaminant of 1 µ Ci/ml of Cs-137. After that it was injected with AFCF three times a day for 3 days stretch, at doses of 3000, 4500 and 6000 mg/monkey. Monkey with no injected of AFCF served as control. The observation of the Cs-137 excretion was done in fecal and urine at days of 1, 2, 3, 7, 9, 14, 21, 28 and 35 after contamination, and the effectivity of AFCF in excretion radionuclide was evaluated by determining the activity in the blood in days of 3, 7, 14, 21, 28, 35 and organ at day of 35. Samples of organ and carcas were immersed in nitric acid and then the activity of Cs-137 was counted with gamma spectrometer using detector NaI(Tl) semiconductor at 661,607 keV. The results showed that three dose of AFCF were able to decrease the activity in blood and organ, and also were able to increase the excretion of Cs-137 through fecal and urine up to day 35 of which each was 46,32% for 3000 mg, 44,20% for 4500 mg and 45,39% for 6000 mg, whereas control only excreted 34,7%. It was concluded that the injected of AFCF orally was proven effective and dose of 3000 mg is the most effective in excretion Cs-137 from the body of long tail monkey.
Keywords : Decontamination Ammonium Iron (III) Hexacyanoferrate (AFCF),
contamination Cs-137, long tail monkey (Macaca fascicularis)
KATA PENGANTAR
Alhamdulillah segala Puji dan Puja serta syukur kehadirat Allah SWT,
Penulis panjatkan atas segala rahmat, karunia, kekuatan serta kesabaran yang
diberikan kepada penulis sehingga dapat menyelesaikan Tugas akhir yang
berjudul “Efektivitas Dekontaminan Ammonium Iron (III) Hexacyanoferrate
(NH4Fe[(CN)6]) Terhadap Cesium-137 Pada monyet Ekor Panjang (Macaca
fascicularis).
Terwujudnya tulisan dalam bentuk skripsi ini, tentunya tidak lepas dari
bantuan dan bimbingan dari berbagai pihak. Rasa terima kasih penulis ucapkan
kepada :
1. Bapak DR. Syopiansyah Jaya Putra, M.Sis, selaku Dekan Fakultas Sains
dan Teknologi.
2. DR. Lily Surayya E.P. M. Env. Stud, selaku Ketua Program Studi Biologi
sekaligus selaku pembimbing II, serta Bapak DR. Mukh Syaifudin selaku
pembimbing I yang telah memberikan bimbingan, waktu dan perhatiannya
dalam penyusunan skripsi ini.
3. Bapak Tur Rahardjo, S.P, selaku pembimbing lapangan yang dengan sabar
memberikan pengarahan dan pemahaman selama pelaksanaan penelitian
sampai selesainya skripsi ini.
4. Ibunda dan Ayahku tercinta, Aa, Teteh dan adik-adikku tersayang, serta
seluruh keluarga tercinta yang telah memberikan doa, dukungan baik moril
maupun materil yang tak terhingga dalam menyelesaikan skripsi ini.
5. Seluruh dosen dan staf karyawan Jurusan Biologi, Fakultas Sains dan
Teknologi, Universitas Islam negeri Syarif Hdayatullah Jakarta
6. Seluruh Staf Bidang Biomedika (Ibu Nurhayati, DR. Sigit Witjaksono,
Ibu Devita dan Bapak Mugiono) serta seluruh Staf Bidang Standarisasi
(Bapak Gatot, Bapak Pujadi, Ibu Rosdiana, Bapak Hermawan Chandra,
Bapak Holnisar, Mas Jono dan Mas Agung) terima kasih Untuk pelajaran
dan kebersamaannya.
7. Sahabat terbaikku Ratih Purwasih yang selalu ada disaat susah, sedih,
bimbang dan selalu menjadi motivasi sehingga selesinya skripsi ini, serta
teman kosan Irakian Atas terima kasih untuk pengertiannya.
8. Teman seperjuanganku Dara, Wiwi terima kasih banyak, Kak bahri, Kak
Sanusi, Wida, Dian, Dyah MTK, Kamal, Mega, Tami, Aida, dan Zaenab
terima kasih banyak semoga Allah membalas semua keikhlasan Kalian,
serta keluarga besar Biologi (khususnya Biologi 2005 “Bioma”) yang telah
memberikan kebersamaan yang indah dan menjadi saksi sebagian
perjalananku.
Dalam penulisan skripsi ini, penulis menyadari sepenuhnya bahwa
penulisan skripsi ini masih jauh dari sempurna dan tidak lepas dari kesalahan dan
kekurangan, hal ini karena keterbatasan kemampuan dan pengetahuan yang
dimiliki. Walaupun demikian penulis berharap hasil tulisan ini dapat bermanfaat
bagi pembaca dan perkembangan ilmu pengetahuan.
Jakarta, Oktober 2009
Penulis,
DAFTAR ISI
Halaman
ABSTRAK ... i
ABTRACT ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... v
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN 1.1. Latar Belakang ... 1
1.2. Rumusan Masalah ... 4
1.3. Hipotesis... 4
1.4. Tujuan Penelitian ... 4
1.5. Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA 2.1. Radioaktivitas ... 6
2.1.1. Tetapan Peluruhan dan Umur Paro ... 6
2.1.2. Aktivitas Radiasi ... 7
2.1.3. Kestabilan Inti Atom ... 8
2.2. Interaksi Radiasi Dengan Materi ... 9
2.2.1. Interaksi Sinar Gamma Dengan Materi ... 9
2.2.2. Detektor Sintilasi ... 10
2.2.3. Detektor Sintilasi NaI(Tl) ... 11
2.2.4. Prinsip Spektrometer Gamma ... 11
2.3. Kontaminasi Bahan Radioaktif ... 12
2.3.1. Kontaminasi Eksterna ... 13
2.3.2. Kontaminasi Interna ... 13
2.4.Waktu Paruh Biologi ... 15
2.4. Jalan Masuk Radionuklida ke Dalam Tubuh ... 16
2.6. Radionuklida Cs-137 ... 16
2.7. Dekontaminasi Radionuklida ... 18
2.8. Ammonium Iron (III) Hexacyanoferrate ... 19
2.9. Monyet Ekor Panjang (Macaca fascicularis)... 21
2.10. Kerangka Berpikir ... 23
BAB III METODOLOGI PENELITIAN 3.1. Tempat dan Waktu Penelitian ... 24
3.2. Alat dan Bahan ... 24
3.3. Metode penelitian ... 25
3.4. Cara Kerja ... 25
3.4.1. Perlakuan Terhadap Hewan Percobaan ... 25
3.4.2. Pengambilan Sampel Feses dan Urin ... 26
3.4.3. Pengambilan sampel Darah ... 26
3.4.4. Pengambilan Sampel Organ dan Karkas ... 27
3.4.5. Pencacahan (counting) ... 27
3.5. Analisis Data... 28
3.5.1. Perhitungan Aktivitas Cs-137 dalam Sampel ... 28
3.5.2. Presentase (%) Aktivitas Cs-137 dalam Sampel... 29
BAB V HASIL PENGAMATAN DAN PEMBAHASAN
4.1. Aktivitas Cs-137 Yang Terakumulasi Dalam Darah ... 30
4.2. Aktivitas Cs-137 Yang Terakumulasi Dalam Organ... 32
4.3. Aktivitas Cs-137 Yang Diekskresikan Melalui Urin... 36
4.4. Aktivitas Cs-137 Yang Diekskresikan Melalui Feses ... 38
4.5. Total Aktivitas Cs-137 Yang Diekskresikan Melalui Urin dan Feses ... 41
BAB V KESIMPULAN DAN SARAN 5.1. Kesimpulan ... 44
5.2. Saran ... 44
DAFTAR PUSTAKA ... 45
LAMPIRAN- LAMPIRAN ... 49
DAFTAR TABEL
Halaman
Tabel 1. Hasil Pencacahan Aktivitas Cs-137 (Bq) yang
Terakumulasi Dalam Darah ………. 49
Tabel 2. Hasil Pencacahan Aktivitas Cs-137 (Bq) yang
Terakumulasi Dalam Organ………. 50
Tabel 3. Hasil Pencacahan Aktivitas Cs-137 (Bq) yang
Diekskresikan Melalui Urin……… 51
Tabel 4. Hasil Pencacahan Aktivitas Cs-137 (Bq) yang
Diekskresikan Melalui Feses……… 53
Tabel 5. Persentase (%) Aktivitas Cs-137 yang
Terakumulasi Dalam Darah……… 55
Tabel 6. Persentase (%) Aktivitas Cs-137 yang
Terakumulasi Dalam Organ……… 55
Tabel 7. Persentase (%) Aktivitas Cs-137 yang
Diekskresikan Melalui Urin……… 56
Tabel 8. Persentase (%) Aktivitas Cs-137 yang
Diekskkresikan Melalui Feses ……… 56
DAFTAR GAMBAR
Halaman
Gambar 1. Detektor Sodium Iodida (NaI) ... 11
Gambar 2. Skema Masuknya Bahan Radioaktif Ke dalam Tubuh
Secara Ingesti ... 14
Gambar 3. Persentase (%) Aktivitas Cs-137 Yang Terakumulasi
Dalam Darah Pasca Pemberian AFCF ... 30
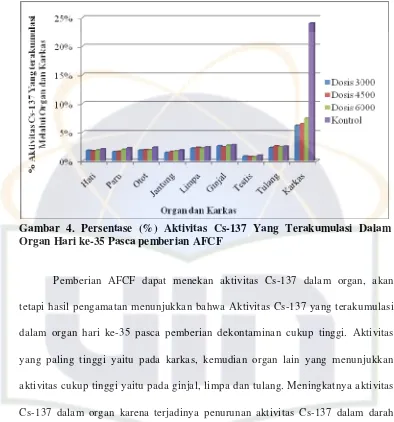
Gambar 4. Persentase (%) Aktivitas Cs-137 Yang Terakumulasi
Dalam Organ Hari ke-35 Pasca Pemberian AFCF ... 33
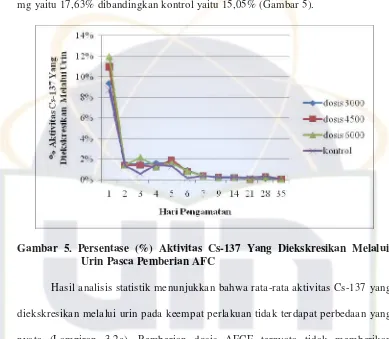
Gambar 5. Persentase (%) Aktivitas Cs-137 Yang Diekskresikan
Melalui Urin Pasca Pemberian AFCF ... 36
Gambar 6. Persentase (%) Aktivitas Cs-137 yang Diekskresikan
Melalui Feses Pasca Pemberian AFCF ... 38
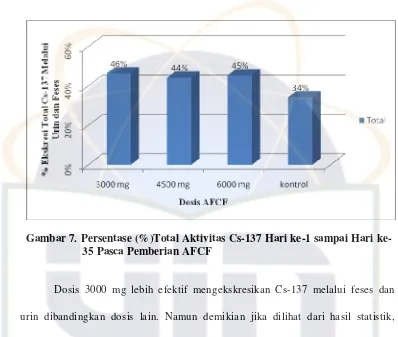
Gambar 7. Persentase (%) Total Aktivitas Cs-137 Hari ke-1
sampai Hari ke-35 Pasca Pemberian AFCF ... 41
Gambar 8. Persentase (%) aktivitas Cs-137 Yang Tersisa Dalam Tubuh
Pasca Pemberian AFCF ... 42
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data Hasil Pencacahan (Counting) ... 49
Lampiran 2. Persentase (%) Aktivitas Sampel... 55
Lampiran 3 Hasil Pengolahan Dengan SPSS 12 ... 57
Lampiran 4. Gambar Alat dan Bahan Yang Digunakan
Dalam Penelitian ... 60
PENDAHULUAN
1.1. Latar Belakang
Pemakaian zat radioaktif dalam berbagai kegiatan industri, kedokteran,
pertanian dan teknologi lainnya saat ini sudah banyak dilakukan. Proses
pengolahan bahan-bahan nuklir juga sudah dilaksanakan sebagai awal kegiatan
industri nuklir di Indonesia. Kemajuan teknologi nuklir yang pesat ini tidak lepas
dari masalah keselamatan kerja terhadap radiasi yang perlu dikuasai dengan baik
dan akan membawa dampak yang serius terhadap resiko terlepasnya unsur-unsur
radioaktif ke lingkungan dan akhirnya terendap dalam tubuh manusia (Wardhana,
2006).
Bahan radioaktif yang terlepas saat terjadi kecelakaan dapat menyebabkan
radiasi terhadap pekerja radiasi dan masyarakat di sekitar instalasi. Bahan
radioaktif masuk ke dalam tubuh baik melalui pernafasan, saluran pencernaan
akibat mengkonsumsi makanan dan minuman yang terkontaminasi maupun
melalui kulit terluka. Beberapa kontaminan tersebut merupakan zat radioaktif
hasil fisi seperti radionuklida Cs-137, I-131 dan Sr-90 dan kontaminan yang
berasal dari instalasi industri yang menggunakan zat radioaktif sebagai sumber
radiasi seperti Co-60, Ir-92 dan lain-lain (Rahardjo et al, 2007). Cs-137
merupakan unsur kimia yang bersifat radioakif dengan memancarkan sinar
gamma dan merupakan salah satu radionuklida hasil proses fisi bahan bakar
uranium dan plutonium di reaktor nuklir.
2
Kemampuan dalam menangani seseorang yang terkena kontaminasi
radionuklida tersebut sangat diperlukan pada suatu kecelakaan instansi nuklir
(Alatas et al, 1996). Radionuklida yang masuk ke dalam tubuh perlu dikaji dan
diteliti aspek-aspek yang berkaitan dengan kesehatan. Salah satu aspek yang
terpenting adalah bagaimana cara mengeluarkan radionuklida dalam tubuh, karena
radionuklida ini berbahaya apabila terendap di dalam tubuh. Sebagai langkah
antisipasi penting dalam penanganan korban pada keadaan kecelakaan nuklir
adalah proses dekontaminasi (Basyarahil, 1997).
Ammonium Iron (III) Hexacyanoferrate (AFCF) merupakan
dekontaminan yang dapat mengikat Cs-137 dalam saluran pencernaan sehingga
mencegah penyerapan Cs-137 serta mempercepat pengeluaran dari dalam tubuh.
Dalam kasus kecelakaan nuklir di Chernobyl, Ukraina tahun 1986 AFCF telah
digunakan sebagai dekontaminan untuk Cs-137 dan Cs-134. Dari beberapa
penelitian pada hewan (tikus, kambing, rusa, biri-biri, ayam broiler) menunjukkan
bahwa dekontaminan tersebut mempunyai potensi dalam mengikat Cs sehingga
mampu meminimalisir kadar zat radioaktif dalam tubuh (Schimansky, 1997).
Pemberian dekontaminasi bertujuan untuk mengurangi penyerapan
radionuklida dalam tubuh dengan cara meningkatkan ekskresi radionuklida baik
melalui urin maupun feses sehingga memperkecil efek biologik yang mungkin
akan timbul. Setiap radionuklida mempunyai dekontaminan yang berbeda dan
masing-masing harus diuji kemampuannya. Berdasarkan hasil penelitian Alatas et
al (1996) dalam studi pemberian dekontaminan Prussian Blue secara oral pasca
ekskresi radionuklida Cs-137 sampai 84,80%. Berdasarkan hasil penelitian Sanusi
(2007) diketahui bahwa pemberian dekontaminan Prussian Blue (PB) secara oral
pasca pemberian Cs-137 secara oral pada monyet ekor panjang dapat
meningkatkan ekskresi radionuklida Cs-137 sampai 26%. Pada penelitian ini
digunakan dekontaminan yang lain yaitu Ammonium Iron (III) Hexacyanoferrate
(AFCF) dengan hewan percobaan yaitu monyet ekor panjang (M. fascicularis).
Ketika bahan radioaktif masuk ke dalam tubuh, maka sangat penting untuk
dilakukan perkiraan dosis dekontaminan, dosis AFCF yang digunakan dalam
penelitian ini yaitu 3000, 4500 dan 6000 mg/ekor. Perkiraan dosis berdasarkan
Letal Dosis (LD) 50, dimana LD 50 AFCF untuk tikus sebesar 2100 mg/kg,
sedangkan untuk monyet digunakan LD 50 dua kali lebih banyak dibandingkan
tikus (Anonimus, 2000).
Agar hasil Litbang (Penelitian Pengembangan dan Perekayasaan)
dekontaminasi ini bermanfaat pada manusia, maka idealnya dilakukan dengan
objek manusia. Namun di Indonesia hal ini tidak mungkin dilakukan. Oleh karena
itu penelitian tersebut akan lebih representatif apabila dilakukan dengan objek
hewan yang dekat dengan karakter manusia. Monyet ekor panjang adalah hewan
yang sangat optimal untuk digunakan sebagai objek, sehingga diharapkan dapat
4
1.2. Rumusan Masalah
1. Apakah pemberian dekontaminan AFCF efektif dalam mengekskresikan
Cs-137 dari dalam tubuh monyet ekor panjang ?
2. Diantara dosis AFCF 3000, 4500 dan 6000 mg/ekor yang diberikan pada
monyet ekor panjang secara oral, dosis manakah yang lebih efektif dalam
mengekskresikan Cs-137?
1.3. Hipotesis
1. Pemberian dekontaminan AFCF mampu mengekskresikan Cs-137 dalam
tubuh monyet ekor panjang.
2. Pemberian tiga dosis AFCF secara oral pada monyet ekor panjang
diperkirakan dosis 6000 mg/ekor lebih efektif dari pada dosis 3000 dan
4500 mg/ekor dalam mengekskresikan Cs-137.
1.4. Tujuan Penelitian
1. Mengetahui efektivitas dekontaminan AFCF dalam mengekskresikan Cs-
137 dari dalam tubuh monyet ekor panjang.
2. Mengetahui dosis dekontaminan AFCF yang efektif dalam
1.5. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi mengenai
efektifitas dan dosis efektif dekontaminan AFCF dalam mengekskresikan Cs-137
6
BAB II
TINJAUAN PUSTAKA
2.1. Radioaktivitas
Di alam terdapat unsur radioaktif seperti uranium (U), thorium (Th),
radium (Ra) dan radionuklida seperti kalium-40 (K-40), carbon-14 (C-14), dan
lain-lain. Ada juga yang dihasilkan dari percobaan nuklir atau kecelakaan fasilitas
nuklir seperti Cs-137 dan Sr-90. Radionuklida masuk ke dalam tubuh manusia
melalui makanan atau pernafasan, untuk meneliti pengaruh bahan radioaktif pada
tubuh manusia, perlu diketahui radioaktivitas dalam tubuh manusia (Akhadi,
2006).
Radioaktivitas adalah aktivitas inti atom yang secara spontan
memancarkan sinar alfa, beta dan gamma. Radioaktivitas disebut juga peluruhan
radioaktif, yaitu transmutasi inti suatu unsur karena memancarkan zarah radioaktif
(Achmad, 2001).
2.1.1. Tetapan Peluruhan dan Waktu Paruh
Peluruhan radioaktif mengikuti hukum laju reaksi orde kesatu, laju
peluruhan berbanding lurus dengan jumlah atom radioaktif yang tertinggal,
dimana N adalah jumlah atom radioaktif dan adalah tetapan peluruhan
(Achmad, 2001).
Dengan mensubstitusi aktivitas radiasi = N, bentuk differensial laju
peluruhan diperoleh :
N(t) = N0 (e - t)
N0 = Banyaknya inti atom yang meluruh
Nt/t = sisa inti atom setelah meluruh
= Tetapan peluruhan
t = lama peluruhan
Setiap atom yang meluruh memancarkan satu zarah radioaktif, yakni yang
dinamakan aktivitas, diberikan oleh N yang satuannya curie dimana 1 curie =
3,7.10 10 peluruhan per detik yang kira-kira sama dengan laju peluruhan 1 gram
radium (Soedojo, 2004). Sebagai ukuran laju peluruhan lebih lazim dipakai waktu
paruh yang didefinisikan sebagai selang waktu setelah peluruhan radioaktif,
banyaknya atom radioisotop tinggal separuh dari ukuran semula, yaitu
t ½ = ln 2/ = 0,693/ (Soedojo, 2004).
2.1.2. Aktivitas Radiasi
Aktivitas Radiasi zat radioaktif menyatakan banyaknya inti atom yang
meluruh per satuan waktu. Atau disebut juga laju peluruhan inti atom tidak stabil
menuju inti stabil dengan radiasi sinar-sinar radioaktif. Jika N adalah banyaknya
inti atom mula-mula, dan A adalah aktivitas radiasi maka diperoleh hubungan
secara matematika ditulis sebagai berikut : A = N, sehingga radioaktivitas dari
setiap bahan radioaktif meluruh secara eksponensial mengikuti persamaan
peluruhan sebagai berikut :
8
dimana At = aktivitas setelah mengalami peluruhan selama waktu t ; A0 =
aktivitas sebelum peluruhan; = tetapan peluruhan; 1/ 2 t = waktu paro; t = waktu
peluruhan (Maskur et al, 2008).
Keaktifan jenis radionuklida didefinisikan bahwa 1 Ci = 3,7 x 1010 Bq.
Satuan Becquerel (Bq) ini dipakai dalam satuan SI sejak tahun 1976, sebelumnya
satuan untuk intensitas suatu sumber radiasi menggunakan satuan Curie, yang
disingkat dengan Ci. Pada umumnya untuk intensitas radiasi yang tinggi
digunakan satuan radiasi Curie, sedangkan untuk intensitas rendah biasanya
memakai satuan Becquerel (Wardhana, 2007).
2.1.3. Kestabilan Inti Atom
Kestabilan suatu inti atom dapat dilihat dari fungsi jumlah proton (Z) di
dalam intinya dan perbandingan antara neutron dan proton (N/Z). Untuk inti-inti
atom ringan, stabil jika (N/Z) 1, misalnya unsur-unsur: 1H 2
perbandingan (N/Z) menyimpang dari 1, biasanya merupakan inti yang kurang
stabil. Sebagai contoh misalnya inti atom 1H3, 6C14, 8O15 dan (N/Z) 1,5 untuk
inti-inti berat (Syarifah, 2009).
Inti-inti atom yang tidak stabil, baik karena komposisi jumlah proton dan
neutronnya yang tidak seimbang ataupun karena tingkat energinya yang tidak
berada pada keadaan dasarnya, cenderung untuk berubah menjadi stabil. Bila
ketidakstabilan inti disebabkan karena komposisi jumlah proton dan neutronnya
yang tidak seimbang, maka inti tersebut akan berubah dengan memancarkan
tingkat energinya yang berada pada keadaan tereksitasi maka akan berubah
dengan memancarkan radiasi gamma (Achmad, 2001).
2.2. Interaksi Radiasi Dengan Materi
Radiasi apabila menumbuk suatu materi maka akan terjadi interaksi yang
akan menimbulkan berbagai efek. Efek-efek radiasi ini bergantung pada jenis
radiasi, energi dan juga bergantung pada jenis materi yang ditumbuk. Pada
umumnya radiasi dapat menyebabkan proses ionisasi atau proses eksitasi ketika
melewati materi.
2.2.1. Interaksi Sinar Gamma Dengan Materi
Berkurangnya energi dari sinar gamma pada saat melewati suatu materi
terjadi karena :
a. Efek Fotolistrik
Pada efek fotolistrik, energi foton diserap oleh elektron orbit, sehingga
elektron tersebut terlepas dari atom. Tiap elektron yang yang dipancarkan
sebanding dengan intensitas (terang) cahayanya, partikel cahaya ini disebut foton
dengan menyimpulkan bahwa tiap foton harus memiliki energi E yang diberikan
oleh persamaan : E = hv , dengan h adalah frekuesi cahaya (Chang, 2004)
b. Hamburan Compton
Pada efek Compton, foton dengan energi hv berinteraksi dengan elektron
10
tersebut dilepaskan dari ikatannya dengan atom dan bergerak dengan energi
kinetik tertentu.
c. Produksi Pasangan
Proses produksi pasangan hanya terjadi bila foton datang / 1,02 MeV.
Apabila foton semacam ini mengenai inti atom berat, foton tersebut akan lenyap
dan sebagai gantinya timbul sepasang elektron-positron. Positron adalah partikel
yang massanya sama dengan elektron dan bermuatan listrik positif yang besarnya
juga sama dengan muatan elektron (Kamil, 2008).
2.2.2. Detektor Sintilasi
Alat ini menggunakan bahan logam yang atom-atomnya dengan mudah
dideteksi oleh radiasi yang datang (efek fotolistrik). Efek fotolistrik adalah
keluarnya elektron-elektron dari permukaan logam ketika terkena radiasi. Bahan-
bahan yang umum digunakan sebagai sintilator adalah kristal-kristal natrium
iodida. Bahan-bahan ini diletakkan di salah satu ujung peralatan yang disebut
tabung foto pengganda (photomultiplier) sehingga foton yang dikeluarkan oleh
sintilator dapat diubah menjadi sinyal listrik. Tabung foto pengganda terdiri atas
beberapa elektroda yang disebut dinoda. Detektor sintilasi lebih sensitif bila
dibandingkan pencacah Geiger-Muller, terutama terhadap sinar gamma yang
berinteraksi lebih kuat dengan zat dibandingkan dengan partikel-partikel
2.2.3. Detektor Sintilasi NaI(Tl)
Detektor sintilasi NaI(Tl) digunakan untuk mendeteksi intensitas sinar
gamma dari bahan radioaktif pada daerah energi 0,1-100 MeV dengan efisiensi
cukup tinggi (10-60%) dan resolusi energi menengah (5-15%). Detektor ini
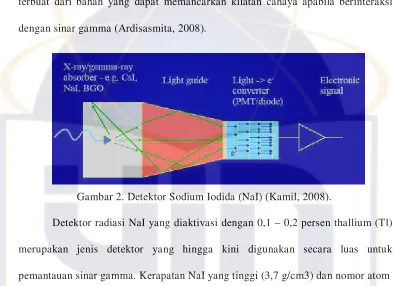
terbuat dari bahan yang dapat memancarkan kilatan cahaya apabila berinteraksi
dengan sinar gamma (Ardisasmita, 2008).
Gambar 2. Detektor Sodium Iodida (NaI) (Kamil, 2008).
Detektor radiasi NaI yang diaktivasi dengan 0,1 – 0,2 persen thallium (Tl)
merupakan jenis detektor yang hingga kini digunakan secara luas untuk
pemantauan sinar gamma. Kerapatan NaI yang tinggi (3,7 g/cm3) dan nomor atom
(Z) yang tinggi dari iodine (I) menjadikan interaksinya dengan radiasi gamma
cukup baik (Akhadi, 2000).
2.2.4. Prinsip spektrometri Gamma
Apabila radiasi gamma memasuki tabung detektor, maka akan terjadi
interaksi antara radiasi gamma dengan bahan NaI(Tl). Interaksi itu dapat
12
interaksi ini maka elektron-elektron atom bahan detektor akan terpental keluar
sehingga atom-atom itu berada dalam keadaan tereksitasi.
Atom-atom yang tereksitasi akan kembali ke keadaan dasarnya sambil
memancarkan kerlipan cahaya. Cahaya yang dipancarkan itu selanjutnya
diarahkan ke foto katoda sensitif. Apabila foto katoda terkena kerlipan cahaya,
maka dari permukaan foto katoda itu akan dilepaskan elektron. Elektron yang
dilepaskan oleh foto katoda akan dipercepat oleh medan listrik dalam tabung
pelipat ganda elektron menuju dinoda pertama.
Hasil akhir jumlah pelipatgandaan elektron bergantung pada jumlah
dinoda. Tabung pelipat ganda elektron yang mempunyai 10 tingkat dinoda
misalnya, pada anoda (dinoda terakhir yang sekaligus berperan sebagai pelat
pengumpul elektron) bisa didapatkan faktor penggandaan elektron antara 107 -
108. Dengan demikian, sinar gamma yang dipantau akan menghasilkan pulsa
listrik sebagai keluaran dari detektor NaI(Tl). Tenaga elektron yang dilepaskan ini
bergantung pada intensitas sinar gamma yang mengenai detektor. Makin tinggi
energi elektron, makin tinggi pula pulsa listrik yang dihasilkannya, sedang makin
banyak elektron yang dilepaskan makin banyak pula cacahan pulsanya (Akhadi,
2000)
2.3. Kontaminasi Bahan Radioaktif
Dalam kecelakaan yang melibatkan zat radioaktif, ada kemungkinan
menjadi 2 macam yaitu kontaminasi eksterna dan kontaminasi Interna
(Darussalam, 1996).
2.3.1. Kontaminasi Eksterna
Kontaminasi eksterna radionuklida adalah penempelan atau pengendapan
suatu bahan radioaktif pada bagian luar tubuh seperti kulit, pakaian, sepatu, jas
lab, sarung tangan dan masker akibat emisi tak terkendali dalam suatu kedaruratan
nuklir. Beberapa radionuklida yang terkumpul di permukaan tubuh bagian luar
sebagai kontaminan eksterna dapat masuk ke dalam tubuh baik melalui pori-pori
kulit maupun melalui kulit terluka (Nurhayati, 1999).
2.3.2. Kontaminasi Interna
Kontaminasi interna adalah masuknya radionuklida ke dalam tubuh akibat
emisi tak terkendali dalam suatu kedaruratan nuklir. Dekontaminasi interna harus
dilakukan secepat mungkin untuk menghindari penyerapan lebih lanjut.
Radionuklida dapat masuk ke dalam tubuh melalui:
1. Saluran pencernaan (ingesti)
Bahan radioaktif dapat tertelan dalam bentuk larutan atau makanan yang
sudah terkontaminasi zat radioaktif. Tempat absorbsi yang utama dalam saluran
pencernaan adalah usus halus.
2. Saluran Pernafasan (inhalasi)
Resiko kontaminasi melalui saluran pernapasan ini tiga kali lipat lebih besar
14
terjadinya proses penyerapan secara langsung bahan radioaktif tersebut ke dalam
darah. Radionuklida yang masuk kedalam saluran pernapasan kemungkinan
berasal dari debu radioaktif yang terlepas kelingkungan seperti yang terjadi pada
kecelakaan reaktor nuklir (fallout) (Nurhayati, 1999).
Menelan (ingesti)
Saluran Pencernaan
Cairan Ekstra Seluler
Jaringan/ Organ Tubuh
Feses
Hati Ginjal Keringat
Urin
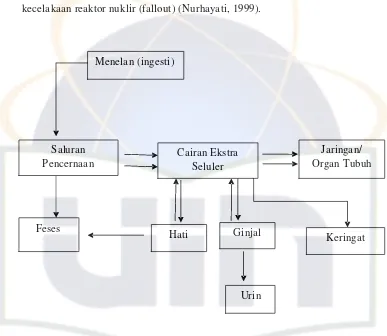
Gambar 2. Skema masuknya bahan radioaktif ke dalam tubuh secara Ingesti
(Nurhayati, 1999).
Keterangan Gambar :
a. Awal mula suatu radionuklida dapat memasuki tubuh karena tertelan
bersama makanan dan minuman.
b. Translokasi dan penimbunan (akumulasi) radionuklida pada bagian-bagian
c. Sebagian radionuklida dalam cairan ekstraselular akan diekskresikan ke
luar tubuh oleh ginjal, hati, ataupun saluran empedu terus ke usus.
d. Sebagian radionuklida yang lain akan diakumulasi (deposit) dalam suatu
jaringan atau organ tubuh.
e. Eliminasi bahan atau unsur radioaktif dari dalam tubuh dapat berlangsung
bersama-sama jalan nafas ke luar (berupa gas), urin, keringat dan tinja
(Darussalam, 1996).
2.4. Waktu Paruh Biologi
Waktu paruh biologi merupakan waktu yang dibutuhkan oleh zat, senyawa
kimia atau radionuklida yang berada dalam organ atau jaringan tubuh untuk
menjadi separuh dari jumlah semula. Waktu paruh ini berkisar antara beberapa
jam sampai bertahun-tahun (Suryowinoto, 1990 dalam Sanusi, 2008).
Waktu paruh biologi dipengaruhi oleh jenis organ atau jaringan, bentuk
senyawa kimia radionuklida dan karakteristik individu. Untuk jenis radionuklida
yang sama, antara individu yang satu dengan lain waktu paruhnya dapat berlainan
(Syaifudin et al, 1995). Semakin besar waktu paruh, berarti semakin lama zat
radioaktif tersebut memancarkan radiasi. Selain itu, tingkat bahaya suatu jenis zat
radioaktif dipengaruhi oleh toksisitas zat radioaktif. Apabila suatu zat radioaktif
memiliki toksisitas tinggi dan waktu paruh panjang maka zat radioaktif selain
secara kimia meracuni tubuh (apabila masuk ke tubuh melalui saluran pencernaan
dan kulit) juga akan menimbulkan paparan radiasi selama tinggal di dalam tubuh
16
2.5. Jalan masuk Radionuklida ke dalam Tubuh
Masuknya radionuklida ke dalam tubuh melalui saluran pernafasan dapat
berupa gas, cairan atau padatan, misalnya partikel aerosol (gas dengan campuran
partikel padat dan cair yang melayang di udara). Radionuklida tersebut setelah
mengalami berbagai proses di dalam tubuh, sebagian dapat terendap pada saluran
pernafasan bagian atas dan paru-paru, sebagian lain dikeluarkan secara exhalasi.
Bagian yang terendap dapat masuk ke saluran pencernaan, dan apabila senyawa
tersebut bersifat mudah larut maka akan segera diserap oleh cairan tubuh dan
akhirnya dikeluarkan melalui urin. Contoh radionuklida bersifat mudah larut yang
masuk melalui saluran pernafasan adalah I-131, Sr-90 dan Cs-137 (Syaifudin et
al, 1995).
2.6. Radionuklida Cs-137
Kata “Caesium” berasal dari bahasa latin “Caesius” yang artinya langit
biru. Nama tersebut didasarkan pada intensitas warna biru dengan λ: 456 nm.
Seperti logam alkali, Cs sangat elektropositif dan memiliki radius kristal ionik
yang tinggi (Kaikkonen, 2006).
Cesium dengan simbol Cs adalah logam yang bisa bersifat stabil (non
radioaktif) atau tidak stabil (radioaktif). Cs yang paling umum dikenal sebagai
radioaktif adalah Cs-137. Cs-137 memiliki struktur yang bersifat lembut, lunak,
berwarna putih perak dan berbentuk cair pada suhu kamar 28 oC (83oF)
Cs-137 yang terdapat di lingkungan berasal dari berbagai sumber, sumber
yang terbesar adalah dari kecelakan Chernobyl yang tersebar dan terdeposit di
seluruh dunia. Cs-137 radioaktif dihasilkan ketika uranium (U235) atau plutonium
(P239) menyerap neutron dan mengalami proses fisi (pembelahan). Cs ditemukan
pada tahun 1941 oleh Glenn T. Seaborg dan Margaret Melhase, akan tetapi pada
tahun 1860 oleh R.W. Bunsen dan G.R. Kirchroff (menggunakan spektroskop)
menamakannya berdasarkan karakteristik 2 garis biru terang pada spektrumnya
(Anonimous, 2005).
Cs-137 merupakan salah satu radioisotop yang sering digunakan dalam
industri. Radioisotop ini digunakan dalam berbagai macam pengukuran alat,
seperti mengukur densitas kelembaban, mengukur ketebalan dari lembaran logam,
juga digunakan sebagai pemancar sumber radiasi gamma untuk penyakit kanker.
Cs juga digunakan untuk diagnosa penyakit, sebagai sumber kalibrasi peralatan
radiasi dan sumber dalam jumlah besar digunakan untuk mensterilkan peralatan
kedokteran (Dotzel, 2003).
Cs-137 memiliki waktu paruh fisik 30 tahun, termasuk radionuklida yang
bersifat mudah larut sehingga mudah diserap oleh jaringan tubuh. Hasil penelitian
menunjukkan bahwa fraksi serapan rata-rata adalah 0,99 untuk senyawa berbentuk
klorida dan 0,82 untuk senyawa oksida (Alatas et al, 1996). Cs-137 juga masuk
ke dalam darah akan terdistribusi atau terserap ke jaringan tubuh, 10% dari Cs
dikeluarkan dengan waktu biologi 2 hari dan 90% dikeluarkan secara lambat
dengan waktu paruh biologi 110 hari dan kurang dari 1% dari Cs terendap dalam
18
Bahan radioaktif memiliki waktu paruh biologi yang berbeda-beda
tergantung jenis individu yang terkontaminasi. Dalam tubuh manusia Cs-137
memiliki waktu paruh biologi selama 110 hari, sedangkan anjing selama 25 hari,
monyet selama 19 hari, tikus selama 6,5 hari dan mencit selama 1,2 hari. Cs-137
diserap oleh seluruh organ tubuh, khususnya ginjal, otot, hati, paru-paru, jantung
dan limpa (Syaifudin et al, 1995).
Dalam dosis tinggi Cs-137 dapat membunuh sedangkan dalam dosis kecil
dapat memicu kanker. Paparan zat-zat berbahaya itu dapat masuk ke dalam tubuh
manusia melalui udara yang terhirup atau termakan, sehingga bahan radioaktif
dapat tersebar pada jaringan halus, khususnya jaringan otot (Dotzel, 2003).
2.7. Dekontaminasi Radionuklida
Dekontaminasi adalah suatu metode pembersihan atau pengeluaran
radionuklida dari tubuh sebanyak mungkin secara cepat dan tepat sebagai usaha
untuk memperkecil efek biologik yang ditimbulkan. Proses ini dapat dilakukan
dengan cara pengikatan secara kimia radionuklida oleh zat dekontaminan dan
pengeluaran senyawa komplek yang terbentuk dari tubuh melalui urin dan feses.
Dengan demikian proses pengikatan yang paling efektif justru pada saat
radionuklida belum terserap dan masuk ke dalam sistem aliran darah. Pemberian
dekontaminan segera setelah terjadi kecelakaan merupakan tindakan yang paling
tepat (Nurhayati, 1999).
Prinsip dekontaminasi zat radioaktif di bagian luar tubuh adalah dengan
Sedangkan prinsip dekontaminasi zat radioaktif pada bagian dalam tubuh adalah
dengan blocking dan embeding zat radioaktif sebelum diserap organ tubuh untuk
selanjutnya diekskresikan dari tubuh. Dekontaminan yang dapat digunakan antara
lain Ethylene Diaminine Tetraacetic Acid (EDTA), Diethylene Triaminine
Pentaacetic Acid (DTPA), Prussian Blue (PB), Kalium Iodine (KI), Ammonium
Iron III Hexacyanoferrate (NH4Fe[Fe(CN)6]) dan potassium Iron
Hexacyanoferrtae (KFe[Fe(CN)6]), tergantung pada jenis radionuklida dan
lokasinya dalam tubuh (Rahardjo, 2008).
2.8. Ammonium Iron (III) Hexacyanoferrate
Ammonium Iron (III) Hexacyanoferrate atau AFCF memiliki rumus kimia
(NH4Fe[Fe(CN)6]). Nama lain dari Ammonium Iron III Hexacyanoferrate adalah
AFCF, ammonium ferric cyanoferrate,ammonium ferric ferrocyanida, ammonium
iron (3+), (1:1:1), (OC-6-II) ferrate (4-hexakis (Cyano-C)-ammonium iron (ii)
hexacyanoferrate, ammonium iron hexacyanoferrate, ammonium besi
hexacyanoferrate (Anonimous, 2008).
AFCF adalah zat yang digunakan untuk mengikat Cs, yakni mencegah
penyerapan radioaktif Cs dari saluran pencernaan. AFCF memiliki berat molekul
285,87 mol, penyerapan maksimum pada 685 nm, ditemukan memiliki absorbansi
sekitar 0,84. AFCF mengandung 30-35% ammonium klorida. Logam transisi
hexacyanoferrate sudah lama dikenal dalam pertukaran ion untuk mengikat Cs.
AFCF tersedia sebagai makanan tambahan untuk peternakan hewan dalam sebuah
+ +
serbuk kontaminan Cs-137 dan Cs-134 terakumulasi dan sisa serbuk tersebut larut
dalam air, untuk mengatasinya diberi dekontaminan dengan proses pertukaran ion
menggunakan AFCF (Schimansky, 1997).
Dekontaminan AFCF mengikat Cs-137 dengan proses pertukaran ion
(Anonimous, 2000). Reaksi yang terjadi adalah :
CN CN CN CN
AFCF lebih efektif dalam mengikat Cs-137 dalam saluran pencernaan
dibandingkan PB (Prussian Blue). Telah dilakukan pengujian bahwa AFCF
merupakan bahan yang praktis dan efisien pada kondisi setelah kecelakaan
Chernobyl karena dapat menambah serat pada hewan pemamah biak dan
membantu dalam memperkecil penyerapan Cs-137 dalam jaringan/otot (Marc,
2002).
AFCF dapat mencegah penyerapan Cs hampir sepenuhnya. Hal ini
dibuktikan dalam penelitian dengan menggunakan hewan percobaan rusa kutub
yang diberi AFCF 0,5 gr/hari dan bentonite sebesar 25 g/hari secara oral
Pemberian 5 mg AFCF secara oral pada tikus dapat mengeliminasi Cs-137
chernobyl, aktivitas Cs-137 telah direduksi dari 360 Bq/kg menjadi 10-30 Bq
dalam kondisi normal 27 hari (Dresow et al, 2000).
Penelitian lain menyebutkan bahwa pemberian AFCF sebanyak 0,2 gr
pada ayam hibro broiler yang telah diberikan campuran cesium-137 sebanyak 1
ml cesium-137 pada makanan dan pemberian secara oral, dalam 13 hari kadar
cesium-137 dalam daging mencapai 80-83% lebih rendah dibandingkan kontrol
yaitu 89% dalam hati dan 83-84% dalam ginjal (Mitrovic et al, 2007).
2.9. Monyet ekor Panjang (Macaca fascicularis)
Monyet ekor panjang merupakan salah satu jenis primata yang
populasinya cukup banyak. M. fascicularis telah digambarkan sebagai salah satu
“primata bukan manusia” yang paling berlimpah dan tersebar luas di dunia.
(Napier dan Napier 1967 dalam Urrochmah, 2007) monyet ekor panjang (Macaca
fascicularis) diklasifikasikan sebagai berikut :
Kingdom : Animalia
Filum : Chordata
Sub Filum : Vertebrata
Kelas : Mamalia
Ordo : Primata
Sub Ordo : Antropoidea
Famili : Cercopithecidae
Genus : Macaca
22
Monyet merupakan satwa primata yang memiliki filogenetika yang dekat
dengan manusia dan memiliki kesamaan anatomis karena mempunyai struktur
umum yang sama, misalnya memiliki organ yang hampir sama meskipun terdapat
perbedaaan-perbedaan anatomis lainnya (Bucaille, 2008).
Keberadaan monyet sebagai hewan coba sering dikaitkan dengan peran
monyet sebagai hewan model untuk menjelaskan kejadian penyakit pada manusia.
Khusus penggunaan monyet sebagai hewan coba, baru diijinkan manakala obat-
obatan ataupun bahan biologi lainnya yang diuji coba pada spesies yang memiliki
filogenik lebih rendah dari primata seperti pada mencit, tikus dan kelinci, bahkan
selain melalui pengujian in vivo tersebut, uji coba perlu didahului dengan uji coba
2.10. Kerangka Berpikir
Pemanfaatan Teknologi Nuklir dalam berbagai bidang
Terjadi Kecelakaan Radiasi
Unsur Radioaktif Terlepas ke lingkungan dan Terendap Dalam Tubuh
Muncul Kontaminasi (Zat Radioaktif) Cs-137
24
BAB III
METODOLOGI PENELITIAN
3.1. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Biomedika, Pusat Teknologi
Keselamatan dan Metrologi Radiasi, Badan Tenaga Nuklir Nasional (PTKMR-
BATAN) yang terletak di Jalan Lebak Bulus No. 49, Pasar Jum’at, Jakarta
Selatan. Waktu penelitian dilakukan pada bulan April sampai Juni 2009.
3.2. Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah alat pencacah
radioaktifitas Cs-137 di dalam sampel, yaitu sistem spektrometer gamma dengan
detektor NaI(Tl) model sumur (Well Type) merek BICRON dilengkapi dengan
perisai timbal (Pb). Kandang hewan uji dibuat dari besi berukuran tinggi 90 cm
dan lebar 60 cm, dilengkapi dengan tempat pakan berupa mangkuk terbuat dari
stainless steel dan tempat minum, di bawah kandang diberi penampung feses dan
urin berupa ember (metabolism cage). Jarum suntik, tempat sampel (vial),
timbangan, gunting, pinset dan kamera digital Fujifilm Finefix F480.
Bahan-bahan yang digunakan dalam penelitian ini adalah monyet ekor
panjang, kontaminan Cs-137 konsentrasi 1 µ Ci/ml, dekontaminan Ammonium
Iron (III) Hexacyanoferrate, obat bius (ketamine hydrochloride), kapas, masker
dan sarung tangan.
3.3. Metode Penelitian
Metode yang digunakan dalam penelitian ini adalah metode deskriptif dan
eksperimen dengan mengamati kondisi fisik dan perlakuan terhadap hewan
percobaan untuk menguji efektifitas AFCF dalam mereduksi Cs-137.
3.4. Cara Kerja
3.4.1. Perlakuan Terhadap Hewan Percobaan
Sebanyak 12 ekor monyet ekor panjang berumur ± 5 tahun dengan berat
badan ± 7 kg yang diperoleh dari bagian Primata IPB-Bogor, dipelihara dan
dikarantina dalam kandang hewan Laboratorium Biomedika selama 7 hari, diberi
makanan dan minuman serta dicek kesehatannya oleh dokter hewan (Lampiran 4).
Hewan dibagi ke dalam 4 kelompok, setiap kelompok terdiri dari 3 ekor dan
diberi perlakuan sebagai berikut :
No (Hewan Uji) Kontaminan Cs-137
1 µ Ci (ml)
Dosis total dekontaminan AFCF
(mg/ekor)
1 KEL 1 (3 ekor monyet) 1 3000
2 KEL 2 (3 ekor monyet) 1 4500
3 KEL 3 (3 ekor monyet) 1 6000
4 KEL 4 (3 ekor monyet) 1 0 (kontrol)
Semua hewan uji pada masing-masing kelompok diberikan kontaminan
Cs-137 sebanyak 1 ml dengan aktifitas 1 µ Ci secara oral, kemudian setelah satu
26
ditentukan pada masing-masing kelompok hewan uji. Pemberian AFCF dilakukan
sebanyak 3 kali sehari selama 3 hari berturut-turut pada monyet dalam keadaan
pingsan.
3.4.2. Pengambilan Sampel Feses dan Urin
Pengambilan sempel feses dan urin pada masing-masing kelompok
perlakuan dengan cara menampung dalam penampung feses dan urin (ember).
Untuk sampel urin diambil sebanyak 10 ml dengan menggunakan pipet posteur,
kemudian sampel dimasukkan ke dalam vial yang telah diberi label. Pengambilan
sampel urin dan feses dilakukan pada hari-hari ke 1, 2, 3, 4, 5, 6, 7, 9, 14, 21, 28
dan 35 pasca pemberian kontaminan Cs-137 dan dekontaminan AFCF.
3.4.3. Pengambilan Sampel Darah
Pengambilan sampel darah dilakukan dengan cara monyet dibius dengan
ketamin hydrochloride sebanyak 0,1 ml, setelah monyet pingsan dilakukan
pengambilan darah pada bagian vena kaki monyet sebanyak 5 ml dengan
menggunakan alat suntik, kemudian dimasukkan ke dalam vial yang telah diberi
label dan dilakukan pencacahan (Lampiran 4.2). Pengambilan sampel darah pada
hari-hari ke 1, 7, 14, 21, 28 dan 35 setelah pemberian kontaminan Cs-137 dan
3.4.4. Pengambilan sampel Organ dan Karkas
Pada hari ke 35 pasca kontaminasi dilakukan proses pembedahan monyet
setelah dibius dengan ketamin secara intramuskuler, setelah mati diambil organ-
organ tubuhnya yaitu hati, jantung, paru-paru, tulang, testis, limpa, otot, ginjal dan
karkas. Sampel organ tersebut ditempatkan pada vial berisi formalin yang telah
diberi label dan dilakukan pencacahan, setelah organ diambil, karkas ditempatkan
dalam wadah plastik (ember) yang direndam dalam 1-2,5 liter asam nitrat 65%,
sampai homogen, setelah homogen dimasukkan dalam vial yang telah diberi label
kemudian dilakukan pencacahan (Lampiran 4.2).
3.4.5. Pencacahan (counting)
Pencacahan sampel dilakukan untuk mengetahui aktivitas Cs-137 yang
terakumulasi dalam tubuh dan diekskresikan oleh monyet. Pencacahan dilakukan
dengan menggunakan Spektrometer gamma dengan cara sampel dalam vial
dimasukkan ke dalam tempat sampel berbentuk sumur yang dilapisi perisai timbal
(shielding), dilengkapi dengan detektor NaI(Tl) (Lampiran 4.1). Sebelum sampel
dicacah, terlebih dahulu dilakukan pencacahan standar dan Background,
kemudian dilakukan pencacahan sampel yang berada dalam vial. Pencacahan
dilakukan pada sampel hari ke-1 sampai sampel hari ke-35 dengan waktu
28
3.5. Analisis Data
Data yang diperoleh dianalisis dengan metode statistik untuk mengetahui
ada tidaknya perbedaan yang nyata antara aktivitas Cs-137 yang terakumulasi
dalam darah, organ dan terekskresi dalam feses dan urine berdasarkan dosis
pemberian AFCF dan waktu pengambilan sampel. Dalam analisis data digunakan
analisis variansi satu arah dengan menggunakan program SPSS 12 sebagai alat
bantu dan disain eksperimen melalui pola Rancangan Acak Lengkap (RAL).
Apabila terdapat berbedaan yang nyata maka dilanjutkan dengan uji Duncan
dengan taraf kepercayaan = 95%.
3.5.1. Perhitungan Aktivitas Cs-137 dalam Sampel (Bq)
Aktivitas Cs-137 dalam sampel dapat dihitung dengan menggunakan rumus
sebagai berikut :
Area Sampel Integral Waktu Cacah (detik)
Area Standar
Waktu Cacah (detik)
Aktivitas Sampel = Aktivitas Cs-137 dalam sampel pada saat pengukuran
(Bq)
cps Sampe = Jumlah cacahan per sekon sampel pada saat
pengukuran
cps Standar = Cacahan per sekon Cs-137 pada pengukuran
BG (Background) = Sumber alami
3.5.2. Presentase (%) Aktivitas Cs-137 dalam Sampel
% Aktivitas sampel = 37000 Bq – aktivitas sampel (Bq)
37000 Bq x 100%
% = 100 – Aktivitas Sampel
Keterangan :
37000 Bq = Aktivitas Cs-137 yang dimasukkan ke dalam tubuh monyet ekor
30
BAB IV
HASIL DAN PEMBAHASAN
4.1. Aktivitas Cs-137 Yang Terakumulasi Dalam Darah
Hasil pengamatan menunjukkan bahwa aktivitas Cs-137 yang
terakumulasi dalam darah pada monyet yang diberi dekontaminan AFCF lebih
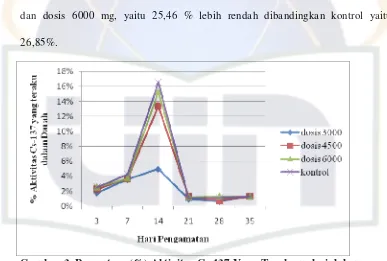
rendah dari pada kontrol (Gambar 3). Aktivitas Cs-137 yang terakumulasi paling
rendah terjadi pada dosis 3000 mg, yaitu 13,15%, dosis 4500 mg yaitu 22,57%
dan dosis 6000 mg, yaitu 25,46 % lebih rendah dibandingkan kontrol yaitu
26,85%.
Gambar 3. Persentase (%) Aktivitas Cs-137 Yang Terakumulasi dalam Darah Pasca Pemberian AFCF
Hasil analisis statistik menunjukkan bahwa rata-rata aktivitas Cs-137 yang
terakumulasi dalam darah pada keempat perlakuan tidak terdapat perbedaan yang
nyata (Lampiran 3.2a), maka pemberian dosis AFCF tidak memberikan pengaruh
yang signifikan terhadap aktivitas Cs-137 yang diekskresikan melalui urin.
Pemberian AFCF dapat menekan aktivitas Cs-137 dalam darah monyet
dibandingkan tanpa pemberian AFCF (kontrol), karena AFCF mampu mengikat
Cs-137 yakni mencegah penyerapan Cs-137, sehingga Cs-137 dapat langsung
diekskresikan melalui feses dan urin. Hasil pengamatan aktivitas Cs-137 harian
yang terakumulasi dalam darah menunjukkan bahwa terjadi peningkatan pada hari
ke-3, ke-7 dan ke-14, kemudian terjadi penurunan pada hari berikutnya kecuali
pada hari ke-35 terjadi peningkatan kembali aktivitas Cs-137 yang terakumulasi
dalam darah (Gambar 3).
Pengamatan hari ke-14 menunjukkan aktivitas Cs-137 yang paling tinggi
terakumulasi dalam darah, yaitu dosis 3000 mg terakumulasi sebesar 4,96%, dosis
4500 mg sebesar 13,36% dan dosis 6000 mg sebesar 15,31%, sedangkan kontrol
sebesar 16,55%. Peningkatan aktivitas Cs-137 pada hari ke-3, ke-7 dan ke-14
disebabkan karena Cs-137 yang terserap dalam darah tidak dikeluarkan dan hanya
terakumulasi dalam darah, di dalam organ tubuh dan diserap kembali oleh organ
tubuh yang lain sehingga aktivitas Cs-137 dalam darah meningkat. Hasil
penelitian Alatas et al (1996) menunjukkan bahwa peningkatan aktivitas Cs-137
yang terakumulasi dalam darah monyet disebabkan karena darah merupakan
media perpindahan radionuklida dari organ satu ke organ yang lain.
Aktivitas Cs-137 dalam darah pada hari ke-21 dan ke-28 mengalami
penurunan karena telah terserap oleh organ lain atau telah diekskresikan melalui
feses dan urin, dengan demikian kondisinya diduga telah kembali normal.
Meningkatnya aktivitas Cs-137 dalam darah hari ke-35 yaitu pada dosis 3000 mg
32
1,29% dan kontrol sebesar 1,28%, karena ada kemungkinan Cs-137 berpindah
dari satu jaringan ke jaringan lain sehingga terjadi peningkatan aktivitas Cs-137
pada hari terakhir pengamatan.
Pengamatan hari ke-1 sampai ke-35 menunjukkan bahwa dosis 3000 mg
paling efektif menekan aktivitas Cs-137 dalam darah dibandingkan dosis 4500
mg, 6000 mg dan 0 (kontrol). Dengan demikian dapat diketahui semakin rendah
dosis yang diberikan ternyata semakin kecil aktivitas Cs-137 yang terakumulasi
dalam darah.
4.2. Aktivitas Cs-137 Yang Terakumulasi Dalam Organ
Kontaminan Cs-137 yang masuk ke dalam sirkulasi darah akan dibawa ke
seluruh tubuh dan kontak dengan jaringan-jaringan/organ tubuh. Hasil
pengamatan Aktivitas Cs-137 yang terakumulasi dalam organ pada hari ke-35
pasca pemberian kontaminan, menunjukkan bahwa aktivitas Cs-137 pada monyet
yang diberi dekontaminan AFCF lebih rendah terakumulasi dalam organ daripada
kontrol (Gambar 4). Aktivitas Cs-137 yang terakumulasi paling rendah terjadi
pada dosis 3000 mg yaitu 21%, dosis 4500 mg yaitu 21,52% dan dosis 6000 mg
yaitu 23,45 % lebih rendah dibandingkan kontrol yaitu 41,23%.
Berdasarkan analisis statistik, menunjukkan bahwa rata-rata aktivitas Cs-
137 yang terakumulasi dalam organ dan karkas pada keempat perlakuan tidak
menunjukkan perbedaan yang nyata (Lampiran 3.2b). Pemberian dosis AFCF
ternyata tidak memberikan pengaruh yang signifikan terhadap aktivitas Cs-137
Gambar 4. Persentase (%) Aktivitas Cs-137 Yang Terakumulasi Dalam Organ Hari ke-35 Pasca pemberian AFCF
Pemberian AFCF dapat menekan aktivitas Cs-137 dalam organ, akan
tetapi hasil pengamatan menunjukkan bahwa Aktivitas Cs-137 yang terakumulasi
dalam organ hari ke-35 pasca pemberian dekontaminan cukup tinggi. Aktivitas
yang paling tinggi yaitu pada karkas, kemudian organ lain yang menunjukkan
aktivitas cukup tinggi yaitu pada ginjal, limpa dan tulang. Meningkatnya aktivitas
Cs-137 dalam organ karena terjadinya penurunan aktivitas Cs-137 dalam darah
pada hari ke-35. Hal ini menunjukkan bahwa telah terjadinya perpindahan Cs-137
dari darah ke dalam cairan tubuh lainnya (limpa dan cairan ekstra vaskuler),
jaringan serta organ-organ.
Aktivitas Cs-137 yang terakumulasi dalam karkas menunjukkan aktivitas
Cs yang paling tinggi yaitu pada dosis 3000 mg sebesar 6,16%, dosis 4500 mg
sebesar 6,48%, dan dosis 6000 mg sebesar 7,42%, sedangkan kontrol sebesar
34
penjumlahan dari aktivitas sisa darah, tulang, otot dan organ/jaringan tubuh
monyet. Basyarahil (1997) menyatakan bahwa aktivitas Cs-137 sangat tinggi
terakumulasi dalam karkas karena serapan dari Cs-137 setelah diikat oleh
dekontaminan AFCF banyak tersisa dalam karkas.
Aktivitas Cs-137 dalam ginjal terlihat paling tinggi setelah karkas. yaitu
pada dosis 3000 mg sebesar 2,63%, dosis 4500 mg sebesar 2,44% dan dosis 6000
sebesar 2,74%, sedangkan pada kontrol lebih tinggi yaitu 2,81%. Tingginya
aktivitas Cs-137 dalam ginjal, karena pengaruh dari peningkatan aktivitas Cs-137
yang terakumulasi dalam darah pada hari ke-35. Meningkatnya aktivitas Cs-137
dalam darah akan menyebabkan aktivitas Cs-137 dalam ginjal meningkat. Dakk
(2002) menyatakan bahwa ginjal mempunyai kemampuan yang tinggi untuk
mengikat zat-zat kimia dan menghimpun toksikan-toksikan melebihi organ-organ
lain.
Tingginya aktivitas Cs-137 yang terakumulasi dalam tulang, yaitu dosis
3000 mg sebesar 2,28%, dosis 4500 mg sebesar 2,61%, dosis 6000 mg sebesar
2,58% sedangkan pada kontrol lebih tinggi yaitu sebesar 2,58%. Hal tersebut
nenunjukkan bahwa banyak terjadi penyerapan Cs-137 di dalam tulang. Data
tersebut sesuai dengan hasil penelitian Alatas et al (1996) yang menyatakan
bahwa tingginya aktivitas Cs-137 yang terakumulasi dalam tulang karena tulang
merupakan salah satu organ target Cs-137.
Terjadinya peningkatan Aktivitas Cs-137 yang terakumulasi dalam organ-
organ target Cs-137 dapat diminimalisir dengan pemberian AFCF sehingga dapat
yang cukup rendah telihat pada organ jantung, otot, hati, paru dan paling rendah
yaitu testis.
Aktivitas Cs-137 yang terakumulasi ditestis menunjukkan nilai yang
paling rendah dibandingkan organ lain. Dosis 3000 mg aktivitas Cs-137 yang
terukur sebesar 0,80%, dosis 4500 mg sebesar 0,73% dan dosis 6000 mg sebesar
0,69%, sedangkan kontrol aktivitas Cs-137 yang terakumulasi dalam testis yaitu
sebesar 0,93%. Hal ini menunjukkan bahwa pemberian AFCF dapat
meminimalisir penyerapan Cs-137 dalam testis.
Pemberian AFCF dapat menekan aktivitas Cs-137 dalam organ monyet
dibandingkan tanpa pemberian AFCF (kontrol), karena pemberian AFCF efektif
mencegah penyerapan Cs-137 melalui pencernaan sehingga pengendapan Cs-137
dalam organ dapat diminimalisir sekecil mungkin. Pemberian AFCF dosis 3000
mg paling efektif menekan aktivitas Cs-137 dalam organ dibandingkan dosis 4500
mg, 6000 mg dan 0 (kontrol). Dengan demikian dapat diketahui semakin rendah
dosis yang diberikan ternyata semakin kecil aktivitas Cs-137 yang terakumulasi
dalam darah
4.3. Aktivitas Cs-137 Yang Diekskresikan Melalui Urin
Urin merupakan produk utama untuk proses penghilangan bahan bersifat
racun/radioaktif. Persenyawaan dalam tubuh yang telah dibiotransformasikan ke
dalam bentuk produk dilarutkan dengan air yang dikeluarkan adalah dalam bentuk
urin. Hasil pengamatan menunjukkan bahwa aktivitas Cs-137 yang diekskresikan
36
kontrol (Gambar 5). Aktivitas Cs-137 yang diekskresikan paling tinggi terjadi
pada dosis 6000 mg yaitu 20,50%, dosis 4500 mg yaitu 17,70% dan dosis 3000
mg yaitu 17,63% dibandingkan kontrol yaitu 15,05% (Gambar 5).
Gambar 5. Persentase (%) Aktivitas Cs-137 Yang Diekskresikan Melalui Urin Pasca Pemberian AFC
Hasil analisis statistik menunjukkan bahwa rata-rata aktivitas Cs-137 yang
diekskresikan melalui urin pada keempat perlakuan tidak terdapat perbedaan yang
nyata (Lampiran 3.2c). Pemberian dosis AFCF ternyata tidak memberikan
pengaruh yang signifikan terhadap aktivitas Cs-137 yang diekskresikan melalui
urin.
Hasil pengamatan aktivitas Cs-137 harian yang diekskresikan melalui urin
pasca pemberian dekontaminan AFCF dengan dosis 3000 mg, 4500 mg, 6000 mg
dan 0 (kontrol) menunjukkan perbedaan dalam mengekskresikan Cs-137.
Aktivitas Cs-137 yang diekskresikan paling tinggi melalui urin terjadi pada hari
Aktivitas Cs-137 yang diekskresikan melalui urin pada hari ke-1
menunjukkan aktivitas yang paling tinggi, yaitu dosis 3000 mg mampu
mengekskresikan sebesar 9,36%, dosis 4500 mg sebesar 10,97%, dosis 6000 mg
sebesar 12,01% dan kontrol sebesar 8,74%. Hal ini disebabkan pengaruh fisiologi
monyet. Hasil penelitian Rahardjo (2007) menyebutkan bahwa terjadinya
peningkatan aktivitas Cs-137 yang diekskresikan melalui urin karena monyet
banyak mengkonsumsi air, sehingga banyak pula mengeluarkan urin dan
menyebabkan proses pelarutan di dalam tubuhnya lebih cepat.
Pengamatan hari ke-2 sampai ke-35 terjadi penurunan aktivitas Cs-137
dalam urin, kecuali pada hari ke-14 dan hari ke-28 terjadi peningkatan. Hari ke-
14 terjadi peningkatan pada dosis 3000 mg, yaitu sebesar 0,20% dan kontrol
sebesar 0,24%. Peningkatan tersebut terjadi karena aktivitas Cs-137 yang
terakumulasi dalam darah pada hari ke-14 cukup rendah pada dosis 3000 mg.
Rendahnya aktivitas Cs-137 tersebut menyebabkan tingginya aktivitas Cs-137
yang diekskresikan melalui urin, karena Cs-137 yang terakumulasi dalam darah
sudah diekskresikan melalui urin.
Pengamatan hari ke-35 terjadi penurunan aktivitas Cs-137 yang
diekskresikan melalui urin. Dosis 3000 mg mampu mengekskresikan Cs-137
melalui urin sebesar 0,07%, dosis 0,05%, dosis 6000 mg sebesar 0,05%
sedangkan kontrol sebesar 0,06%. Terjadinya penurunan aktivitas pada hari ke-35,
diduga karena pada hari ke-35 aktivitas Cs-137 sudah banyak terakumulasi dalam
organ/karkas dan sudah terjadi penyerapan dalam jaringan-jaringan tubuh,
38
menerangkan bahwa perpindahan senyawa kimia dari darah ke dalam cairan atau
organ ekskretori (misalnya urin, paru atau ginjal), menyebabkan berkurangnya
toksik di dalam tubuh.
Dosis 6000 mg paling efektif meningkatkan aktivitas Cs-137 yang
diekskresikan melalui urin dibandingkan dosis 3000 mg, 6000 mg dan kontrol.
Dengan demikian dapat diketahui semakin tinggi dosis yang diberikan
kemungkinan semakin tinggi aktivitas Cs-137 yang diekskresikan melalui urin.
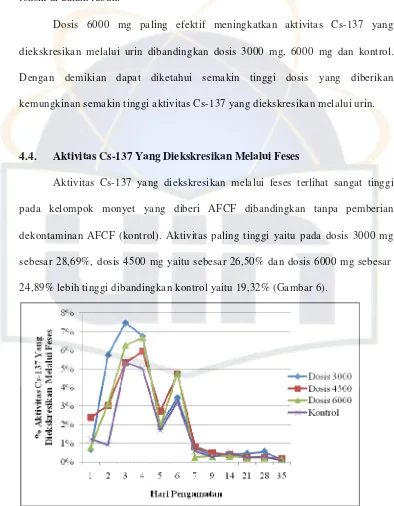
4.4. Aktivitas Cs-137 Yang Diekskresikan Melalui Feses
Aktivitas Cs-137 yang diekskresikan melalui feses terlihat sangat tinggi
pada kelompok monyet yang diberi AFCF dibandingkan tanpa pemberian
dekontaminan AFCF (kontrol). Aktivitas paling tinggi yaitu pada dosis 3000 mg
sebesar 28,69%, dosis 4500 mg yaitu sebesar 26,50% dan dosis 6000 mg sebesar
24,89% lebih tinggi dibandingkan kontrol yaitu 19,32% (Gambar 6).
Hasil analisis statistik menunjukkan bahwa rata-rata aktivitas Cs-137 yang
diekskresikan melalui feses pada keempat perlakuan tidak terdapat perbedaan
yang nyata (Lampiran 3.2d). Hal ini menunjukkan bahwa pemberian dosis AFCF
tidak memberikan pengaruh yang signifikan terhadap aktivitas Cs-137 yang
diekskresikan melalui feses, karena masing-masing perlakuan mampu
mengekskresikan Cs-137 yang hampir sama. Namun hasil persentase menunjukan
bahwa dosis 3000 mg paling efektif mengekskresikan Cs-137 dari dalam tubuh
dibandingkan dosis lain.
Peningkatan Aktivitas Cs-137 yang diekskresikan melalui feses hari ke-1,
yaitu dosis 4500 sebesar 2,39% dan kontrol sebesar 1,21%, sedangkan dosis 3000
mg dan 6000 mg belum menunjukkan peningkatan, Karena hari ke-1 Cs-137 telah
diekskresikan cukup tinggi melalui feses, sehingga cukup sedikit diekskresikan
melalui urin. Namun dosis 4500 mg sudah menunjukkan peningkatan
dibandingkan dosis 3000 mg, 6000 mg dan 0 (kontrol). Peningkatan aktivitas Cs-
137 dosis 4500 mg disebabkan pemberian AFCF pada monyet tidak langsung
dicerna oleh sistem tubuhnya, dekontaminan AFCF langsung mengikat Cs-137
di dalam saluran pencernaan dan langsung dikeluarkan sehingga terjadi
peningkatan aktivitas Cs-137 pada hari pertama.
Aktivitas Cs-137 yang diekskresikan paling tinggi terjadi pada hari ke-3.
Dosis 3000 mg menunjukkan aktivitas yang paling tinggi, yaitu sebesar 7,48%,
dibandingkan dosis 4500 mg sebesar 5,31%, dosis 6000 mg sebesar 3,11% dan
40
sehingga radionuklida Cs-137 dapat terikat oleh AFCF dalam saluran pencernaan
dan dapat dikeluarkan melalui feses dengan jumlah relatif besar. Peningkatan ini
juga dipengaruhi oleh aktivitas darah dan ekskresi Cs-137 melalui urin. Terlihat
pada hari ke-3 rendahnya aktivitas Cs-137 dalam darah dan rendahnya aktivitas
Cs-137 melalui urin, sehingga tingginya aktivitas Cs-137 yang diekskresikan
melalui feses.
Dosis 3000 mg paling efektif meningkatkan aktivitas Cs-137 yang
diekskresikan melalui feses dibandingkan dosis 4500 mg, 6000 mg dan 0
(kontrol). Dengan demikian dapat diketahui, ternyata dosis yang rendah lebih
tinggi dalam mengekskresikan Cs-137 melalui feses dan tingginya aktivitas Cs-
137 yang diekskresikan melalui feses menyebabkan rendahnya aktivitas yang
terakumulasi dalam darah dan organ, sehingga tidak terjadinya pengendapan
radionuklida terlalu lama dalam tubuh. Tingginya aktivitas Cs-137 pada dosis
3000 mg karena dosis 3000 mg paling tinggi menekan Cs-137 dalam darah pada
hari ke-3, sehingga aktivitas Cs-137 banyak diekskresikan melalui feses pada hari
tersebut.
4.5. Total Aktivitas Cs-137 Yang Diekskresikan Melalui Urin dan Feses
Hari ke-1 Sampai ke-35
Hasil total aktivitas Cs-137 yang diekskresikan melalui urin dan feses pada
tubuh monyet terlihat sangat tinggi pada kelompok monyet yang diberi AFCF
dibandingkan tanpa pemberian dekontaminan AFCF (kontrol). Aktivitas Cs-137
sedangkan dosis 4500 mg 44,20%, dosis 6000 mg 45,39% dan kontrol hanya
mampu mengekskresikan 34,36% (Gambar 7).
Gambar 7. Persentase (%)Total Aktivitas Cs-137 Hari 1 sampai Hari ke-35 Pasca Pemberian AFCF
Dosis 3000 mg lebih efektif mengekskresikan Cs-137 melalui feses dan
urin dibandingkan dosis lain. Namun demikian jika dilihat dari hasil statistik,
menunjukkan bahwa antar perlakuan tidak terdapat perbedaan yang signifikan
pada urin dan feses dalam mengekskresikan Cs-137 (Lampiran 3.2). Data tersebut
menunjukkan bahwa semakin rendah dosis yang diberikan mampu
mengekskresikan Cs-137 lebih tinggi. Berbeda dengan hasil penelitian Sanusi
(2007) yang menunjukkan bahwa Prusian Blue (PB) mampu mengekskresikan
Cs-137 melalui urin dan feses lebih kecil dari AFCF yaitu sebesar 26%. Hal ini
menunjukkan bahwa AFCF lebih efektif dibandingkan PB.
Diketahui juga bahwa pengeluaran Cs-137 lebih banyak diekskresikan
42
penelitian yang telah dilakukan oleh Sanusi (2007) yang menunjukkan bahwa Cs-
137 lebih banyak dikeluarkan melalui feses daripada melalui urin. Hal ini diduga
karena cara pemberian radionuklida Cs-137 yang dilakukan secara oral, sehingga
Cs-137 yang diberikan sudah diikat terlebih dahulu oleh AFCF di dalam saluran
pencernaan kemudian dikeluarkan melalui feses lebih banyak. Lamanya proses
ekskresi yang berlangsung di dalam ginjal juga menyebabkan sedikitnya aktivitas
Cs-137 yang diekskresikan melalui urin.
Aktivitas Cs-137 yang diekskresikan melalui urin dan feses sangat
berhubungan dengan waktu paruh biologi. Lab. Farmakologi (1991) menyatakan
bahwa parameter yang penting untuk diketahui dan berhubungan dengan
pengeluaran zat kimia dari dalam tubuh adalah waktu paruh t1/2.
Gambar 8. Persentase (%) Aktivitas Cs-137 yang Tersisa Dalam Tubuh Pasca Pemberian AFCF
Aktivitas Cs-137 dalam tubuh yang diekskresikan melalui urin dan feses
hari ke-1 sampai ke-35 terlihat belum mencapai setengahnya (50%) (Gambar 8).