ISOLASI DAN KARAKTERISASI SENYAWA
STEROID/TRITERPENOID DARI AKAR TANAMAN EKOR NAGA (Rhaphidophora pinnata Schott)
SKRIPSI
Oleh:
SISKA ESPERANZA SINULINGGA 071524065
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
ISOLASI DAN KARAKTERISASI SENYAWA
STEROID/TRITERPENOID DARI AKAR TANAMAN EKOR NAGA (Rhaphidophora pinnata Schott)
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
SISKA ESPERANZA SINULINGGA 071524065
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
Pengesahan Skripsi
ISOLASI DAN KARAKTERISASI SENYAWA
STEROID/TRITERPENOID DARI AKAR TANAMAN EKOR NAGA (Rhaphidophora pinnata Schott)
Oleh:
SISKA ESPERANZA SINULINGGA 071524065
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal : Mei 2011 Disetujui oleh:
Pembimbing I, Panitia Penguji
Dra. Aswita Hafni Lubis, MSi, Apt Dr. M. Pandapotan Nasution, MPS., Apt.
NIP 195304031983032001 NIP 194908111976031001
Pembimbing II Dra. Aswita Hafni Lubis, MSi, Apt NIP 195304031983032001
(Dra. Awaluddin Saragih, MSi, Apt) (Dra. Suwarti Aris, M.Si., Apt.) NIP 195709091985112001 NIP 195107231982032001
(Drs.Panal Sitorus, M.Sc., Apt.) NIP 195310301980031002
Dekan
Isolasi dan Karakterisasi Senyawa Steroid/Triterpenoid
dari Akar Tanaman Ekor Naga (Rhaphidophora pinnata Schott) Abstrak
Daun ekor naga (Rhaphidophorae folium) dapat berkhasiat sebagai anti bakteri dan antikanker. Salah satu kandungan kimia daun tumbuhan ini adalah steroid/triterpenoid. Namun akarnya belum pernah diketahui kegunaannya. Tujuan penelitian ini adalah untuk mengisolasi senyawa steroid/ triterpenoid dari akar ekor naga dan mengidentifikasi isolat dengan Spektrofotometer ultraviolet dan Spektrofotometer inframerah.
Pada penelitian ini dilakukan pemeriksaan karakteristik simplisia, skrining fitokimia, selanjutnya ekstraksi secara perkolasi dengan pelarut n-heksan lalu dilanjutkan dengan isolasi senyawa steroid/triterpenoid. Ekstrak n-heksan dianalisis secara Kromatografi Lapis Tipis (KLT) menggunakan berbagai perbandingan fase gerak, yaitu n-heksan-etilasetat (90:10), (80:20), (70:30), dan (60:40) dengan penampak bercak Liebermann-Burchard. Ekstrak n-heksan dipisahkan secara kromatografi kolom menggunakan fase gerak heksaetilasetat (80:20), dilanjutkan dengan KLT 2 arah menggunakan fase gerak n-heksan-etil asetat (80:20) dan benzen-etilasetat (60:40). Kemudian isolat dikarakterisasi dengan Spektrofotometer Ultraviolet dan Spektrofotometer Inframerah.
Hasil pemeriksaan makroskopik akar ekor naga adalah berbentuk lonjong memanjang, berwarna coklat, tidak berbau, dan tidak berasa dan simplisia
berwarna coklat tua. Hasil mikroskopik terhadap serbuk simplisia menunjukkan adanya jaringan gabus, xylem dengan penebalan bentuk tangga, serabut
sklerenkim, sel batu dan rambut akar. Hasil karakterisasi diperoleh kadar air serbuk simplisia sebesar 6%, kadar sari yang larut dalam air 24,15%, kadar sari yang larut dalam etanol 17,16%, kadar abu total 7,46% dan kadar abu yang tidak larut dalam asam 2,35%. Hasil skrining fitokimia menunjukkan adanya senyawa golongan steroid/triterpenoid, flavonoid, glikosida, saponin, dan tanin. Hasil kromatografi kolom diperoleh kristal pada isolat F3 yang memberikan harga Rf 0,48 (ungu ) , 0,48 (ungu), 0,48 ( ungu), 0,48 (ungu)dan 0,48 (ungu). Hasil spektrofotometri ultraviolet dan inframerah isolat F3 diperoleh panjang
gelombang maksimum (λ) 224 nm dan adanya gugus C=O, C=C aromatik, , C-O,O-H, C-H alifatis, dan C-H metil yang menunjukkan adanya senyawa steroid/triterpenoid
Isolation and Characterization of Steroid/Triterpenoid from Monster fruit root (Rhaphidophora pinnata Schott)
Abstract
The folium of the monster fruit can be efficacious as an antibactery and anticancer. One of the chemical constituents of the folium of this plant is
steroid/triterpenoid. But,the function of its root have never known.The purpose of this research is to isolate the steroid/triterpenoid from the root and to do the characterization of the isolates using ultraviolet and infrared Spectrophotometer.
On this research was examined for characteristics of simplex
,phytochemical screening, extracted by percolation with n-hexane as the solvent then performed the isolation of steroid/triterpenoid compound. The n-hexane extract was analyzed by Thin Layer Chromatography (TLC) using various mobile phase ratio, which were n-hexane-ethylacetate (90:10), (80:20), (70:30), and (60:40) with the Liebermann-Burchard sprayed reagent. The n-hexane extract were separated by column chromatography using mobile phase hexane-ethylacetate (80:20), continued with preparative TLC using mobile phase n-hexane-ethylacetate (80:20)and benzene-ethylacetate (60:40), Then the isolates were characterized by ultraviolet and infrared Spectrophotometer.
The result of macroscopic examination of ekor naga root is elongated oval-shaped, brown in color, odorless, and tasteless, which was dark brown colour. Microscopic results of simplex powder showed the existence of core tissue, xylem with thickening of the stairs ,fiber schlerencym, stone cells, and hair roots. Characterize result are the water content of simplex powder is 6%, the water-soluble extract content is 24,15%, the ethanol-water-soluble extract content is 17,16%, the total ash content is 7,46 % and the acid insoluble ash content is 2,35%. The result of the phytochemical screening showed the existence of flavonoids, glycosides, saponins, tannins, triterpenoids/steroids . The result of the column chromatography was triterpenoid isolate on F3 that gives the Rf value 0,48
(purple) , 0,48 (purple), 0,48 ( purple), 0,48 ( purple) and 0.48 (purple). The result of the ultraviolet and infrared spectrophotometry of F3 isolates obtained
maximum wavelength (λ) 224 nm, the existence of clusters C=O, C=C aromatic, C-O, O-H, C-H alifatis, and C-H methyl that indicated steroid/triterpenoid compound
Keywords: root of monster fruit, steroid/triterpenoid, Thin Layer Cromatography, Spectrophotometer, Column
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT ... iv
DAFTAR ISI ... v
DAFTAR LAMPIRAN ... vii
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
BAB I. PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Hipotesa ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II. TINJAUAN PUSTAKA 2.1 Uraian Tanaman Ekor Naga ... 5
2.1.1 Sinonim ... 5
2.1.2 Nama Daerah ... 5
2.1.3 Sistematika Tanaman Ekor Naga ... 6
2.1.4 Kegunaan Tanaman Ekor Naga ... 6
2.2 Uraian Kimia Triterpenoid ... 6
2.3 Ekstraksi ... 8
2.4 Uraian Tanaman Ekor Naga ... 5
2.1.1 Sinonim ... 5
2.1.2 Nama Daerah ... 5
2.1.3 Sistematika Tanaman Ekor Naga ... 6
2.1.4 Kegunaan Tanaman Ekor Naga ... 6
2.2 Uraian Kimia Triterpenoid ... 6
2.3 Ekstraksi ... 6
2.4 Kromatografi ... 10
2.4.1 Kromatografi Lapis Tipis ... 12
2.4.2 Kromatografi Kolom ... 14
2.5 Spektroskopi ... 15
2.5.1 Spektrofotometer UV ... 16
2.5.2 Spektrofotometrii IR ... 17
BAB III METODOLOGI PENELITIAN 3.1 Alat-alat yang digunakan ... 20
3.2 Bahan-bahan yang digunakan ... 20
3.3 Pembuatan Larutan Pereaksi ... 21
3.3.1 Larutan Pereaksi Bouchardat ... 21
3.3.3 Larutan Pereaksi Molish ... 21
3.3.4 Larutan Pereaksi Besi (III) Klorida ... 21
3.3.5 Larutan Pereaksi Timbal (II) Asetat 0,4M ... 21
3.3.6 Larutan Pereaksi Asam Klorida 2N ... 21
3.3.7 Larutan Pereaksi Natrium Hidroksida 2N ... 22
3.3.8 Larutan Pereaksi Mayer ... 22
3.3.9 Larutan Penyemprot Liebermann – Burchard ... 22
3.4 Pengumpulan dan Pengolahan Sampel ... 22
3.4.1 Pengumpulan Sampel ... 22
3.4.2 Identifikasi Sampel ... 22
3.4.3 Pengolahan Sampel ... 23
3.5 Pemeriksaan Karakteristik Simplisia ... 23
3.5.1 Pemeriksaan Makroskopik ... 23
3.5.2 Pemeriksaan Mikroskopik ... 23
3.5.3 Penetapan Kadar Air ... 24
2.5.4 Penetapan Kadar Sari yang Larut Dalam Air ... 24
3.5.5 Penetapan Kadar Sari yang Larut Dalam Etanol ... 24
3.5.6 Penetapan Kadar Abu Total ... 24
3.5.7 Penetapan Kadar Abu yang Tidak Larut Dalam Asam 25 3.6 Skrining Fitokimia ... 26
3.6.1 Pemeriksaan Alkaloida ... 26
3.6.2 Pemeriksaan Glikosida ... 26
3.6.3 Pemeriksaan Steroid/ Triterpenoid ... 27
3.6.4 Pemeriksaan Flavonoida ... 27
3.6.5 Pemeriksaan Tannin ... 27
3.6.6 Pemeriksaan Saponin ... 27
3.6.7 Pemeriksaan Glikosida Antrakuinon ... 28
3.7 Pembuatan Ekstrak... 28
3.8 Analisis Ekstrak n-heksan secara KLT ... 28
3.9 Fraksinasi Ekstrak n-heksan secara KK ... 31
3.10 Analisis KLT Hasil KK ... 32
3.11 Pencucian Kristal ... 32
3.12 Uji Kemurnian Isolat... 32
3.1.13 Karakterisasi Isolat... 33
3.13.1 Karakterisasi Isolat secara Spektrofotometri UV ... 33
3.13.2 Karakterisasi Isolat secara Spektrofotometri IR .... 33
BAB IV. HASIL DAN PEMBAHASAN ... 35
4.1 Hasil Identifikasi Tumbuhan ... 35
4.2 Hasil Pemeriksaan Makroskopik Akar Ekor Naga ... 36
4.3 Hasil Pemeriksaan Mikroskopik Serbuk Akar Ekor Naga ... 37
4.4 Hasil Pemeriksaan Karakteristik Simplisia ... 38
4.5 Hasil Ekstraksi dan Isolasi ... 39
4.6 Hasil Analisis Ekstrak n-heksan dengan cara KLT ... 40
4.7 Hasil Pemisahan Senyawa Steroid /Triterpenoid dari fraksi n-heksan dengan cara Kromatografi Kolom ... 41
4.8 Hasil Pengujian dengan KLT 2 Arah ... 43
4.10 Hasil Karakterisasi Isolat secara Spektrofotometri IR ... 45
BAB V. KESIMPULAN DAN SARAN ... 47
DAFTAR PUSTAKA ... 48
DAFTAR LAMPIRAN
Lampiran Halaman 1 Hasil Identifikasi Tumbuhan Ekor Naga
(Rhaphidophora pinnata Schott) ... 50 2 Gambar Tumbuhan Ekor Naga (Rhaphidophora
pinnata Schott ) ... 51 3 Gambar Simplisia dan Akar Tanaman
Ekor Naga (Rhaphidophora pinnata Schott) ... 52
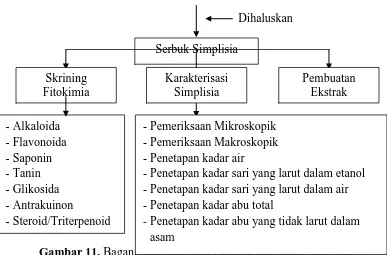
4 Bagan Pembuatan dan Pemeriksaan
Mutu Simplisia ... 53
DAFTAR TABEL
Tabel Halaman
1 Hasil Penetapan Karakterisasi Simplisia Akar Ekor Naga
(Rhaphidophora pinnata Schott) ……… 38
2 Hasil Skrining Fitokimia Serbuk Simplisia Akar Ekor Naga
DAFTAR GAMBAR
Gambar Halaman 1 Tanaman ekor naga (Rhaphidophora pinnata Schott ) ...
50
2 Akar Tanaman ekor naga (Rhaphidophora pinnata Radix ) ... 52
3 Simplisia akar ekor naga (Rhaphidophorae pinnatae Radix ) ... 52
4 Pemeriksaan mikroskopik penampang melintang akar tanaman ekor naga (Rhaphidophora pinnata Radix ) ... 36
5 Pemeriksaan mikroskopik serbuk simplisia akar tanaman ekor naga (Rhaphidophorae pinnatae Radix ) ... 37
6 Kromatogram analisis Kromatografi Lapis Tipis Ekstrak n-heksan akar ekor naga ... 25
7 Kromatogram analisis Kromatografi Lapis Tipis eluat hasil Kromatografi Kolom fraksi n-heksan akar ekor naga... 26
8 Kromatogram KLT 2 Arah Ekstrak n-heksan akar ekor naga ... 28
9 Spektrum Ultraviolet Isolat ... 29
Isolasi dan Karakterisasi Senyawa Steroid/Triterpenoid
dari Akar Tanaman Ekor Naga (Rhaphidophora pinnata Schott) Abstrak
Daun ekor naga (Rhaphidophorae folium) dapat berkhasiat sebagai anti bakteri dan antikanker. Salah satu kandungan kimia daun tumbuhan ini adalah steroid/triterpenoid. Namun akarnya belum pernah diketahui kegunaannya. Tujuan penelitian ini adalah untuk mengisolasi senyawa steroid/ triterpenoid dari akar ekor naga dan mengidentifikasi isolat dengan Spektrofotometer ultraviolet dan Spektrofotometer inframerah.
Pada penelitian ini dilakukan pemeriksaan karakteristik simplisia, skrining fitokimia, selanjutnya ekstraksi secara perkolasi dengan pelarut n-heksan lalu dilanjutkan dengan isolasi senyawa steroid/triterpenoid. Ekstrak n-heksan dianalisis secara Kromatografi Lapis Tipis (KLT) menggunakan berbagai perbandingan fase gerak, yaitu n-heksan-etilasetat (90:10), (80:20), (70:30), dan (60:40) dengan penampak bercak Liebermann-Burchard. Ekstrak n-heksan dipisahkan secara kromatografi kolom menggunakan fase gerak heksaetilasetat (80:20), dilanjutkan dengan KLT 2 arah menggunakan fase gerak n-heksan-etil asetat (80:20) dan benzen-etilasetat (60:40). Kemudian isolat dikarakterisasi dengan Spektrofotometer Ultraviolet dan Spektrofotometer Inframerah.
Hasil pemeriksaan makroskopik akar ekor naga adalah berbentuk lonjong memanjang, berwarna coklat, tidak berbau, dan tidak berasa dan simplisia
berwarna coklat tua. Hasil mikroskopik terhadap serbuk simplisia menunjukkan adanya jaringan gabus, xylem dengan penebalan bentuk tangga, serabut
sklerenkim, sel batu dan rambut akar. Hasil karakterisasi diperoleh kadar air serbuk simplisia sebesar 6%, kadar sari yang larut dalam air 24,15%, kadar sari yang larut dalam etanol 17,16%, kadar abu total 7,46% dan kadar abu yang tidak larut dalam asam 2,35%. Hasil skrining fitokimia menunjukkan adanya senyawa golongan steroid/triterpenoid, flavonoid, glikosida, saponin, dan tanin. Hasil kromatografi kolom diperoleh kristal pada isolat F3 yang memberikan harga Rf 0,48 (ungu ) , 0,48 (ungu), 0,48 ( ungu), 0,48 (ungu)dan 0,48 (ungu). Hasil spektrofotometri ultraviolet dan inframerah isolat F3 diperoleh panjang
gelombang maksimum (λ) 224 nm dan adanya gugus C=O, C=C aromatik, , C-O,O-H, C-H alifatis, dan C-H metil yang menunjukkan adanya senyawa steroid/triterpenoid
Isolation and Characterization of Steroid/Triterpenoid from Monster fruit root (Rhaphidophora pinnata Schott)
Abstract
The folium of the monster fruit can be efficacious as an antibactery and anticancer. One of the chemical constituents of the folium of this plant is
steroid/triterpenoid. But,the function of its root have never known.The purpose of this research is to isolate the steroid/triterpenoid from the root and to do the characterization of the isolates using ultraviolet and infrared Spectrophotometer.
On this research was examined for characteristics of simplex
,phytochemical screening, extracted by percolation with n-hexane as the solvent then performed the isolation of steroid/triterpenoid compound. The n-hexane extract was analyzed by Thin Layer Chromatography (TLC) using various mobile phase ratio, which were n-hexane-ethylacetate (90:10), (80:20), (70:30), and (60:40) with the Liebermann-Burchard sprayed reagent. The n-hexane extract were separated by column chromatography using mobile phase hexane-ethylacetate (80:20), continued with preparative TLC using mobile phase n-hexane-ethylacetate (80:20)and benzene-ethylacetate (60:40), Then the isolates were characterized by ultraviolet and infrared Spectrophotometer.
The result of macroscopic examination of ekor naga root is elongated oval-shaped, brown in color, odorless, and tasteless, which was dark brown colour. Microscopic results of simplex powder showed the existence of core tissue, xylem with thickening of the stairs ,fiber schlerencym, stone cells, and hair roots. Characterize result are the water content of simplex powder is 6%, the water-soluble extract content is 24,15%, the ethanol-water-soluble extract content is 17,16%, the total ash content is 7,46 % and the acid insoluble ash content is 2,35%. The result of the phytochemical screening showed the existence of flavonoids, glycosides, saponins, tannins, triterpenoids/steroids . The result of the column chromatography was triterpenoid isolate on F3 that gives the Rf value 0,48
(purple) , 0,48 (purple), 0,48 ( purple), 0,48 ( purple) and 0.48 (purple). The result of the ultraviolet and infrared spectrophotometry of F3 isolates obtained
maximum wavelength (λ) 224 nm, the existence of clusters C=O, C=C aromatic, C-O, O-H, C-H alifatis, and C-H methyl that indicated steroid/triterpenoid compound
Keywords: root of monster fruit, steroid/triterpenoid, Thin Layer Cromatography, Spectrophotometer, Column
BAB I PENDAHULUAN 1.1Latar Belakang
Indonesia merupakan negara tropis dengan curah hujan yang cukup tinggi ,
sehingga tanahnya banyak ditumbuhi tumbuh-tumbuhan yang dapat di gunakan untuk obat-obat tradisional, hanya saja pengetahuan masyarakat tentang tanaman
serta khasiatnya sangat kurang. Hutan tropis yang kaya dengan berbagai jenis tumbuhan merupakan sumber daya hayati dan sekaligus sebagai gudang senyawa kimia baik berupa senyawa kimia hasil metabolisme primer yang disebut juga
sebagai senyawa metabolit primer seperti protein, karbohidrat, lemak yang digunakan sendiri oleh tumbuhan tersebut untuk pertumbuhannya, maupun
sebagai sumber senyawa metabolit sekunder seperti steroid/triterpenoid, flavonoid dan alkaloid (Lenny,2006).
Senyawa steroid terdapat pada hewan, tanaman tingkat tinggi bahkan
terdapat pula pada beberapa tanaman tingkat rendah seperti jamur (fungi), fungsi steroid antara lain untuk meningkatkan laju perpanjangan sel tumbuhan serta
merangsang pertumbuhan pucuk tumbuhan. Steroid banyak terdapat di alam tetapi dalam jumlah yang terbatas dan mempunyai aktivitas biologis (Aria,2009)
Dibidang farmasi steroid/triterpenoid digunakan untuk pembuatan
obat-obat kontrasepsi, anabolik, dan antiinflamasi, anti diabetes dan gangguan kulit. (Robinson,1995). Banyak jenis tanaman yang telah diteliti dan dilaporkan
memiliki khasiat sebagai antikanker, contohnya adalah tanaman dari suku Araceae yaitu Pinellia yang mengandung sitosterol dan glukosida.
Salah satu tanaman dari suku Araceae yang telah diteliti adalah Ekor Naga
secara tradisional di Singapura (Anonim, 2008). Masyarakat Indonesia juga telah menggunakan tanaman ekor naga sebagai obat anti kanker dan anti bakteri. Daun ekor naga mengandung senyawa steroid/triterpenoid, alkaloid, flavonoid,saponin,
tanin, glikosida , dan glikosida antrakuinon (Nurhanifah,2009). Akar merupakan salah satu bagian penting dari suatu tumbuhan. Akar berfungsi menyerap nutrisi
dari tanah yang kemudian akan diedarkan keseluruh bagian tumbuhan dan sebagai tempat penimbunan makanan. (Gembong, 1994).
Berdasarkan uraian diatas maka penulis tertarik untuk melakukan isolasi
senyawa triterpenoid/steroid dari akar tanaman ekor naga. Penelitian ini diawali dengan melakukan skrining fitokimia, kemudian karakterisasi simplisia,
selanjutnya ekstraksi dilakukan dengan cara perkolasi dengan pelarut n-heksan dan dianalisis dengan Kromatografi Lapis Tipis (KLT) selanjutnya dipisahkan dengan kromatografi kolom , isolat yang diperoleh dikarakterisasi dengan alat
Spektrofotometer ultraviolet (UV) dan Spektrofotometer Infra Red (IR).
1.2Perumusan Masalah
1. Apakah golongan senyawa steroid/triterpenoid, alkaloid, flavonoid, glikosida, glikosida antrakuinon, saponin, dan tanin terdapat didalam
serbuk simplisia akar ekor naga (Rhaphidophora pinnata Schott)?
2. diekstraksi dengan cara perkolasi menggunakan pelarut n-heksan dan
3. Apakah senyawa steroid/triterpenoid dari akar ekor naga dapat diisolasi dari ekstrak n-heksan dan isolatnya dapat dikarakterisasi secara Spektrofotometri UV dan Spektrofotometri IR?
1.3Hipotesa
1. Didalam serbuk simplisia akar ekor naga (Rhaphidophora pinnata Schott)
terdapat steroid/triterpenoid, alkaloid, flavonoid, saponin, glikosida, glikosida antrakuinon dan tanin.
2. Senyawa steroid/triterpenoid yang terkandung dalam ekstrak n-heksan
dapat diisolasi dengan cara Kromatografi Kolom.
3. Senyawa steroid/triterpenoid dari akar ekor naga dapat diisolasi dari
ekstrak n-heksan dan isolatnya dapat dikarakterisasi secara Spektrofotometri UV dan Spektrofotometri IR.
1.4Tujuan Penelitian
1. Untuk mengetahui, apakah didalam serbuk simplisia akar ekor naga (Rhaphidophora pinnata Schott) terdapat steroid/triterpenoid, alkaloid, flavonoid, saponin, glikosida, glikosida antrakuinon dan tanin .
2. Untuk mengetahui, apakah senyawa steroid/triterpenoid dalam ekstrak n-heksan dapat diisolasi dengan cara Kromatografi Lapis Tipis dan
Kromatografi Kolom.
3. Untuk mengetahui, apakah isolat dapat dikarakterisasi secara Spektrofotometri UV dan Spektrofotometri IR.
1.5 Manfaat Penelitian
Manfaat penelitian ini adalah untuk menambah informasi tentang karakteristik simplisia,
BAB II
TINJAUAN PUSTAKA 2.1 Uraian Tanaman Ekor Naga
Tanaman ekor naga sejenis tanaman merambat yang besar, memanjat pada
pohon yang tingginya bisa mencapai 5-15 m, daun berbentuk bulat memanjang, daun berbagi-bagi, ujung daunnya meruncing, mempunyai toreh, dalamnya
melebihi setengah panjang tulang daun yang berjumlah 7-12, dengan batang yang bulat, dan mempunyai akar pelekat dan akar gantung yang panjang bergantungan seperti ular yang meliliti pohon. Tanaman ini berasal dari Himalaya sampai
Australia dan Pasifik (Burkill, 1935; Heyne, 1987). 2.1.1 Sinonim (Lemmens and Bunyapraphatsa, 2003)
Epipremnun pinnatum (L.) Engl, Scindapsus pinnatus (L.) schott,
Rhaphidophora merillii Engl
2.1.2 Nama Daerah (Heyne, 1987)
Indonesia : Tapanawa tairis (Mal.) Sunda : Lolo munding, Lolo tali Jawa : Jalu mampang, Sulang
Bali : Samblung Sumatera Utara : Ekor naga
2.1.3 Sistematika Tanaman Ekor Naga (Arthur, 1981) Divisi : Spermatophyta
Kelas : Monocotyledoneae
Famili : Araceae
Genus : Rhaphidophora
Spesies : Rhaphidophora pinnata Schott.
2.1.4 Kegunaan Tanaman Ekor Naga
Kulit akar gantung dikunyah dengan pinang dan kapur, berguna untuk
menguatkan akar gigi dan dapat menghitamkan gigi sebagai efek sampingnya. Batang digiling dapat menyembuhkan anggota badan yang salah urat (terkilir). Di Singapura, daunnya digunakan sebagai teh herbal untuk mengobati reumatik dan
kanker. Di Pilipina, getah dari batang tanaman digunakan untuk mengobati gigitan ular beracun. Di Vietnam, tanaman ini berguna untuk mengobati batuk, paralisis
dan konjungtivitis (Heyne, 1987; Lemmens, 2003). 2.2 Uraian Kimia Triterpenoid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam
satuan isopren, dimana kerangka karbonnya dibangun oleh dua atau lebih satuan C5 tersebut. Senyawa terpenoid terdapat bebas dalam jaringan tanaman, tetapi banyak diantaranya yang terdapat sebagai alkohol, aldehid (Harbone,1987),
glikosida dan ester asam aromatik (Sastrohamidjojo, 1996). Struktur kimia isopren dapat dilihat pada gambar 1.
Gambar 1. Struktur Kimia Isopren
hijau-biru dengan pereaksi Liebermann-Burchard (asam asetat anhidrid-asam sulfat pekat) (Harborne, 1987).
Triterpenoid memiliki beberapa aktivitas fisiologi, antara lain untuk
penyakit diabetes, gangguan menstruasi, patukan ular, gangguan kulit, kerusakan hati dan malaria (Robinson, 1995), radang (Aguirre, et al., 2006), analgesik
(Delporte, et al., 2007) dan kanker (Atenza, dkk, 2009).
Triterpenoid dapat dibagi menjadi empat golongan senyawa, yaitu triterpenoid sebenarnya, steroid, saponin dan glikosida jantung (Harborne, 1987).
1. Triterpenoid
Pembagian triterpenoid berdasarkan jumlah cincin yang terdapat pada
struktur molekulnya (Robinson, 1995), antara lain:
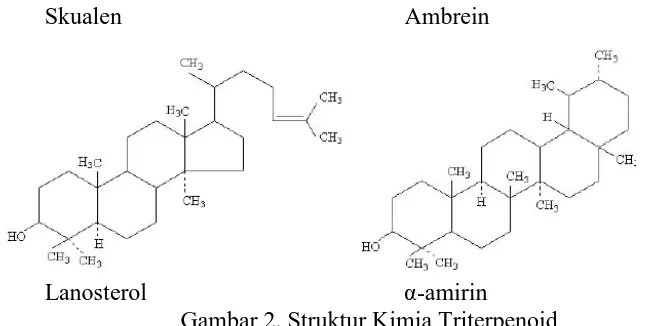
a. Triterpenoid asiklik, yaitu triterpenoid yang tidak mempunyai cincin tertutup dalam cincin molekulnya, contohnya skualen.
b. Triterpenoid trisiklik, yaitu triterpenoid yang mempunyai tiga cincin tertutup dalam cincin molekulnya, contohnya ambrein.
c. Triterpenoid tetrasiklik, yaitu triterpenoid yang mempunyai tiga cincin tertutup
dalam cincin molekulnya, contohnya lanosterol.
d. Triterpenoid pentasiklik, yaitu triterpenoid yang mempunyai tiga cincin tertutup dalam cincin molekulnya, contohnya α-amirin. Struktur kimia
Skualen Ambrein
Lanosterol α-amirin
Gambar 2. Struktur Kimia Triterpenoid
Senyawa triterpenoid tetrasiklik menarik perhatian karena kemungkinan ada kaitan biogenesis dengan steroid, contohnya lanosterol, senyawa antara biosintesis steroid pada hewan. Triterpenoid pentasiklik paling tersebar luas,
umumnya pada tumbuhan berbiji, baik dalam bentuk bebas maupun sebagai glikosida (Robinson, 1995).
2. Steroid
Steroid adalah senyawa yang memiliki kerangka dasar siklopentanafenantren. Pada umumnya, gugus metil berada pada C10 dan C13.
Rantai samping alkil dapat juga berada pada C17. Sterol adalah steroid yang memiliki gugus hidroksi pada C3. Atom karbon tambahan dapat berada pada
rantai samping (IUPAC, 1989). Struktur kimia dan sistem penomoran steroid dapat dilihat pada gambar 3.
Saponin adalah senyawa aktif permukaan yang kuat yang menimbulkan busa jika dikocok dalam air dan pada konsentrasi rendah sering menyebabkan hemolisis sel darah merah. Dalam larutan yang sangat encer sangat beracun untuk
ikan. Diberikan nama saponin karena sifatnya yang menyerupai sabun (bahasa Latin, sapo: sabun). Saponin dibagi menjadi dua jenis, yaitu glikosida triterpenoid
dan glikosida steroid (Robinson, 1995). 4. Glikosida Jantung
Glikosida jantung merupakan glikosida steroid dengan kerangka dasar
siklopentanafenantren, gugus lakton tak jenuh pada rantai samping C17, sebuah gugus hidroksi pada C14 dan glikon selalu terikat pada C3. Aglikon glikosida jantung ada dua, yaitu
kardenolida (gugus lakton pentasiklik pada C17) dan bufadienolida (gugus lakton heksasiklik pada C17) (Robinson, 1995).
2.3Ekstraksi
Ekstraksi adalah kegiatan penarikan zat aktif yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Pemilihan pelarut dan cara ekstraksi yang tepat dapat dipermudah dengan mengetahui terlebih dahulu zat aktif yang dikandung simplisia.
Ekstraksi dipengaruhi oleh derajat kehalusan serbuk dan perbedaan konsentrasi. Jika hanya dengan mencelupkan serbuk simplisia ke dalam pelarut, maka ekstraksi tidak akan sempurna
karena terjadi kesetimbangan antara larutan zat aktif di luar sel dan larutan zat aktif di dalam sel (Depkes, 1986).
Ekstraksi dapat dilakukan dengan berbagai cara (Depkes, 2000), yaitu:
1. Maserasi
Maserasi adalah proses ekstraksi menggunakan pelarut dengan beberapa kali
dilakukan dengan merendam serbuk simplisia dalam cairan penyari, dimana cairan akan berdifusi dengan dinding sel yang mengandung zat aktif. Pengadukan dilakukan untuk menjaga adanya derajat perbedaan konsentrasi antara larutan di luar sel dan di dalam sel.
Larutan yang terpekat didesak keluar dinding sel sampai terjadi keseimbangan konsentrasi antara larutan di luar sel dan di dalam sel. Pengulangan penambahan pelarut setelah
dilakukan penyaringan hasil maserasi pertama dikenal dengan remaserasi.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna, umumnya dilakukan pada temperatur ruangan. Prosesnya terdiri dari beberapa tahapan, yaitu
pengembangan bahan, maserasi antara, dan perkolasi sebenarnya (penampungan ekstrak), terus-menerus sampai diperoleh perkolat.
3. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali
sehingga dapat termasuk proses ekstraksi sempurna. 4. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru, umumnya dilakukan menggunakan alat khusus, sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dan adanya pendingin balik.
5. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur yang lebih
6. Infundasi
Infundasi adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana infus tercelup dalam penangas air mendidih, temperatur terukur 96-980C) selama waktu
tertentu biasanya 15-20 menit. 7. Dekok
Dekok adalah infundasi pada waktu yang lebih lama dan temperatur sampai titik didih air.
2.4Kromatografi
Kromatografi merupakan suatu teknik pemisahan yang menggunakan fase diam (stationary phase) dan fase gerak (mobile phase). Saat ini, kromatografi merupakan teknik pemisahan yang paling umum dimanfaatkan untuk melakukan analisis, baik analisis kualitatif
maupun kuantitatif, atau preparatif dalam bidang farmasi (Rohman, 2007). Kromatografi pertama kali dikembangkan pada tahun 1903 oleh Michael Tswett, seorang ahli botani Rusia
dalam memisahkan pigmen berwarna, sehingga dinamakan kromatografi. Namun sekarang hampir kebanyakan pemisahan secara kromatografi digunakan untuk senyawa tak berwarna (Sastrohamidjojo, 1985).
2.4.1 Kromatografi Lapis Tipis
Penggunaan umum KLT adalah untuk menentukan banyaknya komponen
dalam campuran, identifikasi senyawa, memantau proses reaksi, menentukan efektifitas pemurnian, menentukan kondisi yang sesuai untuk kromatografi kolom, serta untuk memantau kromatografi kolom, melakukan skrining sampel untuk
obat (Rohman, 2007).
Fase diam pada KLT sering disebut penyerap, biasanya dapat melewati
1991). Banyak penyerap yang telah digunakan, termasuk silika gel dengan ketebalan sekitar 0,10 sampai 0,25 mm, didukung oleh plat kaca, aluminium atau plastik (Wall, 2005). Permukaan polar dari gugus hidroksi silika gel berfungsi
menarik molekul sampel. Lapisan silika gel harus sesedikit mungkin mungkin mengandung air, sehingga harus diaktifkan dengan pemanasan pada 1000C selama
1-3 jam. Jika suhu pengaktifan jauh di atas 1100C terjadi dehidrasi yang tak bolak-balik menyebabkan pemisahan kurang efektif. Setelah diaktifkan, lapisan disimpan dalam lingkungan yang kering (Gritter, et al., 1991).
Fase gerak adalah medium angkut, terdiri dari satu atau beberapa pelarut, yang bergerak di dalam fase diam, yaitu suatu lapisan berpori karena adanya gaya kapiler (Stahl, 1985).
Pemilihan sistem pelarut yang dipakai didasarkan atas prinsip like dissolves like, artinya untuk memisahkan sampel yang bersifat nonpolar digunakan sistem pelarut yang bersifat nonpolar juga. Proses pengembangan akan lebih baik bila ruangan pengembangan tersebut telah jenuh
dengan uap sistem pelarut (Adnan, 1997). Pelarut dalam ruangan pengembang dihindarkan dari atmosfer luar untuk menghindari penguapan komponen-komponen (Sastrohamidjojo, 1985) dan campuran pelarut dianjurkan hanya dipakai untuk sekali pengembangan saja karena
susunannya mudah berubah akibat salah satu komponennya menguap (Gritter, et al., 1991). Harga dihitung dengan menggunakan perbandingan sebagaimana persamaan sebagai
berikut:
Harga maksimum adalah 1, sampel bermigrasi dengan kecepatan sama dengan
Faktor-faktor yang mempengaruhi harga Rf pada KLT (Sastrohamidjojo,
1985), antara lain:
1. Struktur kimia dari senyawa yang dipisahkan
2. Sifat dari penyerap dan derajat aktivitasnya 3. Tebal dan kerataan lapisan penyerap 4. Derajat kemurnian fase gerak
5. Derajat kejenuhan uap pengembang pada bejana 6. Jumlah cuplikan
7. Suhu.
2.4.2 Kromatografi Kolom
Penggunaan kolom besar merupakan metode kromatografi untuk
pemisahan campuran dalam jumlah besar (lebih dari 1 g). Campuran yang akan dipisahkan berupa pita pada bagian atas kolom penyerap. Fase gerak dialirkan melalui kolom oleh gaya berat atau oleh tekanan. Pita campuran bergerak melalui
kolom dengan laju yang berbeda, memisah, dan dikumpulkan berupa fraksi (Gritter, et al., 1991).
Ukuran partikel penyerap untuk kolom dengan gaya tarik bumi biasanya lebih besar daripada untuk KLT, yaitu 63-250 µ m, dapat melewati ayakan mesh 70-230; sedangkan untuk kolom dengan tekanan biasanya lebih kecil daripada
diperhatikan agar tidak ada bagian penyerap yang kering, baik selama pengisian maupun pemisahan (Sastrohamidjojo, 1985).
Kromatografi kolom memerlukan waktu yang lama dan bahan yang cukup
banyak, sehingga perlu dipastikan campuran pelarut yang terbaik untuk pemisahan. Masalah ini dapat dipecahkan melalui tiga pendekatan, yaitu
penelusuran pustaka, penerapan data KLT dan pemakaian elusi landaian Fraksi kolom yang mengandung senyawa yang sama yang diperiksa dengan KLT kemudian digabungkan, diuapkan dengan tekanan rendah. Jika pelarut dan
penyerap murni, maka fraksi-fraksi pun murni. Namun mungkin masih diperlukan rekristalisasi untuk memperoleh senyawa murni (Gritter, et al., 1991).
2.5 Spektroskopi
Spekstroskopi adalah studi mengenai interaksi cahaya dengan atom dan molekul. Radiasi cahaya dan elektromagnetik dapat dianggap menyerupai
gelombang (Creswell, et al., 2005). 2.5.1Spektrofotometri Ultraviolet
Spektrum ultraviolet merupakan gambaran antara panjang gelombang
serapan dan intensitas serapan (absorbansi) (Sastrohamidjojo, 1991). Sinar ultraviolet berada pada panjang gelombang 200-400 nm, sedangkan sinar tampak
pada 400-800 nm. Beberapa kegunaan penggunaan spektrofotometri ultraviolet (Dachriyanus, 2002), antara lain:
1. Menentukan jenis kromofor, ikatan rangkap yang terkonjugasi dan auksokrom
dari senyawa organik,
2. Menjelaskan informasi dari struktur berdasarkan panjang gelombang
3. Analisis kuantitatif senyawa organik menggunakan hokum Lambert-Beer. Apabila suatu molekul menyerap radiasi ultraviolet, di dalam molekul tersebut terjadi perpindahan tingkat energi elektron-elektron ikatan di orbital
molekul terluar dari tingkat energi terendah ke tingkat energi yang tertinggi. Baik molekul senyawa organik maupun anorganik dapat menyerap radiasi ultraviolet
(Noerdin, 1985). Semakin kecil perbedaan energi antara tingkat terendah dan tingkat tereksitasi, maka semakin besar panjang gelombang dari serapan. (Silverstein, et al., 1986). Untuk senyawa yang mempunyai sistem konjugasi,
perbedaan energi menjadi lebih kecil sehingga penyerapan terjadi pada panjang gelombang yang lebih besar (Dachriyanus, 2002).
Beberapa istilah yang sering digunakan dalam spektrofotometri ultraviolet (Sastrohamidjojo, 1991), antara lain:
1. Kromofor adalah gugus tak jenuh kovalen yang dapat menyerap radiasi di
daerah ultraviolet, contohnya: C=C, C=O dan NO2.
2. Auksokrom adalah gugus jenuh yang bila terikat pada kromofor akan mengubah panjang gelombang dan intensitas serapan maksimum, contohnya –
Cl, -OH dan NH2.
3. Pergeseran batokromik (pergeseran merah) adalah pergeseran serapan ke arah
panjang gelombang yang lebih panjang disebabkan subtitusi atau pengaruh pelarut.
4. Pergeseran hipsokromik (pergeseran biru) adalah pergeseran serapan ke arah
panjang gelombang yang lebih pendek disebabkan subtitusi atau pengaruh pelarut.
6. Efek hipokromik adalah penurunan intensitas serapan. 2.5.2Spektrofotometri Inframerah
Spektrofotometri inframerah merupakan teknik spektrofotometri tercepat
dan termurah yang digunakan dalam kimia organik. Sampel dapat berupa padatan, cairan atau gas, dan dapat diukur dalam larutan dengan KBr atau minyak mineral.
Kemudian spektrum dapat diperoleh hanya dalam beberapa menit dari material murni parsial dengan tujuan memberikan indikasi bahwa reaksi yang terjadi terjadi seperti yang diinginkan (Cooper, 1980).
Sinar inframerah bila dilewatkan melalui cuplikan senyawa organik, maka sejumlah frekuensi diserap dan sebagian diteruskan tanpa diserap. Daerah
inframerah terletak antara spektrum ultraviolet dan spektrum radio, yakni antara 4000-400 cm-1. Beberapa kegunaan penggunaan spektrofotometri inframerah (Dachriyanus, 2002), antara lain:
1. Menentukan gugus fungsi suatu senyawa organik,
2. Mengetahui informasi struktur suatu senyawa organik dengan membandingkan daerah sidik jarinya.
Identifikasi senyawa yang tidak diketahui gugus fungsinya dapat diuji struktur inframerahnya, kemudian spektrum dideteksi menggunakan data korelasi
untuk memperoleh gugus fungsional apa saja yang terdapat (Sastrohamidjojo, 1991). Langkah-langkah umum untuk memeriksa pita serapan (Pavia et al., 1988) adalah sebagai berikut:
1. Apakah terdapat gugus karbonil? Gugus C=O memberikan puncak pada daerah 1820-1660 cm-1. Puncak ini biasanya merupakan yang terkuat dengan
2. Jika gugus C=O ada, periksa gugus-gugus berikut. Jika tidak ada, langsung ke nomor 3.
a. Asam. Apakah ada O-H? Serapan lebar di daerah 3300-2500 cm-1.
Biasanya tumpang tindih dengan C-H. b. Amida. Apakah ada N-H? Serapan medium di dekat 3500 cm-1,
kadang-kadang dengan puncak rangkap.
c. Ester. Apakah ada C-O? Serapan medium di daerah 1300-1000 cm-1. d. Anhidrida. Mempunyai dua serapan C=O di daerah 1810 dan 1760 cm-1.
e. Aldehida. Apakah ada C-H aldehid? Dua serapan lemah di daerah 2850- 2750 cm-1 yaitu di sebelah kanan serapan C-H.
f. Keton. Jika kelima kemungkinan di atas tidak ada. 3. Bila gugus C=O tidak ada.
a. Alkohol/fenol. Periksa gugus O-H, merupakan serapan lebar di daerah
3600-3300 cm-1 yang diperkuat adanya serapan C-O di daerah 1300-1000 cm-1.
b. Amina. Periksa gugus N-H, yaitu serapan medium di daerah 3500 cm-1.
c. Eter. Periksa gugus C-O (serapan O-H tidak ada), yaitu serapan medium di daerah 1300-1000 cm-1.
4. Ikatan rangkap dua dan/atau cincin aromatik.
a. C=C mempunyai serapan lemah di daerah 1650 cm-1.
b.Serapan medium sampai kuat pada daerah 1650-1450 cm-1 sering
c.Buktikan kemungkinan di atas dengan memperhatikan serapan pada daerah C-H aromatik di sebelah kiri 3000 cm-1, sedangkan C-H alifatis terjadi di sebelah kanan daerah tersebut.
5. Ikatan rangkap tiga.
a.C≡N mempunyai serapan medium dan tajam di daerah 2250 cm-1.
b.C≡C mempunyai serapan lemah tapi tajam di daerah 2150 cm-1. Periksa juga CH asetilenik di dekat 3300 cm-1.
6. Gugus nitro.
Dua serapan kuat di daerah 1600-1500 cm-1 dan 1390-1300 cm-1. 7. Hidrokarbon.
a. Apabila keenam kemungkinan di atas tidak ada. b. Serapan utama di daerah C-H dekat 3000 cm-1.
c. Spektrum sangat sederhana, hanya terdapat serapan lain di daerah
BAB III
METODOLOGI PENELITIAN
Metode yang digunakan metode deskriptif meliputi pengumpulan dan
pengolahan sampel, skrining fitokimia, pemeriksaan karakteristik, pembuatan ekstrak, analisis ekstrak n-heksan dengan Kromatografi Lapis Tipis, yang
dilanjutkan isolasi dengan Kromatografi Kolom, Isolat yang diperoleh diuji kemurniannya dengan Kromatografi Lapis Tipis dua arah dan identifikasi isolat secara Spektrofotometri Ultraviolet dan Spektrofotometri Infrared.
3.1 Alat-alat yang Digunakan
Alat-alat yang digunakan pada penelitian ini adalah neraca kasar (Ohaus), alat-alat
gelas laboratorium (Pyrex, Iwaki), blender (Panasonic), eksikator, mikroskop (Olympus), seperangkat alat destilasi, seperangkat alat penetapan kadar air, seperangkat alat kromatografi kolom, oven listrik (Stork), hair dryer (Maspion), neraca analitik (Vibra AJ), penangas air
(Yenaco), seperangkat alat kromatografi lapis tipis, lemari pengering, Spektrofotometer Ultraviolet (Shimadzu) dan Spektrofometer Infrared (Shimadzu).
3.2 Bahan-bahan yang Digunakan
Bahan-bahan yang digunakan dalam penelitian ini adalah: sebagai sampel digunakan akar tanaman ekor naga. Bahan kimia yang digunakan kecuali dinyatakan lain adalah
berkualitas proanalisa yaitu n-heksan, benzen, etilasetat, etanol, amil alkohol, metanol, eter, isopropanol, α-naftol, besi (III) klorida, iodium, raksa (II) klorida, timbal (II) asetat, kalium
iodida, asam asetat glasial, asam sulfat pekat, asam klorida pekat, serbuk magnesium, bismuth
(III) nitrat, plat pra lapis silika gel GF254, kloralhidrat, n-heksan hasil destilasi dan air suling.
Sebanyak 4 g kalium iodida dilarutkan dalam air, kemudian ditambahkan 2 g iodium dalam air hingga 100 ml (Depkes RI, 1979).
3.3.2 Larutan Pereaksi Dragendorff
Sebanyak 8 g bismut nitrat dilarutkan dalam 20 ml asam nitrat dan 27,2 g kalium iodida dalm 50 ml air. Dicampurkan kedua larutan dan didiamkan sampai memisah sempurna.
Diambil larutan jernih dan encerkan dengan air secukupnya hingga 100 ml (Depkes RI, 1979). 3.3.3 Larutan Pereaksi Molish
Sebanyak 3 g alfa naftol dilarutkan dengan sedikit etanol, kemudian ditambahkan asam
nitrat 0,5 N secukupnya hingga diperoleh 100 ml (Depkes RI, 1979). 3.3.4 Larutan Pereaksi Besi (III) Klorida 1%
Sebanyak 1,0 g besi (III) klorida dilarutkan dalam air suling hingga 100 ml (Depkes RI, 1979).
3.3.5 Larutan Pereaksi Timbal (II) Asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat dilarutkan dalam aquadest bebas CO2 secukupnya hingga 100 ml (Depkes RI, 1979).
3.3.6 Larutan Pereaksi Asam Klorida 2 N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling hingga 100 ml (Depkes RI, 1979).
3.3.7 Larutan Pereaksi Natrium Hidroksida 2 N
Sebanyak 8,00 g natrium hidroksida dilarutkan dalam aquades bebas CO2 hingga diperoleh 100 ml larutan (Depkes RI, 1979).
3.3.8 Larutan Pereaksi Mayer
dicampurkan dengan 10 ml larutan II dan ditambahkan air suling hingga 100 ml (Depkes RI, 1989).
3.3.9 Larutan Penyemprot Liebermann-Burchard
Sebanyak 5 ml asam asetat anhidrida ditambahkan dengan 5 ml asam sulfat pekat, kemudian campuran dimasukkan kedalam 50 ml etanol. Pengerjaan dilakukan dalam kondisi
dingin dan pereaksi dibuat baru.
3.4 Pengumpulan dan Pengolahan Sampel 3.4.1 Pengumpulan Sampel
Pengumpulan sampel dilakukan secara purposif, yaitu tanpa membandingkannya dengan daerah lain. Sampel yang digunakan adalah akar
pelekat tanaman ekor naga (Rhapidophora pinnata Schott), diambil dipinggir jalan Bakaran Batu, Medan- Sumatera Utara.
3.4.2 Identifikasi Sampel
Identifikasi sampel dilakukan di Pusat Penelitian dan Pengembangan Biologi LIPI, Bogor. Hasil Identifikasi menunjukkan bahwa tanaman tersebut adalah ekor naga (Rhaphidophora pinnata Schott ). Family : Araceae.
3.4.3 Pengolahan Sampel
3.5 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air, penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total dan penetapan kadar abu yang tidak larut dalam asam (Depkes RI, 1989).
3.5.1 Pemeriksaan Makroskopik
Pemeriksan makroskopik dilakukan dengan mengamati bentuk luar dari akar ekor naga segar.
3.5.2 Pemeriksaan Mikroskopik
Pemeriksaan mikroskopik terhadap akar ekor naga segar dilakukan dengan cara: akar segar diiris melintang , diletakkan diatas kaca objek yang telah ditetesi dengan kloral hidrat, dipanaskan diatas lampu spritus, kemudian ditutup dengan kaca penutup, diamati dibawah mikroskop. Untuk melihat adanya butir amilum, serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi dengan air suling, kemudian ditutup dengan kaca penutup, diamati dibawah mikroskop.
Pemeriksaan mikroskopik dilakukan terhadap akar ekor naga segar untuk melihat struktur tumbuhan tersebut secara lengkap.
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia dengan cara menaburkan diatas kaca objek yang telah ditetesi dengan kloralhidrat dan ditutup dengan kaca penutup, kemudian dilihat dibawah mikroskop.
3.5.3 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Prosedur kerja:
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan kedalam labu alas bulat, didestilasi selama 2 jam. Kemudian toluen didinginkan selama 30 menit dan volume air pada tabung penerima dibaca dengan ketelitian 0,01 ml
(WHO,1992).
2. Penetapan kadar air simplisia
Sebanyak 5 g serbuk simplisia yang telah ditimbang seksama dimasukkan kedalam labu
alas bulat berisi toluen tersebut, lalu dipanaskan hati-hati selama 15 menit. Setelah toluen mendidih, kecepatan tetesan diatur lebih 2 tetes perdetik, sampai sebagian air terdestilasi,
kemudian kecepatan tetesan dinaikkan sampai 4 tetes tiap detik.Setelah semua air terdestilasi ,bagian dalam pendingin dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan dingin sampai suhu kamar. setelah air dan toluen memisah
sempurna, volume air dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air yang dihitung dalam persen (WHO,1992).
3.5.4 Penetapan Kadar Sari yang Larut Dalam Air
Sebanyak 5 g serbuk yang telah dikeringkan, dimaserasi selama 24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air sampai 1 L) dalam labu bersumbat sambil di
kocok selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring, sejumlah 20 ml filtrat diuapkan sampai kering, dalam cawan dangkal berdasar rata yang telah ditara dan sisa dipanaskan pada suhu 1050C sampai bobot tetap. Kadar sari larut dalam air dihitung
terhadap bahan yang telah dikeringkan (Depkes RI, 1989).
3.5.5 Penetapan Kadar Sari yang Larut Dalam Etanol
ditara dan dipanaskan pada suhu 1050C sampai bobot tetap. Kadar sari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1989).
3.5.6 Penetapan Kadar Abu Total
Sebanyak 2 g serbuk simplisia yang telah digerus dan ditimbang seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan dan dipijarkan pada suhu 6000C sampai arang habis. Kemudian didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (WHO, 1992).
35.7 Penetapan Kadar Abu yang Tidak Larut Dalam Asam
Abu yang telah diperoleh dalam penetapan kadar abu total, dididihkan dalam 25 ml asam klorida 2 N selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring bebas abu, kemudian dicuci dengan air panas. Residu dan kertas saring dipijarkan pada suhu 6000C sampai bobot tetap. Kemudian didinginkan dan ditimbang. Kadar abu tidak larut dalam asam dihitung terhadap bahan yang dikeringkan (WHO, 1992). 3.6 Skrining Fitokimia
Skrining fitokimia serbuk simplisia meliputi pemeriksaan senyawa golongan alkaloida, glikosida, steroid/triterpenoid, flavonoida, saponin, tanin, dan antrakinon.
3.6.1 Pemeriksaan Alkaloid
Serbuk simplisia 0,5 g ditambah 1 ml HCl 2 N dan 9 ml air suling, dipanaskan diatas
penangas air selama 2 menit, didinginkan dan disaring. Filtratnya dipakai untuk uji alkaloid sebagai berikut :
a. Filtrat 3 tetes ditambah 2 tetes larutan pereaksi Mayer, terbentuk endapan menggumpal berwarna putih atau kuning.
b. Filtrat 3 tetes ditambah 2 tetes larutan pereaksi Bauchardat, terbentuk
c. Filtrat 3 tetes ditambah 2 tetes larutan pereaksi Dragendorff terbentuk warna merah atau jingga.
Alkaloid disebut positif jika endapan atau kekeruhan paling sedikit dua
dari tiga tabung reaksi dari percobaan diatas (Depkes RI, 1979). 3.6.2 Pemeriksaan Glikosida
Sebanyak 3 g serbuk simplisia disari dengan 30 ml campuran etanol 95% dengan air suling (7:3) dan 10 ml asam sulfat 2 N, direfluks selama 1 jam, didinginkan dan disaring. Pada 20 ml filtrat ditambahkan 25 ml air suling dan 25
ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran isopropanol dan kloroform (2:3) dilakukan berulang
sebanyak 3 kali. Kumpulan sari air diuapkan dan sisanya dilarutkan dalam 2 ml metanol. Larutan sisa dimasukkan dalam tabung reaksi selanjutnya diuapkan diatas penangas air, pada sisa ditambahkan 2 ml air dan 5 tetes larutan pereaksi
Molish. Tambahkan hati-hati 2 ml asam sulfat melalui dinding tabung, terbentuk cincin ungu pada batas kedua cairan menunjukkan adanya glikosida
(Depkes RI, 1989).
3.6.3 Pemeriksaan Steroid/Triterpenoid
Sejumlah 1 g serbuk dimaserasi dengan 20 ml eter selama 2 jam. Disaring, filtrat
diuapkan dicawan penguap, sisanya ditambahkan asam asetat anhidrat- H2SO4 pekat (pereaksi Lieberman-Burchard), apabila terbentuk warna biru hijau menunjukkan adanya steroida, sedangkan warna merah, merah muda atau ungu menunjukkan adanya triterpenoid (Farnsworth,
1966).
Sebanyak 10 g serbuk simplisia ditambahkan 100 ml air panas, didihkan selama 5 menit dan disaring dalam keadaan panas, kedalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil
alkohol, dikocok dan dibiarkan memisah. Flavonoid positif jika terjadi warna 3.6.5 Pemeriksaan Tanin
Sebanyak 1 g serbuk simplisia disari dengan 10 ml air suling, lalu dipanaskan, disaring. Filtratnya diencerkan dengan akuades sampai tidak berwarna. Larutan diambil sebanyak 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%, jika terjadi warna biru atau hijau
kehitaman menunjukkan adanya tanin (Farnsworth, 1966). 3.6.6 Pemeriksaan Saponin
Sebanyak 0,5 g serbuk simplisia, dimasukkan dalam tabung reaksi, ditambahkan 10 ml air panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk buih yang mantap setinggi 1-10 cm, tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1
tetes HCl 2 N menunjukkan adanya saponin (Depkes RI, 1979). 3.6.7 Pemeriksaan Glikosida Antrakuinon
Sebanyak 0,2 g serbuk simplisia dicampur dengan 5 ml asam sulfat 2 N, dipanaskan
sebentar, setelah dingin ditambahkan 10 ml benzen, dikocok dan didiamkan. Lapisan benzen dipisahkan dan disaring. Dikocok lapisan benzen dengan 2 ml NaOH 2 N, didiamkan. Lapisan
air berwarna merah menunjukan adanya glikosida antrakuinon (Depkes RI, 1979) 3.7 Pembuatan Ekstrak
Pembuatan ekstrak dilakukan secara perkolasi menggunakan pelarut n-heksan.
Sebanyak 500 g serbuk simplisia ekor naga dimasukkan kedalam bejana tertutup dibasahi dengan penyari, aduk dan dibiarkan selama 3 jam, kemudian pindahkan ke dalam alat perkolator.
Lalu dituang larutan penyari n-heksan secukupnya sampai semua simplisia terendam dan terdapat selapis cairan penyari diatasnya, mulut tabung perkolator ditutup dengan
alumunium foil dan dibiarkan selama 24 jam, kemudian kran dibuka dan dibiarkan tetesan ekstrak mengalir dengan kecepatan 1ml/menit. Ditambahkan berulang ulang cairan penyari hingga selalu terdapat selapis cairan penyari diatas simplisia. Perkolasi dihentikan setelah
500mg perkolat yang keluar terakhir diuapkan tidak meninggalkan sisa. (Depkes RI, 1979) Selanjutnya ekstrak diuapkan dengan rotarievaporator pada temperatur tidak lebih dari
500C sampai diperoleh ekstrak kental lalu dikeringkan dengan freeze-dryer.
Bagan pembuatan ekstrak n- heksan akar ekor naga dapat dilihat pada gambar 1 berikut
.Gambar 1. Bagan Pembuatan Ekstrak n-heksan Akar Ekor Naga
Direndam dalam bejana tertutup dengan n-heksan selama 3 jam
Dipindahkan kedalam perkolator
Dituang n-heksan secukupnya Didiamkan selama 24
jam,selanjutnya dibuka kran perkolator dan biarkan cairan menetes dengan kecepatan 1 ml/menit
Tambahkan cairan penyari berulang hingga tersari sempurna
Diuapkan dengan rotaryevaporator Dan dikeringbekukan dengan freeze-dryer
Hasil Rendaman
Perkolat
500g serbuk simplisia
Bagan Isolasi Steroid /Triterpenoid dari Ekstrak n-heksan Akar Ekor Naga dapat dilihat pada gambar 2 berikut :
Gambar 2. Bagan Isolasi Senyawa Steroid/Triterpenoid Ekstrak n-heksan Akar Ekor Naga DiKLT dengan fase gerak n-heksan-etil asetat dengan berbagai perbandingan. Hasilnya dapat dilihat pada hal 39
Dikromatografi kolom dengan pelarut landaian n-heksan-etil asetat (100:0),(90:10),(80:20),(70:30),(50:50),(30:70)
Kromatogram yang sama digabungk Di KLT dengan n- heksan : etil asetat 80:20, Kromatogram dengan harga Rf yang sama digabungkan
Dicuci dengan metanol dingin Diuji dengan KLT 2 Arah
Dikarakterisasi dengan Spektrofotometer UV & Spektrofotometer IR
Ekstrak Kering
Kromatogram
F 1 V1 - 9
F2 V6 -12
F 3
V 13- 17 V 18 -63 F 4
F 5 V 64- 68
F 6
V 69 - 78 V 79 -83 F 7
F3 ( Kristal)
Kristal Murni Diperoleh 83 vial
3.8 Analisis Ekstrak n-heksan secara KLT
Terhadap ekstrak n–heksan dilakukan analisis secara KLT menggunakan plat pra lapis
tipis silika gel GF254 dan fase gerak campuran n-heksan – etilasetat dengan perbandingan (90:10), (80:20), (70:30) dan (60:40). Sebagai penampak bercak digunakan pereaksi
Liebermann-Burchard. Cara kerja:
Ekstrak dilarutkan dengan n-heksan ditotolkan pada plat lapis tipis, kemudian dimasukan ke dalam chamber yang telah jenuh dengan uap fase gerak. Setelah pengembangan selesai plat dikeluarkan dan dikeringkan, plat disemprot dengan penampak bercak Liebermann-Burchard dan dipanaskan di oven pada suhu 110°C selama 10 menit lalu diamati warna yang terbentuk dan dihitung harga Rfnya. (E.Merck, 1978; Gritter).
3.9 Fraksinasi Ekstrak n-heksan secara Kromatografi Kolom
Ekstrak heksan difraksinasi secara KK menggunakan pelarut landaian n-heksan - etilasetat dengan perbandingan (100:0), (90:10), (80:20), (70:30), (60:40), (50:50), (40:60), (30:70), terakhir menggunakan metanol sebagai pencuci. Cara kerja:
Seperangkat alat kromatografi kolom dirangkai dan ke dalam dasar kolom dimasukkan kapas yang telah dicuci dengan metanol sebagai filter. Silika gel 60 mesh 70-230 ASTM dengan ukuran partikel 0,063-0,200 disuspensikan dengan fase gerak n-heksan-etilasetat (80:20), diaduk sampai gelembung udara habis, lalu dimasukkan ke dalam kolom yang telah diisi dengan fase gerak yang sama.
Dinding kolom diketuk-ketuk untuk menghilangkan gelembung udara sambil dialiri dengan fase gerak sampai memadat. Kolom yang telah dikemas dibiarkan selama 24 jam, kemudian kran kolom dibuka sampai genangan pelarut setinggi fase diam. Fraksi n-heksan dilarutkan dengan sedikit fase gerak dan ditambahkan sedikit fase diam dan aduk rata, setelah fase gerak menguap dimasukkan ke dalam kolom secara perlahan-lahan dengan kran tertutup. Setelah sampel turun tepat setinggi fase diam, melalui dinding kolom secara perlahan-lahan dialirkan fase gerak sambil kran kolom dibuka. Tetesan yang keluar diatur agar sama dengan tetesan pelarut dari reservoir. Hasil elusi (eluat) ditampung dalam vial masing-masing sebanyak 5 ml. Selanjutnya terhadap eluat dipantau dengan KLT menggunakan plat pralapis tipis silika gel GF254 dengan fase gerak n-heksan-etilasetat (80:20), dan penyemprot Liebermann-Burchard, untuk pola kromatogram yang sama hasilnya digabungkan menjadi satu fraksi.
3.10 Analisis KLT Hasil Kromatografi Kolom
Eluat yang diperoleh 83 vial. Hasil Kromatografi Kolom dikelompokkan menjadi 7 fraksi berdasarkan eluen yang digunakan , Pada F3 ditemukan kristal , kemudian dilakukan KLT terhadap F3, Hasil KLT ditemukan 1 noda berwarna ungu dengan harga Rf 0,48
3.11 Pencucian Kristal
Kristal hasil isolasi Kromatografi Kolom dicuci berulang kali dengan
metanol dingin tetes demi tetes sampai diper.oleh kristal berwarna putih.
3.12 Uji kemurnian Isolat
yaitu benzen – etil asetat (60:40) dengan fase diam plat pralapis dan penampak bercak pereaksi Liebermann-Burchard.
Cara kerja:
Isolat ditotolkan pada plat pra lapis silika gel GF254 ukuran 8 x 8 lalu dielusi memakai fase gerak I yaitu n-heksan - etilasetat (80:20) hingga mencapai batas pengembangan, kemudian plat dikeluarkan dari dalam chamber dan dikeringkan. Setelah plat kering dielusi kembali dengan arah yang berbeda 90° memakai fase gerak II yaitu benzena–etil asetat (60:40), disemprot dengan memakai penampak bercak Liebermann-Burchard, setelah itu plat dipanaskan pada suhu 110°C selama 10 menit lalu diamati warna yang terbentuk.
3.13 Karakterisasi Isolat
Karakterisasi isolat secara Spektrofotometri ultraviolet dan Spektrofotometri inframerah dilakukan di Laboratorium Penelitian Fakultas Farmasi UGM Jogjakarta.
3.13.1 Karakterisasi Isolat secara Spektrofotometri UV Cara kerja:
Karakterisasi isolat secara spektrofotometri UV dilakukan dengan cara melarutkan isolat dalam pelarut metanol, kemudian dimasukkan kedalam kuvet yang telah dibilas dengan larutan sampel. . Selanjutnya absorbansi larutan sampel diukur pada panjang gelombang 200-400 nm.
3.13.2 Karakterisasi Isolat secara Spektrofotometri IR Cara kerja:
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi yang dilakukan oleh Pusat Penelitian dan Pengembangan Biologi Bogor terhadap tumbuhan yang diteliti adalah tanaman ekor naga (Rhaphidophora pinnata Schott). Hasil identifikasi tumbuhan ekor naga dapat
dilihat pada lampiran 1 halaman 49 dan gambar tumbuhan ekor naga dapat dilihat pada lampiran 2 halaman 50.
4.2 Hasil Pemeriksaan Makroskopik Akar Ekor Naga Segar
Hasil pemeriksaan makroskopik menunjukkan akar berbentuk lonjong memanjang , berwarna coklat dan tidak berbau, tidak berasa.
4.3 Hasil Pemeriksaan Mikroskopik Akar Ekor Naga dan Serbuk Simplisia Akar Ekor Naga
Pemeriksaan mikroskopik penampang melintang akar menunjukkan
adanya bulu akar, epidermis, serabut sklerenkim, xylem dan floem. Gambar mikroskopik penampang melintang akar ekor naga dapat dilihat pada gambar 4 berikut :
Keterangan:
1.Rambut Akar
2. Epidermis dengan jaringan gabus 3. Serabut Sklerenkim
4. Floem 5. Xylem
Pada pemeriksaan mikroskopik serbuk simplisia dijumpai adanya jaringan gabus,
xylem dengan penebalan dinding sel berupa tangga (skalariform), serabut sklerenkim, sel batu dan rambut akar. Gambar mikroskopik serbuk akar ekor naga
dapat dilihat pada gambar 5 berikut:
Gambar 5. Mikroskopik Serbuk Akar Ekor Naga Keterangan:
1. Jaringan gabus
2. Xylem dengan penebalan bentuk tangga 3. Serabut sklerenkim
4. Sel batu 5. Rambut Akar
4.4Hasil Pemeriksaan Karakteristik Simplisia
Simplisia yang kering berwarna coklat tua, gambar simplisia akar ekor naga
(Rhaphidopora pinnata Schott ) dapat dilihat pada lampiran 3 hal 50. Hasil pemeriksaan karakteristik serbuk simplisia akar ekor naga dapat dilihat pada tabel 1 dibawah ini.
Tabel 4.1. Hasil Karakterisasi Serbuk Akar Ekor Naga
No. Penetapan Karakteristik Simplisia Hasil
1. 2. 3. 4. 5.
Kadar sari yang larut dalam air Kadar sari yang larut dalam etanol Kadar abu total
Kadar abu yang tidak larut dalam asam Kadar air
[image:47.595.112.507.545.715.2]Penetapan kadar air dilakukan untuk mengetahui apakah simplisia sudah memenuhi persyaratan, karena air merupakan media yang baik untuk tumbuhnya jamur sehingga dapat mempengaruhi mutu simplisia, ternyata hasilnya memenuhi syarat yaitu 6% lebih kecil dari
10%. Penetapan kadar sari larut air adalah untuk mengetahui kadar senyawa yang bersifat polar, sedang kadar sari larut dalam etanol dilakukan untuk mengetahui senyawa yang terlarut
dalam etanol, baik polar maupun non polar. Penetapan kadar abu total dilakukan untuk mengetahui kadar senyawa anorganik dalam simplisia, sedang penetapan kadar abu tidak larut dalam asam dilakukan untuk mengetahui kadar senyawa yang tidak larut dalam asam.
Perhitungan hasil karakterisasi simplisia dapat dilihat pada lampiran 5 halaman54-58.
[image:48.595.106.425.393.579.2]Hasil pemeriksaan skrining fitokimia dari serbuk simplisia akar ekor naga dapat dilihat pada tabel 2.
Tabel 4.2 Hasil Skrining Fitokimia Serbuk Akar Ekor Naga No. Pemeriksaan Golongan Senyawa Kimia Hasil 1. 2. 3. 4. 5. 6. 7. Alkaloid Flavonoid Glikosida Glikosida Antrakuinon Saponin Tanin Steroid/Triterpenoid - + + - + + + Keterangan: + = Mengandung Golongan Senyawa
- = Tidak Mengandung Golongan Senyawa
4.5 Hasil Ekstraksi dan Isolasi
Ekstraksi dilakukan dengan cara perkolasi dengan menggunakan pelarut
n-heksan hasilnya diperoleh 1,543 g ekstrak n-heksan dari 500 g serbuk simplisia.
4.6 Hasil Analisis Fraksi n-heksan dengan cara Kromatografi Lapis Tipis (KLT)
karena memberikan bercak yang paling banyak dengan pereaksi Liebermann-Burchard, diperoleh 10 noda yaitu 8 senyawa steroid/triterpenoid, Rf 0,02 (biru hijau); 0,23 (biru hijau), 0,32 (ungu),
0,52 (ungu); 0,637 (ungu), 0,75 (ungu ), 0,86 ( merah ungu); dan 2 noda lainnya Rf 0,68 (kuning coklat); 0,81 (kuning coklat).
Kromatogram analisa KLT fraksi n-heksan akar ekor naga (Rhaphidopora pinnata (L.f)schott ) dapat dilihat pada gambar 6 dibawah ini
Gambar 6. Kromatogram Hasil KLT Ekstrak n-heksan Akar Ekor Naga
Keterangan : Fase diam silika gel GF254, A= Fase gerak n-heksan –etil asetat 90:10;
4.7 Hasil Pemisahan Senyawa Steroid /Triterpenoid dari ekstrak n-heksan dengan cara Kromatografi Kolom
Pemisahan lebih lanjut ekstrak n-heksan dengan kromatografi kolom menggunakan fase gerak n-heksan-etil asetat (8:2) dan fase diam silika gel 60 mesh 70-230 ASTM dengan ukuran partikel 0,063-0,200.
Hasilnya ditampung pada vial masing-masing sebanyak 5 ml, diperoleh 83 vial. , kemudian dikelompokkan menjadi 7 fraksi berdasarkan eluen yang digunakan dan pengamatan
visual terhadap warna eluat, yaitu F1 (vial 1-9), F2 (vial 6-13), F3 (vial 13-17), F4 (vial 17-63), F5 (vial 64-68), F6 (vial 69-78), dan F7(vial 79-83). Pada F3 ditemukan kristal, yaitu pada V13,V14,V15, V16,V17 kemudian dilakukan KLT pada kelima vial tersebut .Hasilnya
yaitu diperoleh masing masing 1 noda dengan harga Rf yaitu 0,46,0,46, 0,48, 0,48, 0,48 karena memiliki noda tunggal dengan harga Rf yang hampir sama maka kelima vial digabungkan.
Kromatogram analisis Kromatografi Lapis Tipis eluat hasil kromatografi kolom fraksi n-heksan akar ekor naga (Rhaphidophora pinnata Schott) dapat dilihat pada gambar 7 berikut
Keterangan : Fase diam silika gel GF 254,fase gerak n-heksan- etil asetat (80:20)
4.8 Hasil Pengujian dengan KLT Dua Arah
Pada pemeriksaan KLT dua arah dengan fase gerak n-heksan-etilasetat (80:20) dan benzen-etil asetat (60:40), isolat memberikan satu bercak berwarna ungu dengan penampak
bercak LiebermanBurchard, harga Rf 0,44. Kromatogram uji kemurnian isolat fraksi n-heksan akar ekor naga (Rhaphidophora pinnata (L.f)schott) dapat dilihat pada gambar 8
berikut.
Gambar 8. Kromatogram KLT 2 Arah Fraksi n-heksan Akar Ekor Naga
Keterangan : Fase diam silika gel GF 254,fase gerak n-heksan- etil asetat (80:20), benzena-etilasetat 60:40, Penampak bercak Liebermann-Burchard,
tap = titik awal penotolan, bap 1 = batas akhir pengembangan 1,
4.9 Hasil Karakterisasi Isolat secara Spektrofotometri UV
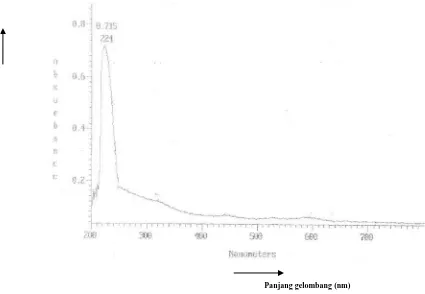
[image:53.595.110.535.248.542.2]Gambar spektrum ultraviolet isolat fraksi n-heksan akar ekor naga (Rhaphidophora pinnata Schott) dapat dilihat pada gambar 9 berikut:
Gambar 9. Spektrum Ultraviolet Isolat
Spektrum ultraviolet isolat memberikan panjang gelombang maksimum pada 224nm
yang menunjukkan adanya gugus kromofor (Sastrohamidjojo,1991).
Panjang gelombang (nm) A
4.10 Hasil Karakterisasi Isolat secara Spektrofotometri IR
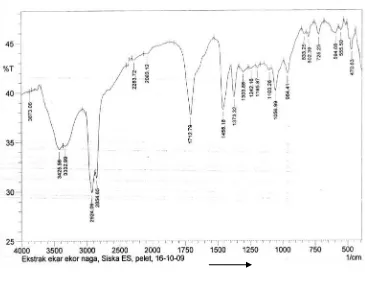
[image:54.595.199.564.195.478.2]Gambar spektrum inframerah isolat fraksi n-heksan akar ekor naga (Rhaphidophora pinnata Schott) dapat dilihat pada gambar 10 berikut :
Gambar 10. Spektrum Inframerah Isolat
Bilangan gelombang (cm-1)
Penafsiran spektrum inframerah isolat, antara lain terdapat serapan kuat pada bilangan
gelombang 1712,79 cm-1 menunjukkan adanya gugus C=O, serapan kuat pada bilangan gelombang 1458,18 cm-1 menunjukkan adanya gugus C=C aromatik, bilangan gelombang 1242,16 cm-1 menunjukkan adanya gugus C-O, bilangan gelombang 2924,06 cm-1
menunjukkan adanya gugus C-H alifatis, bilangan gelombang 3425,58 cm-1 menunjukkan adanya OH, dan bilangan gelombang 1373,32 cm-1 menunjukkan adanya gugus C-H metil
BAB IV
KESIMPULAN DAN SARAN 4.1 Kesimpulan
1. Hasil Skrining menunjukkan adanya senyawa Flavonoid, Saponin, Glikosida, Tanin dan Steroid /Triterpenoid.
2. Hasil analisis KLT pada ekstrak n-heksan akar ekor naga (Rhaphidophora pinnata Schott) dari diperoleh n-heksan-etilasetat (80:20) sebagai fase
gerak terbaik dengan pemisahan terbanyak.
3. Hasil Spektrofotometri ultraviolet diperoleh panjang gelombang maksimum 224 nm dan Hasil Spektrofotometri inframerah isolat
diperoleh adanya gugus C=O, C=C aromatik, C-O, OH, C-H alifatis dan C-H metil yang menunjukkan adanya senyawa steroid/triterpenoid
4.2 Saran
Disarankan kepada peneliti selanjutnya untuk melakukan elusidasi struktur terhadap senyawa steroid/ triterpenoid hasil isolasi yang diperoleh.
DAFTAR PUSTAKA
Anonim . 04 Des 2008. Rhaphidophora pinnata. ADLN Digital Collections. http
Anonim . 28 April 2008. Monster deliciosa.wikipedia.the free wikipedia.
BAB IV
KESIMPULAN DAN SARAN 4.1 Kesimpulan
1. Hasil Skrining menunjukkan adanya senyawa Flavonoid, Saponin, Glikosida, Tanin dan Steroid /Triterpenoid.
2. Hasil analisis KLT pada ekstrak n-heksan akar ekor naga (Rhaphidophora pinnata Schott) dari diperoleh n-heksan-etilasetat (80:20) sebagai fase
gerak terbaik dengan pemisahan terbanyak.
3. Hasil Spektrofotometri ultraviolet diperoleh panjang gelombang maksimum 224 nm dan Hasil Spektrofotometri inframerah isolat
diperoleh adanya gugus C=O, C=C aromatik, C-O, OH, C-H alifatis dan C-H metil yang menunjukkan adanya senyawa steroid/triterpenoid
4.2 Saran
Disarankan kepada peneliti selanjutnya untuk melakukan elusidasi struktur terhadap senyawa steroid/ triterpenoid hasil isolasi yang diperoleh.
DAFTAR PUSTAKA
Anonim . 04 Des 2008. Rhaphidophora pinnata. ADLN Digital Collections. http
Anonim . 28 April 2008. Monster deliciosa.wikipedia.the free wikipedia.
Departemen Kesehatan RI., (1979). Farmakope Indonesia. Edisi ketiga. Jakarta: Depkes RI. Hal. 649, 748.
Departemen Kesehatan RI., (1989). Materia Medika Indonesia. Jilid V. Jakarta: Depkes RI. Hal. 516-522, 536-540, 549-553.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Hal. 1-11
Farnsworth, N.R. (1966), Biological and phytochemical screening of plants, Journal of Pharmaceutical sciences, volume 55, No. 3, Chicago: Rcheis Chemical Company, P. 245-264
Gritter, R. J., Bobbitt, J. dan Schwarting, A. E. (1991). Pengantar Kromatografi. Penerjemah: Padmawinata, K. Ed 2. Penerbit ITB. Bandung. Gembong, T. (1990). Morfologi Tumbuhan. Cetakan keenam. Gadjah Mada
University Press. Yogyakarta. Hal. 54-58
Harborne, J. B. (1987). Metode Fitokimia Penuntun Cara Modern Menganalisis Tumbuhan. Penerjemah: Padmawinata, K dan Soediro, I. Ed. 2. Penerbit ITB. Bandung. Hal. 6,48-49, 147-149, 234
Heyne, K. (1987). Tumbuhan Berguna Indonesia. Jilid I. Cetakan I. Penerjemah : Badan Litbang Kehutanan. Penerbit Yayasan Sarana Wanajaya. Jakarta. Hal. 493-494
Hostettmann, K., Hostettmann, M., dan Marston, A. (1995). Cara Kromatografi Preparatif : Penggunaan pada Isolasi Senyawa Alam. Penerjemah: Padmawinata, K., Penerbit ITB. Bandung. Hal. 9-12, 33-34
Lenny, Sofia. (2006). Senyawa Terpenoid dan Steroid. [Diakses Desember 2010], Diambil dar Nurhanifah. (2009). Skripsi tentang Karakterisasi Simplisia, Skrining Fitokimia
dan Isolasi Senyawa Flavonoida dari Daun Tanaman Ekor Naga (Rhapidophora pinnata Schott).
Pavia, D. L., Lampman, G. M., and Kriz, G. S. (1979). Introduction to Spectroscopy. Philadelphia : Saunders Golden Sunburst Series. Pages 26-27.
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Penerjemah: Padmawinata, K. Penerbit ITB. Bandung. Hal. 139, 152-156
Sastrohamidjojo, H. (1985). Kromatografi. Yogyakarta: Penerbit Liberty. Hal. 1- 13, 26-41
Wijayakusuma,H.,dkk(1996). Tanaman Berkhasiat Obat di Indonesia.Cetakan Kedua.Pustaka Kartini.Jakarta.Hal 7.
Lampiran 1. Hasil Identifikasi Tumbuhan Ekor Naga (Rhapidophora pinnata Schott)