ISOLASI BAKTERI RUMEN KAMBING ASAL KALIGESING
DAN PENGARUH INOKULASINYA TERHADAP
KECERNAAN KALIANDRA (Calliandra calothyrsus) PADA
RUMEN KAMBING
ATUN BUDIMAN
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Isolasi Bakteri Rumen Kambing Asal Kaligesing dan Pengaruh Inokulasinya terhadap Kecernaan Kaliandra (Calliandra Calothyrsus) pada Rumen Kambing adalah karya saya dengan arahan dari komisi pembimbing dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Maret 2011
Atun Budiman
ABSTRACT
ATUN BUDIMAN. Microbe Isolation of Kaligesing Goat Rumen and It’s Inoculation effect to Goat Rumen on digestibility of Calliandra (Calliandra calothyrsus). Under direction of SURYAHADI, KOMANG G. WIRYAWAN, and BUDI TANGENDJAJA.
Research on the Isolation of tannin-digesting bacteria from the Kaligesing goat rumen and test its ability to digest tannin has been done. Isolates were obtained and then inoculated in the rumen systems goat who never consume calliandra. The study was conducted from February 1997 until September 1998. The study was conducted in four stages of research. First study, evaluating the potential of microbes in the rumen fluid of Kaligesing goats on digestibility of calliandra in vitro. A second study, bacteria isolated from Kaligesing goat rumen. A third study, evaluating the isolates in digesting tannin. The fourth study, inoculation of isolates into the rumen systems goat who never consume calliandra on digestibility calliandra in vitro. The first research results indicate that the microbes in the Kaligesing rumen goat capable of significantly better microbes digest calliandra of rumen fluid from calliandra adapted goats and goats who do not eat calliandra. The result of the second study yielded four isolates notated IK1, IK2, IK3, and IK4. The IK1 isolate die during the storage process. The third study results showed that all three isolates are able to digest condensed tannins in defined culture media. The fourth study showed that inoculation of goat rumen isolates in the system who never consume caliandra not meet expectations can enhance significantly on digestibility caliandra in vitro.
RINGKASAN
ATUN BUDIMAN. Isolasi Bakteri Rumen Kambing Asal Kaligesing dan Pengaruh Inokulasinya terhadap Kecernaan Kaliandra (Calliandra calothyrsus)
pada Rumen Kambing. SURYAHADI, KOMANG G. WIRYAWAN, dan BUDI TANGENDJAJA.
Legum kaliandra (Calbandra calothyrsus) merupakan salah satu tanaman pakan yang potensial karena produksi hijauannya termasuk tinggi dibanding tanaman pakan legume lainnya, juga memberi pasokan hijauan yang berkesinambungan karena kaliandra tetap tumbuh baik di musim kemarau.
Keunggulan kaliandra yang disebutkan di atas pemanfaatannya untuk ternak ruminansia belum optimal karena terhambat oleh terkandungnya senyawa anti nutrisi tanin pada tanaman ini. Tanin dapat berikatan dengan zat makanan yang menyebabkan zat makanan sukar dicerna oleh enzim-enzim saluran pencernaan ataupun enzim-enzim ekstraselular mikroba rumen.Berkaitan dengan itu diperoleh informasi bahwa kambing-kambing Peranakan Etawa (PE) di Desa Pandanrejo Kecamatan Kaligesing Kabupaten Purworejo Jawa Tengah sejak tahun 1982 biasa diberi pakan kaliandra dengan proporsi pemberiannya hingga mencapai 60%. Dari informasi ini mendasari pemikiran untuk mengisolasi mikroba rumennya.
Penelitian pertama dilakukan yaitu melakukan pengujian mikroba dalam cairan rumen kambing peranakan Etawa asal Kaligesing (PEK) terhadap kemampuannya mencerna kaliandra secara in vitro. Cairan rumen kambing PEK dibandingkan dengan cairan rumen kambing yang telah diadaptasi dengan kaliandra selama 6 bulan (A), dan cairan rumen dari kambing berpakan rumput gajah sebagai kontrolnya. Masing-masing carian rumen diberi dan tidak diberi
poly ethylene glycol (PEG). Peubah kecernaan diukur pada dua stage yaitu tahap fermentasi di rumen (stage 1) dan tahap hidrolisis enzimatis di pasca rumen (stage 2). Berdasarkan pengamatan peubah kecernaan disimpulkan bahwa mikroba yang terdapat pada cairan rumen kambing PEK lebih tinggi dari cairan rumen kambing A dan kontrolnya. Hal ini menunjukkan bahwa kemampuan mikroba kambing PEK secara terintegrasi unggul dalam mencerna kaliandra. Dengan penambahan PEG, masing-masing cairan rumen meningkat kecernaannya dibanding tanpa pemberian, hal ini menyimpulkan bahwa mikroba dalam kambing PEK belum maksimal dalam mencerna kaliandra. Kandungan tannin dalam kaliandra belum sepenuhnya teratasi oleh mikroba rumen kambing PEK.
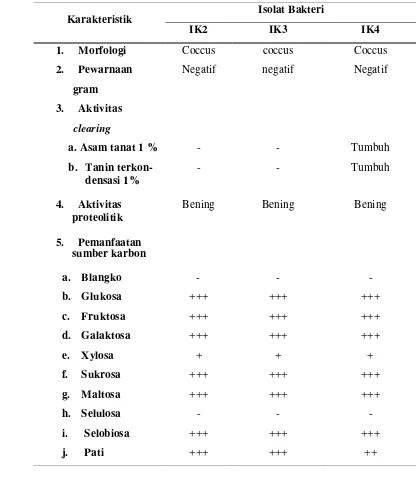
IK2, IK3, IK4. Keempat isolat tersebut selajutnya dilakukan pemurnian dan akhirnya disimpan sebagai stock. Pada saat akan dilakukan pengujian karakteristik, isolat IK1 tidak dapat tumbuh lagi, sehingga hanya tiga isolat yang bisa dilanjutkan pengujiannya. Isolat-isolat tersebut kemudian diuji karakteristiknya berdasarkan morfologi, jenis gram, aktivitas clearing, aktivitas proteolitik, dan kemapuan memanfaatkan jenis-jenis sumber karbon. Berdasarkan pengujian karakteristik ini, ternyata isolat IK 4 mempunyai nilai lebih dibanding dua isolat lainnya.
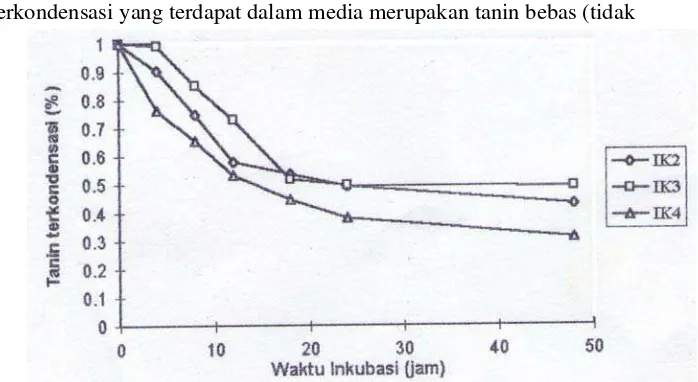
Penelitian ketiga adalah pengujian kemampuan ketiga isolat dalam mencerna tanin serta menganalisis produk metabolit berupa senyawa fenolat. Data diamati secara seri waktu (time series). Hasil pengujian menunjukkan bahwa ketiga isolate mampu mendegradasi tannin dan IK4 berkemampuan terbaik dibanding dua isolat lainnya.
Penelitian keempat adalah menginokulasi ketiga isolat tersebut ke dalam sistem rumen kambing yang tidak pernah mengkonsumsi kaliandra terhadap kecernaan kaliandra. Hasilnya bahwa nilai kecernaannya tidak mengalami peningkatan. Beberapa penjelasan mengenai ini di antaranya adalah bakteri yang diisolasi tidak dapat bekerja sendiri, diduga mekanisme pencernaan kaliandra pada kanbing PEK merupakan aksi kesatuan yang terintegrasi bersama-sama bakteri lainnya yang terdapat pada rumen kambing PEK.
©Hak Cipta IPB, tahun 2011
Hak Cipta dilindungi Undang-undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
ISOLASI BAKTERI RUMEN KAMBING ASAL KALIGESING
DAN PENGARUH INOKULASINYA TERHADAP
KECERNAAN KALIANDRA (Calliandra calothyrsus) PADA
RUMEN KAMBING
ATUN BUDIMAN
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Nutrisi dan Teknologi Pakan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Isolasi Bakteri Rumen Kambing Asal Kaligesing dan Pengaruh Inokulasinya terhadap Kecernaan Kaliandra
(Calliandra Calothyrsus) pada Rumen Kambing Nama : Atun Budiman
NIM : PTK 95055
Disetujui
Komisi Pembimbing
Dr. Ir. Suryahadi, DEA. Ketua
Prof. Dr. Ir. Komang G. Wiryawan Prof. Dr. Ir. Budi Tangendjaja, MAppSc. Anggota Anggota
Diketahui
Ketua Departemen Dekan Sekolah Pascasarjana Ilmu Nutrisi dan Teknologi Pakan
Dr. Ir. Idat Galih Permana, M.Sc.Agr. Dr. Ir. Dahrul Syah, M.Sc.Agr
PRAKATA
Ucapan syukur kepada Sang Pencipta, Allah SWT, adalah keniscayaan yang
harus dilakukan oleh hambaNya yang mendapat kelimpahan nikmat dariNya.
Demikian pula penulis yang sebagai hambaNya dalam hal ini mengucapkan rasa
syukur bahwasanya perjalanan panjang pendidikan di pascasarjana telah mencapai
akhir yang dinantikan.
Salah satu syarat akhir menyelesaikan studi adalah penelitian yang
dilengkapkan dengan pembuatan tesis. Kegiatan akhir ini telah dijalani selama 18
bulan yang dilaksanakan di Laboratorium Mikrobiologi Nutrisi dan Laboratorium
Nutrisi Ternak Perah Fakultas Peternakan IPB Bogor serta di Balai Penelitian
Ternak Ciawi Bogor. Sumber dana utama penelitian ini bersumber dari the
Australia Center for Agricultural Research (ACIAR) dan sumber dana dari
beasiswa Tim Manajemen Program Doktor (TMPD) Dirjen Dikti. Ucapan terima
kasih penulis kepada dua lembaga ini yang telah membiayai penelitian ini.
Selama pra penelitian sampai dengan penulisan tesis, penulis dibimbing dan
diarahkan oleh Komisi Pembimbing, oleh karena itu penulis ucapkan terima kasih
kepada Bapak Dr. Ir. Suryahadi, DEA sebagai ketua, Bapak Prof. Dr. Ir. Komang
G. Wiryawan sebagai anggota, dan Bapak Prof. Dr. Ir. Budi Tangendjaja,
Mapp.Sc. sebagai anggota.
Penelitian ini merupakan penelitian yang dilaksanakan tim. Antara anggota
tim telah terjalin kerjasama yang baik dalam pelaksanaan, diskusi, saling
menyemangati, oleh karena itu kami ucapkan terima kasih kepada rekan-rekan
satu tim : Bapak Usman Sewet, Bapak Syahriani Sahrir, dan Bapak Ali Bain.
Selanjutnya selama aktivitas di laboratorium di Fakultas Peternakan IPB penulis
banyak dibantu oleh teknisi, oleh karena itu saya ucapkan terima kasih kepada Ibu
Yani dan Bapak Adi. Selama kegiatan di laboratorium di Balai Penelitian Ternak,
penulis dibimbing Ibu Elisabeth Wina dan di Kandang dibantu oleh Bapak Udin,
oleh karena itu kepada keduanya penulis ucapkan terima kasih.Kepada Istriku
Yeti Sumiati, anak-anakku Annisa Nuraisyah Budiman dan Insan Arif Budiman,
Tesis ini adalah karya yang dibuat dengan segenap kemampuan penulis dan
ditopang oleh banyak pihak yang membantu, oleh karena itu semoga berfaedah
bagi siapapun yang membacanya.
Bogor, Maret 2011
RIWAYAT HIDUP
Penulis dilahirkan di Majalengka pada tanggal 5 Agustus 1964 dari Bapak Tasmali dan Ibu Rusmi. Penulis merupakan anak ke 10 dari 12 bersaudara.
Pendidikan sarjana ditempuh pada tahun 1985 hingga 1991 pada Fakultas Peternakan Universitas Padjadjaran Bandung. Penulis berkesempatan melanjutkan pendidikan program Magister Sains (S-2) yang didanai oleh Tim Manajemen Program Doktor (TMPD) Direktorat Jendral Pendidikan Tinggi (Dirjen Dikti) Departemen Pendidikan Nasional Republik Indonesia,
DAFTAR ISI
Halaman
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan Penelitian ... 3
Manfaat Penelitian ... 3
Hipotesis ... 3
TINJAUAN PUSTAKA ……… 4
Kaliandra ... 4
Tanin ... 6
Sistem Pencernaan Ternak Ruminansia ... 9
Potensi Ternak Teradaptasi dengan Pakan Kaliandra ... 11
METODE PENELITIAN ……….. 13
Waktu dan Tempat ………. 13
Penelitian I : Pengujian Potensi Miroba Rumen Kambing Peranakan Etawa Asal Kaligesing (PEK) terhadap Kecernaan Kaliandra in Vitro ... 13
Penelitian II : Isolasi Bakteri Rumen Kambing PEK ... 16
Penelitian III : Pengujian Kemampuan Isolat terhadap Pengurangan Kadar Tanin Terkondensasi dalam Media Khusus (Defined Media) ... 20
Penelitian IV : Inokulasi Isolat ke dalam Ekosistem Rumen Kambing yang tidak pernah Menkonsumsi Kaliandra terhadap Kecernaan Kaliandra in Vitro ... 21
Prosedur Analisis Sampel Penelitian ... 23
Komposisi dan Prosedur Pembuatan Media ... 26
HASIL DAN PEMBAHASAN ………. 30
Penelitian I 1: Pengujian Potensi Miroba Rumen Kambing PEK terhadap Kecernaan Kaliandra in Vitro ... 30
Penelitian II : Isolasi Bakteri Rumen Kambing PEK ... 36
Penelitian III : Pengujian Kemampuan Isolat terhadap Pengurangan Kadar Tanin Terkondensasi dan Perubahan Komponen Senyawa Fenolat dalam Media Khusus (Defined Media) ... 39
KESIMPULAN DAN SARAN ... 49
DAFTAR PUSTAKA ... 50
DAFTAR TABEL
Halaman
1 Perbandingan kecernaan (%) in vitro kaliandra terhadap legum lainnya ... 2 Pengaruh pengeringan terhadap kecernaan zat makanan (%) kaliandra pada kelinci dan ruminansia ...
3 Penggolongan tanin tumbuhan ...
4 Nilai rataan kecernaan zat makanan (%) in vitro dari perlakuan sumber cairan rumen sebagai inokulum mikroba ...
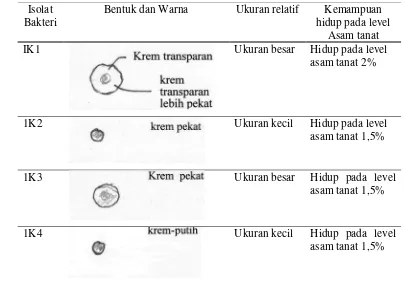
5 Karakteristik visual isolat bakteri rumen kambing PEK ...
6 Karakteristik isolat bakteri rumen kambing PEK ...
7 Nilai rataan kecernaan bahan kering dan organik (%) kaliandra in vitro dari perlakuan inokulasi isolat bakteri rumen kambing PEK dalam ekosistem rumen kambing berpakan rumput Gajah pada stage 1 ...
8 Nilai rataan kecernaan bahan kering dan organik (%) kaliandra in vitro dari perlakuan inokulasi isolat dalam ekosistem rumen kambing berpakan rumput Gajah pada Stage 1 dan 2 ...
9 Nilai pH rumen in vitro stage 1 dari perlakuan inokulasi isolat dalam ekosistem rumen kambing berpakan rumput Gajah ...
10 Nilai NH3 (mM) rumen in vitro stage 1 dari perlakuan inokulasi
DAFTAR GAMBAR
Halaman
1 Perubahan kadar tanin terkondensasi dalam media khusus yang
diinokulasikan isolat bakteri rumen kambing PEK ...
2 Perubahan komponen senyawa fenolat dalam media khusus yang
diinokulasi isolat IK2 ...
3 Perubahan komponen senyawa fenolat dalam media khusus yang
diinokulasi isolat IK3 ...
4 Perubahan komponen senyawa fenolat dalam media khusus yang
DAFTAR LAMPIRAN
Halaman
1. Data kecernaan zat makanan (%) in vitro stage 1 dan 2 dari perlakuan sumber cairan rumen sebagai inokulum mikroba (penelitian I) ... 52
2. Data kecernaan zat makanan (%) in vitro stage 1 dari perlakuan inokulasi isolat bakteri rumen kambing asal Kaligesing dalam ekosistem rumen kambing berpakan rumput Gajah (penelitian IV tahap 1) ... 55
3. Data kecernaan zat makanan (%) in vitro stage 1 dan 2 dari perlakuan inokulasi isolat dalam ekosistem rumen kambing berpakan rumput Gajah (penelitian IV tahap 2) ... 56
4. Data nilai pH rumen in vitro stage 1 dari perlakuan inokulasi isolat dalam ekosistem rumen kambing berpakan rumput Gajah
(penelitian IV tahap 2) ... 57
5. Data nilai NH3 (mM) in vitro stage 1 dari perlakuan inokulasi isolat dalam ekosistem rumen kambing berpakan rumput Gajah
(penelitian IV tahap 2) ... 58
6. Analisis ragam data kecernaan zat makanan (%) in vitro stage 1 dari perlakuan sumber cairan rumen sebagai sumber inokulum mikroba (penelitian I) ... 59
7. Analisis ragam data kecernaan zat makanan (%) in vitro stage 1 dari perlakuan inokulasi isolat bakteri rumen kambing asal Kaligesing dalam ekosistem rumen kambing berpakan rumput Gajah
(penelitian IV tahap 1) ... 61
8. Analisis ragam data kecernaan bahan kering (%) in vitro stage 1 dan 2 dari perlakuan inokulasi isolat dalam ekosistem rumen kambing berpakan rumput gajah (penelitian IV tahap 2) ... 62
9. Analisis ragam data nilai pH rumen in vitro stage 1 dari perlakuan inokulasi isolat dalam ekosistem rumen kambing berpakan rumput Gajah (penelitian IV tahap 2) ... 63
PENDAHULUAN
Latar Belakang
Kaliandra (Calbandra calothyrsus) merupakan salah satu tanaman yang sering dipropagandakan sebagai tanaman konservasi untuk lahan-lahan
marginal dan kehutanan. Tanaman ini telah lama diperkenalkan kepada
peternak sebagai sumber pakan ternak ruminansia, sehingga dilihat dari
kepentingan usaha ternak ruminansia maka upaya konservasi ini memberi
keuntungan bagi para peternak di lingkungan penanamannya.
Keunggulan kaliandra yang khususnya berkaitan dengan kepentingan
pakan ternak adalah : (1) Mempunyai kandungan protein yang cukup tinggi
(±20%); (2) kuantitas panen hijauan cukup baik sekitar 10 ton per hektar
pada kepadatan 10.000 tanaman per hektar dengan tinggi pemotongan 1 m pada
interval pemotongan 12 minggu (Tangendjaja et al. 1992); (3) memberi pasokan hijauan yang berkesinambungan karena kaliandra tetap tumbuh baik di musim
kemarau.
Keunggulan kaliandra yang disebutkan di atas pemanfaatannya untuk ternak
ruminansia belum optimal karena terhambat oleh terkandungnya senyawa anti
nutrisi tanin pada tanaman ini. Senyawa tanin ini terkandung dalam kaliandra
tergolong tinggi, yaitu ±8% (metode analisis presipitasi-protein). Tanin
adalah senyawa yang sangat mudah bereaksi dengan protein membentuk
senyawa kompleks yang stabil. Senyawa tanin dalam sel tanaman terpisah
dari protein dan enzim-enzim sitoplasma. Ketika sel rusak akibat dikonsumsi
ternak maka tanin terbebaskan dan kemudian mengikat zat- zat makanan
(terutama protein) dalam sel tanaman membentuk ikatan kompleks yang stabil
(Harborne 1984). Zat makanan yang terikat dalam tanin sukar dicerna oleh
enzim-enzim saluran pencernaan ataupun enzim-enzim ekstraselular mikroba
rumen. Tanin yang terbebaskan akibat sel rusak tidak hanya mengikat zat
makanan dalam sel tanaman tersebut, akan tetapi mengikat pula enzim-enzim
senyawa protein). Tanin yang terbebaskan dapat berikatan dengan enzim
glicoprotein dalam mulut yang menyebabkan rasa sepat. Rasa sepat menyebabkan ternak kurang menyukai untuk mengkonsumsinya. Pengaruh negatif tanin dalam
kaliandra sebagai pakan ternak ruminansia membatasi keunggulannya.
Pemberian kaliandra dalam keadaan segar adalah yang terbaik dan
menurun setelah pelayuan, dan lebih buruk lagi bila dikenai perlakuan pengeringan
(Tangendjaja et al. 1992). Kenyataan ini mempersempit cara pemberian kaliandra. dalam bentuk lain misalnya bentuk tepung (untuk konsentrat).
Ternak ruminansia yang teradaptasi dengan pakan bertanin tinggi
akan mempunyai kemampuan yang lebih baik dalam memanfaatkan kaliandra,
hal ini mungkin diakibatkan perubahan kondisi faali dan perubahan pada
komposisi mikroba rumen. Adapatasi terhadap pakan bertanin tinggi yang
berlangsung melewati beberapa generasi, karena faktor seleksi (baik alami
atau sengaja) berpeluang memunculkan mikroorganisme rumen yang spesifik
yang berperanan dalam meredam efek negatif tannin. Brooker et al. (1994) melaporkan bahwa Streptococcus caprinus yang ditemukannya pada kambing liar (feral goats) dapat menghidrolisis asam galat (merupakan komponen asam tanin) menjadi pyrogallol dan dapat tumbuh pada kondisi 3% asam tanat. Bakteri ini di bagian luar selnya terdapat sejumlah besar polisakarida
ekstraseluler yang berfingsi melindungi aksi tanin.
Eksplorasi mengenai bakteri-bakteri spesifik ini masih kurang, dan
berkaitan dengan itu diperoleh informasi bahwa kambing-kambing Peranakan
Etawa (PE) di Desa Pandanrejo Kecamatan Kaligesing Kabupaten Purworejo
Jawa Tengah sejak tahun 1982 biasa diberi pakan kaliandra dengan proporsi
pemberiannya hingga mencapai 60% (Subandriyo et al. 1995). Dari informasi ini mendasari pemikiran untuk mengisolasi mikroba rumennya.
Isolat mikroba akan ditunjukkan pada isolat bakteri. Isolat ini akan di uji
aksinya. Isolat yang diperoleh akan diinokulasikan pada cairan rumen
kambing yang belum beradaptasi dengan pakan kaliandra. Inokulasi tersebut
bertujuan memperpendek masa adaptasi dan mengoptimalkan pemanfaatan
Tujuan Penelitian
1. Untuk mendapatkan isolat bakteri toleran/pendegradasi tanin dari
kambing asal Kaligesing.
2. Untuk mengetahui pengaruh inokulasi isolat bakteri tersebut terhadap
kecernaan pakan kaliandra.
Manfaat Penelitian
Isolat bakteri toleran/pendegradasi tanin hasil penelitian ini dapat
dimanfaatkan para peternak kambing untuk mengoptimalkan pemberian pakan
bertanin terutama kaliandra dan meningkatkan produksi ternak yang lebih baik.
Penelitian ini diharapkan pula untuk dijadikan informasi dalam mengkaji lebih
jauh dalam penelitian sejenis.
Hipotesis
Akan diperoleh isolat bakteri toleran/pendegradasi tanin dari
kambing asal kambing Kaligesing dan isolat tersebut mampu meningkatkan
TINJAUAN PUSTAKA
Kaliandra
Tanaman kaliandra (Calliandra calothyrsus) berasal dari Amerika Latin. Masuk ke Indonesia pada tahun 1936 ke pulau Jawa. Pohon ini ditanam
pada mulanya ditunjukan sebagai penahan erosi dan penghijauan, terutama di
lahan milik Kehutanan. Manfaat lain dari tanaman ini dapat dijadikan sumber
pupuk hijau, tanaman pelindung, kayu bakar, dan menghasilkan daun yang
potensial sebagai sumber pakan. Pohon ini terpilih karena kemampuan
tumbuhnya yang baik pada berbagai iklim dan tanah. Kaliandra dapat
tumbuh baik pada ketinggian antara 400 sampai dengan 1800 meter di atas
permukaan laut serta toleransinya terhadap kekeringan berkatagori sedang
yaitu satu sampai tujuh bulan (Tangendjaja et al. 1992).
Tanaman ini termasuk famili Mimosidae, merupakan pohon kecil,
tumbuh bersemak dengan ketinggian berkisar 4-6 meter. Pada
lingkungan yang sesuai pertumbuhannya dapat mencapai 12 meter dengan
diameter batang mencapai 30 cm. Daun berwarna hijau gelap dan warnanya
berwarna coklat kehitaman. Kanopinya melebar ke samping dan sangat padat.
Tipe daun merupakan daun majemuk yang berpasangan. Bunganya berwarna
merah dengan panjang 4-6 cm, sedang buahnya berwarna coklat kehitaman
dengan panjang 8-11 cm dan lebar 12 mm. Bentuk bijinya ellips dan pipih
(Tangendjaja et al. 1992).
Perbanyakan kaliandra umumnya dilakukan dengan menggunakan biji
yang terlebih dahulu disemaikan. Selain itu dapat dilakukan dengan
menggunakan stek pucuk tanaman (Tangendjaja et al. 1992).
Pada kepadatan tanaman 10000 tanaman perhektar, produksi hijauan
kaliandra dapat mencapai 10 ton per hektar di Sei Putih Sumatra Utara- Hasil yang
sama telah dilaporkan pula di beberapa tempat seperti Sulawesi Selatan dan
Jawa Barat. Lebih jauh hasil di Sulawesi Selatan dilaporkan produksi
(Tangendjaja et al. 1992).
Komposisi analisis proksimat kaliandra menunjukkan bahwa
kandungan protein kasarnya berkisar di atar 20%, dan bila yang dianalisis bagian
daun mudanya saja tanpa ranting-ranting yang halus dapat mencapai 30%.
Berdasarkan hasil analisis proksimat di BPT Ciawi Bogor adalah sebagai
berikut : Protein kasar 24 %, lemak kasar 4,1-5,0%, abu 5,0-7,6%, NDF
24,0-34,0%, selulosa 15,0%, lignin10,0-11,8% (Tangendjaja et al. 1992)
Pemanfaatan kaliandra sebagai pakan ternak pada awalnya kurang
berkembang bila dibandingkan dengan lamtoro dan gamal. Hal ini berkaitan
dengan kandungan anti nutrisi tanin yang tinggi pada tanaman tersebut.
Suryadi (1955) melaporkan bahwa kaliandra yang dianalisis dengan
metode Van-HCI mengandung tanin 9,11%. Kehadiran tanin
menyebabkan daya cerna in vitro kaliandara berkisar antara 35% sampai 53%. Nilai tersebut jauh lebih rendah dibandingkan daya cerna legum lain,
kecuali dengan Albizza chinensis. Pada tabel berikut diperlihatkan perbandingan kecernaan in vitro kaliandra terhadaplegum lainnya.
Tabel 1. Perbandingan kecemaan (%) in vitro kaliandra terhadap legum lainnya.
Legum Kecernaan in Vitro Bahan Kering Ahl et al. 1989 Mahyudin et al. 1988
Calliandra calothyrsus 52,7 37,8
Leucaena leucocephala 82,1 63,5
Gliricidia sepium 79,1 69,0
Sesbania sesban 69,3 -
Albizzia chinensis 37,1 -
Samanea samara 69,3 -
Sesbania grandiflora - 71,5
Albizzia falcataria - 49,2
Perlakuan fisik terhadap pakan kaliandra menyebabkan nilai kecernaan
berubah. Pengaruh pengeringan dan pelayuan akan menurunkan nilai
kecernaan. Pada tabel berikut diperlihatkan perubahan nilai kecernaan
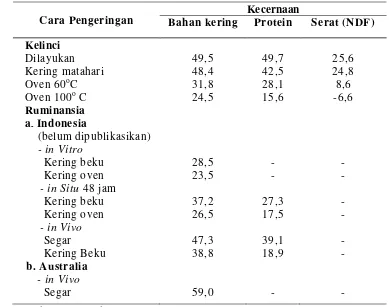
Tabel 2. Pengaruhpengeringan terhadap kecernaan zat makanan (%) kaliandra pada kelinci dan ruminansia
Cara Pengeringan
Kecernaan
Bahan kering Protein Serat (NDF)
Kelinci
Dilayukan 49,5 49,7 25,6
Kering matahari 48,4 42,5 24,8
Oven 60oC 31,8 28,1 8,6
Oven 100o C 24,5 15,6 -6,6
Ruminansia a- Indonesia
(belum dipublikasikan)
- in Vitro
Kering beku 28,5 - -
Kering oven 23,5 - -
- in Situ 48 jam
Kering beku 37,2 27,3 -
Kering oven 26,5 17,5 -
- in Vivo
Segar 47,3 39,1 -
Kering Beku 38,8 18,9 -
b. Australia
- in Vivo
Segar 59,0 - -
Sumber : Tangendjaja et al. (1992)
Tanin
Tanin merupakan senyawa bahan alam dalam tanaman yang terdiri dari
sejumlah besar gugus hidroksi fenolik. Senyawa ini diperlukan oleh
tanaman sebagai sarana proteksi dari serangan hewan, bakteri, jamur, dan
insekta. Proteksi ini terutama selama tanaman dalam masa pertumbuhan (White
1957). Sifat utama tanin ini dapat bereaksi dengan protein atau polimer lainnya
seperti selulosa, hemiselulosa, pektin membentuk suatu kompleks yang
stabil dan tidak larut dalam air (Tangendjaja et al. 1992; Harborne 1984). Dalam industri, tanin dipergunakan untuk penyamakan kulit hewan yang
mentah menjadi kulit siap pakai karena kemampuannya menyambung-silang
Di dalam tumbuhan letak tanin terpisah dari protein dan enzim sitoplasma,
tetapi bila jaringan rusak, misalnya bila hewan memakannya maka reaksi
penyamakan dapat terjadi. Reaksi ini menyebabkan protein tanaman bereaksi
dengan tanin sehingga protein lebih sukar dicerna oleh enzim-enzim pencernaan
hewan (Harborne 1984).
Selain protein sukar dicerna karena bereaksi dengan tanin membentuk
ikatan yang stabil, tanin pun dapat menimbulkan rasa sepat yang dirasakan hewan
yang mengkonsumsinnya. Rasa sepat dapat mengurangi konsumsi. Mekanisme
terjadinya rasa sepat disebabkan senyawa tanin pada tanaman tersebut
berikatan glycoprotein dalam mulut. Selain itu akan berikatan pula dengan
protein mukosa intestin yang mengurangi penyerapan nutrien saliva.
Kandungan tanin dalam daun mulai dari 2% ke atas dari berat keringnya, barulah
tanin berfiingsi sebagai penolak makan (Harborne 1984).
Mekanisme proteksi tanaman bertanin (kaliandra) terhadap serangga dan
insekta yaitu dengan menonaktifkan enzim-enzim protease yang dihasilkan mereka
(Cheeke & Lee 1985).
Tanin selain dapat membentuk kompleks dengan zat makanan, juga
mampu berikatan dengan enzim-enzim pencemaan serta enzim-enzim yang
dikeluarkan oleh mikroba rumen sehingga menjadi nonaktif sehingga zat
makanan tidak tercerna. (Makkar 1993)- Nonaktifnya enzim yang dihasilkan
mikroba ini mungkin diakibatkan oleh ikatan antara tanin dengan dinding sel
yang dapat menggangu permeabilitas dinding sel mikroba tersebut.
Bentuk interaksi yang mungkin terjadi antara tanin dengan protein
atau zat lainnya berupa interaksi ikatan hidrogen, interaksi hidropfobik,
interaksi ikatan ionik, dan interaksi ikatan kovalen (Hagerman 1992; Makkar
1993). Bentuk interaksi ikatan ionik dan interaksi hidrofobik merupakan
bentuk interaksi yang paling banyak membentuk kompleks protein-tanin
(Hagerman 1992).
Ternak yang mengkonsumsi pakan bertanin tinggi dapat menurun
bobot badannya dan yang terlihat sangat nyata pada penurunan
Secara kimia tanin digolongkan dalam dua grup, yaitu tanin
terkondensasi (condens tannin) dan tanin terhidrolisis (hidrolizable tannin).
Meskipun dua grup tanin tersebut mempunyai struktur molekul yang
berbeda akan tetapi efeknya sebagai anti nutrisi hampir sama (Butler &
Rogler 1992).
Tabel 3. Penggolongan tanin tumbuhan
Sumber : Harborne (1984)
Tanin terkondensasi atau flavolan, secara biosintesis dapat dianggap
terbentuk dengan cara kondensasi katekin tunggal (atau galokatekin) yang
membentuk senyawa dimer dan kemudian membentuk oligomer yang lebih
tinggi. Ikatan karbon-karbon menghubungkan satu satuan flavon dengan
berikutnya melalui ikatan 4-8 atau 6-8. Kebanyakan flavolan mempunyai 2
sampai 20 satuan flavon. Nama lain untuk tanin terkondensasi ialah
proantosianidin karena bila direaksikan dengan asam panas, beberapa
ikatan karbon-karbon penghubung satuan terputus dan membebaskan
monomer antosianidin (Harborne 1984).
Tanin terhidolisis terdiri dari dua kelas yang paling sederhana, ialah
depsida galoiglukosa. Pada senyawa ini, inti yang berupa glukosa dikelilingi
lima gugus ester galoil atau lebih. Pada jenis kedua, inti molekul berupa senyawa
dimer asam galat, yaitu asam heksahidroksidifenat, disinipun berikatan dengan
Tata Nama Struktur Bobot molekul
Tanin terkondensasi
Proantosianidin (atau flavolan)
Oligomer katekin flavan 3,4-diol
1000-3000
Tanin terhidrolisis
Galotanin
Elagitanin
Ester asam galat dan glukosa
Ester asam heksahidroksidifenat dan glukosa
1000-1500
1000-3000
Prototanin
Pra zat tanin Katekin (dan galokatekin) flavan 3,4-diol
glukosa. Bila dihidrolisis, elagitanin ini menghasilkan asam elagat (Harborne,
1984)
Tanin terhidrolisis dapat dihidrolisis dengan asam mineral panas yang akan
menghasilkan gula dan asam-asam yang menjadi senyawa pokoknya (Cheeke
& Lee 1985). Tanin terhidrolisis dapat juga terhidrolisis oleh enzim-enzim dalam
saluran pencernaan. Asam galat yang merupakan komponen tanin terhidrolisis
dapat diarbsorbsi tubuh yang kemudian disekresikan melalui urin (Butler &
Rogler 1992).
Sistem Pencernaan Ternak Ruminansia
Rangkaian proses perubahan fisik dan kimia yang dialami oleh bahan
makanan di dalam alat pencernaan pada dasarnya adalah menghaluskan
makanan menjadi partikel yang lebih kecil. Pada ternak ruminansia proses
pencernaan makanannya lebih kompleks dibandingkan dengan jenis ternak
lainnya. Menurut sutardi (1977) proses pencernaan makanan pada ternak
ruminansia terjadi secara mekanis di mulut, secara hidrolisis dengan
penggunaan enzim-enzim alat pencernaan, dan secara fermentatif (penggunaan
enzim-enzim yang dikeluarkan mikroba rumen). Perbedaan prinsip
hidrolisis dan fermentatif adalah pada hidrolisis zat makanan dikatabolisir menjadi
monomer-monomernya, sedangkan fermentatif akan mengkatabolisir lebih lanjut
dari monomer-monomer tersebut menjadi senyawa-senyawa yang lebih
sederhana, misalnya asam-asam lemak terbang (volatile fatty acid/VFA) (Church, 1980).
Proses Pencernaan dalam retikulo-rumen terjadi sangat intensif.
Proses pencernaan tersebut terletak sebelum usus halus. Hal ini sangat
menguntungkan, karena pakan dapat diubah dan disajikan dalam bentuk yang
mudah diserap. Ternak ruminansia juga dapat memanfaatkan pakan berserat
dalam jumlah banyak
-Empat jenis mikroba anaerob terdapat dalam rumen, yaitu bakteri,
protozoa, jamur, dan virus. Dari keempat jenis mikroba tersebut, bakteri
mencapai 1010-1011, sedangkan posisi populasi tertinggi kedua diduduki oleh
protozoa yang mencapai 106-108 cacahan sel per ml isi rumen, pada kondisi
ternak, yang sehat (Ogimoto & Imai, 1984).
Setiap jenis mikroba rumen, musing-masing mampu menghidrolisis
zat makanan menjadi produk intermedier ataupun produk akhir yang
bermacam-macam sehingga kehidupan dalam rumen menjadi rumit
(kompleks). Terjadi interaksi dan interrelasi yang luas di antara mikroba
rumen. Bentuk interaksi tersebut dapat berupa saling bergantung akan
substrat, saling menguntungkan, berkompetisi akan substrat, atau saling
merugikan. Studi ekologi mikroba rumen masih dipusatkan pada dua aspek
utama yaitu pengendalian populasi mikroba rumen dan peningkatan
peranan mikroba rumen dalam mencerna pakan (Erwanto, 1995).
Kehadiran substrat tertentu seperti mimosin, saponin, atau tanin
dalam pakan yang dikonsumsi ternak ruminansia dapat mengganggu
aktivitas mikroba rumen. Kemampuan tanin yang dapat membentuk
ikatan kompleks dengan zat makanan menyulitkan zat makanan dicerna
oleh enzim-enzim pencernaan, selain itu tanin mampu pula berikatan
dengan enzim-enzim protease dan selulase, bahkan mampu pula
berikatan dengan sel mikroba yang menyebabkan non aktifnya sel mikroba
(Leinmuller et al. 1991). Brooker et al. (1994) melaporkan bahwa tanin terkondensasi dapat menghambat kelangsungan hidup beberapa
mikroba. Meskipun demikian terdapat indikasi bahwa beberapa bakteri
mampu toleran terhadap tanin, khususnya pada ternak-ternak yang
beradaptasi pada pakan bertanin tinggi. Streptococcus caprinus adalah jenis bakteri yang mampu hidup dalam media bertanin konsentrasi 3% dan
mampu membentuk daerah bening (clearing zone). Bakteri Streptococcus bovis hanya mampu bertahan dalam media bertanin dengan konsentrasi kurang dari 1%
Ketersediaan amonia dalam rumen sebagai sumber nitrogen utama
untuk sintesis sel mikroba sangat menentukan optimalisasi pertumbuhan
mikroba rumen mampu menggunakan amonia sebagai sumber nitrogen untuk
sintesis protein tubuhnya- Diperkirakan pada mikroba tersebut tidak terdapat
mekanisme transport khusus yang mengangkut asam amino ke dalam sel
tubuhnya. Pernyataan ini di perkuat oleh Bryant (1974) yang menyatakan bahwa
sebagian besar mikroba rumen mampu mengunakan ammonia sebagai
nitrogennya. Oleh karena itu konsentrasi ammonia dalam rumen sangat perlu
untuk di kendalikan. Penelitian in vivo yang di lakukan oleh Mehnez et al. (1977) pada ternak domba memperlihatkan bahwa untuk memaksimumkan laju
fermentasi dalam rumen diperlukan konsentrasi ammonia yang tinggi yaitu
sebesar 23,5 mg% atau setara 16,78 mM.
Potensi Ternak Teradaptasi dengan Pakan Kaliandra
Palatabilitas dan kecernaan yang rendah dari pakan kaliandra menimbulkan
penampilan produksi yang rendah pula. Namun kaliandra mempunyai keunggulan
dibanding legum yang lainnya yaitu lebih ternjamin kontinuitasnya di musim
kemarau.
Ternak ruminansia yang telah terbiasa dengan kaliandra (pakan bertanin
tinggi) akan lebih baik daripada yang belum terbiasa. Pembiasaan pemberian
pakan kaliandra menimbulkan pergeseran komposisi mikroflora rumen ke arah
konsentrasi substrat (kaliandra adalah pakan berprotein tinggi, hal ini
menyenbabkan bakteri proteolitik akan lebih dominan). Sedangkan ternak yang
telah lama beradaptasi dengan pakan kaliandra, tidak hanya mengalami
pergeseran komposisi mikroba atas keadaan substrat akan tetapi mungkin
terbentuk spesies spesifik yang tahan atas kehadiran zat anti nutrisi tanin dan lebih
jauh mampu menghidrolisisnya. Ternak yang tealh beradaptasi ini diharapkan
dapat diisolasi mikroba rumennya sebagai isolate sebagai bahan inokulan untuk
ternak lain yang belum beradaptasi dengan kaliandra. Upaya ini mempunyai dua
tujuan yaitu memperpendek masa adaptasi dan mengoptimalkan pemanfaatan
kaliandra.
Ternak kambing Peranakan Etawa (PE) yang di pelihara di Desa Pandanrejo
kaliandra dengan proporsi hingga 60% (Subandryo et al. 1995). Kaliandra di desa
tersebut telah dibudidayakan sejak tahun 1982, dan merupakan pakan utama
METODE PENELITIAN
Waktu dan Tempat
Penelitian dilaksanakan di Laboratorium Mikrobiologi Nutrisi dan
Laboratorium Nutisi Ternak Perah Fakultas Peternakan IPB Bogor dan di Balai
Penelitian Ternak Ciawi Bogor. Waktu pelaksanaan mulai bulan Februari 1997
sampai dengan September 1998.
Penelitian I
Pengujian Potensi Mikroba Rumen Kambing Peranakan Etawa asal Kaligesing (PEK) terhadap Kecernaan Kaliandra in Vitro
Penelititan ini bertujuan untuk menguji potensi mikroba rumen kambing
PEK (K) dalam mencerna pakan kaliandra (Calliandra calothyrsus). Sebagai pembandingnya (kontrol), maka digunakan kambing yang diberi pakan 100%
kaliandra salama labih dari 6 bulan (A), kambing yang diberi pakan 100% rumput
gajah (R).
Persiapan
Empat ekor ternak kambing dipersiapkan dan dipelihara di kandang
individual di lokasi Kandang Penellitian ternak domba BPT Ciawi. Dua ekor
diberi pakan 100% kaliandra dan dua ekor diberi pakan 100% rumput gajah.
Pemberian jumlah pakan dan air minum tidak dibatasi, pemberian dilakukan dua
kali pada pagi dan sore. Sisa pakan dibuang keesokan harinya dan diganti dengan
yang baru. Kaliandra diberikan dalam bentuk potongan bagian daun dan batang
terkecilnya, sedangkan rumput gajah diberikan dalam bentuk potongan ukuran 2-5
cm. empat ternak tersebut dipelihara dengan perlakuan tersebut salama 6 bulan,
dan kemudian setelah melewati waktu tersebut ternak siap diambil cairan
rumennya untuk bahan inokulum percobaan in vitro.
Dua ekor kambing PEAK yang berumur 6 dan 8 bulan didatangkan dari
Desa Pandanrejo Kecamatan Kaligesing Kabupaten Purworejo Jawa Tengah.
Ternak Ciawi. Setelah dikarantina kemudian ditempatkan di kandang individual
bersama empat ekor kambing lainnya. Dua ternak ini diberi pakan 100%
kaliandara, dua hari kemudian siap diambil cairan rumennya untuk bahan
inokulum percobaan in vitro.
Perlakuan
Pemberian senyawa poly ethylene glicol (PEG) dalam pakan bertanin terbukti terbaik dalam meredam efek negatif tanin, namun karena bahan ini masih
mahal maka tidak ekonomis untuk dilakukan di lapangan. PEG mampu mengikat
tanin sehingga tanin tidak sempat bereaksi dengan zat makanan. Kemampuan
mikroba dalam rumen kambing yang diuji dalam mengatasi tanin, perlu diketahui
kemampuannya bila ditanbahkan PEG, sehingga diketahui potensi maksimumnya.
Dalam penelitian ini cairan rumen yang berasal dari kambing PEK (K)
kambing berpakan 100% kaliandra (A), dan kambing berpakan 100% rumput
gajah (R) merupakn perlakuan utama, sedangkan penambahan PEG pada cairan
rumen merupakan perlakuan yang menyisipi perlakuan utama.
Perancangan penelitian untuk tahap ini adalah Acak Kolompok berpola
faktorial 3×2, yaitu:
1. Faktor pertama
K = Cairan rumen kambing PEK
A = Cairan rumen kambing berpakan 100% kaliandra
R = Cairan rumen kambing berpakan 100% rumput gajah
2. Faktor kedua
P = Penambahan PEG
0 = Tanpa Penambahan PEG
Percobaan in Vitro
Cairan rumen untuk percobaan ini diambil dengan metode oral, yaitu
pengambilan melalui mulut menggunakan selang. Pengambilan cairan rumen
dilakukan pada pagi hari sebelum diberi pakan. Cairan rumen ditampung dalam
thermos kapasitas 400 ml. Thermos didisi penuh cairan rumen dengan tujuan
rumen dalam thermos socepatnnya di bawa ke laboratorium untuk digunakan
dalam percobaan in vitro.
Percobaan in vitro menggunakan metode Tilley and Terri (1963) yang dimodifikasi oleh Close and Menke (1985). Tabung polypropilene 50 ml
digunakan sebagai tabung fermentor. Tabung tersebut telah sebelumnya diisi
tepung daun kaliandra sebanyak 0.5 g. Takaran penggunaan PEG adalah
sebanyak 2 kali kandungan tanin tepung daun kaliandra. Kandungan tanin daun
kaliandra 8%, sehingga pemberian PEG adalah 16%. Setiap tabung yang telah
disiapkan sesuai perlakuan, ditambahkan 30 ml campuran larutan MC Dougall
dan cairan rumen dengan rasio 4:1. Tabung tanpa sampel tepung kaliandra
disiapkan (tabung yang ini disebut blangko), kemudian di perlakukan sama
dengan lainnya. Residu dari blangko selanjutnya dalam penghitungan kecernaan
kaliandra, menjadi pengurang (koreksi) residu kecernaan pakan. Dengan
demikian terdapat 6 tabung perlakuan dan 3 blangko. Percobaan ini dilakukan
dalam dua stage, maka tabung yang dipergunakan menjadi 12 tabung dengan 6
blangko. Tabung sebanyak itu untuk mendapatkan satu peubah.
Larutan campuran Mc Dougall dan cairan rumen terus menerus dialiri gas
CO2 untuk menjamin kodisi anaerob. Selanjutnya campuran tersebut diisikan
dalam tabung fermentor, kemudian segera ditutup dengan sumbat karet berkatup
(katup berfungsi sebagai pelepas gas hasil fermentasi). Tabung kemudian
diinkubasi pada suhu 39 0C selama 48 jam dalam shaker bath (stage 1). Stage 1 merupakan tiruan (artificial) proses pencernaan fermetatif di rumen. Akhir Stage 1, tutup tabung dibuka. Tabung-tabung yang diperuntukkan mendapatkan
kecernaan pada stage 1, selanjutnya isi tabung disaring dengan kertas saring merk
Whatman no 41 menggunakan pompa vakum. Residu yang diperoleh dianalisis
lebih lanjut untuk memperoleh peubah kecernaannya. Sedangkan tabung-tabung
yang diperuntukkan untuk uji kecernaan pada stage 2, maka setiap tabung
ditambahkan berturut-turut 2 ml HCl 4 N dan 0.06 g pepsin (merk Sigma).
dianalisis lebih lanjut untuk mendapatkan peubah kecernaan. Stage 2 merupakan
tiruan (artificial) proses pencernaan hidrolisis enzimatias di pasca rumen.
Jumlah tabung dan kapasitas tampung tabung dalam shaker bath yang terbatas menyebabkan percobaan ini menggunakan perancangan Acak Kelompok.
Waktu pengambilan cairan rumen sebagai kelompok, maka prosedur di atas
diulang tiga kali dalam waktu yang berurutan.
Peubah yang Diamati
Peubah kecernaan diamati dalam dua Stage. Pada Stage 1 (fase fermentatif)
diamati peubah kecernaan bahan kering (BK), bahan organik (BO), protein (P),
serat deterjen netral (neutral detergent fiber/NDF), dan Serat Deterjen Asam (acids detergent fiber/ADF). Peubah yang diamati pada Stage 2 (fase fermentatif dan enziamtis) adalah BK, BO, dan P.
Analisis statistik
Penelitian ini didesain dengan rancangan acak kelompok (RAK) dengan
waktu pengambilan cairan rumen merupakan kelompok. Perlakuan diulang tiga
kali. Data yang diperoleh dianalisis statistik menggunakan analisis ragam.
Perbedaan antar perlakuan diuji dengan uji jarak berganda Duncan (Steel &Torrie,
1993).
Penelitian II
Isolasi Bakteri Cairan Rumen Kambing PEK
Penelitian tahap ini merupakan upaya isolasi bakteri rumen kambing PEK
yang mempunyai potensi toleran terhadap kehadiran tanin dan diharapkan
mempunyai kemampuan menguraikan senyawa tersebut.
Prosedur ini terdiri dari isolasi koloni, pemurnian, identifikasi, dan
Isolasi Koloni
1. Pembiakkan Bakteri pada Media Cair
Disiapkan empat tabung berisi 10 ml media biakan cair (broth) brain heart infusion (BHI)yang masing-masing mengandung asam tanat 1%, 1,5%, 2%, dan 3% . Ke dalam masing-masing tabung dimasukkan 0.5 ml cairan rumen
kambing PEK. Mikroba yang terdapat dalam cairan dibiakkan dalam empat
tabung tersebut diinkubasi dalam inkubator pada suhu 39 0C selama 24 jam.
Asam tanin membentuk kompleks dengan zat makanan dalam media BHI
dalam bentuk gumpalan, oleh karena itu agar terjadi kontak antara mikroba
dengan tanin maka dilakukan pengocokan secara periodik dengan vorteks
selama satu menit. Pengocokan dilakukan selama masa inkubasi yaitu setiap 10
menit pada 3 jam pertama, setiap 30 menit pada 3 jam kedua, dan setiap 3 jam
pada inkubasi selanjutnya.
2. Pembiakkan Bakteri pada Media Agar
Pada akhir inkubasi masing-masing biakan diencerkan 100 kali secara serial
hingga lima kali dengan cara mengencerkan 0.05 ml biakan kedalam 5 ml
media cair BHI, selanjutnya dari campuran tersebut diencerkan kembali
sebanyak 0.05 ml ke media cair BHI, demikian seterusnya hingga lima kali
pengenceran (serial). Pada pengenceran ke-3 (106 kali), ke-4 (108 kali), dan
ke-5 (109 kali) msing-masing diambil 0.1 ml untuk dimasukkan dalam 7 ml media
biakan beragar BHI dalam keadaan cair dengan suhu 47 0C (dengan demikian
pengenceran ke-3 menjadi 107 kali, ke-4 menjadi 109 kali, dan ke-5 1011 kali),
kemudian dengan cepat tabung tersebut diputar horizontal dalam alat pemutar
(roller) sambil dialiri air dingin, sehingga media beragar dalam bentuk cair itu segera membeku membentuk lapisan agar tipis merata dinding tabung. Dengan
cara tersebut bakteri menempel dam menyebar merata dalam agar. Selanjutnya
diinkubasi dalam inkubator pada suhu 39 0C selama 2-3 hari. Bakteri yang
menempel pada agar akan tumbuh membentuk koloni. Koloni dapat dilihat
langsung dengan mata (visual), oleh karena itu koloni ini dapat diamati
bentuk, warna, dan ukurannya. Pembentukan koloni akan terlihat rapat dan
pengenceran tertinggi. Pada pengenceran padat kita akan mendapatkan
sejumlah jenis kelompok koloni, sedangkan untuk mempermudah pengambilan
koloni sebagai isolat serta mempermudah pemurniannya dapat dilakukan pada
pengenceran tinggi (kerapatan koloni yang jarang). Kelompok koloni yang
tidak terdapat pada pengenceran tinggi diambil pada pengenceran yang lebih
rendah.
Penentuan Isolat
Penggunaan level asam tanin dimaksudkan untuk memperoleh isolat bakteri
yang mampu hidup pada beberapa level konsentrasi tanin. Bakteri yang dapat
tumbuh pada level tanin tertinggi merupakan harapan sebagai isolat terbaik.
Koloni-koloni bakteri yang terbentuk pada setiap level konsentrasi tanin
dipilah-pilah sehingga didapatkan beberapa kelompok koloni. Kolompok koloni
yang tumbuh pada level tertinggi ditetapkan sebagai kelompok koloni terpilih.
Dari setiap kelompok koloni terpilih diambil satu koloni sebagai isolat. Setiap
koloni isolat diambil dengan ose untuk dibiakkan ke dalam 10 ml media cair BHI (diinkubasi pada suhu 39 0C selama 24 jam). Dengan demikian diperoleh
beberapa biakan isolat, dan biakan itu selanjutnya dilakukan pemurnian.
Pemurnian isolat
Koloni isolat-isolat yang telah dibiakkan pada 10 ml media cair BHI,
kemudian dibiakan lagi pada 7 ml media agar BHI setelah dilakukan pengenceran
(teknik pembiakan pada media agar ini sama seperti pada tahap isolasi). Koloni
yang terbentuk diamati keseragamannya. Bila koloni-koloni bakteri yang tumbuh
pada media agar BHI masih ada koloni Bakteri yang tidak sama dengan ciri fisik
koloni bakteri isolatnya, maka dilakukan pengambilan (menggunakan ose) satu
koloni bakteri yang sama dengan ciri fisik koloni bakteri isolatnya kedalam 10 ml
media cair BHI untuk dibiakkan kembali (diinkubasi 39 0C selama 24 jam).
Biakan dalam media cair ini kembali dibiakkan pada media agar untuk dilihat
keseragaman koloninya. Bilamana pengamatan belum terlihat seragam maka
kembali salah satu koloni dibiakan dalam media 10 ml media cair BHI dan
berulang-ulang hingga koloni-koloni bakteri yang tumbuh pada media agar
dinyatakan seragam. Setelah dinyatakan seragam maka satu koloni bakteri isolat
diambil dengan ose dan dibiakkan pada 10 ml media cair BHI yang mengandung
1% asam tanin (inkubasi 39 0C selama 24 jam) untuk disimpan.
Penyimpanan
Biakan isolat bekteri yang murni dalam 10 ml media cair BHI mengandung
1% asam tanat, diambil sebanyak 6 ml dicampur 2 ml larutan gliserol 80% (3:1),
dan selanjutnya campuran ini disimpan dalam freezer (suhu beku).
Karakterisasi Isolat
Karakterisasi isolat meliputi:
1. Morfologi Isolat
Pengamatan morfologi dilakukan dengan metode pewarnaan gram.
2. Aktivitas Isolat terhadap Pembeningan Tanin
Disediakan 10 ml media agar BHI mengandung 1% asam tanat dan 1% tanin
terkondensasi dalam botol kaca kapasitas 100 ml, media membeku dibagian
dasar setebar 2-3 mm. Biakan dari penyimpanan (stock) ditumbuhkan sebanyak
0.1 ml pada 10 ml media cair BHI mengandung 1% asam tanat (diinkubasi 39
0
C 24 jam). Biakan tersebut di teteskan pada bagian tengah media agar,
kemudian posisi botol segera dibalikan sehingga media agar menggantung atau
terlerak di bagian atas selanjutnya diinkubasi 39 0C sema 3-5 hari. Koloni
bakteri akan tumbuh dan bilamana terjadi aktivitas pembeningan tanin maka di
sekitar koloni bakteri terjadi area yang berwarna bening (clearing zone) yang menunjukkan bahwa isolat mempunyai aktivitas yang bereaksi atas kehadiran
tanin.
3. Aktivitas Pemanfaatan Sumber Karbon
Sumber karbon yang digunakan adalah glukosa, fruktosa, galaktosa, xylosa,
sukrosa, maltosa, selulosa, selobiosa, dan pati. Sebanyak satu takar spatula
(±0.001 gram) dimasukkan dalam 10 ml media cair non karbon. Sebanyak 0.1
ml biakan isolat dibiakkan pada media yang mengandung sumber-sumber
pada tingkat kekeruhan yang terjadi pada biakan media sumber-sumber karbon
itu dengan membandingkan dengan blangkonya (media cair non karbon tanpa
penambahan sumber karbon).
Penelitian III
Pengujian Kemampuan Isolat terhadap Pengurangan Kadar Tanin Terkondensasi dalam Media Khusus (Defined Media)
Penelitian ini bertujuan untuk menguji kemampuan isolat dalam
menurunkan kadar tanin terkondensasi dalam media biakannya, atau dengan kata
lain isolat diuji kemampuannya mendegradasi tanin terkondensasi. Media biakan
untuk pengujian ini digunakan media khusus. Media ini tidak mengandung zat-zat yang dapat bereaksi dengan tanin -seperti protein dan karbohidrat- membentuk
senyawa kompleks. Pasokan makanan untuk mikroba berupa vitamin-vitamin,
mineral-mineral, dan tanin terkondensasi.
Media khusus dikemas dalam 10 ml dengan kandungan tanin tekondensasi
1% dalam tabung Hungate.
Isolat-isolat dari penyimpanan (freezer) dibiakan sebanyak 0.1 ml dalam 10 ml media cair BHI kemudian diinkubasi 39 0C 24 jam. Selanjutnya biakan
dihitung jumlah bakteri yang hidup melalui metoda penghitungan koloni. Setelah
diketahui jumlah bakteri hasil pembiakan, maka kembali isolat dibiakan kembali
dengan cara yang sama. Isolat-isolat hasil biakan ditransfer ke media khusus
denga jumlah satuan bakteri sebanyak 107. Dengan demikian volume media
biakan berbeda untuk setiap isolat akan tetapi mempunyai jumlah satuan bakteri
yang sama, untuk tujuan tersebut maka media biakan yang jumlah bakterinya
padat diencerkan dengan media khusus.
Isolat-isolat dalam media khusus dibiakkan dalam inkubator bersuhu 39 0C.
Satu jenis isolat akan ditumbuhkan dalam 7 tabung media khusus. Tujuh tabung
1. Kadar tanin tekondensasi
Analisis tanin ini dilakukan dengan metoda Presipitasi-protein (Hagerman &
Butler, 1978).
2. Pengamatan fraksi-fraksi senyawa fenolik (komponen senyawa tanin)
Analisis menggunakan HPLC merk Waters, recorder Sic Cromatocorder, dan Kolom menggunakan Novapak TM C18. Panjang gelombang 280, flow rate 0,9 ml/menit, eluen menggunakan 40% Methanol.
Penelitian IV
Inokulasi Isolat ke dalam Ekosistem Rumen Kambing yang tidak pernah Mengkonsumsi Kaliandra terhadap Kecernaan Kaliandra in Vitro
Penelitian ini bertujuan menguji pengaruh inokulasi isolat bakteri terhadap
ternak yang tidak terbiasa mengkonsumsi pakan kaliandra –dalam hal ini
ternaknya adalah kambing berpakan 100% rumput gajah- terhadap kecernaan
kaliandra. Penelitian ini dilakukan secara in vitro.
Isolat diinokulasikan pada tabung fermentor yang berisi 30 ml larutan
McDougall-Cairan rumen kambing berpakan tumput gajah (4:1), dan 0.5 g tepung
kaliandra sebagai sumber karbon. Dosis isolat yang diinokulasikan adalah 108
cfu/ml media fermentor.
Isolat dari penyimpanan (stock) dibiakkan sebanyak 0.1 ml dalam 10 ml media cair BHI, diinkubasikan 39 0C 24 jam. Kemudian pertumbuhan jumlah
bakteri diamati dengan metode pencacahan koloni dalam media agar BHI. Jumlah
koloni yang tumbuh mencerminkan jumlah bekteri yang dapat tumbuh selama 24
jam pada biakan media cair BHI, sehingga dapat ditentukan berapa ml harus
diambil dari media biakan tersebut untuk setiap satu tabung fermentor.
Dari isolasi diperoleh empat isolat dengan notasi isolat IK1, IK2, IK3, dan
IK4. Isolat IK1 tidak dapat hidup kembali setelah dilakukan penyimpanan dengan
suhu beku dalam media penyimpanan gliserol (gliserol stock), sehingga hanya ada tiga isolat saja yaitu isolat IK2, IK3, dan IK4.
1. Pengaruh inokulasi masing-masing bakteri terhadap kecernaan kaliandra,
dengan notasi perlakuan sebagi berikut.
IIK2 = Inokulasi isolat bakteri rumen II asal kambing Kaligesing
IIK3 = Inokulasi isolat bakteri rumen III asal kambing Kaligesing
IIK4 = Inokulasi isolat bakteri rumen IV asal kambing Kaligesing
Peubah yang diamati adalah kecernaan bahan kering dan organik pada Stage 1.
Percobaan ini bertujuan memilih isolat terbaik dari ketiga isolat, dengan
demikian diperoleh satu isolat unggulan.
2. Berdasarkan pertimbangan atas hasil perlakuan inokulasi di atas, serta
didukung kinerjanya berdasarkan pengujian sebelumnya, maka isolat IK4
ditetapkan sebagai isolat terbaik. Isolat IK4 ini kemudian diperbandingkan lagi
dengan beberapa perlakuan lain untuk melihat gambaran potensi atau
kemampuannya secara lebih jauh dan mendalam.
Semua perlakuan menggunakan inokulum cairan rumen yang berasal dari
kambing berpakan rumput gajah, kecuali perlakuan K. Perlakuan K menggunakan
cairan rumen kambing Kaligesing. Perlakuan K dimaksudkan untuk melihat
sejauh mana tingkat keberhasilan inokulasi dibanding keadaan asalnya sebagai
kontrol positif.
Peubah kecernaan bahan kering dan bahan organik diamati pada stage 1 dan
2. Peubah pH dan NH3 diamati pada stage 1 dengan waktu inkubasi 0, 3, dan 6
jam.
Analisis Statistik
Penelitian ini ddidesain dengan rancangan acak kelompok (RAK) dengan
waktu pengambilan cairan rumen merupakan kelompok. Perlakuan diulang tiga
kali. Data yang diperoleh dianalisis statistik menggunakan analisis ragam.
Perbedaan antar perlakuan diuji dengan Uji Jarak Berganda Duncan (Steel &
Prosedur Analisis Sampel Penelitian
1. Analisis Total Tanin dengan Metode Presipitasi Protein
a. Pembuatan Pereaksi
- Larutan Buffer Asetat pH 5
Menimbang 27.2 g CH3COONa·3H2O, dicampurkan dengan 9.945 g
NaCl, lalu dilarutkan dengan air suling sampai volumenya 700 ml.
Selanjutnya diukur sampai pH 5 dengan ditambahkan asam asetat 0.2 M
(11.4 ml asam asetat galcial/liter air) sedikit demi sedikit sampai
akhirnya menjadi 1 liter larutan.
- Larutan SDS-TEA
Larutan natriumdodedihidrogen sulfat 1% dan trietanolamin 5% dibuat
dalam air suling. Kemudian masing-masing dicampurkan dengan
perbandingan 1:1
- Larutan FeCl3 0.01 M dalam asam korida 0.01 N
Ferriklorida ditimbang sebanyak 0.4055 g lalu dilarutkan HCl 0.01 N
sampai volumenya menjadi 250 ml.
- Larutan Standar Bovine Serum Albumin (BSA)
Ditimbang sebanyak 100 mg BSA lalu dilarutkan dengan larutan buffer
asetat pH 5, sampai volumenya menjadi 50 ml di dalam labu ukur.
Larutan standar BSA ini berkonsentrasi 2 mg/ml.
b. Prosedur Analisis
Sebanyak 1 ml sampel dimasukkan kedalam tabung reaksi, lalu
ditambahkan 9.l methanol 50% dan diaduk dengan vorteks. Larutannya lalu dipipiet sebanyak 1 ml kedalam tabung reaksi yang lain dan
ditambahkam 1 ml BSA. Setelah itu dibiarkan selama 20 menit di ruang
pendingin (bertemperatur 5 0C), kemudian dipusingkan selama 15 menit
dengan 3000 rpm. Cairannya dibuang dan endapannya dicuci
menggunakan larutan buffer asetat pH 5 sebanyak 3 kali dengan
meneteskan secara perlahan melalui dinding tabung reaksi. Endapan
dilarutkan dengan 4 ml SDS-TEA dan ditambah 1 ml larutan FeCl3 dalam
pada temperatur kamar. Serapannya diukur pada panjang gelombang 510
m.
Larutan standar dibuat dengan melarutkan 50 mg asam tanat dengan
Metanol absolut (konsentrasi 1 mg/ml). dibuat deret standar dengan cara
memipet larutan induk di atas sebanyak 0, 1, 2, 3, 4, dan, 5 kemudian
dijadikan 10 ml. larutan standar tersebut mempunyai konsentrasi 0; 0,1;
0,2; 0,3; 0,4; dan0,5 mg/ml. kemudian dipipet sebanyak 1 ml ke dalam
tabung reaksi dan ditambahkan 1 ml larutan standar BSA berkonsentrasi 2
mg/ml, selanjutnya dilakukan cara kerja seperti pada sampel. Warna
larutan yang diperoleh adalah ungu kehitaman.
c. Perhitungan
% Tanin = Faktor pengenceran X mg/ml sampel X 100%
2. Analisis Konsentrasi N-Amonia
Sampel yang berupa cairan rumen atau cairan yang diambil dari tabung
fermentor pasca inkubasi dipusingkan dengan 5000 rpm pada suhu 5 0C
selama 15 menit. Supernatan diambil untuk dianalisis.
Konsentrasi N-Amonia dalam cairan rumen ditentukan dengan metode
mikridifusi Conway. Sebanyak 1 ml supernatan cairan rumen diletakan dalam
salah satu sisi sekat cawan Conway dan pada sisi lainnya diletakan 1 ml
larutan NaOH jenuh. Posisi cawan Conway diletakkan sedemikian rupa
sehingga keduanya tidak tercampur sebelum cawan ditutup rapat. Pada bagian
tengah diletakan 1 ml larutan asam borat berindikator methylene blue
(indikasi warna biru). Cawan lalu ditutup rapat dengan bantuan vaselin.
Supernatan dan larutan NaOH jenuh dicampur rata dengan menggoyang
cawan. Amonia yang dibebaskan dari reaksi akan ditangkap oleh asam borat,
menjadi amonium borat. Perubahan dari asam borat menjadi amonium borat,
terindikasi dengan terjadinya perubahan warna dari biru menjadi merah.
Setelah 24 jam, amonium borat dititrasi dengan H2SO4 0.005 N sampai terjadi
perubahan warna ke warna asalnya (biru). Kadar amonia dihitung dengan
N-Amonia (mM) = jumlah ml H2SO4 X Nilai NH2SO4 X 1000
3. Prosedur Pencacahan Populasi Bakteri
Populasi bakteri rumen dihitung dengan menggunakan metode
pencacahan koloni dimana yang diperhitungkan hanya bakteri hidup. Prinsip
penghitungannya adalah cairan rumen diencerkan secara serial lalu dibiakan
dalam media agar BHI dalam tabung Hungate.
Untuk keperluan pembiakan, diperlukan media tumbuh yang spesifik
untuk semua jenis bakteri yang akan dibiakkan. Media tersebut terlebih
dahulu disiapkan dengan prosedur sebagai berikut.
Bahan-bahan media dicampur dan dimasukkan ke dalam botol yang
telah disterilkan dengan autoclave. Campuran tersebut dipanaskan perlahan-lahan sambil dialiri gas CO2 sampai terjadi perubahan warna coklat menjadi
merah pada suhu 121 0C selama 15 menit dengan tekanan 1.2 kgf/cm2.
Setelah siap digunakan untuk pembiakkan bakteri, media agar dimasukkan
kedalam penangas air pada suhu 47 0C, yaitu suhu dimana agar belum
memadat dan untuk waktu yang singkat tidak mematikan bakteri. Untuk
setiap sampel cairan rumen dibutuhkan tiga tabung Hungate yang berisi media di atas.
Sampel yang berupa media kultur atau cairan rumen diencerkan terlebih
dahulu dengan media pengenceran (Ogimoto & Imai, 1981). Pengenceran
dilakukan sebagai berikut: 0.1 ml sampel dimasukkan kedalam 9.9 ml media
pengenceran, selanjutnya dari tabung tersebut diambil 0.1 ml lagi dan
dimasukkan kedalam 9.9 ml media pengenceran yang lain. Demikian
seterusnya dilakukan hingga lima kali (lima seri tabung). Salanjutnya dari
masing masing seri tabung pengenceran diambil sibanyak 0.1 ml untuk
dimasukkan ke dalam media agar yang disimpan pada bak pemanas bersuhu
47 0C. Segera setelah dimasukkan tabung segera di putar dengan alat pemutar
(roller) pada posisi horizontal dengan dialiri air dingin supaya media agar cepat memadat dan membentuk lapisan tipis merata di dinding tabung bagian
selang waktu itu di lapisan tipis agar itu terbentuk koloni-koloni bakteri yang
tumbuh.
Apabila tabung seri yang kelima terdapat n koloni, maka jumlah bakteri
sampel yang diamati adalah = n/0.1 × 1010 bakteri/ml.
Komposisi dan Prosedur Pembuatan Media
1. Media Khusus(Defined Media)
Larutan mineral I a)
Larutan mineral II b)
Henin + 1,4 napthaquinone c)
Trace elemen d)
Sodium karbonat 5%
Resazurine 0,1%
Amonium klorida
Asam kasamino
larutan VFA e)
Larutan Vitamin f)
6.0 ml
Semua bahan (kecuali sodium karbonat dan larutan vitamin) dicampur dalam
labu erlenmeyer dan ditambahkan air destilata sampai menjadi 91 ml. pH
ditepatkan pada nilai 7.75 dengan menambahkan KOH 10 nM, lalu
ditambahkan 5% sodium karbonat, dan terakhir ditambahkan larutan vitamin.
a) Larutan mineral I:
Na2SO4
c) Hemin + 1,4-naphthaquinone:
50 g hemin ditambah 10 mg 1,4-napthaquinone dilarutkan dalam 1 ml
NaOH 1 N, lalu ditambahkan air desilata sampai mencapai volume 100 ml.
d) Trace elemen:
f) Larutan vitamin
Biotin
Asam folat
Asam para aminobensoat
Pyrydoxamine
c. Larutan mineral makro
Na2HPO4
e. Larutan pereduksi
f. Pembuatan:
400 ml aquades, 200 ml buffer rumen, 200 ml larutan makro, 0.1 ml
larutan mikro, 1 ml resazurin, dan 40 ml larutan pereduksi dicampurkan.
Jumlah komposisi ini untuk mendapatkan larutan Mc Dougall sebanyak
841.1 ml. Campuran ini kemudian dialiri gas CO2 secara terus menerus
hingga warna asal campuran yang berwarna merah akan berubah menhadi
tidak berwarna (bening).
4. Media Pengenceran
Larutan mineral I a)
Larutan mineral II b)
Cystein-HCl·H2O
Na2CO3
Resazurin 0.1%
Aquades
7.5 ml
7.5 ml
0.05 g
0.3 g
0.1 ml
100 ml
a) Larutan mineral I
K2HPO4
Aquades
0.6 ml
100 ml
b) Larutan mineral II
NaCl
(NH4)2SO4
KH2PO4
CaCl2
MgSO4·7H2O
Aquades
1.2 g
1.2 g
0.6 g
0.12 g
0.25 g
HASIL DAN PEMBAHASAN
Penelitian I
Pengujian Mikroba Rumen Kambing PEK terhadap Kecernaan Kaliandra in Vitro
Pengujian mengenai kemampuan mikroorganisme rumen kambing PEK
dalam memanfaatkan pakan kaliandra, yang didekati dengan pengamatan skala
laboratorium melalui percobaan in vitro, memperoleh hasil yang diperlihatkan pada tabel berikut .
Tabel 4. Nilai rataan kecernaan zat makanan kaliandra (%) in vitro dari perlakuan sumber cairan rumen sebagai sumber inokulum mikroba
Per la ku an
Kecernaan Zat Makanan
Bahan Kering Bahan Organik Protein NDF ADF
Stage 1 Stage 2 Stage 1 Stage 2 Stage 1 Stage 2 Stage 1 Stage 1
Kp 38.84a 49.06a 34.27a 43.65b 73.69a 80.48a 65.09a 5966a
Ko 31.99b 43.08abc 30.64ab 36.58ab 41.26b 60.10b 61.68ab 58.19a
Ap 27.54bc 43.47ab 26.77bc 38.22ab 72.66a 75.86a 60.41ab 54.81ab
Ao 23.84bc 34.13bc 22.85c 29.17b 28.35bc 57.85bc 58.18abc 52.92ab
Rp 29.44bc 41.82abc 29.62b 43.47a 63.02a 73.78a 55.93bc 49.98b
Ro 22.98c 29.63c 23.22c 36.00ab 23.85c 52.80c 52.53c 42.88c
Keterangan : Huruf yang sama kearah kolom menunjukan tidak berbeda nyata (P>0.01) menurut Uji Jarak Berganda Duncan. Kp: Cairan rumen kambing PEK dengan pemberian poly ethilene glicol (PEG). Ko: Cairan rumen kambing PEK tanpa pemberian PEG. Ap : Cairan rumen asal kambing yg diadaptasikan pakan kaliandra dengan pemberian PEG. Ao : Cairan rumen asal kambing yg diadaptasikan pakan kaliandra tanpa pemberian PEG. Rp : Cairan rumen asal kambing berpakan rumput gajah dengan pemberian PEG. Ro : Cairan rumen asal kambing berpakan rumput gajah dengan tanpa pemberian PEG.
Dari hasil analisis ragam menunjukkan bahwa tidak terdapat interaksi antara
sumber cairan rumen dan penambahan PEG. Hal ini menunjukkan bahwa tidak
pembahasan difokuskan pada perbedaan di antara sumber cairan rumen tanpa
PEG (Ko, Ao, dan Ro) dan pengaruh penambahan PEG dari setiap sumber cairan
rumen terhadap kecernaan.
Kecernaan Bahan Kering dan Bahan Organik
Kecernaan bahan kering pada stage 1 perlakuan Ko tidak nyata (P>0.01)
lebih tinggi dari Ao, akan tetapi nyata (P<0.01) lebih tinggi dari Ro. Selanjutnya
Ao tidak nyata (P>0.01) lebih tinggi daripada Ro. Sedangkan perbedaan
kecernaan bahan kering pada stage 2, diantara perlakuan Ko, Ao, dan Ro tidak
menunjukan perbedaan hasil yang nyata (P>0.01).
Kecernaan bahan organik pada stage 1 perlakuan Ko nyata (P<0.01) lebih
tinggi dari Ao dan Ro, sedangkan Ao tidak nyata (P>0.01) lebih tinggi daripada
Ro. Perbedaan kecernaan bahan organik pada stage 2, diantara perlakuan Ko, Ao,
dan Ro tidak menunjukan perbedaan hasil nyata (P>0.01).
Peningkatan kecernaan bahan kering dan bahan organik pada stage 1 dari
ketiga sumber cairan rumen ini terjadi secara bertahap (gradual) dari Ro ke Ao
hingga ke Ko. Data-data ini mencerminkan bahwa pemanfaatan bahan kering
kaliandra oleh mikroba rumen kambing asal Kaligesing lebih baik (lebih tinggi)
daripada kambing-kambing yang tidak biasa mengkonsumsi kaliandra. Sedang
pengadaptasian dalam waktu yang tertentu (lebi dari 6 bulan) dapat meningkatkan
pemanfaatan zat makanan kaliandra namun belum memperlihatkan hasil
memuaskan (signifikan). Kecernaan bahan organik pada stage 1 pada perlakuan
Ko memberikan hasil lebih baik dari bahan keringnya (Kecernaan bahan organik
Ko nyata (P<0.01) lebih tinggi dari Ao, sedangkan kecernaan bahan keringnya
tidak nyata (P>0.01), ini memberikan gambaran bahwa fraksi-fraksi utama zat
makanan kaliandra lebih banyak dimanfaatkan oleh mikroba rumen kambing asal
Kaligesing ini dan sedikit memanfaatkan fraksi mineral.
Percobaan in Vitro ini merupakan miniatur proses pencernaan ruminansia, dan pada stage 1 merupakan miniatur proses fermentatif rumen. Dalam proses
fermentatif zat makanan (substrat) dicerna oleh enzim-enzim mikroba, kecuali
proses ini adalah hasil kerja mikroba. Aktivitas kerja mikroba terhadap substrat
dalam rumen sangat berpengaruh terhadap nilai kecernaan substrat, oleh karena
itu perbedaan kecernaan bahan kering dan bahan organik dari sumber cairan
rumen itu adalah cerminan perbedaan kemampuan mikroba dalam mencerna
substrat kaliandra. Adaptasi yang lama dalam mengkonsumsi kaliandra dalam
proporsi pemberian besar dan berlangsung dari generasi ke generasi seperti
kambing asal Kaligesing ini, merupakan faktor penyebab efisiensinya mikroba
dalam mencerna substrat kaliandra. Selain itu mikroba semakin tahan terhadap
kehadiran tanin, bahkan bukan suatu yang mustahil akan terdapat mikroba spesifik
(tertentu) yang mampu melepaskan ikatan kompleks-tanin dari zat makanannya,
sehingga zat makanan tersebut dapat didegradasi menjadi metabolit yang dapat
dimanfaatkan untuk kebutuhan mikroba dan induk semangnya, atau bahkan
mampu memanfaatkan fraksi tanin.
Peningkatan kecernaan mengindikasikan peningkatan terbentuknya
metabolit-metabolit produk akhir dan intermedier. Metabolit-metabolit tersebut
dimanfaatkan untuk kebutuhan mikroba dan induk semangnya. Pemanfaatkan
metabolit oleh mikroba selain untuk keperluan hidupnya juga dipergunakan untuk
meningkatkan populasinya. Mikroba adalah sumber protein induk semangnya
yang diserap di saluran pencernaan pasca rumen.
Kecernaan bahan kering dan bahan organik pada stage 2 secara kuantitatif
meningkat bertahap dari Ro ke Ao lalu ke Ko, namun peningkatan itu tidak
memberikan hasil signifikan ( P>0.01). Pada stage ini ternyata fraksi zat makanan
yang terikat tanin pada Ao dan Ro dapat terhidrolis pada pencernaan pasca rumen
sehingga kecernaan meningkat secara nyata. Hal ini di perkirakan karena tanin
mempunyai sifat dapat terhidrolis pada pH lebih dari 8 dan kurang dari 3
(Leinmuller et al. 1991), sedangkan pada abomasum pH berkisar pada nilai 2.
Pada stage 2 percobaan in vitro ini menyebabkan pH rendah adalah HCl 6 N. Walaupun kecernaan bahan kering dan bahan organik kaliandra tidak nyata
(P>0.01) pada stage 2 dari setiap sumber cairan rumen (Ko, Ao dan Ro), namun
hasil Ko yang lebih tinggi (P<0.01) dari Ro pada stage 1 akan memberikan