PENENTUAN KADAR LOGAM KADMIUM ( Cd ) DAN LOGAM
ZINKUM ( Zn ) DALAM BLACK LIQUOR PADA INDUSTRI
PULP PROSES KRAFT DARI TOBA PULP LESTARI
DENGAN METODE SPEKTROFOTOMETRI
SERAPAN ATOM ( SSA)
SKRIPSI
OLEH:
E L I S A
030802021
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENENTUAN KADAR LOGAM KADMIUM ( Cd ) DAN LOGAM ZINKUM ( Zn ) DALAM BLACK LIQUOR PADA INDUSTRI PULP PROSES
KRAFT DARI TOBA PULP LESTARI DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM ( SSA)
SKRIPSI
Diajukan Sebagai Salah Satu Syarat Mencapai Gelar Sarjana Sains Bidang Ilmu Kimia
OLEH :
E L I S A 030802021
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENENTUAN KADAR LOGAM KADMIUM
( Cd ) DAN LOGAM ZINKUM ( Zn ) DALAM BLACK LIQUOR PADA INDUSTRI PULP PROSES KRAFT DARI TOBA PULP LESTARI DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM ( SSA)
Kategori : SKRIPSI
Nama : E L I S A
Nomor Induk Mahasiswa : 030802021
Program studi : SARJANA (S-I ) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM ( FMIPA ) UNIVERSITAS SUMATERA UTARA
Disetujui di : Medan, September 2007 Komisi Pembimbing I :
Pembimbing 2 Pembimbing I
Drs. Chairuddin M.Sc. Prof.DR. Harlem Marpaung
NIP. 131 653 992 NIP. 130 422 456
Diketahui/Disetujui Oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENENTUAN KADAR LOGAM KADMIUM ( Cd ) DAN LOGAM ZINKUM
( Zn ) DALAM BLACK LIQUOR PADA INDUSTRI PULP PROSES
KRAFT DARI TOBA PULP LESTARI DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM ( SSA)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing- masing disebutkan sumbernya.
Medan, September 2007
E L I S A
PENGHARGAAN
Puji dan syukur penulis ucapkan kepada ALLAH SWT Yang Maha pemurah dan Maha Penyayanng, dengan Limpahan hidayah dan karunia-Nya skripsi ini berhasil diselesaikan dengan sebaik – baiknya dan dalam waktu yang telah ditetapkan.
Penulis mempersembahkan skripsi ini pada kedua orang tua tercinta, Ayahanda Ulil Amri Lbs. Dan Ibunda Samriana, terimakasih untuk semua dukungan moril, materil, kasih sayang, perhatian dan do’a yang selalu diucapkan untuk penulis.Terimaksih kepada temanku Elriska Lbs, yang telah memberikan dukungan sepenuhnya serta do’a dan kasih sayang yang tulus untuk penulis,dan kedua kakakku Yenni Warti dan Leni Wati yang selalu memberi dukungan dan semangat untuk penulis.
Ucapan terima kasih penulis sampaikan kepada :
1) Prof. DR. Harlem Marpaung dan Drs. Chairuddin M.Sc selaku pembimbing pada penyelesaian skripsi ini yang telah memberikan panduan, bimbingan dan dukungan penuh kepercayan kepada saya untuk menyempurnakan kajian ini. 2) Ketua dan sekretaris Departemen Kimia DR. Rumondang Bulan ,MS, dan
Drs. Firman sebayang, MS, yang telah membantu mensahkan skripsi ini 3) Ibu DR. Rumondang Bulan, MS selaku Dosen wali, dan Bapak Prof. DR.
Harlem Marpaung selaku kepala Laboratorium Kimia Analitik, serta seluruh staf pengajar dan pegawai Departemen Kimia FMIPA USU.
4) Sahabat- sahabatku Nurhidayah, Umri, Zurahmi, Nurul, Siska, Puput, Intan, dan rekan- rekan angkatan 2003, 2002 dan 2004 yang memberi dukungan, semangat serta do’a kepada penulis. Tidak lupa pula kepada rekan- rekan Asisten Analitik Bang Lambok,Bang Permanton, Bang Willi, Devi, Butet, Jetty dan bang Budiyanto
5) Bang Humala dan Buk Regar teman sepenelitian saya , yang telah banyak mmembantu saya dalam menyelesaikan penenlitian ini
6) Kak seri Mawarni ,Kak Via dan kak Vika
Untuk semua, Penulis berdo’a kepa ALLAH SWT membalas kebaikan yang telah diberikan kepada penulis.
Penulis menyadari sepenuhnya bahwa skripsi ini masih jauh dari sempurna.Oleh Karena itu , Penulis mengharapkan saran dan masukan untuk kesempurnaan skripsi ini.Akhir kata semoga skripsi ini berguna dan bermamfaat bagi kita semua
Medan, September 2007 Penulis,
ABSTRAK
Telah dilakukan penelitian untuk menganalisis kadmium ( Cd ) dan Zinkum ( Zn )
dalam Black liquor, pada proses pulp kraf Toba Pulp Lestari (TPL). Sampel diambil
dari tanki strong Black liquor secara purposif. Liquor didestruksi menggunakan asam
nitrat dan dianalisis dengan metode Spektrofotometri Serapan Atom (SSA) pada
panjang gelombang 228.80 nm untuk Cd dan 213.90 nm untuk Zn. Dari hasil
penelitian Diperoleh kadar kadmium (Cd) dan Zinkum (Zn) berturut- turut 3.5 mg/L
ABSTRACT
THE ANALYSIS OF CADMIUM METAL ( Cd ) AND ZINCUM METAL ( Zn ) IN
BLACK LIQUOR IN INDUSTRY KRAFT PROCESS PULP FROM TOBA PULP
LESTARI BY ATOMIC ABSORPTION SPECTROFOTOMETRY (AAS )
METHOD
The analysis of Cadmium ( Cd ) and Zinkum ( Zn ) in Black liquor of pulp kraft proces
Toba Pulp Lestari ( TPL ) Has been carried out. The sample was taken from tank
strong Black Liquor in a purposif. Nitrace acid was used in the destruction of the
liquor and then analysed with Atomic Absorption Spectrofometry method (SSA) at
228,80 nm wavelength of Cadmium and 213,90 nm wavelength of Zincum. From the
researce it was found that the concent of Cadmium ( Cd ) and Zincum ( Zn ) were 3.5
mg/L and 11.6 mg/L in sample respectively
DAFTAR ISI
JUDUL Halaman
PERSETUJUAN ii
PERNYATAAN iii
PENGHARGAAN iv
ABSTRAK v
ABSTRACT vi
DAFTAR ISI vii
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
BAB I. PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Permasalahan 4
1.3 Pembatasan Masalah 4
1.4 Tujuan Penelitian 4
1.5 Mamfaat Penelitian 5
1.6 Metode Penelitian 5
1.7 Lokasi Penelitian 5
BAB II. TINJAUAN PUSTAKA 6
2.1 Komposisi Kimia Kayu 6
2.1.1 Hara Essensial Tanaman 6
2.1.2 Komposisi unsur Dalam Tanah & Tanaman 7
2.2 Proses Pembuatan Pulp 8
2.3 Black Liquor 9
2.3.1 Evaporasi Black Liquor 10
2.3.2 Sistem Pembakaran Black Liquor Pada Furnace 10 2.3.3 Sistem Pemasukan Udara Kedalam Ruang Bakar 10
2.3.4 Komposisi Black Liquor 11
2.3.5 Komposisi Senyawa Kimia Anorganik Dalam Black Liquor 11
2.4 Logam 13
2.4.1 Kadmium 13
2.4.2 Zinkum 15
2.5 Spektrofotometer Serapan Atom 16
2.5.1 Prinsip Dasar Analisa Spektrofotomet Serapan Atom 16
2.5.2 Intrumentasi 17
2.5.2.1 Sumber Sinar 17
2.5.2.2 Lampu Katoda Berongga 17
2.5.2.3 Nyala 17
2.5.2.4 Monokromator 18
2.5.2.6 Sistem Pencatat 19
2.6 Metode Destruksi 19
BAB III. METODOLOGI PENELITIAN 21
3.1 Bahan-bahan 21
3.2 Alat-alat 21
3.3 Prosedur Kerja 22 3.3.1 Preparasi Sampel 22 3.3.2 Pembuatan Larutan Standar Logam kadmium 22 3.3.3 Pembuatan Variasi Larutan Standar kadmium 22 3.3.4 Pembuatan Larutan Standar Logam Zinkum 22 3.3.5 Pembuatan Variasi Larutan Standar Zinkum 23 3.3.6 Penentuan Konsentrasi Cd dan Zn dalam Sampel Dengan 23 Spektrofotometer Serapan Atom
3.4 Bagan Penelitian 24
BAB IV. HASIL DAN PEMBAHASAN 25 4.1 Hasil Penelitian Dan Pengolahan Data 25 4.1.1 Data Hasil Pengukuran Logam Kadmium 25 4.1.2 Pengolahan Data Logam Kadmium 26 4.1.2.1 Penentuan Kurva Kalibrasi Dengan Analisis Regresi 26 4.1.2.2 Penurunan Persamaan Garis Regresi 26 4.1.2.3 Perhitungan Logam Kadmium 27 4.1.2.4 Koefisien Kor lasi 27 4.1.3 Data Hasil Pengukuran Logam Zinkum 28 4.1 4 Pengolahan data Logam Zinkum 28 4.1.4.1 Penentuan Kurva Kalibrasi Dengan Analisis Regresi 28 4.1.4.2 Penurunan Persamaan Garis Regresi 29 4.1.4.3 Perhitungan Logam Zinkum 30 4.1.4.4 Koefisien Kor lasi 30
4.2 Pembahasan 31
BAB V. KESIMPULAN DAN SARAN 34
5.1 Kesimpulan 34
5.2 Saran 34
DAFTAR TABEL
Halaman
Tabel 2.1 Komposisi Kimia Antara Hard Woods dan Soft Woods 6 Tabel 2.2 Jenis dan Bentuk Hara Yang di Serap Tanaman Dari Tanah 7 Tabel 2.3 Komposisi Kimia Black Liquor 9 Tabel 2.4 Komposisi White Liquor 9 Tabel 2.5 Komponen Black Liquor 12 Tabel 2.6 Kandungan Anorganik Dalam Black Liquor 12 Tabel 3.1 Kondisi Parameter Spektrofometer Serapan Atom 23 Tabel 4.1 Data Hasil Pengukuran Absorbansi Larutan Standar Ion Logam 25
Kadmium
Tabel 4.2 Data Hasil Pengukuran Absorbansi Logam Cd Pada Black Liquor 25 Tabel 4.3 Data Hasil Penurunan Persamaan Garis Regresi Untuk Unsur Cd 26 Tabel 4.4 Data Hasil Pengukuran Absorbansi Larutan Standar Ion Logam 28
Zinkum
Tabel 4.5 Data Hasil Pengukuran Absorbansi Logam Zn Pada Black Liquor 28 Tabel 4.6 Data Hasil Penurunan Persamaan Garis Regresi Untuk Unsur Zn 28
DAFTAR GAMBAR
Halaman
Gambar 1 Skema Proses Pembuatan Pulp 3 Gambar 2 Skema Peralatan Ringkas Spektrofotometer Serapan 17
DAFTAR LAMPIRAN
Halaman Gambar 1 Kurva Kalibrasi Larutan Standar Kadmium 37 Gambar 2 Kurva Kalibrasi Larutan Standar Zinkum 38 Tabel 1 Standar Kualitas Air Limbah 39 Tabel 2 Standar Kualitas Air Untuk Pertanian dan Perindustrian 40 Tabel 3 Standar Kualitas Air Untuk Peternakan dan Perikanan 41 Tabel 4 Data Hasil Analisis TPL yang Dilakukan Oleh econotech Secara 42
ABSTRAK
Telah dilakukan penelitian untuk menganalisis kadmium ( Cd ) dan Zinkum ( Zn )
dalam Black liquor, pada proses pulp kraf Toba Pulp Lestari (TPL). Sampel diambil
dari tanki strong Black liquor secara purposif. Liquor didestruksi menggunakan asam
nitrat dan dianalisis dengan metode Spektrofotometri Serapan Atom (SSA) pada
panjang gelombang 228.80 nm untuk Cd dan 213.90 nm untuk Zn. Dari hasil
penelitian Diperoleh kadar kadmium (Cd) dan Zinkum (Zn) berturut- turut 3.5 mg/L
ABSTRACT
THE ANALYSIS OF CADMIUM METAL ( Cd ) AND ZINCUM METAL ( Zn ) IN
BLACK LIQUOR IN INDUSTRY KRAFT PROCESS PULP FROM TOBA PULP
LESTARI BY ATOMIC ABSORPTION SPECTROFOTOMETRY (AAS )
METHOD
The analysis of Cadmium ( Cd ) and Zinkum ( Zn ) in Black liquor of pulp kraft proces
Toba Pulp Lestari ( TPL ) Has been carried out. The sample was taken from tank
strong Black Liquor in a purposif. Nitrace acid was used in the destruction of the
liquor and then analysed with Atomic Absorption Spectrofometry method (SSA) at
228,80 nm wavelength of Cadmium and 213,90 nm wavelength of Zincum. From the
researce it was found that the concent of Cadmium ( Cd ) and Zincum ( Zn ) were 3.5
mg/L and 11.6 mg/L in sample respectively
BAB I PENDAHULUAN
1.1. Latar Belakang
Industri kertas merupakan salah satu industri yang terbesar di Dunia dengan
menghabiskan 670 juta ton kayu. Kebutuhan kertas dunia terus meningkat, yang pada
beberapa tahun kedepan diperkirakan pertambahannya mencapai 2% sampai 3%
pertahun akibatnya kebutuhan kayu gelondongan setiap tahunnya akan meningkat
(Durbak, 1993).
Pulp adalah produk utama kayu, terutama digunakan untuk pembuatan kertas,
tetapi juga diproses menjadi turunan selulosa, seperti sutera rayon dan selofan. Tujuan
utama pembuatan pulp kayu adalah umtuk melepaskan serat- serat. Dapat dikerjakan
secara kimia atau secara mekanik, atau penggabungan ke-2 metode ini. Pembuatan
pulp secara kimia adalah proses penghilangan lignin, sehinga serat - serat kayu mudah
dilepaskan pada pembongkaran dari bejana pemasak ( digester ). Hampir semua
produksi pulp kimia di Dunia saat ini masih didasarkan pada proses - prose sulfit dan
sulfat ( kraft )
Dalam proses pulp kraft sistem pemasak alkali bertekanan pada suhu tinggi
dikenal pada tahun 1850-an. Menurut metode yang diusulkan oleh C.watt dan
H.Burgess, Larutan natrium hidroksida ( NaOH ) digunakan sebagai lindi pemasak,
dan lindi bekas yang dihasilkan dipekatkan dengan cara penguapan dan pembakaran.
Leburan yang terdiri atas natrium karbonat diubah kembali menjadi natrium
hidroksida ( NaOH ).
Proses kraft telah hampir menggantikan secara lengkap proses soda yang tua
karena keungulan selektifitas delignifikasi dan kualitas pulp yang dihasilakan tinggi.
pulp sulfit karena beberapa faktor, seperti pemilihan bahan kimia yang lebih
sederhana,lebih ekonomis, dan sifat pulp yang dihasilkan lebih baik.
Meskipun saat ini lebih dari 80% pulp kimi yang dihasilkan di Dunia adalah
pulp kraft, proses ini masih mempunyai beberapa sisi kelemahan yang sukar diatasi,
yaitu gas-gas yang berbau tidak enak, kebutuhan bahan kimia pengelantang yang
tinggi pada pulp kimia kayu lunak. Namun menurut perkembangan terakhir dapat
diharapkan bahwa modifikasi - modifikasi baru dapat mengatasi hal tersebut. (Eero. S,
1995 )
Black Liquor adalah suatu cairan yang mengandung padatan 70%-72% yang
didaur ulang dari digester pada proses pembuatan kertas. Black Liquor warnanya
hitam dikarenakan reaksi kimia yang terjadi antara serpihan kayu, dengan
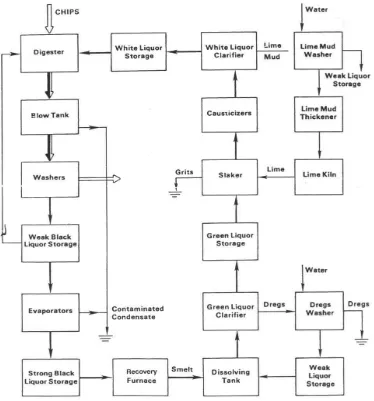
bahan-bahan kimia yang digunakan untuk pemasakan dalam liquor (TPL, 2002). Gambar 1
memperlihatkan skematik proses pembuatan pulp.
Didalam tanah terkandung unsur hara makro seperti (N, P, K, Ca, Mg)
dan unsur hara mikro seperti (Mn, Fe, Zn, Cu, Cd). Tanaman dapat menyerap
unsur hara ini dalam jumlah yang berbeda karena keberadaan unsur-unsur ini juga
beragam didalam tanah oleh karena itu tanaman sangat membutuhkan unsur-unsur
hara tersebut yang menjadi sumber logam yang terdapat didalam tanaman
Gambar 1. Skematik Proses Pembuatan Pulp
Komposisi bahan kimia yang terkandung dalam Black Liquor adalah NaOH,
Na2S, Na2CO3, Na2SO3, Na2SO4, dan Na2S2O3 (Thomas M, 1989) dan juga masih
mengandung bahan total belerang tereduksi (TRS) yang tidak menguap. Berdasarkan
hasil penelitian yang dilakukan Econotech bahwa didalam Black Liquor terdapat
logam-logam yang diantaranya merupakan logam berbahaya antara lain : Timbal,
Besi, Mangan, Nikel, Zink, Cadmium, Chromium, Cobalt, Tembaga dan Arsen.
Keberadaan logam-logam tersebut jika melewati ambang batas maka dapat mencemari
lingkungan. Black Liquor sangat berperan penting dalam industri pulp, karena dapat
sulfat (Na2SO4) agar kekurangan SO42- pada digester dapat dipenuhi pada green liquor
mengalami proses caustisasi menjadi lindi putih (TPL, 2002).
Pada formasi aerosol hasil akhir pembakaran Black Liquor menghasilkan bau
yang tidak sedap. Pada proses pembakaran tidak sempurna Black Liquor juga akan
dihasilkan limbah padat yang masih mengandung logam-logam berat yang sangat
membahayakan lingkungan. Oleh karena hal tersebut diatas maka peneliti tertarik
untuk meneliti tentang logam-logam berat terdapat dalam Black Liquor.
1.2. Permasalahan
Dreg yang merupakan limbah padat dari Black Liquor akan mencemari
lingkungan jika kadar logamnya tinggi. Oleh karena itu perlu dianalisis kadar logam
yang terdapat didalam Black Liquor yang menjadi sumber logam didalam dreg
(limbah padat).
1.3. Pembatasan Masalah
Penelitian ini dibatasi hanya menganalisis kadar logam Kadmium ( Cd ) dan
logam Zinkum ( Zn ) yang terdapat dalam Black Liquor, dengan menggunakan
metode destruksi basah dan memakai pelarut HNO3 pekat. Yang kemudian ditentukan
kadarnya menggunakan metode Spektrofotometer Serapan Atom ( SSA )
1.4. Tujuan
Adapun tujuan dari penelitian ini adalah Menganalisis kadar logam Kadmium
1.5. Manfaat Penelitian
1. Memberikan informasi tentang kadar logam kadmium ( Cd ) dan logam Zinkum (
Zn ) yang terdapat pada Black Liquor
2. Memberikan informasi kepada masyarakat seberapa besar kadar logam cadmium
(Cd ) dan logam zinkum ( Zn ) tersebut dapat mengganggu terhadap lingkungan
sekitar.
1.6. Metodologi Penenlitian
Penenlitian ini bersifat eksperimen laboratorium. Metode penenlitian dilakukan
dengan cara sebagai berikut:
1. Metode pengambilan sample dilakukan secara purposif dalam satu kali
pengambilan dalan satu kali proses di TPL
2. Sampel didestruksi dengan metode destruksi basah dengan menggunakan
pelarut HNO3 pekat
3. Penentuan konsentrasi logam Kadmium ( Cd ) dan Zinkum ( Zn ) dilakukan
secara Spektrofotometer Serapan Atom ( SSA )
1.7. Lokasi Penelitian
1. Preparasi sample dikakukan di Laboratorium Kimia Analitik FMIPA-USU
Medan
2. Analisa kuantitatif logam Kadmium ( Cd ) dan Zinkum ( Zn ) dilakukan di
BAB II
TINJAUAN PUSTAKA
Komposisi Kimia Kayu
Kayu merupakan bahan utama yang dipakai untuk pembuatan pulp dan kertas
karena rendemen seratnya sangat tinggi. Pada pertumbuhannya tanaman ini
membutuhkan senyawa kimia berupa makro molekul primer dan sekunder seperti C,
H, O, N, P dan K. Selain makro molekul tanaman juga membutuhkan unsur mikro
seperti besi, magnesium, dan lain lain. Kayu mengandung senyawa-senyawa kimia
yang berbeda. Senyawa tersebut dapat dikelompokkan menjadi 4 bagian yaitu :
Sellulosa, Hemi sellulosa, Lignin dan Ekstraktif (TAPPI, 1989).
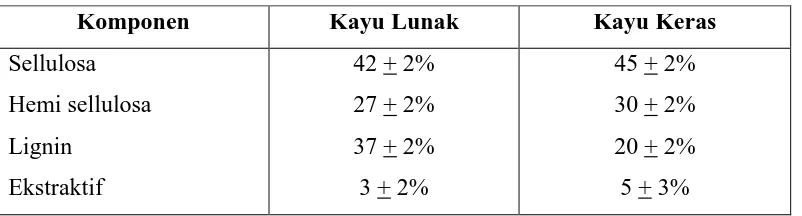
Komposisi dan sifat-sifat kimia ini sangat berperan dalam proses pembuatan
pulp. Secara umum kayu keras (hard wood) mengandung banyak sellulosa, hemi
sellulosa dan ekstraktif dibandingkan dengan kayu lunak (soft wood) tetapi kandungan
ligninnya lebih sedikit (TPL, 2001).
Tabel 2.1. Komposisi Kimia antara Hard Woods dan Soft Woods (Smook, 1992)
Komponen Kayu Lunak Kayu Keras
Sellulosa
Hemi sellulosa
Lignin
Ekstraktif
42 + 2%
27 + 2%
37 + 2%
3 + 2%
45 + 2%
30 + 2%
20 + 2%
5 + 3%
2.1.1 Hara essensial tanaman
Tanaman memerlukan sejumlah unsur hara dalam takaran cukup, seimbang
dan sinambung untuk terus tumbuh dan berkembang. Unsur hara tanaman ini diambil
dari atmosfir dan sistem tanah. Paling sedikt ada 16 macam unsur hara yang
berbeda.Unsur hara yang dibutuhkan dalam jumlah yang banyak disebut unsur hara
makro dan yang dibutuhkab dalam jumah yang sedikit disebut unsur hara mikro.Hal
ini dapat dilihat pada table 2.2
Tabel 2.2 jenis dan bentuk hara yang diserap oleh tanaman dari tanah
No. Jenis hara
tanaman
Simbol kimia Bentuk ion hara yang diserap
oleh tanaman
1. Nitrogen N NO3- dan NH4+
2. Fosfor P H2PO4- dan H2PO42-
3. Potasium K K+
4. Kalium Ca Ca2+
5. Magnesium Mg Mg2+
6. Sulfur S SO4
2-7. Mangan Mn Mn2+
8. Besi Fe Fe2+
9. Boron B BO33+
10. Seng Zn Zn2+
11. Tembaga Cu Cu2+
12. Molibdenum Mo MoO42-
13. Klorida Cl Cl-
( Mas’ud,1992 )
2.1.2. Komposisi unsur dalam tanah dan tanaman
Secara normal tanaman mendapat unsur hara dari tanah kecuali unsur S dan N
dapat diperoleh secara langsung dari atmosfir dalam bentuk gas NO2, NH3, dan SO2.
Kimia tanah menerangkan bahwa ion-ion dalam tanah ketersediaanya sangat beragam,
oleh karena itu penyerapan oleh tanaman juga beragam.Unsur hara yang ada didalam
tanah diperoleh dari proses pelapukan pada permukaan bumi dan kemudian
dibebaskan keatmosfir atau terlindi. Dan akan hanyut kelaut dan satu ketika akan
Pencemaran kimia dapat mengalihkan unsur - unsur kimia dari daur alaminya.
Tanah mempunyai permukaan reaktif dan aktifitas katalitik maka pencemaran oksigen
dan air ini dapat dikuranginya, jadi tanah dapat menurunkan bahaya pencemaran secar
langsung dengan mengenbalikan komponen- komponen kimia tersebut kedaur
alaminya.Dengan demikian dapat mengurangi pencemaran lingkungan yang
disebabkan oleh aktivitas manusia. (Beer, F.T., 1964)
Proses Pembuatan Pulp
Proses pembuatan pulp menurut perlakuan yang diterapkan terhadap bahan
baku dapat digolongkan menjadi beberapa golongan, yaitu :
1. Proses mekanis
2. Proses semi kimia
3. Proses kimia, yang terdiri dari :
a. Proses soda (alkali)
b. Proses sulfit (asam)
c. Proses sulfat (proses kraf)
Proses Pembuatan Pulp Sulfat (Proses Kraft)
Proses pembuatan pulp yang paling banyak dipakai saat ini adalah proses
sulfat atau disebut juga proses kraft. Proses sulfat merupakan pengembangan dari
proses soda. Proses sulfat lebih baik daripada proses soda karena lebih fleksibel dalam
bahan baku, waktu pemasakan lebih singkat, pulp dapat diputihkan sampai derajat
kecerahan tinggi, kekuatan fisik pulp lebih tinggi dan sisa larutan pemasak mudah
untuk didaur ulang (Condar, 1992).
Mc Donald dan Franklin, menyatakan bahwa proses sulfat merupakan salah
satu proses pembuatan pulp secara kimia yang menggunakan larutan pemasak
Natrium Hidroksida (NaOH) dan Natrium Sulfida (Na2S) yang dikenal dengan alkali
aktif. NaOH berfungsi untuk mendegradasi dan melarutkan lignin sehingga mudah
deliginifikasi juga memperhatikan karbohidrat dari degradasi sehingga menghasilkan
rendemen yang tinggi dan kekuatan fisik yang baik.
Black Liquor
Black Liquor berasal dari digester, yaitu alat pemasak serpihan kayu yang
berbentuk silinder. Black Liquor warnanya hitam karena reaksi kimia yang terjadi
antara serpihan kayu dengan bahan kimia yang dimasukkan kedalam white liquor.
Black Liquor mengandung bahan organik dan anorganik yang telah dipisahkan dari
kayu selama proses pemasakan. Komposisi Black Liquor dari sebagian besar kayu
lunak diberikan pada Tabel 2.3. Bandingannya dengan, white liquor dapat dilihat pada
Tabel 2.4..
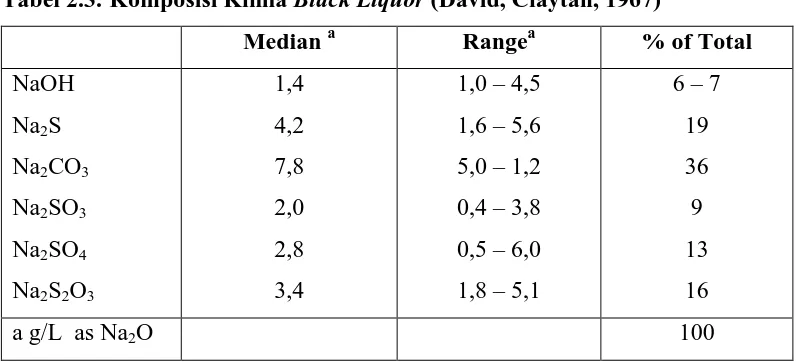
Tabel 2.3. Komposisi Kimia Black Liquor (David, Claytan, 1967)
Median a Rangea % of Total
NaOH
Na2S
Na2CO3
Na2SO3
Na2SO4
Na2S2O3
1,4 4,2 7,8 2,0 2,8 3,4
1,0 – 4,5
1,6 – 5,6
5,0 – 1,2
0,4 – 3,8
0,5 – 6,0
1,8 – 5,1
6 – 7
19
36
9
13
16
a g/L as Na2O 100
Tabel 2.4 Komposisi Kimia White Liquor (Thomas, M, 1989)
Median a Rangea % of Total
NaOH
Na2S
Na2CO3
Na2SO3
Na2SO4
Na2S2O3
95 38 26 4,8 9,1 6,0
18 – 20
30 – 40
11 – 44
2,0 – 6,9
4,4 – 18
4,0 – 8,9
53 21 15 3 5 3
2.3.1. Evaporasi Black Liquor
Pada prinsipnya evaporasi merupakan operasi pendidihan yang khusus tentang
perpindahan panas dalam cairan mendidih. Umumnya sebagai media pemanas adalah
uap yang melewati suatu permukaan logam dan bahan yang dipanasi. Titik didih suatu
cairan turun bila tekanan udara diatasnya lebih rendah 1 atm, oleh karena itu kondisi
operasi evaporasi dilakukan pada tekanan vakum supaya titik didih larutan yang
diharapkan lebih rendah. Hal ini akan mengakibatkan perbedaan suhunya menjadi
lebih besar sehingga diperoleh perpindahan panas yang besar dengan demikian Black
Liquor dengan padatan 14% - 18% dapat menjadi 70% dan siap untuk dipakai
menjadi bahan bakar di Recovery Boiler (TPL, 2002)
2.3.2. Sistem Pembakaran Black Liquor pada Furnace
Black Liquor pekat dimasukkan kedalam ruang bakar dengan jalan
disemprotkan. Black Liquor yang disemprotkan akan membentuk partikel-partikel
yang akan jatuh pada dasar ruang bakar sambil dikeringkan.
Udara untuk pembakaran Black Liquor dialirkan kearah reduksi dan oksidasi.
Proses reduksi diperlukan untuk mengubah natrium sulfat (Na2SO4) menjadi natrium
sulfida (Na2S). sebagian udara diperlukan untuk pembakaran sempurna pada timbunan
arang yang dilewatkan melalui bagian bawah yang disebut dengan udara primer.
Reaksi yang terjadi di ruang bakar adalah :
Na2O + CO2 → Na2 CO3
Na2O + SO2 + ½O2 → Na2 SO4
Na SO4 + 2C → Na2S + 2CO2
Na SO4 + 4C → Na2S + 4CO (TPL, 2002)
2.3.3. Sistem Pemasukan Udara Kedalam Ruang Bakar
Sistem pemasukan udara kedalam furnace dibagi menjadi tiga, yaitu :
a. Udara primer yaitu udara yang masuk ke furnace dari bagian bawah
c. Udara tersier yaitu udara yang masuk dari bagian sebelah atas spraygun
Guna udara primer adalah untuk terjadinya reduksi didalam ruang bakar
disamping itu juga untuk mengatur pembentukan arang dan membantu
berlangsungnya aliran smelt keluar. Udara sekunder berguna untuk menjaga tumpukan
arang jangan terlalu tinggi agar terbentuk arang yang bagus dan juga untuk
menghembus Black Liquor yang menempel di dinding ruang bakar (TPL, 2002).
2.3.4. Komposisi Senyawa Kimia Anorganik dalam Black Liquor
Pada dasarnya material Black Liquor diperoleh dari 2 sumber yaitu kayu dan
white liquor.
Beberapa senyawa kimia anorganik yang terdapat dalam Black Liquor adalah :
Natrium hidroksida (NaOH)
Natrium sulfida (Na2S)
Natrium karbonat (Na2CO3)
Natrium sulfat (Na2SO4)
Natrium hiosulfat (Na2S2O3)
Natrium klorida (NaCl) (Thomas, M, 1989)
Komposisi Black Liquor tergantung pada jumlah alkali (komposisi white
liquor), pulp yang dihasilkan dan spesies kayu yang digunakan.
Didalam black liquor juga terdapat logam-logam yang bersumber dari kayu
yang digunakan, diantaranya : Timbal, Besi, Zink, Kadmium, Mangan, Cobalt, dan
lain-lain. Logam-logam ini juga akan berbahaya jika kadarnya terlalu tinggi dan dapat
mencemari lingkungan. Black liquor dapat berperan penting dalam industri pulp,
karena dapat didaur ulang menjadi lindi hijau dimana poada recovery boiler diasup
oleh natrium sulfat (Na2SO4) agar kekurangan SO4-2
Data dalam beberapa kandungan anorganik dijelaskan dalam tabel 2.5. analisis
untuk NaCl atau Na2SO3 kandungannya tidak dibuat.
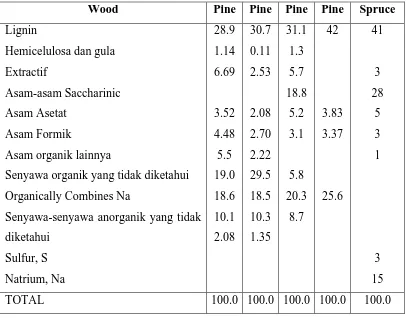
Tabel 2.5. Komponen dalam Black Liquor (Passinen, 1968)
Wood Pine Pine Pine Pine Spruce
Lignin
Hemicelulosa dan gula
Extractif
Asam-asam Saccharinic
Asam Asetat
Asam Formik
Asam organik lainnya
Senyawa organik yang tidak diketahui
Organically Combines Na
Senyawa-senyawa anorganik yang tidak
diketahui Sulfur, S Natrium, Na 28.9 1.14 6.69 3.52 4.48 5.5 19.0 18.6 10.1 2.08 30.7 0.11 2.53 2.08 2.70 2.22 29.5 18.5 10.3 1.35 31.1 1.3 5.7 18.8 5.2 3.1 5.8 20.3 8.7 42 3.83 3.37 25.6 41 3 28 5 3 1 3 15
TOTAL 100.0 100.0 100.0 100.0 100.0
Tabel 2.6 Kandungan Anorganik dalam Black Liquor (Grace T, 1977)
Na2CO3 Na2SO4 R.A.A
As Na2O
Fraksi anorganik pada liquor tidak kelihatan jelas sebab beberapa sodium
terkumpul pada senyawa anorganik anion dan beberapa anion organik. Salah satu
penaksiran kandungan anorganik sodium diberikan pada tabel 2.6. ada juga beberapa
garam anorganik, beberapa diantaranya adalah Na2CO3, Na2SO4, Na2S2O3, Na2S,
NaOH dan NaCl, yang terpenting diantaranya adalah Na2CO3 dan Na2SO4 (sebab
senyawa-senyawa tersebut terdapat pada lapisan endapan), Na2S (pengeluaran yang
berbau busuk dan sisa alkali) dan NaOH (efek-efek samping sisa alkali).
Garam-garam anorganik secara langsung berasal dari white liquor (lindi putih).
Banyaknya komponen white liquor (NaOH dan Na2S) reaksinya dengan kayu
dimasukkan selama proses-proses pulp. Sisa garam-garam anorganik dalam white
liquor (Na2CO3, Na2SO4, Na2S2O3, dan NaCl).
Logam
Logam menurut pengertian orang awam adalah barang yang padat dan berat
yang biasanya selalu digunakan orang untuk alat atau perhiasan, yaitu besi, baja, emas
dan perak. Padahal masih banyak logam lain yang penting dan sangat kecil serta
berperan dalam proses biologis mahluk hidup misalnya, kobalt, mangan dan lain-lain
Logam-logam juga dapat menyebabkan timbulnya suatu bahaya pada mahluk
hidup. Hal ini terjadi jika sejumlah logam mencemari lingkungan. Logam-logam
tertentu sangat berbahaya jika ditemukan dalam konsentrasi tinggi dalam lingkungan,
karena logam tersebut dapat merusak tubuh mahluk hidup. (Darmono, 1995)
2.4.1. Kadmium
Kadmium adalah suatu unsur kimia yang relatif jarang, simbolnya Cd, nomor
atom 48. logam ini putih keperakan dengan berat atom 112.40, berat jenis 8.65 pada
20oC dengan jari-jario 1.54 Å (0.154 nm). Titik lebur 321oC dan titik didih 765oC.
Kadmium dialam tidak dijumpai dalam bentuk bebas, dan mineralnya yang
peleburan dan pemurnian bijih seng yang biasanya mengandung 0,2 – 0,4 %
Kadmium.
Logam ini banyak digunakan untuk pelindung besi dan baja dari korosi. Juga
digunakan dalam baterai Nikel, Kadmium, pewarna, solder, dan sebagai stabiliser
dalam pembuatan plastik. Karena kapasitas menyerap Netron yang besar, khususnya
isotop 113, Kadmium digunakan juga pada reaktor nuklir.
Ammonia Sulfurdioksida menyebabkan korosi yang cepat pada Kadmium.
Asam-asam kuat dapat melarutkan logam ini. Kadmium sangat larut dalam larutan
Ammonium Nitrat pekat dan larutan ini biasa digunakan untuk mengupas Kadmium
dari lapisan besi dan baja. Kadmium adalah bivalen dalam semua senyawa stabilnya
dan ionnya tidak berwarna.
Kadmium dapat menyebabkan keracunan yang aktif pada manusia yang
mendapat unsur ini dari makanan. Uap Kadmium, senyawanya, dan larutannya sama
berbahayanya. Oleh karena itu barang dagang yang mengandung lapisan Kadmium
tidak diperkenankan dipakai didalam industri makanan dan minuman. Percobaan pada
tikus menunjukkan bahwa konsentrasi unsur ini didalam ginjal dan hati akan
meningkat pada keadaan dimana tikus tersebut diberi air dengan konsentrasi
Kadmium 0.1 – 10 mg/L. Secara individual pemberian air dengan konsentrasi rata-rata
0.047 mg/L tidak memberikan gejala.
Unsur ini adalah termasuk unsur non essensial dalam tubuh manusia dan
paling banyak terdapat pada hati dan ginjal. Konsumsi air minum dengan kandungan
Kadmium melebihi standar yang sudah ditetapkan akan sangat merugikan karena
unsur ini akan berakumulasi dalam tubuh. Keadaan ini dapat menimbulkan batu
ginjal, gangguan dalam lambung, kerapuhan tulang, pigmentasi gigi. Konsentrasi
standar maksimum yang diperbolehkan untuk air minum menurut Departemen
2.4.2. Zinkum (Zn)
Zink adalah logam yang putih kebiruan, yang disimbolkan dengan Zn dengan
nomor atom 30 dan berat atom 65,38. Logam ini cukup mudah ditempa dan sangat liat
pada 110-150oC. Zink melebur pada 410oC dan mendidih pada 906oC logamnya
sangat murni dan larut sangat lambat sekali dalam asam dan dalam alkali. Adanya
zat-zat pencemar atau pengotor dengan platinum atau tembaga akan mempercepat reaksi.
Asam nitrat pekat mempunyai pengaruh yang kecil zink, karena rendahnya
kelarutan ZnNO3. Tetapi pelarut zink akan terjadi dalam asam nitrat yang encer sekali
karena tidak ada gas yang dilepaskan. (Vogel A.L.)
Zink terdapat secara luas namun sumber utamanya adalah Sphalerite (ZnFe)S
yang terdapat bersamaan dengan galena. Zn ini adalah mempunyai struktur yang rapat
berupa eksagonal Zn sangat mudah bereaksi dengan asam-asam bukan pengoksidasi.
Tetapi Zn larut dalam basah kuat karena mempunyai bentuk ion zinkat (ZnO2-2)
(Cotton F.A, 1976)
Akibat kekurangan Zinkum.
Defisiensi zinkum dapat terjadi pada golongan rentan, yaitu anak – anak, ibu
hamil dan ibu menyusui serta orang tua. Tanda-tanda kekurangn zinkum adalah
gangguan pertumbuhan dan kematangan seksual, gangguan pencernaan seperti diare,
dan gangguan fungsi kekebalan.
Kekurangan zinkum kronis menggangu sistem saraf dan fungsi otak, serta
menggangu metabolisme vitamin A, juga menggangu fungsi kelenjar tiroid dan laju
metabolisme, gangguan nafsu makan, penurunan ketajaman indera perasa serta
Spektrofotometri Serapan Atom
Peristiwa serapan atom pertama kali diamati oleh Fraunhofer, ketika menelaah
garis-garis hitam pada spektrum matahari. Sedangkan yang memanfaatkan prinsip
serapan atom pada bidang analisis adalah seorang Australia bernama Alan Walsh di
tahun 1955. sebelumnya ahli kimia banyak bergantung pada cara-cara
spektrofotometrik atau metode analisis spektrografik. Beberapa cara ini yang sulit dan
memakan waktu, kemudian segera digantikan dengan Spektroskopi Serapan Atom
(SSA). Metode ini sangat tepat untuk analisis zat pada konsentrasi rendah. Teknik ini
mempunyai beberapa kelebihan dibandingkan metode spektroskopi emisi
konvensional.
Pada metode konvensional, emisi tergantung pada sumber eksitasi. Bila
eksitasi dilakukan secara termal, maka ia bergantung pada sumber eksitasi. Bila
eksitasi dilakukan secara termal, maka ia bergatung pada temperatur sumber. Selain
itu eksitasi termal tidak selalu spesifik, dan eksitasi secara serentak pada berbagai
spesies dalam suatu campuran dapat saja terjadi. Sedangkan dengan nyala, eksitasi
unsur-unsur dengan tingkat energi eksitasi yang rendah dapat dimungkinkan. Tentu
saja perbandingan banyaknya atom yang tereksitasi terhadap atom yang berada pada
tingkat dasar harus cukup besar, karena metode serapan atom hanya tergantung pada
perbandingan ini dan tidak bergantung pada temperatur. Metode serapan sangatlah
spesifik. Logam-logam yang membentuk campuran kompleks dapat dianalisis dan
selain itu tidak selalu diperlukan sumber energi yang besar (Khopkar, SM, 1990).
Prinsip Dasar Analisa Spektrofotometer Serapan Atom
Prinsip penentuan metode ini didasarkan pada penyerapan energi radiasi oleh
atom-atom netral pada keadaan dasar, dengan panjang gelombang tertentu yang
menyebabkan tereksitasinya dalam berbagai tingkatan energi. Keadaan eksitasi ini
tidak stabil dan kembali ke tingkat dasar dengan melepaskan sebagian atau seluruh
energi eksitasinya dalam bentuk radiasi. Sumber radiasi tersebut dikenal sebagai
lampu katoda berongga (Hallow Lamp). Proses-proses yang terjadi dari saat
Interaksi atom-atom dengan berbagai bentuk energi dan pengukuran intensitas
frekwensi radiasi oleh pencatat. Unsur yang diperiksa harus dalam keadaan atom yang
tidak tereksitasi, proses untuk menghasilkan atom tersebut disebut atomisasi (Haswel,
S.J, 1991)
Instrumentasi Sumber Sinar
Telah diketahui bahwa untuk pengukuran absorbans atau serapan atom
diperlukan sumber sinar yang memberikan spektrum pancaran yang terdiri dari
puncak-puncak atau garis-garis pancaran yang sempit. Hal ini perlu oleh karena
spektrum serapan atom didalam nyala juga terdiri dari puncak-puncak serapan dengan
lebar pita yang sempit, kira-kira 0,02 – 0,05 A. Lebar pita panjang gelombang sinar
dari sumber yang akan diserap harus lebih sempit dari pada lebar pita puncak serapan.
Sumber sinar yang memenuhi persyaratan tersebut dan lazim digunakan dalam alat
SSA adalah Lampu Katoda Berongga (Hallow Cathode Tubes) (Khopkar, S.M, 1990).
Lampu Katoda Berongga (Hallow Cathode Tubes)
Lampu katoda berongga itu terdiri dari tabung kaca tertutup yang mengandung
suatu katoda dan suatu anoda. Katoda tersebut berbentuk silinder berongga yang
terbuat dari atau yang permukaannya dilapisi dengan unsur yang sama dengan unsur
yang akan dianalisa. Tabung lampu itu diisi dengan gas mulia neon atau argon,
[image:31.595.107.545.592.637.2]intensitas pancaran lampu yang lebih tinggi.
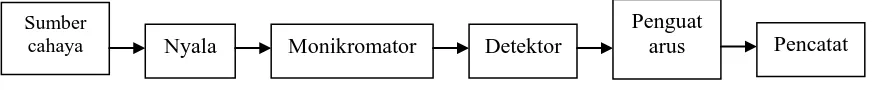
Gambar 2. Instrumen Spektrofotometer Serapan Atom (SSA)
Nyala
Bagian yang terpenting dari suatu nyala adalah alas nyala (base), kerucut
Sumber
cahaya Nyala Monikromator Detektor
Penguat
a. Alas Nyala. Larutan cuplikan masuk kedalam nyala melalui alas nyala, berupa
tetesan-tetesan yang sangat halus. Pada alas nyala ini sudah mulai terjadi
penguapan air dari tetesan-tetesan tersebut. Jadi sebagian dari larutan cuplikan
akan memasuki bagian nyala yang disebut kerucut dalam (inner cone) sebagai
butir-butir halus yang padat.
b. Kerucut Dalam. Bagian nyala ini terjadi penguapan pelarut (desolvasi) lebih lanjut
dan penguraian cuplikan menjadi atom-atom (atomisasi). Dan bagian ini pula
terjadi proses penyerapan sinar oleh atom-atom dan proses eksitasi.
c. Daerah reaksi. Sesudah melalui daerah kerucut dalam, maka atom-atom akan
memasuki bagian nyala yang disebut daerah reaksi (reaction zone). Di dalam
daerah reaksi ini, atom-atom tersebut bereaksi dengan oksigen menjadi
oksida-oksida.
d. Lapisan Luar (Outer Mantle). Oksida yang terjadi dalam daerah reaksi itu
kemudian akan memasuki lapisan luar nyala dan seterusnya keluar meninggalkan
nyala (Ismono, 1981).
Monokromator
Tujuan monokromator adalah untuk memilih garis pancaran tertentu dan
memencilkannya dari garis-garis lain dan kadang-kadang dari pancaran pita molekul.
Dalam spektroskopi absorpsi atom fungsi monokromator adalah untuk memencilkan
garis resonansi dari semua garis yang tidak diserap yang dipancarkan oleh sumber
radiasi. Dalam kebanyakan instrumen komersial digunakan kisi difraksi karena
sebaran yang dilakukan oleh kisi lebih seragam daripada yang dilakukan oleh prisma
dan akibatnya instrumen kisi dapat memelihara daya pisah yang lebih tinggi sepanjang
jangka panjang gelombang yang lebih lebar (Vogel, A.I, 1961).
Detektor
Dalam spektrofotometer absorpsi atom, mengingat kepekaan spektral yang
lebih baik yang diperlukan, digunakan pengganda foton. Keluaran dari detektor
diumpankan ke suatu sistem peragaan yang sesuai, dan dalam hubungan ini
garis resonansi yang telah diseleksi tetapi dapat juga timbul dari emisi dalam nyala.
Emisi ini dapat disebabkan oleh emisi atom yang timbul dari atom-atom yang sedang
diselidiki dan dapat juga dari emisi pita molekul. Jadi sebagai ganti intensitas isyarat
dengan intensitas IA, detektor dapat menerima isyarat dengan intensitas (IA + S)
dengan S ialah intensitas radiasi yang dipancarkan. Karena hanya diperlukan
pengukuran yang timbul dari garis resonansi itu, dan pengganda detektor itu kemudian
distel pada frekuensi ini, dengan cara ini, isyarat-isyarat yang timbul dari nyala, pada
pada hekekatnya berkarakter arus searah, secara efektif disingkarkan (Vogel, A.I,
1961).
Sistem Pencatat
Sistem pencatat yang digunakan pada instrumen SSA berfungsi untuk
mengubah sinyal yang diterima melalui bentuk digital, berarti sistem pencatat
mencegah atau mengurangi kesalahan dalam pembacaan skala secara paralaks,
kesalahan interpolasi diantara pembagian skala dan sebagainya, serta menyeragamkan
tampilnya data (yaitu dalam satuan absorbansi). Sistem pencatat untuk instrumen SSA
sekarang ini dilengkapi dengan suatu mikroprosesor (komputer) sehingga
memungkinkan pembacaan langsung konsentrasi daripada analit di dalam sampel
yang dianalisis (Haswel, S.J, 1991)
2.6. Metode Destruksi
Destruksi merupakan suatu cara perlakuan ( perombakan ) senyawa menjadi
unsur-unsur sehingga dapat dianalisa. Metode destruksi organic dapat dilakukan
dengan dua cara yaitu
a. Metode destruksi kering ( Dry ashing)
b. Metode destruksi basah ( wet Digeston )
Penguraian sample dengan asam- asam kuat baik tungal maupun campuran
dikenal dengan metode destruksi basah sedangakan penguraian sample dengan cara
Metode destruksi basah dilakukan dengan memanaskan contoh ( organic dan
biologis ) dengan adanya asam- asam mineral yamg pekat atau campurandari asam-
assam tersebut. Jika asam yang digunakan cukup untuk mengoksidasi contoh
dipanaskan dalam suhu yang cukup tinggi dan pemanasan dilanjutkan dalam waktu
yang lama maka sebagian besar dari contoh telah teroksidasi dengan sempurna.
(Almatsier,R,. 1987)
Asam- asam kuat yangdapat digunakan untuk mendestruksi sample organic
adalah asasm nitrat ( HNO3 ), asam sulfat (H2SO4 ), asam perklorat ( HClO4 ), asam
klorida ( HCl ) yang dapat digunakansecara tunggal amuapun campuran
Asam kuat yang umum digunakan untuk mendestruksi adalah asam nitrat.
Kebaikan metode desrtuksi basah ini adalah metodenya sangat sederhana, karena
oksidasinya kontiniu dan cepat serta unsur- unsur yang diperoleh mudah larut
sehingga dapr ditentukan dengan metode analisis tertentu.Kekurangan metode ini
adalah reaksi berlangsung sangat kuat dan dapat membuar residu keluar, maka
dilakuakan pemanasan lebih berhati- hati.( Egan,H.,1981 )
Metode destruksi basah dengan menggunakan asam nitrat pekat sebagai
pengoksidasi dengan dikombinasikan menggunakan asam pengoksidasi lain seperti
asam sulfat, asam perklorat dan hidrogen peroksida adalah metode yang paling lazim
digunakan.
Kesempurnaan destruksi ditandai dengan diperolehnya larutan jernih pada
larutan hasil destruksi, yang menunjukkan bahwa semua konstituen yang ada telah
larut sempurna atau penguraian senyawa-senyawa organik telah berjalan dengan baik.
Senyawa-senyawa garam yang terbentuk setelah hasil destruksi merupakan senyawa
garam yang stabil yang dapat disimpan selama beberapa hari, untuk selanjutnya
dianalisis konsentrasi logamnya dengan metode Spektrofotometri Serapan Atom
BAB III
BAHAN DAN METODE PENELITIAN
3.1. Bahan-bahan :
Cd (NO3)2. 4H2O P.a (E.Merck)
ZnSO4.7H2O P.a (E.Merck)
HNO3(p) P.a (E.Merck)
Black Liquor
3.2. Alat-alat :
Spektrofotometer Serapan Atom AvantaG/GF3000
Gelas ukur Pyrex
Labu takar Pyrex
Erlenmeyer Pyrex
Neraca Analitis Mettler AE200
Corong Pyrex
Hot plate PMC
3.3. Prosedur Kerja 3.3.1. Preparasi Sampel
1. Sampel ditimbang sebanyak 5,019 gram lalu dimasukkan kedalam
erlenmeyer kemudian ditambah 25 ml HNO3(p)
2. Kemudian dipanaskan diatas hot plate selama 2 jam lalu didinginkan
3. Sampel yang telah dingin lalu disaring dengan kertas saring whatman
4. Destilat yang diperoleh dimasukkan kedalam labu takar 50 mL dan
ditambahkan akuades sampai tanda batas.
3.3.2. Pembuatan Larutan Standar logam Kadmium
Dilarutkan 2,0675 gram Cd(NO3)2.4H2O dengan akuades dalam labu takar
1000 mL lalu ditambahakan 25 mL HNO3 0,1 N, lalu diencerkan hinga garis
tanda.
3.3.3. Pembuatan Variasi Larutan Standar Cd
1. Dari larutan standar Cd 1000 mg/L dipipet sebanyak 10 mL, lalu
dimasukkan kedalam labu takar 100 mL sehingga diperoleh 100 mg/L
2. Dari 100 mg/L ini dipipet sebanyak 10 mL, lalu dimasukkan kedalam labu
takar 100 mL sehingga diperoleh 10 mg/L
3. Dari 10 mg/L ini dipipet sebanyak 10 mL, lalu dimasukkan kedalam labu
takar 100 mL sehingga diperoleh 1 mg/L
4. Dari 1000 µg/L ini dipipet 50 mL, 20 mL, 10 mL, lalu dimasukkan
kedalam labu takar 100 mL, sehingga diperoleh 500 µg/L , 200 µg/L, dan
100 µg/L digunakan sebagai larutan standar.
3.3.4. Pembuatan Larutan Standar logam Zinkum
Dilarutkan 2,9285 gram ZnSO4.7H2O dengan akuades dalam labu takar 1000
Pembuatan Variasi Larutan Standar Zn
1. Dari larutan standar Zn 1000 mg/L dipipet sebanyak 10 mL, lalu
dimasukkan kedalam labu takar 100 mL sehingga diperoleh 100 mg/L
2. Dari 100 mg/L ini dipipet sebanyak 10 mL, lalu dimasukkan kedalam
labu takar 100 mL sehingga diperoleh 10 mg/L
3. Dari 10 mg/L ini dipipet sebanyak 10 mL, lalu dimasukkan kedalam
labu takar 100 mL sehingga diperoleh 1 mg/L
4. Dari 1000 µg/L ini dipipet 80 mL, 40 mL, 20 mL, lalu dimasukkan
kedalam labu takar 100 mL, sehingga diperoleh 800 µg/L , 400 µg/L,
dan 200 µg/L digunakan sebagai larutan standar.
3.3.5. Penentuan Konsentrasi Kadmium dan Zinkum Dalam sampel Dengan Spektrofotometer Serapan Atom
- Filtrat hasil destruksi ini diatur pH-nya 3-4 dengan pH meter
- Kemudian filtrat hasil destruksi ini dianalisa kadar ion logam
Cd dan Zn nya dengan alat Spektrofotometer Serapan Atom
pada panjang gelombang 228.80 nm untuk Cd dan pada
panjang gelombang 213.9 nm untuk Zn, sebagai gas pembakar
adalah argon-udara dan volume sampel yang diaspirasikan lebih
kurang 1 mL dengan temperatu nyala 23000C
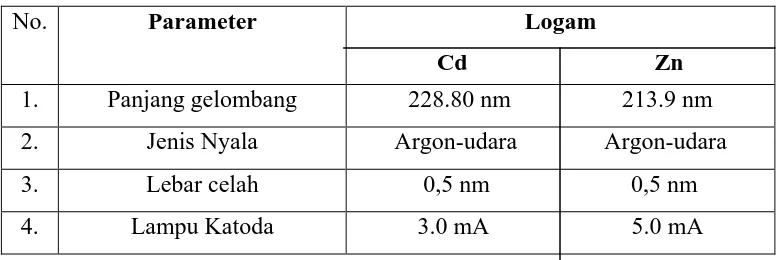
[image:37.595.107.498.624.754.2]3.3.7.Kondisi Paramater Spektrofotometer Serapan Atom
Tabel 3.1 Merek Spektrofotometer Serapan Atom (SSA) : Avanta G/GF3000
No. Parameter Logam
Cd Zn
1. Panjang gelombang 228.80 nm 213.9 nm
2. Jenis Nyala Argon-udara Argon-udara
3. Lebar celah 0,5 nm 0,5 nm
3.4 Bagan Penelitian
Dimasukkan kedalam Erlenmeyer
Ditambahkan 25 mL HNO3 (p)
Dipanaskan diatas hotplate selama 2 jam
Didinginkan
Disaring
Dimasukkan kedalam labu takar
Ditambahkan akuades samapi
Tanda baca
Diatur pHnya dibawah pH 4
Dianalisa dengan SSA
(Greenberg, 2005. Standar Method)
5,019 gram Sampel
Residu Filtrat
BAB IV
HASIL DAN PEMBAHASAN
Hasil Penelitian dan Pengolahan Data
4.1.1 Data Hasil Pengukuran Logam Kadmium (Cd)
Data hasil pengukuran absorbansidari suatu seri larutan standar logam
Kadmium diplotkan terhadap konsentrasi larutan standar dapat dilhat pada tabel
4.1,dan data hasil pengukutan absorbansi logam kadmium pada Black Liquor dapat
dilihat pada tabel 4.2
[image:39.595.106.410.438.522.2]
Tabel 4.1. Data Hasil Pengukuran Absorbansi Larutan Standar Logam Kadmium (Cd) Dengan Spektrofotometer Serapan Atom
No Kadar (µg/L) Absorbansi (A)
1.
2.
3.
100
200
500
0,4032
0,4161
0,6202
Tabel 4.2 Data Hasil Pengukuran Absorbansi Logam Kadmium Pada Black Liquor
Kode Sampel Kadar (mg/L) Absorbansi
[image:39.595.110.414.607.649.2]4.1.2 Pengolahan Data Logam Kadmium
4.1.2.1. Penentuan Kurva Kalibrasi Dengan analisis Regresi
Tabel 4.3 Data Hasil Penurunan Persamaan Garis Regresi Untuk Unsur Kadmium (Cd)
No Xi(ppb) Yi(A) (Xi- X ) (Yi- Y ) (Xi- X )2 (Yi- Y )2 (Xi- X )(Yi- Y )
1 100 0.4032 -166.6667 -0.0766 27777.7889 0.0056 12.7667
2 200 0.4161 -66.6667 -0.0637 4444.4489 0.0041 4.2467
3 500 0.6202 233.3333 0.1404 54444.4289 0.0197 32.7599
∑ 800 1.4395 000.0000 0.0001 26666.6667 0.0297 49.7733
Dimana harga X rata-rata, 266,6667
3 800
= = =
∑
nXiX
Dimana harga Y rata-rata, 0,4798
3 1,4395
= =
=
∑
nYiY
4.1.2.2. Penurunan Persamaan Garis Regresi
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis :
Y = aX + b
Dimana : a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan metode last square sebagai
berikut : a =
∑
∑
− − − 2 ) X (Xi ) Y (Yi ) X (Xi a = 6667 . 26666 7773 . 49Dari nilai a yang diperoleh maka dapat dihitung harga b (intercept) dengan
rumus :
Y = aX + b
b = Y - aX
b = 0,4798 – (0,0005 x 266,6667)
= 0,3465
Maka persamaan yang diperoleh adalah :
Y = 0,0005X + 0,3465
Dengan mensubstitusikan harga-harga X yang ada kedalam persamaan garis
regresi diatas, maka diperoleh Y baru, untuk :
X = 100 ; maka harga Y = 0.3965
X = 200 ; maka harga Y = 0.4465
X = 500 ; maka harga Y = 0.5965
4.1.2.3.Perhitungan Untuk Logam Kadmium
Konsentrasi Cd dalam Black Liquor = 349,480 µg/mL
Cd dalam 50 ml sampel = 349,480 µg/mL x 50 mL
= 17474 µg
Cd dalam 5,019 gr Black Liquor =
gr 5,019
μg 7474 1
= 3481,5 µg /gr
Konsentrasi Cd dalam mg/L = 3,5
4.1.2.4. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut : 2 1 2 ] 2 ) Y i (Y ) X i [(X )] Y i (Y ) X i [(X r − ∑ − ∑ − − =
4.1.3 Data Hasil Pengukuran Logam Zinkum (Zn)
Data hasil pengukuran absorbansidari suatu seri larutan standar logam Zinkum
diplotkan terhadap konsentrasi larutan standar dapat dilhat pada tabel 4.4, dan data
[image:42.595.106.410.294.381.2]hasil pengukutan absorbansi logam Zinkum pada Black Liquor dapat dilihat pada
tabel 4.5
Tabel 4.4 Data Hasil Pengukuran Absorbansi Larutan Standar Logam Zinkum (Zn) Dengan Spektrofotometer Serapan Atom
No Kadar (µg/L) Absorbansi (A)
1.
2.
3.
200
400
800
0,2792
0,3394
0,5148
Tabel 4.5 Data Hasil Pengukuran Absorbansi Logam Zinkum Pada Black Liquor
Kode Sampel Kadar (mg/L) Absorbansi
BL 11,6 0,2378
4.1.4 Pengolahan Data Logam Zinkum
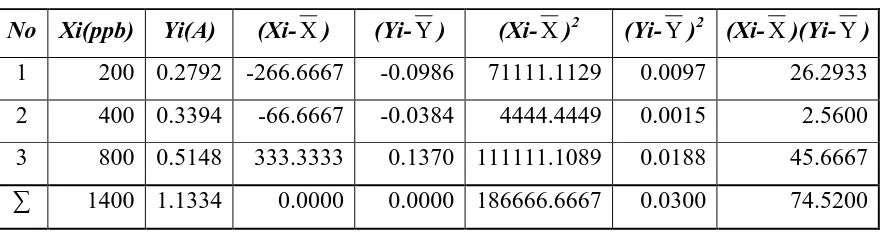
[image:42.595.108.416.449.494.2]4.1.4.1 Penentuan Kurva Kalibrasi Dengan analisis Regresi
Tabel 4.6 Data Hasil Penurunan Persamaan Garis Regresi Untuk Unsur ( Zn )
No Xi(ppb) Yi(A) (Xi-X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
1 200 0.2792 -266.6667 -0.0986 71111.1129 0.0097 26.2933
2 400 0.3394 -66.6667 -0.0384 4444.4449 0.0015 2.5600
3 800 0.5148 333.3333 0.1370 111111.1089 0.0188 45.6667
[image:42.595.109.549.611.728.2]Dimana harga X rata-rata, 466,6667 3
1400
= =
=
∑
nXiX
Dimana harga Y rata-rata, 0,3778
3 1,1334
= =
=
∑
nYiY
4.1.4.2 Penurunan Persamaan Garis Regresi
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis :
Y = aX + b
Dimana : a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan metode last square sebagai
berikut : a =
∑
∑
− − − 2 ) X (Xi ) Y (Yi ) X (Xi a = 6667 , 186666 5200 , 74a = 0,0004
Dari nilai a yang diperoleh maka dapat dihitung harga b (intercept) dengan
rumus :
Y = aX + b
b = Y - aX
b = 0,3778 – (0,0004 x 466,6667)
= 0,1911
Maka persamaan yang diperoleh adalah :
Dengan mensubstitusikan harga-harga X yang ada kedalam persamaan garis
regresi diatas, maka diperoleh Y baru, untuk :
X = 200 ; maka harga Y = 0.2711
X = 400 ; maka harga Y = 0.3511
X = 800 ; maka harga Y = 0.5111
4.1.4.3 Perhitungan Untuk Logam Zinkum
Konsentrasi Zn dalam Black Liquor = 1161,205 µg/mL
Zn dalam 50 ml sampel = 1161,205 µg/mL x 50 mL
= 58060,25 µg
Zn dalam 5,019 gr Black Liquor =
gr 5,019 μg 25 , 58060
= 11568,09 µg /gr
Konsentrasi Zn dalam mg/L = 11,6
4.1.1.5. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut : 2 1 ] 2 ) Y i (Y 2 ) X i [(X )] Y i (Y ) X i [(X r − ∑ − ∑ − − =
4.2 Pembahasan
Analisa Kadar Logam Kadmium ( Cd ) dan logam Zinkum ( Zn ) pada
Black Liquor atau lindi hitam dari TPL ( Porsea ), dengan Spektrofotometer Serapan
Atom ( SSA ).Untuk menentukan konsentrasi logam Cd dan Zn.
Telah dilakukan pengambilan sampel secara purposif yaitu sampel
langsung diambil dari tanki strong Black Liquor dalam satu kali pengambilan untuk
satu kali proses. Kemudian sampel langsung didestruksi memakai pelarut HNO3 (p)
hingga larutan berubah warna dari hitam menjadi kuning pucat. Setelah destruksi
dilakukan sampel dianalisis kadar logamnya dengan SSA .
Konsentrasi logam Cd diperoleh melalui kurva kalibrasi larutan standar
logam Cd ( Gambar I ) pada lampiran. Dibuat dari larutan standar kadmium. Dengan
menggunakan persamaan Least Square diperoleh persamaan garis linier untuk logam
Cd sebagai berikut:
Y = 0.0005X + 0.3465 dengan grafik terlampir ( Gambar I )
Dari tabel 4.2 dapat dilihat hasil pengukuran absorbansi logam kadmium
pada Black Liquor dengan Sprektofotometer Serapan Atom.
Kode Sampel Kadar (mg/L) Absorbansi
BL 3,5 0,5274
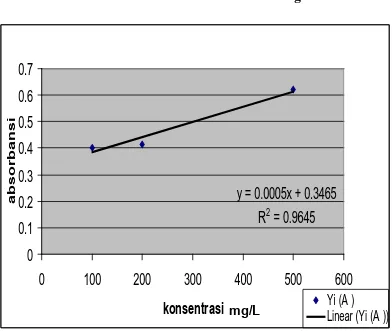
Konsentrasi logam Zn diperoleh melalui kurva kalibrasi larutan standar
logam Zn( Gambar 2) pada lampiran. Dibuat dari larutan standar kadmium. Dengan
menggunakan persamaan Least Square diperoleh persamaan garis linier untuk logam
Zn sebagai berikut:
Dari tabel 4.5 dapt dilihat hasil pengukuan absorbansi logam Zinkum pada
Black Liquor dengan Sprektofotometer Serapan Atom.
Kode Sampel Kadar (mµg/L) Absorbansi
BL 11,6 0,2378
Dari hasil penelitian ini dapat dilihat bahwa kadar logam Cd lebih rendah
dibandingkan kadar logam Zn. Dari sampel diperoleh kadar logam Cd sebesar 0.35
mg/L dan kadar logam Zn sebesar 11,6 mg/L. Hal ini sangat erat kaitannya dengan
kandungan logam- logam yang terdapat dalam Dreg, Lime mud. Hal ini sesuai dengan
penelitian yang telah dilakuakan oleh Econotecht (tabel 4 pada lampiran) diperoleh
berturut- turut kadar logam dari yang paling tinggi adalah Black Liquor, Dreg, dam
lime mud. Hal ini disebabkan karena ada sebagian logam yang kurang sempurna
reaksinya selama recovery furnace atau ada sebagian logam yang mudah mengeuap.
Menurut Econotecht ( tabel 4 pada lampiran ) kadar logam yang diperoleh
dalam black liqour adalah < 5 mg/Kg untuk logam Cd, sedangkan untuk logam Zn
adalah sebesar 10 mg/Kg. Hal ini menunjukkan bahwasanya logam Cd dan Zn
ketersediaannya di tanah sangat kecil dan merupakan unsur mikro bagi tumbuhan.
Karena Black Liquor yang dihasilkan dari proses digester tidak langsung
dibuang kelingkungan tetapi akan mengalami proses recovery furnace, dimana Black
Liquor akan dimasukkan kedalam ruang pembakar melalui proses penyemprotan yang
kemudian akan membentuk partikel- partikel yang akan jatuh pada dasar ruang bakar
yang disebut dengan dreg ( limbah padat ).
Pada proses ini digunakan udara primer untuk mempercepat terjadinya proses
pembakaran, yang memungkinkan berkurangnya konsentrasi logam pada limbah padat
yang dihasilkan seperti yang dijelaskan diatas dimana konsentrasi logam didalam
black liquor lebih tinggi dari pada didalam dreg dan lime mud.
Oleh karena itu jika dreg atau lime mud hasil lanjutan dari black liquor setelah
seperti pembuatan batako, bahan pencampur aspal, maka dari itu perlu dilakukan
analisis lebih lanjut untuk menentukan konsentrasi logam berat apakah kadarnya
sudah aman atau tidak mencemari lingkungan apabila digunakan misalnya untuk
pembuatan batako yang apabila terkena hujan akan tercuci ke ekosistem sekitar yang
akan dapat mengganggu lingkungan tersebut. Oleh karena konsentrasei logam Cd dan
Zn yang terdapat didalam black liquor) tidak memberikan pengaruh yang besar
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Berdasarakan hasil penelitian diperoleh kadar logam Kadmium (Cd ) sebesar
3,5 mg/L dan kadar logam Zinkum (Zn) sebesar 11.6 mg/L dalam 5.019 gram sampel
Black Liquor. Kadar kedua logam ini tidak banyak berpengaruh terhadap lingkungan,
karena black liquor bukan merupakan limbah yang langsung ke lingkungan.
5.2 Saran
Disarankan adanya penelitian lebih lanjut bagaimana caranya untuk
menurunkan kadar kedua logam ini ( Cd dan Zn ) agar tidak melewati batas
DAFTAR PUSTAKA
Almatsier,R.1987. Sampel Pretreatment & Separation. New York: Jhon Wiley and So Ns.
Bear, F.T. 1964. Chemistry of The Soil. Secound Edition. New York: Rainhold
Conrad, F., Cornell, Robert P Green, Gerald Hough.1992. Cooking Liquor Preparation in Chemical Recovery in Alkaline Pulping Processesm. TAPPI Atlanta GA 119-150
Cotton, F. A. 1989, Kimia Anorganik Dasar¸Jakarta : UI-Press
Durbak, I.1993. Disolving Pulp Industry Market Trends. Gen Tech.
D.W. Clayton, P. Dr. 1967. Pulp and Paper Manufacture . Second Edition, Canada:Chemistry of Alkaline Pulping
Damono. 1995. Logam Dalam Sistem Biologi Makhluk Hidup. Jakarta: UI- Press
Egan, H. 1981. Chemical Anallllysis of Food. Eight Edition. New York : Churchill Livingstene.
Grace, T. , sachs,D and Grady,H. 1997. TAPPI 60 ( 4 ) : 122
Haswell, S. J. 1991. Atomic Absorption Spectrophotometry Theory Designand Aplication. New York: Elseiver
Heryando Palar. 2004. Pencemaran dan Toksikologi logam Berat. Edisi Kedua. Jakarta : PT Rineka Cipta.
Ismono, 1981. Cara-Cara Optik dalam Analisa Kimia. Bandung : Departemen Kimia ITB.
Khopkar, S.M. 1990. Konsep Dasar Kimia Analitik. Jakrta : UI- Press
Mas’ud, P. 1992. Telaah Kesuburan Tanah . Yogyakarta : Agkasa bandung
Passinen, K. 1986. Proceedings on The Recovery of Pulping Chemicals. IUPAC-EUCEPA
Raimon. 1992. Perbandingan Metode Destruksi Basah dan Kering terhadar Penentuan logam Fe, Cu dan Zn. Edisi Khusus BIPA. Palembang.
Thomas, M. Grace. 1989. Pulp and Paper Manufacture, Third Edition .USA: The join Text Book Comitte of The Paper Industry.
Training and Development Center. 2001. Digester Pulp. Porsea: TPL
Training and Development Centre. 2002. Energy Seam and Liquor Site. Porsea: TPL
Smook, G.A. 1992. Hand Book for Pulp and Paper Technologist. Secound edition.canada: Vancouver.
Vogel, A.L. 1961. A Text Book of Quantitative Inorganic analysis. Third editioan. London: The Englissh Book Society and Longmans.
Vogel, 1979. Anailsis Anorganik Kuantitatif Makro dan Semi Mikro, Jilid I, Edisi kelima, Jakarta : PT. Kalman Media Pusaka.
Lampiran 1.
Kurva Kalibrasi Larutan Standar Logam Cd
y = 0.0005x + 0.3465
R
2= 0.9645
0
0.1
0.2
0.3
0.4
0.5
0.6
0.7
0
100
200
300
400
500
600
konsentrasi
a
b
s
o
r
b
a
n
s
i
Yi (A )
[image:52.595.110.502.160.491.2]Linear (Yi (A ))
Grafik 1. Kurva Kalibrasi Larutan Standar Logam Cd
Lampiran 2
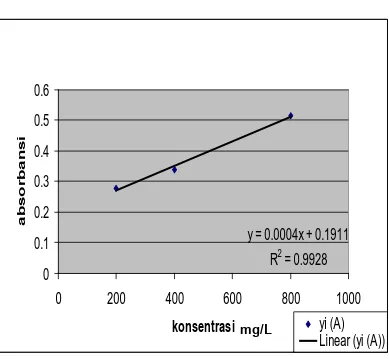
Kurva Kalibrasi Larutan Standar Logam Zn
y = 0.0004x + 0.1911
R
2= 0.9928
0
0.1
0.2
0.3
0.4
0.5
0.6
0
200
400
600
800
1000
konsentrasi
a
b
s
o
r
b
a
n
s
i
yi (A)
[image:53.595.112.501.172.531.2]Linear (yi (A))