RESPONS PERTUMBUHAN BENIH IKAN GURAMI
(
Osphronemus goramy
) YANG DIBERI PAKAN DENGAN
KADAR PROTEIN BERBEDA DAN DIPERKAYA HORMON
PERTUMBUHAN REKOMBINAN
DARMAWAN SETIA BUDI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa tesis berjudul “Respons Pertumbuhan Benih Ikan Gurami (Osphronemus goramy) yang Diberi Pakan dengan Kadar Protein Berbeda dan Diperkaya Hormon Pertumbuhan Rekombinan”
adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan dan tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
RINGKASAN
DARMAWAN SETIA BUDI. Respons Pertumbuhan Benih Ikan Gurami (Osphronemus goramy) yang Diberi Pakan dengan Kadar Protein Berbeda dan Diperkaya Hormon Pertumbuhan Rekombinan. Dibimbing oleh ALIMUDDIN dan MUHAMMAD AGUS SUPRAYUDI.
Ikan gurami memiliki laju pertumbuhan yang relatif lambat. Aplikasi hormon pertumbuhan rekombinan (recombinant growth hormone, rGH) melalui pakan telah terbukti menghasilkan peningkatan pertumbuhan. Secara umum, pemberian GH eksogen dapat meningkatkan kapasitas metabolisme ikan gurami, khususnya metabolisme lemak serta optimasi sintesis dan pemanfaatan protein untuk pertumbuhan pada ikan gurami. Penambahan nutrien non-protein sebagai penghasil energi dapat menurunkan penggunaan protein sebagai sumber energi (protein sparring effect) sehingga dapat meningkatkan fungsi protein dalam menunjang pertumbuhan ikan. Penggunaan pakan dengan kadar protein yang rendah dapat mengurangi harga pakan namun dapat menyebabkan pertumbuhan ikan menjadi lambat sehingga waktu produksi menjadi semakin lama. Kombinasi antara aplikasi rGH dan penggunaan pakan berkadar protein yang berbeda yang diberikan pada benih ikan gurami diharapkan mampu meningkatkan protein sparring effect. Tujuan penelitian ini adalah untuk menguji efek pemberian pakan dengan kadar protein berbeda yang diperkaya dengan rGH terhadap respons pertumbuhan benih ikan gurami.
Protein rGH yang telah disalut (coating) dengan kuning telur dicampur dengan pakan berkadar protein berbeda (34%, 28%, dan 21%; isoenergi) dengan dosis basah 3 mg/kg pakan, masing-masing perlakuan memiliki kontrol perlakuan pakan tanpa penambahan rGH. Setiap perlakuan memiliki 3 ulangan. Ikan gurami (bobot tubuh 15,83±0,13 g) diberi pakan mengandung rGH 2 kali seminggu, secara satiasi. Pemeliharaan ikan dilakukan selama 42 hari di akuarium bervolume 100 liter, dengan padat tebar 10 ekor. Parameter yang diuji meliputi pertambahan biomassa, laju pertumbuhan spesifik (LPS), dan rasio konversi pakan (RKP); indeks hepatosomatik (IHS), retensi protein (RP) dan lemak (RL), ekskresi total amonia nitrogen (TAN), kadar glukosa dan trigliserida darah; serta aktivitas enzim. Analisis data dengan tabel sidik ragam dilakukan menggunakan software statistik SPSS 17.0.
(P<0,05), sedangkan pada perlakuan pakan berprotein 34% pemberian rGH tidak berpengaruh nyata (P>0,05).
Nilai IHS berbanding terbalik dengan kadar protein pakan, sedangkan penambahan rGH secara signifikan (P<0,05) meningkatkan nilai IHS pada setiap perlakuan kadar protein pakan. Peningkatan kadar protein pakan menurunkan kadar glikogen hati dan otot. Nilai RP dan RL pada tiap level protein pakan lebih tinggi (P<0,05) dibandingkan dengan masing-masing kontrolnya, kecuali pada pakan berkadar 28% yang nilai RP dan RL tidak berbeda nyata (P>0,05) dengan kontrolnya (pakan berprotein 28% tanpa rGH). Ekskresi TAN meningkat dengan meningkatnya kadar protein pakan dan penambahan rGH secara signifikan (P<0,05) menurunkan ekskresi TAN.
Pertambahan biomassa tertinggi terjadi pada perlakuan pakan berprotein 21% (214,88±12,31 g); yaitu 35,01% lebih tinggi (P<0,05) dibandingkan kontrolnya (159,17±13,92 g). Pertambahan biomassa terendah terjadi pada perlakuan pakan berprotein 34% (339,37±9,69 g); 16,90% lebih tinggi (P<0,05) dibandingkan kontrolnya (290,33±14,93 g). Pertambahan biomassa dan LPS tertinggi, dan RKP terendah diperoleh pada perlakuan pakan berprotein 34% yang diperkaya rGH. Pertambahan biomassa, LPS, dan RKP pada perlakuan pakan berprotein 28% dengan penambahan rGH menghasilkan nilai yang sama dengan pakan berprotein 34% tanpa suplementasi rGH (P>0,05). Sebagai kesimpulan bahwa pemberian rGH dengan dosis basah 3 mg/kg pada pakan berkadar protein berbeda mampu meningkatkan pertumbuhan dan mengefisiensikan pemanfaatan protein pada benih ikan gurami.
SUMMARY
DARMAWAN SETIA BUDI. Giant Gourami (Osphronemus goramy) Juvenile Growth Response on Fed Diets Different Protein Levels and Enriched with Recombinant Growth Hormone. Supervised by ALIMUDDIN and MUHAMMAD AGUS SUPRAYUDI.
Giant gourami has a relatively slow growth rate. The rGH suplementation in diets has been shown to result in increased growth. In general, administration of exogenous GH is able to increase the metabolism capacity of giant gourami; especially lipid metabolism and the optimation of the synthesis and utilization of protein for growth. The addition of non-protein nutrients as energy source can reduce the use of protein for energy (protein sparring effect). It leads to the improvement of the protein function in supporting the growth of fish. Feed with low protein levels can reduce cost production but slows the growth as the fish can not efficiently utilize low protein diet. The combination of rGH suplementation and dietary protein levels given in giant gourami juvenile are expected to provide good results in the low protein diet by increasing protein sparring effect on feed. The purpose of this study was to examine the effect of dietary protein levels and enriched with recombinant growth hormone (rGH) on the growth of giant gourami fry.
The rGH coated with chicken egg yolk at a wet-based dose of 3 mg/kg of feed was sprayed to artificial feed with different protein levels (34%, 28%, and 21%; isoenergy). Each treatment has a control without rGH supplementation. Giant gourami (BW 15.83±0.13 g) was fed diets containing rGH at apparent satiation 2 times a week, interval 3 days. Fish were reared for 42 days in the 100-L glass aquaria at initial density of 10 fish. The tested parameters were yield, specific growth rate (SGR), and feed conversion ratio (FCR); hepatosomatic index (HSI), protein (PR) and lipid (FR) retention, total ammonia nitrogen (TAN) excretion, triglycerides and glucose levels in blood; and enzymes activity. All data were further analyzed statistically using the ANOVA with SPSS 17.0 statistical software.
HSIwas inversely related to dietary protein levels, and rGH suplementation was significantly (P<0.05) increased to HSI value on each treatment in the dietary protein levels. PR and FR values at rGH treatments were higher than each controls (P<0.05), except the 28% dietary protein levels, PR and FR values were not significantly different (P>0.05) with the control (feed 28% protein without rGH). TAN excretion was increased with increasing dietary protein levels, while rGH suplementation decreased TAN excretion (P<0.05), except at 28% test diet with rGH compared to without rGH supplementation.
The highest biomass gain was found in the 21% protein diet (214.88±12.31 g), which was 35.01% higher (P<0.05) than the control (159.17±13.92 g). The lowest biomass gain was found in the 34% protein diet (339.37±9.69 g), which was 16.90% higher (P<0.05) than the control (290.33±14.93 g). The highest biomass and SGR, and lowest FCR were obtained in the 34% protein diet and supplemented with rGH. Furthermore, biomass, SGR and FCR in the rGH supplemented and 28% protein diet was the same as in that of 34% protein diet without rGH supplementation (P>0.05). As conclusion, the rGH supplementation at a wet-based dose of 3 mg/kg of dietary protein levels could be increasing the growth and protein efficiency of giant gourami juvenile.
© Hak Cipta Milik IPB, Tahun 2014
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Ilmu Akuakultur
RESPONS PERTUMBUHAN BENIH IKAN GURAMI
(
Osphronemus goramy
) YANG DIBERI PAKAN DENGAN
KADAR PROTEIN BERBEDA DAN DIPERKAYA HORMON
PERTUMBUHAN REKOMBINAN
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2014
Judul Tesis : Respons Pertumbuhan Benih Ikan Gurami (Osphronemus goramy) yang Diberi Pakan dengan Kadar Protein Berbeda dan Diperkaya Hormon Pertumbuhan Rekombinan
Nama : Darmawan Setia Budi
NIM : C151120151
Disetujui oleh Komisi Pembimbing
Dr Alimuddin, SPi, MSc Ketua
Dr Ir Muhammad Agus Suprayudi, MSi Anggota
Diketahui oleh
Ketua Program Studi Ilmu Akuakultur
Dr Ir Widanarni, MSi
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala limpahan rahmat dan karunia-Nya sehingga tesis yang berjudul ”Respons Pertumbuhan Benih Ikan Gurami yang Diberi Pakan dengan Kadar Protein Berbeda dan Diperkaya Hormon Pertumbuhan Rekombinan” ini berhasil diselesaikan. Tesis ini bersumber pada hasil penelitian yang dilaksanakan sejak bulan Januari 2014 sampai April 2014 bertempat di Laboratorium Reproduksi dan Genetika Organisme Akuatik serta di Laboratorium Nutrisi Ikan, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Penulis menyadari bahwa selesainya tesis ini tidak lepas dari segala bantuan dan dukungan berbagai pihak, baik ide, pemikiran, tenaga, moril maupun material. Oleh karena itu penulis menyampaikan rasa terima kasih yang mendalam kepada Dr Alimuddin, SPi, MSc dan Dr Ir Muhammad Agus Suprayudi, MSi sebagai komisi pembimbing atas waktu dan bimbingannya mulai dari penyusunan proposal; pelaksanaan penelitian; hingga penulisan tesis. Penulis juga menyampaikan rasa terima kasih kepada Dr Ir Dinar Tri Soelistyowati, DEA sebagai dosen penguji luar komisi dan Dr Dinamella Wahjuningrum, SSi, MSi sebagai komisi program studi yang telah memberikan saran dan semangatnya dalam ujian sidang tesis ini.
Terima kasih disampaikan pada Direktorat Jendral Pendidikan Tinggi (DIKTI) Kementrian Pendidikan dan Kebudayaan (KEMENDIKBUD) atas penyediaan Beasiswa Pendidikan Pascasarjana Dalam Negeri (BPPDN) sehingga penulis dapat memperdalam ilmu di Sekolah Pascasarjana Institut Pertanian Bogor.
Terima kasih dan penghargaan yang tinggi penulis haturkan kepada ayahanda H Sudarmasto, SH dan Ibunda Dra Hj Titin Sukowati atas doa; bantuan; dukungan dan semangatnya. Kepada istri tercinta Nina Hakim Mardiana, SE atas doa; semangat; dan kasih sayangnya. Terima kasih kepada ayah mertua Aiptu Mangesti Budi Utomo dan ibu mertua Rimayati atas segala semangat dan doa yang diberikan. Kepada kakak Yunia Larasati, SPi dan adik Ajeng Kusumawardhani, SPi; kepada kakak ipar Yus Imron Rosyadi, ST; Nani Hakim Mariana, SE; serta Taupan, SE; dan seluruh keluarga besar di Lumajang; terima kasih untuk semua cinta dan perhatiannya.
Terima kasih kepada seluruh rekan-rekan S2 Ilmu Akuakultur angkatan 2012 atas kebersamaannya dalam menempuh studi. Kepada rekan-rekan Laboratorium Fisiologi Reproduksi Ikan: Fajar Maulana, SPi; Deny Wahyudi, SPi; Rangga Garnama, SPi; Anna Octavera, SPi, MSi; Ir Muhammad, MSi; Ir Suci Antoro, MSc; serta adik-adik S1 atas kebersamaan dan kerjasamanya selama penelitian.
Akhir kata, semoga karya ilmiah ini bermanfaat untuk kemajuan ilmu pengetahuan umumnya dan perikanan khususnya.
Bogor, 29 Agustus 2014
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vii
1 PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 3
Manfaat Penelitian 3
2 METODE 3
Produksi rGH 3
Pakan Uji 3
Pemeliharaan 3
Parameter Uji 4
Analisis statistik 7
3 HASIL DAN PEMBAHASAN 7
Hasil 7
Pembahasan 13
4 KESIMPULAN DAN SARAN 16
Kesimpulan 16
Saran 16
DAFTAR PUSTAKA 17
LAMPIRAN 21
DAFTAR TABEL
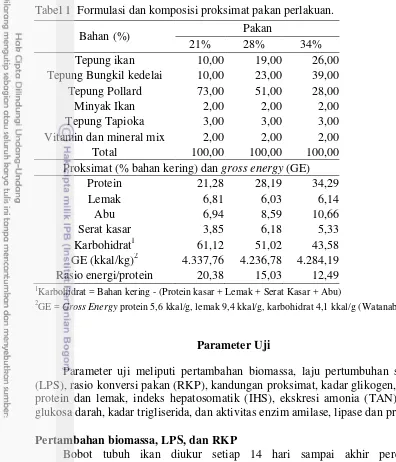
1 Formulasi dan komposisi proksimat pakan perlakuan 4 2 Pertambahan biomassa (g), laju pertumbuhan spesifik (LPS, %),
jumlah konsumsi pakan (JKP, g), dan rasio konversi pakan (RKP) benih ikan gurami yang diberi pakan perlakuan hormon
pertumbuhan rekombinan 8
3 Kadar protein dan lemak tubuh (% basah), serta retensi protein (RP, %) dan lemak (RL, %) benih ikan gurami yang diberi perlakuan
hormon pertumbuhan rekombinan 9
DAFTAR GAMBAR
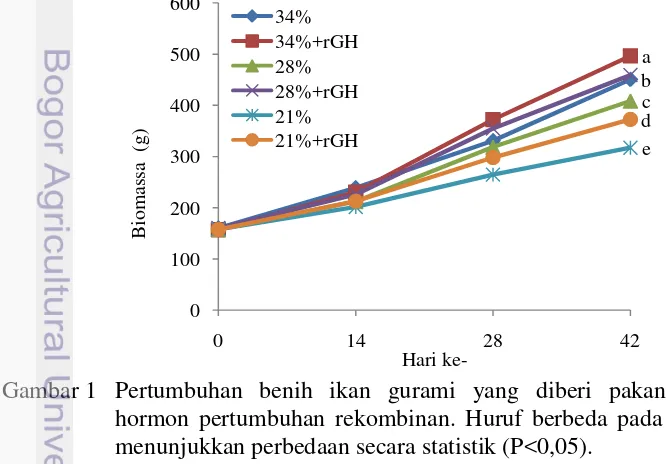
1 Pertumbuhan benih ikan gurami yang diberi perlakuan hormon pertumbuhan rekombinan. Huruf berbeda pada akhir garis
menunjukkan perbedaan secara statistik antar perlakuan (P<0,05) 8 2 Indeks hepatosomatik (IHS) benih ikan gurami yang diberi
perlakuan hormon pertumbuhan rekombinan. Huruf berbeda pada akhir garis menunjukkan perbedaan secara statistik antar perlakuan
(P<0,05) 9
3 Ekskresi total amonia nitrogen (TAN) benih ikan gurami yang diberi perlakuan hormon pertumbuhan rekombinan. Huruf berbeda pada akhir garis menunjukkan perbedaan secara statistik antar perlakuan
(P<0,05) 10
4 Kadar glukosa darah (a) dan trigliserida darah (b) benih ikan gurami yang diberi perlakuan hormon pertumbuhan rekombinan. Huruf berbeda pada akhir garis menunjukkan perbedaan secara statistik
antar perlakuan (P<0,05) 11
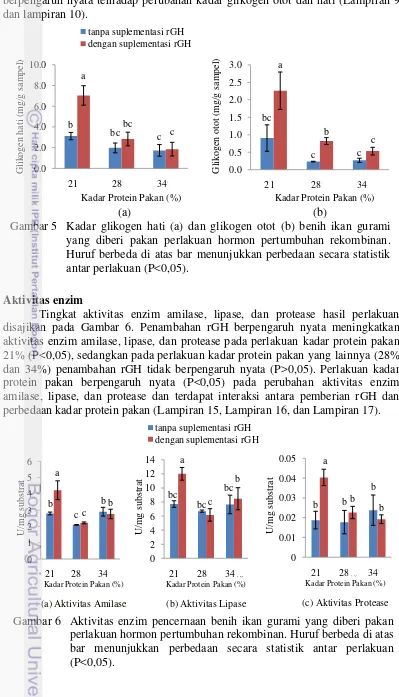
5 Kadar glikogen hati (a) dan glikogen otot (b) benih ikan gurami yang diberi perlakuan hormon pertumbuhan rekombinan. Huruf berbeda pada akhir garis menunjukkan perbedaan secara statistik antar
perlakuan (P<0,05) 12
6 Aktivitas enzim pencernaan benih ikan gurami yang diberi perlakuan hormon pertumbuhan rekombinan. Huruf berbeda pada akhir garis
DAFTAR LAMPIRAN
1 ANOVA dan Uji-Duncan pertambahan biomassa benih ikan gurami
yang diberi perlakuan hormon pertumbuhan rekombinan 21 2 ANOVA dan Uji-Duncan laju pertumbuhan spesifik (LPS) benih
ikan gurami yang diberi perlakuan hormon pertumbuhan rekombinan 22 3 ANOVA dan Uji-Duncan rasio konversi pakan (RKP) benih ikan
gurami yang diberi perlakuan hormon pertumbuhan rekombinan 23 4 ANOVA dan Uji-Duncan jumlah konsumsi pakan (JKP) benih ikan
gurami yang diberi perlakuan hormon pertumbuhan rekombinan 24 5 ANOVA dan Uji-Duncan indeks hepatosomatik (IHS) benih ikan
gurami yang diberi perlakuan hormon pertumbuhan rekombinan 25 6 ANOVA dan Uji-Duncan ekskresi total amonia nitrogen (TAN)
benih ikan gurami yang diberi perlakuan hormon pertumbuhan
rekombinan 26
7 ANOVA dan Uji-Duncan kadar glukosa darah benih ikan gurami
yang diberi perlakuan hormon pertumbuhan rekombinan 27 8 ANOVA dan Uji-Duncan kadar trigliserida darah benih ikan gurami
yang diberi perlakuan hormon pertumbuhan rekombinan 28 9 ANOVA dan Uji-Duncan kadar gilkogen hati benih ikan gurami
yang diberi perlakuan hormon pertumbuhan rekombinan 29 10 ANOVA dan Uji-Duncan kadar glikogen otot benih ikan gurami
yang diberi perlakuan hormon pertumbuhan rekombinan 30 11 ANOVA dan Uji-Duncan kadar lemak tubuh benih ikan gurami yang
diberi perlakuan hormon pertumbuhan rekombinan 31 12 ANOVA dan Uji-Duncan retensi lemak benih ikan gurami yang
diberi perlakuan hormon pertumbuhan rekombinan 32 13 ANOVA dan Uji-Duncan kadar protein tubuh benih ikan gurami
yang diberi perlakuan hormon pertumbuhan rekombinan 33 14 ANOVA dan Uji-Duncan retensi protein benih ikan gurami yang
diberi perlakuan hormon pertumbuhan rekombinan 34 15 ANOVA dan Uji-Duncan aktivitas enzim amilase benih ikan gurami
yang diberi perlakuan hormon pertumbuhan rekombinan 35 16 ANOVA dan Uji-Duncan aktivitas enzim lipase benih ikan gurami
yang diberi perlakuan hormon pertumbuhan rekombinan 36 17 ANOVA dan Uji-Duncan aktivitas enzim protease benih ikan gurami
1
PENDAHULUAN
Latar Belakang
Ikan gurami merupakan ikan ekonomis yang menjadi salah satu komoditas utama perikanan budidaya di Indonesia. Ikan gurami memiliki laju pertumbuhan yang relatif lambat, pada pembesaran tahap pertama dengan pakan berkadar protein 20-26%, untuk mencapai ukuran sebesar 200 g/ekor dari ukuran 15 g/ekor dibutuhkan waktu 120 hari; dan pembesaran tahap ke dua dari ukuran 200 g/ekor hingga ukuran konsumsi sebesar 500 g/ekor dibutuhkan waktu 150 hari (SNI 2006). Hal ini tentunya dapat menjadi kendala terhadap upaya peningkatan produksi ikan gurami nasional. Upaya peningkatan laju pertumbuhan ikan dapat dilakukan dengan berbagai macam cara, alternatif metode mudah dan cepat yang dapat digunakan untuk meningkatkan pertumbuhan ikan gurami adalah aplikasi hormon pertumbuhan rekombinan (recombinant growth hormone, rGH). Aplikasi rGH merupakan penerapan dari teknologi protein rekombinan, yaitu teknologi untuk menghasilkan protein yang bermanfaat secara massal dengan menggunakan bakteri, ragi, atau sel kultur sebagai media perbanyakan (Demain & Vaishnav 2009). Aplikasi rGH telah terbukti dapat meningkatkan pertumbuhan beberapa spesies ikan, di antaranya adalah ikan black seabream (Spondyliosoma cantharus) (Tsai et al. 1997), ikan beronang (Siganus guttatus) (Funkenstein et al. 2005), ikan gold fish (Carassius aurata) (Promdonkoy et al. 2004), ikan nila (Oreochromis niloticus) (Acosta et al. 2007), dan udang vaname (Litopenaeus vannamei) (Subaidah 2013). Penelitian rGH pada ikan gurami telah menghasilkan peningkatan laju pertumbuhan yang cukup signifikan (Irmawati 2013).
Pemberian rGH dapat dilakukan melalui pakan (Moriyama et al. 1993), penyuntikan/injeksi (Promdonkoy et al. 2004), dan melalui perendaman/imersi (Acosta et al. 2007). Aplikasi rGH melalui pakan, di Indonesia, telah dilakukan pada beberapa spesies ikan, di antaranya adalah ikan sidat (Handoyo 2012), ikan nila (Latar 2013), dan udang vaname (Subaidah 2013). Sementara itu pada ikan gurami, pemberian rGH melalui pakan dengan dosis kering 3 mg/kg pakan menghasilkan pertumbuhan yang lebih tinggi dibandingkan kontrol (Safir 2012). Pengaruh pemberian rGH secara oral melalui pakan dengan kadar protein yang berbeda belum diketahui.
2
sparring effect) sehingga dapat meningkatkan fungsi protein dalam menunjang pertumbuhan ikan (Hasan & Khan 2013).
Penelitian tentang kebutuhan energi total, rasio energi/protein pada ikan gurami telah dilakukan. Hasil penelitian tersebut menunjukkan bahwa larva ikan gurami berukuran 0,1-0,7 g membutuhkan kadar protein pakan sebesar 43,29% dengan rasio E/P 8,0 kkal DE/g protein (Mokoginta et al. 1995), sedangkan untuk ikan gurami berukuran 25-30 g membutuhkan kadar protein sebesar 32,14% dengan rasio E/P 8 kkal DE/g protein (Suprayudi et al. 1994).
Secara umum pemberian rGH eksogen meningkatkan kapasitas metabolisme ikan gurami, khususnya metabolisme lemak serta optimasi sintesis dan pemanfaatan protein untuk pertumbuhan pada benih ikan gurami (Irmawati 2013). GH memiliki peran dalam proses pencernaan, penyerapan dan pengangkutan nutrisi pada ikan transgenik (Fu et al. 1998; Cook et al. 2000; Devlin et al. 2004). Pemberian rGH dapat menurunkan kadar lemak dan meningkatkan sintesis protein di dalam tubuh, kandungan lemak yang lebih rendah pada ikan yang laju pertumbuhannya lebih cepat menunjukkan protein sparring effect yang terjadi seiring dengan meningkatnya level GH (Rasmussen et al. 2001). Penurunan kandungan lemak pada ikan gurami yang diberi perlakuan rGH melalui metode perendaman terkait dengan aktivitas enzim lipase (Irmawati 2013). Pada penelitian ini, dilakukan pemberian rGH untuk mengevaluasi respons fisiologi ikan gurami yang diberi pakan dengan kadar protein berbeda.
Perumusan Masalah
Ikan gurami memiliki laju pertumbuhan yang relatif lambat. Aplikasi rGH melalui pakan dengan dosis kering 3 mg/kg pakan menghasilkan peningkatan pertumbuhan sebesar 46,76 % dibandingkan dengan kontrol (Safir 2012). Pemberian rGH dapat menurunkan kadar lemak dan meningkatkan sintesis protein di dalam tubuh. Kandungan lemak yang lebih rendah pada ikan yang laju pertumbuhannya lebih cepat menunjukkan terjadinya protein sparring effect seiring dengan meningkatnya level GH (Rasmussen et al. 2001). Secara umum pemberian rGH eksogen meningkatkan kapasitas metabolisme ikan gurami, khususnya metabolisme lemak serta optimasi sintesis dan pemanfaatan protein untuk pertumbuhan pada benih ikan gurami (Irmawati 2013). Penambahan nutrien non-protein sebagai penghasil energi dapat menurunkan penggunaan protein sebagai sumber energi (protein sparring effect) sehingga dapat meningkatkan fungsi protein dalam menunjang pertumbuhan ikan (Hasan & Khan 2013).
3
Tujuan Penelitian
Tujuan penelitian ini adalah untuk menguji efek pemberian pakan dengan kadar protein berbeda yang diperkaya dengan rGH terhadap respons pertumbuhan benih ikan gurami.
Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini yaitu diperoleh data dasar mengenai aplikasi rGH melalui pakan dengan kadar protein berbeda dalam rangka peningkatan efisiensi pakan.
2
METODE
Produksi rGH
Produksi rGH dilakukan dengan menggunakan bakteri Escherichia coli BL21 yang mengandung konstruksi vektor ekspresi pCold-1/rElGH. Metode kultur bakteri dan metode koleksi rGH dilakukan seperti dijelaskan Alimuddin et al. (2010). Pelet rGH dicuci dengan bufer fosfat salin (PBS) sebanyak 1 kali, dan rGH disimpan pada suhu -80˚C hingga akan digunakan.
Pakan Uji
Pakan uji yang digunakan memiliki kadar kering protein 34%, 28%, dan 21%. Pakan yang digunakan isoenergi, sekitar 4.200 kkal GE/kg pakan. Formulasi dan komposisi pakan dapat dilihat pada Tabel 1. Pakan disemprot dengan rGH yang disalut dengan 20 mg kuning telur ayam dengan dosis basah 3 mg rGH/kg pakan (Safir 2012). Tiap perlakuan pakan memiliki kontrol tanpa penambahan rGH. Setiap perlakuan dan kontrol diberi ulangan sebanyak 3 kali.
Pemeliharaan
4
Parameter Uji
Parameter uji meliputi pertambahan biomassa, laju pertumbuhan spesifik (LPS), rasio konversi pakan (RKP), kandungan proksimat, kadar glikogen, retensi protein dan lemak, indeks hepatosomatik (IHS), ekskresi amonia (TAN), kadar glukosa darah, kadar trigliserida, dan aktivitas enzim amilase, lipase dan protease.
Pertambahan biomassa, LPS, dan RKP
Bobot tubuh ikan diukur setiap 14 hari sampai akhir percobaan. Pertambahan biomassa dihitung berdasarkan persamaan:
Pertambahan biomassa = Bt−B0
Keterangan:
Bt = Biomassa pada akhir perlakuan (g) B0 = Biomassa pada awal perlakuan (g)
Laju pertumbuhan spesifik (LPS) ikan uji dihitung berdasarkan persamaan yang dikemukakan oleh Huisman (1987), yaitu:
LPS = Wt
W0
t
−1 100
Keterangan:
LPS= Laju pertumbuhan spesifik
Wt = Rata-rata bobot individu pada waktu akhir pemeliharaan (g) W0 = Rata-rata bobot individu pada waktu awal pemeliharaan (g) Tabel 1 Formulasi dan komposisi proksimat pakan perlakuan.
Bahan (%) Pakan
Proksimat (% bahan kering) dan gross energy (GE)
Protein 21,28 28,19 34,29 Rasio energi/protein 20,38 15,03 12,49
1
Karbohidrat = Bahan kering - (Protein kasar + Lemak + Serat Kasar + Abu)
2
5 t = Lama waktu pemeliharaan (hari)
Rasio konversi pakan (RKP) dihitung dengan menggunakan persamaan yang dikemukakan oleh Guillaume et al. (1999), yaitu:
RKP = P
Wt + Wm −W0100
Keterangan:
RKP = Rasio konversi pakan
P = Jumlah pakan yang diberikan selama pemeliharaan (g) Wt = Biomassa ikan pada waktu akhir pemeliharaan (g) W0 = Biomassa ikan pada awal pemeliharaan (g)
Wm = Bobot ikan yang mati selama pemeliharaan (g)
Pengukuran indeks hepatosomatik (IHS)
Tiga ikan dari setiap perlakuan diambil secara acak pada akhir percobaan. IHS diukur dengan menimbang bobot hati dibandingkan dengan bobot tubuh ikan gurami hasil perlakuan. IHS dihitung berdasarkan persamaan yang dikemukakan oleh Yang et al. (2002), yaitu:
IHS(%) = bobot organ hati (g)
bobot tubuh ikan (g)100
Analisis proksimat
Analisis proksimat dilakukan terhadap bahan baku pakan, pakan, dan ikan uji. Analisis proksimat untuk kadar air menggunakan metode pemanasan dalam oven bersuhu 105-110˚C; serat kasar menggunakan metode pelarutan contoh dengan asam kuat, basa kuat, dan pemanasan; protein kasar menggunakan metode Kjeldahl; lemak kering dengan menggunakan metode Soxchlet; lemak basah dengan menggunakan metode Folch; kadar abu dengan pemanasan dalam tanur bersuhu 600oC (Watanabe 1988).
Retensi protein dan retensi lemak
Nilai retensi protein dihitung berdasarkan persamaan (Takeuchi 1988):
RP =F−I
P 100
Keterangan :
RP = Retensi protein (%)
F = Kandungan protein tubuh pada akhir percobaan (g) I = Kandungan protein tubuh pada awal percobaan (g) P = Jumlah protein yang dikonsumsi (g)
Nilai retensi lemak dihitung berdasarkan persamaan (Takeuchi 1988):
RL =F−I
L 100
Keterangan :
RL = Retensi lemak (%)
6
Analisis ekskresi total amonia nitrogen (TAN)
Analisis ekskresi TAN ditentukan dengan mengukur jumlah total amonia nitrogen (TAN) dalam media pemeliharaan menggunakan test kit NH3/NH4+ (API
©Mars Fishcare North America Inc, USA). Pengukuran awal dilakukan setelah ikan dipuasakan selama 24 jam dan akuarium diisi dengan air yang baru (0,19±0,08 mg TAN/L). Pengukuran dilakukan 24 jam setelah ikan diberi makan dengan kenyang. TAN dihitung untuk setiap unit pakan yang dikonsumsi per biomassa ikan (mg TAN/g pakan/g ikan), diadopsi dari Handoyo (2013).
Analisis kadar glukosa dan trigliserida darah
Tiga ikan dari setiap perlakuan diambil secara acak pada akhir penelitian. Kadar glukosa diukur dengan metode uji enzimatik kolorimetri dengan uji GLUKOSA liquicolor menggunakan test kit Human mbH, Jerman (Trinder 1969) . Kadar trigliserida diukur dengan metode uji enzimatik kolorimetri menggunakan uji untuk trigliserida dengan lemak clearing factor (LCF) menggunakan liquicolormono TRIGLYCERIDES dengan test kit Human mbH, Jerman (Jacobs &
Vandemark 1960).
Pengukuran aktivitas enzim
Pengukuran aktivitas enzim pencernaan (protease, amilase, dan lipase) dilakukan pada akhir penelitian. Pada setiap kali pengukuran aktivitas enzim, 3 ekor sampel ikan diambil secara acak dari setiap perlakuan dan ditimbang bobot tubuhnya.
Pengukuran aktivitas enzim pencernaan dari saluran pencernaan ikan dilakukan dengan cara memisahkan bagian tubuh ikan dengan organ pencernaan (usus). Hasil homogenasi usus ikan dengan akuades hingga sepuluh kali bobot contoh diperoleh ekstrak enzim kasar. Ekstrak enzim ini selanjutnya disimpan dalam lemari pendingin (suhu -20˚C) sampai pengujian aktivitas enzim dilakukan.
Pengukuran aktivitas enzim protease berpedoman pada metode Bergmeyer dan Grassi (1983). Substrat yang digunakan dalam pengukuran aktivitas enzim adalah kasein. Tirosin digunakan sebagai standar. Satu unit enzim protease didefinisikan sebagai 1 mg tirosin yang dibebaskan dalam 10 menit pada suhu 37˚C.
Pengukuran aktivitas enzim amilase dilakukan dengan menggunakan metode Worthington (1993). Substrat yang digunakan dalam pengukuran amilase adalah pati. Maltosa digunakan sebagai standar. Satu unit amilase didefinisikan sebagai 1 mg maltose yang dibebaskan dari pati dalam waktu 3 menit pada suhu 95˚C; pH 6,9.
7 asam lemak yang dilepaskan selama 6 jam inkubasi dengan substrat dan setelah dikoreksi dengan blanko.
Analisis kadar glikogen hati dan otot
Pengukuran kadar glikogen hati dan otot dilakukan untuk mengevaluasi pengaruh pemberian rGH terhadap metabolisme karbohidrat dalam hal mobilitas glikogen di dalam tubuh. Pengukuran glikogen hati dan otot dilakukan pada akhir penelitian dengan menggunakan 3 ekor ikan yang diambil secara acak dari tiap perlakuan. Analisis kadar glikogen hati dan otot ikan gurami mengacu pada metode Wedemeyer dan Yasutake (1977). Jaringan otot atau hati sekitar 100 mg dididihkan dalam 3 mL KOH 30% hingga larut (selama 20 sampai 30 menit), kemudian ditambahkan 0,5 mL Na2SO4 jenuh dan 3,5 mL etanol95%, selanjutnya dipanaskan sampai mendidih. Setelah dingin, larutan disentrifugasi dan supernatannya dibuang. Glikogen dilarutkan dalam 2 mL air dan diendapkan kembali dengan 2,5 mL etanol 95%. Supernatan dibuang dan glikogen yang mengendap dihidrolisis dengan 2 mL HCl 5 M selama 30 menit dalam waterbath mendidih. Sampel didinginkan dan dinetralkan menggunakan 0,5 M NaOH (digunakan 1 tetes fenolred sebagai indikator). Sampel diencerkan sampai volume yang diketahui (50-100 mL), bergantung pada glikogen yang diharapkan dan selanjutnya kadar glikogen diukur berdasarkan nilai absorbansi spektrofotometer pada panjang gelombang 620 nm.
Analisis statistik
Semua data dianalisis dengan tabel sidik ragam menggunakan software statistik SPSS 17.0 pada P<0,05. Jika hasil yang diperoleh terdapat perbedaan antara perlakuan yang diberikan, maka dilanjutkan dengan uji Duncan.
3
HASIL DAN PEMBAHASAN
Hasil
Pertambahan biomassa, laju pertumbuhan spesifik (LPS), dan rasio konversi pakan (RKP)
8
Respons pertambahan biomassa, LPS, dan RKP menunjukkan tidak ada interaksi (P>0,05) antara kadar protein pakan dan suplementasi rGH.
Sementara itu, Nilai jumlah konsumsi pakan (JKP) berbanding terbalik dengan RKP (Tabel 2). Konsumsi pakan tertinggi terjadi pada perlakuan pakan berkadar protein 34% dengan penambahan rGH, sedangkan konsumsi pakan terendah terjadi pada perlakuan pakan berkadar protein 21% tanpa penambahan rGH. Kedua faktor perlakuan, kadar protein pakan dan suplementasi rGH, berpengaruh nyata (P<0,05) terhadap peningkatan JKP benih ikan gurami. Hasil analisis statistik menunjukkan tidak adanya interaksi (P>0,05) dari kedua faktor perlakuan tersebut terhadap JKP. Selama 42 hari pemeliharaan kelangsungan hidup ikan uji pada semua perlakuan mencapai 100%.
Tabel 2 Pertambahan biomassa (g), laju pertumbuhan spesifik (LPS, %), jumlah konsumsi pakan (JKP, g), dan rasio konversi pakan (RKP) benih ikan gurami yang diberi pakan perlakuan hormon pertumbuhan rekombinan. Perlakuan Pakan
159,17±13,92e** 1,56±0,13e 301,54±40,44c 1,89±0,09a
rGH 214,88±12,31d 1,93±0,05d 356,86±39,10abc 1,66±0,09b
28% Non rGH 250,36±11,59
c
2,13±0,08c 338,70±13,48bc 1,35±0,04c
rGH 298,88±10,54b 2,37±0,04b 399,59±41,53ab 1,34±0,10c
34% Non rGH 290,33±14,93
b
2,32±0,06b 392,14±17,00ab 1,35±0,02c
rGH 339,37±9,69a 2,59±0,03a 405,95±27,419a 1,20±0,05d
Two-way ANOVA
Protein Pakan (P) P<0,000 P<0,000 P<0,009 P<0,000
rGH (R) P<0,000 P<0,000 P<0,014 P<0,001
PxR (Interaksi) P<0,854 P<0,262 P<0,407 P<0,064
Standard Error 2,898 0,017 7,544 0,017
*
Non rGH: pakan kontrol tanpa diperkaya rGH;
**Huruf superskrip yang berbeda pada kolom yang sama menunjukkan secara statistik beda nyata antar perlakuan (P<0,05).
Gambar 1 Pertumbuhan benih ikan gurami yang diberi pakan perlakuan hormon pertumbuhan rekombinan. Huruf berbeda pada akhir garis menunjukkan perbedaan secara statistik (P<0,05).
9
Indeks hepatosomatik (IHS)
Nilai IHS hasil perlakuan dapat dilihat pada Gambar 2. Nilai IHS berbanding terbalik dengan kadar protein pakan, sedangkan penambahan rGH secara signifikan (P<0,05) meningkatkan nilai IHS pada setiap perlakuan kadar protein pakan. Nilai IHS pada pakan berprotein 28% tanpa penambahan rGH tidak berbeda (P>0,05) dengan pakan berprotein 34% dengan penambahan rGH. Tidak ada interaksi (P>0,05) antara kadar protein pakan dan penambahan rGH terhadap IHS (Lampiran 5).
Retensi protein dan retensi lemak
Kadar protein dan lemak tubuh, serta retensi protein (RP) dan lemak ikan (RL) hasil perlakuan disajikan pada Tabel 3. Kedua faktor perlakuan, kadar
Gambar 2 Indeks hepatosomatik (IHS) benih ikan gurami yang diberi pakan perlakuan hormon pertumbuhan rekombinan. Huruf berbeda di atas bar menunjukkan perbedaan secara statistik perlakuan (P<0,05).
b
tanpa suplementasi rGH dengan suplementasi rGH
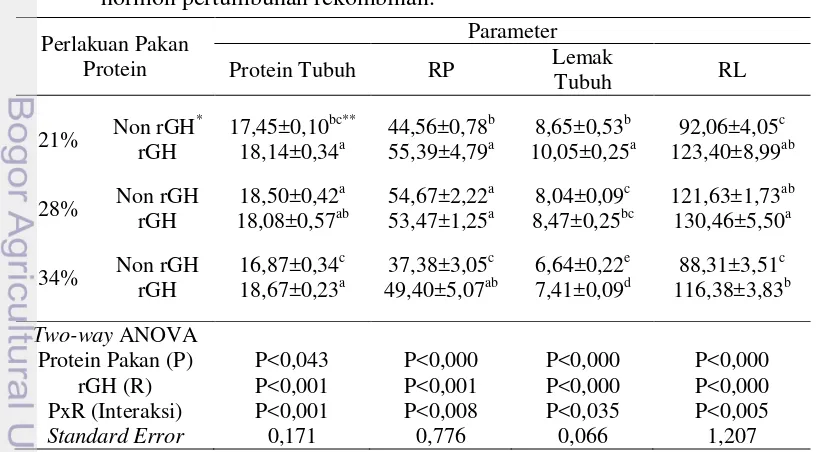
Tabel 3 Kadar protein dan lemak tubuh (% basah), serta retensi protein (RP, %) dan lemak (RL, %) benih ikan gurami yang diberi pakan perlakuan
17,45±0,10bc** 44,56±0,78b 8,65±0,53b 92,06±4,05c
rGH 18,14±0,34a 55,39±4,79a 10,05±0,25a 123,40±8,99ab
28% Non rGH 18,50±0,42
a
54,67±2,22a 8,04±0,09c 121,63±1,73ab
rGH 18,08±0,57ab 53,47±1,25a 8,47±0,25bc 130,46±5,50a
34% Non rGH 16,87±0,34
c
37,38±3,05c 6,64±0,22e 88,31±3,51c
rGH 18,67±0,23a 49,40±5,07ab 7,41±0,09d 116,38±3,83b
Two-way ANOVA
Protein Pakan (P) P<0,043 P<0,000 P<0,000 P<0,000
rGH (R) P<0,001 P<0,001 P<0,000 P<0,000
PxR (Interaksi) P<0,001 P<0,008 P<0,035 P<0,005
Standard Error 0,171 0,776 0,066 1,207
*
Non rGH: pakan kontrol tanpa diperkaya rGH;
10
protein pakan dan suplementasi rGH, berpengaruh nyata (P<0,05) terhadap kadar protein dan lemak tubuh, serta RP dan RL ikan hasil perlakuan. Hasil analisis statistik menunjukkan adanya interaksi (P<0,05) dari kedua faktor perlakuan tersebut pada semua parameter (kadar protein tubuh, kadar lemak, RP, dan RL). Nilai RP dan RL pada tiap level protein pakan lebih tinggi (P<0,05) dibandingkan dengan masing-masing kontrolnya, kecuali pada pakan berkadar 28% yang nilai RP dan RL tidak berbeda nyata (P>0,05) dengan kontrolnya (pakan berprotein 28% tanpa rGH).
Ekskresi total amonia nitrogen(TAN)
Ekskresi TAN hasil perlakuan dapat dilihat pada Gambar 3. Ekskresi TAN meningkat dengan meningkatnya kadar protein pakan. Penambahan rGH secara signifikan menurunkan ekskresi TAN (P<0,05), kecuali pada pakan berprotein 28% yang tidak berbeda (P>0,05) dengan kontrolnya (tanpa penambahan rGH). Tidak ada interaksi antara kadar protein pakan dan penambahan rGH terhadap ekskresi TAN (P>0,05) (Lampiran 6). Selanjutnya, ekskresi TAN pada perlakuan pakan berprotein 28% dengan penambahan rGH tidak berbeda (P>0,05) dengan perlakuan pakan berprotein 34% tanpa penambahan rGH, sedangkan ekskresi TAN pada pakan berprotein 21% dengan penambahan rGH tidak berbeda (P>0,05) dengan perlakuan pakan berprotein 28% tanpa penambahan rGH. Ekskresi TAN terendah terjadi pada pakan berprotein 21% dengan penambahan rGH; 40,11% lebih rendah (P<0,05) dibandingkan kontrol. Perlakuan pakan berprotein 34%; menghasilkan ekskresi TAN 22,16% lebih rendah (P<0,05) dibandingkan kontrol (tanpa penambahan rGH).
Kadar glukosa dan trigliserida darah
Kadar glukosa dan trigliserida darah ditampilkan pada Gambar 4. Penambahan rGH secara signifikan (P<0,05) meningkatkan kadar glukosa darah pada tiap perlakuan kadar protein pakan, namun kadar protein pakan tidak memberikan pengaruh terhadap kadar glukosa (P>0,05). Selanjutnya, tidak ada
11 interaksi (P>0,05) antara kadar protein pakan dan penambahan rGH (Lampiran 7). Kadar glukosa darah pada perlakuan pakan yang diberi rGH (60,67-63,17 mg/dL) lebih tinggi 20,67% dari kontrol (50,00-54,00 mg/dL) (Gambar 4a). Di sisi lain, kadar trigliserida darah pada semua perlakuan tidak berbeda nyata (P>0,05), kecuali perlakuan pakan berprotein 21% tanpa penambahan rGH (185,79±54,64 mg/dL) lebih rendah (P<0,05) dari semua perlakuan (361,75±49,18 sampai 427,87±26,78 mg/dL). Pemberian rGH dan perbedaan kadar protein pakan saling berinteraksi dan berpengaruh nyata terhadap perubahan kadar trigliserida darah (Lampiran 8).
Glikogen hati dan otot
Kadar glikogen hati dan otot hasil perlakuan disajikan pada Gambar 5. Peningkatan kadar protein pakan berpengaruh nyata (P<0,05) terhadap penurunan kadar glikogen hati. Sementara itu penambahan rGH berpengaruh nyata (P<0,05) meningkatkan kadar glikogen hati pada perlakuan pakan berprotein 21%. Kadar glikogen hati tertinggi terjadi pada perlakuan pakan berprotein 21% dengan penambahan rGH (7,04±0,93 mg/g sampel), sedangkan kadar glikogen hati terendah terjadi pada perlakuan pakan berkadar protein 34% tanpa penambahan rGH (1,74±0,56 mg/g sampel) (Gambar 5a).
Peningkatan kadar protein pakan berpengaruh nyata (P<0,05) terhadap penurunan kadar glikogen otot. Sementara itu penambahan rGH menyebabkan terjadinya peningkatan kadar glikogen otot pada perlakuan pakan berprotein 21% dan 28% (P<0,05), sedangkan pada perlakuan pakan berprotein 34% pemberian rGH tidak berpengaruh nyata (P>0,05). Kadar glikogen otot tertinggi terjadi pada perlakuan pakan berprotein 21% diperkaya rGH (2,26±0,53 mg/g sampel), sedangkan kadar glikogen hati terendah terjadi pada perlakuan pakan berkadar protein 28% tanpa penambahan rGH (0,23±0,01 mg/g sampel) (Gambar 5b). Pemberian rGH dan perbedaan kadar protein pakan saling berinteraksi dan
(a) (b)
Gambar 4 Kadar glukosa darah (a) dan trigliserida darah (b) benih ikan gurami yang diberi pakan perlakuan hormon pertumbuhan rekombinan. Huruf berbeda di atas bar menunjukkan perbedaan secara statistik antar perlakuan (P<0,05).
12
berpengaruh nyata terhadap perubahan kadar glikogen otot dan hati (Lampiran 9 dan lampiran 10).
Aktivitas enzim
Tingkat aktivitas enzim amilase, lipase, dan protease hasil perlakuan disajikan pada Gambar 6. Penambahan rGH berpengaruh nyata meningkatkan aktivitas enzim amilase, lipase, dan protease pada perlakuan kadar protein pakan 21% (P<0,05), sedangkan pada perlakuan kadar protein pakan yang lainnya (28% dan 34%) penambahan rGH tidak berpengaruh nyata (P>0,05). Perlakuan kadar protein pakan berpengaruh nyata (P<0,05) pada perubahan aktivitas enzim amilase, lipase, dan protease dan terdapat interaksi antara pemberian rGH dan perbedaan kadar protein pakan (Lampiran 15, Lampiran 16, dan Lampiran 17).
13
Pembahasan
Pemberian rGH mempengaruhi nafsu makan ikan terhadap pakan perlakuan. Penambahan rGH menyebabkan peningkatan nafsu makan ikan yang ditunjukkan dengan peningkatan jumlah konsumsi pakan (P<0,05; Tabel 2). Peningkatan nafsu makan ikan diduga dipengaruhi oleh peningkatan hormon ghrelin yang diinduksi hormon pertumbuhan (Volkoff et al. 2005; Debnanth 2010). Selain itu jumlah konsumsi pakan juga dipengaruhi oleh palatabilitas pakan yang terkait dengan peningkatan kadar protein pakan (P<0,05; Tabel 2). Kadar protein pakan sangat menentukan jumlah asam amino yang terkandung di dalamnya. Palatabilitas pakan berhubungan erat dengan atraktabilitas yang selanjutnya akan mempengaruhi respons pencarian; pengambilan dan penelanan (akseptabilitas) yang berhubungan dengan kandungan nutrien terutama beberapa asam amino bebas seperti glisin, alanin, dan betain; serta energi pakan (Suprayudi et al. 1999; Shamushaki et al. 2007).
Jumlah kosumsi pakan akan mempengaruhi kerja enzim pencernaan. Secara langsung aktivitas enzim pencernaan dipengaruhi oleh substrat (Eusobio & Coloso 2002) dan dipengaruhi oleh rGH secara tidak langung (Debhnant et al. 2010; Mataruga et al. 2012; Irmawati 2013). Pada penelitian ini terlihat bahwa pemberian rGH dan kadar protein pakan memicu aktivitas enzim pencernaan pada ikan uji (Gambar 6). Peningkatan aktivitas enzim pencernaan ini diduga akibat hormon pertumbuhan yang menginduksi hormon ghrelin (Debhnant et al. 2010) yang akan meningkatkan konsumsi pakan sehingga dapat menginduksi aktivitas enzim pencernaan. Hal ini sejalan dengan yang dilaporkan Mataruga et al. (2012), bahwa pemberian ghrelin dapat meningkatkan aktivitas enzim-enzim pencernaan pada serangga (Lymantria dispar). Sementara itu, aktivitas enzim pencernaan baik amilase, protease dan lipase juga dipengaruhi oleh keberadaan substrat dan kompensasi untuk memaksimalkan pemanfaatan nutrien yang jumlahnya terbatas pada saluran pencernaan ikan (Eusobio & Coloso 2002; Krogdahl et al. 2003). Hasil penelitian ini sejalan dengan pendapat tersebut di atas yakni terlihat kecenderungan bahwa pakan berkadar protein yang lebih rendah memiliki aktivitas enzim protease, amilase dan lipase yang sama dibandingkan dengan perlakuan lainnya; pemberian rGH memberikan efek peningkatan aktivitas enzim pada pakan berprotein 21% (Gambar 6). Perubahan aktivitas enzim akibat perbedaan kadar protein pakan dan penambahan rGH berdampak pada metabolisme yang ditunjukkan oleh perubahan kadar glukosa dan trigliserida darah, kadar glikogen hati dan otot, retensi lemak dan protein, ekskresi TAN, indeks hepatosomatik yang selanjutnya berdampak pada laju pertumbuhan dan pertambahan biomassa ikan yang diuji.
14
trigliserida. Peningkatan kadar trigliserida akibat pemberian rGH juga terjadi, terutama pada perlakuan pakan berprotein 21% (Gambar 4b). Tingginya kadar trigliserida setelah ikan dipuasakan selama 24 jam dikarenakan sintesis endogen trigliserida yang berasal dari glukosa (lipogenesis) hasil dari mobilisasi glikogen hati dan asam lemak bebas yang diangkut dari jaringan adiposa ke hati (Groff & Gropper 2000).
Sementara itu, peningkatan kadar glikogen pada hati diduga menyebabkan peningkatan volume hati ikan uji (Gambar 2 dan Gambar 5). Hal ini sejalan dengan Yang et al. (2002) bahwa kenaikan IHS terjadi karena akumulasi glikogen dalam hati pada ikan silver perch (Bidyanus bidyanus). Selain itu, peningkatan IHS erat juga kaitannya dengan peningkatan kadar lemak tubuh ikan uji (Gambar 2 dan Tabel 3), di mana nilai IHS dan kadar lemak tubuh tertinggi terjadi pada perlakuan pakan berprotein 21%. Hal ini sejalan dengan penelitian Cheng et al. (2006) pada ikan kerapu (Epinephelus coioides) bahwa kadar lemak tubuh ikan yang tinggi diikuti dengan kadar lemak hati yang tinggi menyebabkan peningkatan IHS.
Hati adalah pusat metabolisme nutrien di dalam tubuh, dan IHStelah umum digunakan sebagai indikator pertumbuhan (Ighwela et al. 2014). Pada penelitian ini IHS meningkat dengan penambahan rGH sejalan dengan peningkatan pertumbuhan ikan, dan menurun berbanding terbalik dengan peningkatan kadar protein pakan (P<0,05; Gambar 2). Peningkatan IHS juga dilaporkan pada ikan coho salmon transgenik GH yang memiliki IHS sebesar 30% lebih tinggi dibandingkan dengan kontrol (Leggat et al. 2009). Selanjutnya, peningkatan IHS menunjukkan bahwa ukuran hati menjadi lebih besar agar dapat bekerja lebih baik sebagai kompensasi kadar protein pakan yang rendah. Selain itu, nilai IHS yang tinggi menunjukkan penyerapan dan metabolisme protein, lemak, dan karbohidrat yang lebih optimal (Yandes et al. 2003). Peningkatan IHS sebagai akibat dari suplementasi rGH pada ikan gurami terjadi karena peningkatan ukuran hepatosit sehingga jumlah nutrisi terakumulasi dalam hati meningkat (Safir 2012).
Secara keseluruhan persentase komposisi tubuh ikan dari hasil penelitian menunjukkan bahwa ikan yang diberi rGH memiliki kadar lemak tubuh yang lebih besar dibandingkan masing-masing kontrolnya (Tabel 3). Hasil serupa dari pemberian rGH juga diperoleh pada ikan channel catfish (Silverstein et al. 2000) dan ikan sidat (Handoyo 2012). GH berpengaruh pada sintesis protein dan omset lemak (Oommen & Johnson 1998; Fauconneau et al. 1996). Kandungan lemak yang lebih tinggi pada penelitian ini berbeda dengan apa yang diperoleh Irmawati (2013) dan Safir (2012), di mana kadar lemak ikan gurami yang diberi rGH justru mengalami penurunan. Perbedaan ini diduga terjadi karena ukuran ikan dan kandungan nutrisi pakan yang digunakan dalam penelitian ini berbeda. Sesuai dengan Rienecke et al. (2005), bahwa perubahan komposisi tubuh akibat pemberian rGH tergantung pada jenis ikan, ukuran ikan, kandungan nutrisi pakan yang diberikan, dan kondisi lingkungan yang mempengaruhi metabolisme ikan.
15 asupan lemak dari pakan. Hal ini terjadi karena kelebihan glukosa dikonversi menjadi cadangan lemak melalui proses lipogenesis yang disimpan pada jaringan tubuh. Hal ini sejalan dengan pernyataan Kersten+ (2001), bahwa asam lemak dapat disintesis dari glukosa yang merupakan derivat dari karbohidrat jika asupan glukosa berlebih.
Keberadaan energi non protein (karbohidrat dan lemak) mengurangi perombakan protein menjadi energi (protein sparring effect) sehingga retensi protein meningkat dan ekskresi ammonia menurun (Suprayudi et al. 2014). Pada penelitian ini pemberian rGH mampu meningkatan retensi protein (Tabel 3) dan menurunkan ekskresi TAN (Gambar 3). Berdasarkan hasil tersebut, kemampuan retensi protein yang lebih tinggi menyebabkan penurunan ekskresi metabolit nitrogen (dalam bentuk TAN) akibat terjadi protein sparring effect pada ikan selama produksi energi. Hal ini sesuai dengan pernyataan Perez-Sanchez (2000), kemampuan retensi nitrogen (protein) yang tinggi pada ikan yang diberi rGH dibandingkan dengan kontrol menunjukkan bahwa GH mampu meningkatkan pemanfaatan nutrien non-protein sebagai sumber energi (protein sparring effect). Peran GH dalam mengurangi ekskresi TAN juga telah dilaporkan pada ikan striped bass (Farmanfarmaian & Sun 1999) dan ikan nila transgenik (Kobayashi et al. 2007). Di sisi lain, peningkatan kadar protein pakan meningkatkan ekskresi TAN (Gambar 3). Laju pelepasan nitrogen ke air erat kaitannya dengan produksi nitrogen oleh ikan. Sumber utama amonia-N dan urea-N pada ikan adalah katabolisme protein; dengan demikian, tampak bahwa katabolisme protein tergantung pada jumlah asupan protein pada ikan. Penelitian sebelumnya pada benih Australian short-finned eel (Guo et al. 2012) dan bluefin trevally (Suprayudi et al. 2014) menghasilkan hubungan positif antara asupan protein dan ekskresi amonia. Hal ini menunjukkan bahwa peningkatan asam amino yang dideaminasi dan diekskresikan sebagai amonia lebih digunakan untuk menghasilkan energi daripada disimpan untuk pertumbuhan jaringan pada ikan yang diberi pakan berprotein tinggi (Mohanta et al. 2008). Hasil ini juga menunjukkan bahwa rendahnya kadar protein pakan dan suplementasi rGH dapat mengurangi polusi amonia dari akuakultur.
Peningkatan nilai retensi protein dan retensi lemak akibat penambahan rGH pada tiap perlakuan kadar protein pakan juga diikuti oleh perbaikan nilai RKP (Tabel 2 dan Tabel 3). Kadar protein pakan dan penambahan rGH menurunkan RKP ikan gurami, hal ini menunjukkan bahwa pemanfaatan pakan menjadi lebih efisien. Nilai retensi menunjukkan tingkat pemanfaatan nutrien pakan untuk pertumbuhan. Artinya penambahan rGH dapat meningkatkan efisiensi pemanfaatan protein dan lemak pakan untuk pertumbuhan pada ikan uji. Peran hormon pertumbuhan dalam meningkatkan efisiensi pakan juga telah dilaporkan pada ikan mas (Fu et al. 1998), ikan salmon (Devlin et al. 2004), ikan much loach (Nam et al. 2004) dan ikan nila (Kobayashi et al. 2007). Nilai RKP terbesar ditemukan pada perlakuan pakan berprotein 21% tanpa penambahan rGH. Hasil ini menunjukkan bahwa proporsi tinggi dari protein yang ada pada pakan uji rendah protein dikatabolisme untuk mencukupi kebutuhan energi (Guillaume et al. 1999).
16
meningkat seiring dengan peningkatan kadar protein pakan dan penambahan rGH. Peningkatan bobot tertinggi diperoleh pada perlakuan pakan berkadar protein 21%, yakni sebesar 35,01% lebih tinggi (P<0,05) daripada kontrolnya. Peningkatan bobot terendah terjadi pada perlakuan pakan berkadar protein 34%, yaitu sebesar 16,90% lebih tinggi (P<0,05) daripada kontrolnya. Yang et al. (2002) menyatakan bahwa kadar protein pakan yang kurang menghasilkan kinerja pertumbuhan yang rendah pada banyak spesies ikan. Sementara itu, pemberian rGH secara oral pada ikan untuk meningkatkan pertumbuhan juga telah dilaporkan dalam beberapa penelitian sebelumnya (Promdonkoy et al. 2004; Haghighi et al. 2011). Biomassa tertinggi, LPH terbesar, dan RKP terendah ditunjukkan pada perlakuan pakan berkadar protein 34% dan diperkaya rGH. Biomassa dan LPH pada perlakuan pakan protein 28% dan diperkaya rGH adalah sama dengan perlakuan pakan 34% tanpa diperkaya rGH. Dengan demikian penggunaan rGH 3 mg/kg pada pakan berprotein 28% menghasilkan performa budidaya sama dengan yang menggunakan pakan berprotein 34%.
Secara keseluruhan, peningkatan kadar protein pakan dan penambahan rGH memberikan pengaruh nyata terhadap peningkatan performa pertumbuhan benih ikan gurami, namun tidak ada interaksi antara kedua faktor tersebut. Interaksi antara perlakuan kadar protein pakan dan penambahan rGH ditunjukkan pada parameter-parameter pendukung pertumbuhan, antara lain retensi protein dan lemak, kadar trigliserida darah, glikogen hati dan otot, serta aktivitas enzim pencernaan.
Ikan yang digunakan pada penelitian ini berukuran sekitar 15 g/ekor. Jika diklasifikasikan menurut SNI (2006), ikan yang digunakan termasuk dalam kategori benih sebar. Untuk mencapai ukuran konsumsi 500-750 g/ekor, masih dibutuhkan waktu yang cukup lama. Oleh karena itu, diperlukan pengujian lebih lanjut untuk memperoleh hasil yang lebih optimal. Riset pemberian rGH secara oral sebelumnya telah dilakukan oleh Safir (2012) dengan menggunakan pakan komersial berkadar protein sekitar 40%. Uji skala lapang untuk mendapatkan informasi mengenai tingkat efisiensi budidaya masih diperlukan.
4
KESIMPULAN DAN SARAN
Kesimpulan
Pemberian pakan berkadar protein berbeda dengan pengkayaan rGH dosis basah 3 mg/kg mampu meningkatkan pertumbuhan dan efisiensi pemanfaatan protein pada benih ikan gurami.
Saran
17
DAFTAR PUSTAKA
Acosta J, Morales R, Morales A, Alonso M, Estrada MP. 2007. Pichia pastoris expressing recombinant tilapia growth hormone accelerates the growth of tilapia. Biotechnol Lett. 29:1671-1676.
Alimuddin, Lesmana I, Sudrajat AO, Carman O, Faisal I. 2010. Production and
Cheng AN, Chen CY, Liou CH, Chang CF. 2006. Effects of dietary protein and lipids on blood parameters and superoxide anion production in the grouper (Epinephelus coioides). Zool Stud. 45(4): 492-502.
Cook JT, McNiven MA, Richardson GF, Sutterlin AM. 2000. Growth rate, body composition and feed digestibility/conversion of growth enhanced Atlantic salmon (Salmo salar). Aquacult. 188:15-32.
Debnanth S. 2010. A review on the physiology of insulin like growth factor-1 (IGF-1) peptide in bony fishes and its phylogenetic correlation in 30 different taxa of 14 families of teleosts. Adv Envir Biol. 5:31-52
Demain AL, Vaishnav P. 2009. Production of recombinant proteins by microbes and higher organisms. Biotechnol Adv. 27: 297-306.
Devlin RH, Biagi CA, Yesaki TY. 2004. Growth, viability and genetic characteristics of GH transgenic coho salmon strains. Aquacult. 236:607-632. Eusobio PS, Coloso RM. 2002. Proteolityc enzyme activity of juvenile Asian sea
bass (Lates calcarifer Bloch), is increased with protein intake. Aquacult Res. 33:569-574.
Farmanfarmaian A, Sun LZ. 1999. Growth hormone effects on essential amino acid absorption, muscle amino acid profile, retention and nutritional requirements of striped bass hybrids. Gen Anals. 15:107-113
Fauconneau B, Mady MP, Le Bail PY. 1996. Effects of growth hormone on muscle protein synthesis in rainbow trout (Oncorhynchus mykiss) and Atlantic salmon (Salmo salar). Fish Physiol Biochem. 15:49-56.
Fu C, Cui Y, Hung SSO, Zhu Z. 1998. Growth and feed utilization by F4 human growth hormone transgenic carp fed diets with different protein levels. J Fish Biol. 53:115-129.
Funkenstein B, Dyman A, Lapidot Z, de Jesus-Ayson EG, Gertler A, Ayson FG. 2005. Expression and purification of a biologically active recombinant rabbitfish (Siganus guttatus) growth hormone. Aquacult. 250: 504-515.
Groff JL, Gropper SS. 1999. Advanced nutrition and human metabolism. Stamford, USA: Wadsworth Thomson Learning. 201 p.
Guillaume, J., Kaushik, S., Bergot, P. and Metailler, R. 1999. Nutrition and feeding of fish and crustaceans. Chichester, UK: Praxis Publishing. pp. 81-109. Guo ZQ, Zhu XM, Liu JS, Han D, Yang YX, Lan ZQ, Xie SQ. 2012. Effects of
18
juvenile hybrid sturgeon (Acipenser baerii ♀ × A. gueldenstaedtii ♂). Aquacult. 338–341:89–95.
Handoyo B. 2012. Metode pemberian dan respons benih ikan sidat terhadap hormone pertumbuhan rekombinan ikan kerapu kertang [tesis]. Bogor (ID): Institut Pertanian Bogor.
Haghighi M, Sharif RM, Sharifpour I, Sepahdari A, Lashtoo AGR. 2011. Oral recombinant bovine somatothropin improves growth performance in rainbow trout (Oncorhynchus mykiss). Iran J Fish Sci. 10:415-424.
Hasan AJZ, Khan U. 2013. Protein sparring effect and the efficiency of different compositions of carbohydrates, lipids and protein on the growth of rohu (Labeo rohita) fingerlings. World J Fish Marine Sci. 5(3):244-250.
Hemre GI, Mommsen TP, Krogdahl A. 2002. Carbohydrates in fish nutrition: effect on growth, glucose metabolism and hepatic enzymes. Aquacult Nut. 8: 175-194.
Huisman EA. 1987. Principle of fish production. Department of Fish Culture and Fisheries. Wageningen Agricultural University, The Netherland. 187p.
Ighwela KA, Ahmad AB, Abol-Munafi AB. 2014. The selection of viscerosomatic and hepatosomatic indices for the measurement and analysis of Oreochromis niloticus condition fed with varying dietary maltose levels. Internatl J Fauna Biol Stu. 1(3):18-20
Irmawati. 2013. Respons fisiologis, biokimia, dan molekuler ikan gurami yang diberi hormon pertumbuhan rekombinan [disertasi]. Bogor (ID): Institut Pertanian Bogor.
Jacobs NJ, Vandemark PJ. 1960. The purification and properties of the alpha-glycerophosphate-oxidizing enzyme of Streptococcus faecalis 10C1. Arch Biochem Biophys. 88:250–255
Kersten+ S. 2001. Mechanisms of nutritional and hormonal regulation of lipogenesis. EMBO Reports. 21:282-286.
Kobayashi S, Alimuddin, Morita T, Miwa M, Lu J, Endo M, Takeuchi T, Yoshizaki G. 2007. Transgenic Nile tilapia (Oreochromis niloticus) over-expressing growth hormone show reduced ammonia excretion. Aquacult. 270:427-435.
Krogdahl A, Bakke-McKellep AM, Baeverfjord G. 2003. Effects of graded levels of standard soybean meal on intestinal structure, mucosal enzyme activities, and pancreatic response in Atlantic salmon (Salmo salar L.). Aquacult Nut. 9(6): 361-371.
Latar DI. 2013. Efektivitas pemberian hormone pertumbuhan rekombinan melalui pakan dengan bahan penyalut berbeda dan pelleting pada ikan nila [tesis]. Bogor (ID): Institut Pertanian Bogor.
Leggat RA, Raven PA, Momsen TP, Sakhrani D, Higgs D, Devlin RH. 2009. Growth hormone transgenesis influences carbohydrate, lipid, and protein metabolism capacity for energy production in coho salmon (Oncorhynchus kisutch). Comp Biochem Physiol Part B. 154:121-133.
Mataruga VP, Janać B, Vlahović M, Mrdaković M, Ilijin L, Matić D, Milošević V. 2012. Ghrelin effects on the activities of digestive enzymes and growth of Lymantria dispar L. Arch Biol Sci. 64(2):497-502.
19 Mokoginta I, Suprayudi MA, Setiawati M. 1995. Kebutuhan optimum protein dan energi makanan benih ikan gurami (Osphronemus goramy). Bogor (ID): Institut Pertanian Bogor.
Moriyama S, Hiroshi Y, Seiji S, Toshio A, Tetsuya H, Hiroshi K. 1993. Oral administration of recombinant salmon growth hormone to rainbow trout (Oncorhyncus mykiss). Aquacult. 112:99-106.
Nam YK, Noh JK, Cho YS, Cho HJ, Cho KN, Kim CG, Kim DS. 2004. Dramatically accelerated growth and extraordinary gigantism of transgenic mud loach (Misgurnus mizolepis). Transgen Res. 10:353-362.
Oommen OV, Johnson B. 1998. Metabolic effects of bovine growth hormone in a teleost (Anabas testudineus). Annals New York Acad Sci. 839:380-381.
Perez-Sanchez J. 2000. The involvement of growth hormone in growth regulation energy homeostasis and immune function in the gilthead sea bream (Sparus aurata): a short review. Fish Physiol Biotechnol. 22:135-144.
Promdonkoy B, Warit S, Panyim S. 2004. Production of a biologically active growth hormone from giant catfish (Pangasianodon gigas) in Escherichia coli. Biotechnol Lett. 26:649-653.
Rasmussen RS, Rønsholdt B, Ostenfeld TH, McLean E, Byatt JC. 2001. Growth feed utilization, carcass composition and sensory characteristics of rainbow trout treated with recombinant bovine placental lactogen and growth hormone. Aquacult. 195:367-384.
Rienecke M, Bjorn T, Walton WD, Stephen DMC, Isabel N, Deborah MP, Joaquim G. 2005. Growth hormone and insulin-like growth factors in fish: where we are and where to go (Minireview). Gen Comp Endocrinol. 142:20-24. Safir M. 2012. Respons benih ikan gurami (Osphronemus goramy) yang diberi
hormone pertumbuhan rekombinan melalui oral pada dosis berbeda [tesis]. Bogor (ID): Institut Pertanian Bogor.
Shamushaki VAJ, Kasumyan AO, Abedian A, Abtahi B. 2007. Behavioral responses of the Persian sturgeon (Acipenser persicus) juveniles to free amino acid solutions. Marine Freshwater Behav Phisiol. 40(3):219-227.
Silverstein JT, Wolters WR, Shimizu M, Dickhoff MW. 2000. Bovine growth hormone treatment of channel catfish: strain and temperature effects on growth, plasma IGF-1 levels, feed intake and efficiency and body composition. Aquacult. 190:77-88.
[SNI] Standar Nasional Indonesia. 2006. Ikan gurami (Osphronemus goramy Lac.). SNI 01-7241-2006.
Subaidah S. 2013. Respons pertumbuhan dan imunitas udang vaname (Litopenaeus vannamei) terhadap pemberian hormon pertumbuhan rekombinan ikan kerapu kertang [disertasi]. Bogor (ID): Institut Pertanian Bogor.
Suprayudi MA, Setiawati M, dan Mokoginta I. 1994. Pengaruh rasio protein energi yang berbeda terhadap pertumbuhan ikan gurami (Osphronemus goramy). Bogor (ID): Institut Pertanian Bogor.
Suprayudi MA, Bintang M, Takeuchi T, Mokoginta I, Sutardi T. 1999. Defatted soybean meal as an alternative source to substitute fish meal in the feed of giant goramy (Osphronemus goramy). Suisanzozhoku. 47(4): 551-557.
20
Takeuchi T. 1988. Laboratory work chemical evaluation of dietary nutriens. In: Watanabe T (ed). Fish Nutrition and Mariculture. Tokyo: Department of Aquatic Bioscience. Tokyo University of Fisheries. JICA. pp; 179-226.
Trinder P. 1969. Determination of glucose in blood using glucose oxidase with an alternative oxygen receptor. Ann Clin Biochem. 6:24–27
Tsai HJ, Hsih MH, Kuo JC. 1997. Escherichia coli produced fish growth hormone as a feed additive to enhance the growth of juvenile black seabream (Acanthopagrus schlegeli). J Appl Ichthyol. 13:78-82.
Volkoff H, Canosa LF, Unniappan S, Cerda-Reverterver JM, Bernier NJ, Kelly SP, Peter RE. 2005. Neuropeptides and the control of food intake in fish. Gen Comp Endocrinol. 142:3-19.
Watanabe T. 1988. Fish nutrition and mariculture. Department of aquatic Bioscience. Tokyo University of Fisheries. JICA. 233 p.
Wedemeyer GA, Yasutake WT. 1977. Clinical method for the assessment of the effect of environmental stress on fish health. Tech Pap US Fish Wildl Serv. Washington DC. 89 p.
Worthington V. 1993. Worthington enzyme manual: enzymes and related biochemicals worthingthon chemical. New Jersey, US. 399 p
Yandes, Affandi R, Mokoginta I. 2003. Pengaruh pemberian selulosa dalam pakan terhadap kondisi biologis benih ikan gurami (Osphronemus gourami). J Iktiol Indones. 3:27-33.
21 Lampiran 1 ANOVA dan Uji-Duncan pertambahan biomassa benih ikan gurami
yang diberi perlakuan.
Tests of Between-Subjects Effects Dependent Variable:Pertambahan biomassa (g)
Source
Type III Sum of
Squares df Mean Square F Sig.
Corrected Model 63057.303a 5 12611.461 83.403 .000
Intercept 1205883.793 1 1205883.793 7974.824 .000
rGH 11747.379 1 11747.379 77.688 .000
Protein 51261.624 2 25630.812 169.503 .000
rGH * Protein 48.300 2 24.150 .160 .854
Error 1814.536 12 151.211
Total 1270755.632 18
Corrected Total 64871.839 17
a. R Squared = .972 (Adjusted R Squared = .960)
Grand Mean
Dependent Variable:Pertambahan biomassa (g)
95% Confidence Interval
Mean Std. Error Lower Bound Upper Bound
258.831 2.898 252.516 265.146
Pertambahan biomassa (g) Duncana,,b
Perlakuan
Subset
N 1 2 3 4 5
21% 3 159.1667
21%+rGH 3 214.8833
28% 3 250.3567
34% 3 290.3300
28%+rGH 3 298.8767
34%+rGH 3 339.3733
Sig. 1.000 1.000 1.000 .411 1.000
Means for groups in homogeneous subsets are displayed. Based on observed means.
22
Lampiran 2 ANOVA dan Uji-Duncan laju pertumbuhan spesifik (LPS) benih ikan gurami yang diberi perlakuan.
Tests of Between-Subjects Effects Dependent Variable:Specific Growth Rate (%)
Source
Type III Sum of
Squares df Mean Square F Sig.
Corrected Model 1.981a 5 .396 76.773 .000
Intercept 83.377 1 83.377 16154.872 .000
rGH .376 1 .376 72.766 .000
Protein 1.590 2 .795 154.051 .000
rGH * Protein .015 2 .008 1.499 .262
Error .062 12 .005
Total 85.420 18
Corrected Total 2.043 17
a. R Squared = .970 (Adjusted R Squared = .957)
Grand Mean
Dependent Variable:Specific Growth Rate (%)
95% Confidence Interval
Mean Std. Error Lower Bound Upper Bound
2.152 .017 2.115 2.189
Specific Growth Rate (%) Duncana,,b
Perlakuan
Subset
N 1 2 3 4 5
21% 3 1.5633
21%+rGH 3 1.9333
28% 3 2.1367
34% 3 2.3233
28%+rGH 3 2.3700
34%+rGH 3 2.5867
Sig. 1.000 1.000 1.000 .442 1.000
Means for groups in homogeneous subsets are displayed. Based on observed means.
23 Lampiran 3 ANOVA dan Uji-Duncan rasio konversi pakan (RKP) benih ikan
gurami yang diberi perlakuan.
Tests of Between-Subjects Effects Dependent Variable:FCR
Source
Type III Sum of
Squares df Mean Square F Sig.
Corrected Model 1.002a 5 .200 39.922 .000
Intercept 38.515 1 38.515 7668.904 .000
rGH .084 1 .084 16.736 .001
Protein .883 2 .442 87.950 .000
rGH * Protein .035 2 .018 3.488 .064
Error .060 12 .005
Total 39.578 18
Corrected Total 1.063 17
a. R Squared = .943 (Adjusted R Squared = .920)
Grand Mean Dependent Variable:FCR
95% Confidence Interval
Mean Std. Error Lower Bound Upper Bound
1.463 .017 1.426 1.499
FCR Duncana,,b
Perlakuan
Subset
N 1 2 3 4
34%+rGH 3 1.1933
28%+rGH 3 1.3333
34% 3 1.3500
28% 3 1.3533
21%+rGH 3 1.6567
21% 3 1.8900
Sig. 1.000 .748 1.000 1.000
Means for groups in homogeneous subsets are displayed. Based on observed means.
24
Lampiran 4 ANOVA dan Uji-Duncan jumlah konsumsi pakan (JKP) benih ikan gurami yang diberi perlakuan.
Tests of Between-Subjects Effects Dependent Variable:JKP (gram)
Source
Type III Sum of
Squares df Mean Square F Sig.
Corrected Model 25172.065a 5 5034.413 4.915 .011
Intercept 2408529.624 1 2408529.624 2351.372 .000
rGH 8452.600 1 8452.600 8.252 .014
Protein 14733.678 2 7366.839 7.192 .009
rGH * Protein 1985.787 2 992.893 .969 .407
Error 12291.700 12 1024.308
Total 2445993.390 18
Corrected Total 37463.766 17
a. R Squared = .672 (Adjusted R Squared = .535)
Grand Mean Dependent Variable:JKP (gram)
95% Confidence Interval
Mean Std. Error Lower Bound Upper Bound
365.797 7.544 349.361 382.233
JKP (gram) Duncana,,b
Perlakuan
Subset
N 1 2 3
21% 3 301.5433
28% 3 338.6967 338.6967
21%+rGH 3 356.8633 356.8633 356.8633
34% 3 392.1400 392.1400
28%+rGH 3 399.5900 399.5900
34%+rGH 3 405.9467
Sig. .066 .051 .107
Means for groups in homogeneous subsets are displayed. Based on observed means.
25 Lampiran 5 ANOVA dan Uji-Duncan indeks hepatosomatik (IHS) benih ikan
gurami yang diberi perlakuan.
Tests of Between-Subjects Effects Dependent Variable:IHS
Source
Type III Sum of
Squares df Mean Square F Sig.
Corrected Model 1.366a 5 .273 47.442 .000
Intercept 38.160 1 38.160 6628.282 .000
rGH .157 1 .157 27.326 .000
Protein 1.207 2 .603 104.797 .000
rGH * Protein .002 2 .001 .146 .866
Error .069 12 .006
Total 39.595 18
Corrected Total 1.435 17
a. R Squared = .952 (Adjusted R Squared = .932)
Grand Mean Dependent Variable:IHS
95% Confidence Interval
Mean Std. Error Lower Bound Upper Bound
1.456 .018 1.417 1.495
IHS Duncana,,b
Perlakuan
Subset
N 1 2 3 4 5
34% 3 1.1022
34%+rGH 3 1.2622
28% 3 1.2842
28%+rGH 3 1.4806
21% 3 1.7012
21%+rGH 3 1.9057
Sig. 1.000 .729 1.000 1.000 1.000
Means for groups in homogeneous subsets are displayed. Based on observed means.
26
Lampiran 6 ANOVA dan Uji-Duncan ekskresi total amoniak nitrogen (TAN) benih ikan gurami yang diberi perlakuan.
Tests of Between-Subjects Effects Dependent Variable:TAN
Source
Type III Sum of
Squares df Mean Square F Sig.
Corrected Model .023a 5 .005 18.648 .000
Intercept .224 1 .224 919.893 .000
rGH .004 1 .004 17.298 .001
Protein .018 2 .009 36.942 .000
rGH * Protein .001 2 .000 1.030 .387
Error .003 12 .000
Total .250 18
Corrected Total .026 17
a. R Squared = .886 (Adjusted R Squared = .838)
Grand Mean Dependent Variable:TAN
95% Confidence Interval
Mean Std. Error Lower Bound Upper Bound
.112 .004 .104 .120
TAN Duncana,,b
Perlakuan
Subset
N 1 2 3 4
21%+rGH 3 .0569
21% 3 .0949
28%+rGH 3 .0982
28% 3 .1139 .1139
34%+rGH 3 .1337
34% 3 .1718
Sig. 1.000 .181 .146 1.000
Means for groups in homogeneous subsets are displayed. Based on observed means.