PENGGUNAAN PATI JAGUNG GELATINASI SEBAGAI
BAHAN PENGIKAT PADA FORMULASI
TABLET ALLOPURINOL
SKRIPSI
OLEH:
DERI ARISANDI
NIM 121524108
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
PENGGUNAAN PATI JAGUNG GELATINASI SEBAGAI
BAHAN PENGIKAT PADA FORMULASI
TABLET ALLOPURINOL
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
DERI ARISANDI
NIM 121524108
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
PENGESAHAN SKRIPSI
PENGGUNAAN PATI JAGUNG GELATINASI SEBAGAI
BAHAN PENGIKAT PADA FORMULASI
TABLET ALLOPURINOL
OLEH: DERI ARISANDI
NIM 121524108
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 4 Januari 2015
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Drs. Agusmal Dalimunthe, M.S., Apt. Dra. Juanita Tanuwijaya, M.Si., Apt. NIP 195406081983031005 NIP 1195111021977102001
Drs. Agusmal Dalimunthe, M.S., Apt.
Pembimbing II, NIP 195406081983031005
Drs. Fathur Rahman Harun, M.Si, Apt. Dra. Fat Aminah, M.Sc., Apt. NIP 195201041980031002 NIP 195011171980022001
Dra. Nazliniwati, M.Si., Apt. NIP 196005111989022001
Medan, April 2015 Fakultas Farmasi
Universitas Sumatera Utara a.n Dekan,
Wakil Dekan I,
Prof. Dr. Julia Reveny, M.Si., Apt.
iv
KATA PENGANTAR
Bismillahirrahmaanirrahiim,
Puji syukur kepada Allah SWT atas segala limpahan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini, serta shalawat beriring salam untuk Rasulullah Muhammad SAW sebagai suri tauladan dalam kehidupan. Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul “Penggunaan Pati Jagung Gelatinasi sebagai Bahan Pengikat pada Formulasi Tablet Allopurinol”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada, Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU Medan, yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan. Bapak Drs. Agusmal Dalimunthe, M.S., Apt., selaku pembimbing I, serta Bapak Drs. Fathur Rahman Harun, M.Si, Apt., selaku pembimbing II yang telah membimbing dan memberikan petunjuk serta saran-saran selama penelitian hingga selesainya skripsi ini. Ibu Dra. Juanita Tanuwijaya, M.Si., Apt., Ibu Dra. Fat Aminah, M.Sc., Apt., dan Ibu Dra. Nazliniwati, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah mendidik selama perkuliahan.
v
sayang yang tidak ternilai dengan apapun, pengorbanan baik materi maupun motivasi serta doa yang tulus yang tidak pernah berhenti. Abang Rendy Oktaza, Kakak Dela Arnyta dan Adik-adikku tersayang Ade Septiandi dan Debi Oktaviani serta seluruh keluarga yang selalu mendoakan dan memberikan semangat. Penulis juga tidak lupa mengucapkan terima kasih kepada teman-teman ekstensi farmasi angakatan 2012, kakak-kakak, abang-abang dan adek-adek di Laboratorium Teknologi Sediaan Farmasi II dan Laboratorium Farmasi Fisik USU, serta sahabat-sahabatku yang telah memberikan bantuan dan semangat tak terhingga.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, April 2015 Penulis,
vi
PENGGUNAAN PATI JAGUNG GELATINASI SEBAGAI BAHAN PENGIKAT PADA FORMULASI
TABLET ALLOPURINOL ABSTRAK
Latar belakang: Salah satu sumber pati adalah jagung. Pati yang telah mengalami gelatinasi dapat membentuk pasta dari granula-granula pati yang mengembang. Dalam kondisi panas, pasta masih memiliki kemampuan mengalir yang fleksibel dan tidak kaku. Berdasarkan hal tersebut peneliti melakukan penelitian menggunakan pati jagung gelatinasi sebagai pengikat secara granulasi basah dengan menggunakan allopurinol sebagai model obat.
Tujuan penelitian: Untuk menggunakan pati jagung gelatinasi sebagai pengikat dan mengetahui konsentrasinya yang paling baik pada formulasi tablet allopurinol.
Metode: Pati jagung gelatinasi dibuat dengan mensuspensikan 80 gram pati jagung alami dalam 1000 ml air (8% b/v) lalu dipanaskan pada suhu 70°C dibiarkan stabil selama 20 menit sampai terbentuk massa kental kemudian dikeringkan. Pati jagung gelatinasi di uji ukuran partikel, kelarutan, berat jenis dan mikroskopik. Variasi konsentrasi pati jagung gelatinasi yang digunakan sebagai pengikat yaitu (F2) 7%, (F3) 9%, (F4) 11%, (F5) 13%, (F6) 15% dan (F7) 17%. Uji preformulasi berupa uji waktu alir, sudut diam dan indeks tap dilakukan terhadap massa granul sebelum dicetak menjadi tablet. Setelah dicetak menjadi tablet dilakukan evaluasi tablet yaitu uji kekerasan, waktu hancur, friabilitas, penetapan kadar, keseragaman sediaan dan uji disolusi. Selanjutnya data pada penetapan kadar dan uji disolusi dianalisis secara statistik.
Hasil: Pati jagung gelatinasi dapat digunakan sebagai bahan pengikat pada formulasi tablet allopurinol. Hasil uji preformulasi granul memenuhi persyaratan untuk semua formula. Pada evaluasi tablet allopurinol, uji kekerasan, friabilitas, dan waktu hancur memenuhi persyaratan. Semakin ditingkatkan konsentrasi pati jagung gelatinasi, maka akan menghasilkan kekerasan dan friabilitas yang baik, namun waktu hancur tablet yang semakin lambat. Hasil uji penetapan kadar allopurinol seluruhnya memenuhi persyaratan. Pada uji disolusi tablet allopurinol selama 45 menit diperoleh formula F2 sampai F7 memenuhi persyaratan. Kecuali formula F1 dengan bahan pengikat pati jagung alami 10% pada uji disolusi tidak memenuhi syarat yang ditentukan. Analisis data statistik menggunakan kruskal-wallis dilakukan pada penetapan kadar menunjukkan signifikasi p > 0,05 yang berarti memiliki perbedaan tidak nyata pada tiap formula tablet. Sedangkan pada disolusi menunjukkan signifikasi p < 0,05 yang berarti memiliki perbedaan nyata pada tiap formula tablet.
Kesimpulan: Hasil penelitian menunjukkan bahwa pati jagung gelatinasi dapat digunakan sebagai bahan pengikat pada formulasi tablet allopurinol secara granulasi basah dengan range konsentrasi yang baik digunakan adalah 7% - 13%.
vii
GELATINIZED CORN STARCH APLICATION AS A BINDER IN TABLET ALLOPURINOL FORMULATION
ABSTRACT
Background: One source of starch is corn. Starch which has been experiencing gelatinized can form a paste or granules that have been swelled. In hot conditions the paste still has the ability to flow is flexible and not rigid. Based on the researchers a study using corn starch gelatinized as binder in wet granulation and as model drug is allopurinol.
Objective: This research was aim to find out the gelatinized corn starch as binder and determine the best concentration on allopurinol tablet formulation.
Methods: Gelatinized corn starch was made by 80 gram natural corn starch in 1000 ml of water. Then heated at temperatures 70°C stable for 20 minutes left until thick and then dried. Gelatinized corn starch in the test particle size, solubility, desity, and microscopic. Variation concentration of gelatinized corn starch used as binder is yaitu (F2) 7%, (F3) 9%, (F4) 11%, (F5) 13%, (F6) 15% dan (F7) 17%. Test of preformulasi are time for flowing, angle of repose and tapp index of the mass of granules is molded into a tablet before. While evaluations conducted tablet hardness testing, when destroyed, friabilitas, determination of levels, dosage uniformity and dissolution testing.
Results: Gelatinized of corn starch could be used as binder for tablet formulation allopurinol. The results of granule preformulation test meet the requirements for all formula. The evaluation of allopurinol tablet were hardness test, friability test, and disintegration time test, there were meet requirements. Increased concentration of gelatinized corn starch, it was produce good hardness and friability test, but the tablet disintegration time test would be slower. The result of determining the level of allopurinol tablet shows the percentage of level is meet requirements. Dissolution test allopurinol tablet for 45 minutes formula F2 until F7 meet the requirements. Except F1 form formula with natural corn starch binders 10% on dissolution did not meet the requirements set. Statistical data analysis used kruskal-wallis test at the determination of quantitative analysis tablets test showed that significant p > 0,05, which means has not real difference in each tablet formula. Dissolution test showed that significant p < 0,05, which means has real difference in each tablet formula.
Conclusion: The result of the research shows that corn starch gelatinized can be used as binder in tablets formulation allopurinol by the wet granulation method with the best range gelatinized corn stach consentration are 7% - 13%.
viii
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Perumusan Masalah ... 4
1.3Hipotesis ... 4
1.4Tujuan Penelitian ... 5
1.5Manfaat penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian Pati Jagung ... 6
2.2 Klasifikasi Tanaman Jagung ... 7
2.3 Gelatinasi Jagung ... 7
2.4 Allopurinol ... 10
ix
2.4.2 Farmakologi ... 10
2.5 Pengertian Tablet ... 11
2.6 Metode Granulasi Basah ... 12
2.7 Teori Pencampuran ... 13
2.8 Uji Preformulasi ... 14
2.8.1 Waktu alir ... 14
2.8.2 Sudut diam ... 14
2.8.3 Indeks tap ... 15
2.9 Pemeriksaan Kualitas Tablet ... 15
2.9.1 Kekerasan tablet ... 15
2.9.2 Kerapuhan tablet ... 16
2.9.3 Waktu hancur tablet ... 16
2.9.4 Keseragaman sediaan ... 16
2.9.5 Uji penetapan kadar zat berkhasiat ... 16
2.9.6 Disolusi ... 17
2.10 Spektrofotometri ... 17
2.10.1 Instrumen ... 18
2.10.2 Penggunaan ... 19
BAB III METODE PENELITIAN ... 20
3.1 Metode Pembuatan ... 20
3.2 Alat ... 20
3.3 Bahan ... 20
3.4 Pembuatan Pereaksi HCl 0,1 N ... 20
x
3.5.1 Pengumpulan bahan tumbuhan ... 21
3.5.2 Identifikasi tumbuhan ... 21
3.6 Prosedur Penelitian ... 21
3.6.1 Isolasi pati jagung ... 21
3.6.2 Pembuatan pati jagung gelatinasi ... 22
3.7 Pemeriksaan Karakteristik Pati Jagung Gelatinasi ... 22
3.7.1 Distribusi ukuran partikel ... 22
3.7.2 Kelarutan ... 22
3.7.3 Berat jenis ... 23
3.7.4 Mikroskopik ... 23
3.8 Pembuatan Tablet ... 23
3.9 Uji Preformulasi ... 25
3.9.1 Sudut diam ... 25
3.9.2 Waktu alir ... 25
3.9.3 Indeks tap ... 25
3.10 Evaluasi Tablet ... 26
3.10.1 Uji kekerasan ... 26
3.10.2 Uji kerapuhan (friabilitas) ... 26
3.10.3 Uji waktu hancur ... 26
3.10.4 Penetapan kadar ... 27
3.10.4.1 Penentuan kurva serapan dan linieritas kurva kalibrasi allopurinol dalam larutan HCl 0,1 N ... 27
xi
3.10.5 Keseragaman sediaan ... 29
3.10.6 Uji disolusi ... 29
xii
4.5.4.1 Hasil penentuan panjang gelombang
maksimum dalam HCl 0,1 N ... 43
4.5.4.2 Hasil penentuan linieritas kurva kalibrasi Dalam HCl 0,1 N ... 43
4.5.5 Penentuan kadar allopurinol ... 44
4.5.6 Keseragaman kandungan ... 46
4.5.7 Uji disolusi ... 47
4.6 Hasil Uji Statistik Tablet Allopurinol ... 49
4.6.1 Hasil uji statistik penetapan kadar allopurinol ... 49
4.6.2 Hasil uji statistik disolusi allopurinol ... 50
BAB V KESIMPULAN DAN SARAN ... 54
5.1 Kesimpulan ... 54
5.2 Saran ... 54
DAFTAR PUSTAKA ... 55
xiii
DAFTAR TABEL
Tabel Halaman
3.1 Istilah kelarutan ... 22
3.2 Formula tablet allopurinol ... 24
3.3 Kriteria penerimaan zat aktif yang larut dengan disolusi .... 31
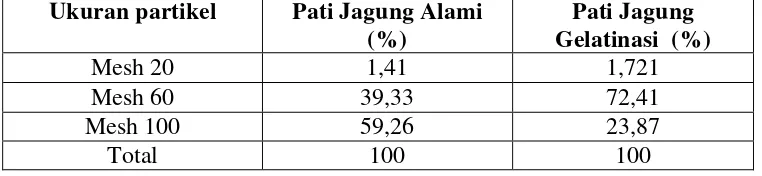
4.1 Data ukuran partikel pati jagung alami gelatinasi ... 33
4.2 Data kelarutan pati jagung gelatinasi ... 34
4.3 Data uji preformulasi massa granul ... 36
4.4 Data hasil evaluasi tablet allopurinol ... 39
4.5 Hasil penetapan kadar tablet allopurinol ... 45
4.6 Hasil keseragaman kandungan tablet allopurinol ... 46
4.7 Hasil uji disolusi tablet allopurinol ... 48
4.8 Hasil uji kolmogorov-smirnov penetapan kadar tablet allopurinol ... 49
4.9 Hasil uji kruskal-wallis penetapan kadar tablet allopurinol ... 49
4.10 Rank hasil uji kruskal-wallis penetapan kadar tablet allopurinol ... 50
4.11 Hasil uji kolmogorov-smirnov disolusi tablet allopurinol ... 50
4.12 Hasil uji kruskal-wallis disolusi tablet allopurinol ... 51
xiv
4.1 Presentase ukuran partikel pati jagung gelatinasi ... 34
xv
17. Analisis data statistik untuk mencari kadar sebenarnya dari allopurinol dalam formulasi tablet ... 85
18. Perhitungan keseragaman kandungan tablet allopurinol ... 87
xvi
20. Perhitungan disolusi tablet allopurinol ... 91 21. Data persen kumulatif disolusi tablet allopurinol ... 93 22. Uji kolmogorov-smirnov dan uji kruskal-wallis
penetapan kadar tablet allopurinol... ... 96 22. Uji kolmogorov-smirnov dan uji kruskal-wallis
vi
PENGGUNAAN PATI JAGUNG GELATINASI SEBAGAI BAHAN PENGIKAT PADA FORMULASI
TABLET ALLOPURINOL ABSTRAK
Latar belakang: Salah satu sumber pati adalah jagung. Pati yang telah mengalami gelatinasi dapat membentuk pasta dari granula-granula pati yang mengembang. Dalam kondisi panas, pasta masih memiliki kemampuan mengalir yang fleksibel dan tidak kaku. Berdasarkan hal tersebut peneliti melakukan penelitian menggunakan pati jagung gelatinasi sebagai pengikat secara granulasi basah dengan menggunakan allopurinol sebagai model obat.
Tujuan penelitian: Untuk menggunakan pati jagung gelatinasi sebagai pengikat dan mengetahui konsentrasinya yang paling baik pada formulasi tablet allopurinol.
Metode: Pati jagung gelatinasi dibuat dengan mensuspensikan 80 gram pati jagung alami dalam 1000 ml air (8% b/v) lalu dipanaskan pada suhu 70°C dibiarkan stabil selama 20 menit sampai terbentuk massa kental kemudian dikeringkan. Pati jagung gelatinasi di uji ukuran partikel, kelarutan, berat jenis dan mikroskopik. Variasi konsentrasi pati jagung gelatinasi yang digunakan sebagai pengikat yaitu (F2) 7%, (F3) 9%, (F4) 11%, (F5) 13%, (F6) 15% dan (F7) 17%. Uji preformulasi berupa uji waktu alir, sudut diam dan indeks tap dilakukan terhadap massa granul sebelum dicetak menjadi tablet. Setelah dicetak menjadi tablet dilakukan evaluasi tablet yaitu uji kekerasan, waktu hancur, friabilitas, penetapan kadar, keseragaman sediaan dan uji disolusi. Selanjutnya data pada penetapan kadar dan uji disolusi dianalisis secara statistik.
Hasil: Pati jagung gelatinasi dapat digunakan sebagai bahan pengikat pada formulasi tablet allopurinol. Hasil uji preformulasi granul memenuhi persyaratan untuk semua formula. Pada evaluasi tablet allopurinol, uji kekerasan, friabilitas, dan waktu hancur memenuhi persyaratan. Semakin ditingkatkan konsentrasi pati jagung gelatinasi, maka akan menghasilkan kekerasan dan friabilitas yang baik, namun waktu hancur tablet yang semakin lambat. Hasil uji penetapan kadar allopurinol seluruhnya memenuhi persyaratan. Pada uji disolusi tablet allopurinol selama 45 menit diperoleh formula F2 sampai F7 memenuhi persyaratan. Kecuali formula F1 dengan bahan pengikat pati jagung alami 10% pada uji disolusi tidak memenuhi syarat yang ditentukan. Analisis data statistik menggunakan kruskal-wallis dilakukan pada penetapan kadar menunjukkan signifikasi p > 0,05 yang berarti memiliki perbedaan tidak nyata pada tiap formula tablet. Sedangkan pada disolusi menunjukkan signifikasi p < 0,05 yang berarti memiliki perbedaan nyata pada tiap formula tablet.
Kesimpulan: Hasil penelitian menunjukkan bahwa pati jagung gelatinasi dapat digunakan sebagai bahan pengikat pada formulasi tablet allopurinol secara granulasi basah dengan range konsentrasi yang baik digunakan adalah 7% - 13%.
vii
GELATINIZED CORN STARCH APLICATION AS A BINDER IN TABLET ALLOPURINOL FORMULATION
ABSTRACT
Background: One source of starch is corn. Starch which has been experiencing gelatinized can form a paste or granules that have been swelled. In hot conditions the paste still has the ability to flow is flexible and not rigid. Based on the researchers a study using corn starch gelatinized as binder in wet granulation and as model drug is allopurinol.
Objective: This research was aim to find out the gelatinized corn starch as binder and determine the best concentration on allopurinol tablet formulation.
Methods: Gelatinized corn starch was made by 80 gram natural corn starch in 1000 ml of water. Then heated at temperatures 70°C stable for 20 minutes left until thick and then dried. Gelatinized corn starch in the test particle size, solubility, desity, and microscopic. Variation concentration of gelatinized corn starch used as binder is yaitu (F2) 7%, (F3) 9%, (F4) 11%, (F5) 13%, (F6) 15% dan (F7) 17%. Test of preformulasi are time for flowing, angle of repose and tapp index of the mass of granules is molded into a tablet before. While evaluations conducted tablet hardness testing, when destroyed, friabilitas, determination of levels, dosage uniformity and dissolution testing.
Results: Gelatinized of corn starch could be used as binder for tablet formulation allopurinol. The results of granule preformulation test meet the requirements for all formula. The evaluation of allopurinol tablet were hardness test, friability test, and disintegration time test, there were meet requirements. Increased concentration of gelatinized corn starch, it was produce good hardness and friability test, but the tablet disintegration time test would be slower. The result of determining the level of allopurinol tablet shows the percentage of level is meet requirements. Dissolution test allopurinol tablet for 45 minutes formula F2 until F7 meet the requirements. Except F1 form formula with natural corn starch binders 10% on dissolution did not meet the requirements set. Statistical data analysis used kruskal-wallis test at the determination of quantitative analysis tablets test showed that significant p > 0,05, which means has not real difference in each tablet formula. Dissolution test showed that significant p < 0,05, which means has real difference in each tablet formula.
Conclusion: The result of the research shows that corn starch gelatinized can be used as binder in tablets formulation allopurinol by the wet granulation method with the best range gelatinized corn stach consentration are 7% - 13%.
1
BAB I PENDAHULUAN
1.1 Latar Belakang
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik. Pati
terdiri dari butiran-butiran kecil yang disebut granula (Jane, 1995). Winarno (2002), menyatakan bahwa granula pati mempunyai sifat merefleksikan cahaya terpolarisasi, sehingga di bawah mikroskop terlihat kristal hitam putih. Sifat inilah yang disebut birefringent. Pada saat granula mulai pecah, sifat birefringent ini akan menghilang.
Granula pati mempunyai bentuk dan ukuran yang berbeda-beda tergantung dari sumbernya. Salah satu sumber pati adalah jagung. Jagung relatif mudah diperoleh karena tanaman jagung dibudidayakan di daerah tropis seperti Indonesia. Jagung berperan penting dalam perekonomian nasional dengan berkembangnya industri pangan yang ditunjang oleh teknologi budi daya dan varietas unggul. Indonesia mengimpor jagung hampir setiap tahun. Pada tahun 2000, impor jagung mencapai 1,26 juta ton, Untuk memenuhi kebutuhan dalam negeri yang terus meningkat (BPS, 2005).
2
Pati jagung mempunyai ukuran granula yang tidak homogen yaitu 1 μm -
7 μm untuk yang kecil dan 15 μm - 20 μm untuk yang besar. Granula besar
berbentuk oval polihedral dengan diameter 6 μm - 30 μm. Granula pati yang lebih
kecil kurang tahan terhadap perlakuan panas dan air dibanding granula yang besar (Singh, dkk., 2005).
Pomeranz (1991) menyatakan bahwa gelatinasi adalah proses pembengkakan granula pati ketika dipanaskan dalam media air. Granula pati tidak larut dalam air dingin, tetapi granula pati dapat mengembang dalam air panas. Naiknya suhu pemanasan akan meningkatkan pembengkakan granula pati. Pembengkakan granula pati menyebabkan terjadinya penekanan antara granula yang satu dengan granul lainnya. Mula-mula pembengkakan granula pati bersifat reversible, tetapi ketika suhu tertentu sudah terlewati, pembengkakan granula pati menjadi irreversible. Kondisi pembengkakan granula pati yang bersifat irreversible ini disebut dengan gelatinasi, sedangkan suhu terjadinya peristiwa ini disebut dengan suhu gelatinasi. Pati yang telah mengalami gelatinasi dapat dikeringkan, tetapi molekul-molekul tersebut tidak dapat kembali lagi ke sifat-sifat semula. Pati gelatinasi yang telah kering tersebut masih mampu menyerap air dalam jumlah yang cukup besar.
3
menggunakan pati jagung gelatinasi sebagai bahan pengikat tablet. Pati gelatinasi merupakan pati yang telah dibuat dengan cara memanaskan suspensi pati hingga suhu 70°C kemudian dikeringkan.
Allopurinol adalah obat utama yang digunakan untuk pengobatan hiperurisemia (yaitu kelebihan asam urat di dalam darah) dan komplikasi ini termasuk pula pirai atau gout. Allopurinol menghambat xantin oksidase digunakan secara oral (Wikipedia Inc, 2014). Allopurinol sangat sukar larut dalam air (Ditjen POM RI, 1995), sehingga untuk membuat formula dalam bentuk sediaan tablet perlu dicari bahan pembantu yang dapat mempersingkat waktu hancur. Tablet diharapkan larut pada waktu disolusi yang sesuai pada literatur, sehingga diperoleh sediaan tablet allopurinol yang larut sempurna pada tapak kerjanya, maka kemungkinan bahan pengikat amilum gelatinasi sesuai digunakan sebagai bahan pembantu pada formulasi tablet allopurinol.
Berdasarkan hal tersebut peneliti melakukan penelitian pembuatan tablet secara granulasi basah menggunakan bahan pengikat amilum gelatinasi dengan allopurinol sebagai model obat. Tablet yang diperoleh dilakukan pengujian beberapa parameter mutu industri yaitu uji friabilitas (Voight, 1994) dan uji kekerasan (Parrot, 1971), parameter mutu yang ditetapkan Farmakope Indonesia edisi III yaitu uji waktu hancur (Ditjen POM, 1979), penetapan kadar allopurinol, uji keseragaman sediaan, dan uji disolusi (Ditjen POM, 1995) sehingga dapat diketahui amilum gelatinasi dari jagung dapat digunakan sebagai bahan pengikat pada pembuatan tablet.
Menurut Moffat (2004) allopurinol mempunyai serapan maksimum pada
4
evaluasi penetapan kadar, keseragaman sediaan,dan disolusi dilakukan dengan cara spektrofotometri Ultra-violet.
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat dirumuskan sebagai berikut:
a. Apakah pati jagung gelatinasi dapat digunakan sebagai bahan pengikat pada pembuatan tablet allopurinol secara granulasi basah?
b. Berapakah konsentrasi pati jagung gelatinasi yang optimal yang dapat sebagai pengikat pada formulasi tablet?
1.3Hipotesis
Berdasarkan perumusan masalah di atas, maka yang menjadi hipotesis dalam penelitian ini adalah:
a. Pati jagung gelatinasi dapat digunakan sebagai bahan pengikat pada pembuatan tablet allopurinol secara granulasi basah.
b. Pati jagung gelatinasi dapat digunakan sebagai pengikat yang optimal dalam rentang konsentrasi tertentu.
1.4Tujuan Penelitian
Berdasarkan hipotesis di atas, maka yang menjadi tujuan dalam penelitian ini adalah:
5
b. Untuk mengetahui konsentrasi pati jagung gelatinasi yang paling baik digunakan sebagai bahan pengikat pada pembuatan tablet allopurinol secara granulasi basah.
1.5 Manfaat Penelitian
6
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Pati Jagung
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik, yang
banyak terdapat pada tumbuhan terutama pada biji-bijian, umbi-umbian. Berbagai macam pati tidak sama sifatnya, tergantung dari panjang rantai atom karbonnya, serta lurus atau bercabang (Jane, 1995). Pati dalam jaringan mempunyai bentuk butir yang berbeda-beda. Umumnya butir pati terdiri dari lapisan-lapisan yang mengelilingi suatu titik yang disebut hillus. Hillus dapat terletak ditengah atau dapat pula dipinggir. Biji jagung mengandung pati 54,1% - 71,7%, karbohidrat pada jagung sebagian besar merupakan komponen pati, sedangkan komponen lainnya adalah pentose, dekstrin, sukrosa, dan gula pereduksi (Fahn, 1992)
Granul pati utuh tidak larut dalam air dingin. Granul pati dapat menyerap air dan mengembang, tetapi dapat kembali seperti semula. Apabila granul pati ditambahkan air panas atau dingin yang kemudian dipanaskan, maka pati dapat mengalami gelatinasi (Winarno, 1995).
Granula pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas.
Fraksi terlarut disebut amilosa dan fraksi yang tidak terlarut disebut amilopektin
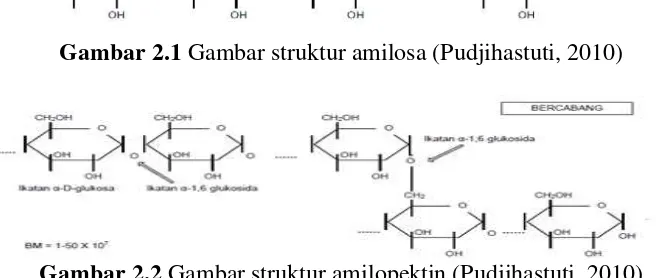
(Winarno, 2002). Amilosa merupakan bagian polimer dengan ikatan α-(1,4) dari unit glukosa, yang membentuk rantai lurus, yang umumnya dikatakan sebagai linier dari pati. Struktur ini mendasari terjadinya interaksi iodamilosa membentuk warna biru (Pudjihastuti, 2010).
7
D-glukosa dalam jumlah yang besar. Perbedaannya ada pada tingkat percabangan
yang tinggi dengan ikatan α-(1,6)-D-glukosa dan bobot molekul yang besar Bila
amilosa direaksikan dengan larutan iod akan membentuk warna biru tua, sedangkan amilopektin akan membentuk warna merah (Taggart, 2004).
Gambar 2.1 Gambar struktur amilosa (Pudjihastuti, 2010)
Gambar 2.2 Gambar struktur amilopektin (Pudjihastuti, 2010)
2.2 Klasifikasi Tanaman Jagung
Divisio : Spermatophyta Sub-divisio : Angiospermae Klass : Monocotyledoneae Ordo : Poales
Famili : Poaceae Genus : Zea
Spesies : Zea mays L (Hartono, 2007)
8
Gelatinasi merupakan proses pembengkakan granula pati ketika dipanaskan dalam media air. Granula pati tidak larut dalam air dingin, tetapi granula pati dapat mengembang dalam air panas. Naiknya suhu pemanasan akan meningkatkan pembengkakan granula pati. Pembengkakan granula pati menyebabkan terjadinya penekanan antara granula pati dengan lainnya (Pomeranz, 1991). Pembengkakan yang diikuti dengan gelatinasi pati terjadi ketika energi kinetik molekul-molekul air menjadi lebih kuat dari pada daya tarik menarik antara molekul pati di dalam granula yang menyebabkan air dapat masuk ke dalam butir-butir pati (Winarno, 1995). Gelatinasi adalah perubahan yang terjadi pada granula pada waktu mengalami pembengkakan yang luar biasa dan tidak dapat kembali ke bentuk semula (Winarno, 2002).
Gelatinasi juga disebut sebagai peristiwa koagulasi koloid dengan ikatan rantai polimer atau penyerapan zat terlarut yang membentuk jaringan tiga dimensi yang tidak terputus sehingga dapat mengakibatkan terperangkapnya air dan terhentinya aliran zat cair yang ada di sekelilingnya kemudian mengalami proses pengorientasian partikel (Meyer, 1973). Suhu gelatinasi adalah suhu pada saat granula pati pecah. Suhu gelatinasi berbeda-beda bagi tiap jenis pati dan merupakan suatu kisaran. Menurut Singh, dkk., (2005) suhu gelatinasi pati jagung 69°C - 72°C.
Rahman (2007) menyatakan bahwa gelatinasi merupakan fenomena kompleks yang bergantung pada:
a. ukuran granula
9
b. persentase amilosa
pati yang memiliki amilosa dengan kadar tinggi suhu gelatinasinya juga akan tinggi.
c. bobot molekul
makin besar bobot molekul dari granul pati pembentukan gel akan semakin lambat.
d. derajat kristalisasi dari molekul pati di dalam granula.
Makin besar derajat kristalisasi dari granula pati, pembentukkan gel semakin lambat.
Menurut Pomeranz (1991), tidak semua granula pati tergelatinasi pada titik yang sama, tetapi terjadi pada suatu kisaran suhu tertentu. Proses gelatinasi melibatkan peristiwa-peristiwa sebagai berikut:
a. hidrasi dan swelling (pengembangan) granula b. hilangnya sifat birefringent
c. peningkatan kejernihan
d. peningkatan konsistensi dan pencapaian viskositas puncak e. pemutusan molekul-molekul linier
f. penyebarannya dari granula yang telah pecah.
10
pati menjadi lebih lambat, akibatnya suhu gelatinasi akan lebih tinggi. Adanya gula akan menyebabkan gel lebih tahan terhadap kerusakan mekanik (Winarno, 2002).
2.4Allopurinol 2.4.1 Tinjauan umum
Rumus molekul : C5H4N4O
Nama kimia : 1H-Pirazolol[3,4-d]pirimidin-4-ol[315-30-0] Berat molekul : 136,11
Pemerian : Serbuk halus putih hingga hampir putih, berbau lemah.
Kelarutan : Sangat sukar larut dalam air dan etanol; larut dalam kalium dan natrium hidroksida; praktis tidak larut dalam kloroform dan dalam eter (Ditjen POM, 1995).
Gambar 2.3. Rumus Bangun Alopurinol (Ditjen POM, 1995).
2.4.2 Farmakologi
Allopurinol bekerja dengan cara mengurangi sintesa asam urat atas dasar persaingan substrat dengan zat-zat purin berlandaskan enzim xanthin oksidase. Enzim yang mengubah hipoxantin menjadi xantin dan selanjutnya menjadi asam urat. Melalui mekanisme umpan balik allopurinol menghambat sintesa purin yang merupakan prekursor xanthin (Katzung, 2004).
11
Allopurinol di dalam tubuh mengalami metabolisme menjadi oksipurinol (alloxantin) yang juga bekerja sebagai penghambat enzim xantin oksidase. Mekanisme kerja senyawa ini berdasarkan katabolisme purin dan mengurangi produksi asam urat, tanpa mengganggu biosintesa purin. Allopurinol dapat meningkatkan frekuensi serangan artritis gout akut sehingga sebaiknya obat anti inflamasi atau kolkisin diberikan bersama pada awal terapi (Katzung, 2004).
Allopurinol kira-kira 80% diserap setelah pemakaian oral.
Persenyawaan hasilnya oksipurinol mempertahankan kemampuannya untuk
menghambat xanthine oxidase dan mempunyai durasi kerja yang cukup
panjang sehingga allopurinol cukup diberikan satu kali sehari (Katzung, 2004).
2.5 Pengertian Tablet
Tablet adalah sediaan padat yang mengandung bahan obat dengan atau tanpa bahan pengisi. Sebagian besar tablet dibuat dengan cara pengempaan dan merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan baja. Tablet dibuat dengan berbagai ukuran, bentuk dan penandaan permukaan tergantung pada desain cetakan (Ditjen POM, 1995).
Untuk mendapatkan tablet yang baik, maka bahan pengisi yang akan dikempa menjadi tablet harus memenuhi sifat- sifat berikut :
12
b. kompatibel, artinya bahan mudah kompak jika dikempa, sehingga dihasilkan tablet yang keras.
c. mudah lepas dari cetakan, hal ini dimaksudkan agar tablet yang dihasilkan mudah lepas dan tidak ada bagian yang melekat pada cetakan, sehingga permukaan tablet halus dan licin (Sheth, dkk., 1980).
Tablet dibuat dengan 3 cara umum yaitu : Granulasi basah, granulasi kering dan cetak langsung. Tujuan granulasi basah dan kering adalah untuk meningkatkan aliran campuran dan atau kemampuan kempa. Granulasi kering dibuat dengan cara menekan massa serbuk pada tekanan tinggi sehingga menjadi tablet yang besar kemudian digiling dan diayak hingga diperoleh granul dengan ukuran partikel yang diinginkan. Cetak langsung merupakan pengempaan langsung dengan kecepatan tinggi tanpa tahap granulasi terlebih dahulu (Ditjen POM, 1995).
2.6 Metode Granulasi Basah
Metode ini merupakan metode pembuatan yang paling banyak digunakan dalam memproduksi tablet kompresi. Langkah-langkah yang diperlukan dalam pembuatan tablet dengan metode ini dapat dibagi sebagai berikut: menimbang dan mencampur bahan-bahan, pembuatan granulasi basah, pengayakan granul basah, pengeringan, pengayakan granul kering, pencampuran bahan pelicin dan bahan penghancur, pembuatan tablet dengan kompresi (Ansel, 1989).
13
menjadi granul, dan dikeringkan dalam almari pengering pada suhu 40oC - 50oC. Setelah kering diayak lagi untuk memperoleh granul dengan ukuran yang diperlukan dan ditambahkan bahan pelicin dan dicetak menjadi tablet dengan mesin tablet (Ansel, 1989).
2.7 Teori Pencampuran
Proses pencampuran merupakan proses yang sangat penting sebelum dilakukan pencetakan tablet. Pencampuran bertujuan untuk memperolah campuran homogen antar partikel-partikel penyusunnya, pencampuran yang kurang baik atau tidak homogen akan menyebabkan kadar zat aktif dalam tablet kurang seragam (Parrott, 1971).
Campuran yang homogen pada pencampuran serbuk dipengaruhi oleh bentuk partikel. Bentuk partikel berpengaruh terhadap gerakan partikel pada waktu pencampuran. Partikel-partikel yang ideal berbentuk bola karena lebih mudah bergerak, sedangkan partikel yang berbentuk jarum dan partikel yang tidak teratur lebih sukar bergerak dan membentuk agregat (Parrott, 1971).
14
Kelengketan dan kelicinan, untuk bahan yang bersifat lengket, maka pada proses pencampuran partikelnya akan bergerombol satu sama lain dan melekat pada dinding mixer sehingga proses pencampuran akan lebih sukar, lain halnya bila didapatkan bahan yang licin, bahan tersebut akan membantu dalam proses pencampuran. Kelembaban, pengaruh kelembaban tinggi yang dominan adalah gaya kapiler, gaya ini mengakibatkan bahan cenderung menggumpal dan melekat pada dinding mixer, sedangkan pada kelembaban yang rendah gaya yang dominan adalah gaya elektrostatik, gaya ini menyebabkan partikel-partikel menjadi bermuatan, cenderung membentuk agregat dan mengalami segregasi. Lama campuran, keefektifan waktu yang digunakan untuk proses pencampuran akan mempengaruhi hasil pencampuran karena campuran yang sudah homogen bila proses pencampurannya dilanjutkan maka pada waktu tertentu tidak homogen lagi (Parrott, 1971).
2.8 Uji Preformulasi
Untuk menghasilkan tablet yang baik maka perlu diketahui sifat fisis dari campuran bahan yang akan dicetak, pemeriksaan kualitas campuran bahan meliputi :
2.8.1 Waktu alir
15
waktu alir yaitu sifat-sifat granul yaitu ukuran partikel, distribusi ukuran partikel dan kelembaban (Lachman, dkk., 1994).
2.8.2 Sudut diam
Sudut diam yaitu sudut tetap yang terjadi antara timbunan partikel bentuk kerucut dengan bidang horisontal. Besar kecilnya sudut diam dipengaruhi oleh bentuk, ukuran dan kelembapan granul. Granul atau serbuk kualitas farmasi mempunyai sudut diam 20° - 40°, sudut yang lebih kecil menunjukkan sifat alir yang baik (Lachman, dkk., 1994).
2.8.3 Indeks tap
Uji indeks tap dilakukan untuk mengamati penurunan jumlah serbuk/granul akibat adanya gaya hentakan, juga untuk mengetahui secara tidak langsung perilaku sifat alir sewaktu kompresi/pencetakan tablet, sifat alir dikatakan baik apabila indeks tap kurang dari 20% (Voight, 1994).
2.9 Pemeriksaan Kualitas Tablet
Pemeriksaan kualitas tablet dilakukan untuk mengetahui mutu fisik dari tablet yang dihasilkan, pemeriksaan kualitas tablet meliputi :
2.9.1 Kekerasan tablet
16
rapuh, tapi bila kekerasan tablet lebih besar dari 8 kg akan didapatkan tablet yang cenderung keras (Parrott, 1971).
Faktor-faktor yang mempengaruhi kekerasan tablet adalah tekanan pada saat pentabletan, sifat bahan yang dikempa serta jumlah serta jenis bahan obat yang ditambahkan saat pentabletan akan meningkatkan kekerasan tablet (Ansel, 1989).
2.9.2 Kerapuhan tablet
Kerapuhan adalah parameter lain dari ketahanan tablet dalam melawan pengikisan dan goncangan, besaran yang dipakai adalah % bobot yang hilang selama pengujian dengan alat friabilator. Faktor-faktor yang mempengaruhi kerapuhan antara lain banyaknya kandungan serbuk (fitnes), kerapuhan di atas 1% menunjukkan tablet yang rapuh dan dianggap kurang baik (Lachman, dkk., 1994).
2.9.3 Waktu hancur tablet
Waktu hancur tablet adalah waktu yang dibutuhkan untuk hancurnya tablet dalam medium yang sesuai sehingga tidak ada bagian tablet yang tertinggal di atas kasa alat pengujian. Faktor-faktor yang mempengaruhi waktu hancur adalah sifat fisika kimia granul dan kekerasan tablet, kecuali dinyatakan lain, waktu hancur tablet tidak bersalut tidak boleh lebih dari 15 menit (Lachman, dkk., 1994).
Waktu hancur yang semakin cepat maka akan semakin cepat pula pelarutan dari bahan berkhasiat sehingga akan lebih cepat berkhasiat dalam tubuh
2.9.4 Keseragaman sediaan
Keseragaman sediaan dapat ditetapkan dengan dua cara, yaitu :
17
2. Keseragaman kandungan, dilakukan terhadap tablet yang 50% bahan aktifnya
urang dari 50 mg. (Ditjen POM, 1995)
2.9.5 Uji penetapan kadar zat berkhasiat
Uji penetapan kadar zat berkhasiat dilakukan untuk mengetahui apakah tablet tersebut memenuhi syarat sesuai dengan etiket. Bila kadar obat tersebut tidak memenuhi syarat maka obat tersebut tidak memiliki efek terapi yang baik dan tidak layak di konsumsi. Uji penetapan kadar dilakukan dengan menggunakan cara-cara yang sesuai pada masing-masing monografi antara lain di Farmakope Indonesia (Dirjen POM RI, 1995).
2.9.6 Disolusi
Disolusi adalah proses melarutnya suatu obat (Ansel, 1989). Saat sekarang ini disolusi dipandang sebagai salah satu uji pengawasan mutu yang paling penting dilakukan pada sediaan farmasi. Pada uji disolusi dapat diketahui bahan obat dalam larutan dengan kecepatan yang seharusnya. Cepatnya obat atau tablet melarut menentukan kadar bahan berkhasiat terlepas didalam tubuh. Karena itu laju larut berhubungan langsung dengan kemanjuran dari tablet dan perbedaan bioavaibilitas dari berbagai formula (Lachman, dkk., 1994).
18
yang terlarut. Tablet harus memenuhi persyaratan seperti yang terdapat dalam monografi untuk kecepatan disolusi (Ansel, 1989).
2.10Spektrofotmetri
Spektrofotometri UV-Vis adalah pengukuran panjang gelombang dan intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi oleh sampel. Sinar ultraviolet dan cahaya tampak memiliki energi yang cukup untuk mempromosikan elektron pada kulit terluar ke tingkat energi yang lebih tinggi (Dachriyanus, 2004).
2.10.1 Instrumen
Menurut Khopkar (1990), suatu spektrofotometer tersusun dari: a. Sumber
Sumber yang biasa digunakan adalah lampu wolfram. Tetapi untuk daerah UV digunakan lampu hydrogen atau lampu deuterium. Kebaikan lampu wolfram adalah energi radiasi yang dibebaskan tidak bervariasi pada berbagai panjang gelombang. Untuk memperoleh tegangan yang stabil dapat digunakan transformator. Jika potensial tidak stabil, kita akan mendapatkan energi yang bervariasi. Untuk mengompensasikan hal ini maka dilakukan pengukuran transmitan larutan sempel selalu di sertai larutan pembanding.
b. Monokromator
Digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya berupa prisma ataupun grating. untuk mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian dapat digunakan celah.
19
Pada pengukuran di daerah tampak kuvet kaca dapat digunakan, tetapi untuk pengukuran pada daerah UV kita harus menggunakan sel kuarsa karena gelas tidak tembus cahaya pada daerah ini. Umumnya tebal kuvetnya adalah 10 mm, tetapi yang lebih kecil ataupun yang lebih besar dapat digunakan. Sel yang biasa digunakan berbentuk persegi, tetapi bentuk silinder dapat juga digunakan. Kita harus menggunakan kuvet untuk pelarut organik. Sel yang baik adalah kuarsa atau gelas hasil leburan serta seragam keseluruhannya.
d. Detektor
Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang. Pada spektrofotometer, tabung pengganda elektron yang di gunakan prinsip kerjanya telah diuraikan.
2.10.2 Penggunaan
Menurut Rohman dan Ganjar (2007), metode spektrofotometri UV-Vis digunakan untuk menetapkan kadar senyawa obat dalam jumlah yang cukup banyak. Cara untuk menetapkan kadar sampel adalah dengan menggunakan perbandingan absorbansi sampel dengan absorbansi baku, atau dengan menggunakan persamaan regresi linier yang menyatakan hubungan antara konsentrasi baku dengan absorbansinya. Persamaan kurva baku selanjutnya digunakan untuk menghitung kadar dalam sampel.
Analisis kuantitatif dengan metode spektofotometri UV-Vis dapat digolongkan atas tiga macam pelaksanaan pekerjaan, yaitu:
a. analisis zat tunggal atau analisis satu komponen
20
21
BAB III
METODE PENELITIAN
3.1 Metode Pembuatan
Metode yang digunakan adalah metode eksperimental meliputi isolasi pati jagung, pembuatan pati jagung gelatinasi, karakterisasi pati jagung gelatinasi, uji preformulasi, pencetakan tablet dan evaluasi tablet.
3.2 Alat
Alat-alat yang digunakan dalam penelitian ini adalah mesin pencetak tablet single punch (Erweka), Desintegran Tester (Copley), Friabilator (Copley), hot plate, neraca listrik (Sartorius), oven, spektrofotometer UV/Vis (Shimadzu), stopwatch, termometer, Strong Cobb Hardness Tester (Copley), Disolution tester (Veego) dan alat-alat gelas.
3.3 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah Allopurinol, Pati Jagung Gelatinasi, Pati Jagung Alami, Laktosa, Mg stearat, Talkum, Amilum Manihot, Aquades, dan HCl 0,1 N.
3.4Pembuatan Pereaksi HCl 0,1 N
22
3.5Penyiapan Bahan Tumbuhan 3.5.1 Pengumpulan bahan tumbuhan
Metode pengumpulan bahan tumbuhan dilakukan secara purposive yaitu tidak membandingkan dengan bahan tumbuhan yang sama dari daerah lain. Sampel yang digunakan adalah jagung lokal yang berumur 60 - 70 hari yang sudah tua tapi masih segar. Jagung diambil dari Jalan Raya Sunggal, Kecamatan Medan Sunggal, Sumatera Utara. Gambar jagung yang diambil dapat dilihat pada lampiran 4.
3.5.2 Identifikasi tumbuhan
Identifikasi tumbuhan di Herbarium Medanense, Universitas Sumatera Utara. Hasil identifikasi dapat dilihat pada lampiran 3.
3.6 Prosedur Penelitian 3.6.1 Isolasi pati jagung
Pati jagung diperoleh dengan cara memisahkan biji jagung dari tongkolnya. Ditimbang sebanyak 11,5 kg jagung pipil dan dicuci sampai bersih. Jagung pipil ditambahkan air dan dihaluskan dengan menggunakan blender sampai diperoleh massa seperti bubur. Lalu diperas dengan menggunakan kain blacu berwarna putih dan bersih. Filtrat direndam lebih kurang selama 24 jam, lalu cairan atas dibuang dan dilakukan pencucian dengan cara menambahkan air suling secara berulang-ulang sampai diperoleh pati yang berwarna putih. Pati yang diperoleh selanjutnya dikeringkan di bawah sinar matahari, kemudian dikeringkan di oven 60°C dihitung rendemennya.
% Rendemen = Berat Pati
23
3.6.2 Pembuatan pati jagung gelatinasi
Timbang 80 gram pati jagung alami kemudian disuspensikan dalam 1000 ml air (8% b/v) lalu dipanaskan di atas termostat pada suhu 70°C aduk perlahan-lahan agar amilum terdispersi merata. Suhu dibiarkan stabil pada suhu 70°C sambil tetap diaduk sampai kental, kemudian didinginkan. Suspensi setelah mencapai suhu kamar dikeringkan dalam lemari pengering di atas porselin dengan suhu 60°C selama satu malam, maka akan terbentuk slug (lembaran padat) dari amilum gelatinasi, kemudian dipecah-pecah atau dihaluskan menggunakan lumpang. Hasilnya di timbang.
3.7 Pemeriksaan Karakteristik Pati Jagung Gelatinasi 3.7.1 Distribusi ukuran partikel
Distribusi ukuran partikel ditentukan dengan ayakan mesh 20, mesh 60 dan mesh 100. Dimana pati jagung gelatinasi disaring dengan ayakan mesh 20, 60 dan 100 (Voight, 1994).
3.7.2 Kelarutan
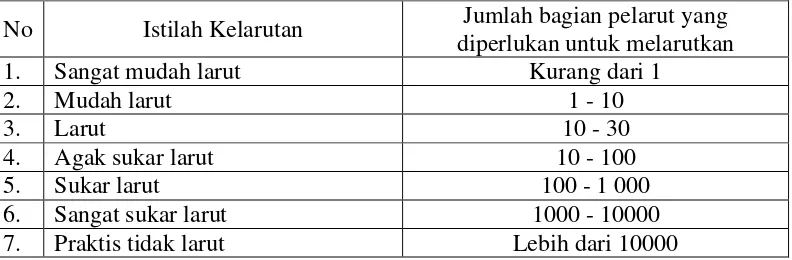
Kelarutan pati jagung alami dan pati jagung gelatinasi diukur di dalam air. Menurut Anief (2007) kelarutan suatu zat yang tidak diketahui secara pasti dapat dinyatakan dengan istilah berikut:
Tabel 3.1 Istilah kelarutan
No Istilah Kelarutan Jumlah bagian pelarut yang diperlukan untuk melarutkan
24
Uji kelarutan dilakukan dengan cara melarutkan 1 gram pati jagung alami atau pati jagung gelatinasi dalam sejumlah tertentu air. Jumlah air ditambahkan dimulai dari jumlah pelarut pada istilah kelarutan sangat mudah larut yaitu kurang dari 1. Apabila pati jagung alami atau pati jagung gelatinasi tidak larut ditambahkan jumlah pelarut pada istilah mudah larut dan seterusnya.
3.7.3 Berat jenis
Pati jagung gelatinasi dimasukkan ke dalam gelas ukur 50 ml lalu dilihat volume awal. Lalu gelas ukur di tap sebanyak 15 kali setelah itu dilihat volumenya. Kemudian pati jagung gelatinasi ditimbang. Lalu berat jenis dihitung dengan rumus: BJ: Berat / Volume
Lalu dihitung bobot jenis dengan rumus:
Bobot jenis = 100%
Keterangan: BJ = Berat Jenis
3.7.4 Mikroskopik
Pati diletakkan di atas objek glass ditambah aquades, lalu ditutup dengan dec glass. Lihat di bawah mikroskop dengan perbesaran 10x40.
3.8 Pembuatan Tablet
25
Formula: R/ Allopurinol 100 mg
Pati jagung gelatinasi % bervariasi (F2-F7 )
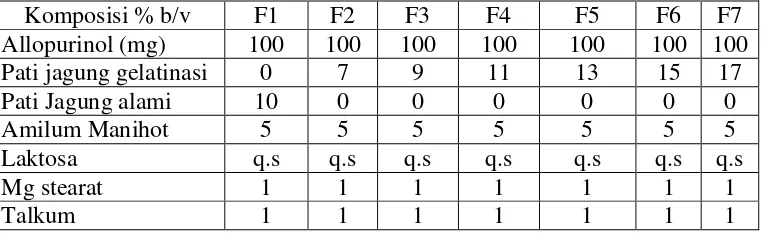
Tabel 3.2 Formula tablet allopurinol
Komposisi % b/v F1 F2 F3 F4 F5 F6 F7
26
3.9 Uji Preformulasi 3.9.1 Sudut diam
Massa granul sebanyak 100 gram dimasukkan ke dalam corong yang telah dirangkai, permukaannya diratakan. Lalu penutup bawah corong dibuka, biarkan granul mengalir sampai habis. Tinggi kerucut yang terbentuk diukur.
Sudut diam diukur dengan rumus:
tg ø = 2h/ D
Keterangan : ø = sudut diam
D = diameter
h= tinggi kerucut (cm )
Persyaratan: Uji dikatakan memenuhi syarat apabila berada pada 20°< 0 > 40°(Cartensen, 1977).
3.9.2 Waktu alir
Uji waktu alir dilakukan menurut metode yang dibuat oleh Cartensen (1977). Granul sebanyak 100 gram dimasukkan ke dalam corong yang telah dirangkai, kemudian permukaannya diratakan. Penutup bawah corong dibuka dan secara serentak stopwatch dihidupkan. Stopwatch dihentikan saat granul telah habis melewati corong dan dicatat waktu alirnya.
Persyaratan: Granul harus habis mengalir dalam waktu lebih singkat dari 10 detik (Lachman, dkk., 1994).
3.9.3 Indeks tap
Ke dalam gelas ukur 100 ml, dimasukkan sejumlah granul hingga 100 ml. Ditap dengan alat yang dimodifikasi sampai konstan. Setelah hentakan, volumenya dihitung dengan rumus:
27
Dimana: V1 = Volume sebelum hentakan V2 = Volume setelah hentakan
Persyaratan: Granul akan mempunyai sifat alir yang baik jika mempunyai indeks tap lebih kecil 20% (Lachman, dkk., 1994).
3.10 Evaluasi Tablet 3.10.1 Uji kekerasan tablet
Alat: Strong Cobb Hardness Tester (Copley)
Tablet diletakkan pada tempat yang tersedia pada alat dengan posisi tidur, alat diatur, kemudian ditekan tombol start. Pada saat tablet pecah angka yang tertera pada layar digital dicatat. Percobaan ini dilakukan untuk 5 tablet.
Persyaratan: Kekerasan tablet antara 4-8 kg (Soekemi, dkk., 1987).
3.10.2 Uji kerapuhan (friabilitas)
Alat: Friabilator (Copley)
Sebanyak 20 tablet yang telah dibersihkan dari debu ditimbang (W1), kemudian kerapuhannya diuji di dalam alat uji friabilitas dengan putaran 25 rpm selama 4 menit. Tablet dikeluarkan dan dibersihkan dari debu. Bobot akhir ditimbang (W2).
% kerapuhan = (w1-w2) /w1 x 100%
Persyaratan: kehilangan berat tablet ≤ 0,8% (Voight, 1994).
3.10.3 Uji waktu hancur
Alat: Desintegration Tester (Copley)
28
Dicelupkan pada air dengan suhu 370C (±10C) dengan tinggi air tidak boleh kurang dari 15 cm, sehingga tabung dapat dinaik turunkan secara teratur 30 kali permenit. Pada kedudukan tertinggi, kawat kasa tepat pada permukaan air, angkat keranjang dan amati seluruh tablet. Tablet dinyatakan hancur jika tidak ada lagi tablet yang tertinggal pada kawat kasa dan dicatat waktu setiap tablet hancur.
Persyaratan: waktu yang dibutuhkan untuk menghancurkan keenam tablet tidak boleh lebih dari 15 menit (Ditjen POM, 1979).
3.10.4 Penetapan kadar
3.10.4.1 Penentuan kurva serapan dan linieritas kurva kalibrasi allopurinol dalam larutan HCl 0,1 N
a. Pembuatan larutan induk baku dalam HCl 0,1 N
Ditimbang 25 mg bahan baku Allopurinol, dimasukkan ke dalam labu tentukur 50 ml. Ditambahkan sedikit HCl 0,1 N dikocok sampai larut, lalu dicukupkan HCl 0,1 N dengan sampai garis tanda, konsentrasi teoritis adalah 500 mcg/ml (LIB I). Selanjutnya dipipet sebanyak 10 ml dari LIB I lalu dimasukkan ke dalam labu tentukur 50 ml lalu dicukupkan dengan HCl 0,1 N sampai garis tanda, kemudian dikocok hingga homogen, sehingga diperoleh larutan dengan konsentrasi teoritis 100 mcg/ml (LIB II).
b .Pembuatan kurva serapan dalam HCl 0,1 N
29
c. Pembuatan kurva kalibrasi
Dipipet LIB II sebanyak (konsentrasi 100 mcg/ml) masing-masing 1,5 ml; 2,5 ml; 3,5 ml;4,5 ml; dan 5,5ml. Masing-masing dimasukkan ke dalam labu tentukur 50 ml, dicukupkan dengan HCl 0,1 N sampai garis tanda. Dikocok homogen sehingga diperoleh larutan dengan konsentrasi 3,0 µg/ml; 5,0 µg/ml; 7,0 µg/ml; 9,0 µg/ml; 11,0 µg/ml. Diukur serapannya pada panjang gelombang maksimum.
3.10.4.2 Penetapan kadar allopurinol
Ditimbang 20 tablet, dicatat beratnya, kemudian digerus sampai homogen. Ditimbang sejumlah serbuk setara dengan 50 mg Allopurinol, kemudian dimasukkan ke dalam labu tentukur 100 ml, tambahkan sedikit HCl 0,1 N kocok hingga larut, tambahkan HCl 0,1 N sampai garis tanda, konsentrasi teoritis 500 mcg/ml. Saring dengan kertas saring, filtrat pertama dibuang 10 ml.
Dari larutan ini pipet 10 ml, masukkan ke dalam labu tentukur 50 ml, encerkan dengan HCl 0,1 N sampai garis tanda. Diperoleh konsentrasi Allopurinol 100 mcg/ml. Selanjut nya dipipet 2 ml. filtrat dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan dengan HCl 0,1 N sampai garis tanda dikocok hingga homogen maka konsentrasi teoritis allopurinol 8 mcg/ml. Kemudian ukur serapannya pada panjang gelombang maksimum yang diperoleh, menggunakan HCl 0,1 N sebagai blanko. Selanjutnya dihitung kadar alopurinol di dalam sampel menggunakan persamaan garis regresi.
Persyaratan: tablet alopurinol mengandung Allopurinol C5H4N4O tidak
30
3.10.5 Keragaman sediaan
Uji keseragaman sediaan pada penelitian ini dilakukan uji keseragaman kandungan karena bobot Allopurinol tiap tablet adalah 100 mg dan bobot satu tablet adalah 250 mg pada F1 dan F2 serta 300 mg pada F3 sampai F7, maka bobot Allopurinol tiap tablet sama dengan 40% pada F1 dan F2 serta 33,3% pada F3 sampai F7 dari bobot tablet.
Diambil secara acak 10 tablet dari masing-masing formula tablet Allopurinol yang dibuat lalu masing-masing digerus dan ditimbang setara 50 mg dimasukkan ke dalam labu tentukur 100 ml dan dilarutkan dengan lalu dicukupkan dengan HCl 0,1 N sampai garis tanda. Dipipet 10 ml lalu dimasukkan ke dalam labu tentukur 50 ml, ditambahkan dengan HCl 0,1 N sampai garis tanda, dipipet 2,0 ml dimasukkan ke dalam labu tentukur 25 ml dicukupkan dengan HCl 0,1 N sampai garis tanda, diukur pada panjang gelombang yang diperoleh dihitung kadar dari masing-masing tablet dan persen simpangan baku relative (%RSD).
Persyaratan keseragaman sediaan dipenuhi jika jumlah zat aktif dalam masing-masing antara 85,0% sampai 115,0% dari yang tertera pada etiket dan simpangan baku relatif kurang atau sama dengan 6,0% (Ditjen POM, 1995).
3.10.6 Uji disolusi
3.10.6.1 Penentuan kurva serapan dan linieritas kurva kalibrasi allopurinol dalam larutan HCl 0,1 N
a. pembuatan larutan induk baku dalam HCl 0,1 N
31
dicukupkan HCl 0,1 N dengan sampai garis tanda, konsentrasi teoritis adalah 500 mcg/ ml (LIB I). Selanjutnya dipipet sebanyak 10 ml dari LIB I lalu dimasukkan ke dalam labu tentukur 50 ml lalu dicukupkan dengan HCl 0,1 N sampai garis tanda, kemudian dikocok hingga homogen, sehingga diperoleh larutan dengan konsentrasi teoritis 100 mcg/ ml (LIB II).
b. pembuatan kurva serapan dalam HCl 0,1 N
Dipipet LIB II sebanyak 2 ml, lalu dimasukkan kedalam labu tentukur 25 ml dan ditambahkan larutan HCl 0,1 N hingga garis tanda, kemudian dikocok homogen sehingga diperoleh larutan dengan konsentrasi teoritis 8 mcg/ ml. Diukur pada panjang gelombang 200 - 400 nm dan sebagai blanko digunakan HCl 0,1 N.
c. pembuatan kurva kalibrasi
Dipipet LIB II sebanyak (konsentrasi 100 µg/ml) masing-masing 1,5 ml; 2,5 ml; 3,5 ml;4,5 ml; 5,5ml, masing- masing dimasukkan ke dalam labu tentukur 50 ml, dicukupkan dengan HCl 0,1 N sampai garis tanda. Dikocok homogen sehingga diperoleh larutan dengan konsentrasi 3,0 µg/ml; 5,0 µg/ml; 7,0 µg/ml; 9,0 µg/ml; 11,0 µg/ml. Diukur serapannya pada panjang gelombang maksimum.
3.10.6.2 Pengujian disolusi tablet
Uji laju disolusi tablet dilakukan dengan menggunakan alat dissolution tester.
Medium : 900 ml HCl 0,1 N Alat : tipe II (metode dayung) Kecepatan putaran : 75 rpm
32
Toleransi (Q) : 75%
Satu tablet dimasukkan dalam wadah disolusi yang berisi 900 ml medium disolusi dengan suhu 370 ± 0,50C. Kemudian diputar dengan kecepatan 75 rpm. Pada waktu 45 menit, larutan adekuat dipipet sebanyak 5 ml dan dimasukkan dalam labu tentukur 100 ml. Selanjutnya larutan yang telah dipipet di dalam labu tentukur 100 ml, diencerkan dengan HCl 0,1 N sampai garis tanda, dan diukur serapannya pada panjang gelombang maksimum yang diperoleh, dan sebagai blanko digunakan HCl 0,1 N. Lalu kadarnya dihitung dengan persamaan regresi. Pengujian dilakukan terhadap 6 tablet.
Dalam waktu 45 menit Allopurinol harus larut tidak kurang dari 75% (Q) dari jumlah yang tertera pada etiket.Toleransi (Q) dan jumlah yang tertera pada etiket yang dapat dilihat pada tabel 3.3.
Tabel 3.3 Kriteria penerimaan zat aktif larut dengan disolusi Tahap Jumlah yang Diuji Kinerja penerimaan
S1 6 Tiap unit sediaan tidak kurang dari Q + 5% S2 6 Rata-rata dari 12 unit ( S1+S2) adalah sama
atau lebih besar dari Q dan tidak satu unit sediaan yang lebih kecil dari Q – 15% S3 12 Rata-rata dari 24 unit (S1+S2+S3) adalah
sama atau lebih besar dari Q, tidak lebih dari 2 unit sediaan yang lebih kecil dari Q– 15% dan tidak satu unit pun yang lebih kecil dari Q – 25%.
(Ditjen POM,1995)
3.11 Analisa Data Secara Statistik
33
inerfrensi untuk diuji normalitas data. Uji normalitas data bertujuan untuk mendeteksi distribusi data atau variable yang digunakan dalam penelitian. Data yang terdistribusi normal merupakan syarat untuk pengujian statistik parametrik, sementara data yang tidak terdistribusi normal pengujian menggunakan statistic nonparametrik. Uji normalitas menggunakan uji Kolmogorov-Smisnov. Hasil analisis data dilihat nilai signifikannya. Jika nilai (p > 0.05) maka H0 diterima,
34
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Sampel
Hasil identifikasi tumbuhan yang dilakukan di Herbarium medanese, Universitas Sumatera Utara menunjukkan bahwa tumbuhan yang diteliti termasuk spesies Zea MaysL dari suku Poaceae.
4.2 Pati Jagung Alami
Berat biji jagung setelah di pipil 11,5 kg. berat pati jagung alami yang didapatkan 915,8 gram.
% Rendemen = Berat Pati
Berat biji jagung segar x 100% =
0,9158
11,5 x 100% = 7,96%
4.3 Pati Jagung Gelatinasi 4.3.1 Distribusi ukuran partikel
Ukuran partikel pati jagung alami dan jagung gelatinasi diperoleh dari pengayakan dengan ayakan bertingkat yaitu mesh 20, 60 dan 100. Sehingga didapatkan masing-masing berat dari ukuran partikel mesh 20, 60, dan 100. Hasil data ukuran partikel dapat dilihat pada Tabel 4.1.
Tabel 4.1 Data ukuran partikel pati jagung alami dan jagung gelatinasi
35
Berdasarkan Tabel 4.1 dan Gambar 4.1 dapat dilihat bahwa pati jagung alami lebih banyak tertahan pada ayakan mesh 100 yaitu 59,26%. Sedangkan pati jagung gelatinasi distribusi ukuran partikelnya terpusat pada ayakan mesh 60 sebanyak 72,41% yang tertinggal dalam ayakan. Pati jagung alami menunjukkan distribusi ukuran partikel yang lebih sempit dibandingkan dengan pati jagung gelatinasi.
Gambar 4.1 Presentase ukuran partikel pati jagung gelatinasi
Gambar 4.1 dapat diketahui bahwa ukuran partikel pati jagung gelatinasi mesh 60 lebih besar presentasenya dibandingkan dengan ukuran partikel dengan mesh 20 dan mesh 100.
4.3.2 Kelarutan
Uji kelarutan dilakukan untuk mengetahui kelarutan pati jagung alami dan pati jagung gelatinasi didalam air. Hasil data kelarutan pati jagung gelatinasi dapat dilihat pada Tabel 4.2
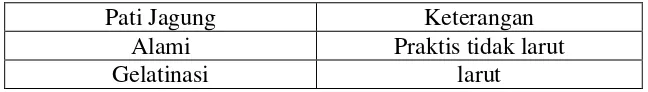
Tabel 4.2 Data kelarutan pati jagung alami dan pati jagung gelatinasi
Pati Jagung Keterangan
Alami Praktis tidak larut
Gelatinasi larut
Mesh 20 Mesh 60 Mesh 100
36
Berdasarkan data dari Tabel 4.2 di atas dapat dijelaskan bahwa pati jagung gelatinasi lebih mudah larut di dalam air dibandingkan dengan pati jagung alami. Hal ini dikarenakan pati jagung gelatinasi memiliki sifat umum yaitu terdispersi di dalam air (Winarno, 1995).
4.3.3 Bobot jenis
Berat seluruh pati gelatinasi 17,9 gram. Volume awal pati gelatinasi sebelum ditap adalah 25 ml, sedangkan volume pati gelatinasi setelah ditap adalah 23 ml.
Berdasarkan perhitungan di atas didapat bahwa bobot jenis pati jagung gelatinasi sebesar 7,852%. Menurut Aulton (1988), pati yang memiliki nilai bobot jenis kurang dari 18% biasanya memberikan sifat alir yang baik.
4.3.4 Mikroskopik
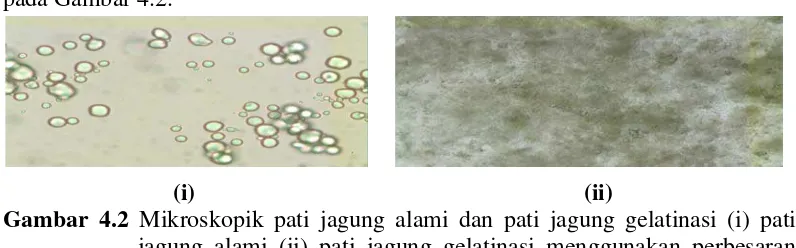
Uji mikroskopik dilakukan untuk mengetahui bentuk hilus dan lamella amilum di bawah mikroskop perbesaran 10x40. Hasil Mikroskopik dapat dilihat pada Gambar 4.2.
(i) (ii)
37
Uji mikroskopik pada amilum jagung alami memiliki bentuk bulat dan bersudut, tidak memiliki lamella, dan memiliki hillus yang terletak ditengah, hal ini sesuai dengan Farmakope Indonesia IV. Amilum jagung gelatinasi memiliki bentuk dan letak hilus yang sama dengan amilum jagung alami serta tidak memiliki lamella, hanya saja amilum gelatinasi memiliki susunan yang berbeda yaitu bergerombol serta memiliki ukuran yang lebih kecil. Ukuran partikelnya yang lebih kecil dibandingkan amilum alami diakibatkan oleh rusaknya struktur amilum pada proses gelatinasi.
4.4 Hasil Uji Preformulasi terhadap Massa Granul
Sebelum massa granul di cetak menjadi tablet umumnya harus melalui serangkaian uji preformulasi. Hal ini penting dilakukan untuk mengetahui kelayakan pencetakan suatu tablet. Pada Tabel 4.3 berikut ini adalah tabel hasil uji preformulasi berbagai formula yang dibuat.
Tabel 4.3 Data uji preformulasi massa granul formula tablet
Formula Waktu Alir (detik) Sudut diam (o) Indeks Tap (%)
38
F7 : Formula tablet dengan konsentrasi pati jagung gelatinasi 17%
4.4.1 Uji waktu alir
Berdasarkan Tabel 4.3 dan gambar 4.3 waktu alir granul dengan bahan pengikat pati jagung gelatinasi dari formula F2 sampai dengan formula F7 terjadi penurunan, mulai dari F2 = 1,88 detik - F7 = 1,70 detik. Pada formula pembanding pati jagung alami mempunyai waktu alir paling tinggi yaitu 2,01 detik. Walaupun terjadi variasi waktu alir dari formula tersebut tetapi tetap masih berada dalam batas penerimaan. Granul dalam bentuk bulat dan permukaan halus akan lebih mudah untuk mengalir (Cartensen, 1977).
Konsentrasi pati jagung gelatinasi yang semakin besar, maka makin cepat waktu alirnya. Hal ini disebabkan karena pati jagung gelatinasi yang digunakan sebagai pengikat mampu membentuk granul, sehingga massanya semakin mudah mengalir yang menyebabkan waktu alir semakin cepat.
Gambar 4.3 Diagram hasil ujiwaktu alir massa granul
4.4.2 Sudut diam
Tabel 4.3 dan gambar 4.4 menjelaskan bahwa penurunan sudut diam dari formula F1-formula F7 yaitu : 35,25 - 28,36. Pada formula pati alami F1
menunjukkan sudut diam yang paling tinggi yaitu 35,25. Menurut (Cartensen, 1977),
39
40. Partikel dengan bentuk yang lebih spheris memberikan sudut diam yang lebih
rendah (Lachman, dkk., 1989).
Hasil uji sudut diam memperlihatkan bahwa dengan penambahan konsentrasi
pati jagung gelatinasi akan memperkecil sudut diam. Hal ini disebabkan semakin
banyak pati yang berbentuk granul akan mempunyai daya alir yang baik. Hal ini
menunjukkan bahwa pati jagung gelatinasi sebagai bahan pengikat memiliki efisiensi yang lebih tinggi dari pada menggunakan pati jagung alami, karena granul tablet yang terbuat dari pati jagung gelatinasi sebagai memiliki ukuran partikel yang lebih besar dibandingkan pati jagung alami. Semakin kecil ukuran partikel maka sudut diam yang terbentuk semakin besar (Voigt, 1994).
Gambar 4.4 Diagram hasil uji sudut diam massa granul
4.4.3 Indeks tap
40
Menurut (Guyot, 1978), granul yang bersifat mengalir bebas adalah partikel yang memiliki indeks tap ≤ 20%. Pengujian indeks tap memiliki peran yang sangat penting dalam hal daya tahan granul terhadap daya kompresi yang diberikan oleh alat pencetak tablet. Semakin rendah presentase indeks tap menunjukkan kualitas yang lebih baik dari sifat fisis massa granul yang akan diformulasikan ke dalam bentuk tablet.
Gambar 4.5 Diagram hasil uji indeks tap massa granul
4.5 Hasil Evaluasi Tablet
Tabel 4.4 Data hasil evaluasi tablet allopurinol
Formula Kekerasan
F1 : Formula tablet dengan konsentrasi pati alami 10%
41
F6 : Formula tablet dengan konsentrasi pati jagung gelatinasi 15% F7 : Formula tablet dengan konsentrasi pati jagung gelatinasi 17%
Evaluasi tablet allopurinol yang dilakukan adalah uji kekerasan tablet, waktu hancur, keseragaman kandungan, penetapan kadar dan uji disolusi tablet. Pada Tabel 4.4 berikut ini adalah tabel hasil uji evaluasi tablet dari berbagai formula yang dibuat.
4.5.1 Uji kekerasan tablet
Kekerasan tablet yang didapat semua memenuhi persyaratan dalam batas 4 - 8 kg. Dari Tabel 4.4 kekerasan tablet formula F1 sampai F7 berkisar 4 - 6 kg. Hal ini dapat menunjukkan bahwa kekerasan tablet dari F1 sampai F7 terjadi optimal. Kekerasan tablet dapat dilihat pada Gambar 4.6.
Gambar 4.6 Diagram hasil ujiKekerasan tablet
Gambar 4.6 menunjukkan kekerasan tablet F1 sebesar 5,65 kg, F2 sebesar 4,24 kg, F3 sebesar 4,53 kg, F4 sebesar 4,86 kg, F5 sebesar 5,07 kg, F6 sebesar 5,17 kg, F7 sebesar 5,47 kg. Dari data tersebut dapat diketahui bahwa kekerasan tablet terus meningkat dari F2 sampai F7 sebanding dengan peningkatan konsentrasi bahan pengikat pati jagung gelatinasi yang digunakan. Hal ini disebabkan karena pati jagung gelatinasi akan menambah gaya lekat (kohesi) antara partikel sehingga kerapatan granul-granul akan semakin tinggi, maka
42
dengan tekanan kompressi yang sama akan dihasilkan kekerasan tablet yang semakin tinggi.
Menurut Lachman, dkk., (1994), perbedaan kekerasan dapat terjadi karena beberapa faktor seperti perbedaan jumlah massa granul yang mengisi die pada saat pencetakan tablet. Selain itu, berbedanya nilai kekerasan juga dapat diakibatkan jumlah bahan tambahan yang digunakan pada formulasi.
4.5.2 Uji waktu hancur
Tabel 4.4 menunjukkan hasil pengujian waktu hancur untuk formula F1 sampai F7 berkisar 1 - 3 menit. Dari data di atas formula F2-F7 yang menggunakan pati jagung gelatinasi sebagai pengikat memiliki waktu hancur yang lebih cepat dibandingkan formula F1. Walaupun perbedaannya tidak terlalu jauh. Dimana F7 dengan pati jagung gelatinasi 17% waktu hancurnya hanya 1,40 menit, tetapi pada F1 dengan pati jagung alami 10% waktu hancur tablet 3,14 menit. Hal ini menunjukkan bahwa bahan pengikat pati jagung gelatinasi lebih baik dari pada pati jagung alami. Terbukti dengan konsentrasi pati jagung gelatinasi yang lebih besar tapi waktu hancur nya lebih cepat dari pada pati jagung alami. Waktu hancur yang semakin cepat maka akan semakin cepat pula pelarutan dari bahan berkhasiat sehingga akan cepat berkhasiat dalam tubuh (Hastuti, 2008).
43
4.5.3. Uji friabilitas
Berdasarkan data dari Tabel 4.4, maka hasil pengujian friabilitas untuk formula F2-F7 berkisar 0,20% - 0,05%. Sedangkan hasil friabilitas pada formula F1 0,03%. Pada formula F2-F7 yang menggunakan pati jagung gelatinasi sebagai pengikat memiliki nilai friabilitas yang lebih besar dibandingkan formula F1 menggunakan pati jagung alami. Friabilitas berkaitan dengan kekerasan tablet, jika kekerasan tablet semakin kecil maka ikatan antara granul menjadi semakin longgar sehingga friabilitas tablet tersebut semakin besar. Pada formula F2-F7 menggunakan pati jagung gelatinasi sebagai pengikat. Hasil friabilitas yang didapat memenuhi persyaratan Farmasi industri yaitu di bawah 0,8%.
Gambar 4.8 Diagram hasil ujiFriabilitas tablet
Nilai friabilitas pada gambar 4.8 untuk formula F1 sebesar 0,03 %, F2 sebesar 0,2 %, F3 sebesar 0,2%, F4 sebesar 0,16%, F5 sebesar 0,09%, F6 sebesar 0,09%, dan F7 sebesar 0,05%. Hal ini menunjukkan bahwa friabilitas tablet dari formula F1 sampai F7 memenuhi persyaratan.
Tablet dikatakan baik apabila memiliki nilai friabilitas di bawah 0,8%, dimana uji friabilitas dilakukan untuk mengetahui keutuhan tablet, karena selama transfortasi, tablet mengalami benturan dengan dinding wadahnya. Semakin kecil
44
harga friabilitas maka semakin kecil angka kerapuhan tablet. Friabilitas suatu tablet dipengaruhi oleh kandungan air dari granul dan tablet (Lachman, dkk.,1994).
4.5.4 Hasil pembuatan kurva serapan dan kurva kalibrasi allopurinol serta penetapan kadar tablet allopurinol
4.5.4.1 Hasil penentuan panjang gelombang maksimum dalam HCl 0,1 N
Menurut Moffat (2005), Allopurinol memberikan serapan maksimum dalam pelarut asam pada panjang gelombang 250 nm. Dari hasil penentuan panjang gelombang maksimum diperoleh pada panjang gelombang maksimum yang sama dengan literatur yaitu 251 nm. Gambar kurva dan data serapan Allopurinol BPFI dapat dilihat pada Gambar 4.9.
Gambar 4.9 Kurva dan data serapan allopurinol baku pembanding konsentrasi
8 μg/ml dalam pelarut HCl 0,1 N.
4.5.4.2 Hasil penentuan linieritas kurva kalibrasi dalam HCl 0,1 N
45
koefisien korelasi diperoleh r = 0,99917, ini menunjukkan bahwa terdapat hubungan yang linier antara serapan dan konsentrasi dan dari hasil perhitungan diperoleh persamaan regresi y = 0,06877 x + 0,00268. Gambar kurva kalibrasi allopurinol baku pembanding dapat dilihat pada Gambar 4.10.
Gambar 4.10 Kurva kalibrasi allopurinol baku pembanding dalam pelarut HCl 0,1 N pada panjang gelombang 251 nm.
4.5.5 Penentuan kadar allopurinol
46
ini mempunyai selisih 1,0 dengan panjang gelombang maksimum literatur yaitu 250 nm. Hasil penentuan kadar Allopurinol dapat dilihat pada Tabel 4.5.
Tabel 4.5 Hasil penetapan kadar tablet allopurinol
No Formula Kadar Rata-Rata (%)
Gambar 4.11 Penetapan kadar tablet dengan presentase bahan pengikat berbeda Keterangan:
F1 : Formula tablet dengan konsentrasi pati jagung alami 10% F2 : Formula tablet dengan konsentrasi pati jagung gelatinasi 7% F3 : Formula tablet dengan konsentrasi pati jagung gelatinasi 9% F4 : Formula tablet dengan konsentrasi pati jagung gelatinasi 11 % F5 : Formula tablet dengan konsentarsi pati jagung gelatinasi 13 % F6 : Formula tablet dengan konsentrasi pati jagung gelatinasi 15% F7 : Formula tablet dengan konsentrasi pati jagung gelatinasi 17%