Lampiran 1. Gambar umbi singkong
Keterangan: a = Umbi singkong b = Pati Singkong c = Pati Sitrat
a
b
Lampiran 2. Flowsheet isolasi pati singkong
Dikupas kulit umbi Dicuci dengan aquadest
Ditimbang (umbi 5 kg)
Diparut dengan menggunakan Parutan Stainless steel
Ditambahkan air sampai menjadi bubur
Diperas dengan menggunakan kain blacu berwarna putih
Direndam selama lebih kurang 24 jam Dibuang cairan atas
Dilakukan pencucian berulang-ulang
Dikeringkan dibawah sinar matahari
Dikeringkan massa lembab dikeringkan dilemari pengering pada suhu 40-50oC selama lebih kurang 72 jam.
Umbi singkong
Residu Filtrat
Pati putih
Lampiran 3. Flowsheet pembuatan pati sitrat
Dicampurkan dengan 200 g asam sitrat Ditambahkan air
Dicampur sampai lembab tanah
Dikeringkan pada suhu 60oC selama 24 jam Disesuaikan suhu oven disesuaikan 135-160oC
selama 2 jam
Dikeluarkan dari oven
Diaduk dalam air selama 10 menit Disaring
Dicuci
Dikeringkan selama satu malam
100 g pati singkong
Lampiran 4. Perhitungan isolasi pati singkong
Pehitungan rendemen pati singkong Berat Umbi Singkong = 5000 gram Berat Pati Singkong = 670 gram
Rendemen Pati Singkong = 100%
Lampiran 5. Contoh perhitungan pembuatan tablet isoniazid
Sebagai contoh diambil tablet isoniazid dengan konsentrasi pati sitrat 5%
Cara kerja : Metode granulasi basah
Lampiran 5. (Lanjutan)
2. Tambahkan mucilago amily sedikit demi sedikit sampai diperoleh massa lembab yang dapat dikempal.
3. Massa diayak dengan ayakan mesh nomor 12 untuk menbentuk granul 4. Granul yang terbentuk dikeringkan pada temperatur 60oC selama 1 hari 5. Granul kering kemudian diayak dengan ayakan mesh 14
6. Perhitungan
Berat granulat kering = 35,15 gram
Berat teoritis = 30 g + 1,2 g + 6 g = 37,2 gram Berat bahan eksternal setelah dikoreksi:
Pati sitrat =
7. Dicampurkan dan dihomogenkan massa granul kering dengan bahan pengembang luar dan bahan pelicin.
Lampiran 6. Spektrum inframerah dari asam sitrat
Lampiran 8. Spektrum Inframerah dari pati sitrat
Lampiran 9. Gambar tablet isoniazid
Keterangan :
Lampiran 10. Hasil uji preformulasi tablet isoniazid
Data hasil uji waktu alir
Pengujian
Data hasil uji sudut diam
Lampiran 10. (Lanjutan)
Syarat : Granul akan mempunyai sifat alir yang baik jika mempunyai I ≤ 20% Sebagai contoh diambil tablet Isoniazid formula F2 (5%)
Lampiran 11. Hasil evaluasi tablet isoniazid
Data hasil uji kekerasan tablet isoniazid
Tablet
Kekerasan ( Kg )
F1 F2 F3 F4 F5 F6
1 5,05 4,85 4,01 5,17 6,01 4,89
2 5,52 5,91 3,82 5,14 5,29 6,30
3 5,40 4,44 4,95 5,54 5,41 4,52
4 4,74 4,44 3,91 6,08 6,71 4,51
5 5,25 5,03 4,21 5,09 6,28 5,35
Rata-rata 5,19 4,92 4,18 5,404 5,94 5,114
Data hasil uji waktu hancur
Tablet
Waktu Hancur ( menit, detik )
F1 F2 F3 F4 F5 F6
1 07.07 05.47 01.30 08.30 08.15 07.21
2 07.21 05.21 01.45 08.23 08.28 07.01
3 07.16 05.32 01.56 08.43 07.43 07.42
4 06.55 05.12 01.15 08.10 08.35 07.18
5 07.21 05.01 01.01 08.35 08.02 07.22
6 07.11 05.02 01.21 08.55 08.25 07.20
Rata-rata 07.07 05.47 01.56 08.41 08.31 07.13
Lampiran 12. Contoh perhitungan friabilitas tablet isoniazid
Rumus : F = (A-B)/A x 100% Keterangan :
F = Friabilitas
A= Bobot tablet sebelum diputar dalam alat Friabilitas Tester selama 4 menit (100 putaran)
B= Bobot tablet setelah diputar dalam alat Friabilitas Tester selama 4 menit (100 putaran)
Syarat friabilitas tablet : Kehilangan bobot tidak boleh lebih dari 1 % (x ≤ 1%), sebagai contoh diambil tablet formula F6
- Bobot 20 tablet sebelum diputar = 7,821 g - Bobot 20 tablet setelah diputar = 7,761 g Friabilitas tablet = 7,821 – 7,761 / 7,821 x 100% = 0,79%
Lampiran 13. Perhitungan pembuatan HCl 0,1N
HCl pekat = 37% setara dengan 12 N
V1 x N1 = V2 x N2
V1 x 12 N = 1000 mL x 0,1 N
V1 = 12N
N 1 , 0
ml 1000
x
Lampiran 14. (Lanjutan)
Dengan nilai r sebagai berikut :
Lampiran 15. Perhitungan kadar tablet isoniazid
Misalnya untuk formula F3 (6% ) Berat 20 tablet = 8076 mg
Berat isoniazid dalam 20 tablet = 20 x 400mg = 8000 mg Berat setara 50 mg isoniazid = �
�x 8076 mg = 50,47 mg
- Pengujian 1 Serbuk ditimbang seksama sebanyak 48,3 mg kemudian dilarutkan sesuai prosedur yang telah disebutkan sebelumnya dan diukur serapan pada panjang gelombang maksimum, Misalnya A(Y) = 0,443 dengan menggunakan persamaan regresi :
Y = 0,0473X + 0,0045
Lampiran 16. Analisis data statistik untuk mencari kadar sebenarnya dari diperoleh t tabel = α /2, dk = 4,0321, data diterma jika t hitung < t tabel.
Lampiran 16. (Lanjutan)
Perhitungan dalam formula tablet lainnya dilakukan dengan cara yang sama.
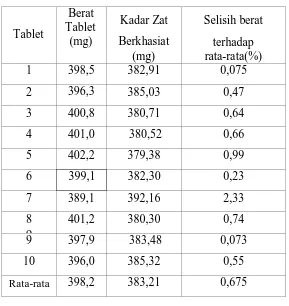
Lampiran 18. Perhitungan keragaman bobot tablet isoniazid
Contoh : Formula 1 ( 4 % )
Ditimbang masing-masing berat 10 tablet:
1. 398,5 6. 399,1
2. 396,3 7. 389,1
3. 400,8 8. 401,2
4. 401,0 9. 397,9
5. 402,1 10. 396,0
Berat rata-rata 10 tablet : 398,2 mg
Rata-rata hasil penetapan kadar = 95,8 % x 400 mg
= 383,2 mg (zat berkhasiat/tablet) Berat tablet 1 = 398,5 mg
Maka kadar zat berkhasiatnya = , �
, � x 383,2 mg = 382,91 mg
Maka % penyimpangan berat terhadap berat rata-rata : = , − ,
, x 100 %
Lampiran 19. Data hasil keragaman bobot tablet isoniazid
Formula Kadar rata – rata ( % )
Simpangan
Baku SD ≤ 6%
RSD Syarat ( % )
F 1 95,8 0,274 0,07 90, 0– 110,0
F 2 94,58 0,365 0,096 90,0 – 110,0
F 3 95,15 0,407 0,106 90,0 – 110,0
F 4 95,50 0,450 0,118 90,0 – 110,0
F 5 95,42 0,370 0,097 90,0 – 110,0
Lampiran 20. Perhitungan hasil uji disolusi
Misalnya pada Formula F3 (6 %) Pengujian I
1. Konsentrasi ( C )
Dengan persamaan regresi Y = 0,0473X + 0,0045 X = Konsentrasi
Y = Absorbansi
Pada t = 45 Menit, Y = 2,533 2. Faktor Pengenceran
Fp = (pengenceran dalam labu 10 ml) / jumlah pemipetan aliquot = 10 / 2
Fp = 5
3. Konsentrasi dalam 1 ml (Cp x Fp) C = 52,396 mcg/ml x 5 = 261,98 mcg/ml 4. konsentrasi dalam 900ml
C dalam 900ml = C dalam 1ml x 900
C = 261,98 mcg/ml x 900 ml = 235.782 mcg/ml 5. Isoniazid yang terlepas
Lampiran 20. (Lanjutan)
6. Persen Kumulatif
% kumulatif = I i i g
� � � � %
Dosis isoniazid = 300 mg % kumulatif = , �
� � %
Lampiran 22. Alat yang digunakan
Keterangan: a. Spektrofotometer Infra Red b. Mikroskop
a.
Lampiran 22. (Lanjutan)
d. e.
Keterangan: c. Spektrofotometer UV-Vis d. Alat pencetak tablet (Erweka) e. Alat uji waktu alir dan sudut diam
Lampiran 22. (Lanjutan)
f.
Keterangan : f. Alat uji kekerasan tablet (Copley) g. Alat uji friabilitas (Copley)
Lampiran 22. (Lanjutan)
g.
h.
Keterangan: g. Alat Uji Waktu Hancur ( Copley)
DAFTAR PUSTAKA
Alanazi, F.K., Elbagory, I.M., Alsarra, I.A., Byomy, M.A., dan Abdulgaoy, M.(2008). Saudi-Corn Starch as a Tablet Excipient Compared With Importad Starch. Saudi Pharmaceutical Journal, 16 (2). Halaman: 113 Anief, M. (2007). Farmasetika. Yogyakarta: Gadjah Mada University Press.
Halaman: 127.
Ansel, H.C., (1989), Pengantar Bentuk Sediaan Farmasi, Edisi IV., UI Press, Jakarta. Halaman: 244.
Aulton, M.E. (1988). Pharmaceutic The Science of Dosage Form Design. Dalam: Anita Lukman (2011). Pemanfaatan Pati Beras Ketan Pragelatinasi Sebagai Matriks Tablet Lepas Lambat Natrium Diklofenak dan Kaptopril. Skripsi. Padang: Fakultas Farmasi. Universitas Andalas. Halaman:8.
Badan Penelitian dan Pengembangan Pertanian. (2011). Inovasi Pengolahan Singkong Meningkatkan Pendapatan dan Diversifikasi Pangan. Bogor. Halaman: 2.
Cartensen. J.T. (1977). Pharmaceutics Of Solids Dosage and Solid Dosage Form. New York: Jhon Wiley and Sons. A Wiley Interscience Publication John. Halaman: 133–135, 154– 159, 216–218.
Chowdary, K. P. R., dan Veeraiah Enturi. (2011). Enhancement of Dissolution and Formulation Development of Efavirenz Tablets Employing Starch Citrate - A New Modified Starch. India: University College of Pharmaceutical Sciences, Andhra University, Visakhapatnam. Halaman: 119-123.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Cetakan Pertama, Padang : Andalas University Press. Halaman: 3-5. Ditjen POM. (1979). Farmakope Indonesia Edisi III.,Departemen Kesehatan RI:
Jakarta. Halaman: 8, 746, 748, 755.
Ditjen POM. (1979). Materia Medika Indonesia. Jilid III. Depatemen Kesehatan RI. Jakarta. Halaman: 153.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Halaman: 4, 74, 999-1000, 1084-1085.
Fessenden, R. J., dan Fessenden, J. S., (1991). Kimia Organik, diterjemahkan oleh Aloysius, H. P., Edisi ke 3, Jilid 2, Jakarta, Erlangga. Halaman: 354. Fleche, G. (1985). Chemical Modification and degradation of starch. Dalam: G.
M. A. Van Beynum dan J. A. Roels, ed. Starch conversion technology. Applied Science Publ., London. Halaman: 6.
Gandjar, I.G., dan Rohman, A. (2012). Analisis Obat Secara Spektrofotometri dan Kromatografi. Yogyakarta: Pustaka Pelajar. Halaman 180-181, 363-396, 407-408.
Hadisoewignyo, L., dan Achmad F. (2013). Sediaan Solida. Cetakan Pertama. Bogor: Institut pertanian Bogor Press. Halaman: 22
Hodge, J. E. dan E. M Osman. (1976). Carbohydrates. Dalam: Muchtadi T.R., P. Haryadi, dan A. B. Azra. (1987). Teknologi Pemasakan Ekstruksi. Pusat Antar Universitas, Institut Pertanian Bogor. Halaman 12.
Khopkar, S.M. (2008). Konsep Dasar Kimia Analitik. UI-Press, Jakarta. Halaman: 215-217, 249.
Koswara, 2006, Teknologi Modifikasi Pati. Ebook Pangan. Halaman: 7.
Lachman, L., Lieberman, H.A., dan Kaning J.L. (1994). Teori dan Praktek Farmasi Industri. Edisi Ketiga. Jakarta: UI Press. Halaman : 651-654, 657-660, 697.
Lidiasari, E., Syafutri, M.I., dan Syaiful, F. (2006). Influence of Drying Temperature Difference On Physical And Chemical Qualities of Partially Fermented Cassava Flour, Jurnal Ilmu-ilmu Pertanian Indunesia, Vol. 8. Halaman: 141-146.
Moffat, A.C., Osselton, M.D., and Widdop, B. (2004). Clarke’s Analysis of Drugs and Poisons. Edisi III. London: Pharmaceutical Press. Halaman: 266.
Parrot, E.L. (1971). Pharmaceutical Technology Fundamental Pharmaceutical. United States of Amerika: Burgess Publishing Company. Halaman: 28, 82-83.
Pavia, D.L., Lampman, G.M., dan Kriz, G.S. (1979). Introduction to Spectroscopy: A Guide for Students of Organic Chemistry. Philadelphia: Saunders College Publishing. Halaman: 13, 26-27, 225.
Sahoo, P.K. (2007). Pharmaceutical Tecnology : Tablet. New Delhi: Delhi Of Pharmaceutical Sciences and Research. Halaman: 27
Sheth, B.B., Bandelin, F.J., dan Shangraw, R.F. (1980). Compressed Tablets in Pharmaceutical Dosage Farms: Tablets. Volume I. New York: Marcel Decker Inc. Halaman: 89- 93.
Silverstein, R.M., Webster, F.X., dan Kiemle, D.J. (2005). Spectrometric Identification of Organic Compounds. Seventh Edition. USA: John Wiley & Sons. Halaman: 1,72.
Siregar, Ch. J. P., dan Wikarsa, S. (2010). Teknologi Farmasi Sediaan Tablet Dasar-Dasar Praktis.Jakarta: EGC Penerbit Buku Kedokteran. Halaman: 178-182.
Soekemi, R.A., Yuanita, T., Fat Aminah, Salim Usman. (1987). Tablet . Medan: PT Mayang Kencana. Halaman: 5 dan 54.
Sudjana. (2005). Metode Statistika. Edisi VI. Bandung: Tarsito. Halaman. 93, 168, 239, 250.
Tan dan Rahardja (2007). Obat-Obat Penting. Edisi Keenam. Jakarta: PT Gramedia. Halaman: 159.
Varro, E.T., Claus E.P., dan Lynn B. (1988). Pharmacognosy. Dalam: Murni Hastuti (2008). Pengaruh Perbedaan Suhu dalam Metode Pembuatan Amilum Singkong Pregelatinasi Terhadap Sifat Fisik Tablet Chlorpheniramin Maleat secara Kempa Langsung. Skripsi. Surakarta: Fakultas Farmasi. Universitas Muhammadiyah Surakarta. Halaman: 16. Vogel, A.I. (1990). Analisis Anorganik Kualitatif Makro dan Semimikro. Bagian I.
Penerjemah: Hadyana Pudjaatmaka. Jakarta: Penerbit Kalman Media Pustaka. Halaman: 72
Voight, R. (1994). Buku Pelajaran Teknologi Farmasi Edisi kelima. Penerjemah: Soedani Noerono. Yogyakarta: Gadjah Mada University Press. Halaman: 159, 221-222.
BAB III
METODE PENELITIAN
3.1 Metode Pembuatan
Metode yang digunakan adalah metode eksperimental meliputi isolasi pati singkong, pembuatan pati sitrat, karakteristik pati sitrat, uji preformulasi, pencetakan tablet dan evaluasi tablet.
3.2 Alat
Alat yang digunakan dalam penelitian ini adalah neraca analitik, termometer, Stopwatch, mortir dan stamfer, ayakan mesh 12, mesh 14, mesh 40, mesh 60,
mesh 100, lemari pengering, alat pencetak tablet (Erweka), Hardness Tester (Copley), Disintegration Tester (Copley), Disolution Tester (Veego), Friability Tester (Copley), Spektrofotometer UV-Vis (UV Mini 1240 Shimadzu), hot plate, alat-alat gelas dan alat laboratorium lainnya.
3.3 Bahan
Bahan yang digunakan adalah BPFI (Baku Pembanding Farmakope Indonesia) Isoniazid, bahan baku obat Isoniazid (Amsal Chem), asam sitrat (Merck), pati singkong alami, pati sitrat, laktosa, Mg. stearat, talkum, HCl (Merck), Aquadest.
3.4 Pengambilan Sampel
Sampel yang digunakan dalam penelitian ini adalah singkong yang diambil secara purposive sampling di Pasar Lhoknibong, Kecamatan Pante Bidari Aceh Timur, Aceh.
3.5 Isolasi Pati Singkong
dikupas, dicuci bersih, ditimbang dan diparut menggunakan parutan Stainless steel. Hasil parutan singkong ditambahkan air suling sampai menjadi seperti
bubur. Lalu diperas dengan menggunakan kain blacu berwarna putih dan bersih. Filtrat diendapkan lebih kurang selama 24 jam, lalu cairan atas dibuang dan dilakukan pencucian dengan cara menambahkan air suling secara berulang-ulang sampai diperoleh pati yang putih. Pati dikeringkan dibawah sinar matahari. Massa lembab dikeringkan di lemari pengering pada suhu 40-50o selama lebih kurang 72 jam, sehingga diperoleh pati singkong yang kering.
3.6 Pembuatan Pati Sitrat (E. Fard dan G.Marton)
Asam sitrat sebanyak 200 g dicampurkan dengan 100 g pati singkong kemudian ditambahkan air secukupnya (± 5 ml) dan dicampur hingga campuran lembab. Sampel ditempatkan dalam oven kedap udara untuk dehidrasi pada suhu 60o selama 24 jam. Dengan cara ini semua uap air yang ada pada permukaan telah dihilangkan dan partikel pati disalutkan dengan asam sitrat. Suhu oven disesuaikan pada 135-160oC dan campuran akan bereaksi dengan perubahan waktu. Bahan yang dihasilkan diaduk didalam air selama 10 menit kemudian disaring, dicuci dan dikeringkan selama 12 jam.
3.7 Pemeriksaan Karakteristik Pati
3.7.1 Distribusi ukuran partikel
3.7.2 Daya pengembangan (Swelling Index)
Pati sitrat sebanyak 200 mg dimasukkan kedalam gelas ukur yang masing-masing berisi 10 ml aquadest dan parafin cair. Campuran tersebut diaduk dan didiamkan selama 12 jam. Volume sedimen dalam tabung reaksi tersebut dicatat. Indeks swelling dapat dihitung sebagai berikut:
Keterangan: S.I % = swelling index (Chowdary dan Veeraraiah, 2011).
3.7.3 Kelarutan
Kelarutan pati sitrat diukur di dalam air dan pelarut organik seperti alkohol. Kelarutan suatu zat yang tidak diketahui secara pasti dapat dinyatakan dengan istilah kelarutan relatif pada Tabel 3.1 berikut:
Tabel 3.1 Istilah kelarutan
No Istilah Kelarutan
Jumlah bagian pelarut yang diperlukan untuk melarutkan
6. Sangat sukar larut 1000-10000
7. Praktis tidak larut Lebih dari 10000
Uji kelarutan dilakukan dengan cara melarutkan 1 gram pati singkong atau pati sitrat dalam sejumlah air tertentu (Anief, 2007).
3.7.4 Bobot jenis
Pati sitrat dimasukkan ke dalam gelas ukur 50 ml dan dilihat volume awal lalu gelas ukur di tap sebanyak 15 kali setelah itu dilihat volumenya. Pati ditimbang lalu berat jenis dihitung dengan rumus:
Bobot jenis = 100%
Keterangan: BJ1 = Berat jenis awal sebelum di tap BJ2 = Berat jenis akhir setelah di tap
3.7.5 Uji mikroskopik
Pati diletakkan di atas object glass lalu ditambahkan 2 tetes akuades. Lalu diamati bentuk hillus, lamela dari pati singkong di bawah mikroskop dengan perbesaran 10x40.
3.7.6 Uji FTIR (Fourier Transform Infrared Spectroscopy)
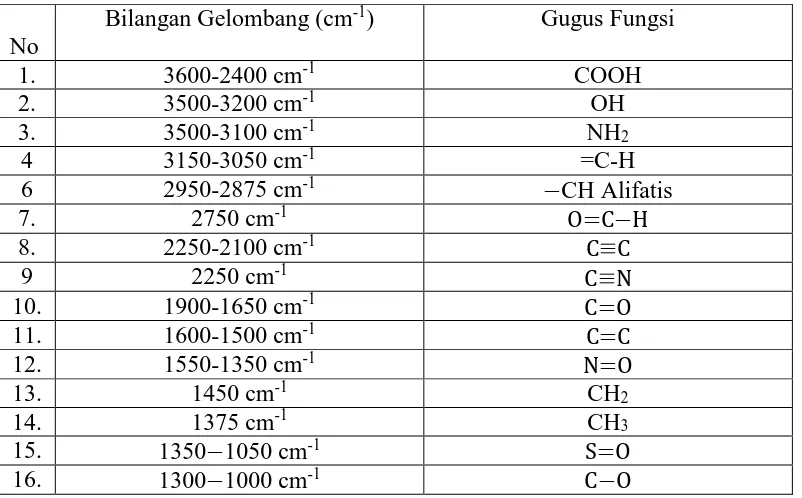
Pengukuran pada spektrum infrared dilakukan pada daerah cahaya infrared tengah (mid-infrared) yaitu pada panjang gelombang 4000-200 cm-1. Energi yang dihasilkan oleh radiasi ini akan menyebabkan vibrasi atau getaran pada molekul. Pita absorpsi sinar infrared sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi (Dachriyanus, 2004). Spektrum infrared tercatat di wilayah spektral seperti yang dinyatakan Khopkar (2008), pada Tabel 3.2 berikut:
Tabel 3.2 Penafsiran spektrum Inframerah
No
Bilangan Gelombang (cm-1) Gugus Fungsi
3.8 Pembuatan Tablet
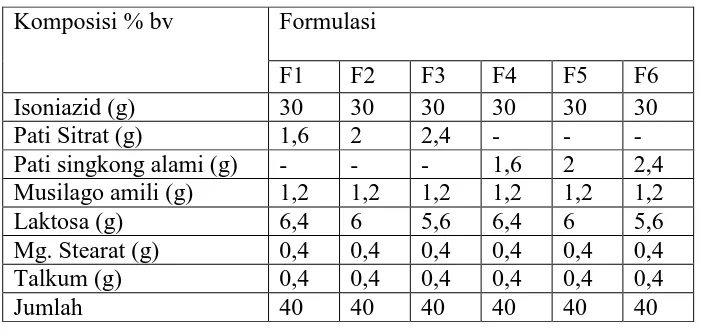
Sediaan tablet Isoniazid dibuat menggunakan pati sitrat sebagai pengembang dengan berbagai konsentrasi (4%, 5%, 6%) dan sebagai pembanding digunakan pati singkong dengan konsentrasi yang sama dan bobot tablet 400 mg dengan dosis isoniazid 300 mg tiap tabletnya seperti yang tertera pada Tabel 3.3 Formula:
Tabel 3.3 Formula tablet isoniazid
Komposisi % bv Formulasi
F1 F2 F3 F4 F5 F6
F1: Formula tablet dengan konsentrasi pati sitrat 4% F2: Formula tablet dengan konsentrasi pati sitrat 5% F3: Formula tablet dengan konsentrasi pati sitrat 6%
Tablet dibuat dengan metode granulasi basah, isoniazid, laktosa, dan amilum manihot sebagai pengembang dalam, dicampur seluruhnya lalu digerus. Tambahkan mucilago dari pati singkong sedikit demi sedikit sampai diperoleh massa lembab yang dapat dikepal, lalu sisa pengikat ditimbang. Massa lembab dilewatkan ke ayakan 12 mesh untuk memperoleh granul. Granul yang terbentuk dikeringkan pada temperatur 60º C selama 4 - 6 jam. Granul kering kemudian dilewatkan pada ayakan mesh 14 lalu dicampur dengan pengembang luar, magnesium stearat dan talkum, lalu diaduk sampai homogen.
3.9 Uji Preformulasi
3.9.1 Sudut diam
Massa granul sebanyak 100 gram dimasukkan kedalam corong yang telah dirangkai, permukaannya diratakan. Lalu penutup bawah corong dibuka, biarkan granul mengalir sampai habis. Tinggi kerucut yang terbentuk diukur. Persyaratan: 200 < θ < 400 (Cartensen, 1977).
Sudut diam diukur dengan rumus:
tg θ = 2h/D
Keterangan : θ = sudut diam D = diameter
H = tinggi kerucut (cm)
3.9.2 Waktu alir
serentak stopwatch dihidupkan. Stopwatch dihentikan saat granul tepat habis melewati corong dan dicatat waktu alirnya.
Persyaratan: granul harus habis mengalir dalam waktu lebih singkat dari 10 detik (Lachman, dkk., 1994).
3.9.3 Indeks tap
Kedalam gelas ukur 25 ml, dimasukkan sejumlah granul hingga 25 ml. Ditap dengan alat yang dimodifikasi sampai konstan. Setelah hentakan, volumenya dihitung dengan rumus:
I = � −�
�
x 100% Dimana: V1 = Volume sebelum ketukan/ mampet
V2 = Volume setelah ketukan/ mampet
Persyaratan: Indeks tap lebih kecil dari 20% (Lachman, dkk., 1994).
3.10 Evaluasi Tablet
3.10.1 Uji kekerasan tablet
Alat: Hardness Tester (Copley)
Sebelum tablet dimasukkan diantara anvil dan punch, tablet dijepit dengan cara memutar skrup pemutar sampai lampu stop menyala, ditekan knop tanda panah ke kanan sampai tablet pecah. Dan dicatat angka yang menunjukkan jarum penunjuk skala pada saat tablet pecah. Percobaan ini dilakukan untuk 5 tablet.
Persyaratan: Kekerasan tablet antara 4 - 8 kg (Parrot, 1971).
3.10.2 Uji kerapuhan/friabilitas
Alat: Friabilator (Copley)
menit. Setelah 4 menit tablet dikeluarkan dan dibersihkan dari debu. Bobot akhir ditimbang (B).
% kerapuhan = x100%
A B A
Persyaratan: Kehilangan berat tablet 0,5 - 1,0% (Sahoo, 2007).
3.10.3 Uji waktu hancur
Alat: Desintegration Tester (Copley)
Cara: Masukkan 1 tablet pada masing-masing tabung dari keranjang, masukkan satu cakram pada tiap tabung dan dijalankan alat, gunakan air bersuhu 370 ± 20 sebagai media kecuali dinyatakan lain dalam masing-masing monografi, pada akhir batas waktu seperti yang tetera dalam monografi, angkat keranjang dan amati semua tablet: semua tablet harus hancur sempurna, bila 1 tablet atau 2 tablet tidak hancur sempurna, ulangi pengujian dengan 12 tablet lainnya: tidak kurang 16 dari 18 tablet yang diuji harus hancur semua. Waktu hancur < 30 menit (Ditjen, POM., 1995).
3.11 Penetapan Kadar
3.11.1 Pembuatan pereaksi (HCl 0,1 N)
Diencerkan 8,3 ml HCl 37% dengan 1 liter akuades (Ditjen, POM., 1979). Perhitungan pembuatan pereaksi dapat dilihat pada lampiran.
3.11.2 Pembuatan larutan induk baku isoniazid
HCl 0,1 N sampai garis tanda. Homogenkan hingga diperoleh konsentrasi 100
g/ml (LIB II).
3.11.3 Pembuatan larutan standar isoniazid
Diambil sebanyak 0,5 mL; 0,75 mL; 1,0 mL; 1,25 mL; dan 1,5 mL dari LIB II isoniazid yang selanjutnya dimasukkan ke dalam 5 labu tentukur 10 mL, kemudian dicukupkan dengan larutan HCl 0,1N untuk membuat larutan standar dengan konsentrasi 5,0 g/mL; 7,5 µg/ml, 10,0 g/mL; 12,5 µg/ml; dan 15,0
g/mL secara berurutan.
3.11.4 Pembuatan spektrum serapan maksimum isoniazid
Dipipet 5,5 mL Larutan Induk Baku II isoniazid dimasukkan ke dalam labu tentukur 50 mL, diencerkan dengan HCl 0,1N hingga garis tanda, lalu dikocok sampai homogen sehingga diperoleh larutan dengan konsentrasi 11,0 g/mL, kemudian diukur serapan pada panjang gelombang 200 – 400 nm.
3.11.5 Penetapan kadar isoniazid
Ditimbang bobot 20 tablet, dicatat beratnya, kemudian digerus sampai homogen. Ditimbang sejumlah serbuk setara dengan 50 mg isoniazid, kemudian dimasukkan ke dalam labu tentukur 50 ml, tambahkan HCl 0,1 N sampai garis tanda, konsentrasi teoritis 1000 mcg/ml. Saring dengan kertas saring, filtrat pertama dibuang kira-kira 5 - 10 ml.
HCl 0,1 N sebagai blanko. Dilakukan pengulangan sebanyak 6 kali pada masing-masing formula.
3.12 Uji Keragaman Bobot
Timbang seksama 10 tablet, satu per satu dan hitung bobot rata-rata. Dari hasil penetapan kadar, yang diperoleh seperti yang tertera dalam masing-masing monografi, hitung jumlah zat aktif dari masing-masing dari 10 tablet dengan anggapan zat aktif terdistribusi homogen. Jika jumlah zat aktif dalam masing-masing dari 10 satuan sediaan terletak antara 85,0% hingga 115,0% dari yang tertera pada etiket, atau jika simpangan baku relatif kurang dari atau sama dengan 6,0%. (Ditjen, POM., 1995).
3.13 Uji Disolusi Tablet
Untuk menguji laju disolusi tablet dilakukan dengan menggunakan alat Dissolution Tester.
Medium : 900 ml HCl 0,1N
Alat : tipe 2 (metode dayung) Kecepatan putaran : 100 rpm.
Waktu : 45 menit
Cara kerja:
blanko digunakan HCl 0,1 N. Kadarnya dihitung dengan persamaan regresi. Pengujian dilakukan terhadap 6 tablet.
Toleransi dalam waktu 45 menit harus tidak kurang dari 80% (Q) C6H7N3O, dari jumlah yang tertera pada etiket (Ditjen, POM.,1995).
Interpretasi: Persyaratan dipenuhi bila jumlah zat aktif yang terlarut dari sediaan yang diuji sesuai dengan tabel penerimaan. Apabila tidak memenuhi persyaratan maka pengujian dilanjutkan sampai tiga tahap, kecuali bila hasil pengujian memenuhi tahap S1 atau S2. Kriteria penerimaan zat aktif yang larut dengan disolusi dinyatakan Ditjen, POM., (1995) dapat dilihat pada Tabel 3.4.
Tabel 3.4 Kriteria penerimaan uji disolusi
unit sediaan yang lebih kecil dari Q-15%
S3 12
Rata-rata dari 24 unit adalah sama dengan atau lebih besar dari Q tidak lebih dari 2 unit sediaan yang lebih kecil dari Q-15% dan tidak 1 unit pun kurang dari Q-25%
3.14 Analisis Data Secara Statistik
Kadar zat aktif sebenarnya yang terkandung dalam sampel dapat diketahui menggunakan uji distribusi t. Data diterima atau ditolak dihitung dengan menggunakan metode standar deviasi dengan rumus :
�� = √∑ �−�̅− 2
Keterangan:
SD = Standar deviasi X = Kadar sampel
N = Jumlah perlakuan
Untuk menghitung t hitung digunakan rumus ;
�ℎ� � = � − �̅
��/√�
Dimana:
x = kadar sampel
�̅ = kadar rata-rata sampel SD = Standar deviasi N = jumlah perlakuan.
Hasil pengujian atau nilai thitung yang diperoleh ditinjau terhadap tabel distribusi t, apabila thitung < ttabel maka data tersebut diterima.
Menurut Sudjana (2002), untuk menentukan kadar suatu zat didalam sampel dengan tingkat kepercayaan 99%, α = 0,01, dk = n-1, dapat digunakan rumus:
μ = � ̅ ± � �, �� x SD √n⁄
Keterangan: µ = kadar zat aktif
�̅ = kadar rata-rata sampel
t = harga t tabel sesuai (dk =
n
-1)BAB IV
HASIL DAN PEMBAHASAN
4.1 Isolasi Pati Singkong
Dari 5000 gram umbi singkong diperoleh pati sebanyak 670 gram. Sehingga rendemen pati singkong 13,4% (Lampiran 4). Pati singkong yang diperoleh berwarna putih, tidak berbau dan tidak berasa. Butir pati singkong berbentuk agak bulat atau bersegi banyak, lamelanya tidak jelas dan hilus berada ditengah berupa titik (Ditjen, POM., 1979).
4.2 Pati Sitrat
4.2.1 Distribusi ukuran partikel
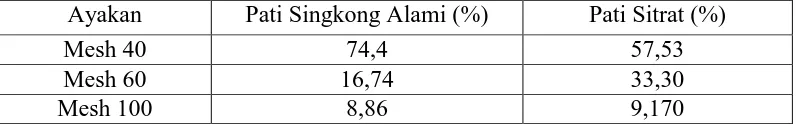
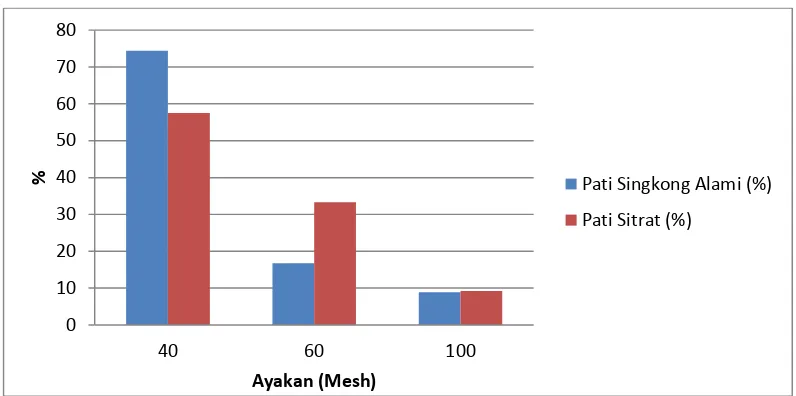
Ukuran partikel pati singkong alami dan pati sitrat diperoleh dari pengayakan dengan ayakan bertingkat yaitu mesh 40, 60 dan 100. Sehingga didapatkan masing-masing berat dari ukuran partikel mesh 40, 60 dan 100. Hasil data ukuran partikel dapat dilihat pada Tabel 4.1.
Tabel 4.1 Data ukuran partikel pati singkong alami dan pati sitrat
Ayakan Pati Singkong Alami (%) Pati Sitrat (%)
Mesh 40 74,4 57,53
Mesh 60 16,74 33,30
Mesh 100 8,86 9,170
Gambar 4. 1 Persentase distribusi ukuran partikel pati sitrat.
4.2.2 Daya pengembang
Kenaikan volume atau pengembang pati sitrat adalah: TSP (Volume Endapan dalam Parafin) : 0,7 ml
TSA (Volume Endapan dalam Air) : 2,1 ml Daya pengembang = 2,1- 0,7 / 0,7 x 100%
= 200%
Berdasarkan perhitungan di atas didapat bahwa daya pengembang pati sitrat sebesar 200%. Menurut Leach dan Cowenn (2001), persyaratan pati dikatakan sebagai pengembang yang baik apabila memiliki daya pengembang sampai 200%.
4.2.3 Kelarutan
Data hasil uji kelarutan dapat dilihat pada Tabel 4.2
Tabel 4.2 Data kelarutan pati singkong dan pati sitrat
Pati Pelarut
Air Alkohol
Berdasarkan data dari Tabel 4.2 diatas dapat dijelaskan bahwa pati singkong dan pati sitrat praktis tidak larut dalam air atau alkohol. Kelarutan dapat dipengaruhi oleh suhu, konsentrasi bahan-bahan dalam larutan dan komposisi pelarutnya (Vogel, 1979).
4.2.4 Bobot jenis
Berat seluruh pati sitrat 32 gram. Bobot jenis pati sitrat awal sebelum ditap adalah 0,790 g/ml, sedangkan bobot jenis akhir pati sitrat setelah ditap adalah
Berdasarkan perhitungan di atas didapat bahwa berat jenis pati sitrat sebesar 14,83%. Menurut Aulton (1988), pati yang memiliki nilai bobot jenis kurang dari 18% biasanya memberikan sifat alir yang baik.
4.2.5 Mikroskopik
Uji mikroskopik dilakukan untuk mengetahui bentuk hilus dan lamela amilum di bawah mikroskop perbesaran 10x40. Hasil Mikroskopik dapat dilihat pada Gambar 4.2.
(i) (ii)
Gambar 4.2 Mikroskopik pati: (i) pati singkong alami, (ii) pati sitrat
4.2.6 Uji FTIR (Fourier Transform Infrared Spectroscopy)
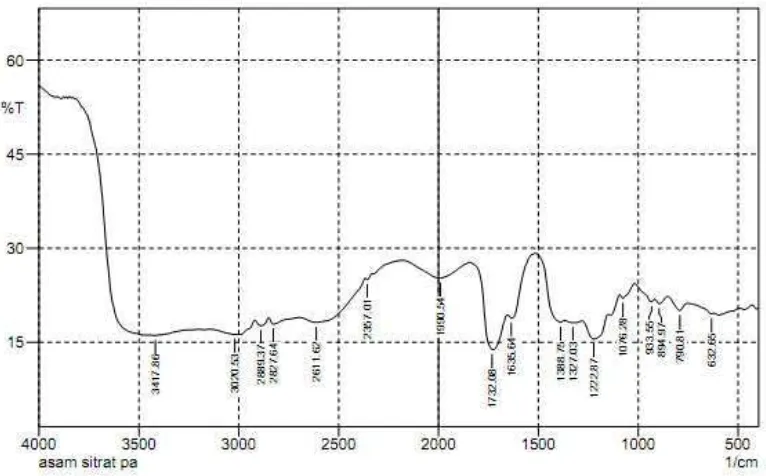
Uji FTIR ini dilakukan untuk mengetahui gugus fungsi dari suatu senyawa pada bilangan gelombang yang sudah ditentukan. Hasil uji Asam sitrat dengan menggunakan FT-IR dapat dilihat pada Gambar 4.3.
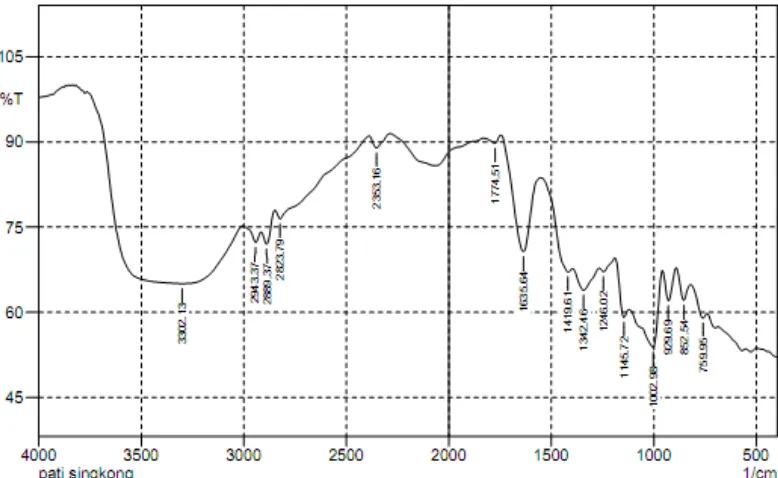
Hasil uji pati singkong dengan menggunakan FT-IR dapat dilihat pada Gambar 4.4.
Gambar 4.4 Spektrum inframerah pati singkong
Jika spektrum inframerah asam sitrat pada Gambar 3.3 dibandingkan dengan spektrum inframerah dari pati sitrat pada Gambar 3.5 diatas dapat dilihat bahwa ada perbedaan pada bilangan gelombang 3591,46 cm-1 menujukkan adanya gugus –OH, pada bilangan gelombang 2989.66–2877.79 cm-1 menunjukkan gugus –CH Alifatis dan yang paling spesifik dari FTIR pati sitrat ini adalah pada bilangan gelombang 1762.94 cm-1 terdapat adanya gugus C=O. Menurut Pavia, et al., (1979), gugus karbonil (C=O) berada pada bilangan gelombang 1725 – 1700 cm-1. Dari hasil FTIR tersebut menunjukan sudah terjadi reaksi antara asam sitrat dengan pati singkong.
4.3 Hasil Uji Preformulasi Massa Granul
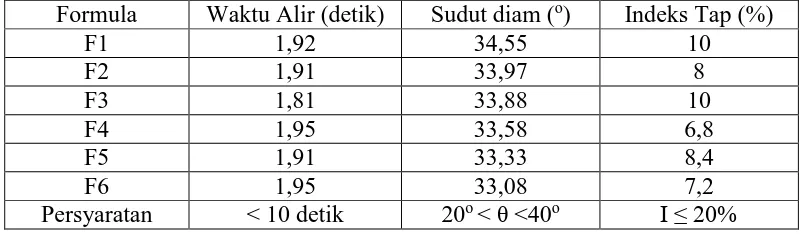
Sebelum massa granul dicetak menjadi tablet umumnya harus melalui serangkaian uji preformulasi. Hal ini penting dilakukan untuk mengetahui kelayakan pencetakan suatu tablet. Pada Tabel 4.3 berikut ini adalah tabel hasil uji preformulasi berbagai formula yang dibuat.
Tabel 4.3 Data uji preformulasi massa granul formula tablet
Formula Waktu Alir (detik) Sudut diam (o) Indeks Tap (%)
4.3.1 Uji waktu alir
Berdasarkan hasil uji waktu alir (Tabel 4.3), dapat dilihat bahwa waktu alir granul dengan bahan pengembang pada F1 sebesar 1,92 detik, F2 sebesar 1,91 detik, F3 sebesar 1,81 detik, F4 sebesar 1,95, F5 sebesar 1,91 detik dan F6 sebesar 1,95 detik. Dari data tersebut dapat dilihat bahwa semua data memenuhi persyaratan. Sifat alir dari setiap formula sangat baik, sehingga tidak mengalami kesulitan pada waktu pencetakan tablet. Menurut Cartensen (1977), waktu yang diperlukan dalam uji waktu alir tidak lebih dari 10 detik, karena jika tidak akan dijumpai
semakin kecil, sehingga meningkatkan kelinciran dan mengakibatkan sudut diamnya menjadi kecil. Menurut Cartensen (1977), granul yang memiliki sifat free flowing mempunyai sudut diam yang lebih kecil dari 40o.
Gambar 4.7 Sudut diam massa granul dengan presentase bahan pengembang
yang berbeda
4.3.3 Indeks tap
Gambar 4.8 Indeks tap massa granul dengan presentase bahan pengembang yang berbeda
4.4 Hasil Evaluasi Tablet
Evaluasi tablet isoniazid yang dilakukan adalah uji kekerasan tablet, waktu hancur, keragaman bobot, penetapan kadar dan uji disolusi tablet. Menurut Ansel (1989), beberapa uji tersebut dilakukan untuk menjamin keseragaman penampilan dan juga efek terapi dari obat tersebut.
Tabel 4.4 Data hasil evaluasi tablet isoniazid
Formula Kekerasan Tablet
F1 : Formula tablet isoniazid dengan konsentrasi pati sitrat 4% F2 : Formula tablet isoniazid dengan konsentrasi pati sitrat 5% F3 : Formula tablet isoniazid dengan konsentrasi pati sitrat 6% F4 : Formula tablet isoniazid dengan konsentrasi pati singkong 4% F5 : Formula tablet isoniazid dengan konsentrasi pati singkong 5% F6 : Formula tablet isoniazid dengan konsentrasi pati singkong 6%
4.4.1 Uji kekerasan tablet
Berdasarkan hasil uji kekerasan tablet (Tabel 4.4), dapat dilihat bahwa kekerasan tablet menunjukkan hasil yang bervariasi yaitu 4,18 sampai 5,94 kg, namun masih berada dalam batas penerimaan persyaratan evaluasi kekerasan tablet. Kekerasan tablet dipengaruhi oleh tekanan kompresi mesin pencetak tablet, kompresibilitas bahan dan penggunaan bahan pengikat. Umumnya semakin besar tekanan yang diberikan, semakin keras tablet yang dihasilkan, walaupun sifat dari granul yang menentukan kekerasan tablet. Menurut Lachman (1994), kekerasan untuk tablet secara umum adalah 4-8 kg.
Gambar 4.9 Kekerasan tablet dapat dilihat dengan presentase jenis bahan
pengembang yang berbeda.
4.4.2 Uji Friabilitas
0,5% sampai 1% masih dapat dibenarkan. Sehingga pada pengujian ini seluruh formula memenuhi persyaratan.
Gambar 4.10 Friabilitas tablet dengan presentase bahan pengembang yang
berbeda
4.4.3 Uji Waktu Hancur
Hasil uji waktu hancur dapat dilihat pada Gambar 4.11.
Gambar 4.11 Waktu hancur tablet dengan presentase bahan pengembang yang
berbeda
Berdasarkan hasil uji waktu hancur (Tabel 4.4 ), dapat dilihat bahwa waktu hancur dari tablet Isoniazid pada F1, F2 dan F3 dengan konsentrasi pati sitrat 4%, 5% dan
6%, semakin tinggi konsentrasi pati sitrat yang digunakan semakin cepat waktu hancurnya. Demikian juga pada F4 sampai F6 semakin tinggi konsentrasi pati singkong yang digunakan semakin cepat waktu hancurnya. Formula dengan pengembang pati sitrat memiliki waktu hancur yang lebih cepat dibandingkan dengan yang menggunakan pati singkong. Hal ini menujukkan bahwa pati sitrat memiliki daya hancur yang lebih baik untuk tablet dengan isoniazid tersebut.
4.5 Hasil Penetapan Kadar Tablet Isoniazid
5.5.1 Hasil pembuatan kurva serapan maksimum dan kurva kalibrasi
Menurut Moffat, dkk. (2005), isoniazid memberikan serapan maksimum pada panjang gelombang sekitar 266,0 nm didalam pelarut asam. Hasil pengukuran secara spektrofotometri ultraviolet larutan isoniazid BPFI dalam HCl 0,1 N yang dilakukan diperoleh serapan maksimum pada panjang gelombang 266,0 nm dan serapan 0,421 (Lampiran 13). Dengan demikian, panjang gelombang maksimum yang didapat sesuai dengan literatur.
Dari hasil penentuan linieritas kurva kalibrasi Isoniazid BPFI dalam rentang
konsentrasi 5 mcg/ml hingga 15 mcg/ml pada maks = 266 nm (Lampiran 14)
formula bervariasi, namun kadar tersebut masih memenuhi persyaratan yang ditetapkan dalam Farmakope Indonesia edisi IV.
Tabel 4.5 Hasil penetapan kadar tablet isoniazid
No Formula Kadar (%)
1 F1 95,80 ± 4,9535
2 F2 94,58 ± 2,7798
3 F3 95,15 ± 2,7957
4 F4 95,50 ± 2,2769
5 F5 95,42 ± 4,1983
6 F6 96,72 ± 3,3779
Syarat: Kadar = 90,0% – 110,0% Keterangan :
F1 = Formula tablet isoniazid dengan konsentrasi pati sitrat 4% F2 = Formula tablet isoniazid dengan konsentrasi pati sitrat 5% F3 = Formula tablet isoniazid dengan konsentrasi pati sitrat 6% F4 = Formula tablet isoniazid dengan konsentrasi pati singkong 4% F5 = Formula tablet isoniazid dengan konsentrasi pati singkong 5% F6 = Formula tablet isoniazid dengan konsentrasi pati singkong 6%
4.6 Keragaman Bobot
Tabel 4.6 Hasil uji keragaman bobot tablet isoniazid
No. Formula
Keragaman Bobot
Kadar (%) Simpangan Baku Relatif (%)
F1 = Formula tablet isoniazid dengan konsentrasi pati sitrat 4% F2 = Formula tablet isoniazid dengan konsentrasi pati sitrat 5% F3 = Formula tablet isoniazid dengan konsentrasi pati sitrat 6% F4 = Formula tablet isoniazid dengan konsentrasi pati singkong 4% F5 = Formula tablet isoniazid dengan konsentrasi pati singkong 5% F6 = Formula tablet isoniazid dengan konsentrasi pati singkong 6%
4.7 Hasil Uji Disolusi
Hasil uji disolusi tablet isoniazid dapat dilihat pada Gambar 4.12 dan Tabel 4.7.
Gambar 4.12 Disolusi tablet isoniazid dengan jenis dan persentase bahan
Tabel 4.7 Hasil uji disolusi tablet isoniazid
No Formula Persentase disolusi (%)
1 F1 78,14
F1 : Formula tablet isoniazid dengan konsentrasi pati sitrat 4% F2 : Formula tablet isoniazid dengan konsentrasi pati sitrat 5% F3 : Formula tablet isoniazid dengan konsentrasi pati sitrat 6% F4 : Formula tablet isoniazid dengan konsentrasi pati singkong 4% F5 : Formula tablet isoniazid dengan konsentrasi pati singkong 5% F6 : Formula tablet isoniazid dengan konsentrasi pati singkong 6%
memenuhi kriteria penerimaan uji disolusi. Dengan demikian dapat dilihat bahwa disolusi tablet yang menggunakan pati sitrat lebih baik dari pada pati singkong dan laju disolusi semakin baik dengan adanya peningkatan konsentrasi pati sitrat.
Gambar 4.13 Disolusi tablet isoniazid dengan jenis dan persentase bahan
pengembang yang berbeda dalam HCl 0,1 N pada menit 45.
Tabel 4.8 Hasil uji disolusi rata-rata dari 12 unit (S1+S2) pada menit 45.
No.
Persentase obat yang terlepas pada menit ke-45
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Pati sitrat yang disintesa dari pati singkong dapat digunakan sebagai bahan pengembang pada pembuatan tablet isoniazid. Hal tersebut dapat dilihat pada uji waktu hancur, dimana tablet yang menggunakan bahan pengembang pati sitrat lebih cepat waktu hancurnya dari pada tablet yang menggunakan bahan pengembang pati singkong alami.
b. Penggunaan pati sitrat dengan konsentrasi yang berbeda sebagai bahan pengembang berpengaruh terhadap waktu hancur dan disolusi, yaitu semakin tinggi konsentrasi pati sitrat maka waktu hancur semakin cepat dan disolusi semakin baik.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Singkong (Manihot utilissima P.)
2.1.1 Klasifikasi tanaman
Singkong atau ketela pohon merupakan tanaman yang berasal dari Amerika, memiliki nama lain ubi kayu, singkong, kasepe dalam bahasa inggris adalah cassava. Singkong termasuk famili Euphorbiaceae yang umbinya dimanfaatkan sebagai sumber karbohidrat dan daunnya dikonsumsi sebagai sayuran. Umbi atau akar pohon yang panjang dengan rata-rata 2-3 cm dan panjang 50-80 cm tergantung dari varietas singkong yang ditanam. Umbinya berwarna putih kekuning-kuningan. Umbi singkong tidak tahan disimpan lama walau di dalam lemari pendingin. Gejala kerusakan di tandai dengan keluarnya warna biru gelap akibat terbentuk asam sianida (HCN) yang bersifat racun bagi manusia (Lidiasari, 2006).
Menurut Rukmana (2002), klasifikasi tanaman singkong adalah sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta Sub-divisio : Angiospermae
Klass : Dicotyledoneae
Ordo : Euphorbiales
Famili : Euphorbiaceae
Genus : Manihot
2.1.2 Kandungan kimia
Singkong segar mempunyai komposisi kimia terdiri dari kadar air 60%, pati 35%, serat kasar 2,5%, kadar lemak 0,5% dan kadar abu 1%, karena merupakan sumber karbohidrat dan serat makanan, namun sedikit kandungan zat gizi seperti protein (Badan penelitian dan pengembangan pertanian, 2011).
2.2 Uraian Pati
Pati adalah karbohidrat kompleks yang tidak larut dalam air, berwujud serbuk putih, tidak berasa dan tidak berbau. Pati merupakan bahan utama yang dihasilkan oleh tumbuhan untuk menyimpan cadangan makanan dalam jangka panjang. Banyaknya kandungan pati pada tanaman tergantung pada asal pati tersebut, misalnya pati yang berasal dari biji beras mengandung pati 50-60% (Winarno, 1986).
Zat pati terdiri dari butiran-butiran kecil yang disebut granula. Bentuk dan ukuran granula merupakan karakteritik setiap jenis pati, karena itu dapat digunakan untuk identifikasi, selain ukuran granula karakteristik lain adalah bentuk granula, lokasi hilum, serta permukaan granulanya (Hodge dan Osman, 1976).
Secara mikroskopik pati singkong berupa butir tunggal dan jarang berkelompok, agak bulat atau persegi banyak, berbentuk topi baja, butir kecil berdiameter 5
sampai 10 m, butir besar berdiameter 20-35 m. Hilus ditengah berupa titik, garis lurus atau bercabang tiga, lamela tidak jelas (Ditjen, POM., 1979).
2.3 Modifikasi Pati
Pati termodifikasi adalah pati yang gugus hidroksilnya telah diubah lewat suatu reaksi kimia atau dengan merusak struktur asalnya (Fleche, 1985).
2.3.1 Modifikasi pati dengan cara fisika (pragelatinasi)
Amilum pregelatinasi merupakan modifikasi dengan proses merubah struktur amilum baik secara fisika maupun mekanik dengan memecahkan semua atau bagian dari granul-granul dengan adanya air, kemudian amilum-amilum itu segera dikeringkan. Jika suatu sistem pati dan air berangsur-angsur dipanaskan dari suhu rendah sampai dengan suhu 60°C, maka yang pertama granul pati akan menyerap air, sehingga granula membengkak dan selanjutnya granul pati akan mengembung membentuk suatu massa yang seperti pasta kental (Varro, dkk., 1988).
2.3.2 Modifikasi pati dengan cara kimia
Modifikasi Pati secara kimia melibatkan sejumlah bahan kimia ke dalam pati. Bahan kimia yang ditambahkan dapat berupa asam, basa, garam, maupun unsur halogen. Berikut ini adalah beberapa modifikasi pati secara kimia:
1. Degradasi dengan asam atau basa. Merupakan reaksi pemecahan pati menjadi molekul-molekul yang lebih sederhana seperti glukosa, maltosa dan dextrin. Bahan kimia yang ditambahkan berupa asam karboksilat, garam dari asam kuat maupun asam lemah.
2. Reduksi dan Oksidasi merupakan proses modifikasi pati menjadi alkohol, pemanis untuk pengidap diabetes. Hasil dari modifikasi ini adalah sorbitol dan manitol. Reaksi reduksi biasanya melibatkan hidrogen dari katalis Raney-Nickel.
dehidrasi dan membentuk anhidrida. Kemudian sitrat anhidrida dapat bereaksi dengan pati dan menghasilkan pati sitrat.
4. Asetilasi yaitu pati termodifikasi yang diperoleh dari mereaksikan pati dengan gugus hidroksil sehingga menghasilkan hemiacetal dan aldehid. Pati cross-linking terbentuk dengan dialdehid. Reaksi asetilasi merupakan reaksi reversible, karena itu gugus asetal tidak stabil selama penyimpanan dan membebaskan asetil aldehid (Johnson, 1979).
2.4 Isoniazid
2.4.1 Tinjauan Umum
Rumus bangun :
Gambar 2.1 Rumus bangun isoniazid
Rumus molekul : C6H7N3O Berat molekul : 137,14
Pemerian : Hablur putih atau tidak berwarna atau serbuk hablur putih, tidak berbau, perlahan lahan dipengaruhi oleh udara dan cahaya.
Kelarutan : Mudah larut dalam air, agak sukar larut dalam etanol, sukar larut dalam kloroform dan dalam eter (Ditjen, POM., 1995).
2.4.2 Farmakologi
dalam makrofag maupun di luar sel (ekstraselular). Obat ini praktis tidak aktif terhadap bakteri lain. Mekanisme kerjanya berdasarkan terganggunya sintesa mycolic acid, yang diperlukan untuk membangun dinding bakteri (Tan dan
Rahardja, 2007).
2.5 Asam Sitrat
2.5 1 Tinjauan Umum
Rumus bangun : CH2(COOH)C(OH)(COOH)CH2COOH. H2O Rumus molekul : C6H8O7.H2O
Nama kimia : asam 2-hidroksipropana-1,2,3-trikarboksilat Berat molekul : 210,14
Kandungan : Tidak kurang dari 99,5% dan tidak lebih dari 101,0% C6H8O7.H2O.
Pemerian : Hablur tidak berwarna atau serbuk putih; tidak berbau; rasa sangat asam; agak higroskopik; merapuh dalam udara kering atau panas
Kelarutan :Larut dalam kurang dari 1 bagian air dan dalam1,5 bagian etanol (95%) P; sukar larut dalam eter P (Ditjen POM., 1979).
2.6 Sediaan Tablet
2.6.1 Uraian tablet
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa bahan pengisi. Sebagian besar tablet dibuat dengan cara pengempaan dan merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan baja (Ditjen, POM., 1995).
Untuk mendapatkan tablet yang baik, maka bahan pengisi yang akan dikempa menjadi tablet harus memenuhi sifat- sifat berikut:
a. Mudah mengalir, artinya jumlah bahan yang akan mengalir dalam corong alir ke dalam ruang cetakan selalu sama setiap saat, dengan demikian bobot tablet tidak akan memiliki variasi.
b. Kompatibel, artinya bahan mudah kompak jika dikempa, sehingga dihasilkan tablet yang keras.
c. Mudah lepas dari cetakan, hal ini dimaksudkan agar tablet yang dihasilkan mudah lepas dan tidak ada bagian yang melekat pada cetakan, sehingga permukaan tablet halus dan licin (Sheth, et al., 1980).
2.6.2 Metode pembuatan tablet
Tablet dibuat dengan 3 cara umum, yaitu granulasi basah, granulasi kering dan kempa langsung.
a. Granulasi Basah
diayak lagi untuk memperoleh granul dengan ukuran yang diperlukan dan ditambahkan bahan pelicin dan dicetak dengan mesin tablet (Anief, 1994).
b. Granulasi Kering
Metode ini digunakan pada keadaan dosis efektif terlalu tinggi untuk pencetakan langsung, obatnya peka terhadap pemanasan, kelembaban, atau keduanya (Lachman, dkk., 1994).
Setelah penimbangan dan pencampuran bahan, serbuk di slugged atau dikompresi menjadi tablet yang lebar dan datar dengan garis tengah sekitar 1 inci. Kempaan harus cukup keras agar ketika dipecahkan tidak menimbulkan serbuk yang berceceran. Tablet kempaan ini dipecahkan dengan tangan atau alat dan diayak dengan lubang yang diinginkan, pelicin ditambahkan dan tablet dikempa (Ansel, 1989).
c. Cetak Langsung
Beberapa bahan obat seperti kalium klorida, kalium iodida, amonium klorida dan metenamin bersifat mudah mengalir, sifat kohesifnya juga memungkinkan untuk langsung dikompresi tanpa memerlukan granulasi (Ansel, 1989).
2.6.3 Komposisi tablet
Tablet oral umumnya di samping zat aktif mengandung, pengisi, pengikat, penghancur dan pelincir. Tablet tertentu mungkin memerlukan pemacu aliran, zat warna, zat perasa, dan pemanis (Lachman, dkk., 1994).
dan bahan-bahan lainnya (Ansel, 1989). a. Pengisi
Digunakan agar tablet memiliki ukuran dan massa yang dibutuhkan. Sifatnya harus netral secara kimia dan fisiologis, selain itu juga dapat dicernakan dengan baik (Voigt, 1995). Bahan-bahan pengisi yaitu: laktosa, sukrosa, manitol, sorbitol, amilum, bolus alba, kalsium sulfat, natrium sulfat, natrium klorida, magnesium karbonat (Soekemi, dkk., 1987).
b. Pengikat
Untuk memberikan kekompakan dan daya tahan tablet, juga untuk menjamin penyatuan beberapa partikel serbuk dalam butir granulat (Voigt, 1994). Pengikat yang umum digunakan yaitu: amilum, gelatin, glukosa, gom arab, natrium alginat, karboksi metil selulosa, polivinilpirolidon dan veegum (Soekemi, dkk., 1987).
c. Penghancur
Untuk memudahkan pecahnya tablet ketika berkontak dengan cairan saluran pencernaan dan mempermudah absorpsi (Lachman, dkk., 1994). Bahan yang digunakan sebagai pengembang yaitu: amilum, gom, derivat selulosa, alginat, dan clays (Soekemi, dkk., 1987).
d. Pelicin
2.6.4 Teori tentang hancurnya tablet
a. Pengembangan (Swelling)
Air merembes kedalam tablet melalui celah antar partikel atau jembatan hidrofil yang terbentuk. Dengan adanya air maka bahan penghancur akan mengembang dimulai dari bagian lokal lalu meluas keseluruh bagian tablet. Akibat pengembangan bahan penghancur menyebabkan tablet pecah dan hancur (Voight, 1994).
b. Porositas dan gaya kapilaritas
Efektivitas bahan penghancur yang tidak dapat mengembang, diyakini berlangsung melalui aksi porositas dan kapiler. Porositas dianggap sebagai jalan masuk atau penetrasi cairan masuk ke dalam tablet. Partikel-partikel bahan pengancur yang umumnya memiliki sifat kohesivitas dan kompresibilitas rendah, dapat meningkatkan porositas dan menyediakan jalan penetrasi cairan ke dalam tablet. Cairan akan ditarik masuk ke jalan penetrasi ini melalui aksi kapiler dan akan menghilangkan ikatan antara partikel yang dapat menyebabkan tablet hancur (Hadisoewignyo, 2013).
c. Deformasi (perubahan bentuk)
Pada saat pengempaan tablet, partikel/granul yang mengalami penekanan proses pencetakan akan berubah bentuknya. Apabila tablet terkena air maka partikel yang membentuk akan kembali ke bentuk semula sebelum tekanan diberikan. Akibat dari perubahan bentuk, maka partikel/granul penyusun tablet akan berdesakan dan tablet akan hancur (Voight, 1995).
2.6.5 Uji preformulasi
sewaktu pencetakan tablet, meliputi waktu alir, sudut diam dan indeks tap.
Pengujian waktu alir dilakukan dengan mengalirkan massa granul melalui corong. Waktu yang diperlukan tidak lebih dari 10 detik, jika tidak maka akan dijumpai kesulitan dalam hal keseragaman bobot tablet. Hal ini dapat diatasi dengan penambahan bahan pelicin (Cartensen, 1977).
Pengukuran sudut diam digunakan metode corong tegak, granul dibiarkan mengalir bebas dari corong ke atas dasar. Serbuk akan membentuk kerucut, kemudian sudut kemiringannya diukur. Semakin datar kerucut yang dihasilkan, semakin kecil sudut diam, semakin baik aliran granul tersebut (Voigt, 1995). Indeks tap adalah uji yang mengamati penurunan volume sejumlah serbuk atau granul akibat adanya gaya hentakan. Indeks tap dilakukan dengan alat volumenometer yang terdiri dari gelas ukur yang dapat bergerak secara teratur keatas dan kebawah. Serbuk atau granul yang baik mempunyai indeks tap kurang dari 20% (Cartensen, 1977).
2.6.6 Evaluasi tablet
a. Kekerasan tablet
Faktor – faktor yang mempengaruhi kekerasan tablet adalah tekanan pada saat pentabletan, sifat bahan yang dikempa, jumlah serta jenis bahan obat yang ditambahkan saat pentabletan akan meningkatkan kekerasan tablet (Ansel, 1981). b. Kerapuhan tablet ( friabilitas)
Kerapuhan adalah parameter lain dari ketahanan tablet dalam melawan pengikisan dan goncangan, besaran yang dipakai adalah % bobot yang hilang selama pengujian dengan alat friabilator. Faktor-faktor ysng mempengaruhi kerapuhan antara lain banyaknya kandungan serbuk (fines), kerapuhan di atas 1% menunjukkan tablet yang rapuh dan dianggap kurang baik (Lachman, 1994).
c. Waktu hancur tablet
Waktu hancur tablet adalah waktu yang dibutuhkan untuk hancurnya tablet dalam medium yang sesuai sehingga tidak ada bagian tablet yang tertinggal diatas kasa alat pengujian. Faktor-faktor yang mempengaruhi waktu hancur adalah sifat fisika kimia granul dan kekerasan tablet, kecuali dinyatakan lain, waktu hancur tablet tidak bersalut tidak boleh lebih dari 15 menit (Lachman, 1994).
d. Kadar zat berkhasiat
Untuk mengevaluasi kemanjuran suatu tablet, jumlah obat dalam tablet harus dipantau pada setiap tablet atau batch, begitu juga kemampuan tablet untuk melepaskan zat atau obat yang dibutuhkan harus diketahui (Lachman, dkk., 1994).
e. Keseragaman sediaan
Menurut (Ditjen, POM., 1995) keseragaman sediaan dapat ditetapkan dengan dua cara, yaitu :
1. Keragaman bobot, dilakukan terhadap tablet yang 50% bahan aktifnya lebih besar atau sama dengan 50 mg.
2. Keseragaman kandungan, dilakukan terhadap tablet yang 50% bahan aktifnya kurang dari 50 mg.
f. Disolusi
Disolusi adalah proses melarutnya suatu obat (Ansel, 1989). Saat sekarang ini disolusi dipandang sebagai salah satu uji pengawasan mutu yang paling penting dilakukan pada sediaan farmasi. Pada uji disolusi dapat diketahui bahan obat dalam larutan dengan kecepatan yang seharusnya. Cepatnya obat atau tablet melarut menentukan kadar bahan berkhasiat terlepas didalam tubuh. Karena itu laju larut berhubungan langsung dengan kemanjuran dari tablet dan perbedaan bioavaibilitas dari berbagai formula (Lachman, 1994).
2.7 Spektrofotometri
2.7.1 Spektrofotometri sinar ultraviolet
Spektrum ultraviolet adalah suatu gambaran yang menyatakan hubungan antara panjang gelombang atau frekuensi sinar UV terhadap intensitas serapan (adsorbansi). Sinar ultraviolet mempunyai panjang gelombang antara 200 - 400 nm. Serapan cahaya oleh molekul dalam daerah spektrum ultra violet tergantung pada struktur elektronik dari molekul yang bersangkutan (Sastrohamidjojo, 1985).
2.7.2 Spektrofotometri sinar inframerah
Spektrofotometri inframerah pada umumnya digunakan untuk: 1. Menentukan gugus fungsi suatu senyawa organik
2. Mengetahui informasi struktur suatu senyawa organik dengan membandingkan daerah sidik jarinya.
Pengukuran pada spektrum inframerah dilakukan pada daerah cahaya inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2.5 - 50 �m atau bilangan gelombang 4000 - 200 cm-1. Energi yang dihasilkan oleh radiasi ini akan menyebabkan vibrasi atau getaran pada molekul. Pita absorpsi sinar inframerah sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi
(Dachriyanus, 2004). Jenis absorpsi energi yang lain, molekul-molekul dieksitasikan ke tingkat energi
BAB I
PENDAHULUAN
1.1 Latar Belakang
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa bahan pengisi (Ditjen, POM., 1995). Tablet dapat berbeda-beda dalam ukuran, bentuk, berat, kekerasan, ketebalan, daya hancurnya dan dalam aspek lainnya tergantung pada cara pemakaian tablet dan metode pembuatannya. Kebanyakan obat-obat pemberian secara oral berada dalam bentuk tablet (Ansel, 1989).
Dewasa ini tablet adalah bentuk sediaan yang paling banyak digunakan, hal ini disebabkan tablet memiliki kelebihan yang tidak dimiliki oleh sediaan farmasi yang lain, baik dari segi produksi, penyimpanan, distribusi maupun pemakaiannya. Berdasarkan hal-hal tersebut maka pembuatan tablet dan upaya untuk lebih mengembangkan teknologi pembuatan tablet terus dilakukan (Siregar dan Wikarsa, 2010).
Pati telah lama digunakan baik sebagai bahan makanan maupun bahan tambahan dalam sediaan farmasi. Penggunaan pati dalam bidang farmasi terutama pada formula sediaan tablet, baik sebagai pengisi, penghancur maupun sebagai bahan pengikat (Alanazi, dkk., 2008).
Menurut Koswara (2006), pati alami seperti pati singkong, pati jagung dan pati-patian lain mempunyai beberapa kekurangan yaitu pasta yang terbentuk keras dan tidak bening, sifatnya konsistensi terlalu lengket, tidak tahan dengan perlakuan asam, kekentalannya rendah, kelarutannya rendah dan kekuatan pengembangnya juga rendah. Kendala-kendala tersebut menyebabkan penggunaan pati terbatas dalam industri, maka dikembangkan teknologi untuk memodifikasi pati sehingga diperoleh pati yang mempunyai karakteristik yang lebih baik.
Singkong atau ubi kayu merupakan salah satu sumber karbohidrat lokal Indonesia yang menduduki urutan ketiga terbesar setelah padi dan jagung. Tanaman ini merupakan bahan baku yang paling potensial untuk diolah menjadi tepung. Modifikasi dengan asam akan menghasilkan pati dengan sifat lebih encer jika dilarutkan, lebih mudah larut, dan berat molekulnya lebih rendah (Koswara, 2006).
Asam sitrat dikategorikan aman digunakan pada makanan. Senyawa ini secara alami terdapat pada semua jenis makhluk hidup. Kelebihan asam sitrat mudah dimetabolisme dan dihilangkan dari tubuh. Chowdary dan Veeraiah (2011), melaporkan bahwa pati sitrat merupakan produk biodegradabel yang memiliki sifat alir dan kemampuan mengembang yang baik, tanpa membentuk gel bila dipanaskan dalam air dan dianggap sebagai pembawa yang baik untuk dispersi padat. Selain itu juga dapat meningkat laju disolusi obat.
atau serbuk hablur putih, tidak berbau dan mempunyai rasa yang agak pahit. Kelarutannya mudah larut dalam air akan tetapi agak sukar larut di dalam etanol, kloroform dan eter, yang berkhasiat sebagai anti tuberkulosis. Isoniazid dapat terurai perlahan-lahan dengan adanya udara dan cahaya sehingga pemilihan bentuk tablet lebih efesien untuk menghidari kerusakan karena penggunaan berulang bila dalam bentuk cair.
Berdasarkan hal tersebut peneliti melakukan penelitian penggunaan pati sitrat yang disintesa dari pati singkong sebagai bahan pengembang tablet isoniazid. Tablet yang diperoleh dilakukan pengujian beberapa parameter mutu industri yaitu uji friabilitas (Voight, 1995) dan uji kekerasan (Parrot, 1971), parameter mutu yang ditetapkan Farmakope Indonesia yaitu uji waktu hancur, penetapan kadar isoniazid, uji keseragaman sediaan, dan uji disolusi (Ditjen, POM., 1995) sehingga dapat diketahui pati sitrat yang disintesa dari pati singkong dapat digunakan sebagai bahan pengembang pada pembuatan tablet isoniazid tersebut.
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat dirumuskan sebagai berikut:
a. Apakah pati sitrat dapat digunakan sebagai bahan pengembang pada pembuatan tablet isoniazid?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas, maka yang menjadi hipotesis dalam penelitian ini adalah:
a. Pati sitrat dapat digunakan sebagai bahan pengembang pada pembuatan tablet isoniazid.
b. Penggunaan pati sitrat dengan konsentrasi yang berbeda berpengaruh sebagai bahan pengembang pada pembuatan tablet isoniazid terhadap waktu hancur dan disolusi.
1.4 Tujuan Penelitian
Berdasarkan hipotesis di atas, maka yang menjadi tujuan dalam penelitian ini adalah:
a. Untuk dapat menggunakan pati sitrat sebagai bahan pengembang pada pembuatan tablet isoniazid.
b. Untuk mengetahui penggunaan pati sitrat dengan konsentrasi yang berbeda berpengaruh sebagai bahan pengembang pada pembuatan tablet isoniazid terhadap waktu hancur dan disolusi.
1.5 Manfaat Penelitian
PENGGUNAAN PATI SITRAT YANG DISINTESA DARI PATI SINGKONG SEBAGAI BAHAN PENGEMBANG TABLET ISONIAZID
ABSTRAK
Latar Belakang: Pati dalam sediaan tablet digunakan sebagai pengisi,
penghancur maupun sebagai bahan pengikat. Pati termodifikasi adalah pati yang gugus hidroksinya telah diubah atau diberi perlakuan tertentu misalnya dengan pemanasan. Pati sitrat merupakan pati modifikasi yang memiliki kemampuan mengembang yang baik serta dapat meningkatkan laju disolusi pada obat. Berdasarkan hal tersebut peneliti melakukan penelitian penggunaan pati sitrat yang disintesa dari pati singkong sebagai bahan pengembang tablet isoniazid.
Tujuan: Penelitian ini bertujuan untuk mengetahui penggunaan pati sitrat yang
disintesa dari pati singkong sebagai bahan pengembang tablet isoniazid.
Metode: Pati sitrat dibuat dengan mereaksikan pati singkong dan asam sitrat pada
temperatur yang tinggi (135-160oC). Pati sitrat yang diperoleh diuji ukuran partikel, kelarutan, daya mengembang, berat jenis, mikroskopik dan Fourier Transform Infrared Spectroscopy (FTIR). Tablet dibuat dengan dua variasi yaitu: tablet isoniazid yang menggunakan pati sitrat konsentrasi F1(4%), F2(5%), F3(6%) dan tablet isoniazid yang menggunakan pati singkong konsentrasi F4(4%), F5(5%), F6(6%). Uji preformulasi yang dilakukan yaitu uji waktu alir, sudut diam dan indeks tap dilakukan terhadap massa granul sebelum dicetak menjadi tablet. Setelah dicetak menjadi tablet dilakukan evaluasi tablet yaitu uji kekerasan, waktu hancur, friabilitas, penetapan kadar, keragaman bobot dan uji disolusi.
Hasil: Hasil dari penelitian ini didapatkan bahwa evaluasi F1 sampai F6
memenuhi persyaratan yang ditentukan. Pada uji disolusi, tablet isoniazid yang menggunakan pati sitrat F1 80,15%, F2 80,78%, dan F3 81,23% memenuhi persyaratan uji disolusi menurut Farmakope Indonesia edisi IV yaitu dalam waktu 45 menit harus terlarut tidak kurang dari 80% (Q) C6H7N3O dalam medium HCl 0,1N, sedangkan tablet isoniazid yang menggunakan pati singkong tidak memenuhi persyaratan uji disolusi.
Kesimpulan: Pati sitrat yang disintesa dari pati singkong dapat digunakan
sebagai bahan pengembang pada pembuatan tablet isoniazid.
THE USE OF CITRATE STARCH SYNTHESIZED FROM CASSAVA STA RCH AS SWELLING AGENT OF ISONIAZID TABLETS
ABSTRACT
Background: Starch in tablet dosage form widely use as filler, disintegrant, and b
inder. The modified starch is a starch which its hydroxyl group has been modified or given specific treatment for example by heating. Citrate starch is a modified sta rch which has good flow property and ability to expand and improve the dissoluti on rate of poorly soluble drugs. Based on descriptions above, the researcher to do research about use of citrate starch that synthesizing from cassava starch as swelli ng substance of isoniazid tablet.
Objective: The aim of this study is to know about use of citrate starch as a swellin
g agent and to determine the influence of the concentration to dissolution and disi ntegration time.
Method: Citrate starch was made by reacting cassava starch and citric acid at
high temperature (135-160 oC). Starch citrate is evaluated of particle size, solubility, swelling index, density, microscopic, Fourier Transform Infrared Spectroscopy (FTIR). The isoniazid tablets was made two variations, that is: disintegration time, friability, assay, diversity of weights and dissolution tests.
Result: This result shows that the evaluation of F1 to F6 comply the specified req
uirements. In the dissolution test, the formula which uses starch citrate F1 80.15% , F2 and F3 80.78% 81.23 complied the requirements of dissolution testing accord ing to Indonesia Pharmacopoeia 4th edition, that is in 45 minutes must be dissolve d not less than 80% (Q) C6H7N3 in medium HCl 0,1 N, while Formula which use cassava starch did not complied the requirements of dissolution test. Conclusion: Citrate starch synthesized from cassava starch can be used as a swelling agent in t he manufacture of isoniazid tablets.
PENGGUNAAN PATI SITRAT YANG DISINTESA
DARI PATI SINGKONG SEBAGAI BAHAN
PENGEMBANG TABLET ISONIAZID
SKRIPSI
OLEH:
INTAN DARMAYASARI
NIM 121524187
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGGUNAAN PATI SITRAT YANG DISINTESA
DARI PATI SINGKONG SEBAGAI BAHAN
PENGEMBANG TABLET ISONIAZID
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara