ISOLASI DAN IDENTIFIKASI SENYAWA SAPOGENIN DARI TERIPANG Stichopus sp.
SKRIPSI
Oleh:
RAHMA DANISYAH NASUTION NIM: 060824009
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
ISOLASI DAN IDENTIFIKASI SENYAWA SAPOGENIN DARI TERIPANG Stichopus sp.
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
RAHMA DANISYAH NASUTION NIM: 060824009
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
ISOLASI DAN IDENTIFIKASI SENYAWA SAPOGENIN DARI TERIPANG Stichopus sp.
Oleh:
RAHMA DANISYAH NASUTION NIM: 060824009
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal: Januari 2009
Pembimbing I, Panitia Penguji,
(Dra. Suwarti Aris, M.Si., Apt.) (Dra. Siti Aman, M.S., Apt.)
NIP: 131 126 695 NIP: 130 517 493
Pembimbing II, (Dra. Suwarti Aris, M.Si., Apt.) NIP: 131 126 695
(Dra. Aswita Hafni Lubis, M.Si., Apt.) (Dra. Misrah Gaffar, M.S., Apt.)
NIP: 131 270 667 NIP: 131 569 407
(Drs. Panal Sitorus, M.Si., Apt.) NIP: 130 872 283
Medan, Januari 2009
Fakultas Farmasi Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Bismillahahirrohmaanirrohiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta sholawat beriring salam untuk rasulullah Nabi
Muhammad SAW sebagai contoh tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul:
“Isolasi dan Identifikasi Senyawa Sapogenin dari Teripang Stichopus sp.”
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Ibu Dra. Suwarti Aris, M.Si., Apt dan ibu Dra. Aswita Hafni Lubis, M.Si.,
Apt, yang telah membimbing dengan penuh kesabaran, tulus dan ikhlas dan
memberikan petunjuk-petunjuk serta saran-saran selama penelitian hingga
selesainya skripsi ini.
2. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi USU Medan, yang telah memberikan fasilitas selama pendidikan
serta pengarahan dan bimbingan dalam menyelesaikan skripsi ini.
3. Ibu Dra. Sudarmi, M.Si., Apt., selaku Penasehat Akademik yang selalu
memberikan bimbingan kepada penulis selama masa perkuliahan.
4. Bapak Drs. Panal Sitorus, M.Si., Apt, selaku Kepala Laboratorium
5. Ibu Dra. Siti Aman, M.S., Apt., Ibu Dra. Misrah Gaffar, M.S., Apt., dan
Bapak Drs. Panal Sitorus, M.Si., Apt., selaku dosen penguji yang telah
memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan
skripsi ini.
6. Bapak dan Ibu Staf Pengajar Fakultas Farmasi USU yang telah mendidik
penulis selama perkuliahan sehingga dapat menyelesaikan skripsi ini.
7. Ayahanda H. Ali Usman Nst, dan Ibunda Almh. Hj. Borgo Lubis, keluarga
besar A.U, kakakku tersayang Dr.Derlina, Hj. Menni, Abangku tersayang
H. Nasrun, Syahmidan, H. Mhd. Halomoan, adik-adikku Dina, Lily, Rasyid,
Ucapan terima kasih dan penghargaan yang tulus tiada terhingga atas
perhatian, nasehat, dorongan semangat dan do’a yang tiada hentinya kepada
penulis.
8. Abang-kakak senior dan kawan-kawanku khususnya: Yani Jambak, Nitha,
Merlin, Een, Faisal, Kak Umi, Renta, Muammar (Mumu), Bang Riza,
terutama buat Bang Umri Ubit yang telah membantu penulis dalam hal
memperoleh sample penelitian, dan teristimewa buat Ade Fuji Kusuma
yang selalu memberikan dorongan semangat dan perhatian, rekan Farmasi
Ekstensi stambuk 2006 lainnya yang tidak dapat disebutkan satu persatu
yang selalu memberikan semangat, dukungan do;a, berbagi suka dan duka
dalam menyelesaikan penilitian dan skripsi ini.
Penulis menyadari sepenuhnya bahwa dalam penulisan maupun penyajian
dalam tulisan ini masih jauh dari kesempurnaan, oleh karena itu dengan segala
Akhirnya, harapan penulis semoga skripsi ini dapat memberi manfaat bagi
kita semua.
Medan, Januari 2009 Penulis,
ABSTRAK
Telah dilakukan uji pendahuluan senyawa kimia golongan saponin,
steroid/triterpenoid serta ekstraksi, isolasi dan identifikasi senyawa sapogenin dari
teripang (timun laut) Stichopus sp.
Ekstraksi dilakukan dengan cara maserasi dengan menggunakan pelarut
etanol 95%, kemudian dihidrolisis dengan asam klorida 2 N, selanjutnya disari
dengan pelarut kloroform. Terhadap ekstrak kloroform dilakukan kromatografi
lapis tipis untuk memperoleh pemisahan yang paling baik, kemudian dilakukan
isolasi dengan menggunakan kromatografi preparatif dengan fase gerak kloroform
- toluen (70:30). Terhadap senyawa yang diisolasi dilakukan uji kemurnian
dengan kromatografi lapis tipis dua arah. Isolat yang diperoleh diidentifikasi
dengan spektrofotometri ultraviolet (UV), spektrofotometri inframerah (IR),
spektrometri massa (MS).
Hasil uji pendahuluan senyawa kimia menunjukkan adanya senyawa
saponin dan steroid/triterpenoid. Dan hasil isolasi dari ekstrak kloroform
diperoleh 4 isolat. Isolat 1 mempunyai harga Rf 0,17, isolat 2 harga Rf 0,35, isolat
3 harga Rf 0,56 dan isolat 4 harga Rf 0,93. Hasil identifikasi isolat 3 secara
spektrofotometri ultraviolet diperoleh panjang gelombang maksimum 236 nm dan
mempunyai gugus fungsi O-H, C-H alifatis, -CH3-, -CH2- dan C-O. Dan hasil
karakteristik spektrometri massa mempunyai BM 388 dan merupakan senyawa
ABSTRACT
Chemical compound preface test of saponin, steroide/triterpenoide,
extraction, isolation and identification sapogenin compound of sea
cucumber/teripang Stichopus sp have been done.
Extraction was done by maseration using ethanol 95%, and hydrolized by
hydrochloric acid 2 N, then extracted by CHCl3. To CHCl3 extract, Thin Layer
Chromatography was done to achieve the best result, then isolated using
preparative chromatography with CHCl3 : toluene (70:30) as solving agent. To
isolated compound, purity test was done using two direction Thin Layer
Chromatography. The isolated result was identified by UV-Spectrophotometric,
Infra Red Spectrophotometric and Mass Spectrophotometric.
The result of chemical compound preface test shows that there is saponin
and steroide/triterpenoide. The result of isolation by extract CHCl3 got 4 isolate.
Isolate 1 with Rf 0,17, isolate 2 Rf 0,35, isolate 3 Rf 0,56 and isolate 4 Rf 0,93.
The result of identification isolate 3 by UV-Spectrophotometric has maximum
wave length 236 nm and purpose group O-H, aliphatic C-H, CH3, -CH-, and C-O.
Characterictic result by Mass-Spectrometri, molecular mass of the compound is
DAFTAR ISI
Halaman
JUDUL .... ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Uraian Hewan... 4
2.2 Kandungan Tubuh Teripang ... 5
2.3 Habitat dan Penyebaran... 6
2.4 Uraian Kimia ... 7
2.5 Ekstraksi ... 10
2.6 Kromatografi ... 11
2.6.1 Kromatografi Lapis Tipis ... 12
2.6.2 Kromatografi Lapis Tipis Preparatif ... 13
2.7 Spektrofotometri Ultra Violet ... 14
2.8 Spektrofotometri Infra Merah ... 15
2.9 Spektrometri Massa ... 18
BAB III METODE PENELITIAN ... 21
3.7.3 Uji warna dengan pereaksi Liebermann-Burchard(LB) ... 26
3.9 Analisis ekstrak etanol dengan cara KLT ... 27
3.10 Isolasi senyawa sapogenin dari ekstrak etanol ... 27
3.11 Analisis ekstrak kloroform dengan cara KLT ... 27
3.12 Pemisahan senyawa sapogenin teripang dengan KLT Preparatif 28 3.13 Uji kemurnian senyawa hasil isolasi dengan KLT ... 29
3.14 Uji kemurnian senyawa hasil isolasi dengan KLT dua arah ... 29
3.15 Identifikasi Isolat ... 30
3.15.1 Identifikasi isolat dengan Spektrofotometri UV ... 30
3.15.2 Identifikasi isolat dengan Spektrofotometri Inframerah ... 30
3.15.3 Identifikasi isolat dengan Spektrometri Massa ... 31
BAB IV. HASIL PERCOBAAN DAN PEMBAHASAN ... 32
BAB V. KESIMPULAN DAN SARAN ... 35
5.1 Kesimpulan ... 35
5.2 Saran ... 35
DAFTAR PUSTAKA ... 36
DAFTAR GAMBAR
Gamba r Halaman
1. Gambar Hewan Teripang segar ... 39
2. Gambar simplisia teripang ... 40
3. Bagan ekstraksi senyawa sapogenin dari hewan teripang... 41
4. Bagan isolasi senyawa sapogenin dari ekstrak kloroform ... 42
5. Gambar Kromatogram hasil KLT ekstrak Etanol ... 43
6. Gambar Kromatogram hasil KLT ekstrak Kloroform ... 44
7. Gambar kromatogram hasil KLT ekstrak kloroform ... 45
8. Gambar kromatogram ekstrak kloroform KLT Preparatif ... 46
9. Gambar kromatogram KLT hasil isolat ... 47
10. Gambar kromatogram hasil KLT dua arah ... 48
11. Gambar spektrum Ultra violet ... 49
12. Spektrum Inframerah ... 50
13. Spektrum massa isolat ... 51
DAFTAR LAMPIRAN
Lampiran Halaman
1. Hasil Identifikasi hewan laut teripang... 38
2. Gambar Hewan Teripang segar ... 39
3. Gambar simplisia teripang ... 40
4. Bagan ekstraksi senyawa sapogenin dari teripang ... 41
5. Bagan isolasi senyawa sapogenin dari ekstrak kloroform ... 42
6. Kromatogram hasil KLT ekstrak etanol ... 43
7. Kromatogram hasil KLT ekstrak kloroform ... 44
8. Kromatogram hasil KLT ekstrak kloroform ... 45
9. Kromatogram ekstrak kloroform secara KLT Preparatif ... 46
10. Kromatogram KLT hasil isolat ... 47
11. Gambar kromatogram hasil KLT dua arah dari isolat ... 48
12. Gambar spektrum Ultra violet ... 49
13. Gambar spektrum Inframerah ... 50
14. Gambar spektrum massa isolat... 51
15. Gambar spektrum massa pembanding ... 52
ABSTRAK
Telah dilakukan uji pendahuluan senyawa kimia golongan saponin,
steroid/triterpenoid serta ekstraksi, isolasi dan identifikasi senyawa sapogenin dari
teripang (timun laut) Stichopus sp.
Ekstraksi dilakukan dengan cara maserasi dengan menggunakan pelarut
etanol 95%, kemudian dihidrolisis dengan asam klorida 2 N, selanjutnya disari
dengan pelarut kloroform. Terhadap ekstrak kloroform dilakukan kromatografi
lapis tipis untuk memperoleh pemisahan yang paling baik, kemudian dilakukan
isolasi dengan menggunakan kromatografi preparatif dengan fase gerak kloroform
- toluen (70:30). Terhadap senyawa yang diisolasi dilakukan uji kemurnian
dengan kromatografi lapis tipis dua arah. Isolat yang diperoleh diidentifikasi
dengan spektrofotometri ultraviolet (UV), spektrofotometri inframerah (IR),
spektrometri massa (MS).
Hasil uji pendahuluan senyawa kimia menunjukkan adanya senyawa
saponin dan steroid/triterpenoid. Dan hasil isolasi dari ekstrak kloroform
diperoleh 4 isolat. Isolat 1 mempunyai harga Rf 0,17, isolat 2 harga Rf 0,35, isolat
3 harga Rf 0,56 dan isolat 4 harga Rf 0,93. Hasil identifikasi isolat 3 secara
spektrofotometri ultraviolet diperoleh panjang gelombang maksimum 236 nm dan
mempunyai gugus fungsi O-H, C-H alifatis, -CH3-, -CH2- dan C-O. Dan hasil
karakteristik spektrometri massa mempunyai BM 388 dan merupakan senyawa
ABSTRACT
Chemical compound preface test of saponin, steroide/triterpenoide,
extraction, isolation and identification sapogenin compound of sea
cucumber/teripang Stichopus sp have been done.
Extraction was done by maseration using ethanol 95%, and hydrolized by
hydrochloric acid 2 N, then extracted by CHCl3. To CHCl3 extract, Thin Layer
Chromatography was done to achieve the best result, then isolated using
preparative chromatography with CHCl3 : toluene (70:30) as solving agent. To
isolated compound, purity test was done using two direction Thin Layer
Chromatography. The isolated result was identified by UV-Spectrophotometric,
Infra Red Spectrophotometric and Mass Spectrophotometric.
The result of chemical compound preface test shows that there is saponin
and steroide/triterpenoide. The result of isolation by extract CHCl3 got 4 isolate.
Isolate 1 with Rf 0,17, isolate 2 Rf 0,35, isolate 3 Rf 0,56 and isolate 4 Rf 0,93.
The result of identification isolate 3 by UV-Spectrophotometric has maximum
wave length 236 nm and purpose group O-H, aliphatic C-H, CH3, -CH-, and C-O.
Characterictic result by Mass-Spectrometri, molecular mass of the compound is
BAB I
PENDAHULUAN
1.1 Latar Belakang
Indonesia merupakan Negara kepulauan yang memiliki panjang pantai
sekitar 81.000 km. Dengan kondisi alam dan iklim yang hampir tidak banyak
mengalami perubahan sepanjang tahun, perairan pantai Indonesia sangat
memungkinkan bila memiliki banyak jenis biota ekonomis. Salah satu diantaranya
yaitu teripang (Martoyo dkk, 2006).
Teripang adalah salah satu anggota hewan berkulit duri (Echinodermata).
Namun tidak semua jenis teripang mempunyai duri pada kulitnya. Ada beberapa
jenis teripang yang tidak berduri (Martoyo dkk, 2006). Tubuh teripang lunak,
berdaging, dan berbentuk silindris memanjang seperti buah ketimun, oleh karena
itu dinamakan ketimun laut seperti buah ketimun. Dari beberapa jenis teripang
tersebut, hanya tiga genus yang ditemukan di perairan pantai Indonesia. Ketiga
genus tersebut adalah Holothuria, Muelleria, Stichopus (Martoyo dkk, 2006).
Indonesia penghasil teripang terbesar di dunia, sayang, tak ada yang
mengolahnya (Trubus, 2006).
Teripang mempunyai nilai ekonomi penting karena kandungan atau kadar
nutrisinya yang tinggi. Dari hasil penelitian, kandungan nutrisi teripang dalam
kondisi kering terdiri dari protein sebanyak 82%, lemak 1,7%, kadar air 8,9%,
kadar abu 8,6%, dan kadar karbohidrat 4,8% (Martoyo dkk, 2006).
Studi di China mengungkapkan bahwa gamat (Sea cucumber, Teripang)
yang serupa dengan komponen ginseng yang aktif, ganoderma, dan
tumbuh-tumbuhan bumbu tonik yang terkenal. Studi China ini menunjukkan adanya anti
kanker pada saponin dan polisakarida yang terkandung di dalam gamat. Studi
modern ini membuktikan bahwa gamat dapat digunakan sebagai suatu tonik dan
suplemen gizi (Anonim, 2008).
Penelitian yang modern ini telah membuktikan bahwa sea cucumber
bermanfaat untuk penyakit musculoskeletal inflame-matory, khususnya arthritis
rematik, osteoarthritis dan penyakit rematik yang mempengaruhi tulang belakang.
Teripang juga mempunyai kemampuan dalam regenerasi sel yang merupakan
alasan utama dipakai menyembuhkan berbagai penyakit (Trubus, 2006).
Berdasarkan hal diatas, maka penulis mengisolasi senyawa sapogenin yang
terdapat pada teripang genus Stichopus. Penelitian ini dilakukan dengan cara
ekstraksi terhadap teripang, hidrolisis ekstrak, dilanjutkan dengan kromatografi
lapis tipis (KLT) dan KLT Preparatif. Isolat yang diperoleh di identifikasi secara
spektrofotometri ultraviolet (UV), spektrofotometri inframerah (IR), spektrometri
massa (MS).
1.2 Perumusan Masalah
1. Apakah teripang Stichopus sp mengandung senyawa sapogenin?
2. Bagaimana cara mengisolasi senyawa sapogenin dari hewan teripang Stichopus
sp. dan apakah isolatnya dapat diidentifikasi secara spektrofotometri
ultraviolet (UV), spektrofotometri inframerah (IR) dan spektrometri massa
1.3 Hipotesis
1. Hewan teripang Stichopus sp.mengandung senyawa sapogenin .
2. Senyawa sapogenin dari hewan teripang Stichopus sp. dapat diisolasi dengan
cara KLT preparatif menggunakan campuran pelarut dengan perbandingan
tertentu dan isolatnya dapat diidentifikasi secara spektrofotometri ultraviolet
(UV), spektrofotometri inframerah (IR) dan spektrometri massa (MS).
1.4 Tujuan Penelitian
1. Untuk mengetahui senyawa sapogenin yang terdapat pada hewan teripang
Stichopus sp.
2. Untuk mengetahui cara mengisolasi senyawa sapogenin dari hewan teripang
Stichopus sp. dan cara mengidentifikasi isolatnya dengan spektrofotometri
ultraviolet (UV), spektrofotometri inframerah (IR) dan spektrometri massa
(MS).
1.5 Manfaat Penelitian
Sebagai informasi tentang senyawa sapogenin hasil isolasi dari teripang
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Hewan
Teripang merupakan salah satu anggota hewan berkulit duri
(Echinodermata). Namun, tidak semua jenis teripang mempunyai duri pada
kulitnya. Ada beberapa jenis teripang yang tidak berdur (Martoyo dkk, 2006)i.
Selain teripang, bintang laut yang termasuk dalam filum Echinodermata
yaitu bintang laut (Asteriodea) dan bulu babi (Echinoidea). Diantara empat famili
teripang, hanya famili Holothuriidae yang dapat dimakan dan bernilai
ekonomis(Martoyo dkk, 2006).
Tubuh teripang lunak, berdaging dan berbentuk silindris memanjang
seperti buah ketimun. Oleh karena itu, hewan ini dinamakan ketimun laut.
Gerakan teripang saangat lambat sehingga hampir seluruh hidupnya berada di
dasar laut. Warna tubuh teripang bermacam-macam, mulai dari hitam, abu-abu,
kecokelat-cokelatan, kemerah-merahan, kekuning-kuningan, sampai putih
(Martoyo dkk, 2006).
Tidak semua jenis teripang yang ditemukan di perairan Indonesia
mempunyai nilai ekonomis penting. Jenis teripang yang dapat dimakan dan
mempunyai nilai ekonomis penting terbatas pada famili Holothuriidae pada genus
Holothuria, Muelleria, dan Stichopus (Martoyo dkk, 2006).
Secara garis besar klasifikasi dari beberapa jenis teripang bernilai ekonomi
Filum : Echinodermata
Sub-filum : Echinozoa
Kelas : Holothuroidea
Sub-kelas : Aspidochirotacea
Ordo : Aspidochirotida
Dari bebarapajenis teripang , hanya tiga genus yang ditemukan di
perairan pantai Indonesia. Ketiga genus tersebut adalah Holothuria, Mulleria,
Stichopus. Dari ketiga genus tersebut ditemukan sebanyak 23 spesies.
Di pasaran internasional, semua jenis teripang tersebut dikenal dengan
nama teat fish. Nama-nama teripang di tiap-tiap Negara juga berbeda-beda, di
Indonesia nama lokalnya teripang (timun laut), Malaysia namanya trepang, gamat,
Hongkong namanya haysom, timun laut, Thailand namanya pling khao, India
namanya attai, dan Jerman namanya seegueke (trepang) (Martoyo dkk, 2006).
2.2 Kandungan Tubuh Teripang
Ekstrak murni teripang mempunyai kecenderungan menghasilkan holotoksin
yang efeknya sama dengan antimicyn dengan kadar 6,25 – 25
mikrogram/milliliter.
Teripang mempunyai nilai ekonomi penting karena kandungan atau kadar
kondisi kering terdiri dari protein sebanyak 82%, lemak 1,7%, kadar air 8,9%,
kadar abu 8,6%, dan kadar karbohidrat 4,8% (Martoyo dkk, 2006).
Studi di China mengungkapkan bahwa gamat (Sea cucumber, Teripang)
juga mengandung saponin glikosida. Komponen ini mempunyai suatu struktur
yang serupa dengan komponen ginseng yang aktif, ganoderma, dan
tumbuh-tumbuhan bumbu tonik yang terkenal. Studi China ini menunjukkan adanya anti
kanker pada saponin dan polisakarida yang terkandung di dalam gamat. Studi
modern ini membuktikan bahwa gamat dapat digunakan sebagai suatu tonik dan
suplemen gizi (Anonim, 2008).
Penelitian yang modern ini telah membuktikan bahwa sea cucumber
bermanfaat untuk penyakit musculoskeletal inflame-matory, khususnya arthritis
rematik, osteoarthritis dan penyakit rematik yang mempengaruhi tulang belakang.
Teripang juga mempunyai kemampuan dalam regenerasi sel yang merupakan
alasan utama dipakai menyembuhkan berbagai penyakit (Trubus, 2006).
2.3 Habitat dan Penyebaran
Teripang dapat ditemukan hampir di seluruh perairan pantai, mulai dari
daerah pasang-surut yang dangkal sampai perairan yang lebih dalam. Teripang
lebih menyukai perairan yang jernih dan airnya relative tenang. Umumnya,
masing-masing jenis memiliki habitat yang spesifik. Misalnya, teripang putih
banyak ditemukan di daerah yang berpasir atau pasir yang bercampur Lumpur
pada kedalaman 1 – 40 meter.
Dihabitatnya, terdapat jenis teripang yang hidup berkelompok dan ada pula
yang hidup soliter (sendiri). Sumber utama makanan teripang di alam yaitu
dan plankton. Jenis makana lain adalah organisme-organisme kecil, protozoa,
algafilamen, rumput laut, dan potongan-potongan kecil hewan maupun tumbuhan
laut serta partikel – partikel pasir.
Penyebaran teripang di Indonesia sangat luas. Beberapa daerah penyebaran
antara lain meliputi perairan pantai Madura, Jawa Timur, Bali, Sumba, Lombok,
Aceh, Bengkulu, Bangka, Riau dan sekitarnya, Belitung, Kalimantan, Sulawesi,
Maluku, Timor dan Kepulauan Seribu (Martoyo dkk, 2006).
Indonesia penghasil teripang terbesar di dunia, sayang, tak ada yang
mengolahnya (Trubus, 2006).
2.4 Uraian Kimia
2.4.1 Triterpenoid dan Steroid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam
satuan isoprene dan secara biosintesis diturunkan dari hidrokarbon C-30 asiklik
yaitu skualena. Triterpenoid dapat dibagi atas empat golongan yaitu triterpenoid
sebenarnya, steroid, saponin dan glikosida jantung (Harbone, 1987).
a. Triterpen sebenarnya
Menurut jumlah cincin yang terdapat dalam struktur molekulnya
digolongkan atas:
1. Triterpen asiklik
2. Triterpen trisiklik
3. triterpen tetrasiklik
b. Steroid
Steroid adalah triterpen yang terbuka dasarnya cincin siklopentana
perhidrofenantren (Harbone, 1987). Inti steroid dasar sama dengan inti lanosterol
dan triterpenoid tetrasiklik lain, tetapi hanya pada dua gugus metal yang terikat
pada sistim cincin, pada posisi 10 dan 13. Nama “sterol” dipakai khusus untuk
steroid alkohol. Sterol biasanya mempunyai gugus hidroksil pada atom C-3 dan
suatu ikatan rangkap pada posisi 5 dan 6 (Manitto, 1981).
Sterol adalah triterpena yang kerangka dasarnya sistem siklopentana
perhidrofenantren. Dahulu sterol terutama dianggap sebagai senyawa satwa
(sebagai hormon kelamin, asam empedu, dan lain-lain) (Harborne, 1987).
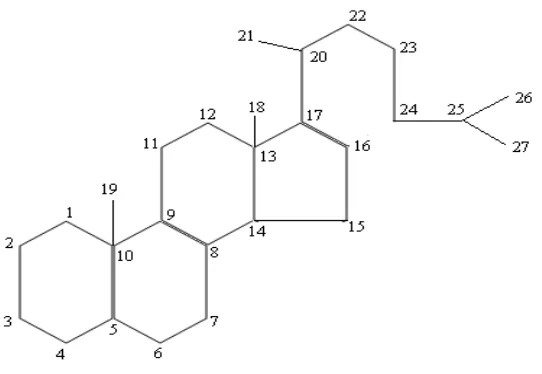
Kerangka dasar dan sistem penomoran steroida (Robinson, 1995) dapat
dilihat pada gambar berikut ini.
Gambar Kerangka dasar steroida dan sistem penomorannya
Dari pandangan kimiawan organik, semua molekul steroida adalah turunan
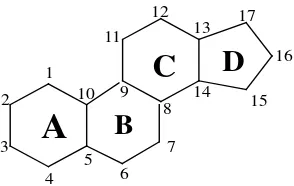
jenuh dari fenantren (hidrokarbon aromatik trisiklik). Gambar 9 berikut ini
B
Gambar Penulisan lambang keempat (A, B, C, D) inti steroida.
Berdasarkan sumber atau asalnya maka steroida dibagi atas empat
golongan (Manitto, 1981), yaitu :
a. Zoosterol yaitu steroida yang berasal dari hewan terutama vertebrata.
b. Fitosterol yaitu steroida yang berasal dari tumbuhan.
c. Mikosterol yaitu steroida yang berasal dari jamur (fungi).
d. Marinosterol yaitu steroida yang berasal dari organisme laut.
c. Saponin
Saponin mula-mula diberi nama demikian karena sifatnya yang khas
menyerupai sabun (bahasa latin sapo = sabun). Saponin adalah senyawa aktif
permukaan yang kuat yang menimbulkan busa jika dikocok dalam air dan dapat
menyebabakan hemolisis sel darah merah (Robinson, 1991).
Saponin steroid tersusun dari suatu aglikon steroid (sapogenin) yang
terikat pada suatu oligosakarida yang biasanya heksosa dan pentosa. Struktur
kimia dari aglikon saponin dibagi atas dua golongan yaitu sapogenin steroid dan
sapogenin triterpenoid pentasiklik (Farnsworth, 1966).
d. Glikosida Jantung 2.5Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
tertentu. Proses ekstraksi akan menghasilkan ekstrak. Ekstrak adalah sediaan
kental yang diperoleh dengan mengekstraksi senyawa aktif dari simplisia
menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut
diuapkan (Depkes, 2000). Penguapan ekstrak dilakukan dengan penguap vakum
putar pada suhu tidak lebih dari 40oC dalam suasana tekanan dikurangi
(Harborne,1987).
Beberapa metode ekstraksi dengan menggunakan pelarut (Depkes, 2000) yaitu :
A. Cara dingin
1. Maserasi
Maserasi adalah proses penyarian simplisia menggunakan pelarut dengan
beberapa kali pengocokan atau pengadukan pada temperatur kamar.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai terjadi
penyarian sempurna yang umumnya dilakukan pada temperatur kamar.
B. Cara panas
1. Refluks
Refluks adalah ekstraksi pelarut pada tempertur titik didihnya, selama waktu
tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin
balik.
2. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur lebih
tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada temperatur
3. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru, dilakukan
menggunakan alat soxhlet sehingga terjadi ekstraksi kontinu dengan jumlah
pelarut relatif konstan dengan adanya pendingin balik.
4. Infundasi
Infundasi adalah ekstraksi dengan pelarut air pada temperatur 90oC selama
15 menit.
5. Dekok
Dekok adalah ekstraksi dengan pelarut air pada temperatur 90oC semala 30
menit.
2.6 Kromatografi
Cara-cara kromatografi dapat dikelompokkan berdasarkan fase gerak dan
fase diam yang digunakan (Sastrohamidjojo, 1985) yaitu :
1. Fase gerak zat cair-fasa diam padat (kromatografi serapan)
- Kromatografi lapis tipis
2. Fasa gerak gas-fasa diam padat
- Kromatografi gas padat
3. Fasa gerak cair-fasa diam cair
- Kromatografi kertas
4. Fasa gerak gas-fasa diam cair
- Kromatografi gas cair
2.6.1 Kromatografi Lapis Tipis
Kromatografi lapis tipis merupakan kromatografi serapan dimana fasa diam
yang disebut larutan pengembang (Gritter. dkk, 1991). Campuran yang akan
dipisah, berupa larutan, ditotolkan berupa bercak. Setelah plat atau lapisan ditaruh
di dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fasa
gerak), pemisahan terjadi selama perambatan kapiler (pengembangan).
Selanjutnya, senyawa yang tidak berwarna harus ditampakkan (dideteksi) (Stahl,
1985).
Deteksi
Terdapat berbagai kemungkinan untuk deteksi senyawa tanwarna pada
kromatogram. Deteksi paling sederhana adalah jika senyawa menunjukkan
penyerapan di daerah UV gelombang pendek (radiasi utama pada kira-kira 254
nm) atau jika senyawa itu dapat dideteksi ke fluoresensi radiasi UV gelombang
panjang (365 nm). Jika dengan kedua cara itu senyawa tidak dapat dideteksi,
harus dicoba dengan reaksi kimia ; pertama tanpa dipanaskan, kemudian bila perlu
dipanaskan. Deteksi biologi pada beberapa kasus dapat dilakukan (Stahl, 1985).
Faktor-faktor yang mempengaruhi gerakan noda dalam kromatografi lapis
tipis yang juga mempengaruhi harga Rf, yaitu :
1. Struktur kimia dari senyawa yang sedang dipisahkan.
2. Sifat dari penyerap dan derajat aktifasinya. Perbedaan penyerap akan
memberikan perbedaan yang besar terhadap harga Rf, meskipun
menggunakan fasa gerak yang sama.
3. Tebal dan kerataan dari lapisan penyerap.
4. Pelarut (derajat kemurnian) fase gerak
5. Derajat kejenuhan dari uap dalam bejana pengembangan yang dilakukan.
7. Jumlah cuplikan yang digunakan.
8. Suhu.
9. Kesetimbangan.
2.6.2 Kromatografi Lapis Tipis Preparatif
Kromatografi lapis tipis preparatif merupakan salah satu metode
pemisahan yang memerlukan pembiayaan yang paling murah dan menggunakan
peralatan sederhana yaitu kromatografi lapis tipis preparatif (KLTP).
Ketebalan penyerap yang sering dipakai adalah 0,5-2 mm. Ukuran plat
kromatografi biasanya 20x20 cm. Pembatasan ketebalan lapisan dan ukuran plat
sudah tentu mengurangi jumlah bahan yang dapat dipisahkan dengan KLTP.
Penyerap yang paling umum digunakan ialah silika gel dan dipakai untuk
pemisahan campuran senyawa lipofilik maupun campuran senyawa hidrofilik.
Penotolan cuplikan dilakukan berupa pita dengan melarutkan cuplikan
dalam sedikit pelarut. Cuplikan ditotolkan berupa pita dengan jarak sesempit
mungkin karena pemisahan bergantung pada lebar pita. Penotolan dapat dilakukan
dengan pipet tetapi lebih baik dengan penotol otomatis. Pelarut yang baik untuk
melarutkan cuplikan adalah pelarut yang atsiri ( heksan, diklormetan, etil asetat)
dan konsentrasi cuplikan harus sekitar 5-10%.
Kebanyakan penjerap KLTP mengandung indikator fluoresensi yang
membantu mendeteksi kedudukan pita yang terpisah sepanjang senyawa yang
dipisahkan menyerap sinar UV.
Untuk senyawa yang tidak menyerap sinar UV, ada beberapa pilihan:
b) menutup plat dengan sepotong kaca menyemprot salah satu sisi dengan
pereaksi semprot
c) menambahkan senyawa pembanding (Hostettmann, 1995).
Setelah pita ditampakkan dengan cara yang tidak merusak maka senyawa
yang tak berwarna dengan penjerap dikerok dari plat kaca. Cara ini berguna untuk
memisahkan campuran beberapa senyawa hingga diperoleh senyawa murni
(Gritter dkk, 1991).
2.7 Spektrofotometri Ultra Violet
Spektrofotometri ultra violet merupakan suatu teknik analisis yang
berdasarkan atas pengukuran serapan suatu larutan yang dilalui radiasi
monokromatis ultra ungu. Serapan molekul di daerah ultra violet bergantung
kepada struktur elektronik dari molekul dan penyerapan sejumlah energi akan
menyebabkan elektron pada tingkat dasar tereksitasi ke orbital yang lebih tinggi
(Silverstein dkk, 1981).
Panjang gelombang di dalam ultra violet biasanya dinyatakan dalam
nanometer (1 nm = 10-9 m). Spektrum serapan yabg lebih kecil dari 200 nm
disebut spektrometri ultra violet jauh (hampa udara). Bagian ultra violet (ultra
violet dekat) dari spektrum elektromagnetik terentang dari 200-400 nm
(Silverstein dkk,1981).
Beberapa istilah yang digunakan di dalam pembahasan spektrum elektronik
meliputi:
a) kromofor, suatu gugus kovalen tidak jenuh yang bertanggung jawab untuk
b) Auksokrom, suatu gugus jenuh dengan elektron tidak terikat dimana bila
tersubstitusi pada suatu kromofor, akan menyebabakan perubahan panjang
gelombang dan intensitas serapan(sebagai contoh OH, NH2, dan Cl).
c) Geseran batokromik, geseran dari serapan ke panjang gelombang yang
lebih panjang karena substitusi auksokrom atau pengaruh pelarut (geseran
merah).
d) Geseran hipsokromik, geseran dari serapan ke panjang gelombang yang
lebih pendek karena hilangnya auksokrom atau pengaruh pelarut (geseran
biru).
e) Hiperkromik, suatu kenaikan dari intensitas serapan.
f) Hipokromik, suatu penurunan dari intensitas serapan (Silverstein dkk,
1986).
Komponen-komponen pokok dari spektrofotometer meliputi sumber tenaga
radiasi yang stabil, sistim yang terdiri atas lensa-lensa, cermin, celah-celah dan
lain-lain, monokromator untuk mengubah radiasi menjadi komponen-komponen
panjang gelombang tunggal, tempat cuplikan yang transparan, dan detektor radiasi
yang dihubungkan dengan sistem meter dan pencatat (Sastrohamidjojo, 1991).
2.8 Spektofotometri Infra Merah
Pancaran infra merah pada umumnya mengacu pada bagian spektrum
elektromagnetik yang terletak diantara daerah tampak dan daerah gelombang
mikro. Bagi kimiawan organik, sebagian besar kegunaannya terbatas di antara
4000 cm-1 dan 666 cm-1 atau 2,5 – 15,0 μm (Silverstein dkk, 1986).
Bila sinar infra merah dilewatkan melalui cuplikan senyawa organik, maka
tanpa diserap. Jika kita menggambarkan antara persen absorbansi atau persen
transmitansi lawan frekuensi maka akan dihasilkan suatu spektrum infra merah
(Sastrohamidjojo, 1991).
Cara menganalisis spektrofotometri infra merah perhatian dipusatkan pada
penentuan ada atau tidaknya beberapa gugus fungsional utama seperti C=O, O-H,
N-H, C-O, C=C, C=N. Berikut ini langkah umum untuk menganalisis pita-pita
yang penting
1. Gugus karbonil (C=O)
Gugus C=O terdapat pada daerah 1820 – 1600 cm-1 (5,6 – 6,1 μm). Puncak ini
biasanya yang terkuat dengan lebar medium dalam spektrum. Serapan tersebut
sangat karakteristik.
Bila gugus C=O ada, ujilah gugus fungsi berikut
a) Asam dapat dilihat pada serapan melebar didekat 3400 – 2400 cm-1
(biasanya tumpang tindih dengan C-H).
b) Amida adanya gugus NH
Serapan medium didekat 3500 cm-1 (2,85 μm) kadang-kadang puncak
rangkap
c) Ester adanya C-O
Serapan kuat didekat 1300 – 1000 cm-1 (7,7 – 10 μm).
d) Anhidrida mempunyai dua serapan C=O didekat 1810 dan 1760 cm-1 (5,5
dan 5,7 μm).
e) Aldehida adanya CH aldehid
Dua serapan lemah didekat 2850 dan 2750 cm-1 (3,50 dan 3,65 μm), yaitu
f) Keton bila kelima kemungkinan di atas tidak ada
2. Bila gugus C=O tidak ada maka ujilah gugus fungsi berikut
a) Alkohol (OH) dengan munculnya serapan melebar didekat 3600 sampai
3300 cm-1 (2,6 – 3,0 μm). Pembuktian selanjutnya yaitu adanya serapan
C-O didekat 1300-1000 cm-1 (7,7-10 μm).
b) Amida (NH) dengan munculnya serapan medium didekat 3500 cm-1
(2,85 μm).
c) Eter dengan melihat serapan C-O (serapan OH tidak ada) didekat 1300
sampai 1000 cm-1 (7,7-10 μm).
3. Ikatan rangkap dua dan cincin aromatik
a) Ikatan rangkap dua (C=C) memiliki serapan lemah didekat 1650 cm-1
(6,1 μm).
b) Serapan medium tinggi kuat pada daerah 1650 – 1450 cm-1 (6,7 μm) sering
menunjukkan cincin aromatik.
c) Kemungkinan adanya gugus tersebut diatas dapat dibuktikan dengan
memperhatikan serapan di daerah CH. Aromatik dan vinil CH terdapat di
atas daerah 3000 cm-1 (3,3 μm). Sedangkan CH alifatik terjadi dibawah
daerah tersebut.
4. Ikatan rangkap tiga
a) Ikatan rangkap tiga (C≡N) memiliki serapan medium dan tajam didekat
2250 cm-1(4,5 μm).
b) Ikatan rangkap tiga (C≡C) memiliki serapan lemah t api tajam di dekat
5. Gugus nitro
Adanya gugus nitro muncul dua serapan kuat pada 1600-1500 cm-1
(6,25-6,67 μm) dan 1690-1300 cm-1 (7,2-7,7 μm).
6. Hidrokarbon
a) Bila keempat serapan gugus fungsi tersebut di atas tidak ada.
b) Serapan utama untuk CH didekat 3000 cm-1(3,3 μm)
c) Spektrumnya sangat sangat sederhana, hanya terdapat serapan lain-lain
didekat 1450 cm-1 (6,90 μm) dan 1375 cm-1 (7,27 μm) (Sastrohamidjojo,
1991).
2.9 Spektrometri Massa
Spektrometri massa adalah suatu teknik analisis yang berdasarkan pada
pemisahan berkas ion-ion yang sesuai dengan perbandingan massa dengan muatan
dan pengukuran intensitas dari berkas ion-ion tersebut. Molekul – molekul
organik ditembakkan dengan berkas elektron dan diubah menjadi ion-ion
bermuatan positip yang bertenaga tinggi (ion-ion molekuler atau ion-ion induk),
yang dapat pecah menjadi ion-ion yang lebih kecil (ion-ion pecahan atau ion-ion
anak), lepasnya elektron dari molekul menghasilkan radikal kation dan proses ini
dapat dinyatakan sebagai M M+. Ion molekul M+ biasanya terurai menjadi
sepasang pecahan/fragmen, yang dapat berupa radikal dan ion, atau molekul yang
kecil dan radikal kation (Sastrohamidjojo,1991).
Spektometri massa menembaki bahan yang sedang diteliti dengan berkas
elektron dan secara kuantitatif mencatat hasilnya sebagai suatu spektrum
massanya (lebih tepat, massa dibagi muatan, tetapi kebanyakan ion bermuatan
tunggal). Terdapat lima bagian komponen dalam spektrometer massa yaitu:
1. Sistem penanganan cuplikan
Ini meliputi alat untuk memasukkan cuplikan, mikromanometer untuk
menentukan jumlah cuplikan yang masuk, alat (lubang molekul) pengukur
cuplikan yang masuk ruang pengionan serta sistem pemompaan. Cairan
dimasukkan dengan menyentuhkan pipet mikro ke piring gelas sintered atau
lubang tertentu terbuat dari air raksa atau galium atau dengan suntikan jarum
hipodermis.
2. Ruang pengionan dan pemercepat
Aliran gas dari lubang molekul masuk ke ruang pengionan (bekerja pada
tekanan 10-6 hingga 10-5 Torr) dan di sini ditembaki pada arah tegak lurus oleh
berkas elektron dari suatu filamen panas. Ion-ion positip yang terbentuk
karena antraksi dengan berkas elektron ini terdorong lewat lubang slit
pemercepat oleh suatu medan elektrostatik lemah antara penolak repeller dan
lubang pemercepat pertama tadi.
3. Tabung penganalisis dan magnet
Tabung logam yang dihampakan (10-7 – 10-8 Torr) berbentuk lengkung,
tempat melayangnya berkas ion dari sumber ion ke pengumpul.
4. Pengumpul ion dan penguat
Pengumpul ion terdiri atas satu atau lebih lubang pengumpul (kolimasi) serta
suatu silinder faraday, berkas ion menumbuk pengumpul dalam arah tegak
lurus, kemudian asyarat diperkuat (ampilikasi) oleh suatu penanda (multiflier)
5. Pencatat
Pencatat yang digunakan secara luas menggunakan lima buah galvanometer
terpisah yang mencatat serentak (Silverstein dkk, 1986).
Keuntungan utama spektrometri massa sebagai metode analisis yaitu
metode ini lebih sensitif dan spesifik untuk identifikasi senyawa yang tidak
diketahui atau untuk menetapkan keberadaan senyawa tertentu. Hal ini disebabkan
adanya pola fragmentasi yang khas sehingga dapat memberikan informasi
mengenai bobot molekul dan rumus molekul. Puncak ion molekul penting
dikenali karena memberikan bobot molekul senyawa yang diperiksa. Puncak
paling kuat pada spektrum, disebut puncak dasar (base peak), dinyatakan dangan
nilai 100% dan kekuatan puncak lain, termasuk puncak ion molekulnya
BAB III
METODOLOGI PENELITIAN
Metode yang digunakan adalah metode eksperimental meliputi
pengumpulan sampel, pemeriksaan golongan saponin, golongan steroid/triterpen,
pembuatan ekstrak, isolasi senyawa sapogenin dari ekstrak, analisis senyawa
sapogenin secara KLT, pemisahan senyawa sapogenin dengan cara KLT
preparatif, uji kemurnian senyawa sapogenin hasil isolasi dengan KLT dua arah
serta identifikasi isolat secara spektrofotometri UV, IR dan MS.
3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah: alat-alat gelas
laboratorium, elektromantel (EM 2000), hair-dryer, lampu UV 366 nm
(Dessaga), neraca analitik (Vibra AJ), neraca kasar (Salter AND), oven listrik
(Strok), penangas air (Yenaco), seperangkat alat kromatografi lapis tipis
(Dessaga), spektrofotometer ultraviolet (Shimadzu mini 1240), spektrofometer
inframerah (Shimadzu) dan spektrometri massa (Shimadzu QP2010S).
3.2 Bahan-bahan
Bahan yang digunakan dalam penelitian adalah hewan teripang segar
(mentimun laut) genus Stichopus.
Bahan kimia yang digunakan kecuali dinyatakan lain berkualitas pro analisa
(E. Merck) yaitu asam klorida pekat, asam asetat anhidrat, asam sulfat pekat, etil
asetat, n-heksan, kalium fosfat monobasa, kloroform, metanol, natrium
hidroksida, toluen, plat pra lapis silika gel GF254,. Etanol 95 % hasil destilasi dan
3.3 Pengumpulan dan Pengolahan Sampel 3.3.1 Pengumpulan Sampel
Pengumpulan sampel dilakukan secara purposif, yaitu tanpa membandingkan dengan daerah lain, sampel yang digunakan adalah hewan
teripang segar yang berasal dari perairan Sabang, Aceh.
3.3.2 Identifikasi Hewan
Identifikasi hewan teripang dilakukan di Pusat Penelitian Oseanografi
(Puslit Oseanografi Lipi), Jakarta. Hasil identifikasi hewan dapat dilihat
pada lampiran 1 halaman 38.
3.3.3 Pengolahan Sampel
Sampel yang digunakan adalah hewan teripang segar, dimana banyaknya
sampel yang diperiksa adalah satu ekor teripang segar dengan berat 1,2 kg.
Cara pengolahan:
1. Pencucian
Hewan teripang dibersihkan dari kotoran dengan cara mencucinya
dibawah air mengalir hingga bersih, ditiriskan kemudian ditimbang
beratnya. Beratnya adalah 1,2 kg.
2. Pengeluaran isi perut
Isi perut dan air dalam tubuh hewan teripang segar dikeluarkan dengan
cara memijat-mijat hingga isi perut dan air dapat keluar melalui anus
dan tubuh teripang menjadi gepeng. Ditiriskan lalu ditimbang,
diperoleh berat 1,18 kg. Kemudian dipotong-potong dengan ukuran ±
3. Pengeringan
Setelah isi perut dikeluarkan, kemudian teripang dikeringkan di dalam
lemari pengering selama 2 minggu sampai kadar air yang ada dalam
tubuh teripang berkurang.Teripang yang sudah kering disebut simplisia
hewan. Simplisia lalu diperkecil potongannya dan ditimbang,
diperoleh berat 48 g. Sebelum digunakan disimpan dalam wadah
plastik kedap udara dan terlindung dari cahaya.
3.4 Lokasi Penelitian
Penelitian dilaksanakan di Laboratorium Farmakognosi Fakultas Farmasi
Universitas Sumatera Utara Medan.
3.5 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakterisasi simplisia meliputi pemeriksaan makroskopik hewan
teripang segar, makroskopik simplisia dan penetapan kadar air.
3.5.1 Pemeriksaan Makroskopik
Pemeriksaan makroskopik dilakukan terhadap hewan teripang segar dan
simplisia dengan cara mengamati warna, bentuk, bau dan ukuran hewan teripang
segar dan simplisia. Gambar teripang segar dan simplisia dapat dilihat pada
lampiran 2 dan 3 halaman 39 dan 40.
3.5.2 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (Destilasi Toluen).
Alat-alat terdiri dari labu alas bulat 500 ml, alat penampung, pendingin, tabung
a) Penjenuhan toluen
Sebanayak 200 ml toluen dan 2 ml air suling dimasukkan kedalam labu
alasbulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2
jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume
air dalam tabung penerima dibaca dengan ketelitian 0,01 ml.
b) Penetapan kadar air simplisia
Cara kerja :
Kedalam labu yang berisi toluen jenuh di atas dimasukkan 5 g simplisia
yang telah ditimbang seksama, lalu dipanaskan hati-hati selama 15 menit, setelah
toluen mendidih, kecepatan tetesan diatur 2 tetes untuk tiap detik sampai sebagian
air terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes tiap detik.
Setelah semua air terdestilasi, bagian bagian dalam pendingin dibilas dengan
toluen, destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan
mendingin pada suhu kamar. Setelah air dan toluen memisah sempurna, dibaca
volume air dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai
dengan kandungan air yang di dalam bahan yang diperiksa. Kadar air dihitung
dalam persen (Depkes, 1979). Hasil dapat dilihat dalam pembahasan halaman 32.
3.6 Pembuatan Larutan Pereaksi 3.6.1 Larutan Asam Klorida 2 N
Sebanyak 17 ml larutan asam klorida pekat ditambahkan air suling hingga
100 ml (Depkes, 1979).
3.6.2 Larutan Kalium Fosfat Monobasa0,2 M
Sebanyak 2,72 g kalium fosfat monobasa dilarutkan dalam air suling bebas
3.6.3 Larutan Natrium Hidroksida 0,2 N
Sebanyak 800 mg natrium hidroksida dilarutkan dalam air suling bebas
karbondioksida hingga 100 ml (Depkes, 1979).
3.6.4 Larutan Dapar Fosfat pH 7,4
Sebanyak 50 ml kalium fosfat monobasa 0,2 M dicampurkan dengan 39,1
ml natrium hidroksida 0,2 N, lalu diencerkan dengan air suling hingga 200 ml
(Depkes, 1979).
3.6.5 Larutan Liebermann-Burchard (LB)
Diambil 20 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat.
Larutan penyemprot sebanyak 5 ml asam asetat anhidrat dengan 5 ml asam sulfat
pekat, kemudian campuran dimasukkan kedalam 50 ml etanol 95%. Pengerjaan
dilakukan dalam kondisis dingin dan pereaksi dibuat baru (Depkes RI, 1995).
3.7 Pemeriksaan Senyawa Saponin 3.7.1 Uji Busa
Sebanyak 0,5 g simplisia dimasukkan ke dalam tabung reaksi,
ditambahkan 10 ml air suling panas, didinginkan kemudian dikocok kuat-kuat
selama 10 detik. Adanya saponin ditunjukkan dengan terbentuknya buih yang
mantap selama tidak kurang dari 10 menit setinggi 1 cm sampai 10 cm dan
dengan penambahan 1 tetes asam klorida 2 N, buih tidak hilang (Depkes RI,
1995).
3.7.2 Uji Hemolisis Darah
Sebanyak 0,5 g simplisia dicampur dengan 50 ml larutan dapar fosfat pH
7,4, dipanaskan sebentar, kira-kira pada suhu 100 0C selama 10 menit, didinginkan
didiamkan selama 30 menit. Terjadinya hemolisis total menunjukkan adanya
saponin yang ditandai dengan terbentuknya lapisan bening di bagian tengah
larutan (Ditjen POM, 1995).
3.7.3 Uji Warna dengan Pereaksi Liebermann-Burchard (LB)
Sebanyak 0,5 g simplisia ditambahkan 10 ml etanol, kemudian
dimasukkan asam klorida 2 N, selanjutnya larutan direfluks selama 10 menit dan
disaring dalam keadaan panas. Filtrat diencerkan dengan 10 ml air suling, setelah
dingin ditambahkan 10 ml n-heksan, dikocok hati-hati dan dibiarkan memisah.
Lapisan n-heksan diambil dan diuapkan pada cawan penguap. Pada sisa ditetesi
20 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat (pereaksi LB). Hasil
positif adanya saponin bila memberikan warna hijau, biru, merah, merah muda
atau ungu (Farnsworth, 1966).
3.8Pembuatan Ekstrak
Cara kerja :
Sebanyak 40 g teripang kering yang telah dipotong - potong kecil, dimasukkan
ke dalam wadah gelas, lalu sebanyak 400 ml etanol 95% dituang ke dalam wadah
gelas (maserator), sesekali diaduk-aduk selama 6 jam, ditutup dan didiamkan
selama 24 jam. Setelah 24 jam, disaring, filtrat ditampung kemudian perlakuan
yang sama diulangi kembali sampai tiga kali perlakuan. Filtrat yang sudah
ditampung digabung dijadikan satu. Hasil terakhir di evaporasi dengan
menggunakan rotari evaporator sampai diperoleh ekstrak kental (Badan POM,
3.9 Analisis ekstrak etanol dengan cara KLT
Terhadap ekstrak etanol teripang dilakukan analisis dengan KLT
menggunakan fase diam: plat pra lapis silika gel GF254, fase gerak: n-heksan – etil
asetat dengan perbandingan (90:10), (80:20), (70:30), (60:40), (50:50) dengan
penampak bercak pereaksi LB.
Cara kerja:
Ekstrak etanol teripang ditotolkan pada plat pra lapis silika gel GF254,
setelah kering plat dimasukkan ke dalam masing-masing bejana yang telah jenuh
dengan uap pengembang, kemudian dikembangkan sampai jarak 1 cm dari tepi
atas plat. Plat dikeluarkan, dikeringkan kemudian disemprot dengan pereaksi LB.
Lalu plat dipanaskan pada suhu 110 0C selama 10 menit (Gritter, 1991).
Perubahan warna yang terjadi diamati dan harga Rf dihitung. Kromatogram
hasil KLT dapat dilihat pada lampiran 6 halaman 43.
3.10 Isolasi senyawa sapogenin dari ekstrak etanol
Cara kerja:
Sebanyak 10 g ekstrak etanol teripang ditambahkan asam klorida 2 N.
Kemudian ekstrak dihidrolisis dengan cara merefluksnya selama ± 6 jam,
selanjutnya filtrat diekstraksi dengan kloroform sebanyak 3 kali. Aglikon
sapogenin berada dalam lapisan kloroform. Ekstrak kloroform hasil hidrolisis
digabung dan dipekatkan (Harbone, 1987). Bagan isolasi senyawa sapogenin
dapat dilihat pada lampiran 4 halaman 41
3.11 Analisis ekstrak kloroform dengan cara KLT
Terhadap ekstrak kloroform teripang dilakukan analisis dengan KLT
toluen dengan perbadingan (90:10), (80:20), (70:30), (60:40), (50:50) dan fase
gerak n-heksan – etil asetat dengan perbandingan (90:10), (80:20), (70:30),
(60:40), (50:50) dengan penampak bercak pereaksi LB.
Cara kerja:
Ekstrak kloroform teripang ditotolkan pada plat pra lapis silika gel GF254,
setelah kering plat dimasukkan ke dalam masing-masing bejana yang telah jenuh
dengan uap pengembang, kemudian dikembangkan sampai jarak 1 cm dari tepi
atas plat. Plat dikeluarkan, dikeringkan kemudian disemprot dengan pereaksi LB.
Lalu plat dipanaskan pada suhu 110 0C selama 10 menit (Gritter, 1991).
Perubahan warna yang terjadi diamati dan harga Rf dihitung. Kromatogram
hasil KLT dapat dilihat pada lampiran 7 dan 8 halaman 44 dan 45.
3.12 Pemisahan Senyawa Sapogenin teripang dengan KLT preparatif
Terhadap ekstrak kloroform dilakukan pemisahan dengan KLT preparatif
menggunakan fase diam: silika gel GF254, fase gerak: kloroform - toluen (70:30)
dan penampak bercak pereaksi LB.
Cara Kerja:
Ekstrak kloroform teripang ditotolkan berupa pita pada plat KLT
berukuran 20 x 20 cm, setelah kering, plat dimasukkan ke dalam bejana yang telah
jenuh dengan uap pengembang. Kemudian dikembangkan sampai jarak 1 cm dari
tepi atas plat, plat dikeluarkan dan dikeringkan. Pada sisi kiri dan kanan plat
disemprot dengan pereaksi LB dan dipanaskan dengan bantuan hair-dryer hingga
diperoleh bercak yang jelas. Bagian plat silika yang sejajar dengan bercak yang
memberikan reaksi positif dengan pereaksi LB dikerok kemudian dilarutkan
Filtrat disaring, diuapkan pelarut metanolnya kemudian disimpan ke dalam
lemari pendingin. Kromatogram hasil KLT preparatif dapat dilihat pada lampiran 9 halaman 46.
3.13 Analisis senyawa hasil isolasi dengan KLT
Terhadap senyawa hasil isolasi dilakukan analisis dengan KLT
menggunakan fase diam: plat pra lapis silika gel GF254, fase gerak:
kloroform-toluen (70:30) dan penampak bercak pereaksi LB.
Cara kerja:
Senyawa hasil isolasi dengan KLT preparatif ditotolkan pada plat pra lapis
silika gel GF254, setelah kering plat dimasukkan ke dalam bejana yang telah jenuh
dengan uap pengembang, kemudian dikembangkan sampai jarak 1 cm dari tepi
atas plat. Plat dikeluarkan, dikeringkan kemudian disemprot dengan pereaksi LB.
Lalu plat dipanaskan pada suhu 110 0C selama 10 menit (Gritter, 1991).
Kromatogram hasil KLT dapat dilihat pada lampiran 10 halaman 47.
3.14 Uji kemurnian senyawa hasil isolasi dengan KLT dua arah
Terhadap senyawa hasil isolasi dilakukan uji kemurnian dengan KLT dua
arah menggunakan fase diam: plat pra lapis silika gel GF254, fase gerak I:
kloroform-toluen (70:30) dan fase gerak II: kloroform-metanol (30:70) sebagai
penampak bercak pereaksi LB.
Cara kerja:
Senyawa hasil isolasi dengan KLT preparatif ditotolkan pada plat silika,
setelah kering dimasukkan ke dalam bejana yang telah jenuh dengan uap
pengembang, dan dikembangkan dengan larutan pengembang I sampai jarak 1 cm
dan dikembangkan kembali dengan larutan pengembang II sampai jarak 1 cm dari
tepi atas plat. Plat dikeluarkan, dikeringkan kemudian disemprot dengan pereaksi
LB. Lalu plat dipanaskan pada suhu 110 0C selama 10 menit (Gritter, 1991).
Kromatogram hasil KLT dapat dilihat pada lampiran 11 halaman 48.
3.15 Identifikasi Isolat
3.15.1 Identifikasi isolat dengan spektrofotometer ultra violet
Cara kerja:
Isolat hasil isolasi dilarutkan dalam pelarut metanol, kemudian dimasukkan
kedalam kuvet yang telah dibilas dengan larutan sampel. Selanjutnya absorbansi
larutan sampel diukur pada panjang gelombang 200-400 nm (Noerdin, 1985).
Spektrum ultraviolet dari isolat dapat dilihat pada lampiran 12 halaman 49.
3.15.2 Identifikasi Isolat dengan Spektrofotometer Inframerah
Cara kerja:
Isolat hasil isolasi digerus halus kemudian ditambahkan KBr, dihaluskan.
Campuran dimasukkan kedalam alat pellet die dihubungkan dengan alat pompa
vakum dan penekan hidrolik 10 menit (tekanan 10000 – 15000 pound per inci).
Pompa vakum dimatikan, pellet die dilepaskan dari pompa hidrolik, kemudian
pellet KBr dikeluarkan. Pellet KBr ditempatkan pada pemegang cuplikan (sell
holder) (Noerdin, 1985). Spektrum inframerah dari isolat dapat dilihat pada
3.15.3 Karakterisasi isolat dengan spektrometri massa (MS)
Cara kerja:
Identifikasi isolat secara kromatografi gas-spektrofotometri massa
dilakukan dengan cara melarutkan isolat dengan pelarut n-hexan kemudian
dimasukkan melalui tempat penyuntikan kedalam suatu aliran gas pembawa pada
pangkal kolom dalam bentuk uap dan mengalami proses pembagian antara fase
gas dan fase tidak bergerak. Hasil pemisahan kromatografi gas difragmentasi oleh
detektor MS sehingga diperoleh fragmen-fragmen pada spektrum. Spektrum
BAB IV
HASIL DAN PEMBAHASAN
Hasil identifikasi yang dilakukan oleh Pusat Penelitian dan Pengembangan
Oseanologi – LIPI Jakarta terhadap teripang yang diteliti adalah filum
Echinodermata, kelas Holothuroidea, ordo Aspidochirotida, famili Stichopodidae,
genus Stichopus.
Hasil uji pendahuluan senyawa kimia menunjukkan adanya senyawa
golongan saponin dan steroid/triterpenoid. Uji pendahuluan senyawa kimia
golongan saponin terdiri dari uji busa dan uji hemolisis darah, sedangkan untuk
golongan steroid/triterpenoid yaitu uji warna dengan pereaksi
Liebermann-Burchard (LB).
Pada karakterisasi simplisia dilakukan pemeriksaan makroskopik teripang
segar Stichopus sp. dan simplisia dapat dilihat dari bentuk, warna, bau, ukuran,
dan pemeriksaan kadar air dengan metode azeotropi (destilasi toluen). Teripang
segar Stichopus sp.yang diteliti mempunyai bentuk bulat panjang berwarna coklat
kekuningan dengan bercak-bercak yang tidak teratur, dan pada bagian bawah
tubuhnya ada tonjolan-tonjolan yang disebut dengan duri berwarna coklat muda
kekuningan, mempunyai panjang 35 cm, lebar 6 cm, tebal 2 cm, berat 1,2 kg,
mempunyai bau yang khas. Sedangkan simplisia mempunyai warna kuning
kecoklatan, berkerut dan mempunyai lipatan lipatan, sedikit berbau. Dan hasil
dari penetapan kadar air diperoleh kadar air 16%. Hasil ini masih sesuai dengan
Menteri Pertanian No. 701/Kpts/TP>830/10/1987 yaitu kadar air maksimum 20 %
(Martoyo dkk, 2006).
Simplisia hewan teripang Stichopus sp. diekstraksi dengan cara maserasi
menggunakan pelarut etanol 95%, selanjutnya ekstrak etanol dihidrolisis selama 6
jam dengan bantuan asam klorida 2 N, kemudian disari/dikocok dengan kloroform
untuk mendapatkan senyawa sapogenin. Hasil maserasi dari 40 g simplisia
teripang diperoleh 12 g ekstrak etanol. Hasil penyarian dari 10 g ekstrak etanol
yang telah dihidrolisis diperoleh 1,5 g ekstrak kloroform.
Hasil KLT dari ekstrak kloroform dengan berbagai macam fase gerak yang
telah digunakan diperoleh hasil pemisahan yang paling bagus adalah kloroform –
toluen (70:30), diperoleh 4 noda. Noda 1 dengan harga Rf 0.17 (merah ungu),
noda 2 harga Rf 0,35 (merah ungu), noda 3 harga Rf 0,56 (ungu) dan noda 4 harga
Rf 0,93 (merah coklat) dengan penampak noda Liebermann-Burchard (LB). Hasil
kromatogram dapat dilihat pada lampiran
Pemisahan ekstrak kloroform dilakukan dengan KLT preparatif
menggunakan fase gerak: kloroform – toluen (70:30) dan penampak noda LB.
Diperoleh 4 pita. Pita 1 dengan Rf 0,17 (merah ungu), pita2 dengan Rf 0,35
(merah ungu), pita 3 dengan Rf 0,56 (ungu) dan pita 4 dengan Rf 0,93 (merah
coklat), dikerok kemudian dilarutkan dalam pelarut metanol. Hasil kromatogram
dapat dilihat pada lampiran
Dari hasil pita yang dikerok dan yang telah dilarutkan dalam metanol
diperoleh kristal (isolat). Dan dilakukan uji kemurnian pita 3 (isolat 3) dengan
KLT dua arah menggunakan fase diam: silika gel GF254, fase gerak I: kloroform -
Liebermann-Burchard (LB) diperoleh satu noda Rf 0,74 (ungu). Hasil
kromatogram dapat dilihat pada lampiran
Hasil identifikasi isolat 3 secara spektrofotometri ultraviolet diperoleh
panjang gelombang maksimum ( λ) 236 nm, dengan absorbansi 0,448,
menunjukkan adanya gugus kromofor yang mengalami transisi π π*
(Creswell, 1982). Hasil spektrum IR menunjukkan pita yang lebar pada bilangan
gelombang 3410,15 cm-1 menunjukkan adanya gugus O-H. Gugus O-H terikat
pada atom C siklis yang diperkuat dengan adanya pita pada bilangan gelombang
1103,28 cm-1 yaitu gugus C-O. Pita kuat pada bilangan gelombang 2931,8 cm-1
menunjukkan adanya gugus C-H alifatis yang diperkuat oleh pita pada bilangan
gelombang 1458,18 cm-1 (gugus –CH2-) dan 1373,32 cm-1 (gugus –CH3-)
(Silverstein dkk, 1986). Dan karakteristik spektrometri massa isolat 3 mempunyai
bobot molekul 388. Dari spektrum massa diperoleh puncak-puncak berurutan
sebagai berikut m/z : 388, 373, 355, 215, 201, 147 yang menunjukkan pola
fragmentasi yang khas dari golongan steroid. Kemungkinan puncak ion fragmen
karakteristiknya adalah sebagai berikut:
1. m/z 388 adalah bobot molekul senyawa.
2. m/z 373 (M+ - 15) adalah akibat terlepasnya molekul CH3
3. m/z 355 (M+ - 33) adalah akibat terlepasnya molekul H2O dan CH3.
4. m/z 215 (M+ - 173) menunjukkan fragmentasi pada cincin B.
5. m/z 201 (M+ - 187) menunjukkan fragmentasi pada cincin C.
6. m/z 147 (M+ - 261) menunjukkan fragmentasi pada cincin D.
Dari hasil analisis data spektrometri massa dapat disimpulkan bahwa isolat
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hasil uji pendahuluan senyawa kimia menunjukkan adanya senyawa
golongan saponin dan steroid/triterpenoid.
Isolasi senyawa sapogenin dari teripang dilakukan dengan cara KLT
Preparatif, dengan menggunakan fase gerak kloroform – toluen (70:30).
Hasil pemisahan isolat dengan KLT preparatif diperoleh tiga senyawa
sapogenin yaitu dengan harga Rf 0,17 (merah ungu), Rf 0,35 (merah ungu), Rf
0,56 (ungu) dengan fase gerak kloroform – toluen (70:30).
Hasil spektrum ultra violet menunjukkan panjang gelombang (λ)
maksimum 236 nm, sedangkan spektrum inframerah menunjukkan adanya gugus
O-H (3410,15 cm-1), gugus C-H alifatis (2931,80 cm-1), gugus C=C (1589,34 cm
-1
), gugus –CH2- (1458,18 cm-1), gugus –CH3- (1373,32 cm-1) dan gugus C-O (
1103,28 cm-1). Dan hasil karakterisasi dari spektrometri massa diperoleh bobot
molekul 388 dan isolat identik dengan kolesterol yaitu cholestan-3-ol (C27H48O).
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk melanjutkan identifikasi
terhadap isolat 1 dan 2 yang terdapat dalam sampel Stichopus sp. Dan elusidasi
struktur senyawa sapogenin yang telah diisolasi dari ekstrak teripang Stichopus
DAFTAR PUSTAKA
Anonim. (2008). Hasil Penelitian Tentang Jeli Gamat (Sea Cucumber Jelly).
http//www.luxor.com
Anonim. (2008). Keampuhan Ekstrak Teripang/Gamat.
Badan POM. (2004). Monograpi Ekstrak Tumbuhan Obat Indonesia. Volume 1. Jakarta: Badan POM. Hal. 25.
http//www.haisom.com
Creswell, C. J, Runguist, O.A, Campbell, M.M. (1982). Analisa Spektrum Senyawa Organik. Edisi II. Terjemahan oleh K. Padmawinata dan Soediro, I. Bandung : ITB. Hal. 25.
Depkes RI. (1979). Farmakope indonesia. Edisi III Jakarta: Departemen Kesehatan RI. Hal. 14, 748.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Cetakan pertama Jakarta. Depkes RI. Hal. 323-324.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Cetakan Pertama. Jakarta: Depkes RI. Hal. 10-11.
Fransworth, N.R. (1966). Biological and Phytochemical Screening Of Plants. Journal Of Pharmaceutical Sciences. Volume 55. no 3. Chicago: Reheis Chemical Company. Pages. 257-260.
Gritter, R.J., Bobitt, J.M, dan Schwarting. A.E. (1991). Pengantar Kromatografi. Terjemahan Padmawinata, K. Edisi II. Bandung : Penerbit ITB. Hal. 1, 6, 107- 109.
Harborne, J.B.(1987). Metode Fitokimia, penuntun cara moderen menganalisa tumbuhan. Penerjemah : K. padmawinata,. Edisi II. Bandung: ITB.Hal. 49, 69-71, 152, 156-158.
Hostettmann, K., Hostettmann, M., Marston, A., (1995). Cara Kromatografi
Preparatif: Penggunaan Pada Isolasi Senyawa Alam. Terjemahan
Padmawinata, K. Bandung: ITB. Hal. 9-12.
Martoyo, dkk. (2006). Budi Daya Teripang. Edisi Revisi. Jakarta: Penebar Swadaya. Hal. 8-17,156.
Silverstein, R. M, Bessler, G. C, dan Morrill, T. C. (1986). Penyidikan Spektrometrik Senyawa Organik. Alih bahasa Hartono, dkk. Jakarta : Erlangga. Hal. 3-5, 7-8, 95-97, 305-308.
Tarigan, P. (1980). Beberapa Aspek Kimia Sapogenin Steroid Pada Tumbuhan di Indonesia. Bandung : Penerbit Alumni. Hal. 18-62.
Lampiran 1
Lampiran 2
Lampiran 3
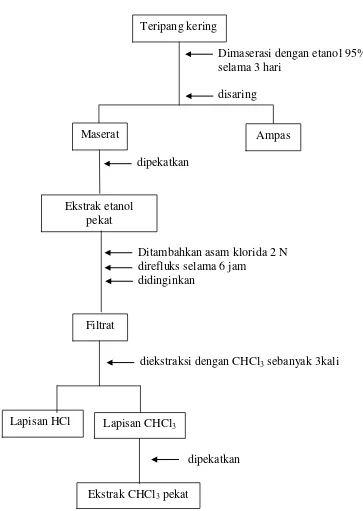
Dimaserasi dengan etanol 95% selama 3 hari
disaring
Ekstrak etanol pekat
Ditambahkan asam klorida 2 N direfluks selama 6 jam
didinginkan
Lapisan HCl
Teripang kering
Maserat Ampas
dipekatkan
Filtrat
diekstraksi dengan CHCl3 sebanyak 3kali
Lapisan CHCl3
dipekatkan
Ekstrak CHCl3 pekat Lampiran 4
Gambar 3. Bagan Ekstraksi Senyawa Sapogenin dari Hewan Teripang
Lampiran 5
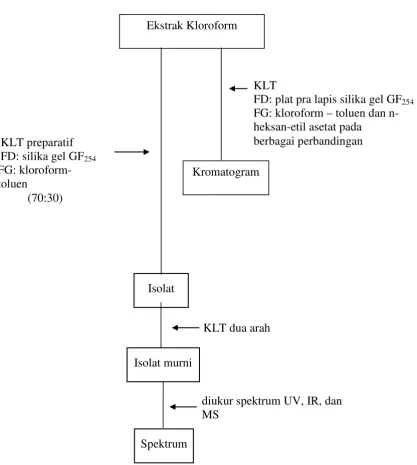
Gambar 4. Bagan Isolasi Senyawa Sapogenin dari Ekstrak Kloroform
Keterangan :
FD : fase diam , FG : fase gerak. KLT preparatif
FD: silika gel GF254
FG: kloroform-toluen
(70:30)
Ekstrak Kloroform
KLT
FD: plat pra lapis silika gel GF254
FG: kloroform – toluen dan n-heksan-etil asetat pada berbagai perbandingan
Kromatogram
Isolat
Isolat murni
diukur spektrum UV, IR, dan MS
Spektrum
Lampiran 6
(1) (2) (3) (4) (5)
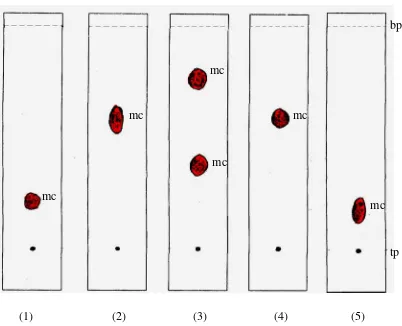
Gambar 5. Kromatogram KLT ekstrak etanol
Keterangan:
Fase diam: plat pra lapis silika gel GF254
fase gerak: (1) n-heksan – etil asetat (90:10), (2) n-heksan – etil asetat (80:20), (3) n-heksan etil asetat (70:30), (4) n-heksan – etil asetat (60:40), (5) n-heksan – etil asetat (50:50)
penampak bercak = Liebermann-Burchard (LB) bp = batas pengembang, tp = titik penotolan mc = merah coklat.
mc mc
mc mc
mc
mc
bp
Lampiran 7
(1) (2) (3) (4) (5) Gambar 6 : Kromatogram KLT ekstrak kloroform dengan fase gerak: n-heksan –
etil asetat.
Lampiran 8
(1) (2) (3) (4) (5)
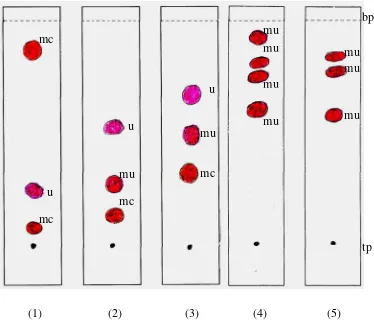
Gambnar 7. Kromatogram KLT ekstrak kloroform dengan fase gerak: klorform –
toluen (70:30).
Keterangan:
Fase diam: plat pra lapis silika gel GF254
fase gerak: (1) kloroform – toluen (90:10), (2) kloroform - toluen (80:20), (3) kloroform - toluen (70:30), (4) kloroform - toluen (60:40), (5) kloroform - toluen (50:50)
penampak bercak = Liebermann-Burchard (LB) bp = batas pengembang, tp = titik penotolan mc = merah coklat, mu = merah ungu, u = ungu.
Lampiran 9
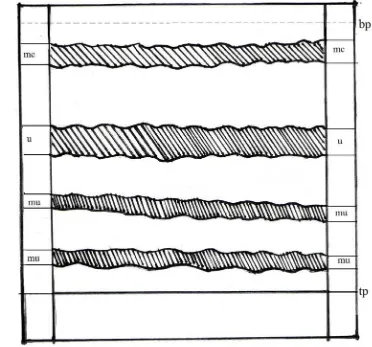
Gambar 8. Kromatogram ekstrak kloroform secara KLT preparatif
Keterangan:
Fase diam: plat kaca silika gel GF254 20X20 cm
Fase gerak: kloroform – toluen (70:30) penampak bercak Liebermann-Burchard (LB) tp = titik penotolan
bp = batas pengembangan
Lampiran 10
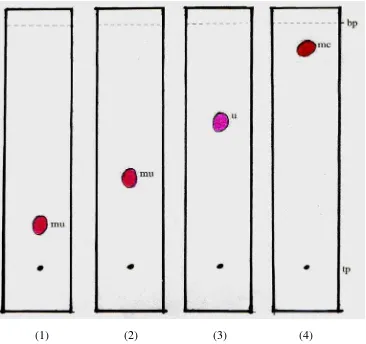
(1) (2) (3) (4) Gambar 9. Kromatogram KLT hasil isolat
Keterangan:
Fase diam: plat pra lapis silika gel GF254
fase gerak: kloroform – toluen (70:30)
Lampiran 11
Gambar 10 : Kromatogram KLT dua arah dari isolat
Keterangan:
Fase diam: plat pra lapis silika gel GF254.
fase gerak I: kloroform – toluen (70:30), fase gerak II: kloroform – metanol (30:70)
penampak bercak = Liebermann-Burchard (LB) u = ungu
Lampiran 12
Lampiran 13
Lampiran 14
Lampiran 15
Gambar 14. Spektrum massa pembanding