KARAKTERISASI KOMPONEN PEMBENTUK RASA
YANG TERDAPAT DALAM EKSTRAK LARUT AIR
TEMPE TERFERMENTASI LANJUT
RAHAYU UTAMI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Karakterisasi Komponen Pembentuk Rasa yang Terdapat dalam Ekstrak Larut Air Tempe Terfermentasi Lanjut adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Maret 2014 Rahayu Utami F251100201
RINGKASAN
RAHAYU UTAMI. Karakterisasi Komponen Pembentuk Rasa yang Terdapat dalam Ekstrak Larut Air Tempe Terfermentasi Lanjut. Dibimbing oleh CHRISTOFORA HANNY WIJAYA dan HANIFAH NURYANI LIOE.
Tempe merupakan produk fermentasi kedelai di Indonesia. Fermentasi tempe biasanya dilakukan selama 24-48 jam. Tempe dikatakan sebagai tempe terfermentasi lanjut setelah lewat 48 jam fermentasi. Tempe terfermentasi lanjut dikenal dengan sebutan tempe semangit dan tempe bosok. Tempe semangit merupakan tempe terfermentasi lanjut dengan lama fermentasi 48-72 jam setelah fermentasi tempe segar, sedangkan tempe bosok merupakan tempe terfermentasi lanjut dengan lama fermentasi lebih dari 72 jam setelah tempe diproduksi. Tempe terfermentasi lanjut mempunyai warna coklat, aroma tajam (pungent odor), dan tekstur yang lunak dibandingkan dengan tempe segar. Tempe terfermentasi lanjut dikenal oleh masyarakat Jawa dapat menyedapkan masakan karena memiliki rasa umami.
Tempe terfermentasi lanjut dibuat dengan beberapa lama fermentasi yaitu 0, 24, 48, 72 dan 96 jam setelah tempe segar. Tempe terfermentasi lanjut kemudian dibuat menjadi ekstrak larut air. Ekstrak larut air ini dianalisis total protein, total asam, total gula, nilai pH, komposisi total asam amino, asam amino bebas, profil HPLC dan analisis faktor dilusi rasa umami. Analisis statistik dengan uji ANOVA dilakukan untuk parameter total protein, total asam, total gula, dan nilai pH. Hasil analisis ANOVA menyatakan bahwa lama fermentasi tidak berbeda nyata terhadap total protein dan nilai pH, tetapi berbeda nyata terhadap total asam dan total gula.
Asam amino bebas dikarakterisasi berdasarkan rasa dan nilai aktivitas rasa. Berdasarkan nilai aktivitas rasa, rasa yang dominan dari ekstrak larut air adalah umami dan pahit. WSE dengan lama fermentasi 72 jam memiliki nilai aktivitas rasa umami lebih tinggi dibandingkan rasa pahit. Rasio rasa umami dan manis terhadap rasa pahit WSE berkisar antara 1.2-1.6. Nilai rasio rasa tersebut berkorelasi positif dengan nilai faktor dilusi rasa umami (r = 0.843 dan p = 0.002). Nilai faktor dilusi rasa umami merupakan hasil uji sensori larutan WSE yang memiliki konesntrasi 5 kali lebih pekat. Rasio tertinggi 1.6 dimiliki oleh WSE dengan lama fermentasi 72 jam yang memiliki faktor dilusi rasa umami tertinggi yaitu 256. Intensitas rasa umami dari tempe terfermentasi lanjut 72 jam ditentukan oleh keberadaan asam amino bebas dengan rasa umami dan pahit.
Secara umum profil HPLC menunjukkan komposisi komponen yang terdapat dalam fraksi WSE. Fraksi 2 dari setiap WSE tempe terfermentasi lanjut mengandung komponen hidrofilik lebih dominan dibandingkan komponen hidrofobik, sedangkan pada Fraksi 3 dari setiap WSE tempe terfermentasi lanjut komponen hidrofobik lebih dominan. Fraksi yang memiliki komponen hidrofilik lebih dominan memiliki intensitas rasa umami lebih tinggi.
SUMMARY
RAHAYU UTAMI. Taste Compounds in Water Soluble Extract of Over-fermented Tempe. Supervised by CHRISTOFORA HANNY WIJAYA and HANIFAH NURYANI LIOE.
Tempe is a fermented soybean food in Indonesia. Tempe was commonly produced about 24-48 hours fermentation. Tempe is referred as over-fermented tempe after the 48 hours fermentation has been completed. The over-fermented tempe known as tempe semangit and tempe bosok. Tempe semangit is over-fermented tempe (slightly overriped) which is obtained by lengthening the fermentation 48-72 hours longer than fresh tempe fermentation, whereas tempe bosok (overripe tempe) needs more than 72 hours of over-fermentation. Therefore, over-fermented tempe has a brown color, pungent odor, and soft textures compared to the white compact cake of fresh tempe. Over-fermented tempe is popular in Javanese culture as an umami seasoning in traditional foods.
Over-fermented tempe have been prepared by several different periods including : 0, 24, 48, 72 and 96 hours after the tempe production. Over-fermented tempe was extracted to obtain water soluble extracts (WSEs). The water soluble extracts (WSEs) were analyzed for crude proteins, total acids, total sugars, pH value, total amino acids, free amino acids, HPLC profile, taste activity value and umami taste dilution factors. Analysis of variance (ANOVA) was performed on crude protein, total acids, total sugars and pH value. As shown by ANOVA, crude protein and pH value were not statistically different between the fermentation periods, but were statistically different on total acids and total sugars.
Free amino acids were characterized for their tasting and taste activity values. Based on the taste activity value, the taste of WSEs was umami and bitter. WSE from sample with 72 hours over-fermentation had umami taste activity value higher than bitter taste activity. The ratios of umami and sweet taste activity value to bitter taste activity were found between 1.2-1.6 in the mentioned WSE. There was a positive correlation between the taste rasio and umami taste dilution factor (r = 0.843 dan p = 0.002). The umami taste dilution factor was the result of sensory analysis of 5 times concentrated WSE. The highest ratio 1.6 belongs to WSE with 72 hours over-fermentation which had the highest dilution factor 256. Umami taste intensity WSE with 72 hours fermentation was determined with the existence of umami and bitter tasting free amino acids.
In general HPLC profile indicated the composition in WSE’s fractions. Fraction 2 of each WSE of over-fermented tempe dominantly consisted of hydrophilic components, in contrast Fraction 3 of each WSE of over-fermented tempe was dominated by hydrophobic components. Fraction dominantly consisted of hydrophilic components having a higher intensity of umami taste.
© Hak Cipta Milik IPB, Tahun 2014
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Ilmu Pangan
KARAKTERISASI KOMPONEN PEMBENTUK RASA
YANG TERDAPAT DALAM EKSTRAK LARUT AIR
TEMPE TERFERMENTASI LANJUT
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2014
Judul Tesis : Karakterisasi Komponen Pembentuk Rasa yang Terdapat dalam Ekstrak Larut Air Tempe Terfermentasi Lanjut
Nama : Rahayu Utami
NIM : F251100201
Disetujui oleh Komisi Pembimbing
Prof Dr Ir C Hanny Wijaya MAgr Ketua
Dr Ir Hanifah Nuryani Lioe MSi Anggota
Diketahui oleh
Ketua Program Studi Ilmu Pangan
Prof Dr Ir Ratih Dewanti-Hariyadi MSc
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah MScAgr
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Agustus 2012 sampai Juli 2013 ini adalah tempe terfermentasi lanjut, dengan judul Karakterisasi Komponen Pembentuk Rasa yang Terdapat dalam Ekstrak Larut Air Tempe Terfermentasi Lanjut.
Terima kasih penulis ucapkan kepada Ibu Prof Dr Ir C Hanny Wijaya MAgr dan Ibu Dr Ir Hanifah Nuryani Lioe MSi selaku pembimbing atas kepercayaan, ilmu, dan bimbingan yang diberikan, serta Prof Dr Ir Made Astawan MS selaku penguji luar komisi yang telah banyak memberikan saran yang konstruktif. Di samping itu, ucapan terimakasih penulis sampaikan kepada Prof Yasuyuki Hashidoko beserta seluruh staf dan teman di Laboratorium Ecological Chemistry Faculty of Agriculture Hokkaido University Jepang, Dirjen Pendidikan Tinggi Kementrian Pendidikan Nasional Republik Indonesia yang telah memberikan dana penelitian melalui program Hibah Kompetensi tahun 2012, seluruh civitas akademika Universitas Sahid Jakarta khususnya Jurusan Teknologi Pangan Fakultas Teknologi Industri Pertanian, seluruh staf pengajar Program Studi Ilmu pangan, dan laboran Laboratorium Departemen ITP IPB.
Ungkapan terimakasih penulis sampaikan kepada bapak, ibu, adik, serta seluruh keluarga atas doa, motivasi, dan kasih sayangnya. Penulis juga mengucapkan terimakasih kepada keluarga besar IPN 2010 khususnya Iza Ayu Saufani, rekan sebimbingan khususnya Irdha Mirdhayati dan Bernadetha Ratna Eka Sari, teman-teman Megakost, sahabat dan rekan-rekan lainnya yang tidak dapat disebutkan satu per satu, yang telah memberikan inspirasi, semangat, motivasi, doa, dan kebersamaan kepada penulis selama kuliah dan penelitian.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL xiv
DAFTAR GAMBAR xiv
DAFTAR LAMPIRAN xv
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan dan Manfaat Penelitian 3
TINJAUAN PUSTAKA 3
Tempe 3
Tempe Terfermentasi Lanjut 4
Perubahan Selama Fermentasi Tempe 5
Senyawa Flavor pada Tempe 6
Karakterisasi Senyawa Rasa 9
Profil Senyawa Rasa Umami 10
METODE 13
Waktu dan Tempat 13
Bahan 13
Alat 13
Prosedur Penelitian 14
Pembuatan tempe terfermentasi lanjut 14
Pembuatan ekstrak larut air 14
Fraksinasi dengan kromatografi filtrasi gel 14
Karakterisasi kimia ekstrak larut air tempe terfermentasi lanjut 15 Karakterisasi sensori ekstrak larut air tempe terfermentasi lanjut 19
HASIL DAN PEMBAHASAN 21
Tempe Terfermentasi Lanjut 21
Ekstrak Larut Air (WSE) 22
Karakterisasi Kimia Ekstrak larut Air 23
Fraksinasi dengan kromatografi gel Sephadex G-25 medium 30
Karakterisasi Sensori 31
Profil HPLC Fraksi Hasil Fraksinasi WSE 33
SIMPULAN DAN SARAN 38
DAFTAR PUSTAKA 38
LAMPIRAN 44
DAFTAR TABEL
1 Hasil sensori dan komponen volatil tempe dengan lama fermentasi 2,5
dan 8 hari 7
2 Senyawa uji yang digunakan untuk uji rasa dasar pada seleksi panelis 19 3 Senyawa uji yang digunakan untuk uji segitiga rasa pada seleksi panelis 20 4 Berat tempe terfermentasi lanjut, berat ekstrak larut air (WSE) dan
rendemen tempe terfermentasi lanjut 22
5 Hasil analisis total protein WSE tempe terfermentasi lanjut yang
dihasilkan dari 600 g tempe segar 23
6 Hasil analisis total asam WSE tempe terfermentasi lanjut yang
dihasilkan dari 600 g tempe segar 24
7 Hasil analisis nilai pH WSE tempe terfermentasi lanjut yang dihasilkan
dari 600 g tempe segar 24
8 Hasil analisis total gula WSE tempe terfermentasi lanjut yang dihasilkan
dari 600 g tempe segar 25
9 Komposisi total asam amino WSE tempe terfermentasi lanjut 26 10 Komposisi asam amino bebas WSE tempe terfermentasi lanjut 27 11 Komposisi residu asam amino WSE tempe terfermentasi lanjut 27
12 Nilai ambang batas asam amino bebas 29
13 Rasio aktivitas rasa asam amino bebas rasa umami-manis terhadap rasa pahit yang terkandung dalam WSE dari tempe terfermentasi lanjut
dengan lama fermentasi yang berbeda 30
14 Nilai faktor dilusi rasa umami dari WSE tempe terfermentasi lanjut dan fraksinya dari hasil fraksinasi dengan kolom Sephadex G-25 medium
(2.0 × 90.0 cm) 32
DAFTAR GAMBAR
1 Profil HPLC ekstrak larut air keju yang dibuat dari susu : sapi (cow),
biri-biri (ewe) dan kambing (goat) 11
2 Profil HPLC dari kecap koikuchi dan hasil analisis dilusi rasanya 12
3 Tempe terfermentasi lanjut 21
4 Komposisi asam amino bebas ekstrak larut air dari tempe terfermentasi
lanjut menurut karakteristik rasa 28
5 Komposisi asam amino bebas ekstrak larut air dari tempe terfermentasi
lanjut menurut nilai aktivitas rasa 29
6 Hasil fraksinasi WSE menggunakan kromatografi gel kolom Sephadex
G-25 medium 31
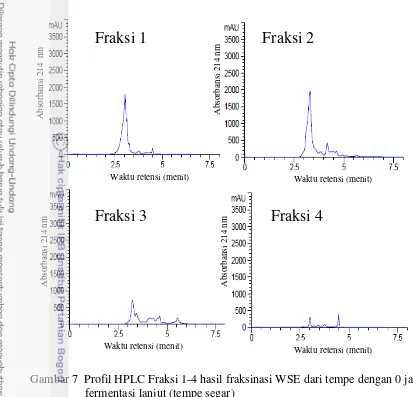
7 Profil HPLC hasil fraksinasi WSE dari tempe dengan 0 jam fermentasi
lanjut (tempe segar) 34
8 Profil HPLC hasil fraksinasi WSE dari tempe dengan 96 jam fermentasi
lanjut 35
9 Profil HPLC Fraksi 2 dari WSE tempe terfermentasi lanjut (0-96 jam)
untuk melihat fraksi hidrofilik hasil fraksinasi Sephadex G-25 36 10 Profil HPLC Fraksi 3 WSE tempe terfermentasi lanjut (0-96 jam) untuk
DAFTAR LAMPIRAN
1 Nilai aktivitas rasa dari asam amino bebas yang terdapat dalam WSE
tempe terfermentasi lanjut yang dihasilkan dari 600 gram tempe segar 44
2 Kuisioner pre-screening 45
3 Form seleksi panelis (uji rasa sederhana) 48
4 Form seleksi panelis (uji segitiga) 49
5 Form pelatihan panelis (uji segitiga) 50
6 Form analisis dilusi rasa 51
7 Hasil analisis sidik ragam (Anova) RAL satu faktor 52
8 Kromatogram larutan standar total asam amino 55
9 Kromatogram total asam amino sampel WSE dari tempe dengan 0 jam
fermentasi lanjut 56
10 Kromatogram profil HPLC hasil fraksinasi sampel WSE dari tempe
dengan 0 jam fermentasi lanjut 57
11 Kromatogram profil HPLC hasil fraksinasi sampel WSE dari tempe
dengan 96 jam fermentasi lanjut 58
12 Kromatogram profil HPLC Fraksi 2 dari WSE tempe terfermentasi lanjut (0-96 jam)
13 Kromatogram profil HPLC Fraksi 3 dari WSE tempe terfermentasi lanjut (0-96 jam)
1
PENDAHULUAN
Latar Belakang
Tempe kedelai atau sering hanya disebut “tempe” saja merupakan salah satu produk fermentasi kedelai tradisional Indonesia yang memiliki flavor khas. Tempe kedelai sudah menjadi menu sehari-hari yang sangat populer bagi masyarakat Indonesia, selain karena rasanya yang enak juga kandungan gizinya yang tidak kalah dengan produk olahan daging (Astuti et al. 2000). Di Indonesia, tempe juga dapat dibuat dari bahan selain kedelai, misalnya tempe gembus dibuat melalui fermentasi pada substrat residu tofu, tempe bongkrek dibuat dari kelapa, dan tempe benguk dibuat dari kacang koro benguk (Winarno 1985). Proses fermentasi selama pembuatan tempe menghasilkan komponen pembentuk flavor tempe yang khas, baik komponen flavor yang berkontribusi terhadap rasa maupun aroma. Selama fermentasi tempe, mikroba berperan penting dalam menghasilkan mutu organoleptik tempe karena mikroba (kapang) dapat menghidrolisis protein menjadi asam amino bebas dan peptida secara enzimatik (Handoyo dan Morita 2006). Banyak penelitian yang menyatakan bahwa asam amino bebas dan peptida memiliki peranan penting sebagai senyawa pembentuk rasa, khususnya rasa umami, pada produk fermentasi. Rasa umami merupakan rasa dasar kelima yang identik dengan rasa MSG (monosodium glutamate). Rasa umami yang dihasilkan pada produk fermentasi lebih kuat daripada produk yang belum mengalami fermentasi. Fermentasi lanjut yang dilakukan pada produk-produk olahan kedelai biasanya bertujuan untuk meningkatkan rasa umaminya, contohnya pada makanan tradisional Jepang seperti miso dan kecap kedelai. Rasa umami pada produk tersebut disebabkan adanya pelepasan asam amino glutamat dari protein selama fermentasi.
Pemanfaatan tempe di Indonesia tidak hanya dalam bentuk segar saja melainkan dalam bentuk tempe terfermentasi lanjut. Masyarakat Jawa, khususnya Jawa Tengah, Yogyakarta dan Jawa Timur mengenal tempe terfermentasi lanjut
ini dengan sebutan “tempe semangit” dan “tempe bosok”. Tempe semangit adalah tempe segar yang mengalami fermentasi berlanjut pada tahap awal, dengan waktu fermentasi satu sampai dua hari sejak tempe segar. Sedangkan tempe bosok diperoleh jika tempe semangit mengalami fermentasi berlanjut dengan waktu fermentasi tiga sampai empat hari sejak tempe segar (Santosa 1996). Fermentasi lanjut ini bertujuan untuk meningkatkan rasa umaminya.
2
2006); kecap Jepang (Lioe et al. 2007); dan doenjang, pasta kedelai Korea (Rhyu dan Kim 2011).
Peningkatan total asam amino bebas dalam tempe terjadi seiring dengan bertambahnya waktu fermentasi (Handoyo dan Morita 2006). Dalam penelitian tersebut juga terungkap jumlah asam amino bebas meningkat 3 sampai 10 kali dibandingkan dengan kontrol (tempe tanpa fermentasi). Dalam hal ini kapang R. oligosporus menghidrolisis protein kedelai menjadi asam amino dan peptida pendek. Lebih lanjut Handoyo dan Morita (2006) menyebutkan bahwa asam amino bebas paling banyak terbentuk pada tempe yang dibuat dengan lama fermentasi 24 sampai 72 jam. Asam amino glutamat bebas memiliki jumlah tertinggi kedua setelah asam amino lisin pada tempe yang difermentasi selama 72 jam sebesar 147.0 mg/100g kedelai. Asam amino glutamat beserta dipeptida yang mengandung asam amino glutamat pada ujung N terminal telah diketahui memiliki rasa umami.
Seperti yang sudah diuraikan sebelumnya bahwa tempe terfermentasi lanjut memiliki citarasa yang khas dan dapat digunakan sebagai penyedap masakan, namun karakteristik komponen pembentuk rasa tempe terfermentasi lanjut tersebut belum diketahui. Penelitian yang telah dilakukan berkaitan dengan tempe terfermentasi lanjut adalah penelitian pembuatan tepung tempe bosok (Yudianto 1997), penelitian yang mengungkapkan komponen volatil flavor tempe dengan lama fermentasi 2, 5 dan 8 hari dengan menggunakan metode distilasi uap-ekstraksi cair-cair simultan (Syahrial dan Muchalal 2001), serta konsentrasi asam amino bebas selama 0, 24, 48 dan 72 jam fermentasi (Handoyo dan Morita 2006).
Karakterisasi komponen pembentuk rasa pada tempe terfermentasi lanjut ini perlu diteliti di sini, sehingga dapat diketahui komponen-komponen apa saja yang berperan penting membentuk rasa tempe terfermentasi lanjut. Dengan demikian hasil penelitian ini dapat digunakan sebagai bahan referensi pemanfaatan flavor, terutama flavor umami yang berasal dari komoditas lokal. Adapun pengujian yang dilakukan dalam penelitian ini meliputi pengujian kimia termasuk komposisi asam amino dan pengujian sensori. Analisis komposisi asam amino dilakukan menggunakan HPLC untuk menentukan total asam amino dan asam amino bebas. Pengujian sensori dilakukan dengan analisis dilusi rasa (taste dilution analysis). Analisis dilusi rasa telah banyak dilakukan untuk menentukan faktor dilusi dari komponen rasa pahit (Frank et al. 2001) dan umami (Kim dan Lee 2003).
Perumusan Masalah
3 oleh indera pencecap sebagai rasa umami dibandingkan peptida. Untuk mengetahui senyawa yang berhubungan dengan rasa umami tempe terfermentasi lanjut, maka kandungan peptida dan asam amino tempe tersebut harus diketahui kemudian dikaitkan dengan hasil uji sensorinya. Untuk mendapatkan peptida dan asam amino bebas dilakukan ekstraksi dari tempe terfermentasi menjadi ekstrak larut air (water soluble extract). Kemudian ekstrak larut air tempe terfermentasi lanjut difraksinasi menggunakan kolom Sephadex G-25 medium.
Rasa yang terbentuk pada produk fermentasi selain tergantung pada komposisi asam amino dan peptida, juga terbentuk karena ada interaksi antar asam amino dan peptida yang mempunyai rasa berbeda. Komponen asam amino dan peptida dapat terdeteksi oleh indera pencecap bila terdapat dalam bentuk larut air. Oleh karena itu analisis komponen pembentuk rasa tempe terfermentasi lanjut dilakukan pada bentuk ekstrak larut airnya (WSE). Penelitian ini selain meneliti komponen asam amino pembentuk rasa tempe terfermentasi lanjut juga mempelajari tentang hubungan antara komponen asam amino dan karakteristik rasa pada tempe fermentasi lanjut yang dibuat dalam bentuk ekstrak larut air (water soluble extract, WSE).
Tujuan dan Manfaat Penelitian
Penelitian ini bertujuan untuk melakukan karakterisasi kimia dan sensori ekstrak larut air (WSE) dari tempe terfermentasi lanjut, serta mengevaluasi keberadaan komponen penyumbang rasa umami. Penelitian ini dapat digunakan sebagai bahan referensi pemanfaatan flavor umami dari komoditas lokal yang sebelumnya dikenal memiliki kemampuan fungsional.
2
TINJAUAN PUSTAKA
Tempe
Tempe merupakan produk berwarna putih dengan tekstur kompak, terbuat dari kedelai kupas yang direbus melalui proses fermentasi menggunakan kapang Rhizopus sp (Codex 2013). Warna putih disebabkan adanya miselia kapang yang tumbuh pada permukaan biji kedelai. Tekstur kompak juga disebabkan oleh miselia kapang yang menghubungkan biji-biji kedelai tersebut.
Tempe di Indonesia dibuat dengan menginokulasikan kedelai dengan kapang Rhizopus sp, terutama R. oligosporus, R. oryzae, R. arrhizus, dan R. stolonifer. Produsen tempe di Indonesia tidak menggunakan kultur murni R. oligosporus, tetapi mereka menggunakan campuran dari kultur Rhizopus sp. Selain itu, tidak ada standar proses dalam pembuatan tempe, sehingga terdapat banyak variasi dalam pembuatan tempe di beberapa daerah dan produsen tempe (Astuti 2000). Pembuatan tempe terdiri dari beberapa tahap, yaitu perendaman, perebusan, inokulasi dengan mikroba, dan inkubasi pada suhu ruang.
4
ditemukan pada Serat Centhini jilid 3 dan dipertegas lagi dalam Serat Centhini jilid 12 bahwa tempe dibuat dari kedelai (Sapuan 1996). Tempe tidak hanya dibuat di Indonesia saja. Penyebaran tempe di luar negeri pada awalnya dimulai di benua Eropa. Tempe di Eropa pertama kali diperkenalkan di Belanda pada tahun 1895 oleh Prinseen Gerling, seorang ahli mikrobiologi yang mempelajari ilmu tentang tempe kepada imigran Indonesia. Tempe diperkenalkan oleh Yap Bwee Hwa di Amerika pada tahun 1958 (Mulyadi 2010). Sejak tahun 1946 tempe mulai populer di Belanda dan pada tahun 1984 tercatat 18 perusahaan tempe di Eropa, dan di Amerika terjadi peningkatan jumlah perusahaan tempe dari 13 perusahaan di tahun 1975 menjadi 53 perusahaan pada tahun 1984 (Karyadi 1996). Masih menurut Karyadi 1996, selain di Eropa dan Amerika tempe juga terkenal di Jepang. Kiku Murata yang merintis dan mempopulerkan tempe di Jepang yang kemudian menjadi Guru Besar di Universitas Osaka. Kiku Murata merupakan salah satu pendiri Japanese Society of Tempe yang bertujuan antara lain mempopulerkan tempe di Jepang serta meneliti lebih lanjut keunggulan tempe sebagai makanan sehat. Pada tahun 1984 tercatat 8 perusahaan besar di Jepang memproduksi tempe secara komersial.
Tempe berhasil disahkan sebagai new work item di CAC pada sidang 34th session of Codex Alimentarius Commission (CAC) di Jenewa 9 Juli 2011 lalu, (Republika Online 2011). Indonesia menjadi koordinator pembuatan standar tempe di Codex Alimentarius Commission dan saat ini draft standar tersebut sudah memasuki tahap 5 dalam sidang Codex Tahun 2013.
Penelitian tentang tempe juga sudah banyak dilakukan oleh peneliti luar negeri antara lain Baumann dan Bisping (1995) meneliti tentang aktifitas proteolitis selama fermentasi tempe. Heskamp dan Barz (1998) meneliti tentang ekspresi enzim protease oleh Rhizopus sp selama fermentasi tempe kedelai. Handoyo dan Morita (2006) meneliti tentang struktur dan sifat fungsional tempe dengan Rhizopus oligosporus. Feng et al. (2007) meneliti tentang komponen volatil oleh Rhizopus oligosporus selama fermentasi tempe kedelai dan barley.
Tempe Terfermentasi Lanjut
Menurut Shurtleff dan Aoyagi (1980) fermentasi tempe dibedakan menjadi beberapa fase, yaitu : tempe koro/underripe (dihasilkan kurang lebih 4-6 jam sebelum menjadi tempe), tempe/mature (dihasilkan setelah inkubasi selama 24-48 jam), tempe semangit/slightly overripe adalah tempe yang dihasilkan 2-3 hari setelah menjadi tempe, dan tempe bosok/overripe (dihasilkan kurang lebih 3-5 hari setelah menjadi tempe). Sudarmadji 1977 membedakan fermentasi tempe menjadi tiga fase, yaitu :
a. Fase pertumbuhan cepat (0-30 jam fermentasi) yaitu fase dimana terjadi kenaikan jumlah asam lemak bebas, penaikan suhu, pertumbuhan kapang yang cepat dengan terbentuknya miselia kapang pada permukaan biji kedelai.
5 c. Fase pembusukan atau fermentasi lanjut (50-90 jam fermentasi) yaitu fase dimana terjadi kenaikan jumlah bakteri dan jumlah asam lemak bebas, pertumbuhan kapang menurun dan pada kadar air tertentu pertumbuhan kapang terhenti. Perubahan flavor karena degradasi protein sehingga terbentuk amonia. Tempe terfermentasi lanjut berperan penting dalam meningkatkan citarasa dari masakan tradisional Jawa, dimana tempe tersebut dapat memberikan rasa dan aroma khas dalam masakan (Gunawan-Putri et al. 2012). Tempe terfermentasi lanjut dikenal oleh masyarakat dengan nama tempe semangit dan tempe bosok. Tempe terfermentasi lanjut telah lama dikenal oleh masyarakat Jawa. Hal ini dibuktikan dengan catatan pada serat Centhini jilid II, yang menyebutkan asem sambel lethokan yang dibuat dari bahan dasar tempe yang telah mengalami fermentasi lanjut. Sampai saat inipun sambel lethok atau disebut pula sambel tumpang masih sering ditemui dalam menu masakan masyarakat Jawa (Astuti 1994). Sambel tumpang dibuat dari tempe semangit, santan, bumbu (bawang putih, bawang merah, cabe merah besar, cabe rawit, kencur, kemiri, gula dan garam), daun salam, lengkuas, daun jeruk. Sambel tumpang disajikan dengan nasi yang diatasnya diberi aneka sayuran yang telah direbus terlebih dahulu lalu disiram dengan sambal tumpang dan diberi peyek sebagai pelengkap, bisa peyek kacang atau peyek teri. Sambel tumpang dapat juga disajikan dengan bubur nasi.
Yudianto 1997, melakukan survey tentang peran tempe terfermentasi lanjut, hasilnya 70% responden menyatakan bahwa tempe tersebut mempunyai efek menyedapkan bila dicampur di dalam masakan. Hal ini karena adanya hidrolisis enzimatik yang terjadi selama proses fermentasi, sehingga terbentuk senyawa asam amino dan peptida yang dapat berkontribusi terhadap karakteristik rasa (Je et al. 2005). Beberapa produk fermentasi garam yang berasal dari kedelai seperti doenjang (Korea), douchiba (Cina), dan miso (Jepang) menghasilkan peptida yang dapat digunakan sebagai peningkat rasa (taste enhancer). Asam amino bebas dan fraksi peptida dengan berat molekul rendah pada Douchiba (makanan fermentasi dari Cina) terbentuk selama proses pematangan fermentasi, proses tersebut menyebabkan terbentuknya rasa umami sebagai interaksi antar komponen rasa (Qin dan Ding 2007).
Perubahan Selama Fermentasi Tempe
Fermentasi dapat terjadi karena adanya aktivitas mikroba penyebab fermentasi pada substrat organik yang sesuai. Terjadinya fermentasi ini dapat menyebabkan perubahan sifat pangan, sebagai akibat pemecahan kandungan-kandungan bahan pangan tersebut. Hasil-hasil fermentasi tersebut terutama tergantung kepada jenis bahan pangan (substrat), macam mikroba dan kondisi lingkungan yang mempengaruhi pertumbuhan dan metabolisme mikroba (Winarno 1980).
6
beberapa vitamin seperti riboflavin, vitamin B12 dan provitamin A (Winarno 1980).
Perubahan kimia protein kedelai terjadi selama proses fermentasi tempe. Enzim proteolitik menyebabkan degradasi protein kedelai menjadi asam amino, sehingga nitrogen terlarut meningkat dari 0.5 menjadi 2.5%. Degradasi protein ini juga menyebabkan peningkatan pH. Nilai pH tempe yang baik berkisar antara 6.3-6.5 (Hidayat et al. 2006).
Fudiyansyah et al. (1995) menjelaskan bahwa selama proses fermentasi ini, kedelai akan mengalami perubahan fisik dan kimia menjadi tempe. Komponen karbohidrat, lemak dan protein yang terdapat pada kedelai akan dipecah menjadi monosakarida, asam lemak dan peptida atau asam amino.
Aktivitas protease terdeteksi setelah fermentasi 12 jam ketika pertumbuhan hifa kapang masih relatif sedikit. Hasil hidrolisis protein yang digunakan oleh kapang sebagai sumber karbon hanya 5%, sisanya terakumulasi dalam bentuk peptida dan asam amino (Hidayat et al. 2006).
Selain asam amino dan peptida, kapang Rhizopus mampu mentransformasi senyawa isoflavon glikosida menjadi isoflavon aglikon selama fermentasi tempe (Purwoko et al. 2001). Tempe dan miso mengandung isoflavon aglikon tertinggi dibandingkan derivat fermentasi kedelai lainnya dikarenakan kapang Rhizopus dan Aspergillus dapat mengubah isoflavon glikosida menjadi aglikon lebih kuat daripada mikroba lainnya (Coward et al. 1993). Isoflavon aglikon diketahui memiliki aktivitas antioksidatif. Mekanisme antioksidatif isoflavon aglikon adalah memangsa radikal bebas oleh gugus fenolat. Senyawa isoflavon glikosida tersebut yaitu genistin, daidzin dan glycitin, sedangkan gugus aglikonnya masing-masing disebut genistein, daidzein dan glycitein (Friedman dan Brandon 2001). Pada tempe selain senyawa glikosida dan gugus aglikon tersebut juga terdapat antioksidan faktor II (6,7,4 trihidroksi isoflavon) yang mempunyai sifat antioksidan paling kuat dibandingkan isoflavon dalam kedelai (Astawan 2009). Dengan demikian, tempe juga bermanfaat sebagai antioksidan karena memiliki senyawa yang memiliki aktivitas antioksidatif.
Asam lemak tidak jenuh ganda (polyunsaturated fatty acids) meningkat selama proses fermentasi tempe terutama asam oleat dan linolenat (Astawan 2009). Peningkatan kandungan asam lemak bebas pada tempe menunjukkan bahwa selama fermentasi terdapat hidrolisis ikatan ester asam lemak yang dikatalisis oleh enzim lipase. Enzim lipase memulai aktivitasnya di awal fermentasi yang ditandai dengan meningkatnya asam lemak bebas yang terdeteksi setelah 12 jam fermentasi. Monogliserida sebagai hasil perombakan lipase mencapai 80% pada akhir fermentasi tempe (Deliani 2008).
Senyawa Flavor pada Tempe
Senyawa Volatil
7 selama proses pertumbuhan biji kedelai (Boue et al. 2003). Kedelai mempunyai rasa langu karena adanya enzim lipoksigenase yang mengkatalisis oksidasi lemak kedelai menjadi senyawa volatil seperti heksanal dan heksanol, tetapi dengan fermentasi kedelai menjadi tempe oleh R.oligosporus terbentuk aroma jamur yang diinginkan (Nout dan Rombouts 1990). Senyawa volatil 1-octen-ol dan 3-oktanon dihasilkan oleh kapang Penicillium spp, Aspergillus spp, dan Fusarium spp. Senyawa 1-octen-3-ol dihasilkan dari asam linoleat karena adanya enzim lipoksigenase dan hidroksiperoksida liase (Chitarra et al. 2004).
Aroma jamur ditemukan setelah proses fermentasi pada fermentasi tempe. Hal ini terjadi karena adanya penghilangan senyawa heksanol dan berkurangnya senyawa heksanal (komponen bau langu), adanya kedua komponen tersebut menutupi persepsi sensori dari 3-oktanon dan 1-okten-3-ol. Feng et al. (2007) mengindikasikan bahwa komponen bau langu dapat hilang selama proses fermentasi kapang. Senyawa volatil yang terdapat pada tempe antara lain asetaldehid, pentanon, etanol, aseton, metil propanal, etil asetat, butanon, 2-butanol, 2-metil-1-propanol, 3-metil-3-buten-1-ol, 2-metil-1-2-butanol, heksanal, formamit (Feng et al. 2007). Hasil sensori dan komponen volatil tempe dengan lama fermentasi 2, 5 dan 8 hari dapat dilihat pada Tabel 1.
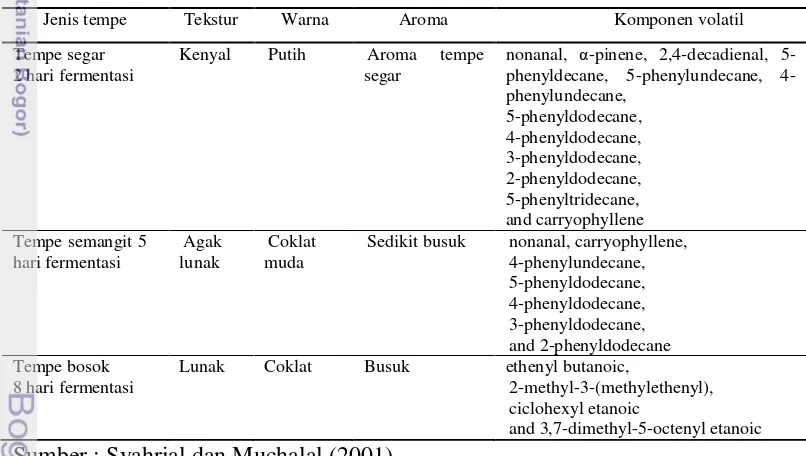
Tabel 1 Hasil sensori dan komponen volatil tempe dengan lama fermentasi 2, 5 dan 8 hari
Jenis tempe Tekstur Warna Aroma Komponen volatil
Tempe segar 2 hari fermentasi
Kenyal Putih Aroma tempe segar
nonanal, α-pinene, 2,4-decadienal, 5-phenyldecane, 5-phenylundecane,
4-Sedikit busuk nonanal, carryophyllene, 4-phenylundecane,
Lunak Coklat Busuk ethenyl butanoic,
2-methyl-3-(methylethenyl), ciclohexyl etanoic
and 3,7-dimethyl-5-octenyl etanoic Sumber : Syahrial dan Muchalal (2001)
8
Senyawa Non Volatil
Flavor rasa termasuk salah satu senyawa non volatil, karena senyawa pembentuk rasa merupakan senyawa larut air sehingga dapat masuk ke dalam saliva dan terdeteksi oleh indera pencecap. Umami adalah rasa dasar kelima setelah manis, pahit, asam dan asin. Rasa umami pertama kali diperkenalkan oleh Prof Kikunae Ikeda pada tahun 1908. Rasa umami adalah rasa gurih yang sedap diberikan oleh asam amino glutamat dan ribonukleotida termasuk inosinat dan guanilat, yang terdapat secara alami pada bahan pangan seperti daging, ikan, sayuran dan produk susu. Rasa umami sendiri sangat halus dan tercampur baik dengan rasa yang lain untuk meningkatkan dan membulatkan flavor, kebanyakan orang tidak dapat mengenali rasa umami ketika merasakannya tetapi rasa umami tersebut memiliki peran yang penting dalam membentuk rasa sedap makanan (Umami Information Center 2013).
Senyawa non volatil pada tempe terbentuk karena adanya hidrolisis protein menjadi peptida dan asam amino selama proses fermentasi. Pada umumnya, hidrolisis enzimatik pada protein memberikan rasa pahit. Tetapi beberapa peptida dapat menghasilkan rasa savory atau umami, seperti peptida yang diisolasi dan dikarakterisasi dari keju (Molina et al. 1999); Miso, pasta kedelai Jepang (Ogasawara et al. 2006); kecap Jepang (Lioe et al. 2007); dan Doenjang, pasta kedelai Korea (Rhyu dan Kim 2011).
Peptida merupakan suatu senyawa yang dihasilkan dengan adanya asam-asam amino yang saling berikatan secara kovalen melalui ikatan peptida (Bailey 1992). Ikatan peptida dibentuk dengan menarik unsur H2O dari gugus
karboksil suatu asam amino dan gugus α-amino dari molekul lain dengan reaksi kondensasi yang kuat (Lehninger 1997). Peptida adalah senyawa yang bersifat zwitterion, bersifat netral dan tidak bermuatan pada titik isoelektriknya. Berdasarkan konstanta keasamannya, peptida bersifat kurang zwitterion dibanding asam aminonya (Shallenberger 1992).
Asam amino glutamat dan dipeptida yang mengandung asam amino glutamat pada ujung N terminal memiliki rasa umami. Ambang batas dari dipeptida (1.5 sampai 3.0 mg mL-1) tersebut lebih tinggi dibandingkan monosodium glutamat (0.3 mg mL-1) (Kato et al. 1989). Hal ini berarti intensitas rasa umami dari peptida tersebut 5 sampai 10 kali lebih rendah dibandingkan MSG. Asam amino glutamat bebas dalam bentuk garam natrium (MSG) memiliki rasa umami (Lioe et al. 2005).
9 tersebut, BMP juga menunjukkan efek sinergistik terhadap garam (NaCl) dan MSG (Wang et al. 1996).
Maehashi et al. (1999) menyatakan bahwa peptida Glu-Glu dan Glu-Val memiliki rasa umami dengan intensitas yang rendah. Beberapa sintesis peptida diketahui memiliki rasa umami, tetapi intensitas rasa umami dari sebagian peptida tersebut lemah ketika diuji dengan penambahan 0.02 % IMP.
Karakterisasi Senyawa Rasa
Pemilihan metode pemisahan peptida disesuaikan dengan sifat kimia peptida, terutama berdasarkan kemampuannya mengion pada pH tertentu atau berdasarkan kepolarannya (Lehninger 1997). Peptida merupakan senyawa nitrogen yang mudah larut dalam air. Untuk mengisolasi peptida, pertama kali perlu dipisahkan dahulu dari protein yang mempunyai berat molekul relatif lebih tinggi dan atau asam amino yang mempunyai berat molekul relatif lebih rendah.
Berbagai metode pemisahan yang umum digunakan untuk mengisolasi dan mengidentifikasi peptida antara lain ultrafiltrasi, pengendapan dengan etanol, elektrodialisis dan kromatografi filtrasi gel.
Ultrafiltrasi
Ultrafiltrasi merupakan teknik pemisahan zat terlarut berdasarkan berat molekul dengan menggunakan membran semipermeabel dan tekanan. Komponen berberat molekul lebih besar dari cut off membran akan tertinggal sebagai retentat sedangkan molekul yang lebih kecil akan melewati membran dan terkumpul sebagai ultrafiltrat (Smith 1994).
Membran ultrafiltrasi terdapat dalam berbagai bentuk, yaitu tubular, spiral, lingkaran, multichannel monolith elements, hollow fibre, dan flat sheet. Setiap membran memiliki nilai cut off. Nilai ini hanya sebagai indikator yang akan menolak 90 % senyawa-senyawa pada ukuran cut off-nya. Nilai cut off dan ukuran pori membran akan menentukan laju alir yang akan dicapai membran. Faktor lain yang dapat mempengaruhi laju alir adalah permukaan membran, jenis larutan, kelarutan, konsentrasi pelarut dan penyebarannya, jenis membran, suhu dan tekanan.
Jenis membran yang digunakan dalam penelitian ini adalah low binding regenerated cellulose. Membran ini dapat dilalui baik oleh pelarut aqueous maupun larutan buffer. Membran ini juga dapat digunakan untuk memisahkan garam atau pelarut dalam larutan yang mengandung biomolekul, baik dengan metode desalting, buffer exchange, maupun diafiltrasi.
Kromatografi Filtrasi Gel
10
separasi/fraksinasi senyawa BM tinggi dan BM rendah, dan pemekatan (Adnan 1997; Sorensen et al. 1999).
Gel merupakan struktur jaringan tiga dimensi berpori yang terbentuk karena adanya ikatan silang yang terjadi selama proses polimerisasi. Gel tersebut secara selektif dapat mengekslusikan molekul-molekul yang besar dari pori-pori yang dimilikinya, tergantung dari banyaknya ikatan silang dalam struktur gel. Molekul yang lebih besar dari ukuran pori-pori gel akan mengalami ekslusi, sedangkan yang lebih kecil dari pori-pori gel akan masuk ke dalam struktur gel tersebut. Molekul besar akan terelusi terlebih dahulu (Adnan 1997).
Peptida dapat dipisahkan dengan kromatografi filtrasi gel menggunakan Sephadex G-25, G-15 dan G-10 (Hagel 1998). Kisaran fraksinasinya berturut-turut 1 000-5 000 Da, < 1 500 Da, dan < 700 Da. Sephadex merupakan butir gel yang dibuat dari polisakarida dekstran. Pada Sephadex terdapat ikatan silang antara dekstran dengan epiklorohidrin (Adnan 1997; Sorensen et al. 1999). Struktur matriks dekstran dengan ikatan silang epiklorohidrin memungkinkan terjadinya interaksi hidrofobik antara komponen aromatik peptida dengan jembatan eter dari ikatan silang tersebut, sehingga pemisahan peptida tidak hanya berdasarkan ukuran atau berat molekul, tetapi juga berdasarkan interaksi hidrofobik.
Ikatan silang dekstran-epiklorohidrin dengan jembatan eternya menentukan sifat gel Sephadex. Gel Sephadex bersifat tidak larut dalam air, tahan dalam alkali, asam lemak, serta zat-zat pengoksidasi dan pereduksi lemah. Tetapi jika diekspos dalam waktu yang lama, gel Sephadex akan pecah. Penggunaan pada suhu di atas 120 ºC juga harus dihindari (Adnan 1997).
Deteksi peptida umumnya dilakukan dengan spektrofotometer pada panjang gelombang sinar UV. Ikatan peptida terdeteksi pada panjang gelombang 214 nm. Peptida yang mengandung residu asam amino asidik terdeteksi pada panjang gelombang 205 nm dan peptida yang mengandung asam amino aromatik terdeteksi pada panjang gelombang 240 nm (Pavia et al. 1996)
Profil Senyawa Rasa Umami
Profil komponen rasa umami dapat dilihat menggunakan instrumen high performance liquid chromatography (HPLC). Analisis dengan HPLC merupakan analisis instrumental dengan prinsip kromatografi dan kolom non polar (misal C18 atau ODS). Teknik analisis ini banyak digunakan untuk menganalisis sampel yang dapat larut dalam pelarut polar dan bersifat non volatil.
Jenis sistem HPLC yang digunakan untuk analisis senyawa rasa adalah sistem kromatografi reversed-phase (RPC) yang dicirikan dengan penggunaan kolom nonpolar seperti kolom C18 sebagai fasa stasionernya dan fasa gerak yang digunakan adalah campuran antara pelarut organik yang hidrofilik dan air, misalnya campuran acetonitril-aquades. Sedangkan jenis elusi yang digunakan adalah elusi gradien, yaitu digunakan lebih dari satu fasa gerak selama proses pemisahan.
11 polar. Molekul non polar akan berinteraksi dengan fasa stasioner sehingga akan tertahan di kolom sedangkan molekul polar akan keluar dari kolom lebih dulu.
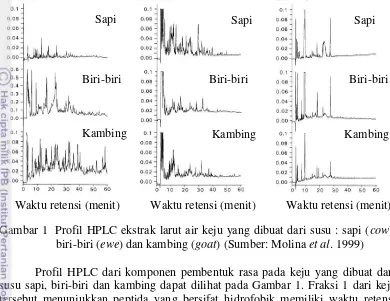
Gambar 1 Profil HPLC ekstrak larut air keju yang dibuat dari susu : sapi (cow), biri-biri (ewe) dan kambing (goat) (Sumber: Molina et al. 1999) Profil HPLC dari komponen pembentuk rasa pada keju yang dibuat dari susu sapi, biri-biri dan kambing dapat dilihat pada Gambar 1. Fraksi 1 dari keju tersebut menunjukkan peptida yang bersifat hidrofobik memiliki waktu retensi yang lebih lama dibandingkan peptida hidrofilik pada kolom reverse phase. Peptida hidrofobik ini muncul pada menit ke 16. Peptida hidrofobik tersebut memberikan rasa pahit pada keju. Pada Fraksi 2 peptida hidrofilik memiliki proporsi yang lebih tinggi dibandingkan dengan peptida hidrofobik. Fraksi 2 memiliki konsentrasi asam amino bebas tertinggi yaitu 178, 128, dan 98 mg mL-1 untuk keju yang dibuat dari susu sapi, biri-biri dan kambing. Sedangkan pada Fraksi 3 profil HPLC menunjukkan hasil yang sama dari ketiga keju tersebut. Penelitian ini menggunakan fase gerak 0.1% trifluoroacetic acid (TFA) dalam air bebas ion dan 0.1% TFA dalam asetonitril dan air bebas ion (60:40 v/v). Kolom yang digunakan adalah C18 Nucleosil 5.
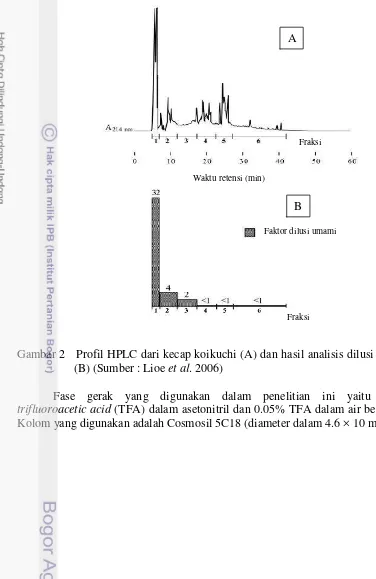
Profil HPLC peptida yang berkontribusi terhadap intensitas rasa umami pada kecap kedelai Jepang dapat dilihat pada Gambar 2. Profil HPLC menunjukkan Fraksi 1 memiliki peak tertinggi di antara Fraksi yang lain. Berdasarkan hasil penelitian tersebut Fraksi 1 mengandung hanya asam amino bebas yaitu asam glutamat, alanin, arginin, glisin, threonin dan serin. Selain itu Fraksi 1 juga mengandung garam. Adanya interaksi antara asam amino berasa umami (asam glutamat dengan keberadaan garam) dan asam amino berasa manis dapat meningkatkan intensitas rasa umami. Hal ini ditunjukkan oleh hasil dilusi rasa pada Fraksi 1 yang lebih tinggi dibandingkan Fraksi yang lain.
Sapi
Biri-biri
Kambing
Sapi Sapi
Biri-biri Biri-biri
Kambing Kambing
12
Gambar 2 Profil HPLC dari kecap koikuchi (A) dan hasil analisis dilusi rasanya (B) (Sumber : Lioe et al. 2006)
Fase gerak yang digunakan dalam penelitian ini yaitu 0.05% trifluoroacetic acid (TFA) dalam asetonitril dan 0.05% TFA dalam air bebas ion. Kolom yang digunakan adalah Cosmosil 5C18 (diameter dalam 4.6 × 10 mm).
A
B Fraksi
Waktu retensi (min)
Faktor dilusi umami
13
3
METODE
Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Agustus 2012 sampai dengan Juli 2013. Penelitian ini dilakukan di beberapa laboratorium yaitu, Laboratorium Terpadu FKH-IPB untuk pembuatan ekstrak larut air, Laboratorium Biokimia ITP-IPB untuk melakukan proses kering beku dengan freeze dryer, Laboratorium Kimia Pangan PAU-IPB dan Kimia Pangan ITP untuk fraksinasi ekstrak larut air dan analisis kimia, Laboratorium Kimia Terpadu-IPB untuk analisis total asam amino, Laboratorium swasta Saraswanti untuk analisis asam amino bebas dan Laboratorium Sensori PAU-IPB untuk analisis sensori.
Bahan
Bahan yang digunakan dalam penelitian ini terdiri dari bahan utama, bahan pembantu dan bahan kimia. Bahan utama yang digunakan adalah tempe segar diperoleh dari industri tempe FreSoia Co di Bekasi Jawa Barat, dan bahan pembantu yang digunakan adalah air bebas ion untuk keperluan persiapan sampel.
Bahan kimia yang digunakan adalah Sephadex G-25 medium (Amersham Pharmacia Biotech AB, Swedia), kolom C18 (15 cm, Zorbak Eclipse XDB-C18, Agilent, USA), asetonitril, kalium sulfat, merkuri oksida, asam sulfat, natrium oksida, asam klorida, natrium tiosulfat, asam borat, alkohol, kalsium karbonat, natrium oksalat, indikator PP, larutan standar glukosa, pereaksi Anthrone, larutan buffer 4.0 dan 7.0, air bebas ion, OPA (orthophtalaldehyde), buffer kalium borat, dan gas nitrogen. Bahan kimia yang digunakan pada analisis HPLC memiliki kualitas HPLC grade (Asetonitril, Merck Co, Germany, CV. Media Labs Bogor), sedangkan bahan kimia selain untuk analisis HPLC memiliki kualitas analisis grade.
Alat
14
Prosedur Penelitian Pembuatan Tempe Terfermentasi Lanjut
Tempe terfermentasi lanjut dibuat dengan memperpanjang masa fermentasi tempe segar. Lama fermentasi lanjut dilakukan selama 0, 24, 48, 72 dan 96 jam. Untuk melanjutkan proses fermentasi, tempe ditaruh di atas rak plastik pada suhu ruang (30 sampai 35 ºC) dan kelembaban 75%. Tempe yang masih terbungkus daun dengan ukuran 600 g dipotong menjadi 2 bagian sebelum dilakukan pemeraman. Hal ini dimaksudkan agar terjadi aliran udara di dalam tempe selama pemeraman, karena jika tertutup rapat maka tempe akan cepat menjadi busuk. Hal ini berhubungan dengan proses respirasi mikroba yang menghasilkan uap air.
Pembuatan Ekstrak Larut Air
Tempe fermentasi lanjut (TFL) kemudian dibuat menjadi ekstrak larut air, sebelum dilakukan karakterisasi. TFL dihomogenkan dengan 2 400 mL air destilat (1:4). Kemudian sampel yang sudah homogen dipanaskan pada suhu 100 °C selama 10 menit dan dibiarkan sampai dingin selama 50 menit sambil diaduk. Campuran sampel kemudian disentrifus pada 4 000 rpm dengan suhu 4 °C selama 30 menit. Hasil supernatan disaring dengan kain saring nilon 80 dan 150 mesh dan dikering-bekukan, selanjutnya disimpan pada suhu minus 20 °C.
Fraksinasi dengan Kromatografi Filtrasi Gel
Fraksinasi dengan kromatografi filtrasi gel dilakukan untuk memisahkan komponen yang terdapat dalam sampel WSE. Komponen tersebut akan terpisah menjadi fraksi-fraksi berdasarkan berat molekul dan interaksi hidrofobik antara sampel dan gel Sephadex G-25. Tahapan fraksinasi yang dilakukan yaitu :
Ultrafiltrasi
Ultrafiltrasi dilakukan dengan tujuan untuk mendapatkan fraksi berberat molekul kurang dari 3 000 Da. Sampel 10 gram ekstrak larut air dilarutkan dengan 50 mL air bebas ion, distirer 60 menit dan disentrifuse pada 8 000 rpm dengan suhu 4 °C selama 30 menit. Supernatan disaring dengan kertas saring. Supernatan diultrafiltrasi menggunakan tabung ultra centrifugal filters pada 4 500 g dengan suhu 4˚C selama 40 menit. Hasil ultrafiltrasi kemudian difraksinasi menggunakan kromatografi filtrasi gel.
Fraksinasi Sephadex G-25
15 silang epiklorohidrin dan dekstran (Scopes 1982). Fase gerak yang digunakan adalah air destilat dengan kecepatan alir 4.25 mL/menit pada suhu ruang. Sebanyak 35 aliquot masing-masing 7.5 mL ditampung dengan tabung reaksi. Eluat yang terdapat dalam masing-masing tabung diukur absorbansinya dengan spektrofotometer pada panjang gelombang 240 nm. Selanjutnya eluat dalam tabung dari peak-peak yang muncul dikumpulkan menjadi fraksi-fraksi. Fraksinasi dilakukan sebanyak 5 kali, sehingga total larutan yang difraksinasi 25 mL. Fraksi yang sama dari 5 kali fraksinasi dikumpulkan. Masing-masing kumpulan fraksi selanjutnya dikeringbekukan. Hasil kering beku dari masing-masing kumpulan fraksi dilarutkan dengan air bebas ion dan ditera sampai 5 mL. Kemudian dipindahkan ke dalam 3 eppendorf (kapasitas 2 mL) dan disimpan dalam freezer untuk analisis sensori.
Karakterisasi Kimia Ekstrak Larut Air Tempe Terfermentasi Lanjut
Karakterisasi kimia dilakukan terhadap ekstrak larut air (WSE) tempe terfermentasi lanjut dan hasil fraksinasi WSE dengan Sephadex G-25. Analisis kimia untuk WSE tempe terfermantasi lanjut meliputi total protein, total asam, total gula, nilai pH, komposisi total asam amino, dan komposisi asam amino bebas. Profil HPLC dilakukan untuk Fraksi hasil fraksinasi WSE dengan Sephadex G-25.
Total Protein (AOAC 1995)
16
Total Asam, Metode Titrasi (AOAC 1995)
Analisis ini bertujuan untuk mengetahui jumlah total asam yang terdapat di dalam setiap sampel WSE.
Sampel sebanyak 1 gram diencerkan dalam labu takar 100 mL. Sampel distirer selama 30 menit, kemudian disaring dengan kertas saring. Sebanyak 25 mL larutan sampel diambil ke dalam erlenmeyer dan ditambahkan 3 tetes indikator fenoftalin. Sampel dititrasi dengan 0.1 N NaOH sampai terbentuk warna merah muda yang tetap.
Total asam tertitrasi =
Total Gula, Metode Anthrone (Pomeranz 2000)
Analisis total gula dilakukan untuk ekstrak larut air tempe yang sudah dikering bekukan. Analisis ini bertujuan untuk mengetahui jumlah gula yang terdapat di dalam setiap sampel WSE.
1) Persiapan sampel
Sampel sebanyak 0.5 gram dimasukkan ke dalam gelas piala 300 mL, lalu ditambahkan 3 × 20 mL alkohol 80 % dan 1 gram CaCO3 (menghindari hidrolisis asam). Sampel dididihkan selama 30 menit (menghindari hidrolisis enzim), kemudian didinginkan. ditambahkan dengan 1.5 - 2.5 mL larutan Pb asetat jenuh sampai larutah menjadi jernih. Sampel dipindahkan ke dalam labu takar 250 mL dan Volume larutan sampel ditepatkan sampai tanda tera dengan air destilata, lalu dikocok dan disaring dengan kertas saring. Sebanyak 30 mL filtrat sampel diambil ke dalam gelas piala lain dan ditambahkan 1.5 gram Na-oksalat kering untuk mengendapkan Pb. Sampel disaring kembali dan diambil filtratnya sebanyak 5 mL untuk analisis total gula.
2) Penetapan total gula dengan metode Anthrone a) Pembuatan kurva standar
Larutan glukosa standar (0.2 mg mL-1), masing-masing sebanyak 0.0;0.2;0.4;0.6;0.8 dan 1.0 mL dimasukkan ke dalam tabung reaksi. Setelah masing-masing ditepatkan menjadi 1.0 mL dengan air destilata, larutan segera ditambah 5 mL pereaksi Anthrone. Tabung reaksi ditutup dan ditempatkan
pada penangas 100 ˚C selama 12 menit. Setelah didinginkan, absorbansi ditambahkan 5 mL pereaksi Anthrone. Tabung reaksi ditutup dan ditempatkan
17 mengalir, absorbansi larutan dibaca pada panjang gelombang 630 nm. Nilai absorbansi dimasukkan ke dalam kurva standar untuk mengetahui konsentrasi gula.
Perhitungan :
Total gula (100) = × 100 % Keterangan :
G = konsentrasi glukosa pada sampel yang diperoleh dari kurva standar FP = faktor pengenceran = 5000
W = berat contoh (gram) Nilai pH
Sebelum digunakan, pH meter dikalibrasi terlebih dahulu dengan menggunakan larutan buffer pH 4.0 dan pH 7.0. Sampel sebanyak 1 gram diencerkan dalam labu takar 100 mL. Sampel distirer selama 30 menit, kemudian disaring dengan kertas saring. Kemudian elektroda pada pH meter dicelupkan ke dalam sampel, sehingga dapat terbaca nilai pH yang diukur. Selesai pengukuran elektroda diangkat dan dibilas dengan aquades.
Komposisi Total Asam Amino (AOAC 2005)
Komposisi asam amino merupakan analisis jumlah total untuk masing-masing asam amino, baik dalam bentuk dipeptida maupun asam amino bebas. Analisis komposisi asam amino dilakukan sesuai dengan prosedur yang dikembangkan oleh Laboratorium Kimia Terpadu, IPB, Bogor. Sampel fraksi kering beku ditimbang sebanyak 1-5 mg, kemudian dilakukan hidrolisis asam dengan memakai 1 mL HCL 6 N dalam wadah tertutup berisi gas nitrogen dan menggunakan autoklaf pada suhu 110 °C di bawah tekanan 4 sampai 5 psi selama 24 jam. Hasil hidrolisis kemudian dikeringbekukan dengan freeze dryer. Dengan cara ini asam amino triptofan rusak, sehingga tidak dapat diukur.
Asam amino diderivatisasi dengan pereaksi OPA, sebelum dianalisis dengan kolom HPLC. Sampel kemudian dihidrolisis dengan melarutkan dalam 5 mL HCl 0.01 N dan ditambahkan buffer kalium borat pH 10.4 dengan perbandingan 1:1. Sebanyak 10 µL campuran ini ditambahkan 25 µL pereaksi OPA, kemudian dibiarkan selama 1 menit agar proses derivatisasi sempurna. Dengan cara ini derivat asam amino prolin tidak terdeteksi, karena berumur pendek. Kemudian sampel siap diinjeksikan ke dalam kolom HPLC.
18
Perhitungan dilakukan dengan rumus :
µmol AA Total = x jumlah standar (µmol)
% AA Total =
Komposisi Asam Amino Bebas
Komposisi asam amino bebas merupakan analisis jumlah total untuk masing-masing asam amino dalam bentuk asam amino bebas. Sampel fraksi kering beku ditimbang sebanyak 1-5 mg, kemudian diderivatisasi dengan pereaksi OPA, sebelum dianalisis dengan kolom HPLC. Sampel kemudian ditambahkan buffer kalium borat pH 10.4 dengan perbandingan 1:1. Sebanyak 10 µL campuran ini ditambahkan 25 µL pereaksi OPA, kemudian dibiarkan selama 1 menit agar proses derivatisasi sempurna. Dengan cara ini derivat asam amino prolin tidak terdeteksi, karena berumur pendek. Kemudian sampel siap diinjeksikan ke dalam kolom HPLC.
Konsentrasi asam amino dalam sampel dihitung dari kromatogram dan dinyatakan dahulu dalam satuan µmol asam amino (µmol AA), kemudian dihitung persentase asam amino (berat/berat kering sampel).
Perhitungan dilakukan dengan rumus :
µmol AA Bebas = x jumlah standar (µmol)
% AA Bebas =
Profil HPLC Fraksi Hasil Fraksinasi WSE
Penentuan profil kromatogram fraksi menggunakan HPLC dilakukan secara gradien menggunakan kondisi sebagai berikut :
Kolom : Zorbax C18 (15 cmx 4,6 cm i.d., 5 µm)
Fase gerak : Solven A adalah asetonitril (99.9%) dan solven B adalah air bebas ion (100%) yang sudah disaring dengan membran nilon 0.45 µm
Waktu elusi : 20 menit
Gradien : Gradien 0 - 20 menit dari solven A konsentrasi 10% (90% solven B) menjadi solven A konsentrasi 20% (80% solven B)
Laju alir : 0.4 mL/menit Suhu : suhu kamar Sampel loop : 20 µ L
19 Karakterisasi Sensori Ekstrak Larut Air Tempe Terfermentasi Lanjut
Analisis sensori deskriptif adalah metode analisis sensori dimana atribut sensori suatu produk atau bahan pangan diidentifikasi, dideskripsikan, dan dikuantifikasi dengan menggunakan panelis yang dilatih khusus untuk tujuan ini. Analisis ini dapat dilakukan untuk semua parameter sensori dan beberapa aspek dalam flavor atau texture profiling. Panelis yang digunakan harus dipilih secara hati-hati, dilatih dan dipertahankan kemampuannya di bawah pengawasan supervisor yang berpengalaman (Apriyantono dan Wijaya, 2006).
Karakterisasi sensori pada penelitian ini dilakukan dengan metode analisis dilusi rasa (taste dilution analysis). Analisis dilusi rasa ini bertujuan untuk menentukan tingkat intensitas dari rasa umami sampel. Pengujian dengan analisis dilusi rasa ini menggunakan panelis terlatih, karena panelis harus dapat mendeteksi rasa umami dengan konsentrasi kecil di dalam sampel. Untuk mendapatkan panelis terlatih dilakukan beberapa tahapan pelaksanaan yaitu seleksi panelis (skrining panelis), pelatihan panelis dan pengujian sampel.
Seleksi Panelis
Tahapan awal seleksi panelis yaitu rekruitmen panelis. Sebanyak 30 orang mahasiswa dan laboran dari Dept ITP diminta kesediaannya mengikuti seleksi calon panelis. Panelis diminta mengisi form kuesioner pre-screening yang berisi tentang kebiasaan makan, kesukaan dan ketidaksukaan ekstrim terhadap jenis makanan tertentu karena alasan kesehatan atau alergi, ketersediaan waktu dan minat mereka dalam uji sensori. Panelis juga diberikan form pernyataan bersedia menjadi panelis terlatih. Kemudian dilakukan wawancara untuk mengetahui kecocokan data dengan informasi yang disampaikan oleh calon panelis. Calon panelis yang terseleksi dan bersedia dilatih menjadi panelis terlatih, kemudian diuji kepekaan dan kekonsistenan indera pencicipnya dengan menggunakan uji rasa dasar dan uji segitiga.
Uji rasa dasar menggunakan uji deskriptif. Panelis diminta mencicip dan menuliskan rasa larutan sampel. Uji rasa dasar ini bertujuan untuk mengetahui kemampuan panelis dalam mengenali dan membedakan rasa dasar. Senyawa uji yang diberikan untuk seleksi panelis dapat dilihat pada Tabel 2. Uji rasa dasar ini dilakukan selama 3 sesi pengujian. Melalui hasil pengujian, calon panelis dinyatakan lolos apabila mampu memberikan 100 % jawaban benar untuk uji rasa dasar (Meilgaard et al.1999).
Tabel 2 Senyawa uji yang digunakan untuk uji rasa dasar pada seleksi panelis
Deskripsi rasa Senyawa uji rasa Konsentrasi (% b/v)
Manis Larutan gula pasir 1.00
Asam Larutan asam sitrat 0.05
Asin Larutan garam 0.20
Pahit Larutan kafein 0.05
Gurih Larutan MSG 0.05
20
Panelis yang lolos tahap seleksi awal, kemudian diseleksi dengan uji segitiga. Uji segitiga bertujuan untuk mengetahui kemampuan panelis dalam membedakan rasa yang memiliki perbedaan konsentrasi. Setiap panelis melakukan 15 set pengujian dibagi menjadi 3 sesi pengujian dilakukan untuk uji segitiga tersebut. Senyawa yang digunakan dalam uji segitiga dapat dilihat pada Tabel 3.
Tabel 3 Senyawa uji yang digunakan untuk uji segitiga rasa pada seleksi panelis
Deskripsi rasa Senyawa uji Konsentrasi (% b/v)
Manis Larutan gula pasir 2.00
5.00
Asam Larutan asam sitrat 0.05
0.08
Asin Larutan garam 0.20
0.40
Pahit Larutan kafein 0.05
0.07
Gurih Larutan MSG 0.05
0.07 Sumber : Silamba 2011
Pelatihan Panelis
Panelis yang sudah dinyatakan lolos dari tahap seleksi, kemudian melakukan pelatihan panelis menjadi panelis terlatih. Tahap pelatihan panelis bertujuan untuk melatih kepekaan dan konsistensi penilaian panelis sehingga panelis dapat dikatakan panelis terlatih.
Untuk pelatihan panelis, panelis dilatih menggunakan sampel standar yaitu : larutan garam (0.05%) untuk rasa asin, larutan MSG (0.02%) untuk rasa umami, larutan gula pasir (0.07%) untuk rasa manis, larutan asam sitrat (0.03%) untuk rasa asam dan larutan kafein (0.07%) untuk rasa pahit. Pelatihan panelis ini dilakukan sebanyak 3 sesi untuk setiap larutan standar. Sampel disajikan dengan metode uji segitiga, dimana dua sampel yang lain air bebas ion. Panelis harus dapat membedakan larutan standar tersebut dengan air bebas ion. Pada uji segitiga ini panelis tidak boleh melakukan pengulangan pencicipan.
Pengujian Sampel
21
4
HASIL DAN PEMBAHASAN
Tempe Terfermentasi Lanjut
Proses fermentasi lanjut dilakukan untuk mendapatkan tempe semangit dan tempe bosok. Selama pembuatan tempe, tempe dikemas dengan daun pisang, hal ini karena daun pisang dapat menjaga aerasi udara yang lebih merata di permukaan tempe dibandingkan dengan plastik (Santosa 1996). Masih menurut Santosa 1996, tempe yang dikemas dengan daun pisang memiliki aktifitas proteolitik yang lebih tinggi daripada tempe yang dikemas dengan plastik. Aktifitas proteolitik ini disebabkan oleh enzim proteolitik yang dihasilkan oleh mikroba dalam tempe, terutama kapang. Aktifitas proteolitik mendegradasi protein menjadi protein yang lebih sederhana dan bersifat lebih larut air, serta menghasilkan asam amino bebas dan amoniak.
Gambar 3 Tempe terfermentasi lanjut
22
pada proses fermentasi tempe dan menentukan keamanan produk tempe yang dihasilkan (Nout dan Rombouts 1990).
Ekstrak Larut Air (WSE)
Komponen senyawa rasa merupakan komponen yang larut air yang bersifat non volatil (tidak mudah menguap). Untuk mendapat komponen larut air, tempe terfermentasi lanjut dibuat menjadi ekstrak larut air (WSE). Beberapa penelitian menyatakan ekstrak larut air mengandung komponen senyawa aktif rasa yang dapat berkontribusi terhadap rasa produk seperti keju (Andersen 2010) dan doenjang (Kim dan Lee 2003).
Pembuatan ekstrak larut air ini dilakukan dengan cara ekstraksi. Pelarut yang digunakan adalah air bebas ion. Penggunaan pelarut air bebas ion dimaksudkan untuk memungkinkan sampel diuji sensori oleh panelis, selain itu dengan air bebas
C memisahkan komponen larut air dengan komponen tidak larut air. Dalam hal ini komponen tidak larut air terdiri dari lemak pada bagian atas dan padatan pada bagian bawah. Komponen larut air terdapat di antara lemak dan padatan. Rendemen ekstrak larut air dari tempe terfermentasi lanjut dapat dilihat pada Tabel 4.
Tabel 4 Berat tempe terfermentasi lanjut, berat ekstrak larut air (WSE) dan rendemen tempe terfermentasi lanjut
Rendemen dihitung dari rasio berat WSE (bk) terhadap berat tempe segar, kemudian dikalikan 100%
Berdasarkan hasil tersebut terlihat bahwa lebih dari 90 % tempe terfermentasi lanjut terdiri dari padatan yang tidak larut air. Hal ini ditunjukkan oleh hasil rendemen yang berkisar 2.3-4.2%. Selain itu, sampel dengan lama fermentasi 0 jam memiliki jumlah ekstrak larut air yang lebih sedikit dibandingkan sampel yang lain, karena pada sampel 0 jam fermentasi lanjut lebih banyak mengandung komponen berberat molekul besar seperti protein yang lebih sukar larut air daripada hasil hidrolisisnya, seperti yang terjadi pada fermentasi lanjut 24 sampai 96 jam. Hasil analisis sidik ragam (ANOVA) menyatakan lama
23 lanjut. WSE yang diperoleh selanjutnya dilarutkan menjadi volume yang sama yaitu 50 mL, kemudian larutan WSE ini digunakan pada penelitian lebih lanjut yang hasilnya dijelaskan di bawah ini.
Karakterisasi Kimia Ekstrak Larut Air
Total Protein
Ekstrak larut air (WSE) tempe terfermentasi lanjut memiliki total protein 34.94-53.43 g 100 g-1. WSE dengan lama fermentasi lanjut 0 jam memiliki total protein terendah dan WSE 96 jam memiliki total protein tertinggi. Hasil analisis total protein menunjukkan adanya peningkatan total protein WSE selama fermentasi lanjut (Tabel 5). Analisis total protein menggunakan metode Kjeldahl yang hasilnya merupakan total protein kasar karena dihitung berdasarkan jumlah nitrogen dalam sampel.
Tabel 5 Hasil analisis total protein WSE tempe terfermentasi lanjut yang dihasilkan dari 600 g tempe segar
Fermentasi lanjut
Adanya peningkatan total protein selama fermentasi lanjut menunjukkan semakin banyak jumlah protein atau komponen bernitrogen (nitrogenous compounds) yang larut air. Selama proses fermentasi tempe, kapang Rhizopus oligosporus menghasilkan protease yang dapat menghidrolisis protein kedelai menjadi asam amino dan peptida rantai pendek yang mudah larut dalam air (Handoyo dan Morita 2006). Hidrolisis oleh protease ini masih berlanjut selama proses fermentasi lanjut, dilihat dengan adanya peningkatan kandungan komponen bernitrogen larut air seperti asam amino (Santosa, 1996). Dengan demikian aktivitas proteolitik masih terjadi selama tahap fermentasi lanjut. Hasil analisis
sidik ragam (ANOVA) menyatakan lama fermentasi tidak berbeda nyata (α=0.05)
terhadap total protein WSE fermentasi lanjut.
Total Asam dan Nilai pH
24
sedangkan lama fermentasi 96 jam memiliki total asam terendah. Total asam WSE menurun dengan meningkatnya waktu fermentasi (Tabel 6). Hasil analisis sidik ragam (ANOVA) menyatakan lama fermentasi berbeda nyata (α=0.05) terhadap total asam WSE fermentasi lanjut.
Tabel 6 Hasil analisis total asam WSE tempe terfermentasi lanjut yang dihasilkan dari 600 g tempe segar
Penurunan total asam WSE berhubungan dengan peningkatan nilai pH selama terjadinya fermentasi lanjut (Tabel 7). Nilai pH WSE meningkat dari 5.4 (fermentasi lanjut 0 jam) menjadi 6.1 (fermentasi lanjut 96 jam).
Tabel 7 Hasil analisis nilai pH WSE tempe terfermentasi lanjut yang dihasilkan
25 Total Gula
Total gula WSE juga mengalami penurunan selama fermentasi lanjut (Tabel 8). Penurunan karbohidrat pada tempe disebabkan oleh pemecahan senyawa polisakarida menjadi molekul gula sederhana karena aktivitas enzim selama fermentasi (Nout dan Kiers 2005).
Tabel 8 Hasil analisis total gula WSE tempe terfermentasi lanjut yang dihasilkan dari 600 g tempe segar
Beberapa enzim tersebut antara lain poligalakturonase, endoselulase, xilanase dan arabinase (Sarrette et al. 1992). Pemecahan senyawa polisakarida ini sudah mulai terjadi saat perendaman biji kedelai sebelum fermentasi tempe dan saat fermentasi tempe kapang Rhizopus menggunakan gula - gula sederhana seperti sukrosa, rafinosa, dan stakiosa sebagai sumber karbon dan energi (Prinyawiwatkul et al. 1995). Sebagai sumber energi, karbohidrat dan protein diperlukan oleh mikroba untuk menghasilkan ATP (adenosin trifosfat) (Rahayu dan Nurwitri 2012). Penggunaan gula sederhana oleh Rhizopus menyebabkan penurunan total gula pada WSE. Hasil analisis sidik ragam (ANOVA) menyatakan lama fermentasi berbeda nyata (α=0.05) terhadap total gula WSE fermentasi lanjut.
Komposisi Asam Amino
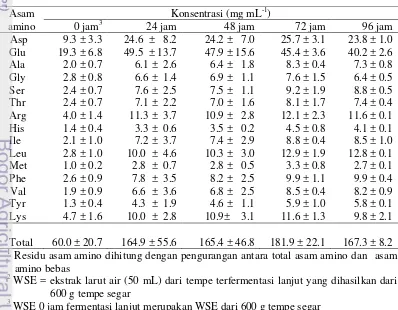
Asam amino dan peptida merupakan hasil dari proses hidrolisis protein oleh protease dari kapang selama fermentasi tempe atau protease dari bakteri selama fermentasi tempe lanjut. Pada saat fermentasi tempe kapang Rhizopus sp menghasilkan enzim protease dan peptidase. Enzim protease kapang Rhizopus sp merupakan protease asam. Hal ini dapat dilihat dari komposisi total asam amino WSE (Tabel 9). Total asam amino basa WSE yaitu histidin, arginin dan lisin terdapat dalam jumlah 14-31 mg mL-1, lebih kecil daripada total asam amino asam WSE yaitu asam aspartat dan asam glutamat antara 29-79 mg mL-1. Hal ini karena bahan baku kedelai memiliki asam aspartat dan asam glutamat dalam jumlah yang lebih tinggi.
26
dibandingkan dengan tempe segar (tempe biasa), karena mengandung asam glutamat bebas dalam konsentrasi relatif tinggi.
Tabel 9 Komposisi total asam amino WSE1 tempe terfermentasi lanjut
1
WSE = ekstrak larut air (50 mL) dari tempe terfermentasi lanjut yang dihasilkan dari 600 g tempe segar
2
WSE 0 jam fermentasi lanjut merupakan WSE dari 600 g tempe segar
Total asam amino lisin pada WSE meningkat selama fementasi lanjut. Lisin merupakan asam amino esensial yang sangat berguna bagi tubuh. Semakin banyak asam amino lisin dalam suatu produk pangan semakin banyak terjadinya biosintesis karnitin. Lisin adalah prekursor untuk biosintesis karnitin, sedangkan
karnitin merangsang proses β-oksidasi dari asam lemak rantai panjang yang terjadi di mitokondria sehingga mengakibatkan kadar lemak dan kolesterol rendah (Susandari et al 2004).
27
Tabel 10 Komposisi asam amino bebas WSE1 tempe terfermentasi lanjut
1
WSE = ekstrak larut air (50 mL) dari tempe terfermentasi lanjut yang dihasilkan dari 600 g tempe segar
2
WSE 0 jam fermentasi lanjut merupakan WSE dari 600 g tempe segar
Tabel 11 Komposisi residu1 asam amino WSE2 tempe terfermentasi lanjut
1
Residu asam amino dihitung dengan pengurangan antara total asam amino dan asam amino bebas
2
WSE = ekstrak larut air (50 mL) dari tempe terfermentasi lanjut yang dihasilkan dari 600 g tempe segar
3
WSE 0 jam fermentasi lanjut merupakan WSE dari 600 g tempe segar