di
Lembaga Farmasi Angkatan Udara (LAFIAU)
Lanud Husein Sastranegara
Bandung
Disusun oleh:
Disusun Oleh :
VIVI HARYATI, S. Farm 073202104
PROGRAM PENDIDIKAN PROFESI APOTEKER
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
FARMASI INDUSTRI
Di
Lembaga Farmasi Angkatan Udara (Lafiau)
Kompleks Lanud Husein Sastranegara
Bandung
3 - 28 Maret 2008
Laporan ini disusun untuk memenuhi salah satu syarat memperoleh
gelar Apoteker pada Fakultas Farmasi Universitas Sumatera Utara
Medan
Disusun Oleh :
Vivi Haryati, S. Farm 073202104
Lembaga Farmasi Angkatan Udara Lanud Husein Sastranegara
Bandung Pembimbing,
Drs. Akmal, M.Si., Apt.
Mayor Kes NRP 527570
Mengetahui,
Kepala Lembaga Farmasi TNI Angkatan Udara Fakultas Farmasi Roostyan Effendie Universitas Sumatera Utara
Puji syukur ke hadirat Allah SWT atas berkat dan rahmat-Nya kepada kita sehingga kegiatan dan penyusunan laporan Praktek Kerja Lapangan di Lembaga Farmasi TNI Angkatan Udara Bandung dapat berjalan dengan baik dan lancar.
Penulis menyadari bahwa pelaksanaan Praktek Kerja Lapangan sampai penyusunan laporan ini dapat terlaksana dengan lancar berkat kerjasama, bantuan, pengarahan dan dukungan dari berbagai pihak, baik secara langsung maupun tidak langsung. Oleh karena itu, pada kesempatan ini penulis ingin menyampaikan terima kasih kepada:
1. Prof. Dr. Sumadio Hadisahputra. Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara Medan.
2. Drs. Wiryanto, M.S., Apt sebagai Koordinator Program Pendidikan Profesi Apoteker Fakultas Farmasi Universitas Sumatera Utara Medan.
3. Kolonel Kes Drs. Purwanto Budi T., M.M selaku Kepala Lembaga Farmasi Angkatan Udara Lanud Husein Sastranegara Bandung yang telah memberikan kesempatan kepada kami untuk melakukan Praktek Kerja Profesi Apoteker. 4. Mayor Kes Drs. Akmal, M.Si., Apt., serta Kapten Kes Siswandi, S.Si., Apt.,
selaku pembimbing dari Lembaga Farmasi Angkatan Udara Lanud Husein Sastranegara Bandung.
(Adi, Nowo), Semua pihak yang tidak dapat kami sebutkan satu per satu atas bantuan dan dukungan yang diberikan, baik secara langsung maupun tidak langsung.
Penulis menyadari bahwa Laporan PKL ini masih jauh dari sempurna. Oleh karena itu penulis sangat mengharapkan adanya kritik dan saran yang membangun dari semua pihak. Dengan segala kerendahan hati, semoga laporan PKL ini dapat bermanfaat bagi Almamater dan mahasiswa seprofesi serta sejawat.
Bandung, Maret 2008
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... v
DAFTAR LAMPIRAN ...ix
DAFTAR GAMBAR...x
RINGKASAN ...xi
BAB I. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan Praktek Kerja ... 3
BAB II. TINJAUAN UMUM INDUSTRI FARMASI ... 4
2.1 Pengertian Industri Farmasi ... 4
2.2 Cara pembuatan Obat yang Baik (CPOB) ... 4
2.2.1 Ketentuan Umum ... 5
2.2.2 Personalia ... 6
2.2.3 Bangunan ... 8
2.2.4 Peralatan ... 10
2.2.5 Sanitasi dan Higiene ... 11
2.2.6 Produksi ... 12
2.2.7 Pengawasan Mutu ... 15
2.2.10 Dokumentasi ... 18
2.3 Validasi ... 18
BAB III. TINJAUAN UMUM LEMBAGA FARMASI TNI AU ... 20
3.1 Sejarah dan Perkembangan ... 20
3.2 Kedudukan, Tugas dan Kewajiban LAFIAU ... 23
3.3 Moto, Visi, dan Misi LAFIAU ... 23
3.4 Struktur Organisasi LAFIAU ... 24
3.4.1 Kepala Bagian Farmasi TNI AU (KALAFIAU) ... 26
3.4.2 Sekretaris LAFIAU (Sesla) ... 26
3.4.3 Bagian Produksi ... 27
3.4.4 Bagian Gudang Pusat Farmasi (Gupusfi) ... 27
3.4.5 Bagian Pengujian dan Pengembangan ... 29
3.4.6 Bagian Penunjangan ... 30
3.5 Sarana dan Fasilitas Produksi ... 30
3.5.1. Bangunan ... 30
3.5.2. Ruang dan Peralatan Produksi ... 31
3.6 Kegiatan Lafiau ... 32
3.6.1 Pengelolaan Perbekalan Kesehatan... 32
3.6.2 Bagian Gudang Pusat Farmasi ... 34
3.6.3.4 Pengemasan ... 50
3.6.4 Bagian Pengujian dan Pengembangan ... 50
3.6.5 Bagian Penunjangan... 52
3.6.5.1 Kepala Unit Penunjang Material ... 52
3.6.5.2 Kepala Unit Pemeliharaan Fasilitas Material ... 53
3.6.6 Pengelolaan Limbah ... 53
3.6.6.1 Pengolahan Limbah Padat ... 53
3.6.6.2 Pengolahan Limbah Cair... 54
BAB IV. KEGIATAN PRAKTEK KERJA PROFESI DI LAFIAU... 57
4.1 Bagian Pengujian dan Pengembangan (Ujibang) ... 57
4.1.1. Pengenalan Bagian Pengujian dan Pengembangan... 57
4.2 Bagian Gudang Pusat Farmasi (GUPUSFI) ... 58
4.3 Bagian Produksi... 58
4.3.1 Produksi Beta Laktam ... 58
4.3.2 Produksi Non Beta Laktam ... 59
BAB V. PEMBAHASAN ... 63
5.1 Personalia ... 64
5.2 Bangunan ... 65
5.3 Peralatan... 68
5.4 Sanitasi dan Higiene ... 68
5.8 Penanganan Keluhan Terhadap Obat, Penarikan Kembali Obat dan Obat
dikembalikan... 71
5.9. Dokumentasi ... 72
BAB VI. KESIMPULAN DAN SARAN ... 73
6.1. Kesimpulan ... 73
6.2. Saran ... 73
Halaman
Lampiran 1. Contoh Berita Acara Penerimaan ... 75
Lampiran 2. Contoh Kartu Stok Barang ... 76
Lampiran 3. Prosedur Tetap Pengujian ... 77
Lampiran 4. Contoh Label di Guhanjabaku ... 78
Lampiran 5. Contoh Surat Perintah Logistik (SPL) ... 79
Lampiran 6. Contoh Bentuk 051 ... 80
Lampiran 7. Contoh Surat Perintah Pengeluaran ... 81
Lampiran 8. Contoh Surat Perintah Produksi... 82
Lampiran 9. Contoh Surat Perintah Pelaksaan Produksi (SP3)... 83
Lampiran 10. Surat Perintah Kerja (SPK) ... 84
Lampiran 11. Denah Ruang Produksi Beta Laktam ... 85
Lampiran 12. Denah Ruang Produksi Non Beta Laktam ... 86
Lampiran 13. Contoh Label Produk Obat Jadi ... 87
Lampiran 14. Catatan Pengujian Penetapan Potensi Secara Mikrobiologi ... 88
Lampiran 15. Instruksi Pengambilan Contoh ... 89
Lampiran 16. Denah Ruang Laboratorium... 90
Lampiran 17. Denah Pengolahan Limbah ... 91
Lampiran 18. Produk – Produk Yang Diproduksi LAFIAU... 92
Halaman
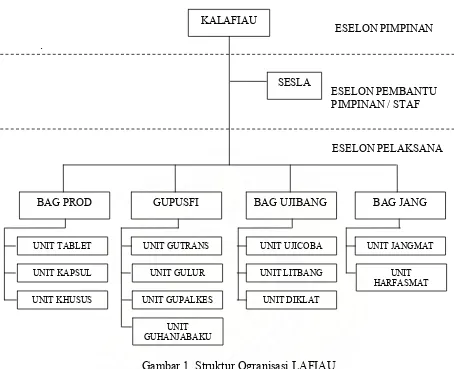
Gambar 1. Struktur Organisasi LAFIAU... 25
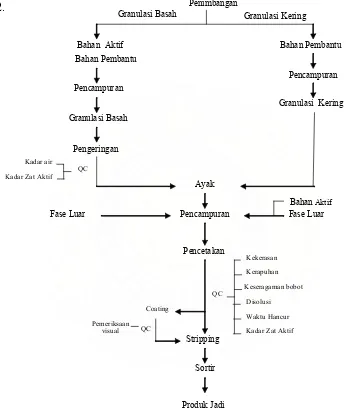
Gambar 2. Alur Produksi Tablet ... 43
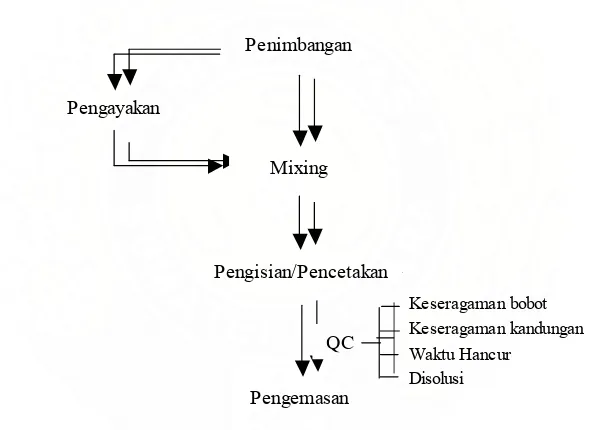
Gambar 3. Alur Produksi Kapsul... 44
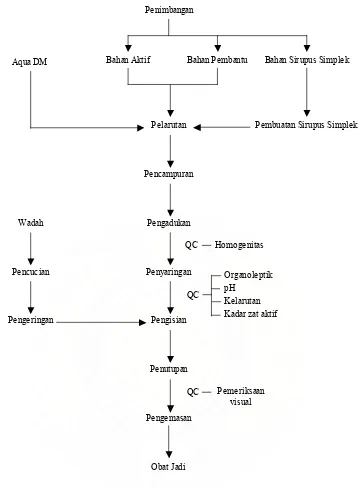
Gambar 4. Alur Produksi Sirup ... 46
Gambar 5. Alur Produksi Salep ... 47
Gambar 6. Alur Produksi Krim... 48
Telah dilakukan Praktek Kerja Profesi (PKP) di Lembaga Farmasi Angkatan Udara (LAFIAU) Lanud Husein Sastranegara Bandung, pada tanggal 3 maret 2008 sampai 28 maret 2008, dengan jumlah jam efektif 300 jam.
PKP ini bertujuan untuk memberikan gambaran yang nyata mengenai struktur organisasi dan peranan apoteker di industri farmasi serta mengetahui dan memahami penerapan CPOB di industri farmasi milik pemerintah.
Badan Pengawas Obat dan Makanan, (2001), Pedoman Cara Pembuatan Obat Yang Baik, Jakarta.
Badan Pengawas Obat dan Makanan, (2001), Petunjuk Operasional Penerapan Cara Pembuatan Obat Yang Baik, Jakarta.
Departemen Kesehatan RI, (1988), Keputusan Menteri Kesehatan RI No. 43/Menkes/SK/II/1978 tentang Pedoman Cara Pembuatan Obat Yang Baik, Jakarta.
Departemen Kesehatan RI, (1988), Keputusan Dirjen POM No.05410/A/SK/XII/1989 Petunjuk Operasional Penerapan Cara Pembuatan Obat Yang Baik, Jakarta.
LAMPIRAN 19. Tugas Khusus
Pembuatan Formula Tablet Simvastatin Tablet
Tablet menurut Farmakope Indonesia Edisi III adalah sediaan padat kompak, dibuat secara kempa cetak, dalam bentuk tabung pipih atau sirkuler, kedua permukaannya rata atau cembung, mengandung satu jenis obat atau lebih dengan atau tanpa zat tambahan.
Tablet merupakan jenis sediaan yang banyak digunakan sampai sekarang karena:
• Memberikan dosis yang tepat pada pemakaiannya.
• Mudah pemakaiannya.
• Cara pembuatannya sederhana.
• Mudah pengemasannya dan distribusinya.
• Stabil pada pengemasannya dan distribusinya.
• Stabilitas kimia dan aktifitas fisiologi dari bahan- bahan obat cukup baik. Tablet yang dinyatakan baik harus memenuhi persyaratan berikut ini:
• Memiliki kemampuan atau daya tahan terhadap pengaruh mekanis selama proses produksi, pengemasan dan distribusi.
• Bebas dari kerusakan seperti pecah- pecah, rompal pada permukaan dan sisi- sisinya.
• Dapat menjamin kestabilan fisik maupun kimia dari zat berkhasiat yang terkandung didalamnya.
Berdasarkan pembuatannya tablet dibagi menjadi : 1. Tablet cetak (Compressed tablet).
Tablet ini dibuat dengan cara mengempa dan tidak mengandung penyalut khusus. Dibuat dari bahan – bahan berupa serbuk atau kristal dengan atau tanpa penambahan bahan pengisi, pengikat, pengembang, pelicin dan bahan – bahan tambahan lainnya.
2. Tablet bersalut (Coated tablet).
a. Tablet bersalut gula yaitu tablet yang disalut dengan lapisan yang yang terdiri dari gula dengan bahan – bahan yang sesuai dengan atau tanpa pemberian warna. Penyalutan ini berguna untuk menutupi rasa dan bau dari bahan – bahan obat dan melindungi bahan – bahan obat yang peka terhadap oksidasi. b. Tablet bersalut selaput (Film Coated tablet). Yaitu tablet yang disalut dengan
lapisan tipis yang dibuat dari bahan – bahan sintetis atau bahan – bahan alam.
c. Tablet bersalut enterik (Enteric coated tablet). Yaitu tablet yang disalut dengan bahan – bahan yang tahan terhadap cairan lambung tetapi hancur dalam cairan usus.
Cara Pembuatan Tablet dibagi atas : I. Cara Kering (granulasi kering)
2. Granulasi dasar I. Cara Kering
1.1. Pencetakan langsung
Cara ini hanya dilakukan untuk bahan – bahan tertentu saja, yang berbentuk kristal/butir-butir granul yang mempunyai sifat-sifat yang diperlukan untuk membuat tablet yang baik dan dapat mengalami peristiwa deformasi plastis pada saat pencetakan.
1.2. Pencetakan Tak Langsung
Disebut juga Slugging = pencetakan ganda = prekompresi. Cara ini dikerjakan bila bahan – bahan obat tidak tahan lembab atau panas dan bersifat kohesif sehingga memudahkan waktu mencetak.
II. Cara Basah 2.1. Granulasi basah
Cara ini paling banyak dan umum digunakan karena menghasilkan granul – granul yang mempunyai sifat – sifat yang dibutuhkan untuk pencetakan tablet dan tablet yang dihasilkan biasanya lebih kompak. Pada cara ini bahan pengikat ditambahkan dalam bentuk larutan misalnya larutan gelatin, mucilago amili. 2.2. Granulasi Dasar
SIMVASTATIN
Rumus Molekul :
BM : 418,6 C25H38O5
R/ Simvastatin 10 mg
Mucilago Amili 10 %
Lactosa q s
Amilum Manihot 5 %
Nipagin 0,1 %
Nipasol 0,1 %
Untuk resep 1 tablet :
R/ Simvastatin 10 mg
Mucilago Amili 15 mg
Lactosa q s
Amilum Manihot 7,5 mg
Nipagin 0,15 mg
Nipasol 0,15 mg
Talkum 2,7 mg Mg Stearat 0,3 mg Untuk resep 1000 tablet :
R/ Simvastatin 10 g
Mucilago Amili 15 g
Lactosa q s
Amilum Manihot 7,5 g
Nipagin 0,15 g
Nipasol 0,15 g
Talkum 2,7 g Mg Stearat 0,3 g KOMPOSISI DAN SPESIFIKASI
KOMPOSISI
• Simvastatin
• Lactosa
• Nipagin
• Nipasol
• Talkum
• Mg stearat SPESIFIKASI 1. Simvastatin
Pemerian : Warna putih atau hamper berbentuk kristal putih.
Kelarutan : Praktis tidak larut dalam air, larut dalam alkohol, larut dalam kloroform, dan larut dalam metil alkohol.
Khasiat : Digunakan Sebagai obat kolesterol Efek saming : Mata kabur, insomnia, dan alergi kulit.
Kandungan : Simvastatin tablet mengandung tidak kurang dari 90,0 % dan tidak lebih dari 110,0 % dari C25H38O5.
Penyimpanan : Terlindung dari cahaya.
LOD : pada suhu 600C selama 2-3 jam 2. Amylum Manihot
Pemerian : Serbuk sangat halus warna putih.
Kelarutan : Praktis tidak larut dalam air dingin dan dalam etanol. Khasiat : Zat tambahan
3. Saccharum Lactis
Kelarutan : Larut dalam 6 bagian air, larut dalam 1 bagian air mendidih, sukar larut dalam etanol 95%, praktis tidak larut dalam kloroform P dan dalam eter P.
Khasiat : Zat tambahan. 4. Nipagin
Pemberian : Hablur kecil, tidak berwarna atau serbuk hablur putih tidak berbau atau berbau khas lemah mempunyai sedikit rasa terbakar.
Kelarutan : Larut dalam 500 bagian air, dalam 20 bagian air mendidih, 3,5 bagian etanol 95%, dalam 3 bagian aseton, mudah larut dalam eter P dan alkali hidroksida.
Khasiat : Zat tambahan dan pengawet. 5. Nipasol
Pemerian : Serbuk hablur putih, tidak berbau dan tidak berasa.
Kelarutan : Sangat sukar larut dalam air, larut dalam 3,5 bagian etanol 90% P ,dalam 3 bagian aseton P, dalam 40 bagian minyak lemak, mudah larut dalam NaOH.
Khasiat : Zat pengawet 6. Talkum
Pemerian : Serbuk hablur, sangat halus licin, mudah melekat bebas dari butiran, warna putih atau putih kelabu.
7. Mg Stearat
Pemerian : Serbuk halus putih, bau lemah khas, mudah melekat dikulit, bebas dari butiran.
Kelarutan : Tidak larut dalam air, etanol dan eter. Khasiat : Zat tambahan
Cara perhitungan 1000 tablet: a. Formula
Simvastatin 10 mg
Formula lengkap
Simvastatin 10 mg = 0,01 g
Mucilago Amili = 10 %
Lactosa = q s
Amilum manihot = 5 %
Nipagin = 0,1 %
Nipasol = 0,1 %
Talkum dan Mg Stearat = 2 %
Talkum : Mg Stearat = 9 : 1 b. Perencanaan bahan
Spesifikasi bahan
• Spesifikasi tablet = Bobot tablet 150 mg = 0,15 g Diameter tablet 6 mm, bulat rata
Mucilago Amili = 10 %
10 % x 150 mg x 1000 tablet = 15000 mg = 15 g
10 % = 10 g Amilum dilarutkan dalam 90 ml air. Cara pembuatan mucilago amili (sebagai pengikat) :
Amilum ditambah dengan air dingin kemudian diaduk sampai airnya merata lalu ditambah dengan aqua DM panas lalu diaduk sampai terbentuk mucilago amili (ditandai dengan warna bening). Sedangkan bahan pengawet (nipagin dan nipasol) dilarutkan dengan aqua DM panas
Amilum manihot = 5 % x 150 mg x 1000 tablet = 7500 mg
= 7,5 g
Campuran Talkum dan Mg Stearat 2 % (9 : 1)
= 2 % x 150 mg x 1000 tablet = 3000 mg Talkum = 9 / 10 x 3000 mg = 2700 mg
= 2,7 g Mg Stearat = 1 / 10 x 3000 mg = 300 mg
= 0,3 g Nipagin = 0,1 %
= 0,1 % x 150 mg x 1000 tablet = 150 mg = 0,15 g
Nipasol = 0,1 %
Lactosa = (1000x0,15g)–(10+ 15+7,5+ 2,7+0,3+0,15+0,15)g = 150 g – 38,5 g
= 114,2 g c. Prosedur kerja
Timbang masing- masing bahan
Bahan obat ditambah bahan pengisi dicampur dengan bahan pengembang dalam, di mixer sampai homogen.
Tambah pengawet sedikit demi sedikit sampai diperoleh massa yang homogen.
Tambahkan bahan pengikat sedikit demi sedikit sampai diperoleh massa yang baik (yaitu massa yang bila dikepal akan bersatu dan bila di tekan akan hancur menjadi gumpalan – gumpalan kecil).
Granulasi massa melalu ayakan nomor 15.
Granulat dikeringkan pada lemari pengering (oven) suhu 60oC, selama 2 sampai 3 jam, cek kadar air.
Granulat kering digranulator dengan ayakan mesh 16. IPC :
• Homogenitas
• Kadar zat aktif
• LOD
Tambahkan bahan pengembang luar dan talkum (bahan pelicin) sambil mixing, kemudian ditambah Mg stearat, sambil dimixing sampai diperoleh massa yang homogen.
• Homogenitas
Cetak masa dengan mesin cetak IPC :
• Kekerasan
• Keseragaman bobot
• Waktu hancur
• Friabilitas
• Kadar zat aktif
DAFTAR PUSTAKA
Departemen Kesehatan RI, 1979, Farmakope Indonesia, Edisi III, Jakarta.
Lachman, L., Liebermann, H.A., and Kanig, J.L. (1998). Teori dan Praktek Farmasi Industri. Judul Asli : The Theory and Practice of Industrial Pharmacy, (Penerjemah : Suyatmi, S.), Edisi Ketiga, UI Press, Jakarta. Soekemi dkk., 1998, Tablet, Jakarta, hal 1 – 4.
6.1. Kesimpulan
Berdasarkan hasil pengamatan kegiatan kerja praktek di LAFIAU dan pembahasan di atas, dapat disimpulkan bahwa:
1. LAFIAU secara umum telah melakukan prosedur dan memenuhi persyaratan yang ditetapkan dalam CPOB, sehingga menghasilkan produk obat yang bermutu dan aman.
2. Lembaga Farmasi TNI AU merupakan industri farmasi yang bersifat nonprofit, seluruh produk yang dihasilkan hanya dipergunakan untuk memenuhi kebutuhan anggota TNI AU dan keluarganya di seluruh Indonesia.
3. Lembaga Farmasi TNI AU dalam melaksanakan manajemen dan kegiatan organisasinya berdasarkan pada satu komando dari Diskesau, sehingga perencanaan kerja dan pengendalian kerjanya dilakukan secara terpusat. 4. Kegiatan, tugas dan fungsi masing- masing bagian di LAFIAU telah
disusun sesuai kebutuhan dan memiliki uraian kerja yang jelas, sehingga menjamin berlangsungnya sistem kepengurusan yang baik dan terkendali. 6.2 Saran
BAB V PEMBAHASAN
Lembaga Farmasi Angkatan Udara (LAFIAU) merupakan salah satu pelaksana teknis dibidang farmasi dari Dinas Kesehatan TNI AU (DISKESAU). Lembaga ini bersifat nonprofit (tidak mengejar laba), produk yang dihasilkannya tidak untuk diperjualbelikan, tetapi sesuai dengan visinya yaitu memenuhi kebutuhan obat yang berkualitas bagi internal anggota TNI AU dan keluarganya diseluruh indonesia yang diberikan secara cuma – cuma dan berperan serta dalam memenuhi kebutuhan obat nasional.
Sebagai pelaksana teknis Diskesau, maka LAFIAU dalam melaksanakan segala fungsi, tugas, dan aktivitasnya adalah berdasarkan kebijakan dan garis komando dari Diskesau. Dalam hal ini, Diskesau berperan sebagai PPIC (Product Planning and Inventory Control). Yang melaksanakan perencanaan produksi
sampai dengan pengendalian produk dan inventarisnya. Dengan kata lain, dalam sistem kesehatan TNI AU termasuk di dalamnya LAFIAU menerangkan sistem kepemimpinan satu garis komando. Sistem ini memiliki keuntungan dibandingkan dengan sistem yang lain, karena seluruh sistem dapat terkendali dan tercatat dengan baik dibawah satu koordinasi yang rapi.
pengerjaan dari maklon yang dapat digunakan untuk meningkatkan biaya perawatan dan kesejahteraan anggota. Berikut ini akan dibahas mengenai pelaksanaan CPOB di LAFIAU
5.1 Personalia
Struktur organisasi LAFIAU disusun dan dirancang sesuai dengan kebutuhan, yang menjamin pelaksanaan kegiatan serta pengawasan yang baik, didukung oleh personil – personil yang berkompeten di bidangnya. Latar belakang pendidikan personil yang ada antara lain : Apoteker S2, Apoteker S1, D3 Farmasi, Asisten Apoteker, Analis Farmasi, STM kimia, STM mesin, dan umum. Dalam segi jumlah, personil yang ada di Lafiau masih kurang memadai.
Pada dasarnya kekurangan personil pada industri terutama skala besar atau mencari untung dapat mempengaruhi kualitas obat, karena tugas akan dilaksanakan tergesa – gesa dengan segala akibatnya atau personil yang menjalankan multi fungsi atau bekerja melewati batas akan mengalami kelelahan fisik dan mental yang pada akhirnya akan menurunkana kinerja personil.
manajer produksi dan manajer pengawasan mutu. Hal ini bertujuan agar pengawasan mutu produk lebih ketat sehingga diperoleh obat yang berkualitas baik.
5.2 Bangunan
Tata letak bangunan di LAFIAU disesuaikan dengan jenis kegiatan dan spesifikasi bangunan. Setiap bangunan produksi telah memenuhi persyaratan dan mendapatkan sertifikat CPOB.
Pemisahan bangunan produksi beta laktam dengan non-beta laktam ditujukan untuk mencegah terjadinya kontaminasi silang. Demikian pula bangunan produksi beta laktam dengan sefalosporin dipisahkan untuk mencegah terjadinya kontaminasi silang yang pada akhirnya dapat menimbulkan resistensi antibiotik dan mencegah reaksi alergi. Bangunan produksi non- beta laktam dan beta laktam merupakan ruangan produksi kelas III, telah sesuai dengan persyaratan CPOB. Bangunan produksi sefalosporin terdiri dari ruangan kelas III, kelas II dan kelas I. Semuanya telah sesuai dengan persyaratan CPOB dan telah mendapatkan sertifikat CPOB.
produksi, meliputi suhu, kelembaban, tekanan udara, cahaya, jumlah maksimum pencemaran partikel dan mikroba seluruhnya telah sesuai dengan persyaratan CPOB.
Sistem pengaturan udara (Air Handling System/ AHS) mengatur pertukaran udara yang masuk ke dalam dan keluar dari ruang produksi, sehingga udara yang masuk maupun keluar adalah udara yang bersih. Tekanan udara didalam ruang produksi non- beta laktam lebih tinggi dari tekanan udara di lingkungan luar, sehingga dapat mencegah masuknya pencemaran dari lingkungan luar ke dalam ruang produksi. Selain itu, tekanan udara dikoridor ruang produksi di buat positif dari pada tekanan udara didalam ruangan pengolahan hal ini bertujuan agar debu dari ruang pengolahan tidak keluar ke koridor, sebaiknya debu dari koridor akan mengalir keruang pengolahan dan selanjutnya akan diserap dengan dust collector. Untuk ruang produksi sirup, tekanan udara dibuat lebih positif dari pada koridor untuk mencegah pencemaran sirup dari debu- debu yang ada dikoridor. Perbedaan tekanannya adalah sekitar 10- 15 Pa. Sedangkan untuk ruang produksi beta laktam, tekanan udara didalam ruang produksi dibuat lebih negatif, agar debu dari proses beta laktam tidak keluar dari ruangan produksi. Sebab debu- debu antibiotik beta laktam tersebut dapat membahayakan resistensi serta dapat menimbulkan reaksi alergi.
menggunakan Pre-filter dan Medium-filter, udara juga disaring lagi menggunakan Hepa-filter (High Eficiency Particulat Air Filter) sehingga udara yang masuk
steril untuk kelas I selain Pre, Medium dan HEPA filter dilengkapi pula dengan LAF (Laminer Air Flow)
Pembersihan ruangan dilakukan secara berkala, biasanya dilakukan seminggu sekali. Akan tetapi, pembersihan juga selalu dilakukan setiap sebelum dan setelah proses produksi. Setiap anggota diharuskan membersihkan diri (minimal membersihkan tangan) sebelum memasuki ruangan produksi, memakai pakaian kerja, masker, tutup kepala, sarung tangan, alas kaki khusus untuk menjaga keselamatan anggota dan mencegah terjadinya kontaminasi dari anggota. Untuk menunjang hal tersebut setiap ruang produksi dilengkapi dengan kamar mandi dan wastafel untuk memudahkan anggota membersihkan diri. Dengan demikian, dapat dikatakan bahwa bangunan produksi secara keseluruhan dilafiau telah memenuhi persyaratan CPOB.
5.3 Peralatan
Peralatan yang ada di LAFIAU sudah sangat memadai untuk dapat menjalankan proses produksi maupun pengujian mutunya. Semua peralatan sebelum digunakan dikualifikasi dahulu, yang meliputi kualifikasi desain, kalifikasi instalasi, operasional dan kinerja. Khusus untuk peralatan yang digunakan untuk pengukuran harus dikalibrasi dahulu. Pemeliharaan peralatan dilakukan secara berkala baik oleh masing- masing bagian, serta oleh bagian penunjangan terutama unit harfasmat (pemeliharaan fasilitas material).
5.4 Sanitasi dan Higiene
Dalam rangka pelaksanaan sanitasi dan higiene terdapat prosedur tetap yang telah diselenggarakan di LAFIAU. Program ini meliputi pemeriksaan kesehatan personil secara rutin (setiap 2 bulan). Pemeliharaan ruangan produksi, peralatan, maupun kebersihan personil. Seperti telah disingung sebelumnya bangunan dan peralatan secara rutin dibersihkan seminggu sekali dan setiap sebelum dan setelah proses produksi. Untuk personil, sebelum memasuki ruang produksi diharuskan membersihkan diri (mandi ataupun mencuci tangan), memakai pakaian kerja, sarung tangan, penutup kepala, alas kaki khusus untuk menjaga keselamatan kerja personil maupun mencegah kontaminasi terhadap obat yang diproduksi. Pakaian kerja secara rutin dicuci/dibersihkan.
5.5 Produksi
membuat rencana produksi selama 1 tahun, serta membuat Batch Record kemudian menyerahkan kepada kepala unit produksi untuk melaksanakan produksi.
Proses produksi dilakukan mengikuti prosedur tetap (protap) yang telah ditetapkan. Fasilitas yang tersedia di bagian produksi LAFIAU cukup lengkap diantaranya fasilitas gedung, peralatan dan fasilitas penunjang seperti pengolahan air limbah dan pengolahan air demineralisata. Air demineralisata diperlukan untuk memproduksi sediaan cair dan sebagai larutan pengikat tablet yang dibuat dengan metode granulasi basah. Ketersediaan air yang memenuhi syarat untuk proses produksi sangat penting. Fasilitas pengolahan air akan menghemat biaya produksi karena LAFIAU tidak perlu lagi membeli air untuk keperluan produksi. Fasilitas penunjang lain yang juga sangat diperlukan dalam suatu industri farmasi adalah fasilitas pengolahan limbah. Karena limbah industri farmasi banyak mengandung bahan – bahan obat yang dapat membahayakan makhluk hidup dan lingkungan sekitar.
Produk jadi selanjutnya dikirim ke gudang transit, setelah memenuhi persyaratan kemudian disimpan di gudang obat jadi dan bahan baku dan dicatat sebagai kekayaan negara. Obat jadi disimpan kemudian didistribusikan ke satuan – satuan kerja (satker) kesehatan TNI AU di seluruh indonesia berdasarkan SPL (Surat Perintah Logistik) dari Diskesau. Metode penyaluran barang berdasarkan sistem FIFO (First In First Out) dan FEFO (First Expired First Out).
5.6 Pengawasan Mutu
bagian pengawasan mutu dalam LAFIAU adalah bagian ujibang yang bertanggung jawab untuk memastikan bahwa:
a. Bahan awal untuk produksi obat memenuhi spesifikasi yang ditetapkan untuk identitas, kekuatan, kemurnian, kualitas dan keamanannya.
b. Tahapan produksi obat telah dilaksanakan sesuai prosedur yang ditetapkan dan telah divalidasi sebelumnya antara lain melalui evaluasi, dokumentasi, produksi terlebih dahulu.
c. Semua pengawasan selama proses dan pemeriksaan laboratorium terhadap suatu batch tersebut telah memenuhi spesifikasi yang telah ditetapkan sebelum didistribusi.
d. Suatu batch obat memenuhi persyaratan mutunya selama waktu beredar yang telah ditetapkan.
5.7. Inspeksi Diri
Inspeksi diri bertujuan untuk mengevaluasi seluruh sistem operasi perusahaan dalam semua aspek yang dapat mempengaruhi mutu produk. Dengan kata lain, inspeksi diri bertujuan untuk memastikan bahwa setiap langkah dalam pembuatan obat dilakukan secara seksama. Inspeksi diri bukan hanya mencari kesalahan atau kelemahan yang ada, tetapi lebih utama untuk mencari cara pencegahan dan mengatasi masalah secara efektif. Inspeksi diri mencakup aspek personalia, bangunan dan peralatan, dokumentasi, produksi, pengawasan mutu, keluhan dan penarikan kembali produk serta distribusi. Tim inspeksi diri terdiri dari tenaga ahli dari komponen kerja dipabrik, perwakilan dari bagian produksi, pengawasan mutu dan teknik. Sekurang- kurangnya tim inspeksi diri terdiri dari tiga orang, mempunyai pengetahuan CPOB dengan baik, independen dan objektif, dapat berasal dari lingkungan dalam atau luar perusahaan.
5.8 Penanganan keluhan Terhadap Obat, Penarikan Kembali Obat dan obat kembalian
mengeluarkan surat perintah untuk penghapusan obat jadi batch tersebut ke lafiau, kemudian diinformasikan satker yang ada untuk menggunakan obat tersebut. 5.9. Dokumentasi
BAB I PENDAHULUAN
1.1 Latar Belakang
Kesehatan merupakan hak asasi dari setiap orang. Salah satu upaya untuk memelihara, menyembuhkan dan meningkatkan kesehatan yaitu dengan menggunakan obat. Sarana penyediaan obat-obatan bagi masyarakat dimulai dari aktivitas industri farmasi dengan memproduksi dan mendistribusikan obat-obat yang bermutu tinggi, berkhasiat, tepat waktu penyediaan, jumlah yang cukup bagi masyarakat, dan terjamin keamanannya serta dengan harga yang terjangkau.
Peranan industri farmasi sebagai produsen obat sangat penting bagi tercapainya suatu kata “mutu”. Mutu harus dicapai, dipertahankan dan ditingkatkan. Dengan menjaga mutu, berarti industri farmasi ikut serta menjaga kesehatan sesama dan mengabdi kepada umat manusia. Oleh karena itu, industri farmasi harus memenuhi suatu standar Cara Pembuatan Obat yang Baik (CPOB) yang telah dicanangkan oleh pemerintah Indonesia atau di dunia internasional dikenal sebagai Good Manufacturing Practices (GMP).
yang dihasilkan antara lain mulai dengan pengadaan bahan baku, proses pembuatan dan pengawasan mutu, personil yang terlibat dalam proses produksi, bangunan dan peralatan.
Lembaga Farmasi Angkatan Udara (Lafiau) Diskesau merupakan salah satu realisasi untuk mencapai kemandirian tersebut. Lembaga ini berfungsi memproduksi obat-obatan dengan mutu, khasiat serta keamanan yang terjamin untuk digunakan oleh prajurit, PNS TNI AU dan keluarganya. Lembaga yang berada di bawah Dinas Kesehatan Angkatan Udara (Diskesau) ini berupaya untuk menerapkan prinsip-prinsip Cara Pembuatan Obat yang Baik (CPOB). Aplikasi CPOB menyangkut seluruh aspek produksi dan pengendalian mutu yang bertujuan untuk menjamin produk obat yang dihasilkan senantiasa memenuhi standar mutu yang ditetapkan.
1.2 Tujuan Praktek Kerja
1. Memberikan gambaran yang nyata mengenai struktur organisasi, peranan apoteker, situasi serta kondisi kerja di industri farmasi.
2. Mempelajari dan memahami pengelolaan Industri Farmasi yang dilakukan dengan baik dan profesional sesuai dengan ketentuan CPOB. 3. Mengetahui gambaran, pelaksanaan, dan perencanaan produksi farmasi
BAB II
TINJAUAN UMUM INDUSTRI FARMASI
2.1Pengertian Industri Farmasi
Industri farmasi menurut surat keputusan menteri kesehatan no. 245/ Men Kes/V /1990 adalah industri obat jadi dan industri bahan baku obat. Industri obat jadi adalah industri yang menghasilkan suatu produk yang telah melalui seluruh tahap proses pembuatan. Sedangkan industri bahan baku adalah bahan baku yang diproduksi oleh suatu industri, bahan baku tersebut adalah semua bahan baik yang berkhasiat maupun tidak berkhasiat, yang digunakan dalam proses pengolahan obat.
2.2Cara Pembuatan Obat yang baik
Industri farmasi merupakan industri yang memproduksi obat yang aman dan berkualitas. Untuk menjamin mutu obat yang berkualitas, maka industri farmasi melakukan seluruh aspek dan rangkaian kegiatan produksinya dengan menerapkan Cara Pembuatan Obat yang Baik (CPOB). CPOB dilaksanakan secara menyeluruh dan terpadu dengan mengadakan pengawasan baik sebelum, selama, dan sesudah proses produksi berlangsung untuk memastikan mutu produk obat agar memenuhi standar yang telah ditetapkan.
dengan menerapkan “Good Manufacturing Practices” dalam seluruh aspek dan rangkaian kegiatan produksi, sehingga obat yang dihasilkan senantiasa memenuhi persyaratan mutu yang ditentukan sesuai dengan tujuan penggunaannya.
Perkembangan yang sangat pesat dalam teknologi farmasi menyebabkan perubahan-perubahan yang sangat cepat pula dalam konsep serta persyaratan CPOB. Konsep CPOB bersifat dinamis yang memerlukan penyesuaian dari waktu ke waktu mengikuti perkembangan teknologi di bidang farmasi. Ruang lingkup CPOB meliputi 10 aspek, yaitu :
1. Ketentuan umum 2. Personalia 3. Bangunan 4. Peralatan
5. Sanitasi dan hygiene 6. Produksi
7. Pengawasan mutu 8. Inspeksi diri
9. Penanganan terhadap keluhan terhadap obat, penarikan kembali obat dan obat kembalian.
10.Dokumentasi 2.2.1 Ketentuan Umum
yang dibuat senantiasa memenuhi persyaratan mutu yang telah disesuaikan dengan tujuan penggunaannya.
Dalam ketentuan umum, ada beberapa landasan yang penting untuk diperhatikan, yaitu :
a. Pengawasan menyeluruh pada proses pembuatan obat untuk menjamin bahwa konsumen menerima obat yang bermutu tinggi.
b. Mutu obat tergantung pada bahan awal, proses pembuatan dan pengawasan mutu, bangunan, peralatan yang digunakan, dan personalia. c. Untuk menjamin mutu suatu obat jadi tidak boleh hanya mengandalkan
pada suatu pengujian tertentu saja, melainkan semua obat hendaknya dibuat dalam kondisi terkendali dan terpadu dengan cermat.
d. CPOB merupakan pedoman yang dibuat untuk memastikan agar sifat dan mutu obat yang dihasilkan sesuai dengan syarat bahwa standar mutu obat yang telah ditentukan tetap tercapai.
2.2.2 Personalia
Semua karyawan harus memiliki pengetahuan, keterampilan dan kemampuan sesuai tugasnya. Karyawan memiliki kesehatan mental dan fisik yang baik sehingga mampu melaksanakan tugasnya secara profesional dan sebagaimana mestinya. Karyawan mempunyai sikap dan kesadaran yang tinggi untuk mewujudkan CPOB.
penuh dan sarana yang cukup yang diperlukan untuk dapat melaksanakan tugasnya secara efektif.
Manajer produksi seorang apoteker yang cakap, terlatih dan memiliki pengalaman praktis yang memadai dibidang industri farmasi dan keterampilan dalam kepemimpinan sehingga memungkinkan melaksanakan tugas secara profesional. Manajer produksi memiliki wewenang dan tanggung jawab khusus penuh untuk mengelola produksi obat.
Manajer pengawasan mutu seorang apoteker yang cakap, terlatih, dan memiliki pengalaman praktis yang memadai untuk memungkinkan melaksanakan tugasnya secara professional. Manajer pengawasan mutu diberi wewenang dan tanggung jawab penuh dalam seluruh tugas pengawasan mutu yang dalam penyusunan, verifikasi dan pelaksanan seluruh prosedur pengawasan mutu. Manajer pengawasan mutu adalah satu-satunya yang memiliki wewenang untuk meluluskan bahan awal, produk antara, produk ruahan dan obat jadi bila produk tersebut sesuai dengan spesifikasinya, atau menolaknya bila tidak cocok dengan spesifikasinya, atau bila tidak dibuat sesuai dengan prosedur yang disetujui dan kondisi yang ditentukan.
Seluruh karyawan yang ikut serta langsung dalam kegiatan pembuatan obat harus dilatih mengenai kegiatan tertentu yang sesuai dengan tugasnya dan mampu melaksanakan prinsip-prinsip CPOB.
2.2.3 Bangunan
Bangunan LAFIAU terdiri dari bangunan produksi, pengawasan dan pengembangan mutu (Quality Control / QC dan Quality Assurance / QA), bagian gudang dan bangunan untuk administrasi. Semua bangunan tersebut terletak saling berdekatan di lingkungan LAFIAU.
Bangunan produksi terdiri dari bangunan untuk produksi Laktam dan produksi non Laktam. Hal ini sudah sesuai dengan persyaratan dalam CPOB untuk menghindari kontaminasi silang. Bagian produksi non Laktam dibagi menjadi dua bagian lagi, yaitu produksi tablet/kaplet dan produksi khusus yang memproduksi sirup serta salep. Disamping bangunan tersebut, saat ini LAFIAU sedang mempersiapkan bangunan yang akan digunakan untuk produksi obat sefalosporin. LAFIAU hanya memiliki 2 jenis area untuk produksi yaitu black area dan grey area karena LAFIAU tidak memproduksi obat-obat steril.
Bangunan hendaknya mendapat penerangan dan ventilasi yang efektif dengan fasilitas pengontrolan udara (suhu, kelembaban, filtrasi) sesuai dengan kegiatan diluar dan didalam. Penentuan rancangan bangunan dan penataan gedung dipertimbangkan kesesuaiannya dengan kegiatan lain untuk menjamin mutu obat dan kelangsungan produksi. Untuk itu daerah pabrik dibagi atas tiga zona :
a. Zona hitam
Zona yang bebas dimasuki sembarang petugas. Pada zona ini dilakukan pekerjaan-pekerjaan yang tidak memerlukan penjagaan ketat terhadap kontaminasi dari udara luar.
b. Zona abu-abu
Zona tempat proses produksi non steril berlangsung. Pada zona ini kebebasan karyawan dan barang yang memasuki ruangan dikurangi. Untuk memasuki daerah ini karyawan terlebih dahulu harus mencuci tangan dan memakai pakaian khusus yang bersih. Barang yang memasuki daerah ini harus diganti kemasannya dengan kemasan khusus.
c. Zona putih
2.2.4 Peralatan
Rancang bangun dan konstruksi peralatan hendaknya memenuhi persyaratan sebagai berikut :
a. Permukaan peralatan yang bersentuhan dengan bahan baku, produk antara, produk ruahan, atau obat jadi tidak boleh bereaksi, mengadisi atau mengabsorbsi, yang dapat mengubah identitas, mutu atau kemurniaannya diluar batas yang telah ditentukan.
b. Peralatan tidak boleh menimbulkan akibat yang merugikan terhadap produk, misalnya karena bocornya katup, menetesnya zat pelumas dan karena hal lain yang sejenis, atau karena perbaikan, pemeliharaan, modifikasi atau adaptasi yang salah.
c. Bahan-bahan yang diperlukan untuk suatu tujuan khusus, seperti pelumas atau pendingin, tidak boleh bersentuhan langsung dengan bahan yang diolah karena hal ini dapat merubah identitas, mutu atau kemurnian bahan baku, bahan antara, produk ruahan atau obat jadi.
d. Peralatan hendaklah dapat dibersihkan dengan mudah, baik bagian dalam maupun bagian luar.
e. Peralatan yang digunakan dalam pengolahan bahan kimia yang mudah terbakar, atau ditempatkan di daerah dimana digunakan bahan yang mudah terbakar, hendaklah dilengkapi dengan perlengkapan elektris yang kedap ekplosi
menurut suatu program dan prosedur yang tepat. Hasil pemeriksaan dan kalibrasi hendaklah dicatat dan catatan tersebut disimpan dengan baik.
g. Peralatan hendaknya ditempatkan sedemikian rupa sehingga dapat menghindari pencemaran silang, dan ditempatkan dengan jarak yang cukup renggang dari peralatan lain untuk memberikan keleluasaan kerja dan menghindari kekeliruan.
h. Peralatan hendaknya dirawat sesuai jadwal yang tepat dan menurut prosedur tertulis untuk perawatan yang telah ditetapkan.
i. Peralatan harus dikalibrasi dan divalidasi untuk menjamin kelancaran kerja. 2.2.5 Sanitasi dan Higiene
Tingkat sanitasi dan higiene yang tinggi hendaklah diterapkan pada setiap pembuatan obat. Ruang lingkup sanitasi dan higiene meliputi semua sumber pencemaran produk seperti personalia, bangunan, peralatan, bahan awal serta wadahnya. Sumber pencemaran hendaklah dihilangkan melalui program sanitasi dan higiene yang menyeluruh dan terpadu.
a. Personalia
b. Bangunan
Bangunan yang digunakan untuk pembuatan obat hendaknya dirancang dan dibangun dengan tepat untuk memudahkan pelaksanaan sanitasi yang baik. Bangunan hendaknya dilengkapi fasilitas sanitasi yang memadai seperti toilet, loker, bak cuci, tempat penyimpan bahan pembersih, insektisida, rodentisida, dan bahan fumigasi. Hendaknya disusun pula prosedur tetap untuk melaksanakan sanitasi dengan jadwal yang teratur, serta diuraikan dengan cukup rinci.
c. Peralatan
Setelah digunakan, peralatan hendaklah dibersihkan bagian luar maupun bagian dalam sesuai prosedur yang telah ditetapkan, serta dijaga dan disimpan dalam kondisi bersih. Sebelum dipakai, kebersihannya diperiksa lagi untuk memastikan bahwa seluruh produk atau bahan dari batch sebelumnya telah dihilangkan. Prosedur tertulis yang cukup rinci untuk pembersihan dan sanitasi peralatan dan wadah yang digunakan dalam pembuatan obat hendaklah dibuat serta ditaati. Prosedur ini dirancang dengan tepat agar pencemaran peralatan oleh bahan pembersih dan sanitasi dapat dicegah.
2.2.6 Produksi
Beberapa hal yang harus diperhatikan dalam kegiatan produksi adalah sebagai berikut :
a. Bahan awal
dinyatakan dalam spesifikasi. Semua pemasukan, pengeluaran, dan sisa bahan hendaknya dicatat.
b. Validasi proses
Luas serta tingkat validasi yang dilakukan tergantung dari sifat dan kerumitan produk dan proses yang bersangkuatan. Program dan dokumentasi validasi hendaklah membuktikan kecocokan bahan yang dipakai, keandalan peralatan dan sistem serta kemampuan petugas pelaksana.
c. Pencemaran
Pencemaran kimiawi atau mikroba terhadap suatu obat dapat merugikan kesehatan dan mengurangi daya terapeutik atau mempengaruhi kualitas suatu produk tidak dapat diterima. Pencemaran silang hendaknya diperhatikan, karena sekalipun sifat dan tingkatannya tidak berpengaruh langsung terhadap kesehatan, hal ini menunjukkan pelaksanaan obat yang tidak sesuai dengan CPOB.
d. Sistem penomoran batch dan lots
pemberiaan nomor, identitas produk dan besarnya batch dan lot yang bersangkutan.
e. Penimbangan dan penyerahan
Penimbangan atau penghitungan dan penyerahan bahan baku, bahan pengemas, produk antara dan produk ruahan dianggap suatu bagian dari siklus produksi dan memerlukan dokumentasi dan rekonsiliasi yang lengkap.
Semua pengeluaran bahan baku, bahan pengemas, produk antara dan produk ruahan termasuk tambahan bahan diluar yang telah diserahkan hanyalah yang telah diluluskan oleh pengawasan mutu dan harus didokumentasikan.
Bahan baku, produk antara dan produk ruahan yang diserahkan harus diperiksa ulang kebenarannya dan harus ditandatangani oleh supervisior produksi sebelum diserahkan ke bagian produksi.
f. Pengembalian
Bahan baku, bahan pengemas, produk antara, dan produk ruahan yang dikembalikan ke tempat penyimpanan hendaklah didokumentasikan dan dirujuk sesuai dengan prosedur. Bahan baku, bahan pengemas, produk antara, dan produk ruahan tidak boleh dikembalikan ke gudang, kecuali bila memenuhi spesifikasi yang ditetapkan.
g. Pengolahan
bahan, produk atau dokumen yang tidak diperlukan untuk pengolahan yang bersangkutan.
2.2.7 Pengawasan mutu
Pengawasan mutu adalah bagian yang esensial dari cara pembuatan obat yang baik untuk memastikan tiap obat yang dibuat senantiasa memenuhi persyaratan mutu yang sesuai. Pengendalian mutu obat dilaksanakan melalui sistem pengawasan yang terencana dan terpadu. Pengawasan mutu ini penting dalam hal penetapan spesifikasi, pengambilan contoh dan pengujian beserta dokumentasi dan prosedur pelulusan yang menjamin bahwa pengujian yang diperlukan benar-benar dilaksanakan, serta pelulusan bahan dan produk untuk dijual tidak akan diberikan sebelum mutunya dinilai memuaskan. Sistem pengawasan mutu dirancang dengan tepat untuk menjamin bahwa tiap obat mengandung bahan yang benar dengan mutu dan jumlah yang telah ditetapkan dan dibuat pada kondisi yang tepat dan mengikuti prosedur standar sehingga obat tersebut senantiasa memenuhi spesifikasi yang telah ditetapkan untuk identitas, kadar, kemurnian, mutu dan keamanannya. Bagian pengawasan mutu dalam suatu pabrik obat bertanggungjawab untuk memastikan bahwa :
a. Tahapan produksi obat telah dilaksanakan secara prosedur yang ditetapkan dan telah di validasi sebelumnya antara lain melalui evaluasi dokumentasi produk terdahulu.
c. Suatu batch memenuhi persyaratan mutunya selama waktu peredaran yang ditetapkan.
Bagian pengawasan mutu ini memiliki wewenang khusus untuk memberikan keputusan akhir meluluskan atau menolak atas mutu bahan baku atau produk obat ataupun hal lain yang mempengaruhi mutu obat.
2.2.8 Inspeksi diri
Tujuan dari inspeksi diri melakukan penilaian apakah seluruh aspek produksi dan pengendalian mutu selalu memenuhi CPOB. Program inspeksi diri dirancang untuk mendeteksi kelemahan dalam pelaksanaan CPOB dan untuk menetapkan tindakan perbaikan. Sehingga dibentuk suatu tim yang cakap dan mampu menilai secara obyektif pelaksanaan CPOB, melaksanakan inspeksi terhadap prosedur produksi dan pengawasan mutu secara menyeluruh. Prosedur pelaksanaan dan catatan mengenai inspeksi diri perlu di dokumentasikan.
Tim inspeksi diri ditunjuk oleh manajemen perusahaan, sekurang-kurangnya tiga orang yang ahli di bidang pekerjaannya dan paham mengenai CPOB. Inspeksi diri hendaknya dilakukan oleh orang yang kompeten dari perusahaan dengan atau tanpa bantuan tenaga ahli dari luar.
hasilinspeksi diri, evaluasi dan tindakan untuk perbaikan yang disampaikan kepada manajemen perusahaan.
2.2.9 Penanganan keluhan terhadap Obat, Penarikan Kembali Obat dan Obat Kembalian
Penarikan kembali obat jadi merupakan proses penarikan kembali obat dari semua mata rantai distribusi bila ditemukan adanya cacat kualitas dan yang berbahaya, atau dilaporkan adanya reaksi merugikan yang membahayakan kesehatan pemakainya selama atau sesudah pendistribusian obat jadi tersebut. Penarikan kembali seluruh obat jadi dapat menyebabkan penghentian sementara atau penghentian tetap terhadap pembuatan suatu jenis obat yang bersangkutan. Berdasarkan evaluasinya obat kembalian dapat dibagi menjadi 3 yaitu :
a. Obat kembalian yang masih memenuhi spesifikasi dan dapat digunakan. b. Obat kembalian yang masih dapat diolah ulang untuk memenuhi spesifikasi. c. Obat kembalian yang tidak memenuhi spesifikasi dan tidak dapat diolah ulang
(harus dimusnahkan).
dan dokumentasi yang berkaitan termasuk catatan batch, catatan distribusi dan catatan hasil pengujian.
2.2.10 Dokumentasi
Dokumentasi pembuatan obat merupakan bagian dari system informasi manajemen yang meliputi spesifikasi prosedur, metode dan instruksi, perencanaan, pelaksanaan, pengendalian serta evaluasi seluruh rangkaian pembuatan obat. Dokumentasi sangat penting untuk memastikan bahwa setiap petugas mendapat instruksi secara rinci dan jelas mengenai bidang tugas yang harus dilaksanakannya sehingga memperkecil resiko terjadinya salah tafsir dan kekeliruan yang biasanya timbul karena hanya mengandalkan komunikasi lisan.
Sistem dokumentasi harus menggambarkan riwayat lengkap dari setiap batch atau lot suatu produk sehingga memungkinkan penyelidikan serta penelusuran terhadap batch atau lot produk yang bersangkutan. Sistem dokumentasi serta digunakan dalam pemantauan dan pengendalian.
2.3 Validasi
Empat tahap penunjang dalam validasi meliputi : a. kalibrasi, verifikasi dan peralatan yang digunakan b. kualifikasi dan validasi peralatan yang digunakan
c. penandatanganan, pemeriksaan, pemantauan atau cuplikan dari tahap kritis yang sudah diketahui atau tahap kunci selama proses.
BAB III
TINJAUAN UMUM LEMBAGA FARMASI TNI AU
3.1 Sejarah dan Perkembangan
Lintasan sejarah lembaga farmasi angkatan udara Roostyan Effendie Perjalanan sejarah dimulai ketika dipangkalan udara belum mempunyai
satuan kesehatan, anggota auri mendapatkan perawatan dan pengobatan
dipoliklinik dan dirumah sakit angkatan darat RI (AD RI). Untuk mengurangi
ketergantungan terhadap DKAD, maka pimpinan berusaha mencukupi kebutuhan
obat dan alkes secara mandiri dengan mendirikan apotik dipangkalan udara andir
yang dipimpin oleh Lmu I Badris Nuch dan Di Cililitan Dipimpin Oleh Ramelan.
Keberadaan apotik tersebut mendorong pimpinan untuk mendirikan depot obat
guna mendukung pelayanan kesehatan dan kegiatan operasional AURI. periode
tahun 1951 sampai dengan 1953 DOP dipimpin oleh Lmu I Amir Andjilin.
Kiprahnya disamping tugas rutin juga turut serta mengirim personil dan logestik
dalam operasi Trikora.
Pada tahun 1964 dibawah Kepimpinan Lu I Drs Roostyan Effendie, mulai
dikembangkan produksi obat - obatan dengan skala lebih besar, dan didatangkan
pula peralatan produksi obat dari USA. Juga dilaksanakan renovasi bangunan
untuk produksi obat sesuai dengan persyaratan teknik farmasi saat itu. Unit
produksi obat diresmikan oleh Deputi Mentri Bidang Logistik tanggal 16 agustus
1965. Selanjutnya tanggal ini ditetapkan sebagai hari jadi Lembaga Farmasi
Berdasarkan Keputusan Panglima Angkatan Udara No. 5 tanggal 5 februari
1968, Puskalkes dikembangkan menjadi 2 unit satuan yang masing - masing
berdiri sendiri yaitu Puskalkes dan Pusprodkes.
Puskalkes bertugas melaksanakan Penerimaan, Penyimpanan, Penyaluran
alat kesehatan, Obat - obatan, Bahan baku dan Embalage. Dipimpin oleh Mayor
Far Drs Soekarsono, Apt, dilanjutkan oleh Mayor Dk Drs Poedjiadi
Soemodimedjo dan kemudian Mayor Far Drs Amin Mustofa, Apt.
Pusprodkes bertugas melaksanakan produksi obat dengan bahan baku dan
embalage dari puspalkes. Dipimpin oleh Kapten Drs Batus Gunawan, Apt
dilanjutkan Mayor Far Drs Sartono, Apt kemudian nama Pusprodkes berubah
menjadi Lembaga Farmasi Angkatan Udara (LAFI AU). Pada tahun 1981 dan
1982 LAFI AU dipercaya melaksanakan pemeriksaan terhadap Ransum tempur
dalam rangka Latgab dan Hut ABRI.
Pada tahun 1985, LAFI AU dan Pobekkes digabung menjadi depo
perbekalan kesehatan TNI Angkatan Udara disingkat POBEKKESAU dibawah
pimpinan Letkol Kes Drs Poedjiadi Soemodimedjo, MT., dilanjutkan oleh
Kolonel Kes Drg Sutarman, kemudian secara berturut- turut Kolonel Kes Drs
Kurnian K.N., Apt., Kolonel Kes Drs A. Ngadeni., Msc., Apt., dan kolonel Kes
Drs H Haruman K., Msc, Apt. Mulai tahun 1991 hingga saat ini, secara bertahap
dilakukan renovasi fasilitas bangunan produksi dalam rangka memenuhi standar
Cara Pembuatan Obat yang Baik (CPOB). Adapun fasilitas yang direnovasi
Laboratorium, Gudang Penyimpanan Bahan Baku dan Obat Jadi, Ruang Sampling
serta Gedung Mako.
Saat ini LAFI AU dipimpin oleh Kolonel Kes Drs Purwanto Budi., Apt.
yang dalam pengambilan kebijakan para pendahuluannya dengan selesainya
pembangunan fasilitas produksi sefalosporin berikut sarana penunjangnya, maka
dilakukan pemenuhan persyaratan sertifikat CPOB produksi tersebut. Tanggal 25
November 2005, badan pengawasan obat makanan RI mengeluarkan 3 dari 4
Sertifikat CPOB yang diajukan, yaitu Sediaan Tablet, Kapsul, dan Sirup kering. 1
sertifikat CPOB yang masih tertunda adalah untuk injeksi kering, hal ini
disebabkan persyaratan yang terus berkembang semakin ketat, sehingga perlu
dilakukan pembenahan fasilitas dan sarana penunjangnya.
Dalam mengemban peran Farmasi Militer diharapkan LAFI AU tidak hanya
berorentasi kepada produk saja, tetapi juga pada Pelayanan Kefarmasian
(Pharmaciutical care), yang berlangsung menjangkau personel Angkatan Udara.
Dalam mengemban peran mencerdaskan bangsa, LAFI AU aktif
membimbing mahasiswa peraktek kerja dan tugas akhir di lembaga ini, serta ikut
menyusun kurikulum dan mengirim personilnya sebagai Dosen pada Pendidikan
D3 Farmasi DiPoltekes Ciumbeleuit Bandung.
Buah pikiran dan keberanian Drs Roostyan Effendie, Apt untuk mulai
memproduksi obat- obatan sesuai dengan ketentuan farmasi setelah memberi
dorongan dan semangat bagi generasi berikutnya sehingga terbentuk lembaga
Farmasi Angkatan Udara seperti saat ini. sebagai bentuk penghargaan jasa beliau
31 juli 2007 maka pada hari ini kamis 1 november 2007, Diresmikan Nama
Lembaga Farmasi Angkatan Udara Roostyan Effendie dan tanggal 16 Agustus
1965 diterapkan sebagai Hari Jadi.
3.2Kedudukan, Tugas dan Kewajiban LAFIAU
LAFIAU adalah pelaksana teknis yang berkedudukan di bawah Dinas
Kesehatan TNI AU. LAFIAU bertugas membina kemampuan dan pelaksanaan
produksi obat jadi, pembekalan dan pengawasan kualitas dan persyaratan teknis
kefarmasian untuk melaksanakan dukungan dan pelayanan kesehatan bagi
anggota TNI AU pada khususnya dan TNI pada umumnya. Dalam rangka
melaksanakan tugasnya, LAFIAU mempunyai kewajiban sebagai berikut :
1. Melaksanakan kegiatan produksi obat jadi serta pengendalian mutu dari bekal
kesehatan TNI AU.
2. Melaksanakan penerimaan, penyimpanan, penyaluran, dan penghapusan bekal
kesehatan berdasarkan kebijaksaan Diskesau (Dinas Kesehatan Angkatan
Udara).
3. Melaksanakan pengawasan atas kualitas dan persyaratan teknis kefarmasian
bekal kesehatan dengan cara pengujian dan percobaan serta penelitian.
4. Melaksanakan penelitian dan pengembangan bidang farmasi
3.3Moto, Visi dan Misi LAFIAU a. Moto
Moto LAFIAU :
b. Visi
Visi LAFIAU :
• Terpenuhi kebutuhan obat berkualitas bagi prajurit TNI AU dan
keluarganya.
• Peran serta dalam penyediaan obat nasional
• Pengelolaan bekal kesehatan.
• Penegakan sistem manajemen mutu dalam kinerjanya.
c. Misi
Misi LAFIAU adalah :
• Melaksanakan produk obat jadi yang memenuhi persyaratan CPOB.
• Melaksanakan penerimaan, pengiriman, penyaluran dan penghapusan
bekal kesehatan berdasarkan kebijaksanaan Diskesau.
• Melaksanakan pengawasan atas kualitas dan persyaratan teknis
kefarmasian bekal kesehatan dengan cara pengujian serta penelitian.
• Melaksanakan Litbang bidang farmasi serta pendidikan dan latihan secara
profesional, efisien, efektif dan modern.
3.4 Struktur Organisasi LAFIAU
Secara struktural LAFI AU merupakan pelaksanaan teknis yang
berkedudukan dibawah Dinas Kesehatan LAFI AU yang bertugas membina
kemampuan dalam pelaksanaan produksi obat jadi, pembekalan dan pengawasan
kualitas sesuai persyaratan teknis kefarmasian, dalam memberikan dukungan dan
pelayanan kesehatan untuk anggota TNI AU pada khususnya dan TNI pada
KALAFIAU
UNIT TABLET UNIT GUTRANS
UNIT GULUR
Gambar 1. Struktur Ogranisasi LAFIAU
Untuk melaksanakan tugas tersebut LAFIAU mempunyai kewajiban :
1. Melaksanakan kegiatan produksi obat jadi serta pengendalian mutu dari bekal
kesehatan TNI AU.
2. Melaksanakan penerimaan, penyimpanan, penyaluran dan penghapusan bekal
kesehatan berdasarkan kebijakan DISKESAU.
3. Melaksanakan pengawasan serta kualitas dan persyaratan teknik
4. Melaksanakan penelitian dan pengembangan dibidang farmasi serta
melaksanakan pendidikan dan latihan.
Struktur organisasi LAFI AU terdiri dari Esselon Pimpinan yaitu Kepala
Lembaga Farmasi Angkatan Udara (Kalafiau), Esselon Pembantu Pimpinan/ Staf
yaitu Sekretaris Lembaga (Sesla) dan Esselon Pelaksana yaitu Kepala Bagian
Produksi (Kabag Prod), Kepala gudang Pusat Farmasi (Kaguspusfi), Kepala
Bagian dan Pengembangan (Kabagujibang) dan Kepala Unit Penunjang
(Kabagjang).
3.4.1 Kepala Bagian Farmasi TNI AU (Kalafiau)
Kalafiau adalah pelaksana teknis Diskesau yang bertanggung jawab
kepada Kadiskesau dalam hal pembinaan kemampuan dan pelaksanaan produksi
farmasi yang diperlukan oleh TNI AU, perbekalan kesehatan yang diperlukan bagi
pelaksana dukungan dan pelayanan kesehatan TNI AU serta pengawas atas
kualitas dan persyaratan teknis kefarmasian bekal kesehatan TNI AU.
3.4.2 Sekretaris Lafiau (Sesla)
Sekretaris Lafiau (Sesla) adalah pembantu staf Kalafiau dalam
menyelenggarakan perencanaan dan pengendalian pentahapan pelaksanaan
kegiatan produksi, perbekalan, serta program dan dukungan kegiatan Lafiau, yang
dalam pelaksanaannya dibantu oleh Kepala Program dan Anggaran, Kepala
3.4.3 Bagian Produksi
Bagian produksi Lafiau adalah pembantu pelaksana Kalafiau
melaksanakan produksi bekal kesehatan. Bagian produksi dipimpin oleh Kepala
Bagian Produksi (Kabagprod) yang bertanggungjawab langsung kepada Kalafiau.
Bagian produksi dalam melaksanakan tugasnya dibantu oleh:
1. Unit produksi tablet yang bertugas melaksanakan produk obat jadi dalam
bentuk tablet.
2. Unit produksi kapsul yang bertugas melaksanakan produksi obat jadi
dalam bentuk kapsul.
3. Unit produksi khusus yang bertugas melaksanakan produksi khusus,
seperti sirup, salep, cairan, antiseptik, tetes, dan lain-lain.
3.4.4 Bagian Gudang Pusat Farmasi (Gupusfi)
Gudang Pusat Farmasi dipimpin oleh Kaguspusfi yang bertanggungjawab
kepada Kalafiau. Kaguspusfi bertugas melaksanakan penerimaan, penyimpanan,
pemeliharaan, penyaluran serta penghapusan bekal kesehatan.
Kaguspusfi dalam melaksanakan tugasnya dibantu oleh :
a. Kepala Unit Gudang Transit (Ka Unit Gutrans), unit ini bertugas menerima
alat kesehatan (alkes) dan perbekalan kesehatan (bekkes) dari hasil pengadaan
Dinas Pengadaan AU (Disadaau) dan obat jadi dari bagian produksi Lafiau,
bersama komite penerimaan barang melaksanakan pemeriksaan terhadap alkes
dan bekkes yang diterima dari hasil pengadaan Disadaau dan obat jadi dari
persyaratan pada kontrak jual beli kepada rekanan yang mengirimkan alkes
dan bekkes, mengirimkan hasil alkes dan bekkes serta bahan baku yang
diterima dan memenuhi syarat ke gudang Palkes dan Guhanjabaku.
b. Kepala unit gudang penyaluran dan pengemasan (Ka Unit Gulur), bertugas
melaksanakan pengemasan/penyiapan barang yang akan dikirim berdasarkan
Surat Perintah Kadiskesau selaku ordonatur materiil kesehatan, mengusahakan
angkutan darat dan udara melalui seksi angkutan Lanud Husein Sastranegara
untuk mendukung kegiatan penyaluran, serta melaksanakan kegiatan
penyaluran barang pada satuan kerja dengan kelengkapan administrasi melalui
sarana yang tersedia.
c. Kepala unit gudang peralatan kesehatan (Ka Unit gupalkes), bertugas
menerima palkes dari gudang transit sesuai berita acara yang telah disahkan
ordonatur, menyimpan, merawat dan mengeluarkan palkes sesuai ketentuan
dan peraturan yang berlaku, serta melaksanakan administrasi pergudangan
terhadap peralatan yang disimpan memalui pembukuan, pengkartuan serta
penyimpanan dokumen yang berkaitan dengan penerimaan dan pengeluaran
barang.
d. Kepala unit gudang obat jadi, bahan baku, embalage (Ka Unit guhanjabaku),
bertugas menerima obat jadi, bahan baku, embalage dari unit gudang transit
sesuai dengan berita acara yang telah disahkan oleh ordonatur, menyimpan,
merawat/memelihara dan mengeluarkan barang (obat jadi, bahan baku,
sesuai dengan ketentuan dan peraturan yang berlaku, serta melaksanakan
administrasi pergudangan terhadap obat jadi, bahan baku, embalage yang
disimpan melalui pembukuan, pengkartuan dan penyimpanan dokumen
yang berkaitan dengan penerimaan dan pengeluaran barang.
3.4.5 Bagian Pengujian dan Pengembangan
Bagian Pengujian dan Pengembangan (Ujibang) adalah pembantu
pelaksana Kalafiau yang bertugas melaksanakan pengujian dan percobaan atas
kualitas bekal kesehatan, melaksanakan penelitian dan pengembangan untuk
meningkatkan hasil produksi obat jadi dan menyelenggarakan perencanaan serta
pelaksanaan pendidikan dan latihan. Bagian Uji Bang dipimpin oleh Kepala
Bagian Ujibang (Kabag Uji Bang) yang bertanggungjawab kepada Kalafiau.
Kabag Pengujian dan Pengembangan dibantu oleh :
a. Kepala Unit Pengujian dan Percobaan (Ka Unit Uji Coba) yang bertugas
melaksanakan percobaan-percobaan dalam rangka perbaikan dan
pengembangan formula obat jadi yang sudah ada, melaksanakan “In Process
Control” dalam setiap tahap produksi, melaksanakan pengujian terhadap
kualitas obat jadi yang dihasilkan oleh Unit Produksi Lafiau, melaksanakan
pemantauan terhadap kualitas bekkes (bekal kesehatan) yang disimpan di Unit
gudang Lafiau dan di satker (satuan kerja) kesehatan TNI AU.
b. Kepala Unit Penelitian dan Pengembangan (Ka Unit Litbang) yang bertugas
melaksanakan kegiatan seperti penelitian dan pengembangan formula-formula
pengembangan potensi yang dimiliki Lafiau, membantu unit produksi untuk
meneliti kerusakan hasil produksi dan memberikan sarana untuk
memperbaikinya dan menyimpan dan menguji “retain sample” sebagai
contoh pertinggal obat jadi yang diproduksi Lafiau.
c. Kepala Unit Pendidikan dan Latihan (Ka Unit Diklat) yang bertugas membuat
perencanaan serta melaksanakan penyelenggaraan pendidikan dan latihan.
3.4.6 Bagian Penunjangan
Bagian penunjangan adalah pembantu pelaksana Kalafiau yang dipimpin
oleh Kepala Bagian Penunjangan (Ka Bagjang) yang bertanggungjawab kepada
Kalafiau. Bagian Penunjangan bertugas mendukung kelancaran operasional
LAFIAU. Dalam pelaksanaan tugasnya Bagian Penunjangan dibantu oleh :
1) Kepala Unit Penunjangan Material (Ka Unit Jangmat) bertugas mendukung
kelancaran operasional produksi dan pembekalan serta pengujian dan
pengembangan
2) Kepala Unit Fasilitas dan Material (Ka Unit Harfasmat) bertugas
merencanakan dan menyelenggarakan pemeliharaan terhadap fasilitas dan
material dalam rangka mendukung kelancaran operasional Lafiau.
3.5 Sarana Dan Fasilitas Produksi 3.5.1 Bangunan
Bangunan di Lafiau terdiri atas bangunan untuk produksi, bangunan untuk
gudang, kantor, dan laboratorium. Bangunan untuk produksi dibagi lagi menjadi
tiga yaitu bangunan untuk produksi beta laktam, non beta laktam, dan
gudang bahan baku dan obat jadi dan gudang peralatan kesehatan. Bangunan
kantor memiliki ruang untuk kantor Kalafiau, ruang rapat, ruang administrasi,
ruang pendidikan, dan aula. Selain itu, Lafiau juga mempunyai bangunan untuk
kantin, ruang ganti, perpustakaan, koperasi, dan mushola.
Bangunan untuk produksi di Lafiau sesuai CPOB dipisahkan antara
bangunan produksi beta laktam dan non beta laktam, dengan tujuan untuk
mencegah kontaminasi silang antara produk beta laktam dan produk non beta
laktam, karena obat golongan ini dapat menyebabkan alergi.
Bangunan produksi dilengkapi dengan fasilitas pengendali udara yang
terdiri dari AC, dust collector baik lokal maupun terpusat, exhaust fun,
dehumidefier. Permukaan bagian dalam ruangan (dinding, lantai, dan langit -
langit) dibuat licin,
3.5.2 Ruang dan peralatan produksi a. Ruang produksi beta laktam
• Bagian-bagian ruang dan perlengkapan. Ruang produksi beta laktam terdiri dari ruang gudang produksi, ruang embalage, ruang timbang, ruang
isi kapsul, ruang striping, ruang hospital packing, ruang produk ruahan,
ruang pengisian sirup kering, ruang simpan alat dan ruang cuci.
• Peralatan. Ruang produksi beta laktam dilengkapi dengan peralatan penimbangan, mesin pencampur, mesin granulator, mesin cetak kaplet,
mesin pengisi kapsul, mesin pengisi sirup kering, oven double door dan
menempel pada pakaian sebelum masuk ke ruang produksi atau keluar dari
ruang produksi.
b. Ruang produksi non beta laktam
• Bagian-bagian ruang dan perlengkapan.
Ruang produksi non beta laktam terdiri dari gedung embalage, gedung
bahan baku, ruang antara, ruang timbang, ruang pencampuran dan granulasi,
ruang pengering, ruang bed dryer, ruang produk antara, ruang produk ruahan,
ruang stripping, ruang hospital packing, ruang produksi sirup, ruang produk
salep dan cream, ruang produk antiseptik, ruang pengisian kapsul, ruang cuci dan
penyimpanan alat.
• Peralatan.
Peralatan yang berada di ruang produksi non beta laktam adalah
timbangan dengan berbagai kapasitas, mesin pencampur serbuk stokes, mesin
granulator stokes, mesin pengering atau oven, mesin cetak kaplet, mesin penyalut
(Coating), mesin pengemas primer (Striping), alat pengukur kadar air fluid
bed dryer, mesin pengisi kapsul otomatis dan semi otomatis, mesin
penghitung (butch counter), deduster, mesin pengaduk dan pengisi salep atau
cream, alat pencampur dan pengisi cairan antiserptik, oven double door, mixer
tank, alat pengisi sirup
3.6 Kegiatan Lafiau
3.6.1 Pengelolaan Perbekalan Kesehatan
Perencanaan dan pengadaan perbekalan kesehatan di LAFIAU
Pusat Kesehatan TNI (Puskes). Perencanaan dan pengadaan perbekalan kesehatan
ini disusun berdasarkan kebutuhan dari satker - satker (satuan kerja) TNI AU.
Pengadaan perbekalan kesehatan dilakukan dengan sistem tender yang diikuti oleh
rekanan yang telah memenuhi persyaratan. Setelah pemenang tender ditentukan,
pengadaan barang dilaksanakan oleh rekanan berdasarkan kontrak jual beli.
Rekanan mengirimkan perbekalan kesehatan ke LAFIAU sesuai dengan kontrak
jual beli tersebut.
Perbekalan kesehatan yang dikirimkan ke LAFIAU oleh rekanan diterima
oleh Panitia Penerima Barang (PPB). Panitia Penerima Barang ditunjuk oleh
KALAFIAU dan diangkat oleh Kadiskesau. Panitia Penerima Barang bertugas
memeriksa perbekalan kesehatan yang diterima meliputi pemeriksaan keutuhan
kemasan, kebenaran identitas, jumlah yang diterima, kesesuaiannya dengan Surat
Pengantar Barang dan Surat Pesanan. Pada saat pemeriksaan barang juga dihadiri
oleh rekanan, sehingga jika ada perbekalan kesehatan yang tidak sesuai kualitas
dan kuantitasnya dapat dikembalikan ke rekanan dan digantikan dengan
perbekalan kesehatan yang sesuai. Untuk bahan baku dilakukan pemeriksaan
laboratorium oleh unit pengujian dan pengembangan untuk kesesuaian spesifikasi
berdasarkan persyaratan di pustaka seperti Farmakope Indonesia atau United
States Pharmacopeia.
Semua perbekalan kesehatan telah diperiksa dan memenuhi spesifikasi
serta sesuai dengan perjanjian, Panitia Penerima Barang akan mengeluarkan
Berita acara penerimaan kemudian diserahkan kepada bagian Minbekkes
yang bertugas memasukkan data barang yang diterima ke dalam kartu stok.
Laporan stok barang dilaporkan ke Diskesau setiap bulan dan setiap tiga bulan,
dengan tujuan untuk mengontrol jumlah barang dan untuk keperluan alokasi
setiap semester. Contoh berita acara penerimaan serta bentuk kartu stok barang
pada lampiran 1 dan 2.
Pengadaan obat jadi selain berasal dari Diskesau atau Puskes TNI, juga
dapat berasal dari produksi LAFIAU sendiri. Obat jadi ini juga diperiksa oleh
panitia penerima barang dan dibuatkan berita acara. Perbekalan kesehatan yang
diterima dari Diskesau atau Puskes TNI dan hasil produksi LAFIAU selanjutnya
disimpan di gudang obat jadi atau bahan baku untuk dialokasikan ke satker -
satker AU di seluruh Indonesia.
3.6.2 Bagian Gudang Pusat Farmasi
Gudang Pusat Farmasi (Gupusfi) merupakan pembantu pelaksana
KALAFIAU yang bertugas menerima, menyimpan, memelihara dan
mengeluarkan serta menghapuskan perbekalan kesehatan yang ada di LAFIAU.
Gupusfi dipimpin oleh Kepala Gudang yang bertanggung jawab kepada
KALAFIAU dalam melaksanakan tugasnya. Kepala Gudang dibantu oleh Unit
Gudang Transit, Unit Gudang Obat Jadi atau Bahan Baku atau embalage, Unit
Gudang Peralatan Kesehatan dan Unit Gudang Pengemasan. Bangunan tempat
perbekalan kesehatan terdiri dari empat gudang yaitu gudang transit, gudang obat
jadi atau bahan baku atau embalage, gudang peralatan kesehatan dan gudang
a. Penerimaan perbekalan kesehatan
Perbekalan kesehatan yang dibawa oleh rekanan diterima oleh Panitia
Penerima Barang dan disimpan di gudang transit untuk diperiksa. Barang yang
belum diperiksa atau dalam tahap pemeriksaan diberi label karantina oleh petugas
gudang transit. Label karantina ini berwarna kuning berisi nama barang, jumlah,
nomor batch atau nomor order, tanggal diterima, unit penerimaan, tanda tangan.
Barang yang diluluskan diberi label “diluluskan” berwarna hijau dan berisi nama
barang, tanggal diterima, jumlah, pembuat/penyalur, nomor batch asal dan data
yang diisi oleh Unit Uji Coba (tanggal tes, nomor lot, tanda tangan dan tanggal
kadaluarsa), sedangkan barang yang ditolak diberi label “ditolak” yang berwarna
merah dan berisi nama barang, jumlah, nomor batch/nomor order, tanggal
diterima dan tanda tangan bagian uji coba.
Bahan baku atau kemasan dianalisis oleh Unit ujibang setelah menerima
Surat Pengiriman contoh bahan baku atau kemasan. Unit Uji Coba bertugas
memberikan persetujuan atau penolakan terhadap bahan baku atau kemasan
berdasarkan hasil analisis. Bahan baku atau kemasan yang diluluskan, Unit Uji
Coba akan merobek label “karantina”, menempelkan label “diluluskan” yang
berwarna hijau dan ditempatkan di daerah yang diluluskan. Bahan baku atau
kemasan yang ditolak, Unit Uji Coba akan merobek label “karantina” dan
menempelkan label “ditolak” yang berwarna merah serta menempatkan di daerah
ditolak. Khusus bahan baku dan kemasan yang ditolak, Unit Uji Coba harus