LAPORAN PRAKTEK KERJA PROFESI FARMASI INDUSTRI
di
LEMBAGA FARMASI DIREKTORAT KESEHATAN
ANGKATAN DARAT
BANDUNG
Disusun Oleh:
Faizah Nurlida Sari, R, S. Farm. 073202027
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadiran Tuhan Yang Maha Esa yang
telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan
Praktek Kerja Profesi dan laporan ini di Lembaga Farmasi Direktorat Kesehatan
Angkatan Darat (Lafi Ditkesad) Bandung.
Praktek Kerja Profesi ini telah memperluas wawasan penulis tentang
gambaran peranan apoteker dalam Industri Farmasi. Praktek Kerja Profesi ini
tidak lepas dari bantuan berbagai pihak. Pada kesempatan ini penulis
mengucapkan rasa terima kasih kepada:
1. Bapak Kolonel CKM Drs. I Made Sudjana, Apt, MM, selaku Kepala
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat, Bapak Mayor
CKM. Drs Junaedi, Apt, selaku Kepala Seksi Sediaan Cair Sediaan Steril
Instalasi Produksi Lembaga Farmasi Direktorat Kesehatan Angkatan
Darat sebagai pembimbing Praktek kerja profesi, beserta seluruh staf dan
karyawan Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
2. Bapak Prof. Dr. Sumadio Hadisahputra, Apt, selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara Bapak Drs. Wiryanto, M.S, Apt.,
sebagai koordinator Program Pendidikan Profesi Apoteker Fakultas
Farmasi Universitas Sumatera Utara dan seluruh Stafr Pegawai Fakultas
Farmasi Universitas Sumatera Utara.
Semoga Tuhan Yang Maha Esa membalas budi baik Bapak dan Ibu dengan
belasan yang berlipat ganda. Penulis berharap semoga tulisan ini dapat
memberikan manfaat bagi kita semua.
Bandung, Maret 2010
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR... iii
DAFTAR ISI ... iv
1.2. Tujuan Praktek Kerja Profesi Apoteker ... 3
BAB II TINJAUAN UMUM INDUSTRI FARMASI ... 4
2.1. Perkembangan Lafi Ditkesad ... 4
2.2. Cara Pembuatan Obat yang Baik ... 5
2.2.1. Manajemen Mutu ... 5
2.2.2. Personalia ... 6
2.2.3. Bangunan dan Fasilitas... 6
2.2.4. Peralatan ... 7
2.2.5. Sanitasi dan Higiene ... 8
2.2.6. Produksi... 8
2.2.7. Pengawasan Mutu... 15
2.2.8. Inspeksi Diri ... 15
2.2.9. Penanganan Keluhan Terhadap Obat, Penarikan Kembali Obat dan Obat Kembalian ... 16
2.2.10. Dokumentasi... 18
BAB III KEGIATAN LAFI DITKESAD ... 19
3.1. Peranan dan Pengadaan Barang ... 19
3.2. Kegiatan Instalasi Pengawasan Mutu ... 20
3.4. Kegiatan Instalasi Produksi... 21
3.4.1. Seksi Sediaan Padat... 21
3.4.2. Seksi Sediaan Cair / Steril ... 28
3.4.3. Seksi Sediaan Khusus... 31
3.4.4. Seksi Kemas ... 32
3.5. Kegiatan Instalasi Simpan... 33
3.6. Fasilitas Pendukung / Utility... 34
3.7. Penanganan Limbah... 36
BAB V PEMBAHASAN ... 41
BAB V KESIMPULAN DAN SARAN ... 45
5.1. Kesimpulan ... 45
5.2. Saran ... 45
DAFTAR PUSTAKA... 47
LAMPIRAN ... 48
DAFTAR TABEL
Halaman
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Struktur Organisasi Lafi Ditkesed... 48
Lampiran 2. Blanko Catatan Pengujian Laboratorium ... 49
Lampiran 3. Blangko Hasil Pengujian Tablet dan Kapsul... 50
Lampiran 4. Alur Proses Produksi Tablet... 51
Lampiran 5. Alur Proses Produksi Kapsul... 52
Lampiran 6. Alur Proses Produksi Sirup Kering ... 53
Lampiran 7. Alur Proses Produksi Salep ... 54
Lampiran 8. Alur Proses Produksi Sirup Basah... 55
RINGKASAN
Telah selesai dilakukan Praktek Kerja Profesi (PKP) di Lembaga
Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) Bandung. PKP ini
dilaksanakan dalam upaya memberikan gambaran peranan apoteker industri
farmasi dan melihat Cara Pembuatan Obat yang Baik (CPOB). PKP dilaksanakan
pada tanggal 3-28 Maret 2008. Kegiatan PKP di industri farmasi Lembaga
Farmasi Direktorat Kesehatan Angkatan Darat (Lafiu Ditkesad) Bandung,
meliputi: tinjauan ke bagian produksi beta laktam dan nonbeta laktam, rancang
bangunan dan fasilitas yang sudah disertifikasi CPOB, pengawasan mutu obat
yang produksi, manajemen persediaan, pengembangan produk dan pengolahan
RINGKASAN
Telah selesai dilakukan Praktek Kerja Profesi (PKP) di Lembaga
Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) Bandung. PKP ini
dilaksanakan dalam upaya memberikan gambaran peranan apoteker industri
farmasi dan melihat Cara Pembuatan Obat yang Baik (CPOB). PKP dilaksanakan
pada tanggal 3-28 Maret 2008. Kegiatan PKP di industri farmasi Lembaga
Farmasi Direktorat Kesehatan Angkatan Darat (Lafiu Ditkesad) Bandung,
meliputi: tinjauan ke bagian produksi beta laktam dan nonbeta laktam, rancang
bangunan dan fasilitas yang sudah disertifikasi CPOB, pengawasan mutu obat
yang produksi, manajemen persediaan, pengembangan produk dan pengolahan
BAB I PENDAHULUAN
1.1 Latar Belakang
Kesehatan merupakan hak azasi manusia, setiap orang mempunyai hak
untuk hidup layak baik dalam kesehatan pribadi maupun keluarganya termasuk di
dalamnya mendapatkan makanan, pakaian, perumahan, dan pelayanan kesehatan
serta pelayanan sosial lain yang diperlukan. Pelayanan kesehatan sebagai salah
satu unsur kesejahteraan umum harus diwujudkan sesuai dengan cita - cita bangsa
Indonesia melalui pembangunan nasional yang berkesinambungan. Untuk
mewujudkan masyarakat Indonesia yang sehat, maka usaha – usaha di bidang
pengobatan dan pelayanan kesehatan perlu ditingkatkan secara terus – menerus.
Tercapainya derajat kesehatan yang optimal harus ditunjang oleh faktor
tersedianya obat yang dapat memenuhi kebutuhan masyarakat dengan harga
terjangkau, berkhasiat, bermutu dan aman digunakan.
Salah satu sarana pelayanan kesehatan untuk melayani kebutuhan akan obat
adalah industri farmasi yang terdiri dari industri bahan baku dan industri bahan
jadi. Industri obat jadi merupakan industri yang menghasilkan suatu produk obat
yang telah melalui seluruh tahap proses pembuatan, sedangkan industri bahan
baku merupakan industri yang memproduksi bahan baku dimana bahan baku
tersebut adalah seluruh bahan, baik bahan berkhasiat atau tidak berkhasiat yang
digunakan dalam proses pengolahan obat. Industri farmasi merupakan tempat
dimana apoteker melakukan pekerjaan kefarmasian terutama menyangkut
dan pengembangan obat. Industri farmasi merupakan gabungan yang kompleks
yang terdiri dari orang–orang yang saling bergantungan dalam profesi,
perdagangan, perusahaan, dan organisasi. Masing – masing terikat pada aktifitas
penyediaan kebutuhan obat secara nasional. Dalam pengertian luas, industri
farmasi meliputi semua orang terlibat atau dibutuhkan, mulai dari obat itu
dirancang oleh seorang ahli sampai obat berada di tangan pasien. Sedangkan
untuk pengertian sempit, industri farmasi sering diartikan dengan riset
obat–obatan dan perusahaan–perusahaan atau industri farmasi yang menyediakan
obat untuk diracik atau dalam bentuk obat siap pakai oleh pasien.
Sasaran utama industri farmasi adalah memproduksi obat jadi dengan
mengutamakan keamanan, keefektifan, kualitas dan harga yang terjangkau oleh
masyarakat. Untuk menghasilkan obat jadi yang memenuhi persyaratan yang
telah ditetapkan sesuai dengan tujuan penggunaannya, setiap industri farmasi
harus menerapkan CPOB (Cara Pembuatan Obat yang Baik).
Salah satu aspek CPOB adalah personil yang memiliki pengetahuan dan
keterampilan yang cukup untuk melaksanakan tugas dan tanggung jawabnya di
industri farmasi. Apoteker sebagai personil yang profesional harus memahami
penerapan CPOB disamping adanya pengetahuan dan keterampilan, baik yang
berhubungan dengan kefarmasian ataupun kepemimpinan.
Sebagai upaya untuk memberikan wawasan yang luas tentang industri
farmasi bagi calon apoteker, maka Fakultas Farmasi Universitas Sumatera Utara
Medan bekerja sama dengan Lembaga Farmasi Direktorat Kesehatan Angkatan
untuk mengenal lingkungan kerja dan memperluas pengetahuan tentang industri
farmasi melalui program Praktek Kerja Profesi Apoteker yang dilaksanakan dari
tanggal 3-28 Maret 2008.
1.2 Tujuan Praktek Kerja Profesi Apoteker
a. Mengetahui gambaran umum tentang kegiatan di suatu industri farmasi
terutama di Lafi Ditkesad Bandung yang berhubungan dengan bagian
produksi, pengawasan mutu, serta bidang penelitian dan pengembangan
sesuai dengan CPOB
b. Mengetahui aspek–aspek CPOB dalam suatu industri farmasi
c. Mempersiapkan para calon apoteker untuk menjalankan profesinya secara
profesional, mandiri serta mampu menghadapi tantangan di sektor industri
BAB II
TINJAUAN UMUM INDUSTRI FARMASI
2.1 Perkembangan Lafi Ditkesad
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad)
merupakan lembaga yang telah ada sejak zaman penjajahan Belanda. Pada saat
itu pemerintah Belanda mendirikan sebuah lembaga yang dinamakan Militaire
Scheikundig Laboratorium (MSL). Lembaga ini berfungsi sebagai tempat
pemeriksaan obat-obat kebutuhan tentara Belanda. Setelah zaman kemerdekaan
lembaga ini diambil alih oleh pemerintah Republik Indonesia dan mengalami
beberapa kali penggantian nama dan perubahan fungsi, hingga pada tahun 1985
dilakukan reorganisasi dari lembaga tersebut menjadi Lafi Ditkesad.
Sebagai lembaga yang bertanggung jawab untuk menyediakan obat-obatan
bagi Angkatan Darat, Lafi Ditkesad memiliki visi menjadi salah satu lembaga
produksi yang mampu memenuhi kebutuhan obat bermutu dan aman bagi prajurit
dan PNS Angkatan Darat serta keluarganya. Seperti halnya dengan lembaga
pemerintah lain, Lafi Ditkesad juga mempunyai misi yaitu :
1) Memberikan jasa informasi yang terbaik terhadap penggunaan obat (Rational
Use of Drugs).
2) Membantu fungsi pelayanan kesehatan atas ketersediaan obat/produk
kesehatan lainnya untuk prajurit dan PNS Angkatan Darat serta keluarganya.
3) Terlibat secara aktif dalam fungsi dukungan kesehatan pada penggunaan
4) Memanfaatkan kapasitas atau kemampuan produksi untuk kepentingan
strategis.
2.2 Cara Pembuatan Obat yang Baik
Pedoman CPOB bertujuan untuk menghasilkan produk obat yang
senantiasa memenuhi persyaratan mutu yang telah ditetapkan sesuai dengan
tujuan penggunaannya.
Obat yang berkualitas adalah obat jadi yang benar-benar dijamin bahwa
obat tersebut :
a. Mempunyai potensi atau kekuatan untuk dapat digunakan sesuai
tujuannya.
b. Memenuhi persyaratan keseragaman, baik isi maupun bobot.
c. Memenuhi syarat kemurnian.
d. Memiliki identitas dan penandaan yang jelas dan benar.
e. Dikemas dalam kemasan yang sesuai dan terlindung dari kerusakan dan
kontaminasi.
f. Penampilan baik, bebas dari cacat atau rusak.
2.2.1 Manajemen mutu
Unsur dasar manajemen mutu adalah:
a. Suatu infrastruktur atau sistem mutu yang tepat mencakup struktur
organisasi, prosedur, dan sumber daya.
b. Tindakan sistematis diperlukan untuk mendapatkan kepastian dengan
pelayanan) yang dihasilkan akan selalu memenuhi persyaratan yang
telah ditetapkan. Keseluruhan tindakan tersebut disebut Pemastian
Mutu.
2.2.2 Personalia
Jumlah personil pada tiap tingkatan harus memadai dan memiliki
pengetahuan, keterampilan serta kemampuan sesuai dengan tugasnya. Personil
juga harus memiliki kesehatan mental dan fisik yang baik, sehingga mampu
melakukan tugasnya secara profesional, memiliki sifat dan kesadaran yang tinggi
untuk mewujudkan CPOB.
2.2.3 Bangunan dan Fasilitas
Bangunan untuk pembuatan obat hendaklah memiliki ukuran dan rancang
bangun konstruksi serta letak yang memadai agar memudahkan dalam
pelaksanaan kerja, pembersihan dan pemeliharaan yang baik.
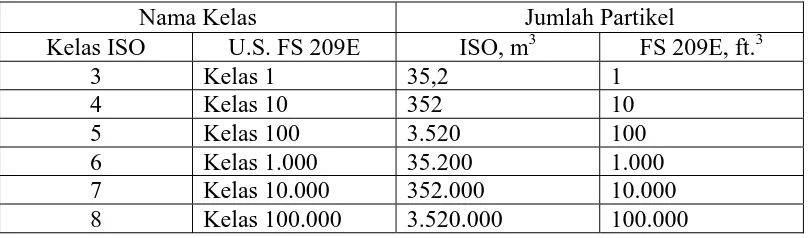
Menurut International Standardization Organization (ISO14644 ), jumlah
partikel di udara ruangan dapat dilihat pada tabel di bawah ini.
Tabel 1. Pembagian kelas ruangan menurut ISO dan U.S FS 209E
Nama Kelas Jumlah Partikel
Kelas ISO U.S. FS 209E ISO, m3 FS 209E, ft.3
3 Kelas 1 35,2 1
4 Kelas 10 352 10
5 Kelas 100 3.520 100
6 Kelas 1.000 35.200 1.000
7 Kelas 10.000 352.000 10.000
2.2.4 Peralatan
Peralatan yang digunakan dalam pembuatan obat hendaklah memiliki
rancang bangun dan konstruksi yang tepat, ukuran yang memadai serta
ditempatkan dengan tepat, sehingga mutu yang dirancang bagi tiap produk obat
terjamin secara seragam dari bets ke bets, serta untuk memudahkan pembersihan
dan perawatannya.
Rancang bangun dan konstruksi peralatan hendaklah memenuhi
persyaratan-persyaratan berikut:
1) Permukaan peralatan yang bersentuhan dengan bahan baku, produk
antara, produk ruahan atau produk jadi tidak boleh bereaksi, mengadisi
atau mengabsorbsi, yang dapat mengubah identitas, mutu atau
kemurniannya di luar batas yang ditentukan.
2) Peralatan yang digunakan untuk menimbang, mengukur, menguji dan
mencatat hendaklah diperiksa ketelitiannya secara teratur serta dikalibrasi
menurut suatu program dan prosedur yang tepat.
3) Peralatan hendaklah dapat dibersihkan dengan mudah baik bagian dalam
maupun bagian luar.
4) Bahan-bahan yang diperlukan untuk suatu tujuan khusus seperti pelumas
atau pendingin, tidak boleh bersentuhan langsung dengan bahan yang
diolah karena hal ini dapat merubah identitas, mutu atau kemurnian bahan
baku, bahan antara, produk ruahan atau obat jadi.
5) Semua peralatan yang dipakai dalam pengolahan bahan kimia yang
yang mudah terbakar, hendaklah dilengkapi dengan perlengkapan elektris
yang kedap eksplosi.
6) Penyaring untuk cairan tidak boleh melepaskan serat ke dalam produk.
Penyaring yang mengandung asbes tidak boleh digunakan walaupun
penyaring khusus yang tidak melepas serat digunakan sesudahnya.
2.2.5 Sanitasi dan Higiene
Tingkat sanitasi dan higiene yang tinggi hendaklah diterapkan pada setiap
aspek pembuatan obat. Ruang lingkup sanitasi dan higiene meliputi personalia,
bangunan, peralatan dan perlengkapan, bahan produksi serta wadahnya dan setiap
hal yang dapat menjadi sumber pencemaran produk.
2.2.6 Produksi
Produksi harus dilaksanakan mengikuti prosedur yang telah ditetapkan
sehingga menjamin obat yang dihasilkan sesuai dengan spesifikasi yang telah
ditentukan.
a. Bahan awal
1) Setiap bahan awal, sebelum dinyatakan lulus untuk digunakan, harus
memenuhi spesifikasi bahan awal yang sudah ditetapkan dan diberi label
dengan nama yang dinyatakan dalam spesifikasi.
2) Setiap penerimaan bahan awal hendaklah dilakukan pemeriksaan secara
visual tentang kondisi umum, keutuhan kemasan, kebocoran dan
kerusakan, serta contoh untuk pengujian diambil oleh petugas dengan
menggunakan metode yang telah disetujui oleh manajer pengawasan
3) Bahan awal yang baru tiba, harus dikarantina, sampai disetujui dan
diluluskan untuk digunakan oleh penanggung jawab pengawasan mutu.
4) Label yang menunjukkan status bahan awal hanya boleh dipasang oleh
petugas yang ditunjuk oleh penanggung jawab bagian pengawasan mutu.
5) Semua bahan awal yang tidak memenuhi syarat hendaklah ditandai secara
jelas, tersimpan terpisah dan secepatnya dimusnahkan atau dikembalikan
kepada pemasok.
b. Validasi proses
1) Semua prosedur produksi hendaklah divalidasi dengan tepat.
2) Perubahan yang berarti dalam proses, peralatan atau bahan hendaklah
disertai dengan tindakan validasi ulang.
c. Pencemaran
Pencemaran kimiawi atau mikroba terhadap suatu obat yang dapat
merugikan kesehatan, mengurangi daya terapeutik atau mempengaruhi
kualitas suatu produk tidak dapat diterima. Perhatian khusus harus diberikan
pada masalah pencemaran silang, karena sekalipun sifat dan tingkatannya
tidak berpengaruh langsung pada kesehatan, hal ini menunjukkan pelaksanaan
pembuatan obat yang tidak sesuai dengan CPOB.
a. Sistem penomoran bets dan lot.
1) Sistem yang menjabarkan cara penomoran bets dan lot secara rinci
diperlukan, untuk memastikan bahwa produk antara, produk ruahan atau
obat jadi suatu bets atau lot dapat dikenali dengan nomor bets atau lot
2) Sistem penomoran bets atau lot harus menjamin bahwa nomor bets atau
lot yang sama tidak digunakan secara berulang.
b. Penimbangan dan penyerahan
1) Bahan baku, bahan pengemas, produk antara dan produk ruahan yang
boleh diserahkan hanyalah yang telah diluluskan oleh bagian pengawasan
mutu.
2) Sebelum dilakukan penimbangan hendaklah dilakukan pemeriksaan
terhadap kebenaran penandaan bahan baku termasuk label pelulusan dari
bagian pengawasan mutu.
3) Setiap penimbangan atau pengukuran hendaknya dilakukan pembuktian
kebenaran, ketepatan identitas, dan jumlah bahan yang ditimbang dan
diukur oleh dua petugas secara terpisah.
4) Bahan baku, produk antara, dan produk ruahan hendaknya diperiksa ulang
kebenarannya dan ditandatangani oleh supervisor produksi sebelum
diserahkan ke bagian produksi.
c. Pengembalian
1) Semua bahan baku, bahan pengemas, produk antara dan produk ruahan
yang dikembalikan ke tempat penyimpanan hendaklah didokumentasikan.
2) Bahan baku, bahan pengemas, produk antara dan produk ruahan tidak
boleh dikembalikan ke gudang kecuali bila memenuhi spesifikasi yang
d. Pengolahan
1) Semua bahan yang dipakai dalam pengolahan hendaklah diperiksa
terlebih dahulu sebelum digunakan.
2) Kondisi daerah pengolahan hendaklah dipantau dan dikendalikan sampai
tingkat yang disyaratkan untuk kegiatan yang akan dilakukan.
3) Semua peralatan yang digunakan dalam pengolahan hendaklah diperiksa
sebelum digunakan.
4) Semua kegiatan pengolahan hendaklah dilaksanakan mengikuti prosedur
tertulis yang telah ditentukan.
5) Semua produk antara atau produk ruahan harus diberi label yang tepat dan
dikarantina sampai diluluskan oleh bagian pengawasan mutu.
e. Produk steril
1) Cara produksi ada dua kategori yaitu aseptis dan sterilisasi akhir.
2) Semua produk steril dibuat dengan kondisi terkendali dan dipantau
dengan teliti serta diperlukan tindakan khusus untuk meyakinkan sterilitas
produk steril yang dibuat.
3) Untuk membuat produk steril diperlukan ruang terpisah yang dirancang
khusus.
4) Pembuatan produk steril memerlukan tiga kualitas ruangan yang berbeda,
yakni: ruang ganti pakaian, ruang bersih untuk persiapan komponen dan
penyiapan larutan dan ruangan steril untuk kegiatan steril
6) Personil yang bekerja dipilih dengan seksama dan harus memperhatikan
standar higiene dan kebersihan perorangan serta mendapatkan pelatihan
sesuai dengan bidangnya.
7) Personil memakai pakaian khusus untuk daerah bersih dan steril serta
ditangani secara terpisah pemakaian dan pencuciannya. Arloji, perhiasan
dan kosmetik tidak boleh dipakai dalam ruangan bersih dan steril.
8) Bangunan untuk ruangan steril dirancang khusus, diberi aliran udara
bertekanan positif secara efektif melalui saringan. Permukaan ruangan
harus kedap air dan tidak retak. Tidak boleh ada bagian yang dapat
menjadi tempat penumpukan debu. Pipa–pipa dipasang dengan tepat dan
saluran pembuangan dipasang terpisah serta tidak boleh ada bak
pencucian.
9) Peralatan dirancang dan dipasang dengan tepat dan mudah dibersihkan.
10) Pengolahan bahan awal dan produk hendaklah dihindari dari pencemaran
jasad renik, baik sebelum dan sesudah sterilisasi. Wadah, pembersih,
jarak waktu sterilisasi, pembuatan larutan dan sumber air selalu dipantau
dengan baik.
11) Sterilisasi dapat dilakukan dengan cara panas basah, panas kering, saring,
etilen oksida atau radiasi sesuai dengan masing-masing cara yang efektif.
f. Pengemasan
1) Kegiatan pengemasan berfungsi untuk membagi-bagi dan mengemas
dilaksanakan di bawah pengawasan ketat untuk menjaga identitas,
keutuhan dan kualitas barang yang sudah dikemas.
2) Sebelum kegiatan pengemasan dimulai hendaklah dilakukan pemeriksaan
untuk memastikan bahwa peralatan dan ruang kerja dalam keadaan bersih
dan bebas dari produk, sisa produk lain atau dokumen yang tidak
diperlukan untuk kegiatan yang dilakukan.
3) Setiap penyerahan produk ruahan dan bahan pengemas hendaklah
diperiksa dan diteliti kesesuaiannya dengan prosedur pengemasan induk
atau perintah pengemasan khusus.
g. Bahan atau produk pulihan
Bahan atau produk dapat diolah ulang atau dipulihkan dengan syarat
bahan atau produk tersebut layak untuk diolah ulang melalui prosedur tertentu
yang disahkan, serta hasilnya masih memenuhi persyaratan spesifikasi yang
ditentukan dan tidak terjadi perubahan berarti terhadap mutunya.
h. Obat kembalian
1) Obat jadi yang dikembalikan dari gudang pabrik misalnya karena label
atau kemasan luar yang kotor dapat diberi label kembali dan harus
hati-hati untuk menghindari campur baur dengan produk lain atau terjadinya
kesalahan pemberian label.
2) Obat jadi yang dikembalikan dari peredaran dan sudah lepas dari
pengawasan pabrik pembuat, setelah dievaluasi secara kritis oleh petugas
pengawasan mutu dan ternyata memenuhi standar, spesifikasi dan
kembali, diberi label kembali atau diolah ulang ke bets berikutnya.
Bilamana ada keraguan terhadap mutu, produk ini tidak boleh
dipertimbangkan untuk didistribusikan kembali atau diolah ulang.
i. Karantina obat jadi merupakan titik akhir pengawasan sebelum obat jadi
diserahkan ke gudang dan siap untuk didistribusikan.
j. Pengawasan distribusi obat jadi
1) Sistem distribusi hendaklah dirancang dengan tepat sehingga menjamin
bahwa obat jadi yang pertama masuk didistribusikan terlebih dahulu.
2) Sistem tersebut mencakup pula cara pencatatan yang tepat sehingga
distribusi tiap bets dapat segera diketahui untuk mempermudah
penyelidikan dan penarikan kembali jika diperlukan.
3) Prosedur tertulis mengenai distribusi obat hendaklah dibuat dan dipatuhi.
4) Penyimpangan terhadap prinsip pertama masuk pertama keluar hanya
diperbolehkan untuk jangka waktu pendek dan hanya atas persetujuan
pimpinan yang bertanggungjawab.
n. Penyimpanan bahan awal, produk antara, produk ruahan dan obat jadi
Semua bahan hendaklah disimpan secara rapi dan teratur untuk mencegah
resiko tercampur baur atau pencemaran serta memudahkan pemeriksaan
dan pemeliharaan.
o. Pembuatan obat berdasarkan kontrak
1) Pembuatan obat berdasarkan kontrak berarti pembuatan sebagian atau
penerima kontrak) untuk kepentingan pihak lain (disebut pemberi
kontrak).
2) Pemberi kontrak hendaklah memastikan bahwa penerima kontrak telah
memiliki izin operasional dan sertifikat CPOB yang sesuai dengan bentuk
sediaan obat yang akan dikontrakkan.
2.2.7 Pengawasan Mutu
Pengawasan mutu adalah bagian yang esensial dari cara pembuatan obat
yang baik untuk memastikan tiap obat yang dibuat senantiasa memenuhi
persyaratan mutu yang sesuai dengan tujuan penggunaannya.
2.2.8 Inspeksi Diri
Inspeksi diri bertujuan untuk melakukan penilaian apakah seluruh aspek
produksi dan pengendalian mutu selalu memenuhi CPOB. Program inspeksi diri
dirancang untuk mencari kelemahan dalam pelaksanaan CPOB dan untuk
menetapkan tindakan perbaikannya. Inspeksi diri harus dilakukan secara teratur
dan dibuat prosedur serta pencatatannya. Tindakan perbaikan yang disarankan
sebaiknya dilaksanakan. Untuk pelaksanaan inspeksi diri ditunjuk tim yang
mampu menilai secara objektif pelaksanaan CPOB.
Hal-hal yang diinspeksi meliputi karyawan, bangunan termasuk fasilitas
untuk karyawan, penyimpanan bahan awal dan obat jadi, peralatan, produksi,
2.2.9 Penanganan Keluhan Terhadap Obat, Penarikan Kembali Obat, dan Obat Kembalian
a. Keluhan dan Laporan
Keluhan dan laporan dapat menyangkut kualitas, efek samping yang
merugikan, dan masalah medis lainnya. Keluhan dan laporan ditangani
secara:
1) Hendaklah dibuat catatan tertulis mengenai semua keluhan dan laporan
yang diterima.
2) Keluhan dan laporan hendaklah ditangani oleh bagian yang bersangkutan
sesuai dengan jenis keluhan dan laporan yang diterima.
3) Terhadap tiap keluhan dan laporan dilakukan penelitian dan evaluasi
secara seksama, termasuk meninjau seluruh informasi yang masuk tentang
pemeriksaan atau pengujian terhadap contoh yang diterima. Bila perlu
dilakukan pemeriksaan terhadap contoh pertinggal bets yang bersangkutan
dan meneliti kembali semua data serta dokumentasi yang berkaitan.
Tindak lanjut terhadap keluhan dan laporan:
a) Tindakan perbaikan yang diperlukan termasuk penarikan kembali bets
obat jadi atau seluruh obat jadi yang bersangkutan dan tindak lanjut
lainnya yang sesuai.
b) Hasil pelaksanaan penanganan keluhan dan laporan termasuk evaluasi
penelitian dan tindak lanjut yang diambil hendaklah dicatat dan
dilaporkan kepada bagian yang bersangkutan dan kepada pejabat
b. Penarikan Kembali Obat Jadi
Penarikan kembali obat jadi dapat berupa penarikan kembali satu atau
beberapa bets atau seluruh obat jadi tertentu dari semua mata rantai distribusi.
Penarikan kembali dilakukan apabila ditemukan adanya produk yang tidak
memenuhi persyaratan kualitas atau atas dasar pertimbangan adanya efek
samping yang tidak diperhitungkan yang merugikan kesehatan.
Penarikan kembali dapat dilakukan atas prakarsa produsen sendiri atau
instruksi instansi pemerintah yang berwenang. Keputusan untuk melakukan
penarikan kembali obat jadi adalah tanggung jawab apoteker penanggung
jawab pabrik dan pimpinan perusahaan. Penarikan kembali obat jadi dapat
pula sekaligus merupakan penghentian pembuatan obat jadi yang
bersangkutan.
c. Obat Kembalian
Obat kembalian adalah obat jadi yang telah beredar dan kemudian
dikembalikan ke produsen karena adanya keluhan kadaluarsa, masalah
keabsahan, atau sebab lain mengenai kondisi obat, wadah, atau kemasan
sehingga menimbulkan keraguan akan keamanan, identitas, kualitas, dan
kuantitas obat jadi yang bersangkutan.
Pabrik hendaklah membuat prosedur untuk menahan, menyelidiki, dan
menganalisis obat yang dikembalikan, serta menetapkan apakah obat tersebut
dapat diproses kembali atau harus dimusnahkan. Terhadap obat kembalian
dilakukan evaluasi yang seksama untuk menentukan apakah obat jadi yang
2.2.10 Dokumentasi
Dokumentasi pembuatan obat merupakan bagian dari sistem informasi
manajemen yang meliputi spesifikasi bahan baku dan produk, prosedur, metode
dan instruksi, perencanaan, pelaksanaan, pembersihan, pemeliharaan,
penyimpanan dan distribusi, pengendalian serta evaluasi seluruh rangkaian
BAB III
KEGIATAN LAFI DITKESAD
Kegiatan Lafi Ditkesad dalam melaksanakan tugas dan fungsi produksi
obat-obatan meliputi perencanaan dan pengadaan barang, penyimpanan barang,
proses produksi, pengawasan mutu, penelitian dan pengembangan, pemeliharaan
dan kegiatan administrasi.
3.1 Perencanaan dan Pengadaan Barang
Perencanaan dan pengadaan barang untuk produksi obat Lafi Ditkesad
dilakukan berdasarkan data dari Sub Direktorat Pembinaan Pelayanan Kesehatan
(Subditbinyankes) yang disusun berdasarkan masukan pola penyakit dari daerah
dan laporan dari masing-masing Kesehatan Daerah Militer (Kesdam), Satuan
Kesehatan (Satkes) dan Rumah Sakit Pusat Angkatan Darat (RSPAD). Rencana
pengadaan obat kemudian dibuat dengan melakukan penyesuaian antara daftar
kebutuhan obat dengan anggaran yang tersedia dan selanjutnya dianalisa dan
dievaluasi oleh Subditbinyankes yang dilakukan setahun sebelum pelaksanaan.
Bagminlog membuat rencana kebutuhan produksi obat Lafi Ditkesad yang
terdiri dari rencana kebutuhan bahan aktif, bahan pembantu dan bahan pengemas
(embalage) dan kebutuhan reagensia untuk kebutuhan Instal Wastu. Perencanaan
tersebut disusun berdasarkan formula dan spesifikasi obat yang telah ditentukan
oleh Lafi Ditkesad, disamping itu Bagminlog juga menyusun rencana dan
anggaran untuk pemeliharaan sarana operasional yang digunakan di tiap bidang
Pengadaan barang dilakukan oleh Ditkesad kemudian dikirim ke Gudang
Pusat II disertai dengan surat Perintah Penerimaan Material (PPnM), selanjutnya
tim komisi penerimaan barang yang dibentuk oleh Dirkesad memeriksa keadaan
barang secara administrasi, fisika dan kimia, yang mana pemeriksaan mutu
dilaksanakan oleh Instalasi Wastu. Setelah barang lulus uji mutu maka dibuatkan
Laporan Hasil Pengujian (LHP) dan Berita Acara (BA) Penerimaan Material, lalu
barang disimpan di Gudang Pusat II, untuk barang yang tidak memenuhi
spesifikasi akan ditolak dan dikembalikan kepada pemasok.
Penyimpanan barang di Lafi Ditkesad dilaksanakan oleh Instalasi Simpan,
setelah dikeluarkannya Perintah Pengeluaran Material (PPM) oleh Dirkesad.
Barang-barang yang berkaitan dengan semua proses kerja yang berlangsung di
Lafi Ditkesad, baik produksi, pengawasan mutu, pengemasan, administrasi,
maupun proses pendukung pengeluarannya melalui Instalasi Simpan.
Barang-barang di gudang tersebut disimpan berdasarkan jenis, sifat atau
keadaan bahan dan pengeluarannya sesuai dengan sistem First In First Out
(FIFO), First Expired First Out (FEFO) dan First Unstable First Out (FUFO).
3.2 Kegiatan Instalasi Pengawasan Mutu (Instal Wastu)
Pengawasan mutu merupakan bagian integral dari suatu produksi obat.
Instal Wastu bertanggung jawab terhadap setiap hal yang menyangkut kualitas
bahan baku obat, bahan pembantu, bahan pengemas, produk antara, produk
ruahan, dan obat jadi yang dihasilkan sampai dengan pemantauan kualitas setelah
didistribusikan (dengan standar waktu kadaluarsa). Instal Wastu juga bertanggung
dan peralatan serta fasilitas penunjang lainnya seperti pemeriksaan kualitas udara,
pengendalian mutu air dan pemeriksaan limbah. Pelaksanaan kegiatan di Instal
Wastu ditunjang oleh fasilitas instrumen HPLC, spektrofotometer dengan sistem
terkomputerisasi, Laminar Air Flow, Read Biotic (pembaca hambatan bakteri),
Climatic Chamber, Dissolution Tester serta berbagai fasilitas penunjang lainnya.
3.3 Kegiatan Instalasi Penelitian dan Pengembangan (Instal Litbang)
Dalam menjalankan tugasnya Instal Litbang melakukan penelitian terhadap
produk baru dan pengembangan produk lama untuk memperoleh kualitas yang
lebih baik. Pelaksanaan kegiatan dimulai dengan pengajuan rencana penelitian
dan pengembangan produk Lafi Ditkesad.
3.4 Kegiatan Instalasi Produksi (Instal Prod)
Kegiatan produksi obat-obatan dilaksanakan oleh Instalasi Produksi yang
meliputi perencanaan, pengaturan, pelaksanaan dan pengendalian. Produk yang
dihasilkan oleh Lafi Ditkesad berupa produk beta laktam dan produk non
betalaktam. Pada Instalasi Produksi terdapat empat seksi yaitu: seksi sediaan
padat, seksi sediaan cair/steril, seksi sediaan khusus dan seksi kemas.
Masing-masing seksi dikepalai oleh seorang Kepala Seksi (Apoteker).
Obat-obat yang diproduksi oleh Lafi Ditkesad tidak diperdagangkan bagi
masyarakat umum, sehingga tidak memiliki nomor registrasi yang didaftarkan di
Badan POM, namun demikian proses produksinya tetap dilaksanakan sesuai
dengan Pedoman CPOB yang dikeluarkan oleh Badan POM.
Rencana produksi dibuat berdasarkan pada banyaknya jenis obat yang
Seluruh proses produksi yang dilaksanakan, dicatat dan didokumentasikan
dalam Catatan Pengolahan dan Pengemasan Bets (Batch Record) yang disusun
oleh tim CPOB dan disetujui oleh Kepala Instal Wastu dan Kepala Instal
Produksi, kemudian didistribusikan dan didokumentasikan. Proses produksi
dimulai dari penimbangan bahan baku yang akan digunakan dan dikeluarkan dari
Instal Simpan berdasarkan Batch Record untuk setiap produk.
3.4.1 Seksi Sediaan Padat (Si Diadat)
Kegiatan di seksi ini meliputi kegiatan penimbangan, pencampuran,
pengeringan, granulasi, pencetakan, penyalutan dan stripping.
a) Sediaan Tablet
Ruang produksi tablet terdiri dari ruang mucilago, ruang campur,
ruang granulator, ruang pengering, ruang pengayakan, ruang cetak, ruang
penyalutan, ruang stripping dan ruang cuci alat. Ruangan-ruangan ini
dilengkapi dengan lampu penerangan yang memadai, AC, ventilator
dengan penghisap debu dan lapisan epoksi pada dinding dan lantai.
Peralatan yang digunakan oleh seksi sediaan padat untuk pembuatan
tablet diantaranya adalah mesin pembuat mucilago dengan energi panas
dari uap, mesin pencampur basah sekaligus campur kering, oven
pengering, granulator, mesin cetak tablet, mesin salut film serta mesin
strip tablet.
Metoda pembuatan tablet yang biasa digunakan adalah metoda cetak
langsung dan metoda granulasi basah. Tablet yang diproduksi adalah
berdiameter 7.5, 10, 12, 13 mm. Proses pembuatan tablet di Lafi Ditkesad
menggunakan metoda granulasi basah dimulai dengan urutan sebagai
berikut:
(1) Proses penimbangan bahan baku
Pada proses ini dilakukan penimbangan terhadap bahan baku dan
bahan tambahan lainnya di ruang timbang pada kelas III.
(2) Proses pembuatan bahan pengikat (mucilago)
Pada proses pembuatan mucilago harus diperhatikan bahwa bahan
mucilago telah dicampur homogen sebelum penambahan aqua
demineralisata panas. Kemudian dilakukan pengadukan sampai
terbentuk massa bening. Pembuatan mucilago ini dilakukan di dalam
tangki pemanas double jacket.
(3) Proses pencampuran bahan berkhasiat dengan fase dalam
Bahan berkhasiat dicampurkan dengan fase dalam, diaduk sampai
homogen. Pada pencampuran ini yang harus diperhatikan adalah waktu
pencampuran, putaran mesin dan kapasitas mesin pencampur agar
dihasilkan massa yang homogen.
(4) Proses granulasi basah
Pada proses granulasi ditambahkan sejumlah bahan pengikat
(mucilago) ke dalam hasil campuran zat berkhasiat dengan fase dalam
dan diaduk hingga homogen sampai terbentuk massa yang dapat
dikepal.
Massa yang diperoleh dikeringkan dalam oven pada suhu dan
waktu tertentu sampai terbentuk massa setengah kering (tergantung
jenis tablet yang dibuat).
(6) Proses pengayakan
Massa setengah kering diayak dengan ayakan mesh tertentu
tergantung dari jenis dan ukuran tablet.
(7) Proses pengeringan
Setelah diayak massa kembali dikeringkan di oven pada suhu dan
waktu tertentu sampai mencapai kadar air sekitar 2-5 % (tergantung
jenis tablet yang dibuat).
(8) Proses pengayakan
Setelah kering, massa diayak kembali dengan ayakan ukuran mesh
tertentu sampai menjadi granul.
(9) Pengawasan mutu
Pada granul yang telah dikeringkan dilakukan uji mutu (IPC)
meliputi pemeriksaan kadar air granul.
(10) Proses pembuatan massa cetak
Setelah granul lulus dalam uji mutu (IPC) dibuat massa cetak
yaitu dengan penambahan pelincir dan penghancur luar kemudian
diaduk hingga homogen.
(11) Pengawasan mutu
Sebelum massa cetak dicetak, dilakukan uji mutu (IPC) terhadap
(12) Proses pencetakan tablet
Setelah lulus uji mutu dilakukan pencetakan tablet dengan mesin
yang sesuai dengan ukuran diameter dan berat tablet yang diinginkan.
Untuk tablet berlapis dua dibuat sedemikian rupa sehingga kedua
lapisan warna sama tebal dan tidak tersisa granul salah satu warnanya
saja pada hopper. Selama pencetakan harus diperhatikan kekerasan dan
keregasan tablet, kemudian hasil pencetakan dialirkan ke dalam alat
deduster untuk menghilangkan debu/fines yang masih ada pada
permukaan tablet.
(13) Pengawasan mutu
Selama pencetakan dilakukan IPC di ruang produksi meliputi
keseragaman bobot, kekerasan dan ketebalan. Sedangkan uji mutu oleh
Wastu meliputi uji waktu hancur, keregasan, diameter tablet, kadar
bahan aktif dan uji disolusi pada hasil pencetakan.
(14) Proses penyalutan
Setelah dicetak, tablet ada yang disalut dan ada yang langsung
distrip. Untuk tablet yang disalut maka pada proses penyalutan harus
diperhatikan suhu, frekuensi penyemprotan, kecepatan putar panci
penyalut dan sudut penyemprotan.
(15) Pengawasan mutu
Pemeriksaan yang dilakukan terhadap tablet salut adalah waktu
(16) Proses penyetripan
Tablet salut ataupun tablet biasa yang telah lulus uji mutu, distrip
dengan menggunakan bahan pengemas Polycello atau Polycellonium
sebagai pengemas primer. Suhu mesin tidak boleh terlalu rendah
karena akan menyebabkan kemasan tidak dapat melekat satu sama lain
dan juga tidak boleh terlalu tinggi karena akan merusak kemasan itu
sendiri. Untuk bahan pengemas Polycello suhu mesin diatur antara ±
60o–80o C, sedangkan untuk bahan pengemas Polycellonium suhu
mesin diatur antara 80o – 100oC.
(17) Pengawasan mutu
Uji mutu (IPC) yang dilakukan pada hasil penyetripan berupa
pemeriksaan uji kebocoran strip. Tablet yang telah distrip didorong ke
seksi kemas untuk dikemas dan dikirim ke Instal Simpan. Untuk
pembuatan tablet dengan metoda cetak langsung dimulai dari proses
penimbangan bahan baku, selanjutnya mengikuti proses pencampuran
massa cetak sampai dengan proses penyetripan dan pengemasan tanpa
melalui proses granulasi.
b) Sediaan Kapsul
Ruang produksi kapsul terdiri dari ruang pencampuran, ruang
pengisian dan polishing, serta ruang stripping. Peralatan yang digunakan
untuk pembuatan kapsul diantaranya adalah mesin pencampur, mesin
pengisi kapsul, mesin polishing dan mesin strip. Proses produksi kapsul
(1) Penimbangan bahan baku
Penimbangan bahan baku antara lain penimbangan bahan aktif,
bahan pengisi, bahan pelincir di ruang timbang pada kelas III.
(2) Pencampuran/granulasi
Setelah semua bahan ditimbang, dilakukan proses pencampuran
hingga homogen. Bahan yang diisikan ke dalam kapsul ada yang harus
digranulasi terlebih dahulu untuk memperbaiki sifat alirnya, sedangkan
untuk bahan yang tidak digranulasi langsung diisikan pada cangkang
kapsul.
(3) Pengawasan mutu
Sebelum diisikan ke dalam cangkang kapsul, hasil pencampuran
massa kapsul dilakukan IPC (In Process Control) oleh Instal Wastu
untuk diperiksa homogenitas dan kadar zat aktifnya.
(4) Pengisian kapsul
Setelah massa kapsul diluluskan oleh Instal Wastu maka massa
kapsul diisikan ke dalam cangkang kapsul. Selama pengisian,
dilakukan pengawasan mutu (IPC) untuk diperiksa keseragaman bobot,
kadar zat aktif dan waktu hancur.
(5) Polishing
Sebelum kapsul distrip, kapsul mengalami polishing terlebih
dahulu untuk menghilangkan debu-debu yang menempel pada bagian
luar cangkang kapsul.
Setelah dipolishing maka kapsul siap distrip dengan cara yang
sama seperti pada proses stripping tablet.
(7) Pengawasan mutu
Pada hasil penyetripan dilakukan uji mutu (IPC) meliputi tes
kebocoran strip. Kapsul yang telah lulus uji mutu siap dikemas dan
dikirim ke Instal Simpan.
3.4.2 Seksi Sediaan Cair/Steril (Si Dia Cair/Steril)
Kepala seksi sediaan cair/steril adalah seorang Apoteker yang
bertanggung jawab kepada Kepala Instal Produksi. Seksi sediaan cair/steril ini
memproduksi obat-obatan yang terdiri dari sediaan salep, sediaan sirup dan
sediaan cairan obat luar.
a) Sediaan Salep
Peralatan yang digunakan antara lain: panci double jacket, mesin
pencampur salep dan mesin pengisi-penutup salep otomatis.
Pembuatan salep dimulai dari:
(1) Penimbangan bahan baku dilaksanakan di di ruang timbang pada
Kelas III.
(2) Pelelehan basis
(3) Basis dilelehkan pada panci double jacket, disaring kemudian
didiamkan selama satu malam.
(4) Pencampuran
(5) Bahan basis yang telah dilelehkan dimasukkan ke dalam mesin
sampai homogen pada suhu 400 C di dalam mesin pencampur
“Homomixer”.
(6) Pengawasan mutu
(7) Pada hasil proses pencampuran dilakukan uji mutu (IPC)
terhadap
homogenitas, pH dan kadar zat aktif.
(8) Pengisian ke dalam tube
(9) Setelah lulus uji mutu, massa salep diisikan ke dalam tube dengan
suhu yang terjaga sekitar 400 C.
(10) Pengawasan mutu
(11) Pada hasil pengisian dilakukan uji mutu (IPC) untuk diperiksa
keseragaman isi tube dengan cara menimbang tube satu persatu
yang dilakukan setiap 15 menit, setelah lulus uji mutu, tube yang
berisi salep dikemas dan dikirim ke Instal Simpan.
b) Sediaan Sirup
Ruang produksi sirup terdiri dari ruang pencampuran, ruang
pengisian, ruang pencucian alat. Peralatan yang digunakan antara lain
mixer, colloid mill, panci double jacket, drum stainless, mesin pengisi
sirup, penutup botol dan pemasangan etiket yang merupakan satu
rangkaian (In Line Process).
Proses pembuatan sirup diawali dengan:
(1) Penimbangan bahan baku yang dilaksanakan di di ruang timbang
(2) Pembuatan larutan gula pekat (Syrupus Simplex)
Pembuatan larutan gula pekat dilakukan pada panci double jacket.
Pemanasan menggunakan uap air yang dihasilkan oleh ketel uap.
(3) Pencampuran
Zat aktif dan zat tambahan lain (zat pewarna dan pengawet)
masing-masing dilarutkan dalam pelarut yang sesuai sampai larut
sempurna, kemudian dicampur dengan larutan gula pekat. Essence
dapat ditambahkan jika diperlukan dan volume ditambahkan
sampai tanda batas yang telah ditentukan.
(4) Pengawasan mutu
Pada hasil pencampuran dilakukan uji mutu (IPC) terhadap
homogenitas larutan, kadar zat aktif, pH larutan dan berat jenis.
(5) Pengisian, penutupan dan labelling
Setelah lulus uji mutu dilakukan pengisian, penutupan dan
pemberian etiket atau label dilakukan dengan mesin ban berjalan
yang bekerja secara semi otomatis. Pada proses ini dilakukan
kontrol setiap 15 menit terhadap keseragaman volume, hasil
penutupan dan pemasangan label.
(6) Pengawasan mutu
Pada produk yang telah dikemas dilakukan pengambilan sampel
untuk dilakukan pemeriksaan mutu meliputi keseragaman
lulus uji mutu dilakukan pengemasan kemudian diserahkan ke
Instal Simpan.
c) Sediaan Injeksi
Ruang produksi injeksi merupakan ruang kelas I dan kelas II yang
terdiri dari ruang penimbangan, ruang pencampuran dan penyaringan,
ruang pengisian dan penutupan, ruang pencucian, pengeringan, sterilisasi,
visual dan ruang kemas. Peralatan yang digunakan untuk pembuatan
injeksi adalah mesin pencuci vial atau ampul, oven, autoclave, mesin
pengisi dan penutup vial atau ampul. Sediaan injeksi untuk saat ini tidak
diproduksi karena sudah dialihkan ke Labiomed Jakarta.
3.4.3 Seksi Sediaan Khusus (Si Diasus)
Seksi sediaan khusus terdiri dari produksi betalaktam dan Sefalosporin.
Produksi Sefalosporin belum dimulai karena bangunan produksi belum jadi.
Proses produksi betalaktam dilakukan pada gedung yang terpisah dengan
produksi non betalaktam untuk menghindari terjadinya pencemaran silang.
Gedung produksi betalaktam telah dilengkapi dengan sistem pengaturan udara
(Air Handling System), air washer, air shower, dan ruang penyangga (air lock).
Lantai, dinding dan langit-langit dilapisi oleh bahan epoksi untuk memudahkan
pembersihan.
Ruang kelas I terdiri dari Laminar Air Flow (LAF), ruang kelas II
meliputi koridor kelas II, air shower, ruang isi vial dan ruang staging steril.
Ruang kelas III meliputi ruang timbang, ruang staging, ruang campur, ruang cetak
ruang isi sirup kering, ruang cuci vial, ruang botol bersih, ruang simpan alat,
ruang IPC, loker kelas III wanita dan pria. Ruang kelas IV meliputi ruang coding,
ruang kemas, ruang karantina obat jadi, ruang gudang sejuk, ruang gudang
botol/vial, ruang cuci botol, ruang simpan alat, ruang laundry dan loker kelas IV
wanita dan pria.
Sistem pengaturan udara (Air Handling System/AHS) untuk ruang kelas I
dan kelas II dilakukan dengan sistem recycle (udara dari kelas III disaring
kemudian ditambah udara segar 10-20 %), sementara untuk ruang kelas III
dengan sistem pengolahan udara terbuka (udara segar yang masuk disaring
dengan pre-filter dan medium filter). Kondisi ruangan di betalaktam selalu diukur
secara berkala untuk mengukur pertukaran udara, suhu udara, kelembaban dan
jumlah partikel serta perbedaan tekanan udara.
Setiap personil yang masuk ke ruangan betalaktam diharuskan
menggunakan pakaian khusus lengkap dengan aksesorisnya yang berupa masker
untuk wajah, sepatu dan sarung tangan. Sebelum memasuki ruangan, diharuskan
melewati air shower yang dimaksudkan untuk menghilangkan partikel-partikel
pengotor yang melekat pada pakaian. Setelah selesai melaksanakan kegiatan
produksi, setiap personel diharuskan untuk membersihkan diri dengan cara
mandi.
3.4.4. Seksi Kemas (Si Kemas)
Kasi kemas adalah seorang Apoteker yang bertanggung jawab kepada Ka
Instal Produksi. Pengemasan dilakukan pada produk ruahan tablet, kapsul, sirup
Untuk sirup dipak ke dalam dus. Sedangkan sediaan salep dimasukkan ke
dalam tube aluminium Setelah pengemasan selesai, dilakukan pemeriksaan QC
oleh Instal Wastu. Setelah diperiksa oleh Instal Wastu, hasil pengemasan diberi
label ”Diluluskan” kemudian seksi kemas membuat laporan administrasi yang
terdiri dari laporan bulanan untuk dilaporkan ke Ka Lafi dan bukti penyerahan
obat jadi untuk Ka Instalasi Simpan.
3.5 Kegiatan Instalasi Simpan (Instal Simpan)
Instalasi Simpan (Instal Simpan) merupakan pelaksana fungsi penerimaan,
penyimpanan dan pengeluaran atas perintah KaLafi serta menyelenggarakan dan
melaksanakan kegiatan pengamanan dan pemeliharaan materiil. Adapun
penyelenggaraan administrasi yang menyertai pemindahan tanggung jawab dari
Instal Simpan ke Gudang Pusat II terdiri dari:
1) BP dari Instal Simpan ke Gudang Pusat II.
2) Surat Kiriman Barang.
Persediaan barang di Instal Simpan diawasi dengan ketat dimana
pemasukan dan pengeluaran barang dicatat di kartu gudang. Bangunan Instal
Simpan terdiri dari ruangan administrasi, ruang sejuk (AC), ruang sampling
(kelas III), ruang timbang, ruang bahan aktif, ruang bahan cair dan ruang produk
jadi, ruang bahan pembantu, ruang embalage, ruang timbang yang dilengkapi AC
3.6. Fasilitas Pendukung/ Utility
Fasilitas pendukung/utility antara lain terdiri dari pengolahan air baku
farmasi, instalasi listrik, instalasi uap/boiller dan instalasi udara bertekanan dan
sistem tata udara (AHS). Sumber air bersih didapat dari suplai Perusahaan Daerah
Air Minum (PDAM) yang kemudian diolah menjadi air baku farmasi melalui
instalasi pengolahan air. Air baku farmasi adalah air yang telah memenuhi syarat
untuk digunakan sebagai bahan baku air untuk produksi steril maupun nonsteril.
Penanggung jawab pengolahan fasilitas utility ini adalah Kepala Instalasi
Pemeliharaan (Instal Har). Fasilitas utility terdiri dari :
1) Instalasi Listrik
Sumber listrik Lafi Ditkesad berasal dari PLN dengan daya sebesar
2000 kW. Pada saat ini belum digunakan generator karena beberapa
pertimbangan antara lain karena jarang terjadi pemadaman listrik dari
PLN dan penggunaan generator terdapat delayed bila listrik dari PLN
padam. Tetapi pada produksi steril diperlukan adanya aliran listrik secara
terus-menerus sehingga dipertimbangkan untuk menggunakan generator.
2) Instalasi Air Demineralisata
Sumber air bersih berasal dari Perusahaan Daerah Air Minum (PDAM)
kemudian diolah menjadi air baku farmasi melalui instalasi pengolahan
air. Pemilihan PDAM sebagai sumber air oleh Lafi Ditkesad adalah
karena banyaknya kandungan logam pada air tanah.
Air yang berasal dari PDAM terlebih dahulu ditampung pada tangki yang
dalam suatu alat filtrasi. Air yang diolah menjadi air demineralisata
mengalami beberapa tahap penyaringan:
a) Saringan Pasir (sand filter)
Saringan pasir berfungsi untuk mengikat kotoran-kotoran dan
kaporit yang terbawa air selama pengolahan air di PDAM.
b) Saringan Karbon (carbon filter)
Saringan karbon berfungsi untuk menyerap bau, rasa, warna,
kontaminan organik dan unsur chlor yang ditambahkan pada
pengolahan air di PDAM.
c) Resin Kation
Resin kation berfungsi untuk menghilangkan ion-ion positif dan
ditukar dengan ion hidrogen.
d) Resin Anion
Resin anion berfungsi untuk menghilangkan ion-ion negatif dan
ditukar dengan ion hidroksida, sehingga menghasilkan air dengan
kandungan Total Dissolved Solid (TDS) kurang dari 8 ppm dan
silika kurang dari 0,1 ppm.
e) Setelah mengalami beberapa tahap pemurnian, air demineralisata
dialirkan ke ruangan-ruangan produksi untuk digunakan.
3) Instalasi Air Suling
Instalasi air suling merupakan kelanjutan dari instalasi air demineralisata
yang dihubungkan dengan alat dan pemroses aquadest, dengan alat ini
4) Instalasi Boiller (Steam)
Air baku untuk menghasilkan uap panas adalah aqua demineralisata yang
ditekan melalui pompa air masuk ke filter kemudian ditampung di dalam
tangki stainless steel untuk mensuplai steam. Air dipanaskan melalui
boiler hingga menjadi uap. Alat ini bekerja secara semi otomatik dengan
alat-alat pengaman yang lengkap. Udara panas yang dihasilkan dialirkan
melalui pipa ke ruang-ruang produksi yang membutuhkannya.
5) Instalasi Udara Bertekanan
Udara bertekanan diperoleh dengan menggunakan alat kompresor yang
bekerja secara otomatis dengan alat pressure switch. Kompresor juga
dilengkapi dengan air dryer, main line filter, mist separator dan micro
mist separator. Instalasi kompresor ini digunakan hanya pada peralatan
yang memerlukan udara bertekanan.
6) Sistem Tata Udara/ Air Handling System (AHS)
Sistem tata udara merupakan suatu penanganan terpadu terhadap seluruh
ruangan yang membutuhkan spesifikasi tentang komponen–komponen
yang mempengaruhi kualitas udara antara lain jumlah partikel, sistem
tekanan positif, jumlah cemaran biologi, kelembaban dan temperatur.
3.8 Penanganan Limbah
Limbah Lafi Ditkesad berasal dari proses produksi dan proses pengujian,
Pada produksi obat non betalaktam, pengolahan limbah padat dilakukan
dengan menggunakan dust collector yaitu limbah (debu) disedot dari ruang
produksi dengan vakum kemudian dikumpulkan dalam kantong penampung dan
dibakar. Khusus untuk limbah dari proses penyalutan tablet, terlebih dahulu
diolah dengan air washer. Sedangkan limbah cair produksi non betalaktam
langsung dialirkan ke Instalasi Pengolahan Air Limbah.
Pada produksi betalaktam, pengolahan limbah terlebih dahulu diolah melalui
air washer, dimana limbah padat (debu-debu) disedot oleh vakum dari ruangan
yang berdebu seperti ruangan strip, isi kapsul, cetak, coating, campur dan ruang
isi sirup kering, kemudian disemprot dengan air bertekanan 4 bar sehingga debu
akan jatuh di bak penampungan. Air dialirkan ke bak destruksi yang dilengkapi
dengan dozing pump dan pH meter. Cairan ini didestruksi untuk memecah cincin
betalaktam dengan menggunakan larutan NaOH 0,1 N yang diteteskan secara
otomatis sampai diperoleh pH 9, kemudian dinetralkan dengan penambahan HCl.
Sedangkan limbah cair produksi obat betalaktam tidak melalui air washer.
Selanjutnya, limbah hasil produksi betalaktam disalurkan ke IPAL untuk
dilakukan pengolahan lebih lanjut.
Pengolahan limbah pada IPAL menggunakan prinsip fisika, kimia dan
mikrobiologi. Tahapan pengolahan air limbah di IPAL meliputi beberapa tahap
proses sebagai berikut:
Air limbah yang masuk dari produksi betalaktam (dari bak destruksi)
maupun non betalaktam dan laboratorium akan ditampung dan
pengotornya diendapkan dalam bak ini. Kemudian dialirkan ke bak
pengendapan (sedimentasi pertama).
2) Bak Sedimentasi Pertama
Disini terjadi proses pengendapan kembali dengan prinsip pengendapan
dan juga berdasarkan tinggi rendahnya bak.
3) Bak Equalisasi
Bak ini dilengkapi dengan pompa untuk mengendalikan fluktuasi jumlah
air kotor yang tidak merata, yaitu pada jam kerja dan di luar jam kerja.
Bak ini juga disertai dengan pengaduk untuk mengaduk bahan-bahan
organik agar tidak mengendap.
4) Bak Aerasi
Air limbah masuk ke dalam bak ini dengan menggunakan pompa secara
kontiniu. Di dalam bak ini terdapat bakteri aerobik yang berguna untuk
menghancurkan zat-zat organik. Bak ini dilengkapi dengan aerator untuk
memasukkan oksigen ke dalam air limbah. Selain itu di dalam bak ini
terdapat pengaduk yang berfungsi untuk mengaduk air limbah sehingga
bakteri menyebar merata dan menjaga agar keseluruhan air limbah
mengalami kontak langsung dengan udara. Untuk menjaga pertumbuhan
bakteri ditambahkan pupuk urea / NPK sebagai nutrisi untuk bakteri.
Air limbah dari bak aerasi mengalir ke dalam bak sedimentasi kedua.
Dalam bak ini hanya terjadi proses pengendapan. Bak berbentuk kerucut
di bagian bawah untuk menampung endapan.
6) Bak Koagulasi
Cairan dari bak sedimentasi kedua masuk ke dalam bak koagulasi. Di
dalam bak ini ditambahkan koagulan PAC (Poly Aluminium Chloride)
dengan menggunakan dozing pump yang disertai dengan pengaduk.
Konsentrasi PAC yang diteteskan dalam larutan yaitu 50 kg PAC dalam
1000 L air. Bak koagulasi berfungsi sebagai bak penampung koagulan.
7) Bak Flokulasi
Dari bak koagulasi cairan dialirkan ke bak flokulasi yang berfungsi untuk
mengendapkan endapan yang masih terbawa. Di dalam bak ini
ditambahkan polimer anionik sebagai flokulan dengan konsentrasi 1 kg
polianionik dalam 1000 L air sehingga terbentuk flok-flok yang kemudian
diendapkan. Dari bak flokulasi, cairan yang sudah jernih mengalir ke bak
kontrol melalui bidang miring, sedangkan cairan yang masih mengandung
endapan dialirkan ke bak sedimentasi ketiga.
8) Bak Pengendapan akhir (Bak Sedimentasi Ketiga)
a) Dari bak flokulasi, cairan yang masih mengandung endapan dialirkan
ke dalam bak sedimentasi ketiga yang berbentuk kerucut di bagian
bawah bak. Pada bak ini diberi karung yang berfungsi sebagai
penyaring untuk menampung endapan, sedangkan cairan yang lebih
b) Bak Penampung Cairan
Dari bak ini cairan yang kemungkinan masih mengandung endapan
dialirkan ke bak sedimentasi pertama untuk dilakukan pengolahan
kembali sampai limbah tersebut benar-benar bersih dari senyawa
kimia yang berbahaya.
9) Bak Bidang Miring
Bak bidang miring berbentuk miring ke satu arah untuk menahan endapan
dan partikel-partikel lain yang masih terdapat dalam air limbah dari bak
flokulasi. Melalui bak bidang miring ini, air dari bak flokulasi mengalir ke
bak kontrol.
10) Bak Kontrol
Cairan yang sudah jernih dialirkan ke bak kontrol yang berisi ikan sebagai
kontrol biologi untuk diperiksa kadar COD dan BOD, jumlah zat padat
total yang terlarut dan pH. Jika hasilnya memenuhi syarat air dapat
dibuang ke saluran pembuangan akhir.
Parameter yang harus dipantau untuk limbah cair adalah :
1. pH
2. Suhu
3. Total Suspended Solid (TSS)
4. Total Dissolved Solid (TDS)
5. Biological Oxygen Demand (BOD)
BAB IV PEMBAHASAN
Penerapan manajemen mutu di Lafi Ditkesad berdasarkan pada sistem mutu
yang terbentuk atas pola kerja yang baik dari struktur organisasi, prosedur kerja
di setiap instalasi, proses produksi serta personil yang terlibat dalam proses
pembuatan suatu produk sehingga produk yang dihasilkan oleh Lafi Ditkesad
memenuhi persyaratan CPOB.
Lafi Ditkesad memiliki personil yang terkualifikasi dan berpengalaman
dalam hal pengetahuan, keterampilan dan kemampuan sesuai yang disyaratkan
dalam CPOB. Penerimaan personil dilaksanakan secara terpusat sehingga apabila
memerlukan tambahan personil memerlukan waktu yang agak lama sehingga
terjadi keterbatasan personil di bagian produksi, mengakibatkan personil
melaksanakan tugas rangkap sehingga pekerjaan yang dilakukan kurang
maksimal.
Pelatihan karyawan di lingkungan Lafi Ditkesad dilaksanakan minimal satu
kali setahun, selain itu minggu terakhir disetiap bulannya pada minggu militer,
kadang-kadang digunakan untuk pelatihan CPOB. Pelatihan CPOB dilaksanakan
dibawah bimbingan atasan yang bersangkutan, para praktisi dan professional di
bidang industri farmasi.
Lokasi bangunan dan fasilitas Lafi Ditkesad cukup memenuhi persyaratan
ketersediaan tenaga kerja yang cukup, bebas pencemaran dan tidak mencemari
lingkungan.
Gedung produksi Lafi Ditkesad terdiri dari gedung produksi beta laktam
dan non betalaktam. Sarana dan prasarana unit produksi non betalaktam sedang
dalam tahap pengembangan dan merencanakan pembangunan untuk produksi
obat golongan sefalosporin. Pemisahan produksi beta laktam dan non betalaktam
bertujuan untuk mencegah terjadinya kontaminasi silang, reaksi alergi, dan
resistensi mikroba.
Penyimpanan bahan baku untuk produk non betalaktam dan betalaktam
dipisahkan berdasarkan persyaratan CPOB untuk menghindari kontaminasi silang
antar produk. Tersedia juga gudang untuk bahan yang membutuhkan suhu
penyimpanan tertentu, dimana gudang selalu terdapat palet yang sudah terbuat
dari plastik dan rak agar bahan baku maupun obat jadi tidak bersentuhan langsung
dengan lantai untuk menghindari udara lembab dari lantai. Selain itu dilengkapi
dengan, alat anti tikus, anti serangga, serta alat pemadam kebakaran.
Daerah produksi telah dilengkapi dengan sistem tata udara yang dilengkapi
sarana pengatur suhu, kelembaban dan tekanan udara. Sarana yang ada dalam
ruang produksi Lafi Ditkesad seperti lantai, dinding, dan langit-langit telah
dilapisi dengan epoksi dan sudut-sudutnya dibuat melengkung.
Mesin-mesin produksi serta peralatan-peralatan penunjang yang dimiliki
Lafi Ditkesad ditempatkan pada posisi yang tepat dan jarak yang cukup dengan
menempatkan satu ruang satu mesin, dan mempunyai jadwal tersendiri dalam
luput dari perhatian adalah apabila untuk memproses bahan yang sama mesin
yang telah digunakan dalam suatu produksi tidak selalu dibersihkan setelah
digunakan, mesin tersebut baru dibersihkan apabila untuk memproses bahan yang
berbeda, hal ini di khawatirkan akan menyebabkan terjadinya kontaminasi untuk
produk yang akan di produksi selanjutnya.
Setiap personil di bagian produksi pada saat memasuki ruang produksi
selalu mencuci tangan dengan desinfektan dan menggunakan pakaian khusus
yang bersih dilengkapi dengan penutup rambut dan sepatu khusus untuk
menghindari pencemaran potensial. Untuk tamu disediakan juga pakaian khusus,
kain penutup rambut, masker dan sepatu khusus. Personil yang akan melakukan
proses pengolahan produk harus menggunakan sarung tangan untuk menghindari
kontak langsung antara tangan dengan bahan baku maupun produk yang
dihasilkan. Cairan desinfektan yang digunakan tidak selalu sama untuk
menghindari resistensi dari bakteri. Personil dilarang merokok, makan, minum
atau menyimpan makanan dan minuman di dalam ruang produksi atau ruangan
lain yang kemungkinan dapat mencemari produk. Yang luput dari pengawasan
adalah di setiap loker yang menuju ruang produksi maupun ruang kerja lain
belum dicantumkan protap untuk membersihkan diri sebelum dan sesudah
bekerja. Walaupun, personil telah terbiasa dengan tahapan ini dan selalu
diberikan pengarahan dan pelatihan, tetapi kemungkinan resiko ketidakdisiplinan
sangat besar, untuk itu sebaiknya disetiap loker diberikan protap mengenai
Alur produksi di Lafi Ditkesad terdiri dari alur material, personil dan alur
proses produksi sesuai dengan yang ditetapkan dalam CPOB. Selama proses
produksi personil yang bekerja di ruang produksi senantiasa memakai pakaian
kerja lengkap sesuai dengan ruang kerjanya. Setiap personil yang akan bekerja di
ruang produksi selain menggunakan pakaian khusus sesuai dengan ruang
kerjanya juga harus melalui ruang antara atau air shower, yang diperuntukkan
masuknya personil sesuai alur yang telah dibuat protapnya, begitu juga untuk
bahan awal harus melewati alur barang yang sudah ditetapkan sesuai CPOB.
Personil yang bekerja pada produksi steril sebelumnya diharuskan
mengganti pakaian dengan pakaian khusus yang tidak melepas serat. Pakaian
tersebut harus menutupi seluruh tubuh, yang dilengkapi dengan masker, alas kaki
khusus, dan sarung tangan. Pakaian ini harus langsung dicuci setelah digunakan
dengan mesin cuci sistem khusus yang tidak melepaskan serat pakaian.
Setiap bahan baku, bahan tambahan dan bahan pengemas sebelum diterima
dilakukan proses pengujian terlebih dahulu. Selama proses produksi berlangsung,
juga dilakukan In proses control untuk menjamin mutu produk baik produk
ruahan maupun produk jadi. Pelaksanaan kualifikasi, kalibrasi dan validasi
dilakukan dalam rangka memastikan bahwa semua proses, alat dan prosedur
mampu menjamin mutu dari produk yang di hasilkan, mulai dari bahan baku
sampai produk jadi. Kegiatan pengawasan mutu di Lafi Ditkesad didukung
dengan instrumen-instrumen yang memenuhi syarat untuk pengujian fisika, kimia
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad)
merupakan unsur pelaksana Direktorat Kesehatan Angkatan Darat yang
memproduksi obat, yang diperuntukkan bagi AD yang terdiri dari prajurit,
AD, PNS yang bekerja dilingkungan AD, beserta keluarganya.
b. Obat jadi yang diproduksi Lafi Ditkesad telah memenuhi persyaratan Cara
Pembuatan Obat yang Baik (CPOB), ini dibuktikan dengan telah
diperolehnya 10 sertifikat CPOB masing-masing 5 sertifikat untuk produk
beta laktam dan 5 sertifikat produk non betalaktam.
c. Lafi Ditkesad terus berusaha meningkatkan pelaksanaan CPOB dengan
tujuan untuk menghasilkan obat yang bermutu, aman dan berkhasiat
dengan upaya pembangunan gedung yang baru, melengkapi dan
memperbaharui peralatan, validasi metode dan meningkatkan sistem
pengawasan mutu secara menyeluruh.
d. Lafi Ditkesad merupakan tempat pembelajaran yang tepat bagi
mahasiswa/i yang sedang mengikuti pendidikan profesi apoteker.
5.2 Saran
a. Sanitasi dan higiene, personil, sarana produksi dan proses produksi perlu
b. Agar dibentuk tim inpeksi diri, untuk dapat melaksanakan inspeksi diri
secara berkala.
c. Perlu dilakukannya pelatihan secara berkala mengenai seluruh aspek
CPOB terkini yang diikuti secara menyeluruh, dari tingkat pimpinan
DAFTAR PUSTAKA
Badan Pengawas Obat dan Makanan. Pedoman Cara Pembuatan Obat yang Baik
(CPOB). Jakarta. 2001
Badan Pengawas Obat dan Makanan. Petunjuk Operasional Penerapan Pedoman
Cara Pembuatan Obat yang Baik. Badan Pengawas Obat dan Makanan.
Jakarta. 2001
Badan Pengawas Obat dan Makanan. Pedoman Cara Pembuatan Obat yang Baik