LAPORAN PRAKTEK KERJA PROFESI APOTEKER
FARMASI INDUSTRI
di
PT. INDOFARMA (Persero) Tbk.
Jalan Indofarma No. 1 Cikarang Barat 17530, Bekasi
(4 – 30 April 2011)
Disusun Oleh:
Suji Fanina, S.Farm. NIM 103202053
PROGRAM STUDI PENDIDIKAN PROFESI APOTEKER FAKULTAS FARMASI
2011
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas
segala berkat dan rahmatNya sehingga pelaksanaan Pelatihan Praktek Kerja
Profesi Apoteker (PPKPA) di PT. Indofarma (Persero) Tbk. yang dilaksanakan
pada tanggal 4 April 2011 sampai 30 April 2011 dapat terselesaikan dengan baik.
Praktek Kerja Profesi di PT.Indofarma (Persero) Tbk. ini sangat
bermanfaat bagi penulis untuk mendapatkan pengetahuan tentang kegiatan yang
ada di industri farmasi secara menyeluruh dan terpadu. PPKPA ini juga
merupakan salah satu syarat yang harus dipenuhi oleh mahasiswa Program Profesi
Apoteker Fakultas Farmasi Universitas Sumatera Utara.
Dalam pelaksanaan dan penyusunan Laporan Praktek Kerja Profesi
Apoteker ini penulis banyak mendapatkan bantuan dan dukungan dari berbagai
pihak, untuk itu penulis ingin mengucapkan terima kasih yang sebesar–besarnya
kepada :
1. Bapak Placidus Sudibyo, selaku Direktur Utama PT. Indofarma (Persero) Tbk.
yang telah memberikan kesempatan kepada penulis untuk melakukan PPKPA.
2. Bapak Probowinanto, S.Sos., selaku koordinator Pelatihan Praktek Kerja
Profesi Apoteker di PT. Indofarma (Persero) Tbk. yang telah membantu dan
memberikan pengarahan kepada penulis.
3. Bapak Drs, Eko Dodi Santoso, Apt., selaku pembimbing PPKPA di PT.
Indofarma (Persero) Tbk. yang banyak memberikan bimbingan dan masukan
4. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah memberikan kesempatan kepada
penulis dalam melaksanakan PPKPA ini.
5. Seluruh staf & karyawan di PT. Indofarma (Persero) Tbk. atas kerjasamanya
selama penulis mengikuti kegiatan PPKPA.
6. Bapak dan ibu dosen Fakultas Farmasi yang telah memberikan pembekalan
dalam rangka pelaksanaan PPKPA di Industri Farmasi.
7. Seluruh keluarga, terutama orang tua yang selalu berdoa untuk penulis,
memberikan semangat dan dukungan.
8. Rekan–rekan PPKPA angkatan 63 dari ISTN, Universitas Pancasila, Uhamka,
UMP, UAD, UI, UII, UNAIR, UMS, UNAND, UBAYA, dan UWM terima
kasih untuk kerjasama dan kenangannya.
Penulis berharap semoga pengetahuan dan pengalaman yang didapat
selama PPKPA di Industri Farmasi yaitu di PT. Indofarma (Persero) Tbk. ini
bermanfaat sebagai bekal untuk menjalankan pengabdian profesi Apoteker
khususnya di Industri Farmasi dan juga bermanfaat bagi para pembaca.
Cibitung, April 2011
DAFTAR ISI
Halaman
Kata Pengantar ... iii
Daftar Isi ... v
Daftar Gambar... viii
Daftar Lampiran ... ix
Ringkasan... x
BAB I PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Tujuan Pelatihan Praktek Kerja Profesi Apoteker (PPKPA)... 2
1.3Pelaksanaan Pelatihan Praktek Kerja Profesi Apoteker (PPKPA)... 3
1.4Manfaat Pelatihan Praktek Kerja Profesi Apoteker (PPKPA)... 3
BAB II TINJAUAN UMUM PT.INDOFARMA (Persero)Tbk ... 4
2.1 Sejarah dan Perkembangan PT.Indofarma (Persero) Tbk... 4
2.2 Visi dan Misi PT.Indofarma (Persero) Tbk ... 8
2.2.1 Visi PT.Indofarma (Persero) Tbk... 8
2.2.2 Misi PT.Indofarma (Persero) Tbk ... 8
2.3 Motto PT.Indofarma (Persero) Tbk ... 9
2.4 Logo PT.Indofarma (Persero) Tbk... 9
2.5 Kedudukan, Fungsi dan Peranan PT.Indofarma (Persero) Tbk ... 10
2.6 Lokasi dan Fasilitas Produksi PT.Indofarma (Persero) Tbk ... 11
2.7.1 Produk Ethical ( OGB, Lisensi, Generik
Dengan Nama Dagang ) ... 12
2.7.2 OTC dan Herbal Medicine... 12
2.7.3 Alat Kesehatan ... 12
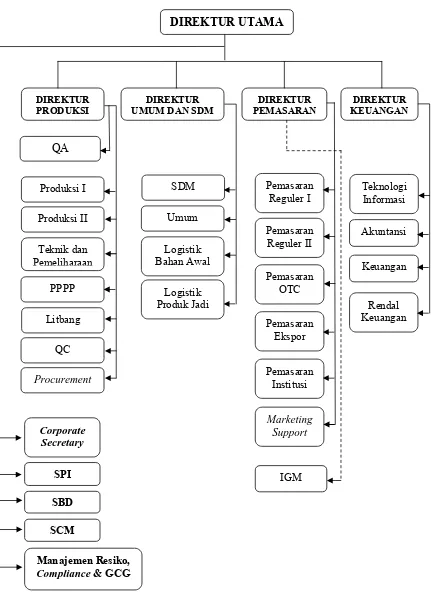
2.8 Struktur Organisasi PT.Indofarma (Persero) Tbk ... 13
BAB III RUANG LINGKUP PT. INDOFARMA (Persero)Tbk... 14
3.1 Direktorat ... 16
3.1.1 Direktorat Produksi ... 16
3.1.1.1 Bidang Produksi I... 16
3.1.1.2 Bidang Produksi II ... 25
3.1.1.3 Bidang Teknik dan Pemeliharaan ... 30
3.1.1.4 Bidang Perencanaan Produksi dan Pengendalian Persediaan / PPPP ... 32
3.1.1.5 Bidang Penelitian dan Pengembangan (Litbang) ... 34
3.1.1.6 Bidang Pengawasan Mutu... 39
3.1.1.7 Bidang Pemastian Mutu ... 43
3.1.1.8 Bidang Pengadaan / Procurement... 44
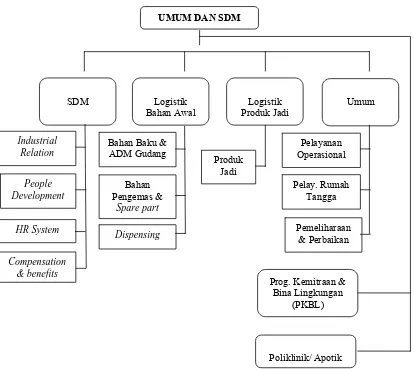
3.1.2 Direktorat Umum dan Sumber Daya Manusia ... 45
3.1.2.1 Bidang Sumber Daya Manusia (SDM) ... 46
3.1.2.2 Bidang Logiktik Bahan Awal ... 47
3.1.2.3 Bidang Logistik Produk Jadi... 50
3.1.2.4 Bidang Umum ... 50
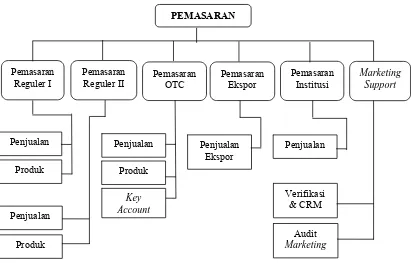
3.1.3 Direktorat Pemasaran ... 54
3.2 Non Direktorat ... 56
BAB IV PEMBAHASAN ……….. 58
4.1.Manajemen Mutu ... 58
4.2 Organisasi dan Personalia ... 59
4.3.Bangunan dan Peralatan... 63
4.4.Sanitasi dan Higiene ... 65
4.5.Produksi ... 66
4.5.1 Bidang Produksi I ... 67
4.5.2 Bidang Produksi II... 67
4.5.3 Bidang Produksi Herbal ... 68
4.5.4 Bidang Pengadaan ... 69
4.5.5 Bidang Logistik Bahan Awal ... ` 69
4.5.6 Bidang Perencanaan Produksi dan Pengendalian Persediaan ... 69
4.5.7 Bidang Penelitian dan Pengembangan (Litbang) ... 70
4.6 Pengawasan Mutu ... 71
4.7 Pemastian Mutu ... 72
4.8 Inspeksi Diri ... 72
4.9 Penanganan Keluhan Terhadap Produk, Penarikan Kembali Produk dan Produk Kembalian ... 74
4.10 Dokumentasi ... 75
4.11 Kualifikasi dan Validasi ... 76
4.12 Pembuatan dan Analisa Berdasarkan Kontrak ... 77
4.13 Sistem Pengelolaan Lingkungan ... 77
5.1 Kesimpulan ... 79
5.2 Saran... 79
DAFTAR PUSTAKA ... 81
DAFTAR GAMBAR
Halaman Gambar 1. Logo PT. Indofarma (Persero) Tbk ... 10
Gambar 2. Struktur Organisasi PT. Indofarma (Persero) Tbk ... 15
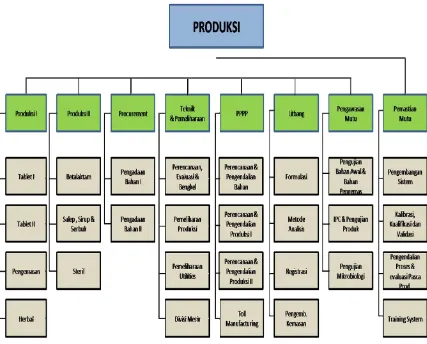
Gambar 3. Struktur Organisasi Direktorat Produksi
PT. Indofarma (Persero) Tbk ... 16
Gambar 4. Hubungan Kerja Bidang PPPP dengan Bidang lain
di PT. Indofarma (Persero) Tbk ... 32
Gambar 5. Struktur Organisasi Direktorat Umum dan Sumber
Daya Manusia (SDM) PT. Indofarma (Persero) Tbk ... 46
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Denah lokasi PT. Indofarma (Persero) Tbk... 82
Lampiran 2. Tata Letak Bangunan PT. Indofarma (Persero) Tbk ... 83
Lampiran 3. Bagan Sistem Pengolahan Air di PT. Indofarma
(persero) Tbk... 84
Lampiran 4. Tabel Instalasi Pengolahan Air di PT. Indofarma
(Persero) Tbk... 85
Lampiran 5. Bagan Sistem Pengaturan Udara PT. Indofarma
(Peresero) Tbk... 86
Lampiran 6. Bagan Sistem Instalasi Pengolahan Air Limbah
RINGKASAN
Telah dilakukan Praktek Kerja Profesi Apoteker di PT. Indofarma
Cibitung - Bekasi. Berlangsung pada tanggal 1 November 2010 sampai dengan 30
November 2010. Praktek Kerja Profesi ini bertujuan mendidik calon apoteker
mampu memahami tugas dan fungsi apoteker serta penerapan CPOB (Cara
Pembuatan Obat yang Baik) di industri Farmasi. Hal ini diharapakan dapat
menjadi bekal bagi penulis untuk menghadapi dunia kerja sehingga dapat
melaksanakan profesi secara baik. Kegiatan Praktek Kerja Profesi (PKP)
Apoteker di PT. Indofarma meliputi tinjauan ke bagian-bagian industri dan tugas
RINGKASAN
Telah dilakukan Praktek Kerja Profesi Apoteker di PT. Indofarma
Cibitung - Bekasi. Berlangsung pada tanggal 1 November 2010 sampai dengan 30
November 2010. Praktek Kerja Profesi ini bertujuan mendidik calon apoteker
mampu memahami tugas dan fungsi apoteker serta penerapan CPOB (Cara
Pembuatan Obat yang Baik) di industri Farmasi. Hal ini diharapakan dapat
menjadi bekal bagi penulis untuk menghadapi dunia kerja sehingga dapat
melaksanakan profesi secara baik. Kegiatan Praktek Kerja Profesi (PKP)
Apoteker di PT. Indofarma meliputi tinjauan ke bagian-bagian industri dan tugas
BAB I PENDAHULUAN
1.1 Latar Belakang
Pembangunan kesehatan secara berkesinambungan telah dimulai sejak
dicanangkannya rencana pembangunan lima tahun I pada tahun 1969. Tujuan
umum Pembangunan Kesehatan Nasional adalah tercapainya mutu hidup dan
lingkungan hidup yang optimal bagi setiap penduduk serta tercapainya derajat
kesehatan yang setinggi-tingginya, meliputi kesehatan badaniah, rohaniah, sosial,
dan bukan hanya keadaan bebas dari penyakit, cacat dan kelemahan. Tujuan
tersebut telah diwujudkan secara nyata dengan adanya berbagai pelayanan
kesehatan yang berdampak pada peningkatan derajat kesehatan masyarakat.
Industri farmasi mempunyai peranan penting dalam upaya peningkatan
derajat kesehatan masyarakat yaitu dengan memproduksi obat yang bermutu dan
berkualitas. Untuk menjamin tercapainya pemenuhan obat yang berkualitas,
pemerintah melalui Badan Pengawas Obat dan Makanan telah berupaya
memberikan suatu Cara Pembuatan Obat yang Baik (CPOB) yang mutlak harus
diterapkan oleh semua industri farmasi.
Sesuai dengan pedoman CPOB, mutu obat bergantung pada bahan awal,
proses pembuatan dan pengawasan mutu, peralatan, bangunan dan personalia
yang terlibat. Berdasarkan hal tersebut maka seorang apoteker diperlukan untuk
mengawasi seluruh kegiatan produksi dan berperan untuk meningkatkan
kesadaran penuh personalia dalam CPOB agar dapat berperan aktif sesuai dengan
PT. Indofarma (Persero) Tbk merupakan perusahaan farmasi nasional milik
negara yang telah memiliki sertifikat CPOB dan ISO 9001. Penerapan CPOB dan
ISO 9001 dalam proses dan kegiatan di PT. Indofarma (Persero) Tbk ini, terkait
dengan adanya kesadaran bahwa sebuah perusahaan farmasi memiliki tanggung
jawab moral pada masyarakat untuk menghasilkan obat yang aman, bermutu serta
terjangkau oleh semua lapisan masyarakat.
Apoteker dalam industri farmasi mempunyai tugas untuk melakukan
pekerjaan kefarmasian yang meliputi pembuatan dan pengendalian mutu obat,
pengadaan, penyimpanan, distribusi obat, serta pengembangan obat modern
maupun obat tradisional.
Berdasarkan pertimbangan diatas, seorang apoteker dalam industri farmasi
harus memiliki pengetahuan, keterampilan, dan pengalaman berkaitan dengan
pekerjaan kefarmasian di industri farmasi. Salah satu cara untuk mencapai tujuan
tersebut adalah dengan diadakannya Pelatihan Praktek Kerja Profesi Apoteker
(PPKPA) bagi mahasiswa profesi fakultas farmasi, sehingga diharapkan
mahasiswa dapat mengenal, mengetahui, memperdalam fungsi dan peran apoteker
di industri farmasi. Dengan demikian calon Apoteker mendapatkan bekal
ketrampilan dan pengalaman praktis yang kelak akan membantu ketika memasuki
dunia kerja terutama di industri farmasi.
1.2 Tujuan Pelatihan Praktek Kerja Profesi Apoteker
Tujuan diadakan Pelatihan Praktek Kerja Profesi Apoteker di PT. Indofarma
1. Melihat gambaran nyata peran Apoteker dan penerapan CPOB di industri
farmasi.
2. Mengetahui dan memahami dasar-dasar pengelolaan industri farmasi dan
keterkaitannya dengan profesi lain.
3. Membantu mahasiswa dalam membekali diri dengan pengetahuan dan
ketrampilan untuk memasuki dunia kerja, khususnya di industri farmasi.
1.3 Pelaksanaan Pelatihan Praktek Kerja Profesi Apoteker
Pelatihan Praktek Kerja Profesi Apoteker di PT. Indofarma (Persero) Tbk
dilaksanakan selama satu bulan dari tanggal 4 – 30 April 2011. Kegiatan yang
dilakukan berupa:
1. Tutorial yang diadakan oleh bidang Umum, Perencanaan Produksi dan
Pengendalian Persediaan (PPPP), Strategi dan Pengembangan Produk dan
Bisnis (Strategic Business Development/ SBD), Lingkungan dan Keselamatan,
Kesehatan Kerja (LK-3), Produksi, Pelaksanaan Program Kemitraan dan Bina
Lingkungan (PKBL), Logistik Bahan Awal (LBA), Sumber Daya Manusia
(SDM), Pengadaan (Procurement), Teknik dan Pemeliharaan/ Utilities.
2. Tinjauan ke Lapangan
3. Pelaksanaan Tugas Khusus pada salah satu bidang di PT. Indofarma (Persero)
Tbk.
4. Presentasi hasil tugas khusus
Melalui materi dan praktek yang diperoleh selama Pelatihan Praktek Kerja
Profesi Apoteker ini diharapkan dapat memantapkan pemahaman serta penerapan
BAB II
TINJAUAN UMUM PT. INDOFARMA (Persero) Tbk.
2.1 Sejarah dan Perkembangan PT. Indofarma (Persero) Tbk.
PT. Indofarma (Persero) Tbk merupakan Badan Usaha Milik Negara
(BUMN) berada di bawah Departemen Kesehatan, berdiri pada tahun 1918 berupa
unit produksi kecil dari Rumah Sakit Pusat Pemerintah Belanda dengan kegiatan
pembuatan salep dan pemotongan kain kasa pembalut yang dilakukan di Centrale
Burgelijke Zienkeninrichring (CBZ), yang sekarang dikenal dengan Rumah Sakit
Dr. Cipto Mangunkusumo di Jakarta.
Pada tahun 1931, pabrik berkembang dengan bertambahnya produksi, yaitu
obat suntik dan tablet. Lalu pada tahun 1935 lokasi pabrik dipindahkan ke Jalan
Tambak No. 2 Manggarai Jakarta dan dikenal dengan ”Pabrik Obat Manggarai”.
Sejak berakhirnya penjajahan Belanda dan masuknya Jepang ke Indonesia,
pada tahun 1942 pabrik obat Manggarai diambil alih dan dikelola oleh perusahaan
farmasi Jepang (dibawah manajemen Takeda). Selama masa tersebut kegiatan
produksi tidak banyak mengalami perkembangan. Saat penyerahan kedaulatan
dari pemerintah Jepang kepada pemerintah Republik Indonesia pada tahun 1950,
pabrik obat Manggarai diambil alih oleh pemerintah Indonesia yaitu Departemen
Kesehatan melalui Direktorat Jenderal Farmasi. Pada tahun 1960-1967, pabrik
tersebut berada di bawah naungan Badan Perlengkapan Kesehatan (Baperkes),
disamping dua badan lain, yaitu Depo Farmasi Pusat dan Lembaga Farmakoterapi,
pada perkembangan selanjutnya disebut Lembaga Farmasi Nasional kemudian
Pada tanggal 14 Februari 1967, melalui Surat Keputusan Menteri Kesehatan
Republik Indonesia No.008/III/AM/67, nama Pabrik Obat Manggarai diubah
menjadi Pusat Produksi Farmasi Departemen Kesehatan dan ditetapkan sebagai
Unit Operatif setingkat Direktorat Jenderal Farmasi. Tugas pokok dari pabrik ini
adalah memproduksi obat–obatan berdasarkan pesanan dari Departemen
Kesehatan RI. Pada tahun 1969-1975 pabrik direnovasi dan tahun 1975
dikeluarkan Surat Keputusan Menteri Kesehatan Republik Indonesia
No.125/IV/KAB/BU/75 tentang struktur organisasi Departemen Kesehatan yang
merupakan pelaksanaan lebih lanjut dari Keputusan Presiden Republik Indonesia
No. 44 dan 45 tahun 1974. Namun pabrik farmasi Departemen Kesehatan ini tidak
tercakup dalam keputusan tersebut sehingga statusnya tidak jelas. Hal ini
berlangsung hingga tahun 1978.
Dengan adanya kebijaksanaan pemerintah tanggal 15 November 1978 dalam
hal ekonomi dan keuangan, harga obat mendadak melambung tinggi sehingga
persediaan obat terutama di puskesmas mengalami kekosongan karena sulit
mendapatkan obat. Peristiwa ini menyadarkan pemerintah untuk menyediakan
peralatan dan sarana yang dibutuhkan agar dapat mengendalikan mekanisme
pengadaan obat dalam jumlah yang cukup serta memenuhi persyaratan mutu,
keamanan dan distribusi yang merata serta harga terjangkau sesuai kemampuan
dan daya beli masyarakat. Maka pabrik farmasi ini diaktifkan kembali sesuai
dengan fungsinya, berdasarkan SK Menteri Kesehatan Republik Indonesia
No.418/MenKes/SK/XII/78 tanggal 6 Desember 1978.
Pada tahun 1979, pabrik ini ditetapkan sebagai Pusat Produksi Farmasi
pula bahwa Pusat Produksi Farmasi bertugas membantu usaha pemerintah dalam
meningkatkan kesejahteraan masyarakat di bidang kesehatan, yaitu memproduksi
obat-obat untuk rumah sakit pemerintah dan pusat kesehatan masyarakat.
Obat-obatan yang dimaksud bersifat esensial, artinya bahwa obat tersebut banyak
dibutuhkan oleh masyarakat. Untuk memenuhi kebutuhan tersebut, maka
diputuskan untuk didirikannya sebuah pabrik yang sekaligus untuk memperluas
pelayanan Pusat Produksi Farmasi Departemen Kesehatan. Pada tahun 1980 mulai
dilakukan studi kelayakan untuk pembangunan pabrik ini.
Pada tanggal 11 Juli 1981, berdasarkan PP No. 20 tahun 1981, Pusat
Produksi Farmasi diubah menjadi Perusahaan Umum dengan nama Indonesia
Farma (Perum Indofarma) yang direalisasikan pada tanggal 1 April 1988 dengan
mulai dibangunnya pabrik baru yang modern seluas 20 hektar sesuai dengan
konsep dan persyaratan CPOB yang berlokasi di desa Gandasari, Cibitung, Bekasi
dengan bantuan alat dan teknologi dari Italia.
Mulai pertengahan tahun 1991, hampir seluruh kegiatan produksi telah
menempati lokasi di Cibitung, kecuali sediaan steril. Tanggal 31 Januari 1995
fasilitas produksi steril diresmikan oleh Menteri Kesehatan Republik Indonesia
dengan dana pembangunan seluruhnya ditanggung oleh Perum Indofarma.
Pada tanggal 2 Januari 1996 Perum Indonesia Farma diubah menjadi
Perseroan Terbatas Indofarma (PT. Indofarma (Persero)) melalui PP No.34
tanggal 20 September 1995. Perubahan status ini bertujuan untuk mengantisipasi
perubahan dan meningkatkan daya saing. Pada tahun 1996-1997 dilakukan
renovasi pada bagian Litbang. Tahun 1999 dibangun Extraction Plant dan selesai
(PT. IGM) sebagai distributor dan pemasaran produk farmasi termasuk alat
kesehatan dengan 30 cabang di seluruh Indonesia. Tahun 2000 dibangun pabrik
makanan bayi di Lippo Cikarang Industrial Estate Jawa Barat.
Mulai tanggal 17 April 2001, PT. Indofarma melakukan penawaran saham
perdana kepada masyarakat dan mendaftarkan seluruh saham perseroan di Bursa
Efek Jakarta dan Bursa Efek Surabaya dengan kode saham INAF serta resmi
menjadi sebuah perusahaan terbuka dengan nama PT. Indofarma (Persero) Tbk.
Dalam rangka untuk merealisasikan visi dan misi perusahaan, maka mulai
dikembangkan kerjasama dengan patner-patner strategi yang dirintis sejak
Oktober 2001 telah dilaksanakan antara lain dengan Oxford Natural Product
(England), Praporn Darsut Ltd (Thailand), Lupin (India), Guangda Produksi
(Cina), Cowick (Polandia), Nowicky Pharma (Austria) dan lain-lain.
Dengan stuktur permodalan yang kuat, PT. Indofarma (Persero) Tbk
mengembangkan produksi sehingga bukan hanya membuat obat-obat esensial dan
generik, melainkan juga obat dengan nama dagang baik etikal maupun OTC (Over
The Counter), obat tradisional (herbal) dan makanan kesehatan. Manajemen PT.
Indofarma (Persero) Tbk yakin bahwa kunci keberhasilan untuk memenangkan
persaingan di era globalisasi adalah operational execellence. Guna memperkuat
struktur bisnis, pada tahun 2007 perusahaan mengoptimalkan fungsi bisnis yang
ada melalui restrukturisasi lanjutan yang memberikan otonomi luas kepada PT.
IGM, terutama dalam hal penggarapan penjualan. Dengan demikian PT.
Indofarma (Persero) Tbk dapat lebih memfokuskan diri pada kegiatan produksi
sedangkan PT. IGM pada kegiatan distribusi/penjualan produk farmasi dan alat
Guna meletakkan fondasi bisnis yang kuat, PT. Indofarma (Persero) Tbk
senantiasa berupaya menerapkan Tata Kelola Perusahaan yang Baik (Good
Corporate Governance). Pada 22 Februari 2007 organ utama perusahaan telah
bersama-sama menandatangani pernyataan komitmen implementasi GCG. Selain
itu, PT. Indofarma (Persero) Tbk membangun kompetensi personil yang
profesional melalui program pembangunan sumber daya manusia yang terarah,
agar mampu membawa perusahaan memasuki era perdagangan bebas.
Dalam rangka meningkatkan fasilitas produksi guna memenuhi ketentuan
standar Cara Pembuatan Obat yang Baik (CPOB) terkini, PT. Indofarma (Persero)
Tbk sejak tahun 2008 mulai melaksanakan renovasi fasilitas produksi di Cibitung.
Pada tahun 2009, telah masuk pada tahap penyelesaian. Dampak positif renovasi
adalah peningkatan kapabilitas untuk menciptakan kondisi yang ideal guna
terjaminnya kualitas dan stabilitas produk yang baik. Dan tentunya terbuka
peluang untuk menjalin kerjasama strategis baik dengan industri lokal dan
regional.
2.2 Visi dan Misi PT. Indofarma (Persero) Tbk. 2.2.1 Visi PT. Indofarma (Persero) Tbk.
Visi PT. Indofarma (Persero) Tbk adalah menjadi perusahaan yang berperan
secara signifikan pada perbaikan kualitas hidup manusia dengan memberi solusi
terhadap masalah kesehatan dan kesejahteraan masyarakat.
2.2.1 Misi PT. Indofarma (Persero) Tbk.
Selain visi PT. Indofarma (Persero) Tbk juga mempunyai misi yaitu:
1. Menyediakan produk dan layanan berkualitas dengan harga terjangkau untuk
2. Melakukan penelitian dan pengembangan produk yang inovatif dengan
prioritas untuk mengobati penderita penyakit dengan tingkat prevalensi tinggi.
3. Mengembangkan kompetensi sumber daya manusia sehingga memiliki
kepedulian, profesionalisme dan kewirausahaan yang tinggi.
2.3 Motto PT. Indofarma (Persero) Tbk
Motto PT. Indofarma (Persero) Tbk adalah insan Indofarma dalam
menjalankan visi dan misi tersebut yaitu “dilandasi ketaqwaan kepada Tuhan
Yang Maha Esa, kita tingkatkan kualitas kesehatan bangsa”.
Insan Indofarma memiliki nilai-nilai inti yang telah disepakati bersama dan
dianut serta mencerminkan budaya korporat yang membentuk filosofi bisnis dan
budaya kerja “Compassionate, Professional, Entrepreneurship “ disingkat “CPE”,
untuk mewujudkan visi dan misi perseroan.
2.4 Logo PT. Indofarma (Persero) Tbk
Perusahaan memiliki logo ”INF” yang melambangkan kependekan nama
perusahaan.
1. Logo tanpa bingkai menggambarkan pengabdian perseroan dibidang
kesehatan masyarakat.
2. Warna biru melambangkan sifat pengabdian perseroan yang tidak terbatas.
Keluasan pengabdian diperluas dengan gradasi warna yang memiliki dimensi
yang luas.
3. Garis luas dan lengkung melambangkan upaya pelayanan perseroan pada
4. Kesatuan garisnya memberikan kesan melindungi dan saling mendukung,
artinya perseroan siap melindungi masyarakat dari penyakit dan mendukung
masyarakat untuk mewujudkan kesehatan.
5. Posisi miring melambangkan dinamika perseroan yaitu tidak terpaku pada
konvensi-konvensi yang sudah ada, mengikuti perkembangan zaman dan
inovatif tetapi mengikuti gerak laju teknologi.
Gambar 1. Logo PT. Indofarma ( Persero ) Tbk.
2.5Kedudukan, Fungsi dan Peranan PT. Indofarma (Persero) Tbk.
PT. Indofarma (Persero) Tbk adalah suatu Badan Usaha Milik Negara
(BUMN) yang memproduksi obat-obat esensial dan merupakan produsen obat
generik berlogo yang terbesar di Indonesia.
PT. Indofarma (Persero) Tbk sebagai suatu BUMN mempunyai fungsi
antara lain sebagai berikut:
1. Menyelenggarakan kemanfaatan umum di bidang farmasi dalam arti yang
seluas-luasnya terutama dalam bidang pengadaan produk farmasi yang sangat
diperlukan oleh sarana kesehatan pemerintah maupun masyarakat umum.
2. Mendapatkan keuntungan berdasarkan prinsip pengelolaan perusahaan untuk
membiayai serta mengembangkan perusahaan dan untuk disumbangkan bagi
3. Memperluas pemerataan penyediaan obat khususnya bagi masyarakat
golongan menengah ke bawah.
4. Mencukupi kebutuhan obat yang dibutuhkan bagi Puskesmas dan Rumah
Sakit Pemerintah.
5. Sebagai Price Leader terhadap obat-obat yang beredar di masyarakat melalui
program Obat Generik Berlogo.
6. Meningkatkan penerapan CPOB sebagaimana direkomendasikan oleh WHO
sebagai hasil produksi berstandar internasional.
2.6Lokasi dan Fasilitas Produksi PT. Indofarma (Persero) Tbk.
Seluruh fasilitas produksi farmasi dan obat herbal dirancang sesuai konsep
CPOB dan dibangun diatas tanah seluas ± 20 hektar di Cibitung, Bekasi, Jawa
Barat. Pabrik lainnya yaitu pabrik makanan bayi seluas ± 0,25 hektar di Cikarang.
Pabrik dan kantor pusat PT. Indofarma (Persero) Tbk terletak di Jalan Indofarma
No. 1, Desa Gandasari, Kecamatan Cikarang Barat-Bekasi, dengan luas tanah
2.000.000 m2 dan luas bangunan 28.035 m2 yang terdiri dari: kantor pusat 20 m2,
pusat pelatihan 750 m2, kantin 300 m2, koperasi 60 m2, poliklinik dan apotek 196
m2, masjid 441 m2, laboratorium 1.440 m2, unit produksi utama 9.921 m2, unit
produksi β laktam 1.440 m2, unit produksi parenteral 2.330 m2, unit produsi obat
tradisional dan gudang 5.250 m2, bangunan utilities 898 m2, gudang bahan kimia
216 m2, instalasi pengolahan limbah cair 204 m2, instalasi limbah padat 44 m2,
menara air 100 m2, cylinder gas chamber 66 m2, rumah jaga 128 m2, lapangan
1.548 m2, unit penelitian dan pengembangan 700 m2, gudang logistik bahan awal
Sistem tata ruang produksi non steril dibagi dua, yaitu kelas empat dan kelas
tiga. Kelas empat meliputi gudang, koridor yang menghubungkan gudang produk
jadi dan daerah pengemasan sekunder. Daerah ini ditandai dengan lantai yang
dicat epoksi agar kotoran tidak mudah melekat dan dinding mudah dibersihkan.
Kelas tiga merupakan daerah yang terkait langsung dengan proses produksi,
misalnya daerah proses pengolahan, pengemasan primer, hingga koridor yang
berhubungan.
2.7Produk PT. Indofarma (Persero) Tbk.
Produk yang dihasilkan oleh PT. Indofarma (Persero) Tbk antara lain
sebagai berikut:
2.7.1 Produk etikal (OGB, lisensi, generik dengan nama dagang)
PT. Indofarma (Persero) Tbk memproduksi obat generic ethical sebagai
produk utama di samping memproduksi obat dengan nama dagang dan lisensi.
Saat ini PT. Indofarma (Persero) Tbk mulai memperluas target pasar dengan
memproduksi obat branded generic atau obat generik dengan nama dagang
namun harganya terjangkau, yang merupakan program pemerintah untuk
penyediaan obat bagi masyarakat.
2.7.2 OTC dan herbal medicines
Dalam rangka mengembangkan Sumber Daya Alam di Indonesia maka PT.
Indofarma (Persero) Tbk telah mengembangkan Obat Asli Indonesia (OAI) yang
dibuat dalam bentuk sediaan obat seperti Prolipid, Pro Uric, Probagin, dan
Biovision, Bioprost, Bioginko dan lain-lain. Obat OTC yang diproduksi antara
lain OBH Indo Plus.
2.7.3 Alat kesehatan
Selain memproduksi obat, anak perusahaan PT. Indofarma (Persero) Tbk
juga bekerjasama dengan SD (Standart Diagnostic) untuk memasarkan diagnostic
kit. Alat kesehatan tersebut disalurkan dari Standart Diagnostic Inc.
2.8 Struktur Organisasi PT. Indofarma (Persero) Tbk.
PT. Indofarma (Persero) Tbk dipimpin oleh seorang Direktur Utama yang
dibantu oleh empat orang staf direksi, yaitu Direktur Produksi, Direktur Umum
dan SDM, Direktur Pemasaran dan Direktur Keuangan. Masing-masing direktur
membawahi bidang dan tiap bidang membawahi beberapa seksi.
Selain itu, ada beberapa bagian yang bertanggung jawab langsung kepada
Direktur Utama (non direktorat), yaitu Corporate Secretary, Strategic Business
Development (SBD), Manajemen Resiko, Compliance and GCG, Satuan
BAB III RUANG LINGKUP
PT. INDOFARMA (Persero) Tbk.
PT. Indofarma (Persero) Tbk merupakan perusahaan farmasi yang
memproduksi obat generik etikal sebagai produk utama disamping memproduksi
obat dengan nama dagang, lisensi, OTC, herbal medicine dan alat kesehatan.
Dalam menjalankan perusahaan, PT. Indofarma (Persero) Tbk menitik beratkan
kegiatan kepada nilai inti perusahaan, yaitu profesional, kewirausahaan dan
kepedulian. Dari segi profesional, perusahaan menjunjung tinggi integritas,
komitmen seluruh insan dan kepurnaan. Dari segi kewirausahaan, dimana
perusahaan berpandangan visioner, inovasi untuk pertumbuhan dan fokus kepada
pelanggan. Dari segi kepedulian, perusahaan menghargai sikap dan pandangan
orang lain, kerja sama tim serta kesetaraan atas kesempatan dan penghargaan.
PT. Indofarma (Persero) Tbk dipimpin oleh seorang Direktur Utama.
Struktur organisasi perusahaan dibagi menjadi dua, yaitu struktur organisasi
direktorat dan struktur organisasi non direktorat. Kedua bagian ini dibawahi
langsung oleh direktur utama. Struktur organisasi direktorat, Direktur Utama
dibantu oleh empat orang direksi, yaitu Direktur Produksi, Direktur Umum dan
SDM, Direktur Pemasaran dan Direktur Keuangan. Sedangkan non direktorat,
direktur utama membawahi langsung lima bagian, yaitu Corporate Secretary,
Strategic Businnes Development (SBD), Manajemen Resiko, Complience and
GCG, Satuan Pengawasan Internal (SPI) dan Supply Chain Management (SCM).
dibawahi oleh direktur pemasaran. Struktur organisasi PT. Indofarma (Persero)
Tbk dapat dilihat pada bagan berikut:
DIREKTUR
3.1 Direktorat
3.1.1 Direktorat Produksi
Direktorat Produksi PT. Indofarma (Persero) Tbk membawahi delapan
bidang dimana setiap bidang dipimpin oleh seorang manager yang dibantu oleh
asisten manager dan supervisor. Struktur organisasi direktorat produksi sebagai
berikut:
Gambar 3. Struktur Organisasi Direktorat Produksi PT. Indofarma (Persero) Tbk. 3.1.1.1Bidang Produksi I
Bidang Produksi I dipimpin oleh seorang manager yang membawahi empat
seksi, yaitu :
Seksi solid I bertanggung jawab dalam pembuatan produk antara tablet dan
kapsul.
2. Seksi Solid II
Seksi solid II bertanggung jawab dalam pencetakan tablet, filling kapsul,
coating
3. Seksi Pengemasan
Seksi pengemasan bertanggung jawab dalam pengemasan tablet dan kapsul
non ß-laktam.
4. Seksi Herbal
Seksi herbal bertanggung jawab dalam produksi herbal.
Visi dari bidang Produksi I adalah commit to SQC (Supply, Quality and
Cost). Bidang Produksi I dalam menjalankan kegiatannya selalu berkomiten
bahwa penyediaan bahan yang sesuai rencana dan tepat waktu akan menjamin
kualitas produk yang dihasilkan sesuai dengan spesifikasinya sehingga efisiensi
biaya tercapai dan keuntungan juga tercapai. Ukuran kinerja bidang Produksi I
ditentukan dengan menggunakan indikator kunci/ Key Performance Indicator,
yaitu monthly production achievement (produksi bulanan yang tercapai), process
cycle time meet standart (waktu tunggu/ lead time), Yield (hasil akhir), succesfull
batch (produk yang berhasil diproduksi) dan effective machine hour (jam kerja
mesin efektif). Untuk dapat mencapai keberhasilan diatas, maka perlu
diperhatikan faktor-faktor yang menentukan, yaitu perencanaan produksi yang
baik, formula, metode, proses produksi yang handal dan tervalidasi, mesin-mesin
tersandarisasi dan lingkungan produksi yang terkualifikasi dan terkondisi dengan
baik.
Fungsi dan tugas dari bidang Produksi I adalah merencanakan produksi,
mengkoordinir pelaksanaan produksi, mengendalikan pelaksanaan produksi dan
sumber daya manusia sebagai pelaksanaannya serta mengawasi pelaksanaan
produksi. Perencanaan produksi dilakukan berdasarkan rencana penjualan,
kemudian disusun RPB (Rencana Produksi Bulanan) oleh bidang PPPP
(Perencanaan Produksi dan Pengendalian Persediaan) yang berisi item produk dan
jumlahnya. Bidang produksi mengkonfirmasi kesanggunpan RPB dengan
memperhitungkan kapasitas mesin, personel dan waktu kerja. RPB selanjutnya di
break down menjadi RPM (Rencana Produksi Mingguan). RPB maupun RPM
yang telah disetujui oleh PPPP selanjutnya direalisasikan dengan penerbitan PP
(Perintah Produksi) dan PK (Perintah Kemas). PP dan CPB (Catatan Produksi
Bets) digunakan sebagai bon permintaan bahan baku kepada bagian penyimpanan
/ LBA (Logistik Bahan Awal). Di gudang, bahan yang diminta bidang Produksi I
dipersiapkan untuk diproses. Penimbangan dilakukan oleh petugas dispensing
dengan disaksikan oleh petugas IPC (In Proces Control), kemudian dilakukan
serah terima bahan baku kepada bidang Produksi I. Proses produksi dilaksanakan
sesuai persyaratan CPOB. Dokumen yang menyertai proses produksi yaitu CPB,
yang berisi Catatan Pengolahan Bets dan Catatan Pengemasan Bets. Setelah
diperoleh produk ruahan, bidang Produksi I membuat Bukti Penyerahan Produk
Ruahan (BPPR) untuk bidang PPPP sebagai dasar untuk dibuat PK (Perintah
Kemas). BPPR dibuat setelah produk ruahan dinyatakan memenuhi syarat
berlaku dan setiap tahap dilakukan IPC, baik oleh personel produksi maupun
personel bidang Pemastian Mutu.
Proses produksi tablet dibidang Produksi I dilakukan dengan metode
Vertical Closed Sistem, yaitu proses dilakukan secara tertutup mulai dari
promixing tanpa menjadi produk ruahan. Metode ini dilaksanakan dibidang
Produksi I karena bentuk bangunan memungkinkan metode tersebut dilakukan
(tiga lantai) dan produksinya besar sehingga efisiensi tenaga tercapai. Keuntungan
sistem ini adalah dapat meminimalkan terjadinya kontaminasi silang, bets dapat
dibuat dalam kapasitas besar, efisiensi dari segi waktu, tenaga, tempat maupun
energi.
A. Seksi Solid I
1. Pembuatan Produk Antara Tablet
Tahap pertama dalam proses produksi adalah pembuatan massa. Seksi ini
bertugas dalam persiapan pengolahan, penyiapan bahan awal, dan pembuatan
massa.
Tahap dalam pengolahan massa tablet dengan metode:
1. Metode cetak langsung (direct compression)
a.Bahan dalam kemasan asli dari Logistik Bahan Awal dibawa ke lantai III
bersama dengan CPB (Catatan Produksi Bets)
b.Di lantai III dilakukan penimbangan ulang
c.Kemudian bahan baku dibawa ke lantai II dengan memasukkan kedalam
penyedot vakum / AZO yang dilengkapi ayakan berputar dan filter dan
ditampung didalam Bin
e. Kemudian campuran bahan dimixing dengan mixer diosna dan
ditampung didalam Bin dan diletakkan di loading station
2. Metode granulasi basah (wet granulation)
a.Bahan baku yang ditimbang di Logistik Bahan Awal dibawa ke lantai III
bersama CPB
b.Di lantai III dilakukan penimbangan ulang
c.Bahan baku dibawa dan diayak ke lantai II dengan menggunakan penyedot
vakum / AZO yang telah dilangkapi ayakan berputar
d.Bahan baku yang telah diayak, ditampung dalam Bin di lantai II dan
diletakkan di loading station
e.Pencampuran bahan awal dilakukan proses pengadukan bahan dengan
bahan pengikat dan dibuat granul sesuai yang dikehendaki menggunakan
mixer batagion atau mixer stokes
f. Granul basah ditampung dalam container di lantai I selanjutnya
dikeringkan dengan fluid bed dryer.
g.Granul kering diayak dengan granulator dengan ayakan mesh tertentu dan
hasilnya ditampung dalam bin dan diperiksa kadar airnya oleh IPC.
h.Granulat dibawa ke lantai II untuk ditimbang ulang kemudian ditambah
bahan penolong.
i. Proses pencampuran akhir menggunakan mixer diosna dan dites
homogenitasnya oleh IPC.
Produksi kapsul dilakukan dalam ruangan dengan kelembaban udara
50-60% karena cangkang kapsul mudah dipengaruhi oleh kelembaban. Alur proses
pembuatan sediaan kapsul adalah sebagai berikut:
1. Bahan yang telah memenuhi syarat ditimbang di dispensing lantai III.
2. Bahan dari mesin penyedot vakum (azo) yang dilengkapi ayakan berputar
(rotatif sieve) dimasukkan ke dalam bin, dialirkan ke mixer diosna di lantai II
melalui loading station.
3. Massa hasil pengadukan selanjutnya dipindahkan ke lantai III. Petugas IPC
akan melakukan pemeriksaan terhadap massa tersebut mengenai homogenitas
dan kadarnya.
B. Seksi Solid II
Seksi ini berada di lantai II, bertugas melakukan pencetakan menjadi produk
ruahan tablet dan pengisian kapsul dari seksi pembuatan massa yang telah
dinyatakan lolos uji, sampai menjadi produk ruahan yang lolos uji dan siap
dikemas.
Tahap-tahap yang dilakukan oleh seksi pencetakan adalah:
1. Persiapan mesin
2. Pengoperasian mesin (pencetakan tablet)
3. Penimbangan produk ruahan
4. Pemberian label nama produk, nomer bets, jumlah dan tanggal pencetakan.
5. Karantina produk ruah menunggu pemeriksaan dari bidang pemastian mutu.
6. Mencatat semua kegiatan yang dilakukan dalam Catatan Pengolahan Bets
Pemeriksaan kualitas produk antara dan produk ruahan oleh operator
dilakukan selama proses berlangsung dan sewaktu-waktu oleh IPC agar produk
yang dihasilkan senantiasa memenuhi persyaratan mutu yang ditetapkan.
Produk ruahan yang sudah lolos uji diserahkan keseksi pengemasan dari
seksi Solid II untuk dikemas menjadi produk jadi.
1. Pencetakan tablet.
1. Bin yang berisi campuran bahan/ massa tablet dibawa ke lantai III dan
ditempatkan pada loading station, dialirkan melalui pipa stainless steel
yang dilengkapi kain tunnel, ke hopper mesin cetak lantai II dan
selanjutnya pencetakan tablet.
2. Tablet yang telah dicetak dikarantina untuk dilakukan kontrol oleh IPC
sebelum dikemas.
2. Pengisisan Kapsul
1. Bahan yang telah dimixing dialirkan ke hopper mesin pengisi kapsul
(capsule filling machine) di lantai II melalui loading station.
2. Kapsul dibersihkan melalui proses polishing.
3. Produk ruahan dikarantina untuk menunggu hasil analisis dari bidang
pemastian mutu. Produk yang telah memenuhi syarat dapat dikemas.
C. Seksi Pengemasan
Proses pengemasan adalah bagian siklus produksi yang dilakukan terhadap
produk ruahan untuk menghasilkan produk jadi. Pengemasan berhubungan
dengan stabilitas obat yang berfungsi melindungi obat terhadap kelembaban, suhu,
cahaya, iklim, dan benturan. Selain itu kemasan juga mempengaruhi daya tarik
Jika ditinjau dari waktu dikeluarkannya PP dan PK, dikenal dua proses yaitu
in line process dan non in line process. In line process yaitu proses dimana hasil
produksi langsung dikemas dalam wadah pengemasnya, PP dan PK dikeluarkan
bersamaan. Jadi mulai dari bahan awal sampai menjadi produk dalam kemasan
akhir, proses tidak terputus. Proses ini diterapkan dalam sirup cair, sirup kering,
salep dan oralit. Sedangkan dalam non in line process, PP dan PK tidak
dikeluarkan bersamaan. Setelah PP dikeluarkan, dilakukan penyiapan bahan awal
sampai menjadi produk yang siap dikemas. Produk ini dikarantina menunggu
dikeluarkannya PK. Proses ini diterapkan dalam pembuatan tablet, kapsul dan
produk steril.
Pengemasan merupakan terminal akhir produksi sebelum dipasarkan,
sehingga suatu produk harus memenuhi syarat-syarat pengemasan yang baik,
yaitu:
1. Melindungi produk.
2. Inert, spesifik bahan pengemasnya.
3. Harus aman, tidak mudah dibuka oleh anak-anak.
4. Menarik terutama untuk kemasan obat bebas.
Tujuan dilakukan perubahan kemasan adalah:
1. Untuk memberikan proteksi obat yang lebih baik.
2. Image baru.
3. Menonjolkan produk tersebut dari produk lainnya (competitor).
4. Promosi.
5. Sumber informasi.
1. Bahan pengemas primer, yaitu bahan pengemas yang langsung berhubungan
dengan produk, misalnya tube, botol, ampul, stripping, dan blister.
2. Bahan pengemas sekunder, yaitu bahan pengemas yang tidak berhubungan
langsung dengan produk obat, tetapi berhubungan dengan pengemas primer
misalnya kotak untuk ampul/ strip/ blister/ salep.
3. Bahan pengemas tersier, yaitu bahan pengemas yang berhubungan langsung
dengan pengemas sekunder, misalnya karton.
Perintah Kemas oleh bidang Pengemasan digunakan sebagai bon
permintaan bahan pengemasan yang diajukan ke bagian penyimpanan/ LBA.
Bahan pengemas dari gudang bila berupa karton akan dilakukan penyablonan
yang berisi nama produk, nomor bets, expired date, sedangkan untuk etiket dan
kotak akan dilakukan coding (pemberian code) antara lain nomor bets,
manufacturing date, expired date, dan HET (Harga Eceran Tertinggi).
Produk ruahan yang akan dikemas dan bahan kemas yang diterima dari
gudang/ LBA semuanya sudah diluluskan oleh Quality Assurance (QA). Proses
pengemasan dapat berupa pengisian ke botol, stripping, blistering dan sachet.
Jenis pengemasan yang digunakan disesuaikan dengan sifat produk ruahan dan
permintaan pasar. Selama proses pengemasan dilakukan pengujian oleh IPC,
misalnya uji kebocoran strip, blister, dan pengisian kedalam sachet.
Selanjutnya dilakukan proses dokumentasi untuk bidang pengemasan
meliputi Catatan Pengolahan Bets, catatan sanitasi, catatan produksi harian yang
terdiri dari kontrol harian mesin, pengepakan dan laporan bulanan.
PT. Indofarma (Persero) Tbk mendirikan Extraction Center yang khusus
memproduksi obat tradisional (Jamu). Bidang herbal memproduksi obat-obat
tradisional yang bahan bakunya dapat berasal dari dalam negeri maupun dari luar
negeri. Obat tradisional yang bahan bakunya berasal dari dalam negeri nama
produk berawal “Pro”, misalnya Prolipid, Probagin dan Prouric. Obat tradisional
yang bahan baku yang diimpor nama produknya berawalan “Bio”, misalnya
Biovision, Bioginko dan lain-lain.
Kegiatan produksi diseksi herbal meliputi sortasi, pencucian simplisia,
ekstraksi, formulasi dan pengemasan. Bahan baku dipenuhi dengan cara membeli
langsung dari supplier, melalui petani binaan atau bekerja sama dengan institusi
lain. Bahan baku tersebut harus memenuhi spesifikasi yang ditetapkan oleh PT.
Indofarma (Persero) Tbk. seperti kadar air (lebih kecil dari 10%), kadar sari larut
dalam air dan kadar sari larut dalam alkohol (tergantung simplisia) mengacu
kepada buku resmi yang ditetapkan yaitu Materia Medika Indonesia.
Sistem produksi sesuai dengan CPOTB (Cara Pembuatan Obat Tradisional
yang Baik). Produksi herbal di PT. Indofarma (Persero) Tbk berupa horizontal
close system dengan menggunakan metode ekstraksi berupa maserasi, perkolasi
dan gabungan keduanya. Pengeringan ekstrak menggunakan tiga metode yaitu
spray dryer, dehumidifier, dan vaccum dryer. Proses pengolahan ekstrak dimulai
dari perajangan kemudian ekstraksi (penyarian), pengentalan, pengeringan kering
yang kemudian menghasilkan ekstrak kering.
Bahan pendukung produksi terdiri dari pelarut seperti etanol dan air yang
digunakan untuk ektraksi, bahan penolong (aerosil, amilum maydis kering,
bahan pengemas (botol plastik, kapas steril, etiket, silika gel, aluminium foil,
karton dan pita perekat). Sarana dan fasilitas yang digunakan bagian herbal
meliputi sumber energi, air dan instalasi penanganan limbah.
3.1.1.2Bidang Produksi II
Bidang Produksi II dipimpin oleh seorang manager. Bidang ini membawahi
tiga seksi, yaitu Seksi β-laktam, Seksi Salep, Sirup, Serbuk dan Seksi Produksi
Steril. Bidang Produksi II bertugas untuk memastikan tersedianya produk tablet,
kapsul dan sirup kering β-laktam, salep, sirup, serbuk, dan produk steril sesuai
dengan target dengan cara merencanakan, mengkoordinasi, dan mengendalikan
aktivitas pengolahan, pengemasan dan kegiatan terkait.
Pelaksanaan proses produksi dibidang Produksi II menggunakan vertical
closed system untuk menghindari kontak dengan lingkungan. Sistem ini
diterapkan untuk produksi oralit. Sedangkan untuk produksi sediaan -laktam,
salep dan sirup menggunakan horizontal closed system dimana penyiapan bahan
awal sampai produk akhir diproses dalam lantai yang sama, karena sediaan yang
diproduksi dalam jumlah yang relatif kecil.
A. Seksi Sediaan β-laktam
Seksi sediaan β-laktam bertugas memproduksi sediaan antibiotika yang
mempunyai inti β-laktam. Bentuk sediaannya berupa tablet, kapsul, dan sirup
kering. Gedung dan fasilitas produksi β-laktam secara fisik dipisahkan dari
produksi lain (non β-laktam). Pemisahan ini dilakukan sebagai tindakan
pengamanan untuk mencegah terjadinya kontaminasi silang dengan produk lain.
Arus keluar-masuk menggunakan air locked system untuk menghindari
rendah dari ruangan lainnya. Pengendalian udara dilakukan dengan sistem Air
Handling Unit (AHU), dimana gedung β-laktam terpisah dari gedung non β
-laktam. Ruangan β-laktam terdiri dari dua kelas, yaitu kelas tiga yang digunakan
untuk proses dispensing, mixing, dan filling, tableting dan pengemasan primer,
dan kelas empat untuk proses pengemasan sekunder sampai obat jadi. Ruangan
kelas tiga dan Kelas empat dipisahkan berdasarkan perbedaan tekanan dimana
tekanan udara kelas empat lebih tinggi daripada tekanan udara di kelas tiga
sehingga kontaminasi dari β-laktam dapat dihindari.
B. Seksi Sediaan Salep, Sirup dan Serbuk 1. Produksi Sediaan Salep Kulit
Alur proses produksi sediaan salep kulit adalah sebagai berikut:
1. Penimbangan bahan awal yang telah lolos uji
2. Pelelehan basis di dalam vessel atau pelelehan (tanpa pengaduk)
3. Basis dipindahkan ke dalam vessel yang dilengkapi pengaduk melalui pompa
dengan filter, kemudian dilakukan pengeringan basis. Massa basis selanjutnya
didinginkan dan dilakukan pemeriksaan kadar air oleh bagian IPC.
4. Bahan aktif, penolong dan pengawet ditambahkan ke dalam massa basis
sambil diaduk.
5. Massa salep dihomogenkan dengan menggunakan homogenizer dan
kemudian divakumkan untuk mengusir udara yang terperangkap.
6. Massa salep yang telah lolos uji dipindahkan ke dalam penampung stainless
steel, lalu dimasukkan ke dalam tube-tube alumunium menggunakan filling
dengan penimbangan 20 tube setiap 15 menit dan dibuat peta kendalinya.
Petugas IPC akan melakukan sampling untuk diuji.
2. Produksi Sediaan Sirup Cair
Sirup yang diproduksi oleh bidang Produksi II ada dua macam, yaitu sirup
cair dan sirup kering. Sirup cair diproduksi secara horizontal closed sistem,
sedangkan sirup kering dilakukan secara vertical closed sistem namun
pengemasannya sama, yaitu secara in line process.
Tahap–tahap produksi sediaan sirup cair:
1. Dispensing bahan–bahan awal yang telah dinyatakan memenuhi syarat.
2. Pembuatan larutan bahan dalam DIW dan pembuatan suspensi induk.
3. Pencampuran larutan bahan dan suspensi induk dalam vessel yang dilengkapi
pengaduk, kemudian dilakukan sirkulasi dengan menggunakan pompa,
flavouring agent ditambahkan pada suhu massa suspensi 40ºC kemudian
dilakukan pengecekan oleh IPC terhadap massa suspensi.
4. Massa suspensi yang telah lulus uji dialirkan ke filling machine melalui
pompa. Filling machine dilengkapi dengan mesin peniup udara kering, mesin
penutup botol dan mesin penempel etiket. Selama proses pengisian dilakukan,
pengawasan terhadap keseragaman bobot dengan pemeriksaan bobot 6 botol
setiap 15 menit dan dibuat peta kendalinya. Petugas IPC akan melakukan
sampling untuk diuji.
5. Pengemasan ke dalam wadah pengemas sekunder dan tersier.
3. Produksi Sediaan Serbuk
Oralit merupakan contoh sediaan padat (serbuk) berbentuk granul yang
diosna. Pemeriksaan kualitas terhadap massa oralit dilakukan bagian Quality
Control yang meliputi kadar, warna, homogienitas, distribusi partikel, dan kadar
air. Untuk oralit kelembaban udara ruangan harus rendah karena produk
mempunyai sifat sangat higroskopis. Pengendalian proses yang dilakukan antara
lain penetapan kadar air.
4. Seksi Produk Steril
Seksi produk steril bertanggung jawab dalam memproduksi sediaan steril,
dipimpin oleh seorang asisten manager yang membawahi dua subseksi, yaitu:
1. Subseksi pengolahan (penimbangan dan pelarutan, pengisian, sterilisasi,
pengolahan cepalosporin dan dokumentasi).
2. Subseksi pengemasan (pengepakan, pemeriksaan kejernihan sediaan ampul,
vial dan tetes mata serta pencetakan label).
Produk yang dihasilkan antara lain:
1. Sedian steril cairan, seperti injeksi vitamin B12, deksametason, diazepam,
lidokain compositum, papaverin HCl, atropine sulfat dan aqua PI, furosemid
injeksi dan metoklopramida (dibuat dengan cara sterilisasi akhir). Sedangkan
gentamicin dan ranitidine injeksi (dibuat secara aseptis).
2. Tetes mata, seperti gentamicin 0,3%.
3. Sediaan steril powder, seperti injeksi derivat sefalosporin yang dibuat secara
aseptis yaitu Cefotaxim, Ceftriaxon.
Ruang produksi steril dibagi menjadi beberapa kelas sesuai dengan
persyaratan CPOB. Pembagian ini didasarkan kepada derajat kebersihannya,
1. Ruang kelas A (white area atau ruang kritis) merupakan ruang kelas di bawah
LAF (Laminar Air Flow) yang dilengkapi dengan HEPA (High Efficiency
Particulare Air) filter berefisiensi 99,995%. Jumlah partikel dengan diameter
0.5 µm untuk setiap m3 tidak boleh lebih dari 3500.
2. Ruang kelas B (clean area ruang steril), sama dengan ruang kelas I tetapi
tanpa LAF. Besarnya pertukaran udara adalah 20/jam. Jumlah partikel dengan
diameter 0.5 µm untuk setiap m3 tidak boleh lebih dari 350.000.
3. Ruang kelas C (grey area atau ruag steril), dilengkapi dengan filter
berefisiensi 95%. Jumlah partikel dengan diameter 0.5 µm untuk setiap m3
tidak boleh lebih dari 3.500.000.
4. Ruang kelas D (black area atau ruang bersih). Jumlah partikel pada ruang ini
dengan diameter 0.5 µm untuk setiap m3 tidak ditetapkan.
Keempat ruangan di atas, masing-masing dipisahkan dengan ruang antara
dan dilengkapi dengan sistem air lock, air shower, pass box dan sistem air
handling unit (AHU) yang memiliki peranan dalam pengaturan suhu, kelembaban,
tekanan dan sirkulasi udara. Aliran udara diatur berdasarkan perbedaan tekanan,
dimana ruangan dengan kelas yang lebih tinggi memiliki tekanan yang lebih
tinggi dari pada kelas yang lebih rendah.
3.1.1.3Bidang teknik dan pemeliharaan
Bidang Teknik dan Pemeliharaan dipimpin oleh seorang manager yang
membawahi empat seksi yaitu seksi Perencanaan, evaluasi dan workshop, seksi
Pemeliharaan, seksi Rekayasa dan seksi Utilities. PT. Indofarma (Persero) Tbk
peralatan produksi. Sarana pendukung pabrik yang digunakan di PT. Indofarma
(Persero) Tbk, antara lain:
1. Listrik
Sistem kelistrikan di PT. Indofarma (Persero) Tbk, menggunakan sumber
kelistrikan dari PLN dan generator milik perusahaan sendiri.
2. Air
Sistem pengelolaan air di PT. Indofarma (Persero) Tbk, menggunakan
sumber air tanah (sumur dalam ± 150 meter), dimana perusahaan memiliki empat
sumur air. Tujuan pengelolaan air ini adalah untuk menghilangkan cemaran
sesuai standar kualitas air yang ditetapkan. Air dihilangkan dari pengaruh zat besi
dan ditampung didalam bak penampung yang berisi kaporit untuk menghilangkan
bakterinya. Air (raw water) dihilangkan lumpur dan partikel-partikelnya dengan
menggunakan multimedia filter, dimana filter-filter ini tersusun dalam suatu
tabung (vessel) dengan bagian bawah tabung diberikan pasir sebagai alas tabung,
filter ini sering juga disebut send filter. Selanjutnya air disaring dengan karbon
aktif, berfungsi sebagai pre-treatment sebelum proses deionisasi untuk
menghilangkan klorin, kloramin, pestisida, bahan-bahan organik, warna, bau dan
rasa dalam air. Selanjutnya air dihilangkan kation dan anionnya (water softener
filter) dengan menggunakan resin untuk menghilangkan atau menurunkan
kesadahan air dengan cara mengikat calsium dan magnesium yang menyebabkan
tingginya tingkat kesadahan air. Air dimurnikan dengan teknik reverse osmosis
yang dapat menurunkan Total Dissolve Solid (TDS) di dalam air. Selanjutnya air
dialirkan ke gedung water system. Air yang digunakan untuk produksi
dengan looping system sehingga dapat memungkinkan air tersebut disirkulasi
selama 24 jam. Sistem ini juga dilengkai dengan ozonasi dan ultraviolet yang
berfumgsi untuk mendistruksi O3 menjadi O2.
3. Tata udara (Air Handling Unit)
Sistem tata udara untuk mengontrol suhu, kelembaban, tekanan udara,
jumlah partikel dan pola aliran udara sesuai dengan yang dibutuhkan untuk setiap
ruangan. Dilengkapi dengan cooling coil/ evaporator yang berfungsi untuk
mengontrol suhu dan kelembaban relatif udara yang akan didistribusikan ke
ruangan produksi. Udara yang dialirkan berasal dari campuran udara balik (return
air) dan udara luar (fresh air). Blower/ static pressure fan berfungsi
menggerakkan udara disepanjang sistem distribusi udara yang terhubung
dengannya. Filter berfungsi untuk mengendalikan dan mengontrol jumlah partikel
dan mikroorganisme yang mengkontaminasi udara yang masuk ke dalam ruangan
produksi. Filter diletakkan didalam rumah filter/ filter house dan dapat dibagi
dalam beberapa tipe berdasarkan efisiensinya, yaitu prefilter (efisiensi
penyaringan 35%), medium filter (efisiensi penyaringan 95%) dan high effisiency
particulate air/ HEPA filter (efisiensi penyaringan 99,997%). Ducting berfungsi
sebagai saluran tertutup tempat mengalirnya udara.
4. Penanganan terhadap debu
Sistem penanganan debu dilakukan dengan menggunakan dust collector
dimana dilengkapi dengan filter/ penyaringan.
Uap air diperoleh melalui unit steam boiler, dugunakan sebagai sumber
panas pada pengeringan granul (dengan oven atau fluid bed dryer) sterilisasi
dengan autoclav dan lain-lain.
3.1.1.4Bidang perencanaan produksi dan pengendalian persediaan / PPPP Bidang Perencanaan dan Pengendalian Produksi dan Persediaan (PPPP)
dipimpin oleh seorang manager yang membawahi empat seksi, yaitu seksi
Perencanaan dan Pengendalian Bahan Baku dan Bahan Pengemas, seksi
Perencanaan dan Pengendalian Produksi I, seksi Perencanaan dan Pengendalian
Produksi II, Herbal serta seksi Toll Manufacturing dan Pelayanan Produk. PPPP
mempunyai peranan strategis dalam peningkatan efisiensi dan produktifitas,
proses pabrikasi, pengendalian persediaan sehingga diharapkan dapat
menghasilkan produk dengan mutu, harga, jumlah, dan waktu serta pelayanan
yang tepat.
Marketing
Perencanaan produk Supply product
Permintaan bahan awal Pengendalian persediaan
Logistik Produksi
SCM
PPPP
Pengadaan
Gambar 4. Hubungan Kerja Bidang PPPP dengan Bidang lain di PT. Indofarma (Persero) Tbk.
Seksi Perencanaan dan pengendalian mempunyai dua fungsi, yaitu fungsi
umum dalam penentuan permintaan marketing dan langkah-langkah yang
diperlukan untuk memastikan tercapainya permintaan tersebut. Fungsi
pengendalian, merupakan alat manajemen untuk memastikan tersedianya bahan
awal, produk ruah, dan produk jadi untuk terpenuhinya permintaan marketing,
serta pengaturan agar tidak terjadi over stock atau out of stock.
Alur proses kegiatan bidang PPPP dibagi menjadi dua tahap, yaitu alur
proses perencanaan dan alur proses pengendalian bahan. Alur proses perencanaan
dimulai dari permintaan produk yang akan diproduksi dari SCM. Berdasarkan hal
tersebut PPPP membuat rencana produksi satu tahun serta rencana kebutuhan satu
tahun dan dimintakan persetujuan kepada Direktur Produksi. Kedua rencana
tersebut digunakan sebagai dasar pembuatan Rencana Kerja dan Anggaran
Perusahaan (RKAP) yang disusun setiap tahun kemudian dijabarkan dalam
Konsep Rencana Produksi Periodik (KRPP) dan Konsep Rencana Kedatangan
Bahan (KRKB) perkuartal. Berdasarkan KRPP dan KRKB perkuartal dibuat
Rencana Produksi Bulanan (RPB). RPB ini digunakan untuk menyiapkan Perintah
Produksi (PP) dan Perintah Kemas (PK) serta penyiapan Surat Pesanan
Permintaan Barang (SPPB) untuk dimintakan persetujuan Direktur Produksi.
Alur proses pengendalian bahan dimulai dari diterbitkannya Perintah
Pengolahan (PP) sekaligus berlaku sebagai bon permintaan bahan ke gudang
penyimpanan bahan baku dan bahan penolong. Kemudian diterbitkannya Bukti
Penyerahan Produk Ruah (BPPR), selanjutnya keluar Perintah Kemas (PK) dan
Bukti Penyerahan Produk Jadi (BPPJ). Berdasarkan PP dan PK bidang Produksi
membuat Rencana Produksi Mingguan (RPM) yang selanjutnya digunakan
laporan produksi dan ditujukan antara lain kepada bidang PPPP sebagai informasi
untuk fungsi pengendalian produksi. Bidang Pengadaan kemudian memberikan
informasi kemajuan proses pengadaan kepada PPPP untuk fungsi pengendalian
bahan.
Seksi perencanaan produksi mempunyai fungsi, antara lain mengumpulkan
data dan analisa (ramalan penjualan, kapasitas produksi, stok produk antara, ruah
dan jadi), menyusun rencana produksi, evaluasi rencana produksi secara periodik,
evaluasi efisiensi dan produkrifitas, evaluasi kendala-kendala produksi dan
koordinasi problem solving.
Seksi Toll Manufacturing dibagi menjadi dua, toll out (dimana perusahaan
membuat produk ke pabrik farmasi lain) dan toll in (dimana perusahaan menerima
pembuatan produk dari pabrik farmasi lain).
3.1.1.5Bidang penelitian dan pengembangan (Litbang)
Bagian Penelitian dan Pengembangan dipimpin oleh seorang manager yang
membawahi lima seksi, yaitu seksi Formulasi, seksi Metode Analisa, seksi Herbal
dan Makanan, seksi Registrasi dan seksi Pengembangan Kemasan.
Bidang Penelitian dan Pengembangan berperan dalam pengembangan
produk baru, peningkatan daya saing produk existing dan upaya peningkatan daya
saing dengan perusahaan farmasi lain. Tugas bidang ini, antara lain:
1. Meneliti dan mengembangkan produk.
2. Mengoptimalkan produk, yang meliputi optimasi formula termasuk optimasi
dan substitusi bahan.
3. Pengembangan metode analisis.
5. Desain kemasan.
6. Mengorganisasi uji klinis obat dan penelitian ketersediaan hayati yang
bekerjasama dengan instansi lain.
7. Mengadakan kerja sama di bidang penelitian dengan instansi lain seperti LIPI
(Lembaga Ilmu Pengetahuan Indonesia) dan perguruan tinggi.
A. Seksi Formulasi
Seksi formulasi bertugas menyiapkan formula dan proses pembuatan obat
baru, mendesain formula, merancang metode pembuatan, pengembangan bahan
substitusi dan reformulasi dan reproses.
Penelitian formulasi meliputi:
1. Penelitian spesifikasi produk.
2. Penentuan bahan yang akan dipakai.
3. Penelitian formula.
4. Pembuatan master formula.
5. Pembuatan alur proses.
6. Merencanakan dan mengusahakan proses produksi yang pendek.
7. Persyaratan obat yang sama atau lebih ketat dari farmakope.
8. Mendesain formula yang mudah dianalisis.
9. Produk yang dihasilkan mempunyai stabilitas yang baik.
10.Efek farmakologi yang baik dan efek samping yang minimal.
11. Melakukan efisiensi formula.
Bagian Formulasi bertugas mengembangkan formula untuk produk baru,
melakukan reformulasi, yaitu memperbaiki formula dari produk yang sudah ada
mengembangkan cara produksi untuk mempersingkat dan memperkecil biaya
produksi, menguji stabilitas produk baru serta membuat prosedur kerja tetap untuk
bagian produksi.
Bagian pengembangan produk harus mengembangkan produk-produk baru,
sehingga dapat dipertimbangkan oleh Direksi, Marketing, SBD. Proses
pengembangan formula tersebut meliputi studi literatur, penetapan spesifikasi
produk, seleksi bahan baku aktif dan penolong, trial uji stabilitas, scalling up ke
skala produksi.
Proses lahirnya produk baru dimulai dengan adanya usulan dari bagian
pemasaran atau divisi lain. Usulan tersebut dibahas oleh tim produk baru yang
terdiri antara lain dari bidang SBD, Litbang, PPPP, Produksi, Pemastian Mutu dan
Pemasaran. Tim produk baru mendiskusikan mengenai bentuk sediaan, dosis,
rencana kemasan dan rencana peluncuran produk. Selain itu bagian Litbang juga
bertugas memilih spesifikasi bahan, trial formula, desain kemasan, penyiapan alat,
dokumen registrasi dan uji stabilitas. Produk baru yang telah siap didaftarkan ke
Badan POM disertai dokumen-dokumen yang diperlukan untuk memperoleh
nomor registrasi. Dengan adanya nomor regristrasi, produk baru tersebut dapat
diproduksi. Produksi skala besar dilakukan bidang produksi bersama-sama dengan
bidang Litbang dan Pemastian Mutu.
Kegiatan pengembangan produk baru dilakukan selama tiga tahun, meliputi:
1. Studi Pustaka
Mencari spesifikasi bahan aktif, bahan pembantu dan obat tidak tercampurkan
yang baik sesuai dengan bentuk sediaan dan kapasitas produksi yang tersedia
serta menentukan peralatan yang akan digunakan.
2. Screening Bahan
3. Trial Formulasi I dan Analisa
Membuat formula yang aman, berkhasiat, bermutu, efektif dan efisien dari
segi proses dan biaya serta mempunyai nilai kompetitif dari kompetitor.
4. Penyediaan Bahan
Bagian Litbang berhubungan dengan bagian Purchasing untuk kesediaan
bahan.
5. Trial Formulasi II
6. Kemas dan Uji Stabilitas
7. Praregistrasi
8. Uji BE
9. Registrasi
Bidang penelitian dan pengembangan juga melakukan reformulasi terhadap
produk-produk yang sudah diproduksi. Reformulasi adalah memperbaiki formula
yang sudah ada hal ini terjadi karena adanya masalah yang timbul pada produk
tersebut baik permasalahan pada formula, proses produksi dan proses
penyimpanan. Usulan reformulasi biasanya berasal dari pemasaran, pengawasan
mutu, produksi serta bagian penelitian dan pengembangan itu sendiri.
B.Seksi Metode Analisis dan Stabilitas Tugas-tugas seksi ini adalah:
1. Memilih dan mempersiapkan metode analisis untuk bahan aktif, bahan baku
yang prosedurnya mengacu pada CPOB. Metode tersebut harus mempunyai
ketepatan, ketelitian yang tinggi, sama atau lebih ketat persyaratannya dari
Farmakope, menggunakan peralatan dan reagensia yang efisiensinya tinggi
2. Validasi dari metode analisa yang digunakan
3. Optimasi metode analisa
4. Kalibrasi alat-alat bersama dengan Quality Assurance (QA)
5. Menyediakan dan standarisasi ulang dari reworking standard
Penelitian stabilitas produk terutama dilakukan untuk produk baru dan
produk reformulasi.
C. Seksi Herbal dan Makanan
Seksi ini mempunyai tugas menyiapkan formula dan proses pembuatan obat
herbal dan makanan. Penelitian formulasi meliputi:
1. Penentuan bahan yang dipakai.
2. Trial formula.
3. Menyusun spesifikasi bahan baku dan produk.
4. Pembuatan master formula, dokumen catatan produksi dari setiap formula.
5. Menyusun metode analisis bahan baku, produk antara, produk ruahan dan
produk jadi.
6. Memonitor stabilitas dari hasil trial tiga bets pertama.
7. Validasi formula dengan cara validasi prospektif (validasi tiga bets pertama).
D. Seksi Registrasi
Seluruh bagian pengembangan produk bekerja sama menyiapkan data
registrasi obat ke Badan POM. Bentuk aplikasinya meliputi:
2. Proses pembuatan
3. Metode analisa
4. Artwork dari desain kemasan
5. Data stabilitas
6. Referensi (literature)
7. Hasil uji klinis
8. Data farmakologi
E. Seksi Pengembangan Kemasan
Prinsip pengembangan kemasan berdasarkan efisiensi bahan kemas,
sehingga dapat meminimalkan biaya produksi. Dalam mengembangkan kemasan,
faktor-faktor yang diperhatikan antara lain:
1. Melihat dari kompetitor
2. Hasil uji stabilitas
3. Kondisi penyimpanan
4. Sifat produk
5. Sifat bahan
Untuk obat-obat generik, desain kemasan telah ditentukan oleh pemeritah
berdasarkan Surat Keputusan Dirjen POM No. 01542/A/SK/VI/90 tanggal 21
Juni 1990.
3.1.1.6Bidang pengawasan mutu/Quality Control (QC) Bidang ini terdiri dari
A. Seksi Pengujian Bahan Awal
Pemeriksaan bahan awal dimulai dari gudang, yaitu bahan masuk digudang
tersebut memenuhi syarat (diterima) atau tidak memenuhi syarat (ditolak). Seksi
pengujian Bahan Awal melakukan pengujian bahan baku, air dan bahan
pengemas.
1. Bahan baku, dimulai dari kegiatan sampling sampai dengan pengujiannya.
a. Di cek label dari pabrik yang meliputi berat bersih, nomor lot, tanggal
pembuatan, expired date (ED), dan logistik.
b. Dicek label karantina digudang meliputi nama barang, nomor kode, nomor
batch, tanggal dibuat, jumlah, tanggal sampling, dan paraf.
c. Sampel diidentifikasi secara fisika atau organoleptis meliputi bau, rasa,
dan warna.
d. Sampel diidentifikasi secara kimia seperti pengujian kadar dan porensi.
e. Uji lain, antara lain meliputi tes kemurnian, pH, dan kadar air.
2. Air, digunakan oleh bidang produksi yang pengujiannya meliputi pH,
kandungan mineral, dan cemaran mikroorganisme.
3. Bahan pengemas, terdiri dari Aproved art work dan prove print (printed
material) untuk suplaier.
Pengemas berhubungan dengan stabilitas obat yang berfungsi melindungi
obat terhadap kelembaban, iklim dan benturan. Selain itu kemasan juga
mempengaruhi daya tarik konsumen terhadap produk.
Produk ruahan yang akan dikemas dan bahan kemas yang diterima dari
gudang pengemasan semuanya sudah diluluskan oleh bidang Quality Assurance
(QA). Proses pengemasan dapat berupa pengisian ke botol, stripping dan sachet.
Jenis pengemas yang digunakan disesuaikan dengan sifat produk ruahan dan
Bahan pengemas dibedakan menjadi tiga macam, yaitu:
1. Bahan pengemas primer, bahan pengemas yang langsung
berhubungan dengan produk seperti tube, botol, ampul, stripping dan blister.
Uji yang dilakukan meliputi :
a. Alumunium foil, tes terhadap elastisitas
(kekuatan tekanan), stripping (suhu 150o C), lebar, penandaan, nomor
register, tulisan dan nama.
b. Tube, meliputi uji kebocoran warna atau cat,
berat, ukuran tebal badan, dan uji kebocoran membran.
c. Ampul, meliputi diameter, kebocoran, tinggi
pemotongan ampul, tinggi badan, keretakan, dan ketebalan kaca.
d. Botol, yaitu diameter, tinggi, ketebalan
dinding botol, kesetaraan volume, keseragaman bobot dan kebocoran.
2. Bahan pengemas sekunder, bahan pengemas yang tidak
berhubungan langsung dengan produk obat, tapi berhubungan dengan
pengemas primer seperti dus ampul dan kotak botol. Uji yang dilakukan
terhadap kotak atau dus meliputi ukuran, panjang, lebar, tinggi, tulisan, bobot,
dan daya rekat.
3. Bahan pengemas tersier, bahan pengemas yang berhubungan langsung dengan
pengemas sekunder misalnya karton. Uji yang dilakukan terhadap karton
meliputi panjang, lebar, tinggi, dan tulisan.
B. Seksi Pengujian Mikrobiologi
Pemeriksaan mikrobiologi adalah pengujian yang menggunakan jasad renik
sejauh mana suatu produk atau penunjang produksi (bahan awal, peralatan,
operator, ruangan) telah memenuhi syarat mikrobiologi.
Sumber kontaminasi mikrobiologi ada tiga, yaitu :
1. Air, yang berasal dari tanah, air hujan, dan tanaman yang membusuk
2. Peralatan, yang disebabkan karena proses pembersihan yang tidak sempurna,
pencucian dengan air yang tidak memenuhi persyaratan, dan debu yang
melekat.
3. Operator, yang berasal dari keringat, hidung (nafas), dan air ludah.
C. Seksi IPC dan Pengujian Produk
Tugas seksi IPC dan Pengujian Produk meliputi pengujian terhadap produk
antara dan produk ruahan. Macam pengujian yang dilakukan adalah:
1. Tablet
Produk antara, uji yang dilakukan adalah identifikasi, distribusi partikel atau
ukuran partikel, bulk density, tapping density, waktu alir serbuk, dan kadar zat
aktif.
Produk ruahan, uji yang dilakukan yaitu keseragaman bobot, waktu hancur,
kekerasan, diameter atau tebal, kadar zat aktif, dan disolusi.
2. Kapsul
Produk antara, uji yang dilakukan yaitu keseragaman bobot, waktu hancur,
kekerasan, diameter atau tebal, kadar zat aktif, dan disolusi.
Produk ruahan, uji yang dilakukan yaitu keseragaman bobot, waktu hancur,
kadar zat aktif, dan disolusi.