LAPORAN PRAKTEK KERJA PROFESI APOTEKER
FARMASI INDUSTRI
Di
PT. INDOFARMA (Persero) Tbk.
Jalan Indofarma No. 1, Cikarang Barat 17530, Bekasi
(3 – 31 Oktober 2011)
Disusun Oleh:
Pipi Saputri, S.Farm. NIM 103202102
PROGRAM STUDI PENDIDIKAN PROFESI APOTEKER
FAKULTAS FARMASI
KATA PENGANTAR
Puji syukur kepada Tuhan Yang Maha Esa atas segala karunia-Nya
sehingga kami dapat menyelesaikan Pelatihan Praktek Kerja Profesi Apoteker
(PPKPA) dan penyusunan laporan umum praktek kerja di industri farmasi PT.
Indofarma (Persero) Tbk. periode 3-31 Oktober 2011.
Praktek Kerja Profesi di PT. Indofarma (Persero) Tbk. memberikan
pengetahuan kepada penulis tentang kegiatan yang ada di industri farmasi secara
menyeluruh dan terpadu. PPKPA ini juga merupakan salah satu syarat yang harus
dipenuhi oleh mahasiswa Program Profesi Apoteker Fakultas Farmasi Universitas
Sumatera Utara.
Penulis mendapatkan banyak bantuan dan dukungan dari berbagai pihak
dalam pelaksanaan dan penyusunan Laporan Praktek Kerja Profesi Apoteker ini,
untuk itu penulis mengucapkan terima kasih kepada:
1. Bapak Drs. Placidus Sudibyo, M.S., Ak., selaku Direktur Utama PT.
Indofarma (Persero) Tbk. yang telah memberikan kesempatan kepada penulis
untuk melakukan PPKPA.
2. Bapak Hugo Koen Christanto, S.Si., Apt., selaku pembimbing PPKPA di PT.
Indofarma (Persero) Tbk. yang banyak memberikan bimbingan dan masukan
kepada penulis.
3. Bapak Yupi Gantina, selaku koordinator PPKPA di PT. Indofarma (Persero)
Tbk.
4. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah memberikan kesempatan kepada
penulis dalam melaksanakan PPKPA ini.
5. Seluruh staf & karyawan di PT. Indofarma (Persero) Tbk. Atas bantuannya
selama penulis mengikuti kegiatan PPKPA.
6. Bapak dan ibu dosen Fakultas Farmasi yang telah memberikan pembekalan
dalam rangka pelaksanaan PPKPA di industri farmasi.
7. Seluruh keluarga, terutama orang tua yang selalu berdoa untuk penulis,
8. Rekan–rekan PPKPA angkatan 64 dari Universitas Pancasila, UAD, UNAND,
UWM, Uhamka, UII, UMS, UBAYA dan ISTN, terima kasih untuk kerjasama
dan kenangannya.
Penulis berharap semoga pengetahuan dan pengalaman yang didapat selama
PPKPA di industri farmasi yaitu di PT. Indofarma (Persero) Tbk. ini bermanfaat
sebagai bekal untuk menjalankan pengabdian profesi Apoteker khususnya di
industri farmasi dan juga bermanfaat bagi para pembaca.
Cibitung, Januari 2012
Penulis
DAFTAR ISI
Halaman
Kata Pengantar ... iii
Daftar Isi ... v
Daftar Gambar ... ix
Daftar Lampiran ... x
Ringkasan ... xi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan Pelatihan Praktek Kerja Profesi Apoteker (PPKPA) ... 3
1.3Pelaksanaan Pelatihan Praktek Kerja Profesi Apoteker (PPKPA) ... 3
1.4 Manfaat Pelatihan Praktek Kerja Profesi Apoteker (PPKPA) ... 4
BAB II TINJAUAN UMUM PT. INDOFARMA (Persero) Tbk ... 5
2.1 Industri Farmasi ... 5
2.1.1 Pengertian Industri Farmasi ... 5
2.1.2 Persyaratan Industri Farmasi ... 5
2.1.3 Izin Usaha Industri Farmasi ... 6
2.2 Cara Pembuatan Obat yang Baik (CPOB) ... 6
2.2.1 Manajemen Mutu ... 7
2.2.2 Personalia ... 8
2.2.4 Peralatan ... 10
2.2.9 Penanganan Keluhan terhadap Produk, Penarikan kembali Produk dan Produk kembalian ... 15
2.2.10 Dokumentasi ... 16
2.2.11 Pembuatan dan Analisis berdasarkan Kontrak ... 16
2.2.12 Kualifikasi dan Validasi ... 16
2.2.12.1 Kualifikasi ... 16
2.2.12.2 Validasi ... 18
BAB III TINJAUAN DAN RUANG LINGKUP PT. INDOFARMA (Persero) Tbk ... 20
3.1 Sejarah dan Perkembangan PT. Indofarma (Persero) Tbk. . 20
3.2 Visi, Misi, Motto dan Logo PT. Indofarma (Persero) Tbk . 23 3.3 Nilai Budaya yang Dikembangkan PT. Indofarma (Persero) Tbk ... 24
3.4 Kebijakan Mutu PT. Indofarma (Persero) Tbk. ... 25
3.5 Kedudukan, Fungsi dan Peranan PT. Indofarma (Persero) Tbk. ... 26
3.6 Lokasi dan Bangunan ... 27
3.7 Produk PT. Indofarma (Persero) Tbk. ... 28
3.8.1 Direktorat Produksi ... 30
3.8.1.1 Bidang Production Planning and Inventory Control (PPIC) atau PPPP (Perencanaan Produksi dan Pengendalian Persediaan ... 30
3.8.1.2 Produksi I ... 34
3.8.1.3 Produksi II ... 41
3.8.1.4 Bidang Penelitian dan Pengembangan (Litbang) Produk ... 49
3.8.1.5 Bidang Pengawasan Mutu/Quality Control (QC) ... 52
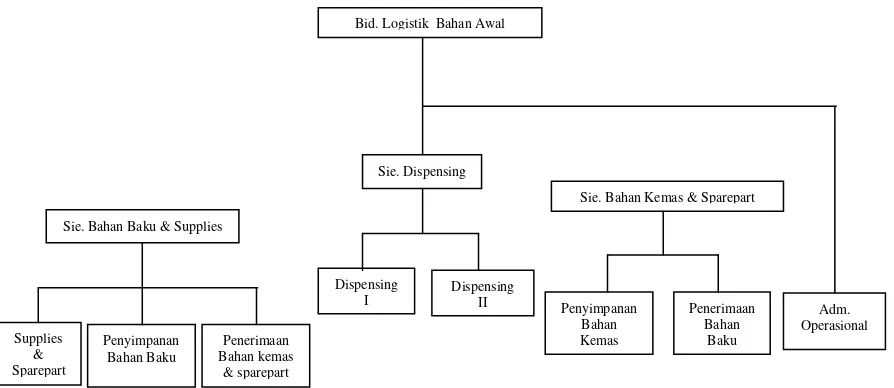
3.8.1.6 Bidang Logistik Bahan Awal ... 57
3.8.1.7 Teknik dan Pemeliharaan ... 60
3.8.2 Direktorat Riset dan Pemasaran ... 64
3.8.2.1 Bidang Logistik Produk Jadi (LPJ) ... 65
3.8.3 Direktorat Keuangan dan Sumber Daya Manusia ... 66
3.8.3.1 Bidang SDM ... 66
3.8.3.2 Bidang Umum ... 66
3.8.3.3 Bidang Akuntansi ... 72
3.8.3.4 Bidang Keuangan ... 72
4.2.4 Peralatan ... 80
4.2.5 Sanitasi dan Higiene ... 81
4.2.6 Produksi ... 82
4.2.7 Pengawasan Mutu/Quality Control (QC) ... 87
4.2.8 Inspeksi Diri ... 88
4.2.9 Penanganan Keluhan terhadap Obat, Penarikan kembali Produk dan Produk kembalian ... 88
4.2.10 Dokumentasi ... 89
4.2.11 Pembuatan dan Analisa berdasarkan Kontrak ... 90
4.2.12 Kualifikasi dan Validasi ... 90
4.2.13 Sistem Pengelolaan Lingkungan ... 90
BAB V KESIMPULAN DAN SARAN ... 92
5.1 Kesimpulan ... 92
5.2 Saran ... 92
DAFTAR PUSTAKA ... 94
DAFTAR GAMBAR
Gambar Halaman
1 Logo PT. Indofarma (Persero) Tbk. ... 24
2 Struktur Organisasi PT. Indofarma (Persero) Tbk. ... 29
3 Hubungan Kerja Bidang PPPP dengan Bidang Lain di PT. Indofarma (Persero) Tbk. ... 31
4 Alur Proses Perencanaan ... 32
5 Alur Proses Pengendalian Produksi ... 33
DAFTAR LAMPIRAN
Lampiran Halaman
1 Tata Letak Bangunan PT. Indofarma (Persero) Tbk. ... 96
3 Bagan Sistem Pengolahan Air di PT. Indofarma
(Persero) Tbk. ... 98
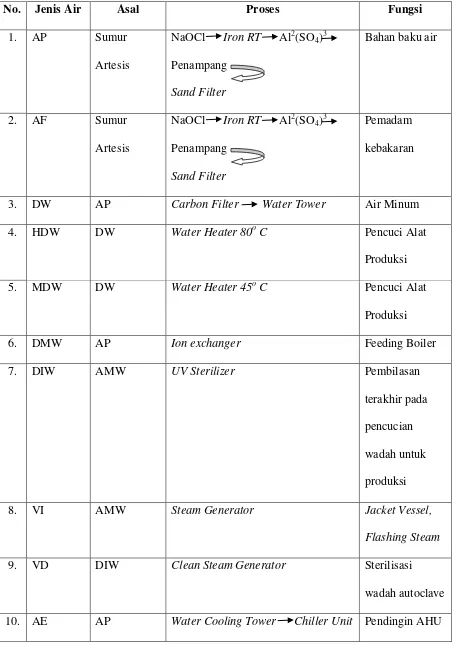
4 Tabel Instalasi Pengolahan Air di PT. Indofarma
(Persero) Tbk. ... 99
5 Bagan Sistem Pengaturan Udara PT. Indofarma
(Persero) Tbk ... 101
6 Bagan Sistem Instalasi Pengolahan Air Limbah
RINGKASAN
Telah dilakukan Pelatihan Praktek Kerja Profesi Apoteker (PPKPA) di PT.
Indofarma (Persero) Tbk. Cibitung - Bekasi. Berlangsung pada tanggal 3-31
Oktober 2011. Praktek Kerja Profesi ini bertujuan mendidik calon Apoteker
mampu memahami tugas dan fungsi Apoteker serta penerapan CPOB (Cara
Pembuatan Obat yang Baik) di industri farmasi. Hal ini diharapkan dapat menjadi
bekal bagi penulis untuk menghadapi dunia kerja sehingga dapat melaksanakan
profesi secara baik. Kegiatan PPKPA di PT. Indofarma (Persero) Tbk. meliputi
RINGKASAN
Telah dilakukan Pelatihan Praktek Kerja Profesi Apoteker (PPKPA) di PT.
Indofarma (Persero) Tbk. Cibitung - Bekasi. Berlangsung pada tanggal 3-31
Oktober 2011. Praktek Kerja Profesi ini bertujuan mendidik calon Apoteker
mampu memahami tugas dan fungsi Apoteker serta penerapan CPOB (Cara
Pembuatan Obat yang Baik) di industri farmasi. Hal ini diharapkan dapat menjadi
bekal bagi penulis untuk menghadapi dunia kerja sehingga dapat melaksanakan
profesi secara baik. Kegiatan PPKPA di PT. Indofarma (Persero) Tbk. meliputi
BAB I PENDAHULUAN
1.1 Latar belakang
Pembangunan kesehatan merupakan salah satu bagian dari pembangunan
nasional. Tujuan pembangunan kesehatan adalah tercapainya kemampuan untuk
hidup sehat bagi setiap penduduk agar dapat mewujudkan derajat kesehatan yang
optimal, baik secara jasmani, rohani dan sosial sebagai salah satu unsur
kesejahteraan umum. Upaya-upaya peningkatan kesehatan yang optimal pada
masyarakat dilakukan melalui peningkatan kesehatan (promotif), pencegahan
penyakit (preventif), penyembuhan penyakit (kuratif) dan pemulihan kesehatan
(rehabilitatif).
Sarana-sarana yang mendukung diperlukan dalam menyelenggarakan
upaya-upaya tersebut. Undang-Undang Republik Indonesia No. 36 tahun 2009
pasal 56 menyebutkan bahwa salah satu sarana kesehatan adalah pabrik obat atau
industri farmasi. Industri farmasi merupakan salah satu elemen penting dalam
mewujudkan kesehatan nasional melalui aktivitasnya dalam bidang produksi obat.
Tingginya kebutuhan obat dalam dunia kesehatan dan vitalnya aktivitas obat
mempengaruhi fungsi fisiologi tubuh manusia, sehingga melahirkan sebuah
tuntutan terhadap industri farmasi agar mampu memproduksi obat yang
berkualitas, aman dan efektif. Oleh karena itu, semua industri farmasi harus
berupaya agar dapat menghasilkan produk obat yang memenuhi standar kualitas
Upaya yang dilakukan industri farmasi dalam rangka meningkatkan
kualitas obat yang diproduksi salah satunya yaitu dengan menerapkan GMP (Good
Manufacturing Practise). Istilah GMP di Indonesia lebih dikenal dengan CPOB
(Cara Pembuatan Obat yang Baik) yang dinamis. CPOB memberi pedoman semua
aspek yang berhubungan dengan produksi dan pengendalian mutu obat
diperhatikan dan ditentukan sedemikian rupa dengan tujuan untuk menjamin
bahwa produk obat dibuat senantiasa memenuhi persyaratan mutu yang telah
ditentukan sesuai dengan tujuan penggunaannya. Mutu obat dipengaruhi dari
beberapa aspek, yaitu bahan awal, personalia, bangunan dan fasilitas, peralatan,
sanitasi dan higiene, inspeksi diri, pengawasan mutu, penanganan keluhan
terhadap obat, penarikan kembali obat dan dokumentasi.
Industri farmasi sebagai produsen obat mempunyai kewajiban moral dan
tanggung jawab sosial untuk senantiasa menghasilkan obat yang bermutu serta
aman saat digunakan maupun disimpan. Upaya pemerintah untuk memenuhi
tersedianya obat bermutu yang terjangkau oleh masyarakat salah satu diantaranya
adalah menunjuk PT. Indofarma (Persero) Tbk. yang bergerak di bidang farmasi
untuk memproduksi obat yang bermutu dengan harga yang kompetitif. Bentuk
nyata dari program tersebut adalah tersedianya obat generik berlogo (OGB) yang
diserahkan kepada PT. Indofarma (Persero) Tbk. untuk memproduksinya. PT.
Indofarma (Persero) Tbk. juga merupakan Techin factory yang terbuka dan
mempunyai tugas untuk menyelenggarakan pendidikan bagi masyarakat, salah
satunya dengan mengadakan kegiatan Pelatihan Praktek Kerja Profesi Apoteker
(PPKPA) bagi calon Apoteker sebagai bekal pengetahuan untuk terjun ke dunia
1.2 Tujuan
Tujuan diadakan Pelatihan Praktek Kerja Profesi Apoteker (PPKPA)
adalah:
1. Melihat gambaran nyata peran Apoteker dan penerapan CPOB di industri
farmasi.
2. Mengetahui dan memahami dasar-dasar pengelolaan industri farmasi dan
keterkaitannya dengan profesi lain.
3. Membantu mahasiswa dalam membekali diri dengan pengetahuan dan
keterampilan untuk memasuki dunia kerja, khususnya di industri farmasi.
1.3 Pelaksanaan
PPKPA dilaksanakan mulai tanggal 3 - 31 Oktober 2011. Kegiatan yang
dilaksanakan antara lain:
1. Tutorial yang diadakan oleh bidang Umum, Perencanaan Produksi dan
Pengendalian Persediaan (PPPP), Strategi dan Pengembangan Produk dan
Bisnis (Strategic Business Development/SBD), Lingkungan dan Keselamatan
Kesehatan Kerja (LK-3), Produksi, Pelaksanaan Program Kemitraan dan Bina
Lingkungan (PKBL), Logistik Bahan Awal (LBA), Sumber Daya Manusia
(SDM), Pengadaan (Procurement), Penelitian dan Pengembangan/Litbang
(R&D), Quality Assurance (QA), Quality Control (QC), Teknik dan
Pemeliharaan/Utilities.
2. Tinjauan ke Lapangan
3. Pelaksanaan Tugas Khusus pada salah satu bidang di PT. Indofarma (Persero)
4. Presentasi hasil tugas khusus
1.4 Manfaat
Melalui materi dan praktek yang diperoleh selama PPKPA ini diharapkan
dapat memantapkan pemahaman serta penerapan ilmu yang telah diperoleh
BAB II
TINJAUAN PUSTAKA
2.1 Industri Farmasi
2.1.1 Pengertian Industri Farmasi
Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik
Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri obat jadi dan
industri bahan baku obat. Industri obat jadi adalah industri yang memproduksi
suatu produk obat yang telah melalui seluruh tahap proses pembuatan, sistem
fisiologis atau keadaan patologi dalam rangka penetapan diagnosis,
pencegahan, penyembuhan, pemulihan, peningkatan kesehatan dan kontrasepsi.
Industri bahan baku adalah industri yang memproduksi bahan baku dimana bahan
baku tersebut adalah seluruh bahan, baik berkhasiat ataupun tidak berkhasiat.
2.1.2 Persyaratan Industri Farmasi
Perusahaan industri farmasi wajib memperoleh izin usaha industri farmasi,
karena itu industri tersebut wajib memenuhi persyaratan yang telah ditetapkan
oleh Menteri Kesehatan. Persyaratan industri farmasi tercantum dalam Surat
Keputusan Menteri Kesehatan RI No. 245//Menkes/SK/V/1990 adalah sebagai
berikut:
a.Industri farmasi merupakan suatu perusahaan umum, badan hukum berbentuk
Perseroan Terbatas atau Koperasi.
b. Memiliki rencana investasi.
c. Memiliki Nomor Pokok Wajib Pajak (NPWP).
CPOB sesuai dengan ketentuan SK Menteri Kesehatan
No.43/Menkes/SK/II/1988.
e. Industri farmasi obat jadi dan bahan baku wajib mempekerjakan secara tetap
sekurang-kurangnya dua orang Apoteker warga negara Indonesia
masing-masing sebagai penanggung jawab produksi dan penanggung jawab
pengawasan mutu sesuai dengan persyaratan CPOB.
f. Obat jadi yang diproduksi oleh industri farmasi hanya dapat diedarkan
setelah memperoleh izin edar sesuai dengan ketentuan perundang-undangan
yang berlaku.
2.1.3 Izin usaha industri farmasi
Izin usaha industri farmasi diberikan oleh Menteri Kesehatan dan
wewenang pemberian izin dilimpahkan kepada Badan Pengawasan Obat dan
Makanan (BPOM). Izin ini berlaku seterusnya selama industri tersebut
berproduksi dengan perpanjangan izin setiap 5 tahun, sedangkan untuk industri
farmasi Penanaman Modal Asing (PMA) masa berlakunya sesuai dengan
ketentuan dalam Undang-Undang No. 1 Tahun 1967 tentang PMA dan
pelaksanaannya.
2.2 Cara Pembuaran Obat yang Baik (CPOB)
CPOB merupakan pedoman yang harus diterapkan dalam seluruh
rangkaian proses di industri farmasi dalam pembuatan obat jadi, sesuai dengan
keputusan Menteri Kesehatan RI No. 43/Menkes/SK/II/1988 tentang Cara
Pembuatan Obat yang Baik. Pedoman CPOB bertujuan untuk menghasilkan
produk obat yang senantiasa memenuhi persyaratan mutu yang telah ditetapkan
Obat yang berkualitas adalah obat jadi yang benar-benar dijamin bahwa
obat tersebut:
- Mempunyai potensi atau kekuatan untuk dapat digunakan sesuai tujuannya.
- Memenuhi persyaratan keseragaman, baik isi maupun bobot.
- Memenuhi syarat kemurnian.
- Memiliki identitas dan penandaan yang jelas dan benar.
- Dikemas dalam kemasan yang sesuai dan terlindung dari kerusakan dan
kontaminasi.
- Penampilan baik, bebas dari cacat atau rusak.
Perkembangan yang sangat pesat dalam teknologi farmasi menyebabkan
perubahan-perubahan yang sangat cepat pula dalam konsep serta persyaratan
CPOB. Konsep CPOB yang bersifat dinamis yang memerlukan penyesuaian dari
waktu ke waktu mengikuti perkembangan teknologi di bidang farmasi.
Aspek-aspek yang merupakan cakupan CPOB tahun 2006 meliputi 12 aspek yang
dibicarakan.
2.2.1 Manajemen Mutu
Industri farmasi harus membuat obat sedemikian rupa agar sesuai dengan
tujuan penggunaannya, memenuhi persyaratan yang tercantum dalam dokumen
izin edar (registrasi) dan tidak menimbulkan resiko yang membahayakan
penggunanya karena tidak aman, mutu rendah atau tidak efektif. Manajemen
bertanggung jawab untuk mencapai tujuan ini melalui suatu “kebijakan mutu”
yang memerlukan partisipasi dan komitmen dari semua jajaran departemen di
dalam perusahaan, para pemasok dan para distributor. Manajemen mutu yang
mencapai tujuan mutu secara konsisten dan dapat diandalkan.
Unsur dasar manajemen mutu adalah:
1. Suatu infrastruktur atau sistem mutu yang tepat mencakup struktur organisasi,
prosedur, proses dan sumber daya.
2. Tindakan sistematis diperlukan untuk mendapatkan kepastian dengan tingkat
kepercayaan yang tinggi, sehingga produk (jasa pelayanan) yang dihasilkan
akan selalu memenuhi persyaratan yang telah ditetapkan. Keseluruhan tindakan
tersebut disebut Pemastian Mutu.
Sistem pemastian mutu hendaklah didukung dengan tersedianya personil
yang kompeten, bangunan dan sarana serta peralatan yang cukup dan memadai.
Tambahan tanggung jawab hukum hendaklah diberikan kepada kepala bagian
manajemen mutu (Pemastian Mutu).
Pemastian Mutu adalah totalitas semua pengaturan yang dibuat dengan
tujuan untuk memastikan bahwa obat dihasilkan dengan mutu yang sesuai dengan
tujuan pemakaiannya.
2.2.2 Personalia
Jumlah personil di semua tingkat harus memadai serta memiliki
pengetahuan, keterampilan dan kemampuan yang sesuai dengan tanggung
jawabnya. Kesehatan mental dan fisik yang baik harus dimiliki personil agar
mampu melaksanakan tugas secara profesional dan hendaklah memiliki sikap dan
kesadaran tinggi untuk mewujudkan CPOB.
2.2.3 Bangunan dan Fasilitas
Bangunan untuk pembuatan obat hendaklah memiliki ukuran, rancangan,
pembersihan dan pemeliharaan, tiap sarana kerja hendaklah memadai sehingga
setiap resiko terjadi kekeliruan, pencemaran silang dan berbagai kesalahan lain
yang dapat menurunkan mutu obat dapat dihindarkan. Hal-hal yang perlu
diperhatikan antara lain:
1. Lokasi bangunan hendaklah dapat mencegah terjadinya pencemaran dari
lingkungan sekelilingnya seperti pencemaran udara, tanah dan air maupun
kegiatan di sekitarnya.
2. Bangunan dirancang dengan baik sehingga dapat terpelihara dan berfungsi
sebagaimana mestinya:
a. Permukaan bagian dalam harus licin, bebas dari keretakan dan sambungan
terbuka serta mudah dibersihkan dan didesinfeksi. Lantai terbuat dari
bahan kedap air, permukaan rata yang memudahkan proses pembersihan
secara cepat dan efisien. Dinding
b. Penataan ruangan disesuaikan dengan tujuan penggunaan, seperti ruang
steril dipisahkan dari ruang produksi lain serta dirancang secara khusus.
Ruangan khusus diperlukan bagi kegiatan pembukaan kemasan, pencucian,
pengolahan dan penutupan wadah, ruangan penyangga udara dan pergantian
pakaian steril.
kedap air dan mudah dicuci. Sudut
dinding hendaklah berbentuk lengkungan. Bangunan hendaklah
mendapatkan penerangan yang efektif dan mempunyai ventilasi yang sesuai.
c. Adanya perbedaan kelas pemisahan ruang di dalam bangunan produksi,
misalnya ruang untuk bahan baku, kamar ganti pakaian dan pengolahan
produksi.
kelembaban dan keamanan tertentu. Pencampuran hendaklah dihindari
dalam proses penyimpanan.
e. Kondisi bangunan diperiksa secara teratur dan dilakukan perbaikan bila
diperlukan.
f. Lubang pemasukan dan pengeluaran udara serta pipa dipasang sedemikian
rupa untuk mencegah timbulnya pencemaran produk.
3. Saluran air limbah hendaklah cukup besar dan mempunyai bak kontrol serta
ventilasi yang baik.
4. Tenaga listrik, suhu, kelembaban dan ventilasi harus tepat supaya tidak
mengakibatkan dampak yang merugikan baik secara langsung ataupun tidak
langsung terhadap produk selama proses pembuatan dan penyimpanan.
2.2.4 Peralatan
Peralatan yang digunakan dalam pembuatan obat hendaklah memiliki
rancangan bangunan dan konstruksi yang tepat, ukuran yang memadai serta
ditempatkan dengan tepat sehingga mutu setiap produk obat terjamin secara
seragam dari bets ke bets serta untuk memudahkan pembersihan dan
perawatannya.
1. Rancang Bangun dan Konstruksi
a. Peralatan yang digunakan tidak bereaksi atau menimbulkan akibat terhadap
bahan yang diolah.
b. Peralatan hendaklah mudah dibersihkan baik bagian dalam maupun bagian
luarnya.
c. Peralatan yang digunakan untuk menimbang, mengukur, menguji dan
menurut program dan prosedur yang tepat, hasil pemeriksaannya dicatat
dan disimpan dengan baik.
d. Penyaring untuk cairan tidak boleh melepaskan serat ke dalam produk dan
tidak boleh mengandung asbes.
2. Pemasangan dan Penempatan
a. Peralatan hendaklah ditempatkan pada posisi yang tepat untuk memperkecil
pencemaran silang antar bahan. Peralatan ditempatkan dengan jarak yang
cukup renggang untuk memberikan keleluasaan kerja.
b. Peralatan utama diberi nomor pengenal yang dipakai pada semua perintah
dan catatan pembuatan bets untuk menunjukkan unit atau alat tertentu.
c. Semua pipa, tangki, selubung hendaknya diberikan pelekat untuk
memperkecil kehilangan energi.
d. Saluran pipa yang menggunakan uap bertekanan hendaknya dilengkapi
dengan peralatan uap dan saluran pembuangan yang berfungsi dengan
baik.
e. Sistem penunjang hendaknya divalidasi untuk memastikan fungsinya sesuai
tujuannya.
3. Pemeliharaan
a. Peralatan hendaknya dirawat sesuai jadwal yang tepat agar berfungsi
dengan baik dan mencegah pencemaran.
b. Prosedur-prosedur tertulis untuk peralatan dibuat dan dipatuhi.
c. Catatan pelaksanaan pemeliharaan pemakaian peralatan utama hendaklah
khusus untuk satu produk saja dapat dimasukkan ke catatan produksi bets
produk tertentu.
2.2.5 Sanitasi dan Higiene
Tingkat sanitasi dan higiene yang tinggi hendaklah diterapkan pada setiap
aspek pembuatan obat. Ruang lingkup sanitasi dan higiene meliputi personalia,
bangunan, peralatan dan perlengkapan, bahan produksi serta wadahnya dan setiap
hal yang merupakan sumber pencemaran produk. Sumber pencemaran hendaknya
dihilangkan melalui suatu program sanitasi dan higiene yang menyeluruh dan
terpadu.
2.2.6 Produksi
Produksi hendaklah dilaksanakan dengan mengikuti prosedur yang telah
ditetapkan dan memenuhi ketentuan CPOB yang menjamin senantiasa
menghasilkan produk yang memenuhi persyaratan mutu serta memenuhi
ketentuan izin pembuatan dan izin edar (registrasi).
Prinsip utama produksi adalah:
- Adanya keseragaman atau homogenitas dari bets ke bets.
- Proses produksi dan pengemasan senantiasa menghasilkan produk yang
seidentik mungkin (dalam batas syarat mutu) baik bagi bets yang sudah
diproduksi maupun yang akan diproduksi.
Prosedur produksi dibuat oleh penanggung jawab produksi bersama
dengan penanggung jawab pengawasan mutu yang dapat menjamin obat yang
dihasilkan memenuhi spesifikasi yang dibutuhkan. M utu produk yang dihasilkan
sangat ditentukan oleh bahan awal, proses produksi, personil dan sistem
Penyimpanan tergantung dari kestabilan bahan awal. Ruangan
penyimpanan hendaklah tersedia dengan suhu yang berbeda-beda. CPOB
mempersyaratkan klasifikasi ruangan berdasarkan suhu menjadi 5 jenis, yaitu:
- Suhu ruangan: 15-30oC
- Suhu ruangan yang dikendalikan: ≤ 25oC
- Sejuk: 8-15oC
- Dingin: 2-8oC
- Beku: dibawah 0oC
Tekanan udara dalam ruangan yang memiliki resiko lebih tinggi
terhadap suatu produk hendaklah selalu lebih tinggi daripada ruangan lain. Bila
suatu pintu dibuka, tekanan atau hembusan udara dari arah ruangan yang beresiko
tinggi hendaklah cukup mampu untuk menciptakan arus udara ke arah ruang yang
beresiko lebih rendah untuk menghindarkan pencemaran balik.
2.2.7 Pengawasan Mutu
Pengawasan mutu merupakan bagian yang esensial dari cara pembuatan
obat yang baik untuk memberikan kepastian bahwa produk secara konsisten
mempunyai mutu yang sesuai dengan tujuan pemakaiannya. Pengawasan mutu
hendaklah mencakup semua kegiatan analitis yang dilakukan di laboratorium,
termasuk pengambilan sampel, pemeriksaan dan pengujian bahan awal, produk
antara, produk ruahan dan produk jadi. Kegiatan ini juga mencakup uji stabilitas,
program pemantauan lingkungan, pengujian yang dilakukan dalam rangka
validasi, penanganan sampel pertinggal, menyusun dan memperbaharui
Laboratorium pengawasan mutu hendaklah terpisah secara fisik dari ruang
produksi. Laboratorium untuk pengawasan selama proses mungkin lebih
memudahkan apabila letaknya di daerah tempat pemprosesan atau pengemasan
dimana dilakukan pengujian fisik seperti penimbangan dan uji monitoring lainnya
secara periodik.
Dokumentasi dan prosedur pelulusan yang diterapkan bagian pengawasan
mutu hendaklah menjamin bahwa pengujian yang diperlukan telah dilakukan
sebelum bahan digunakan dalam produksi dan produk disetujui sebelum
didistribusikan. Personil pengawasan mutu hendaklah memiliki akses ke area
produksi untuk melakukan pengambilan sampel dan investigasi bila diperlukan.
2.2.8 Inspeksi Diri dan Audit Mutu 2.2.8.1Inspeksi Diri
Tujuan inspeksi diri adalah untuk mengevaluasi apakah semua aspek
produksi dan pengawasan mutu industri farmasi memenuhi ketentuan CPOB.
Program inspeksi diri hendaklah dirancang untuk mendeteksi kelemahan dalam
pelaksanaan CPOB dan untuk menetapkan tindakan perbaikan yang diperlukan.
Inspeksi diri dilakukan secara indepeden dan rinci oleh petugas yang kompeten
dari perusahaan. Inspeksi diri dilakukan secara rutin dan disamping itu, pada
situasi khusus, misalnya dalam hal terjadi penarikan kembali obat jadi atau terjadi
penolakan yang berulang. Prosedur dan catatan inspeksi diri hendaklah
didokumentasikan dan dibuat program tindak lanjut yang efektif.
Inspeksi meliputi personil, bangunan, penyimpanan, bahan awal, obat jadi,
produksi, pengawasan mutu, dokumentasi dan pemeliharaan gedung serta
2.2.8.2Audit Mutu
Penyelenggaraan audit mutu berguna sebagai pelengkap inspeksi diri.
Audit mutu meliputi pemeriksaan dan penilaian semua atau sebagian dari sistem
manajemen mutu dengan tujuan spesifik untuk meningkatkan mutu.
Audit mutu umumnya dilaksanakan oleh spesialis dari luar atau
independen atau tim yang dibentuk khusus oleh manajemen perusahaan. Audit
mutu juga dapat diperluas terhadap pemasok dan penerima kontrak.
2.2.9 Penanganan Keluhan terhadap Produk, Penarikan Kembali Produk dan Produk Kembalian
Penarikan kembali produk adalah suatu proses penarikan kembali dari satu
atau beberapa bets atau seluruh bets produk tertentu dari rantai distribusi karena
keputusan bahwa produk tidak layak lagi untuk diedarkan.
Produk kembalian adalah obat jadi yang telah keluar dari industri atau
beredar, yang kemudian dikembalikan ke industri karena kerusakan, daluwarsa,
atau alasan lain misalnya kondisi wadah atau kemasan yang dapat menimbulkan
keraguan identitas, mutu, keamanan obat serta kesalahan administratif yang
menyangkut jumlah dan jenis.
Keluhan dan informasi lain yang berkaitan dengan kemungkinan terjadi
kerusakan obat, dapat bersumber dari dalam maupun dari luar industri, dan
memerlukan penanganan serta pengkajian secara teliti. Keluhan atau informasi
yang bersumber dari dalam industri antara lain dari bagian produksi,
pengawasan mutu, gudang dan pemasaran, sementara dari luar industri antara
lain dapat berasal dari pasien, dokter, paramedik, klinik, rumah sakit, apotek,
2.2.10 Dokumentasi
Dokumentasi adalah bagian dari sistem informasi manajemen dan
merupakan bagian yang esensial dari pemastian mutu. Sistem dokumentasi yang
dirancang atau digunakan hendaklah mengutamakan tujuannya, yaitu
menentukan, memantau dan mencatat seluruh aspek produksi serta
pengendalian dan pengawasan mutu. Dokumentasi sangat penting untuk
memastikan bahwa setiap petugas mendapat instruksi secara rinci dan jelas
mengenai bidang tugas yang harus dilaksanakannya sehingga memperkecil resiko
terjadinya kekeliruan yang biasanya timbul karena mengandalkan komunikasi
lisan.
2.2.11 Pembuatan dan Analisis berdasarkan Kontrak
Pembuatan dan analisis berdasarkan kontrak harus dibuat secara benar,
disetujui dan dikendalikan untuk menghindari kesalahpahaman yang dapat
menyebabkan produk atau pekerjaan dengan mutu yang tidak memuaskan.
Kontrak tertulis antara pemberi kontrak dan penerima kontrak harus dibuat secara
jelas menentukan tanggung jawab dan kewajiban masing-masing pihak. Kontrak
harus menyatakan secara jelas prosedur pelulusan tiap bets produk untuk
diedarkan yang menjadi tanggung jawab penuh kepala bagian Q A .
2.2.12 Kualifikasi dan Validasi 2.2.12.1 Kualifikasi
Kualifikasi adalah “kegiatan pembuktian” bahwa perlengkapan, fasilitas
atau sistem yang digunakan dalam suatu proses/sistem akan selalu bekerja sesuai
dengan kriteria yang diinginkan dan konsisten. Validasi/kualifikasi mesin,
1) Kualifikasi Rancangan (Design Qualification)
Kualifikasi rancangan adalah unsur pertama dalam melakukan validasi
terhadap fasilitas, sistem atau peralatan baru. Tujuannya adalah untuk menjamin
dan mendokumentasikan sistem, peralatan atau bangunan yang akan dipasang
atau dibangun sesuai dengan ketentuan atau spesifikasi yang diatur dalam
ketentuan CPOB yang berlaku. Kualifikasi ini dilakukan sebelum instalasi
(pemasangan) alat/mesin/prasarana produksi.
2) Kualifikasi Instalasi (Installation Qualification)
Kualifikasi instalasi bertujuan untuk menjamin dan mendokumentasikan
sistem atau peralatan yang diinstalasi sesuai dengan spesifikasi yang tertera pada
dokumen pembelian, manual alat yang bersangkutan dan pemasangannya
dilakukan memenuhi spesifikasi yang telah ditetapkan. Kualifikasi instalasi
dilakukan pada waktu instalasi (pemasangan baru), modifikasi atau pemindahan
alat yang bersangkutan.
3) Kualifikasi Operasional (Operational Qualification)
Kualifikasi Operasional bertujuan untuk menjamin dan
mendokumentasikan bahwa sistem atau peralatan yang telah diinstalasi bekerja
(beroperasi) sesuai dengan spesifikasi yang diinginkan. Kualifikasi operasional
dilakukan setelah kualifikasi instalasi (pemasangan baru), modifikasi atau
pemindahan alat yang bersangkutan.
4) Kualifikasi Kinerja (Performance Qualification)
Tujuannya adalah untuk menjamin dan mendokumentasikan bahwa sistem
atau peralatan yang telah diinstalasi bekerja sesuai dengan spesifikasi yang
2.2.12.2Validasi
CPOB mensyaratkan industri farmasi untuk mengidentifikasi validasi yang
perlu dilakukan sebagai bukti pengendalian terhadap aspek kritis dari kegiatan
yang dilakukan. Kegiatan validasi secara keseluruhan hendaklah direncanakan.
Kegiatan validasi meliputi kualifikasi (personil, peralatan dan sistem), kalibrasi
(instrumen dan alat ukur) dan validasi (prosedur dan proses).
a. Validasi Metode Analisa
Validasi Metode Analisa untuk membuktikan bahwa semua metode analisa
(cara/prosedur pengujian) yang digunakan dalam pengujian maupun pengawasan
mutu senantiasa mencapai hasil yang diinginkan secara konsisten
(terus-menerus). Validasi metode analisa menguji atau memvalidasi prosedur tetap
(protap) pengujian yang bersangkutan. Protap tersebut bisa dibuat oleh bagian
pengawasan mutu, apabila protap belum dibuat, maka harus dibuat terlebih
dahulu, baru divalidasi.
b. Validasi Proses Produksi
Tujuannya adalah:
- Memberikan dokumentasi secara tertulis bahwa prosedur produksi yang
berlaku dan digunakan dalam proses produksi rutin (batch processing
record), senantiasa mencapai hasil yang diinginkan secara terus-menerus.
- Mengidentifikasi dan mengurangi masalah yang terjadi selama proses
produksi dan memperkecil kemungkinan terjadinya proses ulang.
- Meningkatkan efektifitas dan efisiensi proses produksi.
c. Validasi Proses Pengemasan
- Memberikan dokumentasi secara tertulis bahwa prosedur pengemasan yang
berlaku dan digunakan dalam proses pengemasan rutin (batch packaging
record) sesuai dengan persyaratan rekonsiliasi yang telah ditentukan secara
konsisten.
- Operator yang melakukan proses pengemasan kompeten serta mengikuti
prosedur pengemasan yang telah ditentukan.
- Proses pengemasan yang dilakukan, tidak terjadi peristiwa mix-up (campur
baur) antar produk maupun antar bets.
d. Validasi Pembersihan
Tujuannya adalah:
- Memberikan dokumentasi secara tertulis bahwa prosedur pembersihan yang
berlaku dan digunakan sudah tepat dan dapat dilakukan berulang-ulang
(reliable and reproducible).
- Peralatan/mesin yang dibersihkan tidak terdapat pengaruh yang negatif
karena efek pembersihan.
- Operator yang melakukan pembersihan kompeten, mengikuti prosedur
pembersihan dan peralatan pembersihan yang telah ditentukan.
- Cara pembersihan menghasilkan tingkat kebersihan yang telah ditetapkan,
BAB III
TINJAUAN DAN RUANG LINGKUP PT. INDOFARMA (Persero) Tbk.
3.1 Sejarah dan Perkembangan PT. Indofarma (Persero) Tbk.
PT. Indofarma (Persero) Tbk. merupakan Badan Usaha Milik Negara
(BUMN) yang berada di bawah Departemen Kesehatan, berdiri pada tahun 1918
berupa unit produksi kecil dari Rumah Sakit Pusat Pemerintah Belanda dengan
kegiatan pembuatan salep dan pemotongan kain kasa pembalut yang dilakukan di
Centrale Burgelijke Zienkeninriching (CBZ), yang sekarang dikenal dengan
Rumah Sakit Dr. Cipto Mangunkusumo di Jakarta. Tahun 1931, pabrik
berkembang dengan bertambahnya jenis produksi, yaitu tablet dan injeksi. Tahun
1935, lokasi pabrik dipindahkan ke Jalan Tambak No. 2 Manggarai, Jakarta
sehingga dikenal dengan sebutan ”Pabrik Obat Manggarai”.
Perusahaan diambil alih oleh Jepang dan dikelola di bawah Manajemen
Takeda setelah terjadi pergantian penjajah sekitar tahun 1942. Perusahaan ini diambil alih oleh Indonesia setelah merdeka dan dinasionalisasi pada tahun 1950.
Pengelolaan diserahkan kepada Departemen Kesehatan Indonesia.
Tanggal 14 Februari 1967, melalui Surat Keputusan Menteri Kesehatan RI
No.008/III/AM/67, nama Pabrik Obat Manggarai diubah menjadi Pusat Produksi
Farmasi Departemen Kesehatan dan ditetapkan sebagai Unit Operatif setingkat
Direktorat Jenderal Farmasi. Tugas pokok pabrik ini adalah memproduksi
obat-obatan berdasarkan pesanan dari Departemen Kesehatan RI. Tahun 1969-1975
Republik Indonesia No.125/IV/KAB/BU/75 tentang struktur organisasi
Departemen Kesehatan yang merupakan pelaksanaan lebih lanjut dari Keputusan
Presiden Republik Indonesia No. 44 dan 45 tahun 1974, namun pabrik farmasi
Departemen Kesehatan ini tidak tercakup dalam keputusan tersebut sehingga
statusnya tidak jelas. Hal ini berlangsung hingga tahun 1978.
Tahap selanjutnya, pada tahun 1979 pabrik ini mulai memproduksi
obat-obat esensial untuk pelayanan masyarakat, status Pabrik Obat Manggarai diubah
menjadi Pusat Produksi Farmasi yang bersifat Nirlaba dan masih di bawah
Departemen Kesehatan. Tahun 1981 pemerintah meningkatkan status perusahaan
menjadi Perusahaan Umum Indonesia Farma disingkat Perum Indofarma.
Tonggak penting lain perjalanan bisnis Indofarma terjadi pada tahun 1988
dengan membangun Pabrik Modern berkapasitas besar di lahan seluas 20 Hektar
di kawasan Cibitung, Bekasi dengan bantuan alat dan teknologi dari Italia. Tahun
1991, seluruh proses produksi di Manggarai, Jakarta, dipindahkan ke Cibitung
kecuali sediaan steril. Tanggal 31 Januari 1995 fasilitas produksi steril diresmikan
oleh Menteri Kesehatan Republik Indonesia dengan dana pembangunan
seluruhnya ditanggung oleh Perum Indofarma.
Tahun 1996 status perusahaan ditingkatkan lagi menjadi PT. Indofarma
(Persero), ini bertujuan untuk mengantisipasi perkembangan di masa datang dan
meningkatkan daya saing. PT. Indofarma (Persero) selain bergerak di manufaktur
obat, juga mulai merambah sampai ke distribusi dan perdagangan (trading) produk
farmasi dan alat kesehatan. Perkembangan selanjutnya pada tahun 2000, bisnis
distribusi dan trading Produk Farmasi dan Alat Kesehatan dipisah dan diserahkan
(IGM). Pengembangan ini sekaligus memungkinkan Indofarma memfokuskan diri
pada bisnis inti di bidang produksi dan pemasaran produk-produk farmasi.
Tahun 2001 Indofarma melakukan penawaran saham perdana kepada
masyarakat dan mendaftarkan seluruh saham perusahaan di bursa efek Jakarta dan
bursa efek Surabaya, serta resmi menjadi sebuah perusahaan terbuka dengan nama
PT. Indofarma (Persero) Tbk. Indofarma mengembangkan produksi dengan
struktur permodalan yang lebih kuat, sehingga bukan hanya membuat obat-obat
esensial dan generik, melainkan juga obat dengan nama dagang baik etikal
maupun OTC, obat tradisional (herbal) dan makanan kesehatan.
Manajemen Indofarma yakin bahwa kunci keberhasilan untuk
memenangkan persaingan di era globalisasi adalah operational execellence. Tahun
2007 perusahaan mengoptimalkan fungsi bisnis yang ada melalui restrukturisasi
lanjutan yang memberikan otonomi luas kepada IGM guna memperkuat struktur
bisnis terutama dalam hal penggarapan penjualan institusi. Indofarma dapat lebih
memfokuskan pada kegiatan produksi sedangkan IGM pada kegiatan distribusi
dan trading produk farmasi dan alat kesehatan.
Perseroan senantiasa berupaya menetapkan tata kelola perusahaan yang
baik (Good Corporate Governance) guna meletakkan fondasi bisnis yang kuat.
Tanggal 22 Februari 2007 organ utama perseroan telah bersama-sama
menandatangani pernyataan komitmen implementasi GCG. Perseroan juga
berupaya membangun kompetensi personal yang profesional melalui program
pengembangan sumber daya manusia yang terarah, agar mampu membawa
perseroan memasuki era perdagangan bebas sebagai perusahaan farmasi
3.2Visi, Misi, Motto dan Logo PT. Indofarma (Persero) Tbk. Visi
Menjadi perusahaan yang berperan secara signifikan pada perbaikan kualitas
hidup manusia dengan memberi solusi terhadap masalah kesehatan dan
kesejahteraan masyarakat.
Misi
Menyediakan produk dan layanan berkualitas dengan harga terjangkau
untuk masyarakat.
Melakukan penelitian dan pengembangan produk yang inovatif dengan
prioritas untuk mengobati penderita penyakit dengan tingkat prevalensi
tinggi.
Mengembangkan kompetensi Sumber Daya Manusia sehingga memiliki
kepedulian, profesionalisme dan kewirausahaan yang tinggi.
Motto
Motto PT. Indofarma (Persero) Tbk. adalah Insan Indofarma dalam
menjalankan visi dan misi tersebut yaitu “dilandasi ketakwaan kepada Tuhan
Logo
Gambar 1. Logo PT. Indofarma (Persero) Tbk.
Logo tanpa bingkai warna biru: Pengabdian INF yang tidak terbatas untuk
kesehatan masyarakat.
Warna biru melambangkan sifat pengabdian perseroan yang tidak terbatas
untuk kesehatan masyarakat. Keluasan pengabdian diperluas dengan
gradasi warna yang mewakili dimensi yang luas.
Ritme garis lurus dan lengkung: Upaya-upaya pelayanan perseroan pada
masyarakat. Kesatuan garisnya memberikan kesan melindungi dan saling
mendukung, artinya perseroan siap melindungi masyarakat dari penyakit
dan mendukung masyarakat untuk mewujudkan kesehatan.
Posisi miring: Dinamika INF, tidak terpaku konvensi lama, mengikuti
perkembangan zaman dan inovatif tetapi mengikuti gerak laju teknologi.
3.3Nilai Budaya yang Dikembangkan PT. Indofarma (Persero) Tbk.
PT. Indofarma (Persero) Tbk. memiliki inti yang telah disepakati bersama
dan dianut, serta mencerminkan budaya korporat, dalam hal ini adalah budaya PT.
Indofarma (Persero) Tbk. Nilai-nilai ini membentuk filosofi bisnis dan budaya
Professional memiliki arti yaitu senantiasa bekerja secara profesional yang
dilandasi integritas, komitmen dan selalu berupaya memberikan hasil yang terbaik.
Entrepreneurship memiliki arti bahwa insan Indofarma senantiasa memiliki jiwa
kewirausahaan berdasarkan pemikiran jauh ke depan, inovatif dan fokus terhadap
kepuasan pelanggan. Compassionate berarti insan Indofarma memiliki rasa peduli
dan welas asih terhadap sesama.
3.4 Kebijakan Mutu PT. Indofarma (Persero) Tbk.
Kebijakan mutu PT. Indofarma (Persero) Tbk. ditetapkan sebagai berikut:
1. Mutu dijadikan prioritas pertama demi kepuasan pelanggan eksternal
maupun internal.
2. Mutu mencakup seluruh kegiatan perusahaan, mulai dari penelitian dan
pengembangan, produksi sampai dengan pemasaran.
3. Mutu dibangun dalam sistem manajemen mutu terpadu oleh semua pihak
melalui perencanaan, pelaksanaan dan pengendalian yang efektif dan
efisien.
4. Mutu terutama ditentukan oleh faktor manusia, karena itu pendidikan dan
pelatihan bagi karyawan terus dikembangkan sesuai kebutuhan dan
perkembangan ilmu pengetahuan dan teknologi.
5. Mutu selalu dijaga dan ditingkatkan sesuai kebutuhan pelanggan dengan
memperhatikan kemampuan daya saing melalui proses yang dapat
menekan biaya mutu.
Karyawan dan pimpinan bekerja sama dalam suasana yang kondusif
menyelesaikan tugas masing-masing secara tuntas dan tepat waktu, sesuai dengan
3.5 Kedudukan, Fungsi dan Peranan PT. Indofarma (Persero) Tbk.
Kedudukan PT. Indofarma (Persero) Tbk. adalah suatu Badan Usaha Milik
Negara (BUMN) yang memproduksi obat-obatan esensial dan merupakan
produsen obat generik berlogo. PT. Indofarma (Persero) Tbk. mempunyai fungsi:
1. Menyelenggarakan kemanfaatan umum di bidang farmasi dalam arti yang
seluas-luasnya terutama dalam bidang pengadaan produk farmasi yang
sangat diperlukan oleh sarana kesehatan, baik di pusat maupun di daerah,
yaitu untuk unit pelayanan kesehatan pemerintah maupun masyarakat
umum.
2. Mendapatkan keuntungan berdasarkan prinsip-prinsip pengelolaan
perusahaan untuk membiayai serta mengembangkan perusahaan dan untuk
disumbangkan bagi pembangunan nasional sesuai dengan kemampuan
perusahaan.
3. Memperluas pemerataan penyediaan obat khususnya bagi masyarakat
golongan menengah ke bawah.
Peranan PT. Indofarma (Persero) Tbk. antara lain dapat dilihat dari setiap
kebijakan operasional maupun arah pengembangan perusahaan yaitu:
1. Andalan utama produsen obat esensial bermutu, dengan demikian
PT. Indofarma (Persero) Tbk. merupakan pemasok terbesar obat esensial
dan menggunakan sebagian besar kapasitas produksinya untuk
memproduksi obat esensial.
2. Adanya kebijakan sekaligus motto perusahaan yaitu ”Untuk Kehidupan
selalu berusaha meningkatkan derajat kesehatan masyarakat menjadi lebih
baik. PT. Indofarma (Persero) Tbk. sebagai Badan Usaha Milik Negara
membantu memenuhi upaya kesehatan yang bersifat menyeluruh dan
terpadu termasuk pemerataan penyediaan obat yang bermutu dengan harga
yang terjangkau.
3. PT. Indofarma (Persero) Tbk. menjadi tempat pelatihan tenaga farmasis
dan profesi lain dalam rangka meningkatkan kualitas sumber daya manusia
di industri farmasi.
3.6Lokasi dan Bangunan
Pabrik dan kantor pusat PT. Indofarma (Persero) Tbk. terletak di Jalan
Indofarma No. 1, Desa Gandasari, Kecamatan Cikarang Barat-Bekasi, dengan luas
tanah 2.000.000 m2 dan luas bangunan 28.035 m2 yang terdiri dari: kantor pusat
20 m2, pusat pelatihan 750 m2, kantin 300 m2, koperasi 60 m2, poliklinik dan
apotek 196 m2, masjid 441 m2, laboratorium 1.440 m2, unit produksi utama 9.921
m2, unit produksi β laktam 1.440 m2, unit produksi parenteral 2.330 m2, unit produksi obat tradisional dan gudang 5.250 m2, bangunan utilities 898 m2, gudang
bahan kimia 216 m2, instalasi pengolahan limbah cair 204 m2, instalasi limbah
padat 44 m2, menara air 100 m2, cylinder gas chamber 66 m2, rumah jaga 128 m2,
lapangan 1.548 m2, unit penelitian dan pengembangan 700 m2
Sistem tata ruang produksi non steril dibagi dua, yaitu kelas empat (black
area) dan kelas tiga (grey area). Kelas empat meliputi gudang, koridor yang
menghubungkan gudang produk jadi dan daerah pengemasan sekunder. Daerah ini
dinding mudah dibersihkan. Kelas tiga merupakan daerah yang terkait langsung
dengan proses produksi, misalnya daerah proses, pengemasan primer hingga
koridor yang berhubungan.
3.7 Produk PT. Indofarma (Persero) Tbk.
Produk yang dihasilkan oleh PT. Indofarma (Persero) Tbk. antara lain
sebagai berikut:
1. Produk Ethical (OGB, Lisensi, Nama Dagang)
PT. Indofarma (Persero) Tbk. memproduksi obat generic ethical sebagai
produk utama di samping memproduksi obat dengan nama dagang dan lisensi.
Saat ini PT. Indofarma (Persero) Tbk. mulai memperluas target pasar dengan
memproduksi obat branded generic atau obat generik dengan nama dagang
dengan harga terjangkau yang merupakan program pemerintah untuk penyediaan
obat bagi masyarakat.
2. OTC dan Herbal Medicines
PT. Indofarma (Persero) Tbk. telah mengembangkan Obat Asli Indonesia
(OAI) seperti Prolipid, Prouric, Probagin dan lainnya dalam rangka
mengembangkan sumber daya alam di Indonesia. Obat OTC yang diproduksi
antara lain OBH Plus. Makanan kesehatan (suplement food) seperti Biovision,
Bioprost dan lain-lain juga diproduksi.
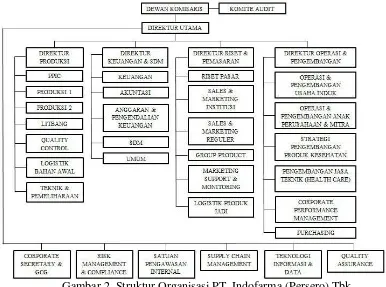
3.8Struktur Organisasi PT. Indofarma (Persero) Tbk.
PT. Indofarma (Persero) Tbk. dipimpin oleh seorang Direktur Utama yang
dibantu oleh empat orang direktur, yaitu Direktur Produksi, Direktur Keuangan
Pengembangan. Direktur ini masing-masing membawahi manager pada setiap
bidangnya dan untuk membantu pelaksanaan tugas, manager didukung oleh
asisten manajer, supervisor dan tenaga terlatih dalam jumlah yang efektif dan
efisien untuk melaksanakan kegiatan produksi sesuai dengan prosedur dan
spesifikasi yang telah ditentukan. Bagian-bagian yang langsung bertanggung
jawab kepada Direktur Utama yaitu Corporate Secretary, Risk Management &
Compliance, Satuan Pengawasan Internal (SPI), Supply Chain Management,
Teknologi Informasi & Data, Quality Assurance.
Struktur organisasi di PT. Indofarma (Persero) Tbk.
Gambar 2. Struktur Organisasi PT. Indofarma (Persero) Tbk.
Direktorat
Direktorat Produksi PT. Indofarma (Persero) Tbk. membawahi tujuh
bidang dimana setiap bidang dipimpin oleh seorang manajer yang dibantu oleh
asisten manajer dan supervisor.
3.8.1.1Bidang Production Planning and Inventory Control (PPIC) atau PPPP (Perencanaan Produksi dan Pengendalian Persediaan)
Bidang Perencanaan dan Pengendalian Produksi dan Persediaan (PPPP)
dipimpin oleh seorang manajer yang membawahi empat seksi, yaitu seksi
Perencanaan dan Pengendalian Bahan Baku dan Bahan Pengemas, seksi
Perencanaan dan Pengendalian Produksi I, seksi Perencanaan dan Pengendalian
Produksi II, Herbal serta seksi Toll Manufacturing dan Pelayanan Produk. PPPP
mempunyai peranan strategis dalam peningkatan efisiensi dan produktifitas,
proses pabrikasi, pengendalian persediaan sehingga diharapkan dapat
menghasilkan produk dengan mutu, harga, jumlah dan waktu serta pelayanan yang
tepat.
Seksi perencanaan dan pengendalian mempunyai dua fungsi. Fungsi
perencanaan merupakan landasan utama dalam penentuan permintaan marketing
dan langkah-langkah yang diperlukan untuk memastikan tercapainya permintaan
tersebut. Fungsi pengendalian, merupakan alat manajemen untuk memastikan
tersedianya bahan awal, produk ruah dan produk jadi untuk terpenuhinya
permintaan marketing, serta pengaturan agar tidak terjadi over stock atau out of
stock.
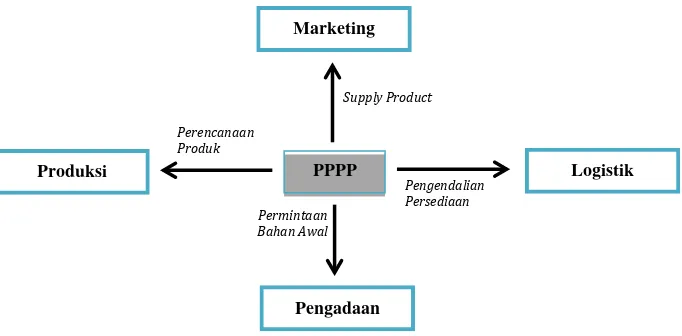
Hubungan kerja PPPP dengan berbagai bidang lain dapat dilihat pada
Gambar 3. Hubungan Kerja Bidang PPPP dengan Bidang lain di PT. Indofarma
(Persero) Tbk.
Alur proses kegiatan bidang PPPP dibagi menjadi dua tahap, yaitu alur
proses perencanaan dan alur proses pengendalian bahan. Alur proses perencanaan
dimulai dari bidang Pemasaran menyerahkan rencana penjualan satu tahun kepada
bidang PPPP. PPPP kemudian membuat rencana produksi satu tahun serta rencana
kebutuhan satu tahun dan disetujui Direktur Produksi. Rencana tersebut digunakan
sebagai dasar pembuatan Rencana Kerja dan Anggaran Perusahaan (RKAP) yang
disusun setiap tahun kemudian dijabarkan dalam Konsep Rencana Produksi
Periodik (KRPP) dan Konsep Rencana Kedatangan Bahan (KRKB) perkuartal.
Rencana Produksi Bulanan (RPB) dibuat berdasarkan KRPP dan KRKB. RPB ini
digunakan untuk menyiapkan Perintah Produksi (PP) dan Perintah Kemas (PK)
serta penyiapan Surat Pesanan Permintaan Barang (SPPB) yang disetujui Direktur
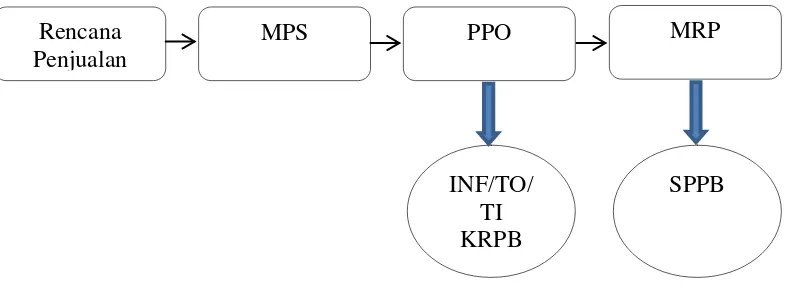
Produksi. Alur proses perencanaan ditunjukkan pada gambar 4 di bawah ini:
Gambar 4. Alur Proses Perencanaan
Fungsi PPPP dalam perencanaan bahan adalah menetapkan standar untuk
perencanaan bahan, meliputi:
a. Jenis spesifikasi bahan yang dibutuhkan
b. Sediaan maximum dan minimum bahan:
• Buffer stock & Reorder point
• Frekuensi pemesanan bahan
• Kapasitas gudang
c. Lead time
d. Jumlah pesanan:
• Jumlah & jadwal produksi
• Minimal packing
• MOQ (Minimum Order Quantity)
Alur proses pengendalian bahan dimulai dari diterbitkannya Perintah
Pengolahan (PP) sekaligus berlaku sebagai bon permintaan bahan ke gudang
penyimpanan bahan baku dan bahan penolong. Bukti Penyerahan Produk Ruah Rencana
Penjualan
MPS PPO MRP
INF/TO/ TI KRPB
(BPPR) kemudian diterbitkan, selanjutnya keluar Perintah Kemas (PK) dan Bukti
Penyerahan Produk Jadi (BPPJ). Bidang Produksi membuat Rencana Produksi
Mingguan (RPM) berdasarkan PP dan PK yang selanjutnya digunakan sebagai
pedoman proses produksi. Proses produksi dilaporkan dalam bentuk laporan
produksi dan ditujukan antara lain kepada bidang PPPP sebagai informasi untuk
fungsi pengendalian produksi. Bidang Pengadaan kemudian memberikan
informasi kemajuan proses pengadaan kepada PPPP untuk fungsi pengendalian
bahan. Alur proses pengendalian ditunjukkan pada gambar 5 di bawah ini:
Gambar 5. Alur Proses Pengendalian Produksi Beberapa tugas PPPP dalam pengendalian bahan adalah:
Monitoring kedatangan bahan sampai dengan bahan tersebut bisa dipergunakan
untuk proses produksi.
Memantau inventory bahan (terutama bahan yang dipakai banyak item)
Analisa terhadap perubahan pasar, disain produk dan kemasan, kegagalan
produk dan kerusakan bahan, nilai persediaan
Monitoring kemajuan dan kendala pengadaan bahan
Koordinasi problem solving
Seksi Toll Manufacturing dibagi menjadi dua, toll out (dimana perusahaan
membuat produk ke pabrik farmasi lain) dan toll in (dimana perusahaan menerima
pembuatan produk dari pabrik farmasi lain). Beberapa hal yang dilakukan dalam
toll manufacturing adalah:
Mencari PTM (Pabrik Penerima Toll Manufacturing) sesuai rencana produksi.
Hal-hal yang perlu diperhatikan adalah:
Fasilitas produksi
Hasil audit PTM
Toll fee
Melakukan monitoring realisasi produk di PTM
Koordinasi problem solving
3.8.1.2Produksi I
Bidang produksi I dipimpin oleh seorang Manajer yang membawahi empat
seksi, yaitu seksi Solid I bertanggung jawab dalam pembuatan massa tablet dan
pembuatan sediaan kapsul, seksi Solid II bertanggung jawab dalam pencetakan
tablet atau Filling kapsul, seksi pengemasan bertanggung jawab dalam
pengemasan dan seksi herbal bertanggung jawab dalam ekstraksi dan pengolahan
bahan herbal.
Proses produksi tablet di produksi I dilakukan dengan metode vertical
closed system, yaitu sistem vertikal tertutup dimana proses produksi dilakukan
dengan memanfaatkan gaya gravitasi. Metode ini dilaksanakan di produksi I
karena bentuk bangunan produksi utama memungkinkan untuk diterapkan metode
tersebut (3 lantai) dan produksinya besar sehingga efisiensi tenaga tercapai.
Keuntungan sistem ini adalah dapat meminimalkan terjadinya kontaminasi silang,
bets dapat dibuat dalam kapasitas besar, efisiensi dari segi waktu, tenaga, tempat
maupun energi.
Bidang produksi I akan melaksanakan kegiatan berdasarkan surat Perintah
Pengolahan (PP) yang dikeluarkan oleh bagian Perencanaan Produksi Dan
(CPB). CPB merupakan dokumen yang berisi semua prosedur dan persyaratan
yang harus dipenuhi selama proses produksi dan segala sesuatu yang menyimpang
yang teramati dicatat pada dokumen tersebut. Perintah Pengolahan disetujui oleh
Manajer Produksi setelah dilakukan pengecekan antara PP dengan Rencana
Produksi Bulanan (RPB) dan Rencana Produksi Mingguan (RPM). Perintah
Pengolahan yang telah disetujui oleh Manajer Produksi I akan digunakan sebagai
Bon Permintaan Bahan Awal (BPBA) kepada bagian Logistik Bahan Awal (LBA).
Bahan yang diminta di gudang, disiapkan dan diserahkan ke bidang produksi I
setelah dilakukan penimbangan oleh petugas dispensing disaksikan oleh petugas
IPC. Bahan dari gudang yang telah diserahkan dari LBA ke seksi Solid I akan
diproses sampai menjadi produk antara. Seksi Solid II akan mengolah produk
antara menjadi produk ruah. Produk ruah dinyatakan telah memenuhi syarat oleh
bagian Quality Control (QC) dengan dikeluarkannya Laporan Analisa Memenuhi
Syarat (LA MS), bagian seksi Solid II akan membuat Bukti Penyerahan Produk
Ruahan (BPPR) kepada seksi Pengemasan dan PPPP akan mengeluarkan Perintah
Kemas (PK). Bagian pengemasan akan membuat bon permintaan bahan pengemas
ke bagian LBA sesuai dengan kebutuhan pengemasan. Persiapan bahan
pengemasan yaitu coding nomor registrasi, nomor bets, tanggal kadaluarsa di
kemasan sekunder dilakukan sebelum proses pengemasan dimulai. Produk jadi
diperoleh setelah proses pengemasan selesai.
Proses pengemasan yang dilakukan bidang produksi I meliputi stripping,
blistering dan bottling. Produk jadi dalam kemasan sekunder akan dikemas ke
dalam karton yang telah disablon sesuai isinya dan diserahkan ke bagian logistik
yang telah dikemas dalam karton akan dikarantina untuk diperiksa secara random
tentang kelengkapan penandaan dan dokumentasinya. Produk jadi yang memenuhi
syarat akan didistribusikan dan diambil contoh pertinggal (retained sample) untuk
tiap betsnya sebagai bahan penelusuran apabila ada keluhan di kemudian hari.
Setiap penyimpangan pada proses produksi akan dicatat dalam catatan
penyimpangan produksi.
A. Seksi solid I
A.1 Pembuatan Massa Tablet
Tugas seksi penyediaan massa meliputi persiapan, pengolahan, penyiapan
bahan awal dan pembuatan massa. Bahan aktif dan bahan penolong dimasukkan
ke dalam alat penampung (bin). Bahan dalam bin kemudian dibawa dengan forklift
dan siap diproses mixing dengan menggunakan mesin Azo-Thumbler di lantai 3
atau Diosna di lantai 2. Tahap berikutnya pengolahan massa dengan beberapa
metode yaitu metode cetak langsung (Direct compression) atau granulasi basah
(Wet Granulation).
Metode cetak langsung (direct compression)
a. Bin yang berisi campuran bahan ditempatkan pada loading station.
b. Campuran bahan dialirkan ke mesin cetak di lantai II melalui pipa stainless
steel yang dilengkapi kain tunnel.
c. Pencetakan tablet.
Metode granulasi basah (wet granulation)
a. Pencampuran bahan awal dilakukan proses pengadukan bahan dengan bahan
batagion atau mixer stokes, dilakukan di lantai II dilewatkan melalui
granulator.
b. Granul basah ditampung dalam container di lantai I
selanjutnya dikeringkan dengan fluid bed dryer.
c. Granul kering diayak dengan granulator dengan ayakan
mesh tertentu dan hasilnya ditampung dalam bin dan diperiksa kadar airnya
oleh IPC.
d. Granulat dibawa ke lantai II untuk ditimbang ulang
kemudian ditambah bahan penolong.
e. Proses pencampuran akhir menggunakan mixerdiosna dan
dites homogenitasnya oleh IPC.
f. Bin yang berisi campuran bahan/massa tablet dibawa ke
lantai III dan ditempatkan pada loading station, dialirkan melalui pipa
stainless steel yang dilengkapi kain tunnel, ke hopper mesin cetak lantai II
dan selanjutnya siap dicetak.
A.2 Pembuatan Sediaan Kapsul
Kelembaban udara ruangan produksi kapsul hendaknya 50-60% karena
cangkang kapsul dapat mengabsorpsi air. Alur proses pembuatan sediaan kapsul
adalah sebagai berikut:
1. Bahan yang telah memenuhi syarat ditimbang di bagian dispensing lantai II.
2. Bahan dari mesin penyedot vakum (azo) yang dilengkapi ayakan berputar
(rotatif sieve) dimasukkan ke dalam bin, dialirkan ke mixer diosna di lantai
3. Massa hasil pengadukan selanjutnya dipindahkan ke lantai III. Petugas IPC
akan melakukan pemeriksaan terhadap massa tersebut mengenai
homogenitas dan kadarnya.
4. Massa selanjutnya dialirkan ke hopper mesin pengisi kapsul (capsulefilling
machine) di lantai II melalui loading station.
5. Kapsul dibersihkan melalui proses polishing.
6. Produk ruahan dikarantina untuk menunggu hasil analisis dari bidang
pemastian mutu. Produk yang telah memenuhi syarat dapat dikemas.
B. Seksi solid II
Seksi solid II bertugas mencetak massa tablet atau massa kapsul sampai
menjadi produk ruah yang lulus uji dan siap dikemas, ini dilakukan di lantai dua.
Tahapan yang dilakukan:
a. Mempersiapkan mesin.
b. Mengoperasikan mesin.
c. Menimbang produk ruahan.
d. Pemberian label, nama produk, nomor bets, jumlah dan tanggal pencetakan.
e. Karantina produk ruah menunggu pemeriksaan dari bidang pemastian mutu.
f. Mencatat semua kegiatan yang dilakukan dalam catatan pengolahan bets.
Pemeriksaan kualitas produk antara dan produk ruah oleh petugas IPC
dilakukan selama proses berlangsung agar produk yang dihasilkan senantiasa
memenuhi persyaratan mutu yang ditetapkan. Produk ruah yang lolos uji
selanjutnya diserahkan ke bidang pengemasan (seksi pengemasan) untuk dikemas
Catatan Produksi Bets, protap kegiatan proses produksi, uraian tugas karyawan
dan catatan produktivitas mesin.
C. Seksi pengemasan
Suatu produk dapat dikatakan produk jadi bila telah melewati tahap
pengemasan. Definisi pengemasan menurut pedoman CPOB Depkes RI tahun
2006 adalah bagian dari siklus produksi yang dilakukan terhadap produk ruah
untuk menghasilkan produk jadi. Pengemasan berkaitan dengan stabilitas obat
yang berfungsi melindungi obat terhadap kelembaban, iklim dan benturan.
Kemasan juga mempengaruhi daya tarik produk terhadap konsumen.
Ditinjau dari waktu dikeluarkannya PP dan PK, dikenal dua proses yaitu in
line process dan non in line process. In line process yaitu proses dimana hasil
produksi langsung dikemas dalam wadah pengemasnya, PP dan PK dikeluarkan
bersamaan, jadi mulai dari bahan awal sampai menjadi produk dalam kemasan
akhir, proses tidak terputus. Proses ini diterapkan dalam sirup cair, sirup kering,
salep dan oralit. Non in line process dimana PP dan PK tidak dikeluarkan
bersamaan. PP dikeluarkan, kemudian dilakukan penyiapan bahan awal sampai
menjadi produk yang siap dikemas. Produk ini dikarantina menunggu released
dari QC. Proses ini diterapkan dalam pembuatan kapsul, tablet dan produk steril.
PK oleh bidang pengemasan digunakan sebagai bon permintaan bahan
pengemasan yang diajukan ke bagian LBA. Bahan pengemasan dari gudang bila
berupa karton akan dilakukan penyablonan yang berisi nama produk, nomor bets,
expired date, sedangkan untuk etiket dan kotak akan dilakukan coding (pemberian
Jalur pengemasan harus telah dibersihkan (line clearance) sebelum
dilakukan proses pengemasan, untuk mencegah terjadinya mixed-up label dan
selama proses pengemasan dilakukan IPC, misalnya uji kebocoran strip, blister,
dan sachet sebanyak empat lempeng strip atau blister selama 15 menit. Proses
dokumentasi selanjutnya dilakukan untuk bidang pengemasan meliputi Catatan
Pengolahan Bets, papan penandaan, catatan sanitasi, catatan produksi harian yang
terdiri dari kontrol harian mesin, pengepakan dan laporan bulanan.
D. Seksi Herbal
PT. Indofarma (Persero) Tbk. mendirikan Extraction Center yang khusus
memproduksi obat tradisional (Jamu). Bidang herbal memproduksi obat-obat
tradisional yang bahan bakunya dapat berasal dari dalam negeri maupun dari luar
negeri. Obat tradisional yang bahan bakunya berasal dari dalam negeri, nama
produk berawal “Pro”, misalnya Prolipid, Probagin dan Prouric. Obat tradisional
yang bahan bakunya diimpor, nama produk berawalan “Bio”, misalnya Biovision,
Bioginko dan lain-lain.
Kegiatan produksi di seksi herbal meliputi sortasi, pencucian simplisia,
ekstraksi, formulasi dan pengemasan. Bahan baku dipenuhi dengan cara membeli
langsung dari supplier, melalui petani binaan atau bekerja sama dengan institusi
lain. Bahan baku tersebut harus memenuhi spesifikasi yang ditetapkan oleh
PT. Indofarma (Persero) Tbk. seperti kadar air (lebih kecil dari 10%), kadar sari
larut air dan kadar sari larut etanol (tergantung simplisia) mengacu kepada buku
resmi yang ditetapkan yaitu Materia Medika Indonesia.
Sistem produksi herbal di PT. Indofarma (Persero) Tbk. sesuai dengan
PT. Indofarma (Persero) Tbk. berupa horizontal close system dengan
menggunakan metode ekstraksi berupa maserasi, perkolasi dan gabungan
keduanya. Pengeringan ekstrak menggunakan dua metode yaitu spray dryer dan
vaccum dryer. Proses pengolahan ekstrak dimulai dari perajangan kemudian
ekstraksi (penyarian), pengentalan, pengeringan kering yang kemudian
menghasilkan ekstrak kering.
3.8.1.3Produksi II
Bidang produksi II dipimpin oleh seorang manajer. Bidang ini membawahi
tiga seksi, yaitu seksi β-laktam, seksi salep, sirup, serbuk dan seksi produksi steril. Bidang produksi II bertugas untuk memastikan tersedianya produk tablet, kapsul
dan sirup kering β-laktam, salep, sirup, serbuk dan produk steril sesuai target dengan cara merencanakan, mengkoordinasi dan mengendalikan aktivitas
pengolahan, pengemasan dan kegiatan terkait. Pelaksanaan proses produksi di
bidang produksi II menggunakan vertical closed system untuk menghindari kontak
dengan lingkungan, sistem ini diterapkan untuk produksi oralit. Produksi sediaan
β-laktam, salep dan sirup menggunakan horizontal closed system dimana
penyiapan bahan awal sampai produk akhir diproses dalam lantai yang sama,
karena sediaan yang diproduksi dalam jumlah yang relatif kecil. Bidang ini
membawahi tiga seksi, yaitu:
A. Seksi Sediaan β-laktam
Seksi sediaan β-laktam bertugas memproduksi sediaan antibiotika yang
mempunyai inti β-laktam. Bentuk sediaannya berupa tablet, kapsul, dan sirup
produksi lain (non β-laktam). Pemisahan ini dilakukan sebagai tindakan
pengamanan untuk mencegah terjadinya kontaminasi silang dengan produk lain.
Arus keluar-masuk menggunakan air locked system untuk menghindari
terjadinya kontaminasi silang. Air locked system mempunyai tekanan udara lebih
rendah dari ruangan lainnya. Pengendalian udara dilakukan dengan sistem Air
Handling Unit (AHU), dimana gedung β-laktam terpisah dari gedung non β
-laktam. Ruangan β-laktam terdiri dari dua kelas, yaitu kelas tiga yang digunakan
untuk proses dispensing, mixing, dan filling, tableting dan pengemasan primer,
dan kelas empat untuk proses pengemasan sekunder sampai obat jadi. Ruangan
kelas tiga dan kelas empat dipisahkan berdasarkan perbedaan tekanan dimana
tekanan udara kelas empat lebih tinggi daripada tekanan udara di kelas tiga
sehingga kontaminasi dari β-laktam dapat dihindari.
Pengaturan sirkulasi udara untuk ruangan ß-laktam dilakukan secara
khusus dan terpisah. Ruangan produksi sedíaan ß-laktam adalah ruang Kelas III
dengan tekanan udara yang diatur untuk menghindari kontaminasi. Ruangan
ß-laktam lebih negatif dibanding koridor di luarnya. Tekanan udara di luar koridor
lebih positif daripada di dalam koridor. Udara di dalam ruang produksi diharapkan
tidak bisa keluar ruangan sehingga tidak mengkontaminasi lingkungan. Udara dari
ruang produksi ß-laktam harus disaring terlebih dahulu agar udara yang keluar
tidak mengandung ß-laktam. Udara dialirkan ke dalam suatu ruang yang di
dalamnya ada tetesan-tetesan air yang akan melarutkan ß-laktam. Udara bersih
ß-laktam dialirkan kembali ke ruang produksi ß-laktam melalui prefilter (efisiensi
40%), medium filter (efisiensi 90%) dan heating coil untuk penyesuaian suhu.