Oleh:
DEVI YULIAWATI
A54103017
PROGRAM STUDI
GIZI MASYARAKAT DAN SUMBERDAYA KELUARGA
FAKULTAS PERTANIAN
(CPO) to The Durability of Torbangun ( Lour.) Soup (Under tuition of Dr. Ir. Evy Damayanthi, MS. and drh. M. Rizal M. Damanik, M.Rep.Sc, PhD.)
merupakan anak pertama dari tiga bersaudara pasangan Bambang Tri Waluyo
dan Titik Wahyuni. Pendidikan TK ditempuh di Taman Kanak-Kanak PTPN VIII
Tanjung Morawa, Sumatera Utara dari tahun 1989-1990 dan Taman
Kanan-Kanak Bhayangkari Curug, Tangerang dari tahun 1990-1991. Pendidikan SD
ditempuh di SD Islamic Village, Karawaci, Tangerang dari tahun 1991-1997.
Penulis melanjutkan pendidikan SLTP di SLTP Dian Harapan Karawaci,
Tangerang dari tahun 1997-1998, dan di SLTP Negeri 1 Subang, Jawa Barat dari
tahun 1998-2000. Pendidikan SMU ditempuh di SMU Negeri 1 Subang, Jawa
Barat dari tahun 2000-2003.
Penulis diterima sebagai mahasiswa Departemen Gizi Masyarakat dan
Sumberdaya Keluarga pada tahun 2003 melalui jalur Undangan Seleksi Masuk
IPB (USMI). Pada periode 2003/2004 pernah menjadi anggota Biro Hubungan
Masyarakat Forum Keluarga Masjid GMSK (FKMG). Pada periode 2004/2005
pernah menjadi anggota Biro Kajian Strategis Himpunan Mahsiswa Peminat Ilmu
Gizi Pertanian (HIMAGITA). Sejak tahun 2004-2006 penulis aktif sebagai staf
Divisi Kajian Strategis Badan Konsultasi Gizi (BKG) dan pada periode 2006/2007
pernah menjabat sebagai ketua Divisi Kajian Strategis Badan Konsultasi Gizi
(BKG). Pada tahun 2007 penulis menjadi asisten untuk mata kuliah Metabolisme
rahmat dan karunia-Nya penulis dapat menyelesaikan skripsi ini. Penulis
menyampaikan penghargaan dan ucapan terima kasih kepada :
1. Ibu Dr. Ir. Evy Damayanthi, M.S. dan Bapak Drh. Rizal Damanik M.Rep.Sc,
PhD sebagai dosen pembimbing skripsi yang telah memberikan semangat
dan masukan ilmu yang sangat berarti dan dengan sabar membimbing
penulis selama penelitian hingga penyelesaian tugas akhir ini.
2. Keluargaku tersayang : Papa, Mama, Eca, Ipam, dan Kkku sebagai sumber
semangat, motivasi, finansial dan kasih sayang yang tidak pernah habis
3. Pak Mashudi yang telah banyak membantu dan menjadi teman untuk
berdiskusi tentang penelitian ini.
4. Ibu Ir. Cesilia Meti Dwiriani, Msc sebagai pembimbing akademik.
5. Ibu Dr.Ir Lilik Kustiyah, MS sebagai dosen pemandu seminar.
6. Ibu Dr. Ir. Sri Anna Marliyati, MS sebagai dosen penguji yang telah begitu
banyak memberikan saran.
7. Bu Dini, Mas Yudi, Pak Lalu, dan Pak Danu di Balitpasca Panen, Cimanggu
Bogor atas bantuan dan bimbingannya.
8. Seluruh dosen dan staf Departemen GM (Teh Popon, Bu Yati, Teh Yati, Pak
Ugan, dan Mas Rena) yang telah mendidik, membimbing, dan membantu
dengan penuh kasih sayang, serta canda ria.
9. Temanku senasib dan sepenanggungan dalam suka dan duka (Betsy dan
Deni Alam’39) : Andi, Inoel, Malie, Bambang, Ade, Wewew, Vivi, Tika, Tegar,
Maning, Nining, MeiMei, Aris, Yudith, Sendi, dan seluruh GMSK’40. Terima
kasih atas kenangan yang begitu indah.
10. Teman-teman di HIMAGITA dan BKG yang telah memberikan warna berbeda
pada dunia.
11. Kakak-kakakku GMSK’37 (Mbak Nisa’14, Mbak Ama, dan Mbak Mada),
GMSK’38, GMSK’39, dan Adik-Adikku GMSK’41,GM’42, serta IKK’42.
12. Semua Pihak yang telah membantu dalam penelitian dan penyusunan skripsi
ini, memberi bantuan spiritual yang tidak dapat terhitung dan tergantikan.
Semoga skripsi ini dapat bermanfaat bagi yang membacanya.
Bogor, Juli 2007
DAFTAR TABEL ... iii
DAFTAR GAMBAR ... iv
DAFTAR LAMPIRAN ... vi
PENDAHULUAN ... 1
Latar belakang... 1
Tujuan ... 2
Manfaat ... 2
TINJAUAN PUSTAKA ... 3
Daun Torbangun ... 3
Santan kelapa ... 5
Reaksi oksidasi ... 8
Antioksidan ... 9
Vitamin A ... 10
Minyak Sawit Kasar ... 12
Mikrobiologi pangan ... 17
BAHAN DAN METODE ... 23
Waktu dan tempat ... 23
Bahan dan alat ... 23
Metode penelitian ... 24
Pengolahan dan analisis data ... 29
HASIL DAN PEMBAHASAN ... 31
Uji kimiawi kerusakkan lemak ... 31
Nilai pH ... 31
Total Asam Tertritasi (TAT) ... 34
Bilangan peroksida ... 37
Thiobarbituric acids (TBA) ... 41
Hasil analisis Vitamin A dan ß-karoten ... 45
Pengaruh pengolahan dan penyimpanan ... 45
Peranan STA dan STM dalam memenuhi Angka Kecukupan Gizi (AKG) Vitamin A Uji organoleptik ... 48
Hasil uji mikrobiologi ... 49
Halaman
Sayur Torbangun vitamin A ... 51
Sayur Torbangun MSK ... 52
Hasil uji hedonik organoleptik ... 55
Aroma ... 55
Warna ... 57
Kekentalan ... 59
Tekstur ... 61
Kelebihan dan kekurangan penggunaan tablet vitamin A dan MSK sebagai antioksidan ... 63
KESIMPULAN DAN SARAN ... 65
Kesimpulan ... 65
Saran ... 66
DAFTAR PUSTAKA ... 67
DAFTAR TABEL
Nomor Halaman
1. Komposisi zat gizi daun Torbangun dan daun katuk ... 4
2. Komposisi zat gizi sayur sop daun Torbangun (150 g) ... 5
3. Pengaruh penambahan air terhadap komposisi kimia santan ... 6
4. Kandungan asam lemak minyak sawit kasar ... 13
5. Karakteristik minyak sawit kasar ... 13
6. Komposisi karotenoid dalam minyak sawit kasar ... 16
7. Komposisi bahan yang digunakan dalam pembuatan sop daun Torbangun pada berbagai jenis analisis ... 25
8. Hasil analisis proksimat sop daun Torbangun ... 25
9. Contoh untuk analisis HPLC ... 28
10. Kandungan vitamin A pada sop daun Torbangun dan bahan penyusunnya (RE/100 g) ... 46
DAFTAR GAMBAR
Nomor Halaman
1. Daun Torbangun. ... 3
2. Reaksi umum proses oksidasi lemak dan minyak ... 8
3. Struktur vitamin A ... 11
4. Tablet vitamin A 20.000 IU merek Kimia Farma ... 11
5. MSK di dalam kemasan botol ... 13
6. Struktur umum ß-karoten ... 17
7. Diagram alir penelitian ... 24
8. Diagram alir proses pengolahan sayur sop daun Torbangun ... 27
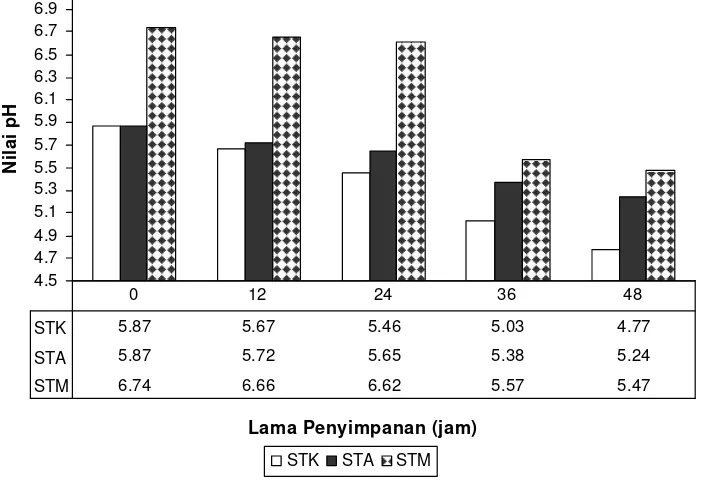
9. Pengaruh sumber antioksidan dan lama penyimpanan terhadap nilai pH sop daun Torbangun ... 31
10. Pengaruh interaksi perlakuan terhadap nilai pH sop daun Torbangun ... 32
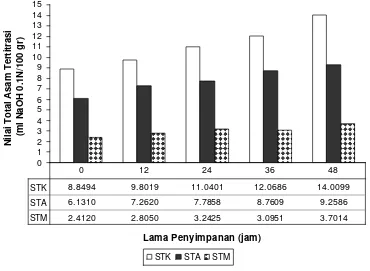
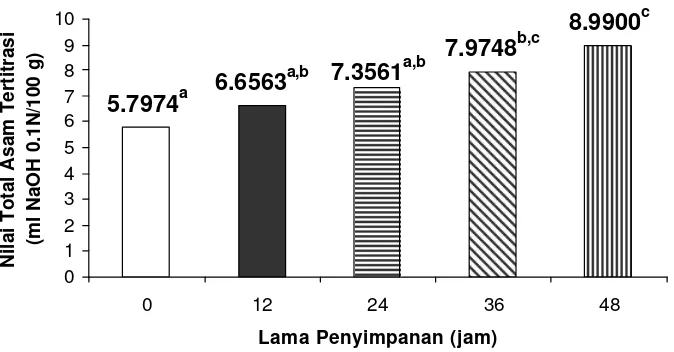
10. Pengaruh sumber antioksidan dan lama penyimpanan terhadap nilai Total Asam Tertitrasi (TAT) sop daun Torbangun ... 34
11. Pengaruh sumber antioksidan terhadap nilai TAT sop daun Torbangun ... 36
12. Pengaruh lama penyimpanan terhadap nilai TAT sop daun Torbangun ... 37
13. Pengaruh sumber antioksidan dan lama penyimpanan terhadap nilai bilangan peroksida sop daun Torbangun ... 38
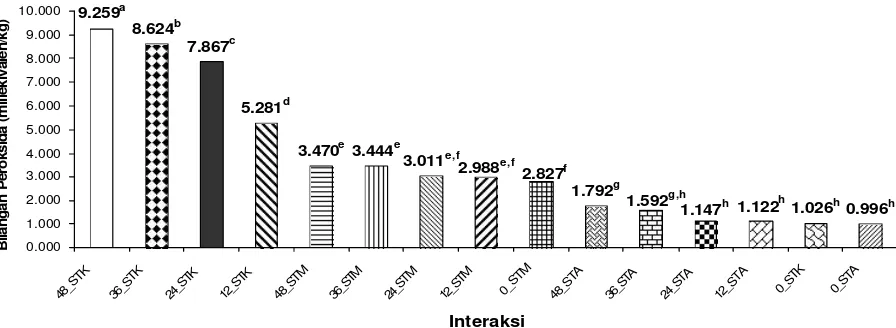
14. Pengaruh interaksi sumber antioksidan dan lama penyimpanan terhadap nilai bilangan peroksida sop daun Torbangun ... 38
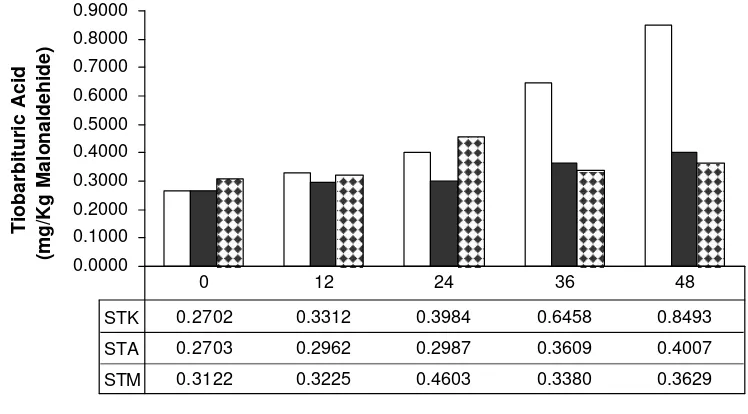
15. Pengaruh sumber antioksidan dan lama penyimpanan terhadap nilai Thiobarbituric acids (TBA) sop daun Torbangun ... 42
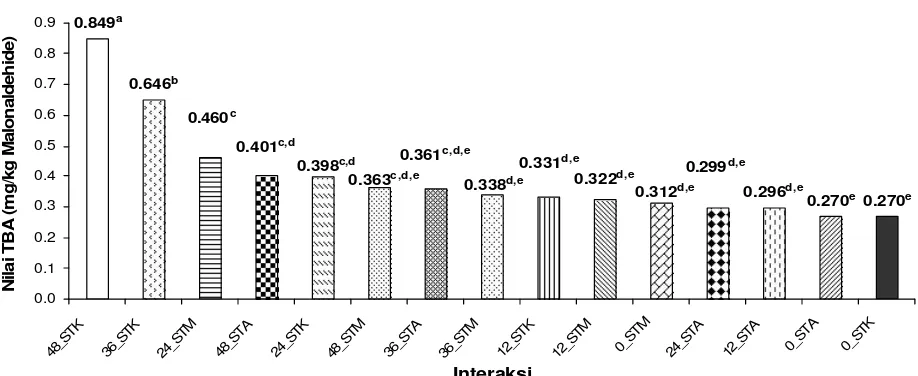
16.Pengaruh interaksi sumber antioksidan dan lama penyimpanan terhadap nilai Thiobarbituric acids (TBA) sop daun Torbangun... 43
17.Perubahan jumlah mikroorganisme sayur Torbangun kontrol (STK) ... 50
18.Perubahan jumlah sayur Torbangun dengan penambahan tablet vitamin A (STA) ... 52
20. Perubahan jumlah mikroorganisme sayur Torbangun dengan penambahan MSK (STM) ... 54
21. Nilai median uji aroma pada jam ke-12 ... 56
22. Nilai median uji aroma pada jam ke-36 ... 56
23. Nilai grand median uji aroma ... 57
DAFTAR GAMBAR
Nomor Halaman
25. Nilai median uji warna pada jam ke-36 ... 58
26. Nilai grand median uji warna ... 59
27. Nilai median uji kekentalan jam ke-12 ... 60
28. Nilai median uji kekentalan pada jam ke-36 ... 60
29. Perbandingan nilai median uji kekentalan pada lama penyimpanan ke-12 jam dan ke-36 jam ... 61
30. Nilai median uji tekstur pada jam ke-12 ... 62
DAFTAR LAMPIRAN
Nomor Halaman
1. Perhitungan konversi tablet vitamin A yang dibutuhkan/Kg bahan . 71
2. Metode analisis uji mutu kimiawi kerusakan lemak ... 72
3. Prosedur analisis HPLC vitamin A dan ß-karoten ... 74
4. Perhitungan retensi vitamin A akibat proses pengolahan, penyimpanan, dan retensi total pada STA ... 75
5. Perhitungan retensi ß-karoten akibat proses pengolahan, penyimpanan, dan retensi total pada STM ... 77
6. Uji mikrobiologi dengan metode Total Plate Count (TPC) ... 79
7. Lembar penilaian organoleptik uji hedonik ... 80
8. Analisis data hasil uji mutu kimiawi kerusakan lemak ... 81
9. Perhitungan retensi vitamin A daun Torbangun pada STK... 86
10. Tingkat kecukupan vitamin A dari STA dan STM ... 87
11. Perhitungan jumlah mikroorganisme ... 88
12. Hasil analisis data organoleptik uji hedonik ... 90
13. Perhitungan biaya penggunaan antioksidan tablet vitamin A dan MSK ... 94
14. Metode analisis proksimat ... 95
15. Tabel data sampel yang dianalisis dengan metode HPLC ... 97
Oleh:
DEVI YULIAWATI
A54103017
PROGRAM STUDI
GIZI MASYARAKAT DAN SUMBERDAYA KELUARGA
FAKULTAS PERTANIAN
(CPO) to The Durability of Torbangun ( Lour.) Soup (Under tuition of Dr. Ir. Evy Damayanthi, MS. and drh. M. Rizal M. Damanik, M.Rep.Sc, PhD.)
merupakan anak pertama dari tiga bersaudara pasangan Bambang Tri Waluyo
dan Titik Wahyuni. Pendidikan TK ditempuh di Taman Kanak-Kanak PTPN VIII
Tanjung Morawa, Sumatera Utara dari tahun 1989-1990 dan Taman
Kanan-Kanak Bhayangkari Curug, Tangerang dari tahun 1990-1991. Pendidikan SD
ditempuh di SD Islamic Village, Karawaci, Tangerang dari tahun 1991-1997.
Penulis melanjutkan pendidikan SLTP di SLTP Dian Harapan Karawaci,
Tangerang dari tahun 1997-1998, dan di SLTP Negeri 1 Subang, Jawa Barat dari
tahun 1998-2000. Pendidikan SMU ditempuh di SMU Negeri 1 Subang, Jawa
Barat dari tahun 2000-2003.
Penulis diterima sebagai mahasiswa Departemen Gizi Masyarakat dan
Sumberdaya Keluarga pada tahun 2003 melalui jalur Undangan Seleksi Masuk
IPB (USMI). Pada periode 2003/2004 pernah menjadi anggota Biro Hubungan
Masyarakat Forum Keluarga Masjid GMSK (FKMG). Pada periode 2004/2005
pernah menjadi anggota Biro Kajian Strategis Himpunan Mahsiswa Peminat Ilmu
Gizi Pertanian (HIMAGITA). Sejak tahun 2004-2006 penulis aktif sebagai staf
Divisi Kajian Strategis Badan Konsultasi Gizi (BKG) dan pada periode 2006/2007
pernah menjabat sebagai ketua Divisi Kajian Strategis Badan Konsultasi Gizi
(BKG). Pada tahun 2007 penulis menjadi asisten untuk mata kuliah Metabolisme
rahmat dan karunia-Nya penulis dapat menyelesaikan skripsi ini. Penulis
menyampaikan penghargaan dan ucapan terima kasih kepada :
1. Ibu Dr. Ir. Evy Damayanthi, M.S. dan Bapak Drh. Rizal Damanik M.Rep.Sc,
PhD sebagai dosen pembimbing skripsi yang telah memberikan semangat
dan masukan ilmu yang sangat berarti dan dengan sabar membimbing
penulis selama penelitian hingga penyelesaian tugas akhir ini.
2. Keluargaku tersayang : Papa, Mama, Eca, Ipam, dan Kkku sebagai sumber
semangat, motivasi, finansial dan kasih sayang yang tidak pernah habis
3. Pak Mashudi yang telah banyak membantu dan menjadi teman untuk
berdiskusi tentang penelitian ini.
4. Ibu Ir. Cesilia Meti Dwiriani, Msc sebagai pembimbing akademik.
5. Ibu Dr.Ir Lilik Kustiyah, MS sebagai dosen pemandu seminar.
6. Ibu Dr. Ir. Sri Anna Marliyati, MS sebagai dosen penguji yang telah begitu
banyak memberikan saran.
7. Bu Dini, Mas Yudi, Pak Lalu, dan Pak Danu di Balitpasca Panen, Cimanggu
Bogor atas bantuan dan bimbingannya.
8. Seluruh dosen dan staf Departemen GM (Teh Popon, Bu Yati, Teh Yati, Pak
Ugan, dan Mas Rena) yang telah mendidik, membimbing, dan membantu
dengan penuh kasih sayang, serta canda ria.
9. Temanku senasib dan sepenanggungan dalam suka dan duka (Betsy dan
Deni Alam’39) : Andi, Inoel, Malie, Bambang, Ade, Wewew, Vivi, Tika, Tegar,
Maning, Nining, MeiMei, Aris, Yudith, Sendi, dan seluruh GMSK’40. Terima
kasih atas kenangan yang begitu indah.
10. Teman-teman di HIMAGITA dan BKG yang telah memberikan warna berbeda
pada dunia.
11. Kakak-kakakku GMSK’37 (Mbak Nisa’14, Mbak Ama, dan Mbak Mada),
GMSK’38, GMSK’39, dan Adik-Adikku GMSK’41,GM’42, serta IKK’42.
12. Semua Pihak yang telah membantu dalam penelitian dan penyusunan skripsi
ini, memberi bantuan spiritual yang tidak dapat terhitung dan tergantikan.
Semoga skripsi ini dapat bermanfaat bagi yang membacanya.
Bogor, Juli 2007
DAFTAR TABEL ... iii
DAFTAR GAMBAR ... iv
DAFTAR LAMPIRAN ... vi
PENDAHULUAN ... 1
Latar belakang... 1
Tujuan ... 2
Manfaat ... 2
TINJAUAN PUSTAKA ... 3
Daun Torbangun ... 3
Santan kelapa ... 5
Reaksi oksidasi ... 8
Antioksidan ... 9
Vitamin A ... 10
Minyak Sawit Kasar ... 12
Mikrobiologi pangan ... 17
BAHAN DAN METODE ... 23
Waktu dan tempat ... 23
Bahan dan alat ... 23
Metode penelitian ... 24
Pengolahan dan analisis data ... 29
HASIL DAN PEMBAHASAN ... 31
Uji kimiawi kerusakkan lemak ... 31
Nilai pH ... 31
Total Asam Tertritasi (TAT) ... 34
Bilangan peroksida ... 37
Thiobarbituric acids (TBA) ... 41
Hasil analisis Vitamin A dan ß-karoten ... 45
Pengaruh pengolahan dan penyimpanan ... 45
Peranan STA dan STM dalam memenuhi Angka Kecukupan Gizi (AKG) Vitamin A Uji organoleptik ... 48
Hasil uji mikrobiologi ... 49
Halaman
Sayur Torbangun vitamin A ... 51
Sayur Torbangun MSK ... 52
Hasil uji hedonik organoleptik ... 55
Aroma ... 55
Warna ... 57
Kekentalan ... 59
Tekstur ... 61
Kelebihan dan kekurangan penggunaan tablet vitamin A dan MSK sebagai antioksidan ... 63
KESIMPULAN DAN SARAN ... 65
Kesimpulan ... 65
Saran ... 66
DAFTAR PUSTAKA ... 67
DAFTAR TABEL
Nomor Halaman
1. Komposisi zat gizi daun Torbangun dan daun katuk ... 4
2. Komposisi zat gizi sayur sop daun Torbangun (150 g) ... 5
3. Pengaruh penambahan air terhadap komposisi kimia santan ... 6
4. Kandungan asam lemak minyak sawit kasar ... 13
5. Karakteristik minyak sawit kasar ... 13
6. Komposisi karotenoid dalam minyak sawit kasar ... 16
7. Komposisi bahan yang digunakan dalam pembuatan sop daun Torbangun pada berbagai jenis analisis ... 25
8. Hasil analisis proksimat sop daun Torbangun ... 25
9. Contoh untuk analisis HPLC ... 28
10. Kandungan vitamin A pada sop daun Torbangun dan bahan penyusunnya (RE/100 g) ... 46
DAFTAR GAMBAR
Nomor Halaman
1. Daun Torbangun. ... 3
2. Reaksi umum proses oksidasi lemak dan minyak ... 8
3. Struktur vitamin A ... 11
4. Tablet vitamin A 20.000 IU merek Kimia Farma ... 11
5. MSK di dalam kemasan botol ... 13
6. Struktur umum ß-karoten ... 17
7. Diagram alir penelitian ... 24
8. Diagram alir proses pengolahan sayur sop daun Torbangun ... 27
9. Pengaruh sumber antioksidan dan lama penyimpanan terhadap nilai pH sop daun Torbangun ... 31
10. Pengaruh interaksi perlakuan terhadap nilai pH sop daun Torbangun ... 32
10. Pengaruh sumber antioksidan dan lama penyimpanan terhadap nilai Total Asam Tertitrasi (TAT) sop daun Torbangun ... 34
11. Pengaruh sumber antioksidan terhadap nilai TAT sop daun Torbangun ... 36
12. Pengaruh lama penyimpanan terhadap nilai TAT sop daun Torbangun ... 37
13. Pengaruh sumber antioksidan dan lama penyimpanan terhadap nilai bilangan peroksida sop daun Torbangun ... 38
14. Pengaruh interaksi sumber antioksidan dan lama penyimpanan terhadap nilai bilangan peroksida sop daun Torbangun ... 38
15. Pengaruh sumber antioksidan dan lama penyimpanan terhadap nilai Thiobarbituric acids (TBA) sop daun Torbangun ... 42
16.Pengaruh interaksi sumber antioksidan dan lama penyimpanan terhadap nilai Thiobarbituric acids (TBA) sop daun Torbangun... 43
17.Perubahan jumlah mikroorganisme sayur Torbangun kontrol (STK) ... 50
18.Perubahan jumlah sayur Torbangun dengan penambahan tablet vitamin A (STA) ... 52
20. Perubahan jumlah mikroorganisme sayur Torbangun dengan penambahan MSK (STM) ... 54
21. Nilai median uji aroma pada jam ke-12 ... 56
22. Nilai median uji aroma pada jam ke-36 ... 56
23. Nilai grand median uji aroma ... 57
DAFTAR GAMBAR
Nomor Halaman
25. Nilai median uji warna pada jam ke-36 ... 58
26. Nilai grand median uji warna ... 59
27. Nilai median uji kekentalan jam ke-12 ... 60
28. Nilai median uji kekentalan pada jam ke-36 ... 60
29. Perbandingan nilai median uji kekentalan pada lama penyimpanan ke-12 jam dan ke-36 jam ... 61
30. Nilai median uji tekstur pada jam ke-12 ... 62
DAFTAR LAMPIRAN
Nomor Halaman
1. Perhitungan konversi tablet vitamin A yang dibutuhkan/Kg bahan . 71
2. Metode analisis uji mutu kimiawi kerusakan lemak ... 72
3. Prosedur analisis HPLC vitamin A dan ß-karoten ... 74
4. Perhitungan retensi vitamin A akibat proses pengolahan, penyimpanan, dan retensi total pada STA ... 75
5. Perhitungan retensi ß-karoten akibat proses pengolahan, penyimpanan, dan retensi total pada STM ... 77
6. Uji mikrobiologi dengan metode Total Plate Count (TPC) ... 79
7. Lembar penilaian organoleptik uji hedonik ... 80
8. Analisis data hasil uji mutu kimiawi kerusakan lemak ... 81
9. Perhitungan retensi vitamin A daun Torbangun pada STK... 86
10. Tingkat kecukupan vitamin A dari STA dan STM ... 87
11. Perhitungan jumlah mikroorganisme ... 88
12. Hasil analisis data organoleptik uji hedonik ... 90
13. Perhitungan biaya penggunaan antioksidan tablet vitamin A dan MSK ... 94
14. Metode analisis proksimat ... 95
15. Tabel data sampel yang dianalisis dengan metode HPLC ... 97
PENDAHULUAN
Latar belakang
Kepercayaan terhadap suatu jenis makanan yang dapat bermanfaat
selama masa kehamilan dan menyusui berkembang luas di dalam kepercayaan
wanita tradisional di Indonesia (Damanik et al. 2004). Makanan merupakan
sumber utama dalam memenuhi kebutuhan gizi janin yang ada di dalam
kandungan dan juga bayi yang telah dilahirkan melalui Air Susu Ibu (ASI).
Sebagai contoh, wanita Batak yang sedang menyusui di Kabupaten Simalungun,
Sumetera Utara mempunyai tradisi dan kepercayaan bahwa dengan
mengkonsumsi daun Torbangun selama satu bulan setelah melahirkan akan
meningkatkan produksi ASI (Damanik et al. 2001). Tradisi tersebut telah berjalan
selama ratusan tahun dan sampai sekarang masih terus dilakukan.
Daun Torbangun tersebut diolah menjadi makanan yang dikenal dengan
sayur sop daun Torbangun. Proses pengolahan sayur sop daun Torbangun
biasanya dilakukan oleh ibu, ibu mertua, atau suami (Damanik et al. 2001). Pada
masa kini, daun Torbangun dimasak dengan menggunakan santan dan
ditambahkan potongan ayam atau ikan untuk meningkatkan palatabilitas.
Selain menambah cita rasa, pengunaan santan dalam pembuatan sop
daun Torbangun dapat menyebabkan kerugian yaitu mudah teroksidasi karena
kandungan lemaknya yang tinggi. Selanjutnya, selama penyimpanan, kerusakan
fisik dan kimia dapat terjadi. Selain itu, penurunan mutu selama penyimpanan
dapat terjadi karena adanya aktivitas mikroba yang tumbuh pada sayur santan
daun Torbangun.
Antioksidan merupakan senyawa yang terdapat secara alami pada
hampir semua bahan pangan. Senyawa tersebut berfungsi untuk melindungi
bahan pangan dari kerusakan karena terjadinya reaksi oksidasi lemak atau
minyak yang menjadikan bahan pangan beraroma tengik. Walaupun antioksidan
terdapat dalam bahan pangan secara alami, jika bahan pangan tersebut
mengalami proses pengolahan, maka akan terjadi degradasi kimia dan fisika,
sehingga fungsinya sebagai antioksidan semakin berkurang. Oleh karena itu,
perlu ditambahkan zat antioksidan yang memberikan dua keuntungan, pada satu
sisi mampu berfungsi sebagai antioksidan sehingga dapat meningkatkan
keawetan, dan di sisi lain mampu memenuhi kebutuhan gizi mikro (vitamin dan
Vitamin A merupakan salah satu vitamin yang dikenal sebagai zat gizi
yang sangat diperlukan tubuh. Selain itu, vitamin A dapat berperan sebagai
antioksidan dan mampu meningkatkan sistem imunitas tubuh. Menurut La
Chance (1996) yang diacu dalam Muchtadi dan Astawan (2001), dengan
konsumsi 3,2 mg karoten/hari mampu memberikan efek protektif. Salah satu
bahan pangan yang kaya akan β-karoten sebagai pro vitamin A adalah minyak
sawit kasar (MSK).
Pengkajian mengenai pengaruh penambahan antioksidan vitamin A dan
karotenoid yang banyak terdapat pada MSK terhadap keawetan sayur sop daun
Torbangun belum pernah dilakukan sebelumnya. Oleh karena itu, peneliti tertarik
untuk mengkaji lebih dalam aspek ini dalam suatu penelitian dengan harapan
hasilnya dapat bermanfaat bagi masyarakat luas.
Tujuan Tujuan Umum :
Penelitian ini bertujuan untuk mengkaji pengaruh penambahan vitamin A
dan minyak sawit kasar (MSK) sebagai antioksidan terhadap keawetan sop daun
Torbangun (Coleus amboinicus Lour.).
Tujuan khusus :
1. Menetapkan konsentrasi antioksidan (vitamin A dan MSK) yang
ditambahkan dan lama penyimpanan maksimal sayur sop daun
Torbangun.
2. Mempelajari pengaruh antioksidan terhadap kerusakan lemak selama
penyimpanan.
3. Menganalisis kadar vitamin A sayur sop daun Torbangun selama
penyimpanan.
4. Menganalisis jumlah mikroorganisme dengan metode Total Plate Count
(TPC) dalam sayur sop daun Torbangun.
5. Mempelajari tingkat kesukaan sayur sop daun Torbangun
Manfaat
Penelitian ini diharapkan dapat menjadi salah satu acuan untuk
pengembangan produksi sayur santan daun Torbangun. Selain itu diharapkan
dengan adanya penelitian ini sayur sop daun Torbangun dapat diterima oleh
TINJAUAN PUSTAKA Daun Torbangun
Tanaman Torbangun (Coleus amboinicus Lour.) termasuk dalam bangsa
solanes, suku labiatae, dan marga coleus (de Padva et al 1999). Tanaman ini
memiliki nama-nama yang berbeda untuk setiap daerah dan suku bangsa, yaitu
ajeran atau ajiran (Sunda), daun kucing (Jawa), Torbangun (Batak), sukan
(melayu), daun kambing (Madura), iwak (Bali), dan kunu etu (Timor)
(Syamsuhidayat & Hutapea 1991, diacu dalam Puspitasari 2003).
Daun Torbangun mempunyai sifat khas, yakni mampu menghangatkan
tubuh. Daun Torbangun juga mampu menetralkan, dan membersihkan darah.
Gambar daun Torbangun ditunjukkan oleh Gambar 1.
Gambar 1 Daun Torbangun.
Deskripsi botani
Daun Torbangun merupakan tanaman semak yang menjalar. Batangnya
berkayu, lunak, dan beruas-ruas. Ruas yang menempel di tanah akan tumbuh
akar, batang muda berwarna hijau pucat. Daun tunggal, mudah patah, berbentuk
bulat telur, tebal, tepinya beringgit, berambut, panjang 6-7 cm, lebar 5-6 cm,
bertulang menyirip, dan berwarna hijau muda. Bunga majemuk, berbentuk
tandan, mahkota bentuk mangkok berwarna ungu. Bagian yang dapat digunakan
yakni seluruh bagian tumbuhan. Jarang berbunga namun mudah sekali dibiakkan
dengan stek dan cepat berakar di dalam tanah (Heyne 1987, diacu dalam
Puspitasari 2003).
Komposisi zat gizi daun Torbangun
Komposisi zat gizi daun Torbangun yang terdapat dalam Daftar
Komposisi Zat Gizi Pangan Indonesia tahun 1990 menyebutkan bahwa dalam
mg, dan karoten total sebesar 13288 µkg. Kandungan kalsium, besi, dan karoten
total pada daun Torbangun tersebut lebih besar dibandingkan dengan daun
katuk (Sauropus androgynus). Data selengkapnya tentang komposisi zat gizi
daun Torbangun dan katuk tercantum dalam Tabel 1 di bawah ini
Tabel 1 Komposisi zat gizi daun Torbangun dan daun katuk
Komposisi zat gizi Daun Torbangun Daun katuk
Energi (kkal)
Protein (g)
Lemak (g)
Hidrat arang (g)
Serat (g)
Abu (g)
Kalsium (mg)
Phosfor (mg)
Besi (mg)
Karoten total (µkg)
Vitamin A
Vitamin B1
Vitamin C
Air
Berat dapat dimakan 27 1.3 0.6 4.0 1.0 1.6 279 40 13.6 13288 0 0.16 5.1 92.5 66 59 6.4 1.0 9.9 1.5 1.7 233 98 3.5 10020 0 0 164 81 42
Sumber: Mahmud et al (1990)
Pemanfaatan daun Torbangun
Pemanfaatan daun Torbangun terutama dilakukan oleh masyarakat etnis
Batak dalam bentuk olahannya, yakni sayur sop daun Torbangun. Masyarakat
etnis batak percaya bahwa sayur sop daun Torbangun mampu meningkatkan
produksi air susu ibu (ASI) (Damanik et al. 2001 & 2004).
Hal tersebut di atas ternyata dapat dibuktikan secara ilmiah. Berdasarkan
hasil penelitian Damanik (2006) bahwa pada saat minggu kedua (hari ke 14
hingga ke 28 setelah suplementasi sayur sop daun Torbangun), wanita yang
telah mengkonsumsi sayur sop daun Torbangun tetap mengalami peningkatan
kuantitas ASI. Selain itu, daun Torbangun juga mampu meningkatkan kesehatan
wanita pasca melahirkan, berperan sebagai uterine cleansing agent, dan dalam
proses melahirkan (Damanik, et al. 2001). Komposisi zat gizi sayur sop daun
Torbangun dapat dilihat pada Tabel 2.
Tabel 2 Komposisi zat gizi sayur sop daun Torbangun (150g)
Zat gizi Rata-rata ± SD
Lemak (g)
Protein (g)
Karbohidrat (g)
Air (g)
Mineral (mg)
Seng
Besi
Kalsium
Magnesium
Pottasium
16,3 ± 4,6
2,4 ± 0,1
5,3 ± 0,3
121,5 ± 14,7
2,8 ± 0,1
6,8 ± 0,1
393,1 ± 6,5
124,1 ± 6,3
1219,2 ± 80,7
Sumber: Damanik et al. (2006)
Santan Kelapa
Santan kelapa adalah sebutan yang digunakan untuk cairan yang
dihasilkan dari proses ekstraksi daging kelapa yang telah diparut secara manual
atau menggunakan alat, dengan atau tanpa penambahan air (Gonzales 1990).
Definisi lain dari santan kelapa adalah produk cair yang diperoleh dengan
menyaring daging buah kelapa (Cocos nucifera) dengan atau tanpa penambahan
bahan tambahan makanan yang diizinkan (SNI 01-3816-1995 tentang santan
kelapa). Santan berbentuk emulsi lemak dalam air dengan ukuran partikel lebih
besar dari 1µ sehingga berwarna putih susu (Kirk & Othmer 1950)
Santan kelapa biasanya dihasilkan dari buah kelapa yang telah matang,
berusia sekitar 12 bulan. Pada usia tersebut, daging buah kelapa telah mengeras
dan tebal, dengan komposisi yang dimiliki adalah : kelembaban 50%, minyak
34%, protein 3.5%, serat 3%, abu 2.2%, dan karbohidrat 7.3%. Santan kelapa
banyak digunakan sebagai bahan tambahan dalam mengolah ikan, daging sapi,
daging unggas, dan sayur-sayuran sebagai makanan. Selain itu, santan kelapa
juga dapat digunakan dalam proses pembuatan kue (Gonzales 1990).
Santan kelapa terdiri atas globula-globula kecil yang terdapat dalam fase
minyak yang terdispersi di dalam air. Globula-globula tersebut hampir sama
Emulsi santan relatif stabil karena memiliki fosfolipid, lesitin, dan sepalin
yang diketahui berfungsi sebagai stabilizer (Gonzales 1990). Stabilitas emulsi
dipengaruhi oleh ukuran partikel, perbedaan densitas kedua fase, viskositas,
muatan partikel, jumlah dan jenis emulsifier serta suhu penyimpanan
(Soemaatmadja 1974). Lemak dalam santan, selain sebagai pelarut vitamin A, D,
E, dan K juga dapat menambah citarasa bahan pangan atau memberi rasa gurih
pada makanan dan menambah kalori (Winarno 1997).
Kualitas santan kelapa selain dipengaruhi oleh teknologi dalam
pemrosesan, juga dipengaruhi oleh perbedaan varietas, tingkat kematangan
buah kelapa, ukuran partikel daging buah, suhu pemrosesan, jumlah air yang
digunakan, dan tekanan yang diberikan saat proses ekstraksi. Rasio berat
daging buah kelapa dengan berat air yang terbaik adalah 1 : 3 agar ekstraksi
berjalan baik, sehingga lemak yang tersisa pada ampas relatif rendah
(Somaatmadja 1974). Penambahan air sangat mempengaruhi komposisi kimia
santan. Tabel 3 menunjukkan komposisi kimia santan murni dan santan dengan
penambahan air.
Tabel 3 Pengaruh penambahan air terhadap komposisi kimia santan.
Zat gizi dan kalori Santan murni + air (1 : 1) Kalori (Kal) Protein (%) Lemak (%) Karbohidrat (%) Kalsium (mg) Phospor (mg) Vitamin A (gram) Air (%) 324.0 4.2 34.3 5.6 14.0 1.9 0.0 54.9 122.0 2.0 10.0 7.6 25.0 0.1 0.0 80.0 Sumber: Cheosakul (1967) diacu dalam Somaatmadja (1974
Hasil penelitian Gonzales (1990) menunjukkan bahwa keefektifan dalam
penambahan air ke dalam daging buah kelapa bergantung pada suhu air dan
lama pencampuran. Efesiensi ekstraksi santan akan meningkat seiring dengan
meningkatnya suhu dan lama waktu pencampuran, yakni lebih dari 80o C saat
protein mulai terkoagulasi.
Menurut Muchtadi (1989), bila dibandingkan dengan proses perebusan,
pengukusan, dan penumisan, maka pemasakan sayuran di rumah tangga, akan
berpengaruh dalam menurunkan kadar antioksidan alami sayuran. Kadar
antioksidan yang mengalami penurunan terjadi pada vitamin C, alfa-tokoferol,
dan senyawa fenol yang terkandung dalam sayuran. Namun, ternyata
alfa-tokoferol yang mungkin disebabkan karena adanya tambahan antioksidan ini dari
minyak kelapa.
Kerusakan santan kelapa
Santan merupakan produk pangan yang mengandung kadar air, protein
dan lemak cukup tinggi, sehingga mudah ditumbuhi oleh mikroorganisme
pembusuk dan santan menjadi mudah rusak. Kerusakan tersebut antara lain
pecahnya emulsi santan, timbulnya aroma tengik, dan perubahan warna menjadi
agak coklat (Soemaatmadja 1974).
Gonzales (1990) menyatakan bahwa selama santan disimpan atau
didiamkan, butir lemak yang diselubungi lapisan protein dan karbohidrat akan
memisah ke bagian atas dan membentuk kepala santan, sedangkan air tertinggal
di bawah. Pemanasan santan juga bertujuan untuk menggumpalkan protein dan
memecah emulsi santan, sehingga butir minyak bergabung serta menguapkan
airnya dan diperoleh minyak. Disamping itu, pemanasan juga dapat membunuh
mikroba dan menginaktivasi enzim (Bailey 1951).
Santan kelapa segar memiliki pH = 6 dan termasuk ke dalam makanan
dengan pH rendah. Gonzales (1990) melaporkan bahwa densitas dan pH santan
dipengaruhi oleh suhu, sedangkan kekentalan dan tegangan permukaan santan
akan meningkat tetap pada suhu di atas 60oC lalu kemudian menurun secara
perlahan. Hal tersebut mengacu pada terjadinya koagulasi protein yang terjadi
mulai suhu 60oC. Namun, menurut Hagenmaier (1980) yang diacu di dalam
Gonzales (1990) menyatakan bahwa koagulasi protein dimulai pada saat suhu
80oC. Protein santan seperti albumin, globulin, prolamin, dan glutelin mudah
terkoagulasi oleh panas dan mengendap pada pH = 4.
Santan kelapa adalah emulsi dari lemak, protein, dan karbohidrat dalam
air yang kemantapannya tidak bertahan lama. Dalam keadaan normal, santan
kelapa hanya tahan disimpan selama 24 jam. Setelah itu santan akan mudah
pecah dan menimbulkan bau serta rasa yang tidak sedap. Kandungan air dan
protein yang tinggi di dalam santan dapat menyebabkan santan mudah
mengalami kerusakan. Dengan adanya air, lemak dapat terhidrolisis menjadi
gliserol dan asam lemak. Adanya asam-asam lemak akan menimbulkan bau dan
Reaksi oksidasi
Oksidasi biasanya dimulai dengan pembentukan peroksida dan
hidroperoksida. Tingkat selanjutnya adalah terurainya asam-asam lemak disertai
dengan konversi hidroperoksida menjadi aldehid dan keton serta asam-asam
lemak bebas. Rancidity terbentuk karena adanya aldehida, bukan peroksida
(Ketaren 1986). Menurut Nawar (1996) reaksi umum proses oksidasi lemak dan
minyak diperlihatkan oleh Gambar 2.
Initiator
→
k1 radikal bebas (R?, ROO?) Initiation (Inisiasi) (1) R? + O2
→
2 k
ROO? (2)
ROO? + RH
→
k3 ROOH + R? Propagation (perambatan) (3)
R? + R?
→
k4 (4) R? + ROO?
→
k5 nonradical products (5) ROO? + ROO?
→
k6 Termination (penghentian) (6)Gambar 2 Reaksi umum proses oksidasi lemak dan minyak (Nawar 1996)
Bentuk kerusakan lemak, terutama ketengikan yang paling penting
disebabkan oleh aksi oksigen udara terhadap lemak. Dalam bahan pangan
berlemak, unsur utama yang mudah mengalami oksidasi spontan adalah asam
lemak tidak jenuh dan sejumlah kecil persenyawaan yang merupakan unsur yang
cukup penting (Ketaren 1986).
Menurut Winarno (1997), kerusakan lemak yang utama adalah timbulnya
bau dan rasa tengik yang disebut proses ketengikan. Hal ini disebabkan oleh
proses otooksidasi radikal asam lemak tak jenuh dalam lemak. Otooksidasi
dimulai dengan pembentukan radikal-radikal bebas yang disebabkan oleh
faktor-faktor yang dapat mempercepat reaksi seperti cahaya, panas, peroksida lemak
atau hidroperoksida, logam-logam berat seperti Cu, Fe, Co, dan Mn, logam
porifirin seperti hematin, hemoglobin, mioglobin, klorofil, dan enzim-enzim
lipoksidase.
Reaksi oksidasi dapat mengakibatkan berbagai macam kerugian,
kerugian-kerugian tersebut antara lain adalah: 1) penurunan nilai ekonomi yang
cukup besar, 2) mempengaruhi efisiensi dari tahap-tahap pengolahan, 3)
kerusakan vitamin, penurunan nilai gizi, dan adanya reaksi polimerisasi
(Sulaeman 1990).
Antioksidan
Salah satu cara yang paling sering dilakukan untuk mencegah terjadinya
oksidasi adalah penambahan antioksidan ke dalam bahan pangan berlipid.
Penggunaan antioksidan ini bertujuan untuk meminimalkan ketengikan,
menghambat pembentukan produk oksidasi yang bersifat toksik yang berdampak
pada penurunan kualitas gizi, dan untuk memperpanjang masa simpan makanan
(Fatimah 2005).
Antioksidan yang digunakan dalam bahan pangan harus memenuhi
syarat-syarat sebagai berikut: 1) aktif pada konsentrasi rendah; 2) tidak
menimbulkan keracunan; 3) tidak menimbulkan bau, rasa, dan warna pada
bahan pangan; 4) mudah dicampur pada bahan pangan; 5) mudah diperoleh dan
murah; 6) mudah dideteksi, diidentifikasi, maupun diukur (Ludenberg 1961 diacu
dalam Priatna 1992).
Antioksidan berdasarkan mekanisme kerjanya dapat dikelompokkan
sebagai pengurai peroksida dan penangkap radikal bebas. Sulfur dan fosfor
dalam bentuk sulfida, dithiocarbamate, fosfat dan dithiophosphate berfungsi
sebagai pengurai peroksida. Nitrogen dan oksigen dalam inhibitor sebagai
arylamines dan phenol berfungsi sebagai penangkap radikal bebas.
Winarno (1997) menyatakan bahwa adanya antioksidan dalam lemak
akan mengurangi kecepatan proses oksidasi. Antioksidan terdapat secara
alamiah dalam lemak nabati, dan kadang-kadang sengaja ditambahkan. Ada dua
macam antioksidan, yaitu antioksidan primer dan antioksidan sekunder.
Antioksidan primer adalah suatu zat yang dapat menghentikan reaksi
berantai pembentuk radikal yang melepaskan hidrogen. Zat-zat yang termasuk
ke dalam golongan ini dapat berasal dari alam dan dapat pula buatan.
Antioksidan primer yang berasal dari alam yang sering ditemukan adalah
tokoferol, sedangkan antioksidan primer yang berasal dari bahan sintetik atau
buatan misalnya adalah Butylated hydroxyanisole (BHA), Butylated
hydroxytoluene (BHT), Propylgallate (PG), dan NDGA (Nordihidroquairetic Acid).
Antioksidan sintetik yang ditambahkan ke dalam lemak atau bahan pangan untuk
mencegah ketengikan biasanya adalah senyawa-senyawa fenol yang biasanya
agak beracun. Oleh karena itu, penambahan antioksidan ini harus memenuhi
Antioksidan sekunder adalah suatu zat yang dapat mencegah kerja
prooksidan sehingga dapat digolongkan sebagai sinergik. Beberapa asam
organik tertentu, biasanya asam di- atau trikarboksilat, dapat mengikat
logam-logam (sequestran).
Menurut Surai (2003) ada bermacam-macam tanggapan sistem
antioksidan dalam melindungi sel-sel dari radikal bebas, sistem tersebut meliputi:
þ Antioksidan yang larut dalam lemak alami (vitamin A, vitamin E, karotenoid, asam urat, dan lain-lain).
þ Antioksidan yang larut dalam air (asam askorbat, asam urat, dan lain-lain).
þ Enzim-enzim antioksidan (katalase, glutathione peroksidase, dan superoksida dismutase)
þ Sistem redoks tiol yang terdiri dari sistem glutathion
Ruxton (1994) dalam Subekti (1997) menyatakan bahwa istilah zat gizi
antioksidan mengacu kepada kemampuan dari suatu zat gizi untuk mencegah
kerusakan oksidatif pada sel. Sebagai contoh adalah ß-karoten, vitamin C,
selenium, dan vitamin E.
Stabilitas antioksidan terhadap panas
Pemilihan antioksidan yang tahan terhadap pemanasan sangat penting
untuk bahan pangan berlemak yang menggunakan suhu tinggi dalam proses
pembuatannya atau dalam aplikasinya. Apabila digunakan antiosidan yang tidak
tahan terhadap panas akan menyebabkan mutu bahan pangan tidak seperti yang
diinginkan karena umur simpan bahan tersebut tidak dipenuhi.
Senyawa-senyawa antioksidan mempunyai ketahanan terhadap panas
yang berbeda-beda. Menurut Francis (1985) dalam Andarwulan dan Fardiaz
(1994) asam askorbat, karotenoid (terutama ß-karoten) dan tokoferol relatif tidak
tahan terhadap panas, udara dan oksigen. Namun, senyawa-senyawa golongan
flavonoid dan tanin relatif tahan panas.
Vitamin A
Vitamin A merupakan nama generik yang menyatakan semua retinoid
dan prekusor atau provitamin A atau karotenoid yang mempunyai aktivitas
biologik sebagai retinol. Vitamin A adalah suatu kristal alkohol berwarna kuning
dan larut dalam lemak atau pelarut lemak. Dalam makanan, vitamin A biasanya
terdapat dalam bentuk ester retinil, yaitu terikat pada asam lemak rantai panjang
Menurut Winarno (1997), pada umumnya vitamin A mempunyai sifat
stabil terhadap panas, asam, dan alkali. Namun, mempunyai sifat yang mudah
teroksidasi oleh udara dan akan rusak bila dipanaskan pada suhu tinggi bersama
[image:31.595.230.393.471.588.2]udara, sinar, dan lemak yang sudah tengik.
Gambar 3 Struktur vitamin A (Winarno 1997)
Diacu dalam Almatsier (2000), vitamin A tahan terhadap panas cahaya
dan alkali, tetapi tidak tahan terhadap asam dan oksidasi. Pada cara memasak
biasa tidak banyak vitamin A yang hilang. Suhu tinggi pada waktu menggoreng
dapat merusak vitamin A, begitupun oksidasi pada minyak yang tengik.
Ketersediaan biologik vitamin A dapat meningkat dengan hadirnya vitamin E dan
antioksidan lain.
Gambar 4 Tablet vitamin A 20.000 IU merek Kimia Farma
Berdasarkan Muhilal dan Sulaeman (2004), angka aman untuk
kecukupan gizi vitamin A yang dianjurkan bagi wanita yang berusia diatas 10
tahun adalah 500 RE. Bagi wanita menyusui dengan usia bayi 0-12 bulan
kebutuhannya ditambah 350 RE.
Hanya vitamin A dalam bentuk retinol dan retinoid saja yang dapat
menyebabkan keracunan akut, karena penyerapannya cukup efisien (mendekati
berasal dari makanan, sifatnya tidak beracun, karena efisiensi penyerapannya
menurun jika intiknya meningkat. Gejala kelebihan vitamin A akan terjadi bila
mengkonsumsi dalam bentuk vitamin A yang berlebih. Karoten tidak dapat
menimbulkan gejala kelebihan, karena absorpsi karoten menurun bila konsumsi
tinggi. Selain itu, sebagian karoten yang diserap tidak diubah menjadi vitamin A,
akan tetapi disimpan di dalam lemak. Bila lemak di bawah kulit mengandung
banyak karoten, warna kulit akan terlihat kekuningan (Almatsier 2000). Pada
orang dewasa yang mengalami keracunan, gejalanya adalah mual, muntah,
tekanan cairan cerebrospinal yang meningkat, pusing, penglihatan kabur, dan
penurunan koordinasi (Allen & Haskell 2002).
Makanan yang kaya akan vitamin A dapat mencegah pembentukan
radikal oksigen dan peroksida lemak, dan ß-karoten sangat efisien dalam
menetralisir radikal oksigen. Vitamin A bersama dengan vitamin C, vitamin E, dan
selenium dapat menetralisir efek peroksida dan mengurangi karsinogenesis
(Weisburger 1991, diacu dalam Subekti 1997).
Degradasi dari vitamin A (retinoid dan karotenoid aktif) pada umumnya
setara dengan degradasi oksidatif dari lemak tak jenuh. Faktor-faktor yang
mempengaruhi oksidasi lemak juga mampu meningkatkan degradasi vitamin A,
baik pada oksidasi langsung maupun efek tak langsung dari radikal bebas
(Fennema 1996).
Degradasi oksidatif dari vitamin A dan karotenoid dalam makanan dapat
terjadi melalui peroksidasi langsung atau penyebab tidak langsung karena hasil
sampingan oksidasi asam lemak berupa radikal-radikal bebas. β-karoten dan
mungkin karoten lain memiliki kemampuan sebagai antioksidan dibawah kondisi
kekurangan oksigen, dan mampu sebagai prooksidan dibawah kondisi
konsentrasi oksigen tinggi (Fennema 1996).
Minyak Sawit Kasar
Minyak Sawit Kasar (MSK) merupakan hasil terpenting dari tanaman
sawit. MSK terbagi menjadi dua, yakni inti sawit kasar yang dapat diolah lebih
lanjut menjadi Processed Palm Oil (PPO) dan minyak inti sawit. Bentuk-bentuk
olah lanjut MSK yang telah banyak dikembangkan secara komersial yang
menunjukkan besarnya nilai manfaat MSK. Contoh MSK yang telah dikemas
Gambar 5 Minyak sawit kasar.
Minyak sawit memiliki ketahanan terhadap oksidasi, tidak terbakar, dan
tidak berbusa pada suhu tinggi (Bakrie 1998). Oleh karena itu, MSK sangat tepat
dipakai untuk kebutuhan sehari-hari rumah tangga, industri, hotel, dan restauran
setelah dilakukan pemurnian terlebih dahulu.
MSK diperoleh dari bagian mesokarp dan bagian inti (kernel) yang
disebut minyak inti sawit. MSK tersusun atas unsur-unsur C, H, dan O seperti
jenis minyak yang lainnya. Komposisi asam lemak MSK dapat dilihat pada Tabel
4, sedangkan Tabel 5 menunjukkan karakteristik MSK. Unsur lainnya dari MSK,
seperti gum (getah atau lendir) yang terdiri dari pospatida, protein, residu,
karbohidrat, air dan resin serta asam lemak bebas (Ketaren 1986).
Tabel 4 Kandungan asam lemak dalam MSK
Jenis asam lemak Jumlah (%) Asam miristat
Asam palmitat Asam stearat Asam oleat Asam linoleat
0,9 – 1,4 % 41,9 – 46,7 % 4,3 – 5,1 % 37,3 – 40,5 % 9,1 – 10,6 %
Sumber Bernardini (1983) diacu dalam Hendrawati (2001)
Tabel 5 Karakteristik MSK
Bilangan Iod Melting point
Bilangan penyabunan Fraksi tak tersabunkan Fraksi asam lemak bebas
50 – 58 27 – 500 C 195 – 205 0,5 – 2 3,7
Sumber Bernardini (1983) diacu dalam Hendrawati (2001)
Seperti umumnya minyak dan lemak yang dapat dikonsumsi, minyak
sawit dan turunannya, seperti palm olein dan palm stearin mudah dicerna,
diserap, dan digunakan pada proses metabolisme normal. Minyak sawit memiliki
kandungan asam lemak yang komposisinya merupakan 51% asam lemak tak
jenuh dan 49% asam lemak jenuh, sedangkan palm olein mempunyai lebih dari
Minyak sawit kaya akan komponen-komponen mikro yang memperkaya
keunikan dan keragaman zat gizinya. Yang terpenting diantaranya adalah
kandungan vitamin E (tokoferol dan tokotrienol) dan karotenoid (umumnya alfa
dan ß-karoten) (Anonymous 2005).
MSK adalah sumber terbanyak karotenoid alami, dengan konsentrasi
antara 700-1000 ppm. Konsentrasi itu setara dengan 15 kali karotenoid yang
terdapat pada wortel. Karotenoid yang terdapat di dalam minyak sawit terutama
adalah ß-karoten (55%), alfa karoten (35%), dan sejumlah kecil likopen,
phytoene, dan zeacarotenes. Karotenoid alami dari minyak sawit ini mempunyai
efek sebagai antioksidan dan anti-kanker, seperti yang telah diuji coba pada
hewan percobaan (Anonymous 2005).
Mutu minyak sawit selain dipengaruhi oleh varietas tanaman, juga
dipengaruhi olah kondisi proses ekstrasi dan kondisi penanganan setelah proses.
Faktor-faktor mutu yang penting dalam penilaian mutu minyak sawit antara lain
kadar asam lemak bebas, kadar air, kadar kotoran, dan terkadang bilangan Iod,
bilangan peroksida, bilangan penyabunan dan warna (Ketaren 1986).
Dalam MSK masih terkandung kotoran-kotoran yang dikelompokkan
menjadi tiga bagian, yaitu:
1. Kotoran yang tidak larut dalam minyak (Fat Insoluble)
2. Kotoran yang terdiri dari biji atau partikel jaringan, lendir dan getah,
serat-serat yang berasal dari kulit sawit, abu atau mineral (Fe, Cu, Mg, dan Ca)
serta air dalam jumlah kecil.
3. Kotoran yang berbentuk suspensi koloid dalam minyak
Kotoran ini terdiri dari fosfolipid, karbohidrat, senyawa yang mengandung
nitrogen, dan senyawa kompleks lainnya.
4. Kotoran yang terlarut dalam minyak (Fat Soluble Compound)
Kotoran yang termasuk dalam golongan ini terdiri dari asam lemak bebas,
sterol, hidrokarbon, mono, dan digliserida yang dihasilkan dari hidrolisa
trigliserida, zat warna yang terdiri dari karotenoid (total karoten yang
terdapat dalam MSK mencapai 800-1000 ppm), klorofil. Zat warna lain
yang dihasilkan dari proses oksidasi dan dekomposisi minyak yang terdiri
dari keton, aldehida, dan resin serta zat lain yang belum dapat
Kerusakan minyak
Pemanasan minyak dengan menggunakan suhu tinggi dan dengan
adanya oksigen, akan merusak asam-asam lemak tak jenuh yang ada di dalam
minyak. Kerusakan minyak akibat pemanasan dapat dilihat dari kenaikan
kekentalan, kenaikan bilangan peroksida, kenaikan kandungan asam lemak
bebas, dan penurunan bilangan iod (Perkins 1967, diacu dalam Hendrawati
2001).
Menurut Ketaren (1986), kerusakan minyak karena pemanasan pada
dasarnya disebabkan oleh beberapa reaksi, antara lain reaksi oksidasi,
polimerasi, dan hidrolisis. Ketengikan pada minyak akibat proses oksidasi terjadi
karena reaksi antara oksigen di udara dengan asam lemak tak jenuh dalam
minyak. Proses oksidasi dapat terjadi pada suhu kamar, selama proses
pengolahan menggunakan suhu tinggi.
Hasil oksidasi minyak tidak hanya mengakibatkan rasa getir dan bau
tengik, tetapi juga menurunkan nilai gizi, karena merusakan vitamin (karoten dan
tokoferol) serta asam lemak esensial dalam lemak. Oksidasi terhadap ikatan
tidak jenuh dalam asam lemak terjadi pada suhu kamar hingga 1000 C dan setiap
satu ikatan tidak jenuh dapat mengabsorpsi dua atom oksigen, sehingga
terbentuk senyawa peroksida yang labil (Ketaren 1986).
Kerusakan minyak juga dapat diakibatkan oleh reaksi hidrolisis. Reaksi
hidrolisis terutama terjadi pada minyak yang mengandung asam lemak jenuh
berantai pendek. Asam lemak tersebut mudah menguap dan berbau tidak enak,
misalnya asam butirat, asam valerat, asam kaproat, dan ester alifatis yaitu metil
nonil keton (Perkins 1967 diacu dalam Hendrawati 2001).
Karoten
Karoten merupakan sumber vitamin A yang banyak terdapat di dalam
bahan makanan nabati. Tubuh manusia mempunyai kemampuan untuk
mengubah sejumlah besar karoten menjadi vitamin A. Dalam tanaman terdapat
beberapa jenis karoten, namun yang lebih banyak ditemukan adalah a-, ß-, ?-
karoten, dan mungkin juga terdapat kriptoxantin. Dalam bahan makanan terdapat
vitamin A dalam bentuk karoten sebagai ester dari vitamin A dan sebagai vitamin
A yang bebas. Keaktifan biologis karoten jauh lebih rendah dibandingkan dengan
vitamin A (Winarno 1997).
Sayuran dan buah-buahan yang berwarna hijau atau kuning biasanya
sayuran dengan kadar karotennya. Semakin hijau daun tersebut, maka akan
semakin tinggi kadar karotennya (Winarno 1997). Namun, menurut West et al.
(2003), ß-karoten dalam sayur-sayuran mempunyai bioavailabilitas yang rendah.
Banyak faktor yang berpotensial mengurangi bioavailabilitas dan
bioefesiensi dari ß-karoten, seperti jenis karotenoid, ikatan molekuler, jumlah
karoten yang dikonsumsi dari makanan, matriks tempat karotenoid bergabung,
efek absorpsi dan biokonversi, status gizi masing-masing individu, faktor genetik,
dan interaksi antar faktor (West et al. 2003).
Kerusakan atau redegradasi karotenoid dapat disebabkan oleh oksidasi.
Mekanisme oksidasi yang terjadi secara kompleks dan tergantung pada
beberapa faktor. Karotenoid dapat dioksidasi melalui reaksi dengan oksigen yang
tergantung pada cahaya, panas, dan adanya prooksidan maupun antioksidan
(Francis 1985).
Menurut Meyer (1982), selama pemasakan, kehilangan karoten adalah
kecil, berkisar 5-10%. Warna karoten sedikit sekali dipengaruhi oleh suasana
asam, basa, volume air atau waktu pemanasan. Nilai gizi karoten dapat
dipertahankan selama pemasakan karena sifatnya yang tidak larut dalam air.
Menurut Muchtadi dan Nuraida (1986) minyak sawit mengandung karoten
sebanyak 600-1000 bps. Karoten pada minyak sawit pada umumnya tidak
disenangi konsumen karena memberikan penampakan yang jelek, oleh karena
itu dalam prosesnya dilakukan pemurnian (pemisahan karoten), yang berarti
membuang komponen penting dari minyak sawit tersebut. Komposisi karotenoid
dalam minyak sawit ada dalam Tabel 6.
Tabel 6 Komposisi karotenoid dalam minyak sawit (Anonymous 2005)
Karotenoid Jumlah (%)
a-karoten ß-karoten ?-karoten likopen phytoene phytofluene cis ß-karoten cis a-karoten ?-karoten d-karoten neurossporene ß-zeakaroten a-zeakaroten 35.2 56.0 0.33 1.30 1.27 0.68 0.68 2.49 0.69 0.83 0.29 0.74 0.23
Diantara jenis-jenis karotenoid, ß-karoten menunjukkan aktivitas sebagai
adanya grup karbonil menunjukkan rendahnya aktivitas provitamin A jika
dibandingkan ß-karoten jika hanya satu cincin yang dipengaruhi, dan tidak
mempunyai aktivitas jika kedua cincin teroksigenasi (Fennema 1996). Gambar
struktur dari ß-karoten dapat dilihat pada Gambar 6.
ß-karoten mempunyai aktivitas sebagai antioksidan dengan mencari-cari
oksigen bebas, hidroksil, dan radikal superoksida, serta dengan mereaksikan
dengan peroksil radikal (ROO). Peroksil radikal menyerang ß-karoten untuk
membentuk ROO- ß-karoten dimana peroksil radikal mengikatkan diri pada C ke
7 dari rantai karbon ß-karoten, elektron yang tidak berpasangan terdelokalisasi
melewati sistem ikatan rangkap terkonjugasi. ß-karoten tidak bertindak sebagai
pendonor H• seperti pada umumnya antioksidan fenolik. Antioksidan seperti
ß-karoten dan ß-karoten lain, menyebabkan penurunan total kerugian dari aktivitas
vitamin A tanpa memperhatikan mekanisme dimana inisiasi radikal bebas terjadi.
Untuk retinol dan retinil ester penyerangan oleh radikal bebas terjadi pada posisi
C14 dan C15 (Fennema 1996).
Gambar 6 Struktur umum ß-karoten
Oksidasi dari ß-karoten melibatkan pembentukan 5,6-epoksida, yang
dapat terisomerisasi menjadi 5,8-epoksida (mutachrome). Paparan cahaya dapat
menyebabkan oksidasi mutachrome menjadi produk degradasi pertama.
Fragmentasi ß-karoten menjadi molekul senyawa yang memiliki berat jenis yang
ringan dapat terjadi selama pemanasan. Volatil-volatil yang dihasilkan dapat
berpengaruh terhadap flavor. Fragmentasi juga dapat terjadi selama proses
Mikrobiologi Pangan
Bahan baku energi yang paling banyak digunakan oleh mikroorganisme
adalah glukosa. Dengan adanya oksigen, beberapa mikroorganisme mencerna
glukosa dan menghasilkan air, karbondioksida, dan sejumlah besar energi (ATP)
yang dapat digunakan untuk pertumbuhan. Metabolisme glukosa tersebut
dilakukan oleh mikroorganisme aerobik. Akan tetapi beberapa mikroorganisme
dapat mencerna bahan baku energinya tanpa adanya oksigen dan hasilnya,
hanya sebagian dari bahan baku energi yang dipecah. Hasil akhir yang diperoleh
bukan karbondioksida, air, dan sejumlah besar energi, tetapi hanya sejumlah
kecil energi, karbondioksida, air, dan produk akhir organik lainnya. Zat-zat produk
akhir ini termasuk sejumlah besar asam laktat, asam asetat, dan etanol, serta
sejumlah kecil asam organik volatil lainnya, alkohol, dan ester dari alkohol
tersebut. Pertumbuhan yang terjadi tanpa adanya oksigen sering dikenal sebagai
fermentasi. Berbagai mikroorganisme mampu memfermentasikan bahan pangan,
namun yang penting adalah bakteri pembentuk asam laktat, asam asetat, asam
propionat, dan beberapa jenis khamir dan kapang (Buckle et.al 1987).
Selain menguraikan karbohidrat, kebanyakan makanan yang
mengandung sejumlah lemak mudah mengalami hidrolisis dan oksidasi sehingga
menyebabkan perubahan citarasa makanan. Meskipun kebanyakan pemecahan
lemak pada makanan merupakan reaksi kimia non mikroba, tetapi berbagai
bakteri, khamir dan kapang mempunyai kemampuan untuk menghidrolisis dan
mengoksidasi lemak (Fardiaz 1992b).
Mengacu kepada Fardiaz (1992b), makanan yang telah mengalami
proses pengolahan biasanya masih mengandung mikroorganisme hidup yang
mempunyai sifat-sifat fisiologi yang tidak normal karena telah mengalami stres
selama pengolahan (pemanasan, pembekuan, iradiasi, dan sebagainya), serta
dari lingkungan sekitarnya. Mikroorganisme semacam ini disebut mikroorganisme
subletal. Mikroorganisme subletal dapat memperbaiki diri bila: 1) sel diinkubasi
pada substrat atau lingkungan yang sesuai, 2) disimpan dalam suhu yang
optimum (25oC – 37oC) dan waktu simpan yang sesuai, 3) sel yang telah sembuh
masih mempunyai ketahanan terhadap komponen selektif di dalam medium
seperti sel normal, 4) setelah sembuh, sel mampu berkembang biak dengan
Mutu Mikrobiologi
Mutu suatu produk menunjukkan identitas produk tersebut. Diacu dalam
Fardiaz (1993), dalam pengujian mutu bahan pangan diperlukan berbagai uji
yang mencakup uji fisik, uji mikrobiologi, dan uji organoleptik. Uji mikrobiologi
merupakan salah satu uji yang sangat penting, karena selain dapat menduga
daya tahan simpan makanan juga dapat digunakan sebagai indikator sanitasi
makanan atau indikator keamanan makanan.
Mikroorganisme indikator pada produk olahan pangan merupakan
mikroorganisme yang dapat digunakan sebagai batasan penetapan mutu suatu
produk olahan pangan (Fardiaz 1992b). Mikroorganisme dapat mengakibatkan
berbagai perubahan fisik dan kimiawi dari suatu bahan pangan. Apabila
perubahan tersebut tidak diinginkan atau tidak dapat diterima oleh konsumen,
maka bahan pangan tersebut mengalami kerusakan (Buckle et al. 1987). Diacu
dalam Fardiaz (1994), dari segi mikrobiologi, makanan yang bermutu baik untuk
dihidangkan adalah makanan yang tidak basi atau berbau menyimpang dan
aman dikonsumsi.
Mikroba dalam Makanan
Diketahui ada tiga hal yang menyebabkan terjadinya pencemaran
makanan, sehingga makanan menjadi tidak aman untuk dimakan. Pertama
adalah penanganan makanan tidak dilakukan dengan mengindahkan
syarat-syarat kebersihan. Kedua adalah alat-alat yang digunakan untuk menyiapkan,
mengolah, memasak, dan menyajikan makanan tidak dibersihkan semestinya,
dan yang terakhir adalah makanan didiamkan terlalu lama di lingkungan yang
temperaturnya memungkinkan berbagai mikroorganisme berkembang biak
(Moehyi 1992).
Meskipun proses pengolahan pada umumnya dapat membunuh
mikroorganisme, tetapi beberapa, termasuk spora dan beberapa sel vegetatif
masih dapat hidup setelah proses pengolahan. Tetapi selama penyimpanan
kering dan beku, mungkin terjadi penurunan jumlah mikroorganisme, yaitu
tergantung dari kondisi penyimpanan, jenis bahan pangan, dan jenis mikroflora
yang dominan (Fardiaz 1992a). Lain halnya dengan yang dikemukakan Buckle et
al. (1987), bahwa seringkali organisme tumbuh lebih baik pada bahan pangan
yang telah dimasak dibandingkan pada bahan pangan mentah, karena zat-zat
gizi tersedia lebih baik dan tekanan persaingan dari mikroorganisme lain telah
Adanya mikroorganisme psikrotrofik pada makanan yang telah diproses
dengan pemanasan biasanya menunjukkan adanya kontaminasi setelah
pengolahan. Meskipun mikroorganisme-mikroorganisme psikotrofik biasanya
mati karena proses pemanasan, mikroorganisme tersebut merupakan sumber
enzim proteolitik, dan lipolitik yang tahan panas dan masih mungkin dapat
menyebabkan kerusakan selama penyimpanan pada makanan yang telah
dipanaskan (Fardiaz 1992a).
Beberapa mikroba dapat mempengaruhi asam, sehingga dapat merubah
nilai pH (keasaman) produk dan lebih lanjut berpengaruh terhadap citarasa
produk. Perubahan komposisi produk akibat adanya aktivitas mikroba ditandai
dengan adanya perubahan bau, timbulnya asam, adanya busa, dan perubahan
warna (Winarno, Fardiaz, & Fardiaz 1980).
Kebanyakan makanan mengandung sejumlah lemak yang mudah
mengalami hidrolisa dan oksidasi sehingga menyebabkan perubahan citarasa
makanan, meskipun kebanyakan pemecahan lemak terjadi karena proses kimia
(reaksi non mikroba), tetapi beberapa bakteri, khamir, dan kapang mempunyai
kemampuan untuk menghidrolisis dan mengoksidasi lemak (Fardiaz 1992a).
Menurut anjuran Food and Drug Administration yang diacu dalam Fardiaz
(1994), untuk menjamin makanan siap santap tidak busuk dan aman dikonsumsi
maka sebaiknya makanan disimpan pada suhu lemari es, yaitu maksimal 40 C
untuk makanan yang dikonsumsi dalam keadaan dingin, atau pada suhu diatas
550 C untuk makanan yang dikonsumsi dalam keadaan hangat atau panas. Suhu
diantara 40C dan 550 C merupakan suhu kritis karena jasad renik dapat
berkembang biak dengan cepat dan menyebabkan kebusukan dan keracunan
makanan.
Hasil penelitian Sari (2001) menunjukkan bahwa sistem kontrol terhadap
suhu harus mempertimbangkan hal-hal sebagai berikut : (1) sifat makanan
termasuk Aw, pH serta jenis dan mikroba yang mungkin mencemari makanan,
(2) masa simpan makanan, (3) cara pengolahan dan pengemasan, (4) cara
mengkonsumsi makanan, misalnya harus dimasak terlebih dahulu atau dapat
langsung dimakan. Alat pengukur suhu harus selalu diperiksa secara teratur dan
diuji ketepatannya.
Uji Mikrobiologi
Metode yang dapat digunakan untuk menentukan jumlah mikroba di
Count (TPC), Most Probable Number (MPN), dan metode hitungan mikroskopik
langsung. Metode lainnya yang dapat digunakan untuk menghitung jumlah
mikroba di dalam bahan pangan adalah metode turbidimetri (kekeruhan) dengan
menggunakan spektrofotometer. Tetapi metode ini sukar diterapkan pada bahan
pangan karena membutuhkan larutan medium yang bening (Fardiaz 1987).
Prinsip dari metode hitungan cawan adalah jika sel mikroba yang masih
hidup ditumbuhkan pada medium agar, maka sel mikroba tersebut akan
berkembang biak dan membentuk koloni yang dapat dilihat langsung dengan
mata tanpa menggunakan mikroskop. Metode HC ini merupakan cara yang
paling sensitif untuk menentukan jumlah mikroba, karena : 1) hanya sel yang
masih hidup yang dihitung, 2) beberapa jenis mikroba dapat dihitung sekaligus,
3) dapat digunakan untuk isolasi dan identifikasi mikroba karena koloni yang
terbentuk mungkin berasal dari satu sel mikroba dengan penampakkan
pertumbuhan yang spesifik (Fardiaz 1987).
Selain keuntungan-keuntungan tersebut, metode HC juga memiliki
beberapa kelemahan, yaitu : 1) hasil perhitungan tidak menunjukkan jumlah sel
mikroba yang sebenarnya karena beberapa sel yang berdekatan mungkin
membentuk satu koloni, 2) medium dan kondisi yang berbeda mungkin
menghasilkan nilai yang berbeda, 3) mikroba yang ditumbuhkan harus dapat
tumbuh pada medium padat dan membentuk koloni yang kompak dan jelas, tidak
menyebar, 4) memerlukan persiapan dan waktu inkubasi yang lama sehingga
pertumbuhan koloni dapat dihitung (Fardiaz 1987).
Uji mikrobiologi yang dilakukan terhadap bahan pangan mentah berbeda
dengan bahan makanan yang telah mengalami proses pengolahan seperti
pemanasan, pengeringan, pendinginan, pembekuan, iradiasi, penambahan
bahan pengawet, dan sebagainya. Kandungan mikroorganisme pada bahan
pangan mentah terutama dipengaruhi oleh jenis bahan pangan, sumber
kontaminasi, dan penanganan atau penyimpanan sebelum dilakukan proses
pengolahan. Kandungan mikroorganisme pada makanan olahan lebih spesifik
karena selain dipengaruhi oleh jenis bahan pangan, juga dipengaruhi oleh
ketahanan mikroorganisme terhadap proses pengolahan yang diterapkan pada
makanan tersebut (Fardiaz 1992b).
Media biakan yang digunakan untuk menumbuhkan bakteri terdapat
dalam bentuk padat, semi padat, dan cair. Media padat diperoleh dengan
bahan pemadat karena tidak diuraikan oleh mikroorganisme. Agar dapat
membeku pada suhu diatas 450C. kandungan agar sebagai media pemadat
dalam media adalah 1.5-2%. Media harus disterilkan terlebih dahulu sebelum
digunakan supaya tidak tercemar oleh mikroorganisme dan tidak menyebabkan
kekeruhan media (Lay 1994).
Total mikroba
Total mikroba adalah jumlah flora mikroba tanpa menunjukkan jenis flora
mikroba tertentu yang ada dalam pangan. Perhitungan total mikroba berperan
dalam menentukan status sanitasi makanan. Bila makanan telah melalui proses
pemanasan dan tetap ditemukan mikroba pada saat pengujian, hal ini berarti
terjadi rekontaminasi atau pertumbuhan mikroba lagi (Shapton, D.A. & Shapton,
N.F. 1993). Berdasarkan standar yang ditetapkan oleh New Hampshire Guideline
yang diacu dalam Shapton, D.A. dan Shapton, N.F. (1993), serta menurut
SNI-01-3816-1995 tentang santan kelapa, batas aman total mikroba dalam bahan
BAHAN DAN METODE Waktu dan Tempat
Penelitian ini telah dilaksanakan pada bulan Juni 2006 hingga Maret
2007. Lokasi yang digunakan untuk melakukan penelitian ini adalah
Laboratorium Pengolahan Pangan, Laboratorium Kimia Gizi, dan Laboratorium
Sanitasi dan Keamanan Pangan, Program Studi S1 Gizi Masyarakat dan
Sumberdaya Keluarga, Fakultas Pertanian, Institut Pertanian Bogor. Analisis
HPLC dilakukan di laboratorium Balai Penelitian Pasca Panen, Cimanggu, Bogor.
Bahan dan Alat
Bahan utama yang digunakan dalam penelitian ini adalah daun
Torbangun (Coleus amboinicus Lour.) serta tablet vitamin A (merek Kimia Farma)
dan Minyak Sawit Kasar (MSK) sebagai antioksidan. Bahan pendukung lainnya
antara lain bumbu-bumbu, yang meliputi akuades, santan, bawang merah,
bawang putih, kunyit, jahe, kemiri, garam, jeruk nipis. Bahan tambahan lainnya
adalah bahan antioksidan, yang terdiri dari tablet vitamin A yang diperoleh dari
apotek Kimia Farma Bogor dan MSK dari Balai Penelitian Serpong serta
bahan-bahan yang digunakan untuk analisis kimia dan uji mikrobiologi.
Bahan kimia yang digunakan untuk uji mikrobiologi antara lain Plate
Count Agar/PCA (merek OXOID), NaCl 0,85%, alkohol 96%, alkohol 70%,
spirtus, aquades. Untuk uji kimiawi kerusakan lemak adalah asam asetat,
khloroform, KI jenuh, Na2S2O3 0,1 N, pati 1%, air destilata, HCl 4 M, Foaming
agent, pereaksi TBA, NaOH 0.1 M, KHP standar atau (COOH)2.2H2O, dan
fenoftalein 0.1% dalam alkohol. Bahan-bahan yang digunakan untuk analisis
HPLC vitamin A dan β-karoten adalah etanol (merek MERCK), akuades, KOH
50% (merek MERCK), asam askorbat (merek MERCK), heksan (merek MERCK),
BHT (merek MERCK), Na2SO4 anhydrous (merek MERCK), fase gerak asetonitril
: metanol : THF (28 : 25 :2) (merek MERCK), alkohol (merek MERCK), dan
sodium askorbat (merek MERCK)
Alat-alat yang digunakan untuk pembuatan sop daun Torbangun adalah
baskom, pisau, panci kaca, gelas ukur, sendok sayur, sendok teh, talenan,
ulekan, saringan, timbangan dan termometer. Alat-alat lain yang digunakan
antara lain adalah alat untuk melakukan analisis kimia, uji mikrobiologi, dan
Alat-alat yang digunakan untuk analisis kimia dan uji mikrobiologi adalah
cawan petri (diameter 10 cm), tabung reaksi (berulir dan tidak berulir),
erlenmeyer (100 ml, 250 ml, 300 ml, 500 ml, dan 1000 ml), gelas piala (500 ml,
1500 ml, dan 2000 ml), gelas ukur (100 ml), labu takar (2000 ml), labu destilasi,
gelas pengaduk, pipet (5 ml, dan 10 ml), Stearer, bulb, bunsen, alat titrasi, alat
destilasi, batu didih, penangas air, blender, neraca analitik, mortar, kertas saring,
sudip, rak tabung reaksi, botol penyemprot, jerigen, baskom, sikat, oven,
inkubator, otoklaf, spektrofotometer, dan lemari es. Peralatan yang digunakan
untuk analisis HPLC adalah neraca analitik, stearer, labu saponifikasi, alat
saponifikasi, corong pemisah, kertas saring (merek Whatman 41), freeze dryer,
evaporator, milipore (merek GELMAN), kolom C-18, dan alat HPLC (merek
WATERS).
Metode Penelitian
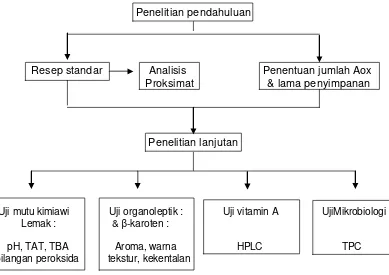
Penelitian ini dibagi dalam dua tahap yaitu : penelitian pendahuluan dan
penelitian lanjutan.
Penelitian pendahuluan
Resep standar Analisis Penentuan jumlah Aox Proksimat & lama penyimpanan
Penelitian lanjutan
Uji mutu kimiawi Uji organoleptik : Uji vitamin A UjiMikrobiologi Lemak : & β-karoten :
[image:44.595.118.507.383.658.2]pH, TAT, TBA Aroma, warna HPLC TPC bilangan peroksida tekstur, kekentalan
Gambar 7 Diagram alir penelitian
1. Penelitian pendahuluan
Penelitian pendahuluan terdiri atas dua tahap, yakni penetapan resep
standar yang digunakan selama penelitian dan penentuan jumlah antioksidan
orang wanita asli suku Batak. Resep standar pembuatan sayur sop daun
Torbangun dapat dilihat pada Tabel 7.
Tabel 7 Komposisi bahan-bahan yang digunakan dalam pembuatan sop daun Torbangun pada berbagai jenis analisis
No Bahan-bahan Resep standar Analisis lemak, TPC,uji hedonik
Analisis HPLC
1 Daun Torbangun segar 250 g 400 g 200 g
2 Santan 575 ml 920 ml 460 ml
3 Bawang putih 2.40 g 3.84 g 1.92 g
4 Bawang merah 9.94 g 15.9 g 7.95 g
5 Kemiri 9.2 g 14.72 g 7.36 g
6 Kunyit 1.79 g 2.86 g 1.43 g
7 Jahe 1.98 g 6.33 g 1.58 g
8 Laos 1.89 g 3.02 g 1.57 g
9 Sereh 1 tangkai 1 tangkai 1 tangkai
10 Merica 0.43 g 0.69 g 0.34 g
11 Garam Secukupnya Secukupnya Secukupnya
12 Air jeruk nipis 2 sdm 3 sdm 2.5 sdm
Total berat formula ± 725 g ± 1320 g ± 660 g
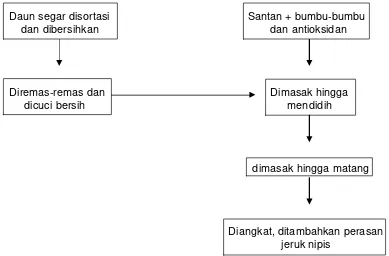
Proses pembuatan sop daun Torbangun adalah sebagai berikut:
1. Daun Torbangun disortasi dan dipisahkan dari tangkai, kemudian
ditimbang.
2. Bumbu-bumbu dibersihkan atau dikupas kemudian ditimbang dan dicuci.
3. Kemiri dan kunyit disangrai atau dibakar terlebih dahulu sebelum
dihaluskan.
4. Daun kemudian diremas-remas dengan menggunakan garam dan diperas
untuk mengurangi bau langu dan cairan hitam dari daun. Setelah itu,
dicuci bersih dan ditiriskan.
5. Bumbu-bumbu dihaluskan. Kemudian, santan dimasak bersama bumbu
dan sereh yang telah ditumbuk hingga mendidih. Setelah santan
mendidih, daun Torbangun dimasukkan, lalu masak hingga matang.
Setelah matang, sop daun Torbangun diangkat dan dihidangkan bersama
air perasan jeruk nipis.
6. Dikemas.
Tabel 8 Hasil analisis Proksimat sop daun Torbangun
Zat Gizi Jumlah (mg/100 g)
Karbohidrat 3.83
Air 84.43
Abu 0.9
Protein 3.84
Jenis antioksidan yang digunakan adalah antioksidan gizi yakni vitamin A.
Vitamin A murni yang digunakan adalah tablet vitamin A 20.000 IU (merek Kimia
Farma). Sebagai pembandingnya, digunakan antioksidan food based approach
yakni MSK karena kaya akan ß-karoten.
Untuk menentukan jumlah tablet vitamin A yang akan ditambahkan,
digunakan standar penambahan vitamin A dan ß-Karoten yakni sebesar 10-300
mg/kg bahan (SNI 01-0222-1995 tentang bahan tambahan makanan). Untuk
tujuan optimalisasi, vitamin A yang ditambahkan adalah sebesar 300 mg/kg
bahan. Perlakuan dalam penelitian adalah sebagai berikut :
• Sop daun Torbangun kontrol, disingkat : STK
• Sop daun Torbangun dengan penambahan vitamin A, disingkat : STA
• Sop daun Torbangun dengan penambahan MSK, disingkat : STM Tablet vitamin A yang digunakan mempunyai kandungan vitamin A
sebesar 20.000 IU (sesuai informasi pada kemasan), dan mempunyai bobot per
tablet adalah 0,44 gram. Dengan menggunakan perhitungan secara konversi,
maka diperoleh penambahan tablet vitamin A adalah sebanyak 21,78 tablet,
dibulatkan menjadi 22 tablet vitamin A/kg sop daun Torbangun. Perhitungan
konversi dapat dilihat pada Lampiran 1.
Penentuan jumlah MSK yang akan ditambahkan adalah dengan cara
menambahkan sedikit demi sedikit MSK, hingga diperoleh angka 35 gram. Angka
35 gram ini dianggap s