SINTESIS HIDROKSIAPATIT BERBASIS CANGKANG
KERANG ALE-ALE (Meretrix meretrix) DAN PELAPISANNYA
PADA PADUAN LOGAM CoCrMo
IDA AYU SUCI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Sintesis Hidroksiapatit Berbasis Cangkang Kerang ale-ale (Meretrix meretrix) dan Pelapisannya pada Paduan Logam CoCrMo adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juli 2016
RINGKASAN
IDA AYU SUCI. Sintesis Hidroksiapatit Berbasis Cangkang Kerang ale-ale (Meretrix meretrix) dan Pelapisannya pada Paduan Logam CoCrMo. Dibimbing oleh ETI ROHAETI dan CHARLENA.
Kerang ale-ale (Meretrix meretrix) merupakan sumber daya alam potensial di Kabupaten Ketapang Provinsi Kalimantan Barat. Penangkapan ale-ale yang berlangsung sepanjang tahun menghasilkan dampak negatif berupa limbah cangkang yang belum dikelola secara maksimal. Cangkang kerang ale-ale memiliki kandungan kalsium tinggi yang berpotensi untuk dimanfaatkan sebagai prekursor kalsium dalam sintesis hidroksiapatit (HAp). HAp yang bersifat biokompatibel dilapiskan pada paduan logam CoCrMo untuk mengurangi terlepasnya ion Co, Cr, dan Mo yang dapat menyebabkan terjadi korosi pada implan tulang. Logam sebagai implan harus memiliki sifat biokompatibel antara lain tahan terhadap korosi dan sesuai bagi sel hidup. Penelitian ini bertujuan memanfaatkan cangkang kerang ale-ale sebagai prekursor Ca untuk mensintesis HAp, melakukan sintesis HAp dari cangkang kerang ale-ale, melakukan karakterisasi hasil pelapisan HAp pada paduan logam CoCrMo, menguji biokompatibilitas paduan logam CoCrMo yang dilapisi HAp melalui uji ketahanan korosi dan menguji cytocompatibility in vitro pada kultur sel endotel Calf Pulmonary Artery Endothelium(CPAE) (ATCC-CCL 209).
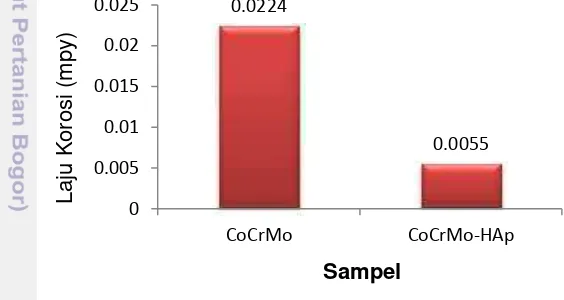
Analisis serbuk cangkang kerang ale-ale menggunakan Spektrofotometer Serapan Atom (AAS) menunjukkan kandungan kalsium dalam cangkang sebesar 68.04%. Hasil sintesis dengan metode presipitasi double stirring menunjukkan HAp yang diperoleh merupakan fasa tunggal HAp. Pelapisan paduan logam CoCrMo menggunakan metode elektroforesis deposisi pada tegangan 120 volt selama 30 menit menunjukkan morfologi pelapisan yang merata dan tidak ditemukan keretakan. Hasil analisis XRD HAp pada paduan logam CoCrMo juga diperoleh fasa tunggal HAp. Uji ketahanan korosi pada media pengkorosi cairan infus NaCl 0.9% menggunakan potensiostat/galvanostat model 273 menunjukkan laju korosi berada pada level 0.0055mils per year(mpy) pada paduan logam yang dilapisi, hasil ini lebih baik dari logam tanpa dilapisi HAp (0.0224 mpy). Uji cytocompatibility in vitro pada kultur sel endotel Calf Pulmonary Artery Endothelium (CPAE) (ATCC-CCL 209) setelah 72 jam inkubasi paduan logam CoCrMo yang dilapisi HAp menunjukkan tidak timbul toksisitas terhadap kultur sel dengan persen inhibisi 33.33%.
Limbah cangkang kerang ale-ale telah berhasil dimanfaatkan sebagai prekursor kalsium dalam sintesis fasa tunggal HAp. Berdasarkan ketahanan korosi dan sifat cytocompatibility yang diperoleh, paduan logam CoCrMo yang dilapisi HAp berpotensi sebagai implan biokompatibel untuk aplikasi implan tulang.
SUMMARY
IDA AYU SUCI. Synthesis of Hydroxyapatite Based ale-ale (Meretrix meretrix) Clamshell and Coating on CoCrMo Alloy. Supervised by ETI ROHAETI and CHARLENA.
Ale-ale clamshell (Meretrix meretrix) is a potential natural resource of Ketapang Regency of West Kalimantan Province. The ale-ale fishing activity in this region takes place throughout the year resulted the negative impact in the form of clamshell waste that has not been managed optimally yet. Ale-ale clamshell contains high calcium content which has the potency to be used as a precursor of calcium in synthesis of hydroxyapatite (HAp). HAp which is biocompatible coated on CoCrMo alloy to reduce the release of metal ions Co, Cr, and Mo which cause the corrosion of bone implant. Metal as implant is required of having the biocompatibility properties i.e corrosion resistance and compatible in living cells. This study aimed to utilize the waste of ale-ale clamshell as a precursor of calcium to synthesize HAp, synthesize of HAp from ale-ale clamshell, characterize the CoCrMo alloy after coating with HAp, examine the biocompatibility of HAp-coated CoCrMo alloy by corrosion resistance test and in vitro cytocompatibility assay in endothelial cell of Calf Pulmonary Artery Endothelium (CPAE) (ATCC-CCL 209).
Analysis of calcium content by using Atomic Absorption Spectroscopy (AAS) showed that ale-ale clamshell was 68.04% (by weight). HAp was synthesized by double-stirring precipitation method, confirmed the formation of single phase of HAp. The coating of CoCrMo alloy which was treated by using electrophoretic deposition method at 120 volts during 30 minutes showed the surface morphology was well-densified and crack-free. The main crystalline phase of coating was still single phase of HAp. Corrosion resistance test in artificial body fluid media by using 0.9% NaCl intravenous fluids which was connected to the potentiostat/galvanostat M273 showed the corrosion rate at the level of 0.0055 mils per year (mpy) on HAp-coated CoCrMo alloy, this result was better than that of uncoated CoCrMo alloy (0.0224 mpy). In vitro cytocompatibility assay in endothelial cell of Calf Pulmonary Artery Endothelium (CPAE) (ATCC-CCL 209) showed there was no toxicity in cell culture with the percent inhibition of 33.33% after 72 hours of coated CoCrMo alloy incubation.
The waste of ale-ale clamshell successfully applied as a precursor of calcium in synthesis of single phase of HAp. Based on this corrosion resistance and cytocompatibility properties, HAp-coated CoCrMo alloy has the potency for bone implant application.
© Hak Cipta Milik IPB, Tahun 2016
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Kimia
SINTESIS HIDROKSIAPATIT BERBASIS CANGKANG
KERANG ALE-ALE (Meretrix meretrix) DAN PELAPISANNYA
PADA PADUAN LOGAM CoCrMo
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2016
Judul Tesis : Sintesis Hidroksiapatit Berbasis Cangkang Kerang ale-ale (Meretrix meretrix) dan Pelapisannya pada Paduan Logam CoCrMo
Nama : Ida Ayu Suci NIM : G451130101
Disetujui oleh
Komisi Pembimbing
Dr Eti Rohaeti, MS
Ketua Dr Charlena, MSiAnggota
Diketahui oleh
Ketua Program Magister Kimia
Prof Dr Dyah Iswantini Pradono, MScAgr
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas
segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan dengan judul “Sintesis Hidroksiapatit Berbasis Cangkang Kerang ale-ale (Meretrix meretrix) dan Pelapisannya pada Paduan Logam CoCrMo”. Penelitian ini dilaksanakan sejak bulan Januari 2015 sampai dengan Januari 2016.
Terima kasih penulis ucapkan kepada Ibu Dr Eti Rohaeti MS dan Ibu Dr Charlena MSi selaku pembimbing, Bapak DrAkhiruddin Maddu MSi selaku dosen penguji luar komisi,Prof Dr Dyah Iswantini Pradono MScAgr selaku Ketua Program Magister Kimia, Bapak Drs Sulistioso Giat Sukaryo MT yang telah banyak memberikan bantuan peralatan dan masukan, Bapak Drs Erizal atas bantuan sterilisasi sampel penelitian, serta seluruh dosen Pascasarjana Kimia atas segala bimbingan dan ilmu yang diberikan. Di samping itu, penghargaan penulis sampaikan kepada Pimpinan dan keluarga besar staf Laboratorium Kimia Analitik IPB, staf Laboratorium Kimia Anorganik IPB, staf Laboratorium Bersama Kimia IPB, staf Laboratorium Biomaterial Badan Tenaga Nuklir Nasional (BATAN) PUSPIPTEK Serpong, beserta staf Laboratorium Terpadu Badan Litbang Departemen Kehutanan yang telah membantu analisis selama penelitian. Ungkapan terima kasih juga penulis sampaikan kepadaKementerian Riset, Teknologi, dan Pendidikan Tinggi Republik Indonesia (KEMENRISTEKDIKTI RI) atas bantuan dana penelitian berupa beasiswa BPPDN. Tak lupa pula ungkapan terima kasih penulis sampaikan kepada teman-teman mahasiswa Sekolah Pascasarjana Kimia angkatan 2013 atas masukan, saran, dan motivasi yang diberikan dalam menyelesaikan penelitian ini. Ungkapan terima kasih juga disampaikan kepada ayah, ibu, dan seluruh keluarga, atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Juli 2016
DAFTAR ISI
UjiCytocompatibility In vitroSel Endotel 10
3 METODE 10
Pengukuran Kadar Ca dalam Serbuk Sampel dengan AAS 11 Kalsinasi Serbuk Sampel dan Konversi menjadi Ca(OH)2 12
Sintesis HAp dengan Metode PresipitasiDouble Stirring 12 Pelapisan Paduan Logam CoCrMo dengan HAp menggunakan
Metode EPD 12
Uji Ketahanan Korosi 13
UjiIn vitroSitotoksisitas pada Sel Endotel CPAE 13
4 HASIL DAN PEMBAHASAN 13
Hasil Analisis XRD Cangkang Kerang ale-ale Sebelum dan
Setelah Kalsinasi 13
Komposisi Cangkang Kerang ale-ale Sebelum Kalsinasi 14
Hasil Sintesis HAp 15
Hasil Karakterisasi Fasa HAp menggunakan XRD 15
Hasil Karakterisasi FTIR pada HAp 16
Hasil Karakterisasi SEM pada HAp 17
Hasil Analisis PSA pada HAp 18
Hasil Analisis XRD Lapisan HAp pada Paduan Logam CoCrMo 19
Hasil SEM HAp pada Paduan Logam CoCrMo 20
Ketahanan Korosi 21
Hasil UjiCytocompatibility In vitroSel Endotel 22
5 SIMPULAN DAN SARAN 24
Simpulan 24
Saran 24
DAFTAR PUSTAKA 25
LAMPIRAN 29
DAFTAR GAMBAR
1 Kerang ale-ale (M. meretrix) 4
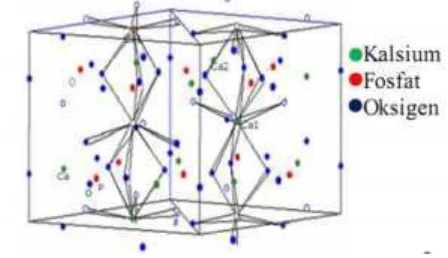
2 Unit sel struktur HAp 4
3 Fenomena antarmuka antara HAp dan sel tubuh 5
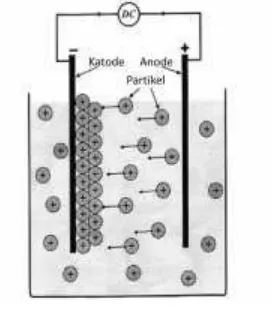
4 Pergerakan partikel ke arah elektrode 7
5 Distorsi lapisan ganda dan mekanisme elektroforesis deposisi 8 6 Difraktogram sinar-x serbuk cangkang kerang ale-ale sebelum kalsinasi 13 7 Difraktogram sinar-x serbuk cangkang kerang ale-ale setelah kalsinasi 14
8 Difraktogram sinar-x HAp 16
9 Spektrum gugus fungsi HAp 16
10 Foto SEM HAp 17
11 Distribusi ukuran partikel HAp 18
12 Foto mikroskop optik setelah dilakukan EPD 19 13 Difraktogram sinar-x HAp pada paduan logam CoCrMo 19
14 Foto SEM HAp pada paduan logam CoCrMo 20
15 Laju korosi 21
16 Morfologi sel endotel 23
DAFTAR LAMPIRAN
1 Diagram alir penelitian 30
2 Data hasil analisis XRD cangkang kerang ale-ale 31 Serbuk cangkang kerang ale-ale sebelum kalsinasi 31 Serbuk cangkang kerang ale-ale setelah kalsinasi 31 Hasil sintesis HAp menggunakan metode presipitasidouble stirring 32 Hasil analisis XRD pelapisan HAp pada paduan logam CoCrMo 33 3 Data joint cristal powder difraction standard(JCPDS) 34
Aragonite : CaCO3 34
Porlandite : Ca(OH)2 34
Hidroksiapatit : Ca10(PO4)6(OH)2 35
4 Perhitungan AAS kandungan kalsium cangkang kerang ale-ale sebelum
Kalsinasi 35
Absorbans standar kalsium 35
Absorbans dan konsentrasi kalsium cangkang kerang ale-ale 36
5 Hasil EDX cangkang kerang ale-ale 37
6 a Penentuanpolah2+k2+l2 38
b Penentuan ukuran kristal HAp hasil sintesis 39
7 Data uji korosi 39
Laju korosi logam CoCrMo tanpa pelapisan HAp 39 Laju korosi logam CoCrMo dengan pelapisan HAp 40
1 PENDAHULUAN
Latar Belakang
Kabupaten Ketapang yang terletak di bagian selatan Provinsi Kalimantan Barat sangat terkenal dengan ciri khas kerangnya yang dinamakan kerang ale-ale. Penangkapan ale-ale (Meretrix meretrix) di wilayah ini berlangsung sepanjang tahun. Kebanyakan daging kerang ale-ale di daerah Ketapang digunakan sebagai kuliner dan limbah cangkangnya terbuang begitu saja atau digunakan untuk menimbun jalan. Cangkang kerang M. meretrix diketahui memiliki kandungan kalsium yang tinggi yaitu 98.81% (Mijan et al.2015). Solusi untuk meningkatkan manfaat sumber daya kerang ale-ale secara optimal dengan memperhatikan aspek jangka panjang adalah mengolah limbah tersebut menjadi prekursor kalsium dalam sintesis hidroksiapatit (HAp).
Hidroksiapatit Ca10(PO4)6(OH)2 memiliki kemiripan dengan komponen
mineral anorganik tulang dan gigi karena sekitar 65% mineral anorganik tulang tersusun atas HAp (Dedourkova et al. 2012). Studi HAp terus dikembangkan karena kebutuhan akan biomaterial ini sangat tinggi terutama dalam bidang kedokteran ortopedi, misalnya untuk pengobatan tulang, baik perbaikan pada tulang yang retak maupun patah tulang (Dedourkova et al. 2012; Bastan dan Ozbek 2013; Poinernet al.2013). Namun, HAp bersifat rapuh dan memiliki sifat mekanik yang rendah (Shi et al. 2014) sehingga dibutuhkan bahan lain untuk implan tulang, yaitu logam. Logam mampu menutupi kelemahan HAp karena memiliki sifat mekanik tinggi yang dapat berfungsi sebagai penopang tubuh dalam menggantikan tulang yang rusak. HAp bersifat biokompatibel sehingga dapat meningkatkan biokompatibilitas implan logam dan meningkatkan ketahanan korosi dari implan logam dengan mengurangi lepasnya ion logam. Selain bersifat biokompatibel, HAp juga bersifat bioaktif yaitu dapat bertindak sebagai tempat pertumbuhan jaringan tulang yang baru (Javidiet al. 2008; Poinernet al.2013).
Permintaan logam sebagai implan menjadi semakin pesat seiring berbagai kasus kerusakan tulang. Logam sebagai implan harus memiliki sifat biokompatibel antara lain tahan terhadap korosi dan sesuai bagi sel hidup. Implan logam harus memiliki ketahanan korosi yang tinggi dalam lingkungan tubuh yang sangat korosif. Selain itu, implan logam akan berhubungan langsung dengan sel hidup di dalam tubuh manusia, sehingga sifat ini menjadi penting dalam pemilihan biomaterial (Poinern et al. 2013). Logam yang tidak biokompatibel, dapat menyebabkan inflamasi di sekitar jaringan tubuh yang diimplan. Paduan logam CoCrMo telah digunakan sebagai logam implan karena memiliki kekuatan mekanik, elastis modulus, ketahanan abrasi, dan ketahanan korosi yang baik, namun paduan logam CoCrMo dapat mengalami pelepasan ion Co, Cr, Mo sehingga menimbulkan pembengkakan dan rasa sakit di sekitar jaringan tubuh yang diimplan (Manivasagamet al.2010).
2
digunakan untuk melapisi logam implan, mampu meningkatkan ketahanan korosi dari implan logam di dalam tubuh. Hal ini dibuktikan dari hasil uji korosi pada larutansimulated body fluidyang menunjukkan hasil ketahanan korosi yang lebih baik pada paduan logam Mg yang dilapisi HAp dengan nilai rapat arus yaitu 0.25 μ A/cm2dibandingkan sebelum dilapisi yaitu 35.39 μ A/cm2.
Beberapa metode yang dapat digunakan dalam pelapisan HAp pada logam antara lain plasma spraying, sol–gel, biomimetic coating, dan elektroforesis deposisi (EPD) (Yoruc dan Koca 2009; Farnoush et al. 2012). Kelebihan penggunaan metode EPD sebagai metode pelapisan di antaranya sederhana, kekuatan pelapisannya tinggi, hasil pelapisan tipis dan merata, ketebalan lapisan dapat dikontrol, dan harga relatif murah (Javidiet al. 2008).
Sukaryo et al. (2010) telah melaporkan bahwa uji sitotoksisitas secara in vitro terhadap sel endotel menunjukkan tidak ada perubahan morfologi atau kematian sel pasca 72 jam inkubasi sampel paduan logam CoCrMo. Namun, sifat cytocompatibility pada paduan logam CoCrMo yang dilapisi HAp penting untuk diketahui. Hal ini terkait dengan data korosi dari hasil penelitian Ionita et al. (2013) menunjukkan bahwa sifat paduan logam CoCrMo setelah dilapisi HAp lebih baik dibandingkan tanpa pelapisan. Selain itu, potensi limbah cangkang kerang ale-ale sebagai prekursor HAp juga belum pernah dilaporkan. Dengan demikian, untuk memperoleh informasi mengenai sifat biokompatibel dari suatu implan tulang, maka dilakukan uji ketahanan korosi terhadap paduan logam CoCrMo setelah dilapisi HAp dan dilakukan uji kultur sel untuk mengetahui viabilitas sel terhadap paparan sampel.
Perumusan Masalah
Jumlah produksi yang besar dari kerang ale-ale menghasilkan dampak negatif pada lingkungan berupa limbah cangkang kerang ale-ale. Padahal limbah ini berpotensi mendatangkan keuntungan bila dikelola maksimal. Cangkang kerang ale-ale memiliki kandungan kalsium yang tinggi yang berpotensi untuk dimanfaatkan sebagai prekursor kalsium dalam sintesis HAp. Penelitian tentang sintesis HAp dari cangkang kerang ale-ale belum pernah dilaporkan. Selain itu, sifat cytocompatibility pada paduan logam CrCrMo yang dilapisi HAp dari cangkang kerang ale-ale juga belum pernah dilaporkan. Berdasarkan hal tersebut, sangat penting untuk melakukan penelitian ini untuk memperkaya pengetahuan tentang bahan baku dalam sintesis HAp dan aplikasinya terutama dalam bidang kedokteran ortopedi.
Tujuan Penelitian
3
Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi bagi potensi pada cangkang kerang ale-ale sebagai prekursor Ca dalam sintesis HAp yang dapat dimanfaatkan dalam bidang medis, dan memberikan sumbangan bagi salah satu segi pengembangan sosial-ekonomi di daerah Ketapang yang sampai sekarang ini belum banyak diketahui dan dikaji.
Ruang Lingkup Penelitian
Penelitian ini dilakukan atas 3 tahapan utama. Tahap pertama adalah preparasi sampel, pengukuran kadar Ca dengan AAS, kalsinasi serbuk sampel, dan konversi menjadi Ca(OH)2. Tahap kedua adalah sintesis HAp dengan metode
presipitasi double stirring dan pelapisan paduan logam CoCrMo dengan HAp menggunakan metode EPD. Tahap ketiga adalah tahap uji ketahanan korosi dan ujiin vitrositotoksisitas pada sel endotel CPAE. Diagram alir penelitian disajikan pada Lampiran 1.
2 TINJAUAN PUSTAKA
Kerang ale-ale (M. meretrix)
Kerang merupakan suatu jenis hewan mollusca (bertubuh lunak) yang termasuk pada anggota kelas bivalvia (bercangkang dua). Meretrix meretrix merupakan salah satu spesies dari kelas bivalvia yang bernilai ekonomis tinggi. Kerang M. meretrix dikenal dengan beberapa nama lokal seperti kerang lamis di perairan Marunda (Setyobudiandi et al. 2004), kerang tahu di muara Angke (Chairunisah 2011), sedangkan di daerah Ketapang Kalimantan Barat,M. meretrix dikenal dengan nama ale-ale. Cangkang kerang ale-ale dapat dilihat pada Gambar 1.
4
Gambar 1 Kerang ale-ale (M. meretrix) (Priyanto 2010)
Hidroksiapatit
Hidroksiapatit merupakan senyawa kalsium fosfat dengan rumus kimia Ca10(PO4)6(OH)2. Nisbah mol Ca/P agar material HAp terbentuk adalah 1.67.
Struktur kristal HAp (Gambar 2) adalah heksagonal dengan parameter kisi a = b = 9.4225 Ǻ dan c = 6.8850 Ǻ (Manafi dan Joughehdoust 2009). HAp termasuk dalam anggota senyawa kalsium fosfat yang potensial dalam rekayasa jaringan. Berbagai senyawa kalsium fosfat lainnya adalah dikalsium fosfat dihidrat (CaHPO4.2H2O), okta kalsium fosfat (Ca8H2(PO4)6·5H2O), dan trikalsium fosfat
(Ca3(PO4)2). HAp merupakan senyawa kalsium fosfat yang paling stabil (Chow
2009).
HAp menjadi biomaterial yang sangat potensial dalam rekayasa jaringan karena memiliki keunggulan berupa sifat biokompatibilitas, bioaktif, dan osteokonduktif nya yang sangat baik (Javidi et al. 2008). Sifat biokompatibel adalah kemampuan biomaterial untuk menyesuaikan dengan kecocokan tubuh penerima, tidak memiliki efek toksik, tidak melukai fungsi biologis seperti peradangan, dan tidak menyebabkan penurunan fungsi sel maupun jaringan tubuh lainnya. Sifat bioaktif adalah interaksi positif yang menghasilkan suatu ikatan yang sangat baik antara biomaterial dengan jaringan tubuh (Bauer et al. 2013). Osteokonduktif adalah kemampuan HAp untuk dilekati sel-sel osteoblas baru dan osteoprogenitor, menyediakan struktur untuk saling berhubungan sehingga sel-sel baru dapat berpindah, dan pembuluh darah baru dapat terbentuk. Sel osteoblas merupakan sel-sel tulang yang membentuk lapisan tulang baru selama tahap pembentukan dalam proses remodeling tulang. Sel osteoprogenitor merupakan sel induk yang merupakan prekursor dari osteoblas.
5
Sifat bioaktif yang dimiliki oleh HAp bermakna sebagai tumbuh jaringan tulang di sekitar implan sehingga HAp merupakan pilihan yang sangat baik sebagai pelapis untuk logam. HAp yang dilapiskan pada implan logam akan mempercepat ikatan antara HAp dengan jaringan tulang di sekitar. Kontak permukaan yang erat antara logam dan jaringan tulang di sekitarnya dibutuhkan untuk pertumbuhan tulang yang baru. Aplikasi HAp sebagai pelapisan implan logam adalah dengan menggabungkan kekuatan logam sebagai substrat dengan sifat bioaktif dari HAp yang dapat menginduksi pertumbuhan jaringan tulang di sekitarnya dan mampu membentuk ikatan kimia baru. HAp juga mampu meningkatkan ketahanan korosi implan logam dalam tubuh manusia serta dapat mengurangi terlepasnya ion logam dari suatu paduan logam (Javidi et al. 2008). Fenomena antarmuka antara HAp dan sel tubuh setelah implan masuk ke dalam tubuh akan mengalami beberapa tahapan. Tahap pertama pada awal proses implan, mulai terjadinya pelarutan permukaan HAp, tahap kedua pelarutan permukaan HAp terus berlanjut, tahap ketiga kondisi kesetimbangan terbentuk antara larutan fisiologis dengan permukaan HAp, tahap keempat terjadi adsorpsi protein-protein dan senyawa bioorganik, tahap kelima terjadi adhesi sel (sel tunggal membentuk jaringan sel-sel di dalam tubuh), tahap keenam proliferasi sel (pertumbuhan sel yang disebabkan oleh pembelahan sel yang aktif), tahap ketujuh awal mula perkembangan sel tulang baru, dan tahap kedelapan tulang baru telah terbentuk (Gambar 3).
Gambar 3 Fenomena antarmuka antara HAp dan sel tubuh (Bertazzoet al.2010)
HAp dapat disintesis dengan menggabungkan sumber prekursor Ca dan P. Prekursor berperan sebagai zat awal yang dibutuhkan dalam pembuatan suatu senyawa. HAp dapat dibuat dari prekursor Ca sintetik maupun dari prekursor Ca bahan alam. Sumber prekursor Ca sintetik antara lain senyawa Ca(OH)2, CaCO3,
Ca(NO3)2, dan CaCl2 (Shojai et al. 2013). Pembuatan HAp dari prekursor bahan
alam antara lain tulang ikan, batu kapur, cangkang telur, dan cangkang kerang. Sumber fosfor yang dapat digunakan untuk sintesis HAp antara lain diamonium hidrogen fosfat (NH4)2HPO4, asam fosfat (H3PO4), dan difosfor pentaoksida
(P2O5). Sintesis HAp dapat dilakukan dengan dua metode yaitu metode basah dan
6
Metode basah memiliki beberapa kelebihan sehingga sering diaplikasikan dalam bidang industri. Kelebihan metode ini di antaranya hasil samping sintesisnya berupa air, sehingga kemungkinan kontaminasi selama proses sangat rendah, dan biaya prosesnya rendah (Kehoe 2008). Metode presipitasi merupakan metode yang sering digunakan dalam sintesis HAp karena metode ini memiliki kontrol komposisi dan karakter fisik HAp yang lebih baik serta mudah diaplikasikan (Pankaew et al. 2010). HAp yang disintesis dengan metode presipitasi dilakukan dengan cara mentitrasi larutan yang mengandung Ca dengan larutan yang mengandung P. Metode presipitasi double stirring (teknik pengadukan magnetik dan ultrasonik) memainkan peranan penting dalam meningkatkan reaksi homogen dan untuk menghasilkan serbuk HAp murni. Yoruc dan Koca (2009) melaporkan bahwa diperoleh serbuk HAp murni dan berukuran nano dengan menggunakan metode presipitasidouble stirring.
Paduan Logam CoCrMo
Implan merupakan suatu biomaterial sintetik yang dimasukkan ke dalam tubuh untuk pengganti jaringan atau organ tubuh yang rusak. Biomaterial sintetik untuk implantasi umumnya berasal material yang sudah biasa digunakan oleh para ahli material. Secara umum, material ini dapat dibagi menjadi beberapa kategori, yaitu logam, keramik, komposit, dan polimer (Poinern et al. 2013). Logam merupakan material yang banyak digunakan untuk implantasi contohnya seperti sekrup untuk pelat yang bebas dari patah, joint prostheses (tulang sendi buatan) untuk bahu, pangkal paha, lutut, pergelangan kaki, dan lainnya. Pada kasus seperti patah atau retak tulang, implan berbasis logam berfungsi untuk menopang tulang sehingga terjadi pemulihan sel-sel tulang. Syarat utama yang harus dimiliki oleh biomaterial berbasis logam untuk implan adalah sesuai dengan sel hidup (excellent biocompatibility),bahan implan yang kuat, daya pakai yang lama, tidak karsinogen, memiliki ketahanan korosi tinggi, dan osteointegrasi yang bagus (Bombacet al. 2007; Manivasagam et al. 2010; Sukaryo dan Adi 2012; Bauer et al.2013).
Tiga elemen dasar pada paduan kobalt yaitu unsur kobalt, khromium, dan molibdenum. Khromium berfungsi untuk meningkatkan kekerasan dan ketahanan korosi. Khromium mampu membentuk lapisan pasif untuk membentengi material utama di bawahnya dari lingkungan sekitar dengan cara membentuk lapisan oksida yang kuat. Molibdenum berfungsi untuk menghasilkan struktur butir yang halus dengan kekuatan tinggi setelah casting atau forging (Prasetyo 2010). Biokompatibilitas paduan logam CoCrMo terkait erat dengan ketahanan korosi yang sangat baik karena terbentuknya lapisan oksida pasif yang spontan terbentuk pada permukaan paduan logam yaitu lapisan oksida Cr2O3, kontribusi minor dari
Co, dan Mo oksida.
7
dilakukan dengan meningkatkan sifat biokompatibilitas, sifat bioaktif, dan interaksi antara tulang dengan material paduan logam implan sehingga diperoleh suatu pembentukan tulang baru (Osteointegrasi) (Nasab et al. 2010). Salah satu solusi alternatif yang dapat dilakukan adalah melakukan modifikasi permukaan implan dengan penambahan komposisi lain di permukaan substrat implan yaitu melakukan pelapisan HAp pada permukaan paduan logam CoCrMo (Manivasagam et al. 2010). Menurut Javidi et al. (2008), HAp dapat digunakan untuk melapisi implan logam sehingga dapat meningkatkan ketahanan korosi, dan mengurangi terlepasnya ion logam ketika berkontak langsung dengan cairan tubuh.
Elektroforesis Deposisi (EPD)
Elektroforesis Deposisi (EPD) merupakan suatu teknik yang menggunakan mekanisme elektroforesis untuk menggerakkan partikel bermuatan dalam larutan atau suspensi karena adanya pengaruh medan listrik, sehingga partikel tersebut akan mengendap pada suatu substrat dan membentuk lapisan tipis dengan ketebalan tertentu (Besra dan Liu 2007; Boccaccini et al. 2010). Metode EPD dapat digunakan untuk melapiskan material pada suatu logam yang bertujuan di antaranya meningkatkan biokompatibilitas dari logam sehingga aman digunakan di dalam tubuh makhluk hidup (Castro et al. 2008). EPD biasanya dilakukan menggunakan dua elektrode sel yaitu katode (elektrode negatif) dan anode (elektrode positif). Mekanisme EPD terdiri atas dua tahap, yaitu tahap pertama, migrasi partikel bermuatan di dalam suspensi karena adanya gaya tarik dari penggunaan medan listrik, kemudian aliran listrik antara dua elektrode positif dan negatif menyebabkan partikel HAp akan bergerak ke arah yang berlawanan dengan muatannya (tahap elektroforesis) (Corni et al. 2008). Tahap kedua merupakan tahap pengendapan, koagulasi partikel membentuk lapisan pada katode (tahap deposisi). Pada tahap ini partikel HAp akan terdeposisi pada permukaan logam yang bertindak sebagai elektrode, kemudian akan menutup rapat permukaan logam secara homogen dalam bentuk lapisan film. Lapisan ini sebagai hasil deposisi partikel HAp yang menempel pada logam. Ilustrasi pergerakan partikel pada proses EPD dapat dilihat pada Gambar 4.
8
Ada beberapa faktor yang dapat mempengaruhi dan meningkatkan efektivitas terjadinya deposisi HAp pada permukaan logam dalam EPD yaitu stabilitas suspensi, besarnya tegangan yang digunakan, dan variasi waktu. Stabilitas suspensi dapat ditingkatkan dengan menambahkan pendispersi (dispersan) pada suspensi. Pendispersi yang dapat digunakan antara lain Tween 80, Span 80, etilendiamina, dan trietanolamina (TEA). TEA menunjukkan kemampuan sebagai pendispersi yang paling baik (Xiao dan Liu 2006). Penambahan TEA pada proses EPD bertujuan membuat suspensi menjadi homogen sehingga partikel HAp yang terdispersi dapat bergerak menuju permukaan logam (Xiao dan Liu 2006). Tegangan listrik yang digunakan pada metode EPD sangat berpengaruh terhadap laju dan struktur lapisan yang terbentuk, oleh karena itu tegangan listrik harus selalu dijaga konstan selama proses pelapisan berlangsung. Semakin tinggi tegangan yang digunakan (tidak melebihi 150V), maka kerapatan lapisan yang menempel pada permukaan logam akan semakin meningkat (Cortez dan Gutierrez 2004). Sumber tegangan tinggi akan lebih menguatkan partikel untuk meningkatkan efektivitas waktu EPD (Pang dan Zhitomirsky 2005).
Pelapisan logam dengan HAp tidak hanya dapat dilakukan dengan metode EPD, namun dapat pula dilakukan dengan berbagai macam metode yaitu biomimetic, sol-gel, laser ablation, ion sputtering, hidrotermal, dan plasma spraying(Wuet al.2006; Yoruc dan Koca 2009; Farnoushet al.2012). Kelebihan metode EPD adalah kekuatan pelapisan yang tinggi, lapisan yang dihasilkan tipis dan merata, deposit HAp yang menempel pada permukaan logam mudah untuk dikontrol, deposit HAp yang diperoleh memiliki kemurnian yang tinggi, prosesnya menggunakan temperatur yang rendah, tanpa transformasi fasa selama pelapisan, dan penggunaan peralatan yang relatif murah (Javidi et al.2008). EPD juga mampu menghasilkan deposit yang seragam dengan homogenitas mikrostruktur yang tinggi dan dapat mengontrol ketebalan lapisan (Besra dan Liu 2007). Pergerakan muatan positif partikel HAp menuju katode dalam sel EPD ditunjukkan oleh Gambar 5.
9
Jika sistem partikellyosphere(partikel bermuatan membentuk lapis rangkap baur atau lyosphere) bergerak, dinamika fluida dan medan listrik yang digunakan akan mendistorsi selubung lapis rangkap bergerak menuju elektrode yang berbeda dengan muatannya, ion-ion bermuatan positif akan menuju ke katode sedangkan ion-ion bermuatan negatif akan menuju ke anode. Hasil dari reaksi kimia ini, terbentuknya lapis rangkap pada katode yang terjadi karena adanya gaya tarik London Van der Waals yang menginduksi terjadinya koagulasi/deposisi ion-ion bermuatan positif menuju katode. Distorsi lapis rangkap yang menyebabkan koagulasi terjadi karena kemungkinan adanya konsentrasi tinggi partikel di dekat elektrode (atau efisiensi tumbukan yang tinggi) (Besra dan Liu 2007).
Pelapisan HAp pada paduan logam CoCrMo menggunakan metode EPD pada penelitian Yunanti (2014) dilakukan dengan berbagai variasi volume larutan HAp, pH, tegangan, dan waktu yang bertujuan untuk memperoleh kondisi optimum. Pada metode EPD tersebut, larutan HAp yang dibuat dihubungkan dengan dua elektrode, yaitu paduan logam CoCrMo yang menjadi sasaran pelapisan HAp pada permukaannya (katode) dan logam platina (anode). Hasil penelitian Yunanti (2014) menginformasikan bahwa metode EPD dapat digunakan untuk melapisi paduan logam CoCrMo dengan senyawa HAp. Sebanyak 0.3 gram HAp dilarutkan dalam etanol-TEA dengan variasi volume, pH, tegangan, dan waktu. Hasil pelapisan optimum yang diperoleh yaitu campuran larutan etanol dan TEA dengan perbandingan 50:2 (mL), pada pH 7, tegangan listrik 120V, dan waktu 30 menit.
Uji Ketahanan Korosi
Peristiwa korosi ditandai dengan terjadinya degradasi suatu material yang berlangsung sedikit demi sedikit akibat adanya serangan elektrokimia yang terjadi ketika suatu logam ditempatkan di dalam lingkungan elektrolitik berlawanan dari tubuh manusia (Adya et al. 2005). Implan di dalam tubuh berhadapan dengan lingkungan korosif meliputi darah dan konstituen lain dari cairan tubuh seperti air, natrium, klor, protein, plasma, dan asam amino. Medium cair dalam tubuh manusia terdiri dari berbagai anion seperti ion klorida, fosfat, dan bikarbonat serta kation seperti Na+, K+, Ca2+, Mg2+, zat organik yang memiliki berat molekul rendah, komponen polimer dengan berat molekul tinggi, dan oksigen terlarut. Molekul-molekul biologis mengganggu produk implan melalui reaksi katodik maupun anodik sehingga implan dapat mengalami suatu korosi. Hidrogen yang dibentuk dari reaksi katodik bertindak sebagai inhibitor korosi, namun kehadiran bakteri dapat meningkatkan korosi dengan cara menyerap hidrogen di sekitar implan. Perubahan nilai pH juga mempengaruhi korosi. Nilai pH normal pada tubuh manusia dipertahankan pada 7. Nilai ini cepat berubah dari 3 sampai 9 karena beberapa penyebab seperti kecelakaan, ketidakseimbangan dalam sistem biologi akibat penyakit, infeksi, dan setelah operasi nilai pH dekat implan bervariasi biasanya dari 5.3 sampai 5.6 (Manivasagamet al.2010).
10
yang berada pada level paling baik adalah laju korosi dengan nilai kurang dari 1 mpy (Fontana 1985).
UjiCytocompatibility In vitroSel Endotel
Cytocompatibility merupakan suatu uji viabilitas sel yang mencerminkan non sitotoksisitas suatu biomaterial. Uji ini penting dalam desain biomaterial untuk aplikasi dalam suatu rekayasa jaringan (Hashmi 2014). Uji sitotoksisitas dalam penelitian ini dilakukan secara in vitro menggunakan media kultur sel endotelcell pulmonary artery endhothelium(CPAE ATCC-CCL 209). Sel endotel memainkan peranan penting dalam penyembuhan luka karena terdapat pada permukaan dalam pembuluh darah dan sel utama yang terlibat dalam angiogenesis (Marques et al. 2008). Angiogenesis merupakan proses pembentukan pembuluh darah baru yang merupakan suatu proses fisiologis tubuh untuk menyediakan nutrisi, oksigen, dan memicu pembentukan jaringan granulasi pada daerah luka. Angiogenesis memainkan peranan penting dalam membangun rangka dan perbaikan pada tulang yang retak atau patah. Hal ini dapat ditangani melalui proses implantasi (Kanczler dan Oreffo 2008). HAp untuk mempercepat proses penyembuhan luka setelah implantasi, mampu meningkatkan proliferasi endotel yang dibutuhkan untuk terjadinya angiogenesis (Pezzatini 2007). HAp sebagai implan juga berguna menjaga konsentrasi kalsium pada darah (Zhang 2012).
3 METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada bulan Januari 2015‒ Januari 2016 di Laboratorium Kimia Analitik Departemen Kimia IPB, Laboratorium Biofisika Material Departemen Fisika IPB, Laboratorium Badan Tenaga Nuklir Nasional (BATAN) PUSPIPTEK Serpong, Pusat Penelitian dan Pengembangan Hasil Hutan, Laboratorium Markas Besar Kepolisian Republik Indonesia, dan Laboratorium Mikrobiologi Pusat Studi Satwa Primata.
Bahan
Bahan-bahan yang digunakan adalah cangkang kerang ale-ale diperoleh dari Ketapang Kalimantan Barat, CaCO3 (Merck), HCl (Merck), paduan logam
CoCrMo (Nilaco Corporation, Japan), batang karbon, (NH4)2HPO4(Merck), air
11
Alat
Alat-alat yang digunakan adalah ayakan 100 mesh, pengaduk magnetik, tanur, indikator pH universal, oven, kertas saring, ultrasonic processor CPX 130, ultrasonic cleanerUS-3, micrometer analog,mikroskop optik,grinding paper grit 1000, dan peralatan uji kultur sel. Sedangkan peralatan karakterisasi terdiri dari Difraksi Sinar-X (XRD) Shimadzu XD-7000, Spektrometer Infra Merah Transformasi Fourier (FTIR) Bruker Tensor 3, Mikroskop Pemancar Elektron (SEM) Carl-Zeiss Bruker EVO MA10, Energy Dispersive X-Ray Spectroscopy (EDX) Bruker, Penganalisa Ukuran Butir (PSA) Vasco DLS, Spektrofotometer Serapan Atom (AAS) Shimadzu AA-7000, EPD PS-520, dan potentiostat/ galvanostat M273.
Prosedur Penelitian
Preparasi sampel
Sampel (cangkang kerang) dibersihkan dari kotoran menggunakan air kemudian direbus selama 1 jam. Selanjutnya sampel dikeringkan di bawah sinar matahari lalu digiling menggunakan mesin penggiling sampai menjadi serbuk halus. Serbuk sampel diayak 100 mesh. Fasa serbuk lolos 100 mesh dianalisis dengan XRD dan analisis unsur dengan EDX (Mijanet al.2015).
Pengukuran kadar Ca dalam serbuk sampel dengan AAS
Preparasi deret standar: Dibuat larutan standar Ca2+ 1000 ppm dengan ditimbang sebanyak 2.497 gram CaCO3 lalu ditambahkan 5 mL HCl pekat,
didiamkan ±5 menit sampai menjadi larut dan jernih, sampel ditera dengan air bebas ion dan dihomogenkan. Kemudian dibuat larutan 100 ppm dengan cara dipipet 10 mL dari larutan induk 1000 ppm dan dimasukkan kedalam labu takar 100 mL, kemudian ditera dengan air bebas ion dan dihomogenkan. Selanjutnya dibuat 2, 4, 8, 12, dan 16 ppm yaitu dipipet 2, 4, 8, 12, dan 16 mL kemudian masing-masing dimasukkan kedalam labu takar 100 mL, lalu ditera dengan air bebas ion dan dihomogenkan. Selanjutnya ditambahkan sedikit strontium agar stabil dalam pengukuran. Sampel diukur dengan AAS dengan λ = 422.7 nm (APHA; AWWA; WEF 2005).
Preparasi sampel: Serbuk sampel cangkang setelah preparasi ditimbang sebanyak 0.1 gram, lalu ditambahkan 5 mL HCl pekat, sampel dipanaskan sambil diaduk dengan pengaduk magnetik ±10 menit sampai menjadi larut dan jernih, kemudian dimasukkan ke dalam labu takar 100 mL, sampel ditera dengan air bebas ion dan dihomogenkan. Setelah itu, sebanyak 1 mL larutan induk dimasukkan ke dalam labu takar 100 mL, sampel ditera dengan air bebas ion dan dihomogenkan. Selanjutnya ditambahkan sedikit strontium agar stabil dalam pengukuran. Kemudian diukur dengan AAS pada λ = 422.7 nm.
12
strontium agar stabil dalam pengukuran. Kemudian diukur dengan AAS denganλ = 422.7 nm.
Kalsinasi serbuk sampel dan konversi menjadi Ca(OH)2
Serbuk sampel dipanaskan di dalam tanur pada suhu 1000 °C selama 3 jam. Abu yang diperoleh dari proses kalsinasi serbuk sampel kemudian dikonversi dengan cara dibiarkan kontak dengan udara pada suhu kamar. Untuk mengetahui keberadaan Ca(OH)2, abu yang telah dibiarkan kontak dengan udara dianalisis
dengan XRD (Modifikasi Pankaewet al.2010).
Sintesis HAp dengan metode presipitasidouble stirring(ultrasonik-magnetik)
Sintesis HAp dilakukan melalui reaksi antara Ca(OH)2 dengan (NH4)2HPO4
dengan rasio mol Ca/P = 1.67. Suspensi Ca(OH)2disiapkan dari Ca(OH)2yang
diperoleh dari tahap kalsinasi-konversi, ditimbang sebanyak 14.7410 gram Ca(OH)2dilarutkan dalam 100 mL air bebas ion dan untuk larutan (NH4)2HPO4
disiapkan dengan cara ditimbang sebesar 15.7840 gram (NH4)2HPO4dilarutkan
dalam 100 mL air bebas ion. Kemudian larutan (NH4)2HPO4 diteteskan pada
suspensi Ca(OH)2. Bersamaan dengan proses tersebut, suspensi disonikasi dengan
menggunakan alat ultrasonic processor pada 130 W, 20 KHz selama 2 jam dan bersamaan itu pula dilakukan pengadukan kuat dengan pengaduk magnetik. pH diatur pada kondisi pH 10. Campuran reaksi kemudian didiamkan pada suhu kamar selama 24 jam, setelah itu disaring dengan kertas saring. Endapan yang diperoleh dibilas dengan air bebas ion. Endapan dikeringkan dalam oven pada suhu 100 oC dan dilanjutkan dengan dipanaskan dalam tanur pada suhu 1000 oC
selama 5 jam. Setelah kering, endapan digerus hingga halus dengan mortar. Fasa dan ukuran kristal serbuk yang dihasilkan dianalisis dengan XRD. Gugus fungsi dievaluasi dengan FTIR. Morfologi permukaan dan ukuran serbuk dikaji dengan SEM. Distribusi ukuran partikel dievaluasi menggunakan PSA (Modifikasi Yoruc dan Koca 2009).
Pelapisan paduan logam CoCrMo dengan HAp menggunakan metode EPD
13
Uji ketahanan korosi
Paduan logam CoCrMo dipotong menjadi ukuran yang sama dan dibentuk menjadi bulat hingga berukuran diameter 14 mm. Sampel dirangkai pada elektrode kerja, kemudian tiga elektrode sebagai instrument uji korosi dicelupkan kedalam labu yang berisi media pengkorosi larutan infus NaCl 500 mL. Elektrode kalomel sebagai standar digunakan sebagai reference elektrode, dua batang karbon sebagaisupporting elektrodes, dan paduan logam CoCrMo sebagai working elektrode. Sel korosi dihubungkan pada perangkat potensiostat/ galvanostat model 273 pada potensial -20 mV sampai 20 mV. Dari pengukuran ini konstanta tafel anodik-katodik secara otomatis dapat diperoleh sehingga laju korosi dapat ditentukan (Modifikasi Effendi dan Jahja 2006).
Ujiin vitrositotoksisitas pada sel endotel CPAE
Sel ditumbuhkan menggunakan pelat biakan 6 sumur dengan jumlah sel 2 × 104 sel/sumur dan sel kemudian diinkubasi selama 24 jam pada suhu 37 °C dengan 5% CO2. Sementara itu, sampel berupa paduan logam CoCrMo dan
paduan logam CoCrMo yang dilapisi HAp berukuran 2 mm disterilisasi dengan iradiasi sinar gamma dosis 15 kGy. Selanjutnya diletakkan sampel yang sudah steril pada kultur sel CPAE yang telah berflokuensi (24 jam usia kultur sel). Kultur sel endotel tanpa perlakuan digunakan sebagai kontrol negatif. Sampel dalam medium kultur kemudian diinkubasi selama 72 jam pada suhu 37 °C dengan 5% CO2. Jumlah sel ditentukan menggunakan hemositometer. Viabilitas
sel diperiksa dengan pewarna biru tripan dan ditentukan persen inhibisinya (Modifikasi Miki dan Morita 2015).
4 HASIL DAN PEMBAHASAN
Hasil Analisis XRD Cangkang Kerang ale-ale Sebelum dan Setelah Kalsinasi
Hasil analisis XRD untuk keberadaan senyawa CaCO3dari serbuk cangkang
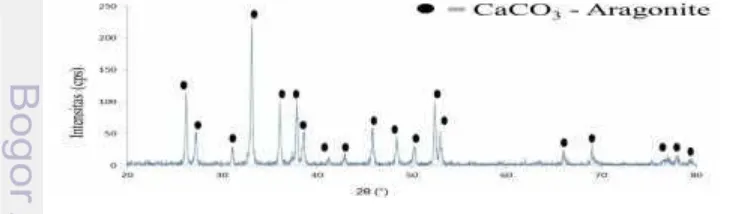
kerang ale-ale sebelum kalsinasi menunjukkan bahwa cangkang kerang ale-ale memiliki satu fasa yaitu CaCO3 (aragonite) (Gambar 6). Puncak difraksi fasa
CaCO3 (aragonite) dicirikan dari puncak difraksi yang khas dengan intensitas tertinggi berada pada sudut 2θ 26.26°, 33.15°, 36.12°, dan 52.45° (berdasarkan data JCPDS No. 41-1475).
14
Kalsinasi serbuk cangkang kerang pada suhu 1000 ºC bertujuan untuk mengubah senyawa CaCO3 menjadi CaO dengan persamaan reaksi CaCO3(S) →
CaO(S) + CO2(g). Kalsinasi pada suhu rendah dapat menyebabkan senyawa CaO
yang dihasilkan berubah kembali menjadi CaCO3 dan dekomposisi CO2 yang
dihasilkan akan cukup rendah, oleh sebab itu kalsinasi dalam proses ini dilakukan pada suhu 1000 °C. Kalsinasi juga dapat menghilangkan senyawa organik dan pengotor yang mengganggu dalam proses pembentukan HAp (Sukaryo et al. 2009). Data hasil analisis XRD serbuk cangkang kerang ale-ale sebelum kalsinasi dapat dilihat pada Lampiran 2a dan standar fasa CaCO3 dapat dilihat pada
Lampiran 3a.
Senyawa CaO yang diperoleh dibiarkan kontak dengan udara agar terjadi hidrasi CaO menjadi Ca(OH)2 melalui persamaan reaksi: 2CaO(S)+ 2H2O(g) →
2Ca(OH)2(S). Pola XRD cangkang kerang ale-ale setelah kalsinasi menunjukkan
bahwa telah terbentuknya fasa Ca(OH)2 (portlandite) yang dicirikan keberadaannya pada sudut 2θ = 18.04°, 28.71°, 34.13°, 47.29°, 50.84°, 54.39°, 59.44°, 62.68°, 64.43°, dan 71.86° (berdasarkan data JCPDS No. 44-1481) (Gambar 7).
Gambar 7 Difraktogram sinar-x serbuk cangkang kerang ale-ale setelah kalsinasi
Adanya puncak lain pada sudut 2θ = 23.11°, 29.42°, 35.95°, 39.41°, 43.15°, 48.52°, 57.30°, dan 60.60° menunjukkan bahwa masih ada sedikit pengotor dari CaCO3yang belum berubah fasa menjadi Ca(OH)2, namun hal ini tidak signifikan
mengganggu untuk memperoleh fasa tunggal HAp. Senyawa Ca(OH)2 yang
diperoleh ini merupakan starting material yang digunakan dalam tahap sintesis HAp. Data hasil analisis XRD serbuk cangkang kerang ale-ale setelah kalsinasi dapat dilihat pada Lampiran 2b dan standar fasa CaCO3 dapat dilihat pada
Lampiran 3b.
Komposisi Cangkang Kerang ale-ale Sebelum Kalsinasi
15
Namun kandungan kalsium dari cangkang kerang ale-ale lebih tinggi dibandingkan cangkang tutut sebesar 64.73% (Herawatyet al.2014).
Hasil analisis unsur menggunakan EDX menunjukkan bahwa kandungan unsur utama dalam cangkang kerang ale-ale adalah kalsium (79.24%), oksigen (17.79%), dan karbon (2.97%) (Lampiran 5). Pada hasil EDX menunjukkan terdapatnya kandungan kalsium dalam cangkang kerang jauh lebih besar dibandingkan unsur oksigen dan karbon. Sejalan dengan penelitian Herawatyet al. (2014) yang menunjukkan kandungan unsur cangkang tutut dengan EDX didominasi unsur kalsium (62.96%), oksigen (36.15%), dan karbon (0.89%). Analisis EDX bertujuan untuk meyakinkan bahwa kandungan unsur utama serbuk sampel adalah kalsium, oksigen, dan karbon sesuai dengan unsur penyusun fasa yang dihasilkan dari analisis XRD yaitu CaCO3. Hasil AAS dan EDX telah
membuktikan bahwa cangkang kerang ale-ale yang kaya akan kalsium berpotensi sebagai prekursor kalsium untuk mensintesis HAp.
Hasil Sintesis HAp
Pemilihan sintesis HAp menggunakan metode presipitasi double stirring (ultrasonik-magnetik) karena HAp murni tidak mudah dihasilkan. Kalsium fosfat memiliki berbagai derivat dan sintesis kalsium fosfat sangat kuat bergantung pada kondisi reaksi (Yoruc dan Koca 2009). Oleh sebab itu alternatif solusi adalah dengan metode presipitasi double stirring yaitu pengadukan dengan bantuan ultrasonik-magnetik secara bersamaan akan membuat partikel HAp yang dihasilkan memiliki tingkat kemurnian tinggi dalam waktu sintesis yang cepat. Sintesis HAp dilakukan dengan mereaksikan Ca(OH)2dari hasil kalsinasi dengan
(NH4)2HPO4 dengan perbandingan mol 10:6 sesuai dengan rasio mol Ca/P 1.67
dan pH 10, dengan persamaan reaksi:
10Ca(OH)2 + 6(NH4)2HPO4 Ca10(PO4)6(OH)2 + 6H2O + 12NH4OH.
Hidroksiapatit dengan pH kurang dari 10 atau melebihi 10 akan menyebabkan terbentuknya senyawa kalsium fosfat lain yang tidak diinginkan. Oleh karena itu pemantauan pH terus dilakukan selama proses sintesis HAp. Pada saat sintesis berlangsung, tidak dilakukan penambahan basa ataupun asam untuk mengontrol pH karena pH yang diperoleh telah mencapai 10. Suhu sintering sangat penting dalam proses menghasilkan HAp murni karena fasa selain HAp dapat terbentuk apabila suhu sintering terlampau tinggi maupun terlampau rendah. Jika suhu sintering terlampau tinggi maka akan terbentuk senyawa apatit karbonat tipe A Ca10(PO4)6CO3 dan jika suhu sintering terlampau rendah maka akan
terbentuk senyawa apatit karbonat tipe B Ca10(PO4)3CO3(OH)2(Shojaiet al.2013).
Hasil Karakterisasi Fasa HAp menggunakan XRD
16
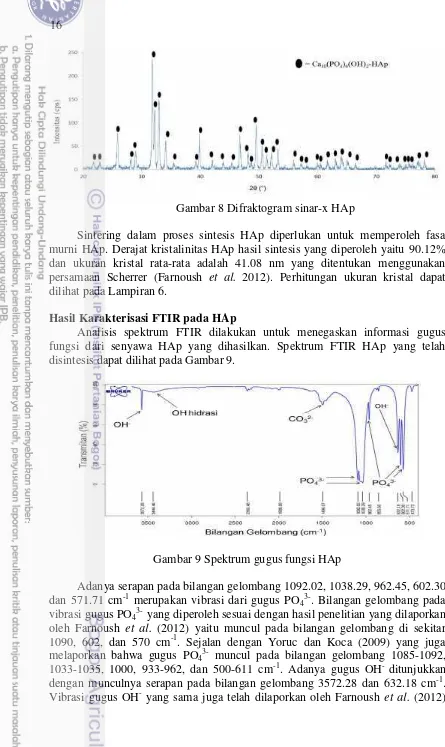
Gambar 8 Difraktogram sinar-x HAp
Sintering dalam proses sintesis HAp diperlukan untuk memperoleh fasa murni HAp. Derajat kristalinitas HAp hasil sintesis yang diperoleh yaitu 90.12% dan ukuran kristal rata-rata adalah 41.08 nm yang ditentukan menggunakan persamaan Scherrer (Farnoush et al. 2012). Perhitungan ukuran kristal dapat dilihat pada Lampiran 6.
Hasil Karakterisasi FTIR pada HAp
Analisis spektrum FTIR dilakukan untuk menegaskan informasi gugus fungsi dari senyawa HAp yang dihasilkan. Spektrum FTIR HAp yang telah disintesis dapat dilihat pada Gambar 9.
Gambar 9 Spektrum gugus fungsi HAp
Adanya serapan pada bilangan gelombang 1092.02, 1038.29, 962.45, 602.30, dan 571.71 cm-1 merupakan vibrasi dari gugus PO
43-. Bilangan gelombang pada
vibrasi gugus PO43- yang diperoleh sesuai dengan hasil penelitian yang dilaporkan
oleh Farnoush et al. (2012) yaitu muncul pada bilangan gelombang di sekitar 1090, 602, dan 570 cm-1. Sejalan dengan Yoruc dan Koca (2009) yang juga melaporkan bahwa gugus PO43- muncul pada bilangan gelombang 1085-1092,
17
yaitu muncul pada serapan pada bilangan gelombang sekitar 3572 dan 632 cm-1. Sejalan dengan hasil penelitian yang dilaporkan oleh Dedourkova et al. (2012) bahwa gugus OH- muncul pada bilangan gelombang 3575 cm-1. Gugus OH- yang sama juga dilaporkan muncul pada bilangan gelombang 628 cm-1 (Yoruc dan Koca 2009). Gugus OH hidrasi muncul pada bilangan gelombang 3444.46 cm-1. Vibrasi gugus OH hidrasi yang sama juga telah dilaporkan oleh Farnoush et al. (2012) yaitu muncul pada bilangan gelombang 3423 cm-1. Sejalan dengan hasil penelitian yang dilaporkan oleh Yoruc dan Koca (2009) yaitu gugus OH hidrasi muncul pada bilangan gelombang 3461, 3437, 3436, dan 3425 (3461-3436, 2926-2924) cm-1. Adanya puncak lemah yang merupakan vibrasi dari gugus CO3
2-ditunjukkan dengan munculnya serapan pada bilangan gelombang 1496.07 cm-1. Vibrasi dari gugus CO32- yang sama juga telah dilaporkan oleh Farnoush et al.
(2012) bahwa spektrum lemah mengindikasikan adanya gugus CO32-muncul pada
bilangan gelombang 1470 dan 1420 cm-1sebagai hasil dari absorpsi atmosfer CO2
pada permukaan partikel HAp. Hal ini sejalan dengan hasil FTIR pada gugus CO32- yang dilaporkan oleh Herawaty et al. (2014) yaitu muncul pada bilangan
gelombang 1454.33 cm-1. Menurut Dedourkova et al. (2012) bahwa adanya substitusi karbonat pada gugus hidroksil atau fosfat dapat disebabkan oleh kelarutan CO2 di lingkungan sekitar terkait dengan pengadukan yang kuat selama
proses sintesis HAp dengan metode presipitasi kimia. Hasil FTIR ini telah menegaskan akan keberadaan senyawa murni HAp.
Hasil Karakterisasi SEM pada HAp
Analisis SEM pada HAp bertujuan untuk melihat morfologi kristal HAp. Foto SEM partikel HAp dapat dilihat pada Gambar 10. HAp yang diperoleh berbentuk bola, ukuran rata-rata pori yang homogen, dan memiliki salah satu diameter partikel bola berukuran nano yaitu sebesar 167.9 nm. Farnoush et al. (2012) juga melaporkan hal yang sama bahwa morfologi HAp dilihat menggunakan SEM diperoleh HAp berbentuk bola dengan ukuran partikel HAp sekitar 65 nm.
Gambar 10 Foto SEM HAp perbesaran (a) 3000X ; (b) 10.000X
Porositas HAp berfungsi menyediakan lingkungan biologi yang baik pada adhesi sel, interaksi selular, proliferasi, dan migrasi (Poinern et al. 2013). Dengan demikian, pori HAp yang terdapat diantara butiran HAp diharapkan memiliki kemampuan sebagai media pertumbuhan tulang baru setelah implantasi. Tampak partikel HAp membentuk aglomerat (Gambar 10a dan b). Foto SEM pada HAp
18
menggunakan metode presipitasi yang sama dilaporkan Yoruc dan Koca (2009) bahwa diperoleh HAp berbentuk bola dan terjadi aglomerasi pada partikel. Hal ini terjadi karena bergabungnya partikel ukuran nano membentuk aglomerat sehingga diperoleh beberapa ukuran mikro. Sejalan dengan Dedourkova et al. (2012) yang memperoleh partikel HAp berbentuk bola dengan ukuran 30-50 nm dan beberapa partikel yang teraglomerasi. Mobasherpouret al.(2007) juga melaporkan hal yang sama bahwa pada SEM partikel HAp yang dihasilkan menggunakan metode presipitasi diperoleh partikel kecil dan partikel aglomerasi.
Hasil Analisis PSA pada HAp
Distribusi ukuran partikel HAp dapat dilihat pada Gambar 11. Analisis PSA pada HAp menunjukkan distribusi ukuran rata-rata partikel berada pada kisaran 670.26 nm. Ukuran rata-rata partikel ini masih cukup besar dari ukuran nano standar (ukuran < 100 nm) (Corni et al. 2008). Ukuran partikel dari hasil penelitian ini lebih besar dari 100 nm, sehingga HAp yang diperoleh belum berukuran nano.
Gambar 11 Distribusi ukuran partikel HAp
Hasil ini berkaitan pada waktu proses kalsinasi dalam menghasilkan HAp yang dilakukan pada suhu tinggi, karena semakin tinggi suhu kalsinasi, mengakibatkan ukuran kristal yang diperoleh akan semakin besar. Hal ini disebabkan oleh semakin banyaknya susunan atom dalam keteraturan sehingga struktur HAp semakin sempurna yang ditandai dengan pertumbuhan dari fasa amorf menjadi fasa kristal (Mobasherpour et al. 2007). Keuntungan memiliki ukuran nano HAp terletak pada kemampuan berintegrasi dengan jaringan tulang, mendorong, dan mendukung pertumbuhan tulang. Salah satu sifat yang menarik dari nano HAp adalah ketika berikatan dengan tulang, membentuk suatu kesatuan yang tidak dapat dibedakan dengan jaringan tulang di sekitarnya.
Suhu yang tinggi pada saat proses sintering HAp, berpengaruh pada fasa kristal HAp yang dihasilkan. Hal ini dibuktikan dari hasil analisis XRD (Gambar 8) yang menghasilkan puncak difraktogram tajam fasa tunggal HAp. Dapat dikatakan bahwa suhu tinggi mempengaruhi derajat kristalinitas HAp yang dihasilkan dan berpengaruh kepada besarnya ukuran kristal yang diperoleh.
19
Manafi dan Joughehdoust (2009) melaporkan bahwa sintesis HAp pada suhu 200 °C dan 150 °C, diperoleh HAp dengan bentuk kristal lebih baik pada suhu 200 °C dibandingkan dengan suhu 150 °C, yang mengindikasikan bahwa terjadi transformasi dari amorf menjadi bentuk kristal pada suhu yang lebih tinggi.
Pencirian Hasil Pelapisan HAp pada Paduan Logam CoCrMo
Paduan logam CoCrMo sebagai sasaran pelapisan HAp bertindak sebagai elektrode negatif (katode) dan batang karbon bertindak sebagai elektrode positif (anode). TEA yang digunakan terbukti mampu membuat larutan menjadi homogen sehingga partikel HAp yang terdispersi bergerak menuju permukaan logam. Paduan logam CoCrMo dipoles dengangrinding paper grit 1000bertujuan agar HAp lebih kuat menempel pada logam (Gambar 12).
Gambar 12 Foto mikroskop optik setelah dilakukan EPD
Hasil Analisis XRD Lapisan HAp pada Paduan Logam CoCrMo
Pola XRD HAp pada paduan logam CoCrMo dapat dilihat pada Gambar 13. Fasa kristal utama hasil pelapisan adalah masih tetap fasa HAp sesuai standar JCPDS No. 09-0432 dan adanya fasa CoCrMo, puncakpada 2θ = 44.47°, yang diduga berasal dari paduan logam CoCrMo yang terdeteksi pada saat analisis XRD. Hal yang sama juga dilaporkan oleh Hiromoto et al. 2005 bahwa fasa CoCrMo muncul padapuncak 2θ = 44.21°.Derajat kristalinitas hasil sintesis yaitu 83.28%.
20
Derajat kristalinitas ini lebih rendah dibandingkan dengan derajat kristalinitas HAp sebelum terjadi pelapisan logam. Hal ini dapat disebabkan oleh pengaruh tegangan dan waktu pelapisan pada proses EPD. Tegangan tinggi dan waktu pelapisan merupakan faktor penting dalam pelapisan untuk menghasilkan partikel kecil (Cortez et al. 2004). Sesuai dengan hasil yang diperoleh menunjukkan tegangan yang digunakan dalam proses EPD dapat memperkecil ukuran partikel, akibatnya derajat kristalinitas yang dihasilkan menjadi lebih rendah karena semakin rendah derajat kristalinitas maka ukuran HAp yang dihasilkan akan semakin kecil. Dengan demikian, pelebaran puncak dari HAp yang melapisi paduan logam CoCrMo merupakan akibat dari ukuran kristal yang menjadi lebih kecil pada material pelapisan. Proses EPD ini berhasil karena tidak merubah struktur utama pada HAp. Data hasil analisis XRD pelapisan HAp pada paduan logam CoCrMo dapat dilihat pada Lampiran 2d.
Hasil SEM HAp pada Paduan Logam CoCrMo
Karakterisasi menggunakan SEM dilakukan untuk melihat morfologi lapisan HAp pada paduan logam CoCrMo. Foto SEM morfologi lapisan HAp pada paduan logam CoCrMo dapat dilihat pada Gambar 14. Tampak bahwa morfologi permukaan HAp pada paduan logam CoCrMo berbentuk bola, partikel homogen, tidak menunjukkan adanya keretakan, dan lapisan HAp tersebar merata di area pelapisan paduan logam CoCrMo. Ketebalan pelapisan yang diperoleh sekitar 0.08 μ m. Hal ini membuktikan bahwa etanol dan dispersan TEA efektif memecah partikel yang teraglomerasi untuk menghasilkan suspensi koloid yang stabil. TEA terbukti sebagai dispersan yang efektif untuk proses EPD.
Gambar 14 Foto SEM HAp pada paduan logam CoCrMo (perbesaran 7000X)
Gugus -OH dari HAp dapat membentuk ikatan hidrogen pada alkohol alifatik dan gugus -OH dari TEA. Rantai alifatik dari TEA mungkin juga bertindak sebagai penghalang sterik antara dua partikel dan meningkatkan stabilitas dispersi. Oleh karena itu, penambahan TEA sangat mendukung pada pelapisan HAp pada logam dalam proses EPD (Xiao dan Liu 2006). Javidi et al. (2008) juga melaporkan bahwa morfologi HAp melapisi permukaan logam stainless steel 316L terlihat seragam dan tidak ditemukannya keretakan.
21
penetrasi jaringan tulang ke dalam HAp dan menyebabkan biointegrasi serta stabilitas mekanik yang baik pada antarmuka tulang sekitarnya dan implan yang dilapisi (Javidi et al. 2008). Pori yang saling berhubungan juga penting untuk jalannya aliran fluida yang mengalir melalui pori material keramik (Poinern et al. 2013).
Ketahanan Korosi
Degradasi bertahap dari suatu material oleh suatu serangan elektrokimia menjadi suatu perhatian besar terutama ketika suatu implan logam ditempatkan dalam lingkungan elektrolit berlawanan dari tubuh manusia. Uji ketahanan korosi bertujuan untuk memperoleh informasi mengenai sifat biokompatibel dari paduan logam CoCrMo yang dilapisi HAp. Dalam hal ini, paduan logam CoCrMo yang dilapisi oleh HAp dikondisikan sebagai implan yang berada dalam tubuh yang akan berkontak langsung dengan cairan infus, yang dikondisikan sebagai medium cairan tubuh. Jumlah material yang akan terlarut dari permukaannya pada lama waktu tertentu diukur sebagai laju korosi. Laju korosi dinyatakan dalam satuan mils per year (1 mpy = 25.410-3 mm year-1). Laju korosi paduan logam CoCrMo yang dilapisi HAp pada media cairan infus NaCl yang dibandingkan dengan paduan logam CoCrMo tanpa pelapisan ditunjukkan pada Gambar 15. Data hasil uji korosi dapat dilihat pada Lampiran 7.
Gambar 15 Laju korosi
Hasil membuktikan bahwa nilai uji korosi untuk paduan logam CoCrMo yang dilapisi HAp empat kali lebih kecil dibandingkan paduan logam CoCrMo yang tidak dilapisi HAp (Gambar 15). Hal ini membuktikan bahwa paduan logam yang dilapisi HAp lebih baik dibandingkan paduan logam tanpa pelapisan. Menurut Fontana (1985) bahwa semakin kecil nilai laju korosi suatu logam, maka akan memiliki ketahanan korosi yang semakin baik. Laju korosi pada paduan logam CoCrMo yang dilapisi HAp berada pada level outstanding dari suatu ketahanan korosi yang merupakan level paling tinggi pada suatu uji ketahanan korosi. Hasil ini menunjukkan bahwa paduan logam CoCrMo yang dilapisi HAp dapat bertindak sebagai lapisan pelindung melawan difusi ion dan korosi dan juga meningkatkan ketahanan korosi dari paduan logam CoCrMo yang berada di lingkungan cairan tubuh. Kondisi terlepasnya ion paduan logam CoCrMo dapat
22
diminimalisir oleh bantuan HAp sebagai agen osteointegrasi. Salmanet al. (2013) melaporkan bahwa aplikasi HAp sebagai pelapis dari implan logam menggabungkan kekuatan dan kekerasan dari logam, dan adanya sifat bioaktif dari material pelapis sehingga dapat menginduksi pertumbuhan jaringan tulang di sekitarnya dan terjadi pembentukan ikatan kimia. Selanjutnya, kehadiran HAp pada pelapisan mampu meningkatkan ketahanan korosi implan, dengan mengurangi pelepasan ion logam dan juga meningkatkan kekuatan pelapisan melalui ikatan kimia.
Menurunnya laju korosi pada paduan logam CoCrMo yang dilapisi HAp juga didukung oleh adanya pembentukan lapisan oksida pada material logam yang memainkan peranan penting sebagai inhibitor terhadap pelepasan ion logam. Lapisan oksida pasif dapat terbentuk pada paduan logam CoCrMo dalam larutan biologis. Khromium mampu membentuk lapisan oksida pasif Cr2O3 pada paduan
logam CoCrMo. Lapisan oksida pasif Cr2O3 pada paduan logam CoCrMo
bertindak sebagai pembatas yang efektif pada korosi, meningkatkan ketahanan dari perilaku transfernya muatan yang mengakibatkan korosi antar muka (Hsu et al. 2005). Oleh karena itu, lapisan oksida Cr2O3 yang terbentuk dapat
meningkatkan ketahanan korosi pada logam. Hal ini didukung pula dari hasil analisis yang dilakukan oleh Effendi dan Jahja (2006) yaitu hasil analisis EDX dan XRD menunjukkan kemungkinan adanya oksida krom.
Hasil UjiCytocompatibility In vitroSel Endotel
Pengujian cytocompatibility dilakukan secara in vitro menggunakan media kultur sel endotel. Uji ini bertujuan untuk menentukan viabilitas sel ketika terjadi kontak langsung dengan sampel. Sel endotel dipilih karena sel endotel merupakan sel utama yang terlibat dalam pembentukan pembuluh darah. Hidroksiapatit diketahui mampu meningkatkan proliferasi endotel yang dibutuhkan untuk terjadinya pembentukan pembuluh darah baru (angiogenesis) (Ruckeret al.2006). Proses pembentukan pembuluh darah baru sangat penting dalam proses perbaikan jaringan yang rusak, pertumbuhan jaringan, maupun proses penyembuhan. Oleh karena itu, paduan logam CoCrMo dilapisi HAp sebagai implan yang berfungsi mempercepat proses penyembuhan tidak boleh menyebabkan sitotoksisitas pada sel endotel.
Persen inhibisi menunjukkan terhambatnya pertumbuhan sel akibat terpapar oleh sampel. Persen inhibisi dinyatakan dalam dosis efektif median (ED50). Jika
persen inhibisi melebihi 50%, maka sampel tergolong toksik (Matsuura et al. 2000). Berdasarkan data persen inhibisi terhadap sel endotel (Tabel 1), paduan logam CoCrMo tanpa pelapisan tergolong toksik.
Tabel 1 Persen inhibisi viabilitas sel endotel terhadap sampel pada 72 jam pasca inkubasi
Sampel Inhibisi (%)
CoCrMo 100
CoCrMo dilapisi HAp 33.33
23
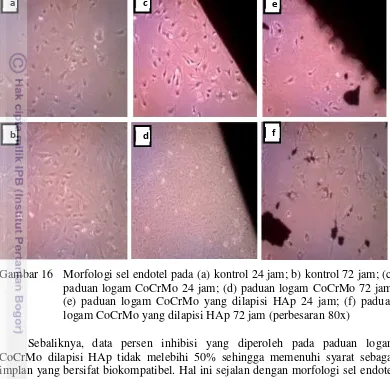
Hal ini dipertegas pula dari morfologi sel pasca inkubasi 72 jam pada sampel paduan logam CoCrMo (Gambar 16d), yang menunjukkan kematian sel hampir keseluruhan dibandingkan dengan sel kontrol (Gambar 16a dan b) dan paduan logam CoCrMo pengamatan 24 jam (Gambar 16c). Hal ini dapat disebabkan paduan logam CoCrMo mengalami pelepasan ion logam CoCrMo.
Gambar 16 Morfologi sel endotel pada (a) kontrol 24 jam; b) kontrol 72 jam; (c) paduan logam CoCrMo 24 jam; (d) paduan logam CoCrMo 72 jam; (e) paduan logam CoCrMo yang dilapisi HAp 24 jam; (f) paduan logam CoCrMo yang dilapisi HAp 72 jam (perbesaran 80x)
Sebaliknya, data persen inhibisi yang diperoleh pada paduan logam CoCrMo dilapisi HAp tidak melebihi 50% sehingga memenuhi syarat sebagai implan yang bersifat biokompatibel. Hal ini sejalan dengan morfologi sel endotel pada paduan logam CoCrMo yang dilapisi HAp pengamatan 24 jam (Gambar 16e) dan 72 jam setelah inkubasi (Gambar 16f), menunjukkan sel endotel dapat hidup dan telah beradaptasi dengan adanya sampel. Data perhitungan uji kultur sel endotel dapat dilihat pada Lampiran 8.
Hasil cytocompatibility ini sesuai dengan meningkatnya ketahanan korosi dari paduan logam CoCrMo yang dilapisi HAp. Sebelumnya, studi sitotoksisitas in vitro pada viabilitas sel L-929 untuk paduan ZK60 (Mg-5.5wt%Zn-0.5wt%Zr) juga melaporkan bahwa dengan meningkatnya ketahanan korosi dari logam yang dilapisi HAp, maka sifat cytocompatibility juga meningkat dibandingkan dengan yang tidak dilapisi HAp (Yang et al. 2015). Selain itu, tingginya derajat kristalinitas HAp yang dihasilkan juga membuktikan pengaruhnya pada respon biologis sel yang baik pada ujiin vitro. Yanget al.(2015) juga melaporkan bahwa paduan ZK60 yang dilapisi HAp memiliki respon sel biologis yang sangat baik secara in vitro seiring dengan meningkatnya bioaktivitas, yang disebabkan oleh
e c
a
f d
24
derajat kristalinitas tinggi dari HAp yang dihasilkan. Viabilitas sel juga dilaporkan oleh Huan et al. (2010) yang mengamati bahwa ketahanan korosi yang rendah mengakibatkan nilai pH meningkat sehingga terjadi korosi, yang akhirnya berdampak pada berkurangnya viabilitas sel.
5 SIMPULAN DAN SARAN
Simpulan
Kandungan kalsium dari limbah cangkang kerang ale-ale dapat dimanfaatkan sebagai starting material dalam sintesis hidroksiapatit. Hasil sintesis dengan metode presipitasi double stirring menunjukkan hidroksiapatit yang diperoleh merupakan fasa tunggal hidroksiapatit. Hasil pelapisan hidroksiapatit pada paduan logam CoCrMo menggunakan metode elektroforesis deposisi menunjukkan lapisan yang merata dan tidak ditemukan keretakan. Hasil analisis Difraksi Sinar-X hidroksiapatit pada paduan logam CoCrMo juga diperoleh fasa tunggal hidroksiapatit. Ketahanan korosi paduan logam CoCrMo yang dilapisi hidroksiapatit memiliki sifat biokompatibel lebih baik dibandingkan paduan logam CoCrMo tanpa pelapisan. Uji cytocompatibility in vitro menunjukkan paduan logam CoCrMo yang dilapisi hidroksiapatit, tidak menyebabkan sitotoksisitas pada kultur sel endotelCalf Pulmonary Artery Endothelium(CPAE) (ATCC-CCL 209) dengan persen inhibisi 33.33%. Berdasarkan ketahanan korosi dan sifatcytocompatibilityini, paduan logam CoCrMo yang dilapisi hidroksiapatit berpotensi sebagai implan biokompatibel untuk aplikasi implan tulang.
Saran
25
DAFTAR PUSTAKA
Adya N, Alam M, Ravindranath T, Mubeen A, Saluja B. 2005. Corrosion in titanium dental implants: literature review. Journal of Indian Prosthodontic Society. 5(3): 126-131.
Aoki, Hideki. 1991. Science and Medical Application of Hydroxyapatite. JAAS: Tokyo, Japan.
[APHA; AWWA; WEF] American Public Health Association; American Water Works Association; Water Environment Federation (US). 2005. Standard methods for the examination of water and wastewater. 21st Ed. Washington DC (US): APHA.
Bastan FE, Ozbek YY. 2013. Producting antibacterial silver-doped hydroxyapatite powders with chemical precipitation and reshaping in a spray dryer. Materials and Technology. 47(4): 431–434.
Bauer S, Schmuki P, Mark K, Park J. 2013. Engineering biocompatible implant surfaces part I : materials and surfaces.Progress in Materials Science. 58:261– 326.doi:10.1016/j. pmatsci.2012.09.001.
Bertazzo S, Zambuzzi W, Campos D, Ogeda T. 2010. Hydroxyapatite surface solubility and effect on cell adhesion. Colloids and Surfaces B Biointerfaces. 78(2):177-184.doi: 10.1016/j.colsurfb.2010.02.027.
Besra L, Liu M. 2007. A review on fundamentals and applications of electrophoretic deposition (EPD). Progress in Materials Science. 52:1– 61.doi:10.1016/j.pmatsci.2006.07.001.
Boccaccini AR, Keim S, Ma R, Li Y, Zhitomirsky I. 2010. Electrophoretic deposition of biomaterials. Journal of the Royal Society Interface. 7:S581– S613.doi: 10.1098/rsif.2010.0156.focus.
Bombac D, Brojan M, FajFar P, Kosel F, Turk R. 2007. Review of materials in medical application.RMZ–Materials and Geoenvironment.54(4): 471-499.
Castro Y, Duran A, Damborenea J, Conde A.2008. Electrochemical behaviour of silica basic hybrid coatings deposited on stainless steel by dipping and EPD. Electrochimica Acta. 53: 6008-6017.doi:10.1016/j.electacta.2008.03.042. Chairunisah R. 2011. Karakteristik asam amino daging kerang tahu (Meretrix
meretrix), kerang salju (Pholas dactylus) dan keong macan (Babylonia spirata). [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Chow LC. 2009. Next generation calcium phosphate-based biomaterials. Dental Materials Journal.28(1):1–10.
Corni I, Ryan MP, Boccaccini AR. 2008. Electrophoretic deposition: from traditional ceramics to nanotechnology. Journal of The European Ceramic Society.28:1353-1367.doi: 10.1016/j.jeurceramsoc.2007.12.011.
Cortez PM, Guiterrez GV. 2004. Electrophoretic deposition of hydroxyapatite submicron particles at high voltages. Materials Letters. 58:1336-1339.doi:10.1016/j.matlet.2003.09.024.
Dedourkova T, Zelenka J, Zelenkova M, Benes L, Svoboda L. 2012. Synthesis of sphere-like nanoparticles of hydroxyapatite. Procedia Engineering. 42:1816– 1821.doi: 10.1016/j.proeng.2012.07.576.