PENYALUT TERHADAP STABILITAS EMULSI MINYAK
CENGKEH DALAM AIR
AZMI SYAHRIAN ZEHN
DEPARTEMEN TEKNIK MESIN DAN BIOSISTEM
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Pengaruh Kecepatan Homogenisasi dan Jenis Penyalut Terhadap Stabilitas Emulsi Minyak Cengkeh dalam Air adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Maret 2016
AZMI SYAHRIAN ZEHN. Pengaruh Kecepatan Homogenisasi dan Jenis Penyalut Terhadap Stabilitas Emulsi Minyak dalam Air. Dibimbing oleh SUTRISNO dan NANIK PURWANTI.
Minyak cengkeh memiliki peluang yang besar pemanfaatannya dalam bidang pangan tetapi keefektifan bahan aktif minyak cengkeh akan menurun bila bereaksi dengan komponen lainnya seperti lemak dan protein. Penelitian ini bertujuan untuk memformulasikan minyak cengkeh dalam bentuk emulsi minyak-dalam-air yang memiliki stabilitas paling baik dengan fase kontinyu berbasis polisakarida. Larutan kitosan dan natrium alginat merupakan fase kontinyu yang digunakan untuk membuat emmulsi dengan kecepatan homogenisasi yang berbeda (5,000 rpm, 10,000 rpm, 15,000 rpm dan 20,000 rpm). Emulsi minyak cengkeh yang terbentuk memiliki karakteristik warna putih susu homogen untuk semua sampel. Stabilitas emulsi dapat diketahui dari ada tidaknya sedimentasi, penampakan emulsi, ukuran emulsi, dan banyaknya minyak yang keluar dari emulsi. Ukuran emulsi minyak cengkeh berdasarkan penelitian ini adalah 1.87 –2.20 µm untuk emulsi berpenyalut kitosan dan 2.14–100.71 µm untuk emulsi berpenyalut natrium alginat. Jika kecepatan homogenisasi meningkat, maka ukuran emulsi yang terbentuk akan semakin kecil. Emulsi yang optimum tercapai pada kecepatan homogenisasi 10,000 rpm karena memiliki stabilitas emulsi yang bagus selama penyimpanan.
Kata kunci : minyak cengkeh, emulsi, kitosan, natrium alginat
ABSTRACT
AZMI SYAHRIAN ZEHN. Effects of Homogenisation Speed and Coating Materials on the Stability of Clove Oil-in-Water Emulsion. Supervised by SUTRISNO and NANIK PURWANTI
Clove oil is a potential material to be applied in foods but its effectiveness decreases if clove oil functional compounds react with other components such as fat and protein. This research aimed to formulate clove oil in the form of oil-in-water emulsion that has a better stability using polysaccharide-based continous phase. Chitosan and sodium alginate solution were the continous phases and different speeds of homogenization (5,000 rpm, 10,000 rpm, 15,000 rpm, and 20,000 rpm) were applied to form the emulsion. Clove oil-in-water emulsion has milky colour. The emulsion stability was detected from its appearance, sedimentation, emulsion size, and release of oil from the emulsion. The size of clove oil emulsion size was 1.87 –2.20 µm when chitosan was used and 2.14 –100.71 µm when sodium alginat was used. The size was smaller with increasing homogenisation speed. The most stable emulsion during storage was obtained by using a homogenization speed of 10,000 rpm.
PENYALUT TERHADAP STABILITAS EMULSI MINYAK
CENGKEH DALAM AIR
AZMI SYAHRIAN ZEHN
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Teknik
Pada
Departemen Teknik Mesin dan Biosistem
DEPARTEMEN TEKNIK MESIN DAN BIOSISTEM
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
Judul : Pengaruh Kecepatan Homogenisasi dan Jenis Penyalut Terhadap Stabilitas Emulsi Minyak Cengkeh dalam Air
Nama : Azmi Syahrian Zehn NIM : F14110095
Disetujui oleh
Prof Dr Ir Sutrisno, MAgr Dr Nanik Purwanti, STP, MSc Pembimbing I Pembimbing II
Diketahui oleh
Dr Ir Desrial M.Eng Ketua Departemen
PRAKATA
Puji syukur penulis ucapkan kepada Allah Yang Maha Esa karena rahmat dan karunia-Nya penulis dapat menyelesaikan skripsi yang berjudul Pengaruh Kecepatan Homogenisasi dan Jenis Penyalut Terhadap Stabilitas Emulsi Minyak Cengkeh dalam Air. Penelitian dilaksanakan sejak bulan Mei 2015 hingga bulan Oktober 2015. Selama penyusunan skripsi ini penulis ingin mengucapkan terima kasih kepada
1. Prof. Dr. Ir. Sutrisno, M.Agr dan Ibu Dr Nanik Purwanti, S.TP, M.Sc selaku pembimbing yang telah memberikan bimbingan dan arahan pada penulis.
2. Ir. Erfin Yundra Febrianto, M.T dan Eka Dian S.Si selaku pembimbing penelitian di Pusat Penelitian Ilmu Pengetahuan dan Teknologi (PUSPIPTEK) Lembaga Ilmu Pengetahuan Indonesia (LIPI) Fisika dan Kimia, atas bimbingannya selama penelitian.
3. Bapak Leo Senobroto dari PT Indesso yang telah menyumbangkan Bapak Jamil selaku teknisi di Badan Pengkajian dan Penerapan Teknologi (BPPT), dan Bapak Solahudin selaku teknisi di LIPI Kimia Serpong yang telah membantu penulis selama penelitian.
6. Teman satu bimbingan Riza, Silvi, Ugik, Putra, Mba Kania, Mirwan, dan teman-teman Regenboog 48 atas bantuan dan dukungannya.
7. Keluarga Forum komunikasi mahasiswa (Forkoma) Kebumen atas doa dan dukungannya kepada penulis.
8. Semua pihak yang secara langsung maupun tidak langsung telah membantu penulis selama penelitian.
Penulis menyadari bahwa dalam karya ilmiah ini masih belum benar-benar sempurna, oleh karena itu kritik dan saran yang bersifat membangun dari semua pihak sangat diharapkan. Penulis berharap karya ilmiah ini nantinya dapat memberi manfaat bagi semua pihak.
Bogor, Maret 2016
DAFTAR ISI
1. Komposisi senyawa minyak cengkeh 15
2. Ukuran diameter rata-rata emulsi minyak cengkeh pada hari ke-0 18 3. Ukuran diameter rata-rata emulsi minyak cengkeh selama penyimpanan 21
DAFTAR GAMBAR
6. Gas Chromathography Mass Spectometry (GCMS) 8
7. Mikropipet 8
8. Timbangan digital 8
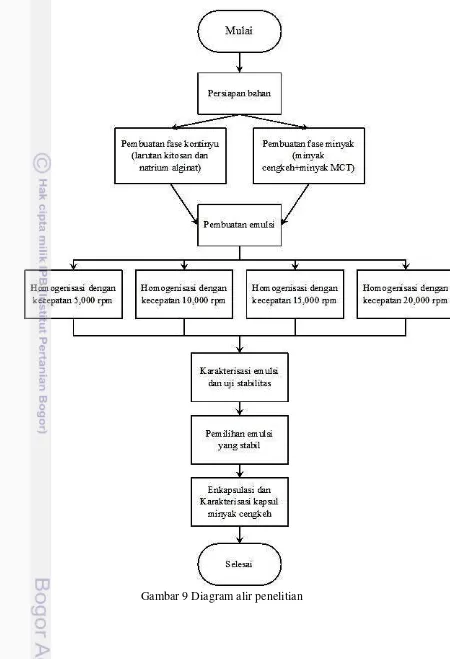
9. Diagram alir penelitian 13
11. Karakteristik emulsi minyak cengkeh berpenyalut (a) kitosan dan (b) natrium alginat
15
12. Penampakan mikroskopi emulsi minyak cengkeh berpenyalut (a) kitosan dan (b) natrium alginat
16
13. Penampakan emulsi minyak cengkeh berpenyalut (a) kitosan dan (b) natrium alginat
16
14. Emulsi minyak cengkeh berpenyalut kitosan pada kecepatan (a) 5,000 rpm, (b) 10,000 rpm, (c) 15,000 rpm, dan (d) 20,000 rpm.
17
15. Emulsi minyak cengkeh berpenyalut natrium alginat dengan kecepatan (a) 5,000 rpm, (b) 10,000 rpm, (c) 15,000 rpm, dan (d) 20,000 rpm.
17
16. Penampakan emulsi minyak cengkeh berpenyalut kitosan pada kecepatan homogenisasi 10,000 rpm selama penyimpanan
19
17. Penampakan emulsi minyak cengkeh berpenyalut natrium alginat pada kecepatan homogenisasi 10,000 rpm selama penyimpanan
20
18. Perubahan ukuran emulsi pada hari ke-0 dan ke-28 pada emulsi minyak cengkeh berpenyalut kitosan
20
19. Perubahan ukuran emulsi pada hari ke-0 dan ke-28 pada emulsi minyak cengkeh berpenyalut natrium alginat
21
20. Foto mikroskopi kapsul minyak cengkeh dengan penyalut (a) kitosan dan (b) natrium alginat pada perbesaran 10x.
23
21. Kapsul emulsi minyak cengkeh berpenyalut kitosan (a,b) dan natrium alginat (c,d)
23
22. Kapul kitosan dan natrium alginat menurut literatur 24
DAFTAR LAMPIRAN
1. Komposisi senyawa minyak cengkeh 28
2. Tinggi sedimentasi emulsi minyak cengkeh 29
3. Distribusi ukuran diameter rata-rata emulsi minyak cengkeh 30
4. Span emulsi minyak cengkeh 31
5. Stabilitas emulsi minyak cengkeh 32
6. Penampakan visual emulsi minyak cengkeh berpenyalut kitosan 33 7. Penampakan visual emulsi minyak cengkeh berpenyalut natrium
alginat
34
8. Penampakan mikroskopi emulsi minyak cengkeh berpenyalut kitosan batch 1
35
9. Penampakan mikroskopi emulsi minyak cengkeh berpenyalut kitosan batch 2
36
10. Penampakan mikroskopi emulsi minyak cengkeh berpenyalut natrium batch 1
37
11. Penampakan mikroskopi emulsi minyak cengkeh berpenyalut natrium alginat batch 2
38
12. Kurva distribusi ukuran partikel emulsi minyak cengkeh berpenyalut kitosan
39
13. Kurva distribusi ukuran partikel emulsi minyak cengkeh berpenyalut natrium alginat
40
16. Grafik prosentase minyak yang keluar dari emulsi selama penyimpanan
43
17. Peristiwa sedimentasi dan creaming pada emulsi minyak cengkeh 44 18. Tahapan peristiwa koalesen yang terjadi pada emulsi minyak
cengkeh
45
19. Penampakan kapsul minyak cengkeh 46
PENDAHULUAN
Latar Belakang
Tanaman cengkeh (Syzygium caryophyllum atau Eugenia caryophyllara
atau Syzygium aromaticum atau Eugenia aromatica) termasuk dalam familia
myrtaceae yang tersebar luas di Indonesia, Malaysia, Pulau Madagaskar dan Tanzania. Tanaman cengkeh mempunyai sifat yang sangat khas karena semua bagian mengandung minyak, mulai dari dahan, ranting, sampai bunga dan daun. Kadar minyak cengkeh bervariasi pada setiap bagian dengan kadar minyak yang paling tinggi terdapat pada bagian bunga (Fitri 2006). Kandungan minyak atsiri di dalam bunga cengkeh mencapai 21.3% dengan kadar eugenol antara 78-95%, dari tangkai atau gagang bunga mencapai 6% dengan kadar eugenol antara 89-95%, dan dari daun cengkeh mencapai 2-3% dengan kadar eugenol mencapai 80-85% (Hadi 2012).
Aplikasi minyak cengkeh antara lain digunakan dalam parfum, perasa (flavoring), formulasi obat oles anti nyamuk, penyerap ultra violet (UV), analgesik, antifungi, dan antiseptik (Lee dan Shibamoto 2001 dan Alma et al. 2007). Dalam bidang kesehatan, minyak cengkeh dapat digunakan sebagai antistres, antimikroba, antiperadangan, antigiardial, kebutuhan pembiusan, antibisul dan sebagainya (Charles 2013). Minyak cengkeh diketahui dapat juga digunakan sebagai antioksidan. Keaktifan antioksidan minyak cengkeh lebih tinggi jika dibandingkan dengan antioksidan yang terkandung dalam lemon, anggur, dan ketumbar. Minyak cengkeh juga memiliki kemampuan yang lebih baik dalam menangkal radikal bebas dan terbaik kedua setelah vitamin C dibandingkan dengan 45 jenis minyak atsiri lainnya (Kim 2011).
Di bidang pangan, minyak cengkeh telah diterapkan pada daging, susu serta minyak goreng (Chatterjee dan Bhattacharjee 2013). Fungsi aktif yang dimiliki minyak cengkeh memberi peluang yang besar untuk pemanfaatannya pada bidang pangan. Meskipun demikian, efektifitas minyak cengkeh menurun secara signifikan ketika berinteraksi dengan komponen makanan lainnya seperti lemak dan protein (Burt 2004). Untuk menaikkan efektifitas bahan aktifnya, minyak cengkeh harus direkayasa supaya dapat terlindungi dari berbagai interaksi dengan komponen makanan lain dan fungsi pelepasannya dapat dikendalikan. Hal ini dapat dilakukan dengan mengenkapsulasi minyak cengkeh dengan material lainnya dengan cara pengemulsian, pembentukan liposomes, atau lemak padat (solid lipid particles). Ukuran kapsul dapat diformulasikan dalam mikrometer, sub-mikro atau nanometer sesuai dengan kebutuhan. Memformulasikan bahan pangan dalam ukuran yang lebih kecil dapat meningkatkan kelarutannya dalam air, dan rasio luas permukaan-ke-volume menjadi besar.
pengisi eugenol dan carvacol yang memiliki ukuran 80 nm kurang efektif untuk menghambat dan menonaktifkan mikroorganisme pembusuk makanan daripada emulsi dengan ukuran 3 µm. Eugenol adalah bahan aktif utama di dalam minyak cengkeh. Hal ini bertentangan dengan hipotesa yang telah dibuat sebelumnya bahwa aktivitas antimikroba komponen minyak atsiri yang berbentuk emulsi dapat meningkat jika ukuran emulsi menurun.
Penelitian ini bertujuan untuk mengembangkan enkapsulasi minyak cengkeh dengan skala mikrometer dengan penyalut yang memiliki muatan yang berbeda. Penelitian ini dirancang berdasarkan hipotesa dari Terjung et al. (2012) bahwa emulsi bermuatan positif akan berinteraksi dengan sel mikroba bermuatan negatif, dan sebaliknya, sehingga efektifitas bahan antimikroba dalam emulsi dapat meningkat. Namun demikian, penelitian ini hanya dirancang untuk mempelajari stabilitas emulsi minyak cengkeh dalam fase kontinyu yang memiliki muatan berbeda. Minyak cengkeh dibentuk menjadi emulsi minyak dalam air (oil-in-water, O/W) menggunakan teknik emulsifikasi konvensional. Efek kecepatan homogenisasi terhadap emulsi yang dihasilkan juga dipelajari.
Perumusan Masalah
Berdasarkan penelitian Terjung et al. (2011), emulsi dengan bahan pengisi eugenoldan carvacol dengan ukuran 80 nm kurang efektif untuk menghambat dan menonaktifkan mikroorganisme pembusuk makanan daripada emulsi dengan ukuran 3 µm. Hal ini menunjukkan bahwa tidak semua partikel yang memiliki ukuran lebih kecil mempunyai kefektifan yang lebih baik dibandingkan dengan partikel berukuran besar. Adapun pengaruh dari bahan salut yang memiliki muatan menyebabkan keefektifan dalam menghambat pertumbuhan bakteri dapat menurun ataupun meningkat.
Tujuan Penelitian
TINJAUAN PUSTAKA
Minyak Cengkeh
Cengkeh merupakan salah satu tanaman perkebunan penghasil minyak atsiri yang dapat digunakan dalam industri farmasi maupun industri pangan dan merupakan tanaman asli Indonesia yang kurang lebih 95% diusahakan oleh rakyat dalam bentuk perkebunan rakyat di seluruh provinsi. Cengkeh merupakan tanaman rempah yang banyak digunakan sebagai bumbu masakan pedas di negara-negara Eropa.
Ekstraksi minyak cengkeh dilakukan pada bagian bunga, tangkai bunga dan daun. Bagian yang paling ekonomis dari ketiga bagian tersebut adalah bagian daunnya, sehingga jenis minyak cengkeh yang paling banyak diperjual belikan adalah minyak daun cengkeh (Nurdjanah et al. 1990).
Minyak daun cengkeh biasanya diperoleh dari daun cengkeh yang telah gugur. Minyak yang dihasilkan mengandung eugenol antara 80-88% dengan kadar eugenol asetat yang rendah tetapi kadar coryopyllene yang tinggi. Penyulingan daun yang berkadar air sekitar 7-12% yang dilakukan pada tangki stainless steel volume 100 liter selama 8 jam, menghasilkan minyak dengan rendemen 3.5% dan total eugenol 76.8% (Nurdjanah et al. 1990).
Sumber ekstraksi minyak cengkeh diantaranya yaitu : (1) Pucuk bunga yang menghasilkan bud oil, terdiri dari 60-90% eugenol, eugenyl acetate, caryophyllene
dan komponen lainnya dalam jumlah kecil, (2) Daun yang menghasilkan leaf oil
terdiri dari 82-88% eugenol, tidak terdeteksi adanya eugenyl acetate dan komponen lainnya dalam jumlah kecil, (3) Ranting menghasilkan stem oil terdiri dari 90-95% eugenol dan beberapa komponen lainnya dalam jumlah kecil (Weiss 1997).
Emulsifikasi
Emulsifikasi adalah suatu proses pencampuran yang melibatkan antara dua cairan atau senyawa yang secara alami tidak dapat bercampur satu sama lain (Ginting 2006). Hasil dari proses ini disebut emulsi. Emulsi pada prinsipnya melibatkan dua fase yaitu fase terdispersi dan fase pendispersi/ fase kontinyu. Berdasarkan fase terdispersinya terdapat tiga jenis emulsi, yaitu emulsi minyak dalam air, emulsi air dalam minyak dan emulsi ganda. Emulsi minyak dalam air dibuat dengan mendispersikan fase minyak ke dalam fase air. Emulsi air dalam minyak dibuat mendispersikan fase air ke dalam fase minyak. Emulsi ganda merupakan emulsi yang dapat tersusun atas air-minyak-air ataupun minyak-air-minyak (Sumardjo et al. 2008).
Ada beberapa teori yang berhubungan dengan sistem emulsi, antara lain Teori Tegangan Permukaan, Teori Oriented-Wedge dan Teori Film Pastis. Tegangan permukaan terjadi bila cairan mengalami kontak dengan cairan kedua yang tidak larut dan tidak saling bercampur. Zat-zat yang dapat menurunkan tegangan permukaan disebut dengan zat aktif permukaan (surfaktan) atau zat pembasah atau zat pengemulsi (emulsifier). Penurunan tegangan permukaan menyebabkan gaya tarik-menarik antar molekul dari masing-masing cairan akan berkurang dan kedua cairan akan dapat bercampur. Teori Oriented-Wedge
menjelaskan fenomena terbentuknya emulsi karena adanya kelarutan selektif dari bagian emulsifier, ada bagian yang bersifat mudah larut dalam air (hidrofil) dan ada bagian mudah larut dalam minyak (lifolil). Teori Film Plastis menjelaskan bahwa emulsifier mengendap pada permukaan masing-masing butiran fase dispersi dalam bentuk film yang plastis. Lapisan tersebut mencegah kontak dan bersatunya fase terdispersi. Makin kuat dan makin lunak lapisan tersebut, makin besar dan stabil emulsinya (Lachman 1994).
Beberapa teknik emulsifikasi yang digunakan untuk memproduksi emulsi minyak-dalam-air (O/W) yaitu emulsifikasi mekanik/ konvensional, emulsifikasi membran, emulsifikasi mikrochanel (microchannel (MC) emulsification), dan penggunaan perangkat mikrofluida lainnya seperti T, Y atau cross junction, atau sistem yang didesain sehingga emulsi terbentuk dengan sendirinya misalnya Edge-based Droplet Generation (EDGE) (Purwanti et al., 2015). Emulsifikasi mekanik merupakan teknik konvensional untuk menghasilkan emulsi dengan menggunakan peralatan seperti high-speedmixer, colloid mills, high-pressure valve atau ultrasonik homogenizer dan mikro fluidasi (McClement 2005).
Enkapsulasi
Enkapsulasi merupakan proses pembuatan kapsul yang biasanya mengandung suatu bahan aktif untuk keperluan tertentu. Proses enkapsulasi digunakan untuk melindungi suatu bahan aktif agar tetap tersimpan dalam keadaan baik dan kemudian zat tersebut dapat dilepaskan pada kondisi tertentu ketika dibutuhkan atau ketika mencapai target yang diinginkan. Ide dasar enkapsulasi berasal dari sel, yaitu permeabilitas selektif membran sel memberikan perlindungan terhadap inti sel dari kondisi lingkungan yang berubah-ubah dan berperan dalam pengaturan metabolisme (Desmawarni 2007).
Berdasarkan ukurannya, kapsul yang berupa partikel yang telah dienkapsulasi dapat dikategorikan menjadi tiga jenis yaitu makrokapsul bila partikel berukuran lebih besar dari 5,000 µm, mikrokapsul berukuran antara 0.2-5,000 µm, dan nanokapsul yang berukuran lebih kecil dari 0.2 µm (Desmawarni 2007). Menurut Jackson dan Lee (1991) faktor yang mempengaruhi struktur dan ukuran mikrokapsul tergantung dari teknik pembuatan, jenis bahan inti, dan polimer (bahan penyalut) yang digunakan.
pengembang, warna dan garam. Salah satu yang terpenting dalam penerapan bahan aktif dalam kapsul adalah menjaga stabilitas bahan aktif tersebut. Salah satu caranya adalah membentuk produk kering yang dapat melindungi bahan aktif dalam kapsul dari penguapan, oksidasi, dan reaksi kimia (Desmawarni 2007).
Beberapa metode enkapsulasi yang telah dievaluasi dan dikomersialisasikan untuk penggunaan pada bahan pangan yaitu metode spray dying (pengering semprot), extrusion, dan spray cooling atau spray chilling. Selain itu, enkapsulasi dapat dilakukan juga dengan teknik koaservasi, kokristalisasi, dan polimerisasi antarmuka (Desmawarni 2007).
Teknik lain yang sering digunakan sebagai tahap awal enkapsulasi adalah emulsifikasi. Teknik ini digunakan dalam kasus zat aktif pangan yang larut dalam air atau minyak. Emulsi minyak-dalam-air dimana bahan penyalut tertentu dilarutkan dalam air dapat dikeringkan dengan beberapa metode pengeringan seperti spray atan freeze drying sehingga diperoleh sediaan kering emulsi/ bahan aktif yang terenkapsulasi (Desmawarni 2007).
Bahan Penyalut
Pada proses enkapsulasi, terdapat dua jenis bahan yang terlibat di dalamnya, yaitu inti dan penyalut. Inti merupakan zat yang akan dikapsulkan bisa berbentuk padat, gas atau cair yang mempunyai sifat permukaan hidrofil atau hidrofob (Durey
et al. 2009). Penyalut adalah zat yang digunakan untuk menyelimuti inti dengan tujuan tertentu. Menurut Gharshalloui et al. (2007), struktur dinding dari bahan penyalut umumnya dirancang untuk melindungi bahan inti dari faktor-faktor yang dapat menyebabkan kerusakan, mencegah terjadinya interaksi antar bahan inti dengan komponen lain, membatasi pergerakan komponen volatil, dan juga mengontrol pelepasan bahan inti pada kondisi yang diinginkan.
Bahan penyalut yang biasanya digunakan bervariasi terdiri dari karbohidrat, protein, lemak, gum dan selulosa. Bahan penyalut untuk enkapsulsi flavor harus memiliki sifat tidak bereaksi dengan inti, berada dalam bentuk yang mudah ditangani, memiliki viskositas rendah pada konsentrasi tinggi, memberikan perlindungan maksimal inti dari faktor eksternal dan dapat menstabilkan emulsi (Rahmalia 2008). Penelitian ini menggunakan minyak cengkeh sebagai bahan inti, dan penyalut yang digunakan adalah kitosan dan natrium alginat.
Kitosan
Kitosan merupakan aminopolisakarida yang terdiri dari kopolier glukosamin dan N-asetil glukosammin. Bahan ini tidak berbau, berupa serbuk atau serpihan berwarna krim sampai putih. Kitosan merupakan hasil deasetilasi kitin, yaitu modifikasi struktur kitin melalui hidrolisis menggunakan larutan basa secara biokimia. Kitosan tersusun atas (1,4)-2-amino-2-deoksi-D-gukosa yang saling berikatan β. Kitosan berbentuk padatan amorf dengan rumus molekul (C6H11NO4)n
aseton. Kitosan akan larut dalam asam organik seperti HCL dan HNO3 pada
konsentrasi 1.1% tetapi tidak larut pada konsentrasi 10%. Sifat kelarutan ini dipengaruhi oleh bobot molekul dan derajat deasetilasi (Amelia 2007). Derajat polisakarida yang penting untuk mendapatkan kelarutan produk yang baik adalah 80-85%. Kitosan secara komersial terdapat dalam berbagai tipe dan grade dengan beragam molekul (antara 10,000 sampai 1,000,000 dalton), beragam derajat dan viskositas (Rowe et al. 2009).
Kitosan memiliki sifat non-toksik, biokompatibel dan biodegradibel. Kitosan memiliki struktur yang mirip dengan selulosa dan memiliki kemampuan membentuk gel dalam suasana asam (seperti dalam lambung) (Amelia 2007). Karena kemampuan ini, kitosan dapat dimanfaatkan untuk membuat sediaan lepas lambat (contoh: pada obat) (Pawestrisini 2011). Mutu kitosan tergantung pada sumber (asal), derajat deasetilasi (DD), distribusi gugus asetil, gugus amino, panjang rantai dan distribusi bobot molekul (BM) (Amelia 2007). Parameter kualitas kitosan sangat bergantung pada derajat deasetilasinya (DD), semakin besar atau tinggi maka kualitas akan semakin tinggi (Utami 2012).
Natrium Alginat
Alginat merupakan hidrokoloid alami yang berasal dari ekstrak ganggang coklat. Senyawa alginat merupakan suatu polimer linier yang terdiri atas dua satuan yang monomerik, β-D-asam monurolat dan α-L-asam gluronik (Wukirsari 2006). Alginat komersial memiliki bobot molekul sekitar 32,000-200,000 dan derajat polimerisasi sebesar 180-930 (Nussinovitch 1997). Garam alginat larut dalam air, tetapi mengendap dan membentuk gel pada pH lebih dari 3. Alginat dalam garam natrium mudah didapatkan, bersifat biokompatibel, tidak beracun dan tidak karsinogen (Brown et al. 2004).
Natrium alginat berupa serbuk berwarna putih hingga kuning pucat, tidak berbau, tidak berasa dan larut dalam air membentuk larutan koloidal. Larutan 1% natrium alginat (b/v) memiliki pH sekitar 7.2. Natrium alginat tidak larut dalam etanol (95%), eter, kloroform, campuran metanol dan air dengan kandungan etanol lebih besar dari 30%, dan juga larutan asam encer dengan pH kurang dari 3 (Rowe Sheskey and Owen 2006).
Natrum alginat tersedia secara komersial dalam berbagai tingkat viskositas. Viskositas larutan natrium alginat tergantung pada konsentrasi, pH dan temperatur. Natrium alginat tidak kompatibel dengan derivat akridin, kristal violet, fenil merkuri asetat dan nitrat, garam kalsium, logam berat, dan etanol dengan konsentrasi lebih dari 5% (Rowe Sheskey and Owen 2006).
Proses enkapsulasi menggunakan natrium alginat yang dicampur dengan larutan CaCl2 menyebabkan Ca2+ bereaksi dengan monovalen anion karboksilat
alginat membentuk jaringan tiga dimensi. Hal tersebut menyebabkan proses gelatinisasi semakin cepat sehingga viskositas kapsul yang dihasilkan semakin baik (Winarno 1996). Winarno (1996) lebih lanjut menjelaskan Ca2+ memiliki dua ion positif yang akan bergabung dalam dua gugus karboksil dan molekul algin, disamping itu ikatan sekunder mungkin saja terjadi diantara ion kalsium sendiri dan gugus hidroksil polimer alginat. Hal tersebut yang menyebabkan penambahan natrium alginat dengan larutan CaCl2 menghasilkan gumpalan dengan ikatan
METODOLOGI
Bahan
Bahan yang digunakan adalah minyak cengkeh disediakan oleh PT Indesso Aroma, Kitosan (Sigma Aldrich, USA), Natrium Alginat (Wako, Kyoto), Tween 80 (Merck, German), Asam asetat (Merck, German), Kalsium Klorida (Merck, German), Hexane (Merck, German) dan aquades.
Alat
Alat yang digunakan adalah seperangkat particle size analyzer (CILAS 1190, USA) pada Gambar 1, magnetic stirer (Toorey Pines Scientific, USA)pada Gambar 2, homogenizer (IKA Ultra-Turrax T25, Jerman) pada Gambar 3, centrifuge
(SORVAL Fresco, USA) pada Gambar 4, mikroskop digital (Best Scope, China) pada Gambar 5 yang dilengkapi dengan sofwate PAX IT untuk akuisisi foto sampel,
Gas Chromatograhpy Mass Spectometry (GCMS) (Agilent Technology 7890B, 5977A USA) pada Gambar 6 yang dilengkapi dengan kolom DB-5MS U1 (panjang 30 m, diameter 0.25 mm Norrowbore, tebal film 0.25 µm, batas temperatur -60oC sampai 325 oC atau 350 oC) (Agilent Technology ,USA) , micropipette (Finnpipette, USA) pada Gambar 7, dan timbangan digital (Henherr scale, China) pada Gambar 8.
Peralatan laboratorium lain yang digunakan dalam penelitian ini adalah gelas piala, gelas beaker, pipet, vial tube, sudip dan termometer (Lampiran 20).
Gambar 4 Homogenizer
Gambar 4 Centrifuge
Gambar 5 Mikroskop digital Gambar 6 GCMS
Gambar 7 Mikropipet
Gambar 8 Timbangan digital
Tempat Pelaksanaan Penelitian
Penelitian dilakukan selama 6 bulan dari bulan Mei - Oktober 2015 di beberapa laboratorium berikut:
1. Laboratorium Fisika, Lembaga Ilmu Pengetahuan Indonesia (LIPI) Fisika, Kawasan Puspiptek Serpong.
2. Laboratorium instrumen organik, Lembaga Ilmu Pengetahuan Indonesia (LIPI) Kimia, Kawasan Puspiptek Serpong.
Metode Penelitian
Pembuatan Larutan Fase Kontinyu
1. Larutan Kitosan (Hosseini 2013)
Larutan kitosan dibuat berdasarkan Hosseini (2013) dengan modifikasi sebagai berikut : 1% (b/b) kitosan dilarutkan ke dalam asam asetat 1% (b/b). Pengadukan dilakukan pada suhu ruang selama semalaman.
2. Larutan Natrium Alginat
Pembuatan larutan natrium alginat berdasarkan metode Chan (2013) dengan modifikasi. Natrium Alginat 2.5% (b/b) dilarutkan dalam aquades. Larutan didiamkan selama 24 jam untuk melepaskan busa atau gelembung sebelum digunakan.
Pembuatan Emulsi
Pembuatan emulsi minyak cengkeh dalam air secara umum merujuk pada metode Terjung et al. (2012) dengan beberapa modifikasi.
A. Fase terdispersi
Fase terdispersi merupakan fraksi minyak yang merupakan campuran minyak dengan medium chain triacylglyceride (MCT oil) dengan perbandingan 1:1. Campuran ini digunakan berdasarkan rekomendasi Terjung et al. (2012) untuk meningkatkan stabilitas emulsi yang mengandung minyak atsiri dengan kandungan phenol (eugenol).
B. Fase kontinyu
Fase kontinyu merupakan pelarut yang terdiri atas surfaktan dan larutan hidrokoloid, yaitu larutan kitosan dan larutan natrium alginat. Fase kontinyu dibuat dengan melarutkan 2% b/b Tween 80 yang berfungsi sebagai surfakan ke dalam setiap larutan di atas. Oleh karena itu, fase kontinyu mengandung 2% b/b Tween 80 dan 98% larutan hidrokoloid.
Proses Pembuatan Emulsi
Pembuatan emulsi dilakukan dengan melarutkan 10% w/w fase minyak ke dalam 90% w/w fase kontinyu. Mekanisme pelarutannya adalah sebagai berikut: 1. Rotor ultra-turrax diset sedemikian rupa sehingga berada di dalam fase
kontinyu kemudian proses homogenisasi dimulai dengan kecepetan yang sudah diset, yaitu 5,000; 10,000; 15,000; dan 20,000 rpm.
2. Minyak diteteskan sedikit demi sedikit sehingga semua terdispersi ke dalam fase kontinyu (dalam 1 menit).
3. Proses homogenisasi berlangsung selama 9 menit dihitung sejak seluruh fase terdispersi larut.
Emulsi dengan satu jenis penyalut dan satu kecepatan dibuat masing-masing 2 batch dan setiap batch dianalisa lebih lanjut masing-masing 3 kali untuk setiap jenis analisa.
Karakterisasi Minyak Cengkeh dan Eugenol menggunakan Gas
Chrmatography Mass Spectometry (GC-MS)
Karakterisasi minyak cengkeh dan eugenol dilakukan menggunakan GC-MS dengan menggunakan kolom non polar DB-5MS (30 m x ϕ 0.25 mm, ketebalan film 0.25 µm). Oven pada GC-MS diatur dengan kondisi sebagai berikut : suhu ditahan pada 40 oC selama 1 menit, kemudian dipanaskan dari suhu 40 oC sampai 280 oC
pada laju 10 oC/menit. Suhu injektor adalah 280 oC. Gas helium sebagai fase gerak disetel pada kecepatan alir 1 ml/menit dengan tekanan 7.0699 psi. Minyak cengkeh dan eugenol sebanyak 100 µl diencerkan dengan hexane 100 kali dan volume yang diinjeksikan pada kolom GC-MS sebanyak 0.2 µl. Komponen yang terkandung pada minyak cengkeh diidentifikasi berdasarkan perbandingan spektrum massa dari pustaka NIST14 dan W10N11 dalam perangkat Mass Spectrometry serta perbandingan terhadap hasil karakterisasi eugenol standar.
Uji Stabilitas Emulsi
A. Stabilitas Visual
Emulsi yang dibuat diamati selama 28 hari (ht), jika terjadi pemisahan fase
terdispersi atau fase kontinyu dari emulsi yang sudah terbentuk. Metode yang digunakan berdasarkan Sapei, Navqi & Rousseau (2012) dimana emulsi ditempatkan dalam gelas dengan ketinggian emulsi sekitar 6 cm dan disimpan dalam suhu 4 oC. Tinggi bagian yang memiliki warna berbeda dari warna emulsi
diukur setiap minggu dan dibandingkan dengan ketinggian emulsi awal (h0) untuk
menentukan stabilitas emulsi (S):
Observasi stabilitas secara visual dilakukan dengan membandingkan foto-foto emulsi di dalam gelas selama 28 hari penyimpanan dengan membandingkan penampakan emulsi yang dilihat menggunakan mikroskop. Penampakan emulsi divisualisasi dengan mikroskop cahaya menggunakan pembesaran 10x yang terhubung dengan Charge Couple Device (CCD) kamera dan software PAX IT untuk akuisisi gambar. Emulsi diamati dengan mikroskop pada suhu ruang (27 oC). Observasi-observasi secara visual di atas dilakukan pada hari ke-0, 7, 14, 21, dan 28 setelah pembuatan emulsi. Hari dimana emulsi dibuat dihitung sebagai hari ke-0.
B. Stabilitas Ukuran Emulsi
Ukuran emulsi diukur menggunakan teknik static light scattering
Nilai refractive index (RI) yang diinput sebagai parameter optikal selama pengukuran adalah: RI minyak = 1.5356, RI larutan kitosan = 1.5, RI larutan natrium alginate = 1.656 (ChemSpider). Pengukuran diameter emulsi dilakukan pada hari ke-0, 7, 14, 21 dan 28 setelah pembuatan emulsi.
C. Pengukuran Bahan Aktif yang Terlarut dalam Fase Kontinyu
Pengukuran konsentrasi bahan aktif yang terlarut ke dalam fase kontinyu dilakukan untuk mengetahui pelepasan bahan aktif dari dalam kapsul dalam kurun waktu tertentu. Pengukuran menggunakan Metode Terjung et al. (2012) dengan modifikasi. Partikel emulsi dipisahkan dari fase kontinyu dengan sentrifugasi. 2 mL emulsi disentrifugasi dengan kecepatan 10,000 kali gravitasi (g) selama 60 menit pada suhu 4 oC. Fase kontinyu, berupa cairan transparan, yang terpisah dari emulsi
diambil dengan pipet untuk dianalisa lebih lanjut kandungan minyak cengkehnya menggunakan GC-MS.
Sebanyak 100 µl fase kontinyu hasil pemisahan dari emulsi diencerkan dengan metanol 100 µl. Tujuan dari pengenceran dengan metanol adalah mengekstrak kandungan minyak yang terlarut dalamm fase kontinyu. Sebanyak 200 µl campuran tersebut kemudian diencerkan menggunakan normal hexane 1000 µl (larutan pertama). Campuran ini kemudian didiamkan selama satu jam dan disonikasi selama 20 menit. Dari larutan pertama, diambil 20 µl sampel dan diencerkan dengan hexane 980 µl sehingga terbentuk larutan kedua. Sampel dari larutan kedua diambil 10 µl dan diencerkan dengan hexane 990 µl. Total pengenceran yang dilakukan menggunakan hexane adalah 50,000 kali. Larutan terakhir merupakan larutan yang disiapkan untuk dianalisis menggunakan GC-MS. Sampel dari larutan terakhir dianalisis menggunakan GCMS dengan kolom non polar DB-5MS (30 m x ϕ 0.25 mm, ketebalan film 0.25 µm). Oven GC-MS diatur dengan kondisi sebagai berikut : suhu ditahan pada 40 oC selama 1 menit, kemudian dipanaskan dari suhu 40 oC sampai 280 oC pada laju 10 oC/menit. Suhu injektor adalah 280 oC. Gas helium sebagai fase gerak disetel pada kecepatan alir 1 ml/menit dengan tekanan 7.0699 psi. Volume yang diinjeksikan pada kolom GC-MS sebanyak 0.2 µl.
Pengukuran konsentrasi bahan aktif ini dilakukan pada hari ke-1 (24 jam setelah pembuatan emulsi), 8, 15, 22 dan 29 setelah pembuatan emulsi.
Pembuatan mikrokapsul dari emulsi minyak cengkeh dalam larutan hidrokoloid
Emulsi minyak cengkeh dalam air yang stabil berdasarkan uji stabilitas di atas disolidifikasi sehingga diperoleh mikrokapsul kering. Teknik solidifikasi menggunakan teknik yang berbeda tergantung bahan penyalut yang digunakan. A. Solidifikasi emulsi minyak cengkeh dalam larutan kitosan
(TPP) dipilih sebagai komponen bermuatan negatif karena kapsul yang terbuat dari kitosan-TPP dilaporkan aman untuk aplikasi bahan pangan (Hosseini et al. 2013). Mengacu pada metode Hosseini (2013), emulsi minyak cengkeh dengan larutan kitosan sebanyak 40 mL diaduk perlahan dengan magnetic stirrer kemudian larutan TPP dengan konsentrasi 0.4% w/w sebanyak 40 mL ditambahkan tetes demi tetes kedalam emulsi yang sedang diaduk. Pengadukan dilanjutkan selama 40 menit setelah semua larutan TPP ditambahkan ke dalam emulsi. Mikrokapsul yang terbentuk dipanen dengan cara sentrifugasi pada kecepatan 9,000 × g selama 30 menit pada suhu 4 °C. Mikrokapsul yang berbentuk endapan kemudian dipisahkan dari supernatant. Endapan yang terbentuk kemudian dikeringkan dengan oven vakum pada suhu 40 oC.
B. Solidifikasi emulsi minyak cengkeh dalam larutan natrium alginat
Solidifikasi emulsi minyak cengkeh dalam larutan natrium alginat dimana natrium alginat berfungsi sebagai penyalut juga didasarkan pada konsep ikatan komponen bermuatan negatif (alginat) dengan komponen bermuatan positif. CaCl2
dipilih sebagai komponen pengikat muatan negatif alginat dan solidifikasi emulsi menjadi mikrokapsul menggunakan metode Chan (2011).
Larutan CaCl2 dengan konsentrasi 1.5% b/b disiapkan dengan melarutkan
CaCl2 ke dalam aquades. 50 mL emulsi minyak cengkeh dalam natrium alginat
diekstrusi dengan jarum ukuran 0.5 mm dan diteteskan ke dalam kolam larutan CaCl2 sambil terus diaduk perlahan dengan magnetic stirer untuk menghindari
lengketnya partikel satu sama lain. Jarak antar ujung jarum dan permukaan larutan adalah 15 cm. Pengadukan dilakukan lebih lanjut selama 30 menit setelah semua emulsi terekstrusi ke dalam larutan CaCl2. Setelah mikrokapsul terbentuk,
mikrokapsul dicuci dengan aquades beberapa kali kemudian dikeringkan dengan oven vakum pada suhu 40 oC.
Karakterisasi Mikrokapsul
Morfologi kapsul minyak cengkeh yang tersalut kitosan dan natrium alginat diobservasi menggunakan Scanning Electron Microscopy (SEM). Kapsul dilapisi dengan emas pada evaporator vakum (Hitachi S03500, Japan) dan dianalisis dengan Silicon Drift X-Ray Detector (Horiba, X-maxN, Japan) pada 10-20 kVa dengan jarak kerja 5,2-5,5 mm.
Analisis Data
HASIL DAN PEMBAHASAN
Karakteristik Minyak Cengkeh dan Eugenol
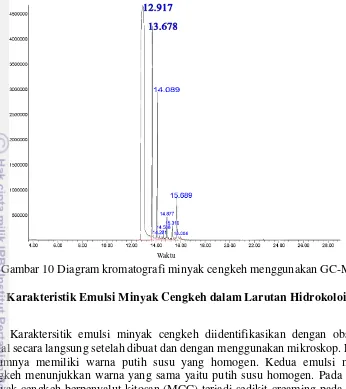
Karakterisasi minyak cengkeh menggunakan GC-MS bertujuan untuk mengetahui komponen-komponen yang terkandung dalam minyak cengkeh. Hasil karakterisasi minyak cengkeh dibandingkan dengan karakterisasi eugenol. Hal ini karena eugenol merupakan senyawa utama yang terkandung pada minyak cengkeh. Gambar 10 menunjukkan hasil analisasi Total Ionic Chromatogram (TIC) menggunakan GC-MS. Gambar tersebut menunjukkan puncak dari senyawa-senyawa yang terkandung dalam minyak cengkeh. Semakin tinggi puncak menandakan bahwa senyawa tersebut memiliki prosentase kandungan yang tinggi di dalam minyak cengkeh. Sedangkan waktu yang tertera merupakan waktu terbacanya senyawa tersebut.
Senyawa yang terdeteksi pada minyak cengkeh dengan metode GC-MS sebanyak 7 senyawa (Tabel 1). Penelitian sebelumnya menyebutkan bahwa minyak cengkeh mengandung 18 senyawa (Alma et al. 2007), 38 senyawa (Bhuiyan et al., 2010) dan 26 senyawa (Hossain et al. 2012). Perbedaan jumlah senyawa ini mungkin diakibatkan oleh perbedaan asal usul minyak cengkeh diperoleh (asal daerah/negara, kultivar, bagian yang diekstrak dan lain-lain). Berdasarkan National Institute of Standards and Tehnology (NIST) pada librari GCMS yang disajikan pada Tabel 1, tiga senyawa yang memiliki prosentase tertinggi yaitu eugenol,
caryophyllene dan humulen. Perbandingan senyawa yang terkadung pada minyak cengkeh yang diperoleh dala penelitian ini dengan penelitian lain dapat dilihat pada Lampiran 1.
Tabel 1 Komposisi senyawa minyak cengkeh
No. Nama Senyawa Waktu retensi
(menit)
Area (%)
1 Eugenol 12.917 72.463
2 Caryophyllene 13.678 14.750
3 Humulen 14.089 5.932
4 Germacrene D 14.291 0.514
5 Aromandendrene 14.588 0.801
6 Calamene 14.877 1.517
Gambar 10 Diagram kromatografi minyak cengkeh menggunakan GC-MS
Karakteristik Emulsi Minyak Cengkeh dalam Larutan Hidrokoloid
Karaktersitik emulsi minyak cengkeh diidentifikasikan dengan observasi visual secara langsung setelah dibuat dan dengan menggunakan mikroskop. Emulsi umumnya memiliki warna putih susu yang homogen. Kedua emulsi minyak cengkeh menunjukkan warna yang sama yaitu putih susu homogen. Pada emulsi minyak cengkeh berpenyalut kitosan (MCC) terjadi sedikit creaming pada bagian atas. Sebaliknya, pada emulsi berpenyalut Natrium Alginat (MCA) terjadi sedikit sedimentasi yang menyebabkan lapisan transparan tipis terdapat di bagian atas. Penampakan emulsi minyak cengkeh dapat dilihat pada Gambar 11.
a b
Gambar 11 Karakteristik emulsi minyak cengkeh berpenyalut (a) kitosan dan (b) natrium alginat
Emulsi minyak cengkeh memiliki karakteristik dengan bentuk bulat (spherical) bila diamati menggunakan mikroskop. Gambar 12 menunjukkan penampakan emulsi minyak cengkeh berpenyalut kitosan dan natrium alginat
Abundance
dilihat dengan mikroskop. Emulsi berbentuk bulat dengan minyak yang terdapat dibagian dalam dan lapisan luar merupakan lapisan penyalut (kitosan atau natrium alginat). Secara mikroskopis, emulsi MCC memiliki ukuran emulsi yang lebih besar dibandingkan dengan emulsi MCA. Ukuran emulsi MCA memiliki emulsi yang kecil dan seragam. Secara visual, ukuran-ukuran emulsi terlihat bervariasi yang menandakan polydispersity.
a b
Gambar 12 Penampakan mikroskopi emulsi minyak cengkeh berpenyalut (a) kitosan dan (b) natrium alginat
Pengaruh Kecepatan Homogenisasi pada Karaktersitik Emulsi
Penampakan emulsi minyak cengkeh dalam air yang dibuat dengan berbagai kecepatan homogenisasi pada hari ke-0, baik menggunakan penyalut kitosan dan natrium alginat, ditunjukkan pada Gambar 13. Secara umum, emulsi MCC berwarna homogen yaitu putih susu yang menandakan emulsi yang stabil. Semua emulsi MCA menunjukkan lapisan tipis transparan di bagian atas dengan warna yang berbeda dari emulsi keseluruhan. Lapisan ini menunjukkan adanya sedimentasi yang terjadi secara spontan setelah emulsi terbentuk. Tinggi lapisan yang mengindikasikan terjadinya sedimentasi pada emulsi minyak cengkeh dapat dilihat pada Lampiran 2. Pada hari ke-0, emulsi MCA memiliki ketinggian lapisan tipis transparan yang berbeda-beda untuk masing-masing kecepatan homogenisasi. Lapisan ini cenderung mengalami kenaikan dengan naiknya kecepatan homogenisasi.
a
b
Gambar 13 Penampakan emulsi minyak cengkeh berpenyalut (a) kitosan dan (b) natrium alginat pada kecepatan homogenisasi yang berbeda.
Secara mikroskopi, kecepatan homogenisasi terlihat mempengaruhi ukuran emulsi yang terbentuk. Emulsi akan semakin kecil bila kecepatan homogenisasi
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm
20,000 rpm 15,000 rpm
semakin cepat. Gambar 14 merupakan penampakan mikroskopi emulsi MCC pada hari ke-0. Emulsi tersebut menunjukkan bahwa keseragaman ukuran pada emulsi dengan kecepatan 20,000 lebih baik dibandingkan dengan emulsi pada kecepatan-kecepatan di bawahnya. Pada emulsi dengan kecepatan-kecepatan 5,000 rpm, terdapat banyak emulsi yang berukuran besar yang mengindikasikan ketidak seragaman ukuran emulsi tersebut atau yang biasa disebut dengan polydisperse.
a b c d
Gambar 14 Emulsi minyak cengkeh berpenyalut kitosan pada kecepatan (a) 5,000 rpm, (b) 10,000 rpm, (c) 15,000 rpm, dan (d) 20,000 rpm.
Penampakan mikroskopi emulsi MCA pada hari ke-0 (Gambar 15) menunjukkan hal yang sama dengan penampakan emulsi MCC. Semakin tinggi kecepatan homogenisasi maka ukuran emulsinya terlihat semakin kecil. Ukuran emulsi MCA terlihat memiliki keseragaman yang lebih baik dibandingkan dengan emulsi MCC. Berdasarkan Gambar 15, kerapatan ukuran emulsi juga meningkat dengan meningkatnya kecepatan homogenisasinya. Ukuran doplet minyak cengkeh dengan kecepatan 20,000 rpm terlihat memiliki ukuran yang lebih kecil dan kerapatan antar emulsi lebih rapat dibandingkan dengan kecepatan homogenisasi lainnya.
a b c d
Gambar 15 Emulsi minyak cengkeh berpenyalut natrium alginat pada kecepatan (a) 5,000 rpm, (b) 10,000 rpm, (c) 15,000 rpm, dan (d) 20,000 rpm.
Hasil pengamatan visual didukung dengan hasil pengukuran ukuran partikel emulsi minyak cengkeh yang semakin seragam dengan bertambahnya kecepatan homogenisasinya. Ukuran emulsi pada berbagai kecepatan pada hari ke-0 ditunjukkan pada Tabel 2. Pada hari ke-0, emulsi MCC terkecil didapat pada kecepatan homogenisasi 10,000 rpm, sedangkan untuk emulsi MCA pada kecepatan homogenisasi 15,000 rpm.
pengukuran memiliki satu puncak yang sempit, atau biasa disebut dengan istilah
monodisperse.
Monodisperse/polydispersity ukuran emulsi dinyatakan dengan nilai span. Nilai span yang bagus biasanya lebih besar dari 0 tetapi kurang dari 1. Nilai span yang semakin kecil menunjukkan ukuran partikel yang semakin seragam. Nilai span secara lengkap dapat dilihat pada Lampiran 4.
Tabel 2 Ukuran diameter rata-rata emulsi minyak cengkeh pada hari ke-0
Jenis Penyalut Ukuran diameter rata-rata (µm)
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm Kitosan 2.03±0.028 1.93±0.148 2.26±0.106 2.08±0.078 Natrium alginat 2.19±0.014 2.91±0 2.14±0.057 2.28±0.030
Stabilitas Emulsi Selama Penyimpanan
Pengujian stabilitas emulsi dilakukan untuk mengetahui apakah ada minyak yang keluar dari emulsi selama penyimpanan. Pengujian dilakukan selama 28 hari setelah pembuatan emulsi. Emulsi disimpan pada lemari pendingin dengan suhu 8-10 oC. Liu (2009) menyatakan stabilitas emulsi dapat dilihat dari beberapa parameter, seperti (i) jenis emulsifier (pengemulsi); (ii) ukuran droplet (ukuran kecil lebih stabil); (iii) viskositas fase kontinyu (fase kontinyu kental mengurangi laju
creaming); dan (iv) rasio perbandingan volume terdispersi dengan fase kontinyunya.
Selain faktor diatas, terdapat juga hal yang berhungan dengan stabilitas emulsi yaitu proses homogenisasi emulsi. Ukuran droplet yang semakin kecil akan menjadikan emulsi lebih stabil. Proses homogenisasi dapat mencegah fase minyak untuk menyatu. Kecepatan homogenisasi yang semakin tinggi akan menyebabkan ukuran droplet menjadi semakin kecil sehingga proses penyalutan minyak oleh penyalut akan lebih baik
Lamanya waktu homogenisasi pada kecepatan putar yang sama berpengaruh terhadap tingkat kestabilan emulsi. Semakin lama waktu homogenisasi akan meningkatkan kestabilan emulsi pada volume yang terus meningkat. Kondisi ini terkait dengan distribusi penyalut dan emulsifier yang digunakan semakin merata dengan semakin lamanya waktu homogenisasi sehingga akan meningkatkan kemampuan pengikatan air oleh penyalut dan emulsifier dan menghasilkan emulsi yang stabil (Ilma 2014).
Sedimentasi MCC mengalami kenaikan sehingga stabilitasnya menurun selama penyimpan. Stabilitas emulsi mengalami penurunan dari 100% menjadi sekitar 91% selama waktu penyimpanan 28 hari. Stabilitas emulsi MCC pada kecepatan homogenisasi 10,000 rpm dan 15,000 rpm memiliki data yang tidak berbeda jauh selama penyimpanan dengan prosentasi akhir sama yaitu 91.37±0.643%. Data secara lengkap dan penurunan stabilitasnya dapat dilihat pada Lampiran 5.
0 7 14 21 28
Gambar 16 Penampakan emulsi minyak cengkeh berpenyalut kitosan pada kecepatan homogenisasi 10,000 rpm selama penyimpanan
Emulsi MCA memiliki sedimentasi yang terlihat jelas pada bagian atas (Gambar 17). Lampiran 7 menunjukkan penampakan secara lengkap emulsi MCA selama peyimpanan. Pada hari ke-0, stabilitas emulsi pada kecepatan homogenisasi 5,000 rpm, 10,000 rpm, 15,000 rpm dan 20,000 rpm secara berturut-turut adalah 98.18±0%, 97.27±1.287%, 97.27±1.287%, dan 96.82±0.643%. Pada Lampiran 5 hari ke-7, emulsi mengalami penurunan stabilitas yang besar kecuali untuk emulsi dengan kecepatan homogenisasi 5,000 rpm yang mengalami penurunan pada hari ke-14. Penurunan stabilitas yang paling besar setelah 28 hari penyimpanan yaitu pada emulsi dengan kecepatan homogenisasi 5,000 rpm.
0 7 14 21 28
Gambar 17 Penampakan emulsi minyak cengkeh berpenyalut natrium alginat pada kecepatan homogenisasi 10,000 rpm selama penyimpanan
Selain penampakan emulsi minyak cengkeh secara makro, penampakan mikroskopis dari emulsi juga bisa digunakan untuk mengetahui kestabilan emulsi tersebut. Secara mikroskopis dapat dilihat fenomena coalesense (penggabungan dua droplet dengan ukuran yang berbeda menjadi satu droplet) sehingga ukuran emulsi semakin besar (Lampiran 18).
Penampakan mikroskopi emulsi MCC secara lengkap dapat dilihat pada Lampiran 8 dan 9. Secara umum, semakin lama penyimpanan maka ukuran emulsi MCC terlihat semakin besar. Emulsi MCC terlihat mengalami perubahan ukuran yang semakin besar untuk setiap kecepatan homogenisasi. Gambar 18 menunjukkan perbedaan penampakan ukuran emulsi pada hari ke-0 dan hari ke-28. Banyak emulsi MCC dengan ukuran yang lebih besar dapat diamati pada hari ke-28 setiap kecepatan homogenisasi (Lampiran 8 dan 9).
Hari 0 Hari 28
Gambar 18 Perubahan ukuran emulsi pada hari ke-0 dan hari ke-28 pada emulsi minyak cengkeh berpenyalut kitosan
Emulsi minyak MCA juga menunjukkan hal yang serupa dengan emulsi MCC. Ukuran emulsi menjadi semakin besar selama penyimpanan untuk semua perlakuan. Perubahan yang terjadi pada emulsi MCA susah diamati karena memiliki ukuran emulsi yang terlihat lebih kecil dibandingkan dengan emulsi MCC. Perubahan ukuran emulsi terlihat jelas pada hari ke-28. Perubahan ukuran emulsi tiap harinya tidak terjadi secara cepat. Peristiwa koalesen tetap terjadi pada emulsi ini tetapi prosesnya lebih lama dibandingkan dengan emulsi MCC. Gambar 19 menunjukkan perbedaan emulsi MCA pada hari ke-0 dan hari ke-28. Perubahan ukutan emulsi MCA secara lengkap dapat dilihat pada Lampiran 10 dan 11.
Hari ke-0 Hari ke-28
Gambar 19 Perubahan ukuran emulsi pada hari ke-0 dan hari ke-28 pada emulsi minyak cengkeh berpenyalut natrium alginat
Stabilitas emulsi juga dapat dilihat dari ukuran rata-rata diameter emulsi minyak cengkeh. Pengambilan emulsi minyak cengkeh dilakukan dengan menggunakan alat PSA. Sampel yang digunakan adalah sampel yang sama untuk setiap minggunya. Ukuran diameter emulsi minyak cengkeh secara lengkap dapat dilihat pada Lampiran 3. Emulsi MCC memiliki rataan ukuran diameter yang seragam yaitu berkisar antara 1.87–2.20 µm. Emulsi MCC pada kecepatan homogenisasi 15,000 rpm cenderung mengalami penurunan selama penyimpanan namun pada hari ke-28 ukurannya kembali meningkat. Peningkatan ukuran emulsi MCC pada hari ke-28 berlaku untuk semua kecepatan homogenisasi. Keseragaman ukuran emulsi MCC cenderung lebih stabil pada kecepatan homogenisasi 20,000 rpm dengan standar deviasi datanya 0.08 µm.
Emulsi MCA memiliki rataan ukuran diameter dengan rentang ukuran 1.79– 2.91 µm. Emulsi cenderung mengalmi fluktuatif setiap harinya. Tetapi emulsi MCA pada kecepatan homogenisasi 10,000 rpm cenderung mengalami penurunan namun pada hari ke-28 mengalami peningkatan ukuran. Ukuran emulsi yang stabil didapat pada kecepatan homogenisasi 5,000 rpm dengan standar deviasi data sebesar 0.205 µm.
Tabel 3 Ukuran diameter rata-rata emulsi minyak cengkeh pada kecepatan homogenisasi 5,000 rpm selama penyimpanan
Hari Ukuran diameter rata-rata emulsi (µm)
Emulsi MCC Emulsi MCA
0 2.03±0.028 2.19±0.014
7 2.20±0.198 2.65±0
14 1.87±0.028 2.56±0,257
21 1.90±0.134 2.29±0.802
28 1.99±0.205 2.60±0
Berdasarkan Lampiran 12, emulsi MCC menunjukkan pergeseran grafik ke kiri atau semakin mengecil ukurannya. Namun pada hari ke-28, grafik bergeser ke kanan. Hal ini dapat dikarenakan ketidakstabilan emulsi yang menyebabkan ukurannya semakin besar. Sedangkan emulsi MCA juga menunjukkan hal yang serupa namun distriusi ukuran emulsinya cendurng lebih terpusat dibandingkan dengan emulsi MCC (Lampiran 13).
minyak cengkeh. Minyak yang keluar dari emulsi setiap harinya akan mengalami peningkatan dikarenakan ketidakstabilan emulsi yang ditandai dengan adanya lapisan sedimen pada emulsi. Sedimentasi yang semakin banyak menandakan minyak yang keluar dari emulsi juga semakin banyak.
Prosentase minyak yang keluar dari emulsi dapat dilihat pada Lampiran 15. Berdasarkan Lampiran 15, minyak yang keluar dari emulsi MCC dengan kecepatan homogenisasi 5,000 rpm mengalami kenaikan pada hari ke-8 sampai hari ke-29. Emulsi pada kecepatan 10,000 rpm mengalami penurunan minyak yang keluar setiap harinya. Sedangkan pada kecepatan homogenisasi 15,000 rpm dan 20,000 rpm mengalami fluktuasi konsentrasi minyak yang keluar dari emulsi. Kecepatan homogenisasi 10,000 rpm menunjukkan prosentase yang lebih baik dibandingkan lainnya karena mengalami penurunan minyak yang keluar dari emulsi.
Pada hari ke-0, prosentase minyak yang keluar dari emulsi MCA cenderung mengalami penurunan dengan meningkatnya kecepatan homogenisasi. Minyak yang keluar dari emulsi MCA memiliki banyak nilai eror yang mengakibatkan prosentasenya melebihi 100%. Hal ini dapat dikarenakan masih ada senyawa eugenol yang tertinggal sepanjang kolom GCMS sehingga pada pengukuran sampel berikutnya akan meningkatkan prosentasenya. Pada hari ke-29, minyak yang keluar dari emulsi MCA hanya terlihat pada kecepatan homogenisasi 5,000 rpm dan 20,000 rpm. Lama penyimpanan emulsi mengakibatkan minyak yang keluar dari emuls MCA mengalami peningkatan kecuali untuk emulsi MCA dengan kecepatan homogenisasi 5,000 rpm yang menujukkan hal sebaliknya. Perubahan prosentase minyak yang keluar dari emulsi dapat dilihat pada Lampiran 16.
Bila dibandingkan antara penyalut emulsi minyak cengkeh maka emulsi MCC lebih baik dibandingkan dengan emulsi MCA. Karakteristik emulsi MCC menunjukkan homogenitas emulsi yang lebih baik dikarenakan sedimentasi atau creaming tidak terjadi dengan sempurna sehingga penampakan emulsinya tetap homogen. Sedangkan pada emulsi MCA secara karateristik pada sedimentasinya sudah terlihat pada hari ke-0 pembuatan emulsi. Hal ini menunjukkan ketidakstabilan emulsi tersebut. Ukuran emulsi MCC memiliki ukuran diameter rata-rata yang lebih kecil dan seragam dibandingkan dengan emulsi MCA. Namum untuk keseragaman ukuran secara mikroskopi, emulsi MCA memiliki penampakan yang lebih seragam dibandingkan dengan emulsi MCC.
Morfologi Kapsul Minyak Cengkeh dengan Hidrokoloid sebagai Penyalut
yang berwarna putih. Emulsi dengan cepat segera terbentuk ketika diteteskan ke dalam larutan CaCl2. Kapsul MCA memiliki bentuk yang lebih baik dibandingkan
dengan kapsul MCC karena tidak dilakukan proses sntrifugasi.
Penampakan mikroskopi kapsul yang dilihat dengan mikroskop cahaya dapat dilihat pada Gambar 20. Kapsul MCC secara mikroskopi berbentuk droplet tidak beraturan Sedangkan untuk kapsul MCA memiliki bentuk yang beragam dan tidak beraturan.
a b
Gambar 20 Foto mikroskopi kapsul minyak cengkeh berpenyalut (a) kitosan dan (b) natrium alginat pada perbesaran 10x.
Morfologi kapsul MCC dan MCA dilihat dengan SEM dapat dilihat pada Gambar 21. Kapsul MCC terlihat mengalami kerusakan pada kapsulnya. Pada perbesaran 50 kali (Gambar 21a) terlihat morfologi padatan yang berlapisan dan berkerut-kerut, sedangkan ini bukan morfologi kapsul yang diharapkan. Ketika gambar diperbesar 2,000 kali (Gambar 21b), morfologi kapsul juga tidak tampak. Tipikal morfologi kapsul yang dibuat dari emulsi MCC adalah seperti Gambar (21a dan 21b). Hal ini dapat diakibatkan karena proses sentrifugasi dan pengeringan. Sentrifugasi 9000 x g menyebabkan minyak cengkeh tertarik keluar dan menyebabkan kapsul menjadi kosong. Pengeringan menggunakan pengeringan vakum mungkin tidak cocok karena minyak dapat tertarik secara tiba-tiba dari dalam kapsul pada saat proses vakum.
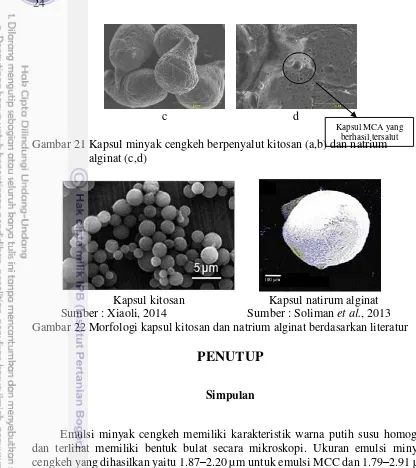
Kapsul MCA menunjukkan aglomerate yang berbentuk bulat tetapi tidak sempurna (Gambar 21c). Sedangkan pada perbesaran 2,000 kali terdapat beberapa emulsi minyak cengkeh yang tersalut (Gambar 21d). Pada kedua perbesaran, tidak dijumpai morfologi kapsul dari emulsi MCA seperti yang diharapkan (Gambar 22). Morfologi kapsul MCA tersebut dapat diakibatkan karena menyatunya individu partikel selama proses solidifikasi. Pemisahan dengan cara ultrasonikasi yang dilakukan tidak terlalu efektif memisahkan gumpalan partikel yang terbentuk. Pecahnya kapsul tidak terindikasi pada kapsul MCA karena proses sentrifugasi tidak dilakukan. Faktor yang lain adanya pengeringan vakum yang bersifat semakin mempererat gumpanan partikel ketika pengeringan selesai.
Kapsul MCA yang berhasil tersalut
c d
Gambar 21 Kapsul minyak cengkeh berpenyalut kitosan (a,b) dan natrium alginat (c,d)
Kapsul kitosan Sumber : Xiaoli, 2014
Kapsul natirum alginat Sumber : Soliman et al., 2013 Gambar 22 Morfologi kapsul kitosan dan natrium alginat berdasarkan literatur
PENUTUP
Simpulan
Emulsi minyak cengkeh memiliki karakteristik warna putih susu homogen dan terlihat memiliki bentuk bulat secara mikroskopi. Ukuran emulsi minyak cengkeh yang dihasilkan yaitu 1.87–2.20 µm untuk emulsi MCC dan 1.79–2.91 µm untuk emulsi MCA.
Emulsi MCC memiliki homoegenitas yang lebih baik secara visual dibandingkan dengan emulsi MCA. Selama penyimpanan, emulsi MCC mengalami sedimentasi dan creaming tetapi kehomogenan dari emulsi tetap terjaga. Sedimen dan creamming pada emulsi tersebut memiliki warna yang hampir sama dengan emulsi sehingga sulit untuk dibedakan. Emulsi MCA mengalami sedimentasi sejak emulsi dibuat sampai hari ke-28, akan tetapi penampakan secara mikroskopi emulsi MCA lebih baik dibandingkan dengan emulsi MCC karena lebih monodisperse.
Saran
Pengambilan gambar mikroskopi emulsi sebaiknya dilakukan pada waktu yang sama untuk setiap pengambilan untuk mendapatkan gambar emulsi yang seragam tiap waktunya. Saat proses homogenisasi dengan kecepatan tinggi, sediakan es memutari gelas beaker agar suhunya dapat terjaga dengan baik karena temperaturnya dapat mencapai 70 oC. Pengukuran senyawa yang keluar
menggunakan GC-MS lebih baik dilakukan validasi metode pengukurannya supaya prosentase yang dihasilkan tidak melebihi 100%. Kecepatan sentrifugasi sampel untuk kapsul kitosan sebaiknya dioptimalkan terlebih dahulu agar kecepatan yang dipakai tidak menyebabkan ekstrak minyak cengkeh dari kapsul. Pengeringan emulsi dipilih menggunakan pengeringan yang sesuai agar hasilnya kapsulnya bagus misalnya freeze drying.
DAFTAR PUSTAKA
Alma MH, Ertas M, Nitz S, and Kollmannsberger H. 2007. Chemical composition and content of essensial oil from the bud of cultivated Turkish clove (Syzygium aromaticum L.). BioResource.2(2): 256–269.
Amelia F. 2007. Perilaku disolusi ketoprofen tersalut gel kitosan-gom guar [Skripsi]. Bogor (ID): Institut Pertanian Bogor.
Bhuiyan NI, Begum J, Nandi NC, and Akter F. 2010. Constituents of the essential oil from leaves and buds of clove (Syzigium caryophyllatum (L.) Alston).
African Journal of Plant Science. 4(11): 451-454.
Brown PJ, Bide M, Burg KJL, Phaneuf MD. 2004. Cellular encapsulation into porous alginate fibers. Ntc project: M04-CL13.
Chan ES. 2011. Preparation of ca-alginate beads containing high oil content: influence of process variables on encapsulation efficiency and bead properties. Carbohydrate Polimers. 84 : 1267-1275.
Charles DJ. 2013. Clove, in antioxidant properties of spices, herbs and other sorces. New York (US): Springer.
Chatterjee D dan Bhattacharjee. 2013. Comparative evaluation of the antioxidant efficacy of encapsulated and un-encapsulated eugenol-rich clove extracts in soybean oil: shelf-life and frying stability of soybean oil. Journal of Food Engineering. 177(4): 545-550.
Desmawarni. 2007. Pengaruh komposisi bahan penyalut dan kondisi spray drying terhadap karakteristik mikrokapsul oleoresin jahe [Skripsi]. Bogor (ID): Institut Pertanian Bogor
Durey R, Shami TC, dan Rao KUB. 2009. Microenkapsulation technology and applications. Defence sci.J., 59(1): 82-95.
Fitri N, Kawira JA. 2006. Perbandingan variabel pada isolasi dan pemurnian eugenol dari minyak daun cengkeh. Media Litbang Kesehatan XVI : 16-21. Gharsallaoui AG, Roudaut G, Chambin O, Voilley A dan Saurel R. 2007.
Hadi S. 2012. Pengambilan minyak atsiri bunga cengkeh (clove oil) mengguanakan pelarut n-heksanan dan benzena. Jurnal Bahan Alam Terbarukan. 1(2): 25-30.
Hosseini SF, Zandi M, Rezai M, Farahmandghavi F. 2013. Two-step method for encapsulation of oregono essential oil in chitosan nanoparticles: preparation, cahracterization and in vitro. Carbohidrat Polymers. 95: 50-56.
Hossain MA et. al. 2012. Constituents of the essential oil from different brands of
Syzigium caryophyllatum L by Gas Chromatography-Mass Spectometry.
Asian Pasific Journal of Tropical Biomedicine. S1446-S1449.
Ilma NA, 2014. Teknik homogenisasi dan pre-peningkatasn skala proses mikroenkapsulasi minyak sawit [Skripsi]. Bogor (ID): Institut Pertanian Bogor
Jackson LS, dan Lee K. 1991. Microencapsulation and the food industry. Lebensm-Wiss-Technol. 24: 289-297.
Kim LS, Yang MR, Lee OH, Lee and Kang SN. 2011. Antioxidant activities of hot water extract from various species. International Jurnal of Molecular Science. 12: 4120-4131.
Lachman. 1994. Teori dan Praktek ilmu farmasi industri edisi III. Depok (ID): UI Press.
Liu S. 2009. Encapsulation of flax oil by complex coacervation [Thesis]. Canada (US): University of Saskatchewan.
McClements DJ. 2005. Food Emulsion Principes, Practice, and Technique, 2nd ed., Boca Raton : CRC Press.
Nurdjanah N, Rusli S dan Vianna A. 1990. Pengeringan bunga cengkeh menggunakan kamar pengering energi surya dan udara panas. Prosiding Seminar Penelitian Pascapanen Pertanian (Buku 1). Bogor(ID): Institut Pertanian Bogor.
Nussinovitch A. 1997. Hydrocolloid Applications. Israel: Chapman and Hall. Pawestrisiswi T. 2011. mikroenkapsulasi double coating menggunakan natrium
alginat dan kitosan sebagai penyalut dan Propranolol HCl sebagai model [Skripsi]. Depok(ID): Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Indonesia.
Purwanti N, Neves MA., Uemura K, Nakajima M and Kobayashi I. 2015. Stability of monodisperse clove oil droplets prepared by microchannel emulsification. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 66-74. Rahmalia R. 2008. Kajian mikroenkapsulai ekstrak vanili dan retensi vanilin selama
penyimpanan [Tesis]. Bogor (ID): Institut Pertanian Bogor.
Rowe RC, Shesky PJ and Owen SC. 2006. Handbook of Pharmaceutical Excipients. London (GB): Pharmaceutical Press and American Pharmacists Association. 159-162, 656-658.
Sapei L, Naqvi MA, Rousseau D. 2012. Stability and release properties of double emulsions for food applications. Jurnal Food Hydrocolloids. 27: 316-323. Schramm LL. 2005. Emulsions, Foams, and Suspensions: Fundamentals and
Applications. Canada (US) :WILEY-VCH Vergal GmmbH & Co.
Soliman EA, El-Moghazy AY, El-Din MSM, Sassoud MA. 2013. Mikroencapsulation of essential oils wiitro evaluation of antifungal activity.
Journal of Enkcapsulation and Adsorpstion Science. 3:48-55.
Sumardjo D, Hanif A, Manurung J, Simanjuntak J (ed). 2008. Pengantar kimia: buku panduan kuliah mahasiswa kedokteran dan program strata1 fakultas bioeksata. Jakarta (ID): Buku Kedokteran EGC.
Terjung N, Loffler M, Gibis J, Hinrichs, Weiss J. 2012. Influence of droplet size on the efficacy of oil-in-water emulsins loaded with phenolic antimicrobials.
Jurnal of Food & Functions. 3: 290-301.
Utami NS. 2012. Studi eksperimen pelepasan paracetamol secara terkendali dari mikrosfer kitosan [Skripsi]. Depok (ID): Fakultas Teknik, Universitas Indonesia.
Xiaoli Z, Yin W, Kun S. 2014. Effect of Erythropoietin loading chitosan-tripoliphosephate nanopartikel on an Iganephropathy Rat model. Journal Experimental and Therapeutic Medicine. 7(6): 1659-1662.
Weiss EA. 1997. Essential Oil Crops. London (UK) : CAB International. Winarno FG. 1992. Kimia Pangan dan Gizi. Jakarta (ID): PT. Gramedia
Lampiran 1 Komposisi senyawa minyak cengkeh hasil analisa menggunakan metode GCMS
No. Nama senyawa
Referensi/ Pustaka Alma
et. al.
Bhuiyan
et. al.
Hossain
et. al.
1 Eugenol Ada Ada Ada
2 Caryophyllene Ada Ada Ada
3 Humulen Ada Ada Tidak
4 Germacrene D Tidak Ada Ada
5 Aromandendrene Tidak Ada Tidak
6 Calamene Tidak Tidak Tidak
Lampiran 2 Tinggi sedimentasi emulsi minyak cengkeh a. Emulsi minyak cengkeh dengan penyalut kitosan
Kec. Homogenisasi
Ketinggian lapisan yang terindikasi creaming pada bagian atas emulsi (mm)
Ketinggian sedimentasi pada bagian bawah emulsi (mm) 5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm
b. Emulsi minyak cengkeh dengan penyalut natrium alginat Kec.
Homogenisasi
Lampiran 3 Distirbusi ukuran diameter rata-rata emulsi minyak cengkeh a. Emulsi minyak cengkeh dengan penyalut kitosan
Kec. Homogenisasi
Ukuran diameter rata-rata emulsi (µm)
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm
b. Emulsi minyak cengkeh dengan penyalut natrium alginat Kec.
Homogenisasi
Ukuran diameter rata-rata emulsi (µm)
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm
: ukuran diameter rata-rata emulsi terlalu besar c. Rataan diameter rata-rata emulsi
Hari/Kec. homogenisasi
Ukuran diameter rata-rata emulsi (µm) MCC 5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm 0 2.03±0.028 1.93±0.148 2.26±0.106 2.08±0.078 7 2.20±0.198 2.09±0.092 2.17±0.184 2.15±0.106 14 1.87±0.028 1.96±0 1.91±0.078 2.08±0.240 21 1.90±0.134 1.91±0,106 1.93±0.049 1.95±0.120 28 1.99±0.205 2.11±0.184 1.98±0.071 1.99±0.106 Standar deviasi
data 0.131 0.094 0.156 0.080
Hari/Kec. homogenisasi
Ukuran diameter rata-rata emulsi (µm) MCA 5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm 0 2.19±0.014 2.91±0 2.14±0.057 2.28±0.030
7 2.65±0 2.50±0.424 2.72±0 2.69±0
14 2.56±0,257 2.49±0.357 2.65±0 2.33±0.068 21 2.29±0.802 2.27±0.591 2.53±0.085 2.26±0.070
28 2.60±0 2.66±0.199 1.79±0 1.94±0
Standar deviasi
Lampiran 4 Span emulsi minyak cengkeh
a. Emulsi minyak cengkeh dengan penyalut kitosan Kec.
b. Emulsi minyak cengkeh dengan penyalut natrium alginat Kec.
Lampiran 5 Stabilitas emulsi minyak cengkeh
a. Emulsi minyak cengkeh dengan penyalut kitosan Kec.
b. Emulsi minyak cengkeh dengan penyalut natrium alginat Kec.
c. Rataan stabilitas minyak cengkeh
Hari/Kec.
14 96.82±0.643 96.36±0 96.82±0.643 96.82±0.643 21 95±1.923 94.10±0.643 94.55±0 92.73±0 28 92.82±1.287 91.37±0.643 91.37±0.643 91.82±0
Hari/Kec. homogenisasi
Stabilitas emulsi MCA (%)
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm 0 98.18±0 97.27±1.287 97.27±1.287 96.82±0.643
7 96.36±0 94.55±0 92.73±0 92.73±0
Lampiran 6 Penampakan visual emulsi minyak cengkeh dengan penyalut kitosan
Hari ke- Batch 1 Batch 2
0
7
14
21
28
Keterangan :
Lampiran 7 Penampakan visual emulsi minyak cengkeh berpenyalut natrium alginat
Hari ke- Batch 1 Batch 2
0
7
14
21
28
Keterangan :
Lampiran 8 Penampakan mikroskopi emulsi minyak cengkeh berpenyalut kitosan batch 1
Hari ke-
Kecepatan homogenisasi
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm
0
7
14
21
Lampiran 9 Penampakan mikroskopi emulsi minyak cengkeh berpenyalut kitosan batch 2
Hari ke-
Kecepatan homogenisasi
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm
0
7
14
21
Lampiran 10 Penampakan mikroskopi emulsi minyak cengkeh berpenyalut natrium alginat batch 1
Hari ke-
Kecepatan homogenisasi
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm
0
7
14
21
Lampiran 11 Penampakan mikroskopi emulsi minyak cengkeh berpenyalut natrium alginat batch 2
Hari ke-
Kecepatan homogenisasi
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm
0
7
14
21
Lampiran 14 Grafik stabilitas sedimentasi emulsi minyak cengkeh a. Emulsi minyak cengkeh dengan penyalut kitosan
b. Emulsi minyak cengkeh dengan penyalut natrium alginate
50
5000 rpm 10000 rpm 15000 rpm 20000 rpm 50
Lampiran 15 Prosentase minyak cengkeh yang keluar dari emulsi
a. Emulsi minyak cengkeh berpenyalut kitosan
Hari Prosentase (%)
5,000 rpm 10,000 rpm 15,000 rpm 20,000 rpm 1 55.82015 77.62539 36.5868 67.58675 8 13.33878 38.49324 37.15045 33.08678 15 16.4917 37.0263 70.19741 56.29804 22 47.703 24.43819 11.2254 16.5522 29 48.31097 18.05951 37.65464 16.7455
b. Emulsi minyak cengekh berpenyalut natrium alginat
Hari Prosentase (%)
5000 rpm 10,000 rpm 15,000 rpm 20,000 rpm 1 50.06735 31.74458 33.10218 12.08314
8 48.43412 * * *
15 * 41.1434 * 43.23049
22 24.44509 39.54136 41.43395 38.9359
29 45.5775 * * 47.00104
Lampiran 16 Grafik prosesntase minyak yang keluar dari emulsi selama penyimpanan
a. Emulsi dengan penyalut kitosan
b. Emulsi dengan penyalut natrium alginat
Keterangan :
: prosentase minyak keluar dari emulsi yang melebihi 100% 0
5000 rpm 10000 rpm 15000 rpm 20000 rpm
0