SKRIPSI
KINETIKA PERUBAHAN ASAM FITAT PADA TEMPE SELAMA PROSES
PEMANASAN
Oleh :
ABDI TUNGGAL CAHYO SUWARTO
F24060460
2011
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Abdi Tunggal Cahyo S. F24060460. Kinetika Perubahan Asam Fitat pada Tempe Selama Proses Pemanasan. Di bawah bimbingan Dr. Ir. Adil Basuki Ahza, MS.
RINGKASAN
Tempe merupakan produk fermentasi tradisional Indonesia dari kacang kedelai dengan menggunakan kapang. Kapang utama yang berperan dalam fermentasi tempe adalah Rhizopus sp. antara lain Rhizopus oryzae, Rhizopus oligosporus, Rhizopus arrhizus, dan Rhizopus stolonifer. Dibandingkan dengan kedelai, tempe memiliki banyak kelebihan. Secara kimiawi hal ini bisa dilihat dari meningkatnya kadar padatan terlarut, nitrogen terlarut, asam amino bebas, asam lemak bebas, nilai cerna, nilai efisiensi protein, serta skor proteinnya. Beberapa penelitian menunjukkan bahwa zat gizi tempe lebih mudah dicerna, diserap, dan dimanfaatkan tubuh dibandingkan dengan yang ada dalam kedelai. Selain sebagai sumber protein, tempe juga memiliki manfaat fungsional yang menjadikan produk ini bernilai tambah tinggi.
Asam fitat ditemukan dalam konsentrasi yang tinggi pada serealia, kacang-kacangan, dan minyak biji-bijian. Pada banyak serealia dan minyak biji-bijian, asam fitat terdapat dalam jumlah 1-5% dari berat total dan menjadi bentuk penyimpanan utama dari fosfor pada tanaman serealia. Tempe yang terbuat dari kacang kedelai akan mengandung asam fitat. Kandungan fitat sebesar 1% atau lebih dalam makanan dapat menyebabkan defisiensi mineral, misalnya defisiensi Ca pada hewan dan manusia yang mengkonsumsi makanan tersebut.
Penelitian ini dibagi menjadi dua tahap, yaitu penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan dilakukan untuk mengetahui profil penetrasi panas tempe sedangkan penelitian utama dilakukan untuk mengukur pengaruh proses termal terhadap kandungan senyawa asam fitat pada tempe. Pada tahap persiapan sampel, sampel tempe dihancurkan dengan penambahan air 1:1 (w/v) kemudian dikemas dalam kantung aluminium foil. Pemanasan sampel dilakukan pada suhu 70, 80, dan 90⁰C dengan waterbath. Berdasarkan penelitian pendahuluan, waktu pemanasan yang diperlukan sampel untuk mencapai suhu 70°C sekitar 4 menit, untuk mencapai suhu 80°C sekitar 5 menit, dan untuk mencapai suhu 90°C diperlukan waktu sekitar 8 menit. Semakin tinggi suhu yang ingin dicapai maka waktu pemanasan awal yang diperlukan semakin lama.
Pengukuran kadar asam fitat pada sampel tempe menghasilkan kadar awal asam fitat pada sampel tempe rata-rata sebesar 2.84 % dari berat kering sampel. Terjadi penurunan kadar asam fitat yang signifikan (62-71%) dari kadar asam fitat awal pada waktu awal perlakuan pemanasan sampel. Penurunan kadar asam fitat yang signifikan pada percobaan ini dipengaruhi oleh beberapa faktor, diantaranya adanya enzim fitase dengan aktivitas tinggi yang dihasilkan kapang Rhizopus oligosporus pada tempe dan kadar asam fitat awal pada sampel yang relatif tinggi. Pada perlakuan pemanasan berikutnya reaksi degradasi asam fitat menjadi lebih lambat. Hal ini disebabkan oleh menurunnya aktivitas enzim fitase karena suhu sampel telah melampaui suhu kerja optimum enzim dan sudah berkurangnya kadar asam fitat pada sampel.
KINETIC OF TEMPE PHYTIC ACID CHANGES DURING
HEATING PROCESS
Abdi Tunggal Cahyo S1 and Adil Basuki Ahza1 1
Department of Food Science and Technology, Faculty of Agricultural Technology, Bogor Agricultural University, Kampus IPB Darmaga, PO. Box 220, Bogor 16002, Indonesia
ABSTRACT
Tempe is Indonesian traditional fermented food which is made from soybean. Despite its high nutrition value, tempe which is produced from soybean, contains phytic acid. This research is aimed at to study the kinetics of tempe phytic acid degradation during thermal process using Arrhenius method. Tempe paste was prepared by blendering ( ratio of 1:1 (w/v) tempe:water), and then treated by three different heating temperatures and five different heating time (70. 80 and 90oC for a 0, 25, 50, 75, and 100 minutes). Degradation of phytic acid content in tempe due to the heating process was order one reaction with ko value of 2.15 x 10-3 min-1, Ea value of -501 cal / mol, and the k value of 2.15 x 10-3. e755, 6 (1 / T).
SKRIPSI
KINETIKA PERUBAHAN ASAM FITAT PADA TEMPE SELAMA PROSES
PEMANASAN
Oleh :
ABDI TUNGGAL CAHYO SUWARTO
F24060460
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
2011
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN
FAKULTAS TEKNOLOGI PERTANIAN
Judul Skripsi : Kinetika Perubahan Asam Fitat pada Tempe Selama Proses Pemanasan
Nama : Abdi Tunggal Cahyo Suwarto
NIM : F24060460
Menyetujui,
Pembimbing
(Dr. Ir. Adil Basuki Ahza, MS.)
NIP : 19521021.197903.1.001
Mengetahui,
Ketua Departemen
(Dr. Ir. Dahrul Syah)
NIP : 19650814.199002.1.001
RIWAYAT HIDUP
Penulis dilahirkan di Kediri, Jawa Timur pada tanggal 24 Desember 1987. Penulis adalah anak ketiga dari tiga bersaudara, pasangan Suwarto dan Srianah. Penulis menyelesaikan pendidikan dasar pada tahun 2000 di SDN Pelem I, Kediri, kemudian melanjutkan pendidikan menengah pertama di SLTPN 2 Pare, Kediri, Jawa Timur hingga tahun 2003. Penulis menamatkan pendidikan menengah atas di SMAN 2 Pare, Kediri pada tahun 2006. Penulis melanjutkan pendidikan tinggi di Institut Pertanian Bogor, Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian melalui jalur USMI (Undangan Seleksi Masuk IPB) pada tahun 2006.
KATA PENGANTAR
Puji syukur penulis ucapkan kehadirat Allah SWT atas segala rahmat dan hidayah-Nya, sehingga penulis dapat menyelesaikan penulisan skripsi dari penelitian yang dilakukan di Laboratorium Departemen Ilmu dan Teknologi Pangan dan Laboratorium SEAFAST Center, IPB dengan judul “Kinetika Perubahan Asam Fitat pada Tempe Selama Proses Pemanasan”. Penelitian dan penulisan skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian pada Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Penghargaan dan ucapan terima kasih yang penulis sampaikan kepada:
1.
Bapak, Ibu, dan keluargaku tercinta atas segala doa, kasih sayang, nasehat, dan motivasi kepada penulis.2.
Dr. Ir Adil Basuki Ahza, MS. selaku dosen pembimbing serta bimbingan dan nasehat dalam menyelesaikan studi di Departemen Ilmu dan Teknologi Pangan.3.
Dr. Ir. Muhammad Arpah, MSi. atas kesediannya menjadi dosen penguji dan atas kritik, saran dan masukan yang diberikan.4.
Antung Sima Firlieyanti, STP, MSc. atas kesediannya menjadi dosen penguji dan atas kritik, saran dan masukan yang diberikan.5.
Seluruh staf pengajar Departemen Ilmu dan Teknologi Pangan IPB atas ilmu yang telah diberikan kepada penulis, semoga menjadi ilmu yang bermanfaat.6.
Teman-temanku di ITP atas kebersamaan dan nasehat selama ini.7.
Teman-teman dan teknisi di laboratorium atas bantuan, masukan, dan semangat yang diberikan selama di laboratorium.8.
Serta semua pihak yang telah membantu penulis selama masa studi di Institut Pertanian Bogor yang tidak dapat disebutkan satu persatu.Bogor, Desember 2010
DAFTAR ISI
Halaman
ABSTRACT ... ii
RINGKASAN ... iii
BIODATA ... iv
KATA PENGANTAR ... v
DAFTAR ISI ... vi
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
I PENDAHULUAN ... 1
A Latar Belakang ... 1
B Tujuan Penelitian...2
II TINJAUAN PUSTAKA ... 3
A Kedelai ... 3
B Tempe dan Senyawa Anti Nutrisi... 3
C Asam Fitat ... 4
D Proses Panas ... 5
E Kinetika Reaksi... 6
III BAHAN DAN METODOLOGI ... 10
A Bahan dan Alat ... 10
B Metode Penelitian ... 10
1. Penelitian Pendahuluan... ... 10
1.1. Persiapan Sampel ... 10
1.2. Penentuan Profil Penetrasi Panas Tempe ... 10
2. Penelitian Utama ... 12
2.1. Persiapan Sampel ... 12
2.2. Pemanasan Sampel ... 12
2.3. Analisis Kandungan Asam Fitat ...12
2.4. Penentuan Kinetika Penurunan Asam Fitat pada Tempe... 13
IV WAKTU DAN TEMPAT ... 14
V HASIL DAN PEMBAHASAN ... 15
A Penelitian Pendahuluan... 15
1. Kalibrasi Termokopel ... 15
2. Penentuan Profil Penetrasi Panas ... 15
B Penelitian Utama ... 16
1. Analisis Kandungan Asam Fitat ... 16
2. Kinetika Penurunan Asam Fitat pada Tempe akibat Pemanasan... 19
VI KESIMPULAN DAN SARAN ... 23
A Kesimpulan ...23
B Saran ... 23
DAFTAR PUSTAKA ... 24
DAFTAR TABEL
DAFTAR GAMBAR
Halaman
1. Struktur asam fitat ……… 4
2. Struktur kompleks fitat mineral ………... 5
3. Hubungan linier pada reaksi ordo nol, satu, dan dua ……….………….. 8
4. Hubungan linier antara ln k dengan kebalikan suhu mutlak ……… 8
5. Bagan alir proses pembuatan tempe ………..……….. 11
6. Pemanasan sampel tempe …………...……… 11
7. Posisi termokopel …………..……… 12
8. Posisi rangka aluminium pada kemasan sampel………..……….. 12
9. Kurva kalibrasi termokopel ………..………. 15
10. Hubungan antara waktu pemanasan dengan suhu sampel ………..……… 16
11. Hubungan antara kadar fitat dengan waktu pemanasan sampel tiap suhu perlakuan ….. 17
12. Kurva kestabilan fitase Rhizopus oligosporus oleh panas………..………… 19
13. Jalur reaksi hidrolisis asam fitat oleh fitase tanaman dan kapang………. 20
DAFTAR LAMPIRAN
Halaman
1. Data hasil pengukuran kalibrasi termokopel ………..………. 27
2. Data hasil pengukuran penetrasi panas ………..……….. 28
3. Data hasil pengukuran kadar air sampel ……….. 29
4. Data hasil pengukuran kurva standar ………... 29
5. Data hasil analisis kadar asam fitat ……….. 30
6. Grafik penentuan kinetika penurunan kadar asam fitat metode Arrhenius ………. 33
I. PENDAHULUAN
A.
LATAR BELAKANG
Tempe merupakan produk fermentasi tradisional Indonesia dari kacang kedelai dengan menggunakan kapang. Kapang utama yang berperan dalam fermentasi tempe adalah Rhizopus sp. antara lain Rhizopus oryzae, Rhizopus oligosporus, Rhizopus arrhizus, dan Rhizopus stolonifer. Masing-masing spesies kapang memiliki kemampuan yang berbeda dalam menghasilkan enzim. Shurtleff dan Aoyagi (1979) menyatakan bahwa analisis yang dilakukan terhadap sampel-sampel tempe dari berbagai tempat di Jawa dan Sumatra ternyata Rhizopus oligosporus selalu terdapat pada tempe yang bermutu baik.
Dibandingkan dengan kedelai, tempe memiliki banyak kelebihan. Secara kimiawi hal ini bisa dilihat dari meningkatnya kadar padatan terlarut, nitrogen terlarut, asam amino bebas, asam lemak bebas, nilai cerna, nilai efisiensi protein, serta skor proteinnya. Beberapa penelitian menunjukkan bahwa zat gizi tempe lebih mudah dicerna, diserap, dan dimanfaatkan tubuh dibandingkan dengan yang ada dalam kedelai. Ini telah dibuktikan pada bayi dan anak balita penderita gizi buruk dan diare kronis. Dengan pemberian tempe, pertumbuhan berat badan penderita gizi buruk akan meningkat dan diare menjadi sembuh dalam waktu singkat (Hermana et al., 2001).
Proses fermentasi pada pengolahan kedelai menjadi tempe akan menurunkan kadar rafinosa dan stakiosa, yaitu suatu senyawa penyebab timbulnya gejala flatulensi (Egounlety dan Aworh, 2003). Kadar asam fitat kedelai juga akan menurun selama proses fermentasi tempe. Penurunan kadar senyawa antinutrisi kedelai selama fermentasi disebabkan oleh aktivitas kapang tempe yang mencerna atau menghasilkan enzim pendegradasi senyawa antinutrisi (Sudarmadji dan Markakis, 1977).
Selain sebagai sumber protein, tempe juga memiliki manfaat fungsional yang menjadikan produk ini bernilai tambah tinggi. Tempe mengandung isoflavon yang merupakan antioksidan yang sangat diperlukan tubuh dalam menghentikan reaksi pembentukan radikal bebas. Potensi tempe yang begitu besar tentu saja menjadikan tempe sebagai produk yang memiliki peluang ekspor tinggi. Hanya saja kendala umur simpan dan mutu menjadi faktor pembatas.
Tempe yang terbuat dari kacang kedelai akan mengandung asam fitat. Kandungan fitat yang tinggi (1% atau lebih) dalam makanan dapat menyebabkan defisiensi mineral, misalnya defisiensi Ca pada hewan dan manusia yang mengkonsumsi makanan tersebut (Wozenski dan Woodburn, 1975).
B.
TUJUAN PENELITIAN
II. TINJAUAN PUSTAKA
A.
Kedelai
Kedelai (Glycine max) termasuk dalam famili Leguminoceae, sub famili Papilionidae, genus Glycine dan spesies max diperkirakan berasal dari Cina. Tanaman ini dibagi menjadi dua golongan, pertama berdasarkan warnanya yaitu kedelai putih/kuning, kedelai coklat, kedelai hijau, dan kedelai hitam. Pembagian kedua berdasarkan umurnya yaitu umur pendek (60-80 hari), sedang (90-100 hari), dan panjang (110-120 hari).
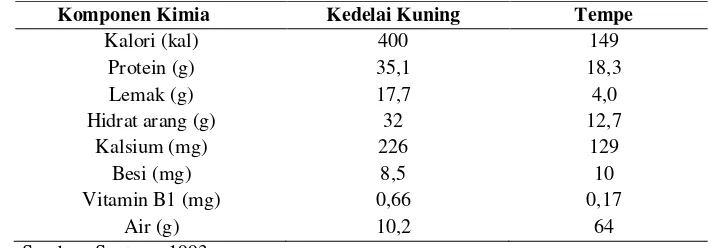
Kedelai mempunyai kandungan protein dan lemak yang tinggi. Secara umum komposisi zat gizi kedelai kuning kering dan tempe dapat dilihat pada Tabel 1.
Tabel 1. Komposisi kimia kedelai dan tempe per 100 gram
Komponen Kimia Kedelai Kuning Tempe
Kalori (kal) 400 149
Protein (g) 35,1 18,3
Lemak (g) 17,7 4,0
Hidrat arang (g) 32 12,7
Kalsium (mg) 226 129
Besi (mg) 8,5 10
Vitamin B1 (mg) 0,66 0,17
Air (g) 10,2 64
Sumber: Santoso, 1993
Komposisi asam amino yang membentuk protein kedelai cukup lengkap. Kandungan lisin kedelai cukup tinggi sehingga dapat digunakan dalam suplementasi pada serealia yang kandungan lisinnya rendah. Kandungan methionin pada protein kedelai rendah, sehingga merupakan faktor pembatas yang harus diperhatikan bila digunakan dalam fortifikasi makanan. Berbagai produk dapat dihasilkan dari kedelai baik sebagai bahan makanan manusia maupun ternak dan bahan industri lainnya. Produk kedelai hasil industri tradisional yang diproduksi dan berpotensi di Indonesia terdiri dari lima jenis produk yaitu: tempe, tahu, tauco, kecap, dan kembang tahu (Muchtadi, 1989).
B.
Tempe dan Senyawa Anti Nutrisi
Menurut Standar Nasional Indonesia (1992), tempe kedelai adalah produk makanan hasil fermentasi biji kedelai oleh kapang tertentu, berupa padatan kompak dan berbau khas serta berwarna putih atau sedikit keabu-abuan. Tempe merupakan produk fermentasi tradisional Indonesia yang umumnya difermentasi dengan menggunakan kapang Rhizopus oligosporus. Kapang lain yang sering ditemukan pada tempe antara lain Rhizopus oryzae, Rhizopus arrhizus, dan Rhizopus stolonifer. Masing-masing spesies kapang memiliki kemampuan yang berbeda dalam menghasilkan enzim. Shurtleff dan Aoyagi (1979) menyatakan bahwa analisis yang dilakukan terhadap sampel-sampel tempe dari berbagai tempat di Jawa dan Sumatra ternyata Rhizopus oligosporus selalu terdapat pada tempe yang bermutu baik.
dan lebih mudah dicerna dibanding kedelai, serta terjadi kerusakan zat-zat anti-nutrisi seperti antitripsin, asam fitat, dan oligosakarida penyebab flatulensi pada kedelai (Hermana, 1985).
Asam fitat dapat membentuk ikatan komplek dengan Fe atau mineral lain seperti Zn, Mg, dan Ca menjadi bentuk yang tidak larut dan sulit diabsorpsi tubuh. Proses perendaman dalam air panas dan fermentasi selama proses pembuatan tempe dapat menurunkan kandungan asam fitat sehingga mineral dapat lebih mudah diserap tubuh (Koswara, 1992). Kapang tempe dapat menghasilkan enzim fitase yang akan menguraikan asam fitat menjadi fosfor dan inositol. Asam fitat berkurang sekitar 30% dari kedelai sebelum fermentasi. Asam fitat dapat menyebabkan defisiensi fosfat, kalsium, dan gangguan penyerapan zat besi (Karyadi, 1985).
Fermentasi akan meningkatkan padatan terlarut dari 13% pada kedelai menjadi 28% pada tempe setelah 72 jam fermentasi. Setengah kandungan protein awal akan dirombak menjadi senyawa yang lebih sederhana dan larut dalam air seperti asam amino dan peptida. Hal ini menunjukkan bahwa daya cerna tempe lebih tinggi dari kedelai (Steinkraus, 1983).
C.
Asam Fitat
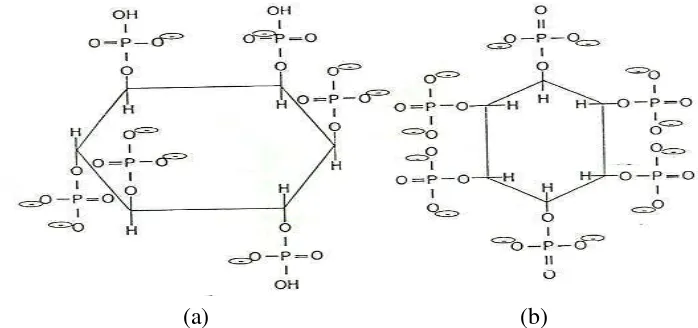
Asam fitat adalah suatu mio-inositol 1, 2, 3, 4, 5, 6-heksafosfat (dihidrogen fosfat) (Oberleas, 1973) yang memiliki fosfor bermuatan negatif yang besar sehingga asam fitat mampu berikatan dengan banyak kation divalen, protein, dan pati. Asam fitat ditemukan dalam konsentrasi yang tinggi pada serealia, kacang-kacangan, dan minyak biji-bijian. Pada tanaman serealia dan minyak biji-bijian, asam fitat terdapat dalam jumlah 1-5% dari berat total dan menjadi bentuk penyimpanan utama dari fosfor pada tanaman serealia (Liener, 1989). Fungsi utama fitat pada tumbuhan adalah untuk menyediakan fosfor dan mio-inositol yang dibutuhkan selama masa perkecambahan benih (Markakis, 1977).
Gambar 1. Struktur asam fitat menurut (a) Erdman (1979) dan (b) Scott et al (1982)
Asam fitat mampu mengkelat mineral-mineral terutama kalsium (Ca), magnesium (Mg), besi (Fe), dan seng (Zn) sehingga menurunkan ketersediaan mineral tersebut bagi tubuh. Kandungan fitat yang tinggi (1% atau lebih) dalam makanan dapat menyebabkan defisiensi mineral, misalnya defisiensi Ca pada hewan dan manusia (Wozenski dan Woodburn, 1975).
Gambar 2. Struktur kompleks fitat-mineral menurut (a) Erdman (1979) dan (b) Scott et al (1982)
Asam fitat dapat juga bereaksi dengan protein membentuk senyawa kompleks. Senyawa kompleks ini dapat mempengaruhi kecepatan hidrolisis protein oleh enzim-enzim proteolitik karena terjadi perubahan konformasi protein. Hal ini menyebabkan ketersediaan biologis dari zat gizi tersebut menurun. Fitat sulit dicerna karena kurangnya sistem kerja enzim endogenous yang mampu mengkatalisis hidrolisis fitat menjadi inositol dan fosfor organik (Muchtadi, 1989). Oleh karena itu asam fitat dianggap sebagai senyawa antinutrisi. Pada dua dekade terakhir, beberapa penelitian menunjukkan bahwa asam fitat memiliki beberapa efek kesehatan, diantaranya menurunkan risiko kanker.
Kadar asam fitat dalam kacang kedelai adalah 1,4% (Sudarmadji dan Markakis, 1977). Kadar asam fitat akan menurun secara drastis akibat perlakuan perendaman dan fermentasi. Perendaman kacang jogo dalam air pada suhu 60°C selama 10 jam menurunkan 90% total kandungan asam fitat. Penurunan nyata kadar asam fitat terjadi pada pemberian perlakuan fermentasi karena kapang fermentasi menghasilkan enzim fitase. Pada oncom, fermentasi menurunkan kadar asam fitat dari kadar awal 1.36% menjadi 0.05% (pada oncom hitam) dan 0.70% (pada oncom merah) (Fardiaz dan Markakis, 1981).
D.
Proses Panas
Proses termal merupakan aplikasi panas pada bahan pangan tertentu yang diharapkan dapat memperpanjang umur simpannya. Proses termal juga memiliki manfaat lain, terutama dalam peningkatan mutu santap. Tujuan utama proses termal adalah membunuh mikroba pembusuk dan patogen dengan pemanasan sehingga dapat meningkatkan keamanannya dan memperpanjang daya awetnya dalam jangka waktu tertentu. Proses termal juga menyebabkan inaktivasi enzim perusak sehingga mutu produk pangan lebih stabil. Namun demikian, proses termal dapat menyebabkan kerugian, yaitu kerusakan zat gizi dan mutu organoleptik (Kusnandar et al., 2006). Proses termal juga dapat menyebabkan perubahan yang merugikan seperti perubahan tekstur dan kerusakan zat gizi seperti vitamin. Setiap produk pangan memiliki tingkah laku yang berbeda oleh pengaruh pemanasan, sehingga akan sangat berguna apabila mengetahui kinetika penurunan mutu oleh panas.
Proses termal secara umum meliputi blansir, pasteurisasi, dan sterilisasi. Proses termal seperti pasteurisasi dan sterilisasi uap diharapkan dapat menjadi metode yang tepat untuk memperpanjang umur simpan tempe karena proses termal dapat menginaktivasi mikroba
penyebab kerusakan. Terbentuknya ammonia merupakan penyebab kerusakan yang utama pada tempe. Enzim proteolitik yang dihasilkan bakteri kontaminan dapat mendegradasi protein sehingga menimbulkan bau. Hal ini menyebabkan tempe segar yang disimpan dalam suhu ruang dan tidak dikemas dengan baik akan bertahan maksimal dua hari (Koswara, 1992).
Blansir adalah perlakuan panas pendahuluan yang sering dilakukan dalam proses pengolahan makanan buah dan sayuran dengan tujuan untuk memperbaiki mutunya sebelum dikenai proses lanjutan. Dengan demikian, proses blansir bukan ditujukan untuk proses pengawetan. Tujuan perlakuan blansir terutama adalah untuk menginaktifasi enzim, mengurangi jumlah mikroba awal (terutama mikroba pada permukaan bahan pangan), melunakkan bahan pangan sehingga mempermudah proses pengisian bahan pangan dalam wadah, dan mengeluarkan udara yang terperangkap pada jaringan bahan pangan yang akan mengurangi kerusakan oksidasi (Kusnandar et al., 2006).
Pasteurisasi merupakan proses perlakuan panas yang membunuh sebagian besar sel vegetatif mikroorganisme yang terdapat di dalam makanan. Pasteurisasi menggunakan suhu dibawah 100°C dengan kombinasi suhu dan waktu yuang digunakan adalah 62,8°C selama 30 menit (konvensional) dan 71°C selama 15 detik (HTST). Dalam beberapa produk makanan, pasteurisasi ditujukan untuk membunuh mikroba patogen, sedangkan dalam produk fermentasi seperti bir, pasteurisasi ditujukan untuk membunuh mikroba pembusuk. Untuk produk lainnya, pasteurisasi yang dikembangkan didasarkan pada daya tahan panas dari mikroba tertentu yang ingin dihancurkan. Pasteurisasi biasanya digunakan pada bahan pangan yang mempunyai pH 3-4 (Fellow, 1992).
Pengertian steril absolut menunjukkan suatu kondisi yang suci hama, yaitu kondisi yang bebas dari mikroorganisme. Pada proses sterilisasi produk pangan, kondisi steril absolut sulit dicapai, karena itulah digunakan istilah sterilisasi komersial atau sterilisasi praktikal. Sterilisasi komersial yaitu suatu kondisi yang diperoleh dari pengolahan pangan dengan menggunakan suhu tinggi dalam periode waktu yang cukup lama sehingga tidak ada lagi mikroorganisme hidup. Pengertian sterilisasi komersial ini menunjukkan bahwa bahan pangan yang telah mengalami proses sterilisasi mungkin masih mengandung spora bakteri (terutama bakteri non-patogen), namun setelah proses pemanasan tersebut spora bakteri non-patogen tersebut bersifat dorman (tidak dalam kondisi aktif bereproduksi), sehingga keberadaannya tidak membahayakan kalau produk tersebut disimpan pada kondisi normal. Dengan demikian, produk pangan yang telah mengalami sterilisasi komersial akan mempunyai daya awet yang tinggi, yaitu beberapa bulan sampai beberapa tahun (Kusnandar et al., 2006).
Sterilisasi komersial erat kaitannya dengan ketahanan bakteri termasuk sporanya. Ketahanan bakteri terhadap proses pemanasan umumnya dinyatakan dengan istilah nilai D dan nilai z. Nilai D adalah waktu dalam menit yang dibutuhkan untuk memusnahkan 90% dari populasi bakteri dalam suatu medium termasuk bahan pangan pada suhu tetap yang tertentu. Nilai z adalah selang suhu terjadinya penambahan atau pengurangan organisme atau spora sepuluh kali lipat dalam waktu yang dibutuhkan baik untuk menurunkan 90% atau pembinasaan seluruhnya (Heldman dan Singh, 2001).
E.
Kinetika Reaksi
pengolahan dan penyimpanan. Perubahan yang terjadi bisa berupa perubahan fisika, kimia, maupun mikrobiologi (Boekel, 1996).
Studi tentang kinetika adalah mempelajari gerakan atau perubahan suatu sistem kimia sebagai fungsi waktu. Beberapa laju perubahan sifat bahan pangan yang dapat dijelaskan dengan kinetika reaksi antara lain kehilangan zat gizi, perubahan flavor, dan perubahan warna (Labuza dan Kamman, 1983).
Penelitian kinetika pada umumnya bertujuan untuk mempelajari perubahan komposisi sebagai fungsi dari waktu. Percobaan didesain sedemikian rupa sehingga tipe perubahan yang lain dapat dikontrol atau dapat diramalkan. Dasar-dasar yang digunakan adalah suatu sistem tertutup yang homogen dan isothermal sehingga zat tidak ada yang masuk atau keluar sistem, gradient konsentrasi atau suhu diasumsikan tidak nyata, serta suhu dijaga konstan selama terjadi perubahan kimia (Swinbourne, 1971).
Laju reaksi merupakan laju penurunan konsentrasi pereaksi atau pertambahan konsentrasi produk per satuan waktu. Reaksi yang terjadi dalam bahan pangan selama pengolahan dan penyimpanan sangat kompleks (Labuza dan Kamman, 1983). Dalam menduga persamaan laju reaksi pada perubahan tersebut lebih mudah digunakan pendekatan empiris. Pada pendekatan empiris perubahan sifat bahan pangan dianggap mengikuti persamaan reaksi sebagai berikut :
A P
Laju reaksi = -d[A] / dt = d[P] / dt
A adalah reaktan pada bahan pangan yang mengalami perubahan; P adalah produk dari perubahan tersebut. Jika t merupakan waktu; n adalah ordo reaksi; dan k adalah nilai konstanta, maka laju perubahan A menjadi P dinyatakan sebagai berikut:
-d[A] / dt = d[P] / dt = k[A]n …………..(1)
Pada reaksi ordo nol (n = 0) persamaan (1) menjadi :
-d[A] / dt = d[P] / dt = k[A]0
dA
A
A0 = -k dt t 0
[A] = [A]0 – kt
Pada reaksi ordo satu (n = 1) persamaan (1) menjadi :
-d[A] / dt = d[P] / dt = k[A]1
dA /[A]
A
A0 = -k dt
t t0
ln [A] = ln [A]0 – kt
log [A] = log [A]0 – (k / 2.303) t
Pada reaksi ordo dua (n = 2) persamaan (1) menjadi :
-d[A] / dt = d[P] / dt = k[A]2
dA
A
A0 /[A]
2
= -k tdt
t0
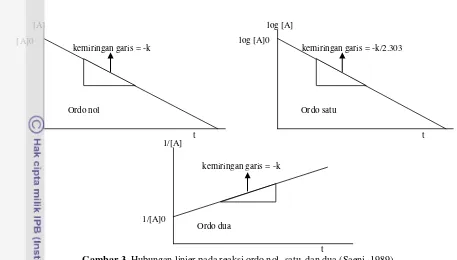
Gambar 3. Hubungan linier pada reaksi ordo nol, satu, dan dua (Saeni, 1989)
Setiap produk pangan memiliki tingkah laku yang berbeda oleh pengaruh pemanasan, sehingga akan sangat berguna apabila mengetahui kinetika penurunan mutu oleh panas. Secara umum kinetika penurunan mutu lebih lambat daripada kinetika inaktivasi mikroba. Menurut Labuza dan Saltmarch (1981) pengaruh perubahan suhu terhadap konstantan laju reaksi dinyatakan dalam persamaan Arrhenius berikut:
k = k0.e-Ea/RT ln k = ln k0 - ��
� (
1
� )
di mana :
k = konstanta laju reaksi Ea = energi aktivasi
k0 = konstanta (tidak tergantung suhu) R = tetapan Planck ( 1,987 kal/mol K) T = suhu mutlak (K)
Gambar 4. Hubungan linier antara ln k dengan kebalikan suhu mutlak (1/T) menurut hubungan Arrhenius (Bird, 1987)
Energi reaktan pada reaksi harus terlebih dahulu dinaikkan ke tingkat energi yang aktif sehingga reaksi dapat berlangsung. Energi yang digunakan untuk menaikkan tingkat energi tersebut disebut energi aktivasi. Nilai energi aktivasi dapat digunakan sebagai parameter besarnya sesuai dengan ketergantungan laju reaksi terhadap suhu. Energi aktivasi yang rendah berarti energi yang [A]
[A]0
t kemiringan garis = -k
Ordo nol
log [A]
log [A]0
t kemiringan garis = -k/2.303
Ordo satu
1/[A]
1/[A]0
t kemiringan garis = -k
Ordo dua
ln k
ln k0
dibutuhkan untuk menaikkan tingkat energi suatu reaktan agar bereaksi adalah kecil sehingga reaksi lebih mudah terjadi (Suhartono, 1987).
Persamaan Arrhenius dapat digunakan untuk menduga laju penurunan mutu makanan dengan menggunakan asumsi-asumsi (Syarief, 1990) :
1. Perubahan mutu makanan hanya disebabkan oleh satu macam reaksi saja. 2. Tidak terjadi faktor lain yang menyebabkan perubahan mutu.
III. BAHAN DAN METODOLOGI
A.
BAHAN DAN ALAT
Bahan yang digunakan dalam penelitian ini adalah tempe kacang kedelai dari produsen M (dengan perlakuan tercantum pada B.1.1.), akuades, aluminium foil, amil alkohol (Merck), kertas saring (Whatman No. 1), HNO3 0,5 M (Merck), FeCl3 (Merck), Amonium tiosianat (Merck), dan
standar asam fitat (P5681 K2-fitat-Sigma).
Alat-alat yang digunakan dalam penelitian ini yaitu termometer, refrigerator, sentrifuse (eppendorf Centrifuge 5810 R) , waterbath shaker, thermocouple (tipe T), thermorecorder (OMEGA® DR130), pipet tetes, erlenmeyer, pipet volumetrik, mikropipet (eppendorf), gelas ukur, blender, waterbath, labu takar, spektrofotometer (spectronic 20D+), tabung reaksi, dan vortex.
B.
METODE PENELITIAN
Penelitian ini dibagi menjadi dua tahap, yaitu penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan dilakukan untuk mengetahui profil penetrasi panas tempe sedangkan penelitian utama dilakukan untuk mengukur pengaruh proses termal terhadap kandungan senyawa asam fitat pada tempe.
1.
Penelitian Pendahuluan
Penelitian pendahuluan dilakukan untuk mengetahui profil penetrasi panas tempe. Penentuan profil penetrasi panas dimulai dengan tahap persiapan sampel tempe kemudian dilanjutkan dengan tahap penentuan profil penetrasi panas ke dalam sampel. Tahap persiapan sampel dilakukan untuk menyeragamkan sampel tempe yang akan dianalisis. Tahap penentuan profil penetrasi panas dilakukan untuk mengukur waktu yang diperlukan agar sampel yang telah dikemas dalam kantung aluminium foil benar-benar telah mencapai suhu yang diinginkan.
1.1.Persiapan Sampel
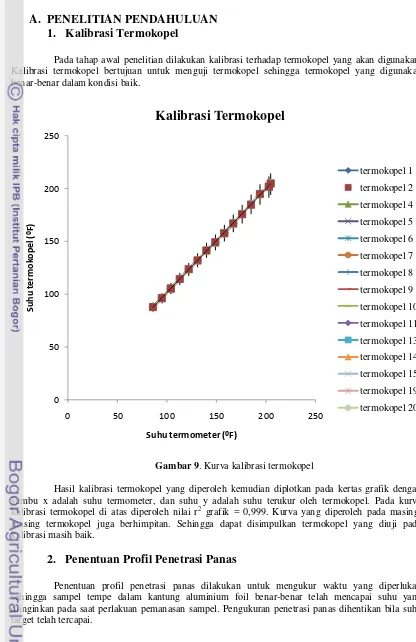
Sampel yang digunakan dalam penelitian ini adalah tempe kacang kedelai yang diperoleh dari produsen M yang beralamat di kawasan perumahan IPB Sindang Barang II. Untuk menjamin keseragaman sampel, maka tempe diberi perlakuan sebagai berikut: tempe yang digunakan merupakan tempe segar. Sampel tempe dipotong dengan pisau agar ukurannya menjadi lebih kecil kemudian ditambah air dengan perbandingan air : sampel = 1:1 (v/w). Sampel kemudian dihancurkan menggunakan blender lalu dikemas dengan kantung aluminium foil yang telah diberi kerangka aluminium setebal 1 cm di pinggir dalam kantung. Kerangka aluminium berfungsi untuk menjaga agar ketebalan kantung sampel seragam sehingga penetrasi panas ke dalam sampel seragam.
1.2.Penentuan Profil Penetrasi Panas Tempe
pindah panas ini, suhu cairan akan semakin seragam dan menyebabkan driving force akan semakin kecil, sehingga kecepatan pergerakan fluida akan semakin menurun. Titik terdingin untuk produk pangan berberntuk cair yang mengalami pindah panas secara konveksi akan berada di titik tengah di 1/3 ketinggian kemasan bagian bawah.
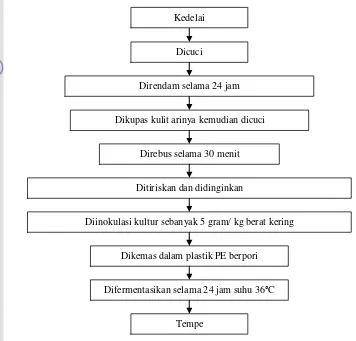
Gambar 5. Bagan alir proses pembuatan tempe yang digunakan sebagai sampel penelitian
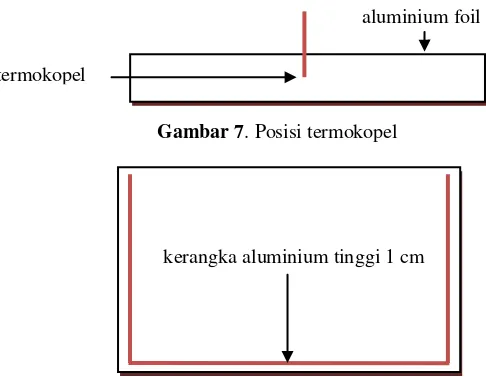
Sampel tempe pada penelitian ini berbentuk semi padat sehingga perambatan panas terjadi secara konduksi dan konveksi. Karena kandungan padatan dalam sampel tinggi, maka perambatan panas dalam sampel terutama terjadi secara konduksi. Hal ini menyebabkan titik terdingin sampel berada di tengah-tengah kemasan sehingga sensor thermocouple diletakkan di bagian tengah kantung sampel. Sensor thermocouple juga diletakkan pada waterbath untuk mengukur suhu dalam waterbath. Sensor thermocouple dihubungkan dengan thermorecorder sehingga suhu sampel tiap menit bisa diketahui. Sampel dipanaskan pada suhu 90, 80, dan 70 °C sampai suhu sampel dan dalam waterbath sama. Suhu sampel yang diperoleh dihubungkan dengan suhu dalam waterbath untuk memperoleh waktu penetrasi panas sampel.
Gambar 6. Pemanasan sampel tempe Dikupas kulit arinya kemudian dicuci
Tempe
Difermentasikan selama 24 jam suhu 36°C
Direbus selama 30 menit
Dikemas dalam plastik PE berpori
Diinokulasi kultur sebanyak 5 gram/ kg berat kering Ditiriskan dan didinginkan
Kedelai
Dicuci
Direndam selama 24 jam
Gambar 7. Posisi termokopel
Gambar 8. Posisi rangka aluminium pada kemasan sampel
2.
Penelitian Utama
Penelitian utama dilakukan untuk mengukur pengaruh proses termal terhadap kandungan senyawa asam fitat pada tempe. Penentuan profil kinetika penurunan kandungan asam fitat pada tempe terdiri dari beberapa tahap, yaitu tahap persiapan sampel tempe, tahap pemanasan sampel tempe, tahap analisis asam fitat, dan tahap penentuan profil kinetika asam fitat. Tahap persiapan sampel dilakukan untuk menyeragamkan sampel tempe yang akan dianalisis. Tahap pemanasan sampel dilakukan untuk memberikan perlakuan termal terhadap sampel. Tahap analisis asam fitat dilakukan untuk mengukur kadar asam fitat dalam sampel setelah perlakuan pemanasan. Tahap penentuan profil kinetika asam fitat dilakukan untuk menentukan profil kinetika penurunan kandungan asam fitat pada tempe berdasarkan data yang diperoleh dari tahap analisis asam fitat.
2.1.Persiapan Sampel
Di bab B.1.1.2.2.Pemanasan Sampel
Aluminium foil yang berisi sampel tempe dimasukkan ke dalam waterbath yang diatur pada suhu pemanasan 90, 80, dan 70°C selama 0, 25, 50, 75, dan 100 menit. Waktu pemanasan sampel dihitung setelah sampel mencapai suhu yang diinginkan dengan berdasar kepada data penetrasi panas sampel yang diperoleh pada penelitian pendahuluan.
2.3.Analisis Kandungan Asam Fitat (Davies dan Reid, 1979)
Pereaksi
Larutan HNO3 0,5 M, larutan FeCl3 (mengandung 50 mg Fe per ml) dalam larutan HNO3 0,5
M, larutan amonium tiosianat 100 g/ liter, amil alkohol, larutan standar Na-fitat 0,2 mM dalam HNO3
0,5 M.
Penetapan Kadar Asam Fitat
Satu gram sampel disuspensikan dalam 50 ml larutan HNO3 0,5 M. Suspensi diaduk
menggunakan magnetic stirrer / shaker selama 2 jam pada suhu ruang. 0,5 ml filtrat kemudian dimasukkan ke dalam tabung reaksi dan ditambahkan 0,9 ml HNO3 0,5 M dan 1 ml FeCl3. Tabung
reaksi ditutup kemudian direndam dalam air mendidih selama 20 menit. Setelah didinginkan ditambah 5 ml amil alkohol dan 1 ml larutan ammonium tiosianat. Selanjutnya disentrifus dalam waktu singkat dan kecepatan rendah. Absorbansi larutan amil alkohol diukur dengan spektrofotometer pada panjang
kerangka aluminium tinggi 1 cm aluminium foil
gelombang 465 nm dengan blanko amil alkohol, 15 menit setelah penambahan ammonium tiosianat. Hasil yang diperoleh dibandingkan pada kurva standar Na-fitat 0,04 mM.
Standar Kadar Asam Fitat
Standar asam fitat (P5681 K2-fitat-Sigma) ditimbang sebanyak 0,8 gram dan dilarutkan
dalam 50 ml HNO3 0,5 M. 0,5 ml standar kemudian dimasukkan ke dalam tabung reaksi dan
ditambahkan 0,9 ml HNO3 0,5 M dan 1 ml FeCl3. Tabung reaksi ditutup kemudian direndam dalam
air mendidih selama 20 menit. Setelah didinginkan ditambah 5 ml amil alkohol dan 1 ml larutan ammonium tiosianat. Selanjutnya disentrifus dalam waktu singkat dan kecepatan rendah. Absorbansi larutan amil alkohol diukur dengan spektrofotometer pada panjang gelombang 465 nm dengan blanko amil alkohol, 15 menit setelah penambahan ammonium tiosianat. Nilai absorban pada pengukuran kurva standar kemudian diplot pada kertas grafik dengan sumbu x konsentrasi standar fitat dan sumbu y nilai absorbansi untuk memperoleh kurva standar asam fitat.
Cara Perhitungan
Persamaan kurva standar : y = 0.212x + 0,693 Absorbansi sampel : 0,717
Kadar standar asam fitat : x = (0,717 – 0.693) / 0,212 = 0,1 ml standar fitat Kadar asam fitat : 0,1 x 0.032 mg = 0,0032 mg asam fitat
2.4.Penentuan Kinetika Penurunan Asam Fitat pada Tempe
Metode yang digunakan dalam penentuan kinetika penurunan asam fitat pada tempe adalah metode Arrhenius (k = ko . e-Ea/RT). Reaksi kehilangan mutu pada makanan dapat dijelaskan oleh ordo
nol dan satu, dan hanya sedikit yang dijelaskan oleh ordo lain (Labuza, 1982). Perhitungan kinetika diawali dengan memplotkan rataan hasil analisis asam fitat terhadap waktu pemanasan per suhu pemanasan. Plot nilai di atas dilakukan pada ordo nol dan ordo satu, dan ordo dua. Pada ordo nol, plot dilakukan antara rataan hasil analisis asam fitat (sumbu y) dengan waktu pemanasan (sumbu x); ordo satu plot dilakukan antara log hasil analisis asam fitat (sumbu y) dengan waktu pemanasan (sumbu x), sedangkan ordo dua plot dilakukan antara 1/hasil analisis asam fitat (sumbu y) dengan waktu pemanasan (sumbu x)..
Hasil plot di atas akan memberikan nilai k, intersep dan koefisien korelasi masing-masing suhu pemanasan. Untuk melihat dan menetukan ordo reaksi kerusakan asam fitat yang dipanaskan dapat ditentukan dari nilai koefisien korelasi yang lebih besar (r2).
Ketika jenis ordo reaksi kerusakan asam fitat telah didapatkan, maka langkah selanjutnya dibuat plot Arrhenius, dengan sumbu x menyatakan nilai 1/T (K-1) dan sumbu y menyatakan nilai ln k pada masing-masing suhu pemanasan yang digunakan. Hasil plot tersebut akan memberikan nilai k dan intersep. Nilai k merupakan gradien dari regresi linier yang didapat dari ketiga suhu pemanasan.
k = ko . e-Ea/RT
Dimana : k = konstanta penurunan mutu ko = konstanta (tidak tergantung suhu)
Ea = Energi aktivasi T = suhu mutlak (K)
R = konstanta Planck (1.987 kal/mol K)
Persamaan garis linear hasil plotting akan mengikuti persamaan Arrhenius, dapat dilihat di bawah ini :
ln k = ln ko + (-Ea/R) . 1/T
IV. WAKTU DAN TEMPAT
V. HASIL DAN PEMBAHASAN
A.
PENELITIAN PENDAHULUAN
1.
Kalibrasi Termokopel
Pada tahap awal penelitian dilakukan kalibrasi terhadap termokopel yang akan digunakan. Kalibrasi termokopel bertujuan untuk menguji termokopel sehingga termokopel yang digunakan benar-benar dalam kondisi baik.
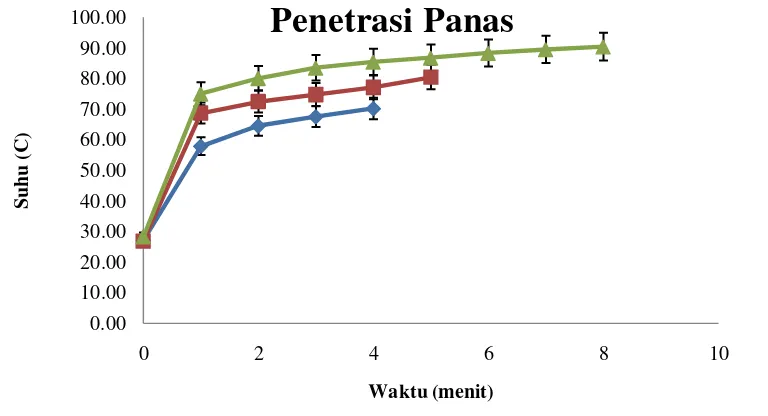
Gambar 9. Kurva kalibrasi termokopel
Hasil kalibrasi termokopel yang diperoleh kemudian diplotkan pada kertas grafik dengan sumbu x adalah suhu termometer, dan suhu y adalah suhu terukur oleh termokopel. Pada kurva kalibrasi termokopel di atas diperoleh nilai r2 grafik = 0,999. Kurva yang diperoleh pada masing-masing termokopel juga berhimpitan. Sehingga dapat disimpulkan termokopel yang diuji pada kalibrasi masih baik.
2.
Penentuan Profil Penetrasi Panas
Penentuan profil penetrasi panas dilakukan untuk mengukur waktu yang diperlukan sehingga sampel tempe dalam kantung aluminium foil benar-benar telah mencapai suhu yang diinginkan pada saat perlakuan pemanasan sampel. Pengukuran penetrasi panas dihentikan bila suhu target telah tercapai.
0 50 100 150 200 250
0 50 100 150 200 250
Su hu te rm ok op el ⁰ F
Suhu termometer ⁰F
Gambar 10. Hubungan antara waktu pemanasan dengan suhu sampel
Dari Gambar 10. dapat dilihat bahwa waktu yang diperlukan sampel untuk mencapai suhu yang diinginkan berbeda-beda tergantung pada suhu yang ingin dicapai. Waktu pemanasan yang diperlukan sampel untuk mencapai suhu 70°C sekitar 4 menit, untuk mencapai suhu 80°C sekitar 5 menit, dan untuk mencapai suhu 90°C diperlukan waktu sekitar 8 menit. Semakin tinggi suhu yang ingin dicapai maka waktu pemanasan awal yang diperlukan semakin lama. Suhu meningkat drastis pada menit-menit awal pemanasan, kemudian suhu meningkat secara perlahan hingga mencapai suhu target.
B.
PENELITIAN UTAMA
1.
Analisis Kandungan Asam Fitat
Analisis kandungan asam fitat dalam penelitian ini dilakukan untuk mengukur konsentrasi asam fitat pada sampel tempe yang telah dipanaskan pada suhu dan waktu tertentu. Asam fitat tidak memiliki reagen dan spektrum absorbsi khusus yang dapat membantu proses analisis. Analisis berdasarkan kepada kemampuan fitat untuk membentuk kompleks stabil tak larut berwarna merah dengan ion feri dalam larutan asam (Oberleas, 1973). Kompleks fitat yang terbentuk kemudian diukur secara spektrofotometri pada panjang gelombang 450 nm, kemudian hasilnya dibandingkan dengan kurva standar asam fitat (Muchtadi, 1989).
0.00 10.00 20.00 30.00 40.00 50.00 60.00 70.00 80.00 90.00 100.00
0 2 4 6 8 10
S
u
h
u
(C
)
Waktu (menit)
Gambar 11. Hubungan antara kadar fitat dengan waktu pemanasan sampel tiap suhu perlakuan
Dari Gambar 11. dapat dilihat bahwa kadar awal asam fitat pada sampel tempe rata-rata sebesar 0.106 mg (2.84 %) per gram berat kering sampel. Hasil ini sedikit berbeda dari penelitian Egounlety dan Aworh (2003) yang mengukur kadar asam fitat pada tempe kedelai fermentasi 24 jam sebesar 1.3 % dari berat kering sampel. Perbedaan ini dapat disebabkan oleh ikut mengendapnya fosfat anorganik dan senyawa polifosfat lain pada tahap ekstraksi asam fitat sehingga ikut terukur pada analisis. Inositol dengan 3 fosfat dan 5 fosfat juga mampu membentuk kompleks tak larut dengan ion ferri dalam kondisi larutan asam sehingga dapat ikut terukur pada analisis asam fitat (Skoglund dan Sandberg, 2002).
Terjadi penurunan kadar asam fitat yang signifikan (62-71%) dari kadar asam fitat awal pada waktu awal perlakuan pemanasan sampel. Menurut de Boland et al. (1975), asam fitat bersifat tahan terhadap pemanasan. Pemanasan flakes kedelai selama 30 menit pada suhu 115⁰C menyebabkan penurunan sedikit kadar asam fitat pada sampel sementara pemanasan flakes kedelai pada suhu yang sama selama 2 jam akan menurunkan 70% kadar asam fitat awal. Pemanasan flakes kedelai ini menyebabkan terjadinya konversi inositol heksafosfat menjadi inositol pentafosfat. Hal ini menunjukkan bahwa penghancuran asam fitat terjadi melalui mekanisme hidrolisis.
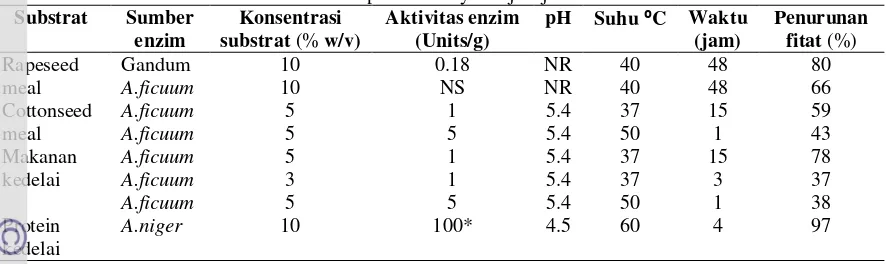
Penurunan kadar asam fitat yang signifikan pada percobaan ini dipengaruhi oleh beberapa faktor, diantaranya adanya enzim fitase dengan aktivitas tinggi yang dihasilkan kapang Rhizopus oligosporus pada tempe (Sudarmadji dan Markakis, 1977) dan kadar awal asam fitat yang relatif tinggi. Fitase (mio-inositol heksafosfat fosfohidrolase, EC 3.1.3.8) merupakan suatu fosfomonoesterase yang mampu mengkatalisis hidrolisis asam fitat menjadi ortofosfat anorganik dan ester-ester fosfat dari mio-inositol yang lebih rendah (Cosgrove, 1970). Fitase yang berasal dari Aspergillus niger mampu menurunkan 97% asam fitat kedelai pada suhu 60⁰C pada pH 4,5 dalam waktu inkubasi 4 jam (Zyla, 1992).
0.0000 0.0020 0.0040 0.0060 0.0080 0.0100 0.0120
0 25 50 75 100
K a d a r
f i t a t
Waktu pemanasan (menit)
Tabel 2. Defosforilasi produk minyak biji-bijian oleh enzim fitase
Substrat Sumber enzim
Konsentrasi substrat (% w/v)
Aktivitas enzim (Units/g)
pH Suhu ⁰C Waktu (jam)
Penurunan fitat (%) Rapeseed meal Gandum A.ficuum 10 10 0.18 NS NR NR 40 40 48 48 80 66 Cottonseed meal A.ficuum A.ficuum 5 5 1 5 5.4 5.4 37 50 15 1 59 43 Makanan kedelai A.ficuum A.ficuum A.ficuum 5 3 5 1 1 5 5.4 5.4 5.4 37 37 50 15 3 1 78 37 38 Protein kedelai
A.niger 10 100* 4.5 60 4 97
* Fosfatase asam. NR—Tidak diukur dan tdak ditentukan; NS—tidak disebutkan.
Sumber : Zyla, 1992
Pada awal waktu pemanasan sampel terjadi penurunan kadar asam fitat yang signifikan akibat peningkatan aktivitas enzim fitase. Aktivitas fitase akan meningkat dengan tajam seiring dengan peningkatan suhu dan tekanan udara (Killmer et al., 1994). Enzim fitase berperan dalam menurunkan energi aktivasi reaksi degradasi asam fitat pada sampel yang dipanaskan sehingga laju reaksi meningkat (Ketaren, 1989). Kadar awal asam fitat yang relatif tinggi juga berpengaruh dalam meningkatkan kecepatan reaksi degradasi asam fitat. Menurut Ketaren (1989), reaksi akan berlangsung lebih cepat dengan semakin tingginya konsentrasi reaktan di dalam sistem reaksi. Pada periode waktu ini, semakin tinggi suhu yang digunakan maka semakin tinggi penurunan kadar asam fitat pada sampel. Menurut Ketaren (1989), reaksi akan berlangsung lebih cepat dengan semakin banyaknya energi yang diberikan ke dalam sistem. Dalam hal ini energi ke dalam sistem berupa pemanasan sampel.
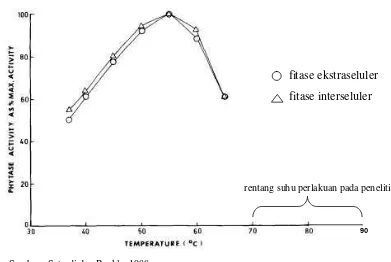
Pada perlakuan pemanasan berikutnya reaksi degradasi asam fitat menjadi lebih lambat. Hal ini disebabkan oleh menurunnya aktivitas enzim fitase karena suhu sampel telah melampaui suhu kerja optimum enzim. Aktivitas maksimum fitase kapang Rhizopus oligosporus terjadi pada suhu 55⁰C pada pH 4,5 (Sutardi dan Buckle, 1988). Suhu perlakuan pada penelitian adalah 70, 80, dan 90⁰C sehingga diperkirakan aktivitas enzim fitase kapang Rhizopus oligosporus telah menurun. Selain itu kadar asam fitat pada sampel juga telah menurun sehingga laju degradasi asam fitat juga akan berkurang.
Sumber : Sutardi dan Buckle, 1988
Gambar 12. Kurva kestabilan fitase Rhizopus oligosporus oleh panas
2.
Kinetika Penurunan Kadar Asam Fitat Tempe akibat Pemanasan
Analisis kinetika dilakukan dengan memplotkan rataan hasil analisis kuantitatif asam fitat terhadap waktu pemanasan per suhu pemanasan. Plot nilai hasil analisis dilakukan pada ordo nol dan ordo satu karena reaksi kehilangan mutu pada makanan pada umumnya dapat dijelaskan oleh ordo nol dan satu, dan hanya sedikit yang dijelaskan oleh ordo lain (Labuza, 1982).Dalam penelitian ini analisis terhadap produk hasil degradasi asam fitat tidak dilakukan sehingga model reaksi yang digunakan dalam penelitian ini adalah:
ksemu
A B
Dimana A adalah asam fitat, B adalah produk degradasi asam fitat oleh pemanasan, dan ksemu
adalah konstanta nilai laju reaksi perubahan asam fitat menjadi produk degradasi asam fitat. Jika t adalah waktu dan n adalah ordo reaksi, maka laju perubahan A menjadi B sesuai dengan persamaan berikut ini :
-d[A]/dt = d[P]/dt = ksemu [A]n
fitase ekstraseluler
fitase interseluler
90
Sumber : Phillippy, 2002
Gambar 13. Jalur reaksi hidrolisis asam fitat oleh fitase tanaman dan kapang
Plot persamaan hasil analisis kinetika metode Arrhenius disajikan dalam tabel berikut ini :
Tabel 3. Tabel persamaan linier perhitungan kinetika metode Arrhenius ordo nol Tabel Persamaan Linier Perhitungan Kinetika metode Arrhenius
Suhu (⁰C) Ordo Nol k r2
70 y = -0.000082x + 0.008244 0.000082 0.8
80 y = -0.000078x + 0.008146 0.000078 0.705
Tabel 4. Tabel persamaan linier perhitungan kinetika metode Arrhenius ordo satu Tabel Persamaan Linier Perhitungan Kinetika metode Arrhenius
Suhu (⁰C) Ordo satu k r2
70 y = -0.009x - 2.033 0.0207 0.928
80 y = -0.007x - 2.098 0.0161 0.884
90 y = -0.008x - 2.105 0.0184 0.885
Tabel 5. Tabel persamaan linier perhitungan kinetika metode Arrhenius ordo dua Tabel Persamaan Linier Perhitungan Kinetika metode Arrhenius
Suhu (⁰C) Ordo Dua k r2
70 y = 9.391x - 18.65 9.391 0.755
80 y = 5.352x + 95.60 5.352 0.915
90 y = 6.818x + 83.92 6.818 0.91
dimana : y adalah kadar asam fitat sampel (mg/g bahan kering); x adalah waktu pemanasan sampel tempe (menit) k adalah laju penurunan kadar asam fitat (menit-1) r adalah koefisien korelasi
Berdasarkan hasil perhitungan di atas maka persamaan laju degradasi asam fitat tempe oleh pemanasan dapat dinyatakan dengan persamaan laju reaksi ordo satu, dengan persamaan sebagai berikut :
-d[A] / dt = d[P] / dt = ksemu [A]1
pada t = 0 maka A = A0
pada t = t maka A = At
d A /[At]
At
A0 = -ksemu dt t t0
ln [At] = ln [A]0 – ksemu t
log [At] = log [A]0 – (ksemu / 2.303) t
dimana [At] adalah konsentrasi asam fitat tempe pada waktu pemanasan t menit, [A0] adalah
konsentrasi asam fitat pada awal waktu pemanasan, ksemu adalah konstanta laju degradasi asam fitat
Apabila nilai-nilai k ordo satu diterapkan dalam rumus Arrhenius, yaitu :
k = ko.e-Ea/RT atau ln k = ko - �� �.
1
�
[image:33.595.113.552.112.383.2]maka akan diperoleh grafik sebagai berikut :
Gambar 14. Grafik hubungan linier antara ln k dengan 1/T pada plot Arrhenius
nilai Ea dapat dihitung dengan :
-Ea/R = 755,6 K (R = 1.986 kal/mol K) -Ea = 755,6 K x 1.986 kal/mol K
Ea = -1501 kal/mol
Sedangkan nilai ko diperoleh dengan : ln ko = -6.141
ko = 2,15 x 10-3 menit-1
sehingga model persamaan Arrhenius untuk panurunan kadar asam fitat pada tempe selama pemanasan adalah :
k = 2,15 x 10-3 . e755,6 (1/T)
Nilai Ea yang negatif menunjukkan bahwa semakin tinggi suhu yang digunakan, maka laju reaksi degradasi asam fitat akan semakin lambat. Hal ini terjadi karena proses penurunan kadar asam fitat pada percobaan selain dipengaruhi oleh panas juga dipengaruhi oleh aktivitas enzim fitase yang memiliki aktivitas maksimum pada suhu 55⁰C. Pada suhu perlakuan (70, 80, dan 90⁰C) aktivitas enzim fitase akan menurun sehingga laju reaksi degradasi asam fitat akan menurun pula.
y = 755.6x - 6.141
-4.1500 -4.1000 -4.0500 -4.0000 -3.9500 -3.9000 -3.8500
0.00270 0.00275 0.00280 0.00285 0.00290 0.00295
ln
k
1/T (K-1)
ln k vs 1/T
VI.
KESIMPULAN DAN SARAN
A.
KESIMPULAN
Penurunan kadar asam fitat tempe akibat proses pemanasan merupakan reaksi ordo satu. Nilai ko degradasi asam fitat tempe karena pemanasan adalah 2,15 x 10-3 menit-1, nilai Ea adalah -1501 kal/mol, dan nilai k adalah 2,15 x 10-3 . e755,6 (1/T).
Nilai Ea yang negatif menunjukkan bahwa semakin tinggi suhu yang digunakan, maka laju reaksi degradasi asam fitat akan semakin lambat. Hal ini terjadi karena proses penurunan kadar asam fitat pada percobaan selain dipengaruhi oleh panas juga dipengaruhi oleh aktivitas enzim fitase dari kedelai dan kapang Rhizopus oligosporus yang memiliki aktivitas maksimum pada suhu 55⁰C.
B.
SARAN
DAFTAR PUSTAKA
Bird, T. 1987. Kimia Fisik Untuk Universitas. Terjemahan: Kwee le Tjien. PT Gramedia, Jakarta.
Boekel, M.A.J.S.V. 1996. Statistical aspects of kinetic modeling for food science problems. J. Food Sci. 61(3) : 477 – 485.
Cosgrove, D.J. 1970. Inositol Phosphatase of Microbial Origin. Inostol Phosphate Intermedate in the Phosphorylation of the Hexaphosphates of Myo-inositol, Scylloinositol, by a Bacterial (Pseudomonas sp.) Phytase. Aust. J. Biol. Sci. 23(6) : 1207 - 20.
Davies, N.T. and H. Reid. 1979. An Evaluation of The Phytate, Zinc, Copper, Iron, and Manganese Content of, and Zn Availability from, Soya-Based Textured-Vegetable-Protein Meat-Substitutes or Meat-Extenders. Brit. J. Nutr. 34 : 579 - 589.
de Boland, A. R., George B.G., and Boyd L.O'Dell.1975. Identification and properties of phytate in cereal grains and oilseed products. J. Agric. Food Chem. 23 (6) : 1186-1189.
Dewan Standardisasi Nasional. 1992. SNI 01-3144-1992 tentang Mutu dan Cara Uji Tempe Kedelai.
Erdman Jr, J. W. (1979). Oilseed phytates: nutritional implications. J. Am. Oil Chem. Soc, 56, 736-41.
Egounlety, M. and O.C. Aworh.2003. Effect of soaking, dehulling, cooking and fermentation with Rhizopus oligosporus on the oligosaccharides, trypsin inhibitor, phytic acid and tannins of soybean (Glycine max Merr.), cowpea (Vigna unguiculata L. Walp) and groundbean (Macrotyloma geocarpa Harms). J. Food Engineerng 56 : 249 - 254.
Fardiaz, D. and P. Markakis. 1981. Degradation of phytic acid in oncom (fermented peanut press cake). J. Food. Sci. 46 : 523 - 525.
Fellow, P. 1992. Food Processing Technology, Principles and Practices. Ellsi Harword, New York.
Hackler, L. R., K. H. Steinkraus, J. P. Van Buren, and D. B. Hand. 1964. Studies on the utilization of tempeh protein by weanling rats. J. Nutrition 82 : 452 - 456.
Hariyadi, P. 2000. Dasar-dasar Teori dan Praktek Proses Termal. Pusat Studi Pangan dan Gizi Institut Pertanian Bogor. Bogor.
Heldman, D. R. and Singh R. P. 2001. Introduction to Food Engineering. Academic Press, London.
Hermana. 1985. Pengolahan Kedelai Menjadi Berbagai Bahan Makanan. Di dalam S. Somaatmadja, M. Ismunadji, Sumarno, M. Syam, S. D. Manurung dan Yuswadi (Eds). Kedelai. Pusat Penelitian dan Pengembangan Tanaman Pangan, Bogor.
Hermana, M. Mahmud, and D. Karyadi. 2001. Composition and nutrition value of tempe: its role in the improvement of the nutritional value of food. Di dalam Agranoff, Jonathan (ed.). The Complete Handbook of Tempe. American Soybean Association, Singapore.
Hesseltine, C. W. 1985. Genus Rhizopus and tempeh microorganisms. Proceedings, Asian Symposium on Non-salted Soybean Fermentation. Tsukuba, Japan, July 1985. p. 20-26. National Food Research Institute Tsukuba Science City.
Karyadi, Darwin. 1985. Prospek pengembangan tempe dalam upaya peningkatan status gizi dan kesehatan masyarakat. Di dalam Simposium Pemanfaatan Tempe dalam Peningkatan Upaya Kesehatan dan Gizi. Departemen Kesehatan RI.
Killmer, O.L., P.A. Seib, and R.C. Hoseney. 1994. Effects of minerals and apparent phytase activity in the development of hard-to-cook state of beans. J. Cereal Chem. 71(5) : 476 – 482.
Koswara, S. 1992. Teknologi Pengolahan Kedelai Menjadi Makanan Bermutu. Pustaka Sinar Harapan, Jakarta.
Kusnandar, F., P. Hariyadi, dan N. Wulandari. 2006. Proses termal. Di dalam : Kusnadar, F., P. Hariyadi, dan E. Syamsir. Modul Kuliah Prinsip Teknik Pangan. Departemen Ilmu dan Teknologi Pangan, IPB.
Labuza, T.P. and M. Saltmarch. 1981. Kinetics of browning and protein quality loss in whey powder during steady state and non steady state storage condition. J. Food Sci. 47 : 92 – 96.
Labuza, T.P. and Kamman, J.F. 1983. Reaction kinetics and accelerated test simulation as a function temperature. Di dalam Computerated Techniques in Food Technology. I. Saguy, (ed), p. 71-90. Marcell Dekker, Inc., New York.
Liener, Irvin E. 1989. Antinutritional Factors. Di dalam. Ruth H. Matthews (ed.). Legumes Chemistry, Technology, and Human Nutrition.Marcell Dekker, Inc. New York.
Lolas, G. M. and Markakis, 1977. The Phytase of Navy Beans (Phaseolus vulgaris). J. Food Sci. 42 : 1094.
Muchtadi, D. 1989. Petunjuk Laboratorium Evaluasi Nilai Gizi Pangan. PAU Pangan dan Gizi IPB, Bogor.
Oberleas, D. 1973. Phytates in: Toxicans Occuring Naturally in Foods. 2nd Ed. National Academy of Sci., Washington DC
Phillippy, B.Q. 2002. Stability of Plant and Microbial Phytases. Di dalam. Reddy, N. Rukma and Shridhar K. Sathe (ed.). Food Phytates. CRC Press LLC.
Saeni, M.S. 1989. Kimia Fisik I. PAU Pangan dan Gizi IPB, Bogor.
Santoso, H.B. 1993. Pembuatan Tempe & Tahu Kedelai Bahan Makanan Bergizi Tinggi. Kanisius, Yogyakarta.
Scott, M.L., M.C. Nesheim, and R.J. Young, 1982. Nutrition of the Chicken, 3th ed. W.F. Humphrey Press Inc., Geneva, NY.
Seidl, D.S. and I.E. Liener. 1971. Biochem. Res, Commun. 42,1101 - 1107.
Shurtleff. W. and A. Aoyagi. 1979. The Book of Tempeh. Harper and Row Publisher, New York.
Skoglund, E. and A.S. Sandberg. 2002. Methods for Analysis of Phytate. Di dalam. Reddy, N. Rukma and Shridhar K. Sathe (ed.). Food Phytates. CRC Press LLC.
Steinkraus, K. H. 1983. Handbook of Indigenous of Fermented Foods. Marcell Dekker Inc., New York.
Sudarmadji, S. 1975. Certain Chemical and Nutritional Aspects of Soybean Tempe. Thesis. Michigan State University, Michigan.
Sudarmadji, S and P. Markakis. 1977. Phytate and Phytase of Soybean Tempe. J. Sci. Food Agric. 28 : 381-394.
Suhartono, M.T. 1987. Pengantar Biokimia. PAU Pangan dan Gizi IPB, Bogor.
Syarief, R. 1990. Teknologi Pengemasan Pangan. Monograf. PAU Pangan dan Gizi IPB. Bogor.
Syarief, R., J. Hermanianto, P. Hariyadi, S. Wiraatmaja, Suliantari, D. Syah, N. E. Suyatma, Y. P. Saragih, J. H. Arisasmita, I. Kuswardani, dan M. Astuti. 1999. Wacana Tempe Indonesia. Universitas Katolik Widya Mandala, Surabaya.
Swinbourne, E.S. 1971. Analysis of Kinetic Data. Meredith Corporation, New York.
Wahyuni, S.H.S. 1995. Biokonversi Dedak Padi oleh Kapang Aspergillus ficuum sebagai Upaya Menurunkan Kadar Fitat dan Pengaruhnya terhadap Kinerja Ayam Petelur. Tesis. Program Pasca Sarjana IPB, Bogor.
Wolf, W.J. and J.C. Cowan. 1977. Soybean as A Food Source. CRC Press. The Chemical Rubber Co., Ohio.
Wozenski, J. Woodburn. 1975. Phytic acid (Myoinositol hexaphosphate) and phytase activity in four cottonseed protein products. J. Cereal Chem.,52, 665 - 669.
Lampiran 1. Data hasil pengukuran kalibrasi termokopel
suhu termometer suhu termokopel (⁰F)
rataan sd rsd analisis rsd hitung
⁰C ⁰F 1 2 4 5 6 7 8 9 10 11 13 14 15 19 20
30 86 87.7 87.8 87.8 87.7 87.8 87.8 87.7 87.7 87.7 87.7 87.7 87.7 87.8 87.8 87.7 87.74 0.051 0.0578 2.0398 35 95 96 96.3 96.4 96.2 96.3 96.3 96.2 96.3 96.2 96.2 96.1 96.2 96.2 96.2 96.2 96.22 0.094 0.0978 2.0116 40 104 105.3 105.4 105.4 105.5 105.4 105.3 105.4 105.4 105.3 105.4 105.3 105.4 105.4 105.5 105.4 105.38 0.064 0.0607 1.9843 45 113 114.4 114.4 114.4 114.4 114.4 114.3 114.3 114.3 114.3 114.3 114.3 114.3 114.3 114.4 114.3 114.34 0.051 0.0443 1.9601 50 122 123.4 123.7 123.8 123.3 123.7 123.7 123.7 123.6 123.4 123.8 123.5 123.7 123.8 123.8 123.8 123.64 0.168 0.1362 1.9371 55 131 132 132.1 132.1 132.1 132.1 132 132 132 132 131.9 131.8 132 132 131.9 132 132.00 0.084 0.0640 1.9181 60 140 141.5 141.5 141.6 141.5 141.4 141.4 141.4 141.4 141.3 141.4 141.3 141.3 141.4 141.3 141.4 141.40 0.088 0.0625 1.8984 65 149 148.9 149.3 149.3 149.1 149 149.1 148.9 149.1 148.9 149 148.7 149 149.1 149.1 149 149.03 0.154 0.1035 1.8834 70 158 157.7 157.8 157.7 157.9 157.9 157.7 157.7 157.7 157.7 157.7 157.6 157.7 157.7 157.7 157.8 157.73 0.082 0.0518 1.8674 75 167 167 167 167 167.2 167 166.9 167 166.9 167 166.9 166.9 166.9 167 167 167 166.98 0.078 0.0464 1.8515 80 176 175.7 175.8 176.4 176 175.9 176.1 175.8 176 175.8 176.1 176 176 176.3 176 176.1 176.00 0.189 0.1074 1.8369 85 185 185 184.9 185.4 185 185 185.1 185.1 184.9 185.2 185.2 184.8 184.6 185 185.3 185.3 185.05 0.210 0.1135 1.8230 90 194 194.3 195.1 195.3 195.1 194.9 194.7 194.5 195 195.1 194.8 194.4 194.8 194.6 194.8 195 194.82 0.286 0.1471 1.8090 95 203 201.4 201.9 202.4 201.8 201.9 201.9 201.9 201.9 202.6 202.5 201.7 202.1 202.4 202.6 202.3 202.08 0.360 0.1783 1.7990 96 204.8 204.1 204.8 205.5 204.8 204.6 204.4 204.6 205 205.4 205.5 204.9 205.1 205.3 205.2 205 204.94 0.409 0.1994 1.7952
Lampiran 2. Data hasil pengukuran penetrasi panas
Waktu
Penetrasi suhu 70⁰C
⁰F ⁰C
Suhu 1 Suhu 2 Suhu 3 Suhu 1 Suhu 2 Suhu 3 0 81.6 80 81.1 27.56 26.67 27.28 1 130.9 142 135.7 54.94 61.11 57.61 2 143.4 153 148 61.89 67.22 64.44 3 153.7 156 151 67.61 68.89 66.11 4 159.2 159 157 70.67 70.56 69.44
Waktu
Penetrasi suhu 80⁰C
⁰F ⁰C
Suhu 1 Suhu 2 Suhu 3 Suhu 1 Suhu 2 Suhu 3 0 80.6 80.1 80.8 27.00 26.72 27.11 1 159.3 152.8 155.1 70.72 67.11 68.39 2 168.1 156.1 163.1 75.61 68.94 72.83 3 169.8 160.3 169.7 76.56 71.28 76.50 4 171.4 167.4 173.6 77.44 75.22 78.67 5 176.6 177.3 176.6 80.33 80.72 80.33
Waktu
Penetrasi suhu 90⁰C
⁰F ⁰C
y = 0.212x + 0.693 R² = 0.984
0.71 0.72 0.73 0.74 0.75 0.76 0.77 0.78 0.79 0.8 0.81
0 0.1 0.2 0.3 0.4 0.5 0.6
A
b
so
rb
a
n
si
Jumlah ml standar pengenceran 5x
Lampiran 3. Data hasil pengukuran kadar air sampel
Kadar Air Sampel
Cawan kosong (g) Sampel Basah (g) Cawan+sampel kering (g) Sampel kering (g) Kadar bahan kering (%) Kadar air (%) Rata-rata SD RSD analisis RSD hitung
2.1893 2.1344 2.5768 0.3875 18.1550 81.8450 81.6329 0.1263 0.1547 2.0620
2.1338 1.7676 2.4628 0.3290 18.6128 81.3872
2.0901 2.1147 2.4778 0.3877 18.3336 81.6664
Lampiran 4. Data hasil pengukuran kurva standar
Volume standar Absorbansi
0.1 0.717
0.2 0.738
0.3 0.751
0.4 0.776
Lampiran 5. Data hasil analisis kadar asam fitat
Sampel Berat Basah (g) Berat Kering (g) Absorban Jumlah Fitat (ml standar) Kadar Fitat (mg/g)
70 (1) 0 2.0815 0.3823 0.826 0.6226 0.0104 Sampel Rata-rata SD RSD analisis RSD hitung
70 (1) 25 2.0329 0.3734 0.741 0.2217 0.0038 70 ; 0' 0.0103 0.000236 2.2968 7.9695
70 (1) 50 2.0939 0.3846 0.738 0.2075 0.0035 70; 25' 0.0039 0.000165 4.2072 9.2122
70 (1) 75 2.0203 0.3711 0.725 0.1462 0.0025 70 ; 50' 0.0035 0.000006 0.1768 9.3864
70 (1) 100 2.0003 0.3674 0.705 0.0519 0.0009 70; 75' 0.0023 0.000255 10.8756 9.9536
70 (2) 0 2.0362 0.3740 0.819 0.5896 0.0101 70;100' 0.0008 0.000085 10.1244 11.6073
70 (2) 25 2.0377 0.3743 0.744 0.2358 0.0040
70 (2) 50 2.0412 0.3749 0.737 0.2028 0.0035
70 (2) 75 2.0528 0.3770 0.721 0.1274 0.0022
70 (2) 100 2.0989 0.3855 0.704 0.0472 0.0008
Suhu perlakuan Waktu pemanasan Rata2
Orde 0
(A0) Orde 1 (log A0) Orde 2 (1/A0)
70
0 0.0103 0.0103 -1.9890 97.4980
25 0.0039 0.0039 -2.4071 255.3280
50 0.0035 0.0035 -2.4612 289.1721
75 0.0023 0.0023 -2.6304 426.9991
Lampiran 5. Data hasil analisis kadar asam fitat
Sampel Berat Basah (g) Berat Kering (g) Absorban Jumlah Fitat (ml standar) Kadar Fitat (mg/g)
80 (1) 0 1.9466 0.3575 0.819 0.5896 0.0106 Sampel Rata-rata SD RSD analisis RSD hitung
80 (1) 25 1.9354 0.3555 0.736 0.1981 0.0036 80 ; 0' 0.0107 0.000174 1.6268 7.9215
80 (1) 50 1.9968 0.3668 0.729 0.1651 0.0029 80; 25' 0.0036 0.000050 1.3862 9.3290
80 (1) 75 2.0506 0.3766 0.725 0.1462 0.0025 80 ; 50' 0.0029 0.000061 2.0903 9.6264
80 (1) 100 1.9503 0.3582 0.712 0.0849 0.0015 80; 75' 0.0025 0.000003 0.1334 9.8667
80 (2) 0 1.9632 0.3606 0.823 0.6085 0.0108 80;100' 0.0014 0.000125 8.7834 10.7227
80 (2) 25 1.9882 0.3652 0.738 0.2075 0.0036
80 (2) 50 2.1048 0.3866 0.732 0.1792 0.0030
80 (2) 75 1.9882 0.3652 0.724 0.1415 0.0025
80 (2) 100 1.9632 0.3606 0.710 0.0755 0.0013
Suhu perlakuan Waktu pemanasan
Rata-rata
Orde 0
(A0) Orde 1 (log A0) Orde 2 (1/A0)
80
0 0.0107 0.0107 -1.9715 93.6566
25 0.0036 0.0036 -2.4434 277.6131
50 0.0029 0.0029 -2.5340 341.9762
75 0.0025 0.0025 -2.6051 402.8333
Lampiran 5. Data hasil analisis kadar asam fitat
Sampel Berat Basah (g) Berat Kering (g) Absorban Jumlah Fitat (ml standar) Kadar Fitat (mg/g)
90 (1) 0 2.0752 0.3812 0.830 0.6415 0.0108 Sampel Rata-rata SD RSD analisis RSD hitung
90 (1) 25 2.0324 0.3733 0.734 0.1887 0.0032 90 ; 0' 0.0109 0.000133 1.2236 7.9007
90 (1) 50 2.058 0.3780 0.727 0.1557 0.0026 90; 25' 0.0032 0.000080 2.5187 9.5064
90 (1) 75 2.0339 0.3736 0.718 0.1132 0.0019 90 ; 50' 0.0027 0.000033 1.2234 9.7654
90 (1) 100 2.061 0.3785 0.709 0.0708 0.0012 90; 75' 0.0021 0.000207 9.9272 10.1285
90 (2) 0 2.0246 0.3719 0.829 0.6368 0.0110 90;100' 0.0012 0.000051 4.3883 11.0634
90 (2) 25 2.0008 0.3675 0.732 0.1792 0.0031
90 (2) 50 2.0227 0.3715 0.727 0.1557 0.0027
90 (2) 75 2.0616 0.3787 0.722 0.1321 0.0022
90 (2) 100 2.0468 0.3759 0.708 0.0660 0.0011
Suhu perlakuan Waktu pemanasan
Rata-rata
Orde 0
(A0) Orde 1 (log A0) Orde 2 (1/A0)
90
0 0.0109 0.0109 -1.9639 92.0330
25 0.0032 0.0032 -2.4978 314.6388
50 0.0027 0.0027 -2.5754 376.1445
75 0.0021 0.0021 -2.6807 479.4090
y = -8E-05x + 0.008 R² = 0.8
y = -8E-05x + 0.008 R² = 0.705
y = -8E-05x + 0.008 R² = 0.685
-0.0020 0.0000 0.0020 0.0040 0.0060 0.0080 0.0100 0.0120
0 20 40 60 80 100 120
A0 Waktu (menit)
Ordo nol
70 80 90 Linear (70) Linear (80) Linear (90)y = -0.009x - 2.033
R² = 0.928 y = -0.007x - 2.098
R² = 0.884 y = -0.008x - 2.105
R² = 0.885
-3.5000 -3.0000 -2.5000 -2.0000 -1.5000 -1.0000 -0.5000 0.0000
0 20 40 60 80 100 120
lo g A 0 Waktu (menit)
Ordo satu
Linear (90)y = 9.391x - 18.65 R² = 0.755
y = 5.352x + 95.60 R² = 0.915
y = 6.818x + 83.92 R² = 0.91
0.0000 200.0000 400.0000 600.0000 800.0000 1000.0000 1200.0000 1400.0000
0 20 40 60 80 100 120
1
/A
0
Ordo dua
Lampiran 7. Tabel perhitungan penentuan kinetika penurunan kadar asam fitat metode Arrhenius
Tabel Persamaan Linier Perhitungan Kinetika metode Arrhenius
Suhu (⁰C) Ordo satu ksemu k (menit-1) ln k T (K) 1/T (K
-1
)
70 y = -0.009x - 2.033 -0.009 0.0207 -3.8763 343 0.00292
80 y = -0.007x - 2.098 -0.007 0.0161 -4.1276 353 0.00283
90 y = -0.008x - 2.105 -0.008 0.0184 -3.9941 363 0.00275
Lampiran 8. Grafik penentuan kinetika penurunan kadar asam fitat metode Arrhenius
y = 755.6x - 6.141
-4.1500 -4.1000 -4.0500 -4.0000 -3.9500 -3.9000 -3.8500
0.00270 0.00275 0.00280 0.00285 0.00290 0.00295
ln
k
1/T (K-1)
ln k vs 1/T
SKRIPSI
KINETIKA PERUBAHAN ASAM FITAT PADA TEMPE SELAMA PROSES
PEMANASAN
Oleh :
ABDI TUNGGAL CAHYO SUWARTO
F24060460
2011
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Abdi Tunggal Cahyo S. F24060460. Kinetika Perubahan Asam Fitat pada Tempe Selama Proses Pemanasan. Di bawah bimbingan Dr. Ir. Adil Basuki Ahza, MS.
RINGKASAN
Tempe merupakan produk fermentasi tradisional Indonesia dari kacang kedelai dengan menggunakan kapang. Kapang utama yang berperan dalam fermentasi tempe adalah Rhizopus sp. antara lain Rhizopus oryzae, Rhizopus oligosporus, Rhizopus arrhizus, dan Rhizopus stolonifer. Dibandingkan dengan kedelai, tempe memiliki banyak kelebihan. Secara kimiawi hal ini bisa dilihat dari meningkatnya kadar padatan terlarut, nitrogen terlarut, asam amino bebas, asam lemak bebas, nilai cerna, nilai efisiensi protein, serta skor proteinnya. Beberapa penelitian menunjukkan bahwa zat gizi tempe lebih mudah dicerna, diserap, dan dimanfaatkan tubuh dibandingkan dengan yang ada dalam kedelai. Selain sebagai sumber protein, tempe juga memiliki manfaat fungsional yang menjadikan produk ini bernilai tambah tinggi.
Asam fitat ditemukan dalam konsentrasi yang tinggi pada serealia, kacang-kacangan, dan minyak biji-bijian. Pada banyak serealia dan minyak biji-bijian, asam fitat terdapat dalam jumlah 1-5% dari berat total dan menjadi bentuk penyimpanan utama dari fosfor pada tanaman serealia. Tempe yang terbuat dari kacang kedelai akan mengandung asam fitat. Kandungan fitat sebesar 1% atau lebih dalam makanan dapat menyebabkan defisiensi mineral, misalnya defisiensi Ca pada hewan dan manusia yang mengkonsumsi makanan tersebut.
Penelitian ini dibagi menjadi dua tahap, yaitu penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan dilakukan untuk mengetahui profil penetrasi panas tempe sedangkan penelitian utama dilakukan untuk mengukur pengaruh proses termal terhadap kandungan senyawa asam fitat pada tempe. Pada tahap persiapan sampel, sampel tempe dihancurkan dengan penambahan air 1:1 (w/v) kemudian dikemas dalam kantung aluminium foil. Pemanasan sampel dilakukan pada suhu 70, 80, dan 90⁰C dengan waterbath. Berdasarkan penelitian pendahuluan, waktu pemanasan yang diperlukan sampel untuk mencapai suhu 70°C sekitar 4 menit, untuk mencapai suhu 80°C sekitar 5 menit, dan untuk mencapai suhu 90°C diperlukan waktu sekitar 8 menit. Semakin tinggi suhu yang ingin dicapai maka waktu pemanasan awal yang diperlukan semakin lama.
Pengukuran kadar asam fitat pada sampel tempe menghasilkan kadar awal asam fitat pada sampel tempe rata-rata sebesar 2.84 % dari berat kering sampel. Terjadi penurunan kadar asam fitat yang signifikan (62-71%) dari kadar asam fitat awal pada waktu awal perlakuan pemanasan sampel. Penurunan kadar asam fitat yang signifikan pada percobaan ini dipengaruhi oleh beberapa faktor, diantaranya adanya enzim fitase dengan aktivitas tinggi yang dihasilkan kapang Rhizopus oligosporus pada tempe dan