PRIMA LUNA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis Optimasi Sintesis Monolaurin Menggunakan Katalis Enzim Lipase Imobil pada Circulated Packed Bed Reaktor adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi dan kutipan dari karya penulis lain, yang diterbitkan maupun yang tidak diterbitkan, telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, April 2011
Circulated Packed Bed Reactor. Supervised by NURI ANDARWULAN and TRI HARYATI
Monolaurin is a special food grade monogliceride, which has a function beside as emulsifier and food preservative, also has an ability to destroy Herpes and HIV-1 virus. It was reported that monolaurin had the greatest antimicrobial activity among monoglycerides. Novozyme® 435 catalyze the esterification of lauric acid and glycerol in organic solvent. The purpose of this research were : 1) to obtain optimum condition to synthesis monolaurin using Novozyme® 435; 2) to analyze the stability of Novozyme®
Continuous circulated packed bed reactor had residence time of 23,57 minute, glycerol/ oil molar ratio of 5:1, solvent/substrate ratio of 8,8:1, and the process produced MAG up to 80%. Optimization of synthesis MAG obtained quadratic equation which was Y= - 61,700 + 6,088 x
435 in continuous system. Continuous Esterification was employed in circulated packed bed reactor. This researchwas using Response Surface Methods (RSM) as experimental design and temperature and time reaction were as variables.
1+3,259 x2 – 0,065 x12 + 0,017 x1x2 – 1,792 x22 with R2 = 0,5408, optimum temperature and time reaction of 46,92oC and 1,1 hour, respectively. The product yield was 81,09% and contained MAG of 83,15%. The product had acid value of 1,78±0,08 %, peroxide value of 0,49 ± 0,14 meq O2/kg MAG, free glycerol content of 0,26%, and melting point 53-53,5oC. The enzyme remain stable during 10 reaction cycles and up to 70% produced of MAG at each cycle.
PRIMA LUNA. Optimasi Sintesis Monolaurin Menggunakan Katalis Enzim Lipase Imobil Pada Circulated Packed Bed Reaktor. Dibimbing oleh: NURI ANDARWULAN dan TRI HARYATI
Monoasilgliserol (MAG) adalah salah satu emulsifier yang banyak digunakan sebagai bahan tambahan pangan. MAG secara luas digunakan dalam produk bakeri, margarine, produk susu, dan confectionary karena sifat emulsifikasi, stabilisasi, dan conditioning (Damstrup et al., 2005). Salah satu jenis MAG, yaitu monolaurin, monogliserida dari asam laurat, merupakan salah satu produk turunan dari minyak, yang memiliki keistimewaan. Kegunaan monolaurin adalah sebagai bahan pengawet pangan dan sanitizer. Saat ini monolaurin sudah banyak digunakan dalam industri kosmetik, farmasi dan obat-obatan. Monolaurin dilaporkan memiliki kemampuan menghancurkan virus herpes dan HIV-1 serta menurunkan resiko penularan virus ini pada bayi dari ibu hamil yang terinfeksi HIV, selain itu monolaurin juga efektif menghambat sel vegetative B. Cereus,
mengakibatkan kerusakan membran, menyebabkan kebocoran protein intraselular dan asam nukleat sehingga menurunkan aktivitas enzim yang berperan dalam metabolisme pada bakteri gram prositif (Cotton dan Marshall, 1997; Kabara 1993). Tujuan penelitian ini adalah : 1) Mencari kondisi optimum untuk sintesis monolaurin melalui proses esterifikasi enzimatis circulated packed bed reactor; 2) Menguji stabilitas enzim Novozyme®
Metode yang digunakan pada penelitian ini adalah reaksi esterifikasi enzimatis circulated packed bed reactor. Rancangan percobaan optimasi pada penelitian ini menggunakan Central Composite Design dari
Response Surface Methods (RSM). Hasil penelitian pendahuluan menghasilkan MAG 77,33 % dengan rendemennya sebesar 82,26% pada proses batch reaksi esterifikasi enzimatis. Kondisi reaksi pada proses reaksi batch tersebut kemudian dikonversi ke esterifikasi menggunakan reaktor packed bed sirkulasi. Kondisi reaksi kontinyu menggunakan rasio asam lemak/gliserol (1:5); volume reaktan 50 ml, rasio substrat/ pelarut (1:8,8), dan residence time 23,57 menit. Hasil optimasi reaksi kontinyu menggunakan respon permukaan tanggap menunjukkan persamaan kuadrat optimasi MAG adalah Y= - 61,700 + 6,088 X
435 dalam reaksi esterifikasi circulated packed bed reactor.
1+3,259 X2 – 0,065 X12 + 0,017 X1X2 – 1,792 X22 . Suhu dan waktu reaksi optimum yaitu 46,92oC dan 1,1 jam. Hasil optimasi diverifikasi sebanyak lima kali menghasilkan MAG 83,19% dan rendemen 81,09. Karakterisasi sifat kimia produk hasil verifikasi memiliki bilangan asam 1,78 ±0,08 %, bilangan peroksida 0,49 ± 0,14 meq O2/kg MAG, kadar gliserol bebas 0,26%, dan memiliki kisaran titik leleh 53-53,5 oC. Berdasarkan jumlah produk MAG yang dihasilkan terlihat bahwa selama 10 kali reaksi terjadi penurunan jumlah produk MAG sekitar 7% dari komposisi MAG awal, sedangkan rendemen produk MAG dan Jumlah MAG selama 10 kali siklus reaksi mengalami penurunan masing-masing sekitar 16% dari rendemen serta jumlah MAG awal.
Hak Cipta milik IPB, tahun 2011 Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atas seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah
b. Pengutipan tersebut tidak merugikan kepentingan yang wajar IPB 2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh Karya
CIRCULATED PACKED BED REAKTOR
PRIMA LUNA
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
NRP : F251080341 Program Studi : Ilmu Pangan
Disetujui
Komisi Pembimbing
Dr. Ir. Nuri Andarwulan, M.Si
NIP. 19630701 198811 2 001 Anggota Dr. Ir. Tri Haryati, MS
Ketua
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana IPB
Ilmu Pangan
Dr. Ir. Ratih Dewanti, M.Sc
NIP. 19620920 198603 2 002 NIP. 19650814 199002 1 001 Dr. Ir. Dahrul Syah, MSc. Agr
Alhamdulillah, penulis panjatkan puji dan syukur kehadirat Allah SWT atas rahmat dan karunia-Nya sehingga penulisan tesis dengan judul ”Optimasi Sintesis Monolaurin Menggunakan Katalis Enzim Lipase Imobil pada Circulated Packed Bed Reaktor” dapat diselesaikan. Tesis ini disusun sebagai salah syarat untuk memperoleh gelar Magister Sains pada Sekolah Pascasarjana, Institut Pertanian Bogor.
Pada kesempatan ini penulis menyampaikan ucapan terima kasih kepada: 1. Ibu Dr. Ir. Nuri Andarwulan, M.Si dan Ibu Dr. Ir. Tri Haryati, MS selaku
dosen pembimbing yang telah banyak memberikan ilmu, arahan, bimbingan dan pendanaan sehingga penulis dapat menyelesaikan tesis ini.
2. Prof. Dr. Ir. Purwiyatno Hariyadi, M.Sc selaku dosen penguji atas ilmu, saran dan masukan bagi sempurnanya karya ilmiah penulis ini.
3. Orang tuaku Papah dan Mamah (Prof. H. Sambas Basuni dan Hj. Nurahmat, SE. M.Pd) yang selalu menjadi inspirasi bagi penulis, Papa dan Mama Palembang (H. Sumanto dan Hj. Swati), adik-adik tercinta (de tiara&de utik) serta keluarga besar atas doa dan semangat yang telah diberikan.
4. Suami dan anak-anak tercinta (Koko Setiawan, Abang Ayyash, dan Dede Nusaibah) atas doa, pengorbanan, semangat dan kasih sayang yang telah diberikan sehingga penulis dapat menyelesaikan tesis ini.
5. Sahabat seperjuangan IPN 2008 : Ibu-ibu manis (Teh Elin, Teh Susi, Mba Titin, Mb Siti, Mb Yeni), Alin, Lia, Ira, Nono, Arief atas segala bantuan dan motivasinya, serta semua pihak yang tidak dapat penulis sebutkan satu-persatu.
6. WAMY (World Assembly Moslem Youth) atas bantuan beasiswa sehingga penulis dapat menyelesaikan tesis ini
Ucapan terima kasih yang sebesar-besarnya kepada Indofood Riset Nugraha 2010 atas bantuan dana penelitian yang telah diberikan sehingga penelitian ini dapat berjalan. Semoga karya ilmiah ini bermanfaat.
Bogor, April 2011
Penulis dilahirkan di Bogor tanggal 08 Juni 1983 dari ayah Prof. Dr. Ir. H. Sambar Basuni, MS dan Ibu Hj. Nurahmat, SE. M.Pd. Penulis merupakan anak pertama dari tiga bersaudara.
Tahun 2001 penulis lulus dari SMUN 1 Bogor dan pada tahun yang sama penulis masuk Institut Pertanian Bogor melalui jalur PMDK. Penulis memilih Departemen Teknologi Pangan dan Gizi, Fakultas Teknologi Pertanian (FATETA). Penulis menyelesaikan pendidikan sarjananya pada bulan Juni tahun 2005. Kemudian pada tahun 2008 penulis melanjutkan studi Magister Sains di Program Studi Ilmu Pangan, Sekolah Pascasarjana, Institut Pertanian Bogor.
PENDAHULUAN Latar Belakang
Monoasilgliserol (MAG) adalah salah satu emulsifier yang banyak
digunakan sebagai bahan tambahan pangan. MAG secara luas digunakan dalam
produk bakeri, margarine, produk susu, dan confectionary karena sifat
emulsifikasi, stabilisasi, dan conditioning (Damstrup et al., 2005). Komersial
MAG banyak terbuat dari gliserolisis minyak atau lemak. Reaksi gliserolisis
dipercepat dengan penggunaan katalis basa inorganik, seperti NaOH atau
Ca(OH)2 pada temperatur tinggi (220-260o
Penelitian sintesis monoasilgliserol (MAG) dan diasilgliserol (DAG)
secara enzimatis telah banyak dilakukan sebelumnya, antara lain Pujiastuti (1998)
dan Nuraeni (2008) telah berhasil memanfaatkan Destilat Asam Lemak Minyak
Sawit (DALMS) sebagai bahan baku pembuatan emulsifier mono- dan
diasilgliserol (M-DAG), kemudian Kitu (2000) telah berhasil memanfaatkan
Destilat Asam Lemak Minyak Kelapa (DALMIK) sebagai bahan baku pembuatan
emulsifier mono- dan diasilgliserol (M-DAG) secara enzimatis.
C). Kandungan MAG dalam
keseimbangan bervariasi antara 10-60% tergantung pada rasio gliserol dengan
minyak dalam campuran reaksi.
Salah satu jenis MAG, yaitu monolaurin, monogliserida dari asam laurat,
merupakan salah satu produk turunan dari minyak, yang memiliki keistimewaan.
Kegunaan monolaurin adalah sebagai bahan pengawet pangan dan sanitizer. Saat
ini monolaurin sudah banyak digunakan dalam industri kosmetik, farmasi dan
obat-obatan. Produk paten dari monolaurin yang sudah beredar adalah
Lauricidin(R). Monolaurin dilaporkan memiliki kemampuan menghancurkan virus
herpes dan HIV-1 serta menurunkan resiko penularan virus ini pada bayi dari ibu
hamil yang terinfeksi HIV, selain itu monolaurin juga efektif menghambat sel
vegetative B. cereus (Cotton dan Marshall, 1997). Monolaurin juga dilaporkan
dapat mengakibatkan kerusakan membran, menyebabkan kebocoran protein
intraselular dan asam nukleat sehingga menurunkan aktivitas enzim yang berperan
Produk monolaurin dapat dibuat dari berbagai macam minyak yang
memiliki kandungan asam laurat tinggi seperti Destilat Asam Lemak Minyak
Kelapa (DALMIK), minyak kelapa, minyak inti sawit, dan asam laurat komersial
itu sendiri. Asam laurat merupakan asam lemak jenuh rantai sedang yang
mengandung 12 atom karbon dan tidak memiliki ikatan rangkap. Asam laurat
mengandung gugus hidrokarbon non polar pada bagian ekornya dan asam
karboksilat yang polar pada bagian kepala. Hal tersebut menyebabkan asam laurat
ini dapat berinteraksi baik dengan air maupun minyak.
Pembuatan MAG dan DAG dilakukan secara kimia dan enzimatis. Cara
kimia merupakan cara yang paling banyak digunakan dalam industri, namun
reaksi kimia seperti ini berlangsung lama, tidak selektif, dan menggunakan energi
dalam jumlah besar. Selain itu, cara ini akan menghasilkan produk samping yang
tidak dikehendaki seperti warna gelap, rasa terbakar, dan flavor yang
menyimpang. Sintesis MAG secara enzimatis menjadi pilihan peneliti beberapa
tahun terakhir, karena aktivitas katalitik enzim yang sangat tinggi dan
kemampuannya bekerja pada suhu relatif rendah (McNeill et al., 1992). Sintesis
enzimatis dapat dilakukan dengan hidrolisis, esterifikasi asam lemak,
transesterifikasi ester asam lemak dan gliserolisis minyak atau lemak dengan
menggunakan enzim lipase. Berkembangnya teknologi enzim imobil
meningkatkan stabilitas enzim (Haryadi, 1996), salah satu enzim imobil yang
banyak digunakan adalah Lipozyme dan Novozyme.
Dengan pertimbangan nilai ekonomi dan kesehatan dari produk turunan
minyak dan lemak, monolaurin, maka perlu upaya kajian teknologi pengolahan
minyak atau lemak untuk menghasilkan produk tersebut. Pada penelitian ini
monolaurin disintesis dengan cara esterifikasi yaitu mereaksikan asam laurat dan
gliserol menggunakan enzim lipase imobil. Faktor-faktor yang menentukan agar
sintesis MAG secara esterifikasi enzimatis berlangsung optimal antara lain: faktor
suhu, waktu reaksi, dosis enzim, dan jumlah pelarut yang digunakan. Suhu dan
waktu reaksi pada penelitian terdahulu, akan digunakan sebagai titik tengah
optimasi setelah diuji cobakan dan hasilnya konstan. Kemudian dilakukan tahap
laurat secara enzimatis serta dilakukan pula pengujian stabilitas enzim imobil
yang digunakan, yaitu Novozyme®
Harga lipase komersial biasanya sangat tinggi karena proses produksinya
yang sulit dan memakan waktu. Selain itu, dalam proses reaksi enzimatis, lipase
tidak dapat digunakan kembali lagi karena terlarut dalam media reaksi. Hal ini
menyebabkan biaya reaksi yang dikatalisis lipase menjadi meningkat. Perlu
adanya penelitian tentang teknik penggunaan kembali lipase, salah satunya adalah
teknik reaksi immobilisasi dengan bantuan support sebagai media pembantu yang
dapat menahan enzim dalam struktur molekulnya. 435.
Recovery dan penggunaan kembali (reuse) enzim dari reaksi esterifikasi
dikarenakan alasan biaya (cost). Oleh karena itu stabilitas lipase dalam reaksi
adalah parameter penting (Rozendaal,1997). Kehilangan aktivitas selama reaksi
inesterifikasi disebabkan oleh dua faktor, yaitu inaktivasi panas lipase dan
kontaminasi oleh komponen minor dalam reaktan. Kontaminasi reaktan dapat
dicegah dengan cara penyaringan secara hati-hati dari reaktan tersebut, tapi lipase
harus tahan pada suhu relatif tinggi yang digunakan dalam reaksi.
Stabilitas enzim imobil diuji dengan cara penggunaan kembali (re-use)
enzim pada reaksi esterifikasi dengan cara enzim dipisahkan dari reaksi, kemudian
dicuci dengan pelarut dan dikeringkan. Setelah itu digunakan kembali pada proses
dan kondisi reaksi yang sama beberapa kali. Hal ini bertujuan untuk melihat
seberapa stabil enzim imobil komersial dapat digunakan dengan menganalisis
parameter rendemen dan komposisi MAG yang dihasilkan.
Tujuan Penelitian
Penelitian ini bertujuan untuk:
1. Mencari kondisi optimum untuk sintesis monolaurin melalui proses
esterifikasi enzimatis circulated packed bed reactor.
2. Menguji stabilitas enzim Novozyme® 435 dalam reaksi esterifikasi
circulated packed bed reactor dengan melihat parameter rendemen dan
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan manfaat sebagai berikut:
1. Pengembangan teknologi pembuatan monolaurin dengan metode enzimatis
2. Informasi seberapa stabil enzim lipase imobil dapat digunakan dalam reaksi
esterifikasi enzimatis circulated packed bed reactor memproduksi
TINJAUAN PUSTAKA Asam Lemak Laurat
Asam laurat atau asam dodekanoat adalah
sedang (middle-chained fatty acid, MCFA) yang tersusun dari 12 atom
utama asam lemak ini adal
laurat, sertapalm kernel oil). Sumber lain adalah susu sapi.
Asam laurat memiliki titik lebur 44°C dan titik didih 225°C sehingga pada suhu
ruang berwujud padatan berwarna putih, dan mudah mencair jika dipanaskan.
Rumus kimia: CH3(CH2)10COOH, berat molekul 200,3 g.mol-1. Asam-asam
lemak rantai pendek memiliki kemampuan kelarutan dalam pelarut air, semakin
panjang rantai asam-asam lemak maka kelarutannya dalam air semakin
berkurang. Asam kaprilat pada 30 oC mempunyai nilai kelarutan 1, yang artinya 1
gram asam kaprilat dapat larut dalam setiap 100 g air pada suhu 30 oC. Sedangkan
asam stearat mempunyai nilai kelarutan sekitar 0,00034 pada suhu 30 o
Sifat fisikokimia asam laurat banyak dimanfaatkan oleh industri yang
menghasilkan produk personal care dan farmasi, misalnya pada industri
C
(Ketaren, 2005). Sifat kelarutan tersebut digunakan sebagai dasar untuk
memisahkan berbagai asam lemak yang tidak jenuh, yaitu dengan proses
kristalisasi.
Natrium laurilsulfat adalah turunan yang paling sering dipakai dalam industri
sabun dan shampoo, sedangkan pada industri kosmetik, asam laurat ini berfungsi
sebagai pengental, pelembab dan pelembut. Asam laurat atau asam lemak berantai
menengah berbeda dengan asam lemak berantai panjang yang memiliki molekul
lebih besar. Sifat-sifat metabolisme asam lemak rantai menengah jauh lebih
mudah dicerna dan diserap usus dan dibawa ke hati untuk diubah menjadi energi.
Itu karena asam lemak rantai menengah memiliki molekul ukuran lebih kecil
sehingga cepat menghasilkan energi untuk tubuh.
Asam laurat banyak terdapat pada minyak kelapa yang telah dikenal sejak
4000 tahun yang lalu sebagai minyak kesehatan dalam obat-obatan Ayurvedic.
Penelitian terakhir menyebutkan kandungan minyak dan lemak dalam minyak
kelapa, yaitu asam lemak rantai sedang (MCFA) dan monogliserida dari asam
lemak dalam air susu ibu (ASI) (Kabara, 1983; Jensen et al., 1992; Jensen, 1996;
Kolezko et al., 1992). Asam lemak jenuh pada minyak kelapa didominasi oleh
asam lemak laurat yang memiliki rantai karbon 12, sehingga minyak kelapa sering
juga disebut minyak laurat. Asam lemak jenuh rantai menengah inilah yang
membuat minyak kelapa murni bermanfaat bagi kesehatan.
Minyak kelapa berdasarkan kandungan asam lemak digolongkan ke dalam
minyak asam laurat (Ketaren, 2005), karena kandungan asam lauratnya paling
besar jika dibandingkan asam lemak lainnya. Komposisi asam lemak minyak
kelapa dapat dilihat pada Tabel 1. Dari Tabel tersebut dapat dilihat bahwa asam
lemak jenuh minyak kelapa lebih kurang 90 persen. Minyak kelapa mengandung
84 persen trigliserida dengan tiga molekul asam lemak jenuh, 12 persen
trigliserida dengan dua asam lemak jenuh dan 4 persen trigliserida dengan satu
asam lemak jenuh.
Tabel 1 Komposisi Asam lemak Minyak Kelapa
Asam Lemak Rumus Kimia Jumlah (%) Asam lemak jenuh:
Asam kaproat C5 H11 COOH 0,0 – 0,8
Asam kaprilat C7 H17 COOH 5,5 – 9,5
Asam Kaprat C9 H19 COOH 4,5 – 9,5
Asam Laurat C11 H23 COOH 44,0 – 52,0
Asam miristat C13 H27 COOH 13,0 – 19,0
Asam palmitat C15 H31 COOH 7,5 – 10,5
Asam stearat C17 H35 COOH 1,0 – 3,0
Asam arachidat C19 H39 COOH 0,0 – 0,4
Asam lemak tidak jenuh:
Asam palmitoleat C15 H29 COOH 0,0 – 1,3
Asam oleat C17 H33 COOH 5,0 – 8,0
Asam linoleat C17 H31 COOH 1,5 – 2,5
Sumber: Thieme (1968) Di dalam Ketaren (2005)
Sumber asam laurat lain adalah minyak inti sawit (PKO). Minyak inti
sawit adalah minyak berwarna putih kekuning-kuningan yang diperoleh dari
proses ekstraksi inti buah tanaman Elaeis guineensis Jacq (SNI 01-0003-1992),
sedangkan Crude Palm Oil (CPO) didapatkan dari ekstraksi daging sawit. Bagian
buah kelapa sawit dapat dilihat pada Gambar 1. Kedua jenis minyak tersebut akan
and Deodorized Palm Oil (RBDPO), RBDPKO, minyak goreng, minyak makan,
margarine, shortening dan lain sebagainya.
Gambar 1 Bagian-bagian buah kelapa sawit (FAO, 2006)
Minyak inti sawit mengandung berbagai komponen asam lemak.
Komposisi trigliserida yang mendominasi minyak inti sawit adalah trilaurin, yaitu
trigliserida dengan tiga asam laurat sebagai ester asam lemaknya. Minyak inti
sawit memiliki kandungan asam laurat yang tinggi dan kisaran titik leleh yang
sempit, sedangkan minyak sawit mentah hanya memiliki sedikit kandungan asam
laurat dan kisaran titik leleh yang luas. Minyak sawit mengandung asam lemak
jenuh asam palmitat (C16) sekitar (40-46%), kandungan asam lemak tidak jenuh
yaitu asam oleat (C 18:1) sekitar (39-45%) dan asam linoleat (7-11%), sedangkan
pada minyak inti sawit didominasi oleh asam laurat (46-52 %), asam miristat
(14-17%), dan asam oleat (13-19%). Kandungan asam lemak dalam kedua jenis
Tabel 2 Komposisi asam lemak minyak sawit dan minyak inti sawit
Asam Lemak Minyak kelapa sawit (%) Minyak inti sawit (%)
Asam kaprilat - 3 – 4
Asam kaproat - 3 – 7
Asam laurat - 46 – 52
Asam miristat 1.1 – 2.5 14 – 17
Asam palmitat 40 – 46 6.5 – 9
Asam stearat 3.6 – 4.7 1 – 2.5
Asam oleat 39 – 45 13 – 19
Asam linoleat 7 – 11 0.5 – 2
Sumber : Eckey (1995)
Minyak inti sawit memiliki kemiripan sifat dan komposisi asam lemak
dengan minyak kelapa, sehingga dalam penggunaannya dapat bersifat sebagai
bahan subtitusi. PKO dan minyak kelapa sering digunakan oleh industri oleokimia
sebagai bahan baku untuk menghasilkan produk surfaktan dan emulsifier.
Kandungan asam laurat yang cukup tinggi pada minyak inti sawit menjadi salah
satu kelebihan karena asam lemak ini memiliki khasiat bagi kesehatan tubuh.
Pengolahan minyak dari kelapa sawit ini akan mengalami peningkatan
seiring dengan semakin tingginya permintaan pasar dan majunya teknologi
rekayasa pengolahan minyak. Teknologi tersebut diharapkan dapat menghasilkan
produk yang dapat diaplikasikan di berbagai aspek industri pengolahan serta dapat
bersaing dengan produk minyak nabati lainnya di pasar dalam negeri maupun
internasional.
Gliserol
Gliserol, disebut juga gliserin, adalah suatu larutan kental yang memiliki
rasa manis, tidak berwarna, tidak memiliki bau, dan bersifat higroskopis. Gliserol
merupakan gula alkohol dan mempunyai tiga gugus hidroksil yang bersifat
hidrofilik sehingga dapat larut dalam air. Oleh karena itu, larutan kental ini
banyak digunakan sebagai pelembab pada kosmetik. Rumus kimia gliserol adalah
C3H8O3 dengan nama kimia propane-1,2,3-triol. Gliserol memiliki berat molekul
92. 10, massa jenis 1,261 g/cm3, titik didih 290oC, dan viskositas 1.5 Pa.s
Gambar 2 Struktur molekul gliserol
Gliserol dapat digunakan sebagai bahan dasar untuk pembuatan
monogliserida, digliserida, dan trigliserida melalui proses reaksi gliserolisis,
esterifikasi atau inesterifikasi secara kimia atau enzimatis. Bila suatu radikal asam
lemak berkaitan dengan gliserol maka akan terbentuk suatu monogliserida. Reaksi
asam lemak dan gliserol dapat dilihat pada Gambar 3. Trigliserida akan terbentuk
bila tiga asam lemak beresterifikasi dengan satu molekul gliserol (Winarno,
2002). Penggunaan gliserol akan menyebabkan reaksi keseimbangan menuju ke
arah kanan reaksi esterifikasi sehingga menghasilkan produk MAG yang cukup
tinggi (Fischer, 1998).
O
H2C-OH O H2C-O-C-R
HC-OH + HO-C-R HC-OH + H 1
2
H
O
2C-OH H2
Gliserol Asam lemak Monoasilgliserol air
C-OH
Gambar 3 Reaksi esterifikasi satu molekul asam lemak dengan satu gliserol (Winarno, 2002)
Monoasilgliserol
Monoasilgliserol atau MAG tersusun atas sebuah asam lemak dan dua
gugus hidroksil bebas yang menempel pada sebuah molekul gliserol. Bagian asam
lemaknya atau rantai asil lemaknya bersifat lipofilik dan dapat bercampur dengan
bahan-bahan yang berlemak, sedangkan grup hidroksilnya bersifat hidrofilik dapat
banyak digunakan dalam pangan, farmasi, dan industri kosmetik (Bornscheuer,
1995). MAG dan turunannya sebanyak 75% digunakan sebagai emulsifier pangan
di dunia dan di Amerika Serikat sekitar 100 juta kilogram digunakan per tahunnya
(Sagalowicz, 2006; Birnbaum, 1981 di dalam Chetpattananondh et al.., 2008).
Menurut Li dan Ward (1993) di dalam Bornscheuer (2005), MAG juga
bermanfaat untuk kesehatan, misalnya MAG yang mengandung n-3-PUFA seperti
EPA dan DHA positif mencegah kerusakan cardiovascular, dan
monopentadecanoglycerol digunakan sebagai bahan tambahan perawatan rambut.
Struktur molekul MAG dapat dilihat pada Gambar 4.
H2
H C OH
C O C R1
H2
Gambar 4 Monoasilgliserol C OH
Pada skala industri, MAG telah banyak diproduksi dengan menggunakan
metode gliserolisis kimia minyak/lemak dan gliserol. Reaksi gliserolisis kimia ini
dilakukan pada suhu tinggi (220 – 250o C) menggunakan katalis basa inorganik
dalam atmosfer gas nitrogen. Penggunaan suhu tinggi memiliki
Gliserolisis kimia komersial biasanya menghasilkan 30-60% MAG, 35-50%
DAG, 1-20% TAG, 1-10% asam lemak bebas dan logam garam basa (Damstrup
et al., 2006). Menurut WHO dan arahan EU, MAG dan DAG dari asam lemak
disyaratkan mengandung kurang lebih 70% MDAG, 30% MAG, dan maksimum
gliserol 7% (Damstrup et al., 2006). Untuk menghasilkan produk MAG dengan
kemurnian tinggi (90-95%), MAG sering dimurnikan dari campuran
kesetimbangan dengan distilasi.
beberapa
kelemahan, seperti warna gelap, rasa terbakar, dan mengkonsumsi energi yang
banyak.
Gliserolisis dengan katalis enzim lipase lebih banyak digunakan beberapa
tahun belakangan, hal ini dikarenakan teknologi yang digunakan lebih baik
membuat produksi MAG yang sensitif terhadap panas dengan asam lemak tidak
jenuh rantai panjang lebih mudah, dimana jika dilakukan dengan proses kimia
sulit dilakukan. MAG dari gliserolisis kimia menjadi bahan atau senyawa
potensial bagi industri dengan fungsional yang lebih baik atau profil nutrisi asam
lemak yang lebih sehat (Damstrup et al., 2005).
Reaksi gliserolisis enzimatis pada suhu rendah memiliki kelemahan karena
mengandung tiga fase, yaitu fase hidrofobik minyak, fase gliserol hidrofilik, dn
fase enzim padat. Karena enzim memiliki karakteristik hidrofilik, gliserol sering
mengikat partikel enzim dan membuat akses molekul minyak ke partikel enzim
menjadi sulit. Hal ini menyebabkan rendemen MAG menjadi relatif rendah dan
waktu reaksi tidak praktis dari sudut pandang industri.
Tabel 3 Kandungan MAG setelah reaksi gliserolisis dalam berbagai pelarut
Pelarut Kandungan MAG
Tidak menggunakan pelarut 0.0 + 0.00
Kloroform 0.0 + 0.00
n-Heptan 1.1 + 0.02
n-Heksan 1.4 + 0.03
Iso-oktan 1.5 + 0.17
Asetonitril 2.0 + 0.07
Toluen 2.9 + 0.20
2- Butanon 5.4 + 0.10
Aseton 11.5 + 0.73
Isopropanol 18.0 + 0.31
Etanol 21.0 + 0.18
3-Pentanon 29.4 + 0.26
Tert-Pentanol 64.9 + 1.12
Tert-Butanol 83.6 + 0.14
Sumber: Damstrup et al. (2005)
Pengunaan pelarut yang cocok pada sistem akan memperbaiki
bercampurnya substrat sehingga sistem akan homogen dan meningkatkan
konversi substrat, waktu reaksi, dan distribusi produk membentuk MAG
(Damstrup et al., 2005). Pelarut seperti n-heksan, n-heptan, dioksan, asetonitril,
aseton, isooktan, 2-metil-2 propanol butanol), 2-metil-2 butanol
(tert-pentanol), atau campuran beberapa pelarut akan berguna untuk reaksi
inesterifikasi lipase. Data pada Tabel 3 menunjukkan kandungan MAG setelah
gliserol/minyak, 5:1; waktu reaksi 150 menit; suhu 50o
MAG terdiri dari beberapa jenis, salah satu diantaranya adalah gliserol
monolaurat atau monolaurin adalah senyawa multifungsi dengan sifat sebagai
emulsifier dan antimikroba (Cotton dan Marshall, 1997). Monolaurin terbentuk
dari reaksi antara gliserol dan asam laurat. Keistemewaan dari monolaurin lainnya
adalah dapat menghambat sel vegetative Bacillus cereus (Cotton et al., 1997).
Penelitian-penelitian sebelumnya juga menunjukkan bahwa monolaurin dapat
menghambat aktivitas Listeria monocytogenes, B. stearothermophilus dan B.
subtilis (Kabara, 1983).
C; pelarut 50 ml/10 g
minyak; dosis enzim 30% (w/w minyak).
Transesterifikasi
Pembuatan MAG dapat dilakukan dengan menggunakan beberapa metode
seperti esterifikasi langsung, reaksi gliserolisis, serta dapat dilakukan secara
enzimatis maupun kimia. Esterifikasi merupakan reaksi antara asam karboksilat
dan alkohol untuk membentuk ester. Reaksi esterifikasi kimia sederhana dapat
dilakukan pada suhu tinggi tanpa menggunakan katalis dan pada suhu yang lebih
rendah dilakukan dengan katalis.
Reaksi esterifikasi langsung terjadi antara ester asam lemak dengan gliserol
dan dilakukan pada suhu tinggi dan waktu yang cukup lama dengan bantuan
katalis asam. Penggunaan suhu yang terlalu tinggi sangat dihindari karena akan
terjadi reaksi sekunder yaitu polimerisasi gliserol, dehidratasi gliserol dengan
pembentukan akrolein. Air yang merupakan hasil samping dari reaksi esterifikasi
ini harus dijerap dengan menggunakan zat kimia tertentu agar reaksi tidak
reversible. Pada metode gliserolisis, lemak/ minyak dalam bentuk trigliserida
direaksikan dengan gliserol dan ditambahkan katalis kimia kemudian dipanaskan
pada suhu yang tidak terlalu tinggi (± 1200
Metode pembuatan MAG secara enzimatis dilakukan pada suhu yang lebih
rendah dibandingkan dengan metode kimia dikarenakan enzim yang digunakan
memiliki karakteristik kerja yang spefisik pada suhu tertentu. Tahapan reaksi C) atau tergantung tingkat kereaktifan
transesterisfikasi antara gliserol dan minyak atau lemak (reaksi gliserolisis) dapat
dilihat pada gambar di bawah ini.
Gambar 5 Reaksi esterisfikasi antara gliserol dan minyak atau lemak (reaksi gliserolisis). (Monteiro et al. 2003)
Reaksi inesterifikasi ini dapat terjadi secara acak maupun terarah. Secara
umum reaksi inesterifikasi dapat terjadi secara batch, semi-continously, atau
continously. Reaksi ini akan berjalan dengan empat tahapan, yaitu: perlakuan awal
minyak, penambahan katalis, terjadi reaksi, dan deaktivasi enzim. Reaksi terjadi
secara acak mengikuti hukum keseimbangan hingga menghasilkan komposisi
MAG, DAG, dan TAG tertentu.
Penggunaan katalis dalam reaksi inseterifikasi akan berpengaruh terhadap
peningkatan laju reaksi yang terjadi. Katalis yang digunakan dalam reaksi
inesterifikasi dapat berupa katalis kimia maupuan katalis enzimatis. Kedua jenis
katalis ini memiliki kelebihan dan kekurangan. Penggunaan katalis kimia lebih
banyak dilakukan, karena katalis kimia memiliki kelebihan antara lain mudah
penanganannya, harganya yang murah, mudah dipisahkan, dan dapat digunakan
dalam konsentrasi yang relatif rendah. Namun penggunaan katalis kimia pun
memiliki kekurangan antara lain terjadinya variasi produk yang beragam karena
gugus asil terdistribusi dengan acak. Menurut Bornscheuer (1995), produk hasil
sintesis secara kimiawi memiliki rendemen yang rendah, warna yang gelap, dan
Penggunaan katalis enzimatis mulai dilirik untuk memperbaiki kekurangan
yang terdapat pada penggunaan katalis kimia. Katalis enzimatis memiliki
keunggulan antara lain produk yang dihasilkan tidak memiliki keragaman besar.
Hal ini dikarenakan penggunaan enzim lipase memiliki kespesifikan tertentu
artinya enzim ini akan memotong ikatan antara gliserol dan asam lemak pada titik
tertentu (Elizabeth dan Boyle, 1997). Sintesis MAG enzimatis dapat dilakukan
dengan hidrolisis, esterifikasi asam lemak, transesterifikasi ester asam lemak dan
gliserolisis minyak atau lemak dengan katalis lipase. Kelemahan metode
enzimatis ini adalah harga enzim yang relatif mahal dan bersifat labil. Namun,
dengan berkembangnya teknologi enzim imobil, enzim dapat digunakan ulang
sampai beberapa kali sehingga mengurangi biaya keseluruhan. Sifat labil enzim
dapat diatasi dengan berkembangnya teknik enzimologi mikroakueus dimana
stabilitas enzim dapat ditingkatkan (Hariyadi, 1996). Mikroakueus adalah kondisi
lingkungan reaksi dengan konsentrasi air terbatas, yaitu tidak lebih dari 0.1% v/v.
Kondisi ini akan mempermudah reaksi sintesis produk, isolasi produk, dan
pemakaian ulang enzim. Kondisi mikroakueus dapat diterapkan dengan
menggunakan pelarut organik sebagai pengganti air dalam reaksi. Kehadiran air
dalam campuran reaksi dapat membentuk asam lemak bebas yang tidak
diinginkan (Damstrup et al., 2005)
Damstrup et al. (2005) telah melakukan penelitian memproduksi MAG
secara enzimatis dengan reaksi gliserolisis menggunakan pelarut organik yang
sesuai. Beberapa pelarut murni dan campuran digunakan dalam sistem reaksi
batch yang menggunakan 5.26 g gliserol, 10 g minyak bunga matahari, 50 ml
pelarut, 3 g Novozym® 435 lipase, suhu reaksi 50o C, selama 150 menit. Dari 13
pelarut yang diuji tert-butanol dan tert-pentanol adalah pelarut murni yang cocok
untuk reaksi gliserolisis cepat dengan menghasilkan kandungan MAG 68-82%.
Pada tahun berikutnya, Damstrup et al. (2006) melakukan penelitian kembali
dengan memproduksi MAG secara gliserolisis enzimatis dalam pelarut tert-
pentanol dengan optimasi menggunakan RSM (Response Surface Methodology).
Bahan yang digunakan adalah 10 g minyak bunga matahari, berbagai rasio
substrat, dan berbagai jumlah pelarut dalam sistem pada suhu 50o C, serta
dosis enzim, waktu reaksi, rasio substrat gliserol/minyak, dan jumlah pelarut.
Parameter yang paling signifikan dalam pengujian untuk menghasilkan MAG
adalah dosis enzim dan waktu reaksi. Kondisi optimal yang menghasilkan
rendemen MAG tinggi adalah dosis enzim 18 % (w/w minyak); rasio
gliserol/minyak 7:1 (mol/mol); jumlah pelarut 500 ml (v/w minyak)dan waktu
reaksi 115 menit. Kandungan MAG yang dihasilkan adalah 76%.
Monteiro et al. (2003) melakukan penelitian reaksi esterifikasi enzimatis
dengan substrat asam laurat dan gliserol (rasio molar 1:5) dalam sistem
homogenus dengan katalis enzim Lipozyme IM. Aktivitas enzim Lipozyme IM
adalah 5-6 BAUN/g (Batch Acidolysis Units Novo). Pelarut yang digunakan
adalah heksan dan tert-butanol (1:1 v/v). Hasil reaksi pada sistem homogenus
n-heksan/tert butanol (1:1 v/v) lebih baik karena produk yang dihasilkan adalah
monolaurin dengan sedikit sekali dilaurin. Sedangkan pada reaksi menggunakan
pelarut heksan saja, produk yang dihasilkan adalah campuran monolaurin dan
dilaurin. Hal ini berarti penggunaan campuran pelarut tert butanol dan heksan (1:1
v/v) dapat meminimalisir terjadinya migrasi asil. Sistem pelarut menjadi lebih
polar dari heksan murni menyebabkan pengambilan air dari medium sehingga
mencegah terjadinya inaktivasi enzim dan meningkatkan konversi substrat
menjadi produk yang diinginkan. Konversi asam laurat menjadi monolaurin
dianalisis menggunakan GC dengan waktu retensi 22 menit sebesar 65% selama 8
jam reaksi.
Haryati et al. (2007, tidak dipubilkasikan) melakukan penelitian reaksi
esterifikasi dilakukan dengan mereaksikan substrat yaitu asam lemak laurat dan
gliserol. Asam lemak laurat dan gliserol direaksikan dalam tabung erlenmeyer
sebanyak 1:5 (mol/mol substrat), ditambah campuran pelarut heksan 250 ml dan
tertier butanol 190 ml, kemudian diagitasi menggunakan orbital shaker dengan
kecepatan 200 rpm. Reaksi dilakukan pada suhu 50o C. Setelah suhu reaksi yang
diinginkan dalam rotary shaker tercapai, ditambahkan enzim lipase dengan
perbandingan 5% (w/w minyak). Reaksi dibiarkan berjalan hingga 55 jam.
Kemudian produk dari enzim dipisahkan dengan cara disaring, kemudian filtrat
pada suhu 7o
Suhu dan waktu reaksi merupakan faktor penting dalam reaksi esterifikasi.
Suhu dan waktu reaksi dijadikan sebagai parameter dalam penelitian ini.
Pemilihan suhu reaksi 50
C. Pemisahan endapan yang merupakan produk hasil fraksinasi
kemudian dilakukan dengan cara penyaringan.
o
Tabel 4 Perbandingan kondisi reaksi esterifikasi menggunakan enzim lipase C dalam reaksi esterifikasi enzimatis telah banyak
dilakukan oleh beberapa peneliti seperti ditunjukkan pada Tabel 4. Sedangkan
pemilihan waktu reaksi 55 jam adalah berdasarkan hasil penelitian terdahulu pada
sintesis monolaurin (Haryati et al., 2007, tidak dipublikasikan).
Parameter Kitu (2000)
Arbianti
et al. (2008) Nuraeni (2008) Damstrup, et al. (2006) Watanabe, et al. (2003)
Substrat 10 g DALMS: 14 g gliserol Asam laurat: gliserol 3:3 DALMS: gliserol 2:3 (mol/mol) Sunflower oil: gliserol 1:7 (mol/mol) Minyak kaya DAG: gliserol 2:1
Jumlah Enzim 1,2 g Sumber lipase biji wijen 90% dari berat substrat
4 % (w/w dari total substrat)
18% (w/w oil)
5% (bk)
Kondisi reaksi Shaker 200 rpm, suhu 60o
Suhu 53
C, 4 jam
o
Shaker 250 rpm, suhu 50 C, 18
jam o
Suhu 50
C, 5 jam
o
Suhu 50 C, 115
menit
o
C, 7 hari
Kromatogram GC untuk standar 1-monolaurin menunjukkan puncak
dengan waktu retensi 11,074 menit (Luas Area 9,32068%) dan 11,709 ( Luas
Area 90,67392%). Adanya dua puncak pada standar tersebut kemungkinan
dikarenakan oleh bentuk isomernya. Berdasarkan waktu retensi puncak standar,
Haryati (2007, tidak dipublikasikan) menyimpulkan bahwa produk yang
dihasilkan pada kromatogram GC dengan waktu retensi 11,162;11,973; 12,210,
dan 12,536 menit dengan luas area total adalah 73,69194 % adalah monolaurin,
sedangkan pada puncak dengan waktu retensi 18,723 DAG dengan luas area
hasil analisis LC-MS terhadap diester yang diperkirakan dilaurin, menghasilkan
kromatogram dengan puncak dominan pada waktu retensi 17,8 menit.
Gambar 6 Kromatogram GC untuk sintesis monolaurin dengan reaksi esterifikasi enzimatis secara batch (Haryati et al., 2007, tidak dipublikasikan)
Enzim Lipase
Lipase (triasilgliserol ester hidrolase, EC. 3.1.1.3) adalah enzim yang
memilki kemampuan mensintesis minyak atau lemak. Lipase juga mengkatalisis
hidrolisis triasilgliserol pada interfase minyak dalam air dan akan membentuk
ikatan ester pada lingkungan dengan kondisi sedikit air. Reaksi yang mungkin
terjadi pada kondisi lingkungan tersebut adalah esterifikasi, transesterifikasi,
polimerisasi, laktonisasi (Divakar dan Manohar, 2007). Lipase sebagai katalis
dapat diperoleh dari berbagai organisme seperti tanaman, hewan, dan
mikroorganisme. Lipase komersial yang tersedia saat ini terutama diperoleh dari
mikroorganisme seperti bakteri, kapang, dan khamir. Pada umumnya lipase dari Waktu Retensi (menit)
R
es
pon D
et
ekt
hewan dan tumbuhan memiliki stabilitas termal yang lebih rendah daripada lipase
mikrobial, sehingga industri lebih banyak menggunakan lipase dari
mikroorganisme. Mikroorganisme penghasil lipase dari bakteri antara lain P.
Flourescens, S. Carnosus, B. Stearothermophillus, C. Viscocum. Lipase yang
berasal dari kapang adalah A. Niger, R. Miehei, R. Delemar. Sedangkan lipase dari
khamir dapat diperoleh dari C. Cylindriceae, C. Auriculariae, C. Curvata, dan
Hansenula aromala (Borgstrom et al., 1984).
Beberapa jenis lipase yang dapat mengkatalisis reaksi esterifikasi adalah R.
Miehei, A. Niger, R. Delemar, G. Candidum, P. Camembertii, R. Arrhizus, C.
Antartica, Pseudomonas sp., C. Viscosum. Lipase-lipase tersebut telah diteliti
dapat menghasilkan MAG sebagai produk utama pada beberapa jenis substrat
(Bornscheuer, 1995). Novozym®
Reaksi yang dikatalisis oleh enzim lipase berlangsung pada sisi aktif enzim.
Menurut Brady et al. (1990) di dalam Hariyadi (1995), sisi aktif lipase terdiri dari
trio residu asam amino yaitu Ser-Asp-His. Dalam struktur enzim, sisi aktif ini
tersembunyi di balik suatu tutup, yaitu polipeptida yang sering disebut lid enzim.
Secara fisiologis lid enzim tersebut berfungsi untuk mencegah kerusakan
proteolitik asam-asam amino sisi aktif, yang akan berdampak negatif terhadap
aktivitas enzim. Lid bersifat fleksibel dan pada waktu membuka menyebabkan
substrat dapat mencapai sisi aktif enzim. Lid mengandung residu triptofan (Trp)
yang bersifat nonpolar. Pada saat enzim inaktif, sisi aktif lipase masih berada
dalam keadaan tertutup karena lid berinteraksi dengan residu hidrofobik di sekitar
inti katalitik. Keberadaan lingkungan hidrofobik (nonpolar) di sekitar enzim akan
memberikan kesempatan bagi lid untuk membuka, karena adanya interaksi antara
area nonpolar lid dengan lingkungan hidrofobik. Perubahan struktur yang 435 yang disuplai oleh Novozymes A/S
(Bagsvaerd, Denmark) adalah lipase komersial yang berasal dari C. Antartica
yang diproduksi submerged fermentation rekayasa genetik dari mikroorganisme
Aspergillus oryzae dan diabsorbsi dalam macroporous resin (Damstrup et al.,
2006). Candida antartica termasuk kedalam kelompok enzim yang
selektifitasnya tidak signifikan dan mengkatalisis reaksi gliserol pada tiga posisi
menyebabkan terbukanya sisi aktif ini, menyebabkan substrat mudah untuk
berafinitas dengan sisi aktif lipase, sehingga terjadi proses katalisis.
Stabilitas Enzim Lipase Imobil
Stabilitas enzim dapat diartikan sebagai kestabilan aktivitas enzim selama
penyimpanan dan penggunaan enzim tersebut,serta kestabilan terhadap senyawa
yang bersifat merusak seperti pelarut tertentu (asam,basa) dan oleh pengaruh suhu
atau pH ekstrim. Stabilitas merupakan sifat penting yang harus dimiliki oleh
enzim dalam aplikasinya sebagai biokatalis. Pasa prinsipnya, ada dua cara yang
dapat ditempuh untuk memperoleh enzim yang mempunyai stabilitas tinggi yaitu:
(1) menggunakan enzim yang memiliki stabilitas ekstrim alami; (2)
mengusahakan peningkatan stabilitas enzim yang secara alami tidak/ kurang
stabil. Peningkatan stabilitas dapat ditempuh melalui: (a) imobilisasi enzim; (b)
modifikasi kimia; dan (c) protein engineering (Janecek, 1993). Lipase merupakan
enzim yang memiliki peran yang penting dalam bioteknologi modern. Banyak
industri yang telah mengaplikasikan penggunaan enzim sebagai biokatalis. Lipase
terkenal memiliki aktivitas yang tinggi dalam reaksi hidrolisis dan dalam kimia
sintesis. Lipase dapat berperan sebagai biokatalis untuk reaksi hidrolisis,
esterifikasi, alkoholisis, asidolisis atau aminolisis. Candida dan Rhizopus yang
merupakan organisme yang paling sering dipakai sebagai sumber sintesis
penghasil lipase (Pandey et al., 1999).
Enzim Lipase akan mengkatalis reaksi pada interfase, dan untuk
menghasilkan kecepatan reaksi yang tinggi, maka area interfase antara reaktan dan
fase enzim yang lebih hidrofilik dibutuhkan. Hal ini dapat dicapai dengan
produksi dispersi lipase yang baik dalam fase organik misalnya dengan
menggunakan surfaktan atau dengan mengimobilisasi enzim pada partikel
pendukung macroporous. Imobilisasi lipase biasanya dipilih untuk proses
inesterifikasi (Rozendaal, 1997). Imobilisasi lipase akan memperbaiki stabilitas,
pemisahan produk, dan pemisahan enzim dari reaksi untuk digunakan kembali
(Nawani et al., 2006).
Penggunaan enzim lipase dalam reaksi esterifikasi untuk menghasilkan
daripada dengan katalis kimia. Hanya saja secara ekonomis penggunaan katalis
enzim lipase lebih mahal. Untuk mengatasi masalah ini enzim lipase digunakan
pada fase imobil sehingga dapat digunakan berulang-ulang dan memungkinkan
untuk diaplikasikan pada proses circulated packed bed reactor. Dengan
perkembangan teknologi peneliti dari Novozymes A/S, Bagsvaerd, Denmark telah
berhasil memproduksi Novozyme®
Enzim lipase imobil menjadi pilihan dalam reaksi untuk mencapai
kecepatan reaksi inesterifikasi. Enzim imobil dilakukan dengan cara
mengadsorpsi enzim ke dalam partikel macroporous dengan interaksi ionik atau
hidrofobik, karena protein tidak dapat larut dalam reaksi campuran. Partikel
macroporous harus memiliki area yang cukup pada permukaan dalam untuk
mengadsorpsi sejumlah lipase dan area permukaan bahan sekitar 10-100 m 435 yang diklaim sebagai enzim yang
harganya terjangkau. Lipase imobil ini kemudian dikomersialisasikan untuk
memenuhi kebutuhan produksi komoditas minyak dan lemak.
2
Enzim imobil yang digunakan pada penelitian ini adalah Novozyme
/g
yang normal digunakan. Diameter rata-rata pori partikel pendukung > 100 nM
banyak dipilih. Kemudian asal bahan kimia permukaan partikel juga penting
diperhatikan.
®
435.
Novozyme® 435 dibeli dari Novozymes A/S (Bagsvaerd, Denmark) adalah lipase
komersial yang berasal dari C. Antartica yang diproduksi rekayasa genetik dengan
submerged fermentation dari mikroorganisme Aspergillus oryzae dan diadsorbsi
dalam macroporous resin (Damstrup et al., 2006). Novozyme®
Novozyme
435 adalah
katalis yang stabil pada suhu tinggi dan pelarut organik. Bisa digunakan pada
operasi reaksi batch dan column tapi khususnya cocok digunakan untuk fixed-bed
reactor.
®
435 digunakan sebagai esterase untuk memproduksi spesifik
ester seperti yang digunakan di industri kosmetik pada suhu proses rendah. Enzim
ini juga digunakan dalam re-sintesis lemak dari gliserol dan asam lemak dimana
asam lemak spesifik dimasukkan. Dengan mengoperasikan pada suhu relatif
rendah (60-70o C), pembentukan produk samping dapat diminimumkan dan akan
Stabilitas enzim merupakan parameter penting dalam reaksi, hal ini
dikarenakan harga enzim yang mahal. Oleh karena itu recovery dan penggunaan
kembali (re-use) dari reaksi sangat dibutuhkan. Kehilangan aktivitas enzim
selama reaksi inesterifikasi dikarenakan dua faktor, yaitu inaktivase enzim lipase
dan kontaminasi dari komponen minor dalam reaktan. Kontaminasi reaktan dapat
dicegah dengan cara penyaringan reaktan secara hati-hati, sedangkan ketahanan
enzim pada suhu tinggi adalah syarat mutlak sebagai katalis.
Nawani, et al. (2006) telah melakukan penelitian tentang imobilisasi
enzim dan stabilitas lipase dari enzim thermofilik yang berasal dari Bacillus sp.
Beberapa uji dilakukan untuk melihat stabilitas dari enzim imobil antara lain uji
kestabilan enzim pada suhu tinggi. Enzim yang diuji adalah enzim dalam aqueous,
diimobilisasi, dan dimobilisasi dengan cross linked pada suhu 0-80o C.
Gambar 7 Pengaruh suhu pada enzim aqueous, imobil, dan imobil cross link (Nawani et al., 2006)
Data pada Gambar 7, .menunjukkan bahwa enzim imobil lebih stabil pada
reaksi suhu tinggi. Kemudian dilakukan juga uji stabilitas enzim dalam siklus
yang circulated packed bed reactor. Metode pengujian mengacu pada
Sigurgisladottir et al. (1993), yaitu enzim yang diimobilisasi dengan Silica dan
HP 20 diuji dalam 25 siklus masing-masing selama 30 menit. Pada setiap siklus, 2
ml campuran reaksi mengandung substrat ditambahkan enzim imobil dan
diinkubasi selama 30 menit dengan shaker yang kontinyu pada suhu 60o C.
Kemudian di sentrifuse dan supernatan diukur absorpsinya pada 420 nm.
Endapan dicuci dengan 0,05 M buffer fosfat (pH 8.0) dan digunakan dalam siklus
berikutnya dengan prosedur yang sama. Hasil pengujian penggunaan enzim dalam
Tabel 5 Retensi aktivitas lipase dalam penyangga padat pada siklus yang berbeda
No
Padatan penyangga
Sisa Aktivitas Enzim (%)
5 siklus 10 siklus 15 siklus 20 siklus 25 siklus
1 HP 20 100 93 86 79 71
2 Silica 100 89 78 58 46
(Sigurgisladottir et al., 1993)
Berdasarkan Tabel di atas, Lipase dalam penyangga padat (imobil) pada
siklus 10 kali belum mengalami penurunan aktivitas enzim yang signifikan.
Menurut penelitian Fernandez-Lorente, et al. (2001) Lipase imobil yang berikatan
hidrofobik dapat digunakan dalam 10 kali reaksi esterifikasi tanpa penurunan
yang signifikan sebagai biokatalis. Yang et al. (2006) melaporkan bahwa stabilitas
enzim pada operasi reaksi gilserolisis minyak bunga matahari secara kontinyu
aktivitas lipase (novozyme 435) cukup stabil selama 31 hari reaksi (Gambar 8).
Tidak terdeteksi asam lemak bebas setelah 15 hari reaksi. Tidak ada penurunan
aktivitas lipase hingga hari terakhir reaksi.
Gambar 8 Stabilitas reaksi kontinyu Novozyme®
gliserolisis minyak bunga matahari. Kondisi reaksi:
435 mengkatalisis
gliserol/minyak 3.5:1 (mol/mol), suhu 40 C, waktu tinggal 40 menit, dan tert butyl alcohol/minyak 2:1 (w/w)
(Yang et al., 2006)
Yang et al. (2003), melakukan penelitian penggunaan ulang Novozyme®
435 dengan recovery lipase pada reaksi esterifikasi dan menggunakan kembali
enzim hasil recovery pada percobaan selanjutnya. Seperti terlihat pada gambar 8,
batch. Sekitar 90% dari aktivitas enzim (selama pembentukan MAG)
dipertahankan setelah 14 kali reaksi (Gambar 9).
Gambar 9 Kandungan MAG vs jumlah reaksi batch pada penelitian penggunaan kembali Novozyme®
reaksi sama (Yang et al., 2003)
METODOLOGI PENELITIAN Waktu Dan Tempat Penelitian
Penelitian dilaksanakan mulai bulan Juni 2010 sampai dengan Februari
2011 bertempat di Laboratorium Kimia SEAFAST Center IPB dan Laboratorium
Kimia Pangan Departemen Ilmu dan Teknologi Pangan (ITP), IPB .
Bahan Dan Alat
Bahan baku untuk sintesis monolaurin adalah asam lemak laurat teknis
komersial, gliserol, enzim lipase Novozyme® 435 dari Novozymes A/S
(Bagsvaerd, Denmark), standar monolaurin dari Sigma, heksan teknis, dan
tert-butanol p.a (Sigma). Bahan kimia yang digunakan (NA2S2O3
Alat-alat yang digunakan dalam penellitian ini adalah rangkaian reaktor
packed bed yang dilengkapi dengan tangki stok, pompa peristaltik (BT 100-1 F),
waterbath (Stephen Haake, Germany) serta wadah penampung produk,
serangkaian peralatan GC (Gas Chromatography) dengan detektor FID (Flame
Ionization Detector), GC-MS Pyrolisis, neraca analitik, Aw-meter (Shibaura
WA-360), pH meter, kertas saring dan peralatan gelas.
) 0.1N, larutan
Wijs, larutan Alkohol 95%, indikator PP dan pati, Larutan NaOH 0.01N, larutan
kloroform, Dimetil formamida (DMF), benzena, dan aquades.
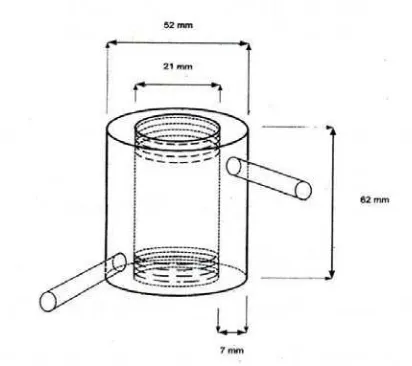
Reaktor packed bed yang digunakan dalam penelitian ini dibuat sesuai
dengan disain pada Gambar 10. Reaktor dibuat dari bahan gelas dan dibuat
berjaket untuk sirkulasi air dari waterbath, sehingga suhu reaktor dapat
dipertahankan. Reaktor juga dilengkapi dengan filter pada bagian atas dan bawah
untuk memisahkan antara enzim dan substrat. Tinggi reaktor 62 mm, diameter
luar 52 mm, diameter dalam 21 mm dan volume kosong 16,5 mililiter. Volume
kerja reaktor 15 mililiter setelah diisi enzim novozyme sebanyak 4,6 gram.
Volume kerja reaktor ditentukan dengan cara menghitung waktu yang diperlukan
oleh substrat dengan laju aliran tertentu untuk mengalir melalui reaktor packed
bed yang berisi enzim novozyme. Hasil perkalian antara waktu untuk mengalir
Gambar 10 Desain reaktor
Skema proses produksi MAG secara circulated packed bed reactor dapat
dilihat pada Gambar 12. Rangkaian alat esterifikasi enzimatis menggunakan
reaktor packed bed dapat dilihat pada Gambar 11 dimana substrat dari wadah
reaktan (B) dialirkan dengan laju tertentu ke dalam reaktor packed bed yang berisi
enzim lipase (A) menggunakan pompa peristaltik(E). Produk yang dihasilkan
ditampung dalam wadah produk (C).
Keterangan : A. Reaktor Enzim B. Wadah Reaktan C.Wadah Produk D. Waterbath
E. Pompa Peristaltik
Gambar 11 Rangkaian alat reaksi esterifikasi menggunakan Reaktor Packed Bed (Soekopitojo, 2003)
[image:35.595.134.472.438.658.2]
Gambar 12 Skema alur reaksi esterifikasi enzimatis circulated packed bed reactor
Metode Penelitian Analisis Sifat Kimia Bahan Baku
Asam laurat dan enzim yang digunakan dalam proses esterifikasi dianalisis
terlebih dahulu untuk menentukan kualitas bahan baku. Analisis yang dilakukan
meliputi kadar air, asam lemak bebas (ALB), dan bilangan peroksida. Enzim
dilakukan karakterisasi terlebih dahulu dengan dilakukan pengukuran pH dan Aw
enzim.
Uji Coba Reaksi Sintesis Monolaurin Secara Batch
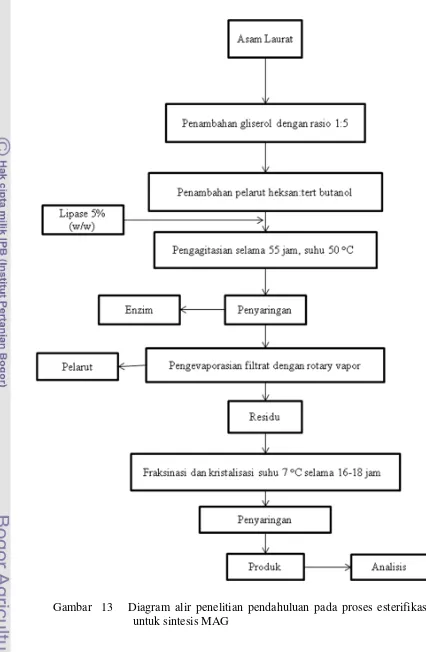
Uji coba hasil penelitian mengacu pada metode penelitian terdahulu. Proses
esterifikasi dilakukan dengan mereaksikan substrat yaitu asam lemak laurat dan
gliserol (Gambar 12). Asam lemak laurat dan gliserol direaksikan dalam tabung
erlenmeyer sebanyak 1 : 5 (mol/mol substrat), ditambah campuran pelarut
organik, kemudian diagitasi menggunakan orbital shaker dengan kecepatan 200
rpm. Reaksi dilakukan pada suhu 50o
Setelah suhu reaksi yang diinginkan dalam rotary shaker tercapai,
ditambahkan enzim lipase dengan perbandingan 5% (w/w minyak). Reaksi
dibiarkan berjalan hingga 55 jam. Kemudian produk dari enzim dipisahkan
dengan cara disaring, kemudian filtrat disentrifuse untuk memisahkan dari pelarut.
Setelah itu di fraksinasi 16-18 jam pada suhu 7 C.
o
C. Endapan yang merupakan
[image:37.595.80.506.66.718.2]
Optimasi dan Verifikasi Reaksi Esterifikasi untuk Sintesis Monoasilgliserol dalam Circulated Packed Bed Reactor
Konversi Reaksi Esterifikasi Proses Batch ke Circulated Packed Bed Reactor Sebelum dilakukan optimasi reaksi, terlebih dahulu dilakukan konversi dari
proses batch ke proses circulated packed bed reactor. Hasil dari proses batch
dipilih yang memiliki hasil dengan kadar MAG dan rendemen tertinggi, serta
rasio substrat dan pelarut yang efektif untuk dilakukan proses secara circulated
packed bed reactor.
Optimasi Reaksi Esterifikasi Circulated Packed Bed Reactor
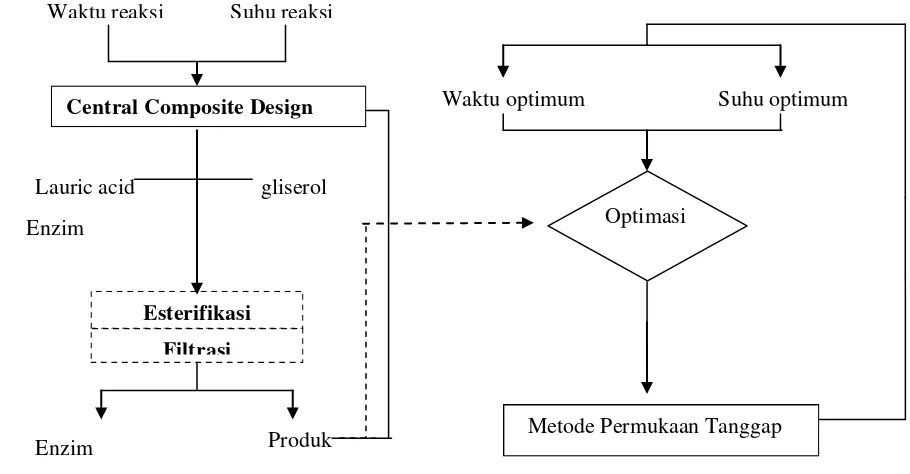
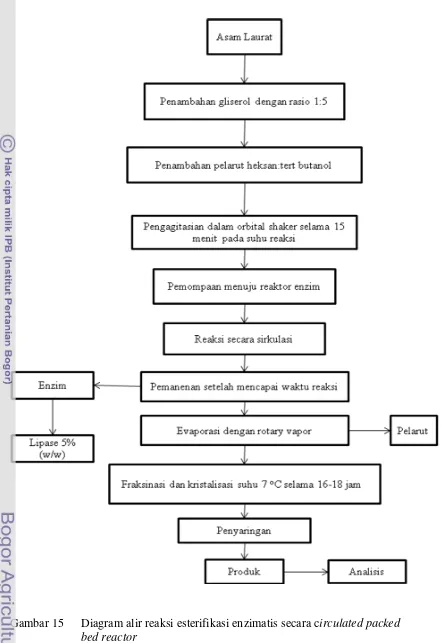
Pada tahap ini dilakukan penelitian untuk mencari kondisi optimum proses
esterifikasi enzimatis secara circulated packed bed reactor yang dapat
menghasilkan produk dengan kadar MAG tinggi. Diagram alir tahap optimasi dan
proses reaksi esterifikasi dapat dilihat pada Gambar 14 dan 15. Rancangan
percobaan yang digunakan pada tahap ini mengikuti rancangan Central
Composite Design (CCD) dari Respon Surface Methodology (RSM) dengan dua
variabel yaitu waktu dan suhu reaksi esterifikasi.
Penentuan titik tengah diambil dari reaksi circulated packed bed reactor
yang menghasilkan kadar MAG dan rendemen terbaik serta dari referensi literatur.
Sebagai contoh perlakuan dan kode perlakuan, serta rancangan percobaan
Gambar 14 Diagram alir proses optimasi sintesis monolaurin dengan metode circulated packed bed reactor
Tabel 6 Perlakuan dan kode perlakuan untuk reaksi esterifikasi
Perlakuan Kode perlakuan
-1,414 -1 0 1 1,414
Suhu 45 oC 46,5 oC 50oC 53,5 oC 55 oC Waktu 1jam 1,3 jam 2 jam 2,7 jam 3 jam
Tabel 7 Rancangan percobaan dengan sistem pengkodean No Suhu ( C) Waktu Reaksi (jam)
1 -1 -1
2 1 -1
3 -1 1
4 1 1
5 -1,414 0
6 1,414 0
7 0 -1,414
8 0 1,414
9 0 0
10 0 0
11 0 0
12 0 0
13 0 0
Sumber : Cochran dan Cox (1962)
Enzim
Enzim
Lauric acid gliserol
Produk
Optimasi
Central Composite Design
Waktu reaksi Suhu reaksi
Metode Permukaan Tanggap
Esterifikasi Filtrasi
Rancangan Percobaan
Rancangan percobaan yang digunakan adalah Central Composite Design.
Model Respon Surface digunakan untuk melihat pengaruh perlakuan waktu dan
suhu reaksi terhadap rendemen produk dan komposisi MAG dalam produk. Titik
tengah perancangan penelitian diambil dari suhu dan waktu reaksi pada hasil
penelitian pendahuluan.
Model Response Surface Methodology atau RSM adalah kumpulan teknik
matematika dan statistik yang digunakan untuk membentuk model dan
menganalisis masalah dalam suatu respon yang dipengaruhi oleh beberapa peubah
dan bertujuan untuk mengoptimalisasi respon tersebut. RSM digunakan untuk
mengetahui hubungan antara faktor percobaan dengan variabel respon.
Berdasarkan hubungan tersebut dapat diperoleh nilai faktor percabaan yang akan
menghasilkan nilai variabel respon yang dikehendaki. Seluruh perlakuan terdiri
dari 13 set percobaan, dimana model umum rancangan percobaan yang digunakan
adalah:
k k k -1,k
Y = β
o+
Σ
β
iX
i+
Σ
β
iiX
i2
+
Σ
β
i,jX
ii=1 i=1 i=1,j=2
Xj +
ε
Keterangan:
Y = Respon Pengamatan
β
oβ
i = = Interceptβ
ii = Pengaruh linierβ
ij Pengaruh kuadratikXi = Kode untuk faktor ke-i = Pengaruh interaksi percobaan
Xj = Kode untuk fakyor ke-j k = Jumlah faktor yang dicobakan
Verifikasi Kondisi Optimum Reaksi Esterifikasi Circulated packed bed reactor
Tahap verifikasi merupakan tahap pengujian terhadap kondisi proses
optimum. Verifikasi dilakukan dengan maksud untuk memperbaiki tingkat
keyakinan bahwa berdasarkan kondisi optimum yang diasumsikan, model yang
dikembangkan dapat mewakili sistem yang sebenarnya. Verifikasi dilakukan
dengan cara mengaplikasikan kondisi proses tersebut sebanyak lima kali ulangan,
Tujuan verifikasi adalah melihat konsistensi produk yang dihasilkan berdasarkan
pada nilai CV (Coeficeient Varians). Parameter yang dianalisis pada tahap
verifikasi adalah komposisi MAG dan rendemen.
Uji Stabilitas Enzim Novozyme 435 pada Reaksi Esterifikasi Circulated packed bed reactor
Uji stabilitas enzim dilakukan setelah didapatkan kondisi optimum proses
esterifikasi yang telah diverifikasi. Enzim dipisahkan dari substrat reaksi, setelah
itu dilakukan pencucian dengan pelarut ± 50 ml, dikering anginkan dan disimpan
di refrigerator pada kondisi tertutup rapat jika tidak langsung digunakan,
kemudian enzim digunakan kembali dalam reaksi dengan prosedur yang sama dan
dilakukan berulang. Reaksi pengulangan dilakukan 10 kali dengan parameter yang
dianalisa adalah komposisi MAG. Diagram alir uji stabilitas enzim dapat dilihat
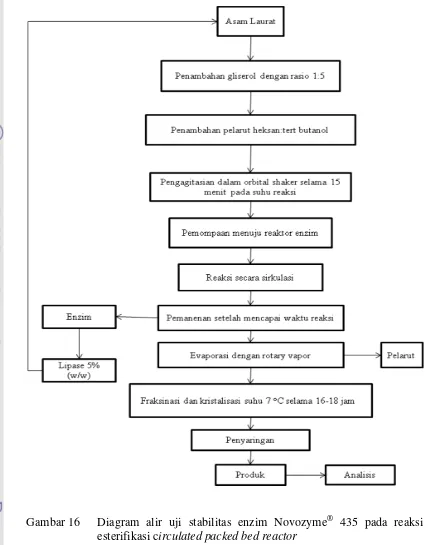
Gambar 16 Diagram alir uji stabilitas enzim Novozyme® 435 pada reaksi esterifikasi circulated packed bed reactor
Pengamatan
Bahan baku dan Produk MAG yang dianalisis merupakan produk hasil
kondisi optimum proses dalam sistesis esterifikasi enzimatis MAG. Tujuan
MAG yang dihasikan. Analisis yang dilakukan meliputi bilangan Peroksida, kadar
asam lemak bebas (ALB), Aw Enzim, pH enzim, analisis semi kuantitatif
komposisi Gliserida dengan GC, Titik Leleh, dan analisis kuantitatif komposisi
Gliserida produk dengan GC-MS Pyrolisis.
Analisis Kadar Air Dalam Minyak (AOAC,1995)
Sejumlah ± 5 g sampel dimasukkan ke dalam cawan yang telah diketahui
beratnya. Kemudian cawan dimasukkan ke dalam oven bersuhu 100o
KA =
C hingga
diperoleh berat yang konstan. Perhitungan kadar air dilakukan dengan
menggunakan rumus :
% 100 ) ( x c b a
c− −
dengan: a = berat cawan dan sampel (g) b = berat cawan dan sampel akhir (g) c = berat sampel awal (g)
Analisis Bilangan Peroksida, Metode Titrimetri (AOAC, 1995)
Contoh minyak ditimbang seberat 5 gram dan dimasukkan ke dalam
erlenmeyer tertutup dan diisi dengan gas N2. sampel ditambah dengan 55 ml
kloroform dan distirer kemudian ditambah asam asetat glasial sebanyak 20 ml.
Larutan KI jenuh ditambahkan sebanyak 0.5 ml kemudian ditutup dengan cepat,
digoyang selama 1 menit. Sampel disimpan di tempat yang gelap selama 5 menit
pada suhu 15oC sampai 25o
BP =
C. Setelah itu, sampel ditambahkan 30 ml air destilata.
Larutan tersebut dititrasi dengan larutan sodium thiosulfat 0.01N dan digoyang
dengan kuat. Larutan pati yang digunakan sebagai indikator ditambahkan ketika
warna kuning larutan hampir hilang dan titrasi diteruskan hingga warna biru
menghilang. Titrasi juga dilakukan terhadap blanko.
1000 ) ( x m xT Vb Vs−
Keterangan : BP = bilangan peroksida (meq O2
Vs = volume sodium thiosulfat untuk titrasi sampel (ml) /kg)
Analisis Kadar Asam Lemak Bebas (ALB) (AOAC, 1995)
Sampel ditimbang sebanyak 5 gram kemudian dilarutkan ke dalam 50 ml
etanol (alkohol) 95%. Larutan ini kemudian ditrasi dengan NaOH 0,01N dengan
indikator fenoftalein hingga terlihat warna merah muda selama 10 detik. Kadar
asam lemak bebas dihitung dengan menggunakan rumus perhitungan :
Kadar Asam =
m x M x T x V 10
Keterangan : V = volume (ml) KOH untuk titrasi
T = normalitas larutan KOH M = berat molekul sampel
m = jumlah sampel yang digunakan
Pengukuran pH Enzim (Hariyadi, 1995)
Sebanyak 0.5 gram enzim disuspensikan dalam 15 ml air destilata. Campuran
diaduk menggunakan magnetic stirer selama 2 menit dan diinkubasikan pada suhu
kamar (±28 o
Pengukuran A
C) selama 30 menit. Selanjutnya dilakukanpengukuran menggunakan
pH meter.
w
Pengukuran aktivitas air (A
enzim (Hariyadi, 1995)
w) enzim dilakukan secara langsung
menggunakan aw-meter Shibaura WA-60. Kalibrasi dilakukan garam NaCl
dengan Aw= 0.7509. Sebanyak 1 gram sampel enzim diletakkan pada tempat
sampel pada Aw-meter Shibaura WA-60. Selanjutnya Aw-meter ditutup dan
ditunggu sampai angka hasil pengukuran pada Aw
Analisa Komposisi Gliserida MAG Dengan Kromatografi Gas (Modifikasi
AOAC Official Method 993.18, 1995)
-meter konstan.
Sampel ditimbang teliti kurang lebih 0.2 mg dimasukkan dalam vial
kemudian ditambahkan 0.2 ml BSTFA [bis(trimethylsilil)trifluoro acetamide] dan
0.1 ml TMCS (trimethylchlorsilane) dan 0.1 ml larutan standart internal n-
tetradecana kemudian dikocok hati-hati dan dipanaskan pada suhu 70o C selama
seperti diatas untuk 0.1 ml larutan referensinya (MAG dan DAG) pada kondisi
operasi yang sama, peak yang muncul diidentifikasi dengan membandingkan
waktu retensi dari referensi. Larutan referensi dibuat dengan menimbang 0.2 mg
referensi dilarutkan dalam piridin menggunakan labu takar 10 ml. Kromatografi
gas yang digunakan dilengkapi dengan split injeksi atau kolom injeksi dan FID
dengan operasi sebagai berikut: suhu kolom awal 50o C dinaikkan menjadi 180o C
dengan kenaikan 15 o C/ menit kemudian dinaikkan lagi menjadi 230 o C dengan
kenaikan 7 o C/menit dan dinaikkan lagi menjadi 380 o C, suhu detektor 390 o C,
suhu injektor 390 o C, kecepatan gas pembawa 0.7 ml N2
Titik leleh (PORIM Test Method, 1995)
/menit, kecepatan aliran
udara 450 ml/menit dan volume injeksi 1 μl.
Titik leleh didefinisikan sebagai suhu dimana sampel menjadi cair dengan
sempurna. Produk mono dan diasilgliserol yang telah disaring dilelehkan dan
dimasukkan ke dalam tabung kapiler (3 buah) setinggi 1 cm. Selanjutnya
disimpan dalam refrigerator pada suhu 4-100C selama 16 jam. Ikatkan tabung
kapiler pada termometer dan masukkan termometer tersebut ke dalam beaker
glass (600 ml) berisi air distilasi (sekitar 300 ml). Atur suhu air dalam beaker
glass pada suhu 8 – 100C di bawah titik leleh sampel dan suhu air dipanaskan
pelan-pelan (dengan kenaikkan 0.50C – 10
Kandungan gliserol bebas (AOCS Official Method Ca 5a-40, 1998)
C/menit) dengan pengadukan (magnetic
stirrer). Pemanasan dilanjutkan dan suhu diamati dari saat sampel meleleh sampai
sampel naik pada tanda batas atas. Titik leleh dihitung berdasarkan rata-rata suhu
dari ketiga sampel yang diamati.
Sebanyak 5 g sampel ditimbang dalam gelas kimia 50 ml. Sampel
dipindahkan ke dalam labu ukur 250 ml dengan penambahan pelarut kloroform
sebanyak 22.5 ml. Sebanyak 125 ml air destilata ditambahkan ke dalam labu ukur
kemudian labu ditutup. Campuran dalam labu dikocok dengan kuat selama kurang
lebih 1 menit. Setelah dikocok, ditambahkan air destilata hingga tanda tera.
Campuran didiamkan beberapa menit hingga terbentuk dua lapisan. Fase air yang
kemudian ditambahkan asam periodat sebanyak 12.5 ml. Labu erlenmeyer dalam
keadaan tertutup alumunium foil. Larutan KI 15% ditambahkan ke dalam labu
kemudian didiamkan selama kurang lebih 1 menit. Ditambahkan sebanyak 100 ml
air destilata ke dalam labu erlenmeyer. Campuran dititrasi dengan menggunakan
larutan natrium tiosulfat 0.1 N hingga warna terbentuk warna kuning. Indikator
pati ditambahkan sebanyak 2 ml kemudian dititrasi kembali hingga warna
kompleks menghilang. Kandungan gliserol bebas dapat dihitung dengan rumus
sebagai berikut
((B-S) x N x 2,302)/W
Keterangan : B – volume titrasi blanko (ml) N – konsentrasi sodium tiosulfat (N) S – volume titrasi sampel (ml) W – berat sampel (g)
Analisa Komposisi Gliserida MAG Dengan Kromatografi Gas- MS Pyrolisis (Modifikasi Ralph et al., 1991)
Sampel, 200-500 µg, dipirolisis dalam tabung kuarsa dalam 120 Pyroprobe
(Chemical Data Systems) pada 600 oC (> 50o C / ms) selama 10 s menggunakan
gas helium sebagai carrier dengan kecepatan linier 20 ml / menit. Sampel dibawa
ke kolom DB-1 60 m X 0,25 mm (J & W Scientific) dipasang pada GC HP 5890
dalam mode splitless. Setting suhu di 80 oC selama 2 menit untuk menjebak dan
fokus komponen volatil, kemudian diprogram pada suhu akhir 275 oC pada 4 OC /
menit, dan waktu running lebih dari 60 min. Senyawa terselusi terdeteksi dengan
Hewlett-Packard 5970 selektif massa detektor dikendalikan oleh HP UNIX
stasiun data dan total ion kromatogram (TICS) terbentuk. Senyawa dielusi selama
HASIL DAN PEMBAHASAN Sifat Kimia Bahan Baku
Asam laurat yang akan digunakan dalam sintesis monolaurin ini harus
memenuhi persyaratan sebagai bahan baku yang meliputi kadar air, kadar asam
lemak bebas (ALB), dan bilangan peroksida. Tujuan analisa bahan baku ini adalah
untuk melihat mutu asam lemak terhadap karakteristik katalis yang digunakan.
Berdasarkan hasil analisis bahan baku, kadar air asam laurat adalah 0,3369 ±
0,017 % (bk). Semakin rendah kadar air yang terkandung dalam bahan baku maka
semakin baik, hal ini dikarenakan keberadaan air dalam bahan baku dapat
menghidrolisis enzim sehingga mengganggu jalannya reaksi esterifikasi.
Kandungan air awal sistem reaksi, jumlah enzim dan rasio mol substrat
merupakan faktor-faktor yang sangat penting dalam mempengaruhi hasil
esterifikasi (Linko et al., 1995). Kadar asam lemak bebas (ALB) bahan baku
adalah 98,9108 ± 0,3389 % , hal ini menunjukkan kandungan asam lemak bebas
yang terdapat pada bahan baku 98,9% adalah asam laurat. Bilangan peroksida
bahan baku asam laurat adalah 1,226± 0.07 meq O2/kg. Menurut De Greyt et al.
(1997), syarat bilangan peroksida yang terdapat pada bahan baku lebih rendah dari
10 meq O2
Komposisi asam lemak dalam bahan baku asam laurat dapat diketahui
kemurniannya dengan gas chromatography (GC). Asam laurat yang digunakan
sebagai bahan baku berdasarkan hasil kromatogram GC hanya memiliki satu
puncak pada waktu retensi 7,312 (Gambar 29a). Berdasarkan hasil GC kandungan
bahan baku adalah 100% asam laurat. Namun, hasil analisis ALB menunjukkan
kandungan asam laurat 99%, sedangkan 1% sisanya kemungkinan asam lemak
bebas lainnya dikarenakan bahan baku yang digunakan adalah asam lemak teknis.
Asam lemak lainnya tidak muncul pada kromatogram GC dikarenakan jumlah
yang terlalu kecil sehingga tidak terdeteksi oleh detektor FID. /kg.
Asam laurat merupakan asam lemak yang banyak terdapat pada minyak
kelapa dan minyak inti sawit. Asam laurat merupakan hasil fraksinasi atau
hidrogenasi dari pembuatan minyak kelapa atau minyak inti sawit. Menurut Kitu
(2000), kandungan terbesar Destilat Asam Lemak Minyak Kelapa adalah asam
didominasi oleh asam laurat (46-52 %) dan asam miristat (14-17%). Semakin
murni bahan baku asam lemak bebas maka reaksi esterifikasi diharapkan dapat
berjalan secara optimal