ISOLASI DAN NANOENKAPSULASI KAROTENOID
LIMBAH SERAT BUAH KELAPA SAWIT
RIAHNA BR KEMBAREN
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
RIAHNA BR KEMBAREN. Isolasi dan Nanoenkapsulasi Karotenoid Limbah
Serat Buah Kelapa Sawit. Dibimbing oleh LAKSMI AMBARSARI dan I MADE
ARTIKA.
Indonesia menghasilkan limbah serat buah kelapa sawit dalam jumlah
besar. Pemanfaatan limbah tersebut sebagai sumber karotenoid dapat
meningkatkan nilai ekonomi. Karotenoid mudah rusak jika terpapar suhu dan
intensitas cahaya yang tinggi. Upaya yang dapat dilakukan untuk meningkatkan
ketahanan karotenoid adalah nanoenkapsulasi dengan penyalut kitosan. Tujuan
penelitian ini adalah mengisolasi karotenoid dari limbah serat buah kelapa sawit
dan membuat nanopartikel karotenoid tersalut kitosan. Karotenoid diekstrak
menggunakan pelarut heksana-aseton (10:1 v/v). Ekstrak kasar dimurnikan
menggunakan kromatografi kolom adsorpsi. Penentuan konsentrasi karotenoid
menggunakan HPLC. Fraksi II diuapkan pelarutnya dengan evaporator dan
dihembuskan gas nitrogen. Proses nanoenkapsulasi menggunakan ultrasonikator
dengan amplitudo 30% selama 60 dan 90 menit. Karakterisasi hasil nanoenkapsul
dilakukan menggunakan
Particle Size Analyzer
(PSA). Hasil nanoekapsulasi
dengan ukuran terkecil dilakukan penentuan efisiensi nanoenkapsulasi dan
karakterisasi menggunakan
Fourier-Transform Infrared Spectroscopy
(FTIR) dan
difraksi sinar-X (XRD). Hasil penelitian diperoleh ekstrak kasar mengandung
beta-karoten sebanyak 1080.3 ppm. Fraksi II mengandung beta-karoten sebesar
3651.3 ppm dengan rendemen 0.46% b/v. Nanoenkapsulasi karotenoid selama 60
menit menghasilkan distribusi ukuran yang lebih kecil yaitu 131-446.5 nm dan
selama 90 menit berukuran 491.9-1796.2 nm. Hasil penentuan efisiensi
nanoenkapsulasi diperoleh efisiensi sebesar 76%. Hasil analisis dengan FTIR
diperoleh karotenoid sudah tersalut oleh kitosan. Hasil analisis dengan XRD
menunjukkan nanoenkapsul karotenoid berstruktur semi kristalin dengan derajat
kristalinitas 50%.
ABSTRACT
RIAHNA BR KEMBAREN. Isolation and Nanoencapsulation of Carotenoids
from Palm Pressed Fiber Waste. Supervised by LAKSMI AMBARSARI and I
MADE ARTIKA.
Indonesia produces palm pressed fiber waste in large quantities.
Utilization of palm pressed fiber waste as a source of carotenoids can increase the
economic value. Carotenoids are easily damaged if exposed
to
high temperatures and light intensity. One effort that can be done to maintain
carotenoids is nanoencapsulation using chitosan as a coating agent. The
purpose of this study was to isolate carotenoids from palm pressed fiber
waste and nanoencapsulate carotenoids using chitosan as a coating agent.
Carotenoids were extracted using hexane-acetone solvent (10:1 v/v). Crude
extract was purified by using column chromatography adsorption and the
concentration of carotenoids was determined by using HPLC. The best fraction of
extract was subjected to solvent removal by using evaporator and nitrogen gas
exhaled. Nanoencapsulation process was carried out by using ultrasonicator with
30% amplitude for 60 and 90 minutes. The size of nanoencapsule was
characterized by using Particle Size Analyzer (PSA). The smaller size of
nanoencapsule was determined by efficiency of nanoencapsulation and using
Fourier Transform Infrared Spectroscopy (FTIR) and X-ray diffraction (XRD).
Results showed that the crude extract from palm pressed fiber waste contained
beta-carotene as much as 1080.3 ppm. Fraction II as the best fraction contained
3651.3 ppm of beta-carotene, yield 0.46% (w / v). Nanoencapsulation of
carotenoids for 60 minutes produced the smaller size distribution 131-446.5 nm
and for 90 minutes sized 491.9-1796.2 nm. Results of determined
nanoencapsulation efficiency was 76%. Based on the results obtained by FTIR
that carotenoids fraction II was coated by chitosan. XRD results showed that
carotenoids nanoencapsule has semi-cristalline structure with 50% of crystallinity
degree.
ISOLASI DAN NANOENKAPSULASI KAROTENOID
LIMBAH SERAT BUAH KELAPA SAWIT
RIAHNA BR KEMBAREN
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Biokimia
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi
: Isolasi dan Nanoenkapsulasi Karotenoid Limbah Serat Buah
Kelapa Sawit
Nama
: Riahna br Kembaren
NIM
: G84070006
Disetujui
Komisi Pembimbing
Dr. Laksmi Ambarsari, MS Dr. Ir. I Made Artika, M. App. Sc
Ketua
Anggota
Diketahui
Dr. Ir. I Made Artika, M. App. Sc.
Ketua Departemen Biokimia
PRAKATA
Puji syukur kepada TUHAN Yang Maha Esa yang telah memberikan
berkat dan hikmat-Nya kepada penulis sehingga penulis mendapatkan kemudahan
dan kekuatan untuk menyelesaikan skripsi ini. Judul yang dipilih dalam skripsi ini
adalah Isolasi dan Nanoenkapsulasi Karotenoid Limbah Serat Buah Kelapa Sawit.
Penulis menyadari bahwa selesainya skripsi ini tidak lepas dari
pihak-pihak yang sudah membantu. Oleh karena itu penulis mengucapkan terima kasih
kepada Dr. Laksmi Ambarsari, Ms dan Dr. I Made Artika, M. App Sc. selaku
pembimbing yang telah memberikan bimbingan, motivasi, dan saran dalam
pengerjaan skripsi ini. Terima kasih kepada Bapak, Ibu dan Adikku Adhitia
Kembaren di Pekanbaru atas setiap doa dan dukungannya. Terima kasih kepada
rekan-rekan tim PKMP PIMNAS 2011: Indra Kurniawan Saputra, M. Iqbal Akbar
M., Anna Manurung, dan Theovany Silaban untuk kerjasamanya dalam PIMNAS
2011. Terima kasih kepada DP2M DIKTI yang sudah mendanai sebagian
penelitian ini melalui pendanaan PKMP 2011. Terima kasih kepada Ibu Pipih
yang sudah memberikan kitosan. Terima kasih kepada Hendry Crist yang sudah
menemani penulis ke PTPN VIII Kertajaya untuk mengambil sampel limbah serat
buah kelapa sawit. Terima kasih kepada Wahyudi Kurniawan Saputra yang telah
menemani serta memberikan tumpangan gratis kepada penulis ke Puspiptek
Serpong. Terima kasih kepada Dasma Sejahtera Turnip yang sudah membantu
penulis mencari jurnal dan mendukung dalam doa. Terima kasih untuk
rekan-rekan Biokimia 44, Ribka Tarigan, Elvita Citrawani, seluruh teknisi lab dan
semua pihak yang telah membantu penulis hingga skripsi ini dapat diselesaikan.
Penulis juga menyadari bahwa skripsi ini masih jauh dari sempurna
sehingga kritik dan saran yang membangun sangat penulis harapkan. Semoga
skripsi ini bermanfaat dan dapat menjadi inspirasi bagi penulis pribadi dan
pembaca.
Bogor, Desember 2012
RIWAYAT HIDUP
Penulis dilahirkan di Pekanbaru pada tanggal 23 Maret 1989 dari ayah
Yahmin Sembiring Kembaren dan ibu Maria br Tarigan. Penulis merupakan anak
pertama dari dua bersaudara. Tahun 2007 penulis lulus dari SMA Negeri 3
Pekanbaru dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur
Undangan Masuk Seleksi (USMI) IPB. Penulis memilih jurusan Biokimia,
Fakultas Matematika dan Ilmu Pengetahuan Alam. Penulis juga memilih program
studi Pengolahan Pangan, departemen Ilmu dan Teknologi Pangan sebagai minor.
DAFTAR ISI
Halaman
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Limbah Serat Buah Kelapa Sawit ... 2
Karotenoid ... 3
Kitosan ... 4
Sonikasi ... 5
Abu Sekam Padi ... 6
Nanoenkapsulasi ... 6
BAHAN DAN METODE
Bahan dan Alat ... 7
Metode Penelitian ... 7
HASIL DAN PEMBAHASAN
Ekstrak Karotenoid ... 8
Hasil Pemurnian dan Penghilangan Pelarut Ekstrak Karotenoid ... 9
Nanoenkapsulasi Karotenoid ... 11
Karakteristik Nanoenkapsul Karotenoid ... 11
SIMPULAN DAN SARAN
Simpulan ... 15
Saran ... 16
DAFTAR PUSTAKA ... 16
DAFTAR TABEL
Halaman
1 Kadar air, kadar abu, dan kadar protein limbah serat buah kelapa sawit ... 3
2 Syarat-syarat kitosan komersil ... 5
3 Ukuran rata-rata nanoenkapsul dan indeks polidispersitas ... 12
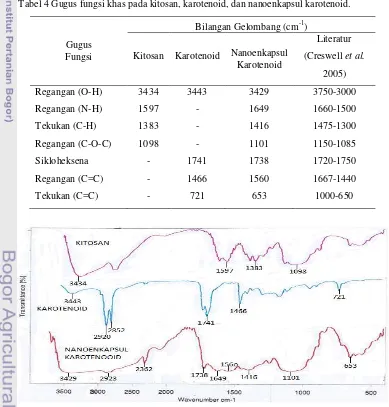
4 Gugus fungsi khas kitosan, karotenoid, dan nanoenkapsul karotenoid ... .14
DAFTAR GAMBAR
Halaman
1 Limbah serat buah kelapa sawit ... 2
2 Struktur molekul beberapa senyawa golongan karotenoid ... 4
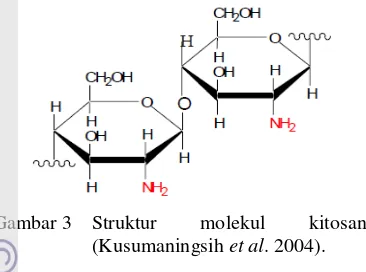
3 Struktur molekul kitosan ... 5
4 Hasil ekstraksi karotenoid ... 9
5 Hasil pengaktifan abu sekam padi ... 10
6 Fraksi I, II, dan III hasil pemekatan ekstrak karotenoid ... 10
7 Sebaran diameter nanoenkapsul karotenoid pada ultrasonikasi 60 menit .... 12
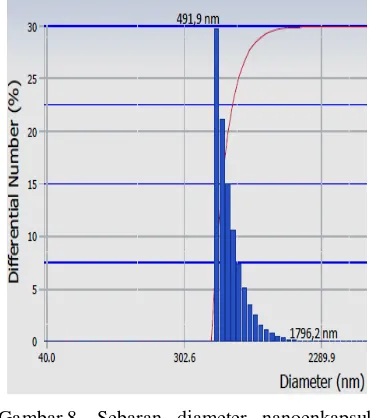
8 Sebaran diameter nanoenkapsul karotenoid pada ultrasonikasi 90 menit .... 12
9 Serpihan fraksi II nanoenkapsul karotenoid ... 13
10 Spektrum FTIR kitosan, karotenoid, dan nanoenkapsul karotenoid ... 14
DAFTAR LAMPIRAN
Halaman
1 Alur kerja penelitian ... 19
2 Spektrum FTIR kitosan, karotenoid dan nanoenkapsul karotenoid ... 20
3 Kromatogram HPLC standar beta-karoten ... 21
4 Kromatogram HPLC ekstrak kasar serat buah kelapa sawit ... 22
1
PENDAHULUAN
Indonesia adalah salah satu negara penghasil crude palm oil (CPO) terbesar di dunia. Luas area perkebunan sawit di Indonesia pada tahun 2010 sebesar 7.8 juta HA (www.ditjenbun.deptan.go.id). Produksi
kelapa sawit Indonesia mengalami
peningkatan, pada tahun 2009 sebesar 18.6 juta ton dan pada tahun 2010 sebesar 19.8 juta
ton. Produksi CPO juga mengalami
peningkatan, pada tahun 2004 sebanyak 12.5 juta ton kemudian meningkat menjadi 12.8
juta ton pada tahun 2005. Dengan
bertambahnya luas lahan perkebunan kelapa sawit dan produksi CPO berarti semakin bertambah pula jumlah limbah pabrik kelapa sawit yang dihasilkan. Tahun 2004 jumlah limbah pengolahan kelapa sawit sebesar 12.4 juta ton tandan kosong kelapa sawit (TKKS), 10.2 juta ton cangkang dan serat, serta sebayak 32.3–37.6 juta ton limbah cair (www.peternakan.litbang.deptan.go.id).
Limbah merupakan kotoran atau buangan yang dihasilkan dari proses pengolahan. Limbah dapat digolongkan menjadi limbah cair dan limbah padat. Limbah padat dari pengolahan kelapa sawit berupa tandan
kosong, tempurung, dan serat buah,
sedangkan limbah cair berupa lumpur sawit. Limbah serat buah umumnya digunakan
sebagai bahan bakar mesin ketel uap boiler
(sumber energi pada pabrik) (Sanagi 2005). Pembakaran serat juga akan mengakibatkan pencemaran udara. Meskipun limbah kelapa sawit berpotensi mencemari lingkungan namun juga berpotensi untuk diberdayakan karena jumlah yang banyak dan terpusat. Usaha-usaha untuk memanfaatkan limbah tersebut sampai saat ini belum dilakukan secara intensif.
Limbah padat utama dari pabrik pengolahan kelapa sawit adalah serat buah kelapa sawit. Limbah serat buah kelapa sawit tersebut sangat melimpah, setiap ton produksi CPO akan dihasilkan 1.79 ton limbah serat buah kelapa sawit (Loebis & Tobing 1989). Limbah serat buah kelapa sawit memiliki kemungkinan masih mengandung karotenoid. Senyawa ini memberikan warna kuning hingga merah pada minyak sawit. Karotenoid adalah prekursor vitamin A dan antioksidan. Karotenoid dibutuhkan oleh industri farmasi, kosmetik, dan pangan sebagai pewarna alami dan antioksidan (May 1994). Salah satu contoh senyawa golongan karotenoid adalah
β-karoten. Βeta-karoten sering digunakan
untuk fortifikasi vitamin pada produk pangan
seperti margarin. Saat ini Indonesia masih mengimpor karotenoid dari luar negeri (Masni 2004).
Pemanfaatan limbah serat buah kelapa sawit sebagai sumber karotenoid dapat meningkatkan nilai ekonomis dan nilai guna limbah tersebut. Sifat fisik karotenoid mudah rusak jika terpapar suhu dan intensitas cahaya
yang tinggi sehingga dapat menurunkan
intensitas warna. Upaya yang dapat dilakukan
untuk mempertahankan karotenoid dari
kerusakan akibat suhu dan intensitas cahaya yang tinggi adalah dengan nanoenkapsulasi. Penggunaan karotenoid pada industri pangan
dan farmasi membutuhkan peningkatan
tingkat dispersi karotenoid dalam air,
sehingga ukuran partikel harus diturunkan ke ukuran submikro atau nano agar tingkat dispersi dalam air meningkat (Hoang et al. 2011).
Nanoenkapsulasi adalah penyalutan suatu bahan atau materi dalam ukuran nano (Mohanraj & Chen 2006). Nanoenkapsulasi karotenoid akan melindungi karotenoid dari kerusakan karena suhu dan intensitas cahaya yang tinggi, membantu penyerapan yang lebih baik dan dapat menghindari rasa dan bau yang kurang menyenangkan (Sozer & Kokini 2009). Metode yang dapat digunakan dalam nanoenkapsulasi adalah metode sonokimia dengan memanfaatkan gelombang ultrasonik yang dihasilkan oleh alat ultrasonikator (Bang & Suslick 2010).
Bahan yang dapat digunakan sebagai penyalut adalah polyethylene glycol (PEG),
maltodekstrin, polylactic acid (PLA) dan
kitosan (Sozer & Kokini 2009). Kitosan banyak terdapat dalam kulit udang, tetapi kulit udang tersebut belum dimanfaatkan secara optimal dan dibuang sehingga mencemari
lingkungan. Kitosan memiliki beberapa
keunggulan jika digunakan sebagai bahan penyalut yang lain, yaitu bentuk fisiknya dapat diubah (dalam bentuk serpihan, manik-manik berpori, gel, fibre, dan membran), biodegradable, murah, mudah dalam penanganannya, dan tidak toksik (Parize et al. 2008). Kitosan juga memilki sifat tahan panas sehingga sangat baik untuk melindungi karotenoid dari pengaruh suhu yang tinggi. Kitosan juga memiliki warna yang transparan sehingga tidak mengganggu warna dari nanoenkapsul karotenoid.
Tujuan penelitian ini adalah mengisolasi karotenoid dari limbah serat buah kelapa sawit dan membuat nanopartikel karotenoid tersalut
kitosan (nanoenkapsulasi karotenoid).
2
dapat diisolasi dari limbah serat buah kelapa sawit dan dapat dinanoenkapsulasi menggunakan kitosan sebagai bahan penyalut. Manfaat penelitian ini adalah menghasilkan karotenoid dari limbah serat buah kelapa sawit, serta karotenoid yang sudah dinanoenkapsulasi menggunakan penyalut kitosan menjadi lebih stabil dan dapat dimanfaatkan untuk industri pangan, kosmetik dan farmasi. Penelitian ini juga memiliki kegunaan untuk mengeksplorasi pemanfaatan limbah menggunakan ilmu biokimia untuk industri terutama industri pangan, kosmetik dan farmasi.
TINJAUAN PUSTAKA
Limbah Serat Buah Kelapa Sawit
Tanaman kelapa sawit (Elaeis guineensis
Jacq) merupakan tanaman berkeping satu yang termasuk famili palmae (Syahputra et al.
2008). Nama genus guineensis berasal dari
kata guinea yaitu tempat ditemukannya kelapa sawit. Laju peningkatan areal penanaman sawit di Indonesia sebesar 14% per tahun. Secara garis besar buah kelapa sawit terdiri dari serabut buah (pericarp) dan inti (kernel). Serabut buah kelapa sawit terdiri dari tiga lapis yaitu lapisan luar atau kulit buah yang
disebut pericarp, lapisan sebelah dalam
disebut mesocarp atau pulp dan lapisan paling
dalam disebut endocarp. Inti buah kelapa
sawit terdiri dari lapisan kulit biji (testa),
endosperm, dan embrio. Mesocarp
mengandung kadar minyak rata-rata sebanyak
56%, inti (kernel) mengandung minyak
sebesar 44%, dan endocarp tidak mengandung minyak (Pardamean 2008).
Hasil utama dari pengolahan kelapa sawit adalah minyak sawit kasar (CPO) dan minyak
inti sawit atau dikenal dengan nama Palm
Kernel Oil (PKO) (Pardamean 2008). Tahapan pengolahan kelapa sawit secara umum terdiri atas pengangkutan buah ke pabrik, perebusan buah (sterilisasi), pelepasan buah dari tandan (striping), pelumatan buah (digesting), pengeluaran minyak (ekstraksi), penyaringan, pemurnian dan penjernihan minyak (klarifikasi), serta pengolahan biji. Minyak sawit kasar merupakan hasil ekstraksi
dari tubuh buah (mesocarp) tanaman kelapa
sawit. CPO harus menjalani pengolahan ekstensif sebelum mencapai konsumen. Salah satu proses adalah pemutihan adsorpsi untuk
menghasilkan RBD (refined, bleached and
deodorized palm oil), pada tahap ini kandungan karotenoid yang tinggi pada
minyak akan dihilangkan. Tahap fraksinasi adalah proses yang memisahkan olein cair atau superolein dari stearin yang padat. Fraksi olein umumnya digunakan untuk minyak goreng, sedangkan stearin digunakan terutama untuk shortening dan margarin (Pardamean 2008).
Minyak kelapa sawit seperti umumnya minyak nabati lainnya adalah merupakan senyawa yang tidak larut dalam air, sedangkan komponen penyusunnya yang utama adalah trigliserida dan nontrigliserida. Minyak dari kelapa sawit lebih murah dan memiliki kandungan karotenoid tinggi jika dibanding minyak nabati dari sumber yang lain. Tanaman kelapa sawit memiliki keunggulan dibandingkan dengan tanaman sumber minyak yang lain seperti minyak kelapa, kedelai, atau minyak biji bunga matahari yaitu kelapa sawit mempunyai produktivitas lebih tinggi dan masa produksi kelapa sawit yang cukup panjang (sekitar 22 tahun) (Pardamean 2008).
Dalam proses pengolahan kelapa sawit tersebut terdapat bahan yang tidak bermanfaat. Limbah yang dihasilkan oleh pabrik pengolahan sawit ada dua jenis, yaitu limbah padat dan limbah cair. Limbah padat dari pengolahan kelapa sawit mempunyai komposisi bahan penyusunnya adalah selulosa, hemiselulosa dan lignin. Limbah padat yang dihasilkan oleh pabrik pengolahan sawit adalah tandan kosong kelapa sawit (TKKS), serat buah, dan bungkil inti sawit. Limbah cair yang dihasilkan adalah lumpur minyak sawit, air drab, air kondesat, air cucian pabrik, air hidrocyclone atau claybath dan sebagainya. Tandan buah segar sebanyak 10.40 juta ton per tahun dapat menghasilkan limbah pengolahan sawit berupa lumpur sawit 0.52 juta ton, bungkil inti sawit sebesar 0.24 juta ton dan serat buah sebesar 1.25 juta ton pertahun (Mirwandhono & Siregar 2004).
Serat buah atau sabut sisa pemerasan adalah residu fibrosa yang diperoleh pada proses pemerasan mesocarp buah kelapa sawit untuk menghasilkan minyak sawit (Gambar 1). Limbah serat buah kelapa sawit memiliki biomassa sekitar 15.7% dari biomassa tandan buah segar. Jumlah serat tersebut sangat
3
melimpah, setiap ton produksi CPO akan dihasilkan 1.79 ton limbah serat (Loebis & Tobing 1989). Limbah serat buah kelapa sawit biasanya dibakar sebagai bahan bakar untuk penyediaan energi pada proses penggilingan
atau mill (Sanagi 2005), bahan baku
pembuatan papan dan sebagai bahan campuran makanan ternak. Limbah serat buah kelapa sawit memiliki penyusun utama selulosa (31.82%), hemiselulosa (22.04%), dan lignin (16.53%) (Irawadi 1991).
Choo et al. (1996) melaporkan bahwa
setelah memberikan perlakuan tertentu terhadap hasil ekstraksi serat perasan sawit menggunakan pelarut yang berbeda, yaitu heksana, kloroform, dan etanol, didapatkan konsentrat yang mengandung karotenoid (4000-6000 ppm), vitamin E (2400-3500 ppm), dan sterol (4500-8500 ppm). Karotenoid yang teridentifikasi terdiri dari α -karoten (19.5%), β-karoten (31.0%), likopen (14.1%), dan pitoena (11.9%), sedangkan vitamin E terdiri dari α-tokoferol (61%), dan sisanya berupa tokotrienol (α-, γ-, dan δ-) dan
sterol terdiri dari β-sitosterol (47%),
kampersterol (24%), dan sigmasterol (15%). Sisa minyak juga terdapat pada limbah
serat buah setelah bagian mesocarp buah
diekstraksi oleh screw press (Sanagi 2005). Kadar minyak atau lemak pada limbah serat buah kelapa sawit sekitar 9.25%. Limbah serat buah kelapa sawit juga mengandung air, mineral, dan protein. Tabel 1 merupakan hasil analisis kadar air, kadar abu, dan kadar protein limbah serat buah kelapa sawit dalam berat kering (BK).
Tabel 1 Kadar air, kadar abu, dan kadar
protein limbah serat buah kelapa sawit.
Sumber : Irawadi 1991.
Karotenoid
Karotenoid adalah senyawa isoprenoid poliena yang diturunkan dari likopena. Semua karotenoid adalah senyawa lipofilik, tidak larut dalam air, larut dalam lemak dan pelarut
organik seperti heksana dan bensena.
Karotenoid merupakan senyawa yang
memberikan karakteristik warna merah dan
jingga pada buah-buahan, ganggang,
mikroorganisme, sayur-sayuran dan kerangka
luar hewan crustacea seperti udang.
Karotenoid yang terdapat di alam cukup banyak jumlahnya (Sanchez et al. 2010).
Karotenoid mempunyai struktur alifatik atau asiklik yang pada umumnya disusun oleh delapan unit isopren dan 2-metil butadien, kedua gugus metil yang dekat pada molekul pusat terletak pada posisi C-1 dan C-5, serta diantaranya terdapat ikatan ganda konjugasi (Gambar 2). Adanya ikatan ganda yang terkonjugasi di dalam molekul karotenoid menandakan adanya gugus kromofor. Makin banyak ikatan ganda terkonjugasi akan makin pekat warna karotenoid tersebut, artinya semakin mengarah ke warna merah. Ikatan ganda ini yang menyebabkan karotenoid peka terhadap oksidasi. Oksidasi karotenoid akan lebih cepat dengan adanya sinar dan katalis logam, khususnya tembaga, besi, dan mangan. Oksidasi terjadi secara acak pada rantai karbon yang mengandung ikatan ganda. Karotenoid juga mudah mengalami isomerisasi oleh panas dan cahaya.
Warna karotenoid mempunyai kisaran dari kuning hingga merah, maka deteksi panjang gelombangnya diperkirakan antara 430-480 nm. Panjang gelombang yang tertinggi biasanya digunakan untuk beberapa xantofil untuk mencegah gangguan klorofil. Beta-karoten menyerap sinar pada daerah ultra-violet sampai ultra-violet tetapi lebih kuat pada daerah tampak antara 400 dan 500 nm dengan puncak 470 nm (Fennema 1996).
Karotenoid mempunyai sifat yang dapat membentuk isomer geometrik yaitu bentuk trans dan cis. Karotenoid terutama terdapat sebagai isomer trans di alam. Bentuk trans dari karoten memiliki derajat aktivitas vitamin A yang lebih tinggi dibandingkan dengan bentuk cis (Sanchez et al. 2010). Kepekaan terhadap oksidasi membuat karotenoid digunakan sebagai antioksidan yang kekuatannya menyamai tokoferol dan askorbat. Reaksi oksidasi dapat menyebabkan hilangnya warna karotenoid dalam makanan dan merupakan mekanisme degradasi utama yang banyak menjadi perhatian.
Karotenoid belum mengalami kerusakan oleh pemanasan pada suhu 60oC (Hoang et al. 2011). Karotenoid lebih tahan jika disimpan dalam lingkungan asam lemak tidak jenuh. Hal ini disebabkan asam lemak tidak jenuh lebih mudah menerima radikal bebas apabila dibandingkan dengan karotenoid, sehingga oksidasi yang pertama kali akan terjadi pada asam lemak dan akibatnya karotenoid terlindung dari oksidasi (Sanchez et al. 2010).
Menurut Meyer (1973), karotenoid dapat dibagi menjadi empat golongan yaitu karoten,
Limbah Kadar
Air Kadar Abu Kadar protein Serat buah kelapa sawit
4
Gambar 2 Struktur molekul beberapa
senyawa golongan karotenoid.
xantofil dan derivat karoten, ester xantofil, serta asam karotenoid. Karoten merupakan
karotenoid hidrokarbon C40H56. Karoten
adalah senyawa mikro yang menyebabkan karakteristik warna jingga-merah pada minyak kelapa sawit. Karoten adalah senyawa pigmen
alami yang terdapat pada kromoplas
tumbuhan dan beberapa organisme fotosintetik lainnya seperti alga, beberapa jenis fungi dan bakteri. Pada tumbuhan tingkat tinggi dan alga, karoten menyerap energi cahaya matahari untuk digunakan pada fotosintesis, dan karoten melindungi klorofil dari kerusakan. Contoh senyawa karoten adalah alfa, beta, dan gamma karoten serta
likopen. Xantofil dan derivat karoten
mengandung oksigen dan hidroksil, misalnya kriptoxantin dan lutein. Ester xanthofil adalah ester xanthofil asam lemak, misalnya zeaxanthin. Asam karotenoid adalah derivat karoten yang mengandung gugus karboksil.
Pada manusia, karoten seperti β-karoten adalah prekursor vitamin A, pigmen essensial
untuk penglihatan dan kesehatan mata. β
-karoten sering digunakan untuk fortifikasi vitamin pada produk pangan seperti margarin.
0.6µg β-karoten setara dengan 1 IU vitamin
A. β-karoten di alam umumnya terdapat dalam bentuk trans, tetapi dapat terisomerisasi karena pengaruh lingkungan seperti suhu dan cahaya ke bentuk cis- β- karoten (Syahputra et
al. 2008). Mengkonsumsi β-karoten lebih
aman dari pada vitamin A yang dibuat secara sintesis dan difortifikasi ke dalam makanan,
sebab dalam tubuh β-karoten alami akan
diserap dan dimetabolisme. Sekitar 25% dari
β-karoten yang diserap pada mukosa usus
tetap dalam bentuk utuh sedangkan 75% sisanya diubah menjadi retinol (vitamin A)
dengan bantuan enzim β-karoten 15, 15’
monooksigenase (Goodwin 1979).
Kekurangan vitamin A merupakan salah satu masalah gizi utama yang diderita oleh anak balita di Indonesia. Fungsi utama vitamin A
adalah untuk proses penglihatan dan pertumbuhan yang normal.
Sifat kereaktifan yang tinggi dari β
-karoten dapat mengakibatkan pergeseran
karakteristik dari aktivitas antioksidan
menjadi prooksidan. Hal ini dapat terjadi
dengan meningkatnya konsentrasi β-karoten
dan tergantung pada lingkungan fisikokimia. Di jaringan yang tekanan oksigennya rendah,
karakteristik aktivitas antioksidan
mendominasi, tetapi pada lingkungan yang tidak sesuai menyebabkan β-karoten dapat meningkatkan aktivitas prooksidannya melalui generasi oksidasi dan pembelahan produk (Hoang et al. 2011). Sifat prooksidan dari β -karoten terjadi pada perokok berat yang mengkonsumsi β-karoten dalam jumlah besar (Hoang et al. 2011).
β-karoten lebih sering ditemukan dalam bentuk agregat (berkumpul), hanya sebagian kecil dari molekul β-karoten ditemukan dalam bentuk monomolekul. Dua agregasi utama dari karotenoid yang dapat diamati yaitu agregat H- dan agregat J-. Kedua agregat tersebut memilliki spektrum spektrofotometri yang berbeda (Hoang et al. 2011).
Beberapa penelitian telah menunjukkan
bahwa adanya kemampuan anti kanker dari β
-karoten sehingga senyawa ini berpotensi sebagai obat pencegahan beberapa jenis kanker (Hoang et al. 2011). Beta-karoten mudah terdegradasi karena oksidasi dan proses termal terutama pada proses pengolahan pangan dengan suhu tinggi dan penyimpanan.
Kitosan
Kitosan adalah polisakarida yang bermuatan positif, mengandung rantai lurus glukosamin dan residu N-asetil
D-glukosamin yang diikat dengan ikatan β-(1-4)
glikosidik (Gambar 3). Kitosan merupakan senyawa turunan kitin yang banyak terdapat pada rangka luar dari insektisida, crustacea (udang, kerang, kepiting, dan lobster), dan jamur. Kitosan tidak larut dalam air, tetapi larut dengan cepat dalam asam organik encer. Kitosan memiliki sifat mudah terdegradasi, biocompatible, tidak beracun dan memiliki aktivitas antibakteri, serta aktivitas adsorpsi (Kumar 2000).
Gugus amina (NH2) yang dimiliki oleh
kitosan ini pada kondisi asam akan
terprotonasi membentuk gugus amina kationik (NH3
+
5
Gambar 3 Struktur molekul kitosan (Kusumaningsih et al. 2004).
amina bebas dan hidroksil pada kitosan menyebabkan kitosan dapat dimodifikasi menjadi berbagai produk, salah satunya
dengan menambahkan crosslinker seperti
glutardialdehid dan tripolifosfat (TPP)
sehingga terbentuk ikatan silang antara rantai polimer kitosan. Kitosan juga dapat membentuk gel karena terbentuknya jaringan tiga dimensi antara molekul kitosan yang terentang pada seluruh volume gel dan menangkap sejumlah air di dalamnya (Tsai et al. 2011).
Secara industri kitosan diperoleh dengan mendeasetilasi kitin dengan alkali. Mutu kitosan tersebut dipengaruhi oleh beberapa parameter yaitu kadar air, kadar abu, kelarutan, derajat deasetilasi (DD), viskositas dan bobot molekul. Berat molekul (BM) kitosan sekitar 1.2x105 dalton tergantung pada derajat deasetilasi yang dihasilkan pada waktu ekstraksi. Syarat-syarat kitosan komersil disajikan dalam Tabel 2. Semakin banyak gugus asetil yang hilang dari polimer kitin, semakin tinggi nilai DD, maka semakin kuat interaksi antar ion dan ikatan hidrogen dari kitosan. Kitosan memiliki titik lebur pada 134.5oC (Sofia et al. 2010).
Beberapa pemanfaatan kitin dan kitosan dalam industri adalah sebagai pengawet dan
Tabel 2 Syarat-syarat kitosan komersil.
Parameter Nilai
Ukuran partikel Serpihan sampai
serbuk
Kadar air ≤10%
Kadar abu ≤2%
Warna larutan Jernih
Derajat deasetilasi (DD) % 70 ≥ Viskositas (cps)
-rendah < 200 cps
-sedang 200-799 cps
-tinggi 800-2000 cps
-ekstra tinggi >2000 cps
Sumber: Knorr 1982.
penstabil warna produk, suplemen serat, pembentuk tekstur, emulsifier, penjernih minuman, dan membran dialisis (Kumar 2000). Kitosan juga dapat bereaksi dengan senyawa bersifat asam seperti polifenol sehingga juga dapat dimanfaatkan untuk menurunkan kadar asam pada buah-buahan dan ekstrak kopi.
Sonikasi
Ultrasonik merupakan gelombang atau suara dengan frekuensi yang sangat tinggi. Ultrasonik memiliki frekuensi melebihi batas pendengaran manusia, yakni di atas 20 kHz. Sejak tahun 1980-an efek dari ultrasonik banyak digunakan para ilmuwan di berbagai sektor untuk ekstraksi dan homogenasi. Hal ini dikarenakan ultrasonik memiliki dampak yang signifikan baik secara fisik maupun kimia terhadap suatu zat. Efek fisika dari ultrasonik dengan intensitas tinggi antara lain adalah emulsifikasi dan kerusakan permukaan. Perambatan gelombang ultrasonik atau akustik dari setiap rentang frekuensi dikaitkan dengan perubahan keadaan media (perturbation) dan transfer energi (Margulis 1995). Gelombang ultrasonik tidak secara langsung berinteraksi dengan molekul-molekul untuk menginduksi suatu perubahan kimia. Interaksi gelombang ultrasonik dengan molekul-molekul terjadi melalui media perantara berupa cairan.
Sonokimia berarti memberikan perlakuan ultrasonik pada suatu bahan dengan kondisi tertentu sehingga bahan tersebut mengalami reaksi kimia akibat perlakuan tersebut. Pemberian gelombang ultrasonik pada suatu larutan menyebabkan molekul-molekul yang terkandung di dalam larutan berosilasi terhadap posisi rata-ratanya. Larutan akan mengalami rapatan dan renggangan.
6
Gelembung dengan radius cukup besar tidak dapat berada di dalam cairan karena gelembung tersebut secara bertahap naik ke permukaan (Margulis 1995). Pada beberapa kasus, ukuran gelembung bisa membesar dan mengecil (berosilasi) mengikuti renggangan dan rapatan gelombang ultrasonik yang diberikan. Ketika gelombang mengecil (collapse), terjadi tekanan yang sangat besar di dalam gelembung. Demikian pula suhu di dalam gelembung menjadi sangat besar.
Daerah persambungan (interface) antara
gelembung dan larutan memiliki temperatur dan tekanan yang menengah. Sementara itu daerah di sekitar gelembung akan menerima gaya geser (shear force) yang sangat tinggi akibat pengecilan ukuran gelembung. Reaksi kimia bisa berlangsung di dalam gelembung akibat tekanan dan temperatur yang sangat tinggi di dalam gelembung ini. Senyawa kimia yang diharapkan bereaksi harus memasuki gelembung. Pengecilan yang tiba-tiba dari gelembung mengakibatkan cairan di sekeliling gelembung mengalami gaya geser yang cukup besar. Gaya ini juga bisa membantu terjadinya reaksi kimia. Ledakan kavitasi tersebut sangat lokal dengan suhu sekitar 5000 K dan tekanan sekitar 1000 bar (Suslick 1990).
Abu Sekam Padi
Tingginya produksi beras akan menyebabkan tingginya sampah penggilingan padi berupa sekam. Sekam padi merupakan salah satu komponen penyusun dari bulir padi yang menyusun 18-28% dari seluruh bobot bulir padi. Sekam padi tersusun dari palea dan lemma. Lemma adalah bagian sekam yang paling lebar. Palea dan lemma terikat dengan suatu struktur pengikat yang menyerupai kait. Setiap kilogram gabah kering digiling, akan dihasilkan sebanyak 0.52 kg beras dan akan dihasilkan juga sekam padi sebanyak 0.48 kg. Kandungan kimia sekam padi terdiri atas 50% selulosa, 25-30% lignin, dan 15-20% silika (Bakri 2009).
Abu sekam padi merupakan sumber biologis dari silika yang dapat digunakan dalam proses pemurnian minyak. Kandungan silika (SiO2) pada abu sekam padi tergantung pada suhu dan waktu pemanasan yang digunakan (Proctor & Palaniappan 1989). Pengabuan dapat menghasilkan abu sekam padi yang mengandung 61% silika, dan 36% karbon. Umumnya abu sekam padi digunakan sebagai abu gosok untuk keperluan rumah tangga, sehingga nilai ekonomis dari abu sekam padi masih rendah. Abu sekam padi dapat digunakan sebagai pengikat logam
berat, menggemburkan tanah (pupuk kompos), dan sumber silika. Sekam padi saat ini telah dikembangkan sebagai bahan baku untuk menghasilkan abu yang dikenal di dunia
sebagai RHA (Rice Husk Ask). RHA
merupakan abu sekam padi yang dihasilkan dari pembakaran sekam padi pada suhu 400-500oC dan akan dihasilkan silika amourphous, dan pada suhu yang lebih besar dari 1000oC akan menjadi silika kristalin (Bakri 2009).
Studi yang dilakukan oleh Liew et al. pada tahun 1993 menggunakan abu sekam padi untuk menjerap karoten dari CPO, hasilnya menunjukkan bahwa abu sekam padi mempunyai aktivitas menjerap lebih tinggi dibandingkan silika dan karbon, tetapi aktivitas tersebut sedikit lebih rendah dari tanah pemucat komersial.
Nanoenkapsulasi
Awalan nano berarti sepermilyar (10-9)
meter. Nano memiliki arti kerdil dalam bahasa Yunani. Istilah nanoteknologi berhubungan dengan material dan sistem pada skala
nanometer atau sekitarnya (Cui 2008).
Tantangan utama dalam sintesis nanomaterial adalah mengontrol karakteristiknya seperti distribusi ukuran partikel, bentuk, morfologi, komposisi komposisi kimia dan struktur
kristal. Karakteristik nanomaterial
menunjukkan sifat fisik dan kimia yang berbeda dari material ukuran besar sebagai konsekuensi memiliki rentang ukuran 1-1000 nm.
Nanopartikel didefinisikan sebagai partikel dengan ukuran sekitar 10-1000 nm (Mohanraj & Chen 2006). Istilah nanopartikel meliputi
dua kondisi yaitu nanospheres dan
nanocapsules. Nanospheres adalah sistem yang memiliki tipe struktur matriks. Pada
sistem nanospheres, suatu bahan tersebar
secara fisik dan merata, serta diserap pada
permukaan penyalut. Nanocapsules adalah
sistem vesicular, suatu bahan pada rongga yang terdiri dari inti dikelilingi oleh membran polimer. Suatu bahan aktif dapat berada di dalam inti (nanocapsule) dan juga terserap di sekeliling permukaan atau matriks kapsul (nanospheres) (Mohanraj & Chen 2006).
Tahapan untuk mendapatkan atau mensintesis nanopartikel dapat digunakan dua pendekatan yaitu top-down dan bottom-up.
Pendekatan top-down artinya pembuatan
partikel nano dimulai dari material bentuk
bulk kemudian dilakukan penghancuran atau
7
nanometer. Pendekatan bottom-up artinya
partike nano terbentuk dari hasil penyusunan, penggabungan atau perangkaian atom-atom
atau molekul-molekul bersama hingga
terbentuk struktur berukuran nanometer
(Balaz 2008). Nanopartikel polimer telah
dipelajari secara ekstensif sebagai pembawa partikulat dalam bidang farmasi dan medis karena dapat sebagai sistem pengiriman obat
terkontrol dan pelepasan obat yang
berkelanjutan, ukuran subselular, dan
biokompatibilitas dengan jaringan dan sel. Beberapa metode untuk mempersiapkan nanopartikel telah dikembangkan selama dua dekade terakhir. Salah satu contoh nanopartikel polimer adalah nanopartikel kitosan. Nanopartikel kitosan didasarkan pada pembentukan kompleks antara kitosan dan polianion secara spontan atau gelasi dari larutan kitosan terdispersi dalam emulsi minyak (Tsai et al. 2011).
Nanopartikel lebih menguntungkan daripada mikropartikel dan liposom. Ukuran submikron nanopartikel menawarkan sejumlah keuntungan yang berbeda dibanding mikropartikel, salah satunya adalah serapan intraseluler yang relatif lebih tinggi dibandingkan dengan mikropartikel. Dua sifat istimewa dari nanoenkapsul adalah melindungi atau mengisolasi zat inti dari pengaruh lingkungan luar dan melepaskannya dengan pola terkontrol (Reis et al. 2006).
Ukuran partikel dan distribusi ukuran adalah karakteristik paling penting dalam sistem nanopartikel. Partikel dengan ukuran paling kecil juga memiliki kemungkinan terjadinya agregasi partikel yang lebih besar selama penyimpanan dan transportasi. Hal ini merupakan tantangan dalam menghasilkan nanopartikel dengan ukuran terkecil dan kestabilan tinggi (Mohanjar & Chen 2006).
Nanoenkapsul adalah partikel berukuran nanometer yang tersusun atas dinding tipis
dari polimeryang menyelimuti material inti
berbentuk cairan atau padatan dengan diameter mulai dari 1 sampai 1000 nm (Reis et al. 2006). Nanoenkapsul memiliki keunggulan lebih dibandingkan mikroenkapsul. Ukuran nanometer dari suatu partikel menyebabkan mampu melewati
penghalang biologi (biological barrier),
memperbaiki tingkat penerimaan jaringan dan meningkatkan penyerapan dan transportasi seluler (Mohanraj & Chen 2006).
Penggunaan nanoenkapsul pada produk pangan dapat membantu penyerapan zat gizi yang lebih baik. Nanoenkapsul dapat menghindari rasa, bau, serta tekstur yang
kurang menyenangkan dari bahan pangan. Beberapa produk pangan menggunakan bahan pelapis sebagai sistem perlindungan, seperti bahan pelapis yang digunakan pada buah-buahan, sayuran, daging, roti, atau keju. Nanoteknologi memungkinkan dibuatnya lapisan tipis untuk melindungi makanan dengan ketebalan kurang dari 1000 nm. Lapisan tipis melindungi dari kelembaban, menjaga rasa dan warna makanan, serta memperpanjang masa kadaluarsa produk pangan.
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan pada penelitian ini adalah limbah serat buah kelapa sawit, kitosan DD 89%, asam asetat 1%, akuades, aseton, heksana, gas Nitrogen, standar β-karoten, dan abu sekam padi. Limbah serat buah kelapa sawit yang digunakan dalam penelitian ini berasal dari PTPN VIII Kertajaya, Banten. Kitosan yang digunakan diperoleh dari Departemen Teknologi Hasil Perikanan, IPB.
Alat-alat yang digunakan adalah labu Erlenmeyer, gelas piala, pengering beku (freeze drying), tabung reaksi, gelas
pengaduk, Particle Size Analyzer (PSA),
thermoshaker, oven, vial, Fourier Transform Infrared Spetroscopy (FTIR), Shimadzu
XRD-7000 X-Ray Diffractometer, High
Performance Liquid Chromatography (HPLC), aluminium foil, kertas saring Whatman No. 1, dan neraca analitik OHAUS GA 200.
Metode Penelitian
Ekstraksi karotenoid (Baharin et al. 1998) Proses ekstraksi dilakukan dengan metode ekstraksi pelarut. Serat buah kelapa sawit ditambahkan pelarut (1:5 b/v) campuran heksana-aseton (10:1 v/v). Pencampuran dilakukan dalam labu Erlenmeyer bertutup, terlindung cahaya dengan menggunakan aluminium foil. Campuran diekstraksi
menggunakan thermoshaker pada kecepatan
putar 200 rpm, pemanasan suhu 45oC selama
30 menit. Setelah tahap tersebut, Erlenmeyer dikeluarkan dari thermoshaker dan didiamkan dalam wadah berisi es selama 15 menit, kemudian dilakukan penyaringan menggunakan kertas saring Whatman no. 1 pada kondisi intensitas cahaya rendah. Hasil
dari proses ini adalah ekstrak kasar
8
senyawa β-karoten menggunakan instrumen
High Performance Liquid Chromatography (HPLC).
Pemurnian dan penghilangan pelarut dari ekstrak karotenoid
Bahan penjerap (adsorben) yang digunakan adalah abu sekam padi. Kolom diisi dengan bahan penjerap yang telah diaktifkan terlebih dahulu (dipanaskan selama
4 jam pada suhu 120oC) kemudian ekstrak
dituang ke dalam kolom, dibiarkan terjerap oleh penjerap, kemudian dielusi dengan bahan pengelusi campuran heksana-aseton (10 : 1 v/v). Cairan yang keluar dari kolom (eluat) ditampung per perubahan warna sampai eluat yang keluar tidak berwarna lagi. Karena tujuan tahap ini adalah untuk memurnikan ekstrak dari pengotor dan memekatkan, sehingga tahap ini tidak didasarkan pada kecepatan alir, hanya perubahan warna yang
keluar dari cerat. Fraksi terbaik yang
menunjukkan konsentrasi karotenoid yang tinggi (warna pekat) disatukan dalam satu tabung, lalu diuapkan pelarutnya dengan evaporator pada suhu 45oC lalu dihembuskan
gas nitrogen. Penghembuskan gas N2 pada
permukaan fraksi cair dilakukan hingga diperoleh konsentrat dengan bobot yang konstan (Masni 2004). Analisis kualitatif dan kuantitatif karotenoid diwakili oleh β-karoten menggunakan HPLC.
Pembuatan nanoenkapsul (Kim et al. 2006) Sebanyak 2 gram kitosan dilarutkan dalam 100 mL asam asetat 1% sehingga diperoleh kitosan 2%. Campuran diaduk dengan magnetik stirer untuk mempercepat pelarutan kemudian ditambahkan 20 ml tripolifosfat 0.5% (b/v) dalam air. Campuran pada gelas piala ditambahkan karotenoid 0.5% (b/v), kemudian ditambahkan tween 80 2% dalam air sebanyak 50 mL sambil diaduk hingga homogen. Campuran tersebut diultrasonikasi pada amplitudo 30% pada variasi waktu 60
dan 90 menit, suhu 25oC. Sebagai kontrol,
dilakukan pembuatan nanoenkapsul dengan tidak ditambahkan karotenoid (tanpa inti karotenoid).
Karakteristik hasil nanoenkapsulasi karotenoid
Analisis distribusi ukuran nanoenkapsul menggunakan Particle Size Analyzer (PSA) (Kim et al. 2006)
Larutan karotenoid hasil ultrasonikasi pada variasi waktu 60 menit dan 90 menit dianalisis
menggunakan instrumen PSA (Particle size
Analyzer) untuk mengetahui distribusi ukuran partikel.
Analisis gugus fungsi spesifik nanoenkapsul menggunakan Fourier-Transform Infrared Spectroscopy (FTIR) (Kim et al. 2006)
Kitosan (kontrol) dan karotenoid hasil ultrasonikasi yang menunjukkan distribusi ukuran partikel yang lebih kecil dikeringkan menggunakan alat kering beku (freeze drying) dan dihasilkan serpihan. Kemudian serpihan dilakukan analisis menggunakan FTIR untuk menentukan gugus fungsi sebelum tersalut dan setelah tersalut.
Efisiensi nanoenkapsulasi (Tachaprutinun et al. 2009)
Sebanyak 0.7 gram serpihan karotenoid dicuci sebanyak tiga kali menggunakan heksana-aseton (10:1 v/v). Satu kali pencucian menggunakan 1 mL heksana-aseton, kemudian setelah kering, bobot serpihan ditimbang kembali. Efisiensi penjerapan (EP) atau efisiensi nanoenkapsulasi dapat dihitung melalui rumus:
��=�����������ℎ���������
��������� ∙100%
Analisis derajat kristalinitas nanoenkapsul menggunakan difraksi sinar-X (XRD)
Serpihan nanoenkapsul karotenoid yang diperoleh dianalisis menggunakan metode
difraksi sinar-X (XRD). Teknik XRD
digunakan untuk mengidentifikasi derajat kristalisasi nanoenkapsul karotenoid. Hasil yang diperoleh dibandingkan dengan literatur.
HASIL DAN PEMBAHASAN
Ekstrak Karotenoid
9
Pelarut yang digunakan dalam penelitian ini adalah campuran heksana-aseton dengan perbandingan 10:1 v/v. Penggunaan bahan pengekstrak heksana-aseton (10:1 v/v) tersebut didasarkan atas sifat kelarutan dan keterikatan karotenoid dalam jaringan tanaman. Heksana merupakan pelarut non-polar, sedangkan aseton merupakan pelarut semi polar. Penambahan aseton 1% pada pelarut heksana pada bahan pengekstrak akan menghasilkan ekstrak dengan konsentrasi
karotenoid yang tinggi (Jaren-Galan et al.
1991).
Karotenoid termasuk senyawa yang bersifat non-polar, karena itu penggunaan pelarut hanya aseton tidak dapat digunakan. Keberadaan karotenoid dalam jaringan tanaman bisa terikat pada senyawa polar maupun non-polar, maka penggunaan bahan pengekstrak campuran heksana dan aseton dapat berperan melarutkan karotenoid yang bebas maupun terikat.
Metode ekstraksi pelarut telah banyak digunakan oleh beberapa penelitian untuk mengekstrak karotenoid, antara lain penelitian oleh Kurilich et al. pada tahun 1999 yang
mengekstrak karotenoid dari Brassica
oleraceae, dan penelitian oleh Masni pada tahun 2004 yang mengekstrak karotenoid dari limbah pabrik kelapa sawit.
Pencampuran ekstrak dengan pelarut dilakukan dalam labu Erlenmeyer tertutup, terlindung cahaya dengan menggunakan aluminium foil dan proses penyaringan ekstrak dilakukan pada kondisi intensitas cahaya rendah. Hal tersebut dilakukan untuk mencegah kerusakan karotenoid akibat intensitas cahaya yang tinggi. Suhu ekstraksi yang digunakan adalah 45oC. Suhu digunakan
untuk meningkatkan hasil ekstraksi
karotenoid. Penggunaan suhu diatas 60oC
dapat mengakibatkan isomerisasi, epoksidasi dan degradasi karotenoid tergantung pada
tingkat suhu dan waktu pemanasan (Hoang et
al. 2011). Penggunaan suhu 45oC tersebut
tidak akan merusak karotenoid. Hasil
ekstraksi didiamkan dalam wadah berisi es
selama 15 menit sebelum dilakukan
penyaringan dengan kertas saring memiliki tujuan agar pengotor asam lemak jenuh memadat dan tersaring di atas kertas saring.
Hasil ekstraksi dari limbah serat buah kelapa sawit berupa larutan berwarna kuning kemerahan karena adanya pigmen karotenoid yang larut di dalam pelarut heksana-aseton (Gambar 4). Adanya kandungan karotenoid pada limbah serat buah kelapa sawit dikarenakan oleh asosiasi karotenoid dalam
Gambar 4 Hasil ekstraksi karotenoid dari limbah serat buah kelapa sawit dengan pelarut heksana-aseton (10:1 v/v).
membran yang tidak dapat diekstraksi oleh proses mekanik screw-press (Sanagi 2005).
Ekstrak kasar limbah serat buah kelapa sawit yang sudah didapatkan, dilakukan analisis kualitatif dan kuantitatif menggunakan instrumen HPLC. Hasil analisis menunjukkan bahwa ekstrak kasar dari limbah
serat buah kelapa sawit mengandung β
-karoten sebanyak 1080.29 ppm. Wulandari (2007) melaporkan bahwa CPO memiliki kandungan karoten (provitamin A) dengan kisaran 500-700 ppm. Tingginya kandungan karoten pada limbah serat buah kelapa sawit dikarenakan asosiasi karoten dalam sel membran yang tidak dapat diekstrak oleh
proses tekanan mekanik screw pada
pengolahan produksi CPO, namun dapat diekstraksi dengan metode ekstraksi pelarut. Penelitian ini menghasilkan konsentrasi β -karoten yang cukup tinggi. Hal ini menunjukkan bahwa limbah serat buah kelapa sawit dapat menjadi sumber karotenoid yang murah.
Penelitian yang dilakukan oleh May (1994) melaporkan bahwa karotenoid yang diekstrak dari limbah serat buah kelapa sawit memiliki komposisi utama β- dan α- karoten sekitar 50% dari total karotenoid. Selain itu juga mengandung pitoena, likopen, γ-karoten dan δ-karoten.
Hasil Pemurnian dan Penghilangan Pelarut Ekstrak Karotenoid
Pengotor seperti asam lemak bebas juga mungkin terdapat dalam ekstrak kasar karotenoid dari limbah serat buah kelapa sawit, maka perlu dilakukan proses pemurnian menggunakan kromatografi kolom adsorpsi. Bahan penjerap yang digunakan adalah abu sekam padi.
10
(Proctor & Palaniappan 1989). Semakin tinggi suhu pemanasan semakin besar energi yang dihasilkan untuk memutuskan ikatan antar atom sehingga banyak atom-atom dari unsur lain yang lepas dan hilang sehingga yang tersisa adalah silika. Pada proses pengaktifan abu sekam padi dapat dihasilkan abu sekam padi yang mengandung 61% silika dan 36%
karbon. Pengaktifan abu sekam juga
menyebabkan pori-pori terbuka, luas permukaan besar dan dengan demikian daya serapnya tinggi. Abu sekam padi hasil
pengaktifan (pemanasan pada suhu 120oC
selama 4 jam) berbeda dengan abu sekam padi sebelum pengaktifan secara penampakan fisik (Gambar 5). Pada abu sekam padi setelah pengaktifan terdapat butiran halus berwarna putih yang merupakan indikasi adanya silika.
Prinsip metode ini adalah penjerapan (adsorpsi) komponen minor oleh adsorben dan melepaskan kembali (desorpsi) komponen tersebut menggunakan pelarut atau eluen. Pada abu sekam padi memiliki kapasitas desorpsi yang lebih baik dibandingkan alumina dan silikat sehingga karotenoid yang terikat pada sisi aktif dari adsorben dapat dengan mudah lepas kembali pada saat proses elusi. Hal ini menyebabkan pekatan dengan konsentrasi karotenoid yang tinggi (Proctor & Palaniappan 1989).
Bahan pengelusi yang digunakan pada metode kromatografi kolom adsorpsi adalah campuran heksana aseton (10:1 v/v). Penambahan aseton 0.1-2% dalam heksana dapat memberikan pemisahan dan pemurnian karotenoid yang baik. Pada pemurnian tersebut akan menjerap bahan pengotor yang lain dan membagi ekstrak menjadi beberapa fraksi berdasarkan perbedaan distribusi molekul-molekul komponen di antara fase gerak dan fase diam serta dipengaruhi perbedaan tingkat kepolaran.
Hasil pemekatan ekstrak karotenoid diperoleh tiga fraksi (fraksi I, II dan III). Fraksi I berwarna kuning, fraksi II berwarna kuning kemerahan dan fraksi III berwarna sedikit kuning (Gambar 6). Fraksi II merupakan fraksi yang memiliki kandungan karotenoid tertinggi. Setelah dilakukan analisis kualitatif dan kuantitatif menunjukkan
bahwa kandungan β-karoten pada fraksi II
sebesar 3651.28 ppm. Hal tersebut juga dapat diduga dari intensitas warna lebih tinggi yaitu intesitas warna pada fraksi II lebih tinggi dibandingkan dengan fraksi I dan III. Intensitas warna yang tinggi menunjukkan konsentrasi suatu senyawa karotenoid yang tinggi. Fraksi I dan III tidak digunakan untuk
a b
Gambar 5 Hasil pengaktifan abu sekam padi.
a. Setelah pengaktifan
(Pemanasan pada suhu 120oC
selama 4 jam).
b. Sebelum pengaktifan.
I II III
Gambar 6 Fraksi I, II, dan III hasil pemekatan ekstrak karotenoid menggunakan kromatografi kolom adsorpsi.
tahap penelitian selanjutnya karena kandungan karotenoid yang lebih rendah. Tujuan dari tahap ini adalah untuk memurnikan ekstrak dari pengotor dan memekatkan, sehingga tahap ini tidak didasarkan pada kecepatan alir, hanya perubahan warna yang keluar dari cerat.
Fraksi II dipilih untuk digunakan pada tahap penelitian selanjutnya. Fraksi II dilakukan penghilangan pelarut menggunakan evaporator dan dihembuskan gas nitrogen (N2). Suhu evaporator yang digunakan adalah 45oC. Suhu tersebut tidak merusak karotenoid.
Gas N2 yang digunakan pada penelitian ini
adalah gas N2 P.A (murni), fungsi gas N2 ini adalah untuk mendesak heksana dan aseton yang tersisa setelah evaporasi menguap sehingga diperoleh ekstrak karotenoid yang murni tanpa pelarut. Keuntungan penguapan
pelarut dengan gas N2 ini adalah tidak
11
Nanoenkapsulasi Karotenoid
Bahan penyalut yang digunakan pada nanoenkapsulasi karotenoid ini adalah kitosan. Kitosan yang digunakan diperoleh dari departemen Teknologi Hasil Perairan (THP) IPB. Kitosan tersebut memiliki derajat deasetilasi (DD) 89% dan mutu kualitas kadar air 10%, serta kadar abu 1.1%. Kualitas tersebut sudah memenuhi standar kitosan komersial. Nilai DD menunjukkan adanya transformasi dari gugus asetil yang berikatan dengan atom nitrogen menjadi gugus amina (terjadi penghilangan gugus asetil). Semakin tinggi nilai DD, kualitas kitosan semakin murni.
Kitosan merupakan polielektrolit kationik, sedangkan beberapa jenis karotenoid memiliki
gugus –OH (polianion) sehingga
memungkinkan untuk membentuk ikatan elektrostatik antara kitosan dan karotenoid serta memungkinkan juga karotenoid berada di dalam jaringan ikatan silang (cross-link) kitosan-TPP (tripolifosfat). Karotenoid dapat terperangkap dalam matriks polimer kitosan
membentuk nanopartikel. Struktur yang
dihasilkan dapat mencegah karotenoid mengalami degradasi oksidatif dan enzimatik (Hoang et al. 2011)
Penambahan tripolifosfat (TPP) berfungsi sebagai pembentuk ikatan silang dengan kitosan. Semakin banyak penambahan TPP, karotenoid yang tersalut kitosan semakin kuat dan mengurangi kerutan nanoenkapsul. Kandungan fosfat pada TPP juga memiliki fungsi untuk meningkatkan kemampuan emulsifikasi (Tsai et al. 2011).
Nanoenkapsul karotenoid tersalut matriks kitosan terbentuk dari pemecahan molekul larutan menggunakan alat ultrasonikator yang menghasilkan gelombang ultrasonik. Gelombang ultrasonik intensitas tinggi dapat menginduksi konsekuensi efek fisika dan kimia yang cukup luas. Efek fisika dari intensitas tinggi adalah emulsifikasi, sedangkan efek kimia gelombang
ultrasonikasi tidak secara langsung
berinteraksi dengan molekul-molekul untuk menginduksi suatu perubahan kimia.
Penggunaan gelombang ultrasonik efektif untuk pembuatan materi berukuran nano. Gelombang ultrasonik dapat menimbulkan efek kavitasi akustik. Efek ini akan digunakan dalam pembuatan bahan berukuran nano dengan metode emulsifikasi. Dalam proses
ultrasonikasi terjadi resonansi, ketika
frekuensi gelombang ultrasonik mendekati frekuensi gelembung kavitasi (f=fo) yang pada waktu tertentu dianalogikan gelembung
akan collapse, pada saat tersebut sistem
memiliki energi yang maksimal yang dapat diserap oleh gelembung kavitasi. Hal ini yang menyebabkan nanopartikel yang terkungkung di dalamnya juga dapat terpisah satu sama lain sehingga didapatkan nanoenkapsul dengan ukuran kecil (Bang & Suslick 2010).
Emulsifier yang digunakan pada pembuatan nanoenkapsul karotenoid yaitu tween 80. Surfaktan tersebut merupakan surfaktan nonionik yang berfungsi sebagai emulsifier pada pembuatan nanoenkapsul. Tween 80 merupakan molekul yang diserap oleh permukaan partikel untuk mencegah
terjadinya gumpalan. HLB (Hydrophile
Lipophile Balance) tween 80 adalah 15.0. Nilai hydrophile lipophile balance tersebut menentukan sistem emulsi surfaktan.
Surfaktan atau pengemulsi lebih hidrofilik memiliki nilai HLB lebih besar dari 10, sedangkan pengemulsi lebih lipofilik memiliki
nilai HLB sekitar 1-10 (Bouchemal et al.
2004). Nilai HLB tween 80 yang tinggi
tersebut menyebabkan sistem yang stabil pada
sistem emulsi o/w (oil in water) karena
didominasi oleh hidrofilik. Pengaruh surfaktan dapat menurunkan tegangan permukaan.
Semakin tinggi konsentrasi surfaktan,
kemampuannya untuk menurunkan tegangan permukaan antar lapisan larutan karotenoid dan matriks kitosan semakin baik. Karotenoid akan terserap pada pemukaan matriks kitosan atau berada pada inti matriks. Sistem emulsi nanoenkapsulasi o/w tersebut menyebabkan hasil nanoenkapsulasi karotenoid dapat didispersikan dalam medium pendispersi air. Hal ini sangat bermanfaat untuk industri pangan dan farmasi karena pada industri tersebut umumnya menggunakan medium pendispersi air.
Ukuran Nanopartikel Karotenoid Tersalut Kitosan
Lama waktu dan besarnya amplitudo yang digunakan dalam tahap ultrasonikasi sangat berpengaruh terhadap energi yang dihasilkan dan proses kavitasi. Pada penelitian ini menggunakan variasi waktu ultrasonikasi yaitu 60 menit dan 90 menit, sedangkan besarnya amplitudo yang digunakan tetap yaitu 30%. Hal ini dilakukan untuk
mengetahui waktu ultrasonikasi yang
12
semakin besar. Besarnya energi sangat berpengaruh terhadap pemecahan molekul di dalam emulsi, sehingga energi yang besar diharapkan dapat mereduksi ukuran nanopartikel menjadi lebih kecil.
Penentuan ukuran dan jumlah nanoenkapsul karotenoid yang dihasilkan
dilakukan menggunakan Particle Size
Analyzer (PSA). PSA adalah instrumen yang dapat mengukur ukuran partikel sampel dalam bentuk emulsi atau larutan. Penggunaan PSA lebih akurat jika dibandingkan dengan Scanning Electron Microscopy (SEM) dan Transmssion Electron Microscopy (TEM) karena pada penggunaan instrumen PSA, partikel didispersikan ke dalam media sehingga partikel tidak saling beraglomerasi (menggumpal). PSA dapat mendeteksi ukuran setiap partikel tunggal, ukuran rata-rata, dan nilai indeks polidispersitas (PI). PI merupakan ukuran lebarnya distribusi ukuran partikel. Nilai PI lebih kecil dari 0.3 menunjukkan bahwa ukuran partikel memiliki distribusi sempit dan ukuran partikel lebih homogen, sedangkan nilai PI lebih besar dari 0.3 menunjukkan distribusi yang lebar dan ukuran partikel cenderung tidak seragam.
Karakteristik dengan PSA dilakukan pada suhu 25oC menggunakan pelarut air, indeks bias 1.3328, dan derajat viskositas 0.8878 cP. Hasil PSA pada fraksi II yang diultrasonikasi selama 60 menit menunjukkan distribusi ukuran 131-446.5 nm (Gambar 7), sedangkan hasil PSA pada fraksi II yang diultrasonikasi selama 90 menit menunjukkan distribusi ukuran 491.9-1796.2 nm (Gambar 8). Hasil tersebut menunjukkan ultrasonikasi selama 60 menit memiliki distribusi ukuran partikel yang lebih kecil (Tabel 3).
Distribusi ukuran nanoenkapsul pada ultrasonikasi selama 90 menit lebih besar disebabkan oleh sistem emulsi yang tidak
stabil (coarse emulsion) sehingga terjadi
aglomerasi (penggumpalan) partikel (Hoang et al. 2011). Sistem emulsi yang tidak stabil ini dapat disebabkan oleh energi yang dihasilkan ultrasonikasi selama 90 menit terlalu besar sehingga merusak sistem emulsi. Selain itu, kenaikan suhu yang terlalu tinggi menyebabkan pelarut mencapai titik didihnya dan menghasilkan gelembung kavitasi yang lebih besar. Aktivitas tersebut selanjutnya menghambat proses transmisi suara ultrasonik dan meniadakan efek energi ultrasonikasi, akibatnya larutan mengalami penggumpalan kembali. Penggunaan surfaktan dalam jumlah kecil dan tingkat pengadukan rendah juga menyebabkan diameter partikel lebih besar.
Gambar 7 Sebaran diameter nanoenkapsul karotenoid pada ultrasonikasi 60 menit.
Gambar 8 Sebaran diameter nanoenkapsul karotenoid pada ultrasonikasi 90 menit.
Tabel 3 Ukuran rata-rata nanoenkapsul dan
indeks polidispersitas pada
ultrasonikasi 60 dan 90 menit.
Ultrasonikasi
Ukuran rata-rata
(nm)
Indeks Polidispersitas
60 menit 159.9 0.69
90 menit 606.5 0.80
13
Penelitian ini menunjukkan bahwa waktu ultrasonikasi optimum pembuatan nanoenkapsul karotenoid adalah 60 menit. Penelitian yang lain seperti yang dilakukan oleh Farichah (2011) pada pembuatan nanopartikel ketoprofen dengan penyalut kitosan juga memperoleh waktu ultrasonikasi optimum 60 menit.
Distribusi ukuran nanoenkapsul karotenoid yang diperoleh luas (ukuran partikel tidak seragam) hal ini juga ditunjukkan oleh nilai indeks polidispersitas yang lebih dari 0.3 (Tabel 3). Hal ini dapat disebabkan oleh
adanya agregasi nanopartikel, beberapa
nanopartikel berinteraksi satu sama lain (Kim et al. 2006). Hal tersebut juga dapat disebabkan oleh konsentrasi surfaktan yang terlalu kecil tidak mampu menstabilkan pecahan partikel yang terbentuk sehingga partikel yang telah terpecah beraglomerasi kembali. Upaya yang dapat dilakukan untuk menghomogenkan distribusi ukuran nanoenkapsul adalah dengan peningkatan konsentrasi surfaktan dan dilakukan proses sentrifugasi.
Dari hasil PSA juga menunjukkan bahwa pada ultrasonikasi selama 60 menit menghasilkan distribusi jumlah partikel berukuran di bawah 1000 nm sebanyak 99.9% dan ultrasonikasi selama 90 menit sebanyak 96.6%. Hasil tersebut menunjukkan bahwa penelitian ini telah berhasil membuat partikel berukuran nano. Hasil ultrasonikasi selama 60 menit dipilih untuk digunakan pada tahap penelitian selanjutnya.
Hasil ultrasonikasi selama 60 menit tersebut kemudian dikeringkan menggunakan
alat pengering beku (freeze drying) dan
dianalisis lebih lanjut menggunakan instrumen Fourier-Transform Infrared Spectroscopy (FTIR), dan difraksi sinar-X (XRD), serta
dilakukan penentuan efisiensi
nanoenkapsulasi. Pengeringan beku umumnya diterapkan untuk meningkatkan stabilitas fisikokimia dari suatu nanopartikel. Teknik pengeringan beku ini melibatkan pembekuan suspensi dan penghilangan kadar air dengan sublimasi pada tekanan rendah. Setelah pengeringan selesai, nanopartikel diperoleh dalam bentuk serpihan atau bubuk kecil kering yang mudah digunakan dan disimpan dalam wadah. Karotenoid dalam bentuk nanoenkapsul memiliki kestabilan selama
penyimpanan yang lebih baik. (Reis et al.
2006).
Fraksi II ultrasonikasi 60 menit setelah dikeringkan diperoleh padatan berupa serpihan berwarna kuning (Gambar 9).
Gambar 9 Serpihan fraksi II nanoenkapsul karotenoid.
Nanoenkapsul karotenoid mengalami agregasi setelah proses kering beku, hal ini ditunjukkan dengan hasil akhir berupa serpihan. Kristalisasi es juga dapat memberikan tekanan mekanik kepada nanopartikel yang menyebabkan destabilisasi nanopartikel
(Abdelwahed et al. 2006). Hal ini dapat
diatasi dengan penambahan senyawa sebagai
krioprotektan dan lioprotektan seperti
trehalose dan laktosa. Senyawa tersebut perlu ditambahkan ke formulasi atau suspensi nanopartikel sebelum pembekuan untuk melindungi nanopartikel dari tekanan atau
stress pembekuan (krioprotektan) dan
pengeringan (lioprotektan) serta
meningkatkan kestabilan pada saat
penyimpanan (Abdelwahed et al. 2006).
Setelah dilakukan perhitungan rendemen, rendemen serpihan fraksi II nanoenkapsul karotenoidasi yang diperoleh adalah sebesar 2.2485% b/v.
Gugus Fungsi Spesifik Nanopartikel Karotenoid Tersalut Kitosan Kitosan (kontrol), karotenoid fraksi II dan karotenoid hasil ultrasonikasi 60 menit setelah dikeringkan dianalisis menggunakan FTIR. Gugus fungsi merupakan identitas suatu senyawa. Analisis FTIR dimaksudkan untuk melihat perubahan gugus fungsi nanoenkapsul karotenoid yang telah dihasilkan. Spektrum FTIR nanoenkapsul karotenoid tersebut dibandingkan dengan spektrum FTIR kitosan dan karotenoid.
Spektrum FTIR kitosan memiliki tiga puncak karakteristik spesifik yaitu pada bilangan gelombang 3434 cm-1 (O-H), 1098 cm-1 (C-O-C), dan 1597 cm-1 (NH2). Pada nanoenkapsul karotenoid fraksi II, puncak spesifik kitosan pada bilangan gelombang 1597 cm-1 dibagi untuk semi-doublet karena interaksi elektrostatik antara gugus amina dari
kitosan dan hidroksil dari kelompok
karotenoid. Selain itu, puncak spesifik dari karotenoid pada bilangan gelombang 1720
cm-1 secara signifikan menurun saat
14
nanopartikel kitosan. Hasil ini menunjukkan bahwa pada nanoenkapsulasi karotenoid terdapat pembentukan kompleks ion antara kitosan dan karotenoid dalam formasi partikel berukuran nano (Kim et al. 2006).
Hasil analisis menggunakan FTIR juga terlihat bahwa terjadi pergeseran bilangan gelombang (perubahan intensitas transmitan di beberapa daerah pita serapan) pada beberapa gugus fungsi pada nanoenkapsul karotenoid dibandingkan dengan kitosan dan karotenoid (Gambar 10). Regangan O-H pada kitosan terdapat pada bilangan gelombang
3434 cm-1, sedangkan nanoenkapsul
karotenoid pada bilangan gelombang 3429 cm-1. Pada karotenoid regangan C=C terbaca
pada bilangan gelombang 1466 cm-1,
sedangkan pada nanoenkapsul karotenoid terbaca di bilangan gelombang 1560 cm-1. Pergeseran tersebut disebabkan adanya
interaksi antara gugus fungsi kitosan dengan tripolifosfat (TPP) dan karotenoid.
Spektrum FTIR pada karotenoid yang nanoenkapsulasi memiliki gugus fungsi khas kitosan dan gugus fungsi khas karotenoid fraksi II (Tabel 4) sehingga dapat disimpulkan bahwa karotenoid fraksi II sudah tersalut oleh penyalut kitosan.
Efisiensi Penjerapan Karotenoid di dalam Kitosan Nanopartikel
Efisiensi penjerapan (EP) merupakan nilai dalam persen yang dapat menggambarkan seberapa banyak karotenoid yang terjerap dalam nanopartikel kitosan. Semakin tinggi nilai EP berarti semakin banyak senyawa yang digunakan berhasil dijerap di dalam materi penyalut. Sebanyak 0.70 gram serpihan nanoenkapsul karotenoid dilakukan pencucian sebanyak tiga kali, lalu ditimbang kembali.
Tabel 4 Gugus fungsi khas pada kitosan, karotenoid, dan nanoenkapsul karotenoid.
Gambar 10 Spektrum FTIR kitosan, karotenoid, dan nanoenkapsul karotenoid. Gugus
Fungsi
Bilangan Gelombang (cm-1)
Kitosan Karotenoid Nanoenkapsul Karotenoid
Literatur (Creswell et al.
2005)
Regangan (O-H) 3434 3443 3429 3750-3000
Regangan (N-H) 1597 - 1649 1660-1500
Tekukan (C-H) 1383 - 1416 1475-1300
Regangan (C-O-C) 1098 - 1101 1150-1085
Sikloheksena - 1741 1738 1720-1750
Regangan (C=C) - 1466 1560 1667-1440
15
Bobot setelah dicuci adalah 0.53 gram. Efisiensi nanoenkapsulasi karotenoid yang diperoleh adalah sebesar 76%. Hal ini menunjukkan bahwa sebanyak 76%
karotenoid terjerap berada di inti
(nanocapsule) sedangkan sisanya berada
dipermukaan kapsul (nanospheres) sehingga
pada saat pencucian karotenoid pada permukaan nanoenkapsul ikut tercuci (pada supernatannya). Nilai efisiensi penjerapan juga berkaitan dengan jumlah nanoenkapsul karotenoid yang terbentuk. Semakin banyak jumlah nanopartikel kitosan, maka semakin besar luas permukaan partikel tersebut. Dengan semakin besarnya luas permukaan maka semakin besar kemampuan nanopartikel kitosan dalam menjerap karotenoid.
Derajat Kristalinitas Nanopartikel Karotenoid Tersalut Kitosan Metode difraksi sinar-X (XRD) adalah salah satu cara untuk mempelajari keteraturan atom atau molekul dalam suatu struktur tertentu. Difraksi sinar-X dapat memberikan informasi tentang struktur polimer, termasuk tentang keadaan amorf dan kristalin polimer. Polimer dapat mengandung daerah kristal yang secara acak bercampur dengan daerah amorf.
Derajat kristalinitas adalah besaran yang menyatakan banyaknya kandungan kristal dalam suatu materi dengan membandingkan luasan kurva kristalin terhadap luasan kurva
kristalin dan amorf. Semakin besar derajat kristalinitas suatu materi maka fasa materi tersebut semakin kristal. Semakin kecil derajat kristalinitas suatu materi, fasa materi tersebut semakin amorf. Diantara fasa amorf dan kristalin suatu materi terdapat fasa semi
kristalin. Hasil analisis menggunakan
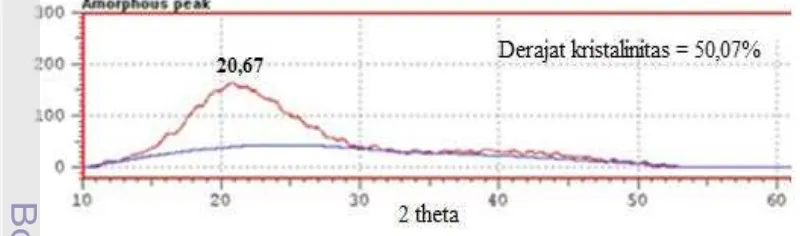
instrumen difraksi sinar X (XRD), nanoenkapsul karotenoid hanya terdapat satu puncak yaitu pada 20.67o 2tetha (Gambar 11). Karotenoid memiliki puncak spesifik kristal tajam dan kitosan memiliki puncak spesifik yang luas atau melebar (Kim et al. 2006).
Ketika karotenoid dinanoenkapsulasi ke
dalam nanopartikel kitosan, puncak tajam
kristalin karotenoid menghilang dan
digantikan dengan hasil puncak yang sedikit melebar.
Derajat kristalinitas nanoenkapsul
karotenoid yang diperoleh adalah 50.1%
sedangkan kitosan murni memiliki
kristalinitas yang rendah yaitu 37% (Farichah 2011). Meningkatnya kristalinitas tersebut disebabkan oleh proses pembuatan kitosan menjadi nanopartikel terisi karotenoid dapat
meningkatkan derajat kristalinitas dari
kitosan. Hasil tersebut menunjukkan bahwa nanopartikel ekstrak karotenoid fraksi II tersalut kitosan berstruktur semi kristalin. Proses nanoenkapsulasi tersebut mengubah bentuk kitosan murni yang berstruktur amorf menjadi semi kristalin saat terisi karotenoid (Farichah2011).
Gambar 11 Hasil XRD nanoenkapsul karotenoid.
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil penelitian ini dapat disimpulkan bahwa karotenoid dapat diisolasi dari limbah serat buah kelapa sawit dan dinanoenkapsulasi menggunakan penyalut kitosan. Fraksi II merupakan fraksi terbaik dengan kandungan β-karoten sebesar 3651.3
ppm. Ultrasonikasi selama 60 menit
16
Saran
Analisis ini akan lebih baik jika dilakukan optimasi pada proses nanoenkapsulasi menggunakan variasi amplitudo gelombang ultrasonik dan konsentrasi surfaktan yang digunakan sehingga ukuran nanoenkapsul yang diperoleh lebih kecil. Selain itu perlu adanya penelitian lanjutan mengenai aktivitas antioksidan karotenoid setelah dilakukan nanoenkapsulasi.
DAFTAR PUSTAKA
Abdelwahed W, Degobert G, Stainmesse S, Fessi H. 2006. Freeze-Drying of
nanoparticles: formulation,
process and storage
considerations. Advance Drug
Delivery Reviews 58: 1688-1713. Baharin BS, Rahman KA, Karim MIA,
Oyaizu T, Tanaka K. 1998. Separation of palm carotene from crude palm oil by adsorption chromatography with a synhetic
polymer adsorbent. J Am Oil
Chem Soc 75(3): 399-404. Bakri. 2009. Komponen kimia dan fisik abu
sekam padi sebagai SCM untuk pembuatan komposit semen. Jurnal Perennial 5(1): 9-14.
Balaz P. 2008. Mechanochemistry,
Nanoscience, and Minerals Engineering. Berlin: Springer. Bang JH, Suslick KS. 2010. Applications of
ultrasound to the synthesis of
nanostructured materials.
Advanced Materials 22(10): 1039-1059.
Boucemal K, Briancon S, Perrier E, Fessi H. 2004. Nano-emulsion formulation using spontaneous emulsification: solvent oil and surfactant
optimisation. International
Journal of Pharmaceutics 280: 241-251.
Choo YM, Yap SC, Ooi CK, Ma AN, Goh SH, Oong AS. 1996. Recovered oil from Palm-Pressed Fiber: a good source of natural carotenoids, vitamin E, and sterol. J Am Oil Chem Soc 73(5): 599-602.
Creswell CJ, Runquist OA, Campbell MM. 2005. Anallisis Spektrum Senyawa Organik. Bandung: ITB Press.
Cui Z. 2008. Nanofabrication: Principles,
Capabilities and Limits. New York: Springer.
Farichah F. 2011. Peningkatan jumlah
nanopartikel kitosan terisi
ketoprofen dengan metode ultrasonikasi berdasarkan ragam waktu amplitudo sonikasi [tesis]. Bogor : Program Pascasarjana, Institut Pertanian Bogor.
Fennema OR. 1996. Food Chemistry. Third
Edition. New York: Marcel Dekker Inc.
Goodwin TW. 1976. Chemistry and
Biochemistry of Plant Pigments II. Second Edition. London: Academic Press.
Hoang LC, Fougere R, Wache Y. 2011. Increase in stability and change in
supramolecular structure of β
-carotene through encapsulation into poly lactic acid nanoparticles. Food Chemistry 124: 42-49.
Irawadi TT. 1991. Produksi enzim
ekstraselular (selulase dan xilanase)
dari Neurospora sitophila pada
substrat limbah padat kelapa sawit [disertasi]. Bogor: Program Pascasarjana. Institut Pertanian Bogor, Bogor.
Jaren-Galan M, Nienaber U, Schwartz SJ.
1999. Paprika (Capsicum annuum)
oleoresin extraction with
supercritical carbon dioxide. J
Agric Food Chem 47(9): 3558-3564.
Kim et al. 2006. Retinol-encapsulated low molecular water soluble chitosan
nanoparticles. International
Journal of Pharmaceutics 319: 130-138.
Knorr D. 1982. Functional properties of chitin
and chitosan. Food Science 47:
593-595.
Kumar MR. 2000. A review of chtitin and chitosan applications. Reactive and Functional Polym