SINTESIS DAN UJI
IN VITRO
HIDROKSIAPATIT
BERPOROGEN KITOSAN DENGAN METODE SOL GEL
AYU ROMAWARNI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
AYU ROMAWARNI. Sintesis dan Uji
In Vitro
Hidroksiapatit Berporogen
Kitosan dengan Metode Sol Gel. Dibimbing oleh ARMI WULANAWATI dan
SULISTIOSO GIAT SUKARYO.
Hidroksiapatit (HAp) memiliki sifat biokompatibilitas yang baik dengan
tulang karena memiliki kesamaan komposisi kimia dengan tulang. Salah satu
metode sintesis HAp adalah metode sol gel. Metode sol gel dapat digunakan
untuk menghasilkan kristal HAp yang baik. HAp berpori dibuat dari kalsium yang
diperoleh dari cangkang telur dengan penambahan asam fosfat dan kitosan.
Penelitian dilakukan dengan ragam volume larutan kitosan yang ditambahkan,
yaitu 30, 40, 50, dan 60 mL. Analisis sampel dilakukan dengan menggunakan
difraksi sinar-X (XRD), mikroskop elektron payaran (SEM), dan spektrofotometer
serapan atom (AAS). Pencirian dengan XRD terhadap HAp-kitosan yang telah
dikalsinasi menunjukkan tidak ada puncak kitosan, hanya terdapat puncak milik
HAp. Pencirian dengan SEM menunjukkan bahwa penghilangan kitosan melalui
kalsinasi menghasilkan HAp dengan pori berukuran mikro. Uji
in vitro
menunjukkan bahwa terjadi penurunan konsentrasi kalsium setelah 6 hari
perendaman sampel dalam larutan
simulated body fluid
(SBF). Penurunan ini
disebabkan oleh pengendapan ion kalsium pada permukaan HAp berpori untuk
membentuk kristal apatit.
ABSTRACT
AYU ROMAWARNI. Synthesis and
In Vitro
Test of Porous
Hydroxyapatite-Chitosan with Sol Gel Method. Supervised by ARMI WULANAWATI and
SULISTIOSO GIAT SUKARYO.
Hydroxyapatite (HAp) has good compatibility with bone as its chemical
composition is similiar to that of bone material. One method to synthesize HAp is
a sol gel method. Sol gel method can be used to produce a good crystallize of
HAp. Porous HAp was made from calcium obtained from eggshell with the
addition of phosphoric acid and chitosan. The study was conducted by varying the
volume of chitosan solution, i.e. 30, 40, 50, and 60 mL. The porous HAp was
characterized using X-ray diffraction (XRD), scanning electron microscope
(SEM), and atomic absorption spectroscopy (AAS). XRD characterization of the
calcined HAp-chitosan showed that the chitosan peak was totally removed,
leaving behind all of the characteristic peaks of HAp. SEM characterization
showed that removal of chitosan through calcination leads to HAp containing
microsize pores.
In Vitro
test showed that calcium ions concentration decreasing
SINTESIS DAN UJI
IN VITRO
HIDROKSIAPATIT
BERPOROGEN KITOSAN DENGAN METODE SOL GEL
AYU ROMAWARNI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Sintesis dan Uji
In Vitro
Hidroksiapatit Berporogen Kitosan dengan
Metode Sol Gel
Nama : Ayu Romawarni
NIM : G44070040
Disetujui
Pembimbing I Pembimbing II
Armi Wulanawati, S.Si, M.Si.
Drs. Sulistioso Giat Sukaryo, MT
NIP 196907252000032001
NIP 195708261988011002
Diketahui
Ketua Departemen Kimia
Prof. Dr. Ir. Tun Tedja Irawadi, M.S.
NIP 19501227 197603 2 002
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT atas segala
karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini
dilaksanakan dari bulan Maret sampai Juli 2011 yang bertempat di Laboratorium
PTBIN BATAN-PUSPIPTEK Serpong serta Laboratorium Kimia Fisik,
Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut
Pertanian Bogor.
Terima kasih penulis ucapkan kepada Ibu Armi Wulanawati, S.Si, M.Si.
dan Bapak Drs. Sulistioso Giat Sukaryo, MT selaku pembimbing selama
penelitian dan penyusunan karya ilmiah ini. Penulis juga mengucapkan terima
kasih kepada Ibu Wahyu, Bapak Bambang Sugeng, Ibu Deswita, Bapak Yosef,
Bapak Wagio dari Badan Atom Teknologi Nuklir (BATAN) Puspiptek Serpong,
Bapak Syawal, Bapak Ismail, Bapak Nano, Ibu Ai dari staf Laboratorium Kimia.
Terima kasih tak terhingga penulis ucapkan kepada keluarga atas segala doa,
dukungan, dan kasih sayangnya.
Semoga tulisan ini dapat bermanfaat bagi penulis maupun pembaca.
Bogor, Juni 2011
RIWAYAT HIDUP
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA ... 1
Hidroksiapatit ... 1
Kitosan ... 1
Metode Sol Gel ... 2
BAHAN DAN METODE ... 2
Bahan dan Alat ... 2
Tahapan Penelitian ... 2
Preparasi Cangkang Telur ... 2
Sintesis Hidroksiapatit ... 2
Preparasi Larutan Kitosan ... 2
Sintesis Hidroksiapatit Berporogen Kitosan ... 2
Pencirian dengan XRD dan SEM ... 3
Uji
In Vitro
dengan Larutan SBF ... 3
HASIL DAN PEMBAHASAN ... 3
Komposisi Cangkang Telur ... 3
Sintesis dan Pencirian Hidroksiapatit ... 4
Sintesis dan Pencirian Hidroksiapatit Berporogen Kitosan ... 4
Morfologi Hidroksiapatit ... 6
Uji
In Vitro
dalam Larutan SBF ... 7
SIMPULAN DAN SARAN ... 7
Simpulan ... 7
Saran ... 8
DAFTAR PUSTAKA ... 8
DAFTAR TABEL
Halaman
1
Komposisi HAp-kitosan ... 3
2
Hasil pengukuran konsentrasi kalsium ... 7
DAFTAR GAMBAR
Halaman
1
Struktur kitosan ... 2
2
Pola difraksi sinar-X cangkang telur setelah kalsinasi ... 4
3
Pola difraksi sinar-X (a) HAp sintesis dan (b) HAp komersial ... 4
4
Pola difraksi sinar-X kitosan ... 5
5
Pola difraksi sinar-X HAp dengan penambahan kitosan (a) 30 mL,
(b) 40 mL, (c) 50 mL, (d) 60 mL ... 5
6
Hasil SEM sampel pada perbesaran 3000x (a) HAp sintesis dan
(b) HAp komersial ... 6
7
Hasil SEM HAp dengan penambahan kitosan (a) 30 mL, (b) 40 mL,
(c) 50 mL, (d) 60 mL pada perbesaran 3000x ... 6
DAFTAR LAMPIRAN
Halaman
1
Diagram alir penelitian ... 11
2
Data JCPDS (a) HAp, (b) CaO, (c) AKA, (d) AKB ... 12
3
Data XRD serbuk cangkang telur ... 14
4
Data komposisi bahan yang digunakan untuk menghasilkan sampel ... 14
5
Data analisis hasil XRD sampel ... 15
6
Morfologi SEM HAp dengan penambahan kitosan 30 mL ... 18
PENDAHULUAN
Tingkat kecelakaan meningkat setiap tahunnya, di antara kecelakaan tersebut tidak sedikit yang tergolong kecelakaan berat atau sampai mengalami kerusakan tulang. Sel-sel tulang sebenarnya memiliki kemampuan untuk memulihkan diri tetapi pemberian pengganti tulang bisa mempercepat pemulihan secara lebih sempurna (Dahlan 2010). Pemilihan material yang tepat sangat diperlukan dalam proses pemberian pengganti tulang, antara lain mudah diperoleh, biokompatibel, bioaktif, dan tidak toksik (Riyani 2005). Material pengganti tulang yang umum digunakan adalah autograf (penggantian satu bagian tubuh dengan bagian tubuh lainnya dalam satu individu), allograf (penggantian tulang manusia dengan tulang yang berasal dari manusia lain), xenograf (penggantian tulang manusia dengan tulang yang berasal dari hewan). Namun, material pengganti tulang ini biasanya tersedia dalam jumlah terbatas (Ratih et al. 2003).
Adanya keterbatasan dalam setiap material, memicu perkembangan riset di bidang material. Hingga saat ini studi mengenai material terus berkembang, terutama material hidroksiapatit (HAp). Baru-baru ini, perhatian khusus pada penyusunan keramik HAp dengan morfologi berpori. HAp berpori telah digunakan dalam aplikasi medis termasuk regenerasi jaringan tulang. Material HAp berpori yang dimasukkan ke dalam tulang yang patah berfungsi untuk membantu dan merangsang pertumbuhan jaringan tulang serta secara bertahap akan digantikan oleh jaringan tulang yang baru (Kim et al. 2007).
Sopyan et al. (2007) menyatakan bahwa
pembentukan HAp berpori dapat dilakukan menggunakan bahan porogen yang akan menghilang selama proses kalsinasi.
Bahan-bahan yang dapat digunakan sebagai porogen antara lain: parafin, naftalena, pati atau beberapa polimer seperti poli(asam laktat), gelatin, alginat, dan kitosan. Pada penelitian ini menggunakan kitosan sebagai porogen karena kitosan banyak terdapat di alam salah satunya dari kulit udang. Sintesis HAp dapat dilakukan dengan 2 metode, yaitu metode kering dan basah (sol gel) (Aoki 1991). Menurut Vijayalakshmi dan Rajeswari (2006) keuntungan menggunakan metode basah (sol gel) dalam prosesnya akan menghasilkan HAp yang memiliki kemurnian yang cukup tinggi.
Dengan demikian, penelitian ini bertujuan membuat hidroksiapatit berpori menggunakan kitosan sebagai porogen dengan metode sol
gel. Selanjutnya dilakukan pencirian dengan
X-ray diffraction (XRD), scanning electron
microscopy (SEM) dan mengevaluasi
pertumbuhan kristal apatit menggunakan
simulated body fluid (SBF).
TINJAUAN PUSTAKA
Hidroksiapatit
Hidroksiapatit merupakan senyawa mineral dan anggota kelompok mineral apatit dengan rumus kimia Ca10(PO4)6(OH)2 sebagai
suatu bahan keramik yang memiliki kesamaan komposisi kimia dengan jaringan tulang asli (Javidi et al. 2008). HAp dapat diperoleh dari
sumber alami atau melalui sintesis kimia. Material HAp dapat disintesis dengan menggabungkan sumber Ca dan P. Sintesis HAp dapat dilakukan dengan metode basah dan metode kering. Metode basah menggunakan prinsip presipitasi atau sol-gel sedangkan metode kering menggunakan prinsip pencampuran 2 senyawa sumber Ca dan P pada suhu tinggi (Aoki 1991). Menurut metode basah, HAp disintesis dengan cara mentitrasi larutan yang mengandung Ca dengan larutan yang mengandung P. Nisbah Ca/P agar material HAp terbentuk adalah 1,67 (Prabakaran et al. 2005). HAp memiliki sifat
biokompatibel dan bioaktif. Biokompatibel adalah kemampuan material untuk menyesuaikan dengan kecocokan tubuh penerima, sedangkan bioaktif adalah kemampuan material bereaksi dengan jaringan dan menghasilkan ikatan kimia sangat baik (Ratih et al. 2003).
Kitosan
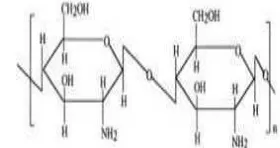
Kitosan merupakan salah satu turunan kitin yang diperoleh melalui proses deasetilasi. Kitosan tersusun atas unit berulang 2-amino-2-deoksi-D-glukopiranosa yang terhubung oleh ikatan β-(1-4) (Gambar 1). Kitosan berbentuk padatan amorf dan dapat larut dalam asam organik seperti asam format, asam asetat, asam sitrat (Austin 1984). Kitosan adalah polimer alam yang memiliki sifat biodegradabel, tidak beracun, dan biokompatibel (Kim et al. 2007). Sifatnya
2
dengan hidroksiapatit untuk membentuk suatu komposit material yang menunjukkan sifat-sifat polimer biomedis seperti non-toksik, biokompatibel, dan biodegradabel (Sutriyo et al. 2005).
Gambar 1 Struktur kitosan.
Metode Sol Gel
Metode sol gel adalah sebuah teknik untuk membentuk material gelas dan keramik. Proses sol gel diawali dengan pembentukan koloid yang memiliki padatan tersuspensi di dalam larutannya (kondisi ini disebut sol). Sol ini kemudian akan mengalami perubahan fase menjadi gel, yaitu koloid yang memiliki fraksi solid yang lebih besar daripada sol. Gel ini akan mengalami kekakuan dan dapat dipanaskan untuk membentuk keramik (Dawnay 1997).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah cangkang telur ayam negeri, H3PO4 80%,
etanol 96%, kitosan komersial, larutan asam asetat 2%, HAp komersial, cairan infus (0,9%
Sodium chloride, Otsu-NS).
Alat-alat yang digunakan adalah alat-alat kaca, neraca analitik, hot plate, pengaduk
magnetik, tanur, X-ray diffraction (XRD)
merk Philips tipe Shimadzu 610, scanning
electron microscopy (SEM), atomic
absorption spectroscopy (AAS) Shimadzu
AA-7000.
Tahapan Penelitian
Penelitian ini terbagi atas beberapa tahap, yaitu tahap pertama preparasi cangkang telur, tahap kedua sintesis hidroksiapatit, tahap ketiga preparasi larutan kitosan, tahap keempat sintesis hidroksiapatit berporogen kitosan, tahap kelima pencirian dengan XRD
dan SEM, tahap keenam uji in vitro dengan
larutan SBF. Diagram alir penelitian dapat dilihat pada Lampiran 1.
Preparasi Cangkang Telur
Preparasi dilakukan berdasarkan modifikasi metode Amrina (2008). Cangkang telur diberi perlakuan meliputi pembersihan, pengeringan dan kalsinasi. Perlakuan diawali dengan pembersihan cangkang telur dari kotoran makro, eliminasi membran cangkang kemudian dikeringkan di suhu kamar. Cangkang yang telah kering lalu dikalsinasi pada suhu 1000 ºC selama 6 jam. Cangkang yang telah dikalsinasikan berbentuk serbuk lalu dilakukan pencirian dengan XRD untuk mengetahui fase yang terkandung di dalamnya.
Sintesis Hidroksiapatit
Hidoksiapatit dibuat melalui modifikasi metode Septiarini (2009). Serbuk cangkang telur hasil kalsinasi ditambahkan etanol 96% sebanyak 50 mL kemudian dicampurkan dengan 3 mL H3PO4 80% yang dilarutkan
dalam 50 mL etanol 96% dilakukan dengan penetesan dari buret. Campuran tersebut diaduk dengan kecepatan pengadukan 300 rpm pada suhu 37 ºC selama 20 menit kemudian dipanaskan dalam penangas air bersuhu 60 ºC selama 1 jam. Larutan diendapkan dalam suhu kamar selama 24 jam kemudian diaduk pada suhu 60 ºC sampai larutan berubah menjadi gel. Gel yang diperoleh dipanaskan dalam tanur pada suhu 1000 ºC selama 5 jam.
Preparasi Larutan Kitosan
Larutan kitosan dibuat melalui modifikasi metode Kim et al. (2007). Larutan kitosan 4%
dibuat dengan melarutkan 4 gram serbuk kitosan ke dalam larutan asam asetat 2%. Larutan ini diaduk dengan kecepatan pengadukan 300 rpm pada suhu kamar selama 3 jam kemudian didiamkan selama 24 jam untuk melarutkan kitosan, kemudian larutan dimasukkan ke dalam labu takar 100 mL dan ditera dengan asam asetat 2%.
Sintesis Hidroksiapatit Berporogen Kitosan
Hidroksiapatit berporogen kitosan dibuat melalui modifikasi metode Lestari (2009). Serbuk cangkang telur hasil kalsinasi yang ditambahkan 50 mL etanol 96% kemudian dicampurkan dengan 3 mL H3PO4 80% yang
kitosan secara perlahan dengan menggunakan buret. Banyaknya larutan kitosan yang ditambahkan dapat dilihat pada Tabel 1. Campuran tersebut kemudian diaduk dengan kecepatan pengadukan 300 rpm pada suhu 37 ºC selama 4 jam untuk mendapatkan campuran larutan yang homogen kemudian dipanaskan dalam penangas air bersuhu 60 ºC selama 1 jam. Larutan diendapkan dalam suhu kamar selama 24 jam kemudian diaduk pada suhu 60 ºC sampai larutan berubah menjadi gel. Gel yang diperoleh dipanaskan dalam tanur pada suhu 1000 ºC selama 5 jam.
Tabel 1 Komposisi HAp-kitosan HAp Massa Volume
CaO (g) kitosan (mL)
1 4.6827 30
2 4.6809 40
3 4.6815 50
4 4.7441 60
Pencirian dengan XRD dan SEM
Pencirian serbuk hidroksiapatit ini menggunakan instrumen XRD dengan sumber Cu dan panjang gelombang 1.5406 Å. Pencirian dengan XRD dilakukan untuk mengetahui fase yang terdapat dalam sampel sedangkan pencirian dengan SEM dilakukan untuk mengetahui morfologi dan ukuran pori.
Uji In Vitro dengan Larutan SBF
Pengujian secara in vitro dilakukan
berdasarkan modifikasi Sharma et al. (2009).
Sampel masing-masing sebanyak 2 gram dibuat menjadi pelet, kemudian pelet dimasukkan ke dalam 100 mL larutan SBF. Sampel direndam dalam larutan SBF. Larutan SBF diambil setelah 6, 13, 20 hari sebanyak 20 mL, kemudian larutan disaring menggunakan kertas saring whatman No 40 selanjutnya ditentukan dengan AAS. Penentuan dengan AAS bertujuan menentukan kadar kalsium (Ca2+) yang terdapat dalam larutan.
HASIL DAN PEMBAHASAN
Komposisi Cangkang Telur
Menurut Pankaew et al. (2010) cangkang
telur ayam mengandung 94% kalsium karbonat. Tingginya kadar kalsium yang dimiliki cangkang telur, mendorong limbah cangkang telur digunakan sebagai sumber kalsium alami dalam proses síntesis hidroksiapatit. Kalsinasi cangkang telur pada suhu 1000 °C selama 6 jam mengakibatkan kalsium karbonat yang terkandung di dalam cangkang telur berubah menjadi kalsium oksida dengan reaksi sebagai berikut :
CaCO3(s) CaO(s) + CO2(g)
Kalsinasi ini dimaksudkan untuk menghilangkan karbonat yang merupakan zat pengganggu dalam proses kristalisasi hidroksiapatit (Dahlan et al. 2009).
Keberadaan ion karbonat dalam cangkang telur memberikan pengaruh dalam sintesis hidroksiapatit. Struktur karbonat dalam hidroksiapatit dapat menempati dua posisi, pertama menggantikan OH- membentuk apatit
karbonat tipe A Ca10(PO4)6CO3 (AKA) pada
suhu tinggi dan kedua menggantikan PO4
3-membentuk apatit karbonat tipe B Ca10(PO4)3(CO3)3(OH)2 (AKB) pada suhu
rendah. Namun keberadaan AKA dan AKB tersebut tidak mengganggu fungsi dari HAp karena senyawa paduan Ca/P yang telah mengalami pemanasan di atas 900 °C memiliki struktur yang stabil dan tidak berbahaya jika ikut diimplankan ke dalam tubuh makhluk hidup (Aoki 1991).
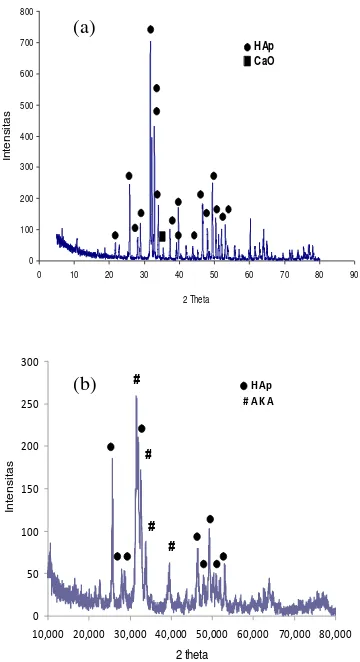
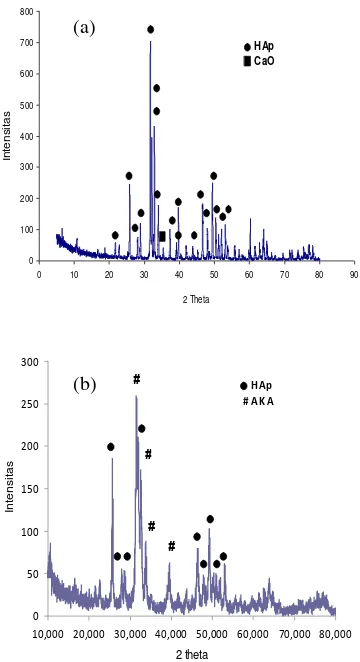
Keberadaan CaO dilakukan pencirian dengan XRD (Gambar 2). Berdasarkan pola difraksi sinar-X cangkang telur dicocokkan dengan data JCPDS (Joint Commitee on
Powder Diffraction Standards) untuk CaO
4
-100 0 100 200 300 400 500 600 700 800 900 10000 20 40 60 80 100
2 Theta In te n si ta s CaO V
Gambar 2 Pola difraksi sinar-X cangkang telur setelah kalsinasi.
Sintesis dan Pencirian Hidroksiapatit
Sintesis hidroksiapatit dengan metode basah (sol gel) pada penelitian ini menggunakan cangkang telur sebagai sumber kalsium yang sebelumnya dikalsinasi untuk membentuk CaO dan sebagai sumber fosfor digunakan H3PO4, seperti yang ditunjukkan
sebagai berikut :
10 CaO + 6 H3PO4 Ca10 (PO4)6 (OH)2
+ 8 H2O
Jumlah CaO dan H3PO4 yang dilarutkan
ditentukan berdasarkan hasil perhitungan stokiometri sehingga menghasilkan rasio konsentrasi Ca/P sebesar 1,67 (Lampiran 4).
Berdasarkan pola difraksi sinar-X HAp dibandingkan dengan data JCPDS diperoleh bahwa pada HAp sintesis, yaitu HAp tanpa penambahan kitosan (Gambar 3) memperlihatkan sebagian besar puncak dimiliki oleh fase HAp dengan intensitas tertinggi yang memilki nilai 2θ sebesar 31.716° dan 32.850° (Lampiran 5). Namun masih terdapat fase lain selain HAp, yaitu fase CaO yang memiliki nilai 2θ sebesar 37.301° dengan intensitas yang rendah. Di sisi lain pada pola difraksi sinar-X HAp komersial yang merupakan HAp tanpa penambahan kitosan (Gambar 3) memperlihatkan 2 puncak tertinggi masing-masing menunjukan fase AKA dan HAp dengan nilai 2θ sebesar 31.620° dan 31.700° (Lampiran 5).
0 100 200 300 400 500 600 700 800
0 10 20 30 40 50 60 70 80 90
2 Theta In te n si ta s HAp CaO 0 50 100 150 200 250 300
10,000 20,000 30,000 40,000 50,000 60,000 70,000 80,000
2 theta In te n si ta s # # # # H Ap # AK A
Gambar 3 Pola difraksi sinar-X (a) HAp sintesis dan (b) HAp komersial.
Hidroksiapatit hasil sintesis memiliki kualitas yang lebih baik dibandingkan HAp komersial karena tidak menunjukkan adanya puncak fase AKA seperti pada hidroksiapatit komersial. Namun pada hidroksiapatit sintesis juga masih belum murni karena masih menunjukkan adanya puncak fase dari CaO. Fase CaO yang terdapat di dalam hidroksiapatit sintesis dapat dihilangkan dengan menyimpan serbuk cangkang telur yang telah dikasinasi di dalam wadah yang tertutup rapat untuk menghindari masuknya uap air dari udara ke dalam serbuk cangkang telur.
Sintesis dan Pencirian Hidroksiapatit Berporogen Kitosan
Hidroksiapatit yang merupakan komponen organik utama dari tulang dapat disintesis dengan mencampurkan kitosan yang berfungsi sebagai porogen untuk membuat struktur berpori. Hidroksiapatit berpori telah dipergunakan untuk pengganti tulang buatan. Kegunaan utamanya untuk perbaikan,
(a)
pertumbuhan kembali jaringan yang hilang, rusak atau mengalami perubahan (Sopyan et al. 2007).
Pola difraksi sinar-X sampel Hidroksiapatit yang dibuat dengan penambahan larutan kitosan yang berbeda-berbeda (30, 40, 50 ,60 mL) ternyata tidak membuat pola difraksi sinar-X sampel berubah. Ini berarti bahwa kehadiran kitosan tidak menyebabkan perubahan bentuk struktural dari HAp. Kitosan dari komposit telah hilang saat dikalsinasi pada suhu 1000 °C. Hal ini dibuktikan dengan tidak terbentuknya pola difraksi sinar-X dari kitosan (Gambar 4) yang memilki 2θ bernilai 20.362° dan 10.527° (Lampiran 5). Pola difraksi sinar-X kitosan memperlihatkan bahwa kitosan memilki struktur yang lebih amorf dibandingkan HAp. 0 50 100 150 200 250 300 350
0 20 40 60 80
2 theta In te n s it a s
Gambar 4 Pola difraksi sinar-X kitosan.
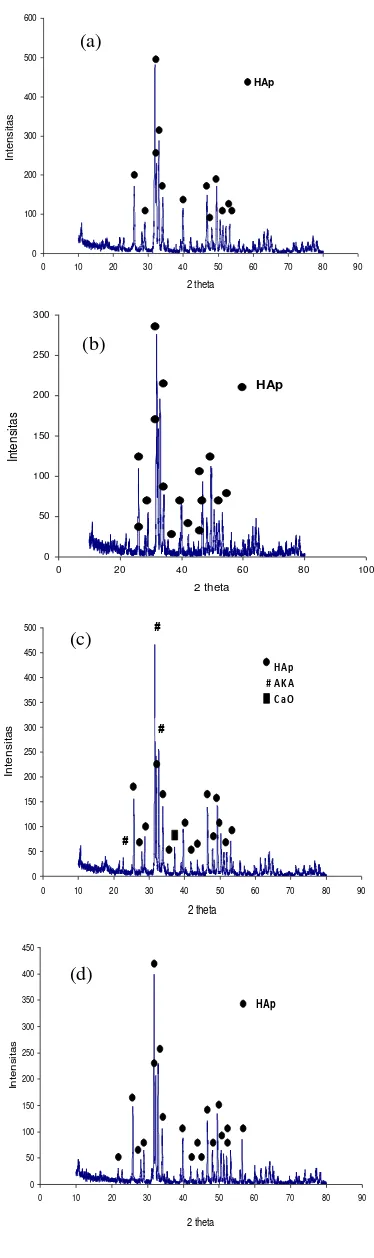
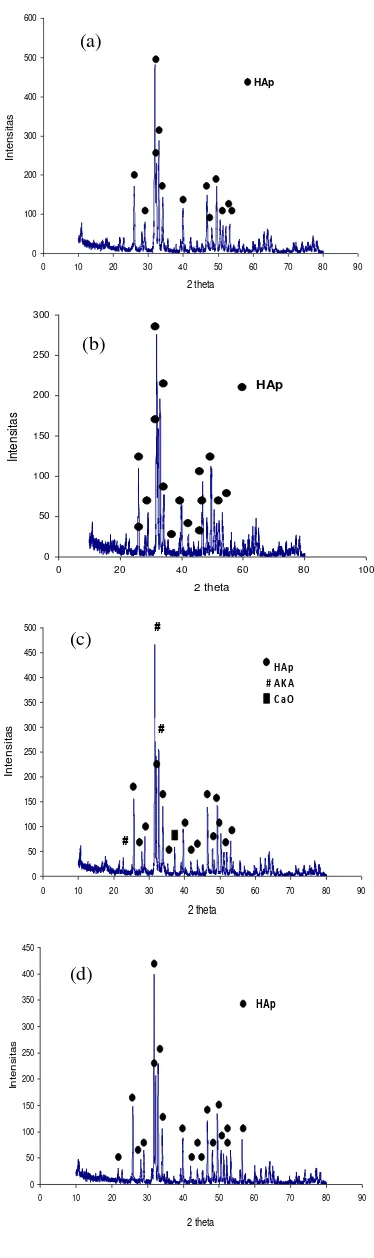
Berdasarkan pola difraksi sinar-X hidroksiapatit dengan penambahan variasi kitosan (Gambar 5) memperlihatkan bahwa masing-masing sampel sebagian besar dalam bentuk HAp. Hal ini berarti, dalam semua sampel telah terbentuk HAp. Puncak sampel HAp dengan penambahan kitosan 30, 40, dan 60 mL menunjukan fase HAp untuk keseluruhan puncak (Lampiran 5). Pola difraksi sinar-X sampel HAp dengan penambahan kitosan 50 mL memperlihatkan 3 puncak tertinggi berupa AKA dan fase HAp dengan nilai 2θ berturut-turut sebesar 31.592°, 32.723°, dan 31.991° (Lampiran 5). Hasil analisis HAp dengan penambahan kitosan 50 mL menunjukkan bahwa produk yang terbentuk bukan HAp murni, akan tetapi juga terdapat senyawa lainnya, yaitu AKA dan CaO. 0 100 200 300 400 500 600
0 10 20 30 40 50 60 70 80 90
2 theta In te n si ta s HAp 0 50 100 150 200 250 300
0 20 40 60 80 100
2 theta In te n si ta s HAp 0 50 100 150 200 250 300 350 400 450 500
0 10 20 30 40 50 60 70 80 90
2 theta In te n si ta s # # # V H Ap # AK A C aO 0 50 100 150 200 250 300 350 400 450
0 10 20 30 40 50 60 70 80 90
2 theta In te n si ta s HAp
Gambar 5 Pola difraksi sinar-X HAp dengan penambahan kitosan (a) 30 mL, (b) 40 mL, (c) 50 mL, (d) 60 mL. (a)
(b)
6
Terbentuknya fase AKA dikarenakan ion karbonat yang mengganggu proses sintesis hidroksiapatit. Keberadaan ion karbonat tidak hanya berasal dari serbuk cangkang telur sebelum dikalsinasi saja tetapi setelah dikalsinasi pun dapat dimasuki ion karbonat dari udara. Ion ini akan terperangkap selama proses sintesis dan sulit untuk dihilangkan karena akan terikat dalam kristal HAp.
Morfologi Hidroksiapatit
Karakterisasi SEM dilakukan untuk mengetahui morfologi hidroksiapatit dengan atau tanpa adanya kitosan. Karakteristik fisik dari HAp berpori yang meliputi ukuran pori, morfologi pori, dan keseragaman pori akan mempengaruhi pertumbuhan tulang ke dalam
implant (Sopyan et al. 2007). Gambar 6
memperlihatkan hasil SEM dari HAp sintesis dan HAp komersial. Pada sampel HAp sintesis yang merupakan HAp tanpa kitosan yang dikalsinasi pada suhu 1000 °C memperlihatkan bahwa morfologi tersusun dari butiran-butiran yang membentuk suatu agregat yang tidak menunjukan struktur berpori. Hal ini terjadi pula pada HAp komersial.
Gambar 6 Hasil SEM sampel pada perbesaran 3000x (a) HAp sintesis dan (b) HAp komersial.
Pada morfologi permukaan HAp dengan penambahan kitosan 30 mL terlihat jelas pori yang terbentuk dibandingkan HAp dengan penambahan kitosan 30, 40, 50, 60 mL (Gambar 7). Partikel HAp berporogen kitosan yang dihasilkan memilki struktur berpori
setelah penghilangan kitosan melalui kalsinasi, kristal HAp tetap bertahan dan mengandung pori-pori. Hal ini ditunjukkan pada sampel HAp dengan penambahan kitosan 30 mL terbentuk pori-pori yang lebih seragam, morfologi pori bulat kecil dengan ukuran pori sekitar 1µm (Lampiran 6). Pada HAp dengan penambahan kitosan 40, 50, 60 mL memperlihatkan butiran-butiran yang membentuk suatu agregat. Meskipun pori yang dihasilkan relatif kecil, tetapi sampel menunjukkan bahwa telah terbentuk HAp berpori dengan menggunakan kitosan sebagai porogennya.
Gambar 7 Hasil SEM HAp dengan penambahan kitosan (a) 30 mL, (b) 40 mL, (c) 50 mL, (d) 60 mL pada perbesaran 3000x.
b
c
d b a
Uji In Vitro dalam Larutan SBF
Larutan simulated body fluid (SBF)
merupakan larutan yang mengandung ion-ion yang komposisinya kurang lebih sama dengan cairan tubuh manusia. Cairan SBF dapat digunakan sebagai media untuk pertumbuhan kristal apatit dalam uji coba in vitro. Uji in
vitro dilakukan untuk mengetahui sifat
bioaktif dari suatu material HAp yang ditandai dengan pertumbuhan kristal apatit. Pertumbuhan kristal apatit membutuhkan ion kalsium dan fosfat (Oudadesse et al. 2011).
Konsentrasi kalsium dapat diidentifikasi menggunakan atomic absorption spectroscopy
(AAS).
Variasi konsentrasi kalsium larutan SBF dengan periode waktu perendaman ditunjukkan pada Tabel 2. Konsentrasi kalsium dalam larutan SBF awal sebesar 1.4157 ppm (Lampiran 7). Kemudian sampel direndam dalam larutan SBF, setelah 6 hari perendaman didapat konsentrasi kalsiumyang lebih besar dari konsentrasi kalsium dalam larutan SBF awal. Peningkatan konsentrasi kalsium dikarenakan ketika sampel direndam dalam larutan SBF, terjadi pertukaran ion antara permukaan sampel dan larutan akibat dari perbedaan potensial kimia sehingga menyebabkan pelepasan ion Ca2+ dari sampel
yang akan membuat bertambahnya ion Ca2+
dalam larutan SBF (Sharma et al. 2009).
Tabel 2 memperlihatkan bahwa konsentrasi kalsium menurun dengan periode waktu perendaman. Penurunan konsentrasi kalsium dihubungkan dengan pertumbuhan kristal apatit dalam sampel. Sharma et al.
(2009) menyatakan bahwa setelah 7 hari perendaman terjadi pengendapan ion Ca2+
pada sampel yang merupakan langkah awal dalam pertumbuhan kristal apatit. HAp berpori menunjukkan kapasitas yang sangat baik untuk membentuk kristal apatit dipermukaannya. Karena adanya pori maka akan memudahkan pertukaran ion dari material dengan larutan SBF.
Tabel 2 Pengukuran konsentrasi kalsium
sampel
Konsentrasi kalsium (ppm) 6 hari 13 hari 20 hari HAp sintesis 13.7078 9.2584 3.6554 HAp 1 25.7586 7.0393 1.2655 HAp 2 8.3146 7.3932 0.8483 HAp 3 8.6573 6.1742 2.5965 HAp 4 13.9326 12.5618 1.5169 Keterangan: HAp 1,2,3,4 berturut-turut adalah
HAp dengan penambahan kitosan 30,40,50,60 mL.
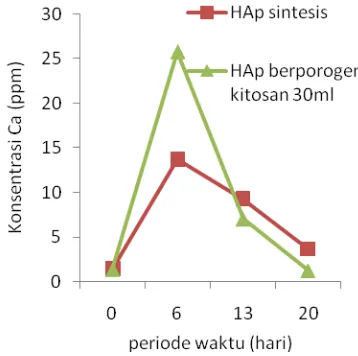
Gambar 8 memperlihatkan bahwa pada HAp sintesis yang tidak memilki porositas, terjadi penurunan konsentrasi kalsium yang tidak terlalu tinggi selama 14 hari perendaman konsentrasi kalsium menurun serbesar 10.0524 ppm, sedangkan sampel HAp dengan penambahan kitosan 30 mL yang memilki porositas, konsentrasi kalsium mengalami penurunan yang tinggi sebesar 24.4383 ppm setelah 14 hari perendaman. Hal ini dapat dijelaskan dengan cepatnya pertumbuhan kristal apatit pada permukaan HAp berpori sehingga dapat dikatakan bahwa HAp berpori dapat meningkatkan sifat bioaktif.
Gambar 8 Konsentrasi kalsium larutan SBF terhadap periode waktu perendaman.
SIMPULAN DAN SARAN
Simpulan
Sintesis Hidroksiapatit berporogen kitosan berhasil dibuat dengan metode sol gel. Pencirian XRD menunjukan bahwa pada sampel sebagian besar telah terbentuk fase HAp walaupun masih terdapat fase lain selain HAp, yaitu AKA dan CaO. Pencirian SEM memperlihatkan pori-pori berukuran mikro yang terlihat jelas pada sampel HAp dengan penambahan kitosan 30 mL. Uji in vitro
8
Saran
Perlu adanya teknik khusus untuk proses penyempurnaan sintesis hidroksiapatit berporogen kitosan agar diperoleh pori-pori dengan ukuran yang optimum, bentuk pori yang teratur dan seragam, serta perlu mengukur konsentrasi fosfat dalam larutan SBF untuk pertumbuhan kristal apatit. Selain itu, perlu dilakukan pencirian dengan XRD dan SEM pada sampel yang telah direndam dalam larutan SBF agar dapat dilihat pertumbuhan kristal apatit.
DAFTAR PUSTAKA
Amrina QH. 2008. Sintesis hidroksiapatit dengan memanfaatkan limbah cangkang telur: Karakterisasi difraksi sinar-X dan
scanning electron microscopy (SEM)
[skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Aoki H. 1991. Science and Medical
Application of Hydroxyapatite. Tokyo:
JAAS.
Austin PA. 1984. Chitinsolvent and solubility
parameters. Dept. Of Commerce, The
University of Delaware.
Dahlan KA, Prasetyanti F, Sari YW. 2009. Sintesis hidroksiapatit dari cangkang telur menggunakan dry method. Jurnal Biofisika 5(2):71-78.
Dahlan KA. 2010. Cangkang telur pengganti tulang. [terhubung berkala]. http://www.doktersahabatkita.com/index/a rticle&id. [18 Juni 2011].
Dawnay EJC. 1997. Growth and
Characterization of Semiconductor
Nanoparticles in Porous Sol-Gel Film.
Departement of Elecrical and Electronic Engineering, Imperial College.
Javidi M et al. 2008. Electrophoretic
deposition of natural hydroxyapatite on medical grade 316L stainless steel. Mater Sci Eng C. 28:8.
Kim HS, Kim JT, Jung YJ. 2007. Preparation of porous chitosan/fibroin-hydroxyapatite composite matrix for tissue engineering.
Macromolecular Research 15(1):65-73.
Lestari A. 2009. Sintesis dan karakterisasi komposit apatit-kitosan dengan metode in-situ dan ex-in-situ [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Muzzarelli RAA. 1997. Depolymerization of Chitin and Chitosan with Hemicellulase,
Lysozyme,Papain, and Lipases. Di dalam:
Muzzarelli RAA, Peter MG, editor. Chitin Handbook. Grottammare: European Chitin Soc.
Oudadesse H, Mostafa A, Bui X.V, Foad E, Kamal G, Legal Y, Cathelineau G. 2011. Physico-chemical assessment of biomimetic nano-hydroxyapatite/polymer matrix for use in bony surgery.
International Journal of Biology and
Biomedical Engineering 5:3.
Pankaew P, Hoonnivathana E, Limsuwan P, Naemchanthara K. 2010. Temperature effect on calcium phosphate synthesized from chicken eggshells and ammonium phosphate. Journal of Applied Sciences
10(24):3337-3342.
Prabakaran K, Balamurugan A, Rajeswari S. 2005. Development of calcium phosphate based apatite from hen’s eggshell. Bull
Mater Sci 28(2): 115-119.
Ratih, Ngatijo, Widjaksana, Latief A, Bambang. 2003. Aplikasi Hidroksiapatit di
Bidang Medis. Yogyakarta: Proc.
Riyani E. 2005. Karakterisasi senyawa kalsium fosfat karbonat hasil presipitasi menggunakan XRD, SEM, dan EDXA pengaruh perubahan ion F dan Mg [skripsi] Departemen Fisika. Fakultas Matematika dan Ilmu Pengetahuan Alam. Bogor: Institut Pertanian Bogor.
Sharma S, Son VP, Bellare JR. 2009. Chitosan reinforced apatite-wollastonite coating by electrophoretic deposition on titanium implants. J Mater Sci: Mater 20:1427–
1436
Sopyan I, Mel M, Ramesh S, Khalid KA. 2007. Porous hidroxyapatite for artificial bone application. Science and Technology
of Advanced Materials 8:116-123.
Sutriyo, Joshita D, Indah R. 2005. Perbandingan pelepasan propanolol hidroklorida dari matriks kitosan, etil selulosa, dan hidroksipropil metil selulosa.
Majalah Ilmu Kefarmasian 2:145-153.
Vijayalakshmi U and Rajeswari S. 2006. Preparation and characterization of microcrystalline hydroxyapatite using sol gel method. Trends Biomaterial Artificial
Lampiran 1 Diagram alir penelitian
Preparasi cangkang telur
Kalsinasi cangkang telur pada suhu 1000 °C selama 6 jam
Pelarutan serbuk CaO dengan larutan H3PO4 80% dalam 50 mL etanol 96%
Pencampuran larutan kitosan 4% sebanyak 30, 40, 50, 60 mL ke dalam campuran, diaduk dengan kecepatan 300 rpm pada suhu 37 °C
Pendiaman campuran selama 24 jam, lalu pemanasan pada suhu 60 °C hingga terbentuk gel
Pemanasan gel pada suhu 1000 °C selama 5 jam
12
Lampiran 2 Data JCPDS (a) HAp, (b)CaO, (c) AKA, (d) AKB
a
Lanjutan Lampiran 2
c
14
Lampiran 3 Data XRD serbuk cangkang telur
Sampel 2-Theta Height Fase
32.150 350 CaO
37.300 876 CaO
serbuk cangkang telur 53.799 519 CaO
64.149 130 CaO
67.350 123 CaO
Lampiran 4 Data komposisi bahan yang digunakan untuk menghasilkan sampel
Sampel Massa CaO (gram) Volume H3PO4 (mL) Massa kitosan (gram)
HAp Sintesis 4.6786 3 -
HAp 1 4.6827 3 4.0027
HAp 2 4.6809 3 4.0088
HAp 3 4.6815 3 4.0088
HAp 4 4.7441 3 4.0009
Keterangan:
HAp Sintesis : HAp tanpa penambahan kitosan HAp 1 : HAp + kitosan 4% sebanyak 30 mL HAp 2 : HAp + kitosan 4% sebanyak 40 mL HAp 3 : HAp + kitosan 4% sebanyak 50 mL HAp 4 : HAp + kitosan 4% sebanyak 60 mL
Contoh perhitungan: Massa P:
ρ H3PO4 80% = 1.64 g/mL
m H3PO4= ρ
v= 1.64 g/mL
1000 mL= 1640 g
= 16.7347 M
V1
M1 = V2M2
V1 16.7347 = 100 mL0.5M
V1 = 3 mL
Konsentrasi Ca/P: Ca/P = 1.67 M Ca = 0.5 1.67 M
Massa Ca:
m CaO = 4.676 g
Massa kitosan 4%:
m = 4 g
Lampiran 5 Data analisis hasil XRD sampel
Sampel 2-Theta Height Fase
22.804 40 HAp
25.809 229 HAp
28.063 59 HAp
28.867 104 HAp
31.716 657 HAp 32.128 363 HAp 32.85 394 HAp
33.994 155 HAp
35.397 34 HAp
HAp Sintesis 37.301 87 CaO
39.745 152 HAp
41.937 40 HAp
43.802 33 HAp
45.256 23 HAp
46.638 175 HAp
48.026 91 HAp
51.203 71 HAp
52.014 78 HAp
53.123 102 HAp
55.792 42 HAp
16
Lanjutan Lampiran 5
Sampel 2-Theta Height Fase
28.8 50 HAp
31.62 256 AKA
31.7 231 HAp
32.64 172 AKA
33.94 98 AKA
HAp komersial 39.7 62 AKA
41.94 24 HAp
43.84 31 HAp
46.58 79 HAp
48.02 45 HAp
49.32 102 HAp
50.38 50 HAp
51.16 48 HAp
52 45 HAp
53.18 59 HAp
25.926 156 HAp
28.183 39 HAp
28.981 66 HAp
31.845 443 HAp 32.23 207 HAp 32.972 264 HAp
34.132 123 HAp
35.528 23 HAp
39.881 105 HAp
HAp 1 42.089 29 HAp
43.938 23 HAp
46.766 131 HAp
48.164 54 HAp
49.553 157 HAp
50.565 77 HAp
51.34 52 HAp
52.151 53 HAp
Lanjutan Lampiran 5
Sampel 2-Theta Height Fase
25.946 89 HAp
28.223 20 HAp
29.014 42 HAp
31.864 263 HAp 32.239 148 HAp 32.991 177 HAp
34.144 63 HAp
35.521 17 HAp
HAp 2 39.899 60 HAp
42.104 21 HAp
43.951 13 HAp
46.785 80 HAp
48.182 36 HAp
48.701 12 HAp
49.575 96 HAp
50.577 50 HAp
51.358 35 HAp
52.156 37 HAp
53.28 46 HAp
55.97 18 HAp
22.667 25 AKA
25.68 146 HAp
25.927 6 HAp
27.926 42 HAp
28.733 67 HAp
31.592 386 AKA 31.991 206 HAp 32.723 236 AKA
33.872 111 HAp
35.269 19 HAp
37.179 46 CaO
HAp 3 39.03 23 HAp
39.617 88 HAp
41.803 25 HAp
43.673 19 HAp
45.139 15 HAp
46.513 121 HAp
47.893 47 HAp
49.302 120 HAp
50.315 65 HAp
18
Lanjutan Lampiran 5
Sampel 2-Theta Height Fase
53.006 58 HAp
HAp 3 53.678 22 HAp
55.692 21 HAp
21.791 21 HAp
22.875 20 HAp
25.907 128 HAp
28.152 33 HAp
28.968 56 HAp
31.819 362 HAp
32.228 197 HAp
32.948 212 HAp
34.105 86 HAp
35.512 17 HAp
HAp 4 39.85 85 HAp
42.034 26 HAp
43.912 21 HAp
45.387 20 HAp
46.743 106 HAp
48.129 52 HAp
49.534 128 HAp
50.528 56 HAp
51.314 47 HAp
52.128 49 HAp
53.24 57 HAp
55.914 21 HAp
Contoh perhitungan:
Lampiran 7 Data pengukuran konsentrasi kalsiumlarutan SBF
Hasil AAS standar kalsium
Larutan
Konsentrasi Ca (ppm) Absorbans Instrumen Perhitungan Terbaca Terkoreksi
Blanko - - 0.0007 0.0000
Standar 1 1.9753 2 0.0381 0.0374
Standar 2 3.9812 4 0.0739 0.0732
Standar 3 8.0941 8 0.1473 0.1466
Standar 4 11.9547 12 0.2162 0.2155
Standar 5 15.9947 16 0.2883 0.2876
Kurva kalibrasi standar kalsium
Hasil AAS larutan SBF
Larutan
Konsentrasi Ca (ppm) Absorbans Instrumen Perhitungan Terbaca Terkoreksi
Blanko - - 0.0036 0.0000
Standar 1 1.8803 2 0.0671 0.0635
Standar 2 3.9639 4 0.1288 0.1252
Standar 3 8.2528 8 0.2558 0.2522
Standar 4 12.0215 12 0.3674 0.3638
20
Kurva kalibrasi standar kalsium
Hasil AAS sampel
Hari
ke- Sampel
Absorbans
Pengenceran
Konsentrasi Ca (ppm) Terbaca Terkoreksi Instrumen Perhitungan
Blanko 0.0048 0.0000 - 0.1094 -
Larutan SBF 0.0328 0.0280 1.00 1.6783 1.4157
6 HAp sintesis 0.2516 0.2468 1.00 13.9383 13.7078
6 HAp 30 mL 0.7580 0.7580 1.00 25.2122 25.7586
6 HAp 40 mL 0.1556 0.1508 1.00 8.5591 8.3146
6 HAp 50 mL 0.1617 0.1569 1.00 8.9009 8.6573
6 HAp 60 mL 0.2556 0.2508 1.00 14.1624 13.9326
13 HAp sintesis 0.1724 0.1676 1.00 9.5005 9.2584
13 HAp 30 mL 0.1329 0.1281 1.00 7.2872 7.0393
13 HAp 40 mL 0.1392 0.1344 1.00 7.6402 7.3932
13 HAp 50 mL 0.1175 0.1127 1.00 6.4243 6.1742
13 HAp 60 mL 0.2312 0.2264 1.00 12.7952 12.5618
Blanko -0.0013 0.0000 - -0.4296 -
20 HAp sintesis 0.1196 0.1196 1.00 3.6533 3.6554
20 HAp 30 mL 0.0477 0.0477 1.00 1.2252 1.2655
20 HAp 40 mL 0.0356 0.0356 1.00 0.8166 0.8483
20 HAp 50 mL 0.0863 0.0863 1.00 2.5287 2.5965
20 HAp 60 mL 0.0563 0.0563 1.00 1.5156 1.5169
Contoh perhitungan: HAp sintesis hari ke-6
Persamaan garis : y = 0.0178x + 0.0028
ABSTRAK
AYU ROMAWARNI. Sintesis dan Uji
In Vitro
Hidroksiapatit Berporogen
Kitosan dengan Metode Sol Gel. Dibimbing oleh ARMI WULANAWATI dan
SULISTIOSO GIAT SUKARYO.
Hidroksiapatit (HAp) memiliki sifat biokompatibilitas yang baik dengan
tulang karena memiliki kesamaan komposisi kimia dengan tulang. Salah satu
metode sintesis HAp adalah metode sol gel. Metode sol gel dapat digunakan
untuk menghasilkan kristal HAp yang baik. HAp berpori dibuat dari kalsium yang
diperoleh dari cangkang telur dengan penambahan asam fosfat dan kitosan.
Penelitian dilakukan dengan ragam volume larutan kitosan yang ditambahkan,
yaitu 30, 40, 50, dan 60 mL. Analisis sampel dilakukan dengan menggunakan
difraksi sinar-X (XRD), mikroskop elektron payaran (SEM), dan spektrofotometer
serapan atom (AAS). Pencirian dengan XRD terhadap HAp-kitosan yang telah
dikalsinasi menunjukkan tidak ada puncak kitosan, hanya terdapat puncak milik
HAp. Pencirian dengan SEM menunjukkan bahwa penghilangan kitosan melalui
kalsinasi menghasilkan HAp dengan pori berukuran mikro. Uji
in vitro
menunjukkan bahwa terjadi penurunan konsentrasi kalsium setelah 6 hari
perendaman sampel dalam larutan
simulated body fluid
(SBF). Penurunan ini
disebabkan oleh pengendapan ion kalsium pada permukaan HAp berpori untuk
membentuk kristal apatit.
ABSTRACT
AYU ROMAWARNI. Synthesis and
In Vitro
Test of Porous
Hydroxyapatite-Chitosan with Sol Gel Method. Supervised by ARMI WULANAWATI and
SULISTIOSO GIAT SUKARYO.
Hydroxyapatite (HAp) has good compatibility with bone as its chemical
composition is similiar to that of bone material. One method to synthesize HAp is
a sol gel method. Sol gel method can be used to produce a good crystallize of
HAp. Porous HAp was made from calcium obtained from eggshell with the
addition of phosphoric acid and chitosan. The study was conducted by varying the
volume of chitosan solution, i.e. 30, 40, 50, and 60 mL. The porous HAp was
characterized using X-ray diffraction (XRD), scanning electron microscope
(SEM), and atomic absorption spectroscopy (AAS). XRD characterization of the
calcined HAp-chitosan showed that the chitosan peak was totally removed,
leaving behind all of the characteristic peaks of HAp. SEM characterization
showed that removal of chitosan through calcination leads to HAp containing
microsize pores.
In Vitro
test showed that calcium ions concentration decreasing
1
PENDAHULUAN
Tingkat kecelakaan meningkat setiap tahunnya, di antara kecelakaan tersebut tidak sedikit yang tergolong kecelakaan berat atau sampai mengalami kerusakan tulang. Sel-sel tulang sebenarnya memiliki kemampuan untuk memulihkan diri tetapi pemberian pengganti tulang bisa mempercepat pemulihan secara lebih sempurna (Dahlan 2010). Pemilihan material yang tepat sangat diperlukan dalam proses pemberian pengganti tulang, antara lain mudah diperoleh, biokompatibel, bioaktif, dan tidak toksik (Riyani 2005). Material pengganti tulang yang umum digunakan adalah autograf (penggantian satu bagian tubuh dengan bagian tubuh lainnya dalam satu individu), allograf (penggantian tulang manusia dengan tulang yang berasal dari manusia lain), xenograf (penggantian tulang manusia dengan tulang yang berasal dari hewan). Namun, material pengganti tulang ini biasanya tersedia dalam jumlah terbatas (Ratih et al. 2003).
Adanya keterbatasan dalam setiap material, memicu perkembangan riset di bidang material. Hingga saat ini studi mengenai material terus berkembang, terutama material hidroksiapatit (HAp). Baru-baru ini, perhatian khusus pada penyusunan keramik HAp dengan morfologi berpori. HAp berpori telah digunakan dalam aplikasi medis termasuk regenerasi jaringan tulang. Material HAp berpori yang dimasukkan ke dalam tulang yang patah berfungsi untuk membantu dan merangsang pertumbuhan jaringan tulang serta secara bertahap akan digantikan oleh jaringan tulang yang baru (Kim et al. 2007).
Sopyan et al. (2007) menyatakan bahwa
pembentukan HAp berpori dapat dilakukan menggunakan bahan porogen yang akan menghilang selama proses kalsinasi.
Bahan-bahan yang dapat digunakan sebagai porogen antara lain: parafin, naftalena, pati atau beberapa polimer seperti poli(asam laktat), gelatin, alginat, dan kitosan. Pada penelitian ini menggunakan kitosan sebagai porogen karena kitosan banyak terdapat di alam salah satunya dari kulit udang. Sintesis HAp dapat dilakukan dengan 2 metode, yaitu metode kering dan basah (sol gel) (Aoki 1991). Menurut Vijayalakshmi dan Rajeswari (2006) keuntungan menggunakan metode basah (sol gel) dalam prosesnya akan menghasilkan HAp yang memiliki kemurnian yang cukup tinggi.
Dengan demikian, penelitian ini bertujuan membuat hidroksiapatit berpori menggunakan kitosan sebagai porogen dengan metode sol
gel. Selanjutnya dilakukan pencirian dengan
X-ray diffraction (XRD), scanning electron
microscopy (SEM) dan mengevaluasi
pertumbuhan kristal apatit menggunakan
simulated body fluid (SBF).
TINJAUAN PUSTAKA
Hidroksiapatit
Hidroksiapatit merupakan senyawa mineral dan anggota kelompok mineral apatit dengan rumus kimia Ca10(PO4)6(OH)2 sebagai
suatu bahan keramik yang memiliki kesamaan komposisi kimia dengan jaringan tulang asli (Javidi et al. 2008). HAp dapat diperoleh dari
sumber alami atau melalui sintesis kimia. Material HAp dapat disintesis dengan menggabungkan sumber Ca dan P. Sintesis HAp dapat dilakukan dengan metode basah dan metode kering. Metode basah menggunakan prinsip presipitasi atau sol-gel sedangkan metode kering menggunakan prinsip pencampuran 2 senyawa sumber Ca dan P pada suhu tinggi (Aoki 1991). Menurut metode basah, HAp disintesis dengan cara mentitrasi larutan yang mengandung Ca dengan larutan yang mengandung P. Nisbah Ca/P agar material HAp terbentuk adalah 1,67 (Prabakaran et al. 2005). HAp memiliki sifat
biokompatibel dan bioaktif. Biokompatibel adalah kemampuan material untuk menyesuaikan dengan kecocokan tubuh penerima, sedangkan bioaktif adalah kemampuan material bereaksi dengan jaringan dan menghasilkan ikatan kimia sangat baik (Ratih et al. 2003).
Kitosan
Kitosan merupakan salah satu turunan kitin yang diperoleh melalui proses deasetilasi. Kitosan tersusun atas unit berulang 2-amino-2-deoksi-D-glukopiranosa yang terhubung oleh ikatan β-(1-4) (Gambar 1). Kitosan berbentuk padatan amorf dan dapat larut dalam asam organik seperti asam format, asam asetat, asam sitrat (Austin 1984). Kitosan adalah polimer alam yang memiliki sifat biodegradabel, tidak beracun, dan biokompatibel (Kim et al. 2007). Sifatnya
PENDAHULUAN
Tingkat kecelakaan meningkat setiap tahunnya, di antara kecelakaan tersebut tidak sedikit yang tergolong kecelakaan berat atau sampai mengalami kerusakan tulang. Sel-sel tulang sebenarnya memiliki kemampuan untuk memulihkan diri tetapi pemberian pengganti tulang bisa mempercepat pemulihan secara lebih sempurna (Dahlan 2010). Pemilihan material yang tepat sangat diperlukan dalam proses pemberian pengganti tulang, antara lain mudah diperoleh, biokompatibel, bioaktif, dan tidak toksik (Riyani 2005). Material pengganti tulang yang umum digunakan adalah autograf (penggantian satu bagian tubuh dengan bagian tubuh lainnya dalam satu individu), allograf (penggantian tulang manusia dengan tulang yang berasal dari manusia lain), xenograf (penggantian tulang manusia dengan tulang yang berasal dari hewan). Namun, material pengganti tulang ini biasanya tersedia dalam jumlah terbatas (Ratih et al. 2003).
Adanya keterbatasan dalam setiap material, memicu perkembangan riset di bidang material. Hingga saat ini studi mengenai material terus berkembang, terutama material hidroksiapatit (HAp). Baru-baru ini, perhatian khusus pada penyusunan keramik HAp dengan morfologi berpori. HAp berpori telah digunakan dalam aplikasi medis termasuk regenerasi jaringan tulang. Material HAp berpori yang dimasukkan ke dalam tulang yang patah berfungsi untuk membantu dan merangsang pertumbuhan jaringan tulang serta secara bertahap akan digantikan oleh jaringan tulang yang baru (Kim et al. 2007).
Sopyan et al. (2007) menyatakan bahwa
pembentukan HAp berpori dapat dilakukan menggunakan bahan porogen yang akan menghilang selama proses kalsinasi.
Bahan-bahan yang dapat digunakan sebagai porogen antara lain: parafin, naftalena, pati atau beberapa polimer seperti poli(asam laktat), gelatin, alginat, dan kitosan. Pada penelitian ini menggunakan kitosan sebagai porogen karena kitosan banyak terdapat di alam salah satunya dari kulit udang. Sintesis HAp dapat dilakukan dengan 2 metode, yaitu metode kering dan basah (sol gel) (Aoki 1991). Menurut Vijayalakshmi dan Rajeswari (2006) keuntungan menggunakan metode basah (sol gel) dalam prosesnya akan menghasilkan HAp yang memiliki kemurnian yang cukup tinggi.
Dengan demikian, penelitian ini bertujuan membuat hidroksiapatit berpori menggunakan kitosan sebagai porogen dengan metode sol
gel. Selanjutnya dilakukan pencirian dengan
X-ray diffraction (XRD), scanning electron
microscopy (SEM) dan mengevaluasi
pertumbuhan kristal apatit menggunakan
simulated body fluid (SBF).
TINJAUAN PUSTAKA
Hidroksiapatit
Hidroksiapatit merupakan senyawa mineral dan anggota kelompok mineral apatit dengan rumus kimia Ca10(PO4)6(OH)2 sebagai
suatu bahan keramik yang memiliki kesamaan komposisi kimia dengan jaringan tulang asli (Javidi et al. 2008). HAp dapat diperoleh dari
sumber alami atau melalui sintesis kimia. Material HAp dapat disintesis dengan menggabungkan sumber Ca dan P. Sintesis HAp dapat dilakukan dengan metode basah dan metode kering. Metode basah menggunakan prinsip presipitasi atau sol-gel sedangkan metode kering menggunakan prinsip pencampuran 2 senyawa sumber Ca dan P pada suhu tinggi (Aoki 1991). Menurut metode basah, HAp disintesis dengan cara mentitrasi larutan yang mengandung Ca dengan larutan yang mengandung P. Nisbah Ca/P agar material HAp terbentuk adalah 1,67 (Prabakaran et al. 2005). HAp memiliki sifat
biokompatibel dan bioaktif. Biokompatibel adalah kemampuan material untuk menyesuaikan dengan kecocokan tubuh penerima, sedangkan bioaktif adalah kemampuan material bereaksi dengan jaringan dan menghasilkan ikatan kimia sangat baik (Ratih et al. 2003).
Kitosan
Kitosan merupakan salah satu turunan kitin yang diperoleh melalui proses deasetilasi. Kitosan tersusun atas unit berulang 2-amino-2-deoksi-D-glukopiranosa yang terhubung oleh ikatan β-(1-4) (Gambar 1). Kitosan berbentuk padatan amorf dan dapat larut dalam asam organik seperti asam format, asam asetat, asam sitrat (Austin 1984). Kitosan adalah polimer alam yang memiliki sifat biodegradabel, tidak beracun, dan biokompatibel (Kim et al. 2007). Sifatnya
2
[image:33.595.129.269.158.232.2]dengan hidroksiapatit untuk membentuk suatu komposit material yang menunjukkan sifat-sifat polimer biomedis seperti non-toksik, biokompatibel, dan biodegradabel (Sutriyo et al. 2005).
Gambar 1 Struktur kitosan.
Metode Sol Gel
Metode sol gel adalah sebuah teknik untuk membentuk material gelas dan keramik. Proses sol gel diawali dengan pembentukan koloid yang memiliki padatan tersuspensi di dalam larutannya (kondisi ini disebut sol). Sol ini kemudian akan mengalami perubahan fase menjadi gel, yaitu koloid yang memiliki fraksi solid yang lebih besar daripada sol. Gel ini akan mengalami kekakuan dan dapat dipanaskan untuk membentuk keramik (Dawnay 1997).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah cangkang telur ayam negeri, H3PO4 80%,
etanol 96%, kitosan komersial, larutan asam asetat 2%, HAp komersial, cairan infus (0,9%
Sodium chloride, Otsu-NS).
Alat-alat yang digunakan adalah alat-alat kaca, neraca analitik, hot plate, pengaduk
magnetik, tanur, X-ray diffraction (XRD)
merk Philips tipe Shimadzu 610, scanning
electron microscopy (SEM), atomic
absorption spectroscopy (AAS) Shimadzu
AA-7000.
Tahapan Penelitian
Penelitian ini terbagi atas beberapa tahap, yaitu tahap pertama preparasi cangkang telur, tahap kedua sintesis hidroksiapatit, tahap ketiga preparasi larutan kitosan, tahap keempat sintesis hidroksiapatit berporogen kitosan, tahap kelima pencirian dengan XRD
dan SEM, tahap keenam uji in vitro dengan
larutan SBF. Diagram alir penelitian dapat dilihat pada Lampiran 1.
Preparasi Cangkang Telur
Preparasi dilakukan berdasarkan modifikasi metode Amrina (2008). Cangkang telur diberi perlakuan meliputi pembersihan, pengeringan dan kalsinasi. Perlakuan diawali dengan pembersihan cangkang telur dari kotoran makro, eliminasi membran cangkang kemudian dikeringkan di suhu kamar. Cangkang yang telah kering lalu dikalsinasi pada suhu 1000 ºC selama 6 jam. Cangkang yang telah dikalsinasikan berbentuk serbuk lalu dilakukan pencirian dengan XRD untuk mengetahui fase yang terkandung di dalamnya.
Sintesis Hidroksiapatit
Hidoksiapatit dibuat melalui modifikasi metode Septiarini (2009). Serbuk cangkang telur hasil kalsinasi ditambahkan etanol 96% sebanyak 50 mL kemudian dicampurkan dengan 3 mL H3PO4 80% yang dilarutkan
dalam 50 mL etanol 96% dilakukan dengan penetesan dari buret. Campuran tersebut diaduk dengan kecepatan pengadukan 300 rpm pada suhu 37 ºC selama 20 menit kemudian dipanaskan dalam penangas air bersuhu 60 ºC selama 1 jam. Larutan diendapkan dalam suhu kamar selama 24 jam kemudian diaduk pada suhu 60 ºC sampai larutan berubah menjadi gel. Gel yang diperoleh dipanaskan dalam tanur pada suhu 1000 ºC selama 5 jam.
Preparasi Larutan Kitosan
Larutan kitosan dibuat melalui modifikasi metode Kim et al. (2007). Larutan kitosan 4%
dibuat dengan melarutkan 4 gram serbuk kitosan ke dalam larutan asam asetat 2%. Larutan ini diaduk dengan kecepatan pengadukan 300 rpm pada suhu kamar selama 3 jam kemudian didiamkan selama 24 jam untuk melarutkan kitosan, kemudian larutan dimasukkan ke dalam labu takar 100 mL dan ditera dengan asam asetat 2%.
Sintesis Hidroksiapatit Berporogen Kitosan
Hidroksiapatit berporogen kitosan dibuat melalui modifikasi metode Lestari (2009). Serbuk cangkang telur hasil kalsinasi yang ditambahkan 50 mL etanol 96% kemudian dicampurkan dengan 3 mL H3PO4 80% yang
dengan hidroksiapatit untuk membentuk suatu komposit material yang menunjukkan sifat-sifat polimer biomedis seperti non-toksik, biokompatibel, dan biodegradabel (Sutriyo et al. 2005).
Gambar 1 Struktur kitosan.
Metode Sol Gel
Metode sol gel adalah sebuah teknik untuk membentuk material gelas dan keramik. Proses sol gel diawali dengan pembentukan koloid yang memiliki padatan tersuspensi di dalam larutannya (kondisi ini disebut sol). Sol ini kemudian akan mengalami perubahan fase menjadi gel, yaitu koloid yang memiliki fraksi solid yang lebih besar daripada sol. Gel ini akan mengalami kekakuan dan dapat dipanaskan untuk membentuk keramik (Dawnay 1997).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah cangkang telur ayam negeri, H3PO4 80%,
etanol 96%, kitosan komersial, larutan asam asetat 2%, HAp komersial, cairan infus (0,9%
Sodium chloride, Otsu-NS).
Alat-alat yang digunakan adalah alat-alat kaca, neraca analitik, hot plate, pengaduk
magnetik, tanur, X-ray diffraction (XRD)
merk Philips tipe Shimadzu 610, scanning
electron microscopy (SEM), atomic
absorption spectroscopy (AAS) Shimadzu
AA-7000.
Tahapan Penelitian
Penelitian ini terbagi atas beberapa tahap, yaitu tahap pertama preparasi cangkang telur, tahap kedua sintesis hidroksiapatit, tahap ketiga preparasi larutan kitosan, tahap keempat sintesis hidroksiapatit berporogen kitosan, tahap kelima pencirian dengan XRD
dan SEM, tahap keenam uji in vitro dengan
larutan SBF. Diagram alir penelitian dapat dilihat pada Lampiran 1.
Preparasi Cangkang Telur
Preparasi dilakukan berdasarkan modifikasi metode Amrina (2008). Cangkang telur diberi perlakuan meliputi pembersihan, pengeringan dan kalsinasi. Perlakuan diawali dengan pembersihan cangkang telur dari kotoran makro, eliminasi membran cangkang kemudian dikeringkan di suhu kamar. Cangkang yang telah kering lalu dikalsinasi pada suhu 1000 ºC selama 6 jam. Cangkang yang telah dikalsinasikan berbentuk serbuk lalu dilakukan pencirian dengan XRD untuk mengetahui fase yang terkandung di dalamnya.
Sintesis Hidroksiapatit
Hidoksiapatit dibuat melalui modifikasi metode Septiarini (2009). Serbuk cangkang telur hasil kalsinasi ditambahkan etanol 96% sebanyak 50 mL kemudian dicampurkan dengan 3 mL H3PO4 80% yang dilarutkan
dalam 50 mL etanol 96% dilakukan dengan penetesan dari buret. Campuran tersebut diaduk dengan kecepatan pengadukan 300 rpm pada suhu 37 ºC selama 20 menit kemudian dipanaskan dalam penangas air bersuhu 60 ºC selama 1 jam. Larutan diendapkan dalam suhu kamar selama 24 jam kemudian diaduk pada suhu 60 ºC sampai larutan berubah menjadi gel. Gel yang diperoleh dipanaskan dalam tanur pada suhu 1000 ºC selama 5 jam.
Preparasi Larutan Kitosan
Larutan kitosan dibuat melalui modifikasi metode Kim et al. (2007). Larutan kitosan 4%
dibuat dengan melarutkan 4 gram serbuk kitosan ke dalam larutan asam asetat 2%. Larutan ini diaduk dengan kecepatan pengadukan 300 rpm pada suhu kamar selama 3 jam kemudian didiamkan selama 24 jam untuk melarutkan kitosan, kemudian larutan dimasukkan ke dalam labu takar 100 mL dan ditera dengan asam asetat 2%.
Sintesis Hidroksiapatit Berporogen Kitosan
Hidroksiapatit berporogen kitosan dibuat melalui modifikasi metode Lestari (2009). Serbuk cangkang telur hasil kalsinasi yang ditambahkan 50 mL etanol 96% kemudian dicampurkan dengan 3 mL H3PO4 80% yang
3
kitosan secara perlahan dengan menggunakan buret. Banyaknya larutan kitosan yang ditambahkan dapat dilihat pada Tabel 1. Campuran tersebut kemudian diaduk dengan kecepatan pengadukan 300 rpm pada suhu 37 ºC selama 4 jam untuk mendapatkan campuran larutan yang homogen kemudian dipanaskan dalam penangas air bersuhu 60 ºC selama 1 jam. Larutan diendapkan dalam suhu kamar selama 24 jam kemudian diaduk pada suhu 60 ºC sampai larutan berubah menjadi gel. Gel yang diperoleh dipanaskan dalam tanur pada suhu 1000 ºC selama 5 jam.
Tabel 1 Komposisi HAp-kitosan HAp Massa Volume
CaO (g) kitosan (mL)
1 4.6827 30
2 4.6809 40
3 4.6815 50
4 4.7441 60
Pencirian dengan XRD dan SEM
Pencirian serbuk hidroksiapatit ini menggunakan instrumen XRD dengan sumber Cu dan panjang gelombang 1.5406 Å. Pencirian dengan XRD dilakukan untuk mengetahui fase yang terdapat dalam sampel sedangkan pencirian dengan SEM dilakukan untuk mengetahui morfologi dan ukuran pori.
Uji In Vitro dengan Larutan SBF
Pengujian secara in vitro dilakukan
berdasarkan modifikasi Sharma et al. (2009).
Sampel masing-masing sebanyak 2 gram dibuat menjadi pelet, kemudian pelet dimasukkan ke dalam 100 mL larutan SBF. Sampel direndam dalam larutan SBF. Larutan SBF diambil setelah 6, 13, 20 hari sebanyak 20 mL, kemudian larutan disaring menggunakan kertas saring whatman No 40 selanjutnya ditentukan dengan AAS. Penentuan dengan AAS bertujuan menentukan kadar kalsium (Ca2+) yang terdapat dalam larutan.
HASIL DAN PEMBAHASAN
Komposisi Cangkang Telur
Menurut Pankaew et al. (2010) cangkang
telur ayam mengandung 94% kalsium karbonat. Tingginya kadar kalsium yang dimiliki cangkang telur, mendorong limbah cangkang telur digunakan sebagai sumber kalsium alami dalam proses síntesis hidroksiapatit. Kalsinasi cangkang telur pada suhu 1000 °C selama 6 jam mengakibatkan kalsium karbonat yang terkandung di dalam cangkang telur berubah menjadi kalsium oksida dengan reaksi sebagai berikut :
CaCO3(s) CaO(s) + CO2(g)
Kalsinasi ini dimaksudkan untuk menghilangkan karbonat yang merupakan zat pengganggu dalam proses kristalisasi hidroksiapatit (Dahlan et al. 2009).
Keberadaan ion karbonat dalam cangkang telur memberikan pengaruh dalam sintesis hidroksiapatit. Struktur karbonat dalam hidroksiapatit dapat menempati dua posisi, pertama menggantikan OH- membentuk apatit
karbonat tipe A Ca10(PO4)6CO3 (AKA) pada
suhu tinggi dan kedua menggantikan PO4
3-membentuk apatit karbonat tipe B Ca10(PO4)3(CO3)3(OH)2 (AKB) pada suhu
rendah. Namun keberadaan AKA dan AKB tersebut tidak mengganggu fungsi dari HAp karena senyawa paduan Ca/P yang telah mengalami pemanasan di atas 900 °C memiliki struktur yang stabil dan tidak berbahaya jika ikut diimplankan ke dalam tubuh makhluk hidup (Aoki 1991).
Keberadaan CaO dilakukan pencirian dengan XRD (Gambar 2). Berdasarkan pola difraksi sinar-X cangkang telur dicocokkan dengan data JCPDS (Joint Commitee on
Powder Diffraction Standards) untuk CaO
kitosan secara perlahan dengan menggunakan buret. Banyaknya larutan kitosan yang ditambahkan dapat dilihat pada Tabel 1. Campuran tersebut kemudian diaduk dengan kecepatan pengadukan 300 rpm pada suhu 37 ºC selama 4 jam untuk mendapatkan campuran larutan yang homogen kemudian dipanaskan dalam penangas air bersuhu 60 ºC selama 1 jam. Larutan diendapkan dalam suhu kamar selama 24 jam kemudian diaduk pada suhu 60 ºC sampai larutan berubah menjadi gel. Gel yang diperoleh dipanaskan dalam tanur pada suhu 1000 ºC selama 5 jam.
Tabel 1 Komposisi HAp-kitosan HAp Massa Volume
CaO (g) kitosan (mL)
1 4.6827 30
2 4.6809 40
3 4.6815 50
4 4.7441 60
Pencirian dengan XRD dan SEM
Pencirian serbuk hidroksiapatit ini menggunakan instrumen XRD dengan sumber Cu dan panjang gelombang 1.5406 Å. Pencirian dengan XRD dilakukan untuk mengetahui fase yang terdapat dalam sampel sedangkan pencirian dengan SEM dilakukan untuk mengetahui morfologi dan ukuran pori.
Uji In Vitro dengan Larutan SBF
Pengujian secara in vitro dilakukan
berdasarkan modifikasi Sharma et al. (2009).
Sampel masing-masing sebanyak 2 gram dibuat menjadi pelet, kemudian pelet dimasukkan ke dalam 100 mL larutan SBF. Sampel direndam dalam larutan SBF. Larutan SBF diambil setelah 6, 13, 20 hari sebanyak 20 mL, kemudian larutan disaring menggunakan kertas saring whatman No 40 selanjutnya ditentukan dengan AAS. Penentuan dengan AAS bertujuan menentukan kadar kalsium (Ca2+) yang terdapat dalam larutan.
HASIL DAN PEMBAHASAN
Komposisi Cangkang Telur
Menurut Pankaew et al. (2010) cangkang
telur ayam mengandung 94% kalsium karbonat. Tingginya kadar kalsium yang dimiliki cangkang telur, mendorong limbah cangkang telur digunakan sebagai sumber kalsium alami dalam proses síntesis hidroksiapatit. Kalsinasi cangkang telur pada suhu 1000 °C selama 6 jam mengakibatkan kalsium karbonat yang terkandung di dalam cangkang telur berubah menjadi kalsium oksida dengan reaksi sebagai berikut :
CaCO3(s) CaO(s) + CO2(g)
Kalsinasi ini dimaksudkan untuk menghilangkan karbonat yang merupakan zat pengganggu dalam proses kristalisasi hidroksiapatit (Dahlan et al. 2009).
Keberadaan ion karbonat dalam cangkang telur memberikan pengaruh dalam sintesis hidroksiapatit. Struktur karbonat dalam hidroksiapatit dapat menempati dua posisi, pertama menggantikan OH- membentuk apatit
karbonat tipe A Ca10(PO4)6CO3 (AKA) pada
suhu tinggi dan kedua menggantikan PO4
3-membentuk apatit karbonat tipe B Ca10(PO4)3(CO3)3(OH)2 (AKB) pada suhu
rendah. Namun keberadaan AKA dan AKB tersebut tidak mengganggu fungsi dari HAp karena senyawa paduan Ca/P yang telah mengalami pemanasan di atas 900 °C memiliki struktur yang stabil dan tidak berbahaya jika ikut diimplankan ke dalam tubuh makhluk hidup (Aoki 1991).
Keberadaan CaO dilakukan pencirian dengan XRD (Gambar 2). Berdasarkan pola difraksi sinar-X cangkang telur dicocokkan dengan data JCPDS (Joint Commitee on
Powder Diffraction Standards) untuk CaO
4
-100 0 100 200 300 400 500 600 700 800 900 10000 20 40 60 80 100
2 Theta In te n si ta s CaO V
Gambar 2 Pola difraksi sinar-X cangkang telur setelah kalsinasi.
Sintesis dan Pencirian Hidroksiapatit
Sintesis hidroksiapatit dengan metode basah (sol gel) pada penelitian ini menggunakan cangkang telur sebagai sumber kalsium yang sebelumnya dikalsinasi untuk membentuk CaO dan sebagai sumber fosfor digunakan H3PO4, seperti yang ditunjukkan
sebagai berikut :
10 CaO + 6 H3PO4 Ca10 (PO4)6 (OH)2
+ 8 H2O
Jumlah CaO dan H3PO4 yang dilarutkan
ditentukan berdasarkan hasil perhitungan stokiometri sehingga menghasilkan rasio konsentrasi Ca/P sebesar 1,67 (Lampiran 4).
Berdasarkan pola difraksi sinar-X HAp dibandingkan dengan data JCPDS diperoleh bahwa pada HAp sintesis, yaitu HAp tanpa penambahan kitosan (Gambar 3) memperlihatkan sebagian besar puncak dimiliki oleh fase HAp dengan intensitas tertinggi yang memilki nilai 2θ sebesar 31.716° dan 32.850° (Lampiran 5). Namun masih terdapat fase lain selain HAp, yaitu fase CaO yang memiliki nilai 2θ sebesar 37.301° dengan intensitas yang rendah. Di sisi lain pada pola difraksi sinar-X HAp komersial yang merupakan HAp tanpa penambahan kitosan (Gambar 3) memperlihatkan 2 puncak tertinggi masing-masing menunjukan fase AKA dan HAp dengan nilai 2θ sebesar 31.620° dan 31.700° (Lampiran 5).
0 100 200 300 400 500 600 700 800
0 10 20 30 40 50 60 70 80 90
2 Theta In te n si ta s HAp CaO 0 50 100 150 200 250 300
10,000 20,000 30,000 40,000 50,000 60,000 70,000 80,000
[image:37.595.325.505.96.427.2]2 theta In te n si ta s # # # # H Ap # AK A
Gambar 3 Pola difraksi sinar-X (a) HAp sintesis dan (b) HAp komersial.
Hidroksiapatit hasil sintesis memiliki kualitas yang lebih baik dibandingkan HAp komersial karena tidak menunjukkan adanya puncak fase AKA seperti pada hidroksiapatit komersial. Namun pada hidroksiapatit sintesis juga masih belum murni karena masih menunjukkan adanya puncak fase dari CaO. Fase CaO yang terdapat di dalam hidroksiapatit sintesis dapat dihilangkan dengan menyimpan serbuk cangkang telur yang telah dikasinasi di dalam wadah yang tertutup rapat untuk menghindari masuknya uap air dari udara ke dalam serbuk cangkang telur.
Sintesis dan Pencirian Hidroksiapatit Berporogen Kitosan
Hidroksiapatit yang merupakan komponen organik utama dari tulang dapat disintesis dengan mencampurkan kitosan yang berfungsi sebagai porogen untuk membuat struktur berpori. Hidroksiapatit berpori telah dipergunakan untuk pengganti tulang buatan. Kegunaan utamanya untuk perbaikan,
(a)
pertumbuhan kembali jaringan yang hilang, rusak atau mengalami perubahan (Sopyan et al. 2007).
Pola difraksi sinar-X sampel Hidroksiapatit yang dibuat dengan penambahan larutan kitosan yang berbeda-berbeda (30, 40, 50 ,60 mL) ternyata tidak membuat pola difraksi sinar-X sampel berubah. Ini berarti bahwa kehadiran kitosan tidak menyebabkan perubahan bentuk struktural dari HAp. Kitosan dari komposit telah hilang saat dikalsinasi pada suhu 1000 °C. Hal ini dibuktikan dengan tidak